Область техники, к которой относится изобретение
Настоящее изобретение относится к области медицины, в частности онкологии, и молекулярной биологии и может быть использовано для ранней диагностики немелкоклеточного рака легких, включая плоскоклеточный рак.
Уровень техники
Рак легких остается одной из основных причин смерти онкологических больных в мире. Смертность от рака легких превышает смертность от рака молочной железы, толстой кишки и простаты, вместе взятых [Jemal A., Siegel R., Ward E., Murray Т., Xu J., Smigal С., Thun M.J. 2006. Cancer statistics, 2006. CA Cancer J Clin. 56, 6-30]. В России показатели смертности от рака легких у мужчин 68,2 случая на 100 тысяч населения, у женщин - 6,8 случая [Заридзе Д.Г. 2004. Эпидемиология и этиология злокачественных новообразований, стр.29-85 - в кн. Канцерогенез/ под ред. Д.Г. Заридзе. - М.: Медицина]. Различают два основных вида рака легких (РЛ): мелкоклеточный (МРЛ) и немелкоклеточный (НМРЛ), составляющих 15-20 и 75-80% соответственно. К НМРЛ относят плоскоклеточный рак легких (ПРЛ), аденокарциному легких (АКЛ), крупноклеточный рак и т.п. Среди разных форм рака легких по частоте встречаемости ПРЛ занимает первое место, АКЛ - второе.
Диагноз в половине случаев НМРЛ устанавливают на далеко зашедшей стадии опухолевого процесса, что делает малореальным радикальное излечение. Современные методы лечения повышают среднюю пятилетнюю продолжительность жизни больных НМРЛ не более чем на 15%. Этот показатель может быть существенно улучшен только с помощью разработки методов ранней диагностики. Основными методами диагностики рака легких служат инструментальные - рентгеновские и эндоскопические. Используют также анализ мокроты на атипичные клетки, биопсию ткани легких, компьютерную томографию, флуоресцентную фиброскопию. Иммунологические методы диагностики находят пока ограниченное клиническое применение. Практическую значимость имеет определение опухолевых маркеров: СЕА - раково-эмбриональный антиген - онкомаркер рака прямой кишки, но может использоваться в оценке рака легких; NSE - нейрон-специфическая энолаза - в ряде случаев используют в оценке состояния пациентов с раком легких; тканевой полипептидный антиген (ТРА)-фрагмент цитокератина, более специфичный маркер рака легких. Эти маркеры применяют для контроля лечения, выявления рецидивов, но не для диагностики РЛ на ранней стадии. Для диагностики НМРЛ широко используют маркеры SCC - антиген плоскоклеточной карциномы и фрагмент цитокератина-19 (CYFRA 21.1) [Pastor A., Menendez R., Cremades M.J., Pastor V., Llopis R., Aznar J. 1997. Diagnostic value of SCC, CEA and CYFRA 21.1 in lung cancer: a Bayesian analysis. Eur Respir J. 10, 603-609; Buccheri G., Torchio P., Ferrigno D. 2003. Clinical Equivalence of Two Cytokeratin Markers in Non-small Cell Lung Cancer. A Study of Tissue Polypeptide Antigen and Cytokeratin 19 Fragments. Chest. 124, 622-632], но они также малопригодны для ранней диагностики РЛ.
Диагностическими признаками злокачественной трансформации клеток могут служить также изменения генома в опухолевых клетках - точечные мутации в кодирующих и регуляторных участках генов, микросателлитная нестабильность, аллельные потери, изменение уровня транскрипции или трансляции генов, метилирование промоторных участков гена и др. В отличие от белковых молекулярно-генетические маркеры обладают значительно большей чувствительностью. Рак легких сопровождается изменением функциональной активности многих генов. В числе перспективных потенциальных маркерных генов, вовлеченных в канцерогенез разных форм НМРЛ, рассматривают ген DAPK1, кодирующий ассоциированную с апоптозом протеинкиназу 1 (death-associated protein kinase 1) [Toyooka S., Toyooka K.O., Miyajima K., Reddy J.L., Toyota M., Sathyanarayana U.G., Padar A., Tockman M.S., Lam S., Shivapurkar N., Gazdar A.F. 2003. Epigenetic down-regulation of death-associated protein kinase in lung cancers, Clin. Cancer Res. 9, 3034-3041].
Ассоциированная с апоптозом протеинкиназа 1 (DAPK1, 160 кДа) участвует в регуляции клеточного цикла и индукции апоптоза [Inbal В., Cohen О., Polak-Charcon S., Kopolovic J., Vadai E., Eisenbach L., Kimchi A. 1997. DAP kinase links the control of apoptosis to metastasis. Nature. 390, 180-184. Kogel D., Prehn J.H., Scheidtmann K.H. 2001, The DAP kinase family of pro-apoptotic proteins: novel players in the apoptotic game. Bioessays. 23, 352-358]. Инактивация гена показана для многих типов опухолей, включая разные формы рака легких, лимфомы, карциному носоглотки, опухоли пищеварительного тракта и шейки матки [Toyooka et al. 2003, supra; Kwong J., Lo K.W., To K.F, Teo P.M., Johnson P.J., Huang D.P. 2002. Promoter hypermethylation of multiple genes in nasopharyngeal carcinoma. Clin Cancer Res. 8, 131-137; Simpson DJ, Clayton RN, Farrell WE. 2002. Preferential loss of Death Associated Protein kinase expression in invasive pituitary tumours is associated with either CpG island methylation or homozygous deletion. Oncogene. 21, 1217-1224].
Ген DAPK1 относят к потенциальным генам-супрессорам опухолевого роста [Yanagawa N., Tamura G., Oizumi H., Takahashi N., Shimazaki Y., Motoyama T. 2003. Promoter hypermethylation of tumor suppressor and tumor-related genes in non-small cell lung cancers. Cancer Sci. 94, 589-592; Toyooka et al., 2003, supra]. Потеря активности таких генов происходит в результате точечных мутаций, аллельных делений, гомозиготных делеций или гиперметилирования CpG-островков генов, особенно в промоторных областях [Belinsky S.A, Klinge D.M., Dekker J.D., Smith M.W., Bocklage T.J., Gilliland F.D., Crowell R.E., Karp D.D., Stidley C.A., Picchi M.A. 2005. Gene promoter methylation in plasma and sputum increases with lung cancer risk. Clin. Cancer Res. 11, 6505-6511]. Для гена DAPK1 с использованием в основном метода иммуноблоттинга выявлено изменение количества соответствующего белка при НМРЛ [Toyooka et al. 2003, supra]. Следует отметить, что транскрипционная активность этого гена в норме и опухолях остается малоизученной, хотя с диагностической точки зрения существенную роль при выборе кандидата на роль диагностического маркера играет высокая стабильность образующегося транскрипта.
Потеря транскрипционной активности при НМРЛ показана для нескольких генов. В работе (Terauchi К., Shimada J., Uekawa N., Yaoi Т., Maruyama M., Fushiki S. 2006. Cancer-associated loss of TARSH gene expression in human primary lung cancer. J. Cancer Res. Clin. Oncol. 132. 28-34) выявлено уменьшение транскрипции гена TARSH, одного из генов, связанных со старением клеток, в опухолевых клеточных линиях и образцах НМРЛ по сравнению с нормой. На основе полученных результатов авторы выдвинули предположение о возможном использовании этого гена в качестве биомаркера для диагностики НМРЛ. Однако в данной работе проведен анализ только 8 образцов ПРЛ, наиболее распространенной формы РЛ. Данный аналог наиболее близок по технической сущности заявленному изобретению и принят за прототип.
Из изложенного ясно, что в данной области существует настоятельная потребность в поиске нового диагностического маркера НМРЛ, позволяющего достоверно и уже на самых ранних этапах диагностировать заболевание, и в разработке на его основе простого, чувствительного, надежного, применимого в условиях клинических или поликлинических медицинских учреждений способа диагностики плоскоклеточного рака легких.
Раскрытие изобретения
Данное изобретение стало возможным в результате проведенного авторами сравнительного анализа уровня транскрипции гена DAPK1 в опухолевых тканях легких различного типа и на разных этапах их злокачественного перерождения и открытия того факта, что уже ранние стадии развития злокачественной трансформации сопровождаются значительным снижением уровня транскрипции гена DAPK1.
Настоящее изобретение в своем аспекте относится к новому маркеру для диагностики плоскоклеточного рака легких, который представляет собой уровень транскрипции гена DAPK1. Сниженный уровень в предположительно пораженной раком ткани человека по сравнению с ее уровнем в здоровой ткани служит диагностическим признаком плоскоклеточного рака легких.
Данный способ включает следующие стадии:
а) получение исходной пары образцов ткани от пациента, где один из образцов получен из предположительно пораженной раком ткани, а второй получен из прилегающей гистологически нормальной (условно-нормальной) ткани;
б) выделение и очистка препаратов РНК из исходной пары образцов;
в) синтез одноцепочечной или двуцепочечной кДНК на матрице РНК с использованием олигонуклеотидных праймеров;
г) нормирование концентрации кДНК DAPK1 по контрольному гену, уровень транскрипции которого постоянен в норме и при плоскоклеточном раке легких;
д) проведение количественной или полуколичественной реакции амплификации фрагмента гена DAPK1 с использованием кДНК, полученной на стадии в), в качестве матрицы и пары геноспецифичных олигонуклеотидных праймеров;
е) сравнение количества амплифицированного фрагмента ДНК DAPK1 для образца, полученного из предположительно пораженной раком ткани, с количеством амплифицированного фрагмента ДНК для образца, полученного из нормальной ткани, где указанные количества амплифицированного фрагмента ДНК отражают уровень транскрипции гена DAPK1, причем уменьшение транскрипции гена DAPK1 служит диагностическим признаком рака легких.
В одном из воплощений способа изобретения на стадии в) олигонуклеотидные праймеры, используемые для синтеза одноцепочечной или двуцепочечной кДНК, выбирают из числа олиго(dT)-содержащих праймеров, случайных гексамеров или их комбинации, а также геноспецифичных праймеров.
В следующем воплощении способа настоящего изобретения для амплификации кДНК на стадии д) используют олигонуклеотидные праймеры, подобранные таким образом, что они специфически гибридизуются с кДНК даже в присутствии в препарате примеси геномной ДНК.
В отдельном предпочтительном воплощении данного изобретения последовательность праймеров представлена SEQ ID NO:1 и 2.
В еще одном воплощении способа настоящего изобретения на стадии д) количественная или полуколичественная реакция амплификации фрагмента гена DAPK1 представляет собой ПЦР в реальном времени или стандартную ОТ-ПЦР.
В одном воплощении заявленного способа на стадии г) в качестве контрольного гена используют ген GAPDH, кодирующий белок глицеральдегид-3-фосфат-дегидрогеназу.
Еще одним аспектом настоящего изобретения является набор праймеров для осуществления полимеразной цепной реакции для определения уровня транскрипции гена DAPK1, имеющих последовательность SEQ ID NO:1 и 2.
Перечень фигур.
Далее изобретение будет более подробно раскрыто со ссылкой на отдельные иллюстративные примеры и фигуры.
Фиг.1 показывает результаты подбора условий определения уровня транскрипции гена DAPK1 в образцах тканей легких. Электрофоретическое разделение в агарозном геле продуктов ПЦР (размер 214 п.н.), полученных после 30, 33 и 35 циклов, проводили в 1,8%-ном агарозном геле. М - маркер молекулярных масс ДНК (ДНК плазмиды pBR222/AluI).
Фиг.2 показывает результаты ОТ-ПЦР-анализа уровня транскрипции гена DAPK1 при ПРЛ с центральной локализацией опухоли (после 30 циклов). Номера образцов указаны над дорожками. Т - опухоль, N - условная норма (прилежащие к опухоли ткани). N1 - N3 - норма. Ген GAPDH (28 циклов ПЦР) использовали как внутренний контроль. Электрофоретическое разделение продуктов ПЦР проводили в 1,8%-ном агарозном геле.
Осуществление изобретения
Данное изобретение обеспечивает новый генетический маркер для диагностики плоскоклеточного рака легких и основанный на определении уровня транскрипции этого маркера простой, надежный способ диагностики НМРЛ на разных стадиях развития злокачественной трансформации, включая начальные. Достоверно обнаруживаемое различие в транскрипции гена DAPK1 в нормальных и опухолевых тканях может быть использовано для обнаружения рака легких.
Образцы ткани легких для анализа
В качестве образцов для проведения анализа могут быть использованы биоптаты, пунктаты, в том числе материал, полученный при бронхоскопии с прямой биопсией (центральный рак легких) и трансторакальной (чрезкожной) пункции опухоли (периферический рак).
Выделение РНК из образцов ткани легких
Способы выделения суммарной РНК из образцов ткани млекопитающих хорошо известны специалистам и, как правило, включают следующие стадии: измельчение в жидком азоте образцов опухолевых и нормальных тканей, лизис клеток, выделение РНК и ее очистку, проверку качества РНК электрофорезом в 1%-ном агарозном геле в присутствии красителя бромида этидия или в денатурирующем полиакриламидном геле, а также спектрофотометрическое определение количества РНК. Гомогенизацию кусочков ткани можно проводить вручную, растирая пестиком в керамической ступке, или с помощью механических гомогенизаторов, например, Omni Mixer или Micro-Dismembrator U фирмы Sartorius (Германия). Для выделения РНК могут быть использованы различные протоколы, широко известные специалистам в данной области. В классических методах выделения РНК используют сильные хаотропные агенты, такие как гуанидинхлорид и гуанидинизотиоцианат, растворяющие белки, и последовательные экстракции фенолом и хлороформом для денатурации и удаления белков [Sambrook J., Fritsch E.F., Maniatis Т., Molecular Cloning. A laboratory Manual. 2nd Edition ed. 1989, Cold Spring Harbour: CSHL Press]. Широко используют также метод с использованием реагента Trizol [GIBCO/Life Technologies]. Для предотвращения разрушения РНК РНКазами могут быть использованы ингибиторы, такие как игибитор RNAsin плацентарного или рекомбинантного происхождения или, например, ванадил-рибозидный комплекс - неспецифический ингибитор РНКаз широкого спектра действия.
Быстрое и качественное выделение РНК можно проводить с использованием ряда коммерчески доступных наборов (Клоноген, Санкт-Петербург; RNeasy kits (Qiagen); SV Total RNA Isolation System, Promega (США) и т.д.).
Чтобы исключить работу с агрессивными агентами, ускорить и упростить выделение РНК, применяют различные приборы, например QuickGene-810 (Life Science, Япония). Для экстракции РНК в этом приборе используют 80 мкм пористую мембрану, которая в 12,5 раз тоньше обычно используемого в таких приборах стеклянного фильтра (1000 мкм). Это позволяет уменьшить деградацию РНК и увеличить ее выход.
Реакция обратной транскрипции: синтез кДНК на матрице РНК, выделенной из образцов ткани легких, и ее перевод в двуцепочечную форму.
Процесс обратной транскрипции, в результате которой на РНК-матрице синтезируют одноцепочечную цепь ДНК, при необходимости, с достройкой второй цепи, позволяет от нестабильных молекул РНК перейти к более стабильным молекулам ДНК и амплифицировать с помощью полимеразной цепной реакции до количеств, необходимых для детекции. ОТ-ПЦР-амплификация позволяет использовать очень малые количества исходной РНК (на уровне 1 нанограмма), а следовательно, и количество исследуемой легочной ткани, из которой выделяют РНК.
Реакцию обратной транскрипции можно проводить с использованием ряда коммерчески доступных препаратов обратных транскриптаз, таких как обратная транскриптаза вируса лейкоза мышей Молони (M-MLV), вируса миелобластоза птиц (AMV), PowerScript (точечная мутация M-MLV-RT), С.Therm Polymerase и др., с помощью которых можно получать продукты амплификации длиною до нескольких тысяч и даже несколько десятков тысяч пар нуклеотидов (т.п.н.). Может быть использована термостабильная ДНК-полимераза Thermus thennophilus (Tth), обладающая обратной транскриптазной активностью в присутствии ионов Mn2+.
Для обратной транскрипции могут быть использованы различные праймеры, например:
1) Олиго(dT)n-содержащие праймеры, которые связываются с эндогенным полиА-хвостом на 3'-конце мРНК (число n обычно равно 12-18, но может достигать и большей величины). Эти праймеры наиболее часто используют для получения полноразмерных кДНК. К олиго(dT)-последовательности часто добавляют на 3'-конце нуклеотиды А, С или G, чтобы «заякорить» праймер на границу транскрипта и поли-А тракта.
2) Случайные гексануклеотидные праймеры (статистические затравки), которые гибридизуются с РНК в многочисленных участках. При обратной транскрипции с этими праймерами получают короткие кДНК. Случайные гексамеры используют для преодоления трудностей, связанных с прочной вторичной структурой РНК, они более эффективны при обратной транскрипции 5'-областей мРНК.
3) Гексамеры или другие короткие олигонуклеотиды (10-12 нуклеотидов) случайного состава могут быть также использованы в комбинации с олиго(dT)-содержащими праймерами.
4) Специфические олигонуклеотидные праймеры используют для транскрипции участка мРНК, представляющего интерес для исследования. Эти праймеры успешно применяют для диагностических целей.
Анализ транскрипции генов можно проводить, используя одноцепочечную или двуцепочечную и амплифицированную кДНК. Для синтеза второй цепи и ее амплификации наиболее часто используют специфичные праймеры. В продаже имеются наборы для синтеза кДНК, основанные на применении различных обратных транскриптаз и различных праймеров для затравки. Для получения кДНК разработан также SMART-метод (switching mechanism at the 5' end of RNA templates of reverse transcriptase), в основе которого лежит свойство обратных транскриптаз добавлять на 3'-конец синтезированной первой цепи кДНК несколько нуклеотидных остатков, преимущественно dC. Эта олиго(dC)-последовательность служит местом отжига олигонуклеотидного адаптера, имеющего комплементарную олиго(dG)-последовательность на 3'-конце. Обратная транскриптаза воспринимает праймер как продолжение РНК-матрицы и продолжает синтез первой цепи [Schmidt W.M., Mueller M.W. 1999. CapSelect: a highly sensitive method for 5' CAP-dependent enrichment of full-length cDNA in PCR-mediated analysis of mRNAs. Nucleic Acids Res. 27, e31]. Таким образом, первая цепь кДНК оказывается фланкирована с одной стороны последовательностью 3'-праймера с олиго(dT) на 3'-конце, а с другой - последовательностью, комплементарной адаптеру. Эти праймеры имеют одинаковые внешние последовательности, отличаясь только на 3'-конце. Затем первую цепь амплифицируют в ПЦР с праймером, соответствующим внешней части 3'-праймера и адаптера. Нуклеотидную последовательность общей части этих праймеров подбирают в зависимости от дальнейших целей, например получения клонотек, применения вычитающей гибридизации и т.д. В результате получают двухцепочечную ДНК, обогащенную полноразмерными последовательностями. За счет использования адаптера с заблокированным 3'-концом достигается существенное снижение фоновой амплификации. При использовании модифицированного SMART-метода за короткое время происходит амплификация исходного материала более чем в 105 раз, поэтому можно работать с очень небольшими количествами РНК (меньше 1 нанограмма), а следовательно, и с небольшим количеством исследуемой ткани [Zhu Y.Y., Machleder E.M., Chenchik A., Li R., Siebert P.D. 2001. Reverse transcriptase template switching: a SMART approach for full-length cDNA library construction. Biotechniques 30, 892-897]. Наборы для получения кДНК этим способом выпускают различные фирмы, например Евроген, Россия (набор MINT), Clontech, США, и т.п.
Анализ уровня транскрипции гена DAPK1 с помощью ПЦР.
Используя первую или вторую цепь кДНК как матрицу, коммерчески доступную от широко спектра производителей термостабильную ДНК-полимеразу (например, Taq, Pfu, Tfl, Tth, Tma и т.д.) и специфические праймеры, сайты для которых расположены в представляющем интерес транскрипте, проводят стандартный, полуколичественный ПЦР, в котором амплифицируемый фрагмент транскрипта детектируется простым гель-электорофорезом, или количественный ПЦР в реальном времени. Выбор специфических праймеров осуществляют способом, хорошо известным специалистам в данной области. Для подбора праймеров и температур отжига целесообразно использовать коммерчески доступные программы или программы, находящиеся в свободном доступе в Интернете. Среди таких программ можно упомянуть Oligo (версия 6.42), PrimerSelect из пакета Lasergene (www.dnastar.com), Primer Premier 5, primers3 (http://frodo.wi.mit.edu/cgi-bin/primer3/primer3_www.cgiC), EasyExonPrimer (Wu X., Munroe D.J. 2006. EasyExonPrimer. Automated Primer Design for Exon Sequences. Appl Bioinformatics.5, 119-120), ExPrimer (Sandhu K.S., Acharya K.K. 2005. ExPrimer: to design primers from exon-exon junctions. Bioinformatics. 21, 2091-2092), PerlPrimer, FastPCR (http:/www.biocenter.helsinki.fi/bi/Programs/fastpcr.htm), PrimerQuest (http://scitools.idtdna.com/Primerquest/). С учетом сложности анализируемого генома длина праймеров может быть выбрана в диапазоне от 18 до 25 п.н.
С целью упростить процедуру осуществления способа для целей клинического анализа и обеспечить максимальную сохранность содержащейся в образце РНК, необходимо свести к минимуму манипуляции с образцом ткани, которые потенциально могут приводить к разрушению РНК. В этой связи в одном из предпочтительных вариантов получения препарата РНК в данном изобретении не используют ДНКазу, свободную от РНКазы. При этом праймеры для ПНР подбирают таким образом, чтобы они специфически гибридизовались с кДНК даже в присутствии в препарате примеси геномной ДНК. Этого можно достигнуть, например, путем подбора праймеров к разным экзонам гена DAPK1. При использовании геноспецифичных праймеров, комплементарных участкам разных экзонов, длина продукта ПЦР, амплифицированного с примесной геномной ДНК, будет значительно больше длины ожидаемого продукта ПЦР, амплифицированного с кДНК. Если хотя бы один из подобранных праймеров перекрывает границу между экзонами, примеси геномной ДНК не будут влиять на результаты реакции амплификации.
В предпочтительном воплощении используют праймеры:
DAPK1_F (SEQ ID NO:1) 5'-GCGACAAGGACGGACACATT-3' и
DAPK1_R (SEQ ID NO:2) 5'-CGCCCATACTTGTTGGAGATGT -3'
Специалисту в данной области будет понятно, что могут быть подобраны и другие пары праймеров, различающиеся, например, по своей длине, по своей локализации относительно последовательности транскрипта гена DAPK1, которые будут обеспечивать специфическую и эффективную амплификацию фрагмента транскрипта гена DAPK1 даже в присутствии примеси геномной ДНК.
Количественная оценка уровня транскрипции достигается с помощью параллельного проведения ПЦР с тестируемым транскриптом и контрольным/стандартным транскриптом. В качестве эндогенного внутреннего контроля, относительно которого проводилось нормирование продуктов амплификации исследуемого гена DAPK1, выбран «ген домашнего хозяйства» - GAPDH, кодирующий глицеральдегид-3-фосфат-дегидрогеназу. Экспрессия «генов домашнего хозяйства» (housekeeping genes) во всех клетках обычно примерно одинакова. Для гена GAPDH в случае НМРЛ, включая ПРЛ, показан наименьший разброс уровней транскрипции в нормальных и опухолевых тканях [Liu D.W., Chen S.T., Liu H.P. Choice of endogeneous control for gene expression in nonsmall lung cancer. 2005. Eur. Respir, J. 26, 1002-1008].
Для анализа уровня транскрипции генов может быть использована не только стандартная ПЦР, но и ПЦР в реальном времени (ПЦР-РВ). В отличие от стандартного метода, где фиксируются только конечные продукты реакции, ПЦР в реальном времени использует флуоресцентно меченные олигонуклеотидные зонды для детекции ДНК в процессе ее амплификации, поэтому позволяет наблюдать накопление амплифицированных фрагментов в экспоненциальной фазе реакции, что увеличивает чувствительность метода. Зонд, комплементарный средней части амплифицируемого фрагмента, содержит на концах флуорофор и тушитель. Когда флуорофор и тушитель связаны с олигонуклеотидным зондом, наблюдается лишь незначительная флуоресцентная эмиссия. Во время процесса амплификации за счет 5'-экзонуклеазной активности Taq-полимеразы флуоресцентная метка переходит в раствор, освобождаясь от соседства с тушителем, и генерирует флуоресцентный сигнал, усиливающийся в реальном времени пропорционально накоплению амплификата.
Подбор зондов для проведения ПЦР-РВ может осуществляться в соответствии со стандартными рекомендациями производителя приборов для ПЦР-РВ. Если отсутствует необходимость мультиплексного анализа нескольких генов одновременно, экономичной альтернативой может быть система, использующая специфический к двухспиральной ДНК краситель SYBR Green, интенсивность флуоресценции которого возрастает в реальном времени пропорционально увеличению количества ампликонов. В таком варианте можно использовать праймеры без зонда.
Для проведения ПЦР в реальном времени различными фирмами разработаны амплификаторы, например: ABI Prism 7000 Sequence Detection System фирмы Applied Biosystems (США), Chromo4, MiniOpticon или iCycler iQ5 MJ Research (Bio-Rad), а также отечественные приборы ДТ-322 (ДНК-Технология), АНК-32 (Институт Аналитического Приборостроения РАН, http://www.syntol.ru/productank.htm) и т.д. Применение ПЦР-РВ позволяет также уменьшить риск контаминации и автоматизировать процесс диагностики. Процесс продолжается от 40 минут до трех часов (в зависимости от используемого амплификатора) и включает одновременное проведение ПЦР, детекцию флуоресцентного сигнала, обработку данных и их представление в графическом виде (полной кинетической кривой) с помощью специального программного обеспечения. Результаты анализа становятся доступными сразу после завершения процесса и не требуют дополнительно очистки и анализа продуктов ПЦР. В качестве основного метода измерения уровня транскрипции генов обычно выбирают сравнительный метод (метод относительных измерений, RQ-метод), основанный на относительном измерении количества исследуемых полинуклеотидных последовательностей, позволяющий проводить двойное сравнение результатов - для контрольных и целевых генов, а также для нормальных и опухолевых образцов кДНК.
Далее настоящее изобретение будет подробно проиллюстрировано со ссылкой на конкретные примеры, представляющие собой наиболее предпочтительные воплощения данного изобретения. При этом должно быть понятно, что изобретение не ограничивается этими описанными воплощениями. Напротив, предполагается, что оно включает любые альтернативы, модификации или эквиваленты, допустимые с учетом сущности и объема изобретения.
Пример 1. Образцы тканей легких.
Анализировали 29 пар образцов легочных тканей (опухоль - условная норма) пациентов с НМРЛ: 25 пар образцов ПРЛ (19 образцов с центральной локализацией опухоли и шесть - с периферической) и четыре пары образцов АКЛ. За условную норму принимали гистологически нормальные ткани легких, взятые из прилегающей к опухоли ткани ближе к краю резекции. Кроме того, использовали ткани легких, полученные постмортально от 10 человек, не имевших в анамнезе заболеваний раком (норма): пять образцов, взятых в центральных областях легких, и пять - в периферических областях. Средний возраст пациентов, среди которых 28 мужчин и одна женщина, составляет 61 год (диапазон 34-76 лет). Диагноз в каждом случае устанавливали на основании результатов клинического, морфологического, эндоскопического и рентгенологического обследований. Все опухолевые образцы охарактеризованы согласно международной системе клинико-морфологической классификации опухолей TNM, где Т (tumor) - Т0-Т4 - категории, отражающие нарастание размера и/или местного распространения первичной опухоли, N (nodulus) - N0-N3 - категории, отражающие различную степень поражения метастазами регионарных лимфатических узлов; М (metastasis) - М0-М1 - характеризует отдаленные метастазы. Все возможные комбинации TNM объединяют в более крупные группы - стадии, отражающие течение опухолевого процесса. I стадия заболевания установлена у шести больных, II - у 18, III - у пяти. Признаков отдаленных метастазов не наблюдали ни у одного из пациентов. Никто из пациентов не подвергался до операции лучевой терапии и химиотерапии.
Пример 2. Выделение РНК из образцов тканей
Суммарную РНК выделяли из замороженных, измельченных в жидком азоте образцов опухолевых и нормальных тканей. Образцы тканей гомогенизировали на приборе Micro-Dismembrator U (Sartorius, Германия). Очистку РНК проводили стандартным методом с использованием гуанидинизотиоцианата и фенола с последующим осаждением этиловым спиртом [Sambrook et al., 1989, supra]. Для удаления примесей гликопротеидов, которыми богаты ткани легких, использовали дополнительное осаждение РНК солевым раствором [Chomczynski P., Mackey К. 1995, Modification of the TRI reagent procedure for isolation of RNA from polysaccharide - and proteoglycan-rich sources. Biotechniques 19, 942-945]. После солевого осаждения все препараты РНК очищали с помощью набора "Rneasy Mini kit" (Qiagen, США) согласно прилагаемому изготовителем протоколу. Такая трехэтапная процедура очистки РНК позволила эффективно избавиться не только от трудно растворимых осадков гликопротеидов, но и от низкомолекулярных РНК. Качество препарата РНК проверяли электрофорезом в 1%-ном агарозном геле в присутствии бромида этидия. Количество РНК определяли спектрофотометрически [Sambrook et al., 1989, supra].
Пример 3. Реакция обратной транскрипции.
Синтез первой цепи кДНК
На матрице РНК, выделенной, как описано в Примере 2, синтезировали одноцепочечную кДНК. Для получения кДНК использовали модифицированный SMART-метод [Zhu Y.Y., Machleder E.M., Chenchik A., Li R., Siebert P.D. 2001. Reverse transcriptase template switching: a SMART approach for full-length cDNA library construction. Biotechniques 30, 892-897], 2 нг - 1 мкг суммарной РНК, праймеры:
SMART (5'-AAGCAGTGGTATCAACGCAGAGTACGCrGrGrG-3') и
CDS (5'-AGCAGTGGTATCAACGCAGAGTAC(T)30N-1N-3'),
и обратную транскриптазу PowerScript (Clontech, США).
Условия реакции:
Состав реакционной смеси (10 мкл):
Прогревали пробу при 72°С, 3 мин и помещали в лед.
Добавляли 5 мкл смеси:
Инкубировали при 42°С, 60 мин. Реакцию останавливали прогреванием при 65°С, 5 мин, добавляли 2 мкл 60 мМ ЭДТА и доводили объем пробы до 20 мкл.
Пример 4. Синтез второй цепи кДНК
Для синтеза второй цепи кДНК и амплификации брали 1/10 часть от объема реакционной смеси, полученной в Примере 3. Синтез проводили с помощью Advantage2 DNA Polymerase с праймером 5'-AAGCAGTGGTATCAACGCAGAGT-3' согласно протоколу «Advantage 2 PCR kit» (Clontech, Heidelberg, Germany).
Условия проведения ПЦР:
Состав реакционной смеси (50 мкл):
Условия амплификации:
95°С, 1,5 мин - 1 цикл
95°С, 20 с; 65°С, 20 с; 72°С, 3 мин - 14-17-20-23 цикла
Для каждого образца подбирали количество циклов, позволяющих получать одинаковое количество амплифицированного материала.
Пример 5. Подбор условий определения уровня транскрипции гена DAPK1 в образцах тканей легких.
Протокол определения уровня транскрипции
При подборе условий определения уровней транскрипции для амплификации двуцепочечной кДНК использовали геноспецифичные праймеры DAPK1_F (SEQ ID NO:1) и DAPK1_R (SEQ ID NO:2), которые были подобраны к разным экзонам гена DAPK1, причем один из праймеров перекрывает границу между экзонами. В этих условиях примеси геномной ДНК не влияют на результаты амплификации.
Размер ПЦР-фрагмента составлял 214 п.н. Подбор условий проведения ПЦР осуществляли на нескольких образцах кДНК. Все праймеры подобраны с помощью программы Primer Designer, разработанной в ИМБ РАН. Амплификацию проводили в 25 мкл смеси, содержащей: 67 мМ Трис-HCl, рН 8,8, 16,6 мМ (NH4)2SO4, 0,1% Tween-20, 2,5 мМ MgCl2, 0,2 мМ каждого из dNTP, 0,1 мкг кДНК, 0,2 мкМ каждого из праймеров, 2 ед. активности ДНК-полимеразы Bio-Taq (Dialat Ltd., Москва).
Условия проведения ПЦР:
Состав реакционной смеси (25 мкл):
Условия амплификации:
94°С, 2 мин - 1 цикл
94°С, 30 с; 56°С, 30 с; 72°С, 45 с - 30, 33 и 35 цикла
72°С, 5 мин - 1 цикл
Образцы кДНК нормировали по контрольному гену GAPDH, кодирующему белок глицеральдегид-3-фосфат-дегидрогеназу. Использовали праймеры, подобранные к разным экзонам гена GAPDH, причем один из праймеров перекрывает границу между экзонами:
GAPDH_F: 5'-GGAGTCAACGGATTTGGTC-3' и
GAPDH_R: 5'-TGGGTGGAATCATATTGGAACAT-3'.
Размер ПЦР-фрагмента составляет 139 п.н. Подбор условий проведения ПЦР осуществляли на нескольких образцах кДНК. Условия амплификации: предварительный прогрев при 94°С 2 мин; 94°С, 30 с, 56°С, 30 с и 72°С, 30 с - 28 и 30 циклов; 72°С, 5 мин -1 цикл.
ПЦР проводили на амплификаторе MasterCycler, Eppendorf (Германия) с нагревающейся крышкой или амплификаторе Терцик, ДНК-технология (Россия). Продукты амплификации анализировали в 1,8%-ном агарозном геле с 0,5 мкг/мл бромида этидия (см. Фиг.1). В результате были подобраны оптимальные условия ОТ-ПЦР (30-33 цикла), при которых получали линейную зависимость между числом циклов и количеством продуктов ПЦР. Все реакции амплификации повторяли трижды.
Интенсивность флуоресценции полос после электрофоретического разделения продуктов ПЦР оценивали количественно с помощью программы для денситометрии фотографий GeneProfiler (http://www/scanalytics.com) и выражали в виде значений относительной интенсивности норма/опухоль (N/T).
Амплифицированные фрагменты гена DAPK1 клонировали в векторе pGEM®-T Easy (Promega) и секвенировали. Их нуклеотидные последовательности полностью совпадали с последовательностями соответствующего фрагмента кДНК. Секвенирование проводили с помощью набора реактивов ABI PRISM® BigDyeТМ Terminator v. 3.1 с последующим анализом продуктов реакции на автоматическом секвенаторе ДНК ABI PRISM 3100-Avant.
Пример 6. Определение уровня транскрипции гена DAPK1 в образцах нормальных и опухолевых тканей.
Протокол определения уровня транскрипции
1. Приготовить master-mix, смешав все компоненты ПЦР кроме матрицы. Master-mix следует готовить из расчета 1 реакция объемом 25 мкл для каждого образца + 1 дополнительная реакция объемом 25 мкл.
Состав реакционной смеси (25 мкл):
2. В пробирки на 0,6 или 0,2 мл (помеченные для проведения 33 циклов амплификации) добавить по 24 мкл master-mix.
3. Добавить в пробирки по 1 мкл матрицы, перемешать пипетированием несколько раз.
4. В отдельной пробирке (контроль) смешать 24 мкл master-mix и 1 мкл стерильной деионизованной воды.
5. Добавить в каждую пробирку по 1 капле минерального масла (МР Biomedicals, LLC) и закрыть крышки пробирок (если ПЦР проводили на амплификаторе Терцик, ДНК-технология). В том случае, если ПЦР проводили на амплификаторе MasterCycler, Eppendorf, масло не добавляли.
6. Поместить пробирки в амплификатор и провести 30 циклов реакции амплификации.
7. После завершения реакции амплификации отобрать 4 мкл продуктов амплификации (30 циклов), продолжить реакции амплификации еще на 3 цикла, отобрать 4 мкл (33 цикла) и смешать с 2 мкл краски 6х Orange Loading Dye. Наносили образцы на 1,8%-ный агарозный гель, содержащий 0,5 мг/л бромида этидия. Также наносили на гель маркер молекулярных масс ДНК, позволяющий оценить размер продуктов амплификации (использовали ДНК плазмиды рВК222/AluI, производства Сибэнзим, Россия). Гель-электрофорез проводили в ТВЕ-буфере, содержащем 10 мг/л бромида этидия. Длина разделения составляет 3-5 см геля. После гель-электрофореза визуализацию продуктов амплификации и их документирование проводить в ультрафиолете при длине волны 302 нм.
Результаты анализа уровня транскрипции гена DAPK1.
Подсчет средних значений изменения уровней транскрипции исследуемых генов и стандартных ошибок проводили с помощью компьютерной программы SPSS 13.0 (SPSS Inc., США). Достоверность наблюдаемых изменений оценивали, исходя из нормального распределения данных. Данные считали достоверными при Р<0,05, где Р - показатель статистической значимости (достоверности) данных.
Нами показано, что в 72% (18/25) образцов ПРЛ уровень транскрипции понижен в 3 и более раз в опухолях по сравнению с условной нормой (p<0,005) (Фиг.2 и Таблица). В семи из 25 образцов транскрипция гена в опухолях практически отсутствует. В одном образце транскрипция гена не обнаружена ни в опухолях, ни в прилежащих к ним тканях. Отсутствие транскрипции гена в образцах ткани, смежной с дисплазией, но морфологически нормальной, показывает возможность распространения опухолевых клеток в нормальные клетки. В шести образцах уровень транскрипции гена в опухолях оставалась на уровне условной нормы. Во всех 10 исследованных образцах нормальной легочной ткани наблюдается транскрипция гена. Связи между изменением уровня транскрипции гена DAPK1, гистологическими различиями и стадиями прогрессии опухоли не обнаружено, однако в опухолях ПРЛ с периферической локализацией наблюдали меньшее изменение уровня транскрипции гена по сравнению с нормой, чем в образцах центрального ПРЛ (Таблица). Возможно, что это связано с большей зависимостью развития центрального ПРЛ от курения пациентов, вредных условий их труда и других неблагоприятных факторов. Понижение уровня транскрипции гена DAPK1 в 3 и более раз в опухолях АКЛ по сравнению с условной нормой наблюдается лишь в 25% образцов. Согласно этим данным изменение уровня транскрипции гена DAPK1 может служить диагностическим признаком при ПРЛ, а не АКЛ.
Настоящим изобретением также предусмотрено, что определение уровня транскрипции гена DAPK1 будет полезным при мониторинге эффективности проводимой противораковой терапии, причем анализ способом настоящего изобретения следует проводить до начала и после окончания курса лечения, а также при необходимости по ходу курса лечения. Повышение уровня транскрипции гена DAPK1 по ходу или по завершении курса лечения будет свидетельствовать о восстановлении активности гена-супрессора опухолевого роста DAPK1, что может говорить о положительных сдвигах при лечении. Понижение уровня транскрипции гена DAPK1 будет свидетельствовать о дальнейшем подавлении активности гена, что может говорить об отсутствии эффективности лечения.
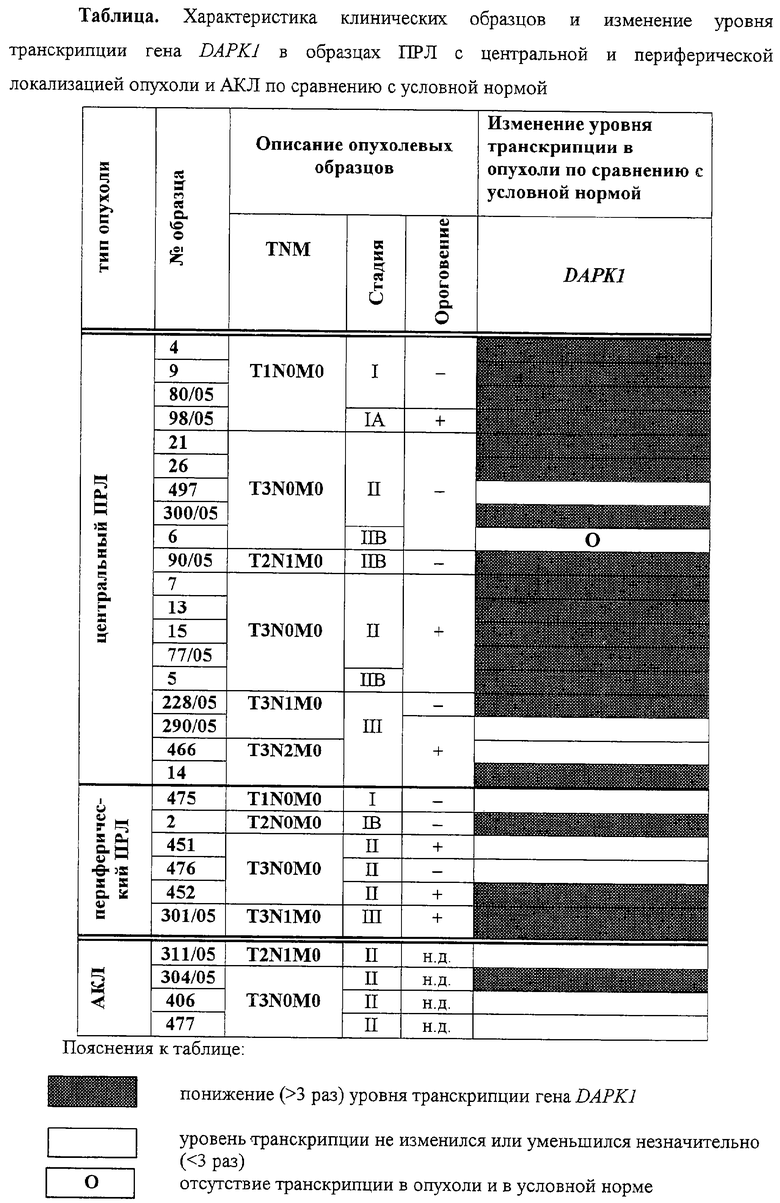
TNM - клинико-морфологическая классификация опухолей:
Т0-Т4 - категории, отражающие местное распространение первичной опухоли; N0-N3 - категории, отражающие различную степень метастатического поражения регионарных лимфатических узлов; М0-М1 - характеризуют наличие отдаленных метастазов. А - отсутствие метастазов, В - поражение одиночных лимфатических узлов, н.д. - нет данных.
Представленное выше подробное описание изобретения и его конкретных воплощений, приведенных в примерах со ссылкой на фигуры, предназначено исключительно для более полного уяснения сущности заявленного изобретения, но не для его ограничения. Специалисту будет ясно, что могут быть сделаны различные изменения, которые, тем не менее, будут соответствовать сущности и объему настоящего изобретения, которые определяются прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ ПЛОСКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2324186C1 |
| СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2330285C1 |
| СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2007 |
|
RU2351936C1 |
| СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2010 |
|
RU2445627C1 |
| СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКОГО И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2390780C1 |
| СПОСОБ ДИАГНОСТИКИ РАКА ТОЛСТОЙ КИШКИ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2374647C1 |
| СПОСОБ ДИАГНОСТИКИ ПЛОСКОКЛЕТОЧНОГО РАКА ЛЕГКОГО И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2014 |
|
RU2586779C2 |
| ОПРЕДЕЛЕНИЕ СНИЖЕНИЯ УРОВНЯ мРНК ГЕНА ZG16 КАК СПОСОБ ДИАГНОСТИКИ РАКА ТОЛСТОЙ КИШКИ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2395234C1 |
| ОПРЕДЕЛЕНИЕ СНИЖЕНИЯ УРОВНЯ мРНК ГЕНОВ ITGA9, HYAL1 И HYAL2 КАК СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКОГО И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2403575C2 |
| СПОСОБ ДИАГНОСТИКИ СВЕТЛОКЛЕТОЧНОЙ ПОЧЕЧНОКЛЕТОЧНОЙ КАРЦИНОМЫ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2393472C1 |


Изобретение относится к области медицины, в частности к онкологии и молекулярной биологии. Способ включает следующие стадии: получение исходной пары образцов ткани от пациента, выделение и очистка препаратов РНК из них, синтез одноцепочечной или двуцепочечной кДНК на матрице РНК с использованием олигонуклеотидных праймеров, нормирование концентрации кДНК DAPK1 по контрольному гену, проведение количественной или полуколичественной реакции амплификации фрагмента гена DAPK1 с использованием кДНК, полученной на стадии в), в качестве матрицы и пары геноспецифичных олигонуклестидных праймеров, последовательность которых представлена SEQ ID NO: 1 и 2, сравнение количества амплифицированного фрагмента ДНК DAPK1 для образца, полученного из предположительно пораженной раком ткани, с количеством амплифицированного фрагмента ДНК для образца, полученного из нормальной ткани, где указанные количества амплифицированного фрагмента ДНК отражают уровень транскрипции гена DAPK1, причем уменьшение транскрипции гена DAPK1 служит диагностическим признаком плоскоклеточного рака легких. Использование способа позволяет с высокой достоверностью диагностировать плоскоклеточный рак легких, в том числе на самой ранней стадии прогрессии опухолевой трансформации. 2 н. и 3 з.п. ф-лы, 2 ил., 1 табл.
а) получение исходной пары образцов ткани от пациента, где один из образцов получен из предположительно пораженной раком ткани, а второй получен из прилегающей гистологически нормальной (условно-нормальной) ткани;
б) выделение и очистка препаратов РНК из исходной пары образцов;
в) синтез одноцепочечной или двуцепочечной кДНК на матрице РНК с использованием олигонуклеотидных праймеров;
г) нормирование концентрации кДНК DAPK1 по контрольному гену, уровень транскрипции которого постоянен в норме и при раке легких;
д) проведение количественной или полуколичественной реакции амплификации фрагмента гена DAPK1 с использованием кДНК, полученной на стадии в), в качестве матрицы и пары геноспецифичных олигонуклестидных праймеров, последовательность которых представлена SEQ ID NO: 1 и 2;
е) сравнение количества амплифицированного фрагмента ДНК DAPK1 для образца, полученного из предположительно пораженной раком ткани, с количеством амплифицированного фрагмента ДНК для образца, полученного из нормальной ткани, где указанные количества амплифицированного фрагмента ДНК отражают уровень транскрипции гена DAPK1, причем уменьшение транскрипции гена DAPK1 служит диагностическим признаком плоскоклеточного рака легких.
| TERAUCHI К | |||
| AT AL Cancer-associated loss of TARSH gene expression in human primary lung cancer | |||
| J Cancer Res Clin Oncol | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| PMID: 16205947 [PubMed - indexed for MEDLINE] | |||
| СПОСОБ ДИАГНОСТИКИ РАКА ЛЕГКОГО | 1995 |
|
RU2121679C1 |
| US 20060024692 A1, 02.02.2006 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2008-06-20—Публикация
2006-10-03—Подача