Область изобретения
Настоящее изобретение относится к соединениям и фармацевтическим композициям, которые являются селективными антагонистами рецепторов А2B аденозина (Ar). Данные соединения и композиции являются полезными в качестве фармацевтических агентов.
Предпосылки создания изобретения
Алкилксантинтеофиллин (соединение А) слабый неселективный
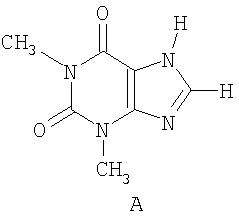
антагонист аденозина (см. Linden, J., et al., Cardiovascular Biology of Purines, eds. G.Burnstock, et al., 1998, стр.1-20) в терапевтическом отношении полезен для лечения астмы. Однако его использование связано с неприятными побочными эффектами, такими как бессонница и диурез. В последние годы использование теофиллина в качестве бронхорасширяющего средства для снятия или облегчения симптомов астмы, вытеснялось лекарствами других классов, т.е. селективными β2-адренергическими агонистами, кортикостероидами, и в последнее время, антагонистами лейкотриена. Данные соединения также имеют ограничения, таким образом, все еще желательна разработка теофиллин-подобных лекарственных средств с пониженными побочными эффектами.
Признано, что теофиллин и его близко родственный аналог кофеин блокируют эндогенный аденозин, действующий как местный модулятор аденозиновых рецепторов в головном мозге и других органах в терапевтически полезных дозах. Аденозин активирует четыре подтипа G белок-сочетаемых аденозиновых рецепторов (Ar), А1/А2А/А2В/А3. Энпрофиллин (соединение В) является еще одним примером ксантина
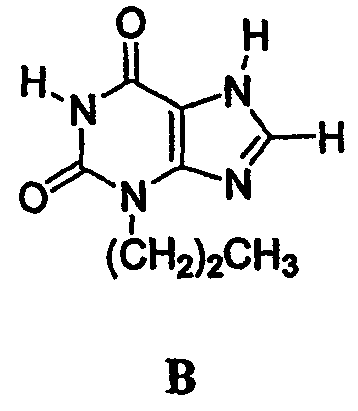
о котором сообщалось, что он блокирует А2В аденозиновые рецепторы и используется для лечения астмы. Однако данное соединение только слабо блокирует А1, А2А и А3 аденозиновые рецепторы. LaNoue et al было показано (патент США 6060481), что селективные антагонисты аденозина А2В являются полезными для улучшения у пациентов чувствительности к инсулину.
Сообщалось, что терапевтические концентрации теофиллина и энпрофиллина блокируют А2В рецепторы человека, и говорилось, что антагонисты, селективные к данному подтипу, могут иметь потенциальное применение в качестве противоастматических агентов (см. Feoktistov, I., et al., Pharmacol. Rev. 1997, 49, 381-402; и Robeva, A.S., et al., Drug Dev. Res. 1996, 39, 243-252). Сообщалось, что энпрофиллин имеет величину Ki 7 мкМ и в некотором отношении является селективным в связывании с А2В Ar человека. (См. Robeva, A.S., et al., Drug Dev. Res. 1996, 39, 243-252 и Linden, J., et al., Mol. Pharmacol. 1999, 56, 705-713). А2В Ar экспрессируются в некоторых клетках молочной железы, таких как линия клеток BR мастоцитомы собачьих, которые, по-видимому, являются ответственными за запуск острой мобилизации Са2+ и дегрануляции. (См. Auchampach, J.A., et al., Mol. Pharmacol. 1997, 52, 846-860 и Forsyth, P., et al., Inflamm. Res. 1999, 48, 301-307). А2В Ar также запускают мобилизацию Са2+ и участвуют в замедленном высвобождении IL8 из HMC-1 клеток молочной железы человека. Другие функции, связанные с А2В AR, представляют контроль клеточного роста и генной экспресии (См. Neary, J., et al., Trends Neuroisci. 1996, 19, 13-18) эндотелий-зависимое расширение сосудов (см. Martin, P.L., et al., J. Pharmacol. Exp. Ther. 1993, 265, 248-253) и секрецию жидкости из эпителия в кишечник (См. Strohmeier, G.R., et al., J. Biol. Chem. 1995, 270, 2387-2394). Сообщалось, что аденозин, действующий благодаря А2В Ar, стимулирует хлоридную проницаемость в клетках, экспрессирующих регулятор переноса фиброза желчного пузыря (См. Clancy, J.P., et al., Am. J. Physiol. 1999, 276, С361-C369.)
В последнее время Linden и др. (патент США 6545002) описали новую группу соединений и фармацевтических композиций, которые являются селективными антагонистами А2В аденозиновых рецепторов (Ar).
Хотя фрагменты, селективные в отношении подтипа аденозиновых рецепторов, доступны для А1, А2А и А3 Ar, для А2В рецептора известно лишь малое число селективных антагонистов и не известно каких-либо неселективных агонистов. Поэтому все еще существует потребность в соединениях, которые являются селективными антагонистами А2В рецептора.
Краткое описание изобретения
Настоящее изобретение предоставляет соединения, которые действуют как антагонисты рецепторов А2В аденозина. Соответственно, настоящее изобретение предоставляет соединения формулы I:
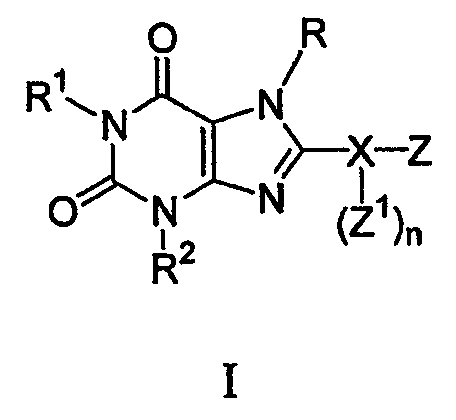
где:
R представляет водород, (С1-С5)алкил, галоген(С1-С8)алкил, (С3-С5)алкенил или (С3-С5)алкинил;
R1 и R2 представляют независимо водород, (С1-С8)алкил, (С3-С8)алкенил, (С3-С8)алкинил, (С1-С8)алкокси, (С3-С8)циклоалкил,
(С3-С8)циклоалкил(С1-С8)алкил-, (С4-С10)гетероцикл,
(С4-С10)гетероцикл(С1-С8)алкил-, (С6-С10)арил,
(С6-С10)арил(С1-С8)алкил-, (С5-С10)гетероарил или
(С5-С10)гетероарил(С1-С8)алкил-;
X представляет 5-10-членное гетероарильное кольцо, имеющее один атом азота и необязательно прерванное 1, 2 или 3 непероксидными окси (-O-), тио (-S-), сульфинильнильными (-SO-), сульфонильными (-S(O)2-) или аминными -N(R9)- группами;
Z представляет -OR3, -SR3, галоген, -S(O)m-NR4R5, -NR4R5 или (С4-С10)гетероцикл, где гетероцикл необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С1-С8)алкила, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc;
каждый Z1 представляет независимо (C1-C8)алкил, (C2-C8)алкенил, (C2-C8)алкинил, -OR6, -SR6, галоген,
R6О(C1-C8)алкил, R7R8N(C1-C8)алкил, галоген(C1-C8)алкил,
-NR7R8, R7R8N(C1-C8)алкил, -С(O)R6, -COOR6 и -С(О)NR7R8;
R3 представляет (С1-С8)алкил, (С3-С8)алкенил, (С3-С8)алкинил,
(С6-С10)арил, (С6-С10)арил(С1-С8)алкил-, (С5-С10)гетероарил,
(С5-С10)гетероарил(С1-С8)алкил-, -С(O)R6 или -С(О)NR7R8;
R4 и R5 представляют независимо водород, (С1-С8)алкил,
(С3-С8)алкенил, (С3-С8)алкинил, (С1-С8)алкокси, (С3-С8)циклоалкил,
(С3-С8)циклоалкил(С1-С8)алкил-, (С6-С18)полициклоалкил,
(С6-С18)полициклоалкил(С1-С8)алкил-, (С3-С10)гетероцикл,
(С3-С10)гетероцикл(С1-С8)алкил-, -NR7R8, (С6-С10)арил,
(С6-С10)арил(С1-С8)алкил-, (С5-С10)гетероарил,
(С5-С10)гетероарил(С1-С8)алкил-, -(C2-C4-Y)q-(CH2)2-4-X1, -С(O)R6,
-СО2R6, -С(О)NR7R8 или -S(O)2-NR7R8; или R4 и R5 вместе с атомами, к которым они присоединены, образуют насыщенное или частично ненасыщенное, моно-, бициклическое- или ароматическое кольцо, имеющее 3, 4, 5, 6, 7 или 8 кольцевых атомов и необязательно содержащее 1, 2, 3 или 4 гетероатома, выбранных из непероксидного окси (-O-), тио (-S-), сульфинила (-SO-), сульфонила (-S(O)2-) и амина -N(R9)- в кольце, где кольцо необязательно замещено 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc;
Х1 представляет -OR6, -С(O)R6, -СО2R6 или -NR7R8; и Y представляет окси (-O-), тио (-S-), сульфинил (-SO-), сульфонил (-S(O)2-) и амин -N(R9)-;
где алкильная, алкенильная, циклоалкильная, алкинильная, арильная, гетероциклическая или гетероарильная группы из R1, R2, R3, R4 и R5 групп необязательно замещены одним или более заместителями, выбранными независимо из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc;
где R6 представляет водород, (С1-С8)алкил, RaО(С1-С8)алкил,
RbRcN(C1-C8)алкил, галоген(C1-C8)алкил, (С3-С10)гетероцикл,
(С3-С10)гетероцикл(С1-С8)алкил-, (С6-С10)арил,
(С6-С10)арил(С1-С8)алкил-, (С4-С10)гетероарил,
(С4-С10)гетероарил(С1-С8)алкил-; где гетероцикл, гетероарил или арил необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc;
где R7, R8 и R9 представляют независимо водород, (С1-С8)алкил, RaО(С1-С8)алкил, RbRcN(C1-C8)алкил, галоген(C1-C8)алкил, (С3-С10)гетероцикл, (С6-С10)арил, (С6-С10)арил(С1-С8)алкил-, (С4-С10)гетероарил, -COORa, -C(O)Ra или C(O)NRbRc; где гетероцикл, гетероарил или арил необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc; или R7 и R8 вместе с атомами, к которым они присоединены, образуют насыщенное или частично ненасыщенное, моно-, бициклическое- или ароматическое кольцо, имеющее 3, 4, 5, 6, 7 или 8 кольцевых атомов, необязательно кольцо, имеющее от 4 до восьми кольцевых атомов и необязательно содержащее 1, 2, 3 или 4 гетероатома, выбранных из непероксидного окси (-O-), тио (-S-), сульфинила (-SO-), сульфонила (-S(O)2-) или амина -N(R9)- в кольце;
Rа представляет водород или (С1-С6)алкил; Rb и Rс каждый независимо представляет водород, (С1-С6)алкил, (С1-С6)алкокси, (С3-С8)циклоалкил, (С1-С6)алкилтио, (С6-С10)арил, (С6-С10)арил(С1-С6)алкил-, гетероарил или гетероарил(С1-С6)алкил-; или Rb и Rс вместе с азотом, к которому они присоединены, образуют пирролидильное, пиперидильное, пиперазинильное, азепинильное, диазепинильное, морфолинильное или тиоморфолинильное кольцо;
где n равно 0, 1, 2, 3, 4, 5, 6, 7 или 8; m равно 1 или 2; и q равно 1, 2, 3 или 4; или их фармацевтически приемлемые соли.
Изобретение предоставляет также фармацевтически приемлемые соли соединения формулы (I). Изобретение представляет также фармацевтическую композицию, содержащую соединение формулы I или его фармацевтически приемлемую соль в сочетании с фармацевтически приемлемым разбавителем или носителем.
В дополнение, изобретение предоставляет терапевтический способ профилактики или лечения патологических состояний или симптомов у млекопитающего, такого как человек, при которых в один или более симптомов патологии вовлечена активность, т.е. сверхактивность, аденозиновых А2В рецепторов, и желателен антагонизм (т.е. блокирование) их активности для облегчения указанных симптомов. Такие заболевания или состояния включают, но не ограничиваются ими, астму, аллергии, аллергические заболевания (например, аллергический ринит и синусит), аутоиммунные заболевания (например, волчанку), диарейные заболевания, устойчивость к инсулину, диабет, предотвращение дегрануляции клеток молочной железы, связанной с ишемическими/реперфузионными повреждениями, сердечный приступ, ингибирование ангиогенеза в неопластических тканях и ингибирование ангиогенеза при диабетической ретинопатии или индуцированной гипербарическим кислородом ретинопатии. Изобретение также предусматривает способ лечения астмы, диарейных заболеваний, устойчивости к инсулину, диабета, ингибирования ангиогенеза в неопластических тканях и ингибирования ангиогенеза при диабетической ретинопатии или индуцированной гипербарическим кислородом ретинопатии у млекопитающих (например, человека), включающий введение млекопитающему, нуждающемуся в таком лечении, эффективного количества, по крайней мере, одного соединения формулы I или его фармацевтически приемлемой соли(ей).
Изобретение предоставляет соединение формулы I для применения в медицинской терапии, предпочтительно, для применения в лечении заболеваний или состояний, связанных с разрушительной активацией или активностью А2В рецептора, включающих астму, диарейные заболевания, устойчивость к инсулину, диабет, ишемическое/реперфузионное повреждение, ингибирование ангиогенеза в неопластических тканях и ингибирование ангиогенеза при диабетической ретинопатии или индуцированной гипербарическим кислородом ретинопатии.
Изобретение предоставляет также применение соединения формулы I для производства медикаментов для лечения патологических состояний или симптомов у млекопитающих, таких как человек, которые связаны с разрушительной активацией или активностью А2В рецептора, включающих указанные выше заболевания или патологии.
Изобретение предусматривает также способ, включающий контактирование соединения формулы I, необязательно имеющего радиоактивный изотоп (радионуклид), такой как, например, тритий, радиоактивный иод (например, 125I для анализов связывания или 123I для спектральной визуализации) и подобные, с целевыми участками или сайтами А2В аденозинового рецептора, включающими указанные рецепторы, ин витро или ин виво, так, чтобы связаться с указанными рецепторами. Клеточные мембраны, включающие сайты А2В аденозинового рецептора, могут использоваться для измерения селективности испытуемых соединений для подтипов рецептора аденозина или могут использоваться в качестве инструмента для идентификации потенциальных терапевтических агентов для лечения заболеваний или состояний, связанных с опосредованием А2В- рецептора, путем контактирования указанных агентов с указанными радиолигандами и рецепторами, и измерения степени смещения радиолиганда и/или связывания агента.
Подробное описание изобретения
Заявители обнаружили, что соединения изобретения, имеющие формулу I, могут быть полезными для лечения заболеваний или состояний, связанных с разрушительной активацией или активностью А2В рецептора.
Если не указано иное, используются следующие определения: галоген представляет фтор, хлор, бром или иод. Алкил, алкокси, алкенил, алкинил и др. означают как прямые, так и разветвленные группы; и ссылка на индивидуальный радикал, такой как “пропил”, охватывает радикал только с прямой цепью, причем, изомер с разветвленной цепью, такой как “изопропил”, конкретно относится к радикалу с разветвленной цепью. Когда алкил является частично ненасыщенным, алкильная цепь может включать одну или более (например, 1, 2, 3 или 4) двойных или тройных связей в цепи.
“Арил” означает фенильный радикал или орто-конденсированный бициклический карбоциклический радикал, имеющий около девяти-десяти кольцевых атомов, в котором, по крайней мере, одно кольцо является ароматическим.
“Аралкил” или “(С6-С10)арил(С1-С8)алкил-” относится к группе формулы арил(С1-С8)алкил-, в которой арил и (С1-С8)алкил имеют определенные выше значения.
“Гетероцикл” охватывает циклический радикал, присоединенный или связанный через кольцевой атом азота или углерода моноциклической, конденсированной бициклической или соединенной через мостик бициклической, насыщенной или ненасыщенной кольцевой системы, содержащей 5-10 кольцевых атомов и, предпочтительно, из 5-6 кольцевых атомов, состоящих из углерода и одного, двух, трех или четырех гетероатомов, каждый из которых выбран из группы, состоящей из непероксидных окси (-O-), тио (-S-), сульфинильнильных (-SO-), сульфонильных (-S(O)2-), аминных -N(R9)- или -N=групп, где R9 имеет определенные выше значения, и необязательно содержащей 1-3 двойных связи (например, -СН=СН- или -CH=N-). Гетероцикл включает, например тетрагидрофурил, дигидрофурил, тетрагидроимидазолил, азанорборнил, пирролидил, пиперидил, пиперизил, морфолинил, азепинил, 1,3-диазепинил, 1,3-бензодиазепинил, 1,4-диазепинил, 1,4-бензодиазепинил, 1,5-диазепинил, 1,5-бензодиазепино и подобные.
“Гетероарил” охватывает радикал, присоединенный через кольцевой атом моноциклического ароматического кольца, содержащего 5-10 кольцевых атомов и, предпочтительно, из 5-6 кольцевых атомов, состоящих из углерода и одного, двух, трех или четырех гетероатомов, каждый из которых выбран из группы, состоящей из непероксидных окси (-O-), тио (-S-), сульфинильнильных (-SO-), сульфонильных (-S(O)2-) или аминных (-N(R9)-) групп, где R9 имеет определенные выше значения. Предпочтительные гетероарильные группы включают имидазолил, триазолил, триазинил, оксазолил, изоксазолил, тиазолил, изотиазолил, тиодиазолил, пирролил, пиразинил, тетразолил, пиридинил, пиримидинил, индолил, изохинолил, хинолил и подобные.
Как понятно любому среднему специалисту в данной области, имидазольное кольцо соединений настоящего изобретения может существовать в таутомерных формах или в виде таутомеров, и, таким образом, они также включены в объем изобретения. Таутомерные изомеры представлены в виде структур (Ia) и (Ib):
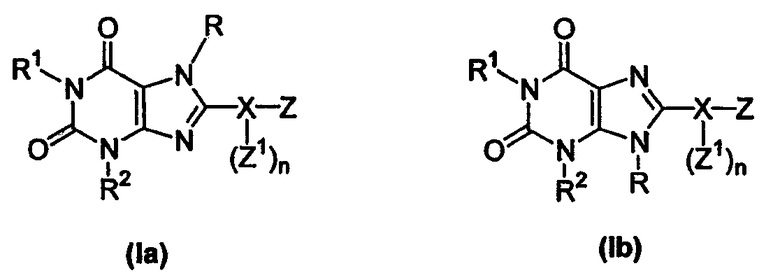
При наименовании или ссылке на одно соединение (I), например, для целей настоящего изобретения следует понимать, что также имеются в виду таутомеры (Ia) и (Ib). Аналогично, при ссылке на соединение (Ia) для целей настоящего изобретения следует понимать, что также имеются в виду таутомеры (I) и (Ib). То же самое справедливо и для ссылок на таутомер (Ib).
“Необязательный” или “необязательно” означает, что описываемое впоследствии событие, условие или состояние происходит необязательно, и что описание включает случаи, когда событие или условие имеет место, и случаи, когда этого не происходит. Например, “необязательно замещенный” означает, что названный заместитель может присутствовать, но необязательно присутствует, и описание включает ситуации, при которых названный заместитель включен, и ситуации, когда названный заместитель не включен.
Термины “включает”, “например”, “такой как” и подобные используются в целях иллюстрации и ими не следует ограничивать настоящее изобретение.
Неопределенность единственного числа существительного при первом его упоминании означает “по крайней мере, один” или “один или более”, когда они используются в данном описании, включая пункты формулы изобретения, если конкретно не указано иное.
Специалистам в данной области будет очевидно, что соединения изобретения, имеющие хиральный центр, могут существовать и быть выделенными в оптически активной и рацемической формах. Некоторые соединения могут проявлять полиморфизм. Следует понимать, что настоящее изобретение охватывает любую рацемическую, оптически активную, полиморфную или стереоизомерную форму или их смеси соединений изобретения, которые обладают полезными свойствами, описанными в данном описании, и в данной области хорошо известно, как получить оптически активные формы (например, расщеплением рацемической формы с помощью методов перекристаллизации, синтезом из оптически активных исходных веществ, путем хирального синтеза или хроматографическим разделением с использованием хиральной неподвижной фазы) и как определить, например, противоопухолевую активность, гербицидную активность или другую терапевтическую активность, используя стандартные испытания, описанные в данном описании, или используя другие аналогичные испытания, которые хорошо известны в данной области.
Конкретные и предпочтительные значения, перечисленные ниже для радикалов, заместителей и интервалов, являются только иллюстративными; они не исключают другие определенные значения и другие значения в определенных интервалах для радикалов и заместителей.
Конкретно, (С1-С8)алкилом может быть метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, 3-пентил, н-гексил, н-гептил, н-октил или разветвленный (С3-С8)алкил; (С2-С8)алкенилом может быть винил, 1-пропенил, 2-пропенил (аллил), 1-бутенил, 2-бутенил, 3-бутенил, 1-пентенил, 2-пентенил, 3-пентенил, 1-гексенил, 2-гексенил, 3-гексенил, 1-гептенил, 2-гептенил, 3-гептенил, 1-октенил, 2-октенил, 3-октенил, 4-октенил или разветвленный (С3-С8)алкенил; (С3-С8)алкенилом может быть 2-пропенил (аллил), 2-бутенил, 3-бутенил, 2-пентенил, 3-пентенил, 1-гексенил, 2-гексенил, 3-гексенил, 2-гептенил, 3-гептенил, 2-октенил, 3-октенил, 4-октенил или разветвленный (С3-С8)алкенил; (С2-С8)алкинилом может быть этинил, 1-пропинил, 2-пропинил (пропаргил), 1-бутинил, 2-бутинил, 3-бутинил, 1-пентинил, 2-пентинил, 3-пентинил, 1-гексинил, 2-гексинил, 3-гексинил, 1-гептинил, 2-гептинил, 3-гептинил, 1-октинил, 2-октинил, 3-октинил, 4-октинил или разветвленный (С3-С8)алкинил; (С3-С8)алкинилом может быть 2-пропинил (пропаргил), 2-бутинил, 3-бутинил, 1-пентинил, 2-пентинил, 3-пентинил, 1-гексинил, 2-гексинил, 3-гексинил, 1-гептинил, 2-гептинил, 3-гептинил, 1-октинил, 2-октинил, 3-октинил, 4-октинил или разветвленный (С3-С8)алкинил; (С1-С8)алкокси может быть метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, пентокси, 3-пентокси, н-гексилокси, н-гептилокси, н-октилокиси или разветвленный (С3-С8)алкокси; галоген(С1-С8)алкилом может быть иодметил, бромметил, хлорметил, фторметил, трифторметил, 2-хлорэтил, 2-бромэтил, 2-фторэтил, 3-фторпропил, 2,2,2-трифторэтил, пентафторэтил или разветвленный галоген(С3-С8)алкил; (С3-С8)циклоалкилом может быть циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклооктил; (С3-С8)циклоалкил(С1-С8)алкилом- может быть циклопропилметил, циклобутилметил, циклопентилметил, циклогексилметил, 2-циклопропилэтил, 2-циклобутилэтил, 2-циклопентилэтил или 2-циклогексилэтил; (С6-С10)арилом может быть фенил, инденил или нафтил; гетероциклом может быть тетрагидрофурил, дигидрофурил, тетрагидроимидазолил, азанорборнил, пирролидил, пиперидил, пиперизинил, морфолинил, азепинил, 1,3-диазепинил, 1,3-бензодиазепинил, 1,4-диазепинил, 1,4-бензодиазепинил, 1,5-диазепинил или 1,5-бензодиазепино.
Арилалкилом может быть фенилэтил, бензил, 2-фенилпропил, 3-фенилпропил, 2-нафилметил или 3-нафтилметил; и гетероарилом может быть имидазолил, триазолил, триазинил, оксазолил, изоксазолил, тиазолил, изотиазолил, пирролил, пиразинил, татразолил, пиридил, пиримидинил, индолил, изохинолил, хинолил или их оксид.
(С1-С8)Алкильными группами могут быть метил, этил, пропил, бутил, пентил, гексил, гептил и октил; алкенильными группами являются этенил, пропенил, бутенил, пентенил и гексенил.
Конкретными циклоалкильными группами являются циклопропил, циклобутил, циклопентил и циклогексил.
Конкретными циклоалкилалкильными группами являются циклопропилметил, циклобутилметил, циклопропилэтил, циклопентилметил, циклогексилметил, 2-циклопентилэтил и 2-циклогесилэтил.
Конкретными арильными группами являются фенил, инденил или нафтил.
Конкретными арилалкильными группами являются бензил и 2-фенилэтил.
Конкретными галогеналкильными группами являются бромэтил, хлорэтил, фторэтил, трифторметил, 2,2,2-трифторэтил или 3-фторпропил.
Конкретным значением для R является водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, н-бутил, изобутил или галоген(С1-С4)алкил.
Еще одним конкретным значением для R является водород, метил, этил, -СН2-СН2-Cl, -СН2-СН2-Br или -СН2-СН2-СН2-F.
Еще одним конкретным значением для R является водород.
Конкретным значением для R1 является водород, (С1-С4)алкил, (С3-С4)алкенил, (С3-С4)алкинил, фенил или фенил(С1-С4)алкил.
Еще одним конкретным значением для R1 является (С3-С6)циклоалкил и (С3-С6)циклоалкил(С1-С4)алкил-.
Еще одним конкретным значением для R1 является циклопропил или циклопропилметил.
Еще одним конкретным значением для R1 является водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, н-бутил, изобутил, фенил, фенетил или бензил.
Еще одним конкретным значением для R1 является водород, метил, этил, аллил, пропаргил, изопропил, н-пропил или (метоксифенил)этил.
Еще одним конкретным значением для R1 является этил, н-пропил или аллил.
Конкретным значением для R2 является водород, (С1-С4)алкил, (С3-С4)алкенил, (С3-С4)алкинил, фенил или фенил(С1-С4)алкил.
Еще одним конкретным значением для R2 является (С3-С6)циклоалкил и (С3-С6)циклоалкил(С1-С4)алкил-.
Еще одним конкретным значением для R2 является циклопропил или циклопропилметил.
Еще одним конкретным значением для R2 является водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, н-бутил, изобутил, фенил, фенетил или бензил.
Еще одним конкретным значением для R2 является водород, метил, этил, аллил, пропаргил, изопропил, н-пропил или (метоксифенил)этил.
Еще одним конкретным значением для R2 является этил, н-пропил или аллил.
Конкретным значением для Х является имидазолил, триазолил, триазинил, оксазолил, изоксазолил, тиазолил, изотиазолил, тиодиазолил, пирролил, пиразинил, татразолил, пиридинил, пиримидинил, индолил, изохинолил или хинолил, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, (С1-С8)алкила, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc.
Еще одним конкретным значением для Х является 2-пиридинил, 3-пиридинил или 4-пиридинил, каждый необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, (С1-С8)алкила, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc.
Конкретным значением для -X(Z1)n-Z является группа, имеющая формулу
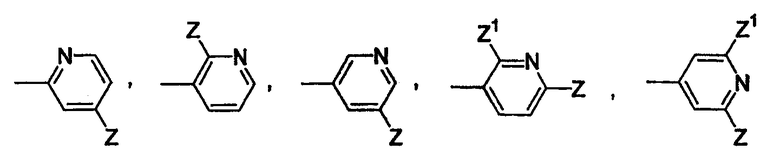
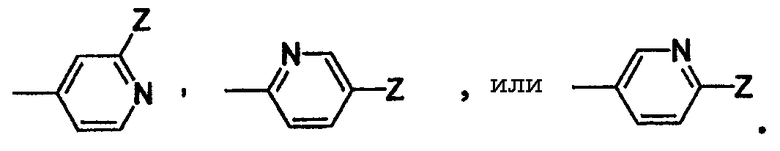
Еще одним конкретным значением для -X(Z1)n-Z является группа, имеющая формулу
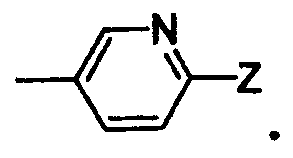
Еще одним конкретным значением для -X(Z1)n-Z является группа, имеющая формулу
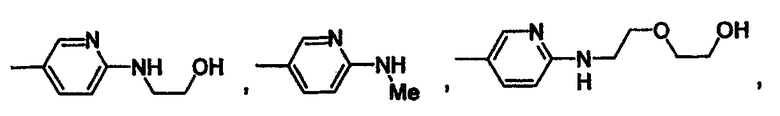
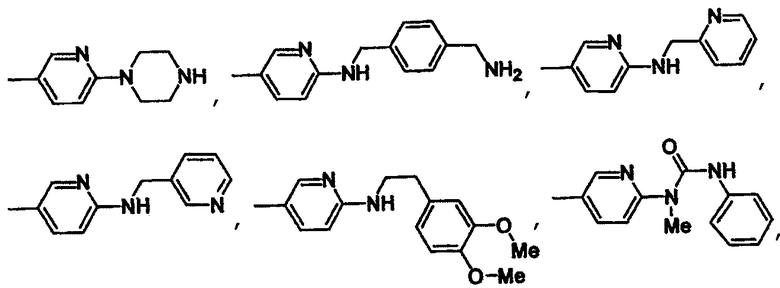
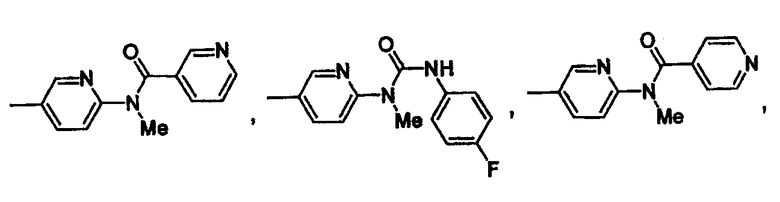
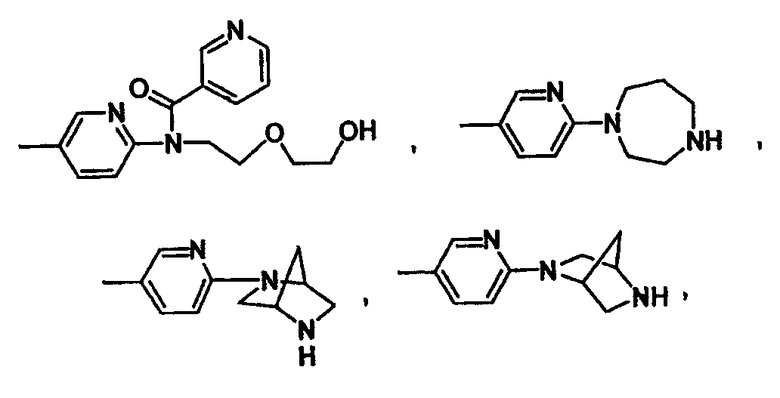
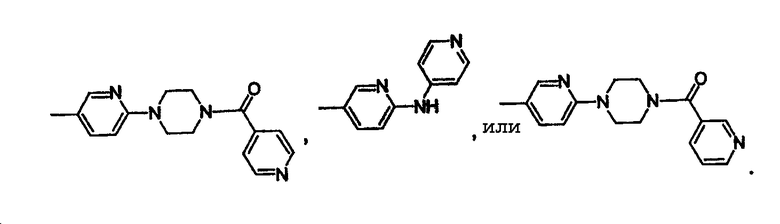
Еще одним конкретным значением для -X(Z1)n-Z является группа, имеющая формулу
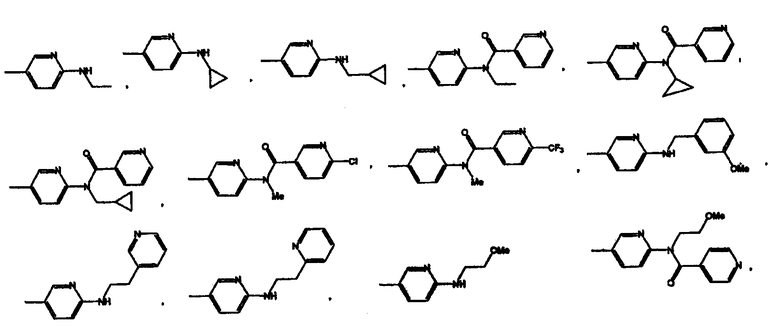
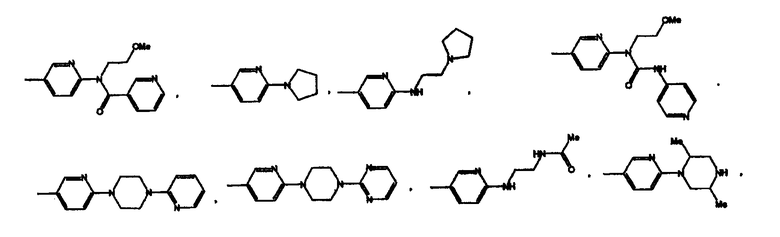
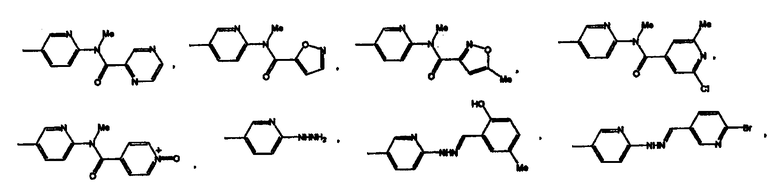
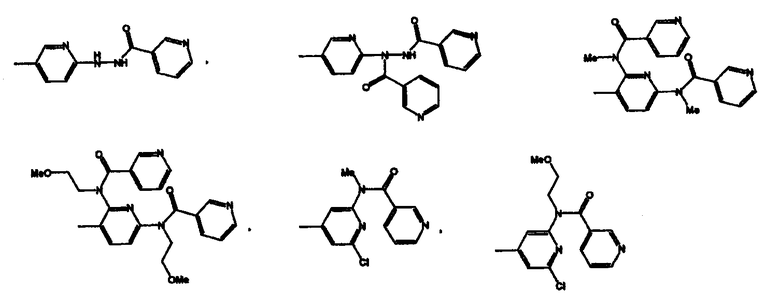
Конкретным значением для Z является -ОН, -О(С1-С4)алкил, -О(С6-С10)арил, -О(С6-С10)арил(С1-С4)алкил, -NR4R5, F, Cl, Br или I.
Еще одним конкретным значением для Z является -NR4R5.
Еще одним конкретным значением для Z является
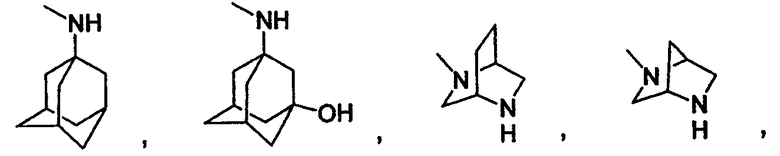
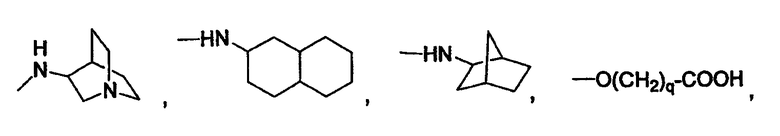
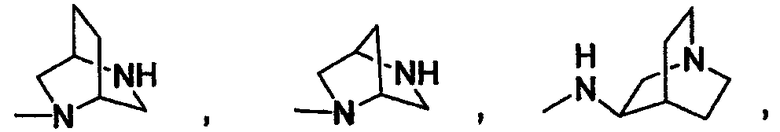
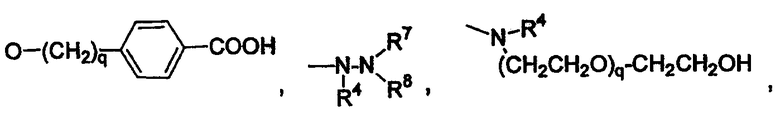
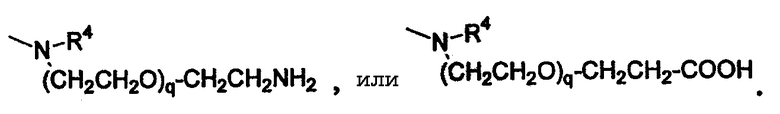
Конкретным значением для R4 является водород, (С1-С6)алкил, (С3-С6)циклоалкил, (С3-С8)циклоалкил(С1-С4)алкил-,
(С3-С6)гетероцикл, (С6-С10)арил, (С6-С10)арил(С1-С4)алкил-,
(С5-С6)гетероарил или (С5-С6)гетероарил(С1-С4)алкил-, -S(O)2-NH2,
-С(O)R6, -СО2R6 или -С(О)NR6R7.
Еще одним конкретным значением для R4 является водород,
(С1-С4)алкил, гидрокси(С2-С4)алкил, (С3-С6)циклоалкил,
(С6-С10)арил, (С7-С10)аралкил, (С5-С6)гетероарил,
-(СН2-СН2-О)q(СН2-СН2)-ORa, -(СН2-СН2-О)q(СН2-СН2)-COORa,
-(СН2-СН2-О)q(СН2-СН2)-NRaRb, -NR7R8, -С(O)R6, -СО2R6 или
-С(О)NR7R8.
Еще одним конкретным значением для R4 является водород, метил, этил, пропил, пентил, гидроксиэтил, гидроксипропил, этоксиэтил, диэтоксиэтил, метилбензил, аминометилбензил, метоксибензил, метоксифенетил, фурилметил, циклопропил, циклопропилметил, циклопентил, циклогексил, тиофенил, -С(O)R6, -СО2R6 или -С(О)NHR7.
Еще одним конкретным значением для R4 является метил, этил, циклопропил, циклопропилметил, -С(O)R6, -СО2R6 или -С(О)NHR7.
Конкретным значением для R5 является водород, (С1-С6)алкил,
(С3-С6)циклоалкил, (С3-С8)циклоалкил(С1-С4)алкил-,
(С3-С6)гетероцикл, (С6-С10)арил, (С6-С10)арил(С1-С4)алкил-,
(С5-С6)гетероарил или (С5-С6)гетероарил(С1-С4)алкил-, -S(O)2NH2,
-С(O)R6, -СО2R6 или -С(О)NR6R7.
Еще одним конкретным значением для R5 является водород,
(С1-С4)алкил, гидрокси(С2-С4)алкил, (С3-С6)циклоалкил,
(С6-С10)арил, (С7-С10)аралкил, (С5-С6)гетероарил,
-(СН2-СН2-О)q(СН2-СН2)-ORa, -(СН2-СН2-О)q(СН2-СН2)-COORa,
-(СН2-СН2-О)q(СН2-СН2)-NRaRb, -NR7R8, -С(O)R6, -СО2R6 или
-С(О)NR7R8.
Еще одним конкретным значением для R5 является водород, метил, этил, пропил, пентил, гидроксиэтил, гидроксипропил, этоксиэтил, диэтоксиэтил, метилбензил, аминометилбензил, метоксибензил, метоксифенетил, фурилметил, циклопропил, циклопропилметил, циклопентил, циклогексил, тиофенил, -С(O)R6, -СО2R6 или -С(О)NHR7.
Еще одним конкретным значением для R5 является метил, этил, циклопропил, циклопропилметил, -С(O)R6, -СО2R6 или -С(О)NHR7.
Конкретным значением для R4 и R5, взятыми вместе с атомом азота, к которому они присоединены, является пирролидильное, пиперидильное, пиперазинильное, азепинильное, диазепинильное, морфолинильное или тиоморфолинильное кольцо, каждое необязательно замещенное 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc.
Конкретным значением для R6 является (С1-С6)алкил,
(С3-С6)циклоалкил, (С3-С6)циклоалкил(С1-С4)алкил-,
(С3-С6)гетероцикл, (С6-С10)арил, (С6-С10)арил(С1-С4)алкил-,
(С5-С6)гетероарил или (С5-С6)гетероарил(С1-С4)алкил-, каждый необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, (С1-С8)алкила, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc.
Конкретным значением для R6 является (С6-С10)арил, (С5-С6)гетероарил, каждый необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, (С1-С8)алкила, галоген(C1-C8)алкила, -COORa и -C(O)NRbRc.
Конкретным значением для R6 является пиридил, необязательно замещенный F, Cl, Br, I, CF3, циано, нитро, -COORa или -CONHRа.
Еще одним конкретным значением для соединения является соединение, где R представляет водород, метил или этил; R1 и R2 представляют независимо метил, этил, аллил, пропаргил, изопропил, н-пропил, циклопропил, циклопропилметил, н-бутил; Х представляет 3-пиридил, замещенный в положении 6 заместителем Z, где Z представляет (C4-C10)гетероцикл или -NR4R5; R4 представляет метил, этил, циклопропил, циклопропилметил, и R5 представляет -С(О)R6, где R6 представляет гетероарил, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, галоген(C1-C8)алкила, -C(O)Ra, -COORa и -C(O)NRbRc, и где Ra, Rb и Rc представляют независимо водород, метил, этил, пропил, изопропил или циклопропил.
Соединения изобретения могут иметь формулу:
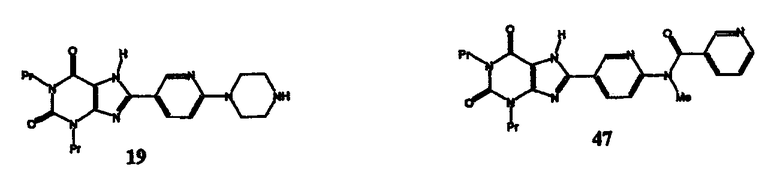

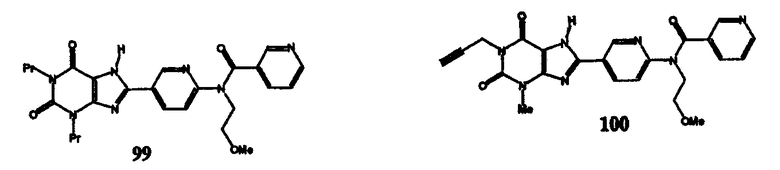
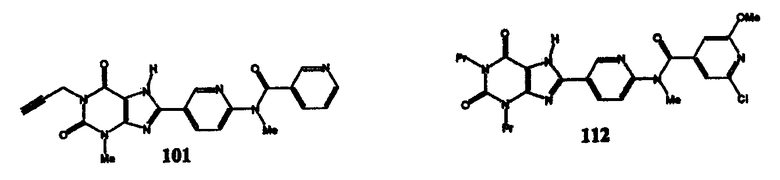
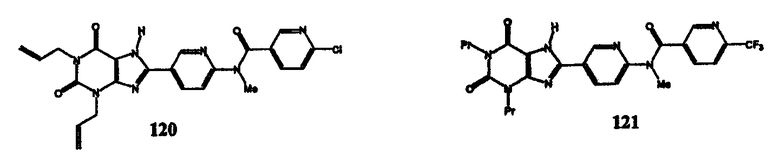

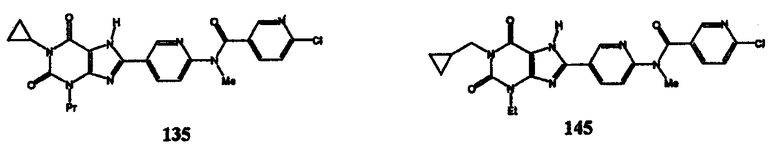
Аспекты изобретения:
настоящее изобретение предоставляет соединение формулы I:

в которой:
R представляет водород, (С1-С5)алкил, галоген(С1-С8)алкил, (С3-С5)алкенил или (С3-С5)алкинил;
R1 и R2 представляют независимо водород, (С1-С8)алкил,
(С3-С8)алкенил, (С3-С8)алкинил, (С1-С8)алкокси, (С3-С8)циклоалкил,
(С3-С8)циклоалкил(С1-С8)алкил-, (С4-С10)гетероцикл,
(С4-С10)гетероцикл(С1-С8)алкил-, (С6-С10)арил,
(С6-С10)арил(С1-С8)алкил-, (С5-С10)гетероарил или
(С5-С10)гетероарил(С1-С8)алкил-;
X представляет 5-10 членное гетероарильное кольцо, имеющее один атом азота и необязательно прерванное 1, 2 или 3 непероксидными окси (-O-), тио (-S-), сульфинильными (-SO-), сульфонильными (-S(O)2-) или аминными -N(R9)- группами;
Z представляет -OR3, -SR3, галоген, -S(O)m-NR4R5, -NR4R5 или (С4-С10)гетероцикл, в котором гетероцикл необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из галогена,
циано, нитро, -ORa, -SRa, (С1-С8)алкила, (С6-С10)арила,
-О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила,
галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc;
каждый Z1 представляет независимо (C1-C8)алкил,
(C2-C8)алкенил, (C2-C8)алкинил, -OR6, -SR6, галоген,
R6О(C1-C8)алкил, R7R8N(C1-C8)алкил, галоген(C1-C8)алкил, -NR7R8,
R7R8N(C1-C8)алкил, -С(O)R6, -COOR6 и -С(О)NR7R8;
R3 представляет (С1-С8)алкил, (С3-С8)алкенил, (С3-С8)алкинил, (С6-С10)арил, (С6-С10)арил(С1-С8)алкил-, (С5-С10)гетероарил, (С5-С10)гетероарил(С1-С8)алкил-, -С(O)R6 или -С(О)NR7R8;
R4 и R5 представляют независимо водород, (С1-С8)алкил,
(С3-С8)алкенил, (С3-С8)алкинил, (С1-С8)алкокси, (С3-С8)циклоалкил,
(С3-С8)циклоалкил(С1-С8)алкил-, (С6-С18)полициклоалкил,
(С6-С18)полициклоалкил(С1-С8)алкил-, (С3-С10)гетероцикл,
(С3-С10)гетероцикл(С1-С8)алкил-, -NR7R8, (С6-С10)арил,
(С6-С10)арил(С1-С8)алкил-, (С5-С10)гетероарил,
(С5-С10)гетероарил(С1-С8)алкил-, -(C2-C4-Y)q-(CH2)2-4-X1, -С(O)R6,
-СО2R6, -С(О)NR7R8 или -S(O)2-NR7R8; или R4 и R5 вместе с атомами, к которым они присоединены, образуют насыщенное или частично ненасыщенное, моно-, бициклическое- или ароматическое кольцо, имеющее 3, 4, 5, 6, 7 или 8 кольцевых атомов и необязательно содержащее 1, 2, 3 или 4 гетероатома, выбранных из непероксидного окси (-O-), тио (-S-), сульфинила (-SO-), сульфонила (-S(O)2-) и амина -N(R9)- в кольце, и где кольцо необязательно замещено 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc;
Х1 представляет -OR6, -С(O)R6, -СО2R6 или -NR7R8; и Y представляет окси (-O-), тио (-S-), сульфинил (-SO-), сульфонил (-S(O)2-) и амин -N(R9)-;
где алкильная, алкенильная, циклоалкильная, алкинильная, арильная, гетероциклическая или гетероарильная группы из R1, R2, R3, R4 и R5 групп необязательно замещены одним или более заместителями, выбранными независимо из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc;
где R6 представляет водород, (С1-С8)алкил, RaО(С1-С8)алкил,
RbRcN(C1-C8)алкил, галоген(C1-C8)алкил, (С3-С10)гетероцикл,
(С3-С10)гетероцикл(С1-С8)алкил-,
(С6-С10)арил,(С6-С10)арил(С1-С8)алкил-, (С4-С10)гетероарил,
(С4-С10)гетероарил(С1-С8)алкил-; где гетероцикл, гетероарил или
арил необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc;
где R7, R8 и R9 представляют независимо водород, (С1-С8)алкил, RaО(С1-С8)алкил, RbRcN(C1-C8)алкил, галоген(C1-C8)алкил, (С3-С10)гетероцикл, (С6-С10)арил, (С6-С10)арил(С1-С8)алкил-, (С4-С10)гетероарил, -COORa, -C(O)Ra или C(O)NRbRc; где гетероцикл, гетероарил или арил необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc; или R7 и R8 вместе с атомами, к которым они присоединены, образуют насыщенное или частично ненасыщенное, моно-, бициклическое- или ароматическое кольцо, имеющее 3, 4, 5, 6, 7 или 8 кольцевых атомов, причем кольцо необязательно имеет от 4 до восьми кольцевых атомов и необязательно содержит 1, 2, 3 или 4 гетероатома, выбранных из непероксидного окси (-O-), тио (-S-), сульфинила (-SO-), сульфонила (-S(O)2-) или амина -N(Rb)- в кольце;
Rа представляет водород или (С1-С6)алкил; Rb и Rс каждый независимо представляет водород, (С1-С6)алкил, (С1-С6)алкокси, (С3-С8)циклоалкил, (С1-С6)алкилтио, (С6-С10)арил, (С6-С10)арил(С1-С6)алкил-, гетероарил или гетероарил(С1-С6)алкил-; или Rb и Rс вместе с азотом, к которому они присоединены, образуют пирролидильное, пиперидильное, пиперазинильное, азепинильное, диазепинильное, морфолинильное или тиоморфолинильное кольцо; и
где n равно 0, 1, 2, 3, 4, 5, 6, 7 или 8; m равно 1 или 2; и q равно 1, 2, 3 или 4; или его фармацевтически приемлемую соль.
Согласно одному аспекту изобретения R представляет водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, н-бутил, изобутил или галоген(С1-С4)алкил. Согласно еще одному аспекту R представляет водород, метил, этил, -СН2-СН2-Cl, -СН2-СН2-Br или -СН2-СН2-СН2-F. В одном из вариантов R представляет водород.
Согласно одному аспекту изобретения предоставляется указанное выше соединение, где R1 представляет водород, (С1-С4)алкил, (С3-С4)алкенил, (С3-С4)алкинил, фенил или фенил(С1-С4)алкил. Согласно еще одному аспекту R1 представляет (С3-С6)циклоалкил и (С3-С6)циклоалкил(С1-С4)алкил-. В одном из вариантов R1 представляет циклопропил или циклопропилметил. В еще одном варианте R1 представляет водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, н-бутил, изобутил, фенил, фенетил, бензил или (метоксифенил)этил. В еще одном варианте R1 представляет этил, н-пропил или аллил.
Согласно одному аспекту изобретения предоставляется указанное выше соединение, где R2 представляет водород, (С1-С4)алкил, (С3-С4)алкенил, (С3-С4)алкинил, фенил, фенил(С1-С4)алкил или (метоксифенил)этил. В одном варианте R2 представляет (С3-С6)циклоалкил или (С3-С6)циклоалкил(С1-С4)алкил-. В еще одном варианте R2 представляет циклопропил или циклопропилметил. В еще одном варианте R2 представляет водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, н-бутил, изобутил, фенил, фенетил или бензил. В еще одном варианте R2 представляет этил, н-пропил или аллил.
Согласно одному аспекту изобретения предоставляется вышеуказанное соединение, где Z представляет -ОН, -О(С1-С4)алкил, -О(С6-С10)арил, -О(С6-С10)арил(С1-С4)алкил, -NR4R5, F, Cl, Br или I.
Согласно еще одному аспекту изобретения предоставляется вышеуказанное соединение, где R4 представляет водород,
(С1-С6)алкил, (С3-С6)циклоалкил, (С3-С6)циклоалкил(С1-С4)алкил-,
(С3-С6)гетероцикл, (С6-С10)арил, (С6-С10)арил(С1-С4)алкил-,
(С5-С6)гетероарил или (С5-С6)гетероарил(С1-С4)алкил-, -S(O)2-NH2,
-С(O)R6, -СО2R6 или -С(О)NR6R7. В одном из вариантов R4 представляет водород, (С1-С4)алкил, гидрокси(С2-С4)алкил, (С3-С6)циклоалкил, (С6-С10)арил, (С7-С10)аралкил, (С5-С6)гетероарил, -(СН2-СН2-О)q(СН2-СН2)-ORa, -(СН2-СН2-О)q(СН2-СН2)-COORa, -(СН2-СН2-О)q(СН2-СН2)-NRaRb, -NR7R8, -С(O)R6, -СО2R6 или -С(О)NR7R8. В еще одном варианте R4 представляет водород, метил, этил, пропил, пентил, гидроксиэтил, гидроксипропил, этоксиэтил, диэтоксиэтил, метилбензил, аминометилбензил, метоксибензил, метоксифенетил, фурилметил, циклопропил, циклопропилметил, циклопентил, циклогексил, тиофенил, -С(O)R6, -СО2R6 или -С(О)NHR7. В еще одном варианте R4 представляет метил, этил, циклопропил, циклопропилметил, -С(O)R6, -СО2R6 или -С(О)NHR7.
Согласно еще одному аспекту изобретения предоставляется вышеуказанное соединение, где R5 представляет водород, (С1-С6)алкил, (С3-С6)циклоалкил, (С3-С6)циклоалкил(С1-С4)алкил-, (С3-С6)гетероцикл, (С6-С10)арил, (С6-С10)арил(С1-С4)алкил-, (С5-С6)гетероарил или (С5-С6)гетероарил(С1-С4)алкил-, -S(O)2NH2, -С(O)R6, -СО2R6 или -С(О)NR6R7. В одном варианте R5 представляет водород, (С1-С4)алкил, гидрокси(С2-С4)алкил, (С3-С6)циклоалкил, (С6-С10)арил, (С7-С10)аралкил, (С5-С6)гетероарил, -(СН2-СН2-О)q(СН2-СН2)-ORa, -(СН2-СН2-О)q(СН2-СН2)-COORa, -(СН2-СН2-О)q(СН2-СН2)-NRaRb, -NR7R8, -С(O)R6, -СО2R6 или -С(О)NR7R8. В еще одном варианте R5 представляет водород, метил, этил, пропил, пентил, гидроксиэтил, гидроксипропил, этоксиэтил, диэтоксиэтил, метилбензил, аминометилбензил, метоксибензил, метоксифенетил, фурилметил, циклопропил, циклопропилметил, циклопентил, циклогексил, тиофенил, -С(O)R6, -СО2R6 или -С(О)NHR7. В еще одном варианте R5 представляет метил, этил, циклопропил, циклопропилметил, -С(O)R6, -СО2R6 или -С(О)NHR7.
Согласно одному аспекту изобретения предоставляется вышеуказанное соединение, где R4 и R5, взятые вместе с атомом азота, к которому они присоединены, представляют пирролидильное, пиперидильное, пиперазинильное, азепинильное, диазепинильное, морфолинильное или тиоморфолинильное кольцо, каждое необязательно замещенное 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc.
Согласно еще одному аспекту изобретения предоставляется вышеуказанное соединение, где R6 представляет (С1-С6)алкил,
(С3-С6)циклоалкил, (С3-С6)циклоалкил(С1-С4)алкил-,
(С3-С6)гетероцикл, (С6-С10)арил, (С6-С10)арил(С1-С4)алкил-,
(С5-С6)гетероарил или (С5-С6)гетероарил(С1-С4)алкил-, каждый необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, (С1-С8)алкила, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc. В одном варианте R6 представляет (С6-С10)арил, (С5-С6)гетероарил, каждый необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, (С1-С8)алкила, галоген(C1-C8)алкила, -COORa и -C(O)NRbRc. В еще одном варианте R6 представляет пиридил, необязательно замещенный F, Cl, Br, I, CF3, циано, нитро, -COORa или CONHRа.
Еще одним конкретным значением для соединения является соединение, где R представляет водород, метил или этил; R1 и R2 представляют независимо метил, этил, аллил, пропаргил, изопропил, н-пропил, циклопропил, циклопропилметил или н-бутил; Х представляет 3-пиридил, замещенный в положении 6 заместителем Z, где Z представляет (C4-C10)гетероцикл или -NR4R5; R4 представляет метил, этил, циклопропил, циклопропилметил, и R5 представляет -С(О)R6, где R6 представляет гетероарил, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, галоген(C1-C8)алкила, -C(O)Ra, -COORa и -C(O)NRbRc, и где Ra, Rb, и Rc представляют независимо водород, метил, этил, пропил, изопропил или циклопропил.
Согласно еще одному аспекту изобретения предоставляется вышеуказанное соединение, где R представляет водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, н-бутил, изобутил или галоген(С1-С4)алкил; R1 и R2 представляют независимо водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, циклопропил, циклопропилметил, н-бутил, изобутил, фенил, фенетил или бензил. В одном из вариантов R представляет водород, метил, этил, -СН2-СН2-Cl, -СН2-СН2-Br или -СН2-СН2-СН2-F; и R1 и R2 представляют независимо водород, метил, этил, аллил, пропаргил, изопропил, н-пропил, циклопропил, циклопропилметил или (метоксифенил)этил.
Согласно одному аспекту изобретения предоставляется указанное выше соединение, где Х представляет имидазолил, триазолил, триазинил, оксазоил, изоксазоил, тиазолил, изотиазолил, тиодиазолил, пирролил, пиразинил, татразолил, пиридинил, пиримидинил, индолил, изохинолил или хинолил, каждый необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена, циано, нитро, (С1-С8)алкила, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc. В одном из вариантов, приведенных выше, Х представляет 2-пиридинил, 3-пиридинил или 4-пиридинил, каждый необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, (С1-С8)алкила, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc. Согласно еще одному варианту -X(Z1)n-Z имеет формулу:
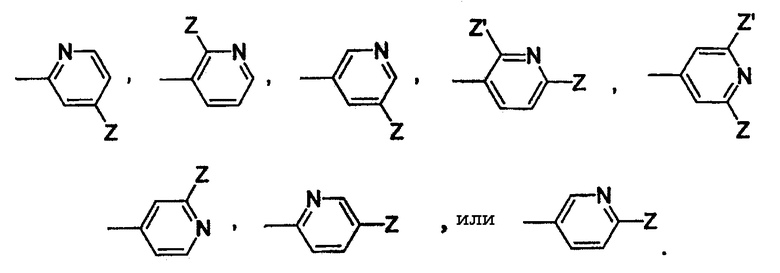
Согласно еще одному варианту -X(Z1)n-Z имеет формулу
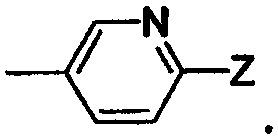
Согласно одному аспекту изобретения предоставляется указанное выше соединение, где Z представляет -ОН, -О(С1-С4)алкил, -ОС(О)NR7R8, (С1-С4)алкил, -NR4R5, F, Cl, Br или I, в котором R4 и R5 представляют независимо водород, (С1-С6)алкил, (С3-С6)циклоалкил, (С3-С6)гетероцикл, (С6-С10)арил, (С7-С12)аралкил, (С5-С6)гетероарил или (С5-С6)гетероарил(С1-С4)алкил-, -S(O)2-NH2, -С(O)R6, -СО2R6 или -С(О)NR6R7. В одном из вариантов Z представляет -NR4R5.
Согласно одному аспекту изобретения предоставляется указанное выше соединение, где R4 и R5 вместе с атомом азота, к которому они присоединены, образуют пирролидильное, пиперидильное, пиперазинильное, азепинильное, диазепинильное, морфолинильное или тиоморфолинильное кольцо, где кольцо необязательно замещено 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc. В одном из вариантов, приведенных выше, R4 и R5 представляют независимо водород, (С1-С4)алкил, гидрокси(С2-С4)алкил, (С3-С6)циклоалкил, (С6-С10)арил, (С7-С10)аралкил, (С5-С6)гетероарил, -(СН2-СН2-О)q(СН2-СН2)-ORa, -(СН2-СН2-О)q(СН2-СН2)-COORa, -(СН2-СН2-О)q(СН2-СН2)-NRaRb, -NR7R8, -С(O)R6, -СО2R6 или -С(О)NR7R8. Согласно еще одному из вариантов R4 и R5 представляют независимо водород, метил, этил, пропил, пентил, гидроксиэтил, гидроксипропил, этоксиэтил, диэтоксиэтил, метилбензил, аминометилбензил, метоксибензил, метоксифенетил, фурилметил, циклопентил, циклогексил, тиофенил, -С(O)R6, -СО2R6 или -С(О)NHR7. Согласно еще одному из вариантов R6 представляет метил, метокси или пиридил, и R7 представляет фенил, фторфенил или метоксифенил.
Согласно одному аспекту изобретения предоставляется указанное выше соединение, где R представляет водород, метил или этил; R1 и R2 представляют независимо метил, этил, аллил, пропаргил, изопропил, н-пропил, циклопропил, циклопропилметил, н-бутил, изобутил; и Z представляет (C4-C10)гетероцикл, где гетероцикл необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, циано, нитро, -ORa, -SRa, (С6-С10)арила, -О(С6-С10)арила, гидрокси(С1-С8)алкила, RbRcN(C1-C8)алкила, галоген(C1-C8)алкила, -NRbRc, -C(O)Ra, -COORa и -C(O)NRbRc.
Согласно одному аспекту изобретения предоставляется указанное выше соединение, где Z выбран из группы, состоящей из:




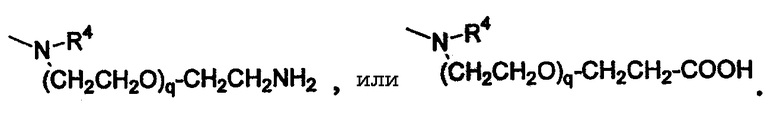
В одном из вариантов, приведенных выше, -X(Z1)n-Z выбран из группы, состоящей из:





В другом варианте, R1 и R2 представляют н-пропил; R представляет водород и n равно нулю.
Согласно одному аспекту изобретения предоставляется указанное выше соединение, где -X(Z1)n-Z выбран из группы, состоящей из:
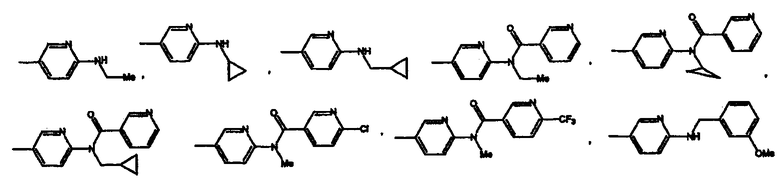
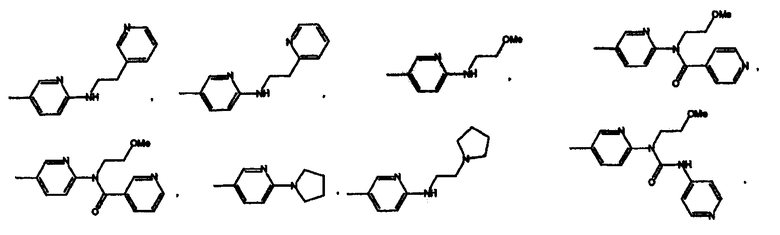
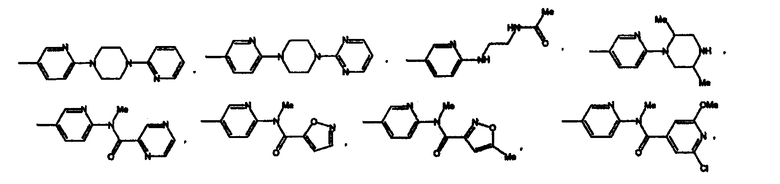

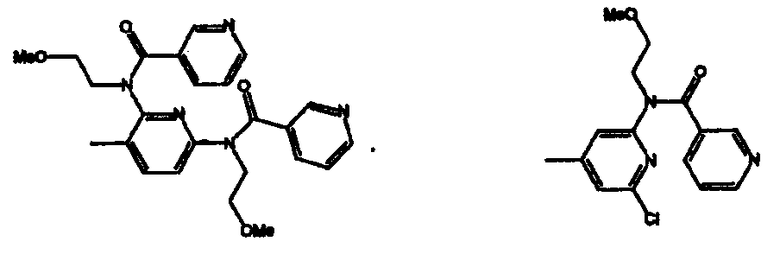
В одном аспекте изобретения, предоставляется соединение, выбранное из группы состоящей из:
или их фармацевтически приемлемых солей, необязательно в виде отдельного стереоизомера или смеси стереоизомеров.
В одном аспекте изобретения предоставляется фармацевтическая композиция, содержащая: (а) терапевтически эффективное количество соединения, описанного выше; и (b) фармацевтически приемлемый эксципиент. В другом аспекте предоставляется фармацевтическая композиция, содержащая: (а) терапевтически эффективное количество соединения выше; и (b) фармацевтически приемлемый эксципиент.
В одном из аспектов изобретения предоставляется терапевтический способ профилактики или лечения патологического состояния или симптома у млекопитающих, при котором вовлечена активность аденозиновых А2В рецепторов и желателен антагонизм их действия, включающий введение млекопитающему эффективного количества соединения настоящего изобретения. Согласно еще одному аспекту предоставляется способ лечения астмы, аллергии, аллергических заболеваний или аутоиммунных заболеваний, включающий введение млекопитающему, нуждающемуся в таком лечении, эффективного количества соединения настоящего изобретения.
Согласно еще одному аспекту предоставляется способ лечения диарейных заболеваний, устойчивости к инсулину, диабета, рака, ишемических/реперфузионных повреждений, диабетической ретинопатии или ретинопатии, вызванной гипербарическим кислородом, включающий введение млекопитающему, нуждающемуся в таком лечении, эффективного количества соединения настоящего изобретения или его фармацевтически приемлемой соли. Согласно еще одному аспекту предоставляется терапевтический способ профилактики или лечения патологического состояния или симптома у млекопитающих, при котором вовлечена активность аденозиновых А2В рецепторов и желателен антагонизм их действия, включающий введение млекопитающему эффективного количества соединения настоящего изобретения.
Согласно еще одному аспекту предоставляется соединение настоящего изобретения для применения в терапевтической медицине. Согласно еще одному аспекту предоставляется применение соединения изобретения для производства лекарственных средств, полезных при лечении заболеваний у млекопитающих, таких как человек.
Вполне понятно, что любой аспект или признак настоящего изобретения, характеризуется ли он или не характеризуется как предпочтительный, может сочетаться с любым другим аспектом или признаком изобретения независимо от того, характеризуется ли он или не характеризуется как предпочтительный. Например, аспект или признак, описанный как предпочтительный, например конкретная R группа или конкретная R1 группа для конкретного соединения формулы I (например, в которой R1 представляет водород, (С1-С5)алкил, галоген(С1-С8)алкил, (С3-С5)алкенил или (С3-С5)алкинил) может сочетаться с любыми другими группами, такими как R2, X, Z, Z1 и др., образуя соединение изобретения, имеющее различное сочетание заместителей, без отклонения от настоящего изобретения.
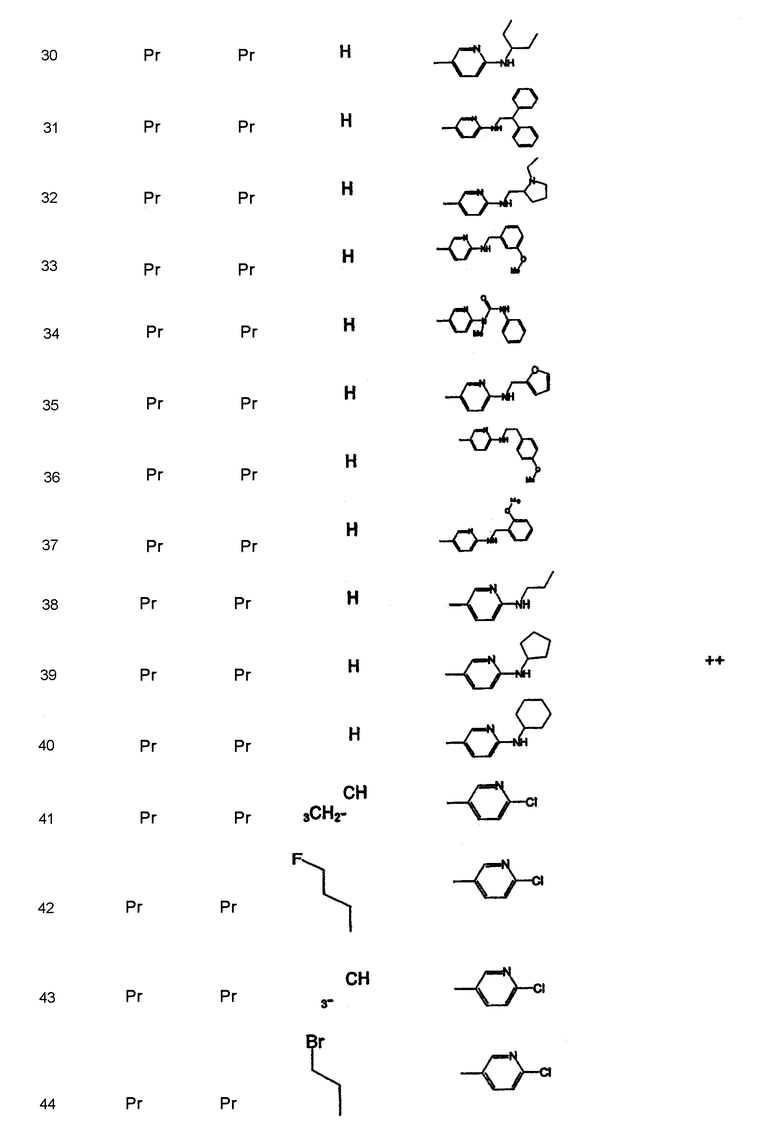
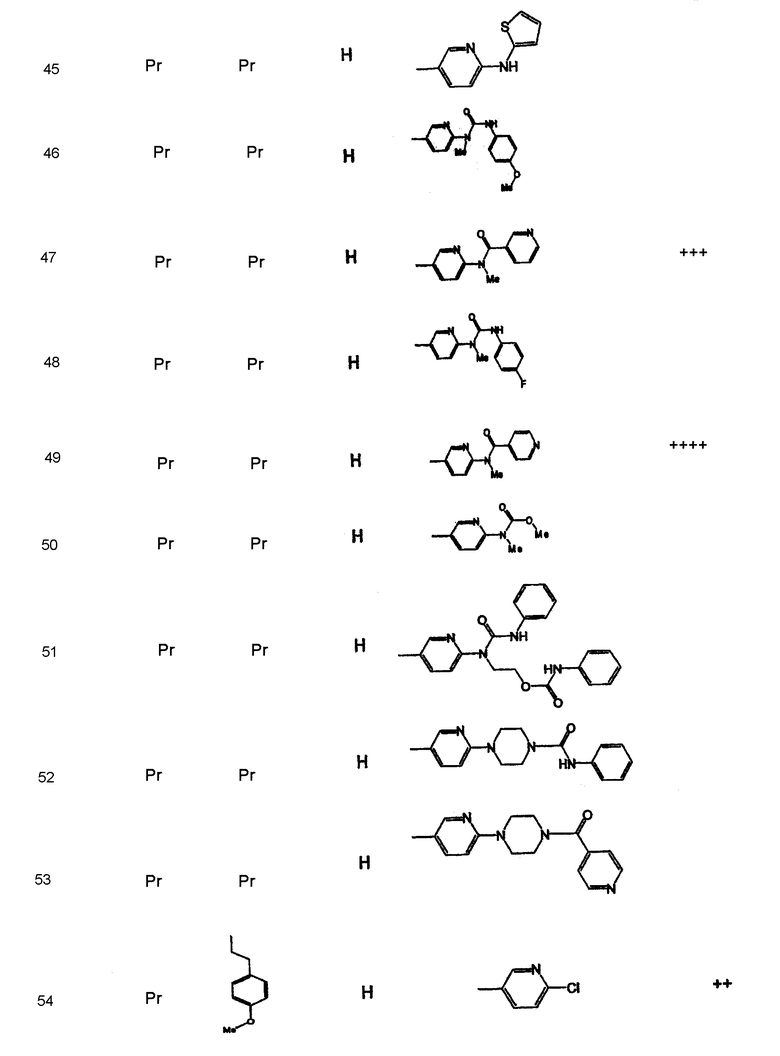
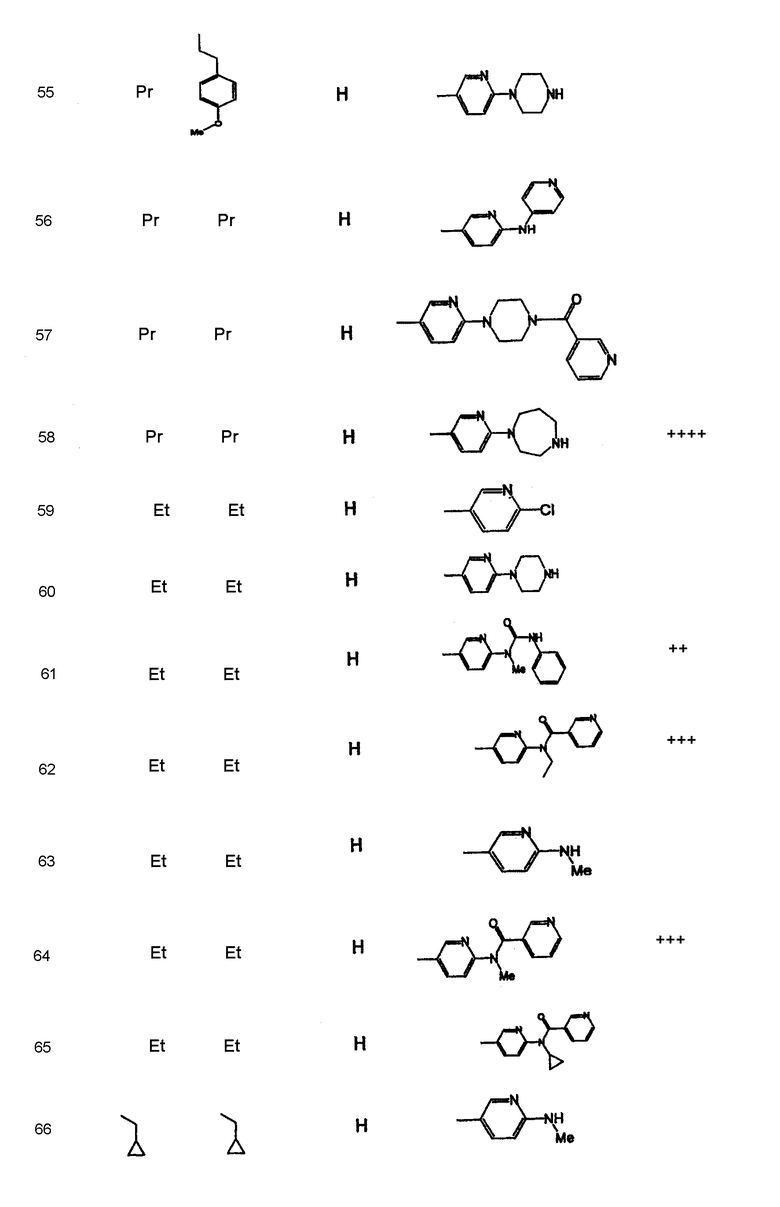
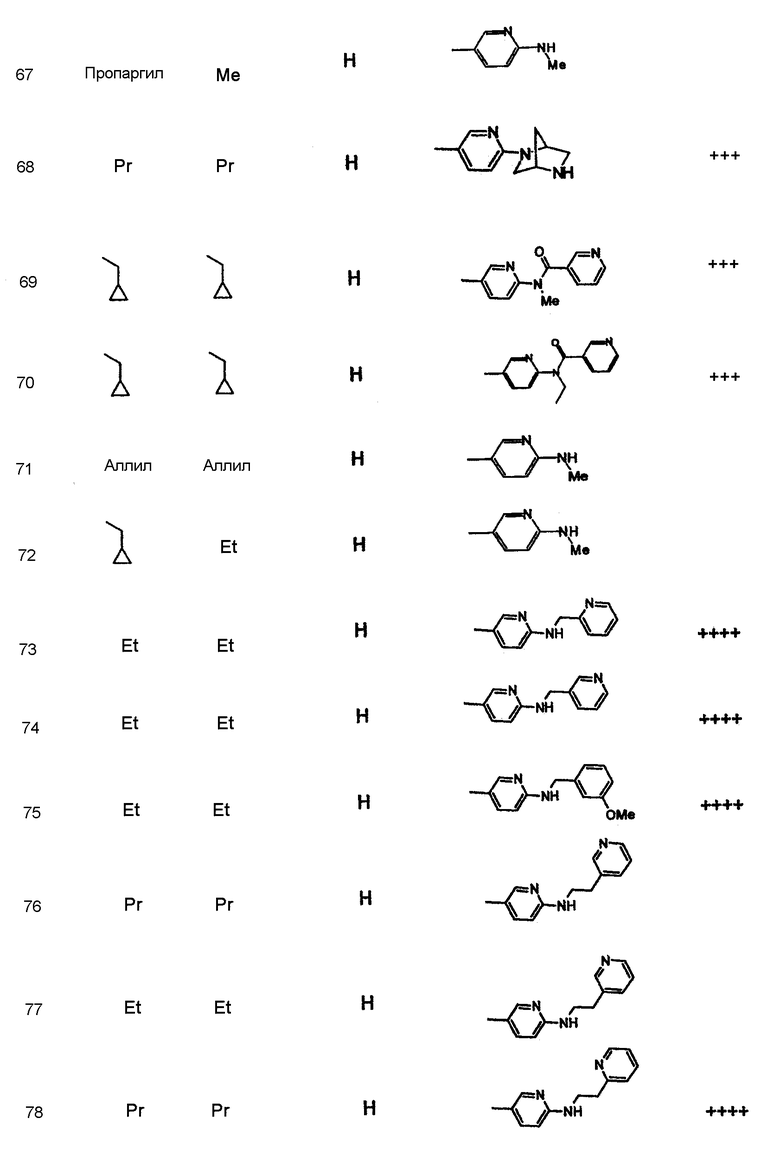
Дополнительные соединения полезные для осуществления изобретения на практике представлены в приведенной ниже таблице:
Активность А2в антагониста
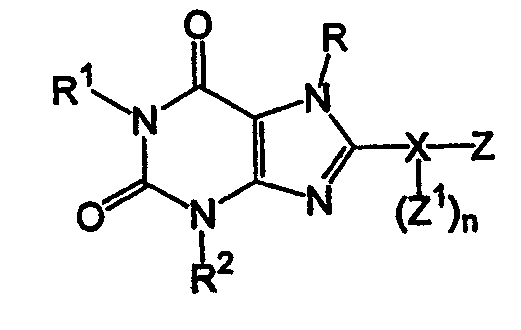
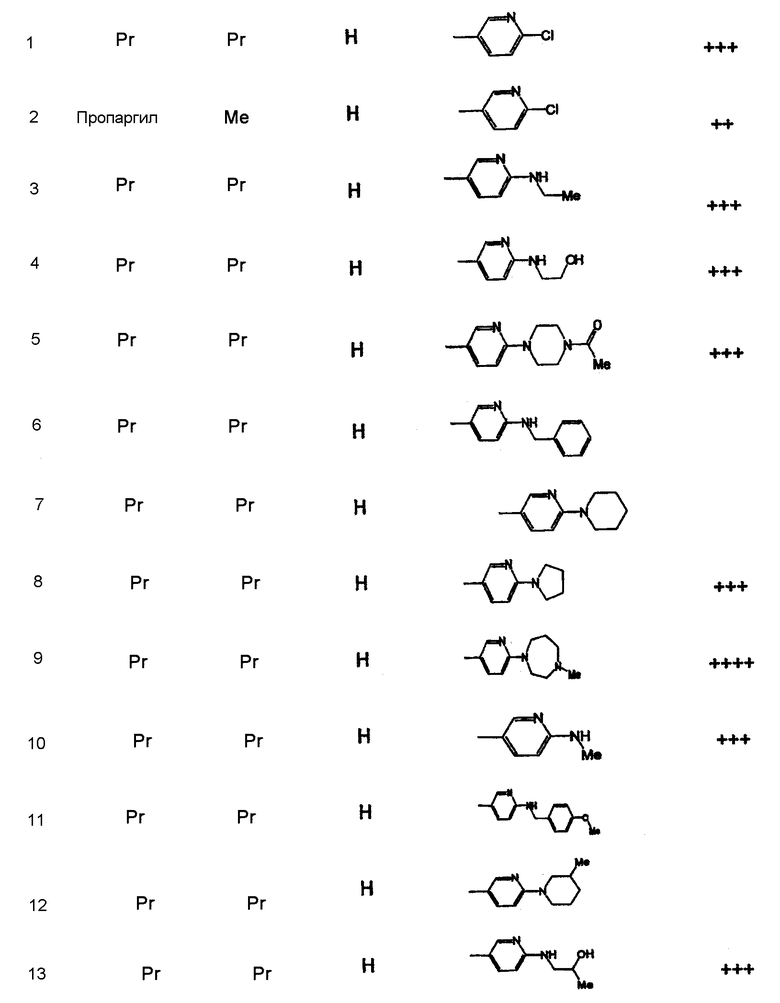
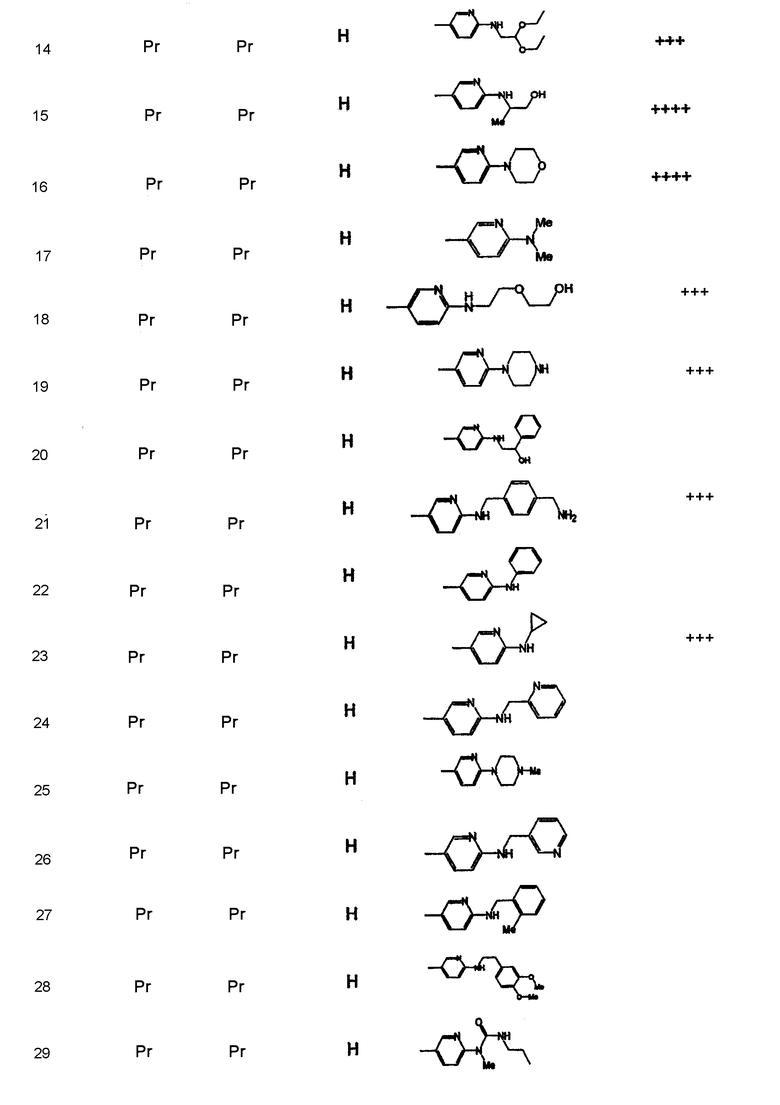
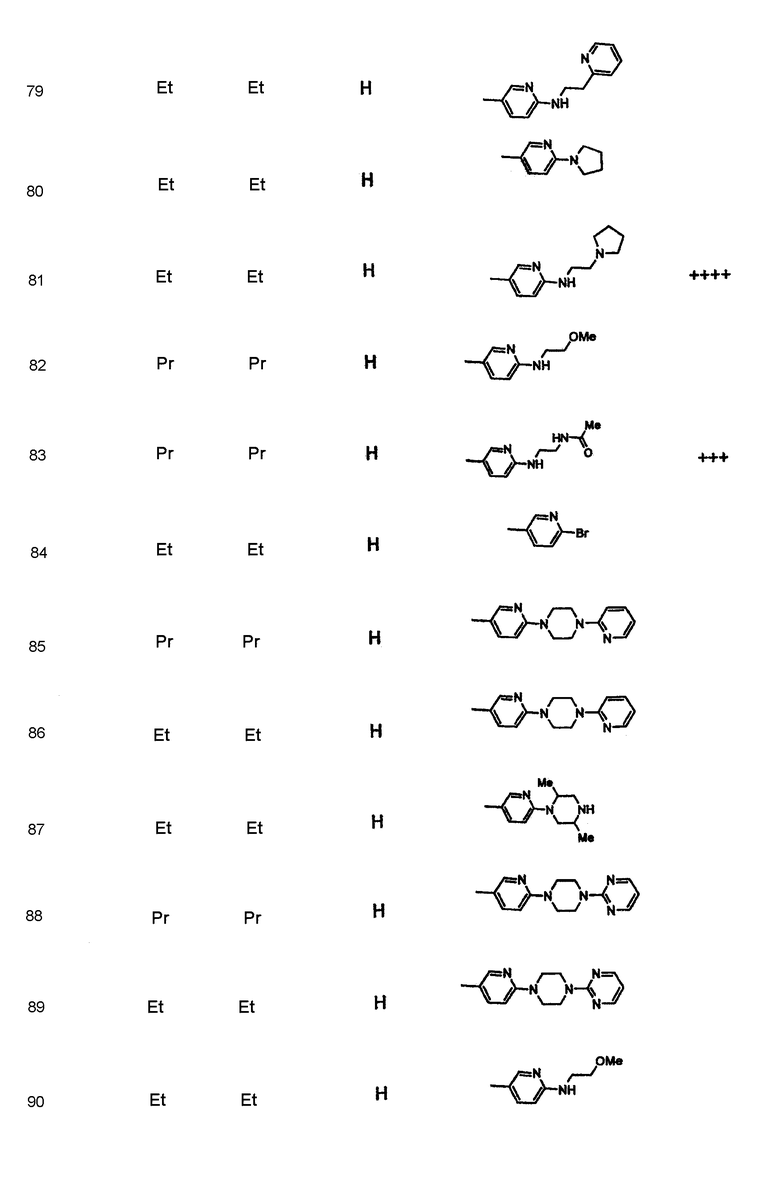
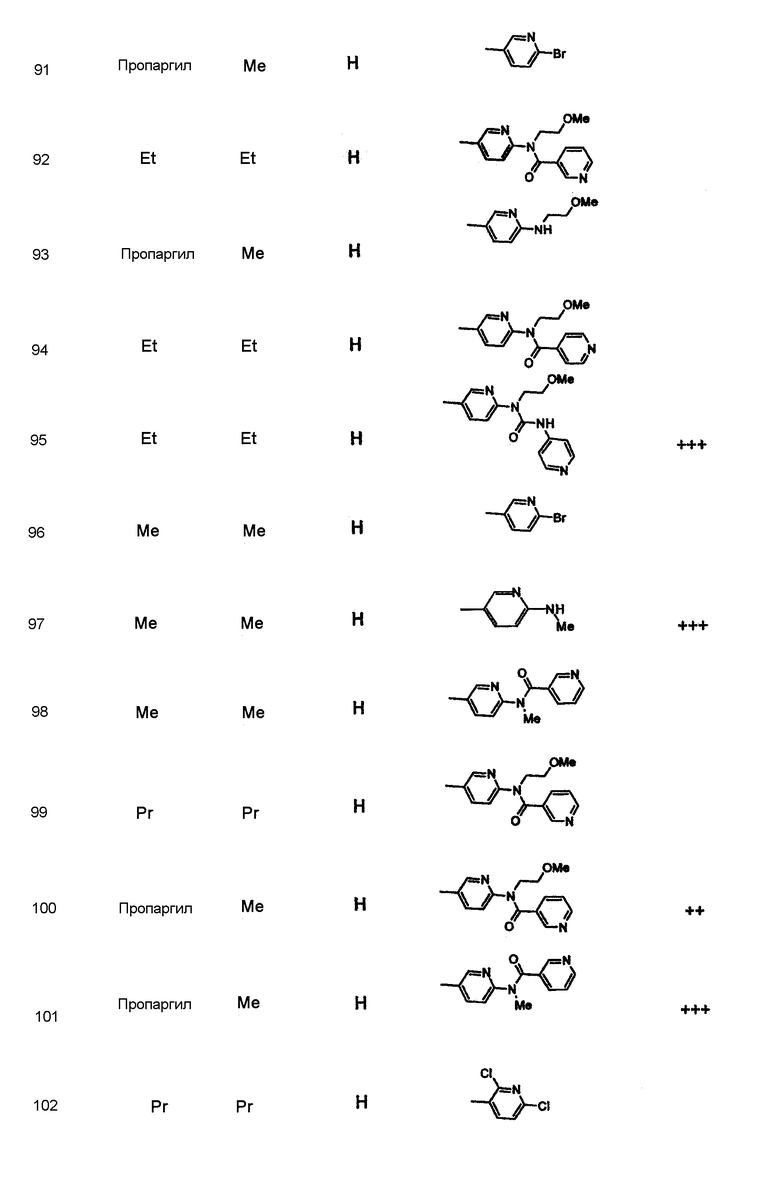
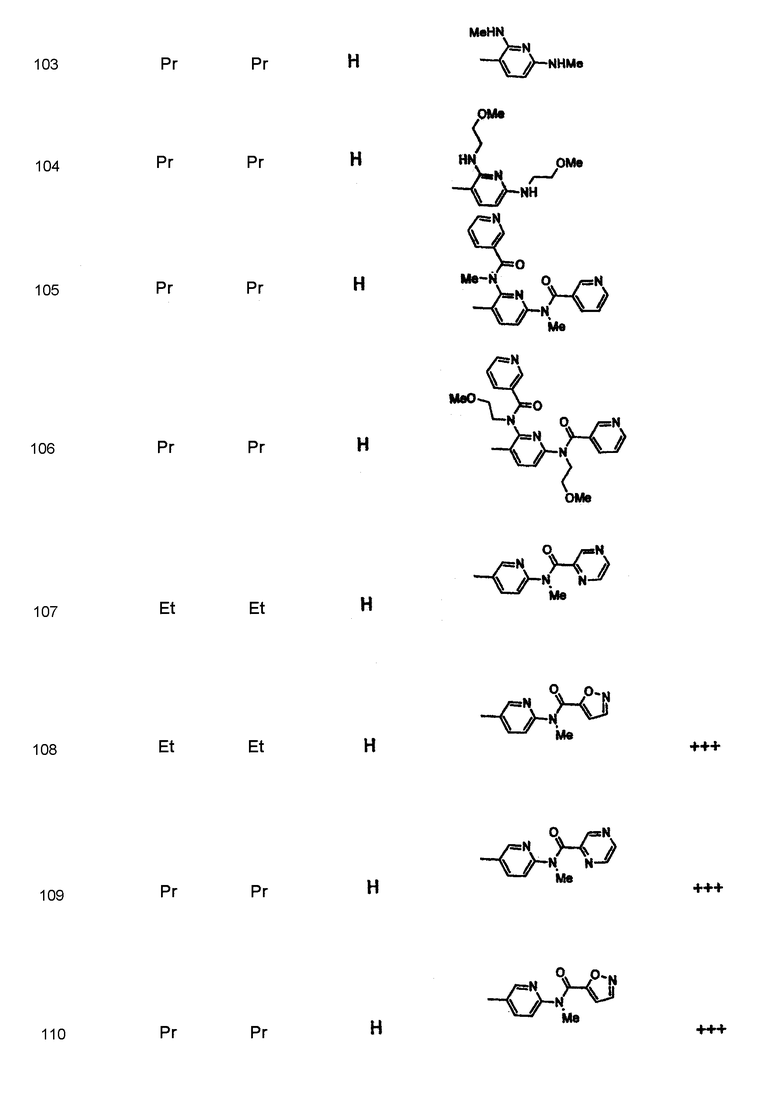
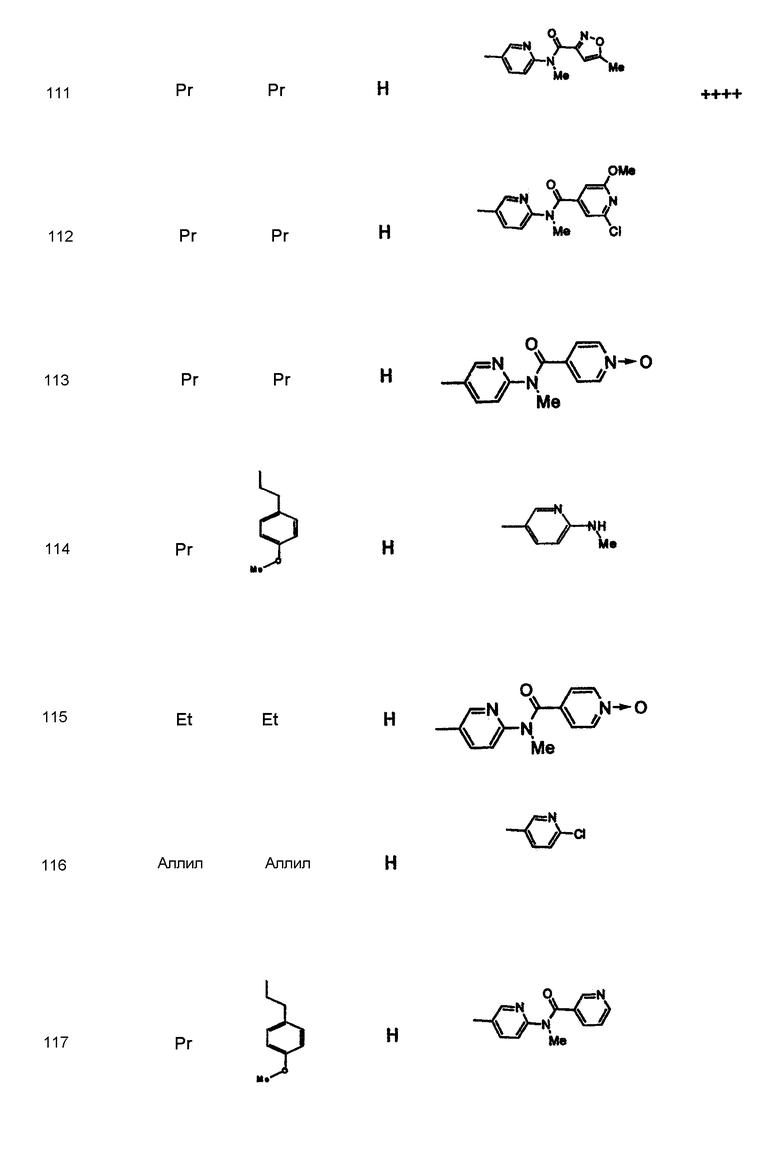
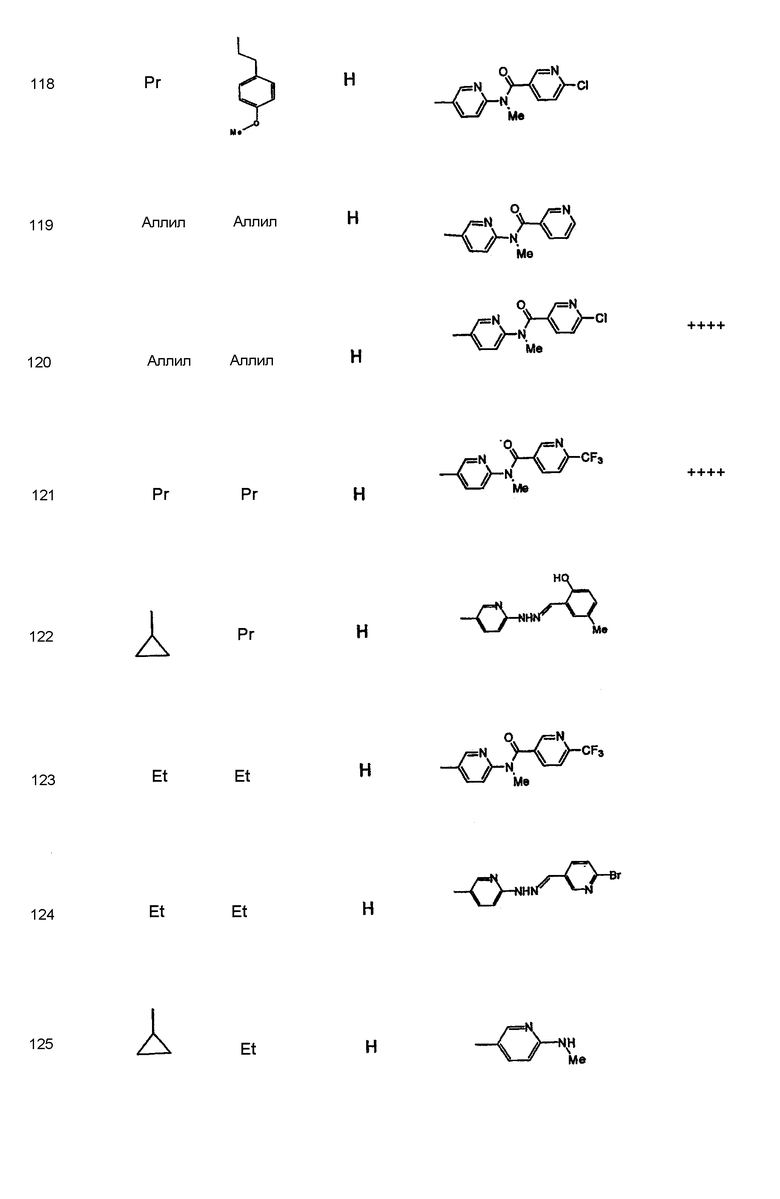
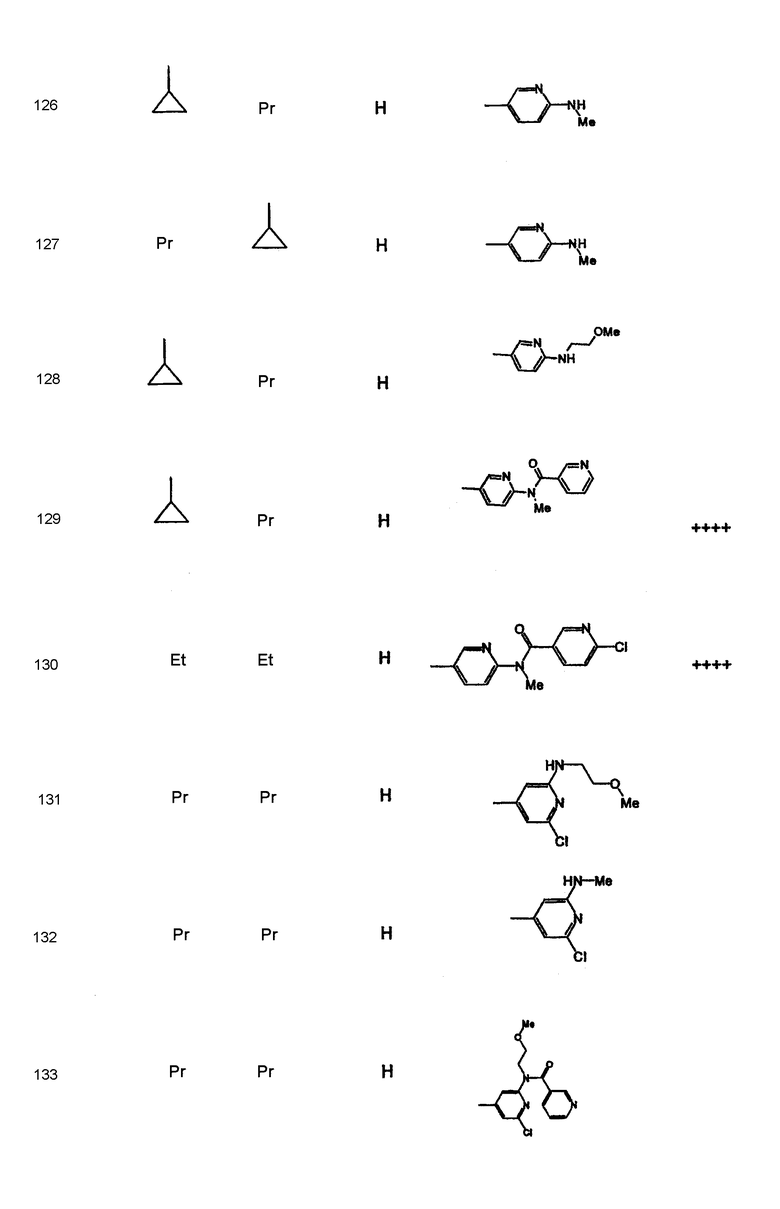
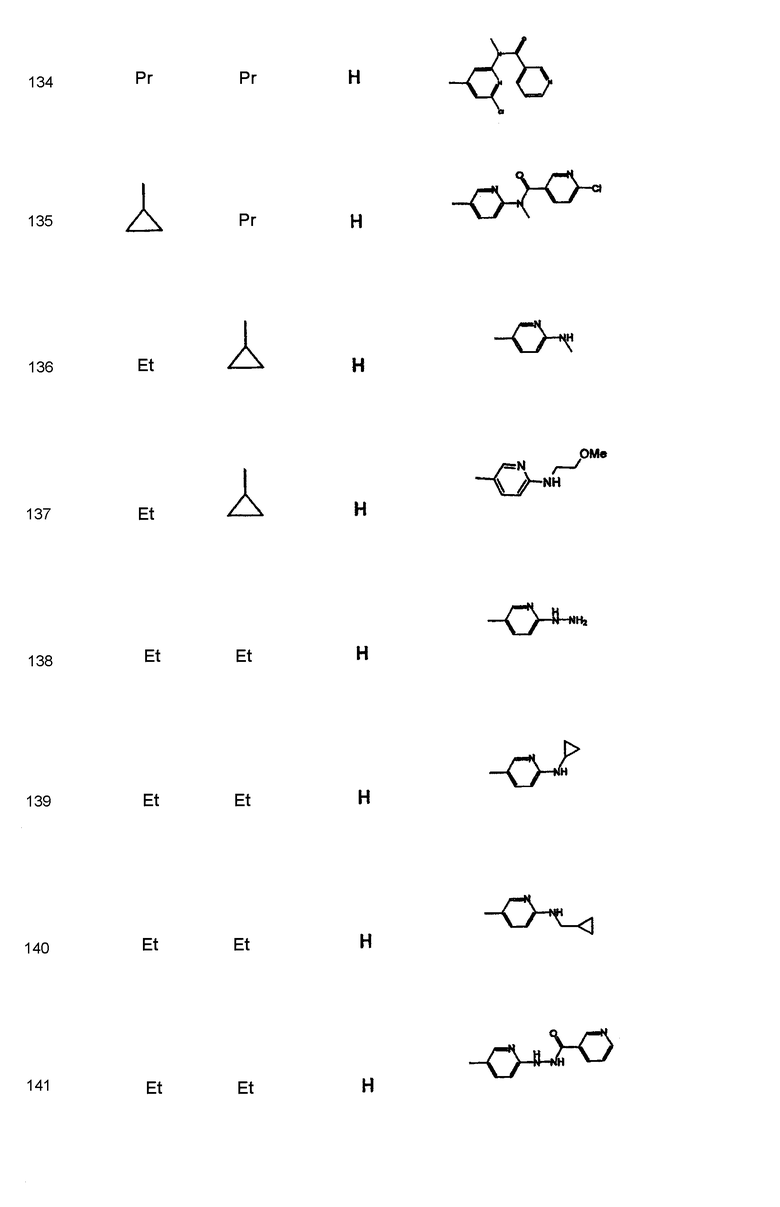
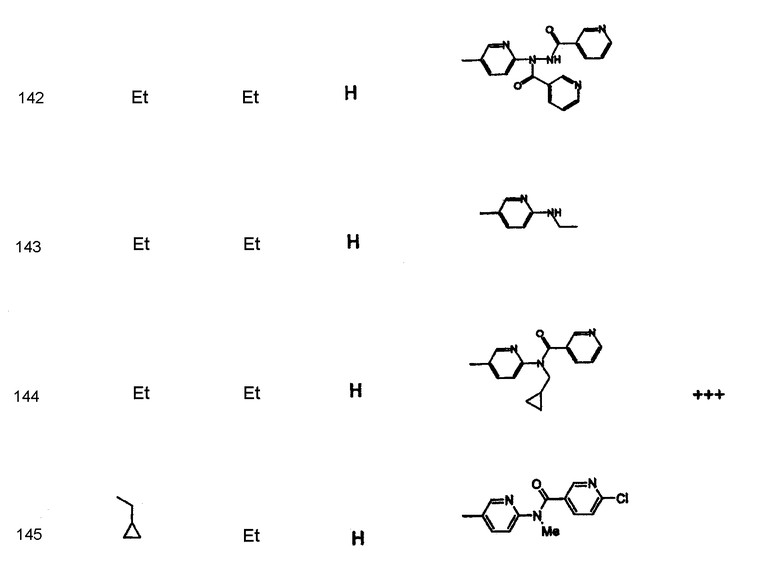
Синтез соединений формулы I
Соединения формулы IA могут быть получены с помощью способов, описанных в P.J. Scammells, et al., J. Med. Chem. 37, 2704-2712 (1994). Диамино-1,3-дизамещенный урацил ацилируют 6-хлорникотиноилхлоридом в пиридине при 5°С с получением соединений формулы (5а). Полученный в результате амид (5а) циклизуют при кипячении с обратным холодильником в водном растворе гидроксида натрия с получением соединения IA. 6-Хлорникотиноилхлорид получают кипячением с обратным холодильником 6-гидроксиникотиновой кислоты в тионилхлориде с использованием ДМФА в качестве катализатора, как показано на схеме реакций 1.
Соединение IA можно алкилировать алкилбромидом или йодидом с получением соединений формулы IB. Соединения IA или IB подвергают взаимодействию с замещенным амином при 150-160˚С в трубчатом автоклаве, получая соединения формулы IC. Соединения формулы IC, где R4 представляет водород, могут быть подвергнуты взаимодействию с изоцианатом или ацилхлоридом, получая соединения формулы I, где R4 представляет -C(O)NHR7 (ID) или -C(O)R6 (IE), соответственно.
Схема реакций 1
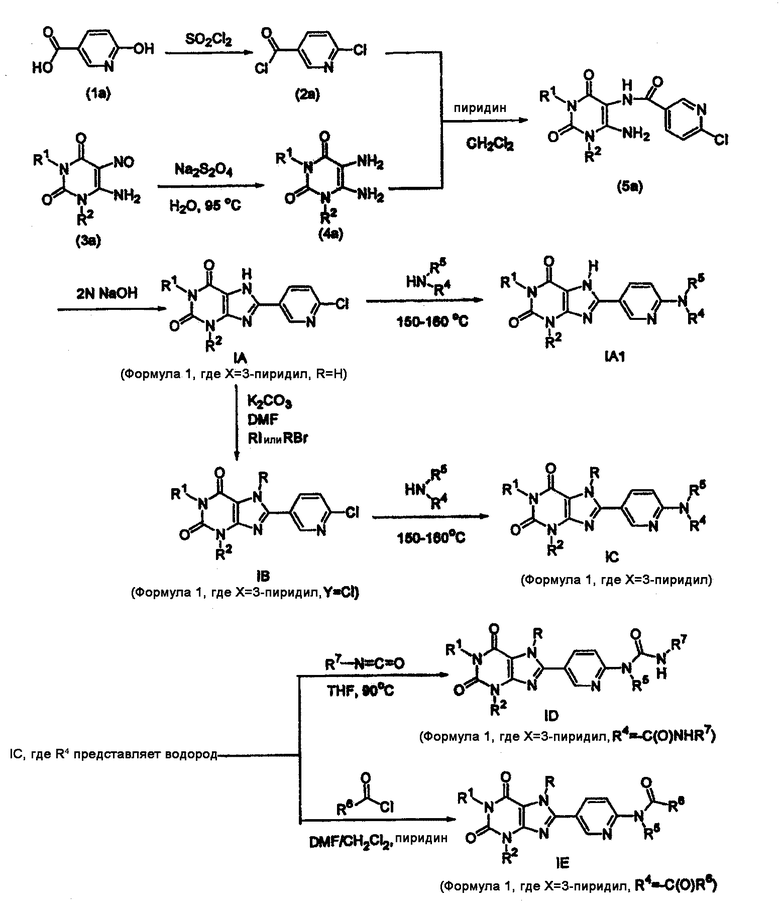
Соединения изобретения, где Z представляет -NR4R5 и R4 и R5 вместе с атомами, к которым они присоединены, образуют кольцо, содержащее NH группу, например, IC или IA1, могут быть получены взаимодействием соединения с изоцианатом или ацилхлоридом, получая соединения, имеющие Формулу IF и IG, как показано на схеме 2, ниже:
Схема реакций 2
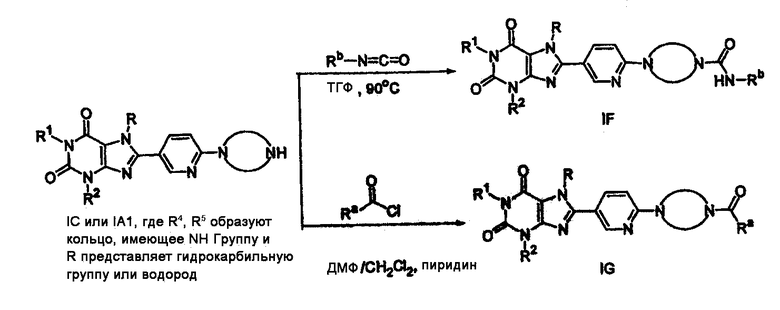
Схема 3 показывает, что соединение IA может быть подвергнуто взаимодействию с гидразином или замещенным гидразином при 100-160°С, получая соединения формулы IA2. Соединения формулы IA2, где R8 представляет водород, может быть подвергнуто взаимодействию с ацилхлоридом, получая соединения формулы IH и IJ. Соединение IA может быть так же подвергнуто взаимодействию с кетоном или альдегидом, получая соединение формулы IL.
Схема реакций 3
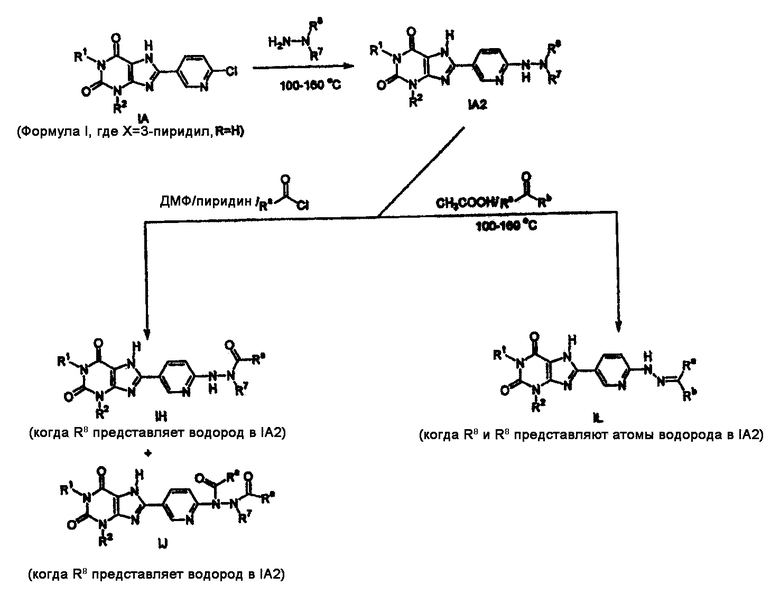
В настоящем описании используются следующие сокращения:
В случаях, когда соединения являются достаточно основными или кислотными для образования стабильных нетоксичных солей кислот или оснований, может быть выгодно вводить соединения в виде солей. Примерами фармацевтически приемлемых солей являются аддитивные соли органических кислот, образуемые с кислотами, которые дают физиологически приемлемый анион, например, тозилат, метансульфонат, ацетат, цитрат, малонат, тартрат, сукцинат, бензоат, аскорбат, α-кетоглутарат и α-глицерофосфат. Можно также получать подходящие неорганические соли, включающие гидрохлоридные, сульфатные, нитратные, бикарбонатные и карбонатные соли.
Фармацевтически приемлемые соли могут быть получены с использованием стандартных методик, хорошо известных в данной области техники, например, с помощью реакции достаточно основного соединения, такого как амин, с подходящей кислотой, дающей физиологически приемлемый анион. Могут быть также получены соли карбоновых кислот со щелочными металлами (например, натриевая, калиевая или литиевая) и щелочноземельными металлами (например, кальциевая).
Специалистам в данной области будет очевидно, что соединения изобретения, имеющие хиральный центр, могут существовать и выделяться в оптически активной и рацемической формах. Некоторые соединения могут проявлять полиморфизм. Должно быть понятно, что настоящее изобретение охватывает любые рацемические, оптически активные, полиморфные или стереоизомерные формы или их смеси соединений изобретения, которые обладают полезными свойствами, описанными выше, причем, в данной области известно, как получать оптически активные формы (например, расщеплением рацемической формы с помощью методов перекристаллизации, путем синтеза из оптически активных исходных веществ или с помощью хирального синтеза или хроматографического разделения с использованием хиральной неподвижной фазы). Общепринято также определять активность антагониста А2В аденозина с использованием стандартных тестов, описанных в данном описании, или путем использования аналогичных тестов или испытаний, которые хорошо известны в данной области.
Соединения формулы I могут быть сформированы в виде фармацевтических композиций и вводиться млекопитающему хозяину, такому как пациент человек, в виде широкого разнообразия форм, приспособленных для выбранного пути введения, т.е. перорально или парентерально, внутривенным, внутримышечным, топическим, ингаляционным или подкожным путями. Примеры фармацевтических композиций описаны в публикации “Remington: The Science and Practice of Pharmacy, A.Gennaro. ed., 20th edition, Lippncott, William & Wilkins, Филадельфия, PA.
Так, настоящие соединения могут быть введены системным путем, например, перорально, в сочетании с фармацевтически приемлемым носителем, таким как инертный разбавитель или ассимилируемый съедобный носитель. Они могут быть заключены в твердые или мягкие желатиновые капсулы, могут быть спрессованы в таблетки или могут быть введены непосредственно при приеме пищи с диетой пациента. Для перорального терапевтического введения активное соединение может быть комбинировано с одним или более эксципиентами и использовано в форме перевариваемых таблеток, щечных таблеток, пастилок, капсул, эликсиров, суспензий, сиропов, вафель и подобных. Такие композиции или препараты должны содержать, по крайней мере, 0,1% активного соединения. Процентный состав композиций и препаратов может, конечно, варьироваться и может удобным образом составлять между примерно 2 и 60% по массе заданной единичной дозированной формы. Количество активного соединения в таких терапевтически полезных композициях является таким, чтобы обеспечить эффективный уровень дозы.
Таблетки, пастилки, пилюли, капсулы и подобные могут также содержать следующие компоненты: связующие, такие как камедь трагаканта, акации, кукурузный крахмал или желатин; эксципиенты, такие как дикальцийфосфат; дезинтегрирующий агент, такой как кукурузный крахмал, картофельный крахмал, альгиновая кислота и подобные; лубрикант, такой как стеарат магния; и может добавляться подслащивающий агент, такой как сахароза, фруктоза, лактоза или аспартам, или вкусовой или ароматизирующий агент, такой как мята перечная, масло грушанки или вишневая вкусовая добавка. Когда единичной дозированной формой является капсула, она может содержать в дополнение к веществам вышеуказанного типа жидкий носитель, такой как растительное масло или полиэтиленгликоль. Разнообразные другие вещества могут присутствовать в качестве покрытий или для того, чтобы иным образом модифицировать физическую твердую форму единичной дозы. Например, таблетки пилюли или капсулы могут быть покрыты желатином, воском, шеллаком или сахаром или аналогичными. Сироп или эликсир может содержать активное соединение, сахарозу или фруктозу в качестве подслащивающего агента, метил и пропилпарабены в качестве консервирующих агентов, краситель и ароматизатор, такой как вишневая или апельсиновая отдушка. Конечно, любой материал, используемый при получении любой формы единичной дозы, должен быть фармацевтически приемлемым и достаточно нетоксичным в применяемых количествах. Помимо изложенного, активное соединение может включаться в препараты и приспособления замедленного высвобождения.
Активное соединение может также вводиться внутривенно или интраперитонально с помощью инфузии или инъекции. Растворы активного соединения или его солей могут приготавливаться в воде, необязательно в смеси с нетоксичным поверхностно-активным веществом. Дисперсии могут также приготавливаться в глицерине, жидких полиэтиленгликолях, триацетине и их смесях, и в маслах. В обычных условиях хранения и использования данные препараты содержат консерванты для предотвращения роста микроорганизмов.
Фармацевтические дозированные формы, подходящие для инъекции или инфузии, могут включать стерильные водные растворы или дисперсии или стерильные порошки, включающие активный ингредиент, которые приспособлены для приготовления стерильных инъецируемых или инфузируемых растворов или дисперсий для немедленного приема или введения, необязательно инкапсулированных в липосомы. Во всех случаях конечная дозированная форма должна быть стерильной, жидкой и стабильной в условиях производства и хранения. Жидким носителем или разбавителем может быть растворитель или жидкая дисперсионная среда, включающая, например, воду, этанол, полиол (например, глицерин, пропиленгликоль, жидкие полиэтиленгликоли и аналогичные), растительные масла, нетоксичные глицериловые сложные эфиры и их подходящие смеси. Надлежащая текучесть может поддерживаться, например, с помощью образования липосом, поддержания требуемого размера частиц в случае дисперсий или с помощью использования поверхностно-активных веществ. Предотвращение действия микроорганизмов может достигаться с помощью различных антибактериальных и антигрибковых агентов, например, парабенов, хлорбутанола, фенола, сорбиновой кислоты, тимерозаля и подобных. Во многих случаях предпочитается включать изотонические агенты, например, сахара, буферы или хлорид натрия. Пролонгированная абсорбция инъецируемых композиций может достигаться путем использования в композициях агентов, задерживающих абсорбцию, например, моностеарата алюминия и желатина.
Стерильные инъецируемые растворы приготавливают путем включения активного ингредиента в требуемом количестве в соответствующий растворитель с разнообразными другими ингредиентами, перечисленными выше, в зависимости от потребности, с последующей стерилизацией с использованием фильтров. В случае стерильных порошков для приготовления стерильных инъецируемых растворов предпочитаемыми способами получения являются методы вакуумной сушки и сушки вымораживанием, которые дают порошок активного ингредиента плюс любой дополнительный желаемый ингредиент, присутствующий в ранее известных стерильно фильтруемых растворах.
Для местного введения настоящие соединения могут применяться в чистой форме, а именно, когда они являются жидкостями. Однако обычно желательно применять их на коже в виде композиций или готовых форм препаратов в сочетании с дерматологически приемлемым носителем, который может быть твердым или жидким.
Полезные твердые носители включают тонко измельченные твердые вещества, такие как тальк, глина, микрокристаллическая целлюлоза, кремнезем, глинозем и подобные. Полезные жидкие носители включают воду, спирты или гликоли или смеси вода-спирт/гликоль, в которых настоящие соединения могут растворяться или диспергироваться в эффективных уровнях содержания, необязательно, с помощью нетоксичных поверхностно-активных веществ. Для оптимизации свойств для заданного использования могут добавляться адьюванты, такие как ароматизаторы и дополнительные антимикробные агенты. Получающиеся в результате жидкие композиции могут применяться с помощью абсорбентных прокладок, используемых для пропитки бинтов и других перевязочных материалов, или распыляться на пораженную поверхность с использованием распылителей типа насоса или аэрозольных распылителей или опрыскивателей.
С жидкими носителями могут применяться загустители, такие как синтетические полимеры, жирные кислоты, соли и эфиры жирных кислот, жирные спирты, модифицированные целлюлозы или модифицированные минеральные материалы, образуя распределяемые пасты, гели, мази, мыла и подобные, для непосредственного использования к коже пользователя.
Примеры полезных дерматологических композиций, которые могут использоваться для доставки соединений формулы I на кожу, являются известными для данной области; например, см. Jacquet et al. (патент США № 4608392), Geria, (патент США № 4992478), Smith et al. (патент США № 4559157) и Wortzman (патент США № 4820508). Полезные дозы соединений формулы I могут быть определены путем сравнения ин витро активности и ин виво активности на моделях животных. Способы экстраполяции эффективных доз у мышей и других животных на людей известны в данной области, см. патент США № 4938949.
Обычно концентрация соединения(ий) формулы I в жидкой композиции, такой как лосьон, составляет примерно 0,1-25 мас.%, предпочтительно примерно 0,5-10 мас.%. Концентрация в полутвердой или твердой композиции, такой как гель или порошок, составляет примерно 0,1-5 мас.%, предпочтительно около 0,5-2,5 мас.%.
Количество соединения или активной соли или ее производного, требуемое для применения при лечении, варьирует не только в зависимости от выбранной конкретной соли, но также и от способа введения, характера состояния, подвергаемого лечению, и от дозы и состояния пациента, и в конечном итоге на усмотрение лечащего врача или клинициста.
Обычно, однако, подходящая доза составляет в интервале примерно от 1,0 до 100 мг/кг, предпочтительно примерно от 10 до примерно 75 мг/кг массы тела в день, более предпочтительно от 5 до примерно 20 мг на килограмм массы тела реципиента в день.
Соединение может удобно вводиться в форме дозированной единицы; например, таблеток, капель и др., содержащих 4-400 мг, предпочтительно 10-200 мг, наиболее предпочтительно 20-100 мг активного ингредиента на форму единичной дозы.
В идеале активный ингредиент следует вводить для достижения в плазме пиковых концентраций активного соединения примерно от 0,02 до примерно 20 мкМ, предпочтительно около 0,1-10 мкМ, наиболее предпочтительно около 0,5 до около 5 мкМ. Данные концентрации могут достигаться, например, путем внутривенной инъекции 0,005-0,5% раствора активного ингредиента, или перорально вводиться в виде болюсов, содержащих около 4-400 мг активного ингредиента.
Соединения изобретения могут вводиться с помощью ингаляции из ингалятора, инсуффлятора, пульверизатора или распылителя или с помощью герметизированного флакона или других средств доставки аэрозольного спрея. Герметизированные флаконы могут включать подходящий пропеллент, такой как двуокись углерода или другой подходящий газ. В случае сжатого аэрозоля дозированная единица может определяться путем обеспечения клапана, отмеряющего дозированное количество. Ингаляторы, инсуффляторы, пульверизаторы полностью описаны в фармацевтической ссылочной литературе, такой как Remington's Pharmaceutical Sciences Volumes 16 (1980) или 18 (1990) Mack Publishing Co.
Желаемая доза может быть удобно представлена в виде однократной или разовой дозы или в виде раздельных доз, вводимых с соответствующими интервалами, например, в виде двух, трех, четырех или более субдоз в день. Субдоза сама по себе может быть дополнительно разделена, например, на ряд дискретных введений с произвольными интервалами; таких как множественные ингаляции из инсуффлятора или с помощью применения множества капель в глаз.
Все приводимые патенты, патентные заявки, книги или справочники и литература включены в данное описание в виде ссылок во всей своей полноте. В случае каких-либо нерегулярностей преобладает раскрытие в описании с любыми определениями, данными в нем. Изобретение описано со ссылкой на разнообразные конкретные и предпочтительные воплощения и технологические приемы. Однако следует понимать, что могут быть произведены многочисленные видоизменения и модификации, не отходя от существа и объема изобретения.
Изобретение теперь будет проиллюстрировано с помощью следующих неограничивающих примеров.
ПРИМЕРЫ
Фармакология
Способность соединений изобретения действовать в качестве антагонистов А2В аденозиновых рецепторов может быть определена с использованием фармакологических моделей, которые известны в данной области, или с использованием методик испытаний, описанных ниже.
кДНК А2В рецептора крысы субклонировали в экспрессионную плазмиду pDouble Trouble и использованием технологических приемов, описанных Robeva, A. et al., в Biochem. Pharmacol., 51, 545-555 (1996). Плазмиду амплифицировали в компетентных JM109 клетках и плазмидной ДНК, выделенной с использованием колонок Wizard Megaprep (Promega Corporation, Madison, WI). А2В рецепторы аденозина вводили в HEK-293 клетки с помощью липофектина, как описано у Felgner, P.L. et al., Proc. Natl. Acad. Sci, USA, 84, 7413-7417 (1987).
Культура клеток
Трансфицированные HEK клетки выращивали в 5% СО2/95% О2 увлажненной атмосфере при температуре 37оС. Колонии выбирали в условиях роста клеток в 0,6 мг/мл G418. Трансфицированные клетки хранили в DMEM с добавлением питательной смеси Hams F12 (1/1), 10% фетальной телячьей сыворотки, 2 мМ глютамина, содержащей 50 МЕ/мл пенициллина, 50 мг/мл стрептомицина и 0,2 мг/мл генетицина (G418, Boehringer Mannheim). Клетки культивировали в круглых чашках диаметром 10 см и субкультивировали до достижения стадии слияния (приблизительно спустя 72 часа).
Исследования радиолигандного связывания
А2В рецепторы: Слившиеся монослои НЕК-А2В клеток промывали PBS с последующей промывкой охлажденным льдом буфером А (10 мМ HEPES, 10 мМ EDTA, рН 7,4) с ингибиторами протеазы (10 мкг/мл бензамидина, 100 мкМ фенилметансульфонилфторида и 2 мкг/мл каждого из апротинина, пепстатина и лейпептина). Клетки гомогенизировали в политроне (Brinkmann) в течение 20 сек, центрифугировали при 30000×g и осадки промывали дважды буфером НЕ (10 мМ HEPES, 1 мМ EDTA, рН 7,4 с ингибиторами протеазы). Конечные осадки после центрифугирования ресуспендировали в буфере НЕ с добавлением 10% сахарозы и замораживали в виде аликвот при -80оС. Для анализов связывания мембраны размораживали и разводили 5-10 кратно НЕ до конечной концентрации белка приблизительно 1 мг/мл. Для определения концентраций белка мембраны и стандарты бычьего сывороточного альбумина растворяли в 0,2% NaOH/0,01% SDS и белок определяли с использованием флуоресценции флуорескамина. Stowell, C.P. et al., Anal. Biochem., 85, 572-580 (1978).
Анализы связывания насыщения для А2В рецепторов аденозина крыс проводили с [3H]ZM214,385 (17 Ки/ммоль, Tocris Cookson, Bristol UK)(Ji, X. et al., Drug Design Discov., 16, 216-226 (1999)) или 125I-ABOPX (2200 Ки/ммоль). Для приготовления 125I-ABOPX, 10 мкл 1 мМ АВОРХ в метаноле/1М NaOH (20:1) добавляли к 50 мкл 100 мМ фосфатного буфера, рН 7.3. Добавляли один или 2 мКи Na125I, с последующими 10 мкл 1 мг/мл хлорамина-Т в воде. После инкубации в течение 20 минут при комнатной температуре добавляли 50 мкл 10мг/мл Na-метабисульфита в воде для гашения реакции. Реакционную смесь наносили на С18 ВЭЖХ колонку, элюировали смесью метанола и 5 мМ фосфата, рН 6,0. Спустя 5 мин с 35% метанолом концентрацию метанола увеличивали до 100% на протяжении 15 мин. Непрореагировавший АВОРХ элюировался через 11-12 минут; 125I-ABOPX элюировался через 18-19 мин с выходом 50-6% по отношению к первоначальному 125I.
В анализах связывания соотношение 127I/125I-ABOPX было 10-20/1. Эксперименты радиолигандного связывания повторяли трижды с 20-25 мкг мембранного белка в общем объеме 0,1 мл НЕ буфера с добавлением 1 Ед/мл аденозиндезаминазы и 5 мМ MgCl2. Время инкубирования составляло 3 часа при 21оС. Неспецифическое связывание измеряли в присутствии 10 мкМ NECA. Конкурентные эксперименты осуществляли с использованием 0,6 нМ 125I-ABOPX. Мембраны фильтровали на фильтрах Whatman GF/C с использованием сборщика клеток Brandel (Gaithersburg, MD) и промывали 3 раза на протяжении 15-20 секунд ледяным буфером (10 мМ Трис, 1 мМ MgCl2, рН 7.4). Вmax и KD величины вычисляли нелинейной интерполяцией методом наименьших квадратов Marquardt для единых сайт-связывающих моделей. Marquardt, D.M., J. Soc. Indust. Appl. Math., 11, 431-441.21 (1963). Величины Ki для различных соединений вычисляли из величин IC50, как описано Linden, J., J. Cycl. Res., 8, 163-172 (1982). Данные от повторных экспериментов приведены в таблице в виде средних значений ±SEM.
Другие рецепторы аденозина: [3H]CPX. Bruns, R.F. et al., Naunyn-Schmiedeberd's Arch. Pharmacol., 335, 59-63 (1987). 125I-ZM241385 и 125I-АВА использовали в анализах радиолигандного связывания по отношению к мембранам, полученным из HEK-293 клеток, экспрессирующих рекомбинантные крысиные А1, А2А и А3 Ar, соответственно. Связывание [3H]R-N6-фенилизопропиладенозина Schwabe, U. et al., Naunyn-Schmiedeberd's Arch. Pharmacol., 313, 179-187 (1980). ([3H]R-PIA, Amersham, Chicago, IL) с А1 рецепторами из мембран коры головного мозга крыс и [3H]CGS 21680. Jarvis, M.F. et al., J. Pharmacol. Exp. Therap., 251, 888-893 (1989). (Dupont NEN, Boston, MA) с А2А рецепторами из мембран полосатого тела крыс выполняли, как описано. Аденозиндезаминаза (3 единицы/мл) присутствовала во время приготовления мембран головного мозга, при предварительной инкубировании 30 мин при 30оС и во время инкубирования с радиолигандами. Все нерадиоактивные соединения первоначально растворяли в ДМСО и разводили буфером до конечной концентрации, при которой количество ДМСО не превышало 2%. Инкубирование заканчивали быстрым фильтрованием на фильтрах Whatman GF/B с использованием сборщика клеток Brandell (Brandell, Gathersburg, MD). Каждую пробирку прополаскивали три раза 3 мл буфера.
Использовали, по крайней мере, шесть различных концентраций конкурентного вещества в диапазоне 3 порядков величин, доведенных приблизительно для IC50 каждого соединения. Величины IC50, вычисленные методом нелинейной регрессии, осуществленным на (Graph-Pad Prism, San Diego, CA), превращали в Ki величины, как описано. Linden, J., J. Cycl. Nucl. Res., 8:163-172 (1982). Hill коэффициенты испытуемых соединений составляли в пределах 0,8-1,1.
Функциональный анализ:
Клетки НЕК-А2В одной из сливающихся Т75 колбы прополаскивали свободным от Са2+ и Mg2+ забуференным фосфатом солевым раствором Дульбекко (PBS) и затем инкубировали в свободном от Са2+ и Mg2+ HBSS с 0,05% трипсина и 0,53 мМ EDTA до тех пор, пока клетки не отделялись. Клетки прополаскивали дважды с помощью центрифугирования при 250×g в PBS и ресуспендировали в 10 мл HBSS, состоящего из 137 мМ NaCl, 5 мМ KCl, 0,9 мМ MgSO4, 1,4 мМ CaCl2, 3 мМ NaHCO3, 0,6 мМ Na2HPO4, 0,4 мМ KH3PO4, 5,6 мМ глюкозы и 10 мМ HEPES, рН 7,4 и Са2+-чувствительного флуоресцентного красителя indo-1-AM (5 мкМ) 37оС в течение 60 минут. Клетки прополаскивали один раз и ресуспендировали в 25 мл свободного от красителя HBSS с добавлением 1 ед./мл аденозиндезаминазы и выдерживали при комнатной температуре. Добавляли антагонисты аденозинового рецептора, приготовленные в виде 100Х исходных растворов в ДМСО или разбавителе и клетки переносили в ванну с 37оС на 2 минуты. Затем клетки (1 миллион в 2 мл) переносили в кювету для перемешивания, выдержанную при 37оС, в Aminco SLM 8000 спектрофлуориметре (SML instruments, Urbana IL). Регистрировали соотношения indo-1 флуоресценции, полученные при 400 и 485 нм (возбуждение, 332 нм) с использованием щели шириной 4 нм. Спустя 100 сек период равновесия добавляли NECA.
Накопление циклического АМР
Генерирование циклического АМР выполняли в DMEM/HEPES буфере (DMEM, содержащий 50 мМ HEPES, рН 7,4, 37оС). Каждую лунку с клетками промывали дважды DMEM/HEPES буфером и затем добавляли 100 мкл растворов аденозиндезаминазы (конечная концентрация 10 МЕ/мл) и 100 мкл растворов ролипрама и цилостамида (конечная концентрация каждого 10 МЕ/мл) с последующим добавлением 50 мкл испытуемого соединения (соответствующая концентрация) или буфера. Спустя 15 минут инкубирование при 37оС заканчивали удалением среды и добавлением 200 мкл 0,1М HCl. Кислотные экстракты хранили при -20оС до анализа. Количества циклического АМР определяли в соответствии с протоколом, по которому использовался сАМР связывающийся белок (РКА) [van der Wenden et al., 1995], с последующими незначительными модификациями. Буфер для анализа состоял из 150 мМ K2HPO4/10 мМ EDTA/0,2% BSA FV при рН 7,5. Образцы (20 мл) инкубировали в течение 90 минут при 0оС. Инкубаты фильтровали через GF/C стекловолокнистые фильтры в сборнике клеток Brandel M-24. Фильтры дополнительно прополаскивали 4 раза по 2 мл 150 мМ K2HPO4/10 мМ EDTA (рН 7,5, 4оС). Фильтры с пробитыми отверстиями подсчитывали в сцинтилляционной жидкости Packard Emulsifier Safe после 2 часов экстракции.
Имеющиеся данные испытания на сродство соединений изобретения приведены в таблице 1. Данные, приведенные для А2В, представляют собой уровень замещения специфического [125I[ABOPX связывания в А2В рецепторах крыс (rA2B), экспрессированных в НЕК-293 клетках.
Синтез и характеристика
Протонную ядерную магнитно-резонансную спектроскопию выполняли на спектрометре Varian-300 МГц спектрометре и спектры снимали в ДМСО-d6 или CDCl3. Если не указано иное, химические сдвиги выражали в виде м.д. в слабом поле от тетраметилсилана или относительных м.д. от ДМСО (2,5 м.д.). Масс-спектрометрию с электрораспылительной ионизацией (ESI) выполняли с использованием масс-спектрометра ThermoFinnigan LCQ.
Все производные ксантина были гомогенными, о чем судили, используя ТСХ (силикагель 60 F254, 0,25 мм, на алюминиевой подложке, EM Science, Gibbstown, NJ) и ВЭЖХ (Shimadzu)с использованием аналитической колонки Varian С18 5 микрон (4,6 нм×150 мм) в системе линейного градиента или изократического растворителя, при объемном расходе 1 мл/мин. Используемая система растворителя представляла собой МеОН (0,1% муравьиная кислота):Н2О (0,1% муравьиная кислота). Пики детектировали УФ-абсорбции при 232 нм и 254 нм. Было показано, что ЯМР- и масс-спектры согласуются с предложенной структурой.
Пример 1. Общая методика
Получение 6-хлорникотиноилхлорида:
6-Гидроксиникотиновую кислоту (1,444 г, 10,4 ммол) суспендировали в тионилхлориде (8 мл). Добавляли ДМФА (0,50 мл). Смесь нагревали при кипячении с обратным холодильником в течение 2 час. После того, как реакционной смеси давали возможность охладиться, тионилхлорид удаляли струей азота, остаток сушили в вакууме в течение ночи и использовали непосредственно на следующей стадии.
Получение 1,3-дипропил-8-(6-хлор-3-пиридил)ксантина (1):
6-Хлорникотиноилхлорид, полученный из 6-гидроксиникотиновой кислоты (1,44 г, 10,4 ммол), в CH2Cl2 (20 мл) добавляли по каплям к раствору 5,6-диамино-1,3-дипропилурацила (1,81 г, 8 ммол) в сухом пиридине (8,2 мл), поддерживаемому при 5оС. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение дополнительных 3 часов. Для гашения реакции добавляли воду (50 мл). Растворитель выпаривали, получая темно окрашенное масло. Масло нагревали при кипячении с обратным холодильником в течение 2 часов в 2 норм. NaOH (20 мл). После охлаждения рН осторожно доводили до 7 концентрированной HCl. Образовавшееся твердое вещество собирали и промывали водой (20 мл), эфиром (20 мл) и хлороформом (20 мл), получая не совсем белое твердое вещество (1,9 г). Продукт использовался на следующей стадии без дополнительной очистки.
Общие методики взаимодействия 1,3-дипропил-8-(6-хлор-3-пиридил)ксантина (1) с замещенными аминами.
Соединение 1 (40 мг, 0,115 ммол) и соответствующий замещенный амин (0,5 мл или 0,5 г) помещали в пробирку под давлением. (Если точка кипения амина составляла выше 80оС, в качестве растворителя добавляли этанол, 4 мл). Пробирку под давлением продували аргоном, герметизировали и перемешивали смесь при 160оС в течение 48-60 часов. После охлаждения добавляли эфир (10 мл). Полученное твердое вещество собирали и очищали колоночной хроматографией на силикагеле или препаративной ТСХ (растворитель А: CH2Cl2:МеОН=20:1 до 10:1 или растворитель В: CH2Cl2:МеОН:ТЕА=20:1:0,1 до 4:1:0,1).
Общие методики получения соединений мочевин:
Аминозамещенное пиридильное соединение (IC) (10 мг) суспендировали в сухом ТГФ (5 мл) в пробирке под давлением. Добавляли изоцианат (0,25 мл). Смесь перемешивали при 90оС в течение 48 часов. После охлаждения растворитель упаривали. Остаток очищали препаративной ТСХ (CH2Cl2:МеОН=11:1).
Общие методики получения амидных соединений:
Аминозамещенное пиридильное соединение (15 мг) и желаемый хлорангидрид кислоты (4-6 эквивалентов) суспендировали в сухом ДМФА (2 мл). К смеси добавляли пиридин (0,1-0,15 мл). Реакционную смесь перемешивали при комнатной температуре в течение 24 часов. Растворитель удаляли и остаток очищали колоночной хроматографией на силикагеле или препаративной ТСХ (CH2Cl2:МеОН=11:1 или этилацетат:гексан:МеОН=15:85:5).
Получение 1,3-диэтил-8-[6-гидразино-3-пиридил]ксантина (138):
Соединение 1 (500 мг, 1,44 ммол) и гидразин (4 мл) помещали в пробирку под давлением. Добавляли этанол (30 мл). Пробирку под давлением продували аргоном, герметизировали и смесь перемешивали при 100-160оС в течение 10-16 часов. После охлаждения полученное твердое вещество собирали и промывали метанолом и эфиром, получая соединение 138 (40 мг). Продукт использовали на следующей стадии без дополнительной очистки.
Общие методики получения соединений формулы IL:
Соединение 138 (31,5 мг, 0,1 ммол) суспендировали в уксусной кислоте (5 мл) в пробирке под давлением. Добавляли альдегид или кетон (0,12 ммол). Пробирку под давлением продували аргоном, герметизировали и смесь перемешивали при 160оС в течение 2-10 часов. После охлаждения полученное твердое вещество собирали и очищали колоночной хроматографией на силикагеле или препаративной ТСХ (CH2Cl2: МеОН=20:1 до 10:1), получая соединение формулы IL.
Примеры
С использованием методики, описанной выше, получали следующие соединения изобретения.
Соединение 1: 1,3-Дипропил-8-(6-хлор-3-пиридил)ксантин
1H ЯМР (ДМСО, d6): δ 0,89 (м, 6H), 1,59 (м, 2H), 1,73 (м, 2H), 3,88 (т, 2H, J=7,2 Гц), 4,00 (т, 2H, J=7,2 Гц), 7,68 (д, 1H, J=8,4 Гц), 8,50 (дд, 1Н, J1=2,4 Гц, J2=8,4 Гц), 9,07 (д, 1H, J=2,4 Гц).
МС: m/z 348 (M+H)+.
Соединение 2: 1-Пропил-3-пропаргил-8-(6-хлор-3-пиридил)ксантин
МС: m/z 316 (М+H)+
Соединение 3: 1,3-Дипропил-8-(6-этиламино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,89 (м, 6H), 1,14 (1,3H, J=7,2 Гц), 1,56 (м, 2H), 1,72 (м, 2H), 3,33 (м, 2H), 3,84 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 6,52 (д, 1H, J=8,7 Гц), 7,09 (т, 1H), 8,00 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,72 (д, 1H, J=2,4 Гц).
МС: m/z 357 (М+H)+.
Соединение 4: 1,3-Дипропил-8-(6-(2-гидроксиэтил)амино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,57 (м, 2H), 1,71 (м, 2H), 3,36 (м, 2H), 3,53 (м, 2H), 3,85 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 4,73 (т, 1H, J=5,4 Гц), 6,57 (д, 1H, J=8,7 Гц), 7,11 (т, 1H), 7,99 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,70 (д, 1H, J=2,4 Гц).
МС: m/z 373 (М+H)+.
Соединение 5: 1,3-Дипропил-8-[6-(4-ацетилпиперазинил)-3-пиридил]ксантин
1Н ЯМР (ДМСО-d6): δ 0,84 (м, 6H), 1,52 (м, 2H), 1,68 (м, 2H), 2,00 (с, 3H), 3,52 (м, 8H), 3,81 (т, 2H, J=7,2 Гц), 3,96 (т, 2H, J=7,2 Гц), 6,92 (д, 1H, J=8,7 Гц), 8,14 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,79 (д, 1H, J=2,4 Гц).
МС: m/z 440 (М+H)+.
Соединение 6: 1,3-Дипропил-8-[6-(бензиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,54 (м, 2H), 1,71 (м, 2H), 3,84 (т, 2H, J=7,2 Гц), 3,98 (т, 2H, J=7,2 Гц), 4,54 (д, 2H, J=6,5 Гц), 6,61 (д, 1H, J=8,7 Гц), 7,22 (м, 1H), 7,31 (м, 4H), 7,66 (т, 1H, J=6,0 Гц), 8,02 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,71 (д, 1H, J=2,4 Гц).
МС: m/z 419 (М+H)+.
Соединение 7: 1,3-Дипропил-8-[6-(1-пиперидинил)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,63 (м, 10H), 3,61 (т, 4H, J=5,7 Гц), 3,85 (т, 2H, J=7,2 Гц), 4,00 (т, 2H, J=7,2 Гц), 6,91 (д, 1H, J=9,0 Гц), 8,12 (дд, 1Н, Ji=2,4 Гц, J2=9,0 Гц), 8,79 (д, 1Н, J=2,4 Гц).
МС: m/z 397 (М+H)+.
Соединение 8: 1,3-Дипропил-8-(6-пирролидинилпирид-3-ил)ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,55 (м, 2H), 1,73 (м, 2H), 1,95 (м, 4H), 3,43 (м, 4H), 3,85 (т, 2H, J=7,5 Гц), 4,00 (т, 2H, J=7,5 Гц), 6,54 (д, 1H, J=9,0 Гц), 8,12 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,79 (д, 1Н, J=2,4 Гц).
МС: m/z 383 (М+H)+.
Соединение 9: 1,3-Дипропил-8-{6-[4-метил(пергидро-1,4-диазаепин-1-ил)]-3-пиридил}ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (уш, 2H), 1,72 (м, 2H), 1,88 (м, 2H), 2,47 (м, 5H), 2,60 (м, 2H), 3,64 (т, 2H, J=6,0 Гц), 3,77 (м, 2H), 3,85 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 6,73 (д, 1H, J=9,0 Гц), 8,12 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,78 (д, 1H, J=2,4 Гц).
МС: m/z 426 (М+2).
Соединение 10: 1,3-Дипропил-8-(6-метиламино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 2,8l(д, 3H, J=4,5 Гц), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 6,52 (д, 1H, J=8,7 Гц), 7,08 (кв, 1H, J=4,5 Гц), 8,01 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,73 (д, 1H, J=2,4 Гц).
МС: m/z 343 (М+H)+.
Соединение 11: 1,3-Дипропил-8-[6-(4-метоксибензиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,59 (м, 2H), 1,71 (м, 2H), 3,71 (с, 3H), 3,87 (т, 2H, J=7,2 Гц), 3,98 (т, 2H, J=7,2 Гц), 4,45 (д, 2H, J=6,3 Гц), 6,58 (д, 1H, J=9,0 Гц), 6,87 (д, 2H, J=8,7 Гц), 7,25 (д, 2H, J=8,7 Гц), 7,60 (т, 1H), 8,01 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,71 (д, 1Н, J=2,4 Гц).
МС: m/z 449 (М+H)+.
Соединение 12: 1,3-Дипропил-8-[6-(3-метилпиперидино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 9H), 1,14 (м, 1H), 1,40-1,80 (м, 8H), 2,55 (дт, 1H, J1=l Гц, J2=10,5 Гц), 2,86 (дт, 1H, J1=2,1 Гц, J2=10,5 Гц), 3,85 (т, 2H, J=7,5 Гц), 4,00 (т, 2H, J=7,5 Гц), 4,30 (д, 2H, J=13,5 Гц), 6,92 (д, 1H, J=9,0 Гц), 8,10 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,79 (д, 1H, J=2,4 Гц).
МС: m/z 411 (М+H)+.
Соединение 13: 1,3-Дипропил-8-[6-(2-гидроксипропил)амино-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,08 (д, 3H, J=6,0 Гц), 1,56 (м, 2H), 1,72 (м, 2H), 3,26 (м, 2H), 3,77 (м, 1H), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 4,76 (д, 1Н, J=4,5 Гц), 6,60 (д, 1Н, J=9,0 Гц), 7,10 (т, 1H, J=6,0 Гц), 7,99 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,69 (д, 1H, J=2,4 Гц).
МС: m/z 387 (М+H)+.
Соединение 14: 1,3-Дипропил-8-[6-(2,2-диметоксиэтил)амино-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 3,29 (с, 6H), 3,45 (т, 2H, J=5,7 Гц), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 4,49 (т, 1H, J=5,4 Гц), 6,62 (д, 1H, J=9,0 Гц), 7,19 (т, 1H, J=5,7 Гц), 8,00 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,71 (д, 1H, J=2,4 Гц).
МС: m/z 417 (М+H)+.
Соединение 15: 1,3-Дипропил-8-[6-(1-гидрокси-2-пропил)амино-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,12 (д, 3H, J=6,6 Гц), 1,56 (м, 2H), 1,74 (м, 2H), 3,27 (м, 2H), 3,46 (м, 1H), 3,85 (т, 2H, J=7,2 Гц), 3,98 (т, 2H, J=7,2 Гц), 4,74 (т, 1H, J=5,4 Гц), 6,56 (д, 1H, J=9,0 Гц), 6,90 (д, 1H, J=7,5 Гц), 7,98 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,69 (д, 1H, J=2,4 Гц).
МС: m/z 387 (М+H)+.
Соединение 16: 1,3-Дипропил-8-(6-морфолино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,57 (м, 2H), 1,73 (м, 2H), 3,55 (м, 4H), 3,69 (м, 4H), 3,85 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 6,94 (д, 1H, J=9,0 Гц), 8,17 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,83 (д, 1H, J=2,4 Гц).
МС: m/z 399 (М+H)+.
Соединение 17: 1,3-Дипропил-8-(6-диметиламино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,55 (м, 2H), 1,75 (м, 2H), 3,09 (с, 6H), 3,85 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 6,73 (д, 1H, J=9,0 Гц), 8,13 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,80 (д, 1H, J=2,4 Гц).
МС: m/z 357 (М+H)+.
Соединение 18: 1,3-Дипропил-8-[[6-(2-гидроксиэтокси)этиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,57 (м, 2H), 1,72 (м, 2H), 3,49 (м, 8H), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 4,59 (т, 1H, J=5,4 Гц), 6,58 (д, 1H, J=9,0 Гц), 7,15 (т, 1H), 8,00 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,71 (д, 1Н, J=2,4 Гц), 13,42 (с, 1H).
МС: m/z 417 (М+H)+.
Соединение 19: 1,3-Дипропил-8-(6-пиперазино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 2,78 (м, 4H), 3,52 (м, 4H), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 6,88 (д, 1H, J=9,0 Гц), 8,13 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,80 (д, 1H, J=2,4 Гц).
МС: m/z 398 (М+H)+.
Соединение 20: 1,3-Дипропил-8-[6-(2-гидрокси-2-фенилэтил)амино-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 3,32 (м, 1H), 3,55 (м, 4H), 3,85 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 4,76 (м, 1H), 5,55 (д, 1H, J=4,5 Гц), 6,63 (д, 1H, J=8,7 Гц), 7,20-7,40 (м, 6H), 8,00 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,72 (д, 1Н, J=2,4 Гц), 13,42 (с, 1H).
МС: m/z 449 (М+H)+.
Соединение 21: 1,3-Дипропил-8-[6-(4-аминометилбензиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,86 (м, 6H), 1,55 (м, 2H), 1,71 (м, 2H), 3,72 (с, 2H), 3,84 (т, 2H, J=7,2 Гц), 3,97 (т, 2H, J=7,2 Гц), 4,50 (д, 1H, J=6,0 Гц), 6,57 (д, 1H, J=9,0 Гц), 7,27 (с, 4H), 7,54 (т, 1H, J=6,0 Гц), 8,00 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,68 (д, 1H, J=2,4 Гц).
МС: m/z 448 (М+H)+.
Соединение 22: 1,3-Дипропил-8-(6-фениламино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,55 (м, 2H), 1,76 (м, 2H), 3,86 (т, 2H, J=7,5 Гц), 4,01 (т, 2H, J=7,5 Гц), 6,93 (м, 2H), 7,29 (т, 2H, J=7,8 Гц), 7,68 (д, 2H, J=7,8 Гц), 8,19 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,87 (д, 1H, J=2,4 Гц), 9,45 (с, 1H).
МС: m/z 405 (М+H)+.
Соединение 23: 1,3-Дипропил-8-(6-циклопропиламино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,44 (м, 2H), 0,72 (м, 2H), 0,87 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 2,58 (м, 1H), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 6,66 (д, 1H, J=9,0 Гц), 7,36 (д, 1H, J=2,7 Гц), 8,10 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,74 (д, 1H, J=2,4 Гц).
МС: m/z 369 (М+H)+.
Соединение 24: 1,3-Дипропил-8-[6-(6-пиридилметиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 3,84 (т, 2H, J=7,2 Гц), 3,98 (т, 2H, J=7,2 Гц), 4,62 (д, 2H, J=6,0 Гц), 6,67 (д, 1H, J=8,7 Гц), 7,25 (м, 2H), 7,73 (м, 2H), 8,04 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,51 (д, 1Н, J=4,8 Гц), 8,69 (д, 1H, J=2,4 Гц).
МС: m/z 420 (М+H)+.
Соединение 25: 1,3-Дипропил-8-(6-(4-метилпиперазино)-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 2,21 (с, 3H), 2,38 (т, 4H, J=4,8 Гц), 3,59 (т, 4H, J=4,8 Гц), 3,85 (т, 2H, J=7,5 Гц), 4,00 (т, 2H, J=7,5 Гц), 6,93 (д, 1H, J=9,0 Гц), 8,15 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,81 (д, 1H, J=2,4 Гц).
МС: m/z 412 (М+H)+.
Соединение 26: 1,3-Дипропил-8-[6-(3-пиридилметиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,71 (м, 2H), 3,84 (т, 2H, J=7,5 Гц), 3,98 (т, 2H, J=7,5 Гц), 4,56 (д, 2H, J=5,7 Гц), 6,63 (д, 1H, J=8,7 Гц), 7,33 (дд, 1H, J1=4,5 Гц, J2=7,8 Гц), 7,71 (м, 2H), 8,04 (дд, 1Н, J1=2,4 Гц, J2=8,7 Гц), 8,43 (дд, 1H, J=1,8 Гц, J2=4,5 Гц), 8,55 (д, 1H, J=1,8 Гц), 8,71 (д, 1H, J=2,4 Гц).
МС: m/z 420 (М+H)+.
Соединение 27: 1,3-Дипропил-8-[6-(2-метилбензиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 2,31 (с, 3H), 3,85 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 4,50 (д, 2H, J=5,4 Гц), 6,62 (д, 1H, J=8,7 Гц), 7,10-7,25 (м, 4H) 7,51 (т, 1H, J=5,4 Гц), 8,01 (дд, 1Н, J1=2,4 Гц, J2=8,7 Гц), 8,72 (д, 1H, J=2,4 Гц).
МС: m/z 433 (М+H)+.
Соединение 28: 1,3-Дипропил-8-[6-[2-(3,4-диметоксифенил)этиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 2,77 (т, 2H, J=7,5 Гц), 3,49 (м, 2H), 3,70 (с, 3H), 3,73 (с, 3H), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 6,55 (д, J=9,0 Гц), 6,74 (дд, 1Н, J1=1,8 Гц; J2=8,4 Гц), 6,85 (м, 2H), 7,17 (т, 1H, J=5,4 Гц), 8,01 (дд, J1=2,4 Гц, J2=9,0 Гц), 8,73 (д, 1H, J=2,4 Гц).
МС: m/z 493 (М+H)+.
Соединение 29: 1,3-Дипропил-8-[6-[(N-пропилкарбамоил)метиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 9H), 1,54 (м, 4H), 1,72 (м, 2H), 3,17 (м, 2H), 3,30 (д, 3H, J=5,4 Гц), 3,86 (т, 2H, J=7,5 Гц), 4,01 (т, 2H, J=7,5 Гц), 7,43 (д, 1H, J=9,0 Гц), 8,01 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,99 (д, 1H, J=2,4 Гц), 9,29 (т, 1H, 5,4 Гц).
МС: m/z 428 (М+H)+.
Соединение 30: 1,3-Дипропил-8-[6-(3-пентиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 12H), 1,37-1,65 (м, 6H), 1,72 (м, 2H), 3,84 (м, 3H), 3,98 (т, 2H, J=7,2 Гц), 6,54 (д, 1H, J=8,7 Гц), 6,90 (д, 1H, J=8,4 Гц), 7,96 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,67 (д, 1H, J=2,4 Гц).
МС: m/z 399 (М+H)+.
Соединение 31: 1,3-Дипропил-8-[6-(2,2-дифенилэтиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,86 (м, 6H), 1,54 (м, 2H), 1,72 (м, 2H), 3,82-4,00 (м, 6H), 4,36 (т, 1H, J=7,5 Гц), 6,53 (д, 1H, J=9,0 Гц), 7,15-7,34 (м, 11H), 7,97 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,75 (д, 1H, J=2,4 Гц).
МС: m/z 509 (М+H)+.
Соединение 32: 1,3-Дипропил-8-[6-[2-(1-этилпирролидинометиламино)]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,04 (т, 2H, J=7,2 Гц), 1,50-1,86 (м, 8H), 2,12 (м, 1H), 2,25 (м, 1H), 2,58 (м, 1H), 2,86 (м, 1H), 3,09 (м, 2H), 3,51 (м, 1H), 3,84 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 6,60 (д, 1H, J=9,0 Гц), 6,98 (уш., 1H), 7,99 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,70 (д, 1H, J=2,4 Гц).
МС: m/z 440 (М+H)+.
Соединение 33: 1,3-Дипропил-8-[6-(3-метоксибензиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,54 (м, 2H), 1,72 (м, 2H), 3,71 (с, 3H), 3,85 (т, 2H, J=7,8 Гц), 3,99 (т, 2H, J=7,8 Гц), 4,51 (д, 2H, J=6,0 Гц), 6,61 (д, 1H, J=9,0 Гц), 6,70-6,91 (м, 3H), 7,22 (т, 1Н, J=7,5 Гц), 7,64 (т, 1H, J=6,0 Гц), 8,02 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,71 (д, 1H, J=2,4 Гц).
МС: m/z 449 (М+H)+.
Соединение 34: 1,3-Дипропил-8-[6-[(N-фенилкарбамоил)метиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ O,88 (м, 6H), 1,57 (м, 2H), 1,75 (м, 2H), 3,44 (с, 3H), 3,86 (т, 2H, J=7,5 Гц), 4,02 (т, 2H, J=7,5 Гц), 7,04 (т, 1Н, J=7,2 Гц), 7,32 (т, 2H, J=7,5 Гц), 7,48 (д, 1H, J=9,0 Гц), 7,60 (м, 3H), 8,47 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 9,12 (д, 1H, J=2,4 Гц).
МС: m/z 462 (М+H)+.
Соединение 35: 1,3-Дипропил-8-[6-(фурфуриламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,57 (м, 2H), 1,73 (м, 2H), 3,87 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 4,52 (д, 2H, J=5,7 Гц), 6,27 (д, 1H, J=3,0 Гц), 6,38 (м, 1H), 6,3 (д, 1H, J=9,0 Гц), 7,56 (м, 2H), 8,03 (дд, 1Н, J1=2,4 Гц, J2=9,0 Гц), 8,73 (д, 1H, J=2,4 Гц).
МС: m/z 409 (М+H)+.
Соединение 36: 1,3-Дипропил-8-[6-[2-(4-метоксифенил)этиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 2,77 (т, 2H, J=7,5 Гц), 3,47 (кв, 2H, т=7,5 Гц), 3,71 (с, 3H), 3,85 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 6,55 (д, J=9,0 Гц), 6,85 (д, 2H, J=8,4 Гц), 7,16 (д, 2H, J=8,4 Гц), 8,00 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,73 (д, 1H, J=2,4 Гц).
МС: m/z 463 (М+H)+.
Соединение 37: 1,3-Дипропил-8-[6-(2-метоксибензиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,86 (м, 6H), 1,56 (м, 2H), 1,71 (м, 2H), 3,82 (с, 3H), 3,87 (т, 2H, J=7,2 Гц), 3,98 (т, 2H, J=7,2 Гц), 4,48 (д, 2H, J=6,0 Гц), 6,62 (д, 1H, J=9,0 Гц), 6,87 (т, 1H, J=7,2 Гц), 6,98 (д, 1H, J=7,5 Гц), 7,20 (м, 2H), 7,46 (т, 1Н, J=6,0 Гц), 8 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,70 (д, 1H, J=2,4 Гц).
МС: m/z 449 (М+H)+.
Соединение 38: 1,3-Дипропил-8-[6-(пропиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 9H), 1,53 (м, 4H), 1,72 (м, 2H), 3,24 (кв, 2H, J=6,3 Гц), 3,85 (т, 2H, J=7,5 Гц), 3,98 (т, 2H, J=7,5 Гц), 6,53 (д, 1Н, J=8,7 Гц), 7,13 (т, 1H, J=5,7 Гц), 7,99 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 8,70 (д, 1H, J=2,4 Гц).
МС: m/z 371 (М+H)+.
Соединение 39: 1,3-Дипропил-8-[6-(циклопентиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,40-1,75 (м, 10H), 1,72 (м, 2H), 3,84 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 4,17 (м, 1H), 6,52 (д, 1H, J=8,7 Гц), 7,10 (д, 1H, J=6,6 Гц), 7,99 (дд, 1Н, J1=2,4 Гц, J2=8,7 Гц), 8,70 (д, 1Н, J=2,4 Гц).
МС: m/z 397 (М+H)+.
Соединение 40: 1,3-Дипропил-8-[6-(циклогексиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,13-1,91 (м, 14H), 1,72 (м, 2H), 3,76 (м, 1H), 3,84 (т, 2H, J=7,5 Гц), 3,98 (т, 2H, J=7,5 Гц), 6,52 (д, 1H, J=9,0 Гц), 7,00 (д, 1H, J=7,8 Гц), 7,97 (дд, 1Н, J1=2,4 Гц, J2=9,0 Гц), 8,69 (д, 1H, J=2,4 Гц).
МС: m/z 411 (М+H)+.
Соединение 41: 1,3-Дипропил-7-этил-8-(6-хлор-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,33 (т, 3H, J=7,2 Гц), 1,59 (м, 2H), 1,73 (м, 2H), 3,87 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 7,74 (д, 1H, J=8,4 Гц), 8,19 (дд, 1H, J1=2,4 Гц, J2=8,4 Гц), 8,74 (д, 1Н, J=2,4 Гц).
МС: m/z 376 (М+H)+.
Соединение 42: 1,3-Дипропил-7-(3-фторпропил)-8-(6-хлор-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 2,09 (м, 1H), 2,18 (м, 1Н), 3,89 (т, 2H, J=7,5 Гц), 3,98 (т, 2H, J=7,5 Гц), 4,29 (т, 1Н, J=5,4 Гц), 4,43 (м, 3H), 7,75 (дд, Jl=0,6 Гц, J2=8,4 Гц), 8,19 (дд, 1Н, J1=2,4 Гц, J2=8,4 Гц), 8,74 (дд, 1H, J1=0,6 Гц, J2=2,4 Гц).
МС: m/z 408 (М+H)+.
Соединение 43: 1,3-Дипропил-7-метил-8-(6-хлор-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 3,86 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 4,01 (с, 3H), 7,74 (д, 1H, J=8,4 Гц), 8,26 (дд, 1H, J1=2,4 Гц, J2=8,4 Гц), 8,82 (д, 1Н, J=2,4 Гц).
МС: m/z 362 (М+H)+.
Соединение 44: 1,3-Дипропил-7-(2-бромэтил)-8-(6-хлор-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,59 (м, 2H), 1,72 (м, 2H), 3,85 (м, 4H), 3,99 (т, 2H, J=7,5 Гц), 4,66 (т, 2H, J=6,0 Гц), 7,76 (д, 1H, J=8,1 Гц), 8,21 (дд, 1H, J1=2,7 Гц, J2=8,1 Гц), 8,76 (д, 1H, J=2,7 Гц).
МС: m/z 456 (М+H)+.
Соединение 45: 1,3-Дипропил-8-[6-(2-тиофенметиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,72 (м, 2H), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 4,70 (д, 2H, J=6,0 Гц), 6,60 (д, 1H, J=8,7 Гц), 6,94-7,03 (м, 2H), 7,35 (дд, 1H, J1=l,5 Гц, J2=5,1 Гц), 7,70 (т, 1H, J=6,0 Гц), 8,04 (дд, 1Н, J1=2,4 Гц, J2=8,7 Гц), 8,75 (д, 1H, J=2,4 Гц).
МС: m/z 425 (М+H)+.
Соединение 46: 1,3-Дипропил-8-[6-[N-(4-метоксифенилкарбамоил)метиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,89 (м, 6H), 1,56 (м, 2H), 1,73 (м, 2H), 3,43 (с, 3H), 3,73 (с, 3H), 3,87 (т, 2H, J=7,2 Гц), 4,02 (т, 2H, J=7,2 Гц), 6,89 (дд, 2H, J=6,9 Гц), 7,48 (м, 3H), 8,47 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 9,11 (д, 1H, J=2,4 Гц).
МС: m/z 492 (М+H)+.
Соединение 47: 1,3-Дипропил-8-[6-[N-никотиноилметиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,57 (м, 2H), 1,73 (м, 2H), 3,49 (с, 3H), 3,86 (т, 2H, J=7,2 Гц), 3,99 (т, 2H, J=7,2 Гц), 7,35 (дд, 1H, J1=7,8 Гц, J2=7,8 Гц), 7,41 (д, 1H, J=8,4 Гц), 7,71 (дт, 1H, J1=1,5 Гц, J2=8,4 Гц,), 8,32 (дд, 1H, J1=2,4 Гц, J2=8,4 Гц), 8,46 (д, 1H, J=2,1), 8,54 (дд, 1H, J1=2,1 Гц, J2=4,8 Гц), 8,98 (д, 1Н, J=2,4 Гц).
МС: m/z 448 (М+H)+.
Соединение 48: 1,3-Дипропил-8-[6-[N-(4-фторфенилкарбамоил)метиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,57 (м, 2H), 1,75 (м, 2H), 3,44 (с, 3H), 3,88 (т, 2H, J=7,5 Гц), 4,03 (т, 2H, J=7,5 Гц), 7,15 (т, 2H, J=8,7 Гц), 7,49 (д, 1H, J=9,0 Гц), 7,62 (м, 2H), 8,47 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 9,12 (д, 1H, J=2,4 Гц).
МС: m/z 480 (М+H)+.
Соединение 49: 1,3-Дипропил-8-[6-[N-изоникотиноилметиламино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,57 (м, 2H), 1,75 (м,2H), 3,47 (с, 3H), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 7,26 (д, 2H, J=5,4 Гц), 7,46 (д, 1H, J=8,7 Гц), 8,34 (дд, 1Н, J1=2,4 Гц, J2=8,7 Гц), 8,54 (д, 2H, J=5,4 Гц), 8,96 (д, 1H, J=2,4 Гц).
МС: m/z 448 (М+H)+.
Соединение 50: 1,3-Дипропил-8-[6-[N-метоксикарбонилметиламино]-3-пиридил]ксантин
МС: m/z 401 (М+H)+.
Соединение 51: 1,3-Дипропил-8-[6-[N-фенилкарбамоил-N-(2-фенилкарбамоилоксиэтил)амино]-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,57 (м,2H), 1,75 (м, 2H), 3,87 (т, 2H, J=7,5 Гц), 4,03 (т, 2H, J=7,5 Гц), 4,34 (м, 4H), 6,92-7,57 (м, 11H), 8,44 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 9,12 (д, 1H, J=2,4 Гц), 9,58 (с, уш.), 1H).
МС: m/z 611 (М+H)+.
Соединение 52: 1,3-Дипропил-8-{6-[4-(N-фенилкарбамоил)]пиперазино-3-пиридил}ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,73 (м, 2H), 3,57 (м, 4H), 3,67 (м, 4H), 3,86 (т, 2H, J=7,2 Гц), 4,01 (т, 2H, J=7,2 Гц), 6,93 (т, 1H, J=7,8 Гц), 6,99 (д, 1H, J=9,0 Гц), 7,23 (т, 2H, J=7,8 Гц), 7,46 (д, 2H, J=7,8 Гц), 8,19 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,61 (с, 1H), 8,85 (д, 1H, J=2,4 Гц).
МС: m/z 517 (М+H)+.
Соединение 53: 1,3-Дипропил-8-{6-[4-(N-изоникотиноил)]пиперазино-3-пиридил}ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,73 (м, 2H), 3,38 (м, 2H), 3,64 (м, 2H), 3,75 (м, 4H), 3,86 (т, 2H, J=7,2 Гц), 4,00 (т, 2H, J=7,2 Гц), 6,96 (д, 1H, J=9,0 Гц), 7,44 (д, 2H, J=5,1 Гц), 8,19 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,69 (д, 2H, J=5,1 Гц), 8,84 (д, 1H, J=2,4 Гц).
МС: m/z 503 (М+H)+.
Соединение 54: 1-пропил-3-(4-метоксифенил)этил-8-(6-хлор-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,84 (т, 3H, J=7,2 Гц), 1,53 (м, 2H), 2,93 (т, 2H, J=7,2 Гц) 3,67 (с, 3H), 3,83 (т, 2H, J=7,2 Гц), 4,20 (т, 2H, J=7,2 Гц), 6,81 (д, 2H, J=8,1 Гц), 7,12 (д, 2H, J=8,1 Гц), 7,68 (д, 1H, J=8,4 Гц), 8,44 (дд, 1H, J1=2,4 Гц, J2=8,4 Гц), 8,98 (д, 1H, J=2,4 Гц).
МС: m/z 440 (MH-H)+.
Соединение 55: 1-пропил-3-(метоксифенилэтил)-8-(6-пиперазино-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 0,84 (м, 3H), 1,52 (м, 2H), 3,38 (м, 2H), 2,77 (м, 4H), 2,94 (т, 2H, J=7,5 Гц), 3,51 (м, 4H), 3,69 (с, 1H), 3,83 (т, 2H, J=7,5 Гц), 4,20 (т, 2H, J=7,5 Гц), 6,83 (д, 2H, J=8,4 Гц), 6,89 (д, 1H, J=9,0 Гц), 7,14 (д, 2H, J=8,4 Гц), 8,14 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,82 (д, 1H, J=2,4 Гц).
МС: m/z 490 (М+H)+.
Соединение 56: 1,3-Дипропил-8-[6-(4-пиридиламино)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,74 (м, 2H), 3,87 (т, 2H, J=7,5 Гц), 4,03 (т, 2H, J=7,5 Гц), 6,30 (д, 2H, J=7,8 Гц), 7,94 (д, 1H, J=8,7 Гц), 8,53 (д, 1H, J=7,8 Гц), 8,60 (дд, 1H, J1=2,4 Гц, J2=8,7 Гц), 9,17 (д, 1H, J=2,4 Гц).
МС: m/z 407 (М+2)+.
Соединение 57: 1,3-Дипропил-8-{6-[4-(N-никотиноил)]пиперазино-3-пиридил}ксантин
1H ЯМР (ДМСО-d6): δ 0,88 (м, 6H), 1,56 (м, 2H), 1,74 (м, 2H), 3,46-3,83 (м, 8H), 3,88 (т, 2H, J=7,5 Гц), 4,00 (т, 2H, J=7,5 Гц), 6,96 (д, 1Н, J=9,0 Гц), 7,50 (дд, 1H, J1=7,8 Гц, J2=7,8 Гц), 7,89 (д, J=7,5 Гц), 8,19 (дд, 1H, J1=2,4 Гц, J2=9,0 Гц), 8,66 (м, 2H), 8,84 (д, 1H, J=2,4 Гц).
МС: m/z 503 (М+H)+.
Соединение 58: 1,3-Дипропил-8-[6-(гексагидро-1,4-диазаепин-1-ил)-3-пиридил]ксантин
1H ЯМР (ДМСО-d6): δ 0,87 (м, 6H), 1,56 (м, 2H), 1,74 (м, 4H), 2,66 (т, 2H, J=5,4 Гц), 2,86 (т, 2H, J=5,4 Гц), 3,68 (м, 4H), 3,85 (т, 2H, J=7,5 Гц), 3,99 (т, 2H, J=7,5 Гц), 6,72 (д, 1H, J=9,0 Гц), 8,10 (дд, 1Н, J1=2,4 Гц, J2=9,0 Гц), 8,77 (д, 1H, J=2,4 Гц).
МС: m/z 412 (М+H)+.
Соединение 59: 1,3-Диэтил-8-(6-хлор-3-пиридил)ксантин
1H ЯМР (ДМСО-d6): δ 1,14 (т, 3H, J=6,9 Гц), 1,26 (т, 3H, J=6,9 Гц), 3,94 (кв, 2H, J=6,9 Гц), 4,09 (кв, 2H, J=6,9 Гц), 7,68 (д, 1H, J=8,4 Гц), 8,46 (дд, 1H, J1=2,4 Гц, J2=8,4 Гц), 9,07 (д, 1H, J=2,4 Гц).
МС: m/z 320 (М+H)+,
Соединение 60: 1,3-Диэтил-8-(6-пиперазино-3-пиридил)ксантин
МС: m/z 370 (M+H)+.
Соединение 61: 1,3-Диэтил-8-[6-[(N-фенилкарбамоил)метиламино]-3-пиридил]ксантин
МС: m/z 434 (M+H)+.
Соединение 62: 1,3-Диэтил-8-[6-[N-никотиноилэтиламино]-3-пиридил]ксантин
МС: m/z 434 (M+H)+.
Соединение 63: 1,3-Диэтил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 315 (M+H)+.
Соединение 64: 1,3-Диэтил-8-[6-[N-никотиноилметиламино]-3-пиридил]ксантин
МС: m/z 420 (M+H)+.
Соединение 65: 1,3-Диэтил-8-[6-[N-никотиноилциклопропиламино]-3-пиридил]ксантин
МС: m/z 446 (M+H)+.
Соединение 66: 1,3-Дициклопропилметил-8-(6-метиламинопиридин-3-ил)ксантин
МС: m/z 367 (M+H)+.
Соединение 67: 1-Пропаргил-3-метил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 311 (M+H)+.
Соединение 68: 8-[6-(2,5-диазабицикло[2.2.2]окт-2-ил)пиридин-3-ил]-1,3-дипропил-3,7-дигидропурин-2,6-дион
МС: m/z 410 (M+H)+.
Соединение 69: 1,3-Дициклопропилметил-8-[6-[N-никотиноилметиламино]-3-пиридил]ксантин
МС: m/z 472 (M+H)+.
Соединение 70: 1,3-Дициклопропилметил-8-[6-[N-никотиноилэтиламино]-3-пиридил]ксантин
МС: m/z 486 (M+H)+.
Соединение 71: 1,3-Диаллил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 339 (M+H)+.
Соединение 72: 1-Циклопропил-3-этил-8-(6-метиламинопиридин-3-ил)ксантин
МС: m/z 342 (M+H)+.
Соединение 73: 1,3-Диэтил-8-[6-(2-пиридилметиламино)-3-пиридил]ксантин
МС: m/z 392 (M+H)+.
Соединение 74: 1,3-Диэтил-8-[6-(3-пиридилметиламино)-3-пиридил]ксантин
МС: m/z 392 (M+H)+.
Соединение 75: 1,3-Диэтил-8-[6-(3-метоксибензиламино)-3-пиридил]ксантин
МС: m/z 421 (M+H)+.
Соединение 76: 1,3-Дипропил-8-[6-[2-(3-пиридил)этиламино]-3-пиридил]ксантин
МС: m/z 434 (M+H)+.
Соединение 77: 1,3-Диэтил-8-[6-[2-(3-пиридил)этиламино]-3-пиридил]ксантин
МС: m/z 406 (M+H)+.
Соединение 78: 1,3-Дипропил-8-[6-[2-(2-пиридил)этиламино]-3-пиридил]ксантин
МС: m/z 434 (M+H)+.
Соединение 79: 1,3-Диэтил-8-[6-[2-(2-пиридил)этиламино]-3-пиридил]ксантин
МС: m/z 406 (M+H)+.
Соединение 80: 1,3-Диэтил-8-(6-пирролидинилпирид-3-ил)ксантин
МС: m/z 355 (M+H)+.
Соединение 81: 1,3-Диэтил-8-[6-[2-(1-пирролидинил)этиламино]-3-пиридил]ксантин
МС: m/z 398 (M+H)+.
Соединение 82: 1,3-Дипропил-8-(6-(2-метоксиэтил)амино-3-пиридил)ксантин
МС: m/z 387 (M+H)+.
Соединение 83: 1,3-Дипропил-8-(6-(2-ацетиламиноэтил)амино-3-пиридил)ксантин
МС: m/z 414 (M+H)+.
Соединение 84: 1,3-Диэтил-8-(6-бром-3-пиридил)ксантин
МС: m/z 364 (M+H)+.
Соединение 85: 1,3-Дипропил-8-{6-[4-(2-пиридил)пиперазино]-3-пиридил}ксантин
МС: m/z 475 (M+H)+.
Соединение 86: 1,3-Диэтил-8-{6-[4-(2-пиридил)пиперазино]-3-пиридил}ксантин
МС: m/z 447 (M+H)+.
Соединение 87: 1,3-Диэтил-8-[6-(транс-2,5-диметилпиперазино)-3-пиридил]ксантин
МС: m/z 398 (M+H)+.
Соединение 88: 1,3-Дипропил-8-{6-[4-(2-пиримидинил)пиперазино]-3-пиридил}ксантин
МС: m/z 476 (M+H)+.
Соединение 89: 1,3-Диэтил-8-{6-[4-(2-пиримидинил)пиперазино]-3-пиридил}ксантин
МС: m/z 448 (M+H)+.
Соединение 90: 1,3-Диэтил-8-(6-(2-метоксиэтил)амино-3-пиридил)ксантин
МС: m/z 359 (M+H)+.
Соединение 91: 1-Пропаргил-3-метил-8-(6-бром-3-пиридил)ксантин
МС: m/z 360 (M+H)+.
Соединение 92: 1,3-Диэтил-8-[6-[N-никотиноил-N-(2-метоксиэтил)амино]-3-пиридил]ксантин
МС: m/z 464 (M+H)+.
Соединение 93: 1-Пропаргил-3-метил-8-(6-(2-метоксиэтил)-3-пиридил)ксантин
МС: m/z 355 (M+H)+.
Соединение 94: 1,3-Диэтил-8-[6-[N-изоникотиноил-N-(2-метоксиэтил)амино]-3-пиридил]ксантин
МС: m/z 464 (M+H)+.
Соединение 95: 1-(5-(1,3-Диэтил-2,3,6,7-тетрагидро-2,6-диоксо-1Н-пурин-8-ил)пиридин-2-ил)-1-(2-метоксиэтил)-3-(пиридин-4-ил)мочевина
МС: m/z 479 (M+H)+.
Соединение 96: 1,3-Диметил-8-(6-бром-3-пиридил)ксантин
МС: m/z 460 (M+H)+.
Соединение 97: 1,3-Диметил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 287 (M+H)+.
Соединение 98: 1,3-Диметил-8-[6-[N-никотиноилметиламино]-3-пиридил]ксантин
МС: m/z 392 (M+H)+.
Соединение 99: 1,3-Дипропил-8-[6-[N-никотиноил-N-(2-метоксиэтил)амино]-3-пиридил]ксантин
МС: m/z 492 (M+H)+.
Соединение 100: 1-Пропаргил-3-метил-8-[6-[N-никотиноил-N-(2-метоксиэтил)амино]-3-пиридил]ксантин
МС: m/z 359 (M+H)+.
Соединение 101: 1-Пропаргил-3-метил-8-(6-[N-никотиноилметиламино]-3-пиридил]ксантин
МС: m/z 416 (M+H)+.
Соединение 102: 1,3-Дипропил-8-(2,6-дихлор-3-пиридил)ксантин
МС: m/z 382 (M+H)+.
Соединение 103: 1,3-Дипропил-8-(2,6-диметиламино-3-пиридил)ксантин
МС: m/z 372 (M+H)+.
Соединение 104: 1,3-Дипропил-8-(2,6-ди(2-метоксиэтил)-3-пиридил)ксантин
МС: m/z 460 (M+H)+.
Соединение 105: 1,3-Дипропил-8-[2,6-ди[N-никотиноилметиламино]-3-пиридил]ксантин
МС: m/z 582 (M+H)+.
Соединение 106: 1,3-Дипропил-8-[2,6-ди[N-никотиноил-N-метоксиэтил]-3-пиридил]ксантин
МС: m/z 670 (M+H)+.
Соединение 107: 1,3-Диэтил-8-[6-[N-(2-пиразинкарбонил)метиламино]-3-пиридил]ксантин
МС: m/z 421 (M+H)+.
Соединение 108: 1,3-Диэтил-8-[6-[N-(изоксазол-5-карбонил)метиламино]-3-пиридил]ксантин
МС: m/z 410 (M+H)+.
Соединение 109: 1,3-Дипропил-8-[6-[N-(2-пиразинкарбонил)метиламино]-3-пиридил]ксантин
МС: m/z 449 (M+H)+.
Соединение 110: 1,3-Дипропил-8-[6-[N-(изоксазол-5-карбонил)метиламино]-3-пиридил]ксантин
МС: m/z 438 (M+H)+.
Соединение 111: 1,3-Дипропил-8-[6-[N-(5-метилизоксазол-3-ил-3-карбонил)метиламино]-3-пиридил]ксантин
МС: m/z 452 (M+H)+.
Соединение 112: 1,3-Дипропил-8-[6-[N-(2-хлор-6-метоксипиридинил-4-карбонил)-N-метиламино]-3-пиридил]ксантин
МС: m/z 512 (M+H)+.
Соединение 113: 1,3-Дипропил-8-[6-[N-(изоникотиноил N-оксид) N-метиламино]-3-пиридил]ксантина
МС: m/z 464 (M+H)+.
Соединение 114: 1-пропил-3-(4-метоксифенил)этил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 435 (M+H)+.
Соединение 115: 1,3-Диэтил-8-[6-[N-(изоникотиноил N-оксид) N-метиламино]-3-пиридил]ксантина
МС: m/z 436 (M+H)+.
Соединение 116: 1,3-Диаллил-8-(6-хлор-3-пиридил)ксантин
МС: m/z 344 (M+H)+.
Соединение 117: 1-Пропил-3-(4-метоксифенил)этил-8-[6-(N-никотиноилметиламино)-3-пиридил]ксантин
МС: m/z 540 (M+H)+.
Соединение 118: 1-Пропил-3-(4-метоксифенил)этил-8-[6-(N-(6-хлорникотиноил)метиламино)-3-пиридил]ксантин
МС: m/z 574 (M+H)+.
Соединение 119: 1,3-Диаллил-8-[6-(N-никотиноилметиламино)-3-пиридил]ксантин
МС: m/z 444 (M+H)+.
Соединение 120: 1,3-Диаллил-8-[6-(N-(6-хлорникотиноил)метиламино)-3-пиридил]ксантин
МС: m/z 478 (M+H)+.
Соединение 121: 1,3-Дипропил-8-[6-(N-[6-(трифторметил)никотиноил]метиламино)-3-пиридил]ксантин
МС: m/z 516 (M+H)+.
Соединение 122: 1,3-Диэтил-8-[6-(2-гидрокси-5-метил)бензальдегидгидразоно]-3-пиридил]ксантин
МС: m/z 434 (M+H)+.
Соединение 123: 1-Циклопропил-3-пропил-8-[6-(N-[6-трифторметил)никотиноил]метиламино)-3-пиридил]ксантин
МС: m/z 446.
Соединение 124: 1,3-Диэтил-8-[6-(бромпиридин-3-карбальдегидгидразоно)-3-пиридил]ксантин
МС: m/z 483 (M+H)+.
Соединение 125: 1-Циклопропил-3-этил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 327 (M+H)+.
Соединение 126: 1-Циклопропил-3-пропил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 341 (M+H)+.
Соединение 127: 1-Пропил-3-циклопропил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 341 (M+H)+.
Соединение 128: 1-Циклопропил-3-пропил-8-(6-(2-метоксиэтил)амино-3-пиридил)ксантин
МС: m/z 385 (M+H)+.
Соединение 129: 1-Циклопропил-3-пропил-8-[6-[N-никотиноилметиламино]-3-пиридил]ксантин
МС: m/z 446 (M+H)+.
Соединение 130: 1,3-Диэтил-8-[6-(N-(6-хлорникотиноил)метиламино)-3-пиридил]ксантин
МС: m/z 454 (M+H)+.
Соединение 131: 1,3-Дипропил-8-(2-хлор-6-метоксиэтиламино)-4-пиридил]ксантин
МС: m/z 421 (M+H)+.
Соединение 132: 1,3-Дипропил-8-(2-хлор-6-метиламино)-4-пиридил]ксантин
МС: m/z 377 (M+H)+.
Соединение 133: 1,3-Дипропил-8-[2-[N-никотиноил-N-(2-метоксиэтил)амино]-6-хлор-4-пиридил]ксантин
МС: m/z 527 (M+H)+.
Соединение 134: 1,3-Дипропил-8-[2-[N-никотиноил-N-метиламино]-6-хлор-4-пиридил]ксантин
МС: m/z 482 (M+H)+.
Соединение 135: 1-Циклопропил-3-пропил-8-[6-[N-(6-хлорникотиноил)метиламино]-3-пиридил]ксантин
МС: m/z 480 (M+H)+.
Соединение 136: 1-Этил-3-циклопропил-8-(6-метиламино-3-пиридил)ксантин
МС: m/z 327 (M+H)+.
Соединение 137: 1-Этил-3-циклопропил-8-(6-(2-метоксиэтил)амино-3-пиридил)ксантин
МС: m/z 371 (M+H)+.
Соединение 138: 1,3-Диэтил-8-[6-гидразино-3-пиридил]ксантин
МС: m/z 316 (M+H)+.
Соединение 139: 1,3-Диэтил-8-[6-(циклопропиламино)-3-пиридил]ксантин
МС: m/z 341 (M+H)+.
Соединение 140: 1,3-Диэтил-8-[6-(циклопропилметиламино)-3-пиридил]ксантин
МС: m/z 355 (M+H)+.
Соединение 141: N'-[5-(1,3-диэтил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)пиридин-2-ил]гидразид
МС: m/z 421 (M+H)+.
Соединение 142: N-[5-(1,3-диэтил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)пиридин-2-ил]-N'-(пиридин-3-карбонил)гидразид
МС: m/z 526 (M+H)+.
Соединение 143: 1,3-Диэтил-8-[6-(этиламино)-3-пиридил]ксантин
МС: m/z 329 (M+H)+.
Соединение 144: 1,3-Диэтил-8-[6-[N-никотиноилциклопропилметиламино]-3-пиридил]ксантин
МС: m/z 460 (M+H)+.
Соединение 145: 1-Циклопропилметил-3-этил-8-[6-[N-(6-хлорникотиноил)метиламино]-3-пиридил]ксантин
МС: m/z 480 (M+H)+.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОМОТИРУЮЩАЯ ДЕФЕКАЦИЮ | 2001 |
|
RU2294762C2 |
| СОЕДИНЕНИЕ, НАЦЕЛЕННОЕ НА БЕЛОК И ЕГО ДЕГРАДАЦИЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2829459C1 |
| ПРОИЗВОДНЫЕ ИМИДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ TAFIa | 2005 |
|
RU2375356C2 |
| ПРОИЗВОДНЫЕ АКРИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2001 |
|
RU2267488C2 |
| НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ BRD4 | 2016 |
|
RU2721120C2 |
| АЦИЛИРОВАННЫЕ ИНДАНИЛАМИНЫ И ИХ ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2002 |
|
RU2339614C2 |
| ИНГИБИТОРЫ ПРОЛИЛГИДРОКСИЛАЗЫ | 2010 |
|
RU2518071C2 |
| ИНГИБИТОРЫ АКТИВНОСТИ ПРОТЕИНТИРОЗИНКИНАЗЫ | 2009 |
|
RU2533827C2 |
| АНТАГОНИСТЫ ВИТРОНЕКТИНОВОГО РЕЦЕПТОРА, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 1997 |
|
RU2198892C2 |
| ЗАМЕЩЕННЫЕ АЗОЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2047604C1 |
Настоящее изобретение относится к замещенным 8-гетероарилксантинам общей формулы I, где R представляет водород, (C1-С5)алкил или галоген(С1-С8)алкил; R1 выбран из (С3-С6)циклоалкила или (С3-С6)циклоалкил(С1-С4)алкила-; R2 выбран из (С1-С8)алкила, (С3-С8)алкенила, (С3-С8)алкинила, (С3-С8)циклоалкила, (С3-С8)циклоалкил(С1-С8)алкила- или (С6-С10)арил(С1-С8)алкила-; Х представляет собой 3-пиридил, замещенный в 6-м положении Z; Z представляет собой -NR4R5 или (С4-С10)гетероцикл, где гетероцикл необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из (С1-С8)алкила; каждый Z1 представляет собой независимо галоген или -NR7R8; R5 выбран из -C(O)R6, -CO2R6 или -C(O)NHR7; R4 выбран из водорода, (C1-C8)алкила, (С3-С8)циклоалкила, (С3-С8)циклоалкил(С1-С8)алкила-, (С3-С10)гетероцикл(С1-С8)алкила-, (С6-С10)арила, (С6-С10)арил(С1-С8)алкила-, (С5-С10)гетероарила, (C5-С10)гетероарил(С1-С8)алкила-, -((CH2)2-4)Y)q-(CH2)2-4-X1 -C(O)R6, -CO2R6 или -C(O)NR7R8; или R4 и R5 вместе с атомами, к которым они присоединены, образуют насыщенное моно- или бициклическое кольцо, имеющее 5, 6, 7 или 8 кольцевых атомов и необязательно содержащее 1 или 2 гетероатома, выбранных из непероксидного окси (-O-) и амина -N(R9)- в кольце, и где кольцо необязательно замещено 1, 2, 3 или 4 заместителями, независимо выбранными из -C(O)Ra и -C(O)NRbRc; X1 представляет собой -OR6; и Y представляет собой окси (-O-); где алкильная, алкенильная, циклоалкильная, алкинильная, арильная, гетероциклическая или гетероарильная группы из R1, R2, R3, R4 и R5 групп необязательно замещены одним или более заместителями, выбранными независимо из (С1-С8)алкила, -ORa, (С6-С10)арила, гидрокси(С1-С8)алкила и RbRcN(C1-C8)алкила; где R6 представляет собой (C1-C8)алкил или (С4-С10)гетероарил; где гетероарил необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, -ORа и галоген(С1-С8)алкила; где R7, R8 и R9 представляют независимо (C1-С8)алкил, RaO(C1-C8)алкил, (С6-С10)арил или (С4-С10)гетероарил; где гетероарил или арил необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из галогена и -ORa; Ra представляет водород или (С1-С6)алкил; Rb и Rc каждый независимо представляет водород или (С6-С10)арил; и где n равно 0, 1 или 2; и q равно 1; или его фармацевтически приемлемая соль. Также изобретение относится к фармацевтической композиции на основе соединения формулы I. Технический результат: получены новые замещенные 8-гетероарилксантинов, которые являются селективными антагонистами рецепторов А2B аденозина (AR). 3 н. и 35 з.п. ф-лы, 1 табл.
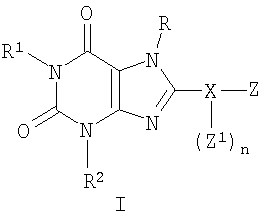
1. Соединение формулы I:
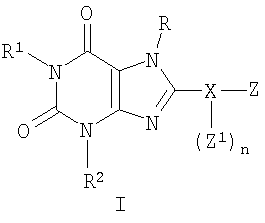
в которой
R представляет водород, (С1-С5)алкил или галоген(С1-С8)алкил;
R1 выбран из (С3-С6)циклоалкила или (С3-С6)циклоалкил(С1-С4)алкила-;
R2 выбран из (С1-С8)алкила, (С3-С8)алкенила, (С3-С8)алкинила, (С3-С8)циклоалкила, (С3-С8)циклоалкил(С1-С8)алкила- или (С6-С10)арил(С1-С8)алкила-;
Х представляет собой 3-пиридил, замещенный в 6-м положении Z;
Z представляет собой -NR4R5 или (С4-С10)гетероцикл, где гетероцикл необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из (C1-C8)алкила;
каждый Z1 представляет собой независимо галоген или -NR7R8;
R5 выбран из -C(O)R6, -CO2R6 или -C(O)NHR7;
R4 выбран из водорода, (С1-С8)алкила, (С3-С8)циклоалкила, (С3-С8)циклоалкил(С1-С8)алкила-, (С3-С10)гетероцикл(С1-С8)алкила-, (С6-С10)арила, (С6-С10)арил(С1-С8)алкила-, (С5-С10)гетероарила, (С5-С10)гетероарил(С1-С8)алкила-, -((CH2)2-4)Y)q-(CH2)2-4-X1, -C(O)R6, -CO2R6 или -C(O)NR7R8;
или R4 и R5 вместе с атомами, к которым они присоединены, образуют насыщенное моно- или бициклическое кольцо, имеющее 5, 6, 7 или 8 кольцевых атомов и необязательно содержащее 1 или 2 гетероатома, выбранных из непероксидного окси
(-O-) и амина -N(R9)- в кольце, и где кольцо необязательно замещено 1, 2, 3 или 4 заместителями, независимо выбранными из -C(O)Ra и -C(O)NRbRc;
X1 представляет собой -OR6; и Y представляет собой окси (-O-);
где алкильная, алкенильная, циклоалкильная, алкинильная, арильная, гетероциклическая или гетероарильная группы из R1, R2, R3, R4 и R5 групп необязательно замещены одним или более заместителями, выбранными независимо из (C1-C8)алкила, -ORа, (С6-С10)арила, гидрокси(С1-С8)алкила и RbRcN(C1-C8)алкила;
где R6 представляет собой (С1-С8)алкил или (С4-С10)гетероарил; где гетероарил необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из галогена, -ORa и галоген(С1-С8)алкила;
где R7, R8 и R9 представляют независимо (С1-С8)алкил, RaO(C1-C8)алкил, (С6-С10)арил или (С4-С10)гетероарил; где гетероарил или арил необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из галогена и -ORa;
Ra представляет водород или (С1-С6)алкил;
Rb и Rc каждый независимо представляет водород или (С6-С10)арил; и
где n равно 0, 1 или 2; и q равно 1;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где R представляет собой водород, метил, этил, изопропил, н-пропил, н-бутил, изобутил или галоген(С1-С4)алкил.
3. Соединение по п.1, где R представляет собой водород, метил, этил, -СН2-СН2-Cl, -СН2-СН2-Br или -CH2-CH2-CH2-F.
4. Соединение по п.1, где R представляет собой водород.
5. Соединение по п.1, где R1 представляет собой циклопропил или циклопропилметил.
6. Соединение по п.1, где R2 представляет собой (С1-С4)алкил, (С3-С4)алкенил,
(С3-С4)алкинил, фенил(С1-С4)алкил или (метоксифенил)этил.
7. Соединение по п.1, где R2 представляет собой (С3-С6)циклоалкил или (С3-С6)циклоалкил(С1-С4)алкил-.
8. Соединение по п.1, где R2 представляет собой циклопропил или циклопропилметил.
9. Соединение по п.1, где R2 представляет собой метил, этил, аллил, пропаргил, изопропил, н-пропил, н-бутил, изобутил, фенетил или бензил.
10. Соединение по п.1, где R2 представляет собой этил, н-пропил или аллил.
11. Соединение по п.1, где Z представляет собой -NR4R5.
12. Соединение по п.1, где R4 представляет собой водород, (С1-С6)алкил, (С3-С6)циклоалкил, (С3-С6)циклоалкил(С1-С4)алкил-, (С6-С10)арил, (С6-С10)арил(С1-С4)алкил-, (С5-С6)гетероарил, (С5-С6)гетероарил(С1-С4)алкил, -C(O)R6, -CO2R6 или -C(O)NR7R8.
13. Соединение по п.1, где R4 представляет собой водород, (С1-С4)алкил, гидрокси(С2-С4)алкил, (С3-С6)циклоалкил, (С6-С10)арил, (С7-С10)аралкил, (С5-С6)гетероарил, -(CH2-CH2-O)q(CH2-CH2)-ORa, -C(O)R6, -CO2R6 или -C(O)NR7R8.
14. Соединение по п.1, где R4 представляет собой водород, метил, этил, пропил, пентил, гидроксиэтил, гидроксипропил, этоксиэтил, диэтоксиэтил, аминометилбензил, метоксибензил, метоксифенетил, фурилметил, циклопропил, циклопропилметил, циклопентил, циклогексил, тиофенил, -C(O)R6, -CO2R6 или -C(O)NHR7.
15. Соединение по п.1, где R4 представляет собой метил, этил, циклопропил, циклопропилметил, -C(O)R6, -CO2R6 или -C(O)NHR7.
16. Соединение по п.1, где R4 и R5, взятые вместе с азотом, к которому они присоединены, представляет пирролидильное, пиперидильное, пиперазинильное, азепинильное, диазепинильное или морфолинильное кольцо, каждое необязательно замещенное 1, 2, 3 или 4 заместителями, независимо выбранными из -C(O)Ra и -C(O)NRbRc.
17. Соединение по п.1, где R6 представляет собой (С1-С6)алкил или (С5-С6)гетероарил, каждый необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ORa и галоген(С1-С8)алкила.
18. Соединение по п.1, где R6 представляет собой (С5-С6)гетероарил, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из галогена и галоген(С1-С8)алкила.
19. Соединение по п.1, где R6 представляет собой пиридил, необязательно замещенный F, Cl, Br, I или CF3.
20. Соединение по п.1, где
R представляет водород, метил или этил;
R1 выбран из циклопропила или циклопропилметила;
R2 выбран из метила, этила, аллила, пропаргила, изопропила, н-пропила, циклопропила, циклопропилметила или н-бутила; и
Х представляет собой 3-пиридил, замещенный в положении 6 заместителем Z, где Z представляет собой (С4-С10)гетероцикл или -NR4R5, где R4 представляет собой метил, этил, циклопропил, циклопропилметил, и R5 представляет собой -C(O)R6, где R6 представляет собой гетероарил, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из галогена и галоген(С1-С8)алкила.
21. Соединение по п.1, где R2 выбран из (С1-С4)алкила, (С3-С4)алкенила, (С3-С4)алкинила или фенил(С1-С4)алкила.
22. Соединение по п.1, где R представляет собой водород, метил, этил, изопропил, н-пропил, н-бутил, изобутил или галоген(С1-С4)алкил; и
R1 выбран из циклопропила и циклопилметила;
R2 представляет собой независимо метил, этил, аллил, пропаргил, изопропил, н-пропил, циклопропил, циклопропилметил, н-бутил, изобутил, фенетил или бензил.
23. Соединение по п.1, где R представляет собой водород, метил, этил, -СН2-СН2-Cl, -СН2-СН2-Br или -CH2-CH2-CH2-F; и
R1 выбран из циклопропила и циклопропилметила;
R2 представляет собой независимо метил, этил, аллил, пропаргил, изопропил, н-пропил, циклопропил, циклопропилметил или (метоксифенил)этил.
24. Соединение по п.1, где Z представляет собой -NR4R5, где R4 выбран из водорода, (С1-С6)алкила, (С3-С6)циклоалкила, (С6-С10)арила, (C7-С12)аралкила, (С5-С6)гетероарила, (С5-С6)гетероарил(С1-С4)алкила-, -C(O)R6, -CO2R6 или -C(O)NR7R8.
25. Соединение по п.1, где Z представляет -NR4R5.
26. Соединение по п.1, где R4 и R5 вместе с азотом, к которому они присоединены, образуют пирролидильное, пиперидильное, пиперазинильное, азепинильное, диазепинильное или морфолинильное кольцо, где кольцо необязательно замещено 1, 2, 3 или 4 заместителями, независимо выбранными из -COORa и -C(O)NRbRc.
27. Соединение по п.1, где R4 выбран из водорода, (С1-С4)алкила, гидрокси(С2-С4)алкила, (С3-С6)циклоалкила, (С6-С10)арила, (С7-С10)аралкила, (C5-С6)гетероарила, -(CH2-CH2-O)q(CH2-CH2)-ORa, -C(O)R6, -CO2R6 или -C(O)NR7R8.
28. Соединение по п.1, где R4 выбран из водорода, метила, этила, пропила, пентила, гидроксиэтила, гидроксипропила, этоксиэтила, диэтоксиэтила, аминометилбензила, метоксибензила, метоксифенетила, фурилметила, циклопентила, циклогексила, тиофенила, -C(O)R6, -CO2R6 или -C(O)NHR7.
29. Соединение по п.1, где R6 представляет собой метил или пиридил, и R7 представляет собой фенил, фторфенил или метоксифенил.
30. Соединение по п.1, где
R представляет собой водород, метил или этил;
R1 выбран из циклопропила или циклопропилметила;
R2 выбран из метила, этила, аллила, пропаргила, изопропила, н-пропила, циклопропила, циклопропилметила, н-бутила и изобутила; и
Z представляет собой (С4-С10)гетероцикл.
31. Соединение по п.1, где Z выбран из группы, состоящей из
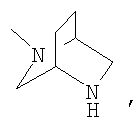
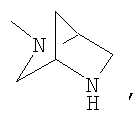
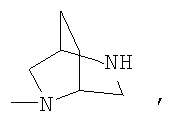
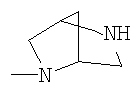
32. Соединение по п.1, где -X(Z1)n-Z выбран из группы, состоящей из
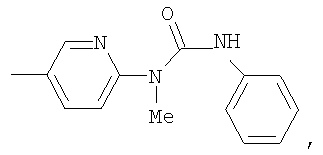
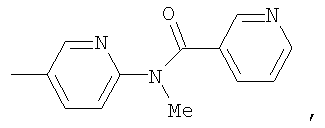
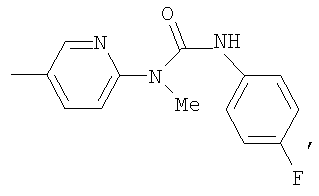
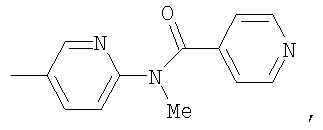
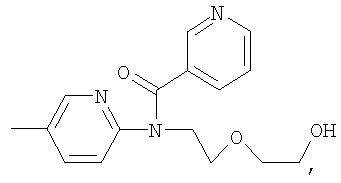
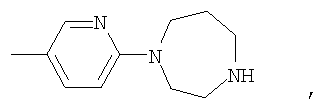
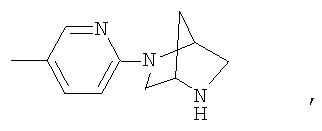
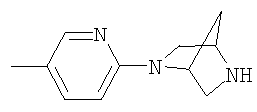
33. Соединение по п.1, где R2 представляет собой н-пропил; R представляет водород и n равно нулю.
34. Соединение по п.1, где -X(Z1)n-Z выбран из группы, состоящей из
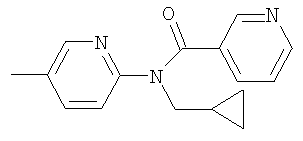
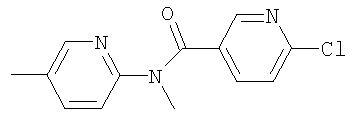
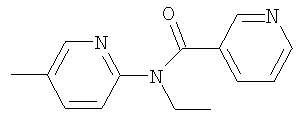
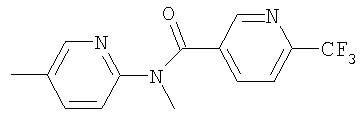
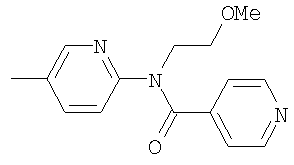
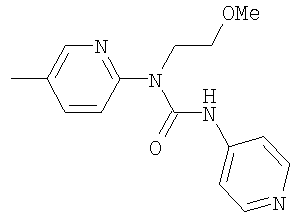
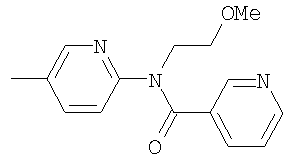

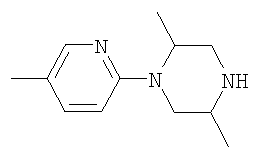
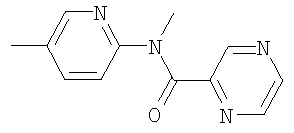
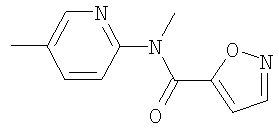
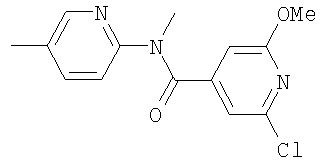
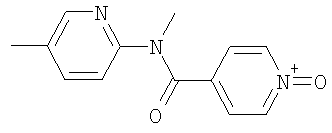
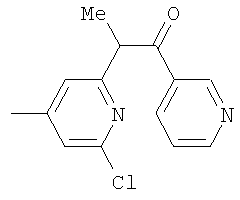
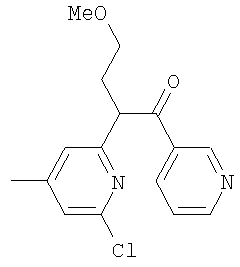
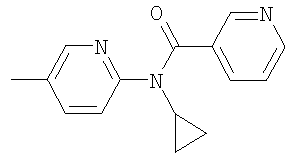
35. Соединение по п.1, которое представляет собой:
1-циклопропил-3-пропил-8-[6-[N-никотиноилметиламино]-3-пиридил]ксантин;
или его фармацевтически приемлемую соль.
36. Соединение по п.1, выбранное из группы, состоящей из:
1,3-дициклопропилметил-8-[6-[N-никотиноилметиламино]-3-пиридил]ксантина;
1,3-дициклопропилметил-8-[6-[N-никотиноилэтиламино]-3-пиридил]ксантина;
1-циклопропил-3-пропил-8-[6-[N-никотиноилметиламино]-3-пиридил]ксантина;
1-циклопропил-3-пропил-8-[6-[N-(6-хлорникотиноил)метиламино]-3-пиридил]ксантина;
1-циклопропил-3-этил-8-[6-[N-(6-хлорникотиноил)метиламино]-3-пиридил]ксантина;
или их фармацевтически приемлемых солей.
37. Фармацевтическая композиция, обладающая активностью антагониста в отношении А2B рецепторов аденозина, содержащая:
(a) терапевтически эффективное количество соединения по п.1 и
(b) фармацевтически приемлемый эксципиент.
38. Фармацевтическая композиция, обладающая активностью антагониста в отношении А2B рецепторов аденозина, содержащая:
(a) терапевтически эффективное количество соединения по п.36 и
(b) фармацевтически приемлемый эксципиент.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| KUZ'MENKO I I ET AL: "Reactions of theophyllines | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| CHEMESTRY OF HETEROCYCLIC COMPOUNDS, vol.36, no.8, 2000, pages 963-970 | |||
| SEKINE, TOSHIKAZU ET AL: "Dimerizations of | |||
| pi.-rich N-heteroaromatic compounds and xanthine derivatives" | |||
| CHEMICAL AND | |||
Авторы
Даты
2009-06-10—Публикация
2004-08-20—Подача