Изобретение относится к новым соединениям формулы (I), которые ингибируют фермент TAFIa (активированный ингибитор активируемого тромбином фибринолиза), способу их получения и применению в качестве лекарственного средства.
Фермент TAFIa образуется, например, за счет активирования тромбина из зимогена ингибитора активируемого тромбином фибринолиза (TAFI). Фермент TAFI называют также как прокарбоксипептидаза В, прокарбоксипептидаза U или как прокарбоксипептидаза R плазмы и он представляет собой подобный карбоксипептидазе В профермент (L. Bajzar, Arterioscler. Thromb. Vasc. Biol., 2511-2518 (2000)).
Во время образования сгустка тромбин генерируется в качестве конечного продукта каскада коагуляций и индуцирует превращение растворимого фибриногена плазмы в нерастворимый фибриновый матрикс. Одновременно тромбин активирует эндогенный ингибитор фибринолиза TAFI. Активированный TAFI (TAFIа), следовательно, образуется во время образования тромба и лизиса из зимогена TAFI под воздействием тромбина, тромбомодулин в комплексе с тромбином усиливает этот эффект примерно в 1250 раз. TAFIа расщепляет основные С-концевые аминокислоты фибриновых фрагментов. Потеря С-концевых лизинов в качестве сайтов связывания плазминогена приводит тогда к ингибированию фибринолиза. Эффективные ингибиторы TAFIа предотвращают потерю этих высокоаффинных лизиновых сайтов связывания плазминогена и, таким образом, способствуют эндогенному фибринолизу за счет плазмина: ингибиторы TAFIа действуют профибринолитически.
Для поддерживания гемостаза в крови возникают механизмы, которые приводят к свертыванию крови и растворению сгустков; они находятся в равновесии. Когда нарушенное равновесие благоприятствует коагуляции, образуется фибрин в гораздо больших количествах, так что патологические процессы тромбообразования у человека могут приводить к тяжелым картинам болезни.
Точно также как избыточная коагуляция может приводить к серьезным, тромботически обусловленным картинам болезни, антитромботическая обработка связана с риском нежелательных кровотечений за счет нарушения образования необходимой гемостатической пробки. Ингибирование TAFIа усиливает - не влияя на коагуляцию и агрегацию тромбоцитов - эндогенный фибринолиз, то есть нарушенное равновесие сдвигается в пользу фибринолиза. Таким образом, можно как противодействовать образованию клинически существенного тромба, так и также усиливать лизис уже существующего сгустка. С другой стороны, не ухудшается образование гемостатической пробки, так что больше нельзя ожидать диатеза кровотечения (Bouma и др., J. Thrombosis and Haemostasis, 1, 1566-1574 (2003)).
Ингибиторы TAFIа уже описаны в Международных заявках WO-03/013526 и WO-03/061653.
Предлагаемые согласно изобретению ингибиторы TAFIа пригодны для профилактического, а также терапевтического применения в отношении человека, страдающего заболеваниями, протекающими с тромбозами, эмболиями, гиперкоагулируемостью или фиброзными изменениями. Они пригодны как для экстренной, так и также для долговременной терапии.
Изобретение относится, следовательно, к соединению формулы (I):
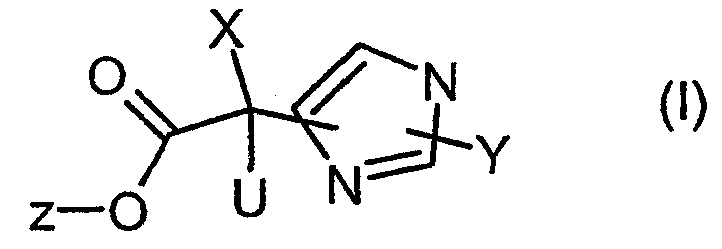
и/или всем стереоизомерным формам соединения формулы (I) и/или смесям этих форм в любом соотношении и/или физиологически приемлемой соли соединения формулы (I), причем
U означает 1) атом водорода; 2) -(С1-С6)-алкил; 3) -(С3-С6)-циклоалкил; 4) фтор; 5) -О-СF3 или 6) -CF3;
Х означает остаток формулы (II):
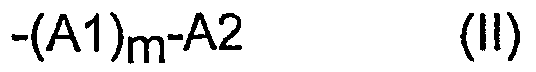 ,
,
где
m означает целое число ноль или 1;
А1 означает 1) -(СН2)n-, где n означает целое число 1, 2 или 3; или 2) -О-(СН2)n-, где n означает целое число ноль, 1, 2 или 3;
А2 означает
1) 4-15-членный гетероцикл, где гетероцикл содержит по меньшей мере один N-атом и замещен аминогруппой и дополнительно, независимо друг от друга, может быть одно-, двух- или трехкратно замещен -(С1-С3)-алкилом, галогеном, -CF3 или -О-CF3;
2) -(С1-С6)-алкил-NH2; или
3) -(С3-С8)-циклоалкил-NH2;
Y означает 1) остаток формулы (III):
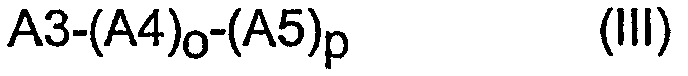 ,
,
причем
а) А3 означает (С3-С8)-циклоалкил или (С2-С6)-алкинилен, где циклоалкил или алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью -О-R10 или R1,
А4 означает -N(R2)2-, где R2 имеет нижеуказанное значение и значение обоих остатков R2 являются независимыми друг от друга,
А5 отсутствует, о означает целое число ноль или 1 и R10 означает атом водорода, -(С1-С6)-алкил или -(С6-С14)-арил;
b) А3 означает -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью -О-R10 или R1,
А4 означает -N(R2)- и
А5 означает а)1) -С(О)-R3; a)2) -C(O)-N(R4)-R5; a)3) -(SO2)-R6 или а)4) -C(O)-O-R7;
о означает целое число 1 и
р означает целое число 1;
с) А3 означает циклический амин с 3-8 атомами в цикле, где циклический амин незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 имеют указанное в п.b) значение, причем
А5 связан с N-атомом А3,
о означает целое число ноль и
р означает целое число ноль или 1; или
d) А3 означает -(СН2)q-(C6-H14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 имеют указанное в п.b) значение,
о означает целое число ноль или 1,
р означает целое число 1, и
q означает целое число ноль, 1, 2 или 3;
е) А3 означает -(СН2)r-Het, где Het означает 4-15-членный гетероцикл и гетероцикл незамещен или, независимо друг от друга, одно, двух- или трехкратно замещен с помощью =О или R1,
А4 и А5 имеют указанное в п.b) значение,
о означает целое число ноль или 1,
р означает целое число 1, и
r означает целое число ноль, 1, 2 или 3;
f) А3 означает -(СН2)q-(C6-H14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -О-,
А5 означает -(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух или трехкратно замещен с помощью R1,
о и р означают целое число 1, и
q означает целое число ноль, 1, 2 или 3;
g) -СН(-(С6-С14)-арил)-(С6-С14)-арил;
причем R1 означает
а) -(С6-С14)-арил, причем арил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С6)-алкилом, -(С0-С4)-алкил-(С3-С8)-циклоалкилом, -CF3, =O, -O-CF3 или галогеном,
b) 4-15-членный гетероцикл,
с) -(С1-С6)-алкил,
d) -(С0-С4)-алкил-(С3-С8)-циклоалкил,
е) -CF3,
f) -O-CF3, или
g) галоген;
причем R2 означает:
а) -(С6-С14)-арил, где арил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен с помощью R1,
b) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -СF3 или
е) атом водорода;
причем R3, R6 и R7 являются одинаковыми или разными и,
независимо друг от друга, означают:
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) 4-15-членный гетероцикл, где гетероцикл незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
е) атом водорода;
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
а) -(С1-С6)-алкил или -(С2-С10)-алкенил, где алкил или алкенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) 4-15-членный гетероцикл, где гетероцикл незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
е) атом водорода, или
R4 и R5 вместе с атомом азота, с которым они связаны, образуют 3-8-членный цикл, который дополнительно к атому азота может содержать еще вплоть до двух дополнительных гетероатомов из ряда, включающего кислород, серу или азот;
Y означает 2) остаток формулы (IV):
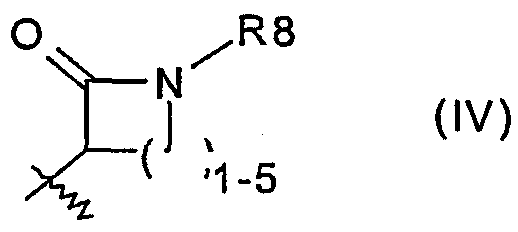
причем R8 означает
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) 4-15-членный гетероцикл, где гетероцикл незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
е) атом водорода;
Y означает 3) остаток формулы (V):
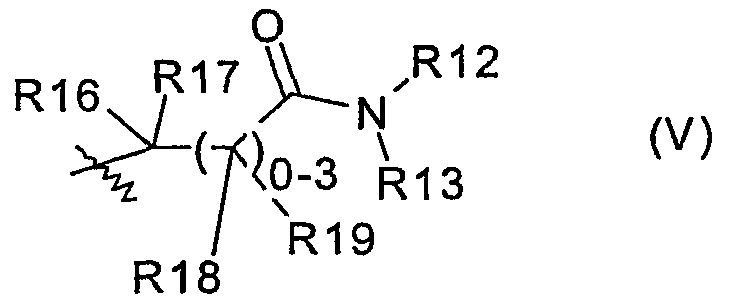
причем в случае а):
R12 означает
1) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
2) -(С0-С3)-алкил-(С3-С6)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
3) -(С0-С3)-алкил-(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
4) -(С0-С3)-алкил-Het, где Het незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1; и
R13 означает
1) -(С0-С3)-алкил-(С6-С14)-арил, где алкил и арил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
2) -(С0-С3)-алкил-Het, где алкил и Het, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1;
причем в случае b):
R12 означает
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
3) -(С0-С3)-алкил-(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
4) -(С0-С3)-алкил-Het, где Het незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1; и
R13 означает -СН(R8)-R9, причем R8 и R9, независимо друг от друга, означают -(С6-С14)-арил или Het, где Het и арил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены -О-(С1-С4)-алкилом или R1, и
R16, R17, R18 и R19 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно- или двухкратно замещен с помощью R1,
3) галоген,
4) -ОН,
5) -NH2,
6) -(С0-С3)-алкил-(С6-С14)-арил, где алкил и арил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
7) -(С0-С3)-алкил-Het, где алкил и Het, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
R16 и R17 или R18 и R19 вместе с атомом углерода, с которым они, соответственно, связаны, образуют 3-8-членный цикл; или
Y означает 4) остаток формулы (VI):
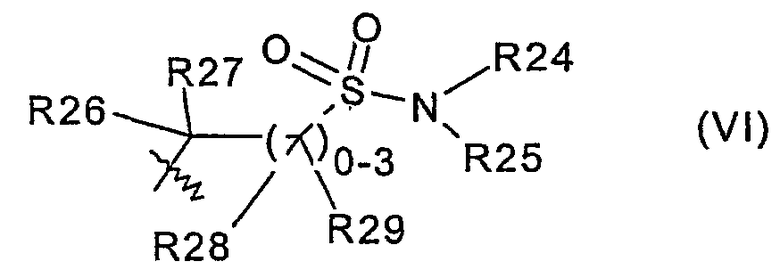
причем
R24 и R25 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно- или двухкратно замещен с помощью R1,
3) -(С0-С3)-алкил-(С6-С14)-арил, где алкил и арил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
4)-(С0-С3)-алкил-Het, где алкил и Het, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
5) -(С0-С3)-алкил-(С3-С6)-циклоалкил, или
R24 и R25 вместе с атомом азота, с которым они связаны, образуют 3-8-членный цикл, который дополнительно к атому азота может содержать еще вплоть до двух дополнительных гетероатомов из ряда, включающего кислород, серу или азот;
R26, R27, R28 и R29 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1,
3) галоген,
4) -ОН,
5) -NH2,
6) -(С0-С3)-алкил-(С6-С14)-арил, где алкил и арил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
7) -(С0-С3)-алкил-Het, где алкил и Het, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
R26 и R27 или R28 и R29 вместе с атомом углерода, с которым они, соответственно, связаны, образуют 3-8-членный цикл;
Z означает
1) атом водорода,
2) -(С1-С6)-алкил,
3) -(С1-С6)-алкил-ОН,
4) -(С0-С4)-алкил-(С3-С6)-циклоалкил,
5) -(С1-С10)-алкил-О-С(О)-О-R1,
6) -(СН2)r-алкил-(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1 и r означает целое число ноль, 1, 2 или 3, или
7) -(СН2)s-Het, где Het незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1 и s означает целое число ноль, 1, 2 или 3.
Дальнейшим объектом изобретения является соединение формулы (Ia):
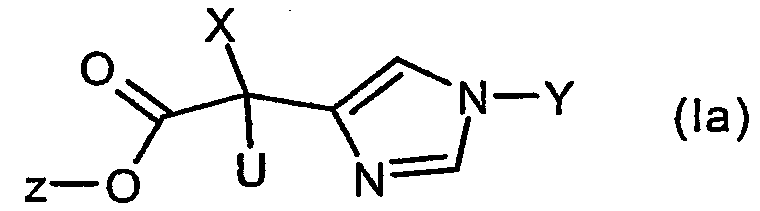
причем
U означает 1) атом водорода; 2) -(С1-С6)-алкил; 3) -(С3-С6)-циклоалкил; 4) фтор; 5) -О-СF3 или 6) -CF3;
Х означает остаток формулы (II),
где
M означает целое число ноль или 1;
А1 означает 1) -(СН2)n-, где n означает целое число 1, 2 или 3; или 2) -О-(СН2)n-, где n означает целое число ноль, 1, 2 или 3;
А2 означает
1) 4-15-членный гетероцикл, где гетероцикл выбирают из группы, состоящей из акридинила, азепинила, азетидинила, азиридинила, бензимидазалинила, бензимидазолила, карболинила, хиназолинила, хинолинила, 4Н-хинолизинила, хиноксалинила, хинуклидинила, хроманила, хроменила, циннолинила, декагидрохинолинила, имидазолидинила, имидазолинила, имидазолила, 1Н-индазолила, индолинила, индолизинила, индолила, 3Н-индолила, изобензофуранила, изохроманила, изоиндазолила, изоиндолинила, изоиндолила, изохинолинила (бензимидазолил), изотиазолидинила, 2-изотиазолинила, изотиазолила, изоксазолила, изоксазолидинила, 2-изоксазолинила, морфолинила, нафтиридинила, октагидроизохинолинила, оксадиазолила, 1,2,3-оксадиазолила, 1,2,4-оксадиазолила, 1,2,5-оксадиазолила, 1,3,4-оксадиазолила, оксазолидинила, оксазолила, пиримидинила, фенантридинила, фенантролинила, феназинила, фенотиазинила, феноксатиинила, феноксазинила, фталазинила, пиперазинила, пиперидинила, птеридинила, пуринила, пиранила, пиразинила, пироазолидинила, пиразолинила, пиразолила, пиридазинила, пиридооксазолила, пиридоимидазолила, пиридотиазолила, пиридотиофенила, пиридинила, пиридила, пиримидинила, пирролидинила, пирролинила, 2Н-пирролила, пирролила, тетрагидроизохинолинила, тетрагидрохинолинила, тетрагидропиридинила, 6Н-1,2,5-тиадазинила, 1,2,4-тиадиазолила, 1,2,5-тиадиазолила, 1,3,4-тиадиазолила, тиантренила, тиазолила, тиенотиазолила, тиенооксазолила, тиеноимидазолила, тиоморфолинила, триазинила, 1,2,3-триазолила, 1,2,4-триазолила, 1,2,5-триазолила, 1,3,4-триазолила и ксантенила, и где гетероцикл замещен аминогруппой и, независимо друг от друга, может быть дополнительно одно-, двух- или трехкратно замещен (С1-С3)-алкилом, галогеном, -CF3 или -O-CF3;
2) -(С1-С6)-алкил-NH2; или
3) -(С3-С8)-циклоалкил-NH2;
Y означает 1) остаток формулы (III), причем
а) А3 означает (С3-С8)-циклоалкил или (С2-С6)-алкинилен, где циклоалкил или алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -N(R2)2-, где R2 имеет нижеуказанное значение и значение обоих остатков R2 является независимым друг от друга,
А5 отсутствует, и
о означает целое число ноль или 1;
b) А3 означает -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -N(R2)-, и
А5 означает а)1) -С(О)-R3; a)2) -C(O)-N(R4)-R5; a)3) -(SO2)-R6 или а)4) -C(O)-O-R7;
о означает целое число 1, и
р означает целое число 1;
с) А3 означает циклический амин из группы, состоящей из пропиламина, азетидина, пирролидина, пиперидина, азепана или азокана, где циклический амин незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 имеют указанное в п.b) значение, причем
А5 связан с N-атомом А3,
о означает целое число ноль, и
р означает целое число ноль или 1; или
d) А3 означает -(СН2)q-(C6-H14)-арил, где арил выбирают из группы, состоящей из фенила, нафтила, антрила или флуоренила, и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 имеют указанное в п.b) значение,
о означает целое число ноль или 1,
р означает целое число 1, и
q означает целое число ноль, 1, 2 или 3;
е) А3 означает -(СН2)r-Het, где Het имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно, двух- или трехкратно замещен с помощью =О или R1,
А4 и А5 имеют указанное в п.b) значение,
о означает целое число ноль или 1,
р означает целое число 1, и
r означает целое число ноль, 1, 2 или 3;
f) А3 означает -(СН2)q-(C6-H14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -О-,
А5 означает -(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух или трехкратно замещен с помощью R1,
о и р означают целое число 1, и
q означает целое число ноль, 1, 2 или 3;
g) -СН(фенил)фенил;
причем R1 означает
а) -(С6-С14)-арил, где арил имеет вышеуказанное значение и причем арил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С6)-алкилом, -(С0-С4)-алкил-(С3-С8)-циклоалкилом, -CF3, =O, -O-CF3 или галогеном,
b) 4-15-членный гетероцикл, где гетероцикл имеет вышеуказанное значение,
с) -(С1-С6)-алкил,
d) -(С3-С8)-циклоалкил,
е) -CF3,
f) -O-CF3, или
g) галоген;
причем R2 означает:
а) -(С6-С14)-арил, где арил имеет вышеуказанное значение и незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен с помощью R1,
b) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -СF3, или
е) атом водорода;
причем R3, R6 и R7 являются одинаковыми или разными и,
независимо друг от друга, означают:
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -(С6-С14)-арил, где арил имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) 4-15-членный гетероцикл, где гетероцикл имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
е) атом водорода;
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
а) -(С1-С6)-алкил или -(С2-С10)-алкенил, где алкил или алкенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -(С6-С14)-арил, где арил имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) 4-15-членный гетероцикл, где гетероцикл имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
е) атом водорода, или
R4 и R5 вместе с атомом азота, с которым они связаны, образуют 3-8-членный цикл, выбираемый из группы, состоящей из пропиламина, азетидина, пирролидина, пиперидина, азепана, азокана, азепина, диоксазола, диоксазина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, [1,4]оксазепана, оксазола, пиперазина, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидинона, пирролина, тетрагидропиридина, тиазола, тиадиазола, тиазолидина, тиазолина, тиоморфолина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола;
Y означает 2) остаток формулы (IV), причем формуле (IV) отвечает соединение, выбранное из группы, состоящей из азетидин-2-она, пирролидин-2-она, пиперидин-2-она, азепан-2-она и азокан-2-она, и которое у атома азота, соответственно, замещено с помощью R8,
причем R8 означает
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -(С6-С14)-арил, где арил имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) 4-15-членный гетероцикл, где гетероцикл имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
е) атом водорода;
Y означает 3) остаток формулы (V),
причем в случае а):
R12 означает
1) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
2) -(С0-С3)-алкил-(С3-С6)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
3) -(С0-С3)-алкил-(С6-С14)-арил, где арил имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
4) -(С0-С3)-алкил-Het, где Het имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1; и
R13 означает
1) -(С0-С3)-алкил-(С6-С14)-арил, где алкил и арил имеют вышеуказанные значения и, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
2) -(С0-С3)-алкил-Het, где алкил и Het имеют вышеуказанные значения и, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1; или
в случае b):
R12 означает
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
3) -(С0-С3)-алкил-(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
4) -(С0-С3)-алкил-Het, где Het незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1; и
R13 означает -СН(R8)-R9, причем R8 и R9, независимо друг от друга, означают -(С6-С14)-арил или Het, где Het и арил, соответственно, имеют вышеуказанные значения и незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены -О-(С1-С4)-алкилом или R1, и
R16, R17, R18 и R19 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1,
3) галоген,
4) -ОН,
5) -NH2,
6) -(С0-С3)-алкил-(С6-С14)-арил, где алкил и арил имеют вышеуказанные значения и, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
7) -(С0-С3)-алкил-Het, где алкил и Het имеют вышеуказанные значения и, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
R16 и R17 или R18 и R19 вместе с атомом углерода, с которым они, соответственно, связаны, образуют 3-6-членный цикл, выбираемый из группы, состоящей из циклопропила, циклобутила, циклопентила или циклогексила; или
Y означает 4) остаток формулы (VI), причем
R24 и R25 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1,
3) -(С0-С3)-алкил-(С6-С14)-арил, где алкил и арил имеют вышеуказанные значения и, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
4) -(С0-С3)-алкил-Het, где алкил и Het имеют вышеуказанные значения и, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
5) -(С0-С3)-алкил-(С3-С6)-циклоалкил, или
R24 и R25 вместе с атомом азота, с которым они связаны, образуют 3-8-членный цикл, выбираемый из группы, состоящей из пропиламина, азетидина, пирролидина, пиперидина, азепана, азокана, азепина, диоксазола, диоксазина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, [1,4]оксазепана, оксазола, пиперазина, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидинона, пирролина, тетрагидропиридина, тиазола, тиадиазола, тиазолидина, тиазолина, тиоморфолина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола;
R26, R27, R28 и R29 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1,
3) галоген,
4) -ОН,
5) -NH2,
6) -(С0-С3)-алкил-(С6-С14)-арил, где алкил и арил имеют вышеуказанные значения и, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
7) -(С0-С3)-алкил-Het, где алкил и Het имеют вышеуказанные значения и, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
R26 и R27 или R28 и R29 вместе с атомом углерода, с которым они, соответственно, связаны, образуют 3-6-членный цикл, выбираемый из группы, состоящей из циклопропила, циклобутила, циклопентила или циклогексила;
Z означает
1) атом водорода,
2) -(С1-С6)-алкил,
3) -(С3-С6)-циклоалкил,
4) -(С1-С10)-алкил-О-С(О)-О-R1,
5) -(СН2)r-алкил-(С6-С14)-арил, где арил имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1 и r означает целое число ноль, 1, 2 или 3, или
6) -(СН2)s-Het, где Het имеет вышеуказанное значение и незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1 и s означает целое число ноль, 1, 2 или 3.
Дальнейшим объектом изобретения является соединение формулы (Iа), причем
U означает атом водорода, -CF3, фтор или -СН3;
Х означает остаток формулы (II), где
M означает целое число 1;
А1 означает 1) -(СН2)-, 2) -О-(СН2)n-, где n означает целое число ноль или 1, или 3) ковалентную связь;
А2 означает
1) аминопиридил, где аминопиридил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен -(С1-С3)-алкилом, галогеном или -CН3;
2) аминотиазолил, где аминотиазолил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен -(С1-С3)-алкилом, галогеном или -СН3;
3) -(С1-С3)-алкил-NH2, или
4) -(С3-С8)-циклоалкил-NH2;
Y означает 1) остаток формулы (III), причем
а) А3 означает (С3-С8)-циклоалкил или (С2-С6)-алкинилен, где циклоалкил или алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью -О-R10 или R1,
А4 означает -N(R2)2-, где R2 имеет нижеуказанное значение и значение обоих остатков R2 является независимым друг от друга,
А5 отсутствует, о означает целое число ноль или 1 и R10 означает атом водорода, -(С1-С6)-алкил или фенил;
b) А3 означает -(С3-С6)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью -О-R10 или R1,
А4 означает -N(R2)-, и
А5 означает а)1) -С(О)-R3; a)2) -C(O)-N(R4)-R5; a)3) -(SO2)-R6 или а)4) -C(O)-O-R7;
о означает целое число 1; и
р означает целое число 1;
с) А3 означает циклический амин с 3-8 атомами в цикле, где циклический амин незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 имеют указанное в п.b) значение, причем
А5 связан с N-атомом А3,
о означает целое число ноль, и
р означает целое число ноль или 1; или
d) А3 означает -(СН2)q-(C6-H14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 имеют указанное в п.b) значение,
о означает целое число ноль или 1,
р означает целое число 1, и
q означает целое число ноль, 1, 2 или 3;
е) А3 означает -(СН2)r-Het, где Het означает пирролидин, бензотиофен или пиперидин, который незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью =О или R1,
А4 и А5 имеют указанное в п.b) значение,
о означает целое число ноль или 1,
р означает целое число 1, и
r означает целое число ноль, 1, 2 или 3;
f) А3 означает -(СН2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -О-,
А5 означает фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
о и р означают целое число 1, и
q означает целое число 1 или 2;
причем R1 означает
а) фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С4)-алкилом,
b) триазолил или пиридинил,
с) -(С1-С4)-алкил,
d) -(С3-С6)-циклоалкил,
е) -CF3,
f) -O-CF3,
g) фтор, или
h) хлор;
причем R2 означает:
а) фенил, где фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен с помощью R1,
b) -(С1-С3)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -СF3, или
е) атом водорода;
причем R3, R6 и R7 являются одинаковыми или разными и,
независимо друг от друга, означают:
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) 4-15-членный гетероцикл, где гетероцикл незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
е) атом водорода;
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
а) -(С1-С6)-алкил или -(С2-С10)-алкенил, где алкил или алкенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -(С6-С14)-арил, где арил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) 4-15-членный гетероцикл, где гетероцикл незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
е) атом водорода, или
R4 и R5 вместе с атомом азота, с которым они связаны, образуют цикл, производимый от азетидина, пирролидина, пиперидина, азепана, азокана, азепина, диоксазола, диоксазина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, [1,4]оксазепана, оксазола, пиперазина, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидинона, пирролина, тетрагидропиридина, тиазола, тиадиазола, тиазолидина, тиазолина, тиоморфолина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола;
Y означает 2) остаток формулы (IV), выбираемый из группы, состоящей из азетидин-2-она, пирролидин-2-она или пиперидин-2-она, причем остаток может быть замещен у атома азота с помощью R8,
причем R8 означает
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) атом водорода, или
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
Y означает 3) остаток формулы (V),
причем в случае а):
R12 означает
1) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
2) -(С0-С3)-алкил-(С3-С6)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
3) -(С0-С3)-алкилфенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1; и
R13 означает
1) -(С0-С3)-алкилфенил, где алкил и фенил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
2) -(С0-С3)-алкилпиридил, где алкил и пиридил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1; или
в случае b):
R12 означает
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
3) -(С0-С3)-алкилфенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
4) -(С0-С3)-алкилпиридил, где алкил и пиридил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1; и
R13 означает -СН(R8)-R9, причем R8 и R9, независимо друг от друга, означают фенил или пиридил, где фенил или пиридил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены -О-(С1-С4)-алкилом или R1, и
R16, R17, R18 и R19 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С3)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1,
3) фтор,
4) -ОН,
5) -NH2, или
6) -(С0-С3)-алкилфенил, где алкил и фенил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1;
или
Y означает 4) остаток формулы (VI), причем
R24 и R25 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С6)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1,
3) -(С0-С3)-алкилфенил, где алкил и фенил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, или
4) -(С0-С3)-алкил-(С3-С6)-циклоалкил, или
R26, R27, R28 и R29 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С3)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1,
3) фтор,
4) -ОН,
5) -NH2, или
6) -(С0-С3)-алкилфенил, где алкил и фенил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1;
и
Z означает атом водорода или -(С1-С4)-алкил.
Дальнейшим объектом изобретения является соединение формулы (Ia), причем
U означает атом водорода;
Х означает остаток формулы (II), где
m означает целое число 1;
А1 означает -СН2-;
А2 означает аминопиридил, где аминопиридил незамещен или,
независимо друг от друга, одно-, двух- или трехкратно замещен галогеном или -CН3;
Y означает 1) остаток формулы (III), причем
а) А3 означает (С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, и
А4 и А5 отсутствуют;
b) А3 означает -(С2-С4)-алкинилен, где алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, и
А4 и А5 отсутствуют;
с) А3 означает циклический амин с 3-8 атомами в цикле, где циклический амин незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, и
А4 и А5 отсутствуют;
d) А3 означает -(СН2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -N(R2)-, где R2 имеет нижеуказанное значение,
А5 означает а)1) -С(О)-R3; а)2) -C(O)-N(R4)-R5; а)3) -(SO2)-R6; или а)4) -C(O)-O-R7;
о означает целое число 1,
р означает целое число 1, и
q означает целое число ноль, 1 или 2;
е) А3 означает -(СН2)r-Het, где Het означает пирролидин или пиперидин, который незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует и А5 имеет указанное в п.d) значение, причем А5 связан с атомом азота А3,
о означает целое число 1, и
r означает целое число ноль, 1, 2 или 3;
f) А3 означает -СН2-фенил, причем фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -О-,
А5 означает фенил, причем фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
причем R1 означает
а) фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С4)-алкилом,
b) триазолил или пиридинил,
с) -(С1-С4)-алкил,
d) -(С3-С6)-циклоалкил,
е) -CF3,
f) -O-CF3,
g) фтор, или
h) хлор;
причем R2 означает атом водорода или -(С1-С3)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
причем R3, R6 и R7 являются одинаковыми или разными и,
независимо друг от друга, означают:
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) атом водорода, или
d) -(С3-С6)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
а) -(С1-С6)-алкил или -(С2-С10)-алкенил, где алкил или алкенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) атом водорода, или
d) -(С3-С6)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
Y означает 2) остаток пирролидин-2-она, причем остаток замещен у атома азота соответственно с помощью R8,
причем R8 означает
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, или
с) -(С3-С6)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
Y означает 3) остаток формулы (V), причем
R12 означает атом водорода или -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, и
R13 означает -СН(R8)-R9, причем R8 и R9, независимо друг от друга, означают фенил или пиридил, где пиридил и фенил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1, и
R16, R17, R18 и R19 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С3)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1, или
3) -(С0-С3)-алкилфенил, где алкил и фенил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1; и
Z означает
1) атом водорода,
2) -(С1-С6)-алкил,
3) -(С1-С6)-алкил-ОН,
4) -(С0-С4)-алкил-(С3-С6)-циклоалкил,
5) -(С1-С10)-алкил-О-С(О)-О-(С3-С6)-циклоалкил.
Дальнейшим объектом изобретения является соединение формулы (Ia), причем
U означает атом водорода;
Х означает остаток формулы (II), где
M означает целое число 1;
А1 означает -СН2-;
А2 означает остаток 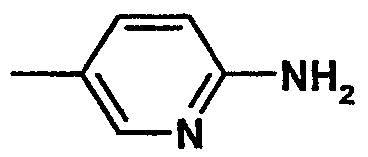 , который незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью F, Cl, Br, J или -CH3;
, который незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью F, Cl, Br, J или -CH3;
Y означает 1) остаток формулы (III), причем
а) А3 означает (С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, и
А4 и А5 отсутствуют;
b) А3 означает -(С2-С4)-алкинилен, где алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 отсутствуют;
с) А3 означает циклический амин с 3-6 атомами в цикле, где циклический амин незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 отсутствуют;
d) А3 означает -(СН2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -N(R2)-, где R2 имеет нижеуказанное значение,
А5 означает а)1) -C(O)-R3; a)2) -C(O)-N(R4)-R5; a)3) -(SO2)-R6 или a)4) -C(O)-O-R7;
о означает целое число 1,
р означает целое число 1, и
q означает целое число ноль, 1 или 2;
е) А3 означает -(СН2)r-Het, где Het означает пирролидин или пиперидин, который незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует и А5 имеет указанное в п.d) значение, причем А5 соединен с атомом азота А3,
р означает целое число 1, и
r означает целое число ноль, 1, 2 или 3;
f) А3 означает -СН2-фенил, причем фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -О-,
А5 означает фенил, причем фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
причем R1 означает
а) фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С4)-алкилом,
b) пиридил или тетразолил,
с) -(С1-С4)-алкил,
d) -(С3-С6)-циклоалкил,
е) -CF3,
f) -O-CF3,
g) фтор, или
h) хлор;
причем R2 означает атом водорода или -(С1-С3)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
причем R3, R6 и R7 являются одинаковыми или разными и, независимо друг от друга, означают
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
d) -(С3-С6)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
с) атом водорода, или
d) -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
Y означает 2) остаток пирролидин-2-она, причем остаток у атома азота соответственно замещен с помощью R8,
причем R8 означает фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
Y означает 3) остаток формулы (V), причем
R12 означает атом водорода или -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1; и
R13 означает -СН(R8)-R9, причем R8 и R9, независимо друг от друга, означают фенил или пиридил, где пиридил и фенил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1;
R16, R17, R18 и R19 являются одинаковыми или разными и, независимо друг от друга, означают
1) атом водорода,
2) -(С1-С3)-алкил, где алкил незамещен или одно- или двухкратно замещен с помощью R1, или
3) -(С0-С3)-алкилфенил, где алкил и фенил, соответственно, незамещены или, независимо друг от друга, одно-, двух- или трехкратно замещены с помощью R1; и
Z означает атом водорода.
Дальнейшим объектом изобретения являются соединения формулы (Ia) из ряда:
3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовая кислота;
метиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты;
изопропиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты;
циклопропилметиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты;
2-гидроксиэтиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты;
1-циклогексилоксикарбонилоксиэтиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)-пропионовой кислоты;
3-(6-аминопиридин-3-ил)-2-(1-циклопентил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-пиперидин-4-ил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(2-оксо-1-фенилпирролидин-3-ил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[(бензгидрилкарбамоил)метил]-1Н-имидазол-4-ил}пропионовая кислота;
изопропиловый эфир 3-(6-аминопиридин-3-ил)-2-{1-[(бензгидрилкарбамоил)метил]-1Н-имидазол-4-ил}пропионовой кислоты;
3-(6-аминопиридин-3-ил)-2-{1-[4-(3-фенилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[2-(1-дифенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[2-(1-бензоилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(1-бензоилпиперидин-2-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-{2-[1-(3-фенилпропионил)-пиперидин-3-ил]этил}-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(1-дифенилацетилпиперидин-3-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-{2-[1-(3-фенилпропионил)-пиперидин-4-ил]этил}-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[2-(1-фенилацетилпиперидин-3-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[2-(1-фенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[1-(4'-метилбифенил-3-карбонил)пиперидин-4-илметил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(1бензоилпиперидин-4-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-бензгидрил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(4-[1,2,4]триазол-1-илбензил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(4-трифторметоксибензил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(1,1-диоксо-1Н-1,6-бензо-[b]тиофен-2-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(5-хлорбензо[b]тиофен-3-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(4-фторфенокси)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(2-феноксибензил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(4-феноксибензил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-проп-2-инил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-бут-2-инил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(4,4-диметилциклогексил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[(бензгидрилметилкарбамоил)-метил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-({[(4-хлорфенил)фенилметил]-карбамоил}метил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-({[бис(4-метоксифенил)метил]-карбамоил}метил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[4-(3-пропилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[4-(толуол-4-сульфониламино)-фенил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(3-пропилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(3-фенетилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(3-бензилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(3-винилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(2-аминотиазол-4-ил)-2-{1-[(бензгидрилкарбамоил)метил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(2-аминотиазол-4-ил)-2-[1-({[(4-хлорфенил)фенилметил]-карбамоил}метил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[4-(3-трет-бутилуреидо)-фенил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[4-(3-бензилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота; или
этиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты.
Под понятием «(С1-С6)-алкил» или «(С1-С10)-алкил» понимают углеводородные остатки, углеродная цепь которых является линейной или разветвленной и содержит 1-6 атомов углерода или 1-10 атомов углерода, например метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, пентил, изопентил, неопентил, гексил, 2,3-диметилбутан, неогексил, гептил, октанил, нонанил или деканил.
Под понятием «-(С0-С4)-алкилен» понимают углеводородные остатки, углеродная цепь которых является линейной или разветвленной и содержит 1-4 атома углерода, например метилен, этилен, пропилен, изопропилен, изобутилен, бутилен или трет-бутилен. «С0-алкилен» означает ковалентную связь.
Под понятием «(С1-С10)-алкил» также понимают углеводородные остатки, как «-(С2-С10)-алкенилен», углеродная цепь которых является линейной или разветвленной и содержит 2-10 атомов углерода и в которых, в зависимости от длины цепи, имеются 1, 2 или 3 двойные связи, как, например, этенилен, пропенилен, изопропенилен, изобутенилен или бутенилен; заместители у двойной связи, если существует принципиальная возможность, могут быть расположены в Е- или Z-положении.
Под понятием «(С1-С10)-алкил» также понимают углеводородные остатки, как «-(С2-С10)-алкинилен», углеродная цепь которых является линейной или разветвленной и содержит 2-10 атомов углерода и в которых, в зависимости от длины цепи, имеются 1, 2 или 3 двойные связи, как, например, этинилен, пропинилен, изопропинилен, изобутинилен, бутинилен, пентинилен или изомеры пентинилена или гексинилена или изомеры гексинилена.
Под понятием «(С3-С8)-циклоалкил» понимают остатки, как таковые, которые производятся от 3-8-членных моноциклов, как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклооктанил.
Под понятием «циклический амин с 3-8 атомами в цикле» понимают остатки, которые производятся от пропиламина, азетидина, пирролидина, пиперидина, азепана или азокана.
Под понятием «-(СН2)n-, -(CH2)q-, -(CH2)r-, где n, q или r означает целое число ноль, 1, 2 или 3» понимают остатки, как метилен, этилен или пропилен. В случае, в котором n, q или r означает целое число ноль, остаток имеет значение ковалентной связи.
Под понятием «R16 и R17 или R18 и R19 вместе с атомом углерода, с которым они связаны, образуют 3-6-членный цикл» понимают остатки, которые производятся от циклопропила, циклобутила, циклопентила или циклогексила.
Под понятиями «R4 и R5 вместе с атомом азота, с которым они связаны, образуют 3-8-членный цикл, который дополнительно к атому азота может содержать еще вплоть до двух дополнительных гетероатомов из ряда, включающего кислород, серу или азот» или «R24 и R25 вместе с атомом азота, с которым они связаны, образуют 3-8-членный цикл, который дополнительно к атому азота может содержать еще вплоть до двух дополнительных гетероатомов из ряда, включающего кислород, серу или азот» понимают остатки, которые производятся от пропиламина, азетидина, пирролидина, пиперидина, азепана, азокана, азепина, диоксазина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазолидина, изотиазолина, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, [1,4]оксазепана, пиперазина, пиразина, пиразолина, пиразолидина, пиридазина, пирролидинона, пирролина, тетрагидропиридина, тиазолидина, тиазолина или тиоморфолина.
Под понятием «остаток формулы (IV)» понимают заместители, которые производятся от азетидин-2-она, пирролидин-2-она, пиперидин-2-она, азепан-2-она и азокан-2-она и замещены у атома азота соответственно с помощью R8.
Под фрагментом 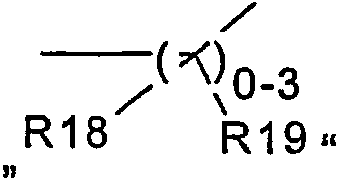 из формулы (V) в случае, когда одно-, двух- или трехкратно имеется место разветвления, понимают остатки, как метилен, этилен или пропилен, которые, соответственно, замещены остатками R18 и R19. В случае когда нет места разветвления, имеется ковалентная связь.
из формулы (V) в случае, когда одно-, двух- или трехкратно имеется место разветвления, понимают остатки, как метилен, этилен или пропилен, которые, соответственно, замещены остатками R18 и R19. В случае когда нет места разветвления, имеется ковалентная связь.
Под фрагментом 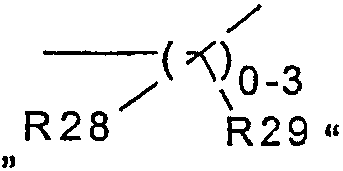 из формулы (VI) в случае, когда одно-, двух- или трехкратно имеется место разветвления, понимают остатки, как метилен, этилен или пропилен, которые, соответственно, замещены остатками R28 и R29. В случае когда нет места разветвления, имеется ковалентная связь.
из формулы (VI) в случае, когда одно-, двух- или трехкратно имеется место разветвления, понимают остатки, как метилен, этилен или пропилен, которые, соответственно, замещены остатками R28 и R29. В случае когда нет места разветвления, имеется ковалентная связь.
В отношении фрагмента (III) нужно принимать во внимание, что связывание с 1Н-имидазолом происходит через А3, а не через А5.
Под понятием «-(С6-С14)-арил» понимают ароматические углеводородные остатки с 6-14 атомами углерода в цикле. -(С6-С14)-арильными остатками являются, например, фенил, нафтил, как, например, 1-нафтил, 2-нафтил, антрил или флуоренил. Предпочтительными арильными остатками являются нафтильные остатки и, в особенности, фенильные остатки.
Под понятием «4-15-членный гетероцикл» или «Het» понимают циклические системы с 4-15 атомами углерода, которые находятся в виде одной, двух или трех, связанных друг с другом циклических систем и которые содержат один, два, три или четыре одинаковых или разных гетероатомов из ряда, включающего кислород, азот или серу. Примерами этих циклических систем являются остатки: акридинил, азепинил, азетидинил, азиридинил, бензимидазалинил, бензимидазолил, бензофуранил, бензотиофуранил, бензотиофенил, бензоксазолил, бензтиазолил, бензтриазолил, бензтетразолил, бензизоксазолил, бензизотиазолил, карбазолил, 4аН-карбазолил, карболинил, хиназолинил, хинолинил, 4Н-хинолизинил, хиноксалинил, хинуклидинил, хроманил, хроменил, циннолинил, декагидрохинолинил, дибензофуранил, дибензотиофенил, дигидрофуран[2,3-b]тетрагидрофуранил, дигидрофуранил, диоксолил, диоксанил, 2Н,6Н-1,5,2-дитиазинил, фуранил, фуразанил, имидазолидинил, имидазолинил, имидазолил, 1Н-индазолил, индолинил, индолизинил, индолил, 3Н-индолил, изобензофуранил, изохроманил, изоиндазолил, изоиндолинил, изоиндолил, изохинолинил (бензимидазолил), изотиазолидинил, 2-изотиазолинил, изотиазолил, изоксазолил, изоксазолидинил, 2-изоксазолинил, морфолинил, нафтиридинил, октагидроизохинолинил, оксадиазолил, 1,2,3-оксадиазолил, 1,2,4-оксадиазолил, 1,2,5-оксадиазолил, 1,3,4-оксадиазолил, оксазолидинил, оксазолил, оксотиоланил, пиримидинил, фенантридинил, фенантролинил, феназинил, фенотиазинил, феноксатилинил, феноксазинил, фталазинил, пиперазинил, пиперидинил, птеридинил, пуринил, пиранил, пиразинил, пироазолидинил, пиразолинил, пиразолил, пиридазинил, пиридооксазолил, пиридоимидазолил, пиридотиазолил, пиридотиофенил, пиридинил, пиридил, пиримидинил, пирролидинил, пирролинил, 2Н-пирролил, пирролил, тетрагидрофуранил, тетрагидроизохинолинил, тетрагидрохинолинил, тетрагидропиридинил, 6Н-1,2,5-тиадазинил, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,2,5-тиадиазолил, 1,3,4-тиадиазолил, тиантренил, тиазолил, тиенил, тиенотиазолил, тиенооксазолил, тиеноимидазолил, тиоморфолинил, тиофенил, триазинил, 1,2,3-триазолил, 1,2,4-триазолил, 1,2,5-триазолил, 1,3,4-триазолил и ксантенил.
Предпочтительными гетероциклами являются остатки: бензофуранил, бензимидазолил, бензоксазолил, бензотиазолил, бензотиофенил, 1,3-бензодиоксолил, хиназолинил, хинолинил, хиноксалинил, хроманил, циннолинил, фуранил, как 2-фуранил и 3-фуранил; имидазолил, индолил, индазолил, изохинолинил, изохроманил, изоиндолил, изотиазолил, изоксазолил, оксазолил, фталазинил, птеридинил, пиразинил, пиразолил, пиридазинил, пиридоимидазолил, пиридопиридинил, пиридопиримидинил, пиридил, как 2-пиридил, 3-пиридил или 4-пиридил; пиримидинил, пирролил, как 2-пирролил и 3-пирролил; пуринил, тиазолил, тетразолил или тиенил, как 2-тиенил и 3-тиенил.
Под понятием «галоген» понимают фтор, хлор, бром или йод.
Под понятием «=О» понимают оксоостаток или карбонил(-С(О)-) или нитрозоостаток (-N=O).
Предлагаемые согласно изобретению соединения можно получать общеизвестными способами или описанными в данном контексте способами.
Функциональные группы используемых промежуточных продуктов, например аминогруппы или карбоксильные группы, при этом можно защищать с помощью пригодных защитных групп. Пригодными защитными группами для аминогрупп являются, например, трет-бутоксикарбонильная группа, бензилоксикарбонильная группа или фталоильная группа, а также тритильная или тозильная защитная группа. Пригодными защитными группами для карбоксильной группы являются, например, сложный алкильный, арильный или арилалкильный эфир. Защитные группы можно вводить и удалять общеизвестными или описанными в данном контексте способами (см. Green T.W., Wutz P.G.M., “Protective Groups in Organic Synthesis” (1991), второе издание, Wiley-Interscience, или Kocienski P., “Protecting Groups” (1994), Thieme).
Понятие «защитная группа» может включать также соответствующие полимерсвязанные защитные группы. Такого рода защищенные соединения формулы (Ia), где функциональные группы остатка Х, в случае необходимости, также могут быть защищены, могут быть, хотя, в случае необходимости, даже фармакологически неактивно, в случае необходимости, после введения млекопитающим путем метаболизации превращаться в предлагаемые согласно изобретению фармакологически активные соединения.
Изобретение относится, далее, к способу получения соединения формулы (I) и/или стереоизомерной формы соединения формулы (I) и/или физиологически приемлемой соли соединения формулы (I), отличающемуся тем, что
а) соединение формулы (I) получают согласно схеме 1, причем Х и Y имеют, соответственно, указанные выше значения:
Схема 1
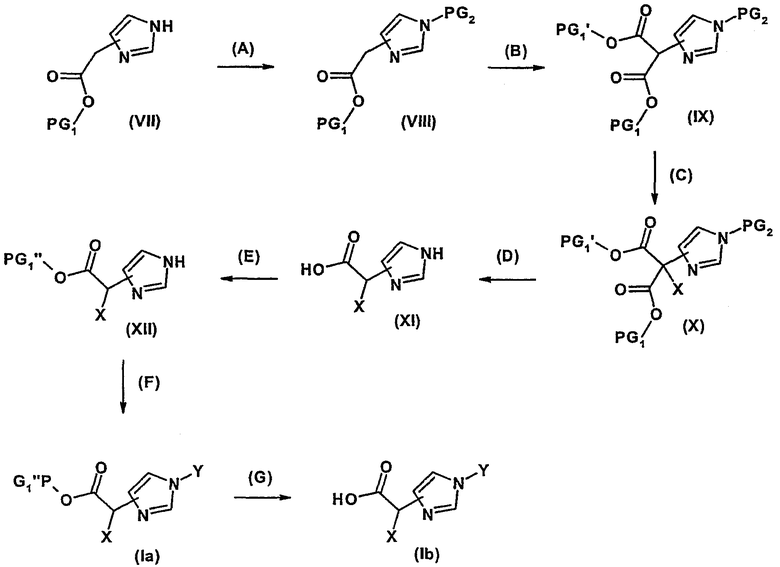
Соединения формулы (VII) можно получать обычными способами, например, из гидрохлорида 4-имидазолуксусной кислоты путем превращения в низших спиртах в присутствии тионилхлорида, причем PG1 означает пригодную карбоксилзащитную группу.
На стадии способа (А) согласно стандартным способам вводят пригодную защитную группу PG2.
Получаемые соединения формулы (VIII) на стадии способа (В) в присутствии основания и в инертном растворителе при температурах от -90°С до 50°С вводят во взаимодействие с соединением формулы (XIII):
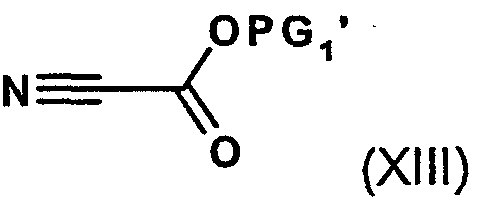
с получением соединений формулы (IX), причем PG1' означает пригодную карбоксилзащитную группу.
Из соединений формулы (IX) на стадии способа (С) в присутствии сильного основания в инертном растворителе при температурах от -90°С до +50°С путем введения во взаимодействие с соединениями формулы (XIV):
X - LG (XIV)
получают соединения формулы (Х), причем содержащиеся в (Х) функциональные группы могут быть защищены пригодными защитными группами и LG означает пригодную активирующую группу, как, например, хлор, бром, йод, мезилат, тозилат или трифлат.
На стадии способа (D) соединения формулы (Х) превращают в соединения формулы (XI) тем, что согласно стандартным способам удаляют защитные группы PG1, PG1' и PG2, а также, в случае необходимости, содержащуюся в (Х) защитную группу и обрабатывают, в случае необходимости, в водно-кислотных условиях при температурах от комнатной температуры до 100°С.
Соединения формулы (XII) можно получать из соединений формулы (XI) на стадии (Е) путем введения в стандартных условиях пригодной карбоксилзащитной группы PG1”.
На стадии (F) можно получать соединения формулы (Ia) путем взаимодействия соединений формулы (XII) в присутствии основания при температурах от -90°С до +60°С в инертном растворителе с соединениями формулы (XV):
Y - LG (XV),
причем LG означает пригодную активирующую группу, как хлор, бром, йод, мезилат, тозилат или трифлат, и Y имеет вышеуказанные значения.
Альтернативно, соединения формулы (Ia) можно получать путем взаимодействия соединений соединения формулы (XII) в условиях реакции Мицонобу с соединениями формулы (XVI):
Y - ОН (XVI),
где Y имеет вышеуказанные значения.
Альтернативно, соединения формулы (Ia) можно получать тем, что соединения формулы (XII) в присутствии основания при температурах от -90°С до +60°С в инертном растворителе вводят во взаимодействие с шестичленными 2-фторнитроароматическими соединениями или шестичленными 4-фторнитроароматическими соединениями. Затем нитрогруппу восстанавливают до аминогруппы согласно стандартным способам, например, при комнатной температуре в низших спиртах с помощью водорода в присутствии катализатора на основе переходного металла или в инертных растворителях в присутствии дигидрата хлорида олова-(II) и ацилируют согласно стандартным способам.
Соединения формулы (Ib) получают на стадии (G) путем удаления в стандартных условиях защитной группы PG1” и, в случае необходимости, содержащейся в (Х) защитной группы.
Соединения формул (XIII), (XIV), (XV) и (XVI) коммерчески доступны, известны из литературы или могут быть получены известными из литературы способами.
Превращения можно осуществлять при нормальном, повышенном или при пониженном давлении. В общем, работают при нормальном давлении.
В качестве растворителей для стадий способа (В), (С) и (F) пригодны инертные органические растворители. К ним относятся, например, простые эфиры, как диоксан, тетрагидрофуран или 1,2-диметоксиэтан; углеводороды, как циклогексан, бензол, толуол или ксилол; нитроароматические соединения, как нитробензол; амиды карбоновых кислот, как диметилформамид или диметилацетамид; алкилсульфоксиды, как диметилсульфоксид; алифатические нитрилы, как ацетонитрил, или другие растворители, как N-метилпирролидинон. Также можно использовать смеси указанных растворителей.
В качестве оснований для стадий способа (В), (С) и (F) пригодны обычные неорганические и органические основания. К ним относятся предпочтительно карбонаты щелочных и щелочноземельных металлов, как карбонат натрия, калия или кальция; гидриды щелочных металлов, как гидрид натрия; амиды, как бис(триметилсилил)амид лития или диизопропиламид лития; органические амины, как пиридин, 4-N,N-диметиламинопиридин, триэтиламин, этилдиизопропиламин, N-метилморфолин, N-метилпиперидин, 1,5-диазабицикло[4,3,0]нон-5-ен (DBN) или 1,8-диазабицикло[5,4,0]ундец-7-ен (DBU); или металлоорганические соединения, как бутиллитий или фениллитий. Особенно предпочтительны гидрид натрия, бис(триметилсилил)амид лития и триэтиламин.
Под условиями реакции Мицонобу, в общем, понимают использование инертных растворителей в присутствии азодикарбоксилата, в случае необходимости, в присутствии добавочного реагента, предпочтительно в области температур от 0°С до комнатной температуры при нормальном давлении. Инертными растворителями являются, например, галогенуглеводороды, как дихлорметан, простые эфиры, как диоксан, тетрагидрофуран или 1,2-диметоксиэтан, углеводороды, как бензол, толуол или ксилол, нитроароматические соединения, как нитробензол, амиды карбоновых кислот, как диметилформамид или диметилацетамид, алкилсульфоксиды, как диметилсульфоксид, алифатические нитрилы, как ацетонитрил, сложные эфиры, как этиловый эфир бензойной кислоты, или другие растворители, как N-метилпирролидинон. Также можно использовать смеси указанных растворителей.
Обычными добавочными реагентами для реакции Мицонобу являются, например, трифенилфосфин, дифенил(2-пиридил)фосфин или (4-диметиламинофенил)дифенилфосфин.
Азодикарбоксилатами являются, например, диэтилазодикарбоксилат, диметилазодикарбоксилат, диизопропилазодикарбоксилат или ди-трет-бутилазодикарбоксилат.
Полученное согласно схеме 1 соединение формулы (I), или пригодный предшественник формулы (I), которое(ый) на основании своей химической структуры образуется в энантиомерных формах, путем солеобразования с энантиомерно чистыми кислотами или основаниями, хроматографии при использовании хиральных неподвижных фаз или дериватизации с помощью хиральных энантиомерно чистых соединений, как аминокислоты, разделения таким образом полученных диастереомеров и отщепления хиральных вспомогательных групп разделяют на чистые энантиомеры (способ b), или полученное согласно схеме 1 соединение формулы (I) либо выделяют в чистой форме, либо , в случае наличия кислотных или основных групп, превращают в физиологически приемлемые соли (способ с).
На стадии способа b) соединение формулы (I), если оно образуется в виде смеси диастереомеров или энантиомеров или при выбранном синтезе образуется в виде их смесей, разделяют на чистые стереоизомеры либо путем хроматографии при использовании, в случае необходимости, хирального носителя, либо, если рацемическое соединение формулы (I) способно к солеобразованию, путем фракционной кристаллизации получаемых с оптически активным основанием или кислотой в качестве вспомогательного вещества диастереомерных солей. В качестве хиральных неподвижных фаз для разделения энантиомеров путем тонкослойной или колоночной хроматографии пригодны, например, модифицированные силикагели (так называемые Pirkle-фазы), а также высокомолекулярные углеводы, как триацетилцеллюлоза. Для аналитических целей после соответствующей известной специалисту дериватизации, также применимы газохроматографические методы при использовании хиральных неподвижных фаз. Для разделения на энантиомеры рацемических карбоновых кислот с помощью оптически активного, как правило, коммерчески доступного основания, как (-)-никотин, (+)- и (-)-фенилэтиламин, хининовые основания, L-лизин или L- и D-аргинин, получают различно растворимые диастереомерные соли, труднее растворимый компонент выделяют в виде твердого вещества, легче растворимый диастереомер осаждают из маточного раствора и из таким образом полученных диастереомерных солей получают чистые энантиомеры. В принципе, таким же образом рацемические соединения формулы (I), содержащие основную группу, как аминогруппа, с помощью оптически активных кислот, как (+)-камфор-10-сульфокислота, D- и L-винная кислота, D- и L-молочная кислота, а также (+)- и (-)-миндальная кислота, переводят в чистые энантиомеры. Хиральные соединения, содержащие спиртовые функциональные группы или аминогруппы, с помощью соответственно активированных или, в случае необходимости, N-защищенных энантиомерно чистых аминокислот также можно переводить в соответствующие сложные эфиры или амиды, или, наоборот, хиральные карбоновые кислоты с помощью карбоксизащищенных энантиомерно-чистых аминокислот можно переводить в амиды или с помощью энантиомерно-чистых гидроксикарбоновых кислот, как молочная кислота, можно переводить в соответствующие хиральные сложные эфиры. Затем хиральность аминокислотного или спиртового остатка, введенного в энантиомерно-чистой форме, можно использовать для разделения изомеров тем, что разделение теперь имеющихся диастереомеров осуществляют путем кристаллизации или хроматографии при использовании пригодных неподвижных фаз и после этого с помощью пригодных способов снова отщепляют введенную хиральную часть молекулы.
Далее, в случае некоторых из предлагаемых согласно изобретению соединений существует возможность использования диастереоизомерно- или энантиомерно-чистых исходных продуктов для получения скелетных структур. Благодаря этому, в случае необходимости, можно использовать также другие или упрощенные способы для очистки конечных продуктов. Эти исходные продукты прежде получают энантиомерно- или диастереомерно-чистыми согласно известным из литературы способам. Это, в особенности, может означать, что при синтезе основных скелетных структур используют либо энантиоселективные способы, либо, однако, разделение энантиомеров (или диастереомеров) осуществляют на более ранней стадии синтеза, а не только на стадии конечных продуктов. Упрощения разделений также можно достигать благодаря тому, что осуществляют две или более стадий.
Кислые или основные продукты соединения формулы (I) могут находиться в форме их солей или в чистой форме. Предпочтительны фармакологически приемлемые соли, например, соли щелочных или щелочноземельных металлов, соответственно, гидрохлориды, гидробромиды, сульфаты, полусульфаты, все возможные фосфаты, а также соли аминокислот, природных оснований или карбоновых кислот.
Получение физиологически приемлемых солей из способных к солеобразованию соединений формулы (I), включая их стереоизомерные формы, согласно стадии способа с) осуществляют само по себе известным образом. Соединения формулы (I) c основными реагентами, как гидроксиды, карбонаты, гидрокарбонаты, алкоголяты, а также аммиак, или органическими основаниями, как, например, триметил- или триэтиламин, этаноламин, диэтаноламин или триэтаноламин, трометамол, или также основными аминокислотами, как, например, лизин, орнитин или аргинин, образуют стабильные соли щелочных металлов, щелочноземельных металлов или в случае необходимости замещенные аммониевые соли. Если соединения формулы (I) включают основные группы, с помощью сильных кислот также можно получать стабильные аддитивные соли кислот. Для этой цели используют как неорганические, так и также органические кислоты, как соляная кислота, бромоводородная кислота, серная кислота, гемисерная кислота, фосфорная кислота, метансульфокислота, бензолсульфокислота, п-толуолсульфокислота, 4-бромбензолсульфокислота, циклогексиламидосульфокислота, трифторметилсульфокислота, 2-гидроксиэтансульфокислота, уксусная кислота, щавелевая кислота, винная кислота, янтарная кислота, глицерофосфорная кислота, молочная кислота, яблочная кислота, адипиновая кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, глюконовая кислота, глюкуроновая кислота, пальмитиновая кислота или трифторуксусная кислота.
Изобретение относится также к лекарственному средству, отличающемуся эффективным содержанием по меньшей мере одного соединения формулы (I) и/или физиологически приемлемой соли соединения формулы (I) и/или, в случае необходимости, стереоизомерной формы соединения формулы (I) вместе с фармацевтически пригодным и физиологически совместимым носителем, добавкой и/или другими биологически активными и вспомогательными веществами.
Благодаря фармакологическим свойствам, предлагаемые согласно изобретению соединения пригодны для профилактики и лечения таких заболеваний, которые поддаются лечению за счет ингибирования TAFIa. Так, ингибиторы TAFIa пригодны как для профилактического, так и также терапевтического применения в отношении человека. Они пригодны как для экстренного лечения, так и также для долговременной терапии. Ингибиторы TAFIa можно использовать в случае пациентов, которые страдают нарушениями хорошего самочувствия или заболеваниями, которые протекают с тромбозами, эмболиями, гиперкоагулируемостью или фибротическими изменениями. К ним относятся инфаркт миокарда, стенокардия и все другие формы острого коронарного синдрома, инсульт, приферические васкулярные заболевания, глубокий венозный тромбоз, эмболия легочной артерии, эмболические или тромботические явления, обусловленные кардиальными аритмиями, сердечно-сосудистые явления, как рестеноз после реваскуляризации, ангиопластики и подобных вмешательств, как стент-имплантации и операции шунтирования. Далее, ингибиторы TAFIa можно использовать в случае всех вмешательств, которые приводят к контакту крови с чужеродными поверхностями, как, например, в случае подвергаемых диализу пациентов и пациентов с постоянными катетерами. Ингибиторы TAFIa можно использовать для уменьшения опасности тромбоза после хирургических вмешательств, как при операциях коленного сустава и тазобедренного сустава.
Ингибиторы TAFIa пригодны для лечения пациентов с диссеминированной интраваскулярной коагуляцией, сепсисом и другими интраваскулярными явлениями, которые протекают с воспалением. Далее, ингибиторы TAFIa пригодны для профилактики и лечения пациентов с атеросклерозом, диабетом и метаболическим синдромом и его последствиями. Нарушения гемостатической системы (например, отложения фибрина) заключаются в механизмах, которые ведут к росту опухоли и метастазированию опухоли; ингибиторы TAFIa пригодны для замедления или предотвращения таких процессов.
Дальнейшими показаниями к использованию ингибиторов TAFIa являются фиброзные изменения легких, как хроническое обструктивное заболевание легких, респираторный дистресс-синдром взрослых (ARDS) и дистресс-синдром глаза, как отложения фибрина после глазных операций. Ингибиторы TAFIa пригодны также для предотвращения и/или лечения при рубцевании.
Введение предлагаемых согласно изобретению лекарственных средств можно осуществлять путем орального, с помощью ингаляции, ректального или трансдермального введения или путем подкожной, внутрисуставной, интраперитонеальной или внутривенной инъекции. Предпочтительно оральное введение. Возможно покрытие ингибиторами TAFIa стента и других поверхностей, которые в организме вступают в контакт с кровью.
Изобретение относится также к способу получения лекарственного средства, который отличается тем, что по меньшей мере одно соединение формулы (I) вместе с фармацевтически пригодным и физиологически приемлемым носителем и, в случае необходимости, другими пригодными биологически активными веществами, добавками или вспомогательными веществами доводят до пригодной для введения формы.
Пригодными твердыми или галеновыми готовыми формами являются, например, грануляты, порошки, драже, таблетки, (микро)капсулы, суппозитории, сиропы, соки, суспензии, эмульсии, капли или инъецируемые растворы, а также препараты с пролонгированным высвобождением биологически активного вещества, при приготовлении которых находят применение обычные вспомогательные средства, как носители, порофоры, связующие, средства для покрытия, способствующие набуханию средства, придающие скользкость средства или смазки, вкусовые вещества, подсластители и способствующие растворению вещества. В качестве часто используемых вспомогательных веществ следует назвать карбонат магния, диоксид титана, лактозу, маннит и другие сахара, тальк, молочный белок, желатин, крахмал, целлюлозу и ее производные, животные и растительные масла, как рыбий жир, подсолнечное масло, арахисовое масло или кунжутное масло, полиэтиленгликоль и растворители, как, например, стерильная вода и одно- или многоатомные спирты, как глицерин.
Предпочтительно, фармацевтические препараты приготовляют и вводят в разовых дозах, причем каждая разовая доза в качестве активного компонента содержит определенное количество предлагаемого согласно изобретению соединения формулы (I). В случае твердых разовых форм, как таблетки, капсулы, драже или суппозитории, это количество может составлять вплоть до 1000 мг, предпочтительно, однако, от примерно 50 мг до 300 мг, а в случае растворов для инъекции в ампульной форме - вплоть до примерно 300 мг, предпочтительно, однако, от примерно 10 мг до 100 мг.
Для лечения взрослых массой примерно 70 кг пациентов, в зависимости от эффективности соединения формулы (I), показаны суточные дозы от примерно 2 мг до 1000 мг биологически активного вещества, предпочтительно, от примерно 50 мг до 500 мг. Смотря по обстоятельствам, однако, также можно вводить более высокие или более низкие суточные дозы. Введение суточной дозы можно осуществлять как путем одноразового введения в форме отдельной разовой дозы или, однако, в виде нескольких более маленьких разовых доз, как также путем многократного введения разделенных доз в определенные интервалы.
Ингибиторы TAFIa можно вводить как в виде монотерапии, так и также в комбинации или совместно с любыми антитромботическими средствами (антикоагулянты и ингибиторы агрегации тромбоцитов), тромболитическими средствами (плазминогенные активаторы любого рода), другими профибринолитически активными веществами, снижающими кровяное давление средствами, регуляторами содержания сахара в крови, снижающими уровень липидов средствами и антиаритмическими средствами.
Примеры
Конечные продукты, как правило, определяют методами масс-спектрометрии (FAB-MC (масс-спектрометрия с ионизацией путем бомбардировки быстрыми атомами) или ESI-МС (масс-спектрометрия с ионизацией электронным распылением)) и 1Н-ЯМР; указываются, соответственно, основной пик или оба основных пика. Температуры указаны в градусах Цельсия, RT означает комнатную температуру (от 21°С до 24°С). Используемые сокращения либо пояснены, либо соответствуют обычным конвенциям.
Если не указано ничего другого, анализы путем жидкостной хроматографии с масс-спектрометрией осуществляют в следующих условиях.
Способ А: колонка: YMC Jsphere 33 x 2,1 мм; уплотнительный материал: 4 мкм; растворитель: СН3СN + 0,05% трифторуксусной кислоты (ТФУК) : Н2О + 0,05% ТФУК, градиент: от 5:95 (0 мин) до 95:5 (3,4 мин), расход: 1 мл/мин, температура: 30°С;
Способ В: колонка: YMC Jsphere ODS H80 20 x 2,1 мм; уплотнительный материал: 4 мкм; растворитель: СН3СN + 0,05% трифторуксусной кислоты (ТФУК) : Н2О + 0,05% ТФУК, градиент: от 4:96 (0 мин) до 95:5 (2,0 мин), расход: 1 мл/мин, температура: 30°С;
Способ С: колонка: YMC Jsphere 33 x 2,1 мм; уплотнительный материал: 4 мкм; растворитель: СН3СN + 0,05% трифторуксусной кислоты (ТФУК) : Н2О + 0,05% ТФУК, градиент: от 5:95 (0 мин) до 95:5 (2,5 мин), расход: 1,3 мл/мин, температура: 30°С.
Если не указано ничего другого, разделения путем хроматографии осуществляют на силикагеле при использовании смесей этилацетат/гептан в качестве растворителя, а также препаративные разделения проводят путем высокоэффективной жидкостной хроматографии (ВЭЖХ) с обращенной фазой (OФ) на силикагеле при использовании содержащих трифторуксусную кислоту смесей воды с ацетонитрилом в качестве растворителя.
Выпаривание растворителей осуществляют, как правило, при пониженном давлении при температуре от 35°С до 45°С.
Пример 1
3-(6-Аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовая кислота
Пример 1а
трет-Бутиловый эфир (5-метилпиридин-2-ил)карбаминовой кислоты
К раствору 30,00 г (277 ммоль) 5-метилпиридин-2-иламина и 3,39 г (28 ммоль) 4-диметиламинопиридина в 150 мл дихлорметана добавляют раствор 60,54 г (277 ммоль) ди-трет-бутилдикарбоната в 50 мл дихлорметана. Полученный раствор перемешивают в течение 16 часов при комнатной температуре и затем концентрируют досуха. Очистка хроматографией на силикагеле приводит к 15,4 г продукта в виде бесцветного твердого вещества.
МС (ES+)[масс-спектрометрия с ионизацией электронным распылением при образовании положительных ионов] = 209 [M+H]+
Пример 1b
Раствор 14,9 г (72 ммоль) соединения, полученного согласно примеру 1а, в 700 мл CCl4 нагревают до кипения. После добавления смеси из 12,8 г (72 ммоль) N-бромсукцинимида и 1,2 г (7 ммоль) 2,2'-азобис(изобутиронитрила) кипятят с обратным холодильником в течение 2,5 часов. Реакционную смесь фильтруют в горячем состоянии, остаток на фильтре промывают дополнительно с помощью CCl4 и из объединенных фильтратов удаляют растворитель. Остаток перекристаллизуют из ацетонитрила, отфильтровывают под вакуумом, промывают ацетонитрилом и смесью ацетонитрила и метил-трет-бутилового эфира (1:1) и высушивают при пониженном давлении. Получают 6,94 г желательного соединения в виде твердого вещества кремового цвета.
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,48 (с, 9Н); 4,71 (с, 2Н); 7,78 (д, 1Н); 7,82 (д, 1Н); 8,32 (с, 1Н).
Пример 1с
Гидрохлорид метилового эфира 4-имидазолуксусной кислоты
5,0 г (30,75 ммоль) 4-имидазолуксусной кислоты растворяют в 50 мл метанола и затем смешивают с 5,6 мл (76,87 ммоль) тионилхлорида. Полученный раствор кипятят с обратным холодильником в течение 4 часов и после охлаждения концентрируют досуха. После высушивания при пониженном давлении получают 5,3 г желательного продукта в виде твердого вещества бледно-желтого цвета.
МС (ES+) = 141 [M+H]+
Пример 1d
Метиловый эфир [1-(толил-4-сульфонил)-1Н-имидазол-4-ил]-уксусной кислоты
Раствор из 5,0 г (28,31 ммоль) соединения, полученного согласно примеру 1с, и 9,8 мл триэтиламина (70,72 ммоль) в 350 мл СН2Cl2, после охлаждения до температуры 0°С смешивают с 7,04 г (36,90 ммоль) п-толуолсульфонилхлорида. Раствор перемешивают в течение 15 минут при температуре 0°С и 15 минут при комнатной температуре, концентрируют и затем промывают раствором хлорида аммония и водой. Органическую фазу сушат над сульфатом натрия и после отфильтровывания концентрируют досуха. Очистка хроматографией на силикагеле приводит к 7,2 г желательного продукта.
Rt (способ А) = 1,71 мин; МС (ES+) = 295 [M+H]+
Пример 1е
Диметиловый эфир 2-(1-толил-4-сульфонил)-1Н-имидазол-4-ил]-малоновой кислоты
К охлажденному до температуры 0°С раствору из 3,0 г (10,19 ммоль) соединения, полученного согласно примеру 1d, в 50 мл абсолютного тетрагидрофурана (ТГФ) медленно прикапывают 9,3 мл (11,1 ммоль) 20%-ного раствора бис(триметилсилил)амида лития в тетрагидрофуране. После перемешивания в течение 30 минут при температуре 0°С добавляют 0,89 мл метилцианоформиата и полученный раствор в течение промежутка времени 1,5 часа медленно нагревают до комнатной температуры. Реакционный раствор затем выливают примерно в 300 мл насыщенного раствора хлорида аммония. Многократно экстрагируют этилацетатом и объединенные этилацетатные экстракты после промывки водой и высушивания над
Na2SO4 концентрируют досуха. Очистка хроматографией на силикагеле приводит к 2,2 г указанного в заголовке соединения.
Rt (способ А) = 1,89 мин; МС (ES+) = 353 [M+H]+
Пример 1f
Диметиловый эфир 2-(6-трет-бутилоксикарбониламинопиридин-3-илметил)-2-[1-(толил-4-сульфонил)-1Н-имидазол-4-ил]малоновой кислоты
Охлажденный до температуры 0°С раствор из 2,2 г (6,24 ммоль) соединения, полученного согласно примеру 1е, в 40 мл абсолютного N,N'-диметилформамида (ДМФА) смешивают с 150 мл (6,26 ммоль) NaH (50%-ный) и перемешивают в течение 1 часа при комнатной температуре. После охлаждения до температуры 0°С добавляют 1,8 г (6,24 ммоль) 2-(6-трет-бутилоксикарбониламино-пиридин-3-ил)метилбромида и полученный раствор перемешивают в течение 30 минут при температуре 0°С. Затем добавляют 50 мл воды и многократно экстрагируют этилацетатом. Объединенные этилацетатные экстракты сушат над Na2SO4, фильтруют и концентрируют досуха. Очистка остатка хроматографией на силикагеле приводит к 2,9 г желательного соединения.
Rt (способ А) = 2,10 мин; МС (ES+) = 559 [M+H]+
Пример 1g
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-(1Н-имидазол-4-ил)-пропионовой кислоты
400,0 мг (0,72 ммоль) соединения, полученного согласно примеру 1f, суспендируют в растворе из 5 мл 37%-ной соляной кислоты и 5 мл воды. Полученную суспензию нагревают в течение 20 минут при температуре 180°С в микроволновой установке. Затем реакционный раствор концентрируют, полученный остаток обрабатывают с помощью 50 мл этанола и снова концентрируют. Остающийся остаток растворяют в 50 мл этанола и раствор после добавки 40 мл насыщенного раствора газообразного HCl в диэтиловом эфире перемешивают в течение 3 часов. Концентрируют досуха, остаток обрабатывают с помощью 20 мл смеси из этилацетата и насыщенного раствора NaHCO3 и реакционный раствор многократно экстрагируют этилацетатом. Объединенные этилацетатные экстракты сушат над Na2SO4, фильтруют и концентрируют. Очистка остатка хроматографией на силикагеле приводит к 134 мг желательного соединения.
Rt (способ А) = 0,20 мин; МС (ES+) = 261 [M+H]+
Пример 1h
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты
Способ 1:
Раствор из 60,1 мг (0,23 ммоль) соединения, полученного согласно примеру 1g, 37,7 мг (0,23 ммоль) бромциклогексана и 100 мкл триэтиламина в 1 мл абсолютного тетрагидрофурана обрабатывают в течение 40 минут при температуре 170°С в микроволновой установке. Затем реакционный раствор обрабатывают небольшим количеством смеси этилацетата и воды (1:1), фазы разделяют, органическую фазу сушат над Na2SO4, фильтруют и концентрируют досуха. Очистка хроматографией с обращенной фазой на силикагеле при использовании смеси СН3CN/вода/0,1% ТФУК в качестве растворителя и сушка вымораживанием объединенных, имеющих значение фракций приводит к 18,0 мг желательного соединения в виде бистрифторацетата в форме аморфного твердого вещества.
Альтернативно способу 1 указанное в заголовке соединение также получают согласно нижеописанному способу 2.
Способ 2
Раствор из 200,0 мг (0,77 ммоль) соединения, полученного согласно примеру 1е, и 39,0 мг (0,77 ммоль, 60%-ный) NaH в 5 мл абсолютного ДМФА перемешивают в течение 1 часа при комнатной температуре и затем смешивают с 123,7 мг (0,77 ммоль) 3-бромциклогексана. Полученный раствор перемешивают в течение 1 часа при комнатной температуре. После добавки 2 мл воды многократно экстрагируют диэтиловым эфиром и объединенные экстракты в диэтиловом эфире сушат над MgSO4. После концентрирования, очистки остатка хроматографией с обращенной фазой на силикагеле при использовании смеси вода/ацетонтрил (5:95) и концентрирования имеющих значение фракций получают 152 мг этилового эфира 3-(6-аминопиридин-3-ил)-2-(1-циклогекс-2-ен-1Н-имидазол-4-ил)пропионовой кислоты. Это соединение затем гидрируют в 15 мл метанола в присутствии Pd/активный уголь (10%) в течение 2 часов при комнатной температуре. После концентрирования и высушивания при пониженном давлении получают 127 мг желательного, указанного в заголовке соединения в виде аморфного твердого вещества.
Rt (способ А) = 0,89 мин; МС (ES+) = 343 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,12 (т, 3H), 1,18 (м, 1H), 1,38 (м, 2H), 1,68, (м, 3H), 1,80 (м, 2H), 2,03 (м, 2H), 3,08 (дд, 1H), 3,15 (дд, 1H), 3,42 (кв, 2H), 4,10 (дт, 1H), 4,24 (м, 1H), 6,95 (д, 1H), 7,75 (м, 3H), 8,10 (с, 2H).
Пример 1i
Гидрохлорид 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор из 13,7 мг (0,03 ммоль) соединения, полученного согласно примеру 1h, в 0,5 мл воды и 0,5 мл 37%-ной соляной кислоты обрабатывают в течение 5 минут при температуре 180°С в микроволновой установке. Затем концентрируют досуха при пониженном давлении, остаток обрабатывают небольшим количеством воды и раствор подвергают сушке вымораживанием. При этом получают 8,0 мг указанного в заголовке соединения в виде бисгидрохлорида в форме аморфного твердого вещества.
Rt (способ А) = 0,80 мин; МС (ES+) = 315 [M+H]+;
1Н-ЯМР (400 МГц, ДМСО-d6): δ = 0,86 (м, 1H), 1,28 (м, 5H), 1,60 (м, 3H), 1,78 (м, 2H), 1,92 (м, 2H), 2,77 (дд, 1H), 2,95 (дд, 1H), 3,55 (дт, 1H), 3,95 (м, 1H), 5,60 (с, 2H), 6,34 (д, 1H), 7,00 (с, 1H), 7,14 (дд, 1H), 7,58 (с, 1H), 7,68 (с, 1H).
Оба энантиомера соединения, полученного согласно примеру 1g, разделяют путем препаративной хроматографии при использовании хиральной фазы; фаза: Chiralpak ADH40; размер колонки: 250 х 4 мм; растворитель: гептан:этанол:метанол = 8:1:1 плюс 0,1% ацетата аммония (в изократическом режиме); расход: 1 мл/мин; температура: 30°С:
энантиомер 1: Rt = 6,13 мин; энантиомер 2: Rt = 46,32 мин.
Пример 2
Метиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор из 50,0 мг (0,16 ммоль) соединения, полученного согласно примеру 1i, в 8 мл метанола смешивают с 3 мл насыщенного раствора HCl в диэтиловом эфире и перемешивают в течение 6 часов при комнатной температуре. Затем раствор концентрируют досуха и полученный остаток высушивают в высоком вакууме. Получают 51 мг указанного в заголовке соединения в виде бисгидрохлорида в форме аморфного твердого вещества.
Rt (способ А) = 0,90 мин; МС (ES+) = 329 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,20 (м, 1H), 1,37 (м, 2H), 1,65 (м, 3H), 1,82 (м, 2H), 2,0 (м, 2H), 3,10 (дд, 1H), 3,18 (дд, 1H), 3,65 (с, 3H), 4,22 (м, 2H), 6,95 (д, 1H), 7,72 (м, 3H), 8,05 (с, 2H).
Оба энантиомера соединения разделяют путем препаративной хроматографии при использовании хиральной фазы; фаза: Chiracel OD/H-61; растворитель: гептан:пропанол:метанол = 15:1:1 плюс 0,1% диэтиламина (в изократическом режиме); расход: 1 мл/мин; температура: 30°С:
энантиомер 1: Rt = 14,05 мин; энантиомер 2: Rt = 17,15 мин.
Пример 3
Изопропиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор из 38,0 мг (0,12 ммоль) соединения, полученного согласно примеру 1i, в 5 мл изопропанола смешивают с 2 мл насыщенного раствора HCl в диэтиловом эфире и перемешивают в течение 4 часов при комнатной температуре. Затем раствор концентрируют досуха и полученный остаток высушивают в высоком вакууме. Получают 25 мг указанного в заголовке соединения в виде бисгидрохлорида в форме аморфного твердого вещества.
Rt (способ А) = 0,92 мин; МС (ES+) = 357 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,02 (д, 6H), 1,15 (м, 3H), 1,38 (м, 2H), 1,68 (м, 3H), 1,85 (м, 1H), 2,03 (м, 1H), 3,05 (дд, 1H), 3,14 (дд, 1H), 3,78 (дт, 1H), 4,20 (м, 2H), 4,90 (м, 1H), 6,90 (м, 1H), 7,74 (м, 3H), 8,00 (м, 1H).
Пример 4
Циклопропилметиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор из 50,0 мг (0,16 ммоль) соединения, полученного согласно примеру 1i, в 2 мл циклопропилкарбинола смешивают с 1 мл насыщенного раствора HCl в диэтиловом эфире и перемешивают в течение 12 часов при комнатной температуре. Затем раствор концентрируют досуха и полученный остаток высушивают в высоком вакууме. Очистка путем хроматографии на силикагеле при использовании смеси
СН2Cl2/метанол в качестве растворителя приводит к 29 мг указанного в заголовке соединения в виде аморфного твердого вещества.
Rt (способ А) = 0,91 мин; МС (ES+) = 369 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,18 (м, 2H), 0,42 (м, 2H), 0,98 (м, 1H), 1,18 (м, 1H), 1,34 (м, 2H), 1,60 (м, 3H), 1,75 (д, 2H), 1,94 (д, 2H), 2,90 (м, 2H), 3,70 (м, 1H), 3,78 (д, 2H), 3,97 (м, 1H), 5,70 (с, 2H), 6,34 (д, 1H), 7,05 (с, 1H), 7,13 (д, 1H), 7,55 (с, 1H), 7,70 (с, 1H).
Пример 5
2-Гидроксиэтиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор из 50,0 мг (0,16 ммоль) соединения, полученного согласно примеру 1i, в 1 мл этиленгликоля смешивают с 0,4 мл насыщенного раствора HCl в диэтиловом эфире и перемешивают в течение 1 часа при комнатной температуре. Затем раствор концентрируют досуха, остаток обрабатывают насыщенным раствором NaHCO3 и многократно экстрагируют этилацетатом. Объединенные этилацетатные экстракты сушат, фильтруют и концентрируют. Полученный остаток высушивают в высоком вакууме, причем получают 33 мг указанного в заголовке соединения в виде масла светло-желтого цвета.
Rt (способ А) = 0,85 мин; МС (ES+) = 359 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,85 (м, 1H), 1,15-1,35 (м, 5H), 1,60 (м, 3H), 1,78 (д, 1H), 1,95 (м, 1H), 2,90 (м, 1H), 3,48 (м, 1H), 4,00 (м, 2H), 5,68 (с, 2H), 6,32 (д, 1H), 7,05 (с, 1H), 7,13 (д, 1H), 7,55 (с, 1H), 7,65 (д, 1H).
Пример 6
1-Циклогексилоксикарбонилоксиэтиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор из 50,0 мг (0,16 ммоль) соединения, полученного согласно примеру 1i, и 39 мг (0,19 ммоль) 1-циклогексилоксикарбонилокси-1-этилхлорида, 13 мг (0,08 ммоль) KI и 26 мг (0,19 ммоль) К2СО3 в 2 мл диметилформамида перемешивают в течение 12 часов при температуре 60°С. Затем смешивают с 5 мл воды и реакционный раствор многократно экстрагируют этилацетатом. Объединенные этилацетатные экстракты сушат, фильтруют и концентрируют досуха. Полученный остаток очищают при использовании силикагеля с помощью смеси СН2Сl2/метанол в качестве растворителя, причем получают указанное в заголовке соединение в виде аморфного твердого вещества.
Rt (способ А) = 0,81 мин; МС (ES+) = 485 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,86 (м, 4H), 1,20-1,40 (м, 8H), 1,63 (м, 2H), 1,70 (м, 2H), 1,95 (м, 1H), 2,90 (м, 1H), 3,45 (м, 1H), 3,52 (с, 3H), 3,70 (м, 1H), 3,94 (м, 1H), 4,13 (м, 2H), 4,52 (м, 1H), 5,68 (д, 1H), 6,30 (т, 1H), 6,55 (м, 1H), 7,00 (с, 1H), 7,13 (м, 1H), 7,72 (м, 2H).
Пример 7
3-(6-Аминопиридин-3-ил)-2-(1-циклопентил-1Н-имидазол-4-ил)-пропионовая кислота
Пример 7а
Циклопентиловый эфир (1-циклопентил-1Н-имидазол-4-ил)уксусной кислоты
Гидрохлорид имидазол-4-уксусной кислоты (5,30 г; 32,60 ммоль) и карбонат цезия (31,90 г, 97,80 ммоль) вносят в абсолютный диметилформамид. Туда добавляют циклопентилбромид (10,5 мл; 97,80 ммоль). Перемешивают в течение 3 часов при температуре 110°С, затем фильтруют через осветляющий слой, остаток промывают с помощью СН2Cl2 и фильтрат концентрируют при пониженном давлении. Остаток обрабатывают этилацетатом и раствор промывают водой и 0,5 н. соляной кислотой. Органическую фазу сушат над Na2SO4 и растворитель затем удаляют при пониженном давлении. После очистки сырого продукта при использовании фильтрующего элемента (70 г силикагеля) получают 2,65 г циклопентилового эфира (1-циклопентил-1Н-имидазол-4-ил)уксусной кислоты.
Rt (способ В) = 0,89 мин; МС (ES+) = 263 [M+H]+
Пример 7b
Метиловый эфир циклопентилового эфира 2-(1-циклопентил-1Н-имидазол-4-ил)малоновой кислоты
Циклопентиловый эфир (1-циклопентил-1Н-имидазол-4-ил)-уксусной кислоты (2,00 г; 7,60 ммоль) растворяют в тетрагидрофуране (ТГФ; 45 мл). После охлаждения реакционного раствора до температуры 0°С прикапывают литийгексаметилдисилазан (20%-ный в тетрагидрофуране; 6,33 мл; 7,60 ммоль). Перемешивают в течение следующего часа при температуре 0°С. Затем добавляют метилцианоформиат (0,66 мл; 8,36 ммоль). Перемешивают в течение 10 минут при температуре 0°С и затем 7 часов при комнатной температуре. Реакционный раствор после этого добавляют к насыщенному раствору NH4Cl. Экстрагируют этилацетатом, органическую фазу промывают водой и сушат над Na2SO4. Растворитель удаляют при пониженном давлении. После очистки сырого продукта путем колоночной хроматографии (120 г силикагеля; этилацетат/н-гептан = 2:1) получают 0,46 г метилового эфира циклопентилового эфира 2-(1-циклопентил-1Н-имидазол-4-ил)малоновой кислоты.
Rt (способ В) = 1,01 мин; МС (ES+) = 321 [M+H]+
Пример 7с
Метиловый эфир циклопентилового эфира 2-(6-аминопиридин-3-илметил)-2-(1-циклопентил-1Н-имидазол-4-ил)малоновой кислоты
Метиловый эфир циклопентилового эфира 2-(1-циклопентил-1Н-имидазол-4-ил)малоновой кислоты (0,46 г; 1,44 ммоль) растворяют в абсолютном диметилформамиде (5 мл). При температуре 0°С добавляют гидрид натрия (50%-ный; 0,07 г; 1,44 ммоль). Перемешивают в течение 1 часа при комнатной температуре и затем снова охлаждают до температуры 0°С. После этого добавляют (5-бромметилпиридин-2-ил)-трет-бутилкарбамат (0,41 г; 1,44 ммоль) и перемешивают в течение 2 часов при комнатной температуре. При охлаждении льдом реакцию гасят водой и затем экстрагируют два раза этилацетатом. Органическую фазу отделяют, сушат над Na2SO4 и растворитель удаляют при пониженном давлении. После очистки сырого продукта при использовании фильтрующего элемента (50 г силикагеля) получают 0,31 г метилового эфира циклопентилового эфира 2-(6-аминопиридин-3-илметил)-2-(1-циклопентил-1Н-имидазол-4-ил)малоновой кислоты.
Rt (способ С) = 1,47 мин; МС (ES+) = 527 [M+H]+
Пример 7d
3-(6-Аминопиридин-3-ил)-2-(1-циклопентил-1Н-имидазол-4-ил)-пропионовая кислота
Метиловый эфир циклопентилового эфира 2-(6-аминопиридин-3-илметил)-2-(1-циклопентил-1Н-имидазол-4-ил)малоновой кислоты (0,30 г; 0,57 ммоль) растворяют в абсолютном этаноле (5 мл). При температуре 0°С добавляют этанольный раствор HCl. Реакционный раствор выдерживают в течение 48 часов при температуре 10°С. Затем концентрируют при пониженном давлении и остаток обрабатывают 2 н. соляной кислотой. Нагревают в микроволновой установке (3 х 4 мин; 180°С). После этого промывают этилацетатом и водную фазу нейтрализуют с помощью 1 н. раствора NaOH и затем подвергают сушке вымораживанием. Остаток обрабатывают метанолом и фильтруют дважды через фильтрующий элемент (С18). После концентрирования фильтрата при пониженном давлении получают 3-(6-аминопиридин-3-ил)-2-(1-циклопентил-1Н-имидазол-4-ил)-пропионовую кислоту.
Rt (способ С) = 0,64 мин; МС (ES+) = 301 [M+H]+;
1Н-ЯМР (ДМСО-d6): δ = 1,60 (м, 2H); 1,73 (м, 4H); 2,18 (м, 2H), 2,87 (ддд, 1H); 3,58 (т, 1H); 3,78 (квт, 2H); 4,45 (т, 1H); 5,52 (с, 2H); 6,29 (д, 1H); 6,95 (с, 1H); 7,11 (дд; 1H); 7,55 (с, 1H); 7,65 8 (с, 1H).
Пример 8
3-(6-Аминопиридин-3-ил)-2-(1-пиперидин-4-ил-1Н-имидазол-4-ил)пропионовая кислота
Пример 8а
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-(бензилокси-карбонил)пиперидин-4-ил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор из 60,1 мг (0,23 ммоль) соединения, полученного согласно примеру 1g, 68,9 мг (0,23 ммоль) 4-бром-1-бензилоксикарбонилпиперидина, 97 мкл (0,69 ммоль) триэтиламина в 1 мл абсолютного тетрагидрофурана обрабатывают в течение 2 часов при температуре 180°С в микроволновой установке. Затем реакционный раствор смешивают с 2 мл смеси диэтиловый эфир/вода (1:1), фазу диэтилового эфира отделяют и сушат над Na2SO4. Фильтрация, удаление растворителя и хроматографическая очистка оставшегося остатка путем препаративной ВЭЖХ при использовании CH3CN/вода/0,1% ТФУК в качестве растворителя приводят к 33 мг указанного в заголовке соединения в виде бис-трифторацетата.
Rt (способ А) = 1,18 мин; МС (ES+) = 478 [M+H]+
Пример 8b
Бисгидрохлорид 3-(6-аминопиридин-3-ил)-2-(1-пиперидин-4-ил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор из 17,7 мг (0,03 ммоль) соединения, полученного согласно примеру 2а, в 0,5 мл воды и 0,5 мл 37%-ной соляной килоты обрабатывают в течение 5 минут при температуре 180°С в микроволновой установке. Затем концентрируют досуха при пониженном давлении, остаток растворяют в небольшом количестве воды и раствор подвергают сушке вымораживанием. При этом получают 11,0 мг указанного в заголовке соединения в виде аморфного твердого вещества.
Rt (способ А) = 0,18 мин; МС (ES+) = 316 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,27 (м, 2H), 2,20 (м, 4H), 2,28 (м, 2H), 3,08 (дд, 1H), 3,17 (дд, 1H), 4,15 (м, 2H), 4,52 (м, 1H), 6,85 (д, 1H), 7,52 (д, 1H), 7,75 (м, 2H).
Пример 9
3-(6-Аминопиридин-3-ил)-2-[1-(2-оксо-1-фенилпирролидин-3-ил)-1Н-имидазол-4-ил]пропионовая кислота
Пример 9а
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-[1-(2-оксо-1-фенилпирролидин-3-ил)-1Н-имидазол-4-ил]пропионовой кислоты
Раствор из 60,1 мг (0,23 ммоль) соединения, полученного согласно примеру 1g, в 1 мл абсолютного диметилформамида смешивают с 11 мг (0,23 ммоль) гидрида натрия (50%-ный) и перемешивают в течение 1 часа при комнатной температуре. Затем добавляют 55,5 мг (0,23 ммоль) (+/-)-3-бром-1-фенил-2-пирролидинона и перемешивают в течение 45 минут при комнатной температуре. Реакционный раствор смешивают с 1 мл воды и многократно экстрагируют диэтиловым эфиром. Объединенные экстракты в диэтиловом эфире сушат над Na2SO4, фильтруют и концентрируют. Очистка полученного остатка путем хроматографии на силикагеле при использовании смеси СН2Сl2/метанол (от 92:8 до 85:15 за 35 минут) в качестве растворителя приводит к 52,2 г указанного в заголовке соединения.
Rt (способ А) = 0,93 мин; МС (ES+) = 420 [M+H]+
Пример 9b
Бисгидрохлорид 3-(6-аминопиридин-3-ил)-2-[1-(2-оксо-1-фенилпирролидин-3-ил)-1Н-имидазол-4-ил]пропионовой кислоты
Раствор из 23,1 мг (0,06 ммоль) соединения,полученного согласно примеру 9а, в 0,5 мл воды и 0,5 мл 37%-ной соляной кислоты обрабатывают в течение 3 минут при температуре 180°С в микроволновой установке. Реакционный раствор могократно обрабатывают этанолом и концентрируют при пониженном давлении. Сушка вымораживанием растворенного в воде остатка приводит к 19,0 мг желательного соединения в виде аморфного твердого вещества.
Rt (способ А) = 0,73 мин; МС (ES+) = 392 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,74 (м, 1H), 3,00 (дд, 1H), 3,12 (дд, 1H), 4,91 (м, 1H), 4,02 (м, 3H), 5,48 (дд, 1H), 6,85 (д, 1H), 7,20 (т, 1H), 7,38 (м, 2H), 7,70 (м, 5H), 7,95 (уш.с, 2H).
Пример 10
3-(6-Аминопиридин-3-ил)-2-{1-[(бензгидрилкарбамоил)метил]-1Н-имидазол-4-ил}пропионовая кислота
Пример 10а
N-Бензгидрил-2-бромацетамид
Охлажденный до температуры 0°С раствор из 2,91 г (14,39 ммоль) бромацетилбромида в 40 мл тетрагидрофурана последовательно смешивают с 2,1 мл (14,39 ммоль) триэтиламина и 2,64 г (14,39 ммоль) бензгидриламина. Затем реакционный раствор концентрируют досуха при пониженном давлении и полученный остаток очищают на силикагеле при использовании этилацетата в качестве растворителя. Выкристаллизовавшийся из имеющих значение фракций продукт отфильтровывают под вакуумом, промывают небольшим количеством холодного диэтилового эфира и высушивают при пониженном давлении, причем получают 0,85 г указанного в заголовке соединения.
МС (ES+) = 305 [M+H]+
Пример 10b
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-{1-[(бензгидрил-карбамоил)метил]-1Н-имидазол-4-ил}пропионовой кислоты
Раствор из 60,1 мг (0,23 ммоль) соединения, полученного согласно примеру 1g, в 1 мл абсолютного диметилформамида смешивают с 11 мг (0,23 ммоль) гидрида натрия (50%-ный) и перемешивают в течение 1 часа при комнатной температуре. Затем добавляют 70,3 мг (0,23 ммоль) соединения, полученного согласно примеру 10а, и перемешивают в течение 1 часа при комнатной температуре. Реакционный раствор смешивают с 1 мл воды и многократно экстрагируют этилацетатом. Объединенные этилацетатные экстракты сушат над Na2SO4, фильтруют и концентрируют. Очистка путем хроматографии полученного остатка на силикагеле при использовании смеси СН2Cl2/метанол (9:1) в качестве растворителя приводит к 71,4 мг указанного в заголовке соединения.
Rt (способ А) = 1,24 мин; МС (ES+) = 484 [M+H]+
Пример 10с
Бистрифторацетат 3-(6-аминопиридин-3-ил)-2-{[(бензгидрил-карбамоил)метил]-1Н-имидазол-4-ил}пропионовой кислоты
Раствор из 14 мг (0,03 ммоль) соединения, полученного согласно примеру 10b, в 1 мл тетрагидрофурана смешивают с 147 мкл 1 н. раствора гидроксида лития и перемешивают в течение 30 минут при комнатной температуре. После добавки еще раз 100 мкл 1 н. раствора гидроксида лития перемешивают в течение ночи при комнатной температуре. Затем значение рН раствора устанавливают нейтральным за счет добавки 1 н. соляной кислоты и выпаривают досуха при пониженном давлении. Хроматографическая очистка полученного остатка путем препаративной ВЭЖХ при использовании смеси (0,1% ТФУК)/СН3СN (5:100) в качестве растворителя приводит к 16 мг желательного соединения.
Rt (способ А) = 1,13 мин; МС (ES+) = 456 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,98 (дд, 1H), 3,14 (дд, 1H), 4,08 (дд, 1H), 5,00 (с, 2H), 6,08 (д, 1H), 6,87 (д, 1H), 7,27 (м, 6H), 7,35 (м, 4H), 7,50 (уш.с, 1H), 7,72 (м, 2H), 7,95 (уш.с, 2H), 9,38 (д, 1H).
Оба энантиомера соединения, полученного согласно примеру 10с, разделяют путем препаративной хроматографии при использовании хиральной фазы; фаза: Chiralpak ADH40; размер колонки: 250 х 4 мм; растворитель: гептан:этанол:метанол = 1:1:1 плюс 0,1% ацетата аммония (в изократическом режиме); расход: 1 мл/мин; температура: 30°С:
энантиомер 1: Rt = 3,42 мин; энантиомер 2: Rt = 12,35 мин.
Пример 11
Изопропиловый эфир 3-(6-аминопиридин-3-ил)-2-{1-[(бензгидрил-карбамоил)метил]-1Н-имидазол-4-ил}пропионовой кислоты
Раствор из 50 мг (87,8 мкмоль) соединения, полученного согласно примеру 10с, в 5 мл изопропанола смешивают с 3 мл насыщенного раствора HCl в диэтиловом эфире и перемешивают в течение 12 часов при комнатной температуре. Затем раствор концентрируют досуха и полученный остаток высушивают в высоком вакууме. Получают 39 мг указанного в заголовке соединения в виде бисгидрохлорида в форме аморфного твердого вещества.
Rt (способ А) = 1,31 мин; МС (ES+) = 498 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,15 (д, 6H), 3,13 (м, 2H), 4,25 (дд, 1H), 4,92 (дт, 1H), 5,10 (с, 2H), 6,15 (д, 1H), 6,94 (д, 1H), 7,28 (м, 2H), 7,33 (м, 8H), 7,53 (с, 1H), 7,75 (м, 2H), 8,05 (уш.с, 1H), 9,50 (д, 1H).
Пример 12
3-(6-Аминопиридин-3-ил)-2-{1-[4-(3-фенилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота
Пример 12а
Метиловый эфир (1-тритил-1Н-имидазол-4-ил)уксусной кислоты
Раствор 2,78 г (19,80 ммоль) соединения, полученного согласно примеру 1с, 5,52 г (19,80 ммоль) трифенилметилхлорида и 2,00 г (19,80 ммоль) триэтиламина в 5 мл диметилформамида перемешивают в течение ночи при комнатной температуре, затем выливают в 200 мл воды и дополнительно перемешивают в течение одного часа при комнатной температуре. Выпавший осадок отфильтровывают под вакуумом. Фильтрат трижды экстрагируют этилацетатом. Объединенные органические фазы сушат над Na2SO4, фильтруют и концентрируют. Выделившееся при этом масло желтого цвета и осадок объединяют и хроматографируют на силикагеле. Получают 4,2 г желательного соединения.
1Н-ЯМР (400 МГц, CDCl3): δ = 3,62 (с, 2H), 3,69 (с, 3H), 6,78 (с, 1H), 7,10-7,18 (м, 6H), 7,30-7,36 (м, 9H), 7,38 (с, 1H).
Пример 12b
Диметиловый эфир 2-(1-тритил-1Н-имидазол-4-ил)малоновой кислоты
3,50 г (9,15 ммоль) соединения, полученного согласно примеру 12а, растворяют в 50 мл безводного тетрагидрофурана и охлаждают до температуры 0°С. К этому раствору при перемешивании прикапывают 1,67 г (9,96 ммоль) бис(триметилсилил)амида лития в виде 20%-ного раствора в тетрагидрофуране. Образовавшуюся смесь перемешивают в течение 30 минут при температуре 0°С и затем смешивают с 0,86 г (10,07 моль) метилцианформиата. Реакционную смесь нагревают до комнатной температуры и перемешивают в течение дальнейших 2 часов, после чего выливают в 400 мл насыщенного водного раствора NH4Cl и дважды экстрагируют этилацетатом. Объединенные органические фазы промывают водой, сушат над Na2SO4, фильтруют и концентрируют. Хроматография остатка на силикагеле приводит к 1,92 г указанного в заголовке соединения. Осуществляемая еще раз хроматография образовавшейся смешанной фракции приводит к дальнейшим 40 мг желательного соединения.
Rt (способ С) = 2,17 мин; МС (ES+) = 498 [M+H]+;
1Н-ЯМР (400 МГц, CDCl3): δ = 3,76 (с, 6H), 4,78 (с, 1H), 6,98 (с, 1H) 7,10-7,18 (м, 6H), 7,28-7,33 (м, 9H), 7,38 (с, 1H).
Пример 12с
Диметиловый эфир 2-(6-трет-бутоксикарбониламинопиридин-3-илметил)-2-(1-тритил-1Н-имидазол-4-ил)малоновой кислоты
Раствор 2,25 г (5,11 ммоль) соединения, полученного согласно примеру 12b, в 40 мл безводного диметилформамида при температуре 0°С смешивают с 0,12 г (5,12 ммоль; 50%-ный) гидрида натрия и перемешивают в течение 5 минут при этой температуре. Затем выдерживают для повышения температуры до комнатной, перемешивают в течение 1 часа, снова охлаждают до температуры 0°С и затем в виде одной порции добавляют 1,47 г (5,11 ммоль) соединения, полученного согласно примеру 1b. При этой температуре продолжают перемешивание в течение 30 минут, после чего при охлаждении льдом смешивают с 50 мл воды и трижды экстрагируют дихлорметаном. Объединенные органические фазы сушат над Na2SO4, фильтруют и концентрируют. Остаток очищают хроматографией на силикагеле. Получают 3,15 г указанного в заголовке соединения.
1Н-ЯМР (400 МГц, CDCl3): δ = 1,53 (с, 9H), 3,63 (с, 2H), 3,72 (с, 6H), 7,01-7,05 (м, 2H), 7,06-7,11 (м, 6H), 7,28-7,37 (м, 10H), 7,42 (с, 1H), 7,70-7,77 (м, 2H).
Пример 12d
Диметиловый эфир 2-(6-трет-бутоксикарбониламинопиридин-3-илметил)-2-(1Н-имидазол-4-ил)малоновой кислоты
К охлажденному льдом раствору 1,00 г (1,55 ммоль) соединения, полученного согласно примеру 12с, в 15 мл СН2Cl2 при перемешивании добавляют 0,20 г (1,70 ммоль, 272 мкл) триэтилсилана и 1,76 г (15,46 ммоль, 1,19 мл) трифторуксусной кислоты и перемешивают далее при температуре 0°С. Спустя 5 часов при охлаждении льдом смешивают с 10 мл воды и устанавливают значение рН 9 с помощью 2 н. раствора NaOH. Выпавший осадок отфильтровывают под вакуумом, растирают в порошок примерно в 20 мл CH2Cl2, отфильтровывают под вакуумом и высушивают. Получают 0,55 г желательного соединения.
1Н-ЯМР (400 МГц, CDCl3): δ = 1,49 (с, 9H), 3,58 (с, 2H), 3,77 (с, 6H), 6,99 (д, 1H), 7,06 (с, 1H), 7,21 (с, 1H), 7,60-7,69 (м, 3H).
Пример 12е
Диметиловый эфир 2-(6-трет-бутоксикарбониламинопиридин-3-ил-метил)-2-[1-(4-нитрофенил)-1Н-имидазол-4-ил]малоновой кислоты
Раствор 404 мг (1,00 ммоль) соединения, полученного согласно примеру 12d, в 10 мл диметилформамида охлаждают до температуры 0°С и при перемешивании порциями смешивают с 80 мг (2,00 ммоль, 60%-ный) гидрида натрия. Перемешивают в течение 1 часа при температуре 0°С, затем добавляют 423 мг (3 ммоль) 4-фторнитробензола и перемешивают при комнатной температуре вплоть до полного превращения. Смесь смешивают с насыщенным водным раствором NaHCO3 и экстрагируют диэтиловым эфиром. Органическую фазу сушат над Na2SO4, фильтруют и концентрируют. Остаток очищают хроматографией на силикагеле. Получают 394 мг указанного в заголовке соединения.
Rt (способ В) = 1,30 мин; МС (ES+) = 526 [M+H]+
Пример 12f
Диметиловый эфир 2-[1-(4-аминофенил)-1Н-имидазол-4-ил]-2-(6-трет-бутоксикарбониламинопиридин-3-илметил)малоновой кислоты
Раствор 384 мг (0,73 ммоль) соединения, полученного согласно примеру 12е, в 10 мл диметилформамида смешивают с 824 мг (3,66 ммоль) дигидрата хлорида олова-(II) и перемешивают в течение ночи при комнатной температуре. Затем растворитель выпаривают и остаток распределяют между диэтиловым эфиром и насыщенным водным раствором NaHCO3. Водную фазу экстрагируют дважды диэтиловым эфиром. Объединенные органические фазы сушат над Na2SO4, фильтруют и концентрируют. Получают 103 мг желательного соединения.
Rt (способ В) = 0,93 мин; МС (ES+) = 496 [M+H]+
Пример 12g
Диметиловый эфир 2-(6-трет-бутоксикарбониламинопиридин-3-илметил)-2-{1-[4-(3-фенилуреидо)фенил]-1Н-имидазол-4-ил}-малоновой кислоты
50 мг (0,10 ммоль) соединения, полученного согласно примеру 12f, растворяют в 10 мл ацетонитрила. Полученный раствор охлаждают до температуры 0°С и смешивают с 14 мг (0,12 ммоль, 13,2 мкл) фенилизоцианата и 20 мг (0,20 ммоль, 28 мкл) три-этиламина. Нагревают до комнатной температуры и добавляют на кончике шпателя 4-диметиламинопиридин. После выдерживания в течение ночи реакционную смесь выпаривают и остаток хроматографируют на силикагеле. Получают 47 мг указанного в заголовке соединения.
Rt (способ В) = 1,28 мин; МС (ES+) = 615 [M+H]+
Пример 12h
3-(6-Аминопиридин-3-ил)-2-{1[4-(3-фенилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота
47 мг (75 мкмоль) соединения, полученного согласно примеру 12g, в 4 мл полуконцентрированной соляной кислоты нагревают до температуры 100°С. Спустя 1,5 часа смесь разбавляют водой и реакционную смесь подвергают сушке вымораживанием. Препаративная ВЭЖХ остатка приводит к 19 мг указанного в заголовке соединения в виде бистрифторацетата.
Rt (способ В) = 0,85 мин; МС (ES+) = 443 [M+H]+;
1Н-ЯМР (400 МГц, ДМСО-d6): δ = 3,07 (дд, 1H), 3,20 (дд, 1H), 4,00 (м, 1H), 6,90 (д, 1H), 6,98 (т, 1H), 7,30 (т, 2H), 7,43 (д, 2H), 7,61 (м, 4H), 7,78 (с, 1H), 7,80 (дд, 2H), 7,90 (с, 2H, уш.), 8,82 (с, 1H, уш.), 8,98 (с, 1H), 9,16 (с, 1H).
Пример 13
3-(6-Аминопиридин-3-ил)-2-{1-[2-(1-дифенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота
Пример 13а
1-[4-(2-Гидроксиэтил)пиперидин-1-ил]-2,2-дифенилэтанон
2-Пиперидин-4-илэтанол (1,12 г; 8,65 ммоль) вносят в диметилформамид (ДМФА, 10 мл). Затем добавляют гидроксибензотриазол (НОВТ, 1,46 г, 9,51 ммоль), 1-этил-3-(3-диметиламинопропил)карбодиимидгидрохлорид (EDC∙HCl, 1,83 г; 9,51 ммоль) и дифенилуксусную кислоту (2,02 г; 9,51 ммоль) в указанной последовательности. После этого реакционную смесь смешивают с N,N-диизопропилэтиламином (DIEA; 1,67 мл; 9,51 ммоль) и перемешивают при комнатной температуре в течение 16 часов. Реакционный раствор концентрируют при пониженном давлении. Остаток обрабатывают диэтиловым эфиром и органический раствор промывают последовательно насыщенным раствором NaHCO3, 2 н. HCl и насыщенным раствором NaCl. Органическую фазу отделяют, сушат над Na2SO4, фильтруют и концентрируют. Таким образом полученный 1-[4-(2-гидроксиэтил)пиперидин-1-ил]-2,2-дифенилэтанон (2,39 г; 8,11 ммоль) вводят во взаимодействие далее без дальнейшей очистки.
Rt (способ В) = 1,33 мин; МС (ES+) = 324 [M+H]+
Пример 13b
1-[4-(2-Бромэтил)пиперидин-1-ил]-2,2-дифенилэтанон
1-[4-(2-Гидроксиэтил)пиперидин-1-ил]-2,2-дифенилэтанон (2,39 г; 8,11 ммоль) растворяют в дихлорметане (20 мл). При комнатной температуре медленно прикапывают трибромид фосфора (1,6 мл; 8,92 ммоль). Реакционную смесь кипятят с обратным холодильником в течение 4 часов. После охлаждения промывают насыщенным раствором NaHCO3, 2 н. HCl и насыщенным раствором NaCl, органическую фазу отделяют и сушат над Na2SO4. Растворитель удаляют при пониженном давлении. После очистки остатка при использовании фильтрующего элемента (силикагель) получают 1-[4-(2-бромэтил)пиперидин-1-ил]-2,2-дифенилэтанон (0,75 г; 2,13 ммоль).
Rt (способ В) = 1,79 мин; МС (ES+) = 386 [M+H]+
Пример 13с
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-{1-[2-(1-дифенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовой кислоты
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-(1Н-имидазол-4-ил)пропионовой кислоты (100 мг; 0,38 ммоль) растворяют в абсолютном диметилформамиде (2 мл). Добавляют гидрид натрия (50%-ный; 19 мг; 0,38 ммоль) и реакционную смесь перемешивают в течение 1 часа при комнатной температуре. Затем добавляют растворенный в абсолютном диметилформамиде (1 мл) 1-[4-(2-бромэтил)пиперидин-1-ил]-2,2-дифенилэтанон (148 мг; 0,38 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 1 часа и затем концентрируют при пониженном давлении. Остаток обрабатывают 1 н. HCl и промывают дихлорметаном (СН2Cl2; 2 раза). Водную фазу подщелачивают с помощью 1 н. раствора NaOH и 3 раза экстрагируют дихлорметаном. Объединенные органические фазы сушат над Na2SO4. После удаления растворителя при пониженном давлении получают этиловый эфир 3-(6-аминопиридин-3-ил)-2-{1-[2-(1-дифенилацетилпиперидин-4-ил)-этил]-1Н-имидазол-4-ил}пропионовой кислоты (71 мг; 0,12 ммоль).
Rt (способ В) = 0,98 мин; МС (ES+) = 566 [M+H]+
Пример 13d
3-(6-Аминопиридин-3-ил)-2-{1-[2-(1-дифенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-{1-[2-(1-дифенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовой кислоты (71 мг; 0,12 ммоль) растворяют в абсолютном этаноле (600 мкл). К полученному раствору добавляют 1 н. раствор NaOH (128 мкл; 0,12 ммоль). Реакционную смесь перемешивают при комнатно температуре в течение 16 часов. Затем нейтрализуют с помощью 1 н. HCl (128 мкл; 0,12 ммоль) и концентрируют при пониженном давлении. Обрабатывают метанолом и фильтруют через С18-колонку. Метанол удаляют и добавляют ацетонитрил и дважды декантируют и остаток затем растирают в порошок в диэтиловом эфире. Осадок отфильтровывают и высушивают в высоком вакууме при температуре 40°С. Получают 3-(6-аминопиридин-3-ил)-2-{1-[2-(1-дифенилацетил-пиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовую кислоту (50 мг; 0,09 ммоль) в виде бесцветного твердого вещества.
Rt (способ С) = 1,20 мин; МС (ES+) = 538 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,90 (м, 1H); 1,02-1,51 (м, 5H); 1,61 (м, 2H); 2,67 (м, 2H); 2,94 (м, 1H); 3,11 (м, 1H); 3,18-3,56 (м, 3H), 3,65 (м, 1H); 3,90 (м, 1H); 4,09 (т; 1H); 5,54 (м; 2H); 6,29 (д,1H); 6,89 (с, 1H); 7,23 (м, 12H); 7,65 (м, 1H).
Пример 14
3-(6-Аминопиридин-3-ил)-2-{1-[2-(1-бензоилпиперидин-4-ил)-этил]-1Н-имидазол-4-ил}пропионовая кислота
Указанное в заголовке соединение (54 мг; 0,12 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 0,88 мин; МС (ES+) = 448 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,10 (м, 2H); 1,41 (м, 1H); 1,60 (м, 3H); 1,72 (м, 1H); 2,71 (м, 2H); 2,95 (м, 2H); 3,48 (м, 3H); 3,92 (т, 2H); 4,45 (м, 1H); 5,57 (с; 2H); 6,28 (д, 1H); 6,90 (с, 1H); 7,11 (д, 1H); 7,32 (м, 2H); 7,43 (м, 3H); 7,49 (с, 1H); 7,61 (с, 1H).
Пример 15
3-(6-Аминопиридин-3-ил)-2-[1-(1-бензоилпиперидин-2-илметил)-1Н-имидазол-4-ил]пропионовая кислота
Указанное в заголовке соединение (41 мг; 0,09 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 0,81 мин; МС (ES+) = 434 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,12 (м, 2H); 1,39 (м, 1H); 1,61 (м, 1H); 1,92 (м, 1H); 2,80 (м, 4H); 3,48 (м, 5H); 4,20 (м, 1H); 5,60 (с; 2H); 6,28 (д, 1H); 6,90 (м, 1H); 7,10 (д, 1H); 7,35 (м, 6H); 7,61 (с, 1H).
Пример 16
3-(6-Аминопиридин-3-ил)-2-(1-{2-[1-(3-фенилпропионил)пиперидин-3-ил]этил}-1Н-имидазол-4-ил)пропионовая кислота
Указанное в заголовке соединение (15 мг; 0,03 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 1,04 мин; МС (ES+) = 476 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,15 (м, 3H); 1,55 (м, 3H); 1,75 (м, 1H); 2,59 (м, 2H); 2,77 (м, 2H); 2,92 (м, 2H); 3,40 (м, 4H); 3,65 (м, 1H); 3,89 (т, 2H), 4,15 (м, 1H); 5,55 (с, 2H); 6,28 (д, 1H); 6,89 (м, 1H); 7,13 (м, 2H); 7,22 (м, 4H); 7,45 (с, 1H); 7,63 (м, 1H).
Пример 17
3-(6-Аминопиридин-3-ил)-2-[1-(1-дифенилацетилпиперидин-3-ил-метил)-1Н-имидазол-4-ил]пропионовая кислота
Указанное в заголовке соединение (19 мг; 0,03 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 1,13 мин; МС (ES+) = 524 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,85-1,75 (м, 5H); 2,55-3,07 (м, 4H); 3,07-3,83 (м, 6H); 4,09 (м, 1H); 5,62 (м, 2H); 6,29 (м, 1H); 6,89 (м, 1H); 7,23 (м, 12H); 7,65 (м, 1H).
Пример 18
3-(6-Аминопиридин-3-ил)-2-(1-{2-[1-(3-фенилпропионил)пиперидин-4-ил]этил}-1Н-имидазол-4-ил)пропионовая кислота
Указанное в заголовке соединение (81 мг; 0,17 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 1,00 мин; МС (ES+) = 476 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,92 (м, 2H); 1,32 (м, 1H); 1,55 (м, 4H); 2,55 (м, 2H); 2,85 (м, 4H); 3,40 (м, 4H); 3,79 (м, 1H); 3,88 (т, 2H), 4,33 (д, 1H); 5,65 (с, 2H); 6,29 (д, 1H); 6,89 (с, 1H); 7,13 (м, 2H); 7,22 (м, 4H); 7,45 (с, 1H); 7,63 (м, 1H).
Пример 19
3-(6-Аминопиридин-3-ил)-2-{1-[2-(1-фенилацетилпиперидин-3-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота
Указанное в заголовке соединение (28 мг; 0,06 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 0,93 мин; МС (ES+) = 462 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,90 (м, 2H); 1,35 (м, 1H); 1,58 (м, 4H); 2,80 (м, 2H); 2,95 (м, 2H); 3,40 (м, 4H); 3,69 (с, 1H); 3,85 (т, 2H), 4,33 (д, 1H); 5,60 (с, 2H); 6,29 (д, 1H); 6,90 (с, 1H); 7,10 (дд, 1H); 7,19 (м, 3H); 7,27 (м, 2H); 7,48 (с, 1H); 7,61 (м, 1H).
Пример 20
3-(6-Аминопиридин-3-ил)-2-{1-[2-(1-фенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота
Указанное в заголовке соединение (41 мг; 0,08 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 0,91 мин; МС (ES+) = 462 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,92 (м, 2H); 1,25 (м, 1H); 1,58 (м, 4H); 2,65-4,20 (м, 12H); 5,65 (м, 2H); 6,29 (м, 1H); 6,90 (м, 1H); 7,20 (6H); 7,60 (м, 2H).
Пример 21
3-(6-Аминопиридин-3-ил)-2-{1-[1-(4'-метилбифенил-3-карбонил)пиперидин-4-илметил]-1Н-имидазол-4-ил}пропионовая кислота
Указанное в заголовке соединение (33 мг; 0,06 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 1,21 мин; МС (ES+) = 524 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,12 (м, 2H); 1,45 (м, 2H); 1,95 (м, 1H); 2,36 (с, 3H); 2,80-3,60 (м, 6H); 3,71 (т, 1H); 3,85 (д, 2H); 4,45 (м, 1H); 6,49 (д, 1H); 6,60 (м, 2H); 6,87 (с, 1H); 7,29 (м, 4H); 7,58 (м, 4H); 7,65 (м, 1H); 7,72 (м, 2H).
Пример 22
3-(6-Аминопиридин-3-ил)-2-[1-(1-бензоилпиперидин-4-илметил)-1Н-имидазол-4-ил]пропионовая кислота
Указанное в заголовке соединение (46 мг; 0,10 ммоль) синтезируют аналогично указанному в примере 13.
Rt (способ С) = 0,81 мин; МС (ES+) = 434 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,10 (м, 2H); 1,45 (м, 2H); 1,95 (м, 1H); 2,80-3,10 (м, 4H); 3,50 (м, 2H) 3,62 (т, 1H); 3,82 (д, 2H); 4,48 (м, 1H); 6,03 (м, 2H); 6,48 (д, 1H); 6,90 (д, 1H); 7,19 (д, 1H); 7,35 (м, 2H); 7,42 (м, 3H); 7,55 (с, 1H); 7,61 (с, 1H).
Пример 23
3-(6-Аминопиридин-3-ил)-2-(1-бензгидрил-1Н-имидазол-4-ил)-пропионовая кислота
Раствор 50 мг (0,19 ммоль) этилового эфира 3-(6-аминопиридин-3-ил)-2-(1Н-имидазол-4-ил)пропионовой кислоты (пример 1g) в 0,5 мл диметилформамида при комнатной температуре смешивают с 11 мг (0,23 ммоль, 50%-ный) гидрида натрия и перемешивают в течение 1 часа. Затем добавляют 48 мг (0,19 ммоль) бромдифенилметана и перемешивают 3,5 часа при комнатной температуре. После этого нагревают еще в течение 2 часов при температуре 60°С, после охлаждения добавляют 1 мл воды, экстрагируют этилацетатом, органическую фазу сушат над Na2SO4, фильтруют и концентрируют. Хроматография на силикагеле приводит к этиловому эфиру 3-(6-аминопиридин-3-ил)-2-(1-бензгидрил-1Н-имидазол-4-ил)пропионовой кислоты.
Таким образом полученный продукт обрабатывают с помощью 0,4 мл полуконцентрированной соляной кислоты и в течение 3 минут при температуре 180°С обрабатывают в микроволновой установке. Путем сушки вымораживанием, после охлаждения, реакционной смеси получают 5 мг указанного в заголовке соединения в виде бисгидрохлорида.
Rt (способ А) = 1,04 мин; МС (ES+) = 399 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 3,05 (дд, 1H); 3,11 (дд, 1H); 3,70 (м, 1H); 4,12 (м, 1H); 6,38 (дд, 1H); 7,02 (с, 1H), 7,12 (дд, 1H), 7,23-7,51 (м, 6H), 7,67 (д, 1H), 7,72 (м, 1H); 8,02 (с, уш, 2H), 9,03 (с, 1H).
Пример 24
3-(6-Аминопиридин-3-ил)-2-[1-(4-[1,2,4]триазол-1-илбензил)-1Н-имидазол-4-ил]пропионовая кислота
Раствор 60 мг (0,23 ммоль) этилового эфира 3-(6-аминопиридин-3-ил)-2-(1Н-имидазол-4-ил)пропионовой кислоты (пример 1g) в 0,5 мл диметилформамида при комнатной температуре смешивают с 11 мг (0,23 ммоль, 50%-ный) гидрида натрия и перемешивают в течение 1 часа. Затем добавляют 55 мг (0,23 ммоль) 1-[4-(бромметил)фенил]-1Н-1,2,4-триазола и перемешивают в течение 3 часов при комнатной температуре. После этого добавляют 1 мл воды, экстрагируют этилацетатом, органическую фазу сушат над Na2SO4, фильтруют и концентрируют. Путем хроматографии на силикагеле получают этиловый эфир 3-(6-аминопиридин-3-ил)-2-[1-(4-[1,2,4]триазол-1-илбензил)-1Н-имидазол-4-ил]-пропионовой кислоты. Таким образом полученный продукт обрабатывают с помощью 0,4 мл полуконцентрированной соляной кислоты и в течение 3 мин при температуре 180°С обрабатывают в микроволновой установке. Путем сушки вымораживанием, после охлаждения, реакционной смеси получают 5 мг указанного в заголовке соединения в виде бисгидрохлорида.
Rt (способ А) = 0,16 мин; МС (ES+) = 390 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 3,03 (дд, 1H); 3,21 (дд, 1H); 4,21 (м, 1H); 5,45 (с, 2H); 6,91 (д, 1H); 7,50 (д, 2H); 7,60 (с, 1H); 7,70-7,78 (м, 2H); 7,86 (д, 1H); 7,95 (д, 2H); 8,08 (с, уш, 2H); 8,26 (с, 1H); 9,28 (с, 1H), 9,38 (с, 1H).
Пример 25
3-(6-Аминопиридин-3-ил)-2-[1-(4-трифторметоксибензил)-1Н-имидазол-4-ил]пропионовая кислота
Указанное в заголовке соединение получают аналогично указанному в примере 24.
Rt (способ А) = 1,04 мин; МС (ES+) = 407 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,98 (дд, 1H); 3,12 (дд, 1H); 4,02 (м, 1H); 5,33 (с, 2H); 6,84 (д, 1H); 7,30 (дд, 1H); 7,35-7,46 (м, 4H); 7,68 (м, 2H); 7,93 (с, br, 2H), 8,75 (с, уш, 1H).
Пример 26
3-(6-Аминопиридин-3-ил)-2-[1-(1,1-диоксо-1Н-1,6-бензо[b]тиофен-2-илметил)-1Н-имидазол-4-ил]пропионовая кислота
Указанное в заголовке соединение получают аналогично указанному в примере 24.
Rt (способ А) = 0,88 мин; МС (ES+) = 411 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,10 (с, 2H); 3,06 (дд, 1H); 3,18 (дд, 1H); 3,99 (м, 1H); 7,40 (д, 1H); 7,22 (д, 1H); 7,60 (с, 1H); 7,70-7,82 (м, 5H); 7,98 (с, уш, 2H); 7,99 (с, 1H); 8,46 (с, 1H).
Пример 27
3-(6-Аминопиридин-3-ил)-2-[1-(5-хлорбензо[b]тиофен-3-илметил)-1Н-имидазол-4-ил]пропионовая кислота
Указанное в заголовке соединение получают аналогично указанному в примере 24; его получают в виде бистрифторацетата при использовании препаративной ВЭЖХ.
Rt (способ А) = 0,98 мин; МС (ES+) = 413 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,98 (дд, 1H); 3,13 (дд, 1H); 4,06 (м, 1H); 5,61 (с, 2H); 6,78 (д, 1H); 7,42-7,53 (м, 2H); 7,63 (д, 1H); 7,70 (с, 1H); 7,84-7,98 (м, 3H); 8,02 (с, 1H); 8,09 (д, 1H); 8,92 (с, уш, 1H).
Пример 28
3-(6-Аминопиридин-3-ил)-2-{1-[3-(4-фторфенокси)бензил]-1Н-имидазол-4-ил}пропионовая кислота
Указанное в заголовке соединение получают аналогично указанному в примере 24; его получают в виде бистрифторацетата при использовании препаративной ВЭЖХ.
Rt (способ А) = 1,09 мин; МС (ES+) = 433 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,98 (дд, 1H); 3,13 (дд, 1H); 4,08 (м, 1H); 5,30 (с, 2H); 6,81 (д, 1H); 6,95 (дд, 2H); 7,07 (м, 3H); 7,23 (дд, 2H); 7,40 (дд, 1H); 7,44 (м, 1H); 7,69 (м, 2H); 7,93 (с, уш, 2H); 8,87 (с, уш, 1H).
Пример 29
3-(6-Аминопиридин-3-ил)-2-[1-(2-феноксибензил)-1Н-имидазол-4-ил]пропионовая кислота
Указанное в заголовке соединение получают аналогично указанному в примере 24, его получают в виде бистрифторацетата при использовании препаративной ВЭЖХ.
Rt (способ А) = 1,05 мин; МС (ES+) = 415 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,97 (дд, 1H); 3,13 (дд, 1H); 4,03 (м, 1H); 5,37 (с, 2H); 6,82 (м, 2H); 6,90 (д, 2H); 7,17 (м, 2H); 7,30 (д, 1H); 7,32-7,43 (м, 4H); 7,69 (м, 2H); 7,92 (с, уш, 2H); 8,82 (с, уш, 1H).
Пример 30
3-(6-Аминопиридин-3-ил)-2-[1-(4-феноксибензил)-1Н-имидазол-4-ил]пропионовая кислота
Указанное в заголовке соединение получают аналогично указанному в примере 24, его получают в виде бистрифторацетата при использовании препаративной ВЭЖХ.
Rt (способ А) = 1,08 мин; МС (ES+) = 415 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,99 (дд, 1H); 3,13 (дд, 1H); 4,07 (м, 1H); 5,28 (с, 2H); 6,84 (д, 1H); 7,01 (м, 3H); 7,17 (дд, 1H); 7,32 (д, 2H); 7,40 (м, 3H); 7,48 (м, 1H); 7,68 (м, 2H); 7,90 (с, уш, 2H); 8,88 (с, уш, 1H).
Пример 31
3-(6-Аминопиридин-3-ил)-2-(1-проп-2-инил-1Н-имидазол-4-ил)-пропионовая кислота
Пример 31а
Диметиловый эфир 2-(6-трет-бутоксикарбониламинопиридин-3-илметил)-2-(1-проп-2-инил-1Н-имидазол-4-ил)малоновой кислоты
Раствор 100 мг (0,25 ммоль) диметилового эфира 2-(6-трет-бутоксикарбониламинопиридин-3-илметил)-2-(1Н-имидазол-4-ил)-малоновой кислоты (пример 12d) в 2 мл диметилформамида последовательно смешивают с 322 мг (0,99 ммоль) карбоната цезия, а также с 20 мкл (0,27 ммоль, 80%-ный в толуоле) пропаргилбромида. Смесь перемешивают в течение 3 часов при комнатной температуре, затем выливают в воду и экстрагируют диэтиловым эфиром. Путем хроматографической очистки на силикагеле получают 27 мг указанного в заголовке соединения.
1Н-ЯМР (400 МГц, CDCl3): δ = 1,49 (с, 9H); 1,52 (д, 1H); 2,52 (м, 1H); 3,60 (с, 2H); 4,67 (д, 2H); 6,98 (д, 1H); 7,12 (с, 1H); 7,21 (с, 1H); 7,60 (с, 1H); 7,68 (д, 1H).
Пример 31b
3-(6-Аминопиридин-3-ил)-2-(1-проп-2-инил-1Н-имидазол-4-ил)-пропионовая кислота
Раствор 40 мг (0,09 ммоль) соединения, полученного согласно примеру 31а, в 1,4 мл полуконцентрированной соляной кислоты нагревают в течение 9 часов при температуре 95°С. Путем сушки вымораживанием, после охлаждения, получают 21 мг указанного в заголовке соединения в виде бисгидрохлорида.
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 3,11 (дд, 1H); 3,20 (дд, 1H); 3,78 (с, 1H); 4,21 (т, 1H); 5,12 (д, 2H); 6,92 (д, 1H); 7,54 (с, 1H); 7,75 (м, 2H); 8,04 (с, уш, 2H); 9,03 (с, 1H).
Пример 32
3-(6-Аминопиридин-3-ил)-2-(1-бут-2-инил-1Н-имидазол-4-ил)-пропионовая кислота
Пример 32а
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-бут-2-инил-1Н-имидазол-4-ил)пропионовой кислоты
Раствор 60 мг (0,23 ммоль) этилового эфира 3-(6-аминопиридин-3-ил)-2-(1Н-имидазол-4-ил)пропионовой кислоты (пример 1g) в 0,5 мл диметилформамида при комнатной температуре смешивают с 11 мг (0,23 ммоль, 50%-ный) гидрида натрия и перемешивают в течение 1 часа. Затем добавляют 31 мг (37 мкл, 0,23 ммоль) 1-бром-2-бутина и перемешивают в течение 1 часа при комнатной температуре. Смешивают затем с 1 мл воды и экстрагируют диэтиловым эфиром. Органическую фазу сушат над Na2SO4, фильтруют и концентрируют. Путем хроматографии остатка на силикагеле получают 28 мг указанного в заголовке соединения.
Rt (способ А) = 0,69 мин; МС (ES+) = 313 [M+H]+
Пример 32b
3-(6-Аминопиридин-3-ил)-2-(1-бут-2-инил-1Н-имидазол-4-ил)-пропионовая кислота
Раствор 25 мг (0,08 ммоль) соединения, полученного согласно примеру 32а, в 2 мл тетрагидрофурана смешивают с 88 мкл 1 н. раствора NaOH и перемешивают в течение 4 часов при комнатной температуре. Затем и еще раз после перемешивания в течение ночи добавляют по 40 мкл 1 н. раствора NaOH. После дальнейшего перемешивания в течение 24 часов нейтрализуют с помощью 2 н. HCl и реакционную смесь подвергают сушке вымораживанием. Путем препаративной ВЭЖХ получают 5 мг указанного в заголовке соединения в виде бистрифторацетата.
Rt (способ А) = 0,23 мин; МС (ES+) = 285 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,88 (с, 3H); 3,12 (м, 2H); 4,18 (м, 1H); 5,02 (с, 2H); 6,93 (д, 1H); 7,56 (с, 1H); 7,78 (м, 2H); 8,04 (с, уш, 2H); 8,97 (с, уш, 1H).
Следующие соединения получают аналогично указанному в примере 1.
Пример 33
3-(6-Аминопиридин-3-ил)-2-[1-(4,4-диметилциклогексил)-1Н-имидазол-4-ил]пропионовая кислота в виде бисгидрохлорида
Rt (способ С) = 0,93 мин; МС (ES+) = 343 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,93 (с, 3H); 1,00 (с, 3H); 1,33 (м, 2H); 1,48 (м, 2H); 1,85 (м, 4H); 3,04 (дд, 1H); 3,20 (дд, 1H); 4,11 (т, 1H); 4,16 (м, 1H); 6,90 (д, 1H); 7,73 (д, 2H); 7,81 (с, 1H); 8,02 (с, 2H, уш); 9,14 (с, 1H).
Аналогично указанному в примере 10 получают нижеследующие соединения.
Примеры 34-36
3-(6-Аминопиридин-3-ил)-2-{1-[(бензгидрилметилкарбамоил)-метил]-1Н-имидазол-4-ил}пропионовая кислота в виде бистрифторацетата.
Rt (способ С) = 1,18 мин; МС (ES+) = 470 [M+H]+
3-(6-Аминопиридин-3-ил)-2-[1-({[(4-хлорфенил)фенилметил]-карбамоил}метил)-1Н-имидазол-4-ил]пропионовая кислота в виде бистрифторацетата.
Rt (способ С) = 1,22 мин; МС (ES+) = 490 [M+H]+
или
3-(6-Аминопиридин-3-ил)-2-[1-({[бис(4-метоксифенил)метил]-карбамоил}метил)-1Н-имидазол-4-ил]пропионовая кислота в виде бистрифторацетата.
Rt (способ В) = 0,92 мин; МС (ES+) = 516 [M+H]+
Пример 37
3-(6-Аминопиридин-3-ил)-2-{1-[4-(3-пропилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота
Пример 37а
Метиловый эфир 3-(6-трет-бутоксикарбониламинопиридин-3-ил)-2-[1-(толуол-4-сульфонил)-1Н-имидазол-4-ил]пропионовой кислоты
Раствор 1,00 г (3,39 ммоль) метилового эфира (1-бензолсульфонил-1Н-имидазол-4-ил)уксусной кислоты (пример 1d) в 100 мл тетрагидрофурана охлаждают до температуры -78°С и в течение 3 минут смешивают, в три порции, с 3,74 мл (3,74 ммоль, 1 М раствор в тетрагидрофуране) бис(триметилсилил)амида лития. Перемешивают в течение 5 минут при этой температуре и затем смешивают, в одну порцию, с 0,65 г (2,26 ммоль) трет-бутилового эфира (5-бромметилпиридин-2-ил)карбаминовой кислоты (пример 1b). Оставляют перемешиваться в течение 1 часа при температуре -78°С и затем доводят до комнатной температуры. Смесь вносят в смесь из этилацетата и насыщенного раствора NaHCO3. После встряхивания органическую фазу отделяют, сушат над Na2SO4, фильтруют и концентрируют досуха. Остаток перекристаллизуют из смеси этилацетат/гептан. Образовавшиеся кристаллы отфильтровывают под вакуумом, промывают небольшим количеством этилацетата и гептана и высушивают. Получают 0,66 г указанного в заголовке соединения.
Rt (способ В) = 1,30 мин; МС (ES+) = 501 [M+H]+
Пример 37b
Метиловый эфир 3-(6-трет-бутоксикарбониламинопиридин-3-ил)-2-(1Н-имидазол-4-ил)пропионовой кислоты
К раствору 0,65 г (1,29 ммоль) метилового эфира 3-(6-трет-бутоксикарбониламинопиридин-3-ил)-2-[1-(толуол-4-сульфонил)-1Н-имидазол-4-ил]пропионовой кислоты (пример 37а) в 25 мл метанола добавляют 0,80 г (5,24 ммоль) 1-гидроксибензотриазолгидрата и смесь перемешивают в течение 2 часов при комнатной температуре. Растворитель выпаривают при пониженном давлении и остаток очищают на силикагеле при использовании смеси растворителей из СН2Cl2 и 10%-ного раствора аммиака в метаноле. Путем второй колоночной хроматографии на силикагеле получают 341 мг указанного в заголовке соединения.
Rt (способ В) = 0,78 мин; МС (ES+) = 347 [M+H]+;
1Н-ЯМР (400 МГц, ДМСО-d6): δ = 1,46 (с, 9H), 3,08 (м, 2H); 3,52 (с, 3H); 3,87 (т, 1H); 6,92 (с, 1H); 6,98 (д, 1H); 7,55 (с, 1H); 7,63 (д, 1H); 7,98 (с, 1H).
Способ 37с
3-(6-Аминопиридин-3-ил)-2-{1-[4-(3-пропилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота
Указанное в заголовке соединение получают путем превращения соединения, полученного согласно примеру 37b, аналогично указанному в примерах 12е-12g и последующего, известного из литературы обычного отщепления защитной группы в смеси СН2Cl2/ТФУК (1:1). Затем осуществляют замещение как указывается в примере 10с. Путем препаративной ВЭЖХ получают 8 мг указанного в заголовке соединения в виде бистрифторацетата.
Rt (способ В) = 0,73 мин; МС (ES+) = 409 [M+H]+;
1Н-ЯМР (400 МГц, ДМСО-d6): δ = 0,88 (т, 3H); 1,45 (дт, 2H); 3,07 (м, 3H); 3,18 (м, 1H); 3,97 (т, 1H); 6,28 (т, 1H); 6,89 (д, 1H); 7,51 (м, 4H); 7,21 (д, 2H); 7,31 (д, 1H); 7,86 (с, 2H, уш); 8,19 (с, 1H).
Пример 38
3-(6-Аминопиридин-3-ил)-2-{1-[4-(толуол-4-сульфониламино)-фенил]-1Н-имидазол-4-ил}пропионовая кислота
Пример 38а
Метиловый эфир 3-(6-трет-бутоксикарбониламинопиридин-3-ил)-2-{1-[бис(4-(толуол-4-сульфонил)амино)фенил]-1Н-имидазол-4-ил}-пропионовой кислоты
Готовят раствор 115 мг (0,26 ммоль) метилового эфира 2-[1-(4-аминофенил)-1Н-имидазол-4-ил)-3-(6-трет-бутоксикарбониламино-пиридин-3-ил)пропионовой кислоты (получают согласно примеру 37b) в 20 мл СН3СN. Раствор охлаждают до температуры 0°С, затем добавляют 60 мг (0,32 ммоль) п-толуолсульфонилхлорида, 73 мкл (53 мг, 0,53 ммоль) триэтиламина и 0,3 мг (2,6 мкмоль) 4-диметиламинопиридина. Смесь нагревают до комнатной температуры и выдерживают в течение ночи. Путем колоночной хроматографии на силикагеле получают 112 мг указанного в заголовке соединения.
Rt (способ В) = 1,45 мин; МС (ES+) = 746 [M+H]+
Пример 38b
3-(6-Аминопиридин-3-ил)-2-{1-[4-(толуол-4-сульфониламино)-фенил]-1Н-имидазол-4-ил}пропионовая кислота
Раствор 109 мг (0,146 ммоль) соединения, полученного согласно примеру 38а, в 1 мл тетрагидрофурана смешивают с 190 мкл (0,190 ммоль) 1 н. водного раствора LiOH. Смесь нагревают до температуры 40°С и в течение 2 дней перемешивают при этой температуре. После нагревания при температуре 60°С в течение нескольких часов раствор охлаждают до комнатной температуры, нейтрализуют с помощью 1 н. HCl и тетрагидрофуран удаляют при пониженном давлении. Полученный водный раствор очищают путем препаративной ВЭЖХ и получают чистую 3-(6-трет-бутоксикарбониламинопиридин-3-ил)-2-{1-[4-(толуол-4-сульфониламино)фенил]-1Н-имидазол-4-ил}пропионовую кислоту. Соединение растворяют в 1 мл ТФУК и перемешивают при комнатной температуре. Спустя 30 минут ТФУК удаляют при пониженном давлении, остаток растворяют в воде и лиофилизируют. Получают 24 мг указанного в заголовке соединения в виде бистрифторацетата.
Rt (способ В) = 0,84 мин; МС (ES+) = 487 [M+H]+;
1Н-ЯМР (400 МГц, ДМСО-d6): δ = 1,22 (с, 3H); 3,02 (дд, 1H); 3,13 (дд, 1H); 3,92 (т, 1H); 6,87 (д, 1H); 7,21 (д, 2H); 7,88 (д, 2H); 7,53 (д, 2H); 7,62 (с, 1H); 7,68 (д, 2H); 7,72 (с, 1H); 7,77 (д, 1H); 7,88 (с, 2H, уш); 8,44 (с, 1H, уш).
Пример 39
3-(6-Аминопиридин-3-ил)-2-{1-[3-(3-пропилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота
Указанное в заголовке соединение получают аналогично указанному в примере 38. Только омыление промежуточного продукта - эфира карбоновой кислоты - осуществляют другим образом.
Метиловый эфир 3-(6-аминопиридин-3-ил)2-{1-[3-(3-пропилуреидо)бензил]-1Н-имидазол-4-ил}пропионовой кислоты (120 мг, 0,275 ммоль) растворяют в тетрагидрофуране. Добавляют водный раствор, содержащий LiOH, (1 н., 275 мкл) и водный раствор пероксида водорода (30%, 27 мкл). Раствор перемешивают в течение ночи при комнатной температуре и затем в течение 4 часов при температуре 50°С. Реакционный раствор нейтрализуют с помощью водного раствора HCl (1 н.) и затем растворитель удаляют. Остаток обрабатывают небольшим количеством метанола и фильтруют через С18-колонку (500 мг). Метанол удаляют и полученный продукт кристаллизуют из диэтилового эфира (100 мг, 0,237 ммоль).
Rt (способ С) = 0,93 мин; МС (ES+) = 423 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 0,85 (т, 3H), 1,42 (кв, 2H); 2,65 (м, 1H), 2,92 (м, 1H); 3,02 (м, 2H); 3,45 (м, 2H); 5,00 (с, 2H); 5,50 (с, 2H); 6,25 (д, 1H); 6,60 (д, 1H); 6,73 (с, 1H); 7,05 (д, 1H); 7,21 (т, 1H); 7,23 (с, 1H); 7,33 (д, 1H); 7,50 (м, 1H); 7,62 (с, 1H); 9,12 (с, 1H).
Пример 40
3-(6-Аминопиридин-3-ил)-2-{1-[3-(3-фенетилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота
Соединение получают аналогично указанному в примере 39.
Rt (способ В) = 0,86 мин; МС (ES+) = 485 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,72 (м, 2H); 2,85 (м, 1H), 2,95 (м, 1H); 3,25 (м, 2H); 3,50 (с, 2H); 4,95 (с, 1H); 5,05 (с, 1H); 5,45 (с, 1H); 5,55 (с, 1H); 6,28 (дд, 1H); 6,65 (т, 1H); 6,92 (с, 1H); 7,08-7,31 (м, 9H); 7,62 (м, 2H); 9,15 (с, 1H).
Пример 41
3-(6-Аминопиридин-3-ил)-2-{1-[3-(3-бензилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота
Соединение получают аналогично указанному в примере 39.
Rt (способ В) = 0,84 мин; МС (ES+) = 471 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,65 (м, 1H); 2,92 (м, 1H), 3,45 (м, 2H); 3,75 (м, 1H); 4,25 (д, 2H); 5,00 (с, 2H); 5,50 (с, 2H); 6,25 (м, 1H); 6,65 (м, 1H); 6,78 (с, 1H); 7,08-7,40 (м, 9H); 7,62 (м, 2H); 9,45 (с, 1H).
Пример 42
3-(6-Аминопиридин-3-ил)-2-{1-[3-(3-винилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота
Соединение получают аналогично указанному в примере 39.
Rt (способ В) = 0,60 мин; МС (ES+) = 407 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,68 (м, 1H); 2,92 (м, 1H), 3,45 (м, 2H); 3,82 (м, 1H); 4,18 (м, 2H); 5,00 (с, 2H); 5,50 (с, 2H); 6,25 (д, 1H); 6,62-6,77 (м, 3H); 7,09 (м, 1H); 7,25 (м, 2H); 7,45 (м, 1H); 7,62 (м, 2H).
Пример 43
3-(2-Аминотиазол-4-ил)-2-{1-[(бензгидрилкарбамоил)метил]-1Н-имидазол-4-ил}пропионовая кислота
Соединение получают аналогично указанному в примерах 37а-37b и 10b. Отщепление защитной группы осуществляют, как описано.
Rt (способ С) = 1,13 мин; МС (ES+) = 462 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,75 (м, 1H), 3,10 (м, 1H); 3,50 (с, 2H); 3,75 (м, 1H); 3,98 (д, 2H); 6,07 (с, 1H); 6,10 (д, 1H); 6,65 (с, 1H); 7,20-7,35 (м, 9H); 7,39 (с, 1H); 7,40 (т, 1H); 8,78 (д, 1H).
Пример 44
3-(2-Аминотиазол-4-ил)-2-[1-({[(4-хлорфенил)фенилметил]-карбамоил}метил)-1Н-имидазол-4-ил]пропионовая кислота
Соединение получают аналогично указанному в примерах 37а-37b и 10b. Отщепление защитной группы осуществляют, как описано.
Rt (способ С) = 1,26 мин; МС (ES+) = 496 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 2,78 (м, 1H), 3,10 (м, 1H); 3,50 (с, 2H); 3,75 (м, 1H); 3,95 (д, 2H); 6,08 (с, 1H); 6,11 (д, 1H); 6,65 (с, 1H); 7,20-7,41 (м, 9H); 7,60 (т, 1H); 8,85 (д, 1H).
Соединения согласно примерам 45 и 46 получают аналогично тому, как описывается выше.
Пример 45
3-(6-Аминопиридин-3-ил)-2-{1-[4-(3-трет-бутилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота в виде бистрифторацетата
Rt (способ В) = 0,75 мин; МС (ES+) = 423 [M+H]+;
1Н-ЯМР (400 МГц, ДМСО-d6): δ = 1,29 (с, 9H); 3,10 (дд, 1H); 3,28 (дд, 1H); 4,09 (т, 1H); 6,72 (д, 2H); 7,28 (д, 1H); 7,33 (д, 2H); 7,56 (д, 1H); 7,85 (с, 1H); 7,92 (с, 1H); 7,99 (с, 1H); 9,03 (с, 1H); 9,28 (с, 1H).
Пример 46
3-(6-Аминопиридин-3-ил)-2-{1-[4-(3-бензилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота в виде бистрифторацетата
Rt (способ В) = 0,81 мин; МС (ES+) = 457 [M+H]+;
1Н-ЯМР (400 МГц, ДМСО-d6): δ = 3,03 (дд, 1H); 3,18 (дд, 1H); 3,99 (т, 1H); 4,32 (д, 2H); 6,79 (т, 1H); 6,90 (д, 1H); 7,22 (м, 1H); 7,32 (м, 4H); 7,49 (д, 2H); 7,53 (д, 2H); 7,72 (с, 2H); 7,28 (д, 1H); 7,88 (с, 2H, уш); 8,71 (с, 1H, уш); 8,86 (с, 1H).
Пример 47
Этиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты
Указанное в заголовке соединение синтезируют в виде гидрохлорида аналогично указанному в примере 2.
Rt (способ С) = 0,87 мин; МС (ES+) = 343 [M+H]+;
1Н-ЯМР (500 МГц, ДМСО-d6): δ = 1,12 (т, 3H), 1,13-1,27 (м, 1H), 1,31-1,41 (м, 2H), 1,61-1,73 (м, 3H), 1,80-1,86 (м, 2H), 1,98-2,05 (м, 2H), 3,12 (дд, 1H), 3,18 (дд, 1H), 4,12 (м, 2H), 4,21-4,27 (м, 2H), 6,93 (д, 1H), 7,72-7,78 (м, 3H), 8,08 (с, 2H), 9,12 (с, 1H).
Фармакологические примеры
Полученные вещества тестировали на ингибирование TAFIa при использовании набора «Actichrome Plasma TAFI Activity», выпускаемого фирмой American Diagnostica (регистрационный номер 874). При этом к 1 мкл 5 мМ раствора вещества в диметилсульфоксиде добавляли 29 мкл буфера для теста (20 мМ Гепес, 150 мМ NaCl, рН 7,4) и 10 мкл TAFIa (American Diagnostica; регистрационный номер 874TAFIa; 2,5/мл) и в течение 15 минут инкубировали при комнатной температуре в 96-луночном титрационном микропланшете. Ферментативную реакцию инициировали путем добавки 10 мкл TAFIa «Developer» (предварительно при разведении водой в соотношении 1:2). За протеканием реакции во времени наблюдали в течение 15 минут при 420 нм, используя аппарат для прочтения титрационных микропланшетов (SpectraMax plus 384; фирма Molecular Devices).
Значения ИК50 (концентрация, вызывающая 50%-ное ингибирование) рассчитывали из средних значений (двойное определение) ряда разведения вещества с помощью программного обеспечения Graft 4 (Erithacus Software, UK).
Результаты представлены в таблице.
ИК50 [мM]
| название | год | авторы | номер документа |
|---|---|---|---|
| МАКРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ МОЧЕВИНЫ И СУЛЬФАМИДА В КАЧЕСТВЕ ИНГИБИТОРОВ TAFIa | 2009 |
|
RU2502736C2 |
| ЗАМЕЩЕННЫЕ ДИАМИНОКАРБОНОВЫЕ КИСЛОТЫ | 1998 |
|
RU2196768C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПУРИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1997 |
|
RU2228335C2 |
| ЗАМЕЩЕННЫЕ АЗОЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2047604C1 |
| НОВЫЕ ДИАМИДЫ ПИРИМИДИН-4,6-ДИКАРБОНОВОЙ КИСЛОТЫ ДЛЯ СЕЛЕКТИВНОГО ИНГИБИРОВАНИЯ КОЛЛАГЕНАЗ | 2003 |
|
RU2344129C2 |
| СПИРОЦИКЛИЧЕСКИЕ НИТРИЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕАЗЫ | 2012 |
|
RU2621695C2 |
| ЗАМЕЩЕННЫЕ БЕНЗИМИДАЗОЛЫ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2000 |
|
RU2261248C2 |
| ХИНОЛИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ЛЕКАРСТВЕННОГО СРЕДСТВА, ИНГИБИРУЮЩЕГО ТРАНСПОРТЕР УРАТОВ | 2016 |
|
RU2715229C2 |
| СПИРОЦИКЛИЧЕСКИЕ НИТРИЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕАЗЫ | 2007 |
|
RU2478620C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ IkB-КИНАЗЫ ПРИ ОБЕЗБОЛИВАЮЩЕМ ЛЕЧЕНИИ | 2003 |
|
RU2320338C2 |
Изобретение относится к производным имидазола формулы (Ia):
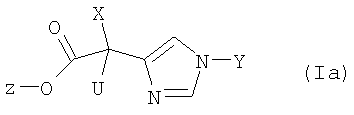
и/или к стереоизомерным формам соединения формулы (Ia), и/или к физиологически приемлемой соли соединения формулы (Ia), причем U означает 1) атом водорода; Х означает остаток формулы (II): -(А1)m-А2(II), где m означает целое число 1; А1 означает 1) -(CH2)n-, где n означает целое число 1; А2 означает 1) аминопиридил; Y означает 1) остаток формулы (III): А3-(А4)о-(А5)р (III), причем а) A3 означает
(С3-С8)-циклоалкил или (С2-С6)-алкинилен, где циклоалкил или алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, А4 отсутствует, А5 отсутствует; b) A3 означает -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, А4 означает -N(R2)- и А5 означает а) 1) -C(O)-R3; a) 2) -C(O)-N(R4)-R5; a) 3) -(SO2)-R6; о означает целое число 1 и p означает целое число 1; с) A3 означает циклический амин с 3-8 атомами в цикле, где циклический амин незамещен, А4 отсутствует; и А5 имеет указанное в п.b) значение, причем А5 связан с N-атомом A3, о означает целое число ноль и p означает целое число ноль или 1; или d) A3 означает -(CH2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, А4 отсутствует; и А5 имеет указанное в п.b) значение, p означает целое число 1 и q означает целое число ноль или 1; е) A3 означает -(CH2)r-Het, где Het означает бензотиофен или пиперидин, который незамещен или, независимо друг от друга, одно, двух- или трехкратно замещен с помощью =O или R1, А4 отсутствует; и А5 имеет указанное в п.b) значение, p означает целое число 1 и r означает целое число 1 или 2; f) A3 означает - (CH2)q-фенил, где фенил незамещен, А4 означает -O-, А5 означает -фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, о и p означают целое число 1 и q означает целое число ноль, 1; g) -CH(-фенил)-фенил; причем R1 означает а) фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С6)-алкилом, b) триазолил, с) -(С1-С6)-алкил, d) -(С0-С4)-алкил-(С3-С8)-циклоалкил, е) -О-CF3 или g) галоген; причем R2 означает: а) атом водорода; причем R3 и R6 являются одинаковыми или разными и, независимо друг от друга, означают: а) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, b) -фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают: а) -(С1-С6)-алкил или -(С2-С10)-алкенил, где алкил или алкенил незамещен, b) -фенил, где фенил незамещен, с) атом водорода; Y означает 2) остаток формулы (IV): 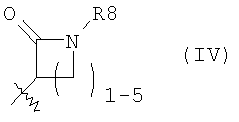 причем R8 означает а) -фенил, где фенил незамещен; Z означает 1) атом водорода, 2) -(С1-С6)-алкил, 3) -(С1-С6)-алкил-ОН, 4) -(С0-С4)-алкил-(С3-С6)-циклоалкил, 5) -(С1-С10)-алкил-O-С(O)-O-R1. Изобретение также относится к способу получения соединения формулы (Ia) и к лекарственному средству для ингибирования фермента TAFIa на его основе. Технический результат - получение новых соединений и лекарственного средства на их основе для использования в медицине в целях профилактики и лечения заболеваний, протекающих с тромбозами, эмболиями, гиперкоагулируемостью или фибротическими изменениями. 3 н. и 5 з.п. ф-лы, 1 табл.
причем R8 означает а) -фенил, где фенил незамещен; Z означает 1) атом водорода, 2) -(С1-С6)-алкил, 3) -(С1-С6)-алкил-ОН, 4) -(С0-С4)-алкил-(С3-С6)-циклоалкил, 5) -(С1-С10)-алкил-O-С(O)-O-R1. Изобретение также относится к способу получения соединения формулы (Ia) и к лекарственному средству для ингибирования фермента TAFIa на его основе. Технический результат - получение новых соединений и лекарственного средства на их основе для использования в медицине в целях профилактики и лечения заболеваний, протекающих с тромбозами, эмболиями, гиперкоагулируемостью или фибротическими изменениями. 3 н. и 5 з.п. ф-лы, 1 табл.
1. Производное имидазола формулы (Ia):
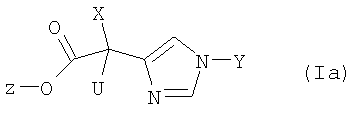
и/или стереоизомерные формы соединения формулы (Ia) и/или физиологически приемлемая соль соединения формулы (Ia), причем
U означает 1) атом водорода;
Х означает остаток формулы (II):
 ,
,
где m означает целое число 1;
А1 означает 1) -(СН2)n-, где n означает целое число 1;
А2 означает
1) аминопиридил;
Y означает 1) остаток формулы (III);
 ,
,
причем
a) A3 означает (С3-С8)-циклоалкил или (С2-С6)-алкинилен, где циклоалкил или алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует,
А5 отсутствует;
b) A3 означает -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -N(R2)- и
А5 означает а) 1) -C(O)-R3; a) 2) -C(O)-N(R4)-R5; a) 3) -(SO2)-R6;
о означает целое число 1 и
p означает целое число 1;
c) A3 означает циклический амин с 3-8 атомами в цикле, где циклический амин незамещен,
А4 отсутствует; и А5 имеет указанное в п.b) значение, причем
А5 связан с N-атомом A3,
о означает целое число ноль и
p означает целое число ноль или 1; или
d) A3 означает -(CH2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует; и А5 имеет указанное в п.b) значение,
p означает целое число 1 и
q означает целое число ноль или 1;
e) A3 означает -(CH2)r-Het, где Het означает бензотиофен или пиперидин, который незамещен или, независимо друг от друга, одно, двух- или трехкратно замещен с помощью =O или R1,
А4 отсутствует; и А5 имеет указанное в п.b) значение,
p означает целое число 1 и
r означает целое число 1 или 2;
f) A3 означает -(CH2)q-фенил, где фенил незамещен,
А4 означает -O-,
А5 означает -фенил, где фенил незамещен или, независимо друг от друга, одно-, двух или трехкратно замещен с помощью R1,
o и p означают целое число 1 и
q означает целое число ноль, 1;
g) -СН(-фенил)-фенил;
причем R1 означает
a) фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С6)-алкилом,
b) триазолил,
c) -(С1-С6)-алкил,
d) -(С0-С4)-алкил-(С3-С8)-циклоалкил,
e) -O-CF3 или
g) галоген;
причем R2 означает:
а) атом водорода;
причем R3 и R6 являются одинаковыми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил или -(С2-С10)-алкенил, где алкил или алкенил незамещен,
b) -фенил, где фенил незамещен,
c) атом водорода;
Y означает 2) остаток формулы (IV):
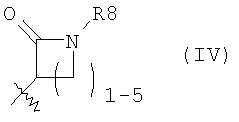
причем R8 означает
а) -фенил, где фенил незамещен;
Z означает
1) атом водорода,
2) -(С1-С6)-алкил,
3) -(С1-С6)-алкил-OH,
4) -(С0-С4)-алкил-(С3-С6)-циклоалкил,
5) -(С1-С10)-алкил-O-С(O)-O-R1.
2. Соединение по п.1 формулы (Ia), где
U означает 1) атом водорода;
Х означает остаток формулы (II):
 ,
,
где m означает целое число 1;
А1 означает 1) -(СН2)n-, где n означает целое число 1;
А2 означает
1) аминопиридил;
Y означает 1) остаток формулы (III):
 ,
,
причем
a) A3 означает (С3-С8)-циклоалкил или (С2-С6)-алкинилен, где циклоалкил или алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует,
А5 отсутствует;
b) A3 означает -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -N(R2)- и
А5 означает а) 1) -C(O)-R3; a) 2) -C(O)-N(R4)-R5; a) 3) -(SO2)-R6;
о означает целое число 1 и
p означает целое число 1;
c) A3 означает циклический амин с 3-8 атомами в цикле, где циклический амин незамещен,
А4 отсутствует; и А5 имеет указанное в п.b) значение, причем
А5 связан с N-атомом A3,
p означает целое число ноль или 1; или
d) A3 означает -(СН2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует; и А5 имеет указанное в п.b) значение,
p означает целое число 1 и q означает целое число ноль или 1;
e) A3 означает -(CH2)r-Het, где Het означает бензотиофен или пиперидин, который незамещен или, независимо друг от друга, одно, двух- или трехкратно замещен с помощью =O или R1,
А4 отсутствует; и А5 имеет указанное в п.b) значение,
p означает целое число 1 и
r означает целое число 1 или 2;
f) A3 означает -(СH2)q-фенил, где фенил незамещен,
А4 означает -O-,
А5 означает -фенил, где фенил незамещен или, независимо друг от друга, одно-, двух или трехкратно замещен с помощью R1,
о и p означают целое число 1 и
q означает целое число ноль, 1;
g) -СН(-фенил)-фенил;
причем R1 означает
a) -фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С6)-алкилом,
b) триазолил,
c) -(С1-С6)-алкил,
d) -(С0-С4)-алкил-(С3-С8)-циклоалкил,
e) -O-CF3 или
g) галоген;
причем R2 означает:
а) атом водорода;
причем R3 и R6 являются одинаковыми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил или -(С2-С10)-алкенил, где алкил или алкенил незамещен,
b) -фенил, где фенил незамещен,
c) атом водорода;
Y означает 2) остаток формулы (IV), причем формуле (IV) отвечает соединение из группы, состоящей из азетидин-2-она, пирролидин-2-она, пиперидин-2-она, азепан-2-она и азокан-2-она, и у атома азота, соответственно, замещено с помощью R8, причем R8 означает а) -фенил, где фенил незамещен;
Z означает
1) атом водорода,
2) -(С1-С6)-алкил,
3) -(С3-С6)-циклоалкил,
4) -(С1-С10)-алкил-O-С(O)-O-Р1.
3. Соединение по п.1 или 2 формулы (Ia), где
U означает 1) атом водорода;
X означает остаток формулы (II):
 ,
,
где m означает целое число 1;
А1 означает 1) -(СН2)n-, где n означает целое число 1;
А2 означает
1)аминопиридил;
Y означает 1) остаток формулы (III):
 ,
,
причем
a) A3 означает (С3-С8)-циклоалкил или (С2-С6)-алкинилен, где циклоалкил или алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует,
А5 отсутствует;
b) A3 означает -(С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 означает -N(R2)- и
А5 означает а) 1) -C(O)-R3; a) 2) -C(O)-N(R4)-R5; a) 3) -(SO2)-R6;
о означает целое число 1 и
p означает целое число 1;
c) A3 означает циклический амин с 3-8 атомами в цикле, где циклический амин незамещен,
А4 отсутствует и А5 имеет указанное в п.b) значение, причем
А5 связан с N-атомом A3,
о означает целое число ноль и
p означает целое число ноль или 1; или
d) A3 означает -(CH2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует; и А5 имеет указанное в п.b) значение,
p означает целое число 1 и
q означает целое число ноль или 1;
e) A3 означает -(CH2)r-Het, где Het означает бензотиофен или пиперидин, который незамещен или, независимо друг от друга, одно, двух- или трехкратно замещен с помощью =O или R1,
А4 отсутствует; и А5 имеет указанное в п.b) значение,
p означает целое число 1 и
r означает целое число 1 или 2;
f) A3 означает -(CH2)q-фенил, где фенил незамещен,
А4 означает -O-,
А5 означает -фенил, где фенил незамещен или, независимо друг от друга, одно-, двух или трехкратно замещен с помощью R1,
о и p означают целое число 1 и
q означает целое число ноль, 1;
причем R1 означает
a) -фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С6)-алкилом,
b) триазолил,
c) -(С1-С6)-алкил,
d) -(С0-С4)-алкил-(С3-С8)-циклоалкил,
e) -O-CF3 или
f) галоген;
причем R2 означает:
а) атом водорода;
причем R3 и R6 являются одинаковьми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) -фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил или -(С2-С10)-алкенил, где алкил или алкенил незамещен,
b) -фенил, где фенил незамещен,
c) атом водорода;
Y означает 2) остаток формулы (IV), выбираемы из группы, состоящей из азетидин-2-она, пирролидин-2-она или пиперидин-2-она, причем остаток может быть замещен у атома азота с помощью R8,
причем R8 означает
а) -фенил, где фенил незамещен; и
Z означает атом водорода или -(С1-С6)-алкил.
4. Соединение по п.1 или 2 формулы (Ia), причем
U означает атом водорода;
Х означает остаток формулы (II),
где m означает целое число 1;
А1 означает -СН2-;
А2 означает аминопиридил;
Y означает 1) остаток формулы (III), причем
a) A3 означает (С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, и
А4 и А5 отсутствуют;
b) A3 означает -(С2-С4)-алкинилен, где алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, и
А4 и А5 отсутствуют;
c) A3 означает циклический амин с 3-8 атомами в цикле, где циклический амин незамещен, и
А4 и А5 отсутствуют;
d) A3 означает -(СН2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 отсутствует; А5 означает а) 1) -C(O)-R3; a) 2) -C(O)-N(R4)-R5; a) 3) -(SO2)-R6;
p означает целое число 1 и
q означает целое число ноль, 1;
e) A3 означает -(CH2)r-Het, где Het означает пиперидин, который незамещен или, независимо друг от друга, одно, двух- или трехкратно замещен с помощью R1,
А4 отсутствует и А5 имеет указанное в п.d) значение, причем А5 связан с атомом азота A3,
p означает целое число 1 и
r означает целое число 1 или 2;
f) A3 означает -CH2-фенил, причем фенил незамещен,
А4 означает -O-,
А5 означает фенил, причем фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
причем R1 означает
a) фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С4)-алкилом,
b) триазолил,
c) -(С1-С4)-алкил,
d) -(С3-С6)-циклоалкил,
e) -О-CF3,
f) фтор или
g) хлор;
причем R2 означает атом водорода;
причем R3 и R6 являются одинаковыми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил или -(С2-С6)-алкенил, где алкил или алкенил незамещен,
b) фенил, где фенил незамещен,
c) атом водорода;
Y означает 2) остаток пирролидин-2-она, причем остаток замещен у атома азота, соответственно, с помощью R8,
причем R8 означает
а) фенил, где фенил незамещен; и
Z означает
1) атом водорода,
2) -(С1-С6)-алкил,
3) -(С1-С6)-алкил-OH,
4)-(С0-С4)-алкил-(С3-С6)-циклоалкил,
5) -(С1-С10)-алкил-O-С(O)-O-(С3-С6)-циклоалкил.
5. Соединение по п.1 формулы (Ia),
где U означает атом водорода;
Х означает остаток формулы (II),
где m означает целое число 1;
А1 означает -СН2-;
А2 означает остаток 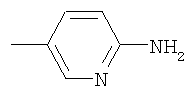 , который незамещен;
, который незамещен;
Y означает 1) остаток формулы (III), причем
a) A3 означает (С3-С8)-циклоалкил, где циклоалкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, и А4 и А5 отсутствуют;
b) A3 означает -(С2-С4)-алкинилен, где алкинилен незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
А4 и А5 отсутствуют;
c) A3 означает циклический амин с 3-6 атомами в цикле, где циклический амин незамещен,
А4 и А5 отсутствуют;
d) A3 означает -(СН2)q-фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1, А4 отсутствует;
А5 означает а) 1) -C(O)-R3; a) 2) -C(O)-N(R4)-R5; a) 3) -(SO2)-R6;
p означает целое число 1 и
q означает целое число ноль, 1;
e) A3 означает -(CH2)r-Het, где Het означает пиперидин, который незамещен или, независимо друг от друга, одно, двух- или трехкратно замещен с помощью R1,
А4 отсутствует и А5 имеет указанное в n.d) значение, причем А5 соединен с атомом азота A3,
p означает целое число 1 и
r означает целое число 1 или 2;
f) A3 означает -СН2-фенил, причем фенил незамещен,
А4 означает -O-,
А5 означает фенил, причем фенил незамещен или, независимо друг от друга, одно-, двух или трехкратно замещен с помощью R1;
причем R1 означает
a) фенил, причем фенил незамещен или одно-, двух- или трехкратно, независимо друг от друга, замещен -(С1-С4)-алкилом,
b) -(С1-С4)-алкил,
c) -(С3-С6)-циклоалкил,
d) -О-CF3,
e) фтор или
f) хлор;
причем R2 означает атом водорода;
причем R3, R6 являются одинаковыми или разными и, независимо друг от друга, означают
a) -(С1-С6)-алкил, где алкил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1,
b) фенил, где фенил незамещен или, независимо друг от друга, одно-, двух- или трехкратно замещен с помощью R1;
причем R4 и R5 являются одинаковыми или разными и, независимо друг от друга, означают:
a) -(С1-С6)-алкил или -(С2-С6)-алкенил, где алкил или -(С2-С6)-алкенил незамещен,
b) фенил, где фенил незамещен,
c) атом водорода;
Y означает 2) остаток пирролидин-2-она, причем остаток у атома азота, соответственно, замещен с помощью R8,
причем R8 означает фенил, где фенил незамещен; и
Z означает атом водорода.
6. Соединение по п.1 формулы (Ia), отличающееся тем, что оно представляет собой соединение:
3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовая кислота;
метиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты;
изопропиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты;
циклопропилметиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1 Н-имидазол-4-ил)пропионовой кислоты;
2-гидроксиэтиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты;
1-циклогексилоксикарбонилоксиэтиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)-пропионовой кислоты;
3-(6-аминопиридин-3-ил)-2-(1-циклопентил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-пиперидин-4-ил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(2-оксо-1-фенилпирролидин-3-ил)-1 Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[(бензгидрилкарбамоил)метил]-1Н-имидазол-4-ил}пропионовая кислота;
изопропиловый эфир 3-(6-аминопиридин-3-ил)-2-{1-[(бензгидрилкарбамоил)метил]-1Н-имидазол-4-ил}пропионовой кислоты;
3-(6-аминопиридин-3-ил)-2-{1-[4-(3-фенилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[2-(1-дифенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[2-(1-бензоилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(1-бензоилпиперидин-2-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-{2-[1-(3-фенилпропионил)-пиперидин-3-ил]этил}-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(1-дифенилацетилпиперидин-3-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-{2-[1-(3-фенилпропионил)-пиперидин-4-ил]этил}-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[2-(1-фенилацетилпиперидин-3-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[2-(1-фенилацетилпиперидин-4-ил)этил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[1-(4'-метилбифенил-3-карбонил)пиперидин-4-илметил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(1-бензоилпиперидин-4-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-бензгидрил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(4-[1,2,4]триазол-1-илбензил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(4-трифторметоксибензил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(1,1-диоксо-1Н-1,6-бензо-[b]тиофен-2-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(5-хлорбензо[b]тиофен-3-илметил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(4-фторфенокси)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(2-феноксибензил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(4-феноксибензил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-проп-2-инил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-(1-бут-2-инил-1Н-имидазол-4-ил)пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-(4,4-диметилциклогексил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[(бензгидрилметилкарбамоил)-метил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-({[(4-хлорфенил)фенилметил]-карбамоил}метил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-[1-({[бис(4-метоксифенил)метил]-карбамоил}метил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[4-(3-пропилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[4-(толуол-4-сульфониламино)-фенил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(3-пропилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(3-фенетилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(3-бензилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[3-(3-винилуреидо)бензил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(2-аминотиазол-4-ил)-2-{1-[(бензгидрилкарбамоил)метил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(2-аминотиазол-4-ил)-2-[1-({[(4-хлорфенил)фенилметил]-карбамоил} метил)-1Н-имидазол-4-ил]пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[4-(3-трет-бутилуреидо)-фенил]-1Н-имидазол-4-ил}пропионовая кислота;
3-(6-аминопиридин-3-ил)-2-{1-[4-(3-бензилуреидо)фенил]-1Н-имидазол-4-ил}пропионовая кислота; или
этиловый эфир 3-(6-аминопиридин-3-ил)-2-(1-циклогексил-1Н-имидазол-4-ил)пропионовой кислоты.
7. Способ получения соединения формулы (Ia) по одному или нескольким из пп.1-6, включающий стадии
а1) введения известным способом подходящей защитной группы PG2, такой как трет-бутоксикарбонил, бензилоксикарбонил, фталоил, тритил, или тозил, в соединение формулы (VII):
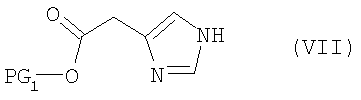
где PG1 означает карбоксилзащитную группу,
с образованием соединения формулы (VIII)
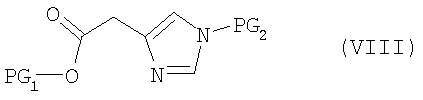
а2) взаимодействия полученного соединения формулы (VIII) с соединением формулы (XIII)
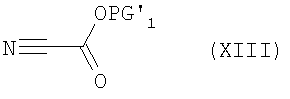
с образованием соединения формулы (IX)
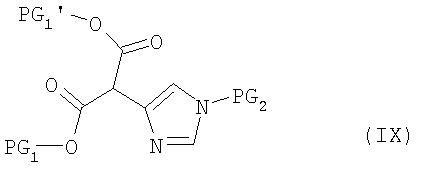
где PG1' означает карбоксилзащитную группу;
а3) взаимодействия полученного соединения формулы (IX) с соединением формулы X-LG (XIV) с образованием соединения формулы (X)
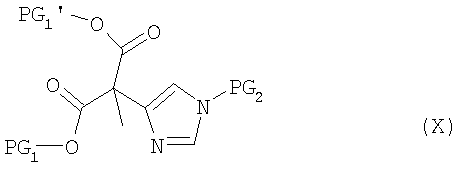
где Х определен в п.1, причем содержащиеся в (X) функциональные группы могут быть защищены пригодными защитными группами и LG означает пригодную активирующую группу, как, например, хлор, бром, иод, мезилат, тозилат или трифталат;
а4) превращения полученного соединения формулы (X) в соединение формулы (XI) путем удаления известным способом защитных групп PG1, PG1' и PG2 и, в случае необходимости, защитной группы, присутствующей в Х
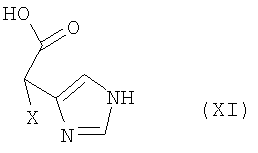
а5) введения подходящей карбоксилзащитной группы PG1'' в подходящих условиях в соединение формулы (XI) с образованием соединения формулы (XII)
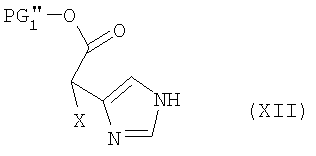
а6) с последующим превращением соединения формулы (XII) в соединение формулы (Ia)
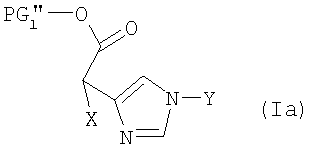
путем взаимодействия:
(а6.1) с соединением формулы Y-LG (XV), где LG представляет собой подходящую
активирующую группу, значения которой указаны выше и Y определен в п.1; или
(а6.2) с соединением формулы Y-OH (XVI) в условиях реакции Мицонобу, где Y
определен в п.1; или
(а6.3) с 6-членным 2-фтор- или 4-фторнитроароматическим соединением
с последующим восстановлением нитрогруппы до аминогруппы стандартным способом;
а7) и удалением защитной группы PG1'' в подходящих условиях с образованием соединения формулы (Ib),
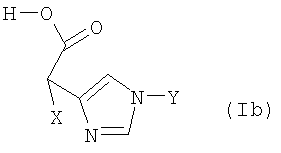
и, в случае необходимости, удалением защитной группы, присутствующей в X, и превращением соединения (Ib) в целевое соединение формулы (Ia);
b) в случае необходимости разделения полученного соединения формулы (Ia), которое на основании своей химической структуры образуется в энантиомерных формах, на чистые энантиомеры путем хроматографии при использовании хиральных неподвижных фаз; или
c) полученное по способу а) или b) соединение формулы (Ia) либо выделяют в свободной форме, либо, в случае наличия кислотных или основных групп, превращают в физиологически приемлемые соли.
8. Лекарственное средство для ингибирования фермента TAFIa, содержащее эффективное количество по меньшей мере одного соединения формулы (Ia) по одному или нескольким из пп.1-6 вместе с фармацевтически пригодным и физиологически приемлемым носителем, добавкой и/или другими вспомогательными веществами.
| WO 03013526 A1, 20.02.2003 | |||
| BARROW et al, J | |||
| MED | |||
| CHEM., v.46, 2003, p.5294-5297 | |||
| RU 2001120723 A, 27.06.2003. |
Авторы
Даты
2009-12-10—Публикация
2005-04-07—Подача