Настоящее изобретение относится к новым соединениям и их фармацевтически приемлемым солям, которые ингибируют основные карбоксипептидазы, в частности карбоксипептидазу U, и соответственно их можно применять в профилактике и лечении болезней, где ингибирование карбоксипептидазы U является полезным, таких как тромбоз и гиперкоагуляция в крови и ткани, атеросклероз, спайки, кожные рубцы, рак, фиброзные состояния, воспалительные заболевания, и таких состояний, при которых полезно поддерживание или увеличение уровней брадикинина в организме млекопитающих, таких как человек. В дополнительных аспектах данное изобретение относится к соединениям по изобретению для применения в терапии; к способам получения таких новых соединений; к фармацевтическим композициям, содержащим по меньшей мере одно соединение по изобретению или его фармацевтически приемлемую соль в качестве активного ингредиента, и к применению активных соединений в изготовлении лекарств для медицинского применения, указанного выше.
Фибринолиз является результатом ряда ферментативных реакций, приводящих к разрушению фибрина плазмином. Активация плазминогена является центральным процессом фибринолиза. Расщепление плазминогена с образованием плазмина осуществляется с участием активаторов плазминогена, активатора плазминогена тканевого типа (t-PA) или активатора плазминогена урокиназного типа (u-PA). В результате первоначального разрушения фибрина плазмином образуются карбокси-концевые остатки лизина, которые служат обладающими высоким сродством сайтами связывания плазминогена. Так как плазминоген, связанный с фибрином, значительно легче активируется в плазмин, чем свободный плазминоген, этот механизм обеспечивает регулирование фибринолиза по типу положительной обратной связи.
Одним из эндогенных ингибиторов фибринолиза является карбоксипептидаза U (CPU). CPU также известна как карбоксипептидаза В плазмы, активный тромбин-активируемый ингибитор фибринолиза (TAFIa), карбоксипептидаза R и индуцируемая карбоксипептидазная активность. CPU образуется во время коагуляции и фибринолиза из своего предшественника proCPU под действием протеолитических ферментов, таких как тромбин, комплекс тромбин-тромбомодулин или плазмин. CPU отщепляет основные аминокислоты на карбоксильном конце фибриновых фрагментов. Потеря карбокси-концевых лизинов и, следовательно, лизиновых сайтов связывания плазминогена затем способствует ингибированию фибринолиза. Предполагается, что эффективные ингибиторы карбоксипептидазы U, ингибируя потерю лизиновых сайтов связывания плазминогена и, таким образом, увеличивая скорость образования плазмина, облегчают фибринолиз.
В качестве ингибитора карбоксипептидазы N упоминается 2-меркаптометил-3-гуанидиноэтилтиопропионовая кислота. Недавно было показано, что это соединение ингибирует CPU (Hendriks, D. et al., Biochimica et Biophysica Acta, 1034 (1990), 86-92).
В качестве ингибитора карбоксипептидазы N упоминается гуанидиноэтилмеркаптоянтарная кислота. Недавно было показано, что это соединение ингибирует CPU (Eaton, D. L, et al., The Journal of Biological Chemistry, 266 (1991), 21833-21838).
Ингибиторы CPU раскрыты в WO 00/66550, WO 00/66557, WO 03/013526 и WO 03/027128, и фармацевтический препарат, содержащий ингибитор CPU и ингибитор тромбина раскрыт в WO 00/66152. Ингибиторы карбоксипептидазы В плазмы раскрыты в WO 01/19836. Ингибиторы TAFIa раскрыты в WO 02/14285.
В настоящее время установлено, что соединения формулы (I) особенно эффективны в качестве ингибиторов карбоксипептидазы U и, следовательно, полезны в качестве лекарственных средств для лечения или профилактики состояний, где ингибирование карбоксипептидазы U является полезным.
Таким образом, в настоящем изобретении предложено соединение формулы (I)
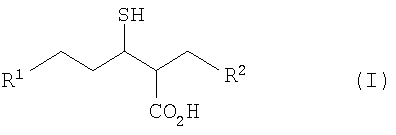
где R1 представляет собой фенил {возможно замещенный галогеном, гидрокси, циано,
C1-4алкилом (который возможно монозамещен циано, гидрокси или фенилом), C1-4алкокси (который возможно замещен тетрагидрофуранилом), CF3, OCF3, метилендиокси, C(O)R3, S(O)2R4, фенилом (который возможно замещен галогеном), фенокси (который возможно замещен галогеном) или тетрагидрофуранилокси}, нафтил, пиридинил, 1,2,3,4,-тетрагидропиримидин-2,4-дионил (возможно замещенный С1-4алкилом) или тетрагидротиенил;
R2 представляет собой аминопиридинил, аминотиазолил или 3-азабицикло[3.2.1]октил;
R3 представляет собой гидрокси, С1-4алкокси (который возможно замещен фенилом (возможно замещенным галогеном) или пиридинилом), NR5R6 или N-связанное 5- или 6-членное гетероциклическое кольцо {незамещенное или монозамещенное гидрокси, оксо, С1-4алкилом (который возможно замещен гидрокси или NHфенилом), группой CO2(C1-4алкил) или фенилом (который возможно замещен галогеном)};
R4 представляет собой NR7RS или N-связанное 5- или 6-членное гетероциклическое кольцо {незамещенное; монозамещенное гидрокси, оксо, С1-4алкилом (который возможно замещен гидрокси или NHфенилом), группой CO2(C1-4алкил) или фенилом (который возможно замещен галогеном), или конденсированное с бензольным кольцом, которое возможно замещено C1-4алкокси};
R5, R6, R7 и R8 независимо представляют собой водород, C1-4алкил {возможно замещенный галогеном, циано, гидрокси, фенилом (который возможно замещен галогеном или метилендиокси), пиридинилом, CO2H или группой CO2(C1-4алкил)} или C2-4алкенил;
при условии, что когда R1 представляет собой 6-аминопиридин-3-ил, тогда R2 представляет собой замещенный фенил, нафтил, пиридинил, 1, 2, 3, 4 - тетрагидропиримидин-2,4-дионил (возможно замещенный С1-4алкилом) или тетрагидротиенил,
или его фармацевтически приемлемая соль или сольват, или сольват такой соли.
Соединения формулы (I) существуют в изомерных формах, и настоящее изобретение охватывает все такие формы и их смеси во всех соотношениях. В объем настоящего изобретения также входят оба чистых энантиомера, рацемические смеси и смеси двух энантиомеров в равных или неравных соотношениях. Очевидно, что все возможные диастереомерные формы также входят в объем данного изобретения.
Термин C1-4алкил означает прямую или разветвленную алкильную группу, имеющую от 1 до 4 атомов углерода в цепи. Примеры алкила включают метил, этил, н-пропил, изо-пропил, н-бутил, изо-бутил, втор-бутил и трет-бутил.
Термин С1-4алкокси означает алкил-O-группу, где алкил имеет прямую или разветвленную цепь, и примеры включают метокси и этокси.
Галоген включает фторо, хлоро, бромо и йодо (но предстваляет собой, например, фторо или хлоро).
N-Связанным 5- или 6-членным гетероциклическим кольцом является, например, пирролидинильное, пиперидинильное или пиперазинильное кольцо.
В одном конкретном аспекте настоящего изобретения предложено соединение формулы (I), где R1 представляет собой фенил {возможно замещенный галогеном, гидрокси, циано, С1-4алкилом (который возможно монозамещен циано или гидрокси), С1-4алкокси, CF3, OCF3, метилендиокси, C(O)NH2, S(O)2NH2 или фенилом (который возможно замещен галогеном)}, пиридинил или тетрагидротиенил; R2 представляет собой аминопиридинил, аминотиазолил или 3-азабицикло[3.2.1]октил; при условии, что когда R2 представляет собой 6-аминопиридин-3-ил, тогда R1 представляет собой замещенный фенил, пиридинил или тетрагидротиенил, или его фармацевтически приемлемая соль или сольват, или сольват такой соли.
В другом аспекте данного изобретения предложено соединение формулы (I), где R1 представляет собой фенил {возможно замещенный (например, имеющий 1 или 2 заместителя) галогеном, гидрокси, циано, С1-4алкилом (который возможно монозамещен циано, гидрокси или фенилом), C1-4алкокси, CF3, OCF3, метилендиокси, фенокси (который возможно замещен галогеном), тетрагидрофуранилокси или тетрагидрофуранилметокси}, нафтил, пиридинил или тетрагидротиенил.
В еще одном аспекте настоящего изобретения предложено соединение формулы (I), где R1 представляет собой фенил {замещенный (например, монозамещенный) галогеном, гидрокси, циано, С1-4алкилом (который возможно монозамещен циано или гидрокси), С1-4алкокси (например, метокси), CF3 или метилендиокси} или тетрагидротиенил.
В еще одном аспекте настоящего изобретения предложено соединение формулы (I), где R1 представляет собой фенил {монозамещенный галогеном (например, хлоро или фторо), гидрокси, циано, C1-4алкилом (монозамещенным циано), CF3 или метилендиокси} или тетрагидротиенил.
Аминопиридинил представляет собой, например, 6-аминопиридин-3-ил. Аминотиазол представляет собой, например, 2-аминотиазол-5-ил. 3-Азабицикло[3.2.1]октил представляет собой, например, 3-азабицикло[3.2.1]окт-8-ил.
В дополнительном аспекте настоящего изобретения предложено соединение формулы (I), где R2 представляет собой аминопиридин (например, 6-аминопиридин-3-ил).
Соединения по настоящему изобретению могут быть получены путем адаптации способов, описанных в литературе (например, в WO 00/66557), или путем использования или адаптации способов Примеров 1, 26 или 51, приведенных ниже. Следует принимать во внимание, что при адаптации способов, описанных в литературе или в Примерах 1, 26 или 51, может требоваться защита функциональных групп промежуточных соединений защитными группами. Способы получения некоторых промежуточных соединений показаны на Схемах 1 и 2.
Например, соединение формулы (I) может быть получено путем взаимодействия соединения формулы (II)
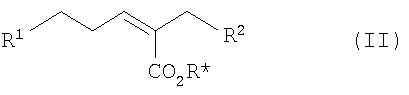
где R1 такой, как определено выше, или включает группу, которая затем может подвергнуться реакции с образованием группы R1, R* представляет собой подходящую защитную группу (такую как C1-6алкильная группа (например, трет-бутил)) и R2 является таким, как определено выше, или аминная функциональная группа R2 может быть защищена (например, трет-бутоксикарбонильной группой), с тиолом формулы L-SH, где L является подходящей защитной группой (например, 4-метоксибензильной), в присутствии подходящего катализатора (например гидрида натрия) и в подходящем растворителе (например, N,N-диметилформамиде) с образованием соединения формулы (III)
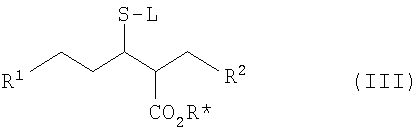
и, возможно, взаимодействия функциональной группы в R1 (например, R1 может включать в себя кислотную группу, которая может подвергаться реакции сочетания с аминной функциональной группой с образованием амида в присутствии катализатора (такого как HATU)), и последующего удаления защитных групп, если это необходимо.
Функциональные группы, которые желательно защитить, включают гидрокси, карбоксилатную и аминогруппы. Подходящие защитные группы гидроксигруппы включают триалкилсилил или диарилалкилсилил (например, трет-бутилдиметилсил ил, трет-бутилдифенилсилил или триметилсилил), тетрагидропиранил, метоксиметил, бензилоксиметил и 4-метоксибензил. Подходящие защитные группы карбоксилата включают этиловые, трет-бутиловые и бензиловые сложные эфиры. Подходящие защитные группы амино включают трет-бутилоксикарбонил, 2,4,6-триметоксибензил и бензилоксикарбонил. Применение защитных групп описано в "Protective Groups in Organic Synthesis", third edition, T.W.Greene & P.G.M. Wutz, Wiley-lnterscience (1999). Защитной группой также может быть полимерная смола, такая как смола Ванга (Wang) или 2-хлортритилхлоридная смола.
Соединения по изобретению являются ингибиторами карбоксипептидазы U, и соответветственно предполагается, что они полезны в тех состояниях, где ингибирование карбоксипептидазы U является полезным, например, в лечении или профилактике тромбоза и гиперкоагуляции в крови и тканях, атеросклероза, спаек, кожных рубцов, рака, фиброзных состояний, воспалительных заболеваний и таких состояний, при которых полезно поддерживание или увеличение уровней брадикинина в организме млекопитающих, таких как человек.
В дополнительном аспекте изобретения соединение формулы (I) или его фармацевтически приемлемую соль или сольват, или сольват такой соли применяют в лечении или профилактике тромбоза. В другом аспекте данного изобретения соединение формулы (I) или его фармацевтически приемлемую соль или сольват, или сольват такой соли применяют в способе изготовления лекарства для лечения или профилактики тромбоза.
Известно, что гиперкоагуляция может приводить к тромбоэмболическим заболеваниям. Состояния, связанные с гиперкоагуляцией и тромбоэмболическими заболеваниями, которые могут быть упомянуты, включают резистентность к протеину С и врожденную или приобретенную недостаточность антитромбина III, протеина С, протеина S и кофактора гепарина II. Другие состояния, про которые известно, что они связаны с гиперкоагуляцией и тромбоэмболическими болезнями, включают циркуляторный и септический шок, циркуляцию антифосфолипидных антител, гипергомоцистеинемию, гепарин-индуцированную тромбоцитопению и нарушения фибринолиза. Соответственно, соединения по изобретению показаны как в терапевтическом, так и профилактическом лечении таких состояний.
Другие болезненные состояния, которые могут быть упомянуты, включают терапевтическое и/или профилактическое лечение венозного тромбоза и эмболии легких, артериального тромбоза (например, при инфаркте миокарда, нестабильной стенокардии, ударе, вызванном тромбозом, и тромбозе периферических артерий) и системной эмболии, обычно от предсердия во время фибрилляции предсердий или от левого желудочка после трансмурального инфаркта миокарда.
Кроме того, соединения по изобретению показаны в лечении состояний, где имеется нежелательный избыток proCPU/CPU.
Кроме того, предполагается, что соединения по изобретению полезны в профилактике реокклюзии и рестеноза (т.е. тромбоза) после тромболиза, чрескожного транслюминального вмешательства (РТI) и операций коронарного шунтирования; в профилактике ретромбоза после микрохирургии и сосудистой хирургии вообще.
Дополнительные показания включают терапевтическое и/или профилактическое лечение диссеминированного внутрисосудистого коагулирования, вызванного бактериями, множественными травмами, интоксикацией или другим механизмом, фибринолитическое лечение, когда кровь находится в контакте с инородными поверхностями в организме, такими как трансплантаты сосудов, сосудистые стенты, сосудистые катетеры, механические и биологические искусственные клапаны или любое другое медицинское приспособление, и фибринолитическое лечение, когда кровь находится в контакте с медицинскими приборами вне тела, например, во время сердечно-сосудистой операции с использованием аппарата искусственного кровобращения или при гемодиализе.
Кроме того, предполагается, что соединения по изобретению полезны в профилактике развития атеросклероза и отторжения трансплантата у пациентов, подвергнутых трансплантации органов, например пересадке почки.
Также предполагается, что соединения по изобретению полезны в ингибировании созревания и прогрессирования опухоли.
Кроме того, предполагается, что соединения по изобретению полезны в лечении любого состояния, способствующим фактором для которого является фиброз. Такие фиброзные состояния включают кистозный фиброз, легочное фиброзное заболевание, например хроническую обструктивную болезнь легких (COPD), респираторный дистресс-синдром взрослых (ARDS), фиброзно-мышечную дисплазию, фиброзную болезнь легких и отложения фибрина в глазу во время офтальмологической операции.
Также предполагается, что соединения по изобретению полезны в лечении воспаления. В частности, данное изобретение можно применять для лечения или профилактики воспалительных болезней, таких как астма, артрит, эндометриоз, воспалительные заболевания кишечника, псориаза и атопических дерматитов.
Также предполагается, что соединения по изобретению полезны в лечении нейродегенеративных болезней, таких как болезни Альцгеймера и Паркинсона.
Также предполагается, что соединения по изобретению полезны в лечении состояний, при которых полезно поддерживание или увеличение уровней брадикинина. Такие состояния включают гипертензию, стенокардию, сердечную недостаточность, легочную гипертензию, почечную недостаточность и органную недостаточность.
Соединения по изобретению также можно объединять и/или вводить совместно с любым антитромботическим агентом с разным механизмом действия, таким как антикоагулянт (например, антагонист витамина K, нефракционированный или низкомолекулярный гепарин, синтетический фрагмент гепарина, такой как фондапаринукс, ингибитор тромбина, ингибитор фактора Xa или другой ингибитор фактора коагуляции/фермента, рекомбинантный фактор коагуляции, такой как рекомбинантный человеческий активированный протеин C) или с антитромбоцитарным агентом (таким как ацетилсалициловая кислота, дипиридамол, тиклопидин, клопидогрел или другой антагонист ADP (адензиндифосфат)-рецепторов [таких как P2Y12 или P2Y1], ингибитор рецепторов тромбоксана и/или ингибитор синтетазы, антагонист рецепторов фибриногена, миметик простациклина или ингибитор фосфодиэстеразы). Кроме того, соединения по изобретению можно объединять и/или вводить совместно с тромболитиками, такими как тканевый активатор плазминогена (природный, рекомбинантный или модифицированный), стрептокиназа, урокиназа, проурокиназа, анизоилированный активаторный комплекс стрептокиназы с плазминогеном (APSAC), активаторы плазминогена слюнных желез животного и подобные, в лечении тромботических болезней, в частности инфаркта миокарда, ишемического удара и массивной эмболии легких.
Соединения по изобретению должны обладать селективностью по отношению к карбоксипептидазе U по сравнению с карбоксипептидазой N>100:1, например >1000:1, при использовании анализа, описанного ниже.
Ингибирующее действие соединений по настоящему изобретению оценивали, используя анализ, описанный в Dirk Hendriks, Simon Scharpé and Marc van Sande, Clinical Chemistry, 31, 1936-1939 (1985), и Wei Wang, Dirk F. Hendriks, Simon S. Scharpé, The Journal of Biological Chemistry, 269, 15937-15944 (1994).
Таким образом, в настоящем изобретении предложено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, или сольват такой соли, как определено выше, для применения в терапии.
В дополнительном аспекте настоящего изобретения предложено применение соединения формулы (I) или его фармацевтически приемлемой соли или сольвата, или сольвата такой соли, как определено выше, для изготовления лекарства для применения в терапии.
В контексте настоящего изобретения термин "терапия" включает "профилактику", если нет конкретных указаний на обратное. Термины "терапевтический" и "терапевтически" следует понимать соответственно.
В изобретении также предложен способ лечения состояния, где ингибирование карбоксипептидазы U является полезным, у млекопитающего, страдающего от указанного состояния, или имеющего риск указанного состояния, который включает введение млекопитающему терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли или сольвата, или сольвата такой соли, как определено выше.
Для вышеупомянутых терапевтических применений вводимая доза будет меняться в зависимости от применяемого соединения, способа введения, требуемого лечения и указанного расстройства.
Соединения формулы (I) и их фармацевтически приемлемые соли, сольваты или сольваты их солей можно применять независимо друг от друга, но в общем случае их следует вводить в форме фармацевтической композиции, в которой соединение формулы (I), соль, сольват или сольват соли (активный ингредиент) объединено с фармацевтически приемлемым адъювантом, разбавителем или носителем. В зависимости от способа введения фармацевтическая композиция будет, например, содержать от 0,05 до 99 мас.%(массовый процент), например от 0,05 до 80 мас.%, например от 0,10 до 70 мас.%, например от 0,10 до 50% масс.активного ингредиента, при этом все массовые проценты основаны на суммарной массе композиции.
Таким образом, в настоящем изобретении также предложена фармацевтическая композиция, содержащая соединение формулы (I), или его фармацевтически приемлемую соль или его сольват, или сольват такой соли, как определено выше, вместе с фармацевтически приемлемым адъювантом, разбавителем или носителем.
Кроме того, в изобретении предложен способ приготовления фармацевтической композиции по изобретению, при котором смешивают соединение формулы (I), или его фармацевтически приемлемую соль, или сольват, или сольват такой соли, как определено выше, с фармацевтически приемлемым адъювантом, разбавителем или носителем.
Также в данное изобретение включены производные соединений формулы (I), которые обладают биологическим действием соединений формулы (I), такие как пролекарства. Пролекарствами являются, например, (пивалоилокси)метиловые эфиры и [(этоксикарбонил)окси]метиловые эфиры карбоновых кислот.
Следующие примеры иллюстрируют данное изобретение.
ПРИМЕРЫ
Общие экспериментальные методики
Масс-спектры регистрировали на масс-спектрометре VG Platform II или Micromass ZQ, оснащенном интерфейсом для электрораспыления (LC-MS). Масс-спектры высокого разрешения регистрировали на масс-спектрометре Micromass LCT, оснащенным интерфейсом для электрораспыления (LC-HRMS). 1H ЯМР-измерения выполняли на спектрометрах Varian UNITY plus 400, 500 или 600, работающих на частотах 400, 500 и 600 МГц соответственно. ЯМР-спектры регистировали в ДМСО,
D2O, CD3CN или их смесях. Химические сдвиги выражены в миллионных долях (м.д.=ppm) с использованием в качестве внутреннего стандарта растворителя. Хроматографические разделения выполняли с использованием силикагеля 60 фирмы Меrск (0,063-0,200 мм). Соединения, приведенные ниже, были названы с использованием ACD/Name версия 6.06/11 июня 2002, Advanced Chemistry Development Inc., Canada.
ПРИМЕР 1
Данный пример иллюстрирует получение 2-[(6-аминопиридин-3-ил)метил]-5-(1,1'-бифенил-3-ил)-3-меркаптопентановой кислоты.
(а) 3-(1,1'-Бифенил-3-ил)пропаналь
К раствору 3-йод-1,1'-бифенила (0,964 г, 3,44 ммоль) и тетрабутиламмония хлорида (0,956 г, 3,44 ммоль) в сухом DMF (3 мл) добавляли аллиловый спирт (0,351 мл, 5,16 ммоль), гидрокарбонат натрия (0,723 г, 8,60 ммоль) и ацетат палладия(II) (31 мг, 0,14 ммоль) и смесь перемешивали при комнатной температуре в течение 18 ч. Затем реакционную смесь разбавляли EtOAc и твердое вещество отфильтровывали (Celite). Фильтрат три раза промывали водой, сушили (Na2SO4) и концентрировали. В результата флэш-хроматографии (гептан/трет-бутилметиловый эфир, 4:1) остатка получали 3-(1,1'-бифенил-3-ил)пропаналь (0,601 г, 83%).
(б) трет-Бутил-5-(1.1'-бифенил-3-ил)-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)пент-2-еноат
Раствор трет-бутил-3-{6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}-2-(диэтоксифосфорил)пропаноата (1,058 г, 2,31 ммоль) в сухом THF (4 мл) добавляли к раствору гидрида натрия (0,111 г, 60% в минеральном масле, 2,77 ммоль) в сухом THF (3 мл) при 0°С и смесь перемешивали при 0°С в течение 60 мин. К этой смеси добавляли раствор 3-(1,1'-бифенил-3-ил)пропаналя (0,582 г, 2,77 ммоль) в сухом THF (3 мл) и реакционную смесь оставляли для достижения комнатной температуры на 22 часа. Затем добавляли EtOAc и органическую фазу промывали насыщенным водным NH4CI и водой, сушили (Na2SO4) и концентрировали. В результате флэш-хроматографии остатка (толуол/EtOAc, 15:1) получали трет-бутил-5-(1,1'-бифенил-3-ил)-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)пент-2-еноат (1,105 г, 93%) в виде смеси E/Z-изомеров.
(в) трет-Бутил-5-(1,1'-бифенил-3-ил)-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]пентаноат
Раствор 4-метокси-α-толуолтиола (0,58 мл, 4,17 ммоль) в сухом, дегазированном DMF (2 мл) обрабатывали при комнатной температуре каталитическим количеством гидрида натрия (60% в минеральном масле), а затем раствором трет-бутил-5-(1,1'-бифенил-3-ил)-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)пент-2-еноата (1,073 г, 2,08 ммоль) в сухом, дегазированном DMF (5 мл). Через 20 часов при комнатной температуре реакционную смесь разбавляли EtOAc и три раза промывали водой. Органический слой сушили (Na2SO4), концентрировали и подвергали флэш-хроматографии (гептан/EtOAc, 3:1, и толуол/EtOAc, 12:1) с образованием трет-бутил-5-(1,1'-бифенил-3-ил)-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]пентаноата (1,251 г, 90%).
г) 2-[(6-Аминопиридин-3-ил)метил]-5-(1,1'-бифенил-3-ил)-3-меркаптопентановая кислота
трет-Бутил-5-(1,1'-бифенил-3-ил)-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]пентаноат (0,669 г, 1,00 ммоль) растворяли в триэтилсилане (0,75 мл) и трифторуксусной кислоте (6,0 мл). Раствор нагревали до 60°С в течение 3 часов и затем концентрировали. В результате очистки остатка HPLC с обращенной фазой (колонка С-8, линейный градиент 40%→100% MeCN в 5%-ном водном MeCN, содержащем 0,15% трифторуксусной кислоты) после лиофильной сушки получали указанное в заголовке диастереомерное соединение в виде трифторуксуснокислой соли (0,342 г, 68%).
1H ЯМР (400 МГц, CD3CN/D2O): δ 7.70 (dd, J=2,1, 9,2 Гц, 0,5Н), 7.66 (dd, J=2,1, 9,2 Гц, 0,5Н), 7.61-7.58 (m, 2H), 7.53-7.51 (m, 1H), 7.46-7.41 (m, 4H), 7.38-7.32 (m, 2H), 7.22-7.16 (m, 1H), 6.88 (d, J=9,1 Гц, 0,5Н), 6.84 (d, J=9,1 Гц, 0,5Н), 3.10-2.74 (m, 6H), 2.17-2.04 (m, 1H), 1.91-1.78 (m, 1H). 13С ЯМР (101 МГц, CD3CN/D2O): δ 175.3, 174.9, 153.0, 146.0, 145.8, 142.3, 141.1, 140.9, 134.0, 133.9, 129.4, 129.2, 127.9, 127.9, 127.8, 127.3, 127.2, 127.1, 124.9, 124.8, 124.4, 124.1, 113.9, 113.8, 53.6, 53.0, 41.3, 40.5, 37.9, 33.1, 33.0, 31.2, 30.3. HRMS (масс-спектрометрия высокого разрешения) (ESI) : рассчитано для C23H25N2O2S 393,1637 (М+Н)+, найдено 393,1650.
ПРИМЕР 2
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-(1-нафтил)пентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (400 МГц, CDCl3): δ 8.14-8.10 (d, 1H), 7.93-7.89 (d, 1H), 7.80-7.54 (m, 1H), 7.67-7.35 (m, 6H), 6.83-6.77 (m, 1H), 3.52-3.35 (m, 1H), 3.22-3.12 (m, 2H), 2.90-2.80 (m, 3H), 2.25-2.13 (m, 1H), 2.05-1.87 (m, 1H). HRMS (ESI): рассчитано для C21H23N2O2S 367,1480 (М+Н)+, найдено 367,1497.
ПРИМЕР 3
2-[(6-Аминопиридин-3-ил)метил]-5-(3-цианофенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (400 МГц, CD3CN/D2O): δ 7.73 (dd, J=2,2, 9,3 Гц, 0,51-1), 7.70 (dd, J=2,2, 9,3 Гц, 0,5Н), 7.58-7.40 (m, 5H), 6.90 (d, J=9,1 Гц, 0,5Н), 6.88 (d, J=9,3 Гц, 0,5Н), 2.99-2.88 (m, 2Н), 2.82-2.71 (m,4H), 2.12-2.00 (m, 1Н), 1.88-1.74 (m, 1H).
13С ЯМР (101 МГц, CD3CN/D2O): δ 175.5, 174.9, 153.0, 146.0, 145.8, 143.1, 133.9, 132.4, 132.3, 130.3, 130.3, 129.8, 124.3, 124.0, 119.4, 113.9, 113.9, 111.6, 53.8, 52.8, 41.1, 40.2, 37.4, 32.5, 32.5, 31.1, 30.5. HRMS (ESI): рассчитано для C18H20N3O2S 342,1276 (М+Н)+, найдено 342,1277.
ПРИМЕР 4
5-[3-(Аминокарбонил)фенил]-2-[(6-аминопиридин-3-ил)метил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с 3-йод-N-(2,4,6-триметоксибензил)бензамида. 3-Йод-N-(2,4,6-триметоксибензил)бензамид синтезировали из 3-йодбензойной кислоты с использованием стандартных методик.
1H ЯМР (400 МГц, CD3CN/D2O): δ 7.72-7.67 (m, 1H), 7.65-7.61 (m, 2H), 7.52-7.49 (m, 1H), 7.42-7.35 (m, 2H), 6.89 (d, J=9,3 Гц, 0,7Н), 6,85 (d, J=9,1 Гц, 0,3Н), 3.00-2.87 (m, 2H), 2.81-2.72 (m, 4H), 2.13-2.00 (m, 1H), 1.90-1.86 (m, 1H).
13С ЯМР (101 МГц, CD3CN/D2O): δ 175.7, 175.1, 171.5, 161.7, 161.4, 153.0, 146.0, 145.8, 142.1, 142.0, 133.9, 133.4, 132.7, 129.1, 127.8, 127.7, 125.5, 124.3, 124.0, 114.0, 113.9, 53.7, 52.6, 41.0, 39.9, 37.7, 37.6, 32.8, 32.7, 31.0, 30.4. HRMS (ESI): рассчитано для
C18H22N3O3S 360,1382 (М+Н)+, найдено 360,1378.
ПРИМЕР 5
2-[(6-Аминопиридин-3-ил)метил]-5-[2-фтор-4-(трифторметил)фенил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (400 МГц, CD3CN/D2O): δ 7.75-7.71 (m, 1H), 7.56 (d, J=1,6 Гц, 1H), 7.47-7.35 (m, 3H), 6.91 (d, J=9,3 Гц, 1H), 3.04-2.91 (m, 1H), 2.88-2.74 (m, 4H).
13C ЯМР (101 МГц, CD3CN/D2O): δ 175.4, 174.9, 162.0, 161.4, 159.6, 153.0, 146.0, 145.9, 134.0, 133.2, 133.0, 129.9, 124.2, 124.0, 121.4, 114.0, 113.9, 112.8, 112.6, 53.8, 53.0, 41.5, 40.8, 36.3, 36.2, 31.2, 30.6, 26.5. HRMS (ESI): рассчитано для C18H19F4N2O2S 403,1103 (М+Н)+, найдено 403,1137.
ПРИМЕР 6
2-[(6-Аминопиридин-3-ил)метил]-5-(3-хлорфенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (500 МГц, CD3CN/D2O): δ 7.75 (dd, 0,5H), 7.72 (dd, 0,51-1), 7.56 (d, 0,5Н), 7.54 (d, 0,51-1), 7.30-7.10 (m, 4H), 6.92 (d, 0,5H), 6.91 (d, 0,5H), 3.02-2.65 (m, 6Н), 2.10-2.00 (m, 1H), 1.88-1.74 (m, 1H). MS (ESI): 351,1 (М+Н)+.
ПРИМЕР 7
2-[(6-Аминопиридин-3-ил)метил]-5-(1,3-бензодиоксол-5-ил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (400 МГц, CD3СN/D2О): δ 7.72 (dd, 1H), 7.69 (d, 0,5H), 7.55 (s, 0,5H), 7.53 (s, 0,5H), 6.89 (m, 1H), 6.77-6.60 (m, 3Н), 5.88 (s, 2H), 3.0-2.70 (m, 5H), 2.58-2.68 (m, 1H), 1.92-2.08 (m, 1H), 1.69-1.81 (m, 1H). HRMS (ESI): рассчитано для C18H20N2O4S 361,1222 (М+Н)+, найдено 361, 1236.
ПРИМЕР 8
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-пиридин-2-илпентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с 3-пиридин-2-илпропаналя.
1H ЯМР (600 М Гц, D2O): δ м.д. 1.90-2.37 (m, 2H), 2.70-2.98 (m, 3H), 3.05-3.11 (m, 1H), 3.12-3.24 (m, 1H), 3.32-3.41 (m, 1H), 6.89 (d, 1H), 7.57 (s, 1H), 7.75 (dd, 1H), 7.80-7.85 (m, 1 Н), 7.88 (d, 1 Н), 8.39-8.46 (m, 1 Н), 8.54-8.60 (m, 1Н).
MS (ESI): 318,2 (М+Н)+.
ПРИМЕР 9
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-(3,4,5-триметоксифенил)пентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (600 МГц, CD3СN/D2O): δ м.д. 1.71-1.87 (m, 1H), 1.98-2.10 (m, 1H), 2.58-2.70 (m, 1H), 2.73-2.87 (m, 4H), 2.90 (d, 0,5H), 2.88-3.02 (m, 0,5H), 3.65 (s, 3H), 3.75 (s, 3H), 3.75 (s, 3Н), 6.48 (s, 1H), 6.49 (s, 1H), 6.88 (d, 0,5H), 6.89 (d, 0,5H), 7.52 (d, 1Н), 7.67-7.72 (m, 1H). MS (ESI): 407,2 (М+Н)+.
ПРИМЕР 10
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-пиридин-3-илпентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с 3-пиридин-3-илпропаналя.
1H ЯМР (600 МГц, CD3СN/D2O): δ м.д. 1.78-1.90 (m, 1Н), 2.03-2.19 (m, 1H), 2.71-2.78 (m, 1H), 2.78-3.02 (m, 4H), 3.07-3.18 (m, 1H), 6.90 (d, 1H), 7.56 (s, 1H), 7.73-7.76 (m, 1H), 7.91-7.95 (m, 1H), 8.40-8.44 (m, 1H), 8.55-8.59 (m, 2H).
MS (ESI): 318,2 (М+Н)+.
ПРИМЕР 11
2-[(6-Аминопиридин-3-ил)метил]-5-[4-(цианометил)фенил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (500 МГц, CD3CN/D2O): δ 7.99 (dd, 0,5H), 7.96 (dd, 0,5H), 7.81 (d, 0,5Н), 7.80 (d, 0,5H), 7.56-7.46 (m, 4H), 7.17 (d, 0,5H), 7.15 (d, 0,5H), 4.11 (s, 2H), 3.26-2.97 (m, 6H), 2.40-2.25 (m, 1H), 2.17-2.02 (m, 1H).
MS (ESI): 356,2 (М+Н)+.
ПРИМЕР 12
2-[(6-Аминопиридин-3-ил)метил]-5-(2-гидроксифенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с 1-йод-2-[(4-метоксибензил)окси]бензола. 1-Йод-2-[(4-метоксибензил)окси]бензол синтезировали из 2-йодфенола с использованием стандартных методик.
1H ЯМР (500 МГц, 90% CD3CN/D2O): δ м.д. 1.72-1.87 (m, 1H), 2.00-2.15 (m, 1H), 2.60-2.75 (m, 1H), 2.77-2.94 (m, 4,6H), 3.06-3.11 (m, 0,4H), 6.75-6.81 (m, 2H), 6.90-6.94 (m, 1H), 7.02-7.13 (m, 2H), 7.56 (d, 0,6H), 7.57 (d, 0,4H), 7.75 (dd, 0,6H), 7.77 (dd, 0,4H). MS (ESI): 333,2 (M+H)+.
ПРИМЕР 13
2-[(6-Аминопиридин-3-ил)метил]-5-[4-(аминосульфонил)фенил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с 4-йод-N-(2,4,6-триметоксибензил)бензолсульфонамида. 4-Йод-N-(2,4,6-триметоксибензил)бензолсульфонамид синтезировали из 4-йодбензолсульфонилхлорида с использованием стандартных методик.
1H ЯМР (500 МГц, 75% CD3CN/D2O): δ м.д. 1.79-1.92 (m, 1H), 2.04-2.18 (m, 1H), 2.76-2.88 (m, 4H), 2.90-3.07 (m, 2H), 6.92 (d, 0,5H), 6.93 (d, 0,5H), 7.40 (d, 1H), 7.42 (d, 1H), 7.57 (d, 0,5Н), 7.58 (d, 0,5H), 7.72-7.81 (m, 3Н). MS (ESI): 396,1 (М+Н)+.
ПРИМЕР 14
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-(4-метоксифенил)пентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (500 МГц, 75% CD3CN/D2O): δ м.д. 1.73-1.85 (m, 1H), 1.99-2.11 (m, 1H), 2.61-2.72 (m, 1H), 2.75-2.95 (m, 4,5H), 2.98-3.04 (m, 0,5H), 3.75 (s, 1,5H), 3.76 (s, 1,5H), 6.82-6.88 (m, 2H), 6.92 (d, 0,5H), 6.93 (d, 0,5H), 7.12 (d, 0,5H), 7.15 (d, 0,5Н), 7.56 (s, 0,5H), 7.58 (s, 0,5H), 7.72-7.78 (m, 1H). MS (ESI): 347,2 (M+H)+.
ПРИМЕР 15
2-[(6-Аминопиридин-3-ил)метил]-5-(4-гидроксифенил)-3-меркаптопентановую кислоту синтезировали из 2-[(6-аминопиридин-3-ил)метил]-3-меркапто-5-(4-метоксифенил)пентановой кислоты, используя условия, обычные для гидролиза метоксигруппы (концентрированная водная соляная кислота при нагревании с обратным холодильником в атмосфере аргона в течение 24 часов).
1H ЯМР (500 МГц, 25% CD3CN в D2O): δ м.д. 1.73-1.85 (m, 1H), 1.94-2.09 (m, 1H), 2.59-2.68 (m, 1H), 2.75-2.87 (m, 4H), 2.90 (d, 0,5H), 2.98-3.03 (m, 0,5H), 6.71-6.76 (m, 2H), 6.90-6.95 (m, 1H), 7.00-7.07 (m, 2H), 7.54-7.57 (m, 1H), 7.71-7.76 (m, 1H). MS (ESI): 333,2 (M+H)+.
ПРИМЕР 16
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-[4-(трифторметокси)фенил]пентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (500 МГц, CD3СN/D2O): δ м.д. 1.76-1.88 (m, 1H), 2.01-2.14 (m, 1H), 2.66-3.07 (m, 6H), 6.94 (d, 1H), 7.16-7.25 (m, 2H), 7.26-7.34 (m, 2H), 7.59 (d, 1H), 7.78 (dd, 1H). MS (ESI): 401,3 (M+H)+.
ПРИМЕР 17
2-[(6-Аминопиридин-3-ил)метил]-5-(1,3-диметил-2,4-диоксо-1,2,3,4-тетрагидропиримидин-5-ил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (500 МГц, CD3СN/D2O): δ м.д. 1.57-1.76 (m, 1H), 1.92-2.06 (m, 1H), 2.31-2.45 (m, 1H), 2.53-2.63 (m, 1H), 2.75-3.07 (m, 4H), 3.22 (s, 1,5H), 3.23 (s, 1,5H), 3.30 (s, 1,5H), 3.30 (s, 1,5H), 6.94 (d, 1H), 7.30 (s, 0,5H), 7.32 (s, 0,5H), 7.59-7.64 (m, 1H), 7.80 (dd, 1H). MS (ESI): 379,2 (M+H)+.
ПРИМЕР 18
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-(тетрагидро-2-тиенил)пентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с 3-тиен-2-илпропаналя.
1H ЯМР (500 МГц, 90% CD3CN/D2O): δ м.д. 1.48-1.60 (m, 3H), 1.70-1.90 (m, 3Н), 2.00-2.10 (m, 2Н), 2.70-3.10 (m, 6H), 3.25-3.33 (m, 1Н), 6.92 (d, 1H), 7.59 (s, 1H), 7.78 (dd, 1H). MS (ESI): 327,3 (M+H)+.
ПРИМЕР 19
2-[(6-Аминопиридин-3-ил)метил]-5-[3-(гидроксиметил)фенил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с 1-йод-3-{[(4-метоксибензил)окси]метил}бензола. 1-Йод-3-{[(4-метоксибензил)окси]метил}бензол синтезировали из (3-йодфенил)метанола с использованием стандартных методик.
1H ЯМР (500 МГц, CD3СN/D2О): δ м.д. 1.94-2.10 (m, 1H), 2.21-2.37 (m, 1H), 2.78-3.24 (m, 6H), 4.77 (s, 1H), 4.78 (s, 1H), 7.09 (d, 0,5H), 7.12 (d, 0,5H), 7.34-7.44 (m, 3H), 7.48-7.54 (m, 1H), 7.73 (d, 0,5H), 7.74 (d, 0.5H), 7.91 (dd, 0,5H), 7.96 (dd, 0,5H). MS (ESI): 347,3 (M+H)+.
ПРИМЕР 20
2-[(6-Аминопиридин-3-ил)метил]-5-[2-(2,4-дихлорфенокси)фенил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (400 МГц, CDCI3): δ 7.64 (d, 1H), 7.51 (d, 1H), 7.40 (d, 1H), 7.27 (m, 1H), 7.18-7.04 (m, 3H), 7.78-7.69 (m, 3H), 3.15-2.92 (m, 2H), 2.87-2.65 (m, 4H), 2.21-2.08 (m, 1H), 1.89-1.75 (m, 1H). HRMS (ESI): рассчитано для C23H22Cl2N2O3S 477,0806 (М+Н)+, найдено 477,0170.
ПРИМЕР 21
2-[(6-Аминопиридин-3-ил)метил]-5-(3,5-диметилфенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1.
1H ЯМР (500 МГц, CD3CN/D2O): δ м.д. 1.72-1.85 (m, 1H), 1.97-2.11 (m, 1H), 2.23 (s, 3H), 2.24 (s, 3H), 2.57-2.66 (m, 1H), 2.75-2.87 (m, 4H), 2.90 (d, 0,5H), 2.99-3.05 (m, 0,5H), 6.78-6.85 (m, 3H), 6.88-6.94 (m, 1H), 7.54 (d, 0,5H), 7.56 (d, 0,5H), 7.71 (dd, 0,5H), 7.73 (d, 0,5H). MS (ESI): 345,2 (М+Н)+.
ПРИМЕР 22
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-(4-пропилфенил)пентановую кислоту синтезировали по методике, описанной для Примера 1.
1H ЯМР (500 МГц, CD3CN/D2O): δ м.д. 0.84 (t, 3Н), 1.49-1.58 (m, 2H), 1.70-1.81 (m, 1H), 1.96-2.04 (m, 1H), 2.50 (t, 2H), 2.60-2.70 (m, 1H), 2.71-2.93 (m, 4H), 2.93-3.01 (m, 1H), 6.88 (d, 1H), 7.07-7.10 (m, 4H), 7.54 (d, 1H), 7.71 (dd, 1H). MS (ESI): 359,2 (М+Н)+.
ПРИМЕР 23
2-[(6-Аминопиридин-3-ил)метил]-5-(4-бензилфенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с (4-йодфенил)(фенил)метанона.
1H ЯМР (500 МГц, 80% CD3CN/D2O): δ м.д. 1.72-1.82 (m, 1H), 2.00-2.10 (m, 1H), 2.72-2.62 (m, 1H), 2.78-3.04 (m, 5Н), 3.9 (s, 2H), 6.90 (d, H), 7.08-7.29 (m, 9H), 7.55 (d, 1H), 7.73 (dd, 1H). HRMS (ESI): рассчитано для C24H27N2O2S 407,1793 (M+H)+, найдено 407,1804.
ПРИМЕР 24
2-[(2-Амино-1,3-тиазол-5-ил)метил]-3-меркапто-5-фенилпентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с трет-бутил-3-{2-[(трет-бутоксикарбонил)амино]-1,3-тиазол-5-ил}-2-(диэтоксифосфорил)пропионата. трет-Бутил-3-{2-[(трет-бутоксикарбонил)амино]-1,3-тиазол-5-ил}-2-(диэтоксифосфорил)пропаноат синтезировали, как показано на Схеме 1.
1H ЯМР (500 МГц, 90% CD3CN/D2O): δ м.д. 1.78-1.90 (m, 1H), 2.00-2.11 (m, 1H), 2.68-2.77 (m, 1H), 2.78-3.2 (m, 4,5H), 3.05-3.11 (m, 0.5H), 6.85-6.88 (m, 1H), 7.16-7.33 (m, 5H). MS (ESI): 323,2 (M+H)+.
ПРИМЕР 25
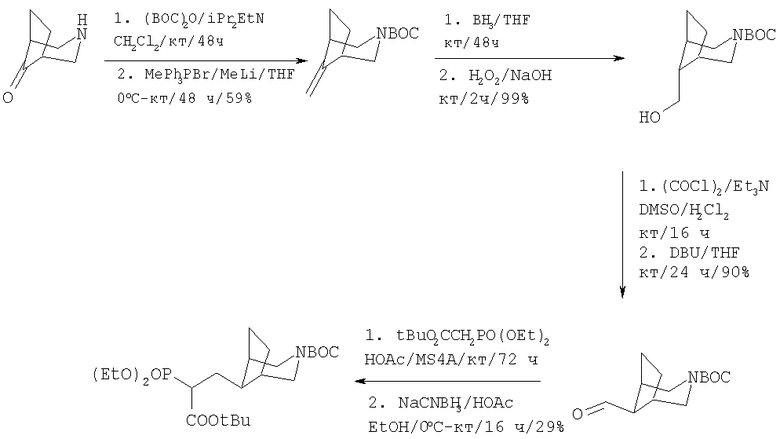
2-(3-Азабицикло[3.2.1]окт-8-илметил)-3-меркапто-5-фенилпентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с трет-бутил-8-[3-трет-бутокси-2-(диэтоксифосфорил)-3-оксопропил]-3-азабицикло[3.2.1]октан-3-карбоксилата. трет-Бутил-8-[3-трет-бутокси-2-(диэтоксифосфорил)-3-оксопропил]-3-азабицикло[3.2.1]октан-3-карбоксилат синтезировали, как показано на Схеме 2.
1H ЯМР (400 МГц, CD3СN/D2O): δ 7.90-7.80 (m, 2H), 7.80-7.70 (m, 3H), 3.80-3.60 (m, 2H), 3.60-3.35 (m, 4Н), 3.35-3.18 (m, 1H), 3.18-3.00 (m, 1H), 2.90-1.80 (m, 11H). MS (ESI): 333,5 (M+H)+.
ПРИМЕР 26
Этот пример иллюстрирует получение 2-[(6-аминопиридин-3-ил)метил]-3-меркапто-5-(3-{[метил(2-фенилэтил)амино]карбонил}фенил)пентановой кислоты.
(а) 3-{5-трет-Бутокси-4-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-оксопентил}бензойная кислота
KOH (5 мл 1 М раствора в этаноле) добавляли к раствору этил-3-{5-трет-бутокси-4-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-оксопентил}бензоата (0,27 г, 0,406 ммоль, синтезированного в соответствии с методикой Примера 1) в этаноле (2 мл) и смесь перемешивали при комнатной температуре в течение 2 часов и затем при 50°С в течение 2 часов. Затем реакционную смесь разбавляли диэтиловым эфиром и водой. Органическую фазу экстрагировали 0,1 М водным раствором КОН и объединенную органическую фазу подкисляли (рН 5) 3 М водным раствором HCl. Затем водную фазу экстрагировали диэтиловым эфиром и органическую фазу промывали солевым раствором, сушили и концентрировали. В результате очистки остатка посредством HPLC с обращенной фазой (колонка С-8, линейный градиент 40%→100% MeCN в 5%-ном водном MeCN, содержащем 0,1 М ацетата аммония) получали остаток, который растворяли в толуоле и воде и концентрировали с получением 3-{5-трет-бутокси-4-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-оксопентил}бензойной кислоты (0,12 г, 54%).
(б) трет-Бутил-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-(3-{[метил(2-фенилэтил)амино]карбонил}фенил)пентаноат
N-Метилфенетиламин (20 мкл, 0,14 ммоль), HATU (55 мг, 0,15 ммоль) и iPr2EtN (46 мкл, 0,26 ммоль) добавляли к раствору 3-{5-трет-бутокси-4-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-оксопентил}бензойной кислоты (84 мг, 0,132 ммоль) в DMF (2 мл) в атмосфере аргона при 0°С. Реакционную смесь перемешивали в течение 2 часов и затем гасили льдом. Добавляли диэтиловый эфир и воду и водную фазу экстрагировали диэтиловым эфиром. Объединенную органическую фазу сушили и концентрировали. В результате флэш-хроматографии (гептан/EtOAc, 3:1) получали трет-бутил-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-(3-{[метил(2-фенилэтил)амино]карбонил}фенил)пентаноат (81 мг, 81,4%).
(в) 2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-(3-
{[метил(2-фенилэтил)амино]карбонил}фенил)пентановая кислота
трет-Бутил-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-(3-{[метил(2-фенилэтил)амино]карбонил}фенил)пентаноат (80 мг, 0,106 ммоль) растворяли в триэтилсилане (0,4 мл) и трифторуксусной кислоте (3,0 мл). Раствор нагревали до 60°С в течение 1 часа и затем концентрировали. После очистки остатка посредством HPLC с обращенной фазой (колонка С-8, линейный градиент 20%→100% MeCN в 5%-ном водном MeCN, содержащем 0,15% трифторуксусной кислоты), после лиофильной сушки получали указанное в заголовке диастереомерное соединение в виде трифторуксуснокислой соли (64 мг, 100%).
1H ЯМР (400 МГц, CD3CN/D2O): δ 7.76-6.63 (m, 12H), 3.71 (m, 1H), 3.40 (m, 1H), 3.21-2.54 (m, 11H), 2.12-1.63 (m, 2H). HRMS (ESI): рассчитано для С27Н31N3О3S 478,2164 (М+Н)+, найдено 478,2133.
ПРИМЕР 27
3-[5-(6-Аминопиридин-3-ил)-4-карбокси-3-меркаптопентил]бензойную кислоту синтезировали в соответствии с методикой Примера 26, начиная с 3-{5-трет-бутокси-4-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-оксопентил}бензойной кислоты.
1H ЯМР (400 МГц, D2O): δ 8.05-8.01 (dd, 1H), 8.01-7.99 (s, 1H), 7.90-7.86 (dd, 1H), 7.73-7.70 (s, 1H), 7.68-7.58 (m, 2H), 7.08-7.04 (d, 1H), 3.18-3.08 (m, 1H), 3.06-2.90 (m, 5H), 2.36-2.26 (m, 1H), 2.14-2.04 (m, 1H). HRMS (ESI): рассчитано для C18H20N2O4S 361,1222 (М+Н)+, найдено 361, 1212.
ПРИМЕР 28
2-[(6-Аминопиридин-3-ил)метил]-5-[3-(3,4-дигидроизохинолин-2(1H)-илкарбонил)фенил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, CD3CN/D2O): δ 7.73 (m, 1Н), 7.52 (s, 1H), 7.44-7.11 (m, 8H), 6.90 (m, 1H), 4.81 (s, 1H), 4.54 (s, 1H), 3.89 (br, 1H), 3.57 (br, 1H), 2.99-2.65 (m, 8H), 2.09 (m, 1H), 1.85 (m, 1H). HRMS (ES1): рассчитано для С27Н29N3О3S 476,2008 (М+Н)+, найдено 476, 2002.
ПРИМЕР 29
2-[(6-Аминопиридин-3-ил)метил]-5-{3-[(6,7-диметокси-3,4-дигидроизохинолин-2(1H)-ил)карбонил]фенил}-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (400 МГц, CD3CN/D2O): δ 7.68 (m, 1H), 7.49 (s, 1H), 7.38-7.22 (m, 4H), 6.90-6.72 (m, 2,5H), 6.47 (s, 0,5H), 4.69 (s, 1H), 4.44 (s, 1H), 3.96-3.46 (m, 8H), 3.01-2.59 (m, 8H), 2.17-1.67 (m, 2H). HRMS (ESI): рассчитано для С29Н33N3O5S 536,2219 (М+Н)+, найдено 536, 2248.
ПРИМЕР 30
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-{3-[(2-пиридин-2-илэтокси)карбонил]фенил}пентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (400 МГц, CD3CN/D2O): δ 8.64 (d, 1H), 8.46 (dd, 1H), 7.98 (d, 1H), 7.88 (dd, 1H), 7.77-7.64 (m, 3Н), 7.58-7.31 (m, 3Н), 6.89 (dd, 1H), 4.65 (t, 2H), 3.50 (t, 2H), 2.99-2.62 (m, 6H), 2.03 (m, 1H), 1.79 (m, 1H). HRMS (ESI): рассчитано для C25H27N3O4S 466,1803 (М+Н)+, найдено 466, 1813.
ПРИМЕР 31
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[2-(2,6-дихлорфенил)этокси]карбонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (400 МГц, CD3CN/D2O): δ 7.69 (m, 3Н), 7.51 (s, 1H), 7.38-7.28 (m, 4H), 7.12 (m, 1H), 6.84 (m, 1H), 4.48 (m, 2H), 3.62 (m, 0,5H), 3.31 (m, 2H), 3.10 (m, 0,5H), 2.98-2.53 (m, 5H), 2.0 (m, 1H), 1.75 (m, 1H). HRMS (ESI): рассчитано для C26H26CI2N2O4S 533,1069 (М+Н)+, найдено 533, 1071.
ПРИМЕР 32
2-[(6-Аминопиридин-3-ил)метил]-5-[3-(этоксикарбонил)фенил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26, начиная с этил-3-{5-трет-бутокси-4-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-оксопентил}бензоата.
1H ЯМР (500 МГц, CD3CN/D2O): δ 7.90 (d, 1Н), 7.87 (s, 1H), 7.74 (d, 1H), 7.58 (s, 1H), 7.53 (d, 1H), 7.48 (t, 1H), 6.91 (d, 1H), 4.41 (q, 2H), 2.95-3.03 (m, 1H), 2.95-2.82 (m, 4H), 2.75-2.80 (m, 1H), 2.14-2.23 (m, 1H), 1.95-2.03 (m, 1H), 1.41 (t, 3H). HRMS (ESI): рассчитано для C20H25N2O4S 389,1535 (М+Н)+, найдено 389,1555.
ПРИМЕР 33
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[(2-фторэтил)амино]карбонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, 10% CD3CN в D2O): δ 7.95 (dd, 0,5H), 7.90 (dd, 0,5H), 7.86-7.81 (m, 2H), 7.75 (dd, 0,5H), 7.73 (dd, 0,5H), 7.70-7.60 (m, 2H), 7.13 (d, 0.5H), 7.07 (d, 0,5H), 4.89-4.86 (m, 1H), 4.8-4.76 (m, 1H), 3.91-3.94 (m, 1H), 3.85-3.89 (m, 1H), 3.25-3.12 (m, 2,5H), 3.11-2.98 (m, 3H), 2.92-2.97 (m, 0.5H), 2.41-2.24 (m, 1H), 2.21-2.01 (m, 1H). HRMS (ESI): рассчитано для C20H25FN3O3S 406,1600 (М+Н)+, найдено 406, 1560.
ПРИМЕР 34
2-[(6-Аминопиридин-3-ил)метил]-5-{3-[(диметиламино)карбонил]фенил}-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, 5% CD3CN/D2O): δ 7.77 (dd, 0,5H), 7.72 (dd, 0,5H), 7.52-7.54 (m, 1H), 7.45-7.32 (m, 2H), 7.25-7.29 (m, 2H), 6.91 (d, 0,5H), 6.93 (d, 0,5H), 3.07 (s, 3H), 2.95 (два s, 3H), 3.05-2.71 (m, 6H), 2.19-2.0 (m, 1H), 1.99-1.82 (m, 1H). HRMS (ESI): рассчитано для C20H26N3O3S 388,1695 (М+Н)+, найдено 388, 1683.
ПРИМЕР 35
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-{3-[(виниламино)карбонил]фенил}пентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, 10% CD3CN/D2O): δ 7.71 (два dd, 1H), 7.53 (два dd, 0,5H), 6.89 (m, 1H), 6.77-6.60 (m, 3H), 5.88 (s, 2H), 3.0-2.70 (m, 5H), 2.62 (m, 1H), 2.00 (m, 1H), 1.75 (m, 1H). HRMS (ESI): рассчитано для C20H24N3O3S 386,1538 (M+H)+, найдено 386, 1470.
ПРИМЕР 36
2-[(6-Аминопиридин-3-ил)метил]-5-[3-({[2-(1,3-бензодиоксол-5-ил)этил]амино}карбонил)фенил]-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, 20% CD3CN/D2O): δ м.д. 1.88-2.06 (m, 1H), 2.10-2.27 (m, 1H), 2.79-3.11 (m, 8Н), 3.68 (t, 2H), 6.00 (s, 2Н), 6.85 (m, 1H), 6.90 (m, 2H), 6.96 (d, 0,7Н), 7.01 (d, 0,ЗН), 7.47 (m, 1,21-1), 7.51 (m, 0,6Н), 7.56 (s, 0,7H), 7.58 (s, 0,3H), 7.62 (s, 2H), 7.76 (d, 0,7H), 7.81 (d, 0,3H). HRMS (ESI): рассчитано для С27Н29N3О5S 508, 1906 (М+Н),+ найдено 508, 1935.
ПРИМЕР 37
2-[(6-Аминопиридин-3-ил)метил]-5-{3-[(дибензиламино)карбонил]фенил}-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, 50% CD3CN/D2O): δ м.д. 2.28-2.40 (m, 1H), 2.52-2.63 (m, 1H), 3.25-3.53 (m, 6H), 4.99 (s, 2H), 5.23 (s, 2H), 7.46 (d, 0,4H), 7.48 (d, 0,6H), 7.71 (d, 2H), 7.83-8.00 (m, 12H), 8.08 (s, 1H), 8.25 (dd, 0,4H), 8.28 (dd, 0,6H).
HRMS (ESI): рассчитано для C32H33N3O3S 540,2321 (М+Н)+, найдено 540, 2340.
ПРИМЕР 38
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[(2-гидроксиэтил)(метил)амино]карбонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, 50% CD3CN/D2O): δ м.д. 1.71-2.11 (m, 2H), 2.67-2.96 (m, 6H), 2.89 (s, 1,5H), 3.01 (s, 1,5H), 3.34 (q, 1H), 3.52-3.57 (m, 1H), 3.59 (t, 1H), 3.77 (t, 1H), 6.74-6.86 (m, 1H), 7.12-7.41 (m, 4H), 7.45 (s, 1H), 7.58-7.63 (m, 0,5H), 7.65-7.69 (m, 0,5H).
HRMS (ESI): рассчитано для C21H28N3O4S 418,1800 (М+Н)+, найдено 418,1752.
ПРИМЕР 39
2-[(6-Аминопиридин-3-ил)метил]-5-{3-[(3-гидроксипирролидин-1-ил)карбонил]фенил}-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (400 МГц, CD3CN/D2O): δ 8.35-8.15 (m, 1H), 8.05 (br s, 1H), 8.00-7.75 (m, 4Н), 7.50-7.35 (m, 1H), 6.16 (br m, 0,5Н), 6.02 (br m, 0,5H), 5.02 (br m, 0,5H), 4.88 (br m, 0,5H), 4.50-3.60 (m, 4H), 3.55-3.20 (m, 7H), 3.0-2.2 (m, 4H). HRMS (ESI): рассчитано для C22H28N3O4S 430,1829 (М+Н)+, найдено 430, 1801.
ПРИМЕР 40
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[4-(4-хлорфенил)пиперазин-1-ил]карбонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (400 МГц, CD3CN): δ 7.75-7.67 (m, 1H), 7.52-7.47 (dd, 1H), 7.40-7.28 (m, 5Н), 7.12-7.07 (m, 3H), 6.90-6.84 (m, 1H), 4.00-3.50 (m, 4H), 3.40-3.20 (m, 4H), 3.03-2.90 (m, 1H), 2.87-2.70 (m, 5H), 2.17-2.03 (m, 1H), 1.97-1.89 (m, 1H). HRMS (ESI): рассчитано для C28H31CIN4O3S 539,1884 (M+H)+, найдено 539, 1868.
ПРИМЕР 41
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[бензил(метил)амино]карбонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (400 МГц, CD3CN): δ 7.75-7.18 (m, 11H), 6.88-6.80 (d, 1H), 4.80-4.70 (s, 1H), 4.53-4.45 (s, 1H), 3.00-2.95 (m, 1H), 2.93-2.90 (s, 3H), 2.88-2.78 (m, 5H), 2.05-2.00 (m, 1H), 1.99-1.94 (m, 1H). HRMS (ESI): рассчитано для С26Н29N3O3S 464,2008 (M+H)+, найдено 464, 1972.
ПРИМЕР 42
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-[3-(пирролидин-1-илкарбонил)фенил]пентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, 95% CD3CN в D2O): δ 7.75 (dd, 0,5H), 7.69 (dd, 0,5H), 7.51-7.54 (m, 1H), 7.44-7.30 (m, 4H), 6.91 (d, 0,5H), 6.87 (d, 0,5H), 3.53 (t, 2H), 3.30-3.40 (m, 2H), 3.00-2.79 (m, 5,5H), 2.67-2.74 (m, 0,5H), 2.18-1.8 (m, 6H). HRMS (ESI): рассчитано для
C22H28N3O3S 414,1851 (М+Н)+, найдено 414, 1837.
ПРИМЕР 43
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[4-(этоксикарбонил)пиперидин-1-ил]карбонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, CD3CN/D2O): δ 1.28 (t, 3Н), 1.59-1.79 (m, 2H), 1.86-1.96 (m, 2Н), 2.0-2.22 (m, 2H), 2.68-2.75 (m, 1H), 2.80-3.12 (m, 7H), 3.13-3.25 (m, 1H), 3.65 (d, 1Н), 4.18 (q, 2H), 4.40-4.48 (m, 1H), 6.95-7.00 (m, 1H), 7.27-7.31 (m, 2H), 7.36-7.48 (m, 2H), 7.60 (s, 1H), 7.78 (dd, 0,5H), 7.82 (dd, 0,5H). HRMS (ESI): рассчитано для С26Н34N3O5S 500,2219 (М+Н)+, найдено 500, 2233.
ПРИМЕР 44
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[4-(гидроксиметил)пиперидин-1-ил]карбонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (400 МГц, CD3CN): δ 7.65-7.71 (dd, 1H), 7.49-7.52 (d, 1H), 7.18-7.36 (m, 4Н), 6.82-6.85 (dd, 1H), 3.41-3.47 (m, 4H), 2.77-3.10 (m, 7H), 2.0-2.1 (m, 2H), 1.68-1.92 (m, 5H). HRMS (ESI): рассчитано для C24H32N3O4S 458,2114 (М+Н)+, найдено 458, 2097.
ПРИМЕР 45
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-{3-[(3-оксопиперазин-1-ил)карбонил]фенил}пентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, CD3CN/D2O): δ м.д. 1.77-1.90 (m, 1H), 1.99-2.12 (m, 1H), 2.75-3.0 (m, 6Н), 3.25-3.58 (m, 4H), 3.80-4.10 (m, 1H), 4.2 (s, 1H), 6.89 (d, 0,5H), 6.91 (d, 0,5H), 7.24-7.29 (m, 2H), 7.31-7.42 (m, 2H), 7.52 (s, 1H), 7.71 (dd, 0,4H), 7.74 (dd, 0,6H).
HRMS (ESI): рассчитано для C22H27N4O4S 443,1753 (М+Н)+, найдено 443, 1766.
ПРИМЕР 46
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[бензил(3-этокси-3-оксопропил)амино]карбонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 26.
1H ЯМР (500 МГц, CD3CN/D2O): δ м.д. 1.06 (t, 1H), 1.19 (t, 2H), 1.67-1.88 (m, 1H), 1.90-2.15 (m, 1H), 2.40-3.0 (m, 8H), 3.40-3.58 (m, 0,7H), 3.58-3.66 (m, 1,3H), 3.91 (q, 0,7H), 4.07 (q, 1,3H), 4.47 (s, 1,3H), 4.69 (s, 0,7H), 6.80-6.92 (m, 1H), 7.1-7.4 (m, 9Н), 7.46 (s, 0,7H), 7.50 (s, 0,3H), 7.60-7.74 (m, 1H). HRMS (ESI): рассчитано для C30H36N3O5S 550,2376 (M+H)+, найдено 550, 2361.
ПРИМЕР 47
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[(цианометил)(метил)амино]сульфонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с N-(цианометил)-3-йод-N-метилбензолсульфонамида. N-(Цианометил)-3-йод-N-метилбензолсульфонамид синтезировали из 3-йодбензолсульфонилхлорида с использованием стандартных методик.
1H ЯМР (500 МГц, CD3CN/D2O): δ 7.79 (dd, 0,5H), 7.76 (dd, 0,5H), 7.74-7.69 (m, 2Н), 7.64-7.54 (m, 3H), 6.95 (d, 0,5H), 6.94 (d, 0,5H), 4.29 (s, 2H), 3.11-3.00 (m, 2H), 2.86 (s, 3H), 2.98-2.78 (m, 4H), 2.20-2.09 (m, 1H), 1.95-1.83 (m, 1H). HRMS (ESI): рассчитано для
C20H25N2O4S2 449,1317 (М+Н)+, найдено 449, 1329.
ПРИМЕР 48
2-[(6-Аминопиридин-3-ил)метил]-5-(3-{[(2S)-2-(анилинометил)пирролидин-1-ил]сульфонил}фенил)-3-меркаптопентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с N-({(2S)-1-[(3-йодфенил)сульфонил]пирролидин-2-ил}метил)анилина. N-({(2S)-1-[(3-йодфенил)сульфонил]пирролидин-2-ил}метил)анилин синтезировали из 3-йодбензолсульфонилхлорида с использованием стандартных методик.
1H ЯМР (500 МГц, CD3OD): δ 7.71 (dd, J=2,1, 9,1 Гц, 1H), 7.59-7.45 (m, 7H), 7.31-7.29 (m, 3H), 6.89 (d, J=9,3 Гц, 1H), 3.83-3.75 (m, 1H), 3.53 (ddd, J=3,1, 6,0, 13,0 Гц, 1H), 3.44-3.36 (m, 2H), 3.26-3.18 (m, 1H), 3.00-2.70 (m, 6H), 2.05-1.97 (m, 1H), 1.82-1.65 (m, 3H), 1.57-1.50 (m, 1H), 1.42-1.32 (m, 1H). HRMS (ESI): рассчитано для С28Н34N4O4S2 555,2100 (М+Н)+, найдено 555, 2032.
ПРИМЕР 49
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-{3-[(метиламино)сульфонил]фенил}пентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с N-(2-фурилметил)-3-йод-N-метилбензолсульфонамида. N-(2-Фурилметил)-3-йод-N-метилбензолсульфонамид синтезировали из 3-йодбензолсульфонилхлорида с использованием стандартных методик.
1H ЯМР (500 МГц, CD3OD): δ 7.85 (dd, J=2,1, 9,1 Гц, 1H), 7.69-7.65 (m, 3H), 7.51-7.50 (m, 2H), 6.94 (dd, J=0,5, 9,1 Гц, 1H), 3.12-3.07 (m, 2H), 3.00-2.96 (m, 1H), 2.93-2.77 (m, 3H), 2.51 (s, 3H), 2.16-2.10 (m, 1H), 1.91-1.83 (m, 1H). HRMS (ESI): рассчитано для C18H23N3O4S2 410,1208 (M+H)+, найдено 410, 1207.
ПРИМЕР 50
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-(3-{[метил(2-фенилэтил)амино]сульфонил}фенил)пентановую кислоту синтезировали по методике, описанной для Примера 1, начиная с 3-йод-N-метил-N-(2-фенилэтил)бензолсульфонамида. 3-Йод-N-метил-N-(2-фенилэтил)бензолсульфонамид синтезировали из 3-йодбензолсульфонилхлорида с использованием стандартных методик.
1H ЯМР (400 МГц, CDCl3): δ 7.64 (s, 1Н), 7.54-7.57 (d, 3H), 7.39-7.40 (d, 3Н), 7.24-7.27 (t, 3Н), 7.14-7.20 (m, 3Н), 6.75 (s, 2H), 3.23-3.27 (t, 2H), 2.96-3.03 (m, 3H), 2.80-2.84 (t, 3Н), 2.72 (s, ЗН), 2.07 (s, 1H), 1.69-1.80 (dd, 1H), 1.53-1.55 (d, 1H). MS (ESI): 514.3 (M+H)+.
ПРИМЕР 51
Этот пример иллюстрирует получение 2-[(6-аминопиридин-3-ил)метил]-3-меркапто-5-[3-(тетрагидрофуран-3-илокси)фенил]пентановой кислоты
(а) трет-Бутил(3-йодфенокси)диметилсилан
Имидазол (7,8 г, 115 ммоль) добавляли к раствору 3-йодфенола (12,7 г, 58 ммоль) и трет-бутил(хлор)диметилсилана (9,9 г, 65 ммоль) в дихлорметане (80 мл) при 0°С. Реакционную смесь перемешивали при комнатной температуре в течение ночи. Суспензию три раза промывали водой и один раз солевым раствором, сушили и концентрировали с образованием неочищенного трет-бутил(3-йодфенокси)диметилсилана (20 г, 93%).
(б) трет-Бутил-2-({6-[(трет-бутоксикарбонил)
амино]пиридин-3-ил}метил)-5-(3-гидроксифенил)-3-[(4-метоксибензил)тио]пентаноат
Ледяную уксусную кислоту (190 мкл, 3,3 ммоль) добавляли к раствору трет-бутил-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-5-(3-{[трет-бутил(диметил)силил]окси}фенил)-3-[(4-метоксибензил)тио]пентаноата (800 мг, 0,89 ммоль, синтезированному в соответствии с методикой Примера 1, начиная с трет-бутил(3-йодфенокси)диметилсилана) в сухом THF (10 мл). Добавляли тетрабутиламмония фторида тригидрат (489 мг, 1,5 ммоль) и смесь перемешивали при комнатной температуре в течение 12 ч. Добавляли EtOAc (150 мл), раствор промывали насыщенным водным раствором NaHCO3, водой и солевым раствором, сушили и концентрировали. В результате флэш-хроматографии (CH2Cl2/EtOAc, 10:1) получали трет-бутил-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-5-(3-гидроксифенил)-3-[(4-метоксибензил)тио]пентаноат (660 мг, 98%).
(в) трет-Бутил-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-[3-(тетрагидрофуран-3-илокси)фенил]пентаноат
1,1'-Азо-бис-(N,N-диметилформамид) (134 мг, 0,78 ммоль) добавляли к раствору три-н-бутилфосфина (221 мкл, 0,89 ммоль) в толуоле (2 мл). Последовательно добавляли тетрагидрофуран-3-ол (36 мкл, 44 ммоль) и тзет-бутил-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-5-(3-гидроксифенил)-3-[(4-метоксибензил)тио]пентаноат (154 мг, 0,25 ммоль). Реакционную смесь перемешивали в течение 12 ч при 80°С. Добавляли толуол (100 мл), смесь промывали солевым раствором, сушили и концентрировали. В результате флэш-хроматографии (толуол/EtOAc, от 100:0 до 70:30) получали трет-бутил-2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-[3-(тетрагидрофуран-3-илокси)фенил]пентаноат (75 мг, 35%).
(г) 2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-
[3-(тетрагидрофуран-3-илокси)фенил]пентановая кислота
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-[3-(тетрагидрофуран-3-илокси)фенил]пентановую кислоту синтезировали в соответствии с методикой Примера 1, начиная с трет-бутилового эфира 2-({6-[(трет-бутоксикарбонил)амино]пиридин-3-ил}метил)-3-[(4-метоксибензил)тио]-5-[3-(тетрагидрофуран-3-илокси)фенил]пентаноат.
1H ЯМР (500 МГц, CD3CN/D2O (1:1)): δ 7.72 (dd, 1H), 7.53 (d, 1H), 7.22 (dd, 1Н), 6.90 (d, 1H), 6.83 (d, 1H), 6.76-6.72 (m, 2H), 4.98 (m, 1H), 3.93-3.79 (m, 4H), 2.99-2.84 (m, 3H), 2.83-2.66 (m, 3Н), 2.27-2.18 (m, 1H), 2.07-1.96 (m, 2H), 1.83-1.73 (m, 1H). HRMS (ESI): рассчитано для C21H27N2O4S 403,1692 (M+H)+, найдено 403,1698.
ПРИМЕР 52
2-[(6-Аминопиридин-3-ил)метил]-3-меркапто-5-[3-(тетрагидрофуран-3-илметокси)фенил]пентановую кислоту синтезировали в соответствии с методикой Примера 51.
1H ЯМР (400 МГц, CD3CN): δ 7.75-7.69 (d, 1H), 7.58-7.56 (s, 1H), 7.25-7.18 (m, 1Н), 6.88-6.75 (m, 4Н), 3.98-3.58 (m, 6Н), 3.10-3.00 (m, 1H), 2.95-2.82 (m, 3Н), 2.74-2.65 (m, 2H), 2.13-2.03 (m, 1H), 1.98-1.66 (m, 4H). MS (ESI): 417,9 (М+Н)+.
ПРИМЕР 53
Активность некоторых примеров в анализе, описанном в Dirk Hendriks, Simon Scharpé and Marc van Sande, Clinical Chemistry, 31, 1936-1939 (1985), представлена в таблице.
Сокращения
Схема 1

Схема 2
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПРОИЗВОДНЫЕ ФОСФИНАНОВ И АЗАФОСФИНАНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2017 |
|
RU2729641C2 |
| ЗАМЕЩЕННЫЙ 2-АМИНОПИРИДИН В КАЧЕСТВЕ ИНГИБИТОРА ПРОТЕИНКИНАЗЫ | 2014 |
|
RU2671212C2 |
| ЦИКЛОАЛКЕНИЛАРИЛЬНЫЕ ПРОИЗВОДНЫЕ ДЛЯ ИНГИБИРОВАНИЯ ТРАНСПОРТНОГО БЕЛКА ХОЛЕСТЕРИНОВЫХ ЭФИРОВ | 2012 |
|
RU2597266C2 |
| СПОСОБ СИНТЕЗИРОВАНИЯ НОВОГО ХИРАЛЬНОГО ЛИГАНДА, ХЕЛАТА МЕТАЛЛА, РАЗЛИЧНЫХ НЕПРИРОДНЫХ АМИНОКИСЛОТ, МАРАВИРОКА И ЕГО ОСНОВНЫХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ | 2017 |
|
RU2727723C1 |
| ЗАМЕЩЕННЫЕ ТРИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБ ПРИМЕНЕНИЯ | 2016 |
|
RU2744766C2 |
| ТИАЗОЛИЛФЕНИЛБЕНЗОЛСУЛЬФОНАМИДОПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2012 |
|
RU2606497C2 |
| Соединения, полезные в качестве пестицидов, и промежуточные соединения, композиции и способы, связанные с ними | 2016 |
|
RU2821715C2 |
| МОЛЕКУЛЫ С ПЕСТИЦИДНОЙ ФУНКЦИЕЙ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ, СВЯЗАННЫЕ С НИМИ | 2016 |
|
RU2735602C2 |
| ПРОИЗВОДНОЕ ЦИКЛОПЕНТИЛАКРИЛАМИДА | 2009 |
|
RU2565070C2 |
| ИНДОЛОПИРРОЛОКАРБАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ САХАРОВ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ РОСТА ОПУХОЛЕЙ | 1997 |
|
RU2167880C2 |
Описывается соединение, представляющее собой 2,5-дизамещенную 3-меркаптопентановую кислоту формулы (I) или ее фармацевтически приемлемую соль, где R1 представляет собой фенил, возможно замещенный, нафтил, пиридинил, 1,2,3,4-тетрагидропиримидин-2,4-дионил, замещенный С1-4алкилом, или тетрагидротиенил; R2 представляет собой аминопиридинил, аминотиазолил или 3-азабицикло[3.2.1]октил; R3 представляет собой С1-4алкокси, возможно замещенный фенилом (замещенным галогеном) или пиридинилом; NR5R6 или N-связанное 5- или 6-членное гетероциклическое кольцо, представляющее собой пирролидинильное, пиперидинильное или пиперазинильное кольцо, незамещенное или монозамещенное, или конденсированное с бензольным кольцом, которое возможно замещено C1-4алкокси; R4 представляет собой N-связанное пирролидинильное кольцо, монозамещенное
C1-4алкилом, который замещен NHфенилом; R5 и
R6 независимо представляют собой водород, C1-4алкил, возможно замещенный, или C2-4алкенил, и способ его получения. Соединения ингибируют карбоксипептидазу и их можно применять в профилактике и лечении болезней, где ингибирование карбоксипептидазы и является полезным. 2 н. и 5 з.п. ф-лы, 1 табл.
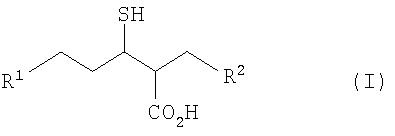
1. Соединение, представляющее собой 2,5-дизамещенную 3-меркаптопентановую кислоту формулы (I)
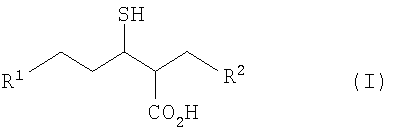
где R1 представляет собой фенил {возможно замещенный галогеном, гидрокси, циано, C1-4алкилом (который возможно монозамещен циано, гидрокси или фенилом), C1-4алкокси (который возможно замещен тетрагидрофуранилом), CF3, OCF3, метилендиокси, C(O)R3, S(O)2NH2, S(O)2NН(С1-4алкил), S(O)2N(C1-4алкил)2 (причем алкил замещен циано или фенилом), S(O)2R4, фенилом, фенокси (который замещен галогеном) или тетрагидрофуранилокси}, нафтил, пиридинил, 1,2,3,4-тетрагидропиримидин-2,4-дион-ил (замещенный C1-4алкилом) или тетрагидротиенил;
R2 представляет собой аминопиридинил, аминотиазолил или 3-азабицикло[3.2.1]октил;
R3 представляет собой гидрокси, C1-4алкокси (который возможно замещен фенилом (замещенным галогеном) или пиридинилом), NR5R6 или N-связанное 5- или 6-членное гетероциклическое кольцо, представляющее собой пирролидинильное, пиперидинильное или пиперазинильное кольцо {незамещенное или монозамещенное гидрокси, оксо, C1-4алкилом (который замещен гидрокси), группой CO2(C1-4алкил) или фенилом (который замещен галогеном); или конденсированное с бензольным кольцом, которое возможно замещено C1-4алкокси};
R4 представляет собой N-связанное пирролидинильное кольцо, монозамещенное
C1-4алкилом (который замещен NHфенилом);
R5 и R6 независимо представляют собой водород, C1-4алкил {возможно замещенный галогеном, циано, гидрокси, фенилом (который возможно замещен метилендиокси) или группой CO2(C1-4алкил)} или C2-4алкенил;
при условии, что когда R2 представляет собой 6-аминопиридин-3-ил, тогда R1 представляет собой замещенный фенил, нафтил, пиридинил, 1,2,3,4-тетрагидропиримидин-2,4-дион-ил (замещенный C1-4алкилом) или тетрагидротиенил;
или его фармацевтически приемлемая соль.
2. Соединение формулы (I) по п.1, где R1 представляет собой фенил {возможно замещенный галогеном, гидрокси, циано, C1-4алкилом (который возможно монозамещен циано или гидрокси), C1-4алкокси, CF3, OCF3, метилендиокси, C(O)NH2, S(O)2NH2 или фенилом}, пиридинил или тетрагидротиенил.
3. Соединение формулы (I) по п.1, где R1 представляет собой фенил {возможно замещенный галогеном, гидрокси, циано, C1-4алкилом (который возможно монозамещен циано, гидрокси или фенилом), C1-4алкокси, CF3, OCF3, метилендиокси, фенокси (который замещен галогеном) или тетрагидрофуранилокси}, нафтил, пиридинил или тетрагидротиенил.
4. Соединение формулы (I) по п.1, где R1 представляет собой фенил {замещенный галогеном, гидрокси, циано, C1-4алкилом (который возможно монозамещен циано или гидрокси), C1-4алкокси, CF3 или метилендиокси} или тетрагидротиенил.
5. Соединение формулы (I) по пп.1, 2, 3 или 4, где R2 представляет собой 6-аминопиридин-3-ил, 2-аминотиазол-5-ил или 3-азабицикло[3.2.1]окт-8-ил.
6. Соединение формулы (I) по пп.1, 2, 3 или 4, где R2 представляет собой 6-аминопиридин-3-ил.
7. Способ получения соединения формулы (I), включающий взаимодействие соединения формулы (II):
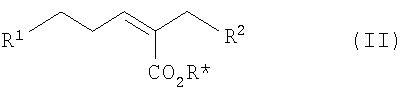
где R1 такой, как определено в п.1, или содержит группу, которую впоследствии можно подвергнуть взаимодействию с образованием группы R1, R* является подходящей защитной группой, и R2 такой, как определено в п.1, или аминная функция R2 может быть защищена, с тиолом формулы L-SH, где L является подходящей защитной группой, в присутствии подходящего катализатора и в подходящем растворителе, с образованием соединения формулы (III)
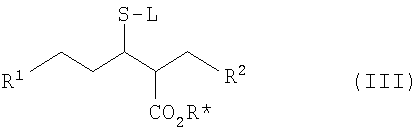
и, возможно, взаимодействие функциональной группы в R1, и последующее удаление защитных групп, если это необходимо.
| Способ улавливания самородков золота и платины из россыпных месторождений | 1939 |
|
SU66557A1 |
Авторы
Даты
2009-08-27—Публикация
2003-06-10—Подача