Изобретение относится к медицине, в частности к педиатрии. Способ основан на использовании простого и малоинвазивного метода выявления митохондриальной недостаточности и нарушений клеточной биоэнергетики у детей с недифференцированными формами задержки нервно-психического и физического развития на основании цитохимического анализа активности ферментов энергетического обмена в лейкоцитах периферической крови. Отсутствие адекватных, относительно простых и малотравматичных методов исследования до настоящего времени тормозило создание диагностических программ, направленных на раннее выявление наследственных нарушений биоэнергетического обмена у детей. Техническая сложность, высокая стоимость и инвазивность некоторых диагностических методов, принятых в мировой практике в качестве стандартных способов диагностики нарушений клеточной энергетики [в частности, биопсии скелетной мышцы (прототип) (Клембовский А.И., Сухоруков В.С. Митохондриальная недостаточность у детей. Арх. патол. 1997; 59:5:3-7) и молекулярно-генетического анализа], затрудняет их использование для ранней диагностики митохондриальной патологии, лабораторного контроля над динамикой состояния больных, определения ожидаемого клинического эффекта терапии митохондриальных нарушений у детей.
Целью разработки способа и изобретения является получение адекватной информации о состоянии энергетического обмена посредством минимального количества материала, необходимого для исследования, то есть обеспечивающего щадящие (малоинвазивные) условия обследования больного.
Цитохимический анализ ферментного статуса дегидрогеназ лимфоцитов периферической крови (сукцинатдегидрогеназы, альфаглицерофосфатдегидрогеназы, глутаматдегидрогеназы, лактатдегидрогеназы и малатдегидрогеназы) предлагается как метод ранней диагностики митохондриальной недостаточности. Данные энзимы занимают ключевые позиции в аэробном и анаэробном энергообеспечении клетки и снижение их активности является маркером митохондриальной дисфункции.
Способ информативен, полученные результаты адекватно отражают состояние процессов клеточного энергообмена. Доказательством адекватности применения морфометрического анализа лимфоцитов при митохондриальных болезнях является установленная корреляция функциональной активности митохондрий лимфоцитов с тестом RRF ("рваные" красные волокна) в биоптатах мышц.
Показаниями к применению метода цитохимического анализа являются: недифференцированная задержка статико-моторного, психоречевого и физического развития; респираторный и нейродистресс-синдромы в раннем возрасте; повышенная утомляемость, мышечная слабость и гипотония, непереносимость физической нагрузки, птоз, офтальмоплегия, боли в мышцах, судороги, миоклонии, атаксия, нистагм, головные боли, спастические парезы, периферическая нейропатия; повторная рвота, не связанная с приемами пищи; нарушения сердечного ритма, кардиомиопатия (дилатационная или гипертрофическая); снижение зрения: пигментный ретинит, атрофия зрительного нерва; тугоухость; почечные тубулярные нарушения; нарушение функции печени; особенности генеалогии (наличие аналогичных случаев патологии у сибсов и других родственников; выкидыши, мертворождения у матери пробанда); повышенный уровень молочной и пировиноградной кислот в крови натощак. Противопоказаниями к применению метода цитохимического анализа являются: прием пациентом витаминов, кофакторов метаболических реакций (пантотенат или пангамат кальция, оротат калия, липамид или липоевая кислота, фолиевая кислота и др.), стимуляторов энергетического обмена (янтарная кислота, препараты карнитина, коэнзим Q и др.), гормональных препаратов (L-тироксин и др.), некоторых антиконвульсантов (производные вальпроевой кислоты, фенобарбитал), хлорамфеникола (левомицетин), некоторых антидепрессантов и анальгезирующих средств; острые воспалительные заболевания или хронические болезни в стадии обострения или неполной ремиссии. При условии наличия одного из этих факторов необходимо указывать это в сопроводительном документе.
Материально-техническое обеспечение метода: световой микроскоп; микроскоп с видеокамерой; предметные стекла; покровные стекла; одноразовые скарификаторы; дистиллированная вода; фиксатор (ацетон-трилон); весы; термостат; наборы реактивов фирмы ООО МНПК "Химтехмаш", ГосНИИ "ИРЕА"; компьютер; программа "Видеотест".
Цитохимическое выявление активности митохондриальных ферментов осуществляли наборами реактивов фирмы ООО МНПК "Химтехмаш", ГосНИИ "ИРЕА": сукцинатдегидрогеназы (СДГ), α-глицерофосфатдегидрогеназы (α-ГФДГ), глутаматдегидрогеназы (ГДГ), малатдегидрогеназы (МДГ), лактатдегидрогеназы (ЛДГ) лейкоцитов периферической крови (метод Пирса (1957) в модификации Р.П.Нарциссова (1986) с последующей визуальной и компьютерной морфометрией (пакет программ "Видеотест", методика B.C.Сухорукова, Е.В.Тозлиян). Ферментативная активность при визуальной морфометрии выражалась в условных единицах, соответствующих среднему числу гранул формазана, являющегося продуктом цитохимической реакции. С помощью последующей компьютерной телеметрии определяли количество депозитов, их площадь, интервал яркости (разнородность), среднюю оптическую плотность, интегральную оптическую плотность гранул.
В качестве контрольных использовались параметры исследуемых ферментов, полученные при проведении морфометрического анализа у 55 практически здоровых детей.
Для мазка на предметные стекла (5 стекол - 5 ферментов) необходимо 5 капель крови из пальца. Стекла маркируются, фиксация мазков производится в ацетон-трилоне в течение 40 секунд - 1 минуты, после высыхания (около 20 минут) образцы опускаются в бюксы с соответствующим реактивом и ставятся на 1 час в термостат или на водяную баню. Затем дважды промываются в чистой воде и сушатся.
В световом микроскопе подсчитывается количество гранул в 30-50 клетках (малых лимфоцитов) и выводится средняя количественная оценка (активность фермента в условных единицах, среднее количество гранул в лимфоците, гр/лф., оцениваются также качественные параметры гранул (форма, размеры, распределение, интенсивность окрашивания, тенденция к кластерообразованию).
Балльная оценка качественных параметров гранул при визуальной оценке представлена в таблице 1.
Введение балльной системы было необходимо для оценки тяжести проявлений и последующей статистической обработки полученных данных.
Для компьютерной морфометрии мазки заключаются под покровные стекла (для этого используется разогретый желатиновый раствор). Методом компьютерного анализа оцениваются следующие параметры: площадь гранул, эллипс, интервал яркости, средняя оптическая плотность, интегральная оптическая плотность по всем гранулам, мелким, средним, кластерам 5-ти определяемых ферментов.
Так как в литературе отсутствуют данные по морфометрическим показателям исследуемых нами ферментов у здоровых детей разного возраста, нами исследована активность сукцинатдегидрогеназы, α-глицерофосфатдегидрогеназы, глутаматдегидрогеназы, малатдегидрогеназы, лактатдегидрогеназы по возрастам. Результаты представлены в таблице 2. Эти данные необходимы для проведения сравнительного анализа между результатами у исследуемого пациента и нормой и вывода заключения о наличии или отсутствии нарушений в активности ферментов энергетического обмена у данного пациента.
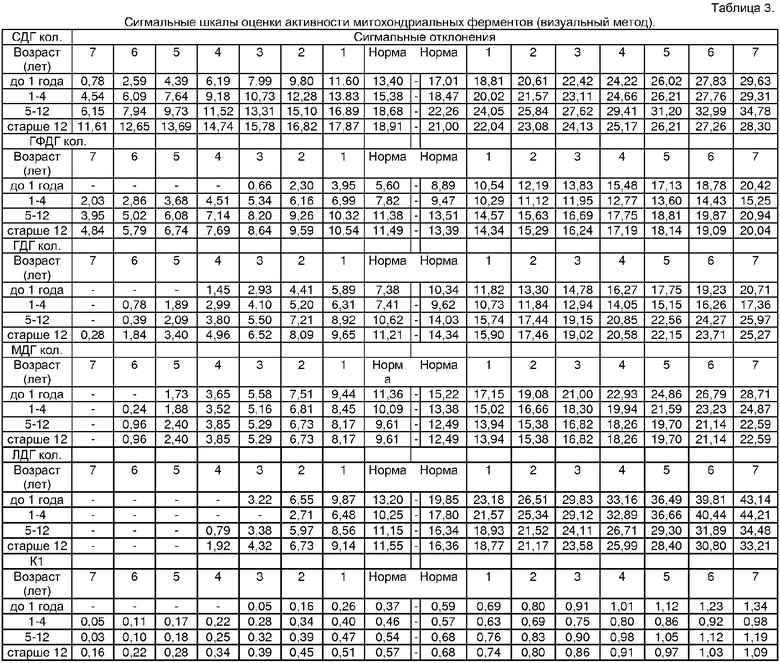
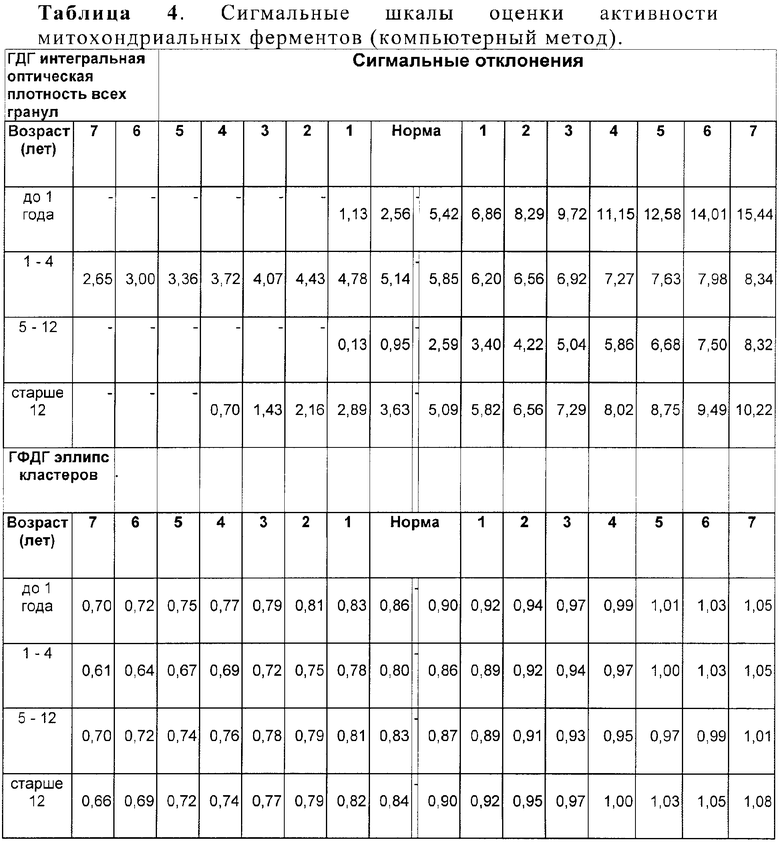
Для удобства интерпретации результатов морфометрического анализа активности митохондриальных ферментов нами предложены сигмальные таблицы: для визуального метода (таблица 3) и для компьютерного метода (таблица 4), а также формулы расчета митохондриального цитохимического коэффициента и таблицы вероятностей для каждого метода.
В группу сравнения (контрольная группа) вошли 55 здоровых детей. Дети этой группы были отобраны на педиатрическом приеме в день здорового ребенка в детской поликлинике. Возраст детей колебался от 1 месяца до 18 лет.
Для оценки диагностической ценности морфометрического метода использовался математический анализ (непараметрические методы, в частности анализ соответствий (или частотных таблиц), метод дискриминантных функций, корреляционный и факторный анализ). Диагностическая ценность визуального метода составляет 86%, а компьютерного анализа активности митохондриальных ферментов - 93%.
Подозрение на наличие митохондриальной недостаточности должны вызывать следующие изменения параметров морфометрического исследования (критерии разработаны в научно-исследовательской лаборатории общей патологии под руководством B.C.Сухорукова, в МНИИ педиатрии и детской хирургии):
- сочетанное снижение количества гранул определяемых ферментов (сукцинатдегидрогеназы, α-глицерофосфатдегидрогеназы, глутаматдегидрогеназы, малатдегидрогеназы, лактатдегидрогеназы) и выраженное кластерообразование (патологическое скопление большого количества гранул (митохондрий) у одного из полюсов клетки;
- изолированное снижение количества гранул одного из ключевых ферментов аэробного обмена - сукцинатдегидрогеназы и повышение количества гранул ключевого фермента анаэробного обмена лактатдегидрогеназы ;
- сочетанное снижение количества гранул α-глицерофосфатдегидрогеназы и глутаматдегидрогеназы ;
- изменение качественных параметров гранул изучаемых ферментов по результатам визуальной оценки (нарушение распределения гранул в клетке, изменение формы и размера гранул, наличие кластеров);
- сочетанное изменение параметров по результатам компьютерной морфометрии (снижение средней оптической плотности гранул, увеличение площади мелких и средних гранул, увеличение площади кластеров, уменьшение эллипса мелких и средних гранул, снижение интервала яркости мелких гранул; сочетанное изменение вышеперечисленных параметров) определяемых ферментов;
- выраженное повышение количества гранул сукцинатдегидрогеназы, α-глицерофосфатдегидрогеназы, глутаматдегидрогеназы, малатдегидрогеназы (при отсутствии признаков инфекционно-воспалительного процесса, хронической инфекции в стадии обострения или неполной ремиссии);
- снижение количества гранул сукцинатдегидрогеназы и повышение количества гранул α-глицерофосфатдегидрогеназы ;
- повышение оптических характеристик по всем гранулам определяемых ферментов.
С целью объективной оценки вышеперечисленных изменений морфометрических параметров с помощью методов математического анализа выделены наиболее значимые, на основании чего был разработан митхондриальный цитохимический коэффициент, предложена формула для его расчета (варианты).
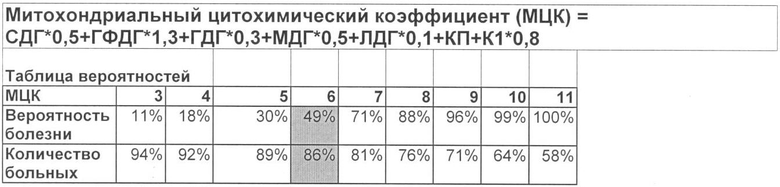
Условные обозначения: СДГ - количество сигнальных отклонений количественного признака фермента сукцинатдегидрогеназы (определяется в соответствии с представленной таблицей), ГФДГ - количество сигмальных отклонений количественного признака фермента α-глицерофосфатдегидрогеназы (определяется в соответствии с представленной таблицей), ГДГ - количество сигмальных отклонений количественного признака фермента глутаматдегидрогеназы (определяется в соответствии с представленной таблицей), МДГ - количество сигмальных отклонений количественного признака фермента малатдегидрогеназы (определяется в соответствии с представленной таблицей), ЛДГ - количество сигмальных отклонений количественного признака фермента лактатдегидрогеназы (определяется в соответствии с представленной таблицей), КП - качественные параметры (в соответствии с балльной оценкой, таблица 1), К1 - коэффициент 1 (ГФДГ/СДГ- соотношение активности α-глицерофосфатдегидрогеназы к сукцинатдегидрогеназе) - определяется в соответствии с представленной таблицей.
Прогнозирование заболевания:
МЦК до 3 - диагноз маловероятен;
МЦК от 3 до 6 - диагноз вероятен;
МЦК более 6 - вероятность заболевания высока (более 50 %).
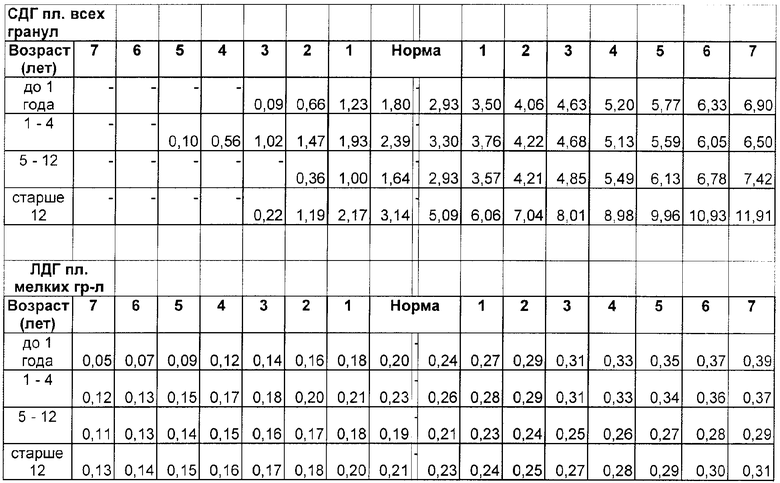
Условные обозначения: СДГпл.все - сукцинатдегидрогеназа площадь всех гранул в сигмах по таблице, ГФДГэлл.кл. - глицерофосфатдегидрогеназа эллипс кластеров в сигмах по таблице, ГДГинт.опт.пл.в. - глутаматдегидрогеназа интегральная оптическая плотность всех гранул в сигмах по таблице, ЛДГпл.мелк. - лактатдегидрогеназа площадь мелких гранул в сигмах по таблице.
Прогнозирование заболевания:
МЦК до 3 - диагноз маловероятен;
МЦК от 3 до 3,2 - диагноз вероятен;
МЦК более 3,2 - вероятность заболевания высока (более 50%).
Таким образом, определяют активность ферментов сукцинатдегидрогеназы, глицерофосфатдегидрогеназы, глутаматдегидрогеназы, малатдегидрогеназы, лактатдегидрогеназы в условных единицах, соответствующих среднему числу гранул формазана, вычисляют соотношение активности глицерофосфатдегидрогеназы к активности сукцинатдегидрогеназы, определяют величину сигмального отклонения количественного признака активности каждого из вышеперечисленных ферментов и соотношения активности глицерофосфатдегидрогеназы к активности сукцинатдегидрогеназы с учетом возраста в соответствии с разработанной таблицей № 3; определяют качественные показатели (КП) гранул в баллах: 0 - не изменены, т.е.отсутствуют кластеры, нормальная форма и размер гранул, нормальное распределение гранул; 1 - умеренные изменения, т.е.единичные кластеры, наличие мелких гранул, нарушение распределения гранул в некоторых клетках; 2 - выраженные изменения, т.е. кластерообразование, обилие мелких гранул, выраженные нарушения распределения гранул во всех клетках; исходя из полученных данных определяют суммарный морфометрический показатель - митохондриальный цитохимический коэффициент (МЦК) по формуле
СДГ*0,5+ГФДГ*1,3+ГДГ*0,3+МДГ*0,5+ЛДГ*0,1+КП+К1*0,8,
где СДГ, ГФДГ, ГДГ, МДГ, ЛДГ - величины сигмальных отклонений активности каждого из ферментов, соответственно, определенные в соответствии с таблицей № 3;
K1 - коэффициент, равный величине сигмального отклонения соотношения активности глицерофосфатдегидрогеназы к активности сукцинатдегидрогеназе, определенный в соответствии с таблицей №3;
КП - качественные параметры в баллах.
По увеличению показателя МЦК судят об увеличении вероятности развития митохондриального заболевания, при этом при значениях МЦК до 3 - диагноз маловероятен (до 11%); при значениях МЦК от 3 до 6 - диагноз вероятен (11-49%); при значениях МЦК более 6 - вероятность заболевания высока (более 50 %).
С помощью компьютерного морфометрического анализа активности ферментов биоэнергетического обмена лимфоцитов периферической крови определяют: показатель площади всех гранул фермента сукцинатдегидрогеназы, показатель эллипса кластеров фермента глицерофосфатдегидрогеназы, интегральную оптическую плотность всех гранул фермента глутаматдегидрогеназы, площадь мелких гранул фермента лакататдегидрогеназы; определяют величину сигмального отклонения соответствующего показателя каждого из вышеперечисленных ферментов с учетом возраста в соответствии с разработанной таблицей №4, исходя из полученных данных определяют суммарный морфометрический показатель - митохондриальный цитохимический коэффициент (МЦК) по формуле:
СДГпл.все*0,5+ГФДГэлл.кл.*0,7+ГДГинт.о.пл.в.*2,1+ЛДГпл.мелк.*0,8, где СДГпл.все, ГФДГэлл.кл., ГДГинт.опт.пл.в., ЛДГпл.мелк. - величины сигмальных отклонений каждого из соответствующих показателей вышеперечисленных ферментов, определенные в соответствии с таблицей №4,
По увеличению показателя МЦК судят об увеличении вероятности развития митохондриального заболевания, при этом при значениях МЦК до 3 - диагноз маловероятен (до 34%); при значениях МЦК от 3 до 3,2 - диагноз вероятен (34-48%); при значениях МЦК более 3,2 - вероятность заболевания высока (более 50 %).
Таким образом, митохондриальный цитохимический коэффициент (МЦК) - это суммарный морфометрический показатель, получаемый при анализе цитохимической активности митохондриальных ферментов, указывающий на вероятность наличия у данного пациента нарушений клеточной биоэнергетики.
Эффективность использования метода
В отделении врожденных и наследственных заболеваний Московского НИИ педиатрии и детской хирургии Росздрава было осмотрено 135 детей с недифференцированной задержкой нервно-психического и нарушениями физического развития. Возраст детей колебался от 4 месяцев до 18 лет. На основании наличия недифференцированной задержки нервно-психического и физического развития в сочетании с повышенной утомляемостью, мышечной слабостью и гипотонией, особенностями анамнеза и генеалогии, повышенным уровнем молочной и пировиноградной кислот в крови натощак, было выделено 100 детей, которым для установления диагноза было проведено морфометрическое исследование активности ферментов энергетического обмена и комплексное клинико-лабораторное обследование.
На основании результатов комплексного обследования все дети были разделены на 3 группы. В первую группу вошло 30 детей с митохондриальными заболеваниями и органическими ацидемиями, в том числе: с синдромами MELAS (n=2), Кернса-Сейра (n=5), DIDMOAD (нейросенсорная глухота, атрофия зрительных нервов, ювенильный сахарный диабет, несахарный диабет, n=1), Барта (задержка роста, психомоторного развития, миопатический синдром, кардиомиопатия, n=1), неклассифицированной митохондриальной энцефаломиопатией (n=14), изовалериановой (n=1), метилмалоновой (n=1), 3-гидрокси-3-метилглутаровой ацидемией (n=1) и болезнями окисления жирных кислот (n=4).
Вторую группу составили 19 детей с наследственными заболеваниями, сопровождающимися нарушениями нервно-психического и физического развития и признаками митохондриальных нарушений: синдромами Элерса-Данлоса (n=4), Марфана (n=3); тапеторетинальной абиотрофией (n=5), синдромами Ретта (n=4), Лоу (n=1), Аарскога (n=1), галактоземией (n=1).
В 3-ю группу вошел 51 ребенок, у которого при обследовании не было установлено признаков митохондриальной дисфункции. Из них у 24-х нарушения в нервно-психическом и физическом развитии были обусловлены последствиями неблагоприятного течения беременности и родов. У остальных детей были диагностированы: алкогольная эмбриофетопатия, лейкоэнцефалит, некоторые наследственные нервно-мышечные заболевания.
Большая часть детей (68%) была старше 5 лет. Соотношение мальчиков и девочек примерно одинаково.
Характеристика параметров цитохимического анализа активности ферментов энергетического обмена в разных группах обследованных детей в возрасте 5-15 лет представлена в таблице 5.
Активность сукцинатдегидрогеназы у детей с митохондриальными энцефаломиопатиями была достоверно снижена по сравнению с группой здоровых детей (р<0,05), у детей с органическими ацидемиями достоверно снижена по сравнению с группой немитохондриальных больных (р<0,002) и группой здоровых детей (р<0,024). Среднее значение активности сукцинатдегидрогеназы в группе детей с митохондриальными энцефаломиопатиями достоверно выше, чем у детей с органическими ацидемиями. Это связано с гетерогенностью данной группы, в которую входили больные с патологически высокими показателями сукцинатдегидрогеназы (у 2 детей с синдромом Кернса-Сейра). Повышение активности сукцинатдегидрогеназы, по-видимому, служит отражением компенсаторной реакции митохондрий на дефект энергетического обмена.
Во 2-й группе достоверное снижение активности сукцинатдегидрогеназы по сравнению с группой немитохондриальных больных и здоровых было характерно для детей с синдромом Марфана (р<0,001) и тапеторетинальной абиотрофией (р<0,05).
Активность глицерофосфатдегидрогеназы и глутаматдегидрогеназы у детей в I группе была достоверно снижена (р<0,05), а активность лактатдегидрогеназы достоверно повышена по сравнению с показателями у детей в Ш и IV группах, что указывало на компенсаторную активацию гликолиза в условиях снижения энергетически выгодных процессов аэробного обмена. Во II группе отмечались сходные изменения: достоверное снижение активности α-глицерофосфатдегидрогеназы при повышении лактатдегидрогеназы (по среднему групповому значению). Обращало внимание, что у детей с синдромом Ретта активность сукцинатдегидрогеназы не отличалась от таковой в группе контроля, в то время как активность а-глицерофосфатдегидрогеназы и глутаматдегидрогеназы была достоверно снижена по сравнению с показателями в Ш и IV группах. Эти изменения свидетельствуют о нарушении процессов клеточного энергообмена, менее выраженных, чем у детей I группы и при некоторых нозологический формах во II группе, и, вероятно, являющихся вторичными.
Распределение детей, показавших положительный результат при цитохимическом анализе, в зависимости от данных комплексного обследования представлено в таблице 6.
Нами проведен сравнительный анализ различных методов выявления нарушений клеточной биоэнергетики. Для подсчета показателей чувствительности и специфичности морфометрического метода на основе комплексного клинико-биохимического и морфологического обследования как эталонного были использованы следующие подходы: чувствительность определялась как отношение числа положительных результатов к общему числу комплексно доказанных случаев митохондриальной недостаточности и нарушений биоэнергетического обмена; специфичность определялась как отношение числа отрицательных результатов к общему числу больных без митохондриальной недостаточности и нарушений биоэнергетического обмена по данным комплексного обследования. Сравнительная характеристика различных методов представлена в таблице 7.
В таблице 7. представлена сравнительная характеристика различных методов выявления признаков митохондриальной недостаточности в лимфоцитах периферической крови и биоптатах скелетной мышцы.
Чувствительность визуальной морфометрии составляет приблизительно 98%, специфичность - 86%, специфичность компьютерной мофометрии выше 91%. Диагностическая значимость методов 86% и 93% соотвественно.
Таким образом, на основании проведенного исследования у 49% детей с недифференцированными формами задержки нервно-психического и физического развития была выявлена митохондриальная недостаточность, наличие которой было подтверждено результатами последующего комплексного обследования.
Разработанный способ (варианты), основанный на цитохимическом анализе активности ферментов энергетического обмена, может быть использован с целью прогнозирования митохондриальных нарушений у детей с недифференцированными формами задержки нервно-психического и физического развития.
Следующие клинические примеры приводятся в подтверждение работоспособности способа, его клинической ценности. Примеры приведены для случаев с выявленной высокой вероятностью митохондриальной неостаточности. В случаях с малой и средней вероятностью также были получены достоверные результаты, которые затем были подтверждены более глубоким обследованием.
Клиническое наблюдение 1.
Анастасия Л., 16 лет, история болезни N 4067. Поступила в отдел врожденных и наследственных заболеваний у детей с нарушениями психики с жалобами на снижение зрения, нарушения памяти и речи, двигательные расстройства.
Из анамнеза жизни: девочка от 1 беременности, протекавшей на фоне пиелонефрита. Роды срочные, стремительные (5 часов). Состояние при рождении было удовлетворительным. Масса 3 кг; длина тела 50 см. Раннее психомоторное и речевое развитие - по возрасту. Младший сибс пробанда, 12 лет- здоров. Родословная отягощена (рисунок 15): двоюродный сибс (девочка, 3 года) по линии матери - страдает судорожным синдромом. Мать пробанда предъявляет жалобы на частые мигренеподобные головные боли.
Из анамнеза заболевания: первые признаки появились в 13 лет, изменилась походка (по типу "утиной"), девочка стала часто падать, появилась мышечная слабость, быстрая утомляемость, резко снизилась острота зрения, появились трудности в обучении, речевые расстройства, снизилась память.
При осмотре физическое развитие среднее, дисгармоничное (избыток массы тела 1 степени), индекс Дю Ранта-Лайнера 125 (норма 89-110), что соответствовало ожирению 1 степени. Обращала внимание диффузная гипотония, признаки дистонии мышц конечностей. При неврологическом обследовании выявлялись патологические стопные знаки, интенция при выполнении координаторных проб, неустойчивость в пробе Ромберга, атактическая походка. При биохимическом исследовании отмечались повышенные уровни молочной и пировиноградной кислот в сыворотке крови натощак (2,2 ммоль/л и 0,11 ммоль/л, соответственно).
Ребенку было проведено цитохимическое исследование активности ферментов энергетического обмена (визуальный и компьютерный метод). Было выявлено резкое снижение активности сукцинатдегидрогеназы, α-глицерофосфатдегидрогеназы, глутаматдегидрогеназы и малатдегидрогеназы (снижение количества гранул, уменьшение эллипса гранул, увеличение площади мелких гранул, увеличение количества кластеров, снижение средней оптической плотности по всем гранулам). Активность лактатдегидрогеназы была повышена (увеличение количества гранул и резкое повышение средней оптической плотности по всем гранулам).
Компьютерный метод морфометрического анализа выявил: СДГпл.вс.гр. - 9,9 (что составило в соответствии с таблицами 5 сигмальных отклонений); ГФДГэл.кл. - 0,96 (соответственно - 3 сигмальных отклонения); ГДГинт.опт.пл.вс.гр. - 1,8 (3 сигмальных отклонения); ЛДГпл.мелких гр. - 0,29 (5 сигмальных отклонений).
Рассчитываем МЦК в соответствии с формулой:
5×0,5+3×0,7+3×2,1+5×0,8=14,9
МЦК=14,9
Митохондриальный цитохимический коэффициент составил 14,9 баллов. Вероятность болезни (нарушений клеточной биоэнергетики) у пробанда, согласно разработанным таблицам, около 100%.
Ребенку на основании результатов цитохимического анализа активности ферментов энергетического обмена для уточнения диагноза было рекомендовано провести комплексное обследование.
Данные лабораторных и функциональных исследований. Клинические анализы крови и мочи без особенностей. Исследование равновесия кислот и оснований крови выявило нормальный показатель рН крови 7,39 (норма 7,34-7,45), при снижении парциального давления кислорода до 69 мм рт.ст. (норма 80,0-100,0). Дефицита оснований не обнаружено (BE 1,4 ммоль/л).
В биохимическом анализе крови основные показатели обмена белков, липидов, электролитов не нарушены.
При проведении нагрузочных тестов с глюкозой было выявлено патологическое повышение уровня молочной и пировиноградной кислот в сыворотке крови через 1 и 3 часа (2,6 ммоль/л и 2,8 ммоль/л, 0,11 и 0,14 ммоль/л, соответственно).
Исследование перекисного окисления липидов выявило повышение уровня гидроперекисей - 2,2 (норма 1,56-2 отн.ед/мл), снижение антиокислительной активности плазмы -26 (норма 30-40%).
На ЭКГ - синусовая брадиаритмия, неполная блокада правой ветви пучка Гиса.
На ЭЭГ выявлены умеренные признаки регуляторных нарушений в структурах мезо-диэнцефального уровня.
При офтальмоскопии глазного дна установлена частичная атрофия зрительных нервов.
При МРТ-исследовании головного и спинного мозга патологических изменений не выявлено.
Световая микроскопия мышечной ткани не выявила патологических изменений. Однако, при электронно-микроскопическом анализе были обнаружены выраженные изменения в виде деструкции крист митохондрий, их вакуолизации.
Комплексный анализ результатов обследования пробанда (генеалогического, клинического и лабораторного) позволил подтвердить предположительный по результатам цитохимического анализа активности митохондриальных ферментов диагноз о наличии у ребенка митохондриальной патологии, в конкретном случае неклассифицированной формы митохондриальной энцефаломиопатии. Диагноз был установлен на основании совокупности полученных данных:
- наличие у матери и родственников по материнской линии клинических признаков патологии типа митохондриальной энцефаломиопатии;
- манифестация болезни у пробанда после 6-летнего возраста;
- прогрессирующий характер заболевания;
- особенности клинической симптоматики: плохая переносимость физической нагрузки, проявления энцефаломиопатии в виде слабости, утомляемости, диффузной мышечной гипотонии с признаками дистонии мышц конечностей, координаторных расстройств, атактической походки, нарушений речи, снижения памяти, нарушения интеллектуального и физического развития, а также снижения зрения;
- особенности биохимических нарушений - повышение уровня молочной и пировиноградной кислот в крови натощак и после нагрузки глюкозой, нарушение перекисного окисления липидов, что служит признаком энергетической недостаточности, характерным для митохондриальной патологии;
- результаты цитохимического анализа: снижение активности ферментов аэробного обмена, компенсаторная активация гликолиза;
- выраженные морфологические признаки митохондриальных нарушений: наличие патологически измененных митохондрий.
Ребенку была назначена комплексная терапия, включающая препараты янтарной кислоты (янтавит 50 мг/сут по схеме: 3 дня "+" 1 день "-"), карнитина (Элькар 20% раствор по 3,0 мл 2 раза в день), коэнзим Q10 300 мг/сут, цитохром С 4,0 мл внутримышечно 10 инъекций 2 курса с 2-недельным интервалом, витамин С 100 мг/сут и антиоксиданты (аевит 100 мг/сут). Через 3 месяца, на фоне адекватно подобранной терапии, отмечалась положительная динамика в клиническом статусе (уменьшилась слабость, улучшились координация движений, речь, настроение, эмоциональная активность и контакт ребенка с окружающими), со стороны биохимических (снижение уровня молочной и пировиноградной кислот в крови, повышение антиокислительной активности плазмы) и цитохимических показателей (умеренное повышение активности сукцинатдегидрогеназы, снижение активности лактатдегидрогеназы).
Клиническое наблюдение 2.
Илья С., история болезни N 1748, впервые поступил в отдел врожденных и наследственных заболеваний в возрасте 12 лет с жалобами на нарушение концентрации внимания, снижение школьной успеваемости, быструю утомляемость, опущение век, снижение зрения и слуха. Из анамнеза жизни: в родословной аналогичных заболеваний нет. Родители и младший сибс здоровы. Пробанд родился от 1-й беременности, протекавшей с легким токсикозом в первой половине. На 4-м месяце беременности мать перенесла ангину. Роды в срок, физиологические. Масса при рождении 3500 г, длина 51 см. До 1 года находился на грудном вскармливании. Психомоторное и физическое развитие протекало нормально до школьного возраста. Из анамнеза болезни: в 10 лет было обращено внимание на задержку роста, снижение слуха. В 11 лет появился двусторонний птоз век. При неврологическом обследовании по месту жительства была исключена миастения. В 13 лет было отмечено ограничение подвижности глазных яблок, появились жалобы на быструю утомляемость, ухудшение зрения. Ребенок был направлен в Московский НИИ педиатрии и детской хирургии. Данные объективного обследования. Физическое развитие очень низкое: рост 138 см (<3 перцентиля), масса 25 кг (<3 перцентиля). Индекс Дю Ранта-Лайнера составлял 82,9 (норма 89-110), что свидетельствовало о снижении роста с диспропорциональным дефицитом массы тела. Кожные покровы чистые, подкожная клетчатка и мышечная ткань развиты недостаточно. В легких дыхание везикулярное. В сердце выслушивается легкий систолический шум на верхушке. Живот мягкий, безболезненный. Аппетит сохранен. Стул нормальный. Неврологический статус: гипомимичное лицо, двусторонний птоз, наружная офтальмоплегия, носовой оттенок голоса, диффузная мышечная гипотония и гипотрофия, рваномерное снижение сухожильных и периостальных рефлексов S=D. Психологический статус: эмоциональная неустойчивость, умеренная дизартрия, познавательная деятельность не нарушена, интеллектуальный уровень нормальный, IQ 98 ед.
Учитывая жалобы, данные анамнеза и клинического осмотра, было проведено цитохимическое исследование активности ферментов энергетического обмена (визуальный метод морфометрического анализа). В результате было выявлено снижение активности СДГ-16,1 гр/лф (при норме 18,0-23,0 гр/лф) - 2 сигмальных отклонения, выраженное повышение активности α-ГФДГ - 21,5 гр/лф (норма 11,0-14,0 гр/лф) - 8 сигмальных отклонений, активность ГДГ в пределах нормы - 12,5 гр/лф (норма 10,0-15,0 гр/лф) - 0 сигмальных отклонений, МДГ - 9,5 - 1 сигмальное отклонение; выраженное повышение активности ЛДГ - 30,85 гр/лф (норма 10,0-17,0 гр/лф) - 6 сигмальных отклонений, коэффициент К1 (α-ГФДГ/СДГ) - 1,3 (норма 0,5-0,7) - 8 сигмальных отклонений, что указывало на преобладание процессов анаэробного обмена (гликолиза). Качественные изменения гранул были значительно изменены: уменьшение площади гранул, снижение их оптической плотности, выраженное кластерообразование и соответствовало 2 баллам.
Таким образом, согласно разработанной формуле:
Митохондриальный цитохимический коэффициент:
2×0,5+8×1,3+0×0,3+1×0,5+6×0,1+2+8×0,8= 20,9
МЦК=20,9 баллов.
Вероятность болезни (нарушений клеточной биоэнергетики) у пробанда, согласно разработанным таблицам, около 100%. Ребенку на основании результатов цитохимического анализа активности ферментов энергетического обмена для уточнения диагноза было рекомендовано провести комплексное обследование.
Данные лабораторных и функциональных исследований: на основании данных электрокардиографии и эхокардиоскопии установлено наличие вторичной гипертрофической кардиомиопатии с нарушением сердечной проводимости в виде блокады правой ножки пучка Гиса. При офтальпологическом исследовании обнаружены признаки пигментного ретинита. При проведении аудиометрии выявлена двусторонняя нейросенсорная тугоухость II-III степени. При лабораторном исследовании не установлено нарушений параметров кислотно-основного состояния крови. В крови определялось высокое содержание молочной (2,62 ммоль/л, при норме 1,0-1,7 ммоль/л) и пировиноградной (0,17 ммоль/л, при норме 0,05-0,09 моль/л) кислот. На фоне стандартного глюкозотолерантного теста уровни молочной и пировиноградной кислот увеличивались соответственно до 3,86 и 0,22 ммоль/л. При морфологическом исследовании биоптатов мышечной ткани (четырехглавой мышцы бедра) с использованием световой микроскопии и гистохимических методов выявления активности митохондриальных ферментов (сукцинатдегидрогеназы, цитохромоксидазы) обнаружены феномен RRF, субсарколеммальные скопления конгломератов кальция, липидов. При ультраструктурном исследовании установлены выраженное увеличение количества митохондрий, патологические изменения части органелл (вакуолизация матрикса, разрушение крист), наличие паракристаллических включений. Проведен молекулярно-генетический анализ ДНК митохондрий, выявлена обширная делеция митохондриальной ДНК протяженностью около 5 тыс. пар нуклеотидов. Диагноз синдрома Кернса-Сейра ребенку был выставлен на основании совокупности полученных данных: клинических (низкий рост, птоз, офтальмоплегия, кардиомиопатия с блокадой правой ножки пучка Гиса, пигментный ретинит, тугоухость), цитохимических, биохимических, морфологических исследований, результатов молекулярно-генетического анализа ДНК митохондрий. Ребенку была назначена диета с ограничением поступления углеводов до 10 г/кг, цитомак 4,0 мл внутримышечно 10 инъекций (4 курса в год), коэнзим Q 10 100 мг/сут, L-карнитин 1000 мг/сут, аскорбиновая кислота 1 г/сут, витамин Е 500 мг/сут, никотинамид 60 мг/сут, рибофлавин 60 мг/сут. Медикаментозное лечение проводилось курсами продолжительностью 4 мес с месячным перерывом. Через год после начала лечения выявлено улучшение общего состояния мальчика, нормализация индексов физического развития (индекс Дю Ранта-Лайнера 93,7), что указывало на ликвидацию дефицита массы тела. Положительная динамика в виде уменьшения степени гипертрофии межжелудочковой перегородки. Положительная цитохимическая динамика: повышение активности СДГ - 17,5 гр/лф (при исходном 16,1 гр/лф, норма 18,0-23,0 гр/лф), снижение активности α-ГФДГ- 15,1 гр/лф (при исходном 21,5 гр/лф, норма 11,0-14,0 гр/лф), тенденция к снижению активности ЛДГ-27,3 гр/лф (при исходном 30,85 гр/лф, норма 10,0-17,0 гр/лф),снижение коэффициента К1 (α-ГФДГ/СДГ) - 0,86 (при исходном 1,3, норма 0,5-0,7), что указывало на активацию энергетически выгодного аэробного пути энергетического метаболизма). Однако повышенный уровень молочной кислоты в крови сохранялся 2,9 ммоль/л (при норме 1,0-1,7 ммоль/л). Комплексное лечение было продолжено.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ПОЛИСИСТЕМНОЙ МИТОХОНДРИАЛЬНОЙ НЕДОСТАТОЧНОСТИ У ДЕТЕЙ | 2005 |
|
RU2312347C2 |
| ПРИМЕНЕНИЕ ЧРЕЗКОЖНОГО МОНИТОРИРОВАНИЯ ГАЗООБМЕНА ДЛЯ ДИАГНОСТИКИ ЭНЕРГОДЕФИЦИТНЫХ СОСТОЯНИЙ | 2010 |
|
RU2442535C2 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЯ ЭНЕРГЕТИЧЕСКОГО МЕТАБОЛИЗМА ЛИМФОЦИТОВ ПРИ ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ У ДЕТЕЙ | 2014 |
|
RU2579317C1 |
| СПОСОБ ЛЕЧЕНИЯ ПОЗНАВАТЕЛЬНЫХ НАРУШЕНИЙ У ДЕТЕЙ С ТУБЕРОЗНЫМ СКЛЕРОЗОМ ПУТЕМ КОРРЕКЦИИ МИТОХОНДРИАЛЬНОЙ ДИСФУНКЦИИ | 2004 |
|
RU2271201C2 |
| СПОСОБ ЛЕЧЕНИЯ ДЕТЕЙ С ПОЛИКИСТОЗНОЙ БОЛЕЗНЬЮ ПОЧЕК | 2005 |
|
RU2316322C2 |
| СПОСОБ ЦИТОХИМИЧЕСКОГО ПРОГНОЗИРОВАНИЯ АДАПТАЦИИ СЕРДЕЧНОЙ ДЕЯТЕЛЬНОСТИ У НОВОРОЖДЕННЫХ ДЕТЕЙ | 2008 |
|
RU2353935C1 |
| Способ прогнозирования риска развития длительного клеточного энергодефицита у детей, родившихся в сроке сверхранних преждевременных родов, на первом году жизни | 2019 |
|
RU2701724C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ СТОМАТОЛОГИЧЕСКОЙ ИМПЛАНТАЦИИ НИКЕЛИДА ТИТАНА | 2002 |
|
RU2237242C2 |
| СПОСОБ ДИАГНОСТИКИ ПАРАДОНТИТА У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ | 2002 |
|
RU2222812C1 |
| Способ прогнозирования течения острых респираторных заболеваний у детей раннего возраста | 1980 |
|
SU942697A1 |
Изобретение относится к медицине, в частности к педиатрии. Для осуществления способа прогнозирования митохондриальных заболеваний у детей с недифференцированными формами задержки нервно-психического развития проводят цитохимический анализ активности ферментов биоэнергетического обмена лимфоцитов периферической крови. Далее определяют активность ферментов СДГ, ГФДГ, ГДГ, МДГ, ЛДГ, вычисляют соотношение активности ГФДГ к активности СДГ, величину сигмального отклонения количественного признака активности ферментов и величину соотношения активности ГФДГ к активности СДГ с учетом возраста пациента. Или определяют показатель площади всех гранул фермента СДГ, показатель эллипса кластеров ГФДГ, интегральную оптическую плотность всех гранул ГДГ, площадь всех мелких гранул ЛДГ и величину сигмального отклонения показателя каждого фермента с учетом возраста. Исходя из полученных данных определяют митохондриальный цитохимический коэффициент (МЦК) и по увеличению МЦК судят об увеличении вероятности развития митохондриального заболевания. Использование изобретения позволяет получить адекватную информацию о состоянии энергетического обмена, используя минимальное количества необходимого материала, и обеспечивает щадящие (малоинвазивные) условия обследования больного. 2 н.п. ф-лы, 7 табл.
1. Способ прогнозирования митохондриальных заболеваний у детей с недифференцированными формами задержки нервно-психического и физического развития, отличающийся тем, что проводят цитохимический анализ активности ферментов биоэнергетического обмена лимфоцитов периферической крови обследуемого ребенка, определяют активность ферментов сукцинатдегидрогеназы, глицерофосфатдегидрогеназы, глутаматдегидрогеназы, малатдегидрогеназы, лактатдегидрогеназы в условных единицах, соответствующих среднему числу гранул формазана, вычисляют соотношение активности глицерофосфатдегидрогеназы к активности сукцинатдегидрогеназы, определяют величину сигмального отклонения количественного признака активности каждого из вышеперечисленных ферментов и соотношения активности глицерофосфатдегидрогеназы к активности сукцинатдегидрогеназы с учетом возраста в соответствии с разработанной таблицей №3; определяют качественные показатели (КП) гранул в баллах: 0 - не изменены, т.е. отсутствуют кластеры, нормальная форма и размер гранул, нормальное распределение гранул; 1 - умеренные изменения, т.е. единичные кластеры, наличие мелких гранул, нарушение распределения гранул в некоторых клетках; 2 - выраженные изменения, т.е. кластерообразование, обилие мелких гранул, выраженные нарушения распределения гранул во всех клетках; исходя из полученных данных, определяют суммарный морфометрический показатель - митохондриальный цитохимический коэффициент (МЦК) по формуле
СДГ·0,5+ГФДГ·1,3+ГДГ·0,3+МДГ·0,5+ЛДГ·0,1+КП+К1·0,8,
где СДГ, ГФДГ, ГДГ, МДГ, ЛДГ - величины сигмальных отклонений активности каждого из ферментов, соответственно, определенные в соответствии с таблицей №3;
К1 - коэффициент, равный величине сигмального отклонения соотношения активности глицерофосфатдегидрогеназы к активности сукцинатдегидрогеназы, определенный в соответствии с таблицей №3;
КП - качественные параметры в баллах,
по увеличению показателя МЦК судят об увеличении вероятности развития митохондриального заболевания, при этом при значениях МЦК до 3 - диагноз маловероятен (до 11%); при значениях МЦК от 3 до 6 - диагноз вероятен (11-49%); при значениях МЦК более 6 - вероятность заболевания высока (более 50%).
2. Способ прогнозирования митохондриальных заболеваний у детей с недифференцированными формами задержки нервно-психического и физического развития, отличающийся тем, что проводят цитохимический анализ активности ферментов биоэнергетического обмена лимфоцитов периферической крови, определяют показатель площади всех гранул фермента сукцинатдегидрогеназы, показатель эллипса кластеров фермента глицерофосфатдегидрогеназы, интегральную оптическую плотность всех гранул фермента глутаматдегидрогеназы, площадь мелких гранул фермента лактатдегидрогеназы; определяют величину сигмального отклонения соответствующего показателя каждого из вышеперечисленных ферментов с учетом возраста в соответствии с разработанной таблицей №4, исходя из полученных данных, определяют суммарный морфометрический показатель - митохондиальный цитохимический коэффициент (МЦК) по формуле
СДГпл.все·0,5+ГФДГэлл.кл.·0,7+ГДГинт.о.пл.в.·2,1+ЛДГпл.мелк.·0,8,
где СДГпл.все, ГФДГэлл.кл., ГДГинт.о.пл.в., ЛДГпл.мелк. - величины сигмальных отклонений каждого из соответствующих показателей вышеперечисленных ферментов, определенные в соответствии с таблицей №4, по увеличению показателя МЦК судят об увеличении вероятности развития митохондриального заболевания, при этом при значениях МЦК до 3 - диагноз маловероятен (до 34%); при значениях МЦК от 3 до 3,2 - диагноз вероятен (34-48%); при значениях МЦК более 3,2 - вероятность заболевания высока (более 50%).
| КЛЕМБОВСКИЙ А.И., СУХОРУКОВ B.C | |||
| Митохондриальная недостаточность у детей | |||
| Архив патологии, 1997:59:5:3-7 | |||
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ПОЛИСИСТЕМНОЙ МИТОХОНДРИАЛЬНОЙ НЕДОСТАТОЧНОСТИ У ДЕТЕЙ | 2005 |
|
RU2312347C2 |
| SCHAEFER AM et al | |||
| The epidemiology of mitochondrial disorders-past, present and future, Biochim Biophys Acta | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| CHINNERY PF | |||
| New approaches to the treatment of mitochondrial disorders. | |||
Авторы
Даты
2009-09-10—Публикация
2008-06-09—Подача