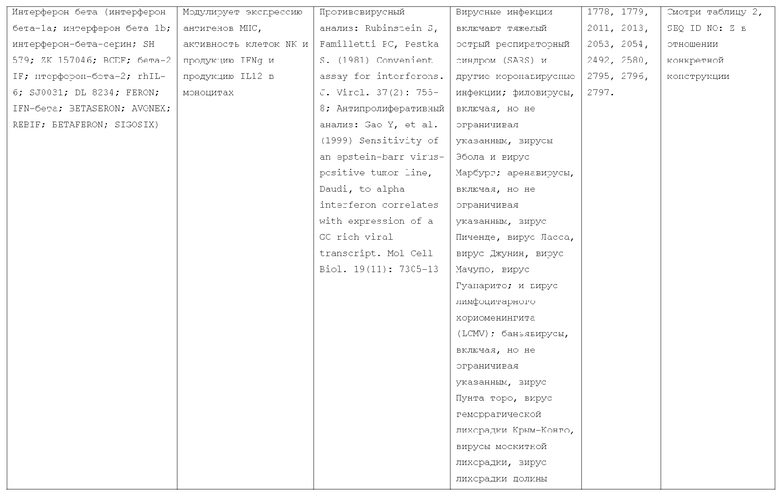
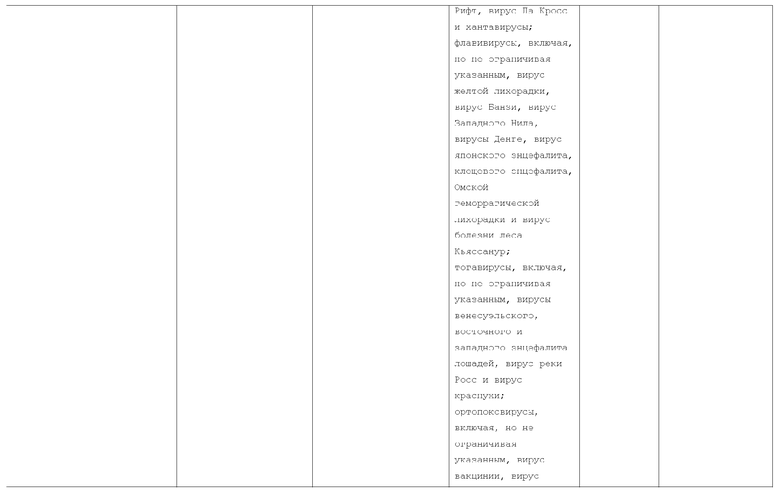
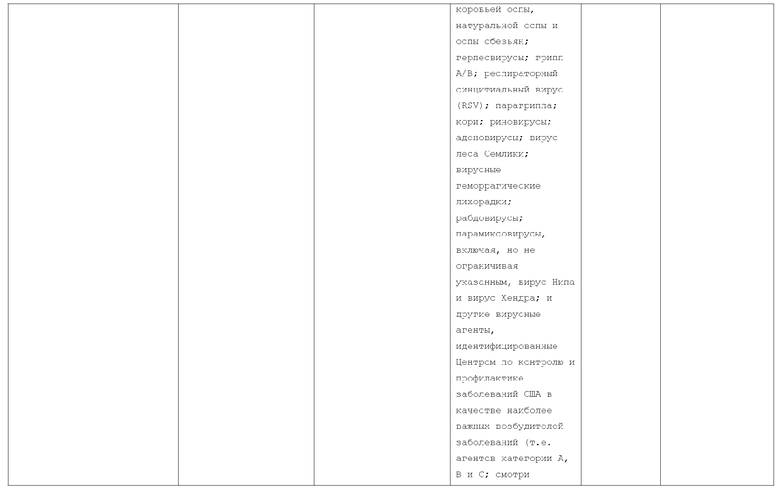
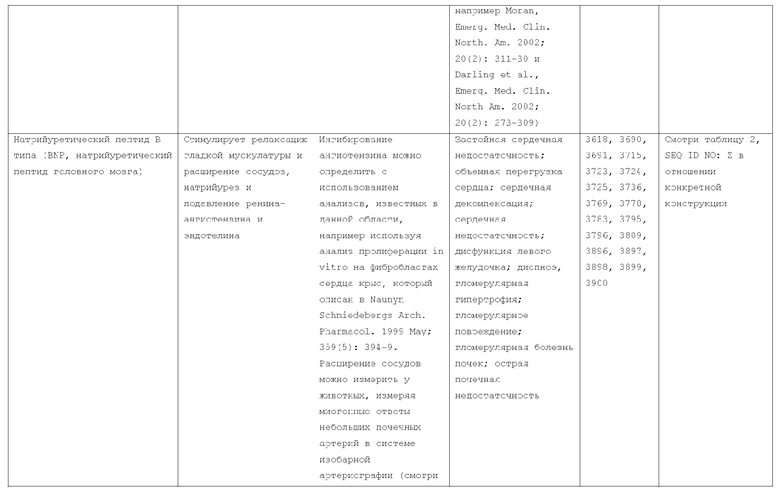
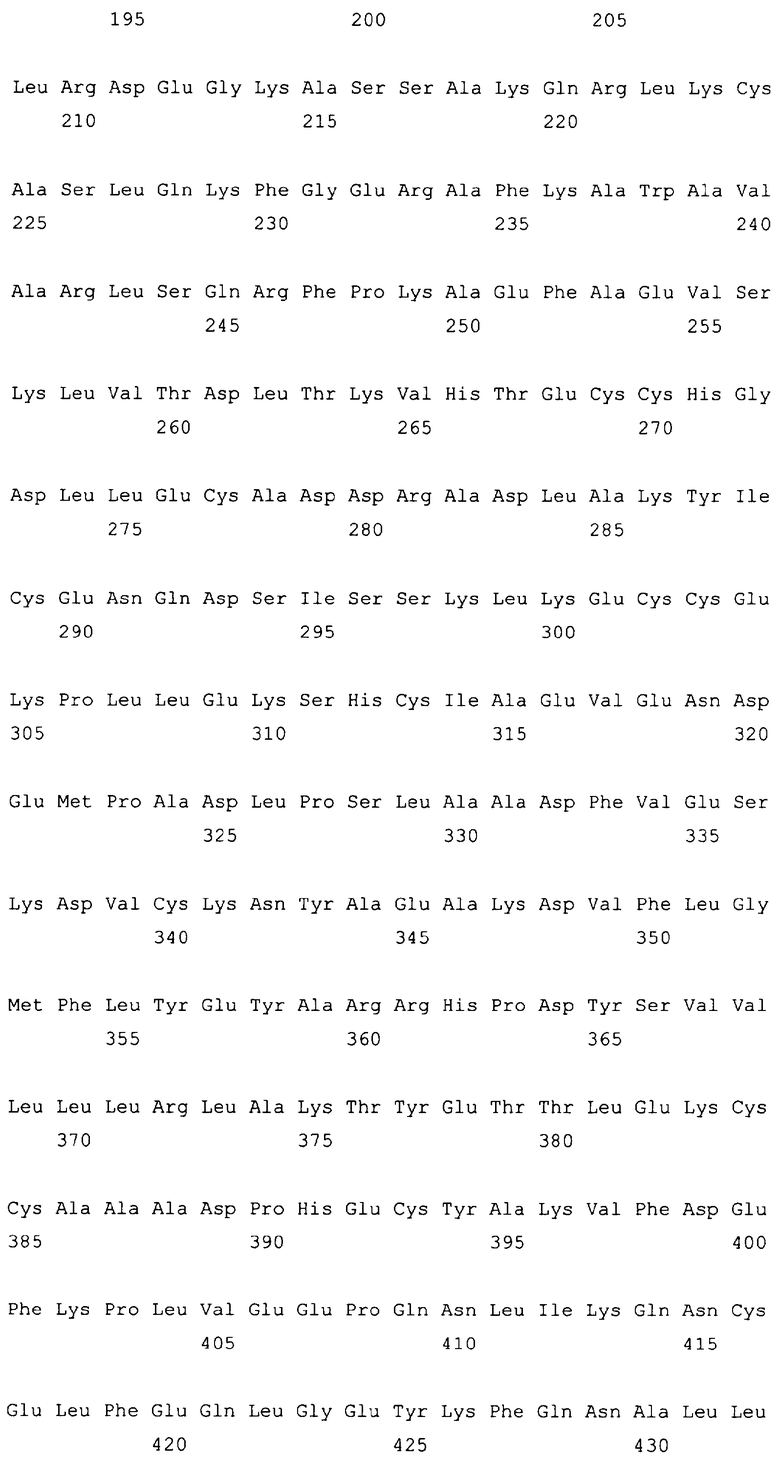
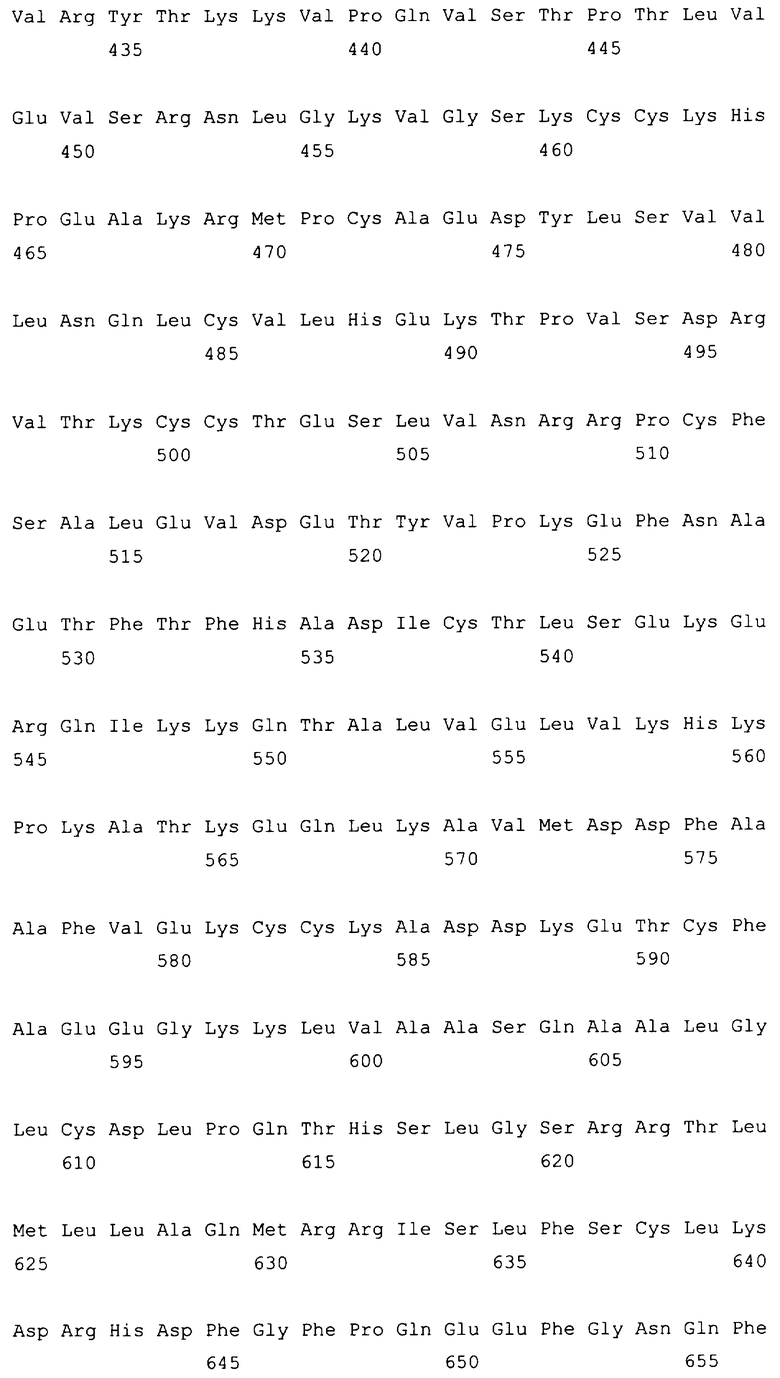
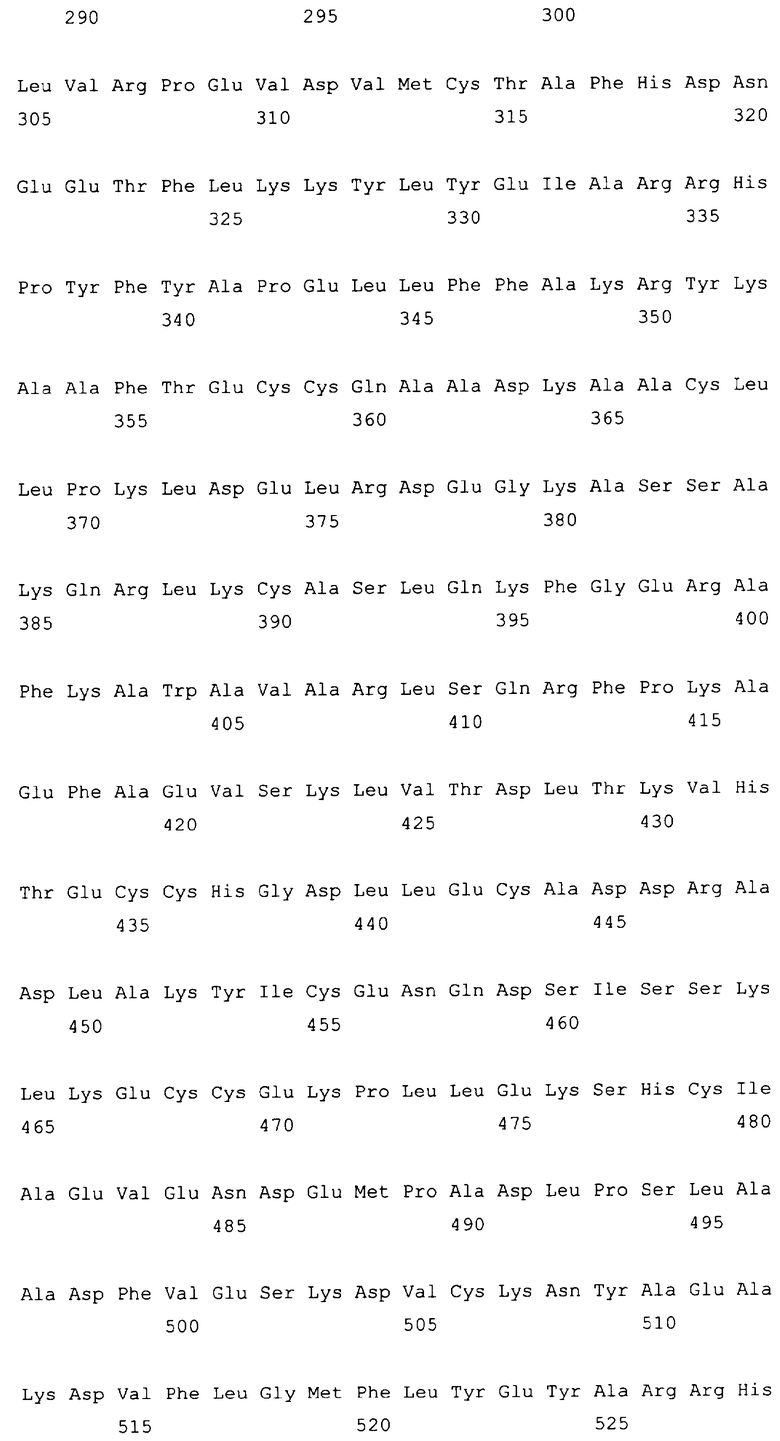
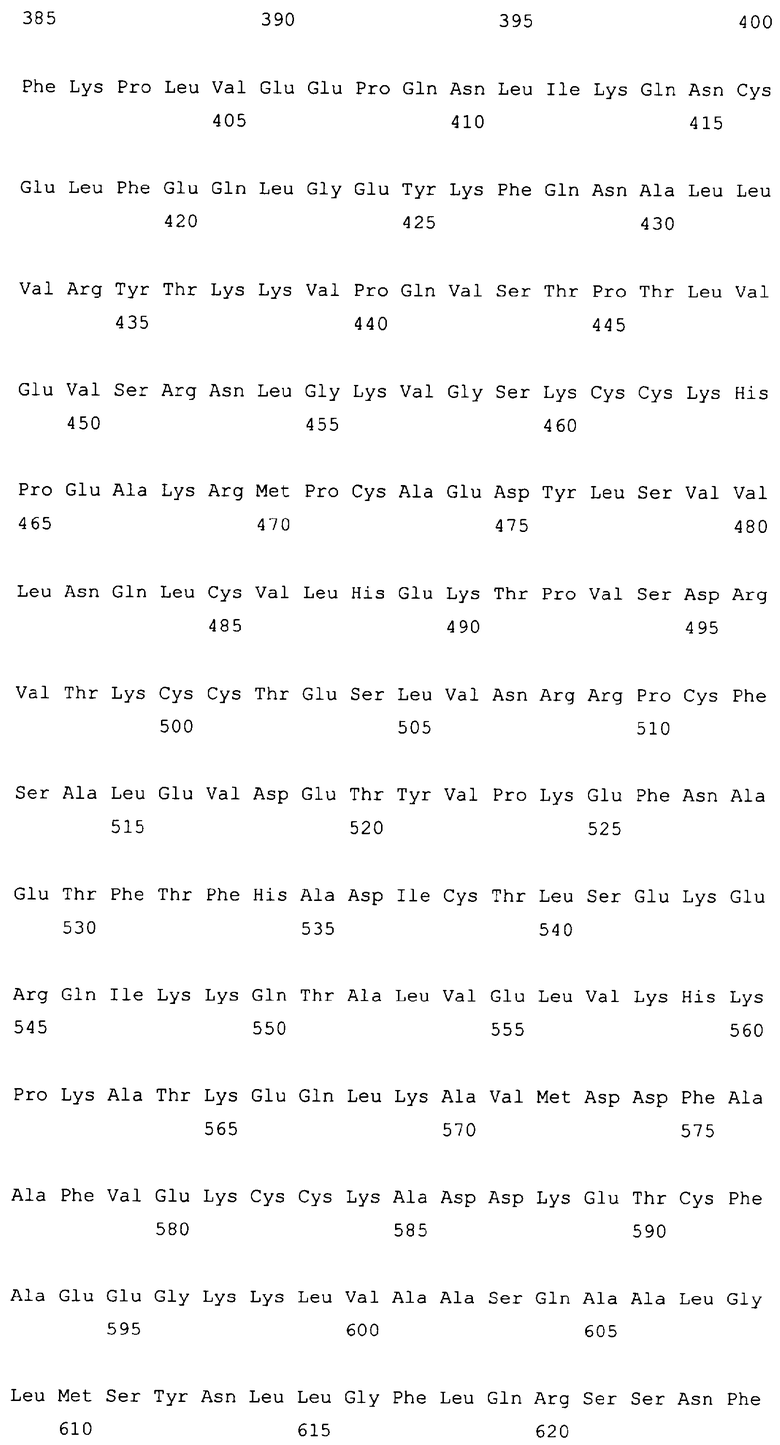
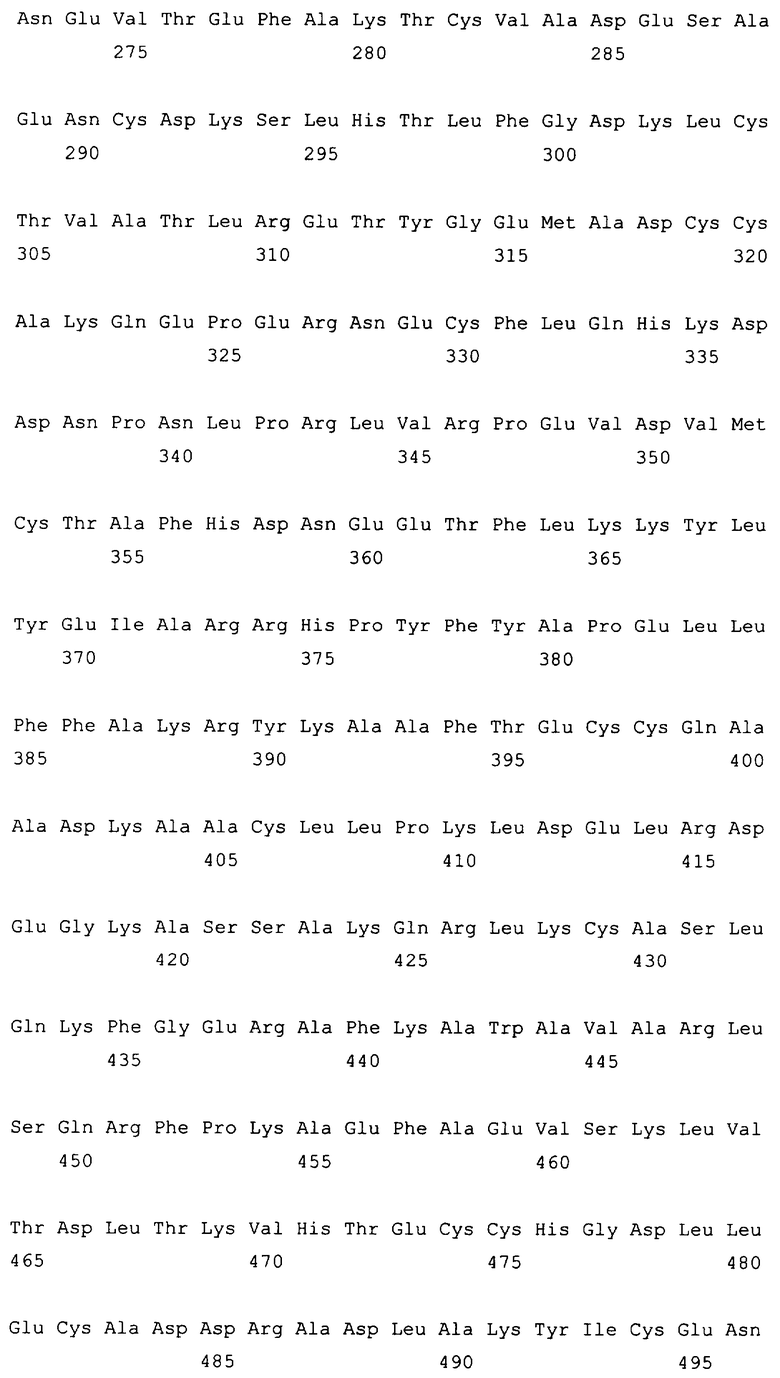
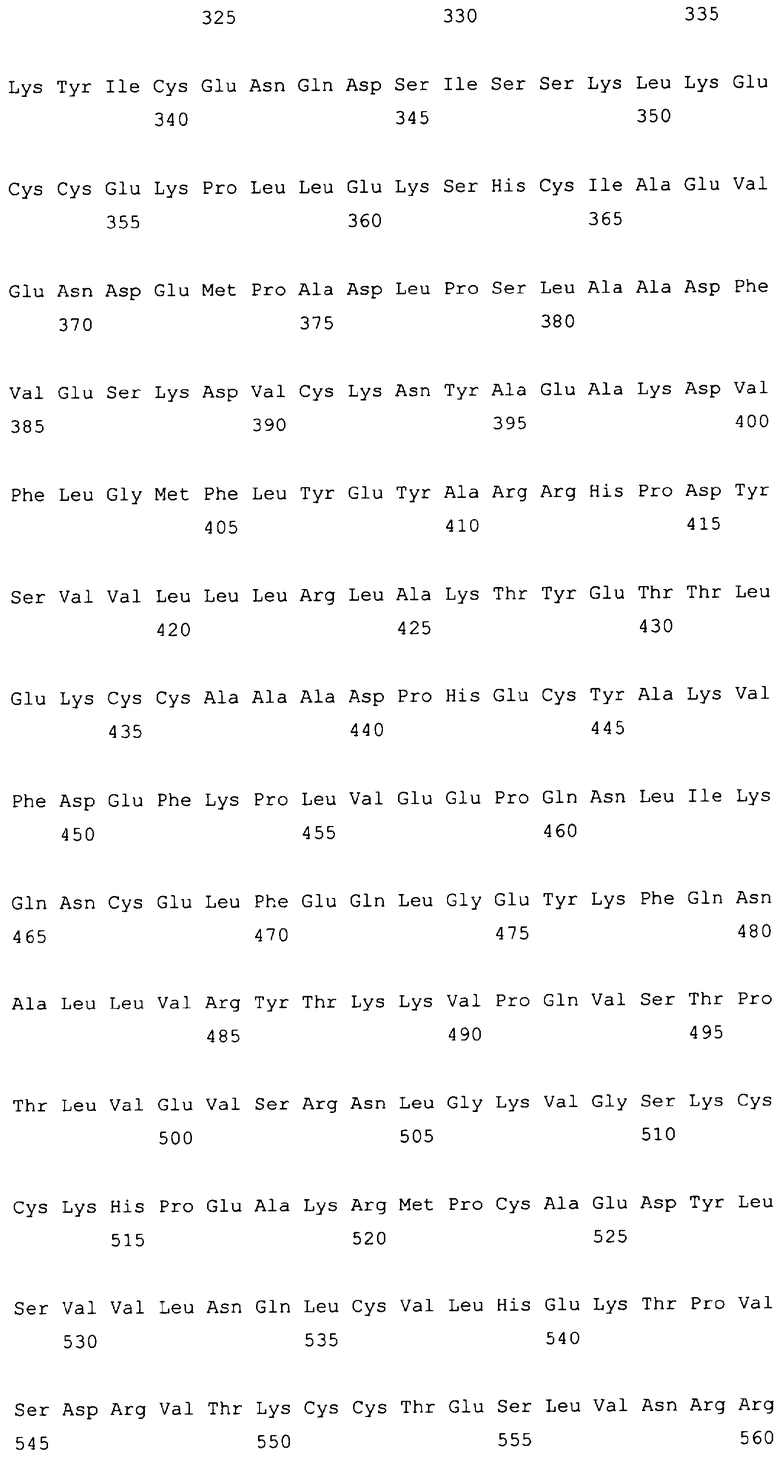
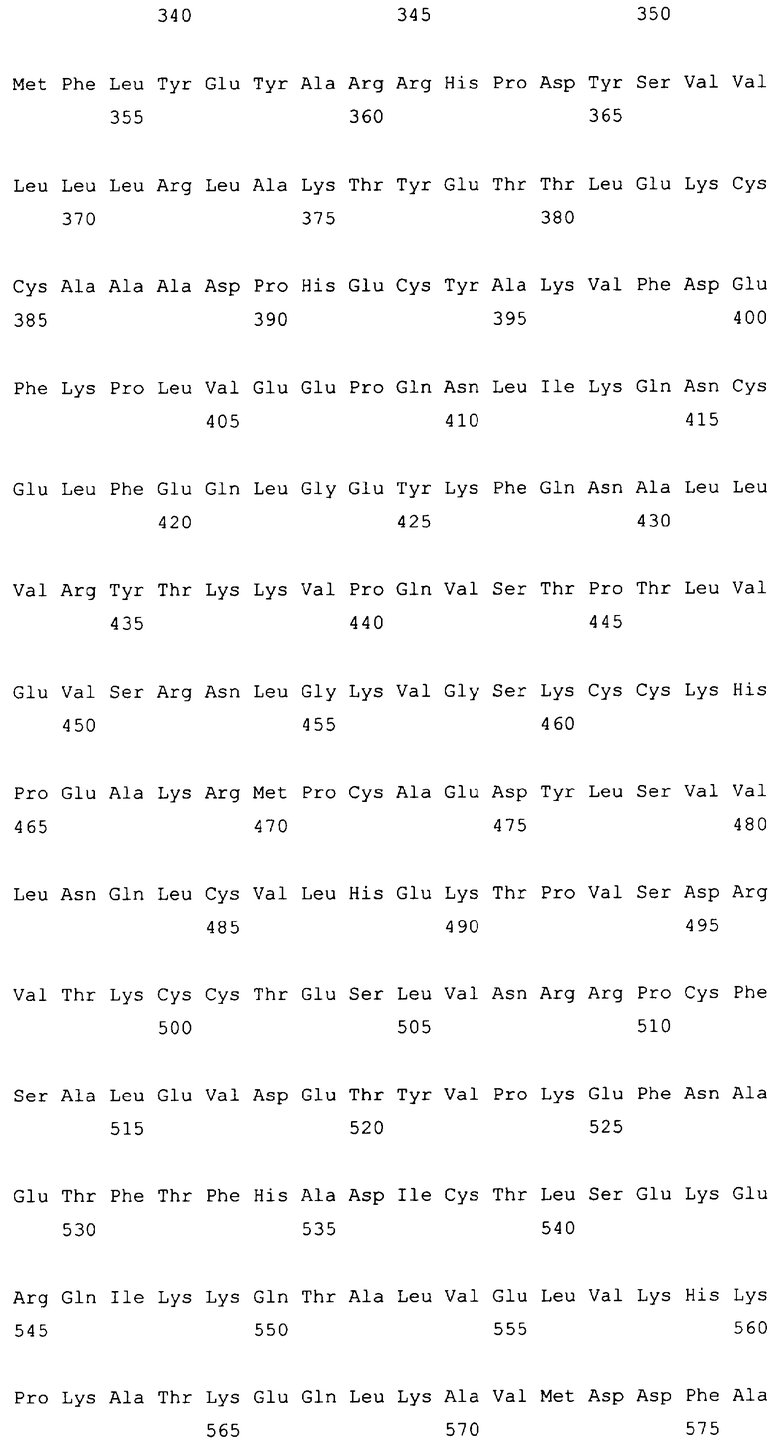
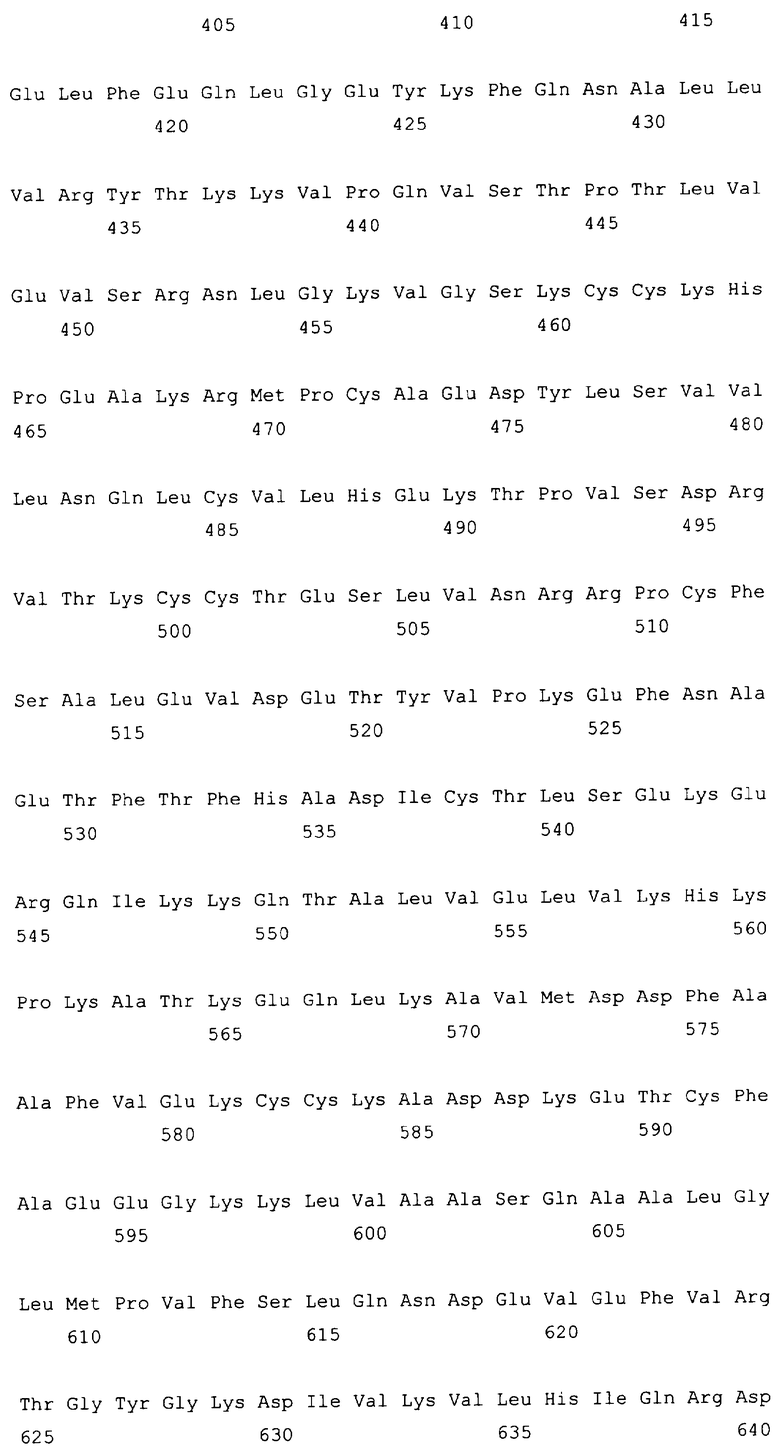
Текст описания приведен в факсимильном виде.












































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































| название | год | авторы | номер документа |
|---|---|---|---|
| КЛЕТКИ-ХОЗЯЕВА И СПОСОБЫ ИСПОЛЬЗОВАНИЯ | 2014 |
|
RU2663587C2 |
| СЛИТЫЕ КОНСТРУКЦИИ ЛЕКАРСТВЕННОГО СРЕДСТВА И КОНЪЮГАТЫ | 2005 |
|
RU2428431C2 |
| СПОСОБ ПРОДУЦИРОВАНИЯ ПОЛИПЕПТИДА В ДРОЖЖАХ | 1995 |
|
RU2167939C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЛОГИЧНОГО БЕЛКА | 1994 |
|
RU2143495C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВ В ТРАНСФОРМИРОВАННЫХ ДРОЖЖЕВЫХ КЛЕТКАХ | 1999 |
|
RU2238323C2 |
| ВАРИАНТЫ АЛЬБУМИНА | 2013 |
|
RU2670063C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКИХ РАССТРОЙСТВ | 2014 |
|
RU2704285C2 |
| СЛИТЫЕ СЕРПИНОВЫЕ ПОЛИПЕПТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2642310C2 |
| СЛИТЫЕ СЕРПИНОВЫЕ ПОЛИПЕПТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2727452C1 |
| СПОСОБ МИКРОБИОЛОГИЧЕСКОГО СИНТЕЗА ЦЕЛЕВОГО СЕКРЕТИРУЕМОГО БЕЛКА В ДРОЖЖАХ Saccharomyces cerevisiae | 2012 |
|
RU2502805C1 |


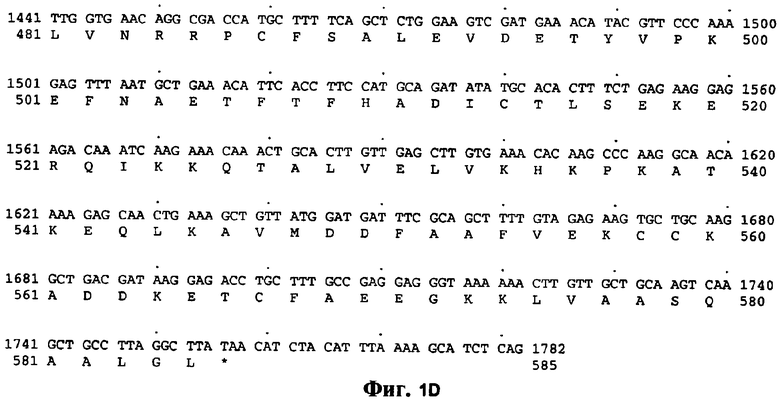
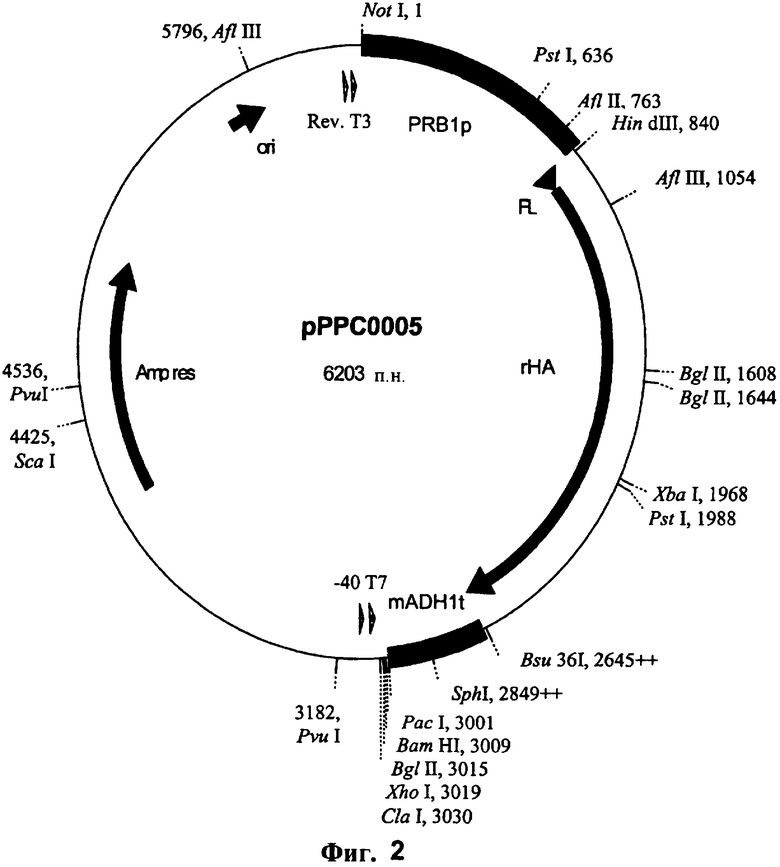
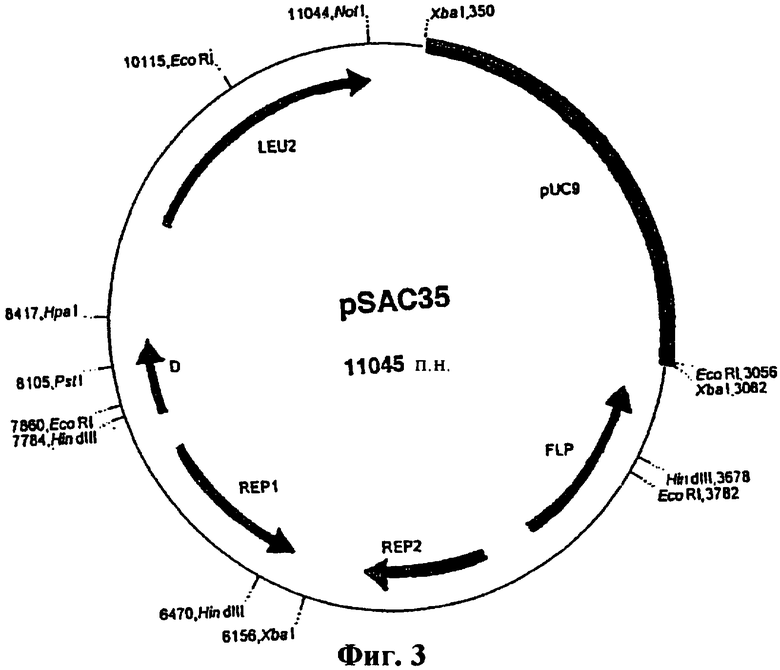
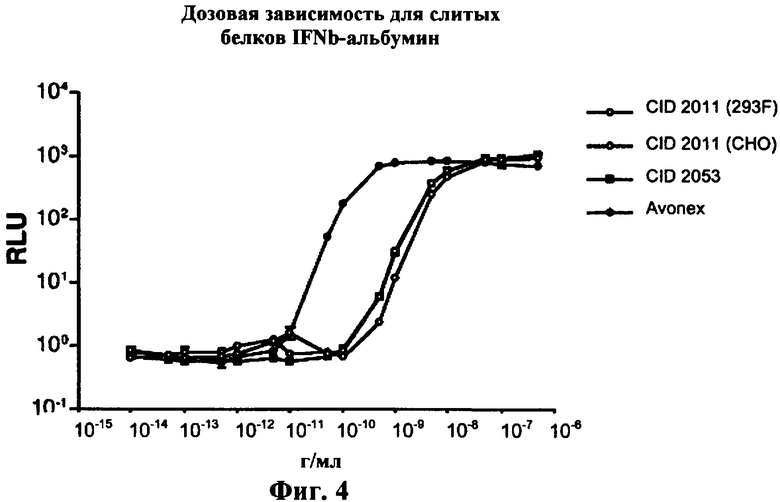
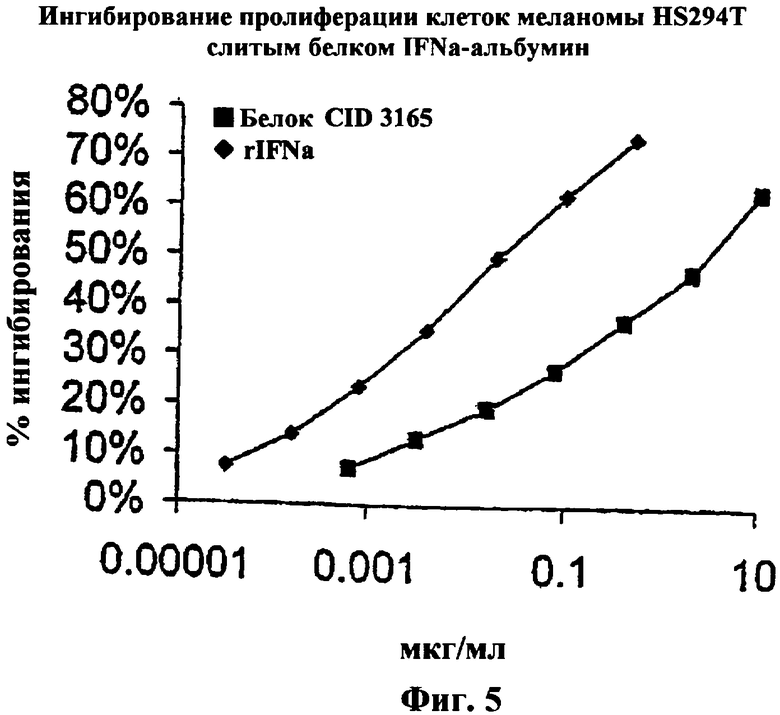
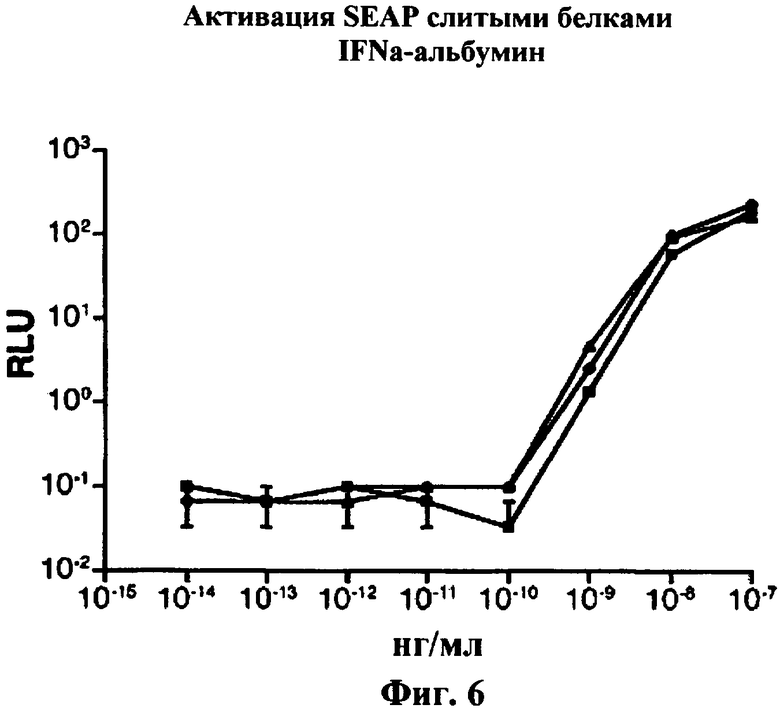
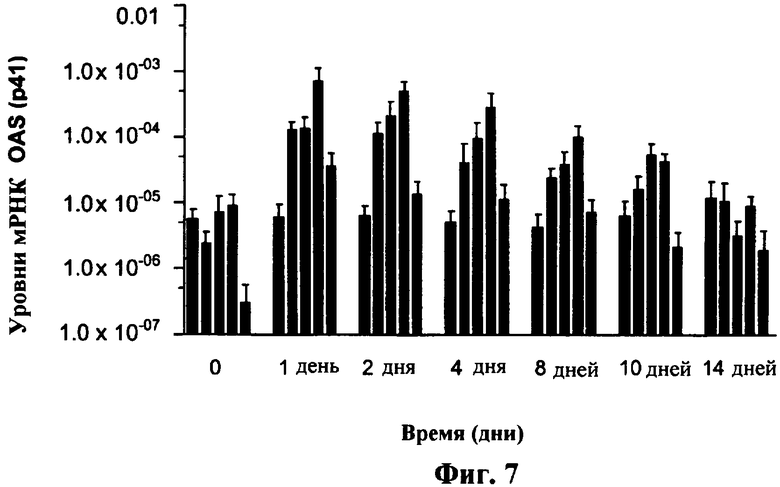
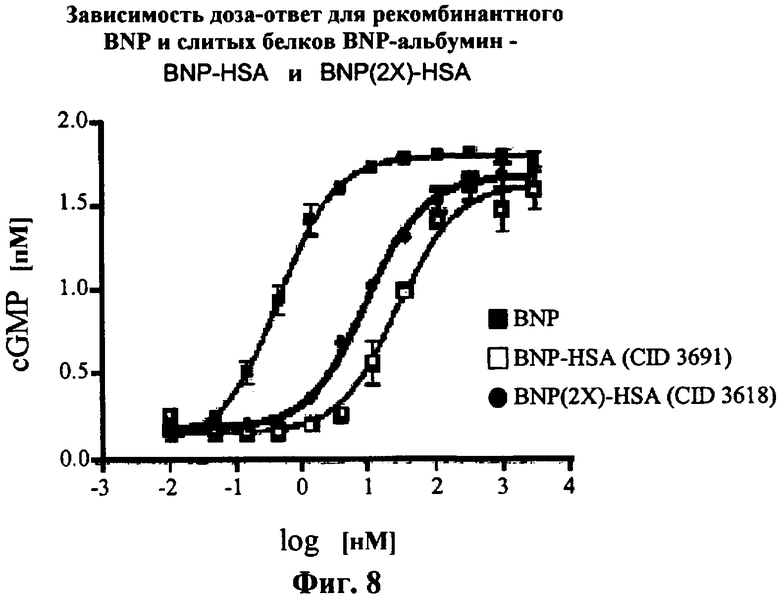
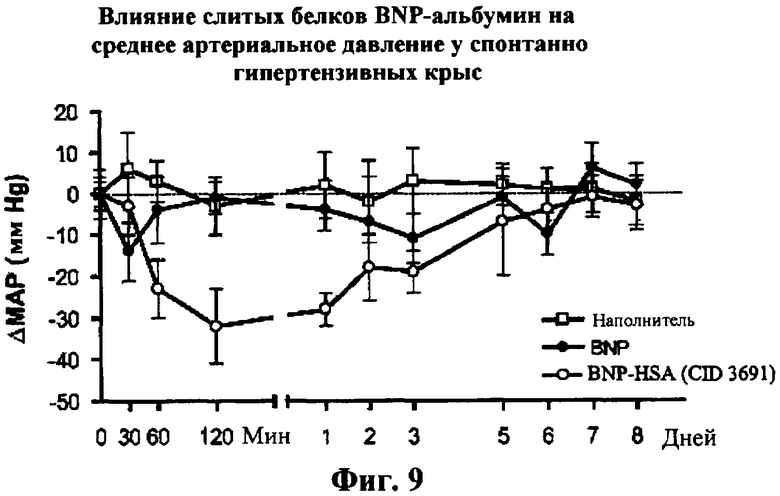
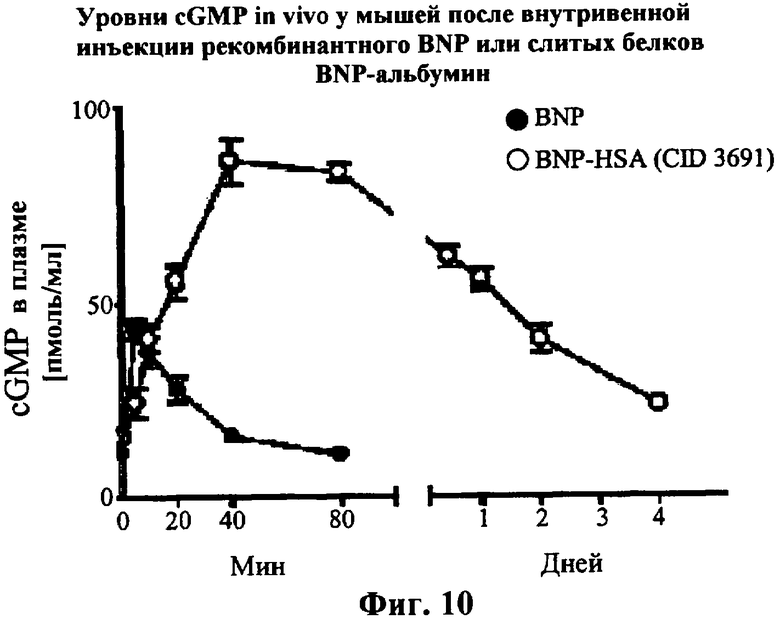
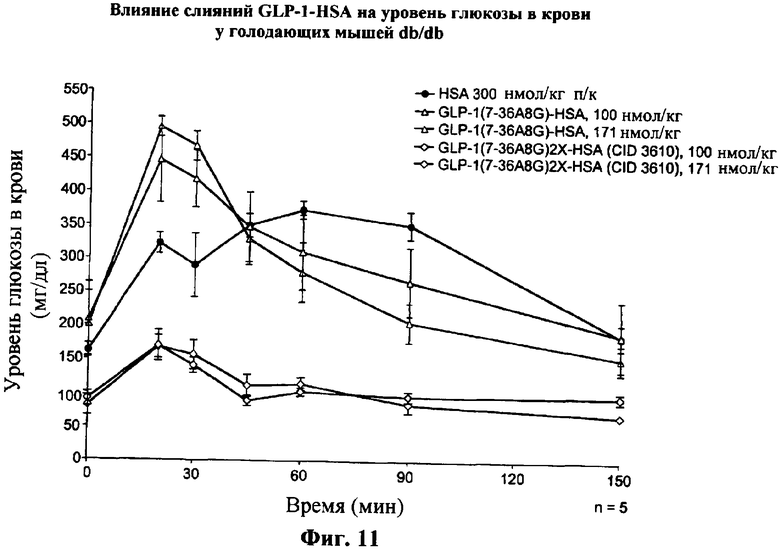
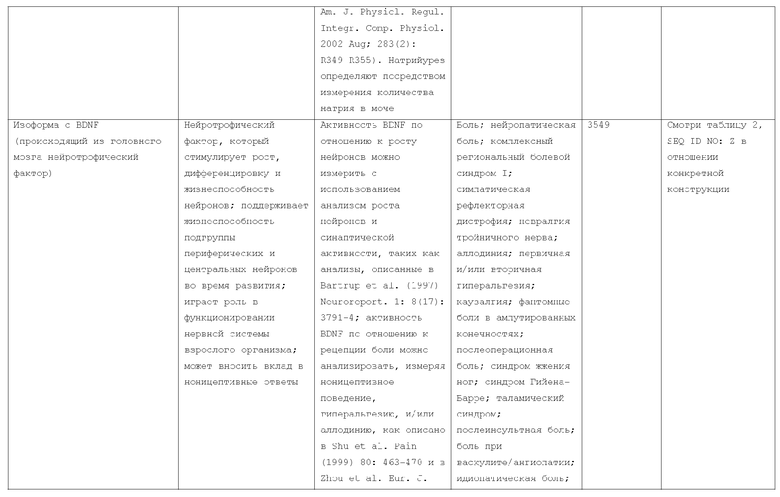
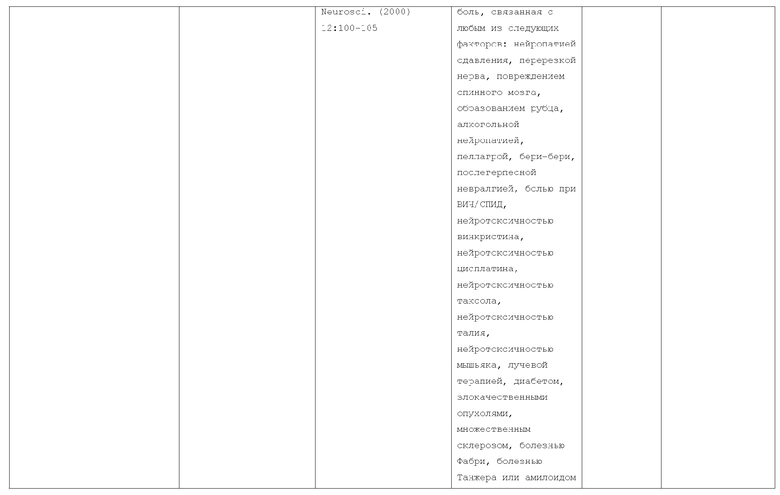
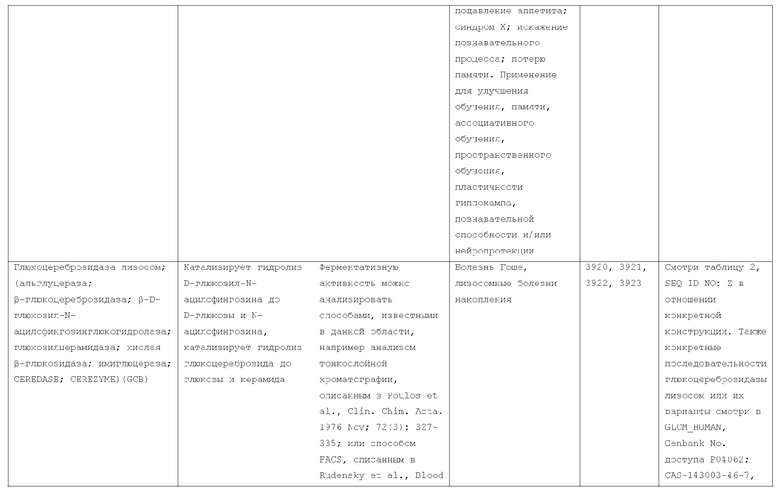
Изобретение относится к слитым белкам альбумина. Сущность изобретения включает слитый с альбумином белок, содержащий два или более тандемно ориентированных полипептидов GLP-1 или его фрагментов, содержащих (7-36 A8G)), молекулы нуклеиновой кислоты, кодирующией слитые белки альбумина согласно изобретению, а также векторы, содержащие указанные нуклеиновые кислоты, клетки-хозяева, трансформированные векторами, содержащими указанные нуклеиновые кислоты, способы получения слитых белков альбумина согласно изобретению и их применения. Кроме того, настоящее изобретение относится к фармацевтической композиции, содержащей слитые белки альбумина, и способу лечения заболеваний, расстройств или состояний с использованием слитых белков альбумина согласно изобретению. Преимущество изобретения заключается в повышении стабильности терапевтического полипептида. 9 н. и 25 з.п. ф-лы, 11 ил.
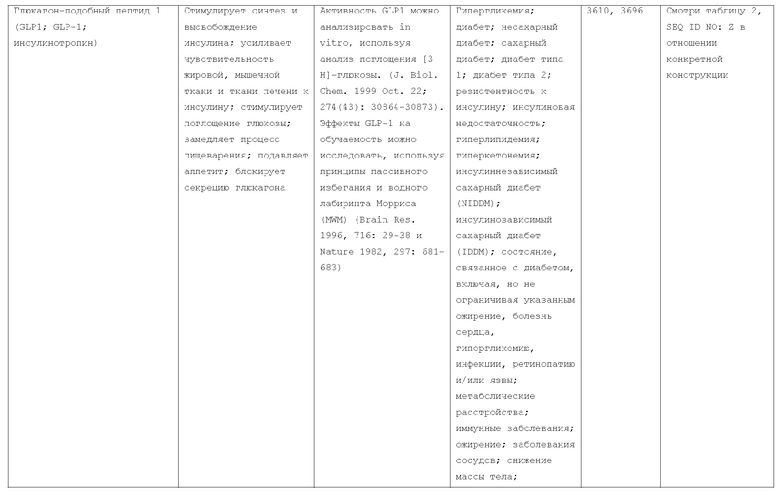
1. Слитый с альбумином белок, содержащий два или более тандемно ориентированных полипептидов GLP-1, причем указанные полипептиды GLP-1 выбраны из GLP-1 дикого типа, его фрагмента GLP-1 (7-36(A8G)) и вариантов GLP-1, слитых с альбумином, фрагментом альбумина или его вариантом, где указанный фрагмент альбумина или вариант альбумина увеличивает время полужизни неслитых полипептидов GLP-1 в плазме, где указанный слитый белок обладает активностью GLP-1, и где слитый с альбумином белок дополнительно содержит лидерную последовательность.
2. Слитый с альбумином белок по п.1, где указанные тандемно ориентированные полипептиды GLP-1 выбраны по меньшей мере из одной последовательности GLP-1 дикого типа, слитой по меньшей мере с одной последовательностью фрагмента GLP-1 (7-36(A8G)).
3. Слитый с альбумином белок по п.1, где указанные тандемно ориентированные полипептиды GLP-1 выбраны по меньшей мере из одной последовательности GLP-1 дикого типа, слитой по меньшей мере с одной последовательностью варианта GLP-1.
4. Слитый с альбумином белок по п.1, где указанные тандемно ориентированные полипептиды GLP-1 выбраны по меньшей мере из одной последовательности фрагмента GLP-1 (7-36(A8G)), слитой по меньшей мере с одной последовательностью варианта GLP-1.
5. Слитый с альбумином белок по любому из пп.1-4, где указанным по меньшей мере одним фрагментом GLP-1 или одним вариантом GLP-1 является GLP-1 (7-36(A8G)).
6. Слитый с альбумином белок по п.5, где указанные фрагменты GLP-1 или варианты GLP-1 выбраны из двух тандемно ориентированных GLP-1 (7-36 (A8G)).
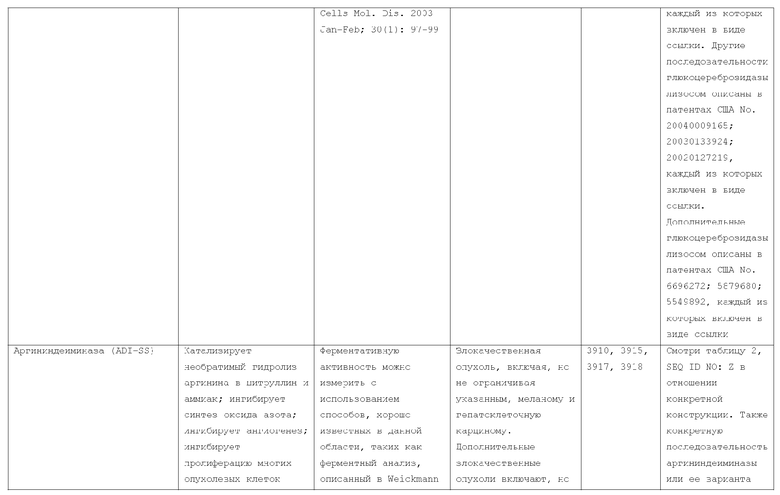
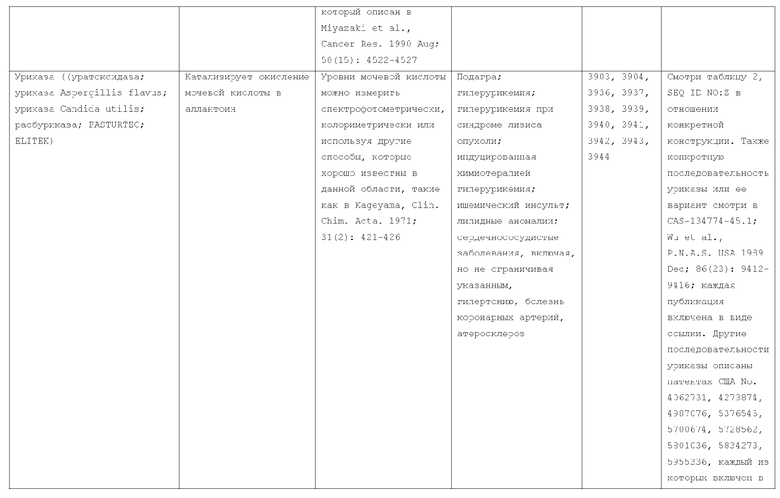
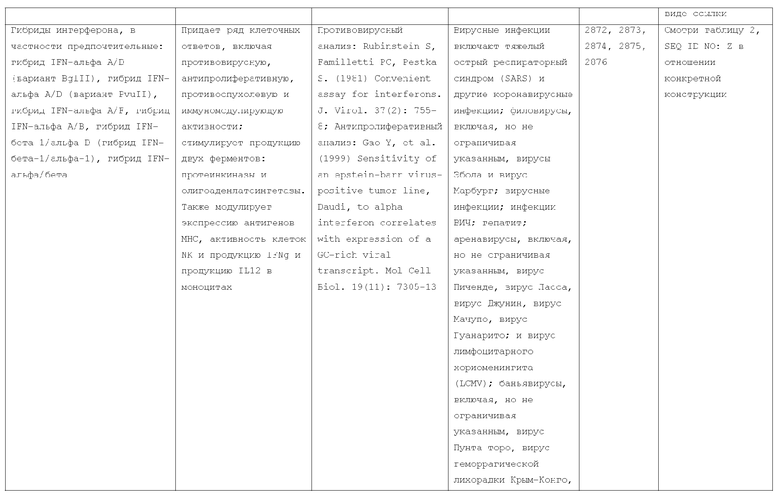
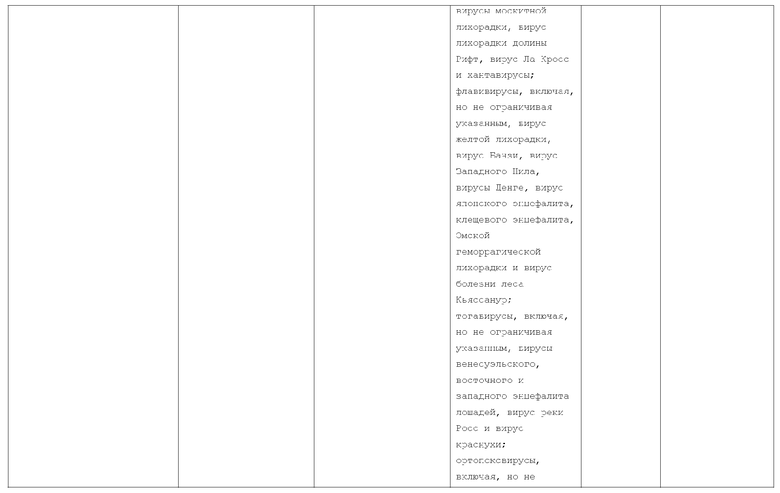
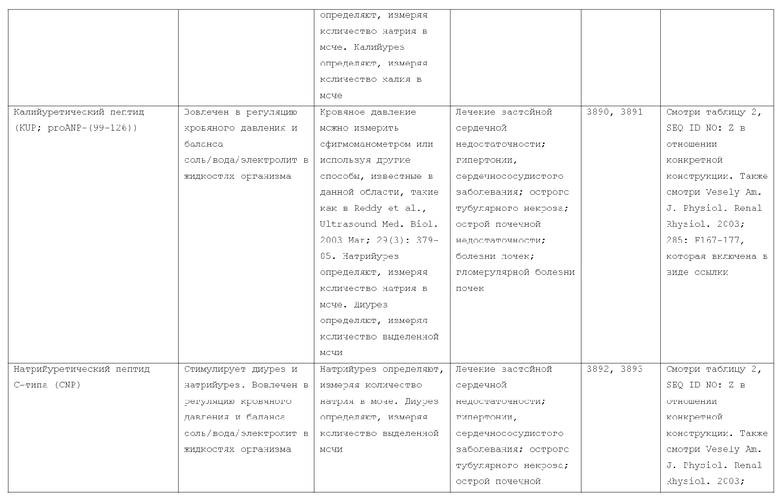
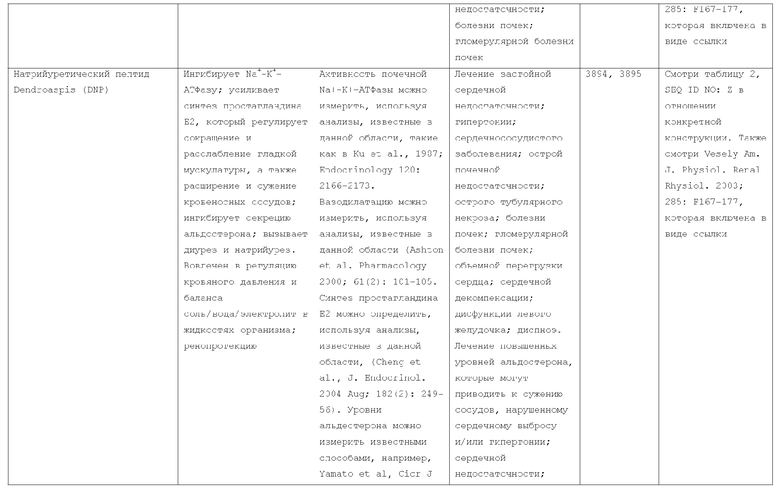
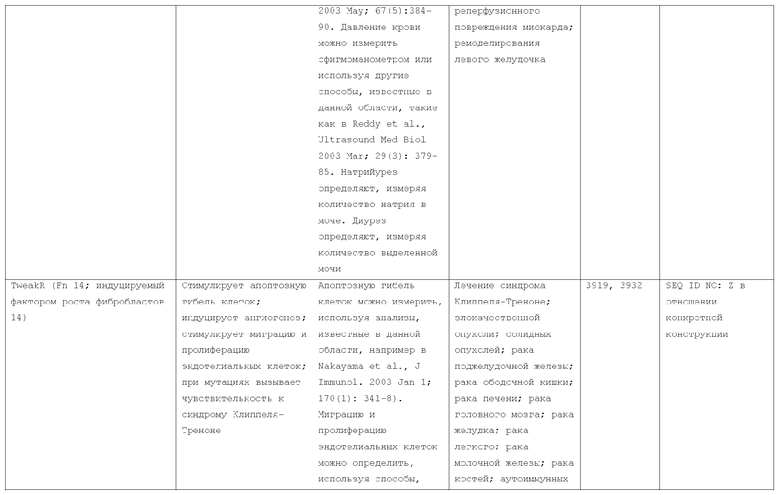
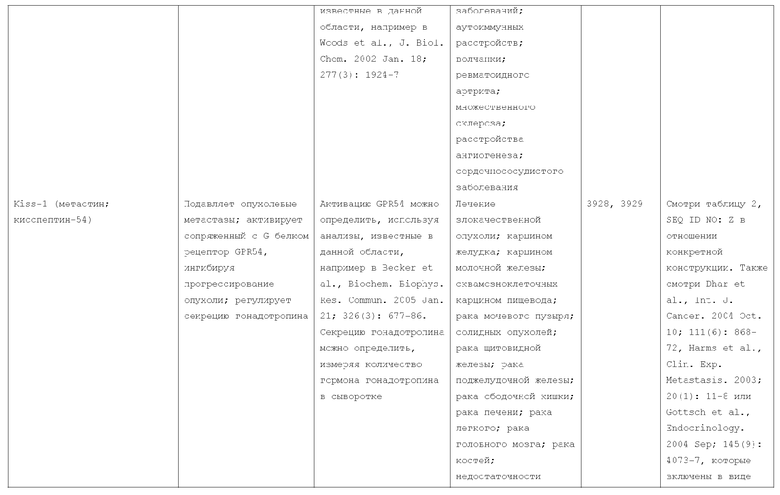
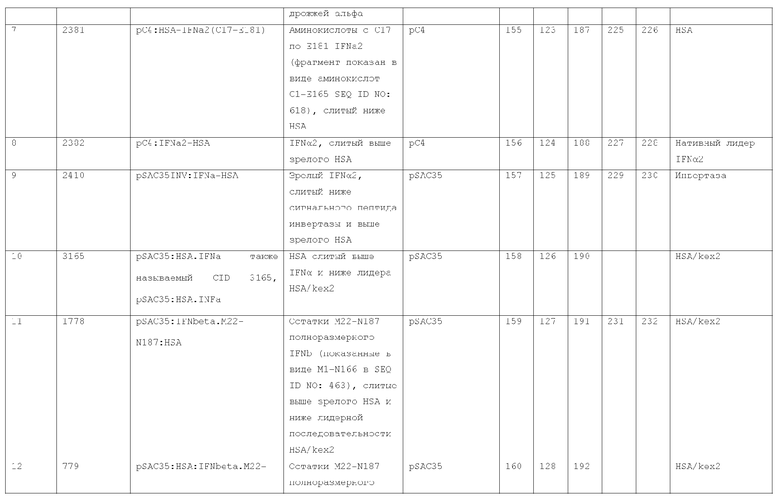
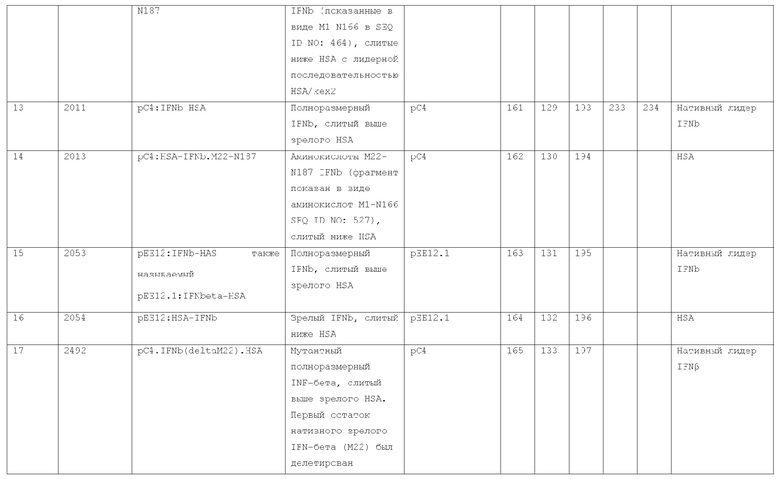
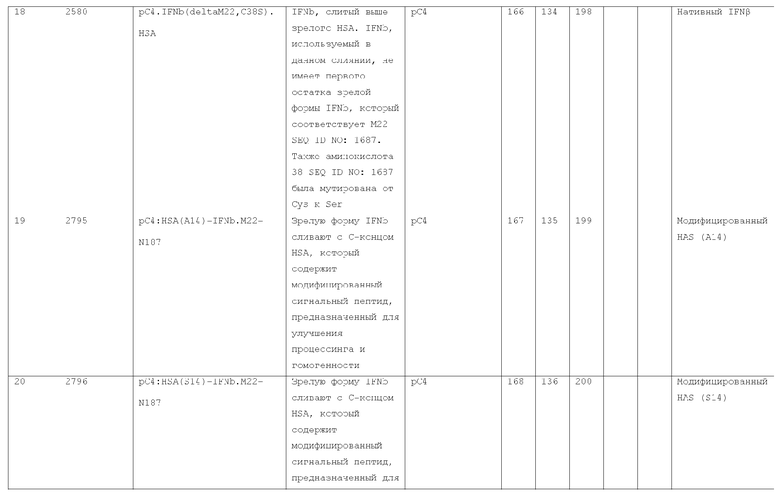
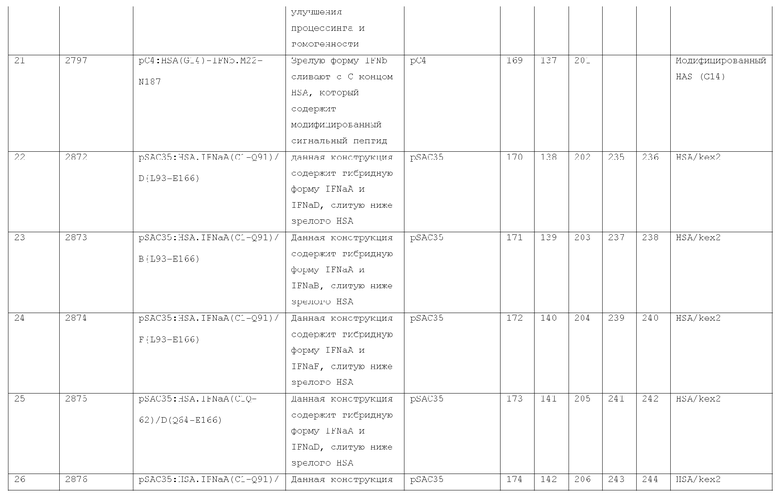
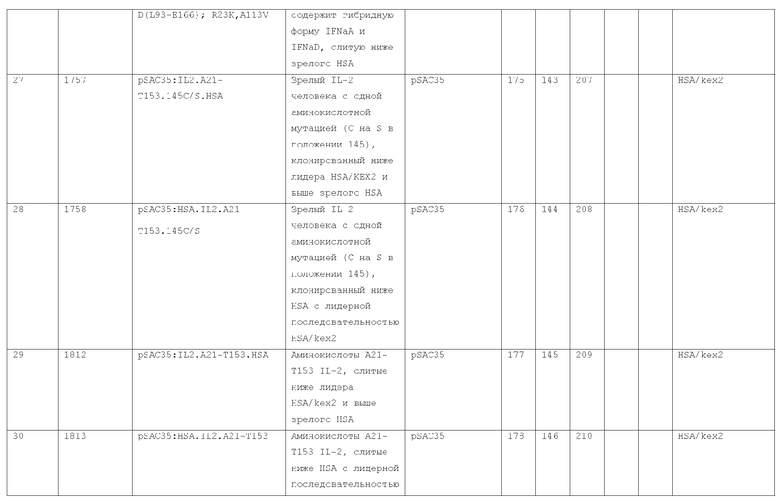
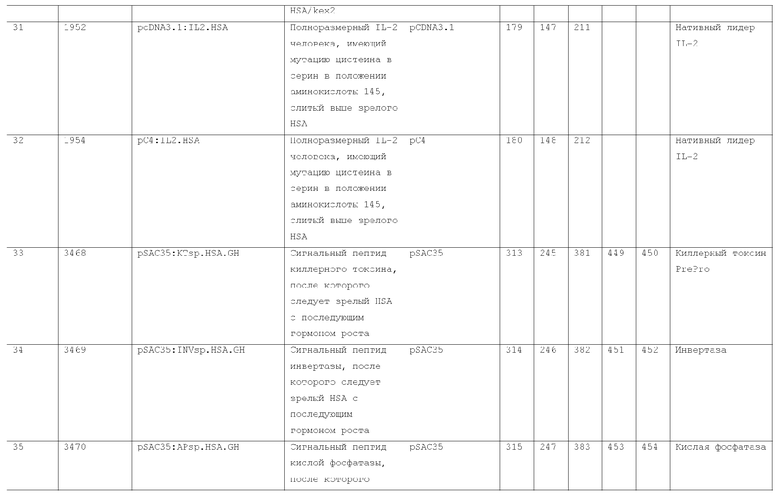
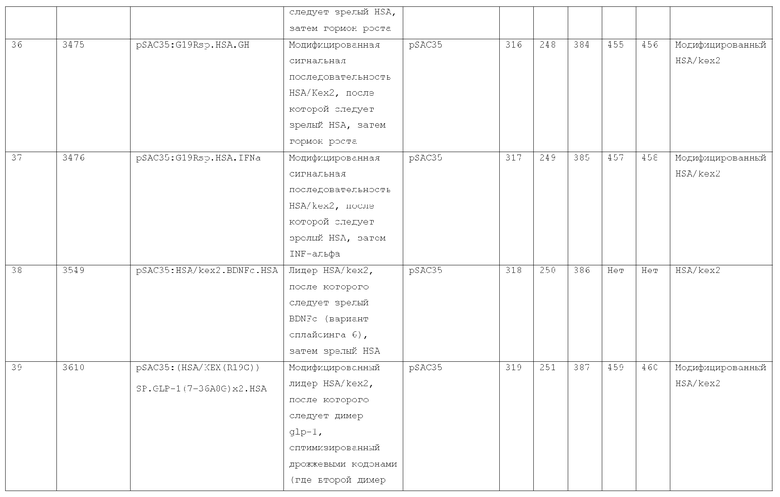
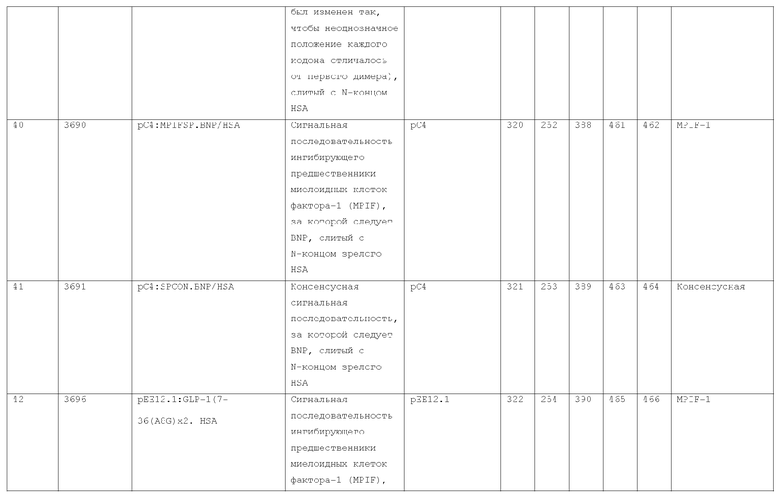
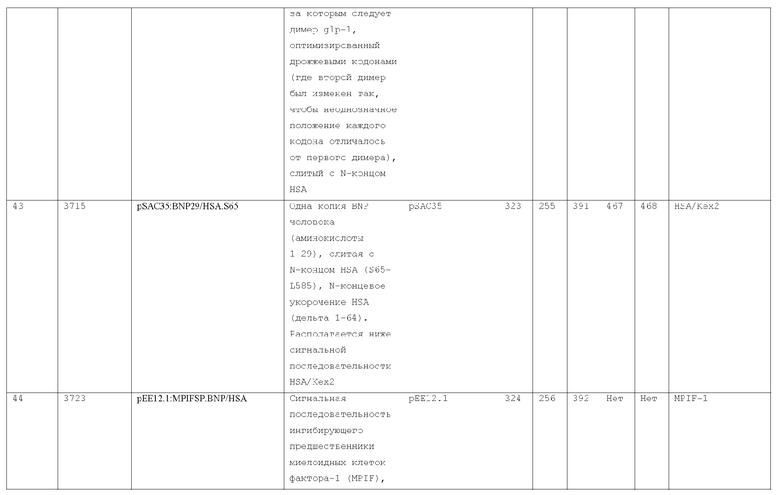
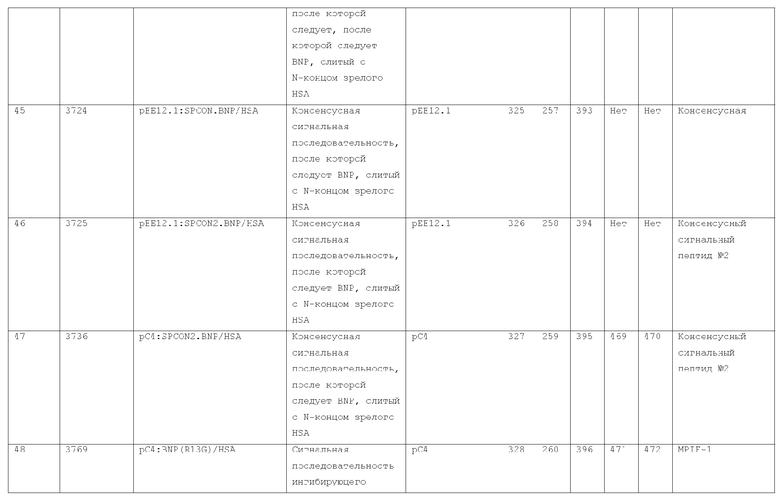
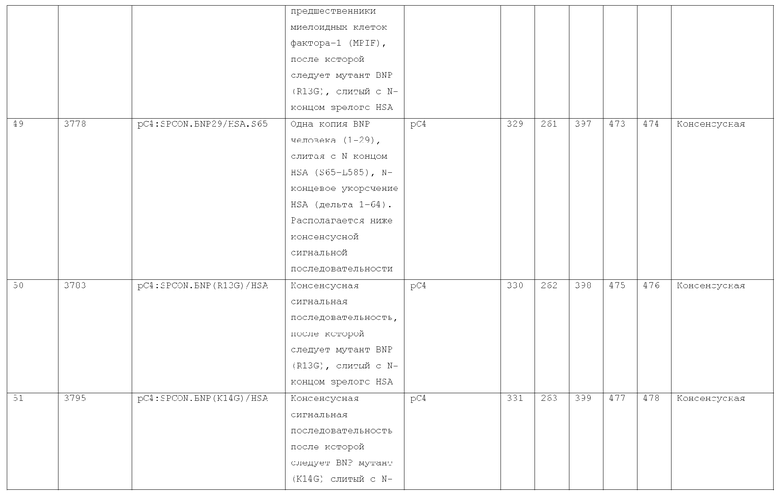
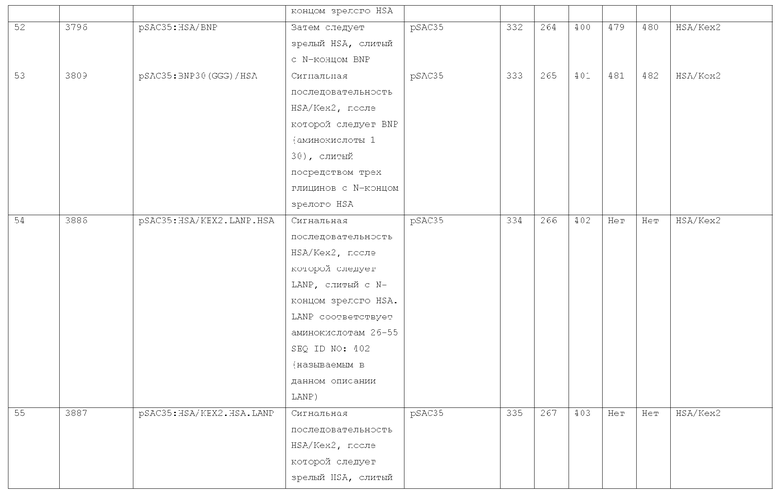
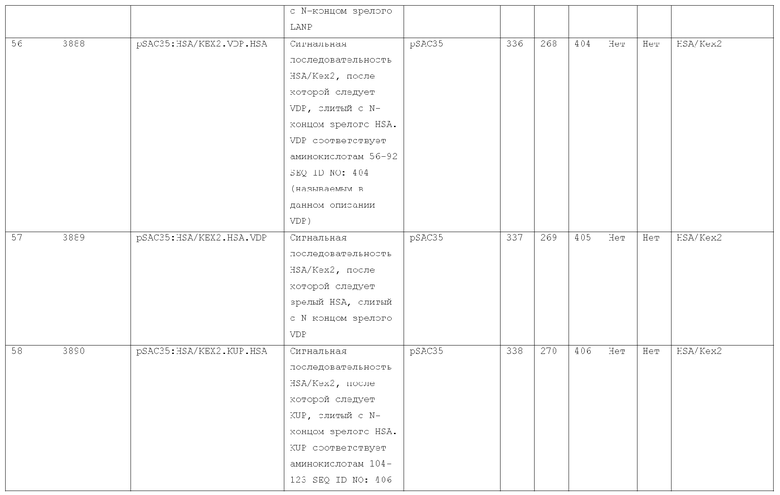
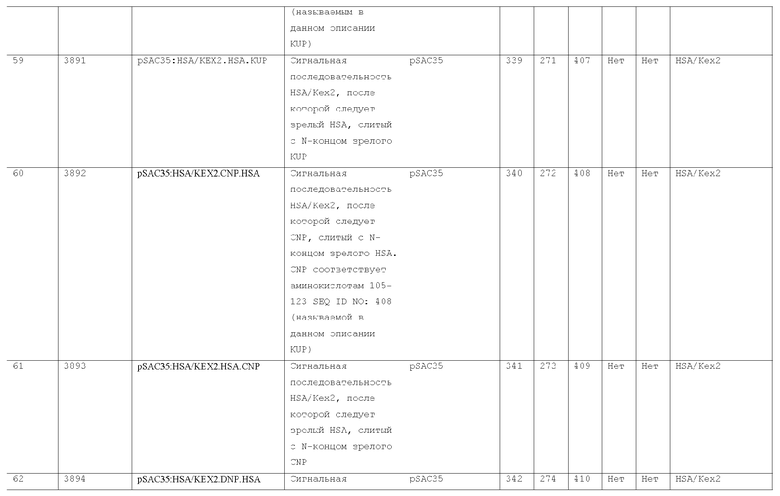
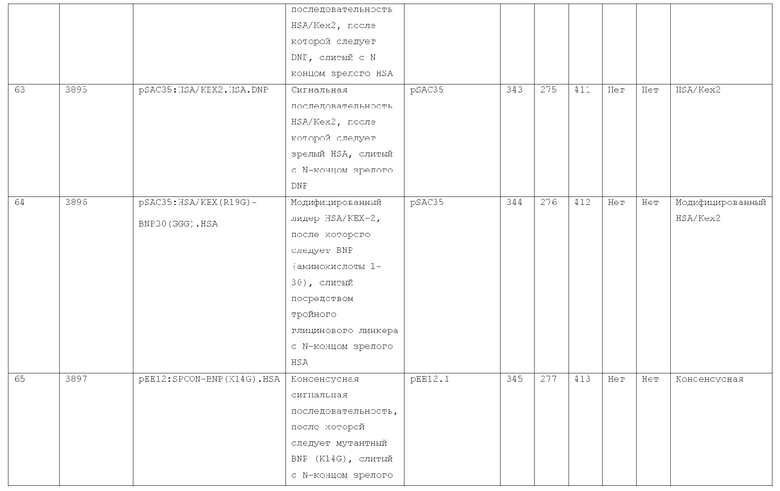
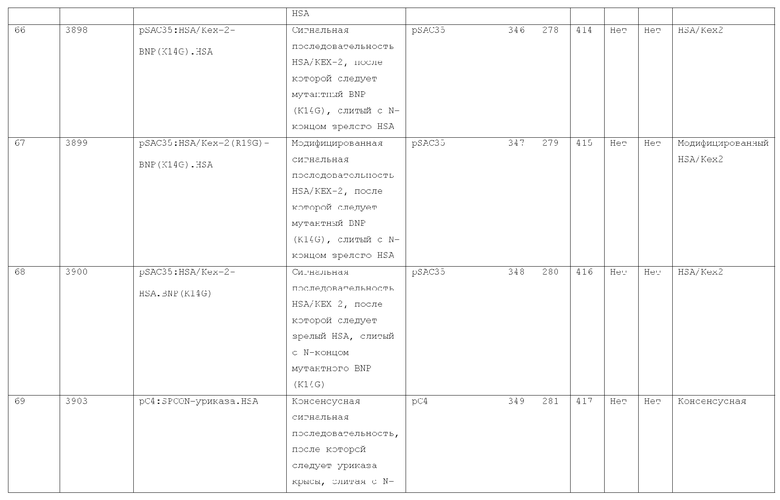
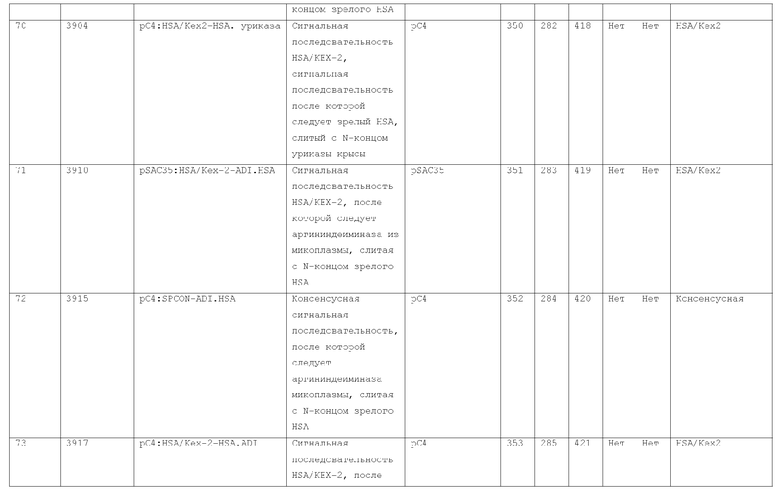
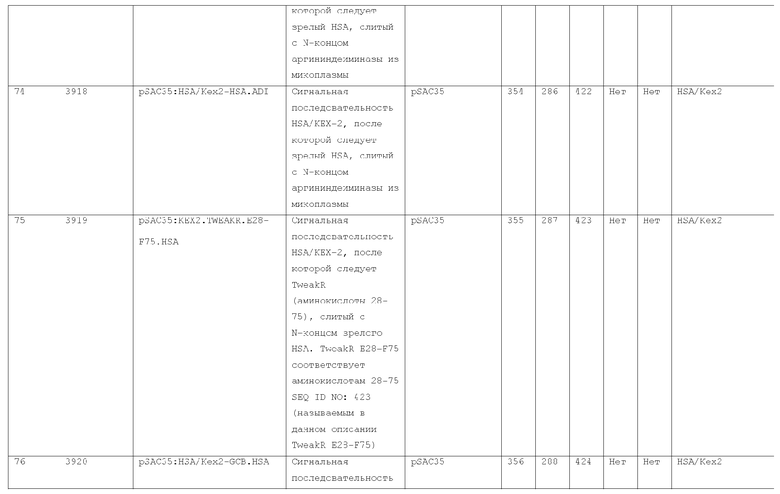
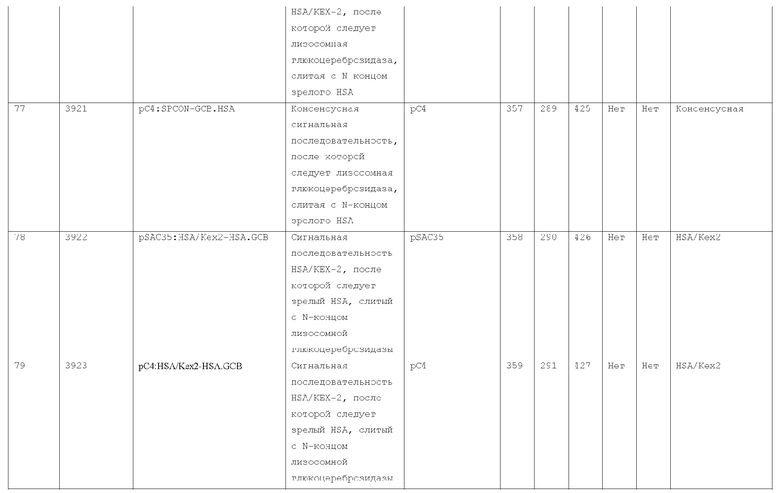
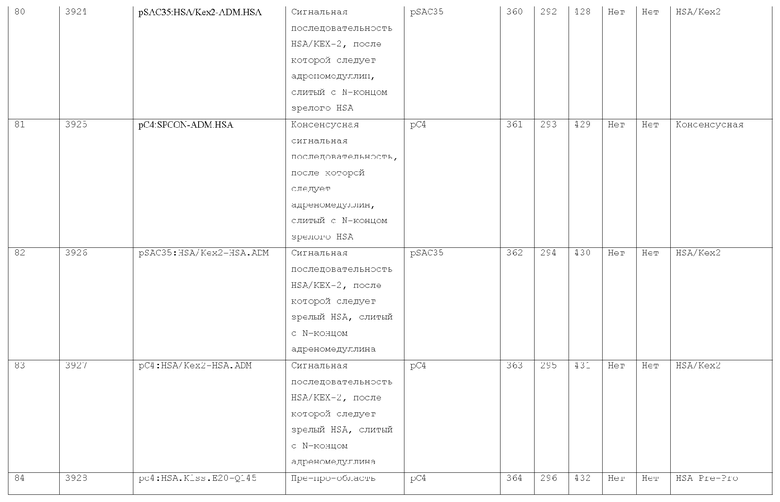
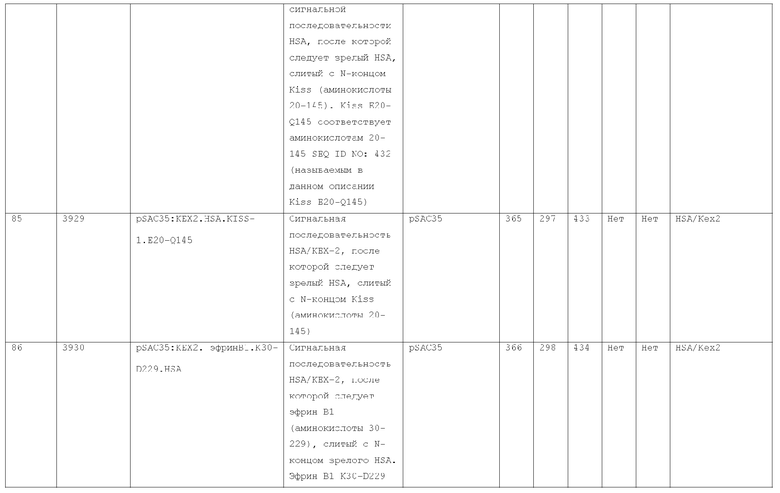
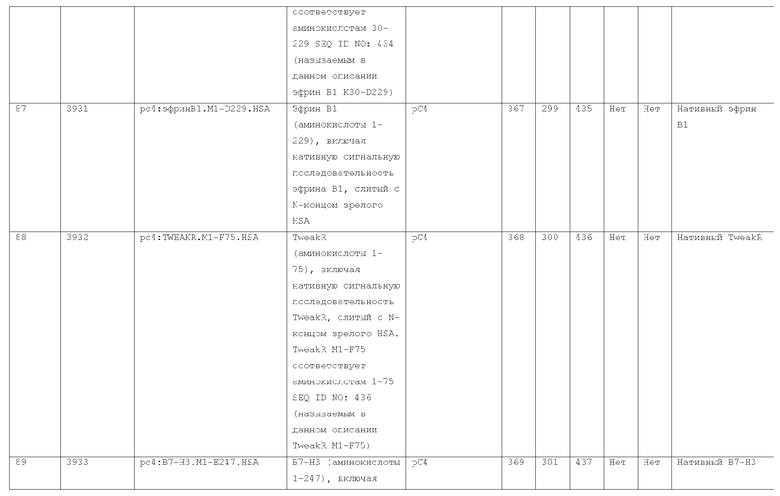
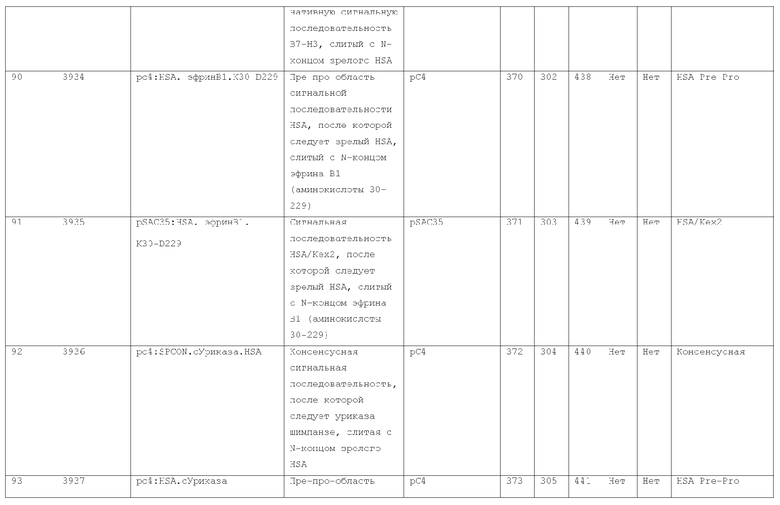
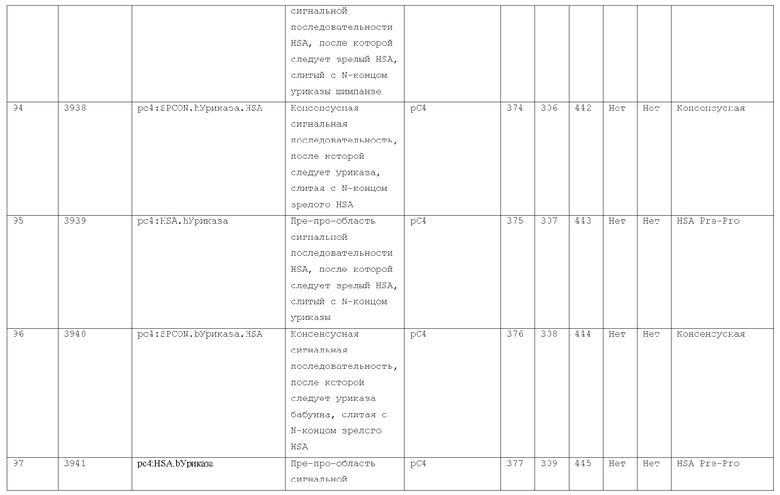
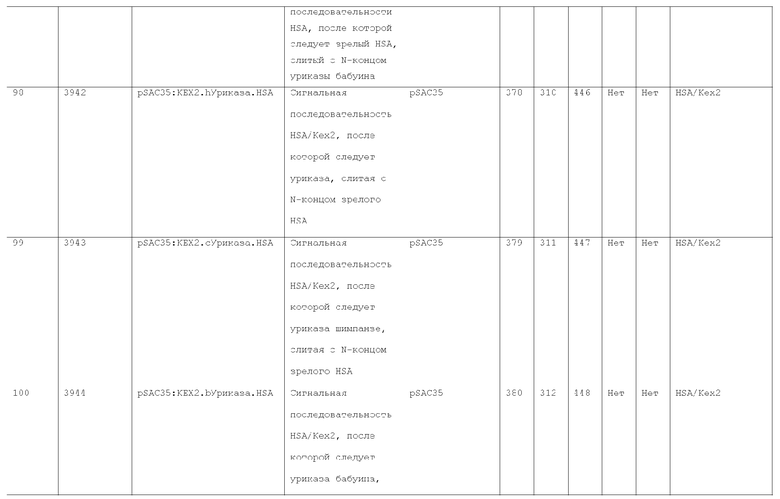
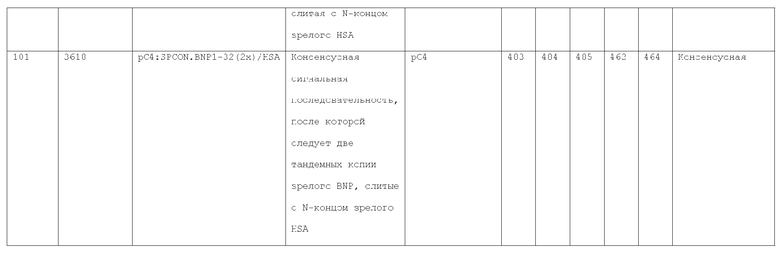
7. Слитый с альбумином белок по п.1, продуцируемый из хозяйской клетки, содержащей конструкцию, которая экспрессирует указанный слитый с альбумином белок, где указанная конструкция выбрана из следующих конструкций, определяемых в таблице 2:
(a) конструкции ID 3610; и
(b) конструкции ID 3696.
8. Слитый с альбумином белок по любому из пп.1-7, где указанные по меньшей мере два тандемно ориентированных полипептида GLP-1 слиты с N-концом или с С-концом указанного альбумина, фрагмента альбумина или варианта альбумина.
9. Слитый с альбумином белок по любому из пп.1-8, где указанный альбумин представляет собой человеческий альбумин.
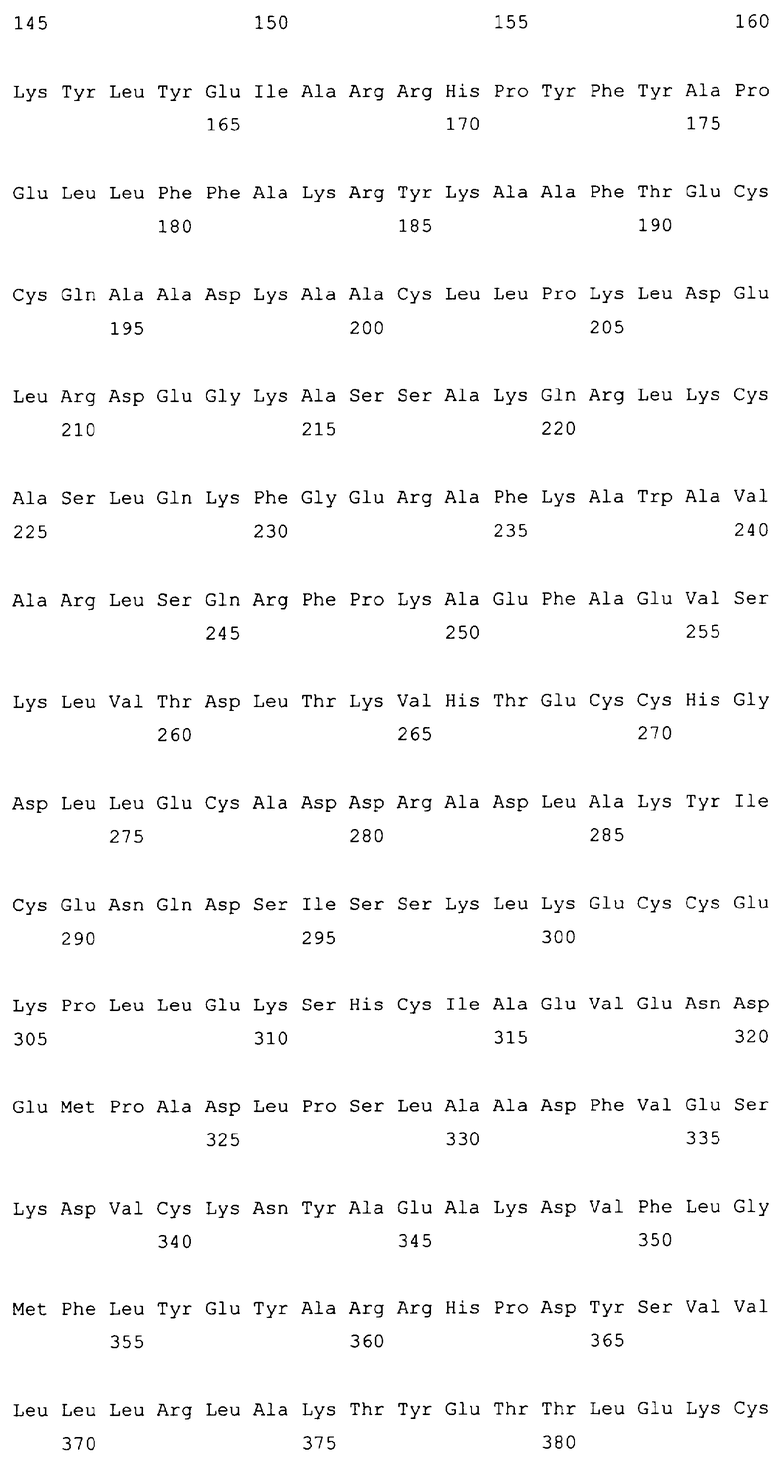
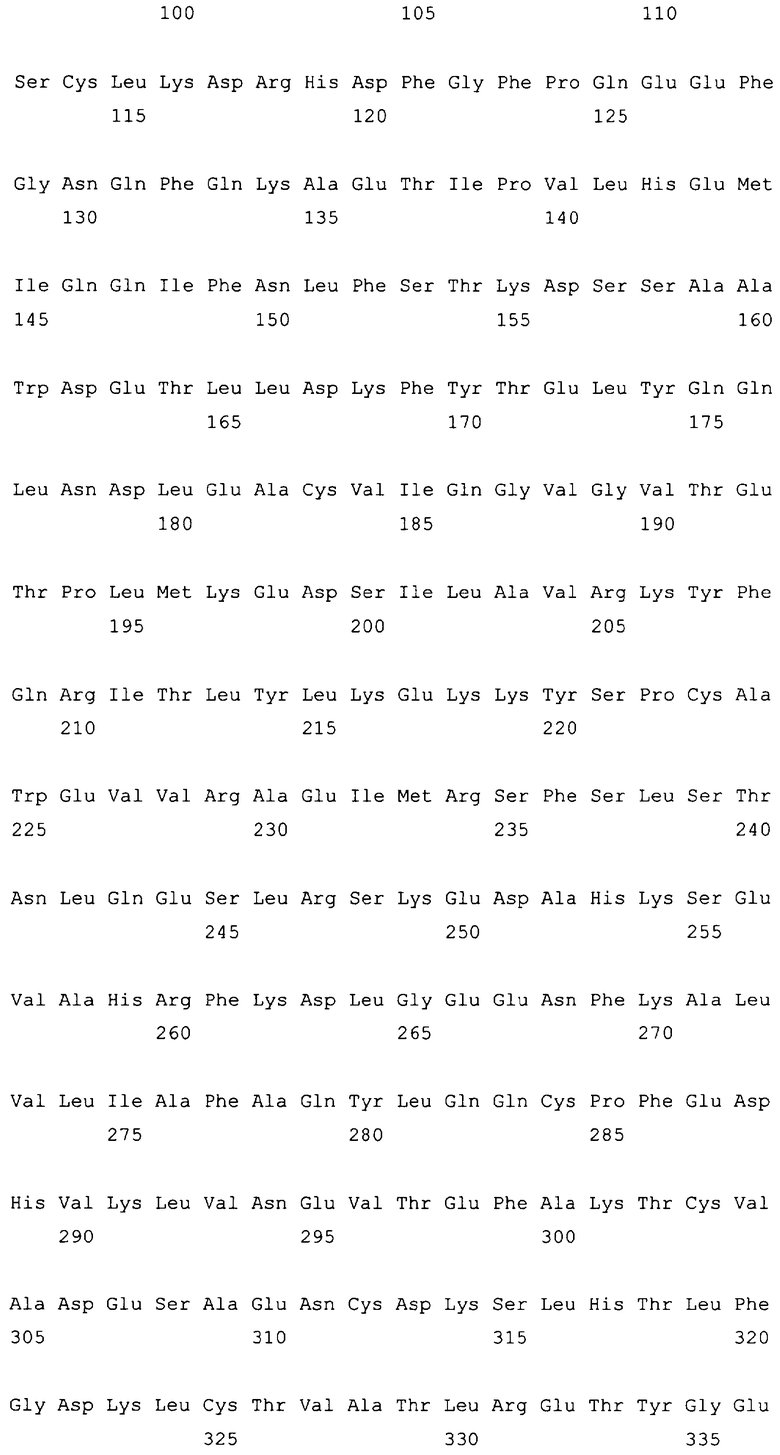
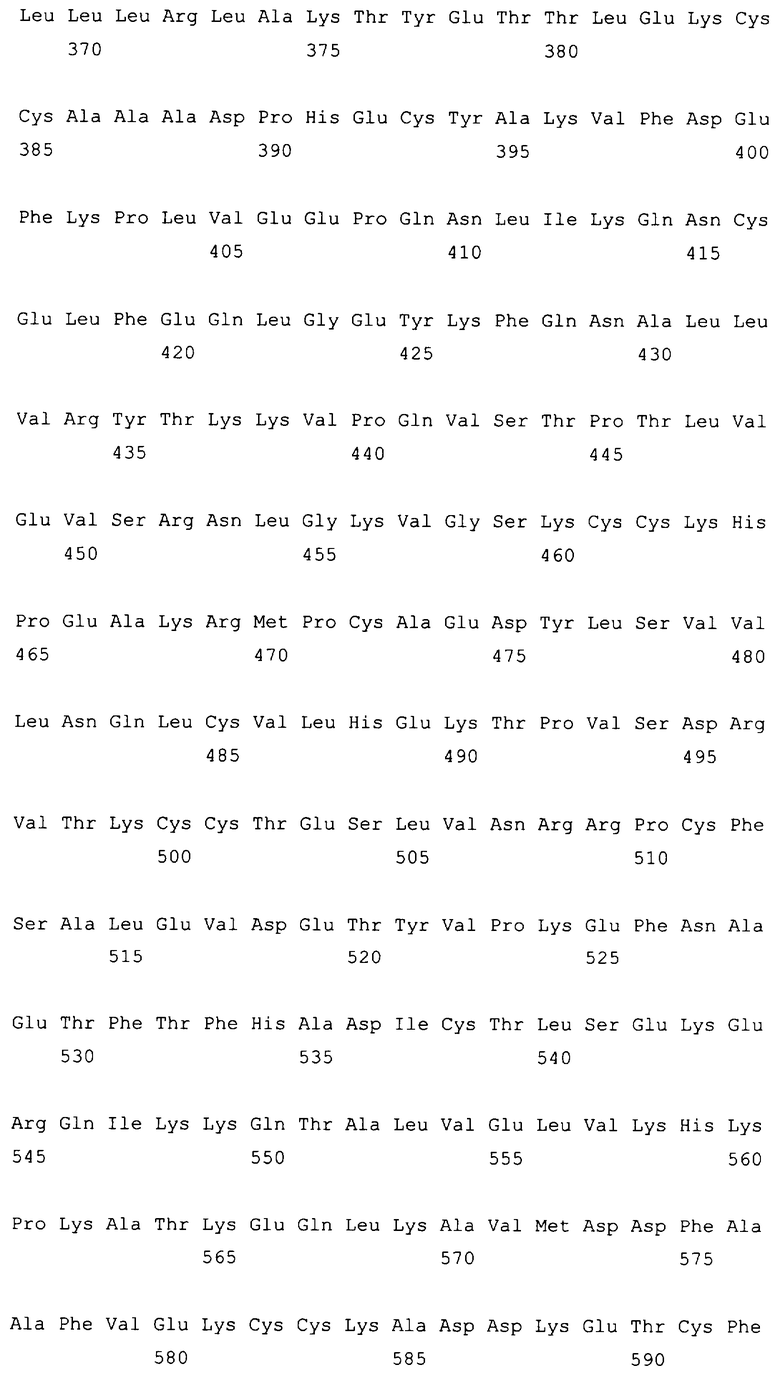
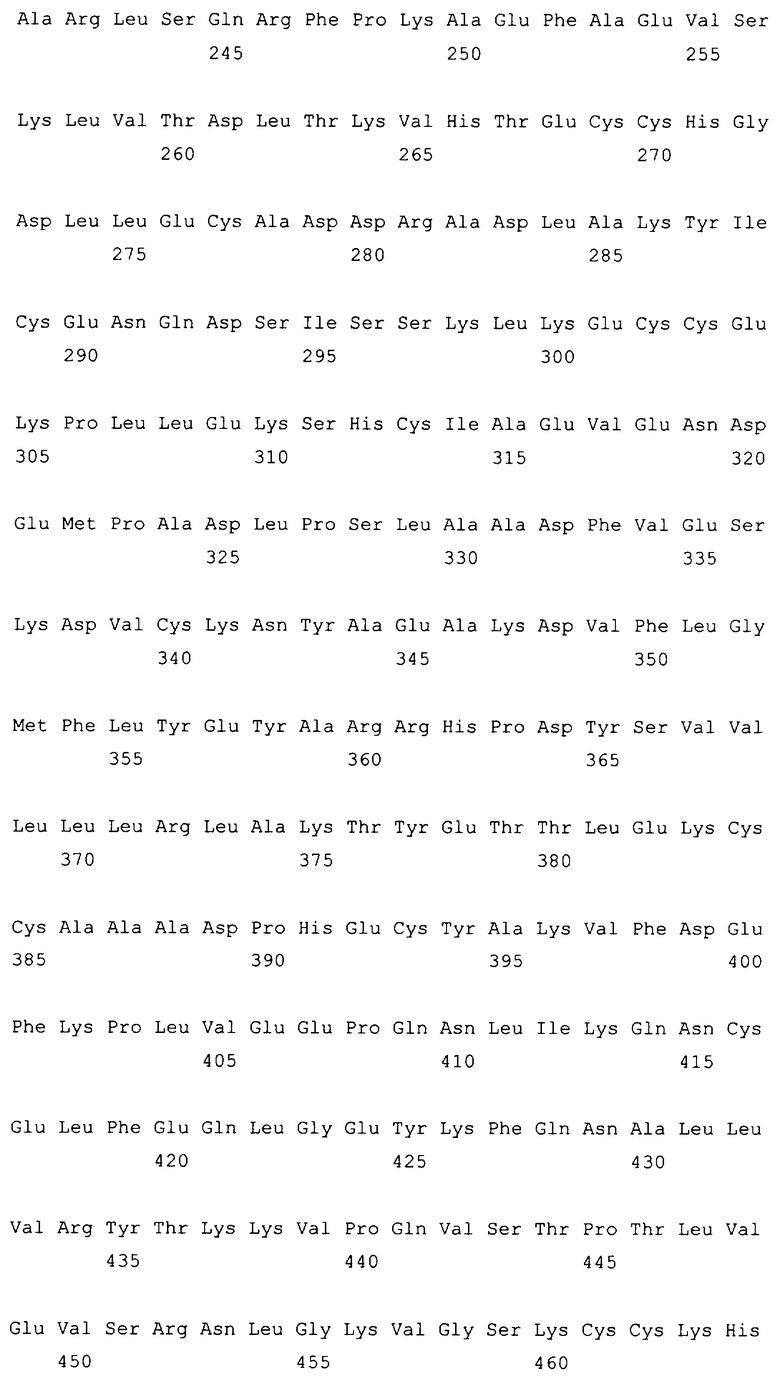
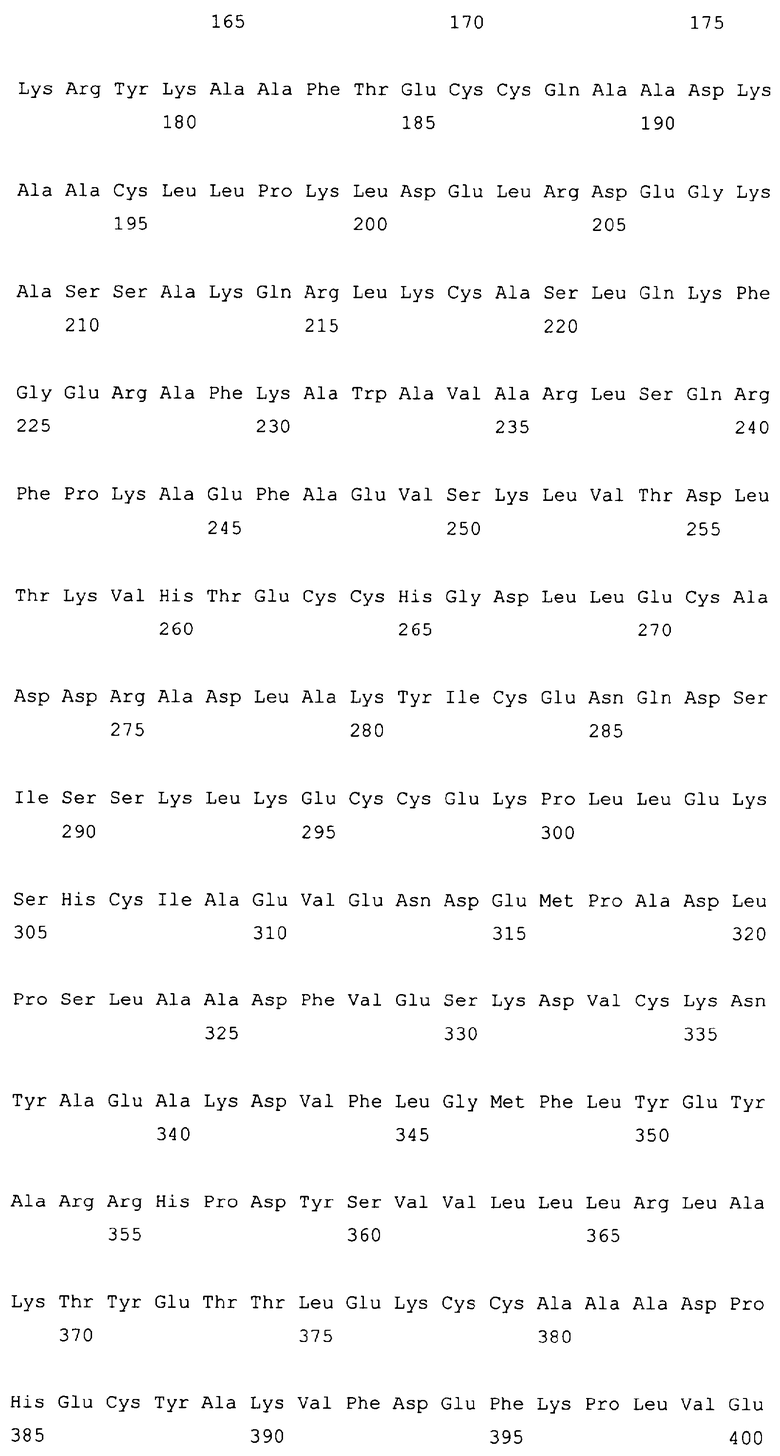
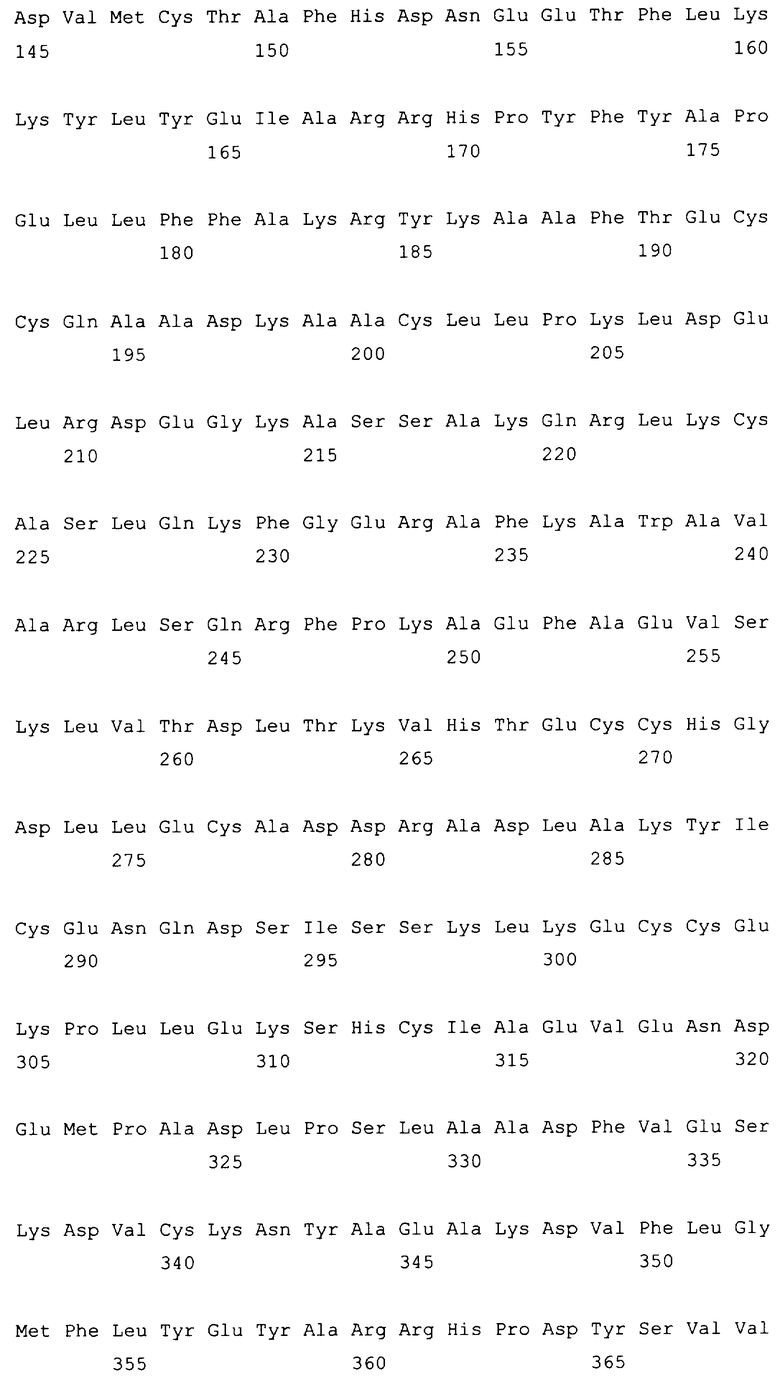
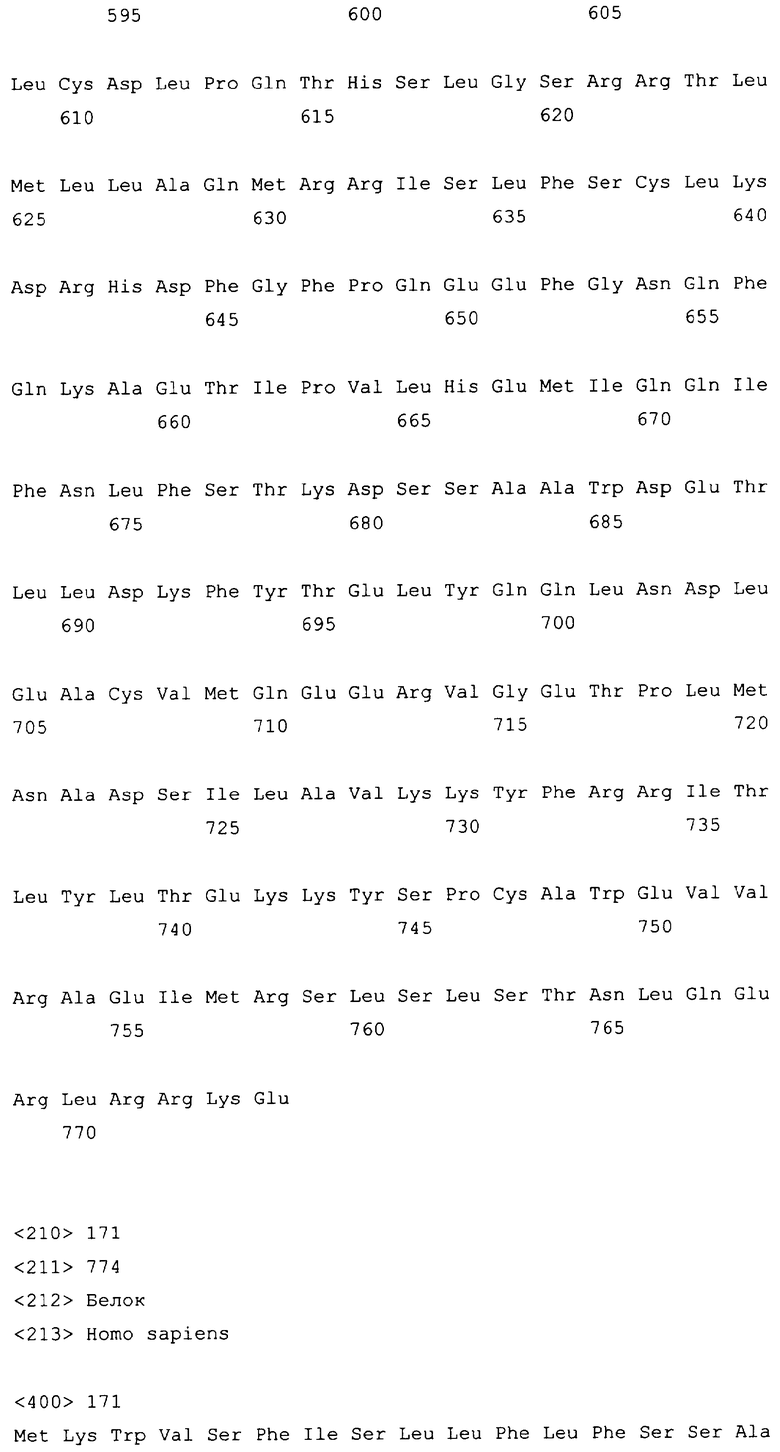
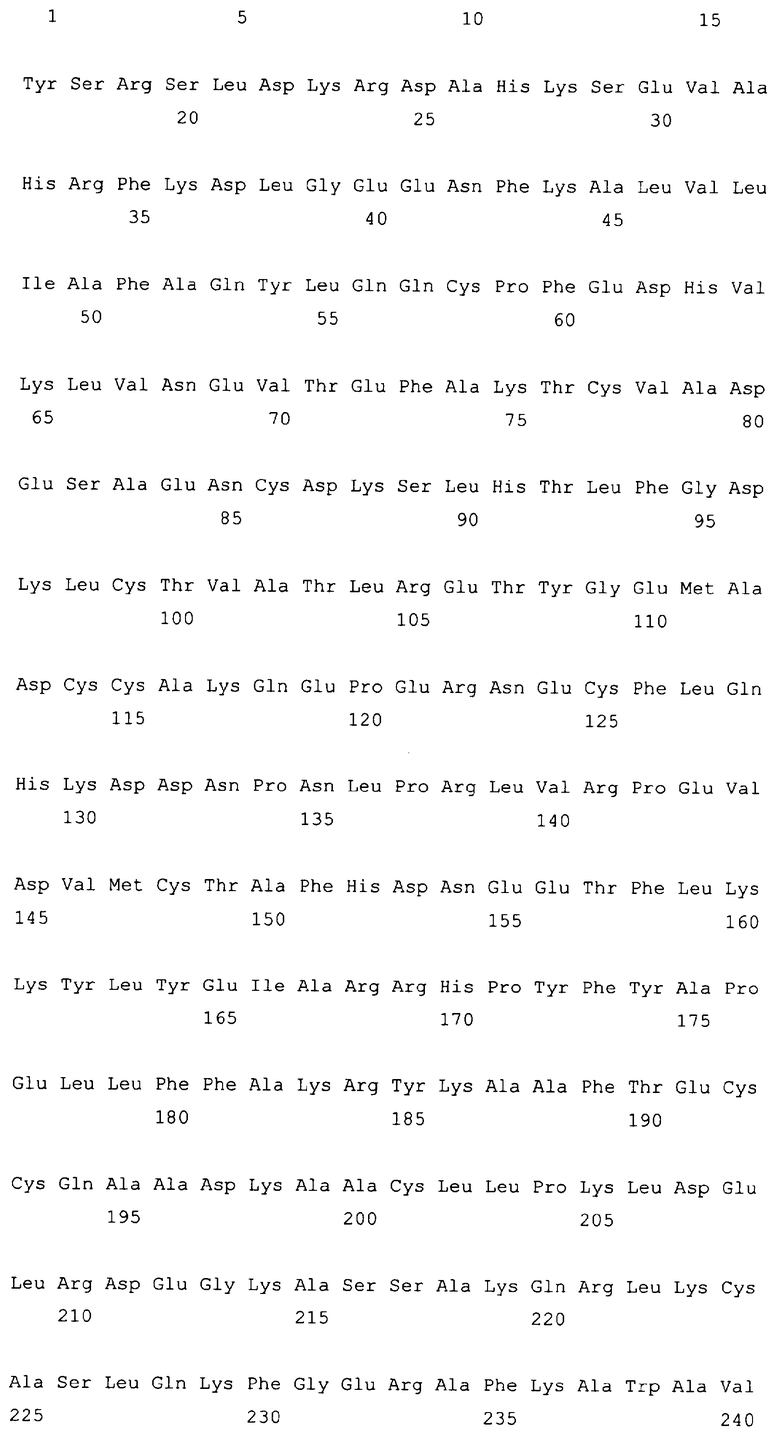
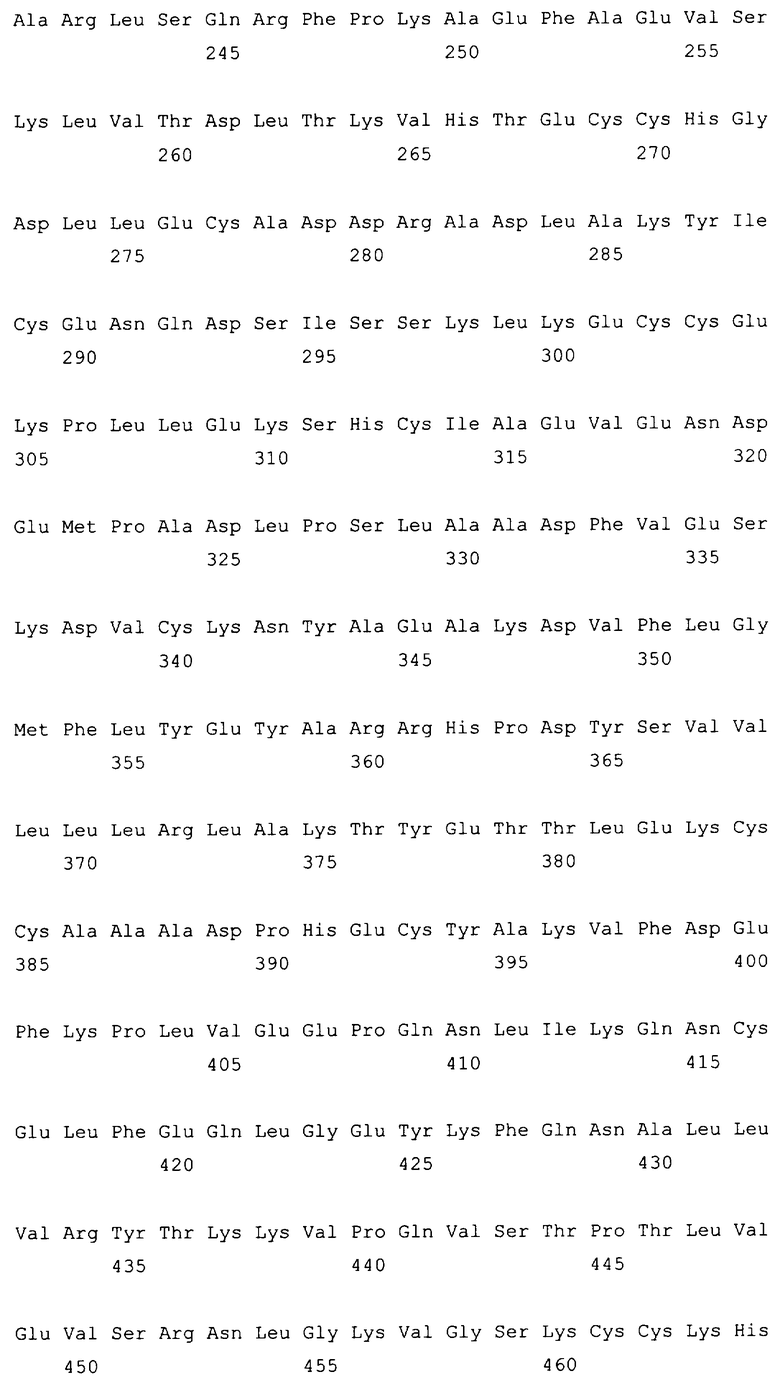
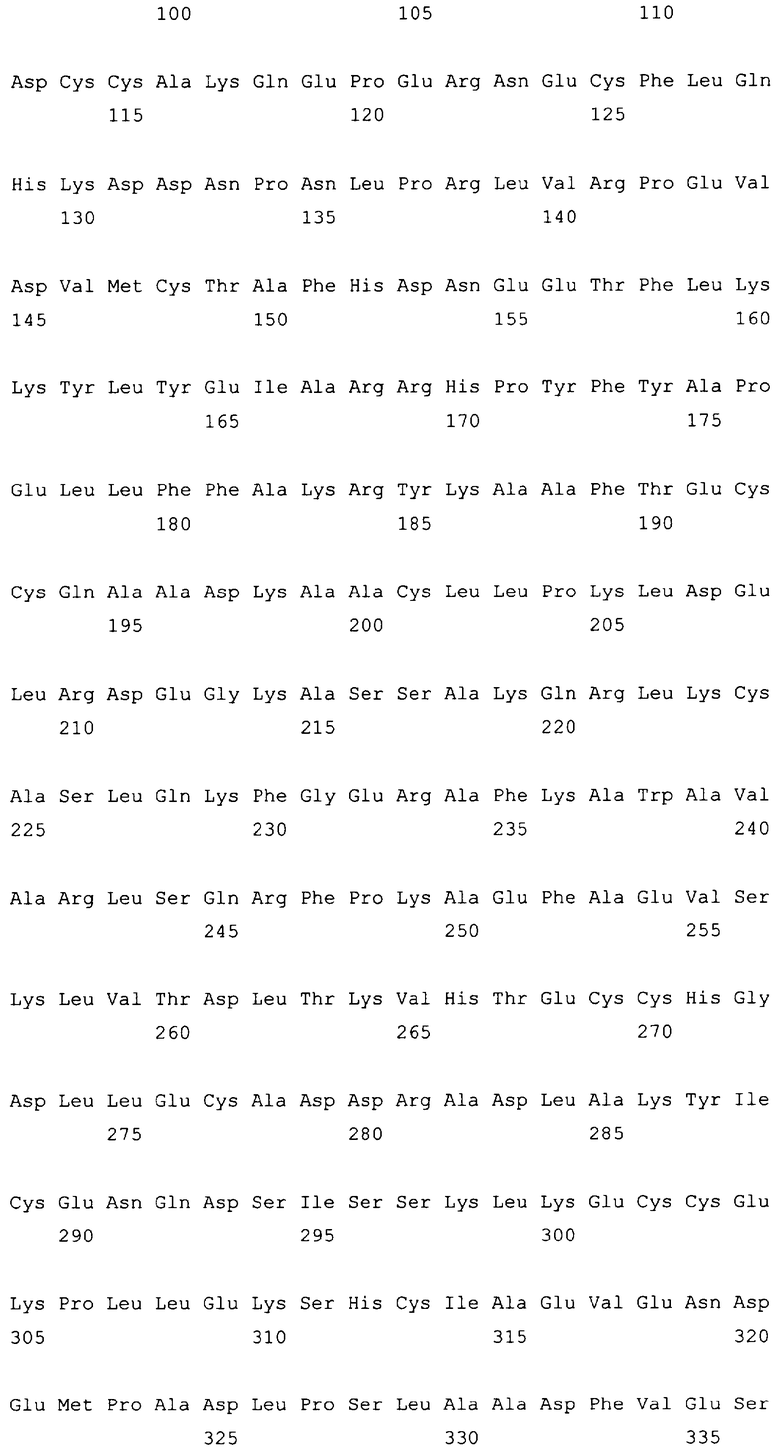
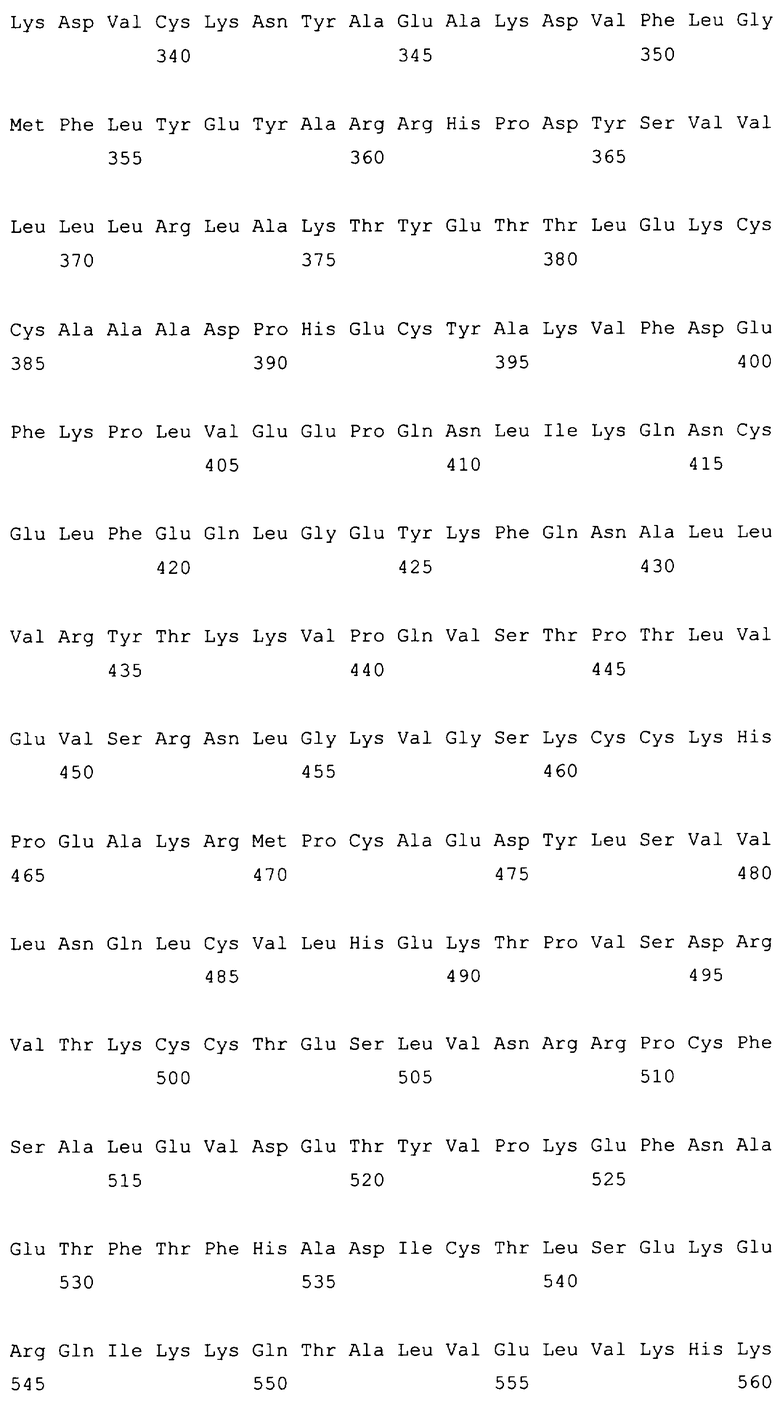
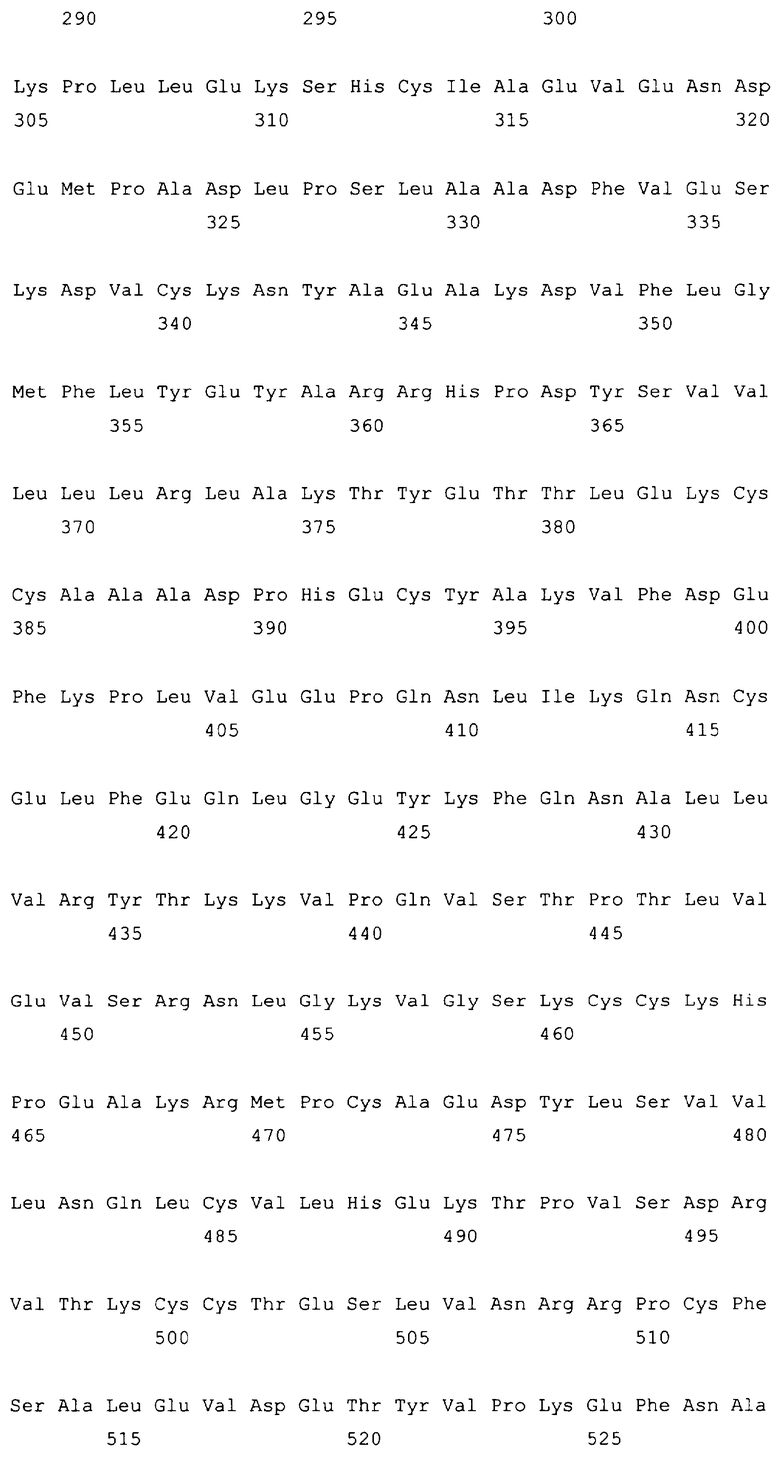
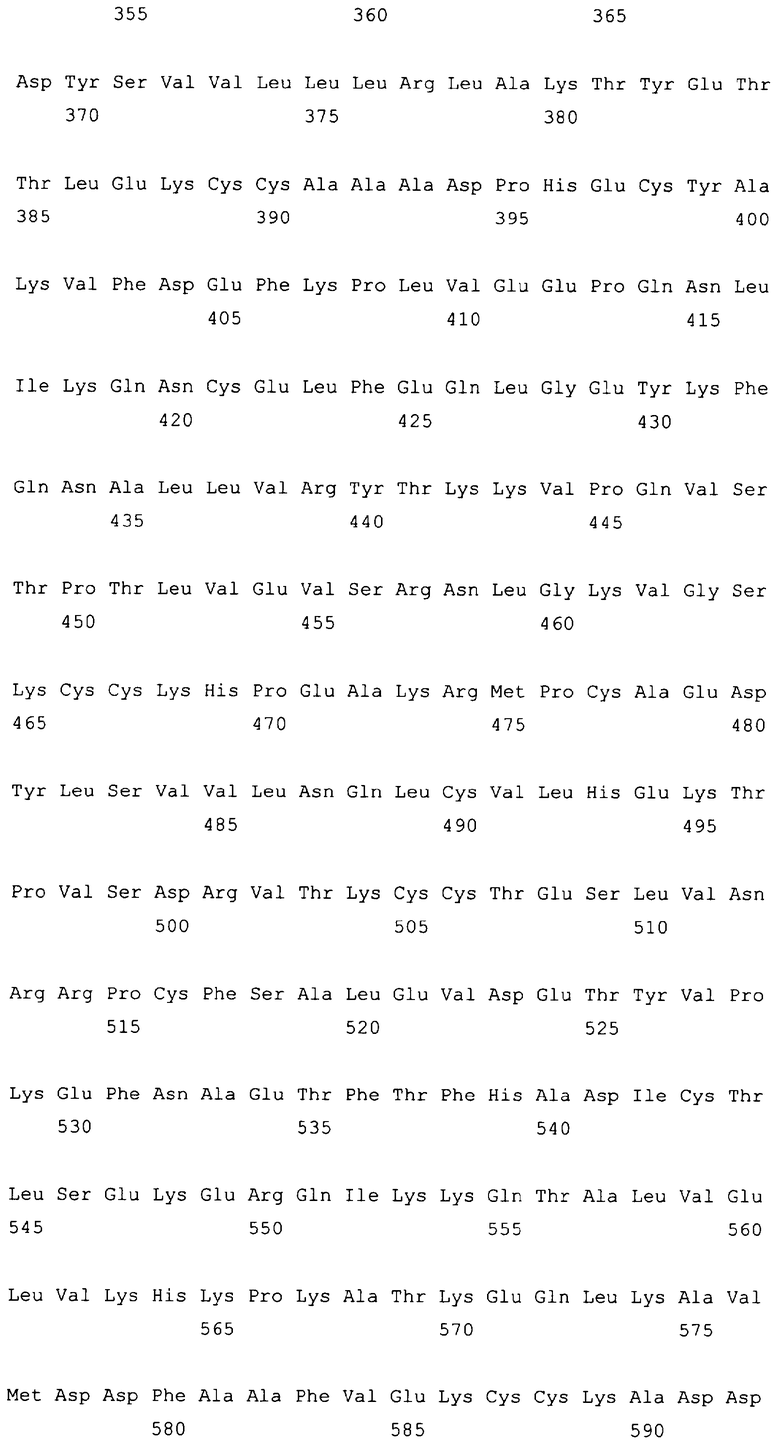
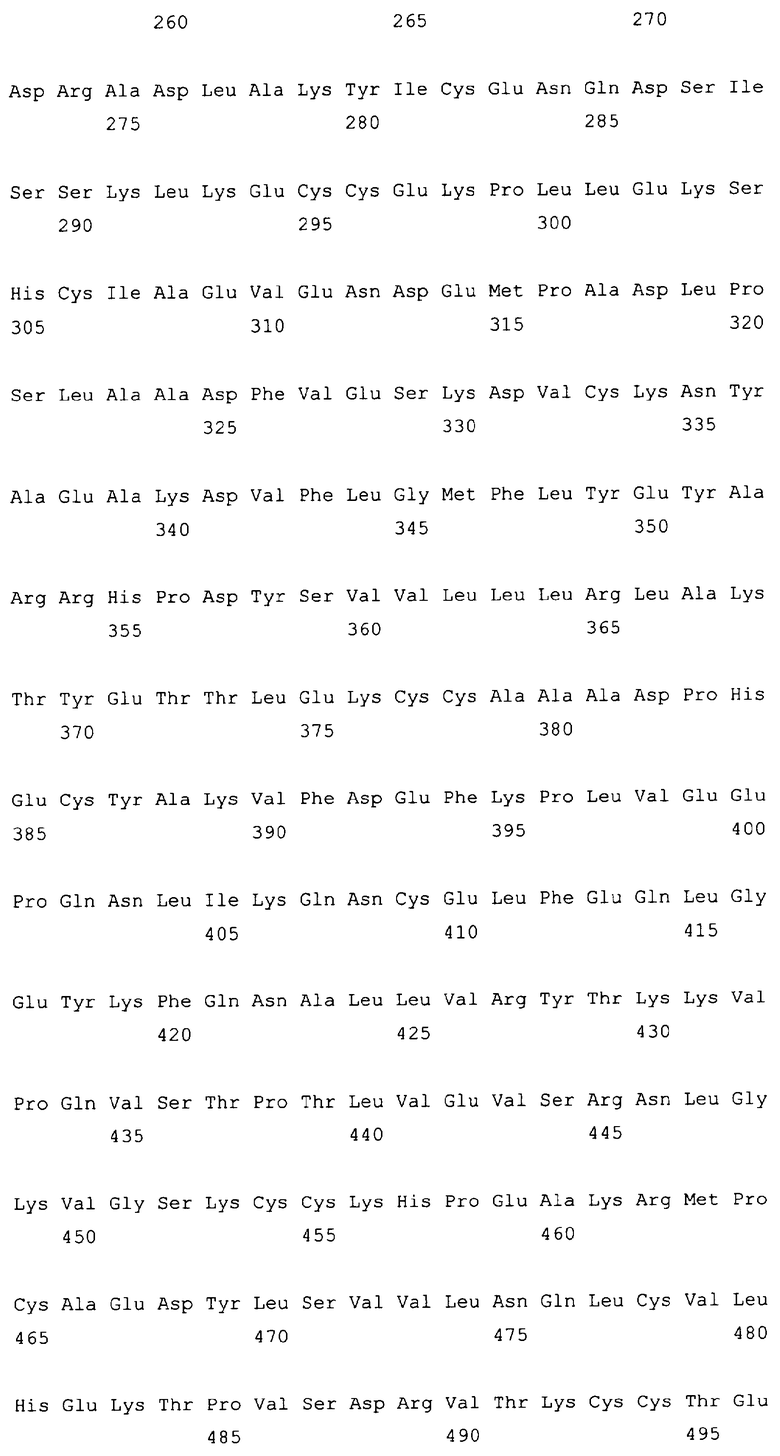
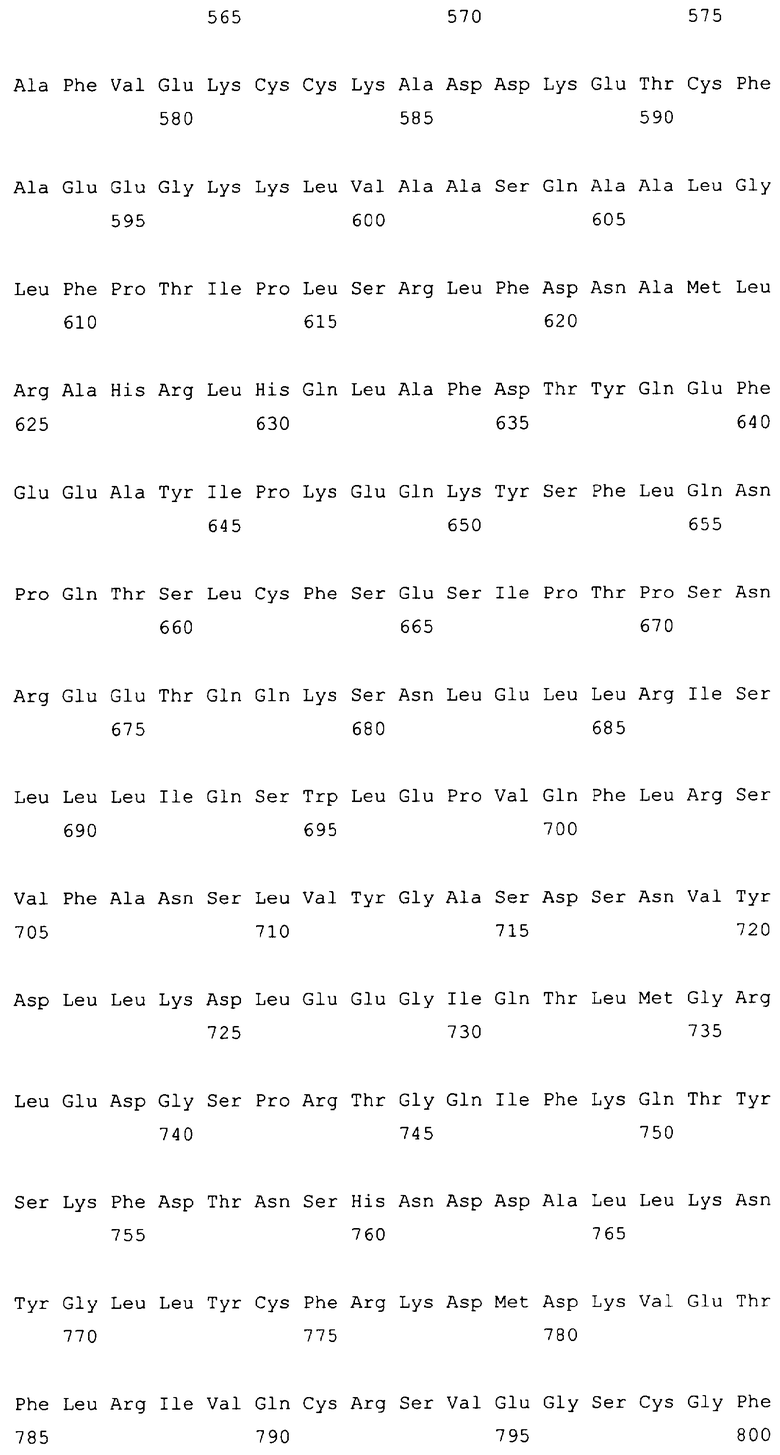
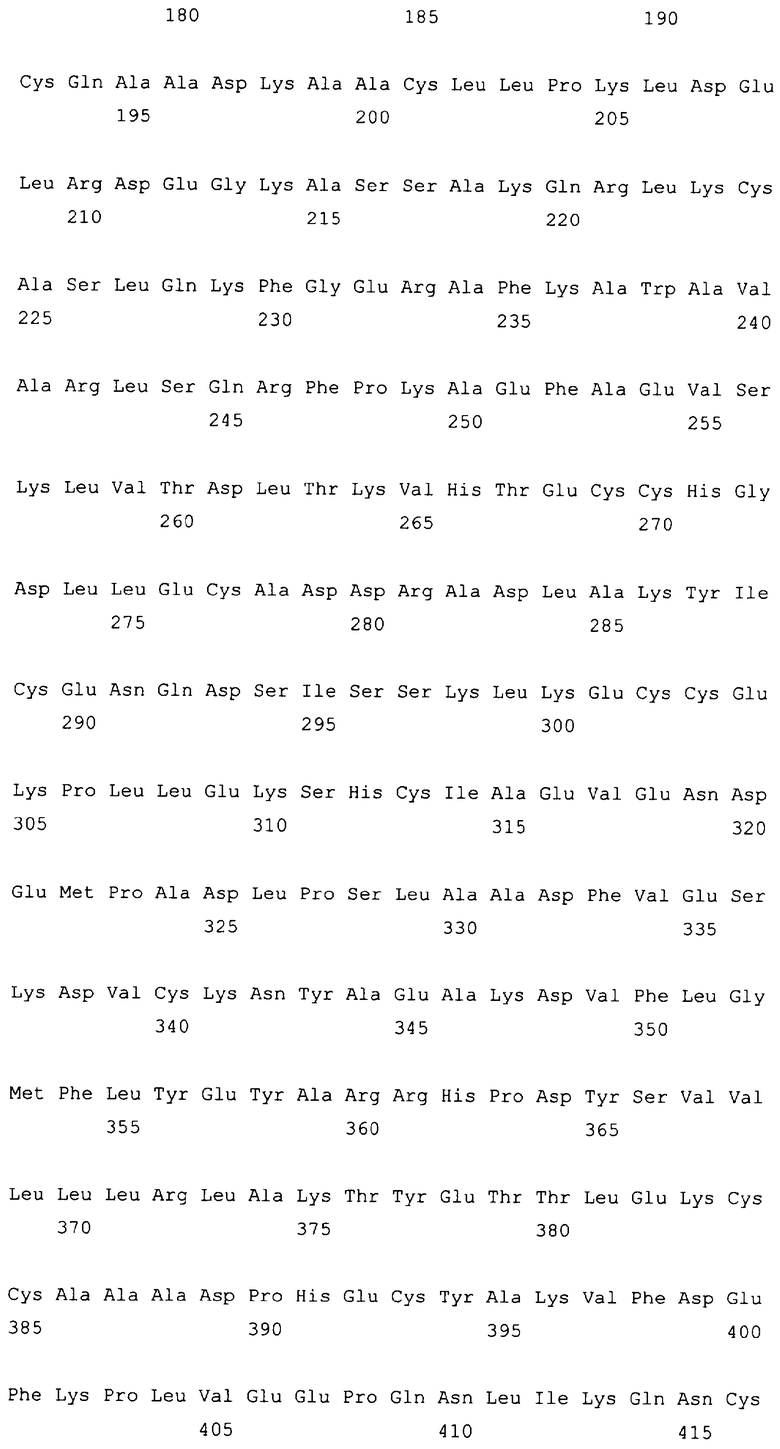
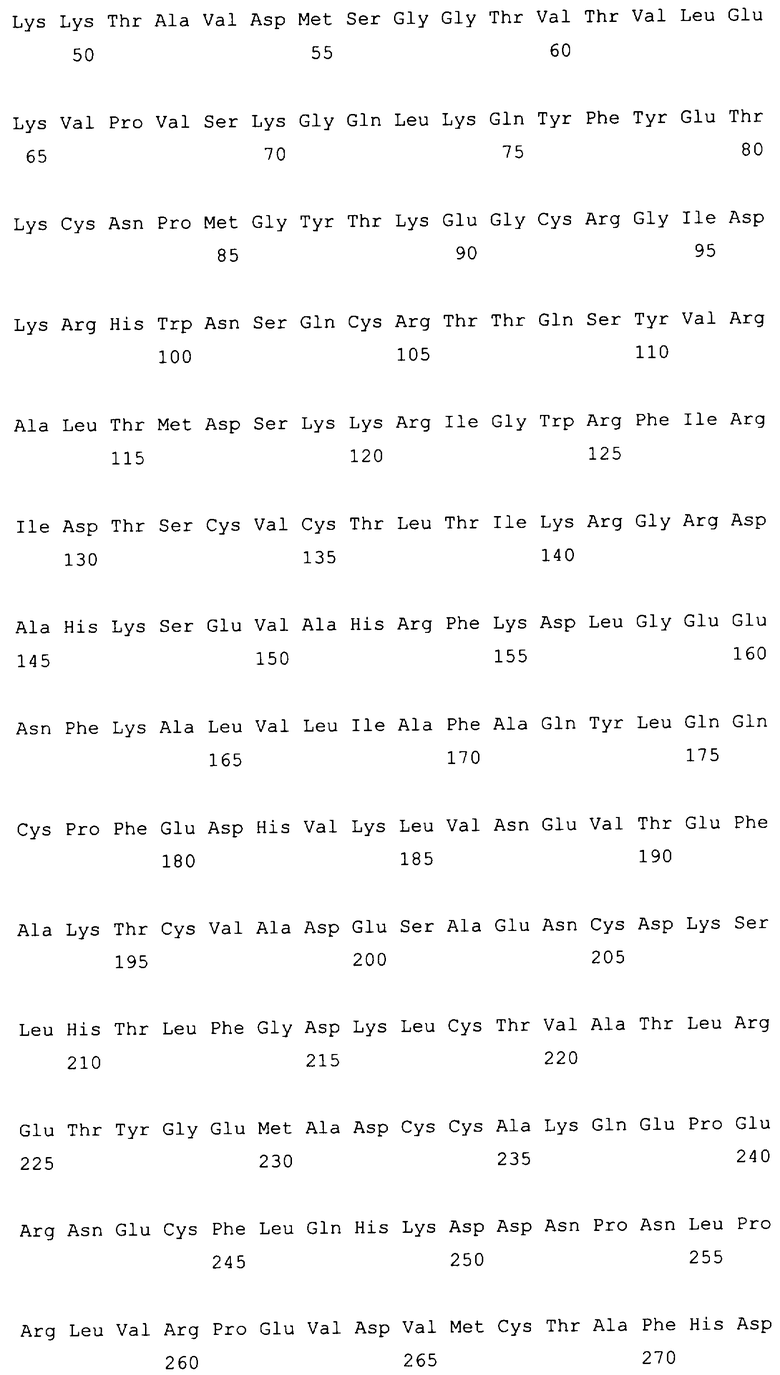
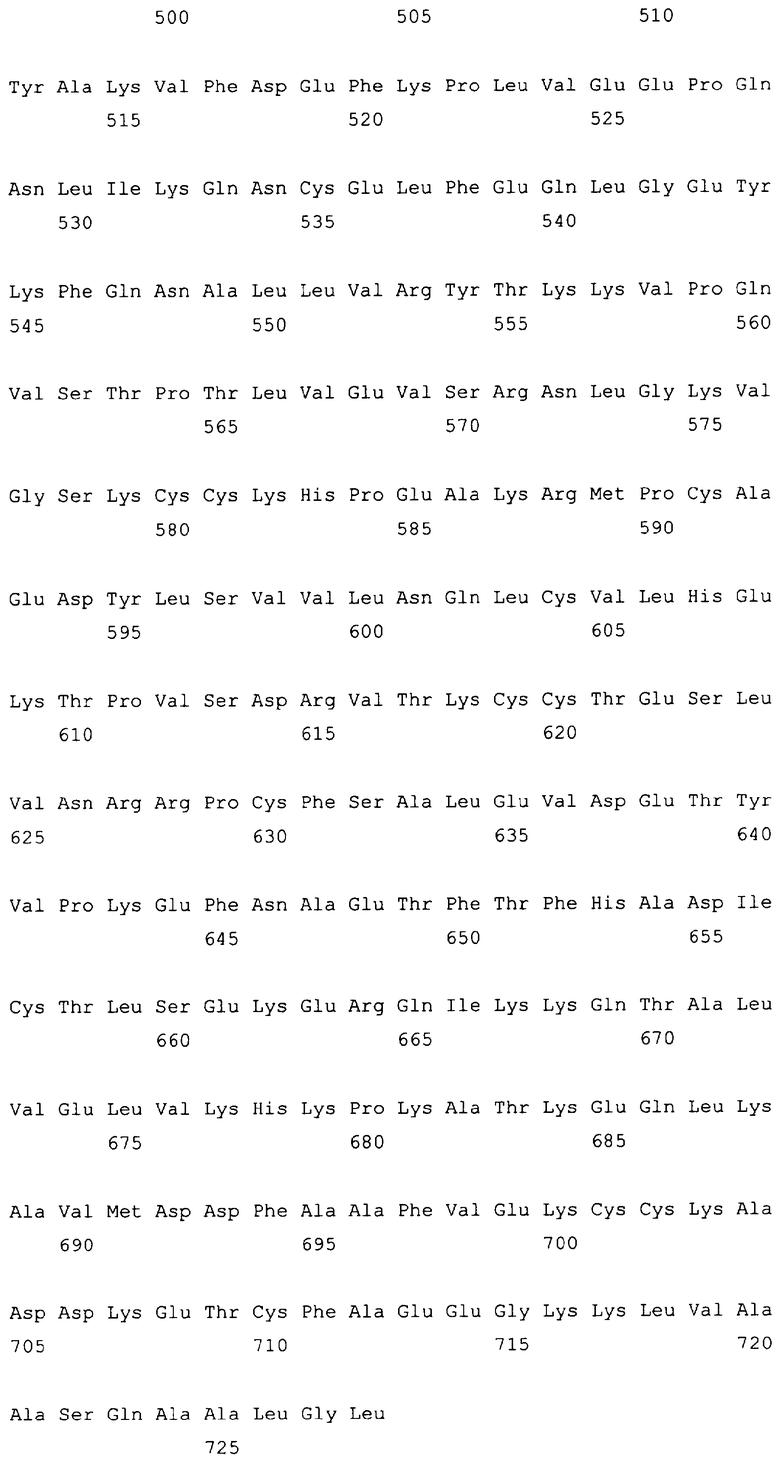
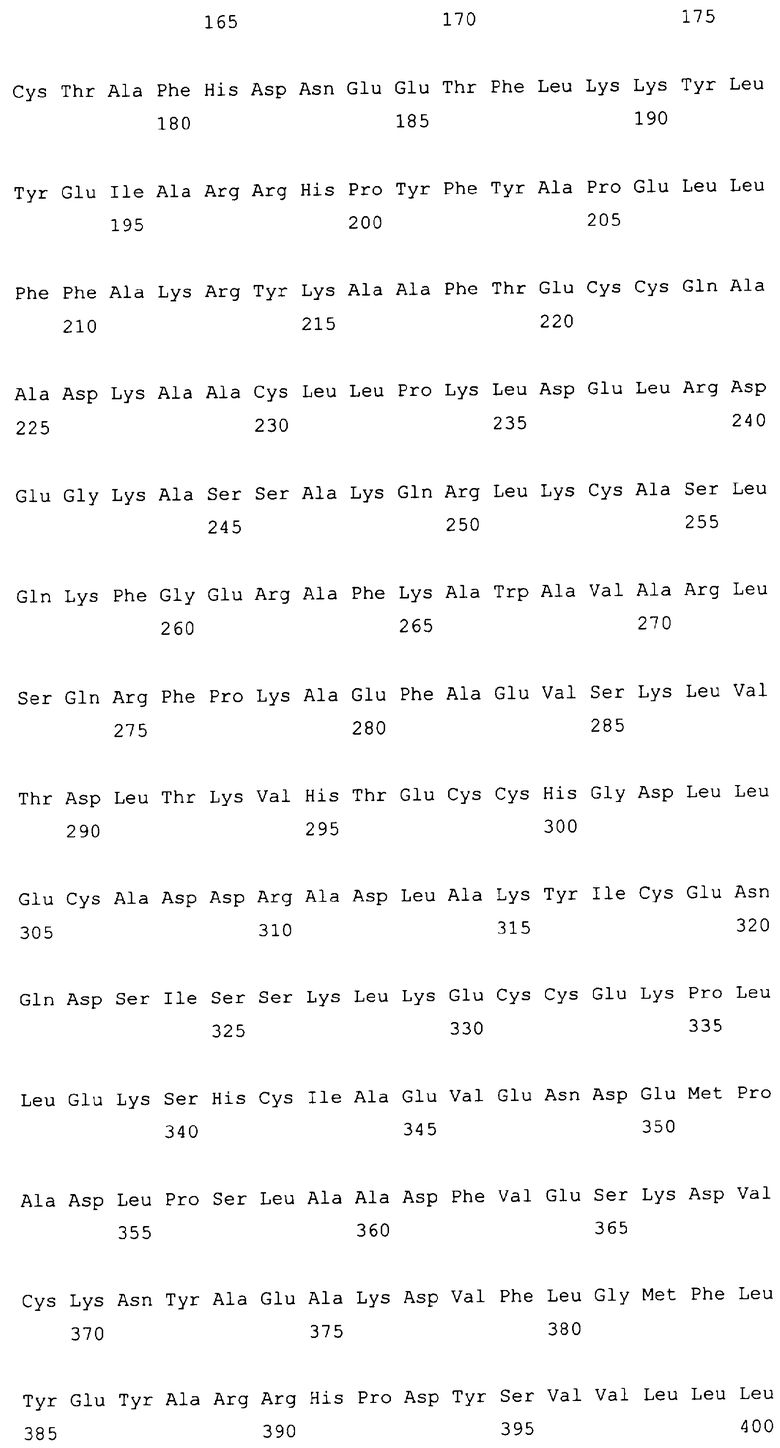
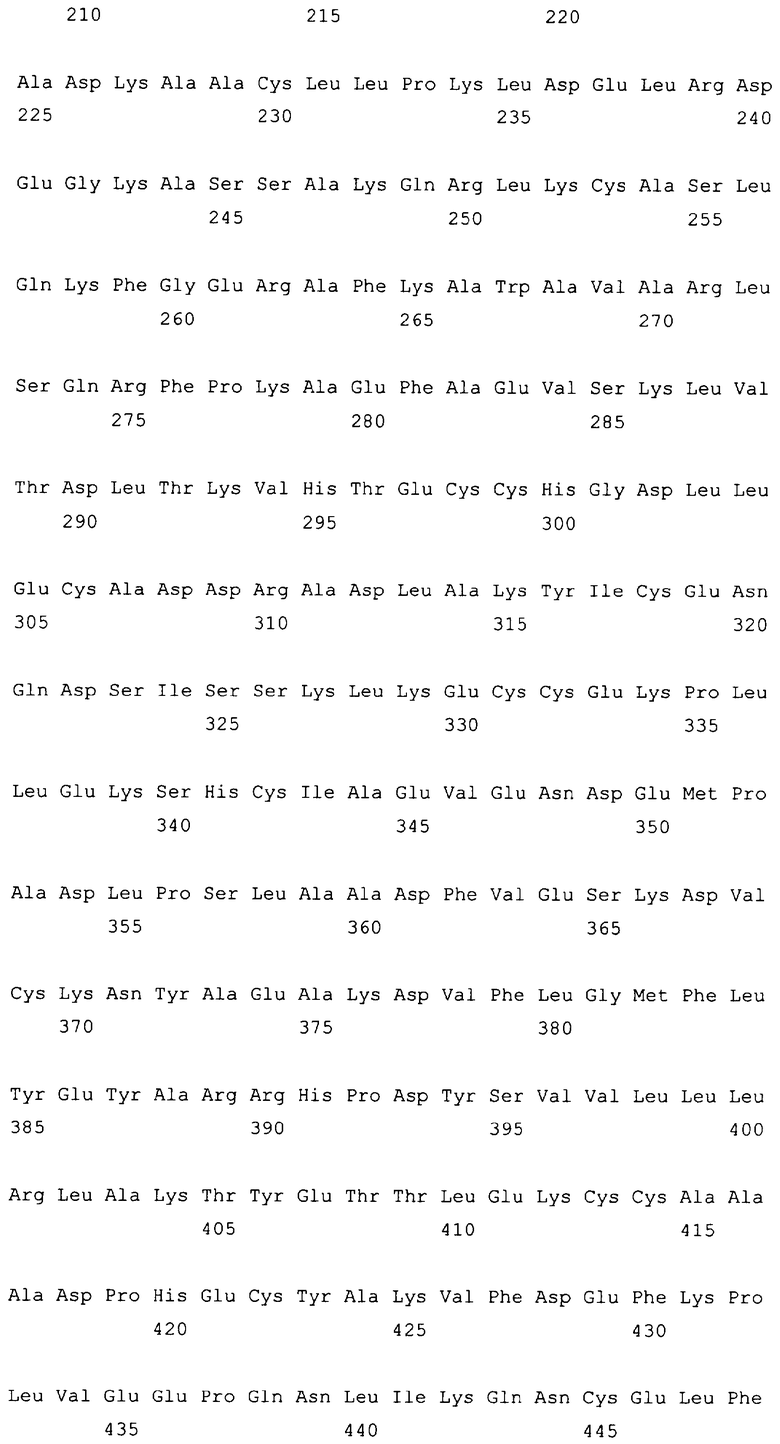
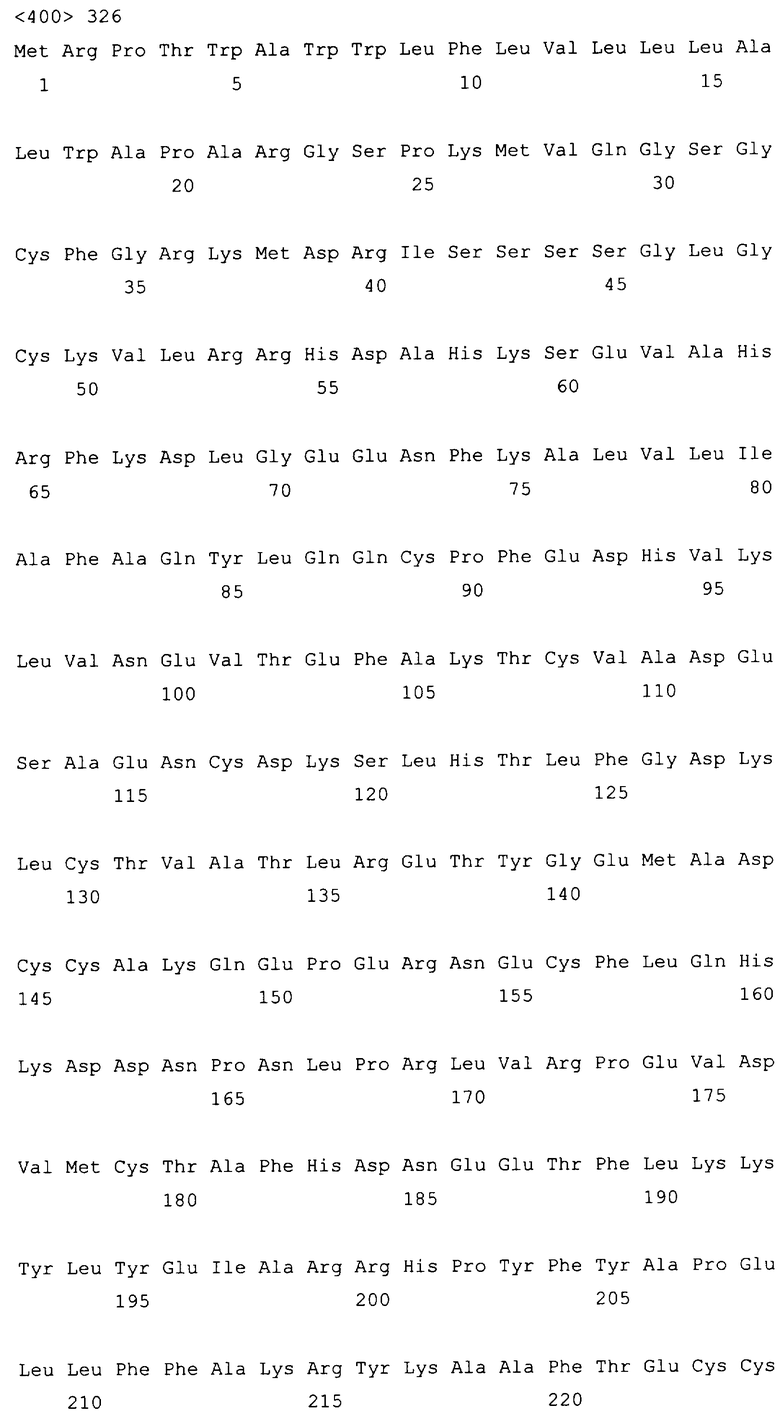
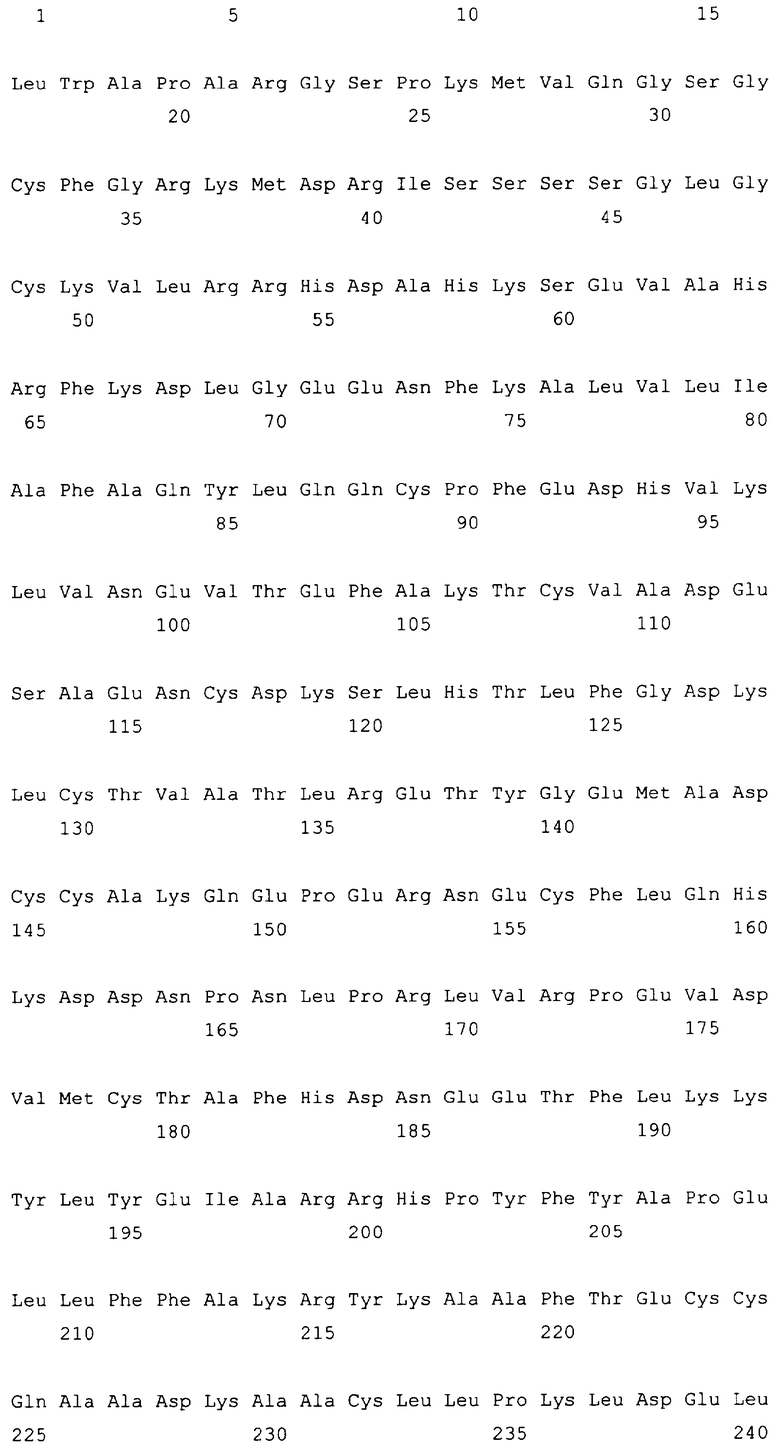
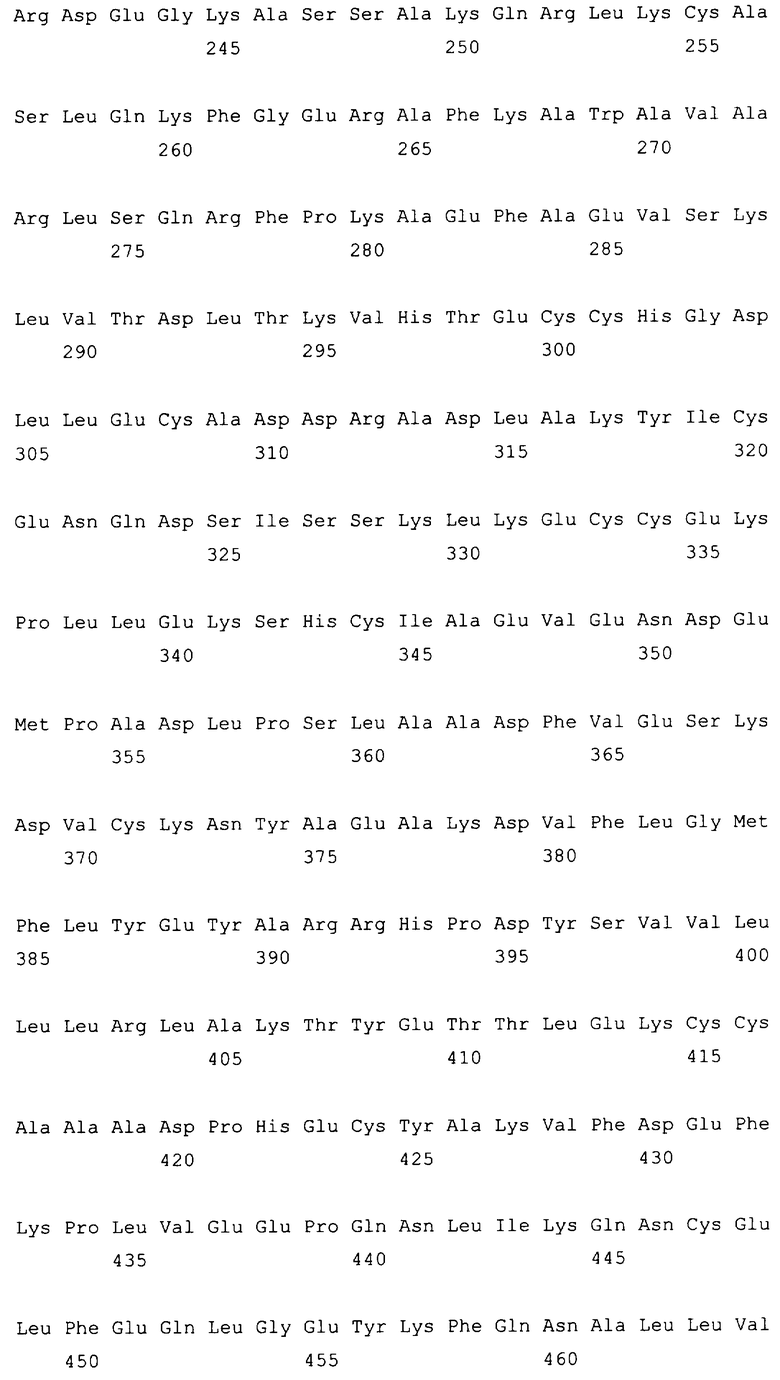
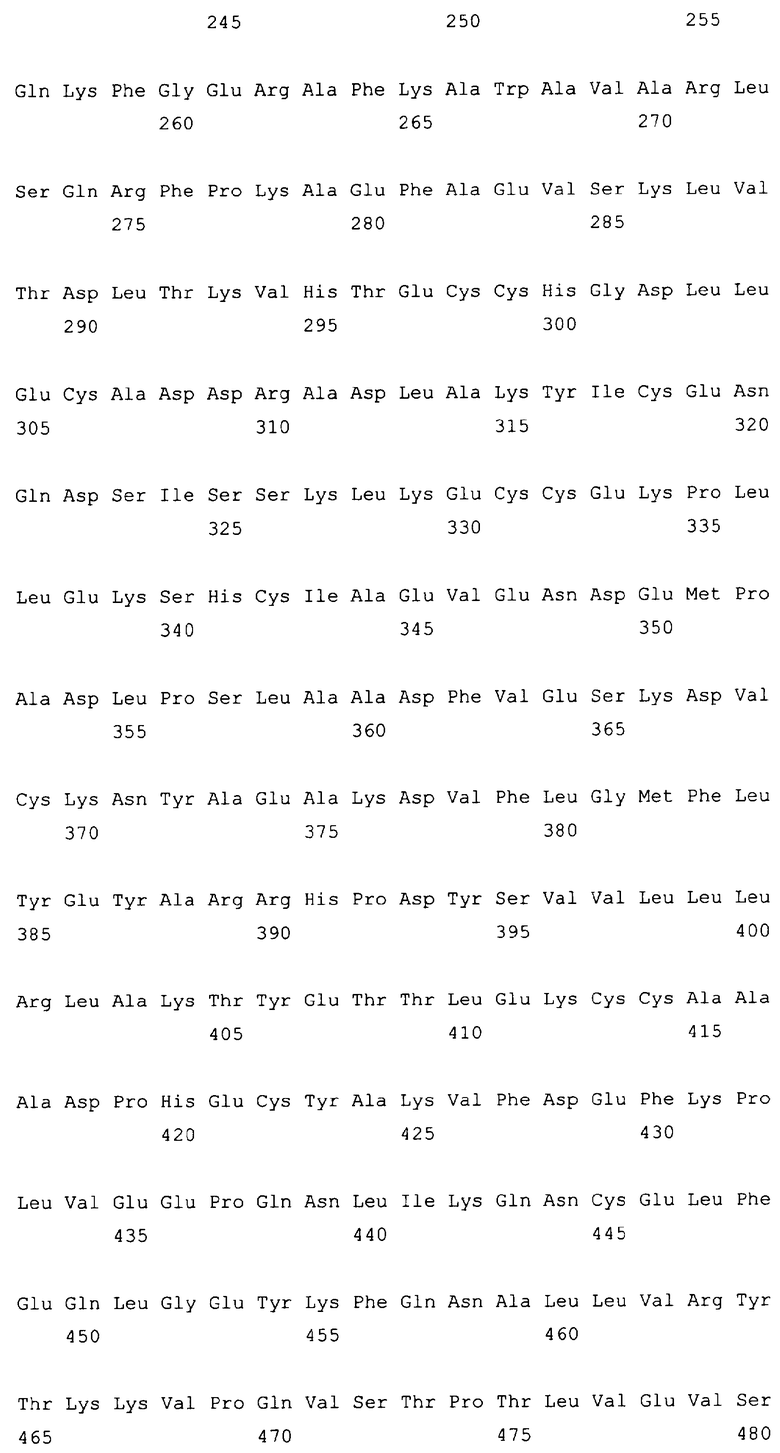
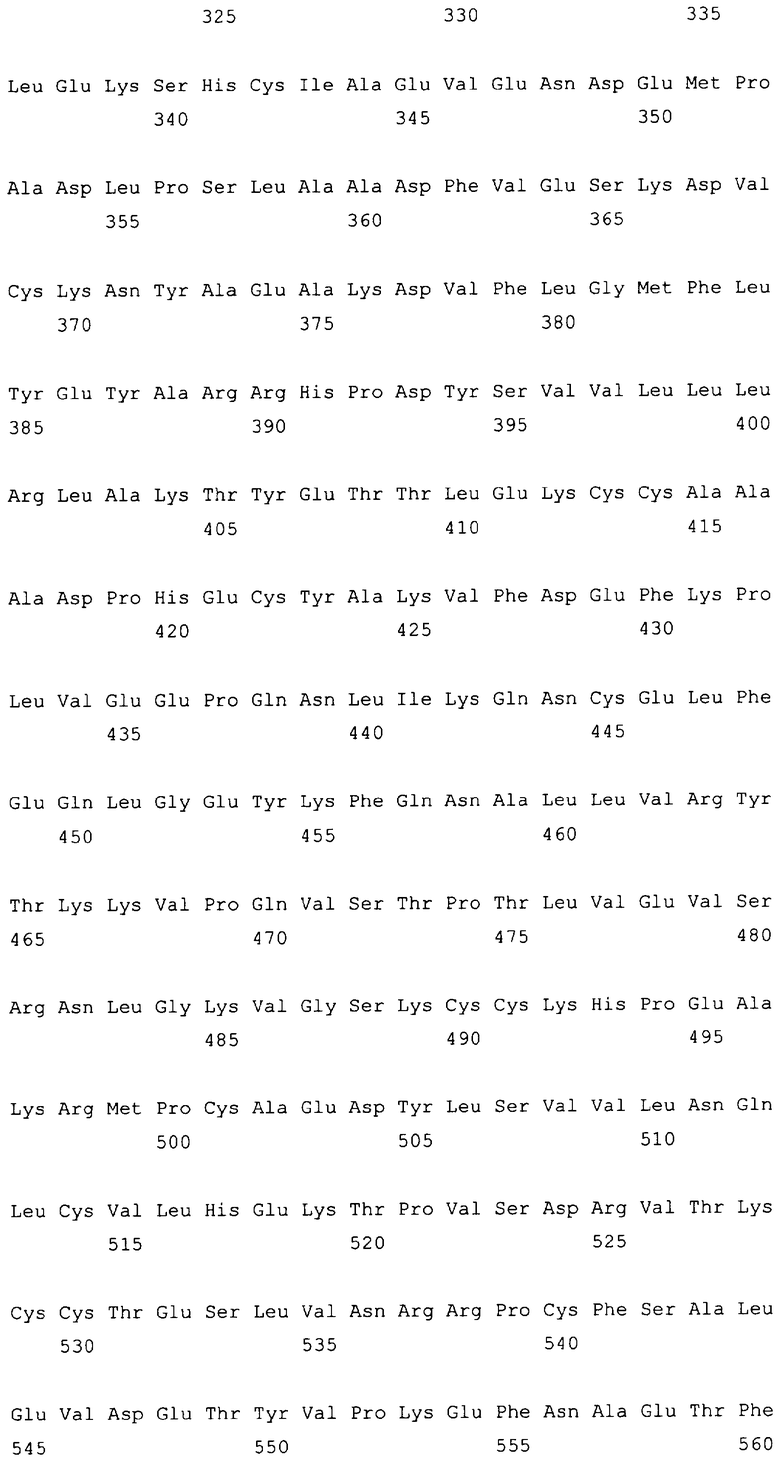
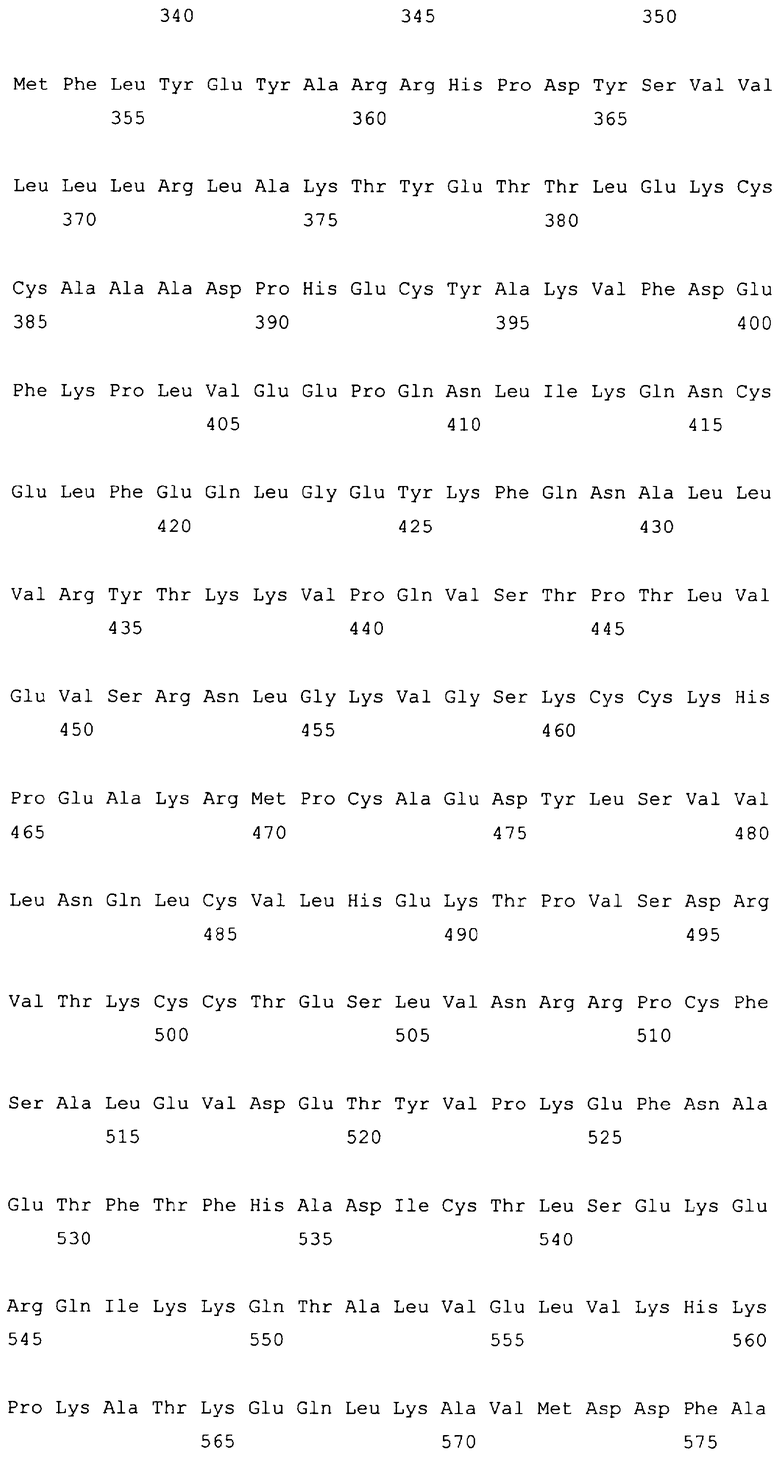
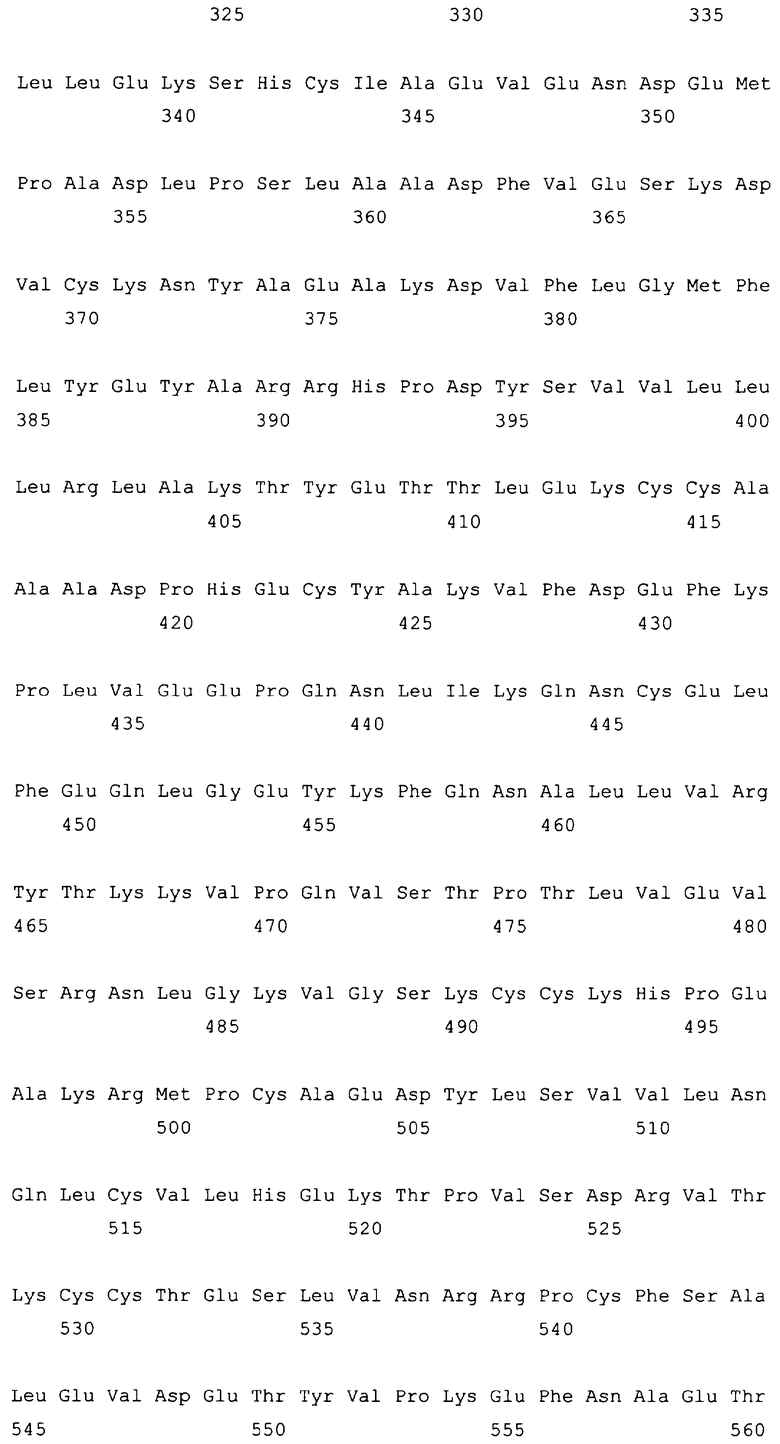
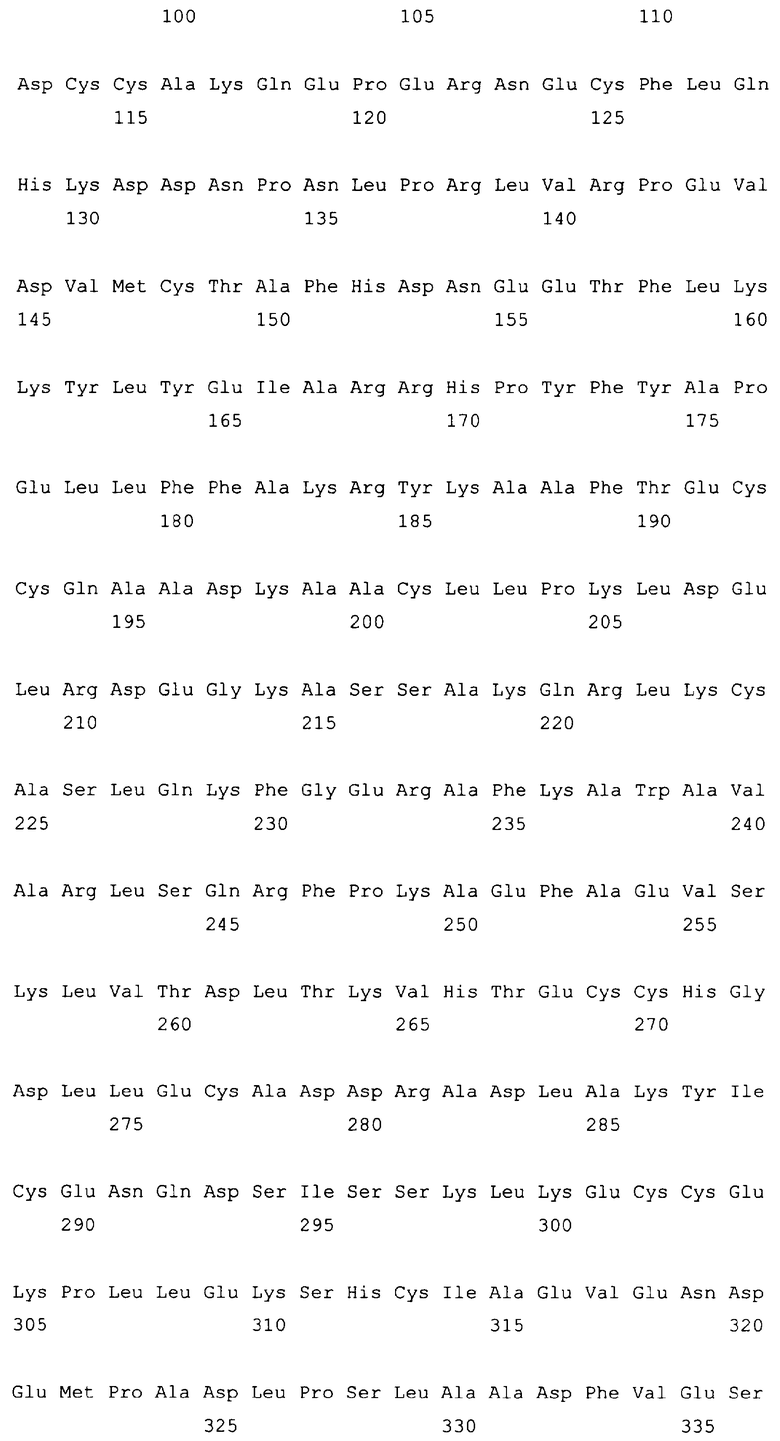
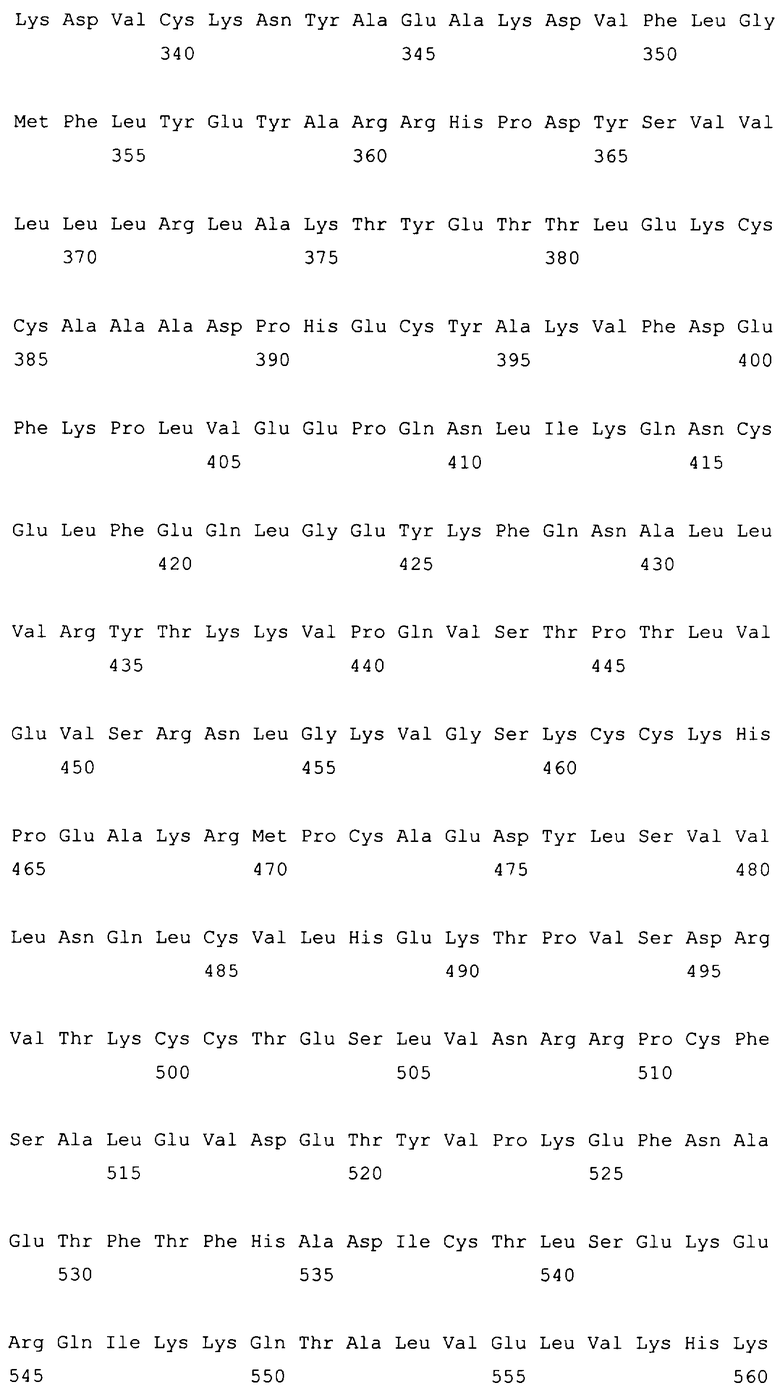
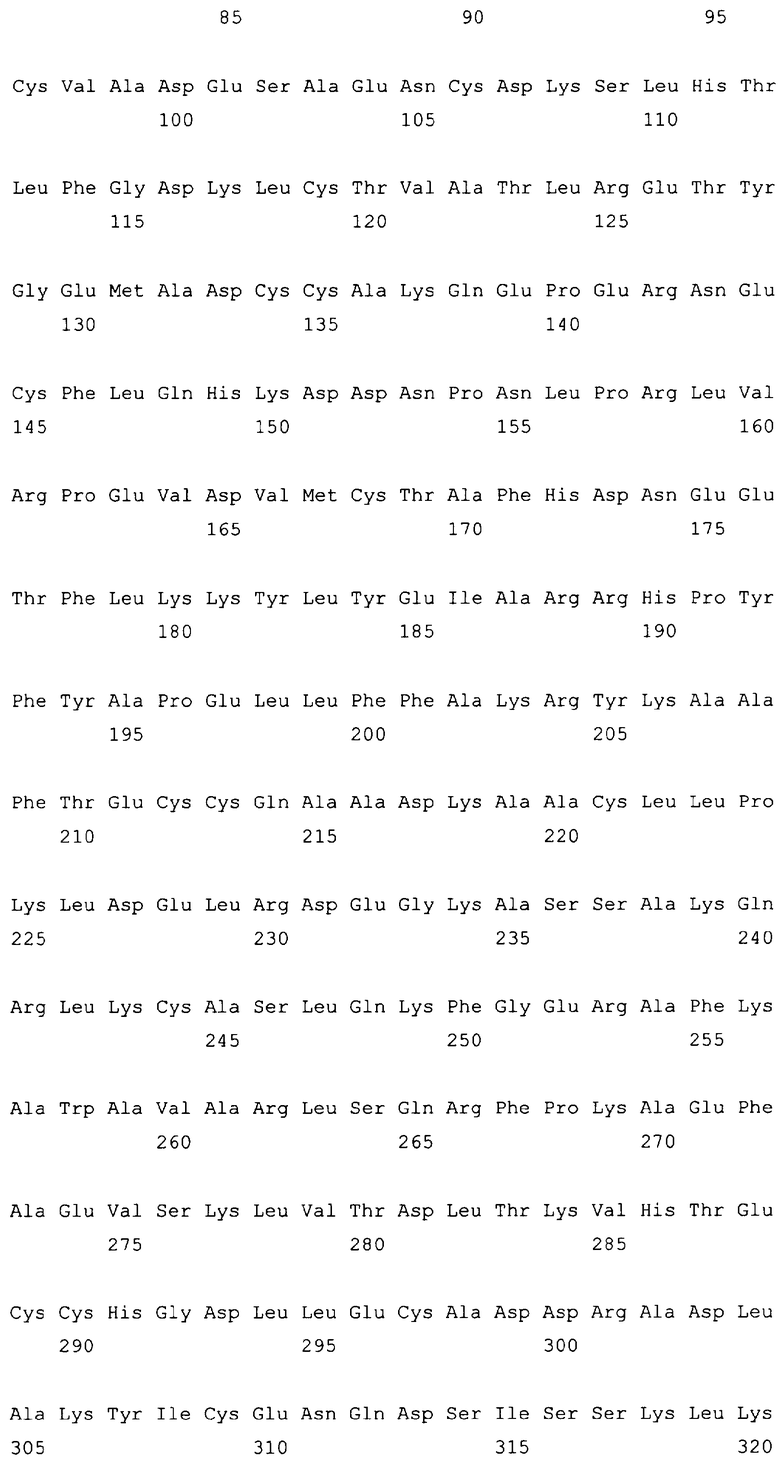
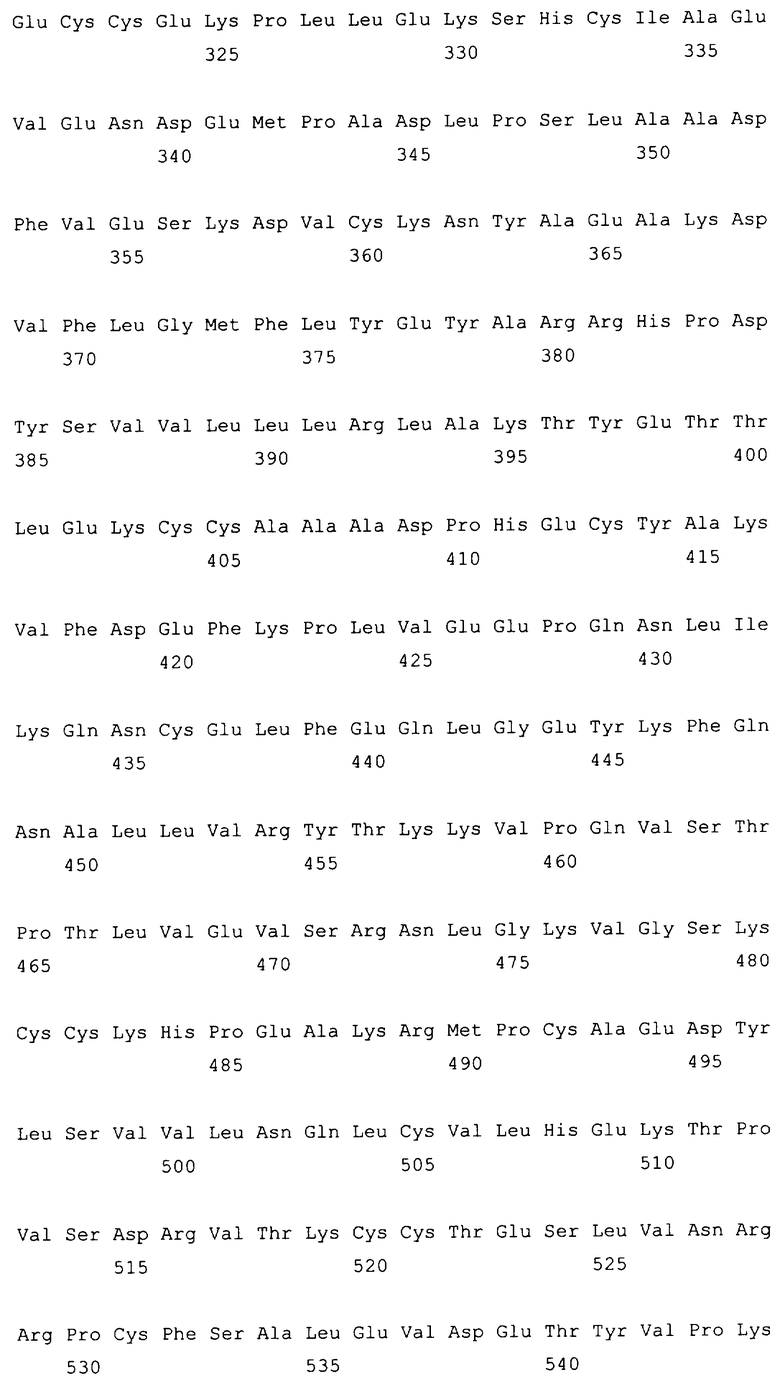
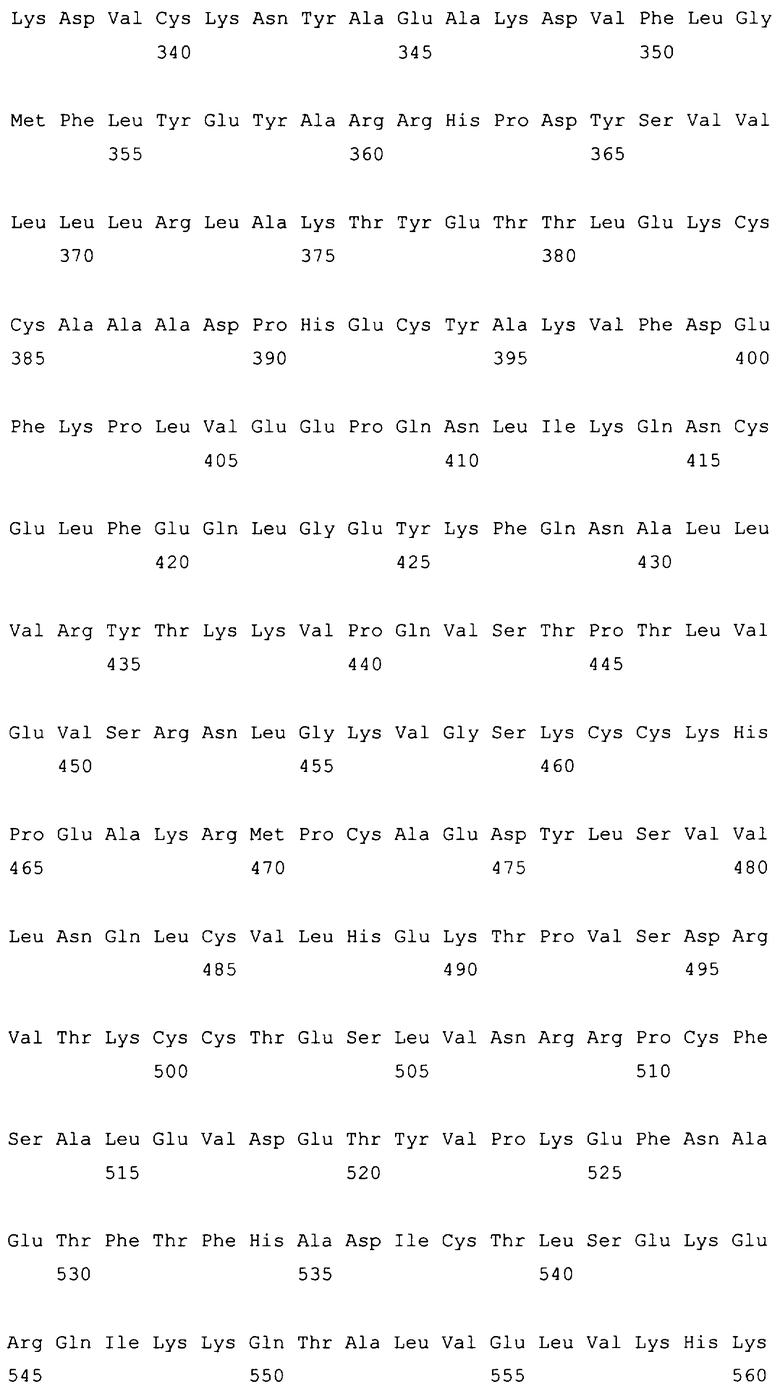
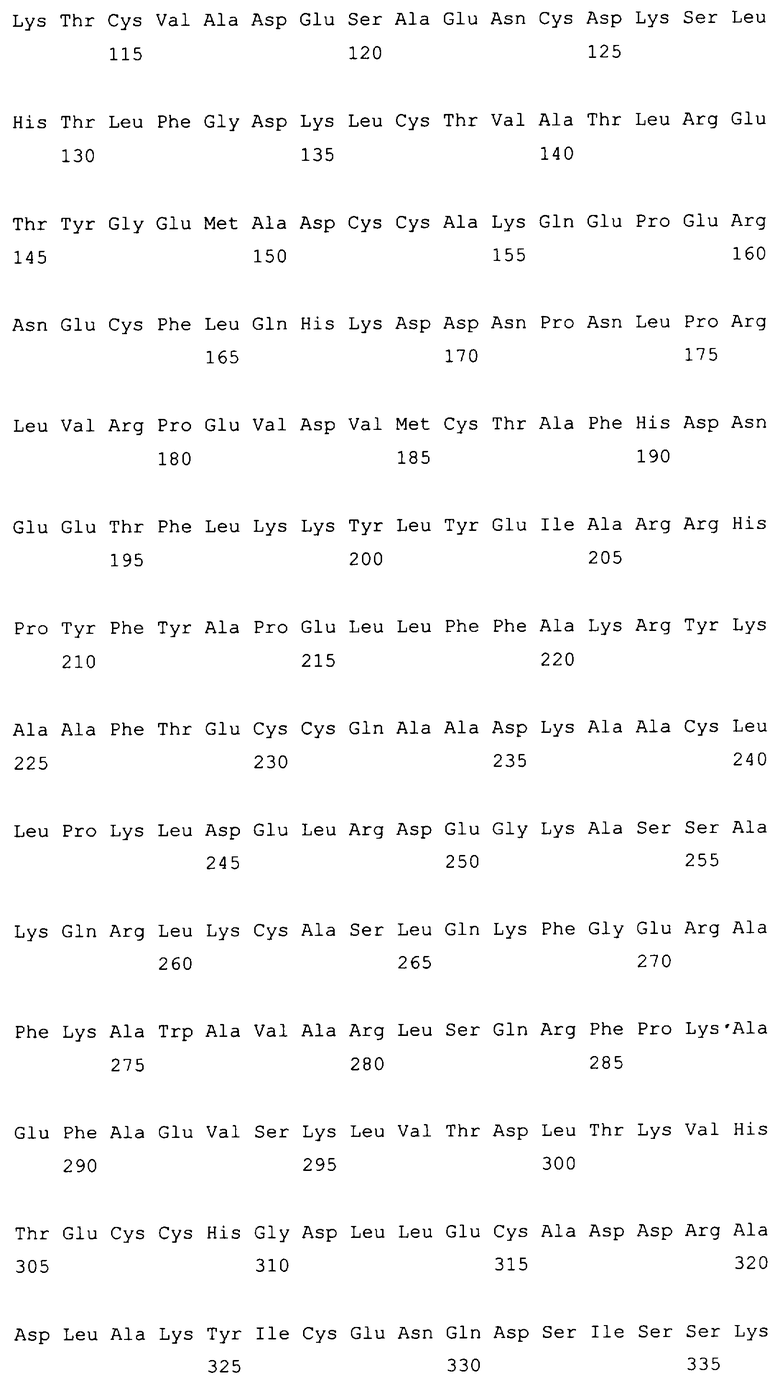
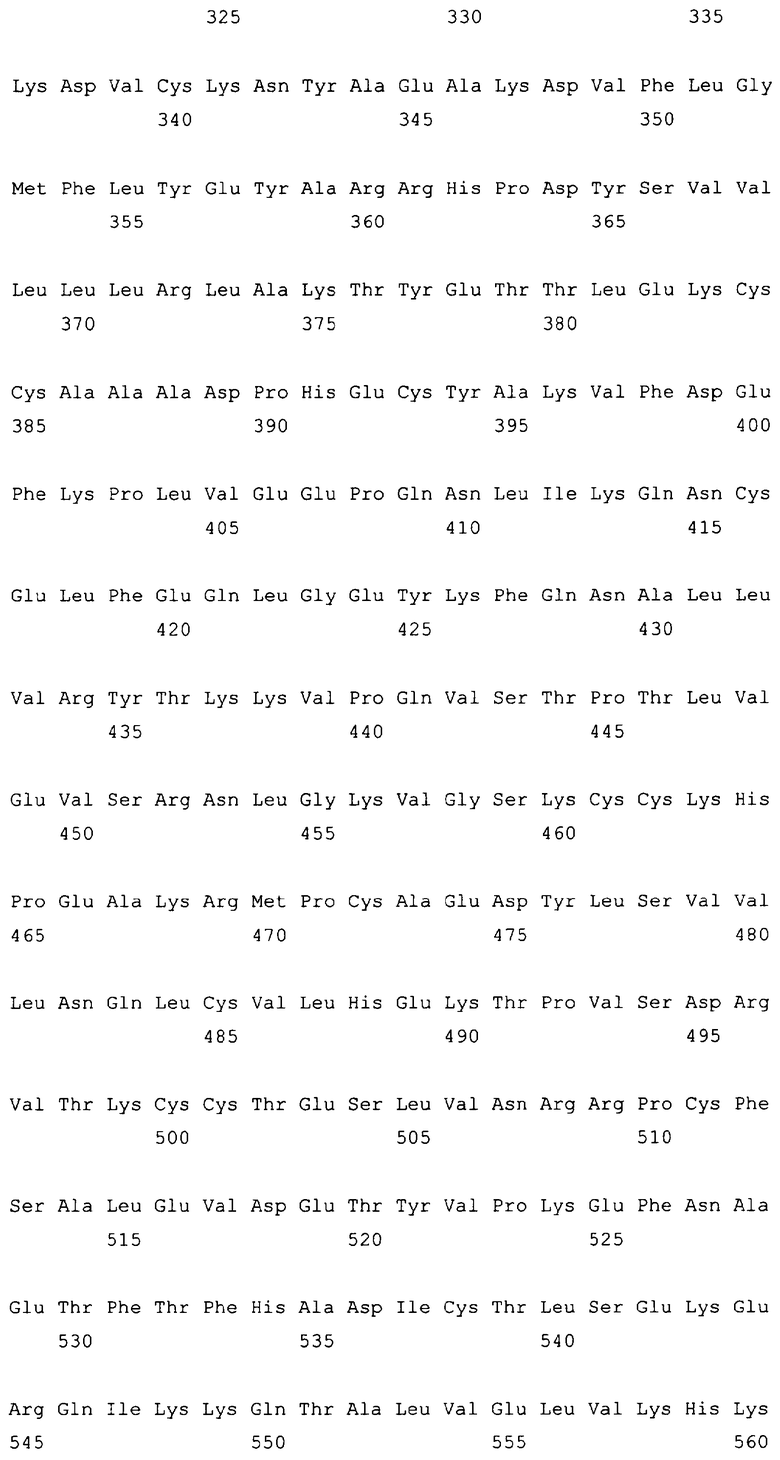
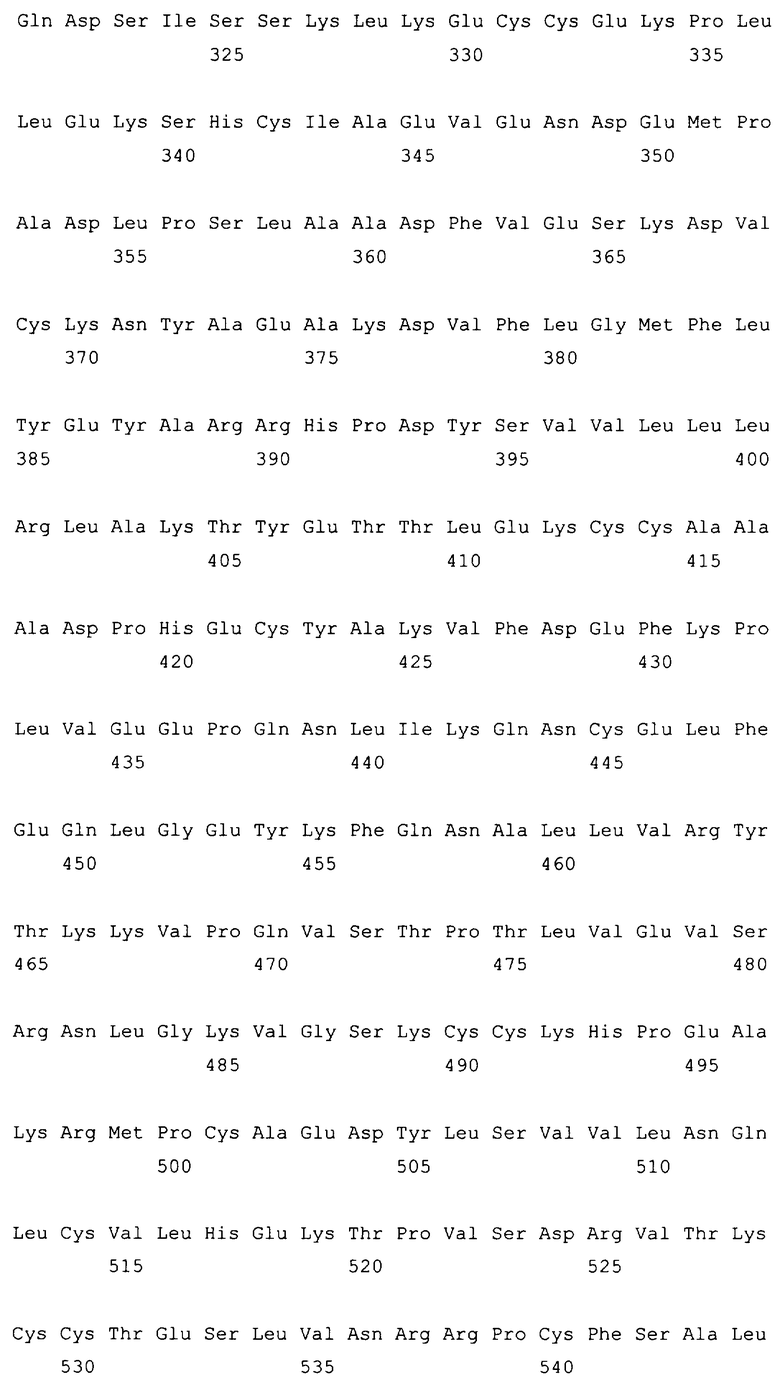
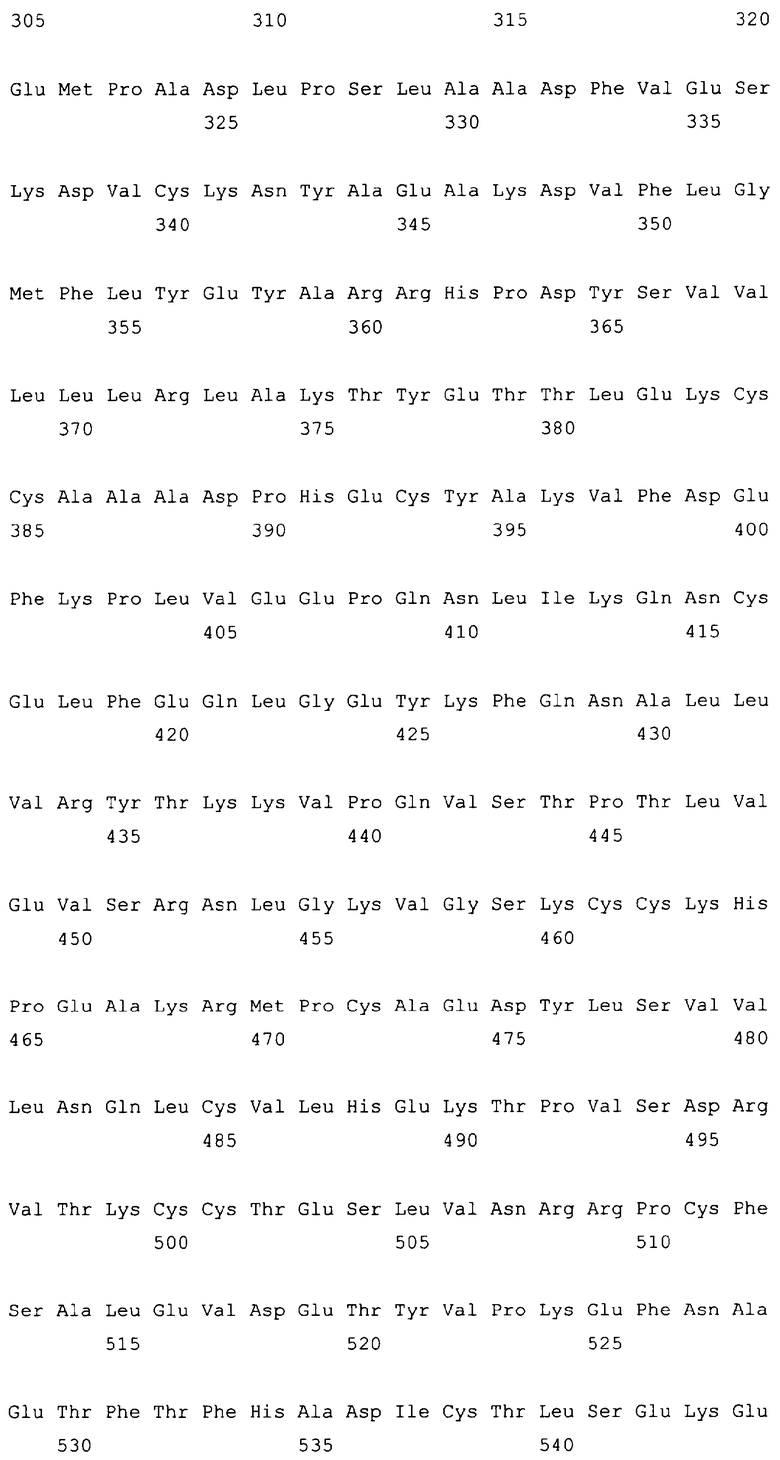
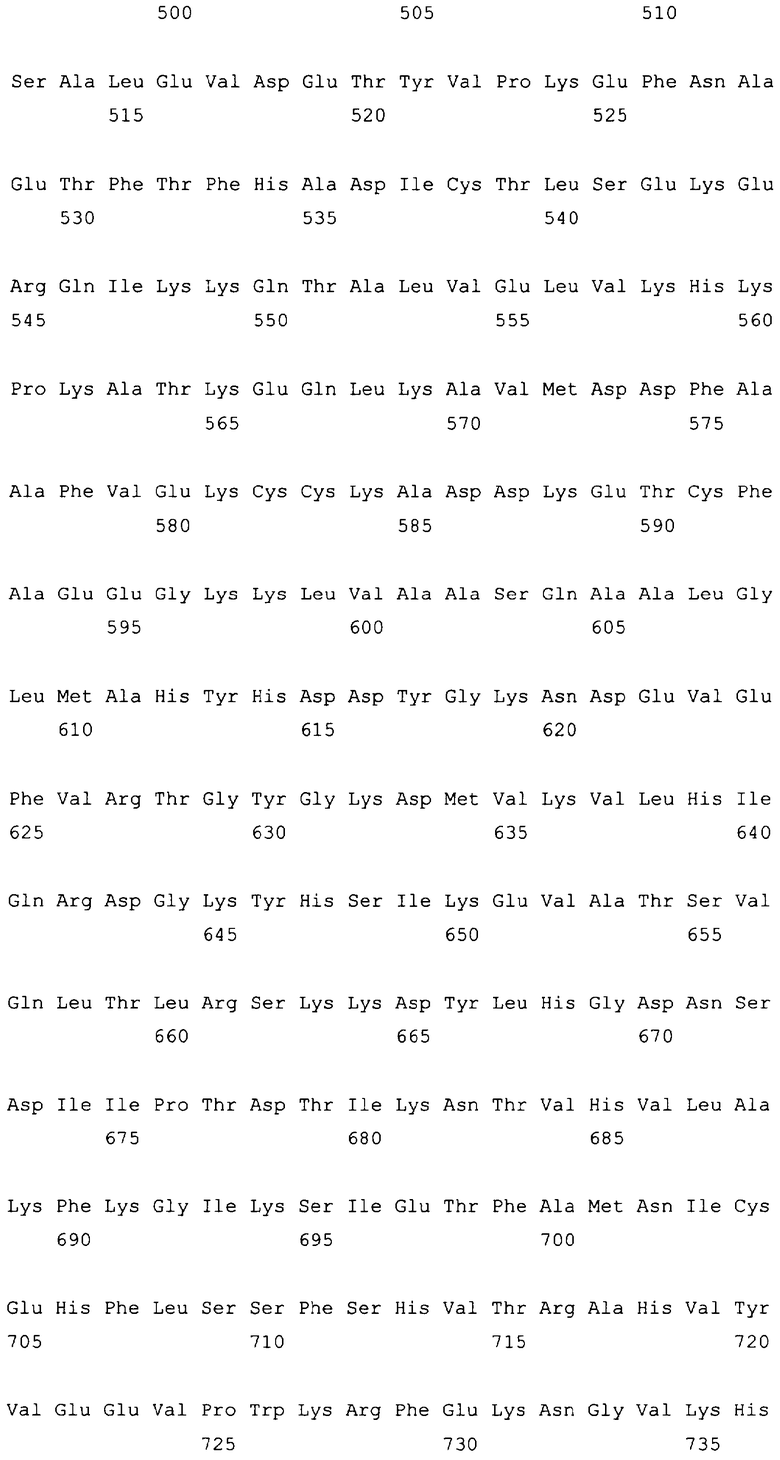
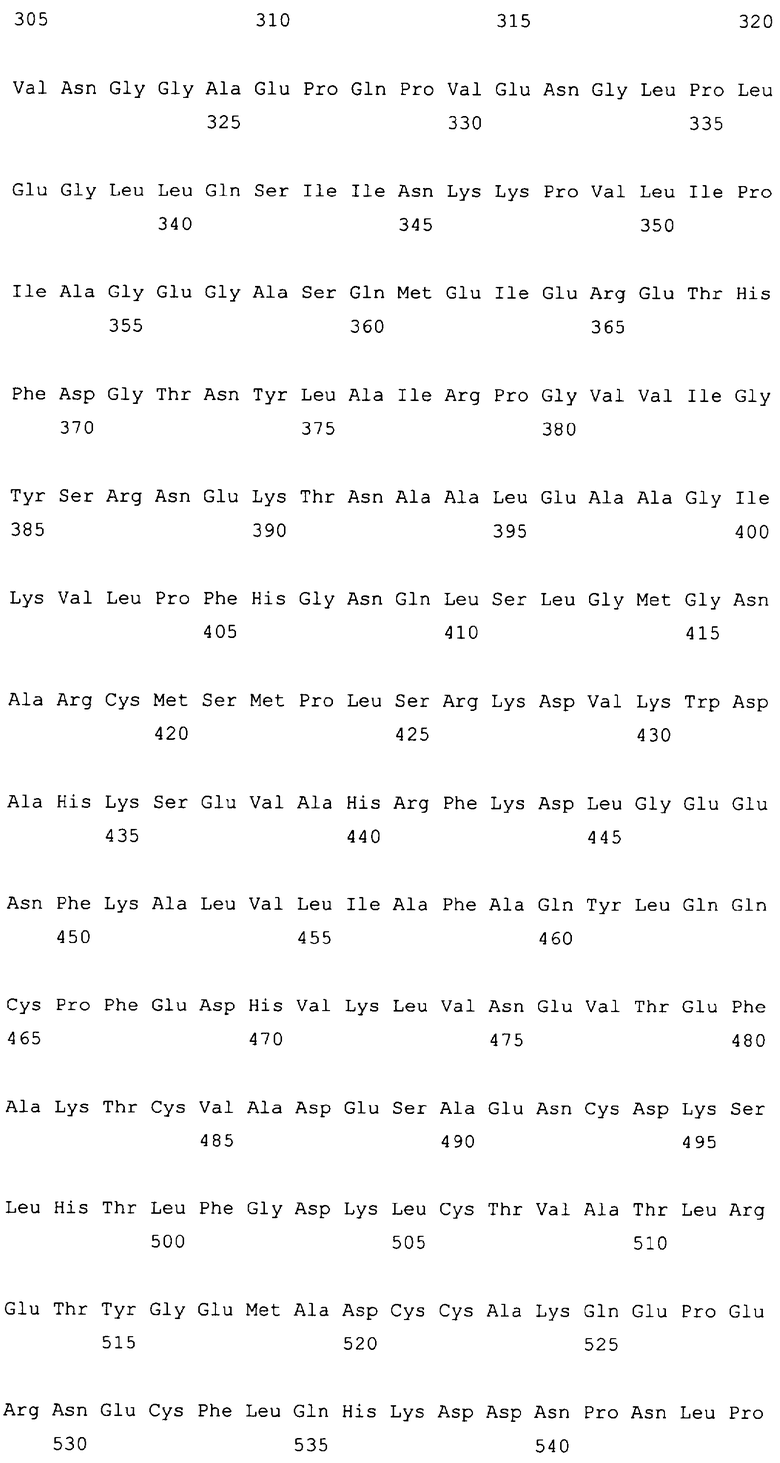
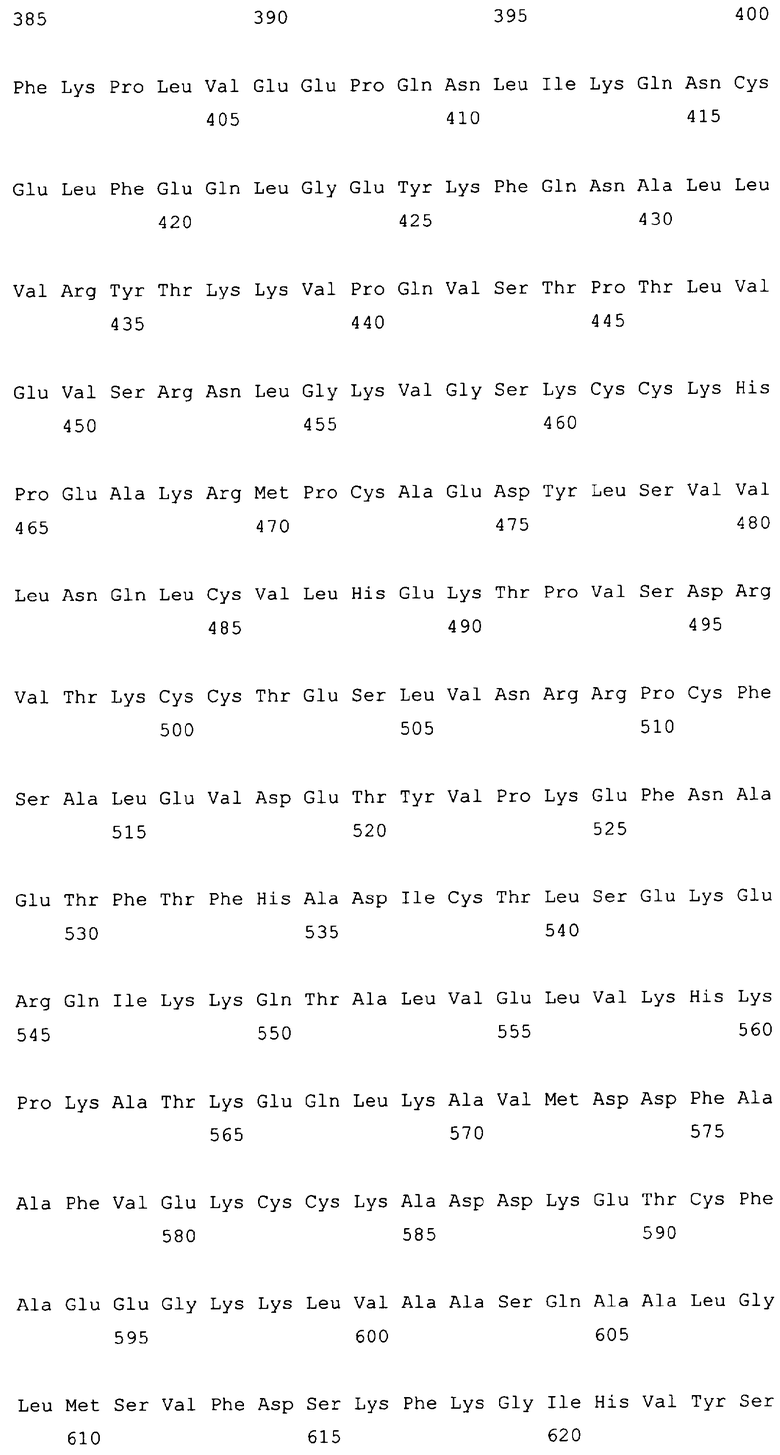
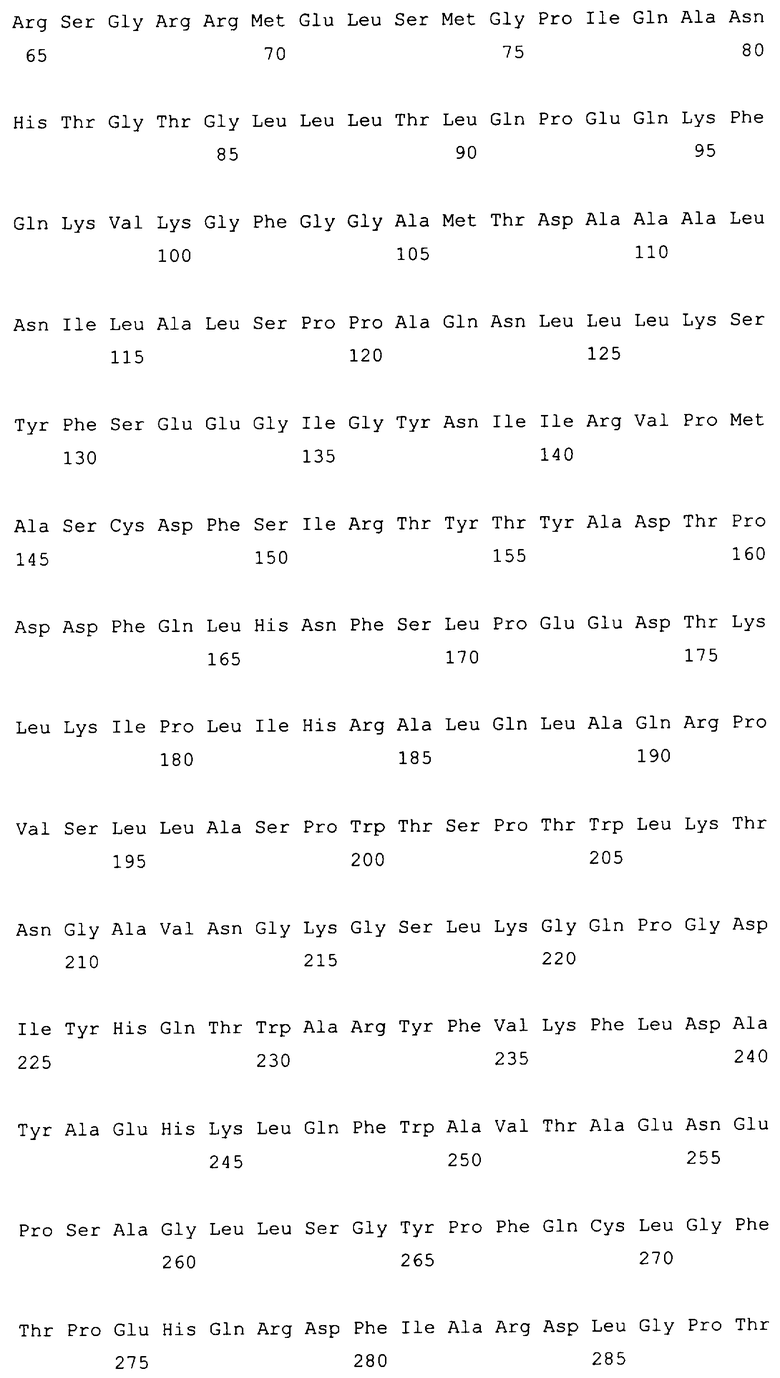
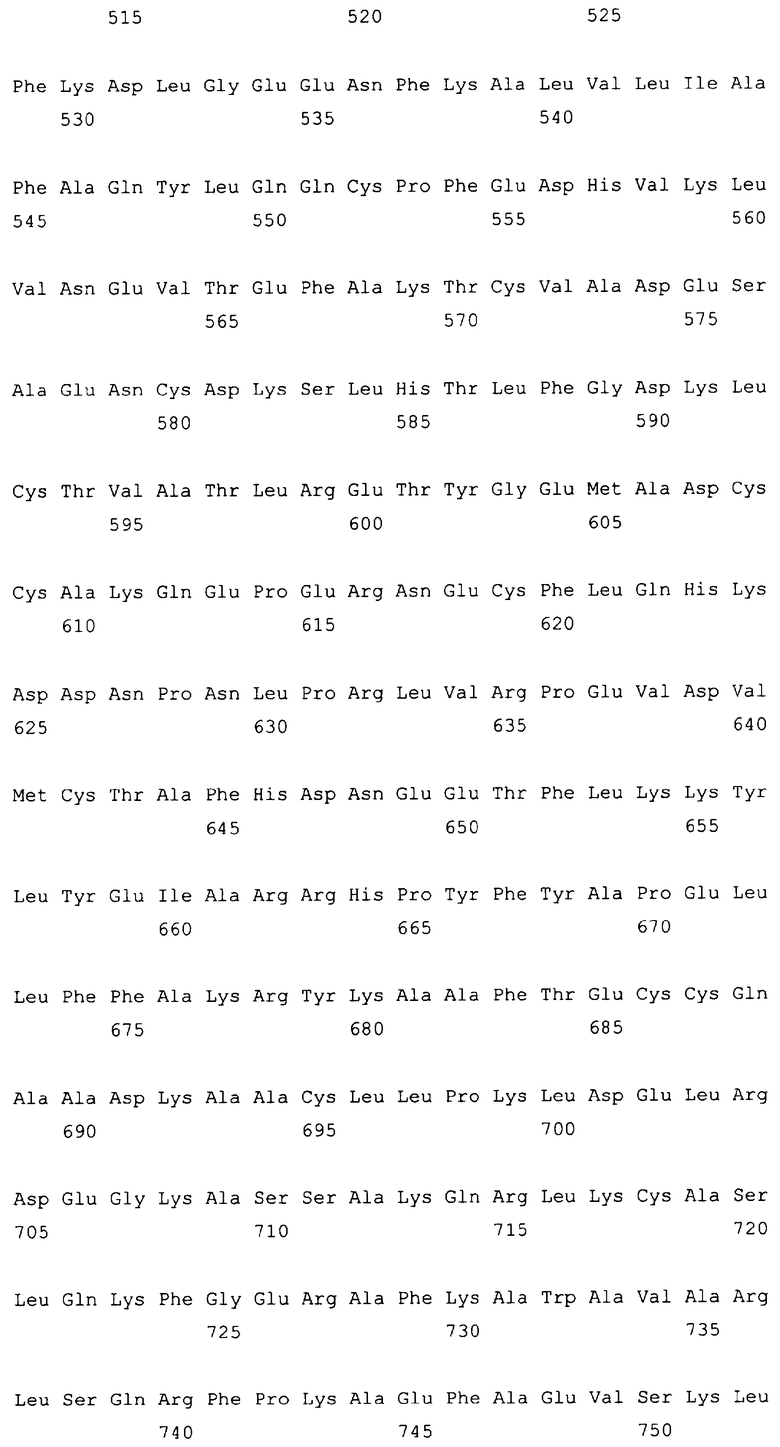
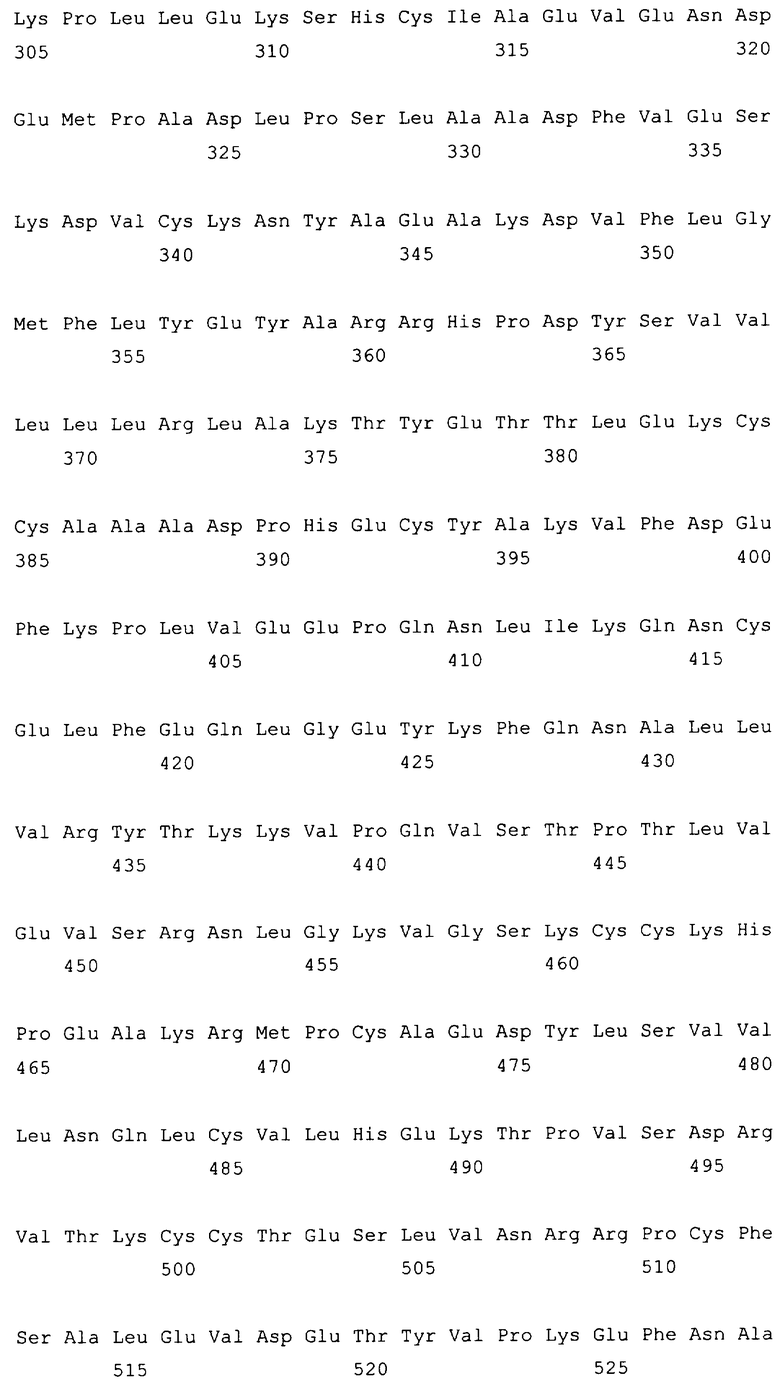
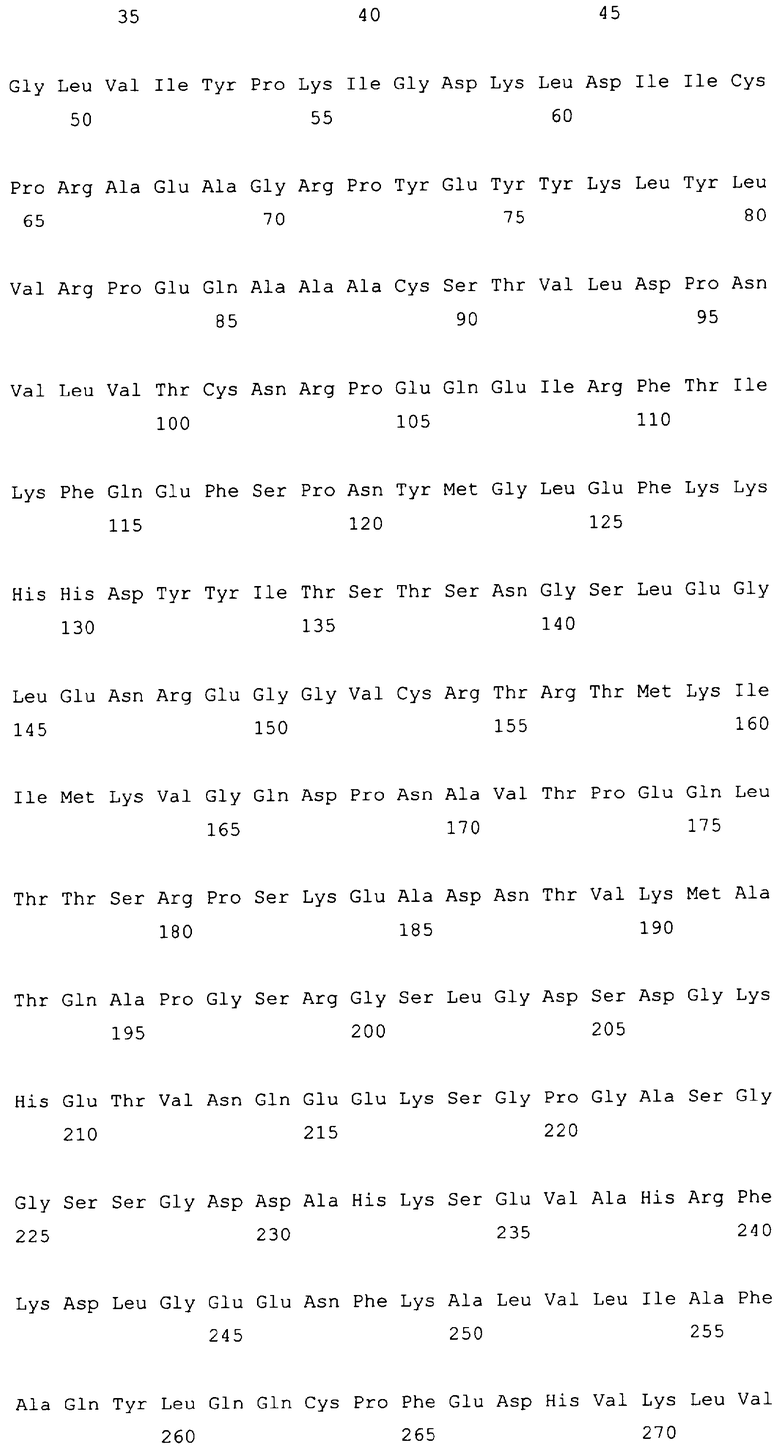
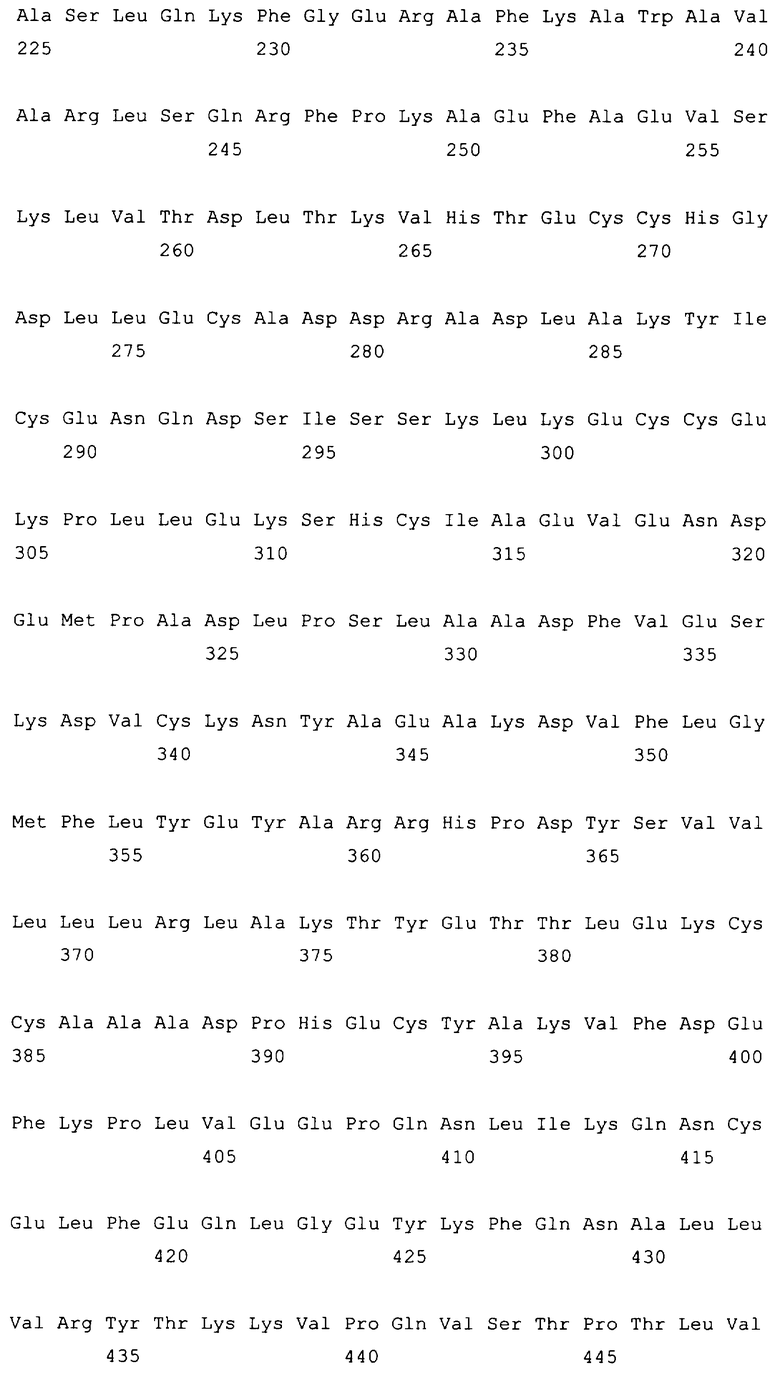
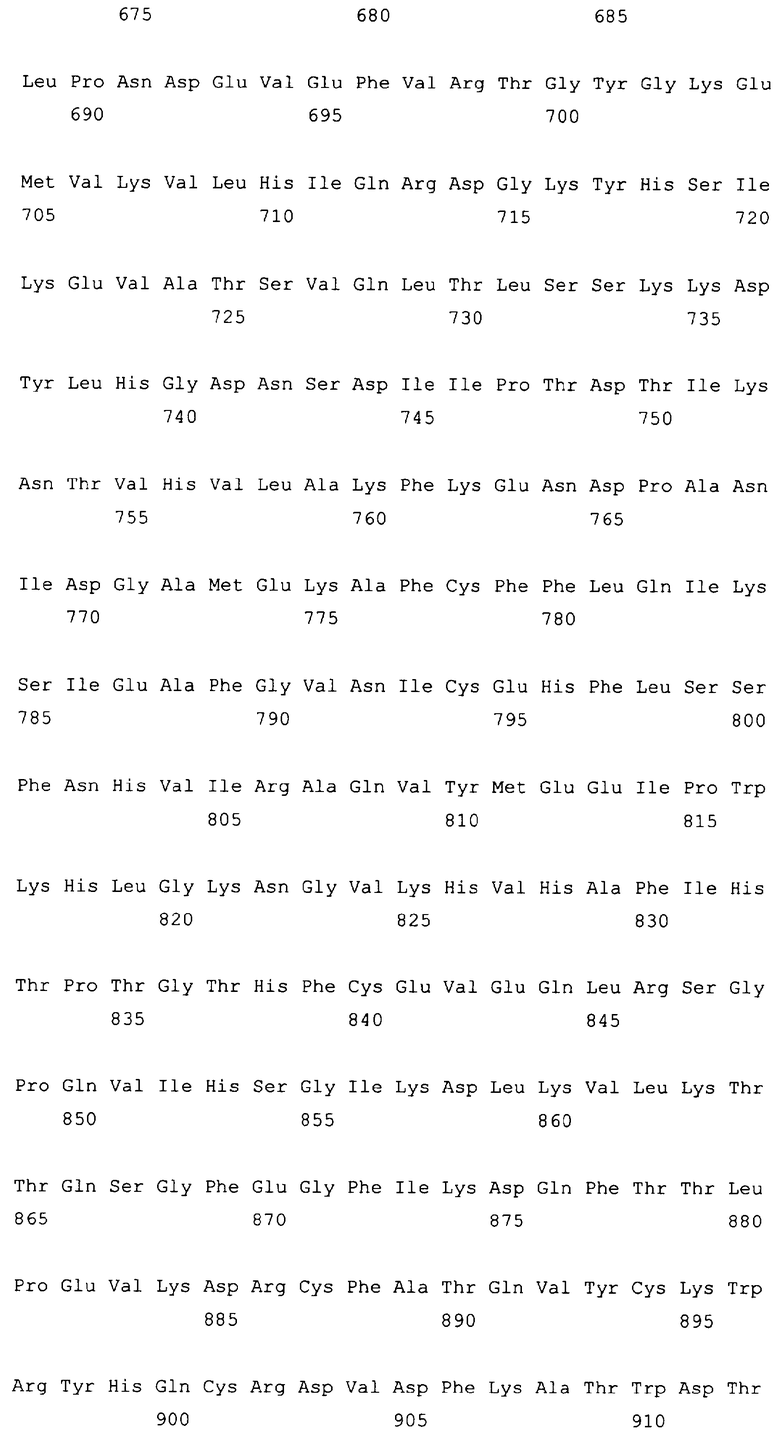
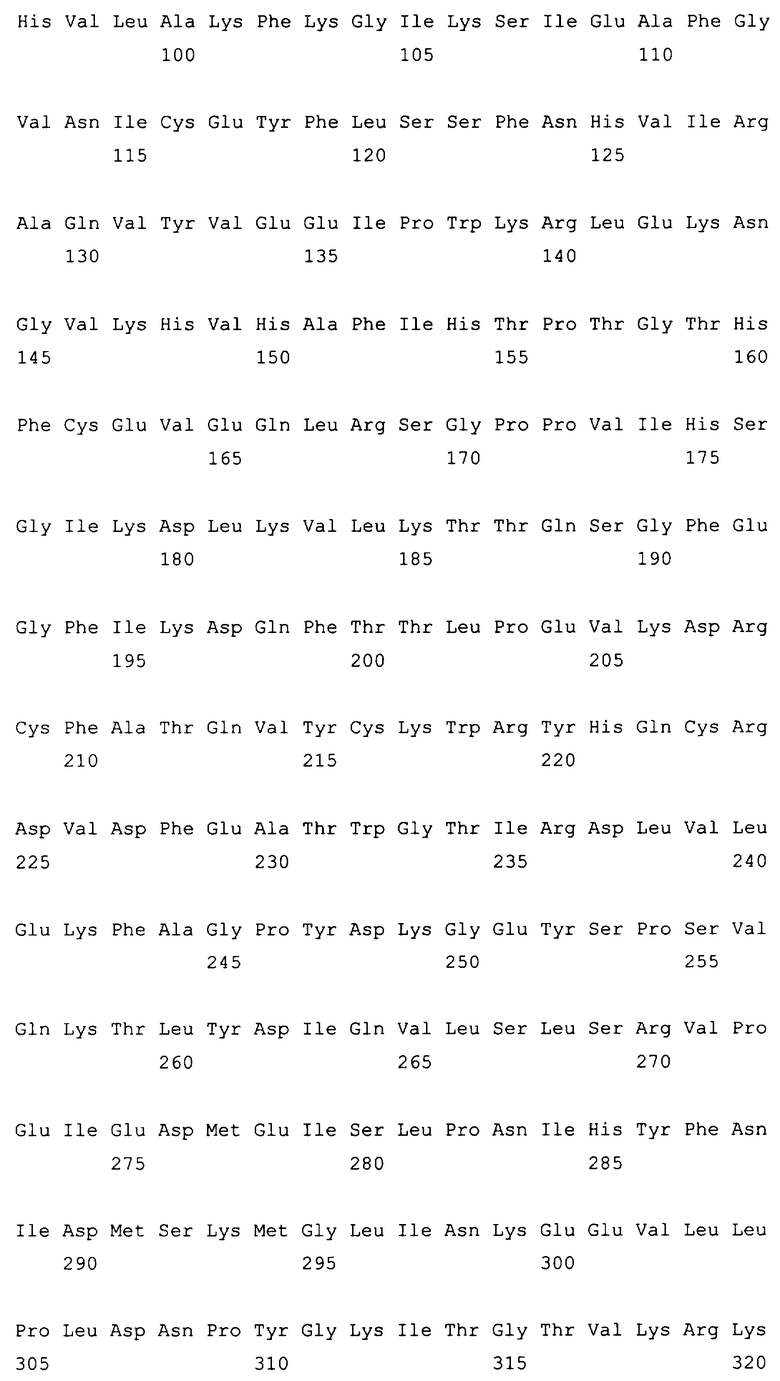
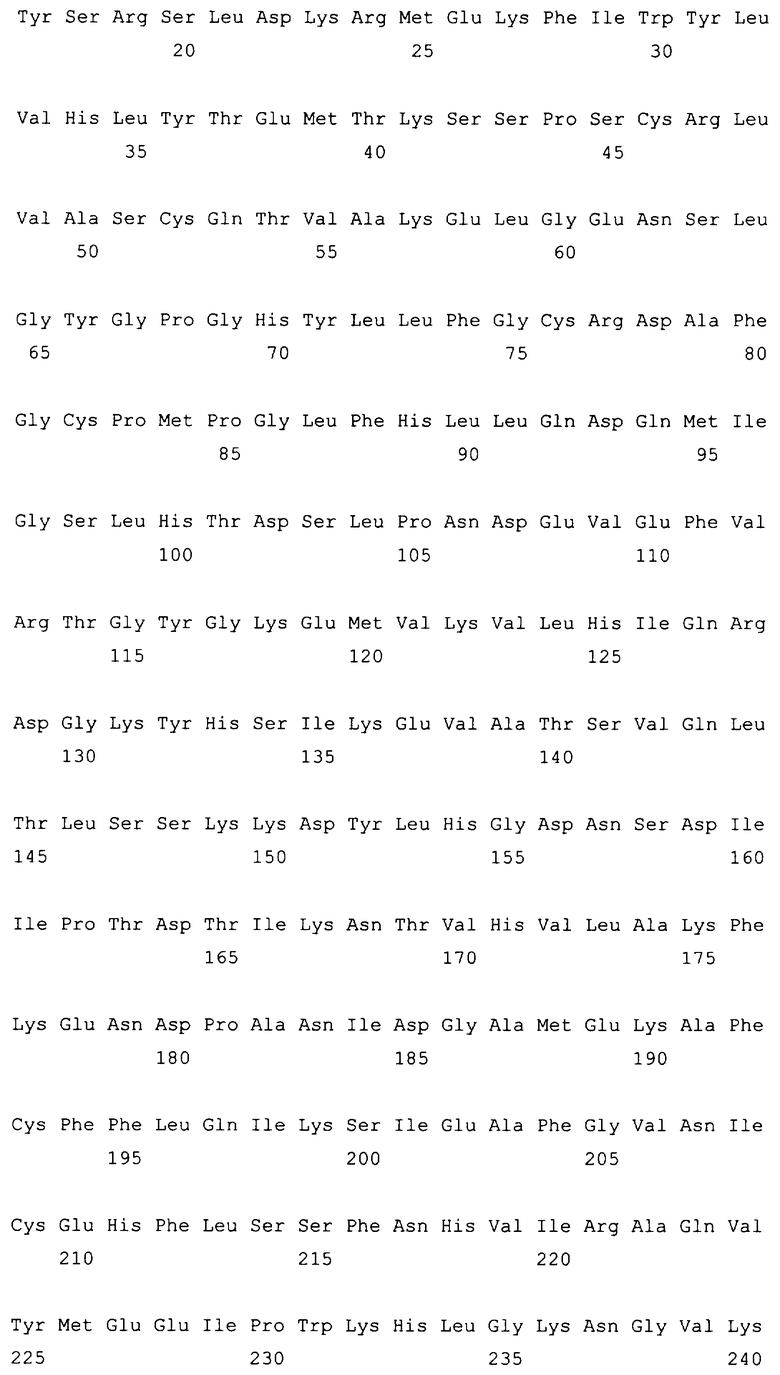
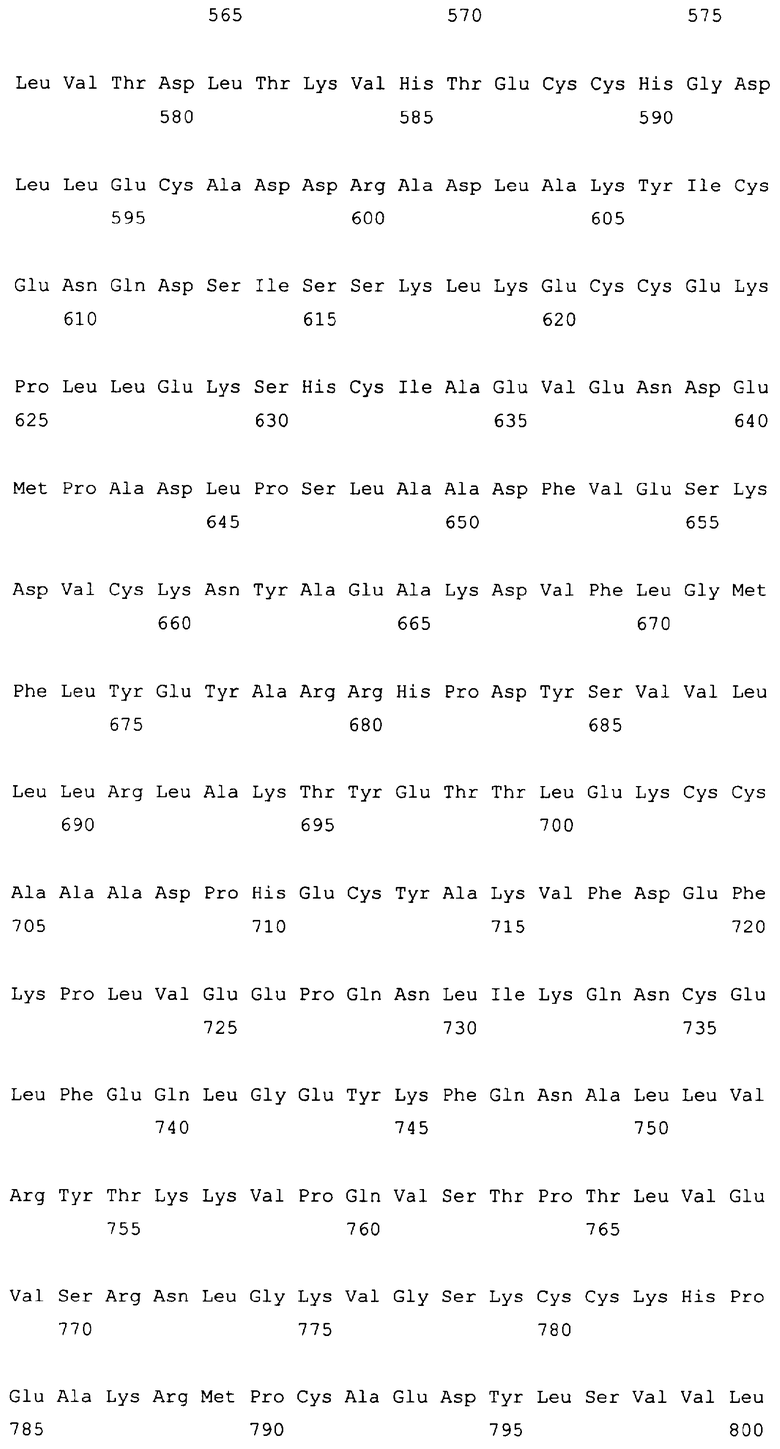
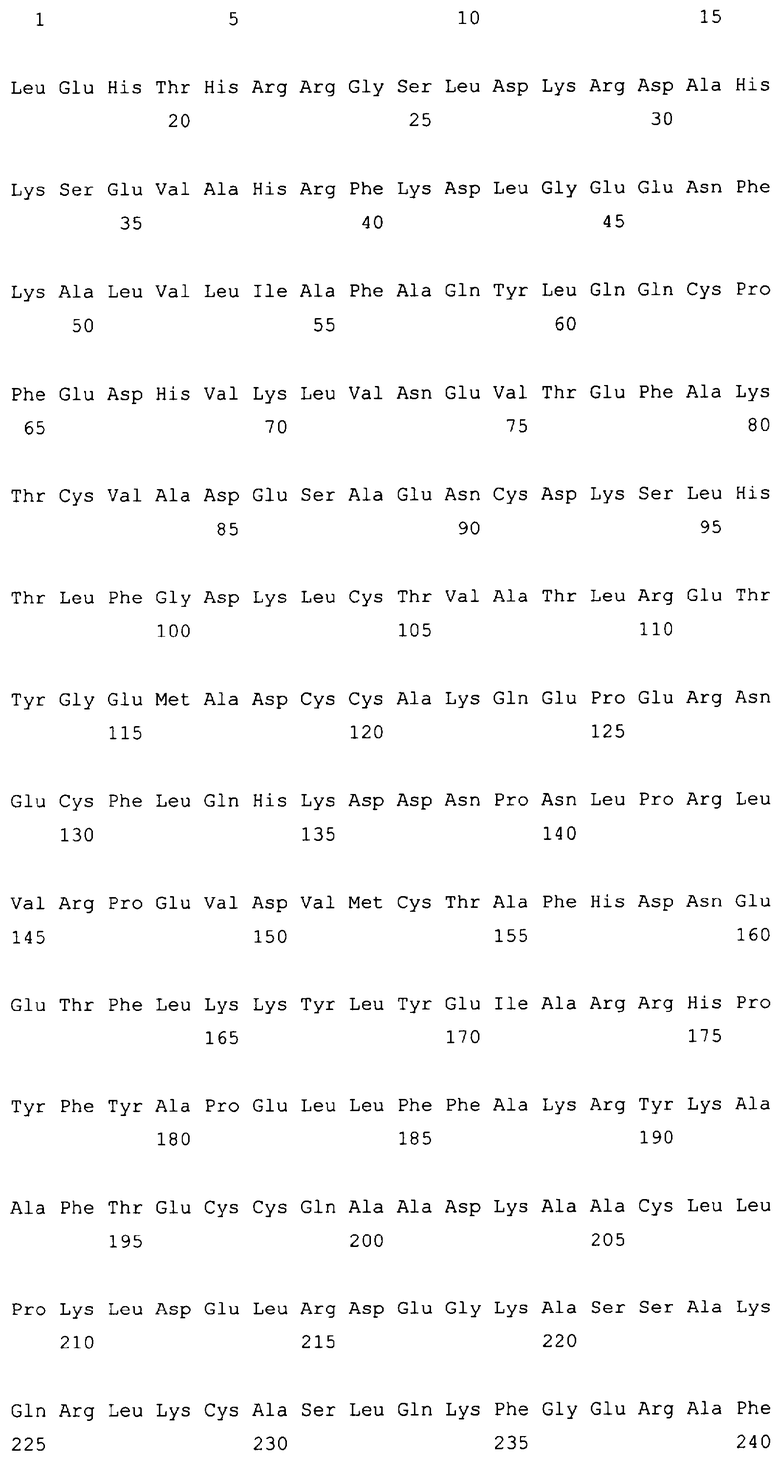
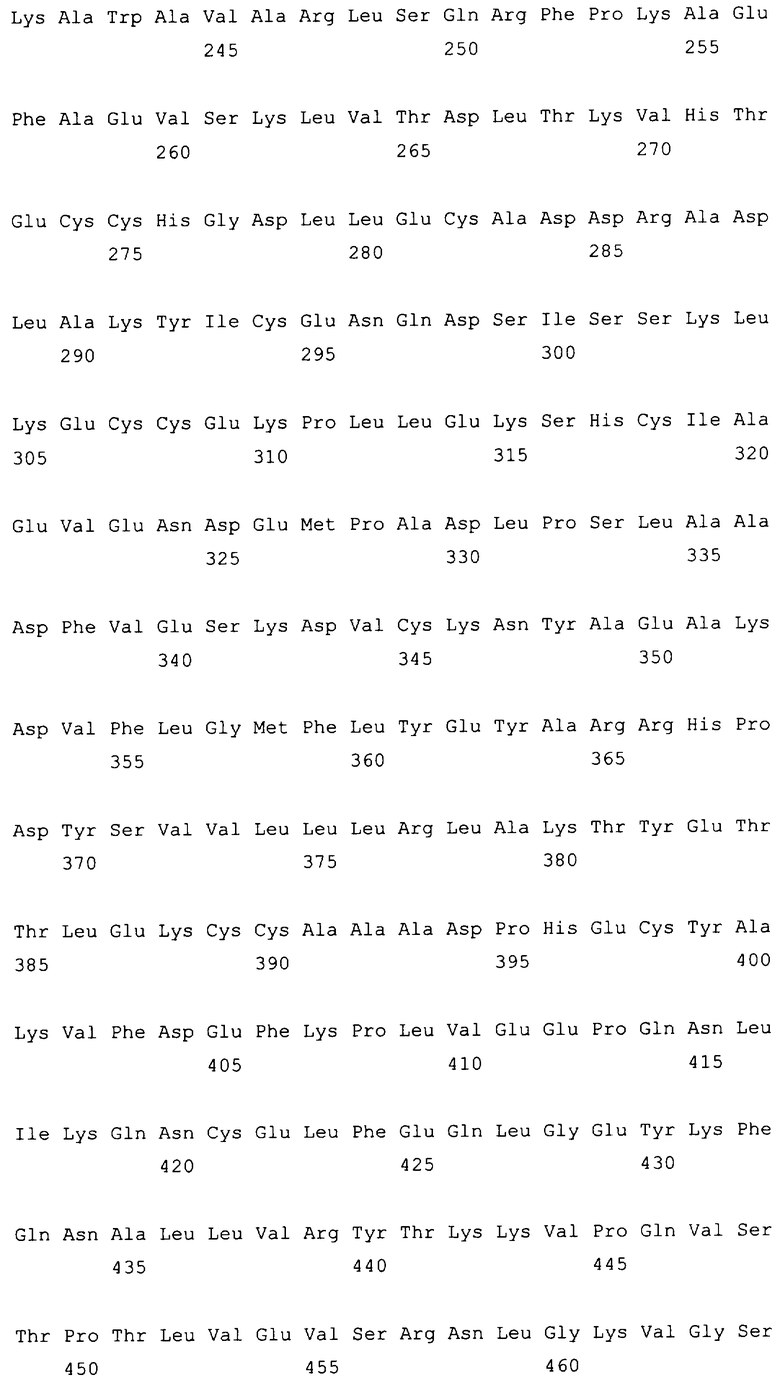
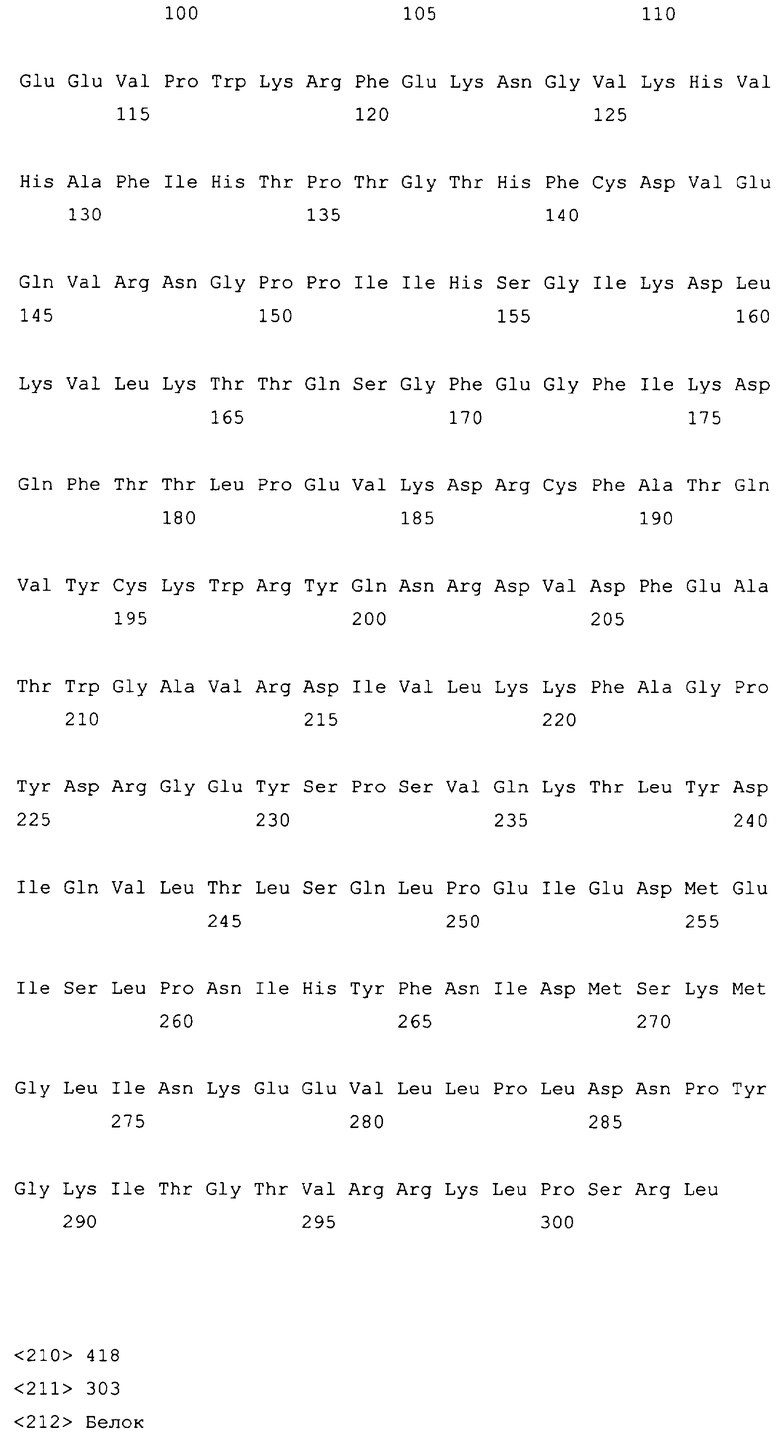
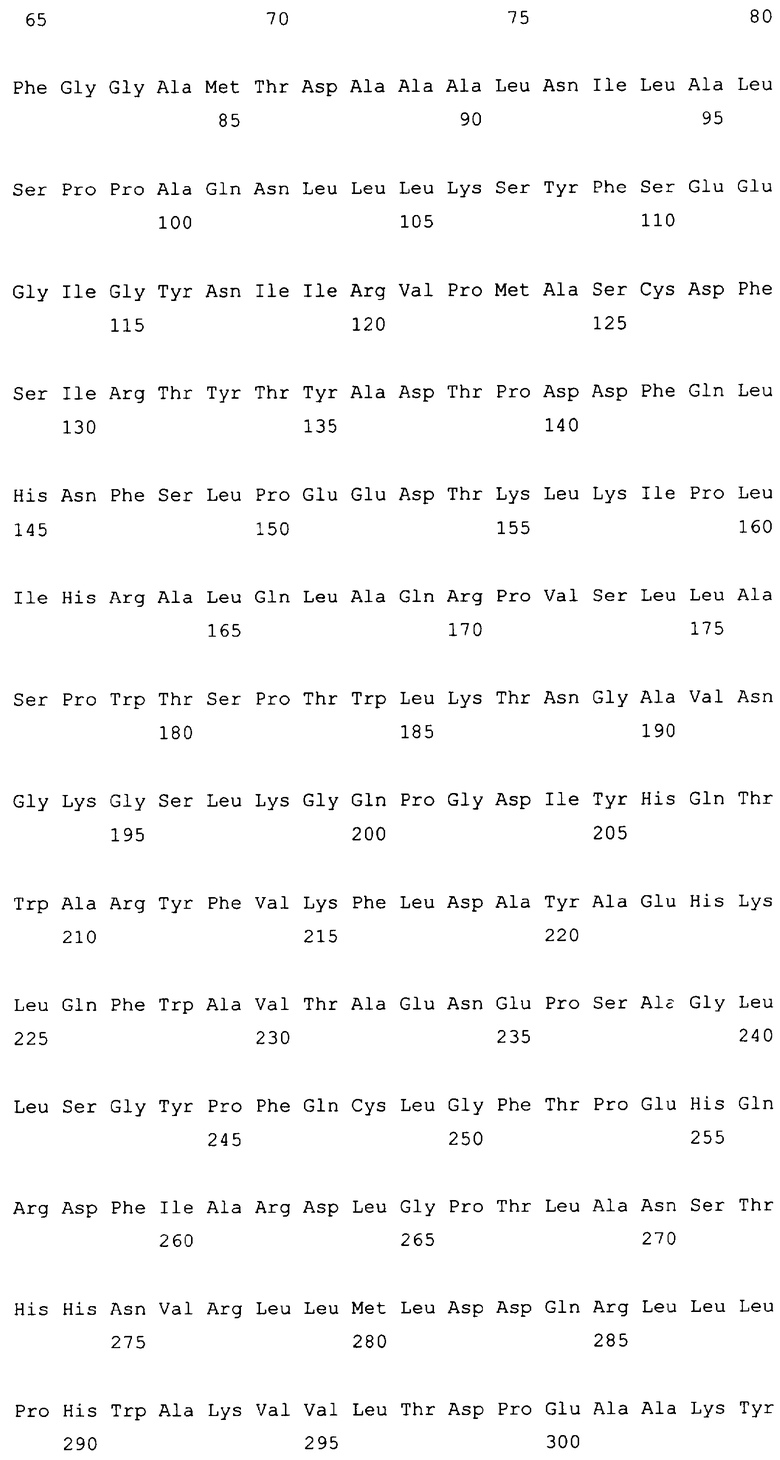
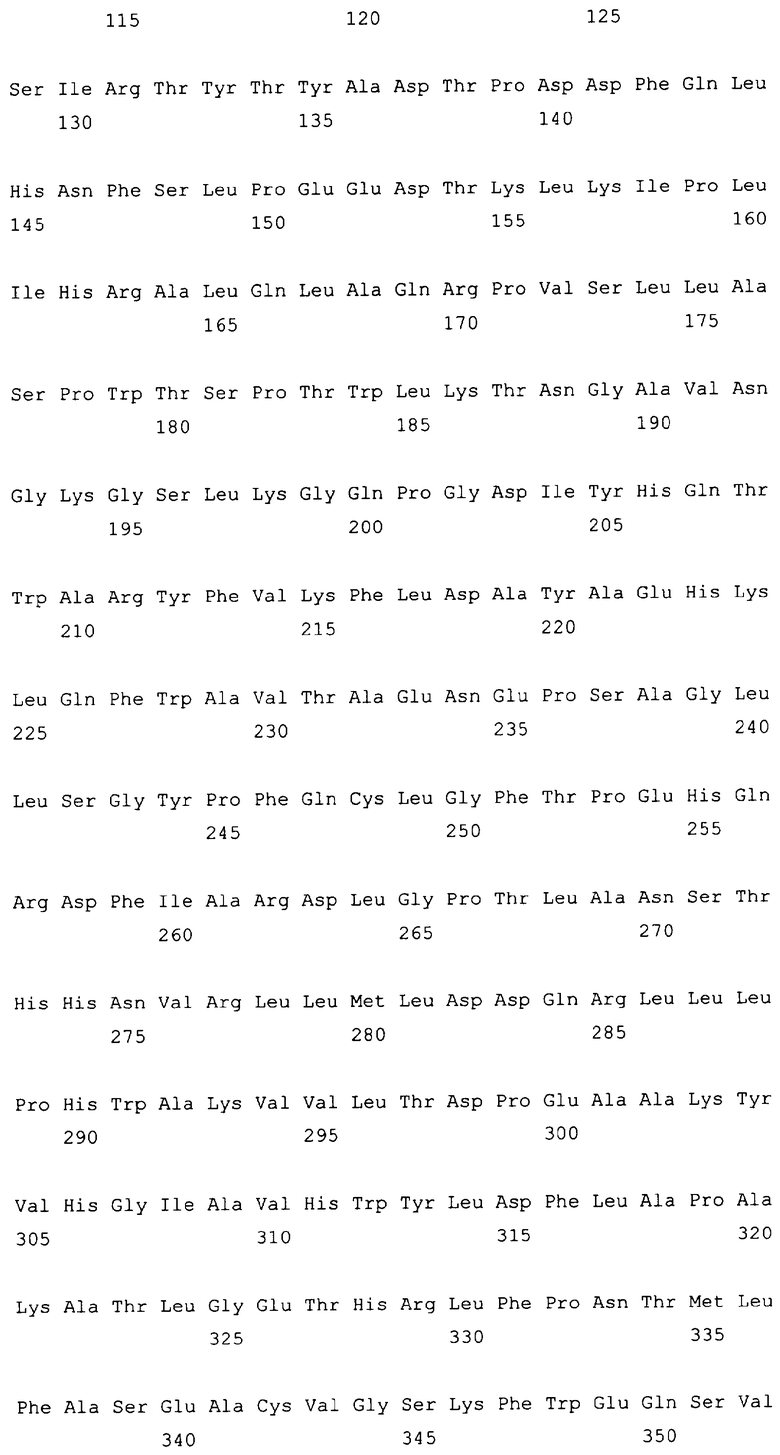
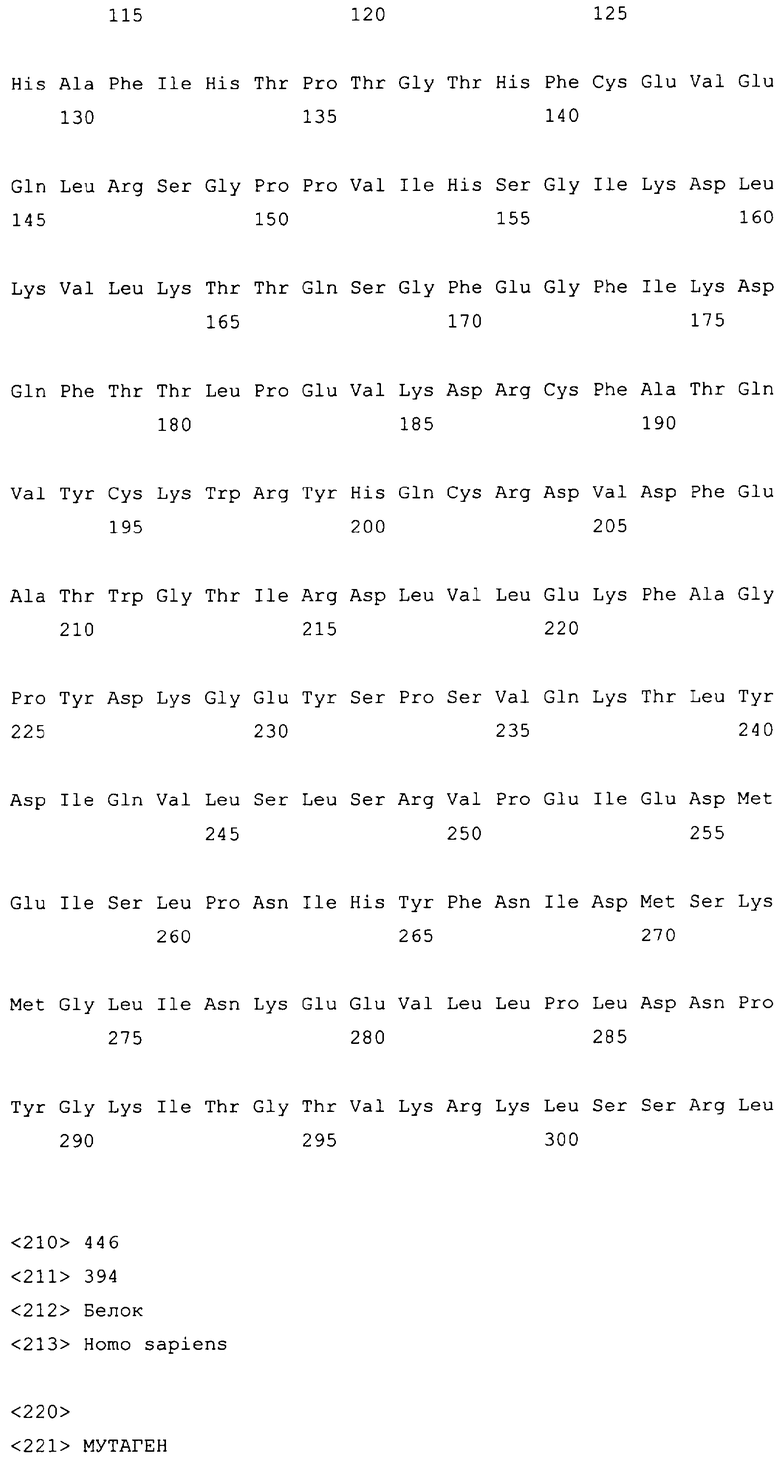
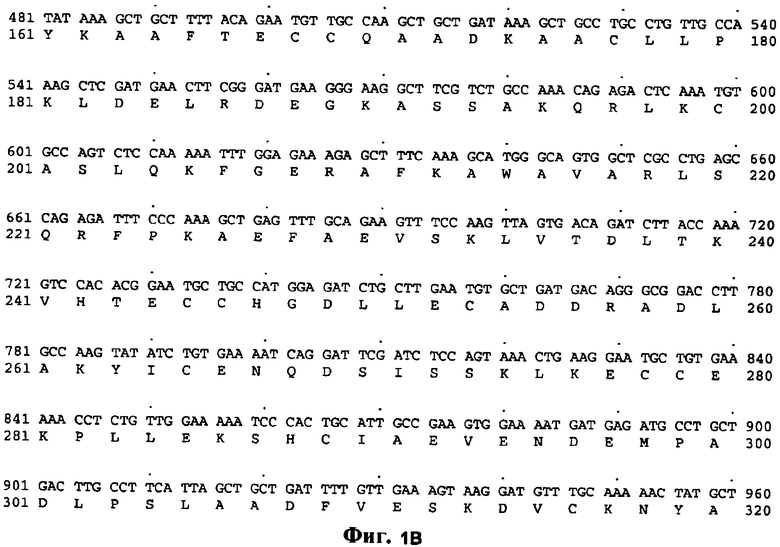
10. Слитый с альбумином белок по любому из пп.1-9, содержащий последовательность SEQ ID NO: 1.
11. Слитый с альбумином белок по любому из пп.1-10, где указанные два или более тандемно ориентированных полипептидов GLP-1 генетически слиты с указанным альбумином, фрагментом альбумина или его вариантом.
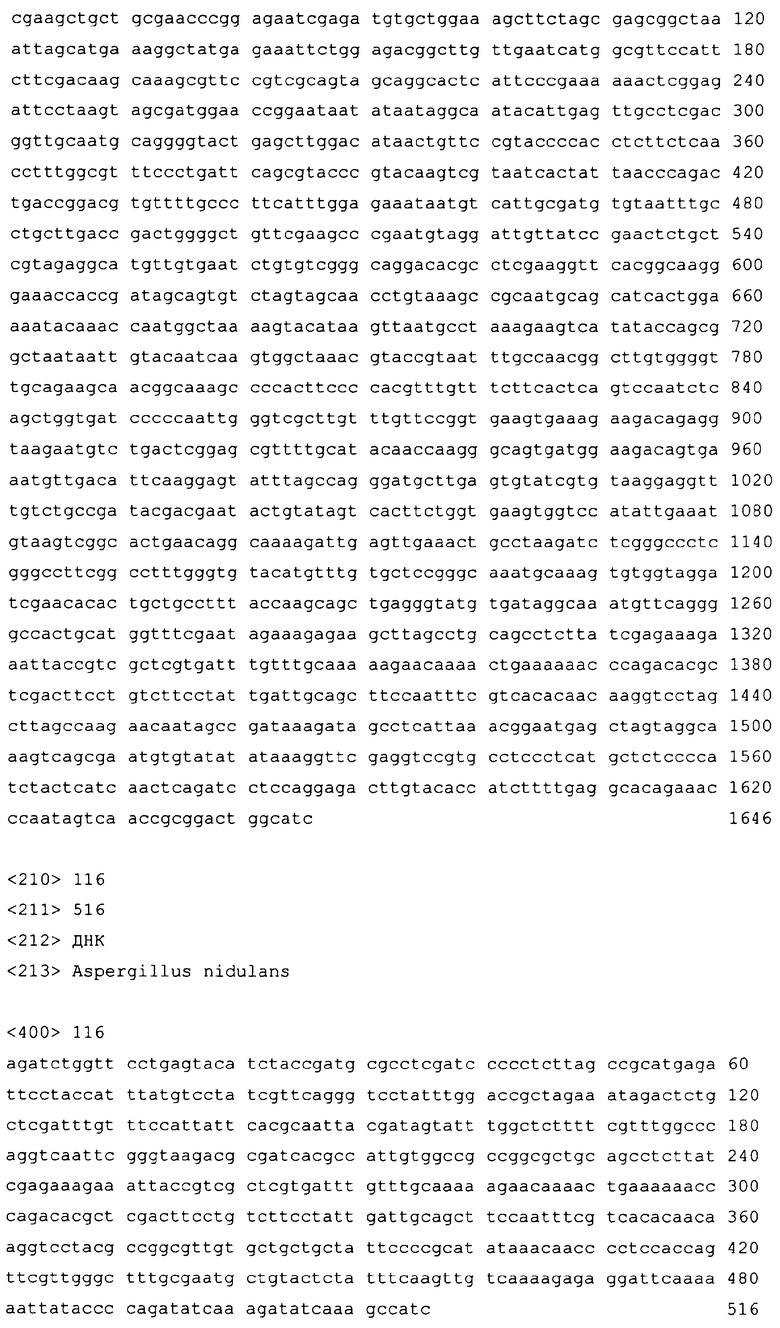
12. Полинуклеотид, кодирующий слитый с альбумином белок по любому из пп.1-11.
13. Вектор, содержащий полинуклеотид по п.12.
14. Хозяйская клетка, содержащая вектор по п.13.
15. Хозяйская клетка по п.14, которая представляет собой клетку дрожжей или клетку млекопитающего.
16. Хозяйская клетка по п.15, где указанными дрожжами являются S. Cerevisiae, К. lactis или Р. pastoris.
17. Хозяйская клетка по п.15 или 16, где указанные дрожжи являются дефицитными по гликозилированию.
18. Хозяйская клетка по любому из пп.15-17, где указанные дрожжи являются дефицитными по гликозилированию и по протеолитическим ферментам (протеазам).
19. Хозяйская клетка по п.15, где указанная клетка млекопитающего представляет собой клетку СНО, клетку COS или клетку NS0.
20. Слитый с альбумином белок по любому из пп.1-11, который является гликозилированным или негликозилированным.
21. Слитый с альбумином белок по любому из пп.1-11 и 20, который экспрессирован в дрожжах.
22. Слитый с альбумином белок по п.21, где указанные дрожжи относятся к S. Cerevisiae, К. lactis или Р. pastoris.
23. Слитый белок альбумина по п.21 или 22, где указанные дрожжи являются дефицитными по гликозилированию.
24. Слитый с альбумином белок по любому из пп.21-23, где указанные дрожжи являются дефицитными по гликозилированию и по протеолитическим ферментам (протеазам).
25. Слитый с альбумином белок по любому из пп.1-11 и 20, который экспрессируется клеткой млекопитающего.
26. Слитый с альбумином белок по п.25, где указанная клетка млекопитающего представляет собой клетку СНО, клетку COS или клетку NS0.
27. Слитый с альбумином белок по любому из пп.1-11 и 20-26, где лидерная последовательность выбрана из группы, состоящей из
(a) пре-про-области лидерной последовательности HSA;
(b) лидерной последовательности киллерного токсина;
(c) лидерной последовательности HSA/Kex2;
(d) сигнальной последовательности фактора альфа спаривания дрожжей;
(e) модифицированной лидерной последовательности HSA/kex2;
(f) лидерной последовательности MPIF-1; и
(g) консенсусной лидерной последовательности.
28. Слитый с альбумином белок по п.27, где указанная лидерная последовательность является модифицированной лидерной последовательностью HSA/Kex2, кодирующей аминокислоты последовательности SEQ ID NO: 112.
29. Композиция, содержащая слитый с альбумином белок по любому из пп.1-11 и 20-27 и фармацевтически приемлемый носитель.
30. Способ продуцирования слитого с альбумином белка, включающий в себя
(a) трансформацию хозяйской клетки, содержащей по меньшей мере один вектор по п.13;
(b) культивирование хозяйской клетки в условиях, подходящих для экспрессии слитого с альбумином белка;
(c) выделение слитого с альбумином белка.
31. Способ по п.30, где выделенный слитый с альбумином белок подвергают дальнейшему процессингу для удаления лидерной последовательности.
32. Слитый с альбумином белок, продуцируемый способом по п.30, где указанный слитый белок лишен лидерной последовательности.
33. Способ лечения заболевания, состояния или расстройства у пациента, включающий в себя введение указанному пациенту эффективного количества слитого с альбумином белка по любому из пп.1-11, 20-28 и 31, где указанное заболевание, состояние или расстройство выбрано из гипергликемии, диабета, несахарного диабета, резистентности к инсулину, недостаточности инсулина, гиперлипидемии, гиперкетонемии, ожирения, расстройств метаболизма, снижения массы тела, подавления аппетита, ухудшения познавательных процессов и потери памяти, синдрома Х и/или диабета, ассоциированного с сердечным заболеванием, инфекциями, ретинопатией, язвами, иммунными расстройствами и сосудистыми расстройствами.
34. Способ стимуляции синтеза и высвобождения инсулина, усиления чувствительности жировой, мышечной или печеночной ткани к поглощению инсулина, стимуляции поглощения глюкозы, замедления процесса пищеварения или блокирования секреции глюкагона у пациента, включающий в себя введение указанному пациенту эффективного количества слитого с альбумином белка по любому из пп.1-11, 20-28 и 31.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US 5506120 A, 09.04.1996 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2009-10-10—Публикация
2005-02-09—Подача