Изобретение относится к медицине, в частности к хирургической реабилитации онкологических больных с послеоперационными вентральными грыжами.
Целью настоящего изобретения является повышение эффективности хирургического лечения послеоперационных вентральных грыж путем стимуляции раневого процесса в зоне пластики.
Многочисленные исследования показывают, что частота ПОВГ продолжает увеличиваться, составляя 20-22% от общего числа грыж. Это связано, прежде всего, с увеличением общего количества проведенных операций и их сложностью на органах брюшной полости и малого таза, а также с увеличением числа пациентов пожилого и старческого возраста. Несмотря на развитие науки, технических возможностей, навыков хирургов и хирургических приемов 2-15% всех лапаротомий заканчивается формированием послеоперационной грыжи.
В возникновении ПОВГ у больных со злокачественными новообразованиями много общего в сравнении с больными неонкологического профиля. Однако существуют и свои специфические особенности, связанные как непосредственно с заболеванием, так и специальными методами лечения, что позволяет говорить об особенностях данной проблемы. Прежде всего это связано с исходным состоянием онкологического больного, которое характеризуется анемией, гипопротеинемией, компенсированным или субкомпенсированным состоянием иммунитета, потерей в весе. Масштабность оперативного вмешательства на органах брюшной полости (вскрытие 2-х и более анатомических областей, органоуносящий характер, циторедуктивные вмешательства, лимфодиссекция) ведет к депрессии репаративных процессов в операционной ране.
В настоящее время для лечения больных со злокачественными новообразованиями используются специальные методы лечения - химиотерапия и лучевая терапия. Однако данные литературы и собственный клинический опыт свидетельствует об отрицательном влиянии лучевой и химиотерапии на не пораженные опухолью ткани. Лекарственные препараты, применяемые с целью замедления развития или необратимого повреждения опухолевых клеток, замедляют фазу воспаления, что ведет к торможению процесса заживления ран. Общеизвестно, что сосуды, располагающиеся в поле облучения, претерпевают серьезные морфологические изменения в виде склероза мышечной оболочки, ломкости интимы, возникает фиброз окружающих тканей. Отсюда следует предположить, что замедленный раневой процесс, угнетение ростковых факторов, ведущих к формированию полноценной соединительной ткани, способствуют формированию рецидивной и рецидивирующей грыжи и определяют особенности пластических операций у онкологических больных. Пересадка клеток костного мозга в зону пластики приводит к формированию тканеспецифичных ростков донорской ткани, что свидетельствует о более эффективном процессе регенерации с целью полноценного формирования соединительнотканного рубца.
Одним из осложнений, встречающихся после пластики послеоперационных вентральных грыж является высокая частота рецидива, которая по данным разных авторов колеблется от 14% до 54%. Данная ситуация не может удовлетворить онкологов ввиду так называемой «лечебной загруженности» больного, а в ряде случаев ограниченного жизненного прогноза. Повторные пластические пособия удлиняют реабилитационный период и не способствуют улучшению качества жизни онкологического больного.
В практике существуют способы профилактики рецидива данного осложнения, заключающиеся в стремлении формирования полноценного рубца в зоне пластики. На наш взгляд, ни один из существующих способов не гарантирует эффективности, так как каждый из них имеет определенные недостатки. Известен способ введения диспергированного биоматериала «Аллоплант» (стимулятор регенерации) с целью ускорения созревания соединительнотканного сращения по линии швов при пластике вентральных грыж (О.В.Галимов, С.А.Муслимов, В.О.Ханов, A.M.Шумкин. Способ применения «Стимулятора регенерации» в хирургическом лечении послеоперационных вентральных грыж. // Анналы хирургии. 2000. - №4. - С.61-63). Последний представляет собой специально обработанные волокна соединительной ткани и вводится методом обкалывания в 10 точках, расположенных на расстоянии 0,5 см от края апоневроза по 0,5 мл сухого порошкообразного вещества, растворенного в 5 мл 2%-ного лидокаина. Недостатком этого способа является то, что препарат является заместительным «строительным» материалом. К недостаткам этого способа можно отнести и то, что препарат представляет собой чужеродную ткань.
Нами с целью профилактики рецидива грыжеобразования предложен способ введения аутологичного костного мозга в количестве 10 мл в зону сформированной дубликатуры.
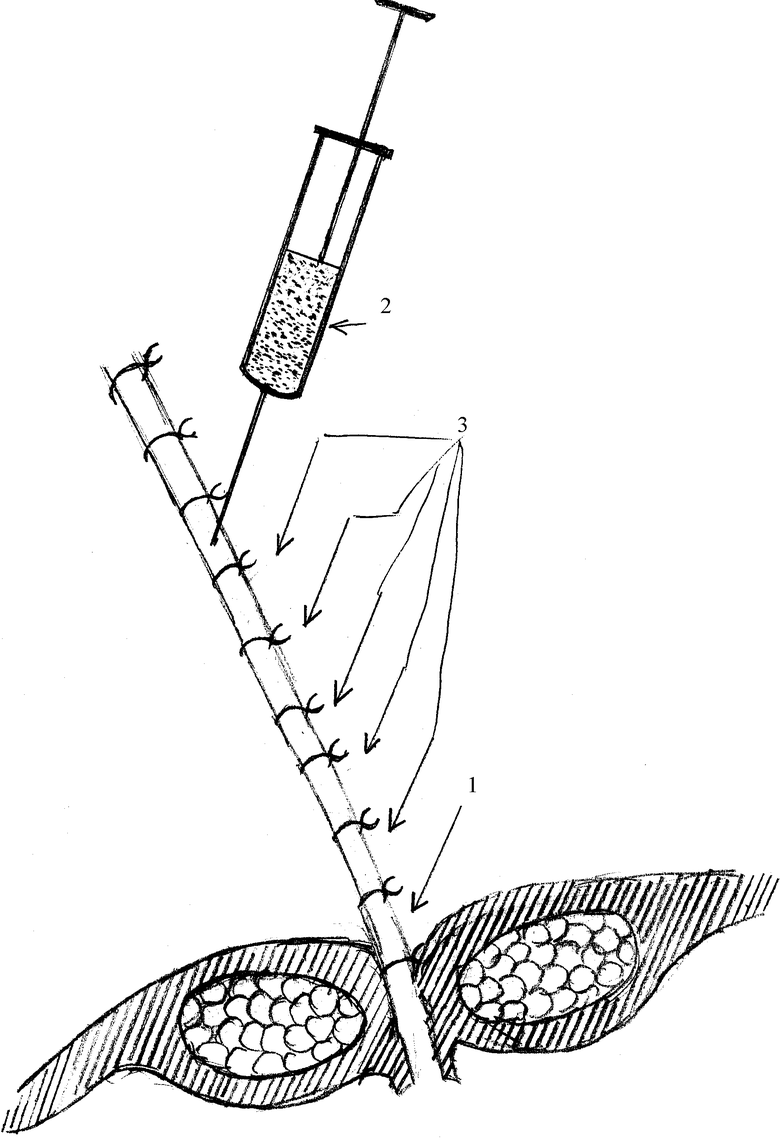
Способ осуществляется следующим образом. Во время выполнения пластического пособия после создания мышечно-апоневротической дубликатуры полиспастными швами (см. чертеж, позиция №1) в асептических условиях пунктируется крыло подвздошной кости и забирается в стерильный шприц 10 мл взвеси костного мозга (см. чертеж, позиция №2). Далее последняя вводится равномерно через швы между листками сформированной дубликатуры инъекционным методом по 0,5 мл (см. чертеж, позиция №3). Далее осуществляется динамическое, клиническое и лабораторное наблюдение за течением раневого процесса в госпитальном периоде.
Раневой процесс контролировали цитологическим методом. Так цитологическое исследование мазков с зоны пластики на 10-е сутки показало исчезновение элементов костного мозга, цитологическая картина соответствовала воспалительно-регенеративному типу с наличием клеток фибропластического типа. При контрольных исследованиях тип мазка соответствовал некротическому или дегенеративно-воспалительному типу.
В последующем, на поликлиническом этапе, проводили активное диспансерное наблюдение за общим состоянием и состоянием передней брюшной стенки.
При анализе доступных заявителю источников патентной и научно-медицинской информации не обнаружены методы, направленные на достижение той же цели со сходными существенными признаками, включенными в отличительную часть формулы предлагаемого способа, то есть не обнаружены способы, при которых производится пункция крыла подвздошной кости с целью получения взвеси костного мозга и введением последней в зону дубликатуры мышечно-апоневротических лоскутов.
1. Киселева Раиса Васильевна, 1937 г.р., № истории болезни 322. Диагноз: Рак Фатерова соска рТ1N0МО. 13.01.06 г. папиллосфинктерэктомия с раздельной пластикой протоков. 18.01.08 г - герниолапаротомия, пластика с подсадкой аутологичного костного мозга.
2. Ханжова Жайран Абабакаровка, 1967 г.р., № истории болезни 840. Диагноз: Лейомиосаркома матки, рак шейки матки рТ1N0МО, комбинированная терапия в 2006 г. (пангистерэктомия, 4 курса ПХТ - винкристин, доксирубицин, циклофосфан). 5.02.08 г - герниолапаротомия, пластика с подсадкой аутологичного костного мозга.
3. Туманова Екатерина Ивановна, 1930 г.р., № истории болезни 2158. Диагноз: Рак мочевого пузыря pT2N0M0, резекция мочевого пузыря с пересадкой правого мочеточника в 2007 г. 18.03.08 г. - герниолапаротомия, пластика с подсадкой аутологичного костного мозга.
Изобретение относится к медицине, в частности к хирургии вентральных грыж у больных со злокачественными новообразованиями. После проведения герниолапаротомии иссекается рубец и избыточная подкожно-жировая клетчатка. Мобилизуются мышечно-апоневротические лоскуты. Проводится пластика передней брюшной стенки полиспастными швами с формированием дубликатуры. Пунктируется крыло подвздошной кости. Забирается взвесь аутологичного костного мозга в количестве 10 мл. Пунктат вводится равномерно между листками сформированной дубликатуры. 1 ил.
Способ профилактики рецидива послеоперационной вентральной грыжи у больных со злокачественными новообразованиями, включающий в себя создание мышечно-апоневротической дубликатуры, отличающийся тем, что, с целью повышения эффективности хирургического лечения послеоперационных вентральных грыж между листками мышечно-апоневротической дубликатуры, вводится равномерно 10 мл взвеси пунктата костного мозга инъекционным методом, полученным при пункции крыла подвздошной кости.
| ГАЛИМОВ О.В | |||
| и др | |||
| Способ применения стимулятора регенерации в хирургическом лечении послеоперационных вентральных грыж | |||
| Аннады хирургии | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННЫХ ВЕНТРАЛЬНЫХ ГРЫЖ | 1999 |
|
RU2181028C2 |
| СПОСОБ УШИВАНИЯ ЛАПАРОТОМНОЙ РАНЫ С СОЗДАНИЕМ ДУБЛИКАТУРЫ | 2003 |
|
RU2263472C2 |
| ЗИМИН Ю.И | |||
| Выбор метода пластики стенки при вентральных грыжах | |||
| Хирургия, 1990, 7, 102-105 | |||
| DREWA T | |||
| et | |||
| al | |||
| Abdominal wall repair | |||
Авторы
Даты
2009-10-27—Публикация
2008-06-17—Подача