Цитокины играют важную роль в регулировании кроветворения и иммунных ответов, а также могут влиять на развитие лимфоцитов. Семейство цитокинов человека класса II включает субтипы интерферона-α (IFN-α), интерферон-β (IFN-β), интерферон-γ (IFN-γ), IL-10, IL-19 (патент США № 5985614), MDA-7 (Jiang et al., Oncogene 11, 2477-2486 (1995)), IL-20 (Jiang et al., Oncogene 11, 2477-2486 (1995)), IL-22 (Xie et al., J. Biol. Chem. 275, 31335-31339 (2000)) и AK-155 (Knappe et al., J. Virol. 74, 3881-3887 (2000)). Большинство цитокинов связывают и передают сигналы посредством цитокиновых рецепторов класса I или класса II. Члены семейства рецепторов цитокинов человека класса II включают интерферон-αR1 (IFN-αR1), интерферон-γ-R2 (IFN-γ-R2), интерферон-γ R1 (IFN-γ R1), интерферон-γR2 (IFN-γR2), IL-10R (Liu et al., J. Immunol. 152, 1821-1829 (1994)), CRF2-4 (Lutfalla et al., Genomics 16, 366-373 (1993)), IL-20Rβ (Blumberg et al., Cell 104, 9-19 (2001) (известен также как zcytor7 (патент США № 5945511) и CFR2-8 (Kotenko et al., Oncogene 19, 2557-2565 (2000)), IL-20Rβ (Blumberg et al., там же, (2001)) (известен также как DIRS1 (PCT WO 99/46379)), IL-22RA1 (рецептор-α1 для IL-22, сообщение направлено в HUGO на экспертизу) (известен также как IL-22R (Xie et al., J. Biol. Chem. 275, 31335-31339 (2000)), zcytor11 (патент США № 5965704) и CRF2-9 (Kotenko et al., Oncogene 19, 2557-2565 (2000)) и тканевый фактор.
Рецепторы цитокинов класса II обычно представляют собой димеры, образованные двумя отдельными цепями рецептора, субъединицами α и β рецептора (Stahl et al., Cell 74, 587-590 (1993)). В общем случае субъединицы α являются основными белками, связывающимися с цитокинами, а субъединицы β требуются для образования высоко аффинных участков для связывания, а также для передачи сигнала. Исключение составляет рецептор IL-20, в котором обе субъединицы необходимы для связывания с IL-20 (Blumberg et al., там же, (2001)).
Рецепторы цитокинов класса II идентифицируют по консервативной области связывания цитокина, размером приблизительно в 200 аминокислот (D200), расположенной во внеклеточной части рецептора. Указанная область связывания цитокина включает два домена фибронектина типа III (FnIII), каждый размером приблизительно 100 аминокислот (Bazan J.F., Proc. Natl. Acad. Sci. USA 87, 6934-6938 (1990); Thoreau et al., FEBS Lett., 282, 16-31 (1991)). Каждый домен FnIII содержит консервативные остатки Cys, Pro и Trp, которые определяют складчатую структуру семи β-цепей аналогично константной области иммуноглобулинов (Uze et al., J. Interferon Cytokine Res. 15, 3-26 (1995)). Консервативные структурные элементы семейства рецепторов цитокинов класса II позволяют идентифицировать новые члены указанного семейства на основании степени гомологичности первичной последовательности аминокислот.
Интерлейкины представляют собой семейство цитокинов, которые опосредуют иммунологические ответы, в том числе, воспалительные реакции. Центральное место в формировании иммунного ответа принадлежит Т-клетке, которая продуцирует многие цитокины и формирует приобретенный иммунитет к антигенам. Цитокины, продуцируемые Т-клеткой, подразделяют на тип 1 и тип 2 (Kelso, A. Immun. Cell Biol. 76: 300-317 (1998). Цитокины типа 1 включают IL-2, интерферон-гамма (IFN-γ), LT-α и участвуют в воспалительных ответах, в формировании иммунитета к вирусам, иммунитета к внутриклеточным паразитам и принимают участие в реакции отторжения трансплантата. Цитокины типа 2 включают IL-4, Il-5, IL-6, IL-10 и IL-13 и участвуют в гуморальных ответах, в формировании иммунитета к гельминтам и в аллергических ответных реакциях. Цитокины, которые имеют сходство так с типом 1, так и с типом 2, включают IL-3, GM-CSF и TNF-α. Ряд сведений позволяет предположить, что популяции Т-клеток, продуцирующих цитокины типа 1 и 2, предпочтительно мигрируют в различные типы воспаленной ткани.
С терапевтической точки зрения особый интерес представляют интерфероны (обзоры по интерферонам см. De Maeyer and De Maeyer-Guignard, “Interferons” в The Cytokine Handbook, 3 rd Edition, Thompson (ed.), pages 491-516 (Academic Press Ltd. 1998) и Walsh, Biopharmaceuticals: Biochemistry and Biotechnology, pages 158-188 (John Wiley & Sons 1998)). Интерфероны проявляют самую разнообразную биологическую активность и могут применяться для лечения некоторых аутоиммунных заболеваний, в частности, рака, а также для усиления иммунного ответа против инфекционных агентов, в том числе вирусов, бактерий, грибов и простейших. В настоящее время идентифицированы шесть форм интерферона, которые делят на две большие группы. Так называемые интерфероны “типа I” включают IFN-α, IFN-β, IFN-ω, IFN-δ и интерферон-τ. В настоящее время IFN-γ и один субкласс IFN-α являются единственными интерферонами типа II.
Интерфероны типа I, которые, как полагают, происходят от одного родительского гена, сохранили достаточно сходную структуру и способны осуществлять свое действие посредством одного и того же рецептора на поверхности. α-Цепь рецептора IFN-α/β человека содержит внеклеточную N-концевую область, которая обладает свойствами рецептора цитокина класса II. IFN-γ не обладает значительной степенью гомологии с IFN типа I или с IFN-α-субтипом типа II, однако, обладает рядом биологических активностей, сходных с IFN типа I.
Практикующие врачи используют преимущества, предоставляемые множественностью активности интерферонов, для лечения широкого круга состояний. Например, одна из форм IFN-α разрешена к применению в более чем 50 странах для лечения таких болезненных состояний как лейкемия “волосатых” клеток, почечная карцинома, карционома базальных клеток, злокачественная меланома, СПИД-ассоциированная саркома Капоши, множественная миелома, хроническая миелогенная лейкемия, не-ходжкинская лимфома, папилломатоз гортани, грибовидный микоз, остроконечная кондилома, хронический гепатит В, гепатит С, хронический гепатит D, и хронический не вирусный гепатит А, гепатит не-В/С. Администрация США по контролю за продуктами питания и лекарственными средствами одобрила применение IFN-β для лечения рассеянного склероза, хронических заболеваний нервной системы. IFN-γ применяют для лечения хронических гранулематозных заболеваний, при этом интерферон усиливает иммунный ответ пациента, чтобы разрушить инфекцию, вызванную бактериями, грибками, патогенными простейшими. Клинические исследования показывают также, что IFN-γ может применяться при лечении СПИДа, лейшманиоза и лепроматозной лепры.
IL-28, IL-28B и IL-29 составляют недавно открытое новое семейство белков, последовательность которых гомологичная последовательности интерферонов типа I и которые обладают геномной гомологией по отношению к IL-10. Указанное новое семейство описано в совместной патентной заявке РСТ WO 02/086087 и Sheppard et al., Nature Immunol. 4:63-68, 2003); оба документа включены в настоящее описание посредством ссылки. По своим способностям индуцировать антивирусное состояние в клетках IL-28 и IL-29 функционально напоминают интерфероны типа I, однако, в отличие от интерферонов типа I они не проявляют антипролиферативную активность против некоторых линий В-клеток.
Известно, что IL-28 и IL-29 имеют нечетное количество цистеинов (заявка РСТ WO 02/086087 и Sheppard et al., выше). Экспрессия рекомбинантных IL-28 и IL-29 может привести к гетерогенной смеси белков, образованной внутримолекулярными дисульфидными связями во многих конформациях. Разделение указанных форм может быть сложным и трудоемким. Поэтому желательно предоставить молекулы IL-28 и IL-29, которые после экспрессии дают один тип формирования внутримолекулярных дисульфидных связей, а также разработать способы формирования складчатой структуры и очистки указанных препаратов, с целью сохранения их гомогенности. Таким образом, в настоящем изобретении предлагаются композиции и способы получения гомогенных препаратов IL-28 и IL-29.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
В настоящем описании широко используют ряд терминов. С целью облегчения понимания изобретения приводятся следующие определения.
Если не указано иное, определения в единственном числе, “по крайней мере, один” обозначает один или более одного.
Термин “аффинная метка” применяется в настоящем описании для обозначения полипептидного сегмента, который может быть присоединен ко второму полипептиду, с целью очистки или детектирования второго пептида или же с целью создания участка для присоединения второго пептида к субстрату. В принципе, в качестве аффинной метки может применяться пептид или белок, для которого существует антитело или другой специфический связывающий агент. Аффинные метки включают полигистидиновую метку, белок А (Nilsson et al., EMBO J. 4: 1075, 1985; Nilsson et al., Methods Enzymol. 198: 3, 1991), глутатион-S-трансферазу (Smith and Johnson, Gene 67: 31, 1988), аффинную метку Glu-Glu (Grusenmeyer et al., Proc. Natl. Acad. Sci. USA 82: 7952-4, 1985), вещество Р, пептид Flag™ (Hopp et al., Biotechnology 6: 1204-10, 1988), пептид связывания стрептавидина или другой антигенный эпитоп или домен связывания. См. общие сведения в Ford et al., Protein Expression and Purification 2: 95-107, 1991. ДНК, кодирующие аффинные метки, доступны от коммерческих поставщиков (в частности, от компании Pharmacia Biotech, Пискатауэй, Нью-Джерси).
Термин “аллельный вариант” используется в настоящем описании для обозначения любой из двух или нескольких альтернативных форм гена, занимающих тот же самый хромосомный локус. Аллельный вариант обычно возникает в результате мутации и может привести к фенотипному полимофизму внутри популяции. Генная мутация может быть молчащей мутацией (изменений в кодируемом полипептиде не происходит) или может кодировать полипептиды, которые имеют измененную последовательность аминокислот. Термин аллельный вариант используется в настоящем описании также для обозначения белка, кодируемого аллельным вариантом гена.
Термины “аминоконцевой” и “карбоксиконцевой” используются в настоящем описании для обозначения положений в полипептидах. В соответствии с контекстом указанные термины применяют со ссылкой на конкретную последовательность или часть полипептида для обозначения близости или относительного положения. Например, некоторая последовательность, размещенная карбокситерминально относительно сравниваемой последовательности в полипептиде, располагается проксимально к карбоксильному концу сравниваемой последовательности, но не обязательно у карбоксильного конца полипептида полной длины.
Термин “пара комплемент/антикомплемент” обозначает неидентичные фрагменты которые в определенных условиях образуют не ковалентно связанную устойчивую пару. Например, биотин и авидин (или стрептавидин) являются прототипными членами пары комплемент/антикомплемент. Другими примерами пар комплемент/антикомплемент являются пары антитело/антиген (или гаптен или эпитоп), смысловая/антисмысловая полипептидные пары и т.п. В том случае, когда желательна последующая диссоциация пары комплемент/антикомплемент, сродство связывания пары комплемент/антикомплемент должно составлять <109 М-1.
Термин “вырожденная нуклеотидная последовательность” обозначает последовательность нуклеотидов, которая включает один или несколько вырожденных кодонов (по отношению к сравниваемой молекуле полинуклеотида, кодирующего полипептид). Вырожденные кодоны содержат различные триплеты нуклеотидов, но кодируют один и тот же остаток аминокислоты (например, триплеты GAU и GAC каждый кодируют Asp).
Термин “экспрессирующий вектор” применяют для обозначения молекулы ДНК, линейной или циклической, включающей фрагмент, который кодирует представляющий интерес полипептид, операбельно присоединенный к дополнительным сегментам, обеспечивающим его транскрипцию. Подобные дополнительные сегменты включают последовательности промотора и терминатора транскрипции, а также могут включать одну или несколько точек начала репликации, один или несколько селектируемых маркеров, энхансер, сигнал полиаденилирования и т.д. Экспрессирующие векторы обычно получают из плазмидных или вирусных ДНК или же они могут содержать элементы и тех и других.
Термин “изолированный” применительно к полинуклеотидам обозначает полинуклеотид, который выделен из его естественной генной среды и таким образом освобожден от других посторонних или нежелательных кодирующих последовательностей и существует в форме, которая подходит для использования в системе продуцирования белка, полученной методами генной инженерии. Подобные изолированные молекулы представляют собой такие молекулы, которые выделены из естественной среды и включают кДНК и геномные клоны. Изолированные молекулы ДНК по настоящему изобретению свободны от других генов, с которыми они обычно связаны, но могут включать нативные 5' и 3' не транслируемые участки, такие как промоторы и терминаторы транскрипции. Идентификация ассоциированных участков должна быть понятна для специалистов в данной области техники (см., например, Dynan and Tijan, Nature 316: 774-78, 1985).
“Изолированный” (или “выделенный”) полипептид или белок представляет собой полипептид или белок, который находится в условиях, отличных от условий его естественного окружения, т.е. не в крови или в ткани животного. В предпочтительной форме изолированный полипептид практически не содержит других полипептидов, в особенности других полипептидов животного происхождения. Полипептиды предпочтительно предоставляют в высоко чистой форме, т.е. с чистотой более 95%, более предпочтительно, с чистотой более 99%. При использовании в этом контексте, термин “изолированный” не исключает присутствие того же самого полипептида в альтернативных физических формах, таких как димеры или иным образом гликозилированные или функционализованные формы.
При использовании термина “уровень” по отношению к иммунным клеткам, таким как NK-клетки, Т-клетки, в частности цитотоксические Т-клетки, В-клетки и т.п., повышенный уровень обозначает либо увеличенное количество клеток, либо повышенную активность функций клеток.
Термин “уровень” по отношению к вирусным инфекциям относится к изменению уровня вирусной инфекции и включает, но этим не ограничиваясь, изменение уровня CTLs или NK-клеток (как указано выше), уменьшенную вирусную нагрузку, повышенный титр антивирусного антитела, пониженные серологические уровни аланинаминотрансферазы или улучшение, которое определяют гистологическим анализом ткани-мишени или органа-мишени. Установление того, являются ли указанные изменения уровня значимой разницей или значимыми изменениями, легко может быть установлено специалистом в данной области техники.
Термин “операбельно связан” по отношению к сегментам ДНК обозначает, что сегменты расположены таким образом, что они согласованно выполняют предназначенную им функцию, например, транскрипция начинается у промотора и протекает далее через кодирующий сегмент к терминации транскрипции.
Термин “ортолог” обозначает полипептид или белок, полученный из одного вида, который является функциональным двойником полипептида или белка, выделенного из других видов. Различия в ортологах являются результатом видообразования.
“Паралоги” являются различимыми, но структурно родственными белками, производимыми организмом. Полагают, что паралоги возникают вследствие дубликации генов. Например, α-глобин, β-глобин и миоглобин являются паралогами по отношению друг к другу.
“Полинуклеотид” представляет собой одноцепочечный или двухцепочечный полимер, составленный из дезоксирибонуклеотидных или рибонуклеотидных оснований, которые читаются от 5'-конца к 3'-концу. Полинуклеотиды включают РНК и ДНК и могут быть выделены из природных источников, синтезированы in vitro или получены комбинированием природных или синтетических молекул. Размеры полинуклеотидов выражают в парах оснований (сокращенно “п.о.”), нуклеотидах (“н”) или тысячах оснований (“т.о.”). Если позволяет контекст, то последние два термина могут описывать полинуклеотиды, которые являются одноцепочечными или двухцепочечными. Если термин применяют по отношению к двухцепочечным молекулам, то его используют для обозначения полной длины и в этом случае следует понимать, что он эквивалентен термину “пары оснований”. Для специалиста должно быть очевидным, что две цепочки двухцепочечного полинуклеотида могут слегка различаться по своей длине, и их концы могут иметь уступы как результат ферментативного расщепления; таким образом, не все нуклеотиды внутри двухцепочечного полинуклеотида могут быть парными.
“Полипептид” представляет собой полимер, составленный остатками аминокислот, которые соединены пептидными связями независимо от того, продуцируются они в природе или получаются синтетически. Полипептид, содержащий меньше приблизительно 10 аминокислотных остатков, обычно называют “пептидом”.
Термин “промотор” используют в настоящем описании по его известному из области техники значению для обозначения части гена, содержащего последовательности ДНК, которые обеспечивают связывание РНК-полимеразы и инициацию транскрипции. Последовательности промотора обычно, но не всегда, располагаются у 5'-конца некодирующих участков генов.
“Белок” представляет собой макромолекулу, составленную одной или несколькими полипептидными цепочками. Белок может также содержать непептидные компоненты, такие как углеводные группы. Углеводы и другие непептидные заместители могут быть добавлены к белку в клетке, в которой белок продуцируется, и различаются в зависимости от типа клетки. Белки определяют в настоящем описании в терминах структур аминокислотного скелета; заместители, такие как углеводные группы, обычно не указываются, но они, тем не менее, могут присутствовать.
Термин “рецептор” обозначает ассоциированный с клеткой белок, который связывается с биоактивной молекулой (в частности, с лигандом) и опосредует влияние лиганда на клетку. Соединенные с мембраной рецепторы характеризуются мультипептидной структурой, которая включает внеклеточный домен связывания лиганда и внутриклеточный домен эффектора, который обычно принимает участие в передаче сигнала. Связывание лиганда с рецептором приводит к конформационным изменениям в рецепторе, которые вызывают взаимодействие между доменом эффектора и другой молекулой или другими молекулами в клетке. Указанное взаимодействие, в свою очередь, приводит к изменению обмена веществ в клетке. Результаты обмена веществ, которые связаны с взаимодействием рецептора и лиганда, включают транскрипцию гена, фосфорилирование, дефосфорилирование, усиление продукции циклических АМФ, мобилизацию клеточного кальция, мобилизацию мембранных липидов, адгезию клеток, гидролиз липидов инозитола и гидролиз фосфолипидов. В общем случае, рецепторы могут быть рецепторами, связанными с мембраной, цитозольными или ядерными рецепторами; мономерными (например, рецептор тироидстимулирующего гормона, бета-адренергический рецептор) или мультимерными (в частности, рецептор для PDGF, рецептор гормона роста, рецептор IL-3, рецептор для GM-CSF, рецептор для G-CSF, рецептор эритропоэтина и рецептор IL-6) рецепторами.
Термин “секреторная сигнальная последовательность” обозначает последовательность ДНК, которая кодирует полипептид (“секреторный полипептид”), в качестве компонента большего по размеру полипептида, направляет больший по размеру полипептид по секреторному пути в клетке, в которой он синтезируется. Больший по размеру полипептид обычно отщепляют, чтобы удалить секреторный пептид при движении по секреторному пути.
Термин “вариант сплайсинга” используют в настоящем описании для обозначения альтернативных форм РНК, транскрибированных из гена. Вариация сплайсинга естественным образом возникает при использовании альтернативных участков сплайсинга внутри транскрибированной молекулы РНК или реже между раздельно транскрибированными молекулами РНК и может привести к нескольким молекулам мРНК, транскрибированным из одного и того же гена. Варианты сплайсинга могут кодировать полипептиды, имеющие измененную аминокислотную последовательность. Термин вариант сплайсинга используют в настоящем описании также для обозначения белка, кодируемого вариантом сплайсинга мРНК, транскрибированной из гена.
Следует понимать, что молекулярные массы и размеры полимеров, определяемых качественными аналитическими методами (в частности, электрофорезом), имеют приблизительные значения. В том случае, когда эти значения обозначают как “около” Х или “приблизительно” Х, то следует понимать, что указанное значение Х приведено с точностью ± 10%.
“zcyto20”, “zcyto21”, “zcyto22” являются прежде использовавшимися обозначениями для IL-28A человека, IL-29 человека и IL-28В человека, соответственно. Нуклеотидная и аминокислотная последовательность для IL-28A приведены в SEQ ID NO: 1 и SEQ ID NO: 2, соответственно. Нуклеотидная и аминокислотная последовательность для IL-29 приведены в SEQ ID NO: 3 и SEQ ID NO: 4, соответственно. Нуклеотидная и аминокислотная последовательность для IL-28В приведены в SEQ ID NO: 5 и SEQ ID NO: 6, соответственно. Указанные последовательности полностью описаны в РСТ заявке WO 02/086087, совместно поданной компанией ZymoGenetics, Inc., которая включена в настоящее описание посредством ссылки.
“zcyto24” и “zcyto25” являются прежде использовавшимися обозначениями для IL-28 мыши, и они приведены, соответственно, в SEQ ID NO: 7, 8, 9 и 10. Полинуклеотиды и пептиды полностью описаны в РСТ заявке WO 02/086087, совместно поданной компанией ZymoGenetics, Inc., которая включена в настоящее описание посредством ссылки.
“zcytor19” является прежде использовавшимся обозначением для α-субъединицы IL-28, и она приведена в SEQ ID NO: 11. Полинуклеотиды и пептиды приведены в РСТ заявке WO 02/20569, поданной компанией Schering, Inc., и заявке WO 02/44209, принадлежащей компании ZymoGenetics, Inc., которые включены в настоящее описание посредством ссылки. “Рецептор IL-28” обозначает α-субъединицу IL-28 и субъединицу CRF2-4, образующую гетеродимерный рецептор.
В настоящем изобретении предлагаются молекулы полинуклеотидов, включая молекулы ДНК и РНК, кодирующие мутантные IL-28 и IL-29, содержащие замены цистеина, которые приводят к экспрессии препарата рекомбинантных IL-28 и IL-29, который представляет собой гомогенный препарат. В соответствии с настоящим изобретением гомогенным препаратом IL-28 и IL-29 является препарат, в котором, по крайней мере, на 98% сохраняется единая внутримолекулярная структура дисульфидных связей в очищенном полипептиде. В других вариантах осуществления настоящего изобретения единая дисульфидная конформация в препарате очищенного полипептида на 99% является гомогенной. В общем случае, как указано в настоящем описании, указанные мутанты, содержащие замены цистеина, сохраняют некоторую биологическую активность, свойственную IL-28 и IL-29 дикого типа. Например, молекулы по настоящему изобретению могут связываться с рецептором IL-28 с определенной специфичностью. В общем случае, связывание лиганда с родственным рецептором является специфическим в том случае, когда значение KD составляет в интервале от 100 нМ до 100 пМ. Специфическое связывание в диапазоне значений KD от 100 мМ до 10 нМ соответствует связыванию с низкой аффинностью. Специфическое связывание в диапазоне значений KD от 2,5 пМ до 100 пМ соответствует связыванию с высокой аффинностью. В другом примере биологическая активность мутантных IL-28 и IL-29, содержащих замены цистеина, проявляется в том случае, когда молекулы способны проявлять определенный уровень антивирусной активности, связанной с IL-28 и IL-29 дикого типа. Определение уровня антивирусной активности подробно описывается в настоящем изобретении.
При ссылке на IL-28 указанный термин означает как IL-28А, так и IL-28В. Ранее IL-28А обозначали как zcyto20 (SEQ ID NO: 1 и 2), IL-29 обозначали как zcyto21 (SEQ ID NO: 3 и 4), а IL-28В обозначали как zcyto22 (SEQ ID NO: 5 и 6). (См. РСТ заявка WO 02/086087 и Sheppard et al., выше). Мышиные ортологи для IL-28 ранее обозначали как zcyto24 (SEQ ID NO: 7 и 8), zcyto25 (SEQ ID NO: 9 и 10).
Ген IL-28А дикого типа кодирует полипептид из 200 аминокислот, как показано в SEQ ID NO: 2. Сигнальную последовательность для IL-28А можно прогнозировать как составленную из аминокислотных остатков от -25 (Met) до аминокислотного остатка -1 (Ala) из SEQ ID NO: 2. Зрелый пептид для IL-28А начинается у аминокислотного остатка 1 (Val) из SEQ ID NO: 2. Спирали IL-28А прогнозируются следующим образом: спираль А определена аминокислотными остатками с 31 (Ala) по 45 (Leu); спираль В определена аминокислотными остатками с 58 (Thr) по 65 (Gln); спираль С определена аминокислотными остатками с 69 (Arg) по 86 (Ala); спираль D определена аминокислотными остатками с 95 (Val) по 114 (Ala); спираль Е определена аминокислотными остатками с 126 (Thr) по 142 (Lys); а спираль F определена аминокислотными остатками с 148 (Cys) по 169 (Ala); как показано в SEQ ID NO: 2.
Ген IL-29 дикого типа кодирует полипептид из 200 аминокислот, как показано в SEQ ID NO: 4. Сигнальную последовательность для IL-29 можно прогнозировать как составленную из аминокислотных остатков от -19 (Met) до аминокислотного остатка -1 (Ala) из SEQ ID NO: 4, SEQ ID NO: 119, SEQ ID NO: 121. Зрелый пептид для IL-29 начинается у аминокислотного остатка 1 (Gly) из SEQ ID NO: 4. IL-29 описан в РСТ заявке WO02/02627. Спирали IL-29 прогнозируются следующим образом: спираль А определена аминокислотными остатками с 30 (Ser) по 44 (Leu); спираль В определена аминокислотными остатками с 57 (Asn) по 65 (Val); спираль С определена аминокислотными остатками с 70 (Val) по 85 (Ala); спираль D определена аминокислотными остатками с 92 (Glu) по 111 (Gln); спираль Е определена аминокислотными остатками с 118 (Thr) по 139 (Lys); а спираль F определена аминокислотными остатками с 144 (Gly) по 170 (Leu); как показано в SEQ ID NO: 4.
Ген IL-28B дикого типа кодирует полипептид из 200 аминокислот, как показано в SEQ ID NO: 6. Сигнальную последовательность для IL-28B можно прогнозировать как составленную из аминокислотных остатков от -21 (Met) до аминокислотного остатка -1 (Ala) из SEQ ID NO: 6. Зрелый пептид для IL-28B начинается у аминокислотного остатка 1 (Val) из SEQ ID NO: 6. Спирали IL-28B прогнозируются следующим образом: спираль А определена аминокислотными остатками с 31 (Ala) по 45 (Leu); спираль В определена аминокислотными остатками с 58 (Thr) по 65 (Gln); спираль С определена аминокислотными остатками с 69 (Arg) по 86 (Ala); спираль D определена аминокислотными остатками с 95 (Gly) по 114 (Ala); спираль Е определена аминокислотными остатками с 126 (Thr) по 142 (Lys); а спираль F определена аминокислотными остатками с 148 (Cys) по 169 (Ala); как показано в SEQ ID NO: 6.
В настоящем изобретении предлагаются мутации в последовательностях IL-28 и IL-29 дикого типа, как показано в SEQ ID NO: 1, 2, 3, 4, 5 и 6, которые приводят к экспрессии индивидуальных форм молекул IL-28 или IL-29. Поскольку, как полагают, гетерогенность форм является результатом образования разнообразных комбинаций внутримолекулярных дисульфидных связей, то конкретные варианты осуществления настоящего изобретения включают мутации по остаткам цистеина в последовательностях IL-28 и IL-29 дикого типа. При экспрессии IL-28 и IL-29 в E. сoli присутствует N-концевой или аминоконцевой метионин. Например, в SEQ ID NO: 12-17 показаны нумерации нуклеотидных и аминокислотных последовательностей для IL-28А, IL-29 и IL-28В, когда присутствует N-концевой Met. В Таблице 1 приведены возможные комбинации пар цистеина, соединенных внутримолекулярными дисульфидными связями, для IL-28А, IL-28В и IL-29 дикого типа.
Таблица 1
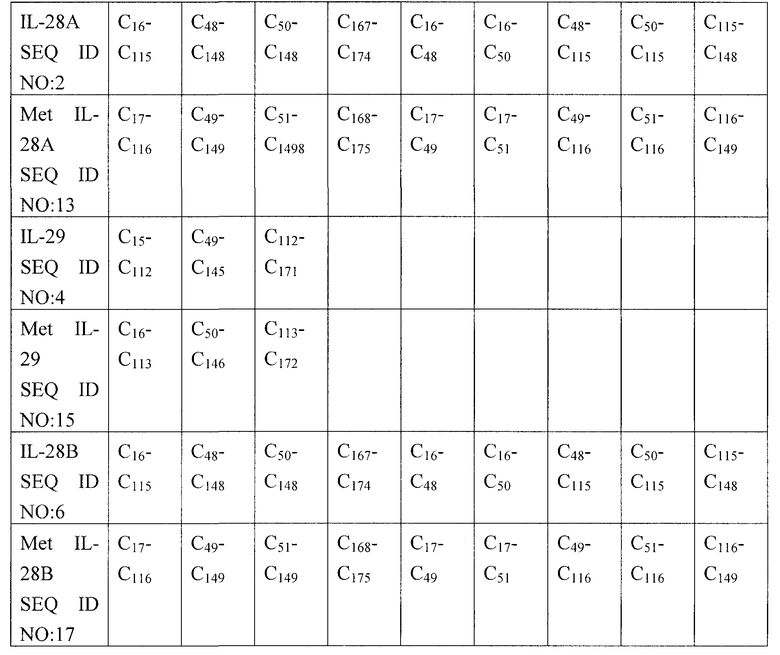
Молекулы полинуклеотидов и полипептидов по настоящему изобретению имеют мутации по одному или нескольким цистеинам, имеющимся в молекулах IL-28А, IL-29 и IL-28В дикого типа, и, тем не менее, они сохраняют биологическую активность, как указано в настоящем описании. В Таблице 2 приведены примеры мутаций с заменой цистеина, в частности, точечных мутаций с заменой цистеина (C) на серин (S).
Таблица 2

Было показано, что все члены рассматриваемого семейства связываются с одним и тем же цитокиновым рецептором класса II, IL-28R. α-Субъединицу IL-28 ранее обозначали как рецептор zcytor19. Не вдаваясь в теорию, можно считать, что указанные молекулы проявляются во всех сигналах, передающихся через рецептор IL-28 по одному и тому же пути. Рецептор IL-28 описан в совместно поданной РСТ патентной заявке WO 02/44209, которая включена в настоящее описание посредством ссылки; Sheppard et al., выше; Kotenko et al., Nature Immunol. 4: 69-77, 2003; и РСТ WO 03/040345. IL-28R является членом цитокиновых рецепторов класса II, которые характеризуются наличием в их внеклеточных доменах одного или нескольких рецепторных модулей цитокина (CRM). Другие цитокиновых рецепторы класса II включают zcytor11 (патент США № 5965704 совместного владения), CRF2-4 (номер доступа Z17227 в базе данных GenBank), IL-10R (номера доступа U00672 и NM_001558 в базе данных GenBank), DIRS1, zcytor7 (патент США № 5945511 совместного владения) и тканевый фактор. Рецептор IL-28, как и все известные рецепторы класса II, за исключением альфа-цепи рецептора к интерферону-альфа/бета, содержит в своем внеклеточном домене лишь CRM одного класса II.
Цитокины с пучками из четырех спиралей группируют также по длине составляющих их спиралей. Цитокины “динноцепочечной” формы обычно состоят из спиралей, содержащих 24-30 остатков, и они включают IL-6, цилиарный нейротрофический фактор (CNTF), фактор ингибирования лейкемии (LIF) и человеческий гормон роста (hGH). Цитокины “короткоцепочечной” формы обычно состоят из спиралей, содержащих 18-21 остатков, и они включают IL2, IL-4 и GM-CSF. Исследования с использованием CNTF и IL-6 показали, что спиралью из CNTF можно заменить эквивалентную спираль в IL-6, при этом химера приобретает способность связывать CNTF. Таким образом, оказывается, что функциональные домены четырехспиральных цитокинов определяются степенью структурной гомологии, независимо от идентичности последовательности, и могут сохранять функциональную целостность в химере (Kallen et al., J. Biol. Chem. 274: 11859-11867, 1999). Таким образом, мутантные полипептиды IL-28 и IL-29, содержащие замены цистеина, могут быть полезны для получения химерных слитых молекул, в частности, с другими интерферонами, с целью определения и модулирования специфичности связывания рецептора. Особый интерес представляют слитые белки, которые объединяют спиральные и петлевые области интерферонов и цитокинов, таких как TNF-α, IL-10 и человеческий гормон роста.
В настоящем изобретении предлагаются молекулы полинуклеотидов, включая молекулы ДНК и РНК, которые кодируют, например, мутантные полипептиды IL-28 или IL-29, содержащие замены цистеина. Например, в настоящем изобретении предлагаются вырожденные нуклеотидные последовательности, кодирующие приведенные в настоящем описании полипептиды IL-28A C48S, Met IL-28A C49S, IL-28A C50S, Met IL-28A C51S, IL-29 C171S и Met IL-29 C172S. Для специалистов должно быть понятно, что ввиду вырожденности генетического кода в указанных молекулах полинуклеотидов возможны значительные вариации в последовательностях. SEQ ID NO: 30, 31, 32, 33, 34 и 35 являются вырожденными последовательностями ДНК, которые охватывают все молекулы ДНК, кодирующие IL-28A C48S, Met IL-28A C49S, IL-28A C50S, Met IL-28A C51S, IL-29 C171S и Met IL-29 C172S, соответственно. Для специалистов должно быть понятно, что вырожденные последовательности SEQ ID NO: 30, 31, 32, 33, 34 и 35 обозначают также все последовательности РНК, кодирующие SEQ ID NO: 30, 31, 32, 33, 34 и 35, путем замены T на U и, таким образом, также рассматриваются в настоящем описании.
Полипептиды IL-28A по настоящему изобретению включают также мутации во втором цистеине, С2, зрелого полипептида. Например, С2 от N-конца или аминового конца в полипептиде с SEQ ID NO: 2 является цистеином в аминокислотном положении 48 или положении 49 (с дополнительным N-концевым Met), если полипептид экспрессируется в E. сoli (см., например, SEQ ID NO: 13). Указанный второй цистеин (которых имеется семь, как в IL-28B), или С2 в IL-28A, может быть мутирован, например, заменой на серин, аланин, треонин, валин или аспарагин. Мутантные молекулы IL-28A С2 по настоящему изобретению включают, например, молекулы полинуклеотидов, приведенные в SEQ ID NO: 20 и 22, в том числе молекулы ДНК и РНК, которые кодируют мутантные по С2 полипептиды IL-28A, как показано в SEQ ID NO: 21 и 23, соответственно. SEQ ID NO: 36 и 37 являются дополнительными полипептидами IL-28A С2 по настоящему изобретению.
Помимо мутантов IL-28A С2, настоящее изобретение включает также полипептиды IL-28A, содержащие мутации в положении третьего цистеина, С3, зрелого полипептида. Например, С3 от N-конца или аминового конца в полипептиде с SEQ ID NO: 2 является цистеином в положении 50 или положении 51 (с дополнительным N-концевым Met), если полипептид экспрессируется в E. сoli (см., например, SEQ ID NO: 13). Мутантные молекулы IL-28A С3 по настоящему изобретению включают, например, молекулы полинуклеотидов, приведенные в SEQ ID NO: 24 и 26, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-28A С3, как показано в SEQ ID NO: 25 и 27, соответственно. SEQ ID NO: 38 и 39 являются дополнительными полипептидами IL-28A С3 по настоящему изобретению.
Полипептиды IL-28A по настоящему изобретению включают, например, SEQ ID NO: 2, 13, 19, 21, 23 и 25, которые кодируются молекулами полинуклеотидов IL-28A, приведенными в SEQ ID NO: 1, 12, 18, 20, 22 и 24, соответственно. Дополнительные полипептиды IL-28A по настоящему изобретению включают, например, SEQ ID NO: 36, 37, 38 и 39.
Полипептиды IL-28В по настоящему изобретению включают также мутации во втором цистеине, С2, зрелого полипептида. Например, С2 от N-конца или аминового конца в полипептиде с SEQ ID NO: 6 является цистеином в аминокислотном положении 48 или положении 49 (с дополнительным N-концевым Met), если полипептид экспрессируется в E. сoli (см., например, SEQ ID NO: 17). Указанный второй цистеин (которых имеется семь, как в IL-28А), или С2 в IL-28В, может быть мутирован, например, заменой на серин, аланин, треонин, валин или аспарагин. Мутантные молекулы IL-28В С2 по настоящему изобретению включают, например, молекулы полинуклеотидов, приведенные в SEQ ID NO: 122 и 124, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-28В С2, как показано в SEQ ID NO: 123 и 125, соответственно. Дополнительные мутантные молекулы IL-28В С2 по настоящему изобретению включают молекулы полинуклеотидов, приведенные в SEQ ID NO: 130 и 132, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-28В С2, приведенные в SEQ ID NO: 131 и 133, соответственно (публикация РСТ WO 03/066002 (Kotenko et al.)).
Помимо мутантов IL-28В С2, настоящее изобретение включает также полипептиды IL-28В, включающие мутации в положении третьего цистеина, С3, зрелого полипептида. Например, С3 от N-конца или аминового конца в полипептиде с SEQ ID NO: 6 является цистеином в положении 50 или положении 51 (с дополнительным N-концевым Met), если полипептид экспрессируется в E. сoli (см., например, SEQ ID NO: 17). Мутантные молекулы IL-28В С3 по настоящему изобретению включают, например, молекулы полинуклеотидов, приведенные в SEQ ID NO: 126 и 128, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-28В С3, как показано в SEQ ID NO: 127 и 129, соответственно. Дополнительные мутантные молекулы IL-28В С3 по настоящему изобретению включают молекулы полинуклеотидов, приведенные в SEQ ID NO: 134 и 136, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-28В С3, приведенные в SEQ ID NO: 135 и 137, соответственно (публикация РСТ WO 03/066002 (Kotenko et al.)).
Полипептиды IL-28В по настоящему изобретению включают, например, SEQ ID NO: 6, 17, 123, 125, 127, 129, 131, 133, 135 и 137, которые кодируются молекулами полинуклеотидов IL-28В, приведенными в SEQ ID NO: 5, 16, 122, 124, 126, 128, 130, 132, 134 и 136, соответственно.
Полипептиды IL-29 по настоящему изобретению включают также, например, мутации в пятом цистеине, С5, зрелого полипептида. Например, С5 от N-конца полипептида с SEQ ID NO: 4 является цистеином в положении 171 или положении 172 (с дополнительным N-концевым Met), если полипептид экспрессируется в E. сoli (см., например, SEQ ID NO: 15). Указанный пятый цистеин, или С5 из IL-29, может быть мутирован, например, заменой на серин, аланин, треонин, валин или аспарагин. Указанные мутантные полипептиды IL-29 С5 имеют структуру дисульфидных связей С1(Cys15 из SEQ ID NO: 4)/С3(Cys112 из SEQ ID NO: 4) и С2(Cys49 из SEQ ID NO: 4)/С4(Cys145 из SEQ ID NO: 4). Дополнительные мутантные молекулы IL-29 С5 по настоящему изобретению включают молекулы полинуклеотидов, приведенные в SEQ ID NO: 26, 28, 82, 84, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-29 С5, приведенные в SEQ ID NO: 27, 29, 83, 85, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161, соответственно. Дополнительные мутантные молекулы IL-29 С5 по настоящему изобретению включают молекулы полинуклеотидов, приведенные в SEQ ID NO: 86, 88, 94 и 96, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-29 С5, приведенные в SEQ ID NO: 87, 89, 95 и 97, соответственно (публикация РСТ WO 03/066002 (Kotenko et al.)). Дополнительные мутантные молекулы IL-29 С5 по настоящему изобретению включают молекулы полинуклеотидов, приведенные в SEQ ID NO: 102, 104, 110 и 112, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-29 С5, приведенные в SEQ ID NO: 103, 105, 111 и 113, соответственно (публикация РСТ WO 02/092762 (Baum et al.)).
Помимо мутантов IL-29 С5, настоящее изобретение включает также полипептиды IL-29, содержащие мутации в положении первого цистеина, С1, зрелого полипептида. Например, С1 от N-конца полипептида с SEQ ID NO: 4 является цистеином в положении 15 или положении 16 (с дополнительным N-концевым Met), если полипептид экспрессируется в E. сoli (см., например, SEQ ID NO: 15). Указанные мутантные полипептиды IL-29 С1 должны, таким образом, иметь прогнозируемую структуру дисульфидных связей С2(Cys49 из SEQ ID NO: 4)/С4(Cys145 из SEQ ID NO: 4) и С3(Cys112 из SEQ ID NO: 4)/С5(Cys171 из SEQ ID NO: 4). Дополнительные мутантные молекулы IL-29 С1 по настоящему изобретению включают молекулы полинуклеотидов, как показано в SEQ ID NO: 74, 76, 78 и 80, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-29 С1, приведенные в SEQ ID NO: 75, 77, 79 и 81, соответственно. Дополнительные мутантные молекулы IL-29 С1 по настоящему изобретению включают молекулы полинуклеотидов, приведенные в SEQ ID NO: 90, 92, 98 и 100, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-29 С1, приведенные в SEQ ID NO: 91, 93, 99 и 101, соответственно (публикация РСТ WO 03/066002 (Kotenko et al.)). Дополнительные мутантные молекулы IL-29 С1 по настоящему изобретению включают молекулы полинуклеотидов, приведенные в SEQ ID NO: 106, 108, 114 и 116, в том числе молекулы ДНК и РНК, которые кодируют мутантные полипептиды IL-29 С1, приведенные в SEQ ID NO: 107, 109, 115 и 117, соответственно (публикация РСТ WO 02/092762 (Baum et al.)).
Полипептиды IL-29 по настоящему изобретению, например, SEQ ID NO: 4, 15, 27, 29, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161, которые кодируются молекулами полинуклеотидов IL-29, приведенными в SEQ ID NO: 3, 14, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160, могут дополнительно включать сигнальную последовательность, приведенную в SEQ ID NO: 119, или сигнальную последовательность, приведенную в SEQ ID NO: 121. Кроме того, настоящее изобретение включает полипептиды IL-29, приведенные в SEQ ID NO: 40 и 41. Молекула полинуклеотида, кодирующего полипептид сигнальной последовательности SEQ ID NO: 119, приведена в SEQ ID NO: 118. Молекула полинуклеотида, кодирующего полипептид сигнальной последовательности SEQ ID NO: 120, приведена в SEQ ID NO: 121.
В соответствии с одним аспектом, в настоящем изобретении предлагается изолированный полипептид, содержащий последовательность, которая, по крайней мере, на 90% или на 95% идентична последовательностям аминокислотных остатков, выбранным из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. Полипептид необязательно может включать, по крайней мере, 15, по крайней мере, 30, по крайней мере, 45 или, по крайней мере, 30 последовательных аминокислот в аминокислотных последовательностях, приведенных в SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. В другом варианте осуществления настоящего изобретения изолированный полипептид составлен из аминокислотных остатков, выбранных из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. Полипептид может содержать консервативные замены аминокислот, по сравнению с аминокислотными последовательностями, выбранными из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161.
В соответствии с другим аспектом, в настоящем изобретении предлагается слитый белок, содержащий полипептид, который включает последовательность аминокислотных остатков, выбранную из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161; и полиалкилоксидный фрагмент. Полиалкилоксидный фрагмент необязательно может быть полиэтиленгликолем, таким как mPEG/пропионовый альдегид размером 20 кДа или mPEG/пропионовый альдегид размером 30 кДа. Полиэтиленгликоль может быть линейным или разветвленным. Полиэтиленгликоль может быть ковалентно присоединен к N-концу или С-концу полипептида.
В соответствии с другим аспектом, в настоящем изобретении предлагается слитый белок, содержащий первый полипептид и второй полипептид, соединенные пептидной связью, при этом первый полипептид содержит последовательность аминокислотных остатков, выбранную из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161; и второй полипептид. Второй полипептид необязательно может быть фрагментом антитела. Фрагмент антитела необязательно может представлять собой F(ab'), F(ab), Fab', Fab, Fv, scFv и/или минимальную распознаваемую единицу. Второй полипептид необязательно может быть альбумином человека. Второй полипептид необязательно может быть полипептидом, выбранным из группы, включающей аффинные метки, токсины, радионуклиды, ферменты и флуорофоры.
В Таблице 3 представлены однобуквенные коды, которые используют в SEQ ID NO: 30, 31, 32, 33, 34 и 35 для обозначения вырожденных положений нуклеотидов. “Разрешения” означают нуклеотиды, обозначенные кодовой буквой. “Комплемент” обозначает код для комплементарного(ых) нуклеотида(ов). Например, кодовая буква Y обозначает либо С, либо Т, а ее комплемент R обозначает A или G, при этом А комплементарна Т, а G комплементарна С.
Таблица 3
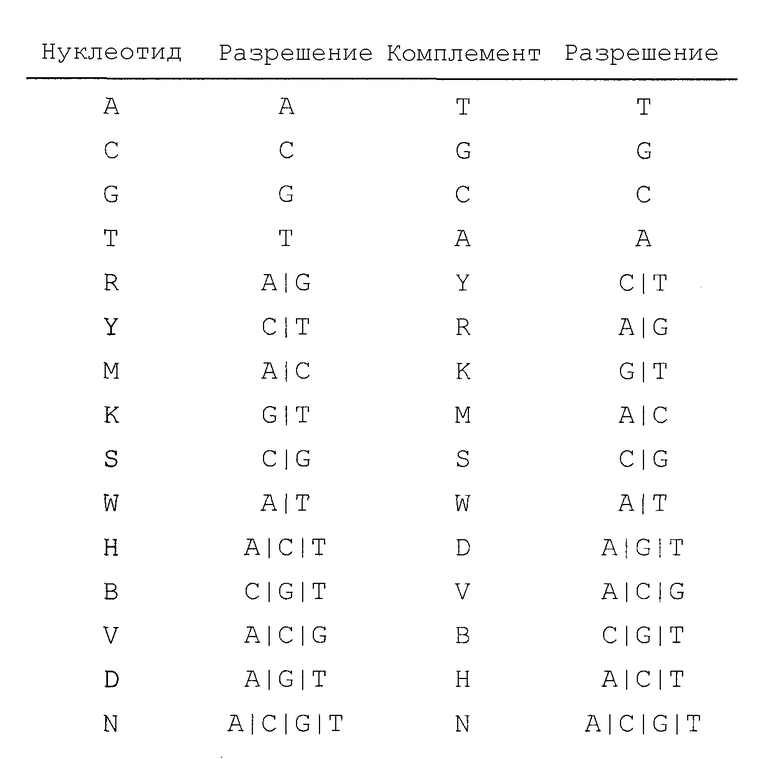
Вырожденные кодоны, которые используют в SEQ ID NO: 30, 31, 32, 33, 34 и 35, охватывающие все возможные кодоны для данной аминокислоты, приведены в Таблице 4.
Таблица 4
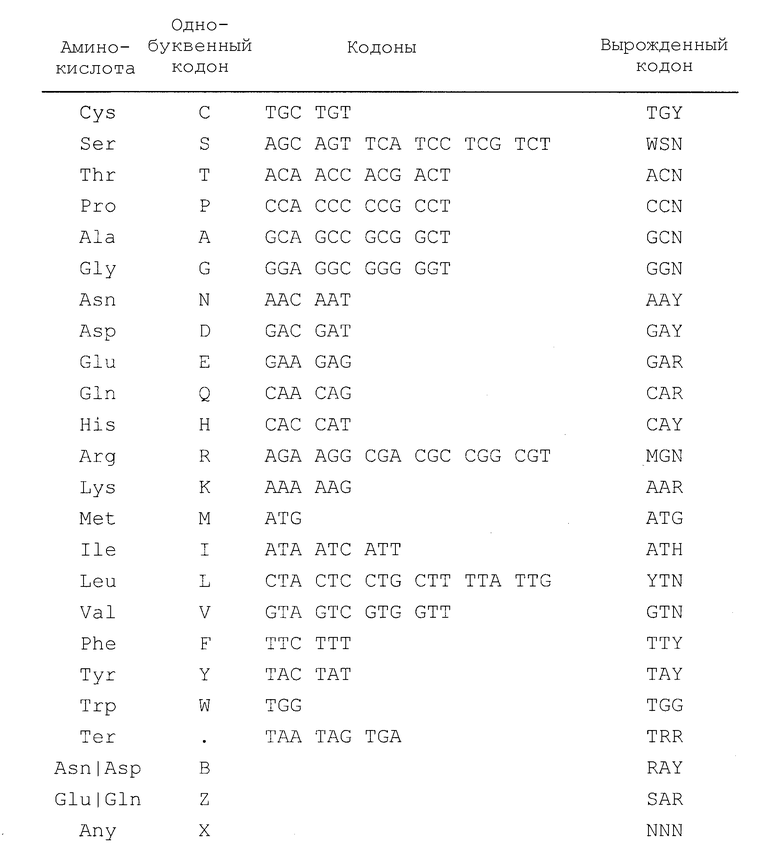
Для специалиста должно быть понятно, что некоторая неопределенность вносится при установлении вырожденного кодона, который представляет все возможные кодоны, кодирующие каждую аминокислоту. Например, вырожденный кодон для серина (WSN) может, при некоторых обстоятельствах, кодировать аргинин (ARG), а вырожденный кодон для аргинина (MGN) может, при некоторых обстоятельствах, кодировать серин (AGY). Похожая связь существует между кодонами, кодирующими фенилаланин и лейцин. Таким образом, некоторые полинуклеотиды, охватываемые вырожденными последовательностями, могут кодировать вариантные аминокислотные последовательности, однако, специалист в данной области легко сможет идентифицировать вариантные последовательности, проведя сравнение с аминокислотной последовательностью, например, SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. Вариантные последовательности могут быть легко протестированы на функциональность, как описано в настоящем описании.
Для специалиста должно быть понятно, что различные виды могут проявлять “предпочтение в использовании кодона”. Общие сведения см. Grantham et al., Nuc. Acids Res. 8: 1893-912, 1980; Haas, et al., Curr. Biol. 6: 315-24, 1996; Wain-Hobson, et al., Gene 13: 355-64, 1981; Grosjean and Fiers, Gene 18: 199-209, 1982; Holm, Nuc. Acids Res. 14: 3075-87, 1986; Ikemura, J. Mol. Biol. 158: 573-97, 1982. По тексту настоящего описания термин “предпочтение в использовании кодона” или “предпочтительные кодоны” представляет собой термин, используемый в данной области техники, и он обозначает кодоны для трансляции белка, которые наиболее часто используются в клетках определенного вида, и тем самым отдается предпочтение одному или нескольким представителям возможных кодонов, кодирующих каждую аминокислоту (см. Таблицу 4). Например, аминокислоту треонин (Thr) могут кодировать ACA, ACC, ACG или ACT, однако, в клетках млекопитающих наиболее часто используемым кодоном является АСС; в других видах, например, в клетках насекомых, дрожжах, вирусах или бактериях предпочтительными могут быть другие кодоны для Thr. Предпочтительные кодоны для определенного вида могут быть введены в полинуклеотиды по настоящему изобретению с помощью различных известных из области техники методов. Введение последовательностей с предпочтительными кодонами в рекомбинантную ДНК может, например, увеличить продукцию белка за счет того, что трансляция белка становится более эффективной в конкретном типе клеток или видах. Поэтому последовательность с вырожденным кодоном, приведенная в SEQ ID NO: 30, 31, 32, 33, 34 и 35, служит в качестве матрицы для оптимизации экспрессии полинуклеотидов в различных типах клеток и видах, которые обычно используют в данной области и которые приводятся в настоящем описании. Последовательности, содержащие предпочтительные кодоны, могут быть протестированы и оптимизированы для экспрессии в различных видах и протестированы на их функциональность, как указано в настоящем описании.
В соответствии с другим аспектом, в настоящем изобретении предлагается изолированный полинуклеотид, выбранный из группы, включающей SEQ ID NO: 1, 3, 5, 7, 9, 12, 14, 16, 18, 20, 22, 24, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160.
В соответствии с другим аспектом, в настоящем изобретении предлагается изолированный полинуклеотид, который способен гибридизоваться с последовательностью, выбранной из группы, включающей SEQ ID NO: 1, 3, 5, 7, 9, 12, 14, 16, 18, 20, 22, 24, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160, или ее комплементом в условиях гибридизации под действием 50%-ного формамида, 5xSSC (1xSSC: 0,15 М хлорида натрия и 15 мМ цитрата натрия), 50 мМ фосфата натрия (рН 7,6), 5х раствора Денхардта (100х раствор Денхардта: 2% (масс./об.) фикола 400, 2% (масс./об.) поливинилпирролидона, 2% (масс./об.) бычьего сывороточного альбумина, 10% сульфата декстрана и 20 мг/мл денатурированной фрагментированной ДНК спермы лосося при температуре от приблизительно 42°С до приблизительно 70°С, при этом изолированный полинуклеотид кодирует полипептид, обладающий антивирусной активностью. Кодируемый полипептид необязательно обладает антивирусной активностью к гепатиту В и/или гепатиту С. Изолированный полинуклеотид необязательно может кодировать, по крайней мере, часть последовательности, выбранной из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. Изолированный полинуклеотид может кодировать полипептид, представленный последовательностями SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161.
В соответствии с другим аспектом, в настоящем изобретении предлагается изолированный полинуклеотид, кодирующий полипептид, при этом кодируемый полипептид выбирают из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161.
В соответствии с другим аспектом, в настоящем изобретении предлагается изолированный полинуклеотид, кодирующий полипептид, при этом последовательность кодируемого полипептида, по крайней мере, на 90% или на 95% идентична последовательности, выбранной из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161, и при этом кодируемый полипептид обладает антивирусной активностью. Кодируемый полипептид необязательно обладает антивирусной активностью по отношению к гепатиту В и/или гепатиту С.
Как указано ранее, изолированные полинуклеотиды по настоящему изобретению включают ДНК и РНК. Способы получения ДНК и РНК известны из области техники. В общем случае РНК выделяют из ткани или клетки, которая продуцирует большое количество мутантной РНК IL-28 или IL-29, содержащей замены цистеина. Подобные ткани и клетки идентифицируют методом нозерн-блоттинга (Thomas, Proc. Natl. Acad. Sci. USA 77: 5201, 1980) или скринингом кондиционированной среды из различных типов клеток на активность к клеткам-мишеням или тканям. Как только установлена активность РНК-продуцирующих клеток или тканей, полная РНК может быть получена экстракцией изотиоцианатом гуанидина с последующим выделением центрифугированием в градиенте CsCl (Chirgwin et al., Biochemistry 18: 52-94, 1979). Poly (A)+ RNA получают из полной РНК по методу, разработанному Aviv и Leder (Proc. Natl. Acad. Sci. USA 69: 1408-12, 1972). Комплементарную ДНК (кДНК) получают из Poly (A)+ RNA известными способами. В качестве альтернативы, можно выделить геномную ДНК. Полинуклеотиды, кодирующие мутантные полипептиды IL-28 или IL-29, содержащие замены цистеина, затем идентифицируют и изолируют, например, методом гибридизации или ПЦР.
Полноразмерные клоны, кодирующие мутантные IL-28 или IL-29, содержащие замены цистеина, могут быть получены по обычным способам клонирования. Предпочтительны клоны комплементарной ДНК (кДНК), хотя для ряда применений (в частности, для экспрессии в трансгенных животных) может оказаться предпочтительным использовать геномный клон или модифицировать клон кДНК с тем, чтобы включить в него, по крайней мере, один геномный интрон. Методы получения кДНК или геномных клонов хорошо известны и легко могут быть осуществлены специалистами в данной области техники; они включают использование раскрываемой в настоящем изобретении последовательности или ее части для приготовления зонда или праймера из библиотеки. Экспрессионные библиотеки можно зондировать антителами к фрагментам рецептора IL-28 или другими специфически связывающимися партнерами.
Для специалистов является очевидным, что последовательность, приведенная, например, в SEQ ID NO: 1, 3, 5, соответственно, представляет собой мутации единичных аллелей в полосах IL-28 и IL-29 человека и что возможны вариации в аллелях и альтернативный сплайсинг. Например, вариант IL-29 был идентифицирован там, где аминокислотный остаток 169 (Asn), показанный в SEQ ID NO: 4, является остатком Arg, как описано в WO 02/086087. Подобные аллельные варианты включены в настоящее изобретение. Аллельные варианты этой последовательности могут быть клонированы зондированием кДНК или геномных библиотек от различных индивидов согласно стандартным методикам. Аллельные варианты последовательности ДНК, приведенной в SEQ ID NO: 1, 3 и 5, включая аллельные варианты, содержащие молчащие мутации, и аллельные варианты, в которых мутации приводят к изменениям в аминокислотной последовательности, входят, помимо мутаций по цистеину, в объем настоящего изобретения, так же, как и белки, которые представляют собой аллельные варианты последовательностей SEQ ID NO: 2, 4 и 6. кДНК, генерированные из альтернативно подвергнутых сплайсингу мРНК, которые сохраняют свойства мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, входят в объем настоящего изобретения, так же, как и полипептиды, кодируемые указанными молекулами кДНК и мРНК. Аллельные варианты и варианты сплайсинга указанных последовательностей могут быть клонированы зондированием кДНК или геномных библиотек от различных индивидов или тканей согласно стандартным методикам, известным из области техники, и мутации в полинуклеотидах, кодирующих цистеин или остатки цистеина, могут быть внесены, как указано в настоящем описании.
Согласно способам осуществления настоящего изобретения, изолированный вариант или молекулы нуклеиновой кислоты, кодирующие мутантные IL-28 и IL-29, которые содержат замены цистеина, могут гибридизоваться в строгих условиях с молекулами нуклеиновых кислот, имеющих нуклеотидную последовательность SEQ ID NO: 18, 20, 22, 24, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160, или с молекулами нуклеиновых кислот, имеющих нуклеотидную последовательность, комплементарную SEQ ID NO: 18, 20, 22, 24, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160. В общем случае строгие условия выбирают таким образом, чтобы температура была приблизительно на 5°С меньше чем температура плавления (Tm) для конкретной последовательности при заданной ионной силе и рН. Tm представляет собой температуру (при заданной ионной силе и рН), при которой 50% целевой последовательности гибридизуется в зонд с идеальным попарным расположением оснований.
Пара молекул нуклеиновых кислот, такая как ДНК-ДНК, РНК-РНК и ДНК-РНК, может гибридизоваться, если нуклеотидные последовательности обладают некоторой степенью комплементарности. В гибридах допустимо несоответствие пар оснований в двойной спирали, но на устойчивость гибрида оказывает влияние степень ошибочного спаривания. Tm гибрида с ошибочно спаренными основаниями понижается на 1°С на каждые 1-1,5% ошибочно спаренных оснований. Варьирование строгости условий гибридизации позволяет контролировать степень ошибочного спаривания, которая получается в гибриде. Степень строгости повышается по мере увеличения температуры гибридизации и понижения ионной силы используемого при гибридизации буфера.
Специалист в данной области техники легко адаптирует указанные условия при использовании для конкретного полинуклеотидного гибрида. Значение Tm для конкретной целевой последовательности является температурой (при заданных условиях), при которой 50% целевой последовательности гибридизуется в идеально спаренную последовательность зонда. Условия, которые влияют на Tm, включают размер и содержание пар оснований в полинуклеотидном зонде, ионную силу раствора, в котором проводится гибридизация, и присутствие дестабилизирующих агентов в растворе, в котором проводится гибридизация. Из области техники известно большое количество уравнений для расчета величины Tm конкретно для ДНК, РНК и ДНК-РНК гибридов и последовательностей полинуклеотидных зондов различной длины (см., например, Sambrook et al, Molecular Cloning: A Laboratory Manual, Second Edition (Cold Spring Harbor Press 1989); Ausubel et al, (eds.), Current Protocols in Molecular Biology (John Wiley and Sons, Inc. 1987); Berger and Kimmel (eds.), Guide to Molecular Cloning Techniques, (Academic Press, Inc. 1987); and Wetmur, Сrit. Rev. Biochem. Mol. Biol. 26:227 (1990)). Программное обеспечение для секвенирования, такое как OLIGO 6.0 (LSR; Лонг-Лейк, Миннесота) и Primer Premier 4.0 (Premier Biosoft International; Пало-Альто, Калифорния), а также сайты в Интернете являются доступным инструментарием для проведения анализа конкретной последовательности и расчета значения Tm на основе заданных пользователем критериев. Подобные программы могут анализировать также последовательность в заданных условиях и идентифицировать подходящие последовательности зондов. Обычно гибридизацию более длинной полинуклеотидной последовательности, содержащей > 50 пар оснований, проводят при температуре, приблизительно на 20-25°С меньшей, чем расчетное значение Tm. Для зондов меньшего размера, содержащих < 50 пар оснований, гибридизацию обычно проводят при температуре, приблизительно на 5-10°С меньшей, чем расчетное значение Tm. Указанные условия обеспечивают максимальную скорость гибридизации ДНК-ДНК и ДНК-РНК гибридов.
После гибридизации молекулы нуклеиновых кислот можно, с целью удаления негибридизованных молекул нуклеиновых кислот, промыть в строго контролируемых условиях или в очень строго контролируемых условиях. Типичные строгие условия промывки включают промывку в растворе 0,5х - 2х SSC с 0,1% додецилсульфатом натрия (SDS) при 55-65°С. Таким образом, молекулы нуклеиновых кислот, кодирующие вариантные или мутантные полипептиды IL-28 или IL-29, содержащие замены цистеина, гибридизуются с молекулой нуклеиновой кислоты, имеющей нуклеотидную последовательность SEQ ID NO: 18, 20, 22, 24, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160, соответственно (или ее комплементом), в строгих условиях промывки, в которых строгие условия промывки составляют 0,5х - 2х SSC с 0,1% SDS при 55-65°С, в том числе 0,5х SSC с 0,1% SDS при 55°С или 2х SSC с 0,1% SDS при 65°С. Специалист легко подберет для компонентов эквивалентные условия, например, заменив SSC на SSPE в промывочном растворе.
Типичные очень строгие условия промывки включают промывку в растворе 0,1х - 0,2х SSC с 0,1% додецилсульфатом натрия (SDS) при 50-65°С. Другими словами, молекулы нуклеиновых кислот, кодирующие вариантный или мутантный полипептид IL-28 или IL-29, содержащий замены цистеина, гибридизуются с молекулой нуклеиновой кислоты, имеющей нуклеотидную последовательность SEQ ID NO: 18, 20, 22, 24, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160 (или ее комплементом), в очень строгих условиях промывки, в которых строгость условий промывки эквивалентна 0,1х - 0,2х SSC с 0,1% SDS при 50-65°С, в том числе 0,1х SSC с 0,1% SDS при 50°С или 0,2х SSC с 0,1% SDS при 65°С.
В настоящем изобретении предлагаются также изолированные полипептиды IL-28 или IL-29, у которых последовательность в значительной степени идентична полипептидам по настоящему изобретению, например, SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. Термин “значительная степень идентичности последовательности” используют в данном описании для обозначения полипептидов, последовательность которых, по крайней мере, на 80%, по крайней мере, на 90%, по крайней мере, на 91%, по крайней мере, на 92%, по крайней мере, на 93%, по крайней мере, на 94%, по крайней мере, на 95%, по крайней мере, на 96%, по крайней мере, на 97%, по крайней мере, на 98%, по крайней мере, на 99% или более чем на 99% идентична последовательностям, приведенным в SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161, или их ортологам. Настоящее изобретение включает также полипептиды, аминокислотная последовательность которых, по крайней мере, на 80%, по крайней мере, на 90%, по крайней мере, на 91%, по крайней мере, на 92%, по крайней мере, на 93%, по крайней мере, на 94%, по крайней мере, на 95%, по крайней мере, на 96%, по крайней мере, на 97%, по крайней мере, на 98%, по крайней мере, на 99% или более чем на 99% идентична полипептиду или его фрагменту по настоящему изобретению. Кроме того, настоящее изобретение включает полинуклеотиды, которые кодируют подобные полипептиды. Полипептиды IL-28 или IL-29 по настоящему изобретению предпочтительно являются рекомбинантными полипептидами. В другом аспекте, полипептиды IL-28 или IL-29 по настоящему изобретению имеют, по крайней мере, 15, по крайней мере, 30, по крайней мере, 45 или, по крайней мере, 60 последовательных аминокислот. Например, полипептид IL-28 или IL-29 по настоящему изобретению относится к полипептиду, имеющему, по крайней мере, 15, по крайней мере, 30, по крайней мере, 45 или, по крайней мере, 60 последовательных аминокислот из SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. Способы определения процента идентичности приводятся ниже.
В настоящем изобретении рассматриваются также вариантные молекулы нуклеиновой кислоты, которые могут быть идентифицированы с помощью двух критериев: определением сходства между кодируемым полипептидом и аминокислотной последовательностью SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161, соответственно, и/или гибридизационным анализом, как указано выше. Подобные варианты включают молекулы нуклеиновых кислот: (1) которые гибридизуются с молекулой нуклеиновой кислоты, имеющей нуклеотидную последовательность SEQ ID NO: 18, 20, 22, 24, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160, соответственно (или ее комплементом), в строгих условиях промывки, где строгие условия промывки составляют 0,5х - 2х SSC с 0,1% SDS при 55-65°С; или (2) которые кодируют полипептид, последовательность которого, по крайней мере, на 80%, по крайней мере, на 90%, по крайней мере, на 91%, по крайней мере, на 92%, по крайней мере, на 93%, по крайней мере, на 94%, по крайней мере, на 95%, по крайней мере, на 96%, по крайней мере, на 97%, по крайней мере, на 98%, по крайней мере, на 99% или более чем на 99% идентична аминокислотной последовательности SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. В качестве альтернативы, варианты могут быть охарактеризованы как молекулы нуклеиновых кислот: (1) которые гибридизуются с молекулой нуклеиновой кислоты, имеющей нуклеотидную последовательность SEQ ID NO: 18, 20, 22, 24, 26, 28, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158 и 160, соответственно (или ее комплементом), в очень строгих условиях промывки, где строгие условия промывки составляют 0,1х - 0,2х SSC с 0,1% SDS при 50-65°С; и (2) которые кодируют полипептид, последовательность которого, по крайней мере, на 80%, по крайней мере, на 90%, по крайней мере, на 91%, по крайней мере, на 92%, по крайней мере, на 93%, по крайней мере, на 94%, по крайней мере, на 95%, по крайней мере, на 96%, по крайней мере, на 97%, по крайней мере, на 98%, по крайней мере, на 99% или более чем на 99% идентична аминокислотной последовательности SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161, соответственно.
Процент идентичности последовательности определяют обычными способами. См., например, Altschul et al., Bull. Math. Bio. 48: 603 (1986) и Henikoff and Henikoff, Proc. Natl. Acad. Sci. USA 89: 10915 (1992). Если кратко, то сравнение первичной структуры двух аминокислотных последовательностей проводят таким образом, чтобы оптимизировать вес выравнивания, используя величину штрафа за открытие делеции, равную 10, величину штрафа за продолжение делеции, равную 1, и числовую матрицу “BLOSUM62” Henikoff and Henikoff (там же), как показано в Таблице 4 (аминокислоты обозначены стандартными однобуквенными кодами).
Общее количество идентичных совпадений
--------------------------------------------- х 100
[длина более длинной последовательности плюс
количество гэпов, введенных в более длинную
последовательность для проведения сравнения
двух последовательностей]

Для специалистов должно быть понятно, что существует множество доступных разработанных алгоритмов для сравнения первичной структуры двух аминокислотных последовательностей. Алгоритм поиска сходства “FASTA”, разработанный Pearson and Lipman, представляет собой удобный метод исследования уровня идентичности, которым обладают раскрываемая в настоящем описании аминокислотная последовательность и аминокислотная последовательность предполагаемого варианта IL-28 или IL-29. Алгоритм FASTA описан у Pearson and Lipman, Proc. Natl. Acad. Sci. USA 85: 2444 (1988) и у Pearson, Meth. Enzymol. 183: 63 (1990).
Если кратко, то FASTA в первую очередь характеризует сходство последовательности путем идентификации участков, общих для рассматриваемых последовательностей (например, SEQ ID NO: 2) и тестируемой последовательности, которая имеет либо наибольшую плотность идентичности (если значение переменной ktup равно 1), либо наибольшее количество пар идентичностей (если ktup = 2) без учета консервативных замен аминокислот, вставок или делеций. Затем регистрируются десять участков с наибольшей плотностью идентичностей путем сравнения сходства всех парных аминокислот с помощью матрицы аминокислотных замещений, и концы участков “подрезают”, чтобы включить лишь те остатки, которые вносят вклад в достижение наибольшего веса выравнивания. Если существует несколько участков с весом выравнивания, превышающим величину “отсечки” (рассчитанной по определенной формуле на основании длины последовательности и значения ktup), то подрезанные исходные участки изучают, с целью определить, могут ли участки быть объединены с получением приблизительного выравнивания с гэпом. Наконец, выравнивают участки двух аминокислотных последовательностей с наибольшим весом выравнивания, используя модификацию алгоритма Нидлмана-Вунша-Селлерса (Needleman and Wunsch, J. Mol. Biol. 48: 444 (1970); Sellers, SIAM J. Appl. Math. 26: 787 (1974)), которая учитывает вставки и делеции аминокислот. Предпочтительными параметрами для анализа в FASTA-формате являются: ktup = 1, штраф за открытие делеции = 10, штраф за продолжение делеции = 1 и матрица замещения = BLOSUM62. Указанные параметры можно ввести в программу FASTA путем модификации файла числовой матрицы (“SMATRIX”), как поясняется в Приложении 2 в Pearson, Meth. Enzymol. 183: 63 (1990).
FASTA-формат можно использовать также для определения идентичности последовательности молекул нуклеиновых кислот с помощью приведенного выше отношения. Для проведения сравнений нуклеотидных последовательностей значение ktup может составлять в интервале от одного до шести, предпочтительно, от трех до шести и, наиболее предпочтительно, равняться трем, а значения других параметров устанавливают по умолчанию.
Мутантные полипептиды IL-28 или IL-29, содержащие замены цистеина, или полипептиды с существенно сходной идентичностью последовательности характеризуются тем, что они содержат замены, делеции и добавления аминокислот. Указанные изменения преимущественно незначительны, т.е. представляют собой консервативные замены аминокислот (см. Таблицу 6) и другие замены, которые не оказывают значительного воздействия на укладку или активность полипептида; небольшие делеции, обычно от одной до приблизительно 30 аминокислот; и аминоконцевые или карбоксиконцевые удлиняющие сегменты, такие как аминоконцевые остатки метионина, небольшие линкерные пептиды, содержащие вплоть до приблизительно 20-25 остатков, или аффинная метка. Таким образом, настоящее изобретение включает полипептиды, содержащие от приблизительно 146 до 207 аминокислотных остатков, которые образуют последовательность, по крайней мере, на 80%, по крайней мере, на 90%, по крайней мере, на 91%, по крайней мере, на 92%, по крайней мере, на 93%, по крайней мере, на 94%, по крайней мере, на 95%, по крайней мере, на 96%, по крайней мере, на 97%, по крайней мере, на 98%, по крайней мере, на 99% или более чем на 99% идентичную соответствующей области последовательности SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. Полипептид, включающий аффинную метку, может, кроме того, содержать сайт протеолитического расщепления между полипептидом IL-28 или IL-29 и аффинной меткой. Указанные сайты предпочтительно включают сайты расщепления тромбина и сайты расщепления фактора Ха.
Консервативные аминокислотные замены
Можно провести определение аминокислотных остатков, образующие области и домены, которые являются критичными для поддержания структурной целостности. В пределах указанных областей можно установить специфические остатки, которые более или менее устойчивы к изменениям и поддерживают общую третичную структуру молекулы. Методы анализа структуры последовательности включают, но этим не ограничиваясь, сравнение первичной структуры множества последовательностей с высокой степенью аминокислотной или нуклеотидной идентичности, вторичные структурные предпочтения, бинарные структуры, комплементарную упаковку и скрытые полярные взаимодействия (Barton, Current Opin. Struct. Biol. 5: 372-376, 1995 и Cordes et al., Current Opin. Struct. Biol. 6: 3-10, 1996). В общем случае, при разработке модификаций в молекулах или при идентификации конкретных фрагментов определение структуры сопровождается оценкой активности модифицированных молекул.
Изменения в аминокислотной последовательности в мутантных полипептидах IL-28 или IL-29, содержащих замены цистеина, проводят таким образом, чтобы минимизировать разрушение структуры высшего порядка, которая важна для проявления биологической активности. Например, в том случае, когда мутантный полипептид IL-28 или IL-29, содержащий замены цистеина, имеет одну или несколько спиралей, то изменения в аминокислотных остатках осуществляют таким образом, чтобы не разрушить геометрию спиралей и других компонентов молекулы, где изменения в конформации ослабляют некоторые критические функции, например, связывание молекул со своими партнерами по связыванию. Влияние изменений аминокислотной последовательности могут быть предсказаны, например, с помощью компьютерного моделирования, как описано выше, или определены анализом кристаллической структуры (см., например, Lapthorn et al., Nat. Struct. Biol. 2: 266-268, 1995). Другие методы, хорошо известные из области техники, сравнивают складчатую структуру вариантного белка со стандартной молекулой (например, молекулой нативного белка). Например, можно провести сравнение конфигурации цистеина в варианте и стандартной молекуле. Масс-спектрометрия и химическая модификация с использованием восстановления или алкилирования обеспечивает способы определения остатков цистеина, которые связаны с образованием дисульфидных связей или же не участвуют в образовании подобных связей (Bean et al., Anal. Biochem. 201: 216-226, 1992; Gray, Protein Sci. 2: 1732-1748, 1993; и Patterson et al., Anal. Chem. 66: 3727-3732, 1994). Обычно считают, что если модифицированная молекула не имеет той же конфигурации цистеина, что и стандартная молекула, то складчатая структура пострадает. Другим хорошо известным и признанным способом установления складчатой структуры является круговой дихроизм (CD). Измерение и сравнение спектров CD, генерируемых модифицированной молекулой и стандартной молекулой, является рутинной процедурой (Johnson, Proteins 7: 205-214, 1990). Другим хорошо известным методом анализа укладки и структуры является кристаллография. Известные методы анализа складчатой структуры и структурного сходства между белками и полипептидами являются ядерный магнитный резонанс (NMR, ЯМР), ферментативное картирование пептидов и картирование эпитопов (Schaanan et al., Science 257: 961-964, 1992).
Можно генерировать профиль гидрофильности Хоппа/Вудса для последовательности мутантного белка IL-28 или IL-29, содержащего замены цистеина, которая приведена в SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161 (Hopp et al., Proc. Natl. Acad. Sci. USA 78: 3824-3828, 1981; Hopp, J. Immunol. Meth. 88: 1-18, 1986 и Triquier et al., Protein Engineering 11: 153-169, 1998). Установление профиля основывается на скольжении по окну из шести остатков. Скрытые остатки G, S и Т и открытые остатки Н, Y и W игнорируются. Для специалистов должно быть понятно, что при разработке модификаций аминокислотной последовательности мутантного полипептида IL-28 или IL-29, содержащего замены цистеина, принимают во внимание гидрофобность или гидрофильность, с тем чтобы не нарушить общую структуру и биологический профиль. Особый интерес для замены представляют гидрофобные остатки, выбранные из группы, включающей Val, Leu или Ile, или группы, включающей Met, Gly, Ser, Ala, Tyr и Trp.
Идентичность незаменимых аминокислот также можно установить путем анализа сходства последовательности между IFN-α и членами семейства IL-28A, IL-28B и IL-29 (как указано в Таблицах 1 и 2). Используя такие методы, как приведенный ранее анализ в формате “FASTA”, в семействе белков идентифицируют области, обладающие высокой степенью сходства, и используют их для анализа аминокислотной последовательности консервативных областей. Альтернативным подходом к идентификации вариантного полинуклеотида, который основывается на структуре, является выявление способности молекулы нуклеиновой кислоты, кодирующей потенциальный вариантный ген IL-28 или IL-29, гибридизоваться с молекулой нуклеиновой кислоты, как указано выше.
Другими способами идентификации незаменимых аминокислот в полипептидах по настоящему изобретению являются такие известные из области техники методики как сайт-направленный мутагенез или мутагенное сканирование аланином (Cunningham and Wells, Science 244: 1081 (1989), Bass et al., Proc. Natl. Acad. Sci. USA 88: 4498 (1991), Coombs and Corey, “Site-Directed Mutagenesis and Protein Engineering”, в Proteins: Analysis and Design, Angeletti (ed.), pages 259-311 (Academic Press, Inc. 1998)). В последнем методе одиночные мутации аланина вводят в каждый остаток в молекуле и полученные в результате мутантные молекулы, содержащие замены цистеина, тестируют на биологическую и биохимическую активность, как указано ниже, с целью идентифицировать аминокислотные остатки, которые являются критическими для активности молекулы. См. также Hilton et al., J. Biol. Chem. 271: 4699 (1996).
Настоящее изобретение включает также функциональные фрагменты мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, и молекулы нуклеиновых кислот, которые кодируют подобные функциональные фрагменты. “Функциональный” мутантный IL-28 или IL-29, содержащий замены цистеина, или его фрагмент, определяемый в настоящем описании, отличается своей пролиферативной и дифференцирующей активностью, своей способностью активировать или подавлять специализированные функции клетки или своей способностью специфично связываться с антителом против IL-28 или IL-29 или с рецептором IL-28 (как растворимым, так и иммобилизованным). Специализированные активности мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, и их испытания рассматриваются ниже. Как указано выше, полипептиды IL-28 или IL-29 характеризуются наличием укладки из шести спиралей. Таким образом, в настоящем изобретении далее предлагаются слитые белки, включающие: (а) молекулы полипептидов, содержащие одну или несколько из указанных выше спиралей; и (b) функциональные фрагменты, содержащие одну или несколько из указанных спиралей. Другой полипептидной частью слитого белка может являться другой цитокин с уложенными спиралями или интерферон, такой как IFN-α, или же не нативный и/или не родственный секреторный сигнальный пептид, который облегчает секрецию слитого белка.
Мутантные полипептиды IL-28 или IL-29, содержащие замены цистеина, по настоящему изобретению, включая полноразмерные полипептиды, биологически активные фрагменты и слитые полипептиды, могут быть получены обычными способами с помощью клеток, в которые был введен вектор экспрессии, кодирующий полипептид. По тексту настоящего описания термин “клетки, в которые был введен вектор экспрессии”, включает как клетки, над которыми провели непосредственные манипуляции, с целью введения экзогенных молекул ДНК, так и их потомство, которое содержит введенные ДНК. Подходящими клетками-хозяевами являются такие типы клеток, которые могут быть трансформированы или трансфицированы экзогенными ДНК и выращены в питательной среде, и они включают бактерии, клетки грибов и культивированные клетки высших эукариот. Методики манипулирования с клонированными молекулами ДНК и методики введения экзогенных ДНК в различные клетки-хозяева приводятся у Sambrook et al., Molecular Cloning. A Laboratory Manual, 2nd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, 1989 и Ausubel et al., eds., Current Protocols in Molecular Biology, John Wiley and Sons, Inc., NY, 1987.
В соответствии с другим аспектом, настоящее изобретение предоставляет экспрессирующий вектор, который включает следующие операбельно связанные элементы: промотор транскрипции; сегмент ДНК, кодирующий рассматриваемый в настоящем описании полипептид; и терминатор транскрипции.
Настоящее изобретение предоставляет также экспрессирующий вектор, который содержит изолированную и очищенную молекулу ДНК, включая следующие операбельно связанные элементы: промотор транскрипции; сегмент ДНК, кодирующий полипептид, последовательность которого, по крайней мере, на 90% или 95% идентична полипептиду, выбранному из группы, включающей SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161; и терминатор транскрипции. Молекула ДНК может также включать секреторную сигнальную последовательность, операбельно связанную с сегментом ДНК. Кодируемый белок может также содержать аффинную метку, как указывается в настоящем описании. Настоящее изобретение предоставляет также выращенную клетку, содержащую вышеуказанный вектор экспрессии. Кодируемый полипептид необязательно может содержать, по меньшей мере, 15, по меньшей мере, 30, по меньшей мере, 45 или, по меньшей мере, 60 последовательных аминокислот из аминокислотной последовательности, приведенной в SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. Кодируемый белок необязательно может обладать антивирусной активность, в частности, против гепатита В и гепатита С.
В соответствии с другим аспектом, настоящее изобретение предоставляет культивируемую клетку, содержащую раскрытый выше экспрессирующий вектор.
В соответствии с другим аспектом, настоящее изобретение предоставляет способ получения белка, который включает: выращивание указанной выше клетки в условиях, в которых экспрессируется сегмент ДНК; и выделение белка, кодируемого сегментом ДНК.
В общем случае, последовательность ДНК, кодирующая мутантный полипептид IL-28 или IL-29, содержащий замены цистеина, операбельно связывается в экспрессирующем векторе с другими генетическими элементами, необходимыми для его экспрессии, которые обычно включают промотор и терминатор транскрипции. Вектор обычно содержит также один или несколько селектируемых маркеров и одну или несколько точек начала репликации, хотя для специалиста должно быть понятно, что в некоторых системах селектируемые маркеры могут предоставляться отдельными векторами, а репликация экзогенной ДНК достигается интегрированием в геном клетки-хозяина. Выбор промоторов, терминаторов, селектируемых маркеров, векторов и других элементов представляет собой обычный этап разработки и легко может быть осуществлена специалистом в данной области. Многие подобные элементы описаны в литературе и доступны из коммерческих источников.
Чтобы направить мутантные полипептиды IL-28 или IL-29, содержащие замены цистеина, по секреторному пути клетки-хозяина, в экспрессирующий вектор вводят секреторную сигнальную последовательность (известную также как лидерная последовательность, препропоследовательность или препоследовательность). Секреторная сигнальная последовательность может быть из мутантного IL-28 или IL-29, содержащего замены цистеина, например, SEQ ID NO: 119 или 121, или же может быть получена из другого секретируемого белка (в частности, t-PA; см. патент США № 5641655) или синтезирована de novo. Секреторная сигнальная последовательность операбельно присоединяется к последовательности ДНК мутантного IL-28 или IL-29, содержащего замены цистеина, т.е. две последовательности соединяются в корректной рамке считывания и размещаются таким образом, чтобы направить вновь синтезированный полипептид по секреторному пути клетки-хозяина. Секреторные сигнальные последовательности обычно размещаются у 5' конца последовательности ДНК, кодирующей представляющей интерес полипептид, хотя некоторые сигнальные последовательности могут располагаться в других местах представляющей интерес последовательности ДНК (см., в частности, Welch et al., патент США № 5037743; Holland et al., патент США № 5143830).
Разнообразные подходящие рекомбинантные клетки-хозяева включают, но этим не ограничиваясь, грамотрицательные прокариотные организмы-хозяева. Подходящие штаммы E. coli включают W3110, полученные из К12 штаммы ММ294, TG-1, JM-107, BL-21 и UT5600. другие подходящие штаммы включают BL21(DE3), BL21(DE3)pLysS, BL21(DE3)pLysE, DH1, DH4I, DH5, DH5I, DH5IF', DH5IMCR, DH10B, DH10B/p3, DH11S, C600, HB101, JM101, JM105, JM109, JM110, K38, RR1, Y1088, Y1089, CSH18, ER1451, ER1647, E. coli K12, E. coli K12 RV308, E. coli K12 C600, E. coli HB101, E. coli K12 C600 R.sub.k-M.sub.k-, E. coli K12 RR1 (см., например, Brown (ed.), Molecular Biology Labfax (Academic Press 1991)). Другие грамотрицательные прокариотные хозяева могут включать Serratia, Pseudomonas, Caulobacter. Прокариотные хозяева могут включать грамположительные организмы, такие как Bacillus, например, B. subtilis и B. thuringienesis, и B. thuringienesis var. israelensis, а также Streptomyces, например, S. lividans, S. ambofaciens, S. fradiae и S. griseofuscus. Подходящие штаммы Bacillus subtilus включают BR151, YB886, MI119, MI120 и В170 (см., например, Hardy, “Bacillus Cloning Methods”, в DNA Cloning: A Practical Approach, Glover (ed.) (IRL Press 1985)). Стандартные методики размножения векторов в прокариотных хозяевах хорошо известны специалистам (см., например, Ausubel et al. (eds.), Short Protocols in Molecular Biology, 3 rd Edition (John Wiley & Sons 1995); Wu et al., Methods in Gene Biotechnology (CRC Press, Inc. 1997)). В одном из вариантов осуществления настоящего изобретения способы по изобретению используют мутантные IL-28 или IL-29, содержащие замены цистеина, которые способны экспрессироваться в штамме W3110, депонированном в Американской коллекции типовых культур (АТСС) под номером ATCC # 27325.
Если необходимо масштабное получение мутантных IL-28 или IL-29, содержащих замены цистеина, с использованием экспрессирующей системы по настоящему изобретению, то может использоваться циклическая ферментация. В общих чертах, циклическая ферментация заключается в том, что на первой стадии готовят колбу для посева путем выращивания штаммов E. coli, экспрессирующих мутантный IL-28 или IL-29, содержащий замены цистеина, на подходящей питательной среде при встряхивании до достижения оптической плотности (OD) в интервале от 5 до 20 при 600 нм. Подходящая питательная среда должна содержать азот из таких источников как сульфат аммония, фосфат аммония, хлорид аммония, дрожжевой экстракт, гидролизат животных белков, гидролизат растительных белков или гидролизованный казеин. Фосфаты поставляются из фосфата калия, фосфата аммония, фосфорной кислоты или фосфата натрия. Другими компонентами являются хлорид магния или сульфат магния, сульфат двухвалентного железа или хлорид двухвалентного железа и следовые количества других элементов. Для улучшения роста среду для роста дополняют углеводами, такими как фруктоза, глюкоза, галактоза, лактоза или глицерин. В качестве альтернативы, для получения высокого выхода мутантного белка IL-28 или IL-29, содержащего замены цистеина, применяют способ циклического культивирования с подпиткой. Штаммы E. coli, продуцирующие мутантные IL-28 или IL-29, которые содержат замены цистеина, выращивают в условиях, аналогичных тем, которые описаны для сосуда, используемого на первой стадии для приготовления посевного материала при циклической ферментации.
После ферментации клетки отделяют центрифугированием, ресуспендируют в гомогенизирующем буфере и гомогенизуют, например, в гомогенизаторе APV-Gaulin (Invensys APV, Тонаванда, Нью-Йорк) или в другом устройстве для разрушения клеток, таком как шаровые мельницы или ультразвуковые дезинтеграторы. В качестве альтернативы клетки сразу же извлекают из ферментатора и гомогенизуют в гомогенизаторе APV-Gaulin. Промытый препарат из внутриклеточных телец включения солюбилизуют раствором гидрохлорида гуанидина (5-8 М) или мочевины (7-8 М), содержащего восстановитель, такой как бета-меркаптоэтанол (10-100 мМ) или дитиотреитол (5-50 мМ). Растворы могут быть приготовлены в Трис, фосфате, HEPES или других подходящих буферирующих веществах. Тельца включения можно также солюбилизовать раствором мочевины (2-4 М), содержащим лаурилсульфат натрия (0,1-2%). В процессе выделения очищенного мутантного IL-28 или IL-29, содержащего замены цистеина, из трансформированного штамма-хозяина E. coli, в котором мутантный IL-28 или IL-29, содержащий замены цистеина, накапливается в виде рефрактильных телец включения, клетки разрушают и тельца включения отделяют центрифугированием. Затем тельца включения солюбилизуют и денатурируют в 6 М растворе хлорида гуанидина, содержащего восстановитель. Восстановленный мутантный IL-28 или IL-29, содержащий замены цистеина, затем окисляют в процессе осуществления контролируемой стадии ренатурации. После восстановления укладки мутантный IL-28 или IL-29, содержащий замены цистеина, можно пропустить через фильтр, с целью осветления и отделения нерастворимых белков. Раствор затем фильтруют, с целью осветления и отделения нерастворимых белков. После того, как восстанавливают укладку мутантного IL-28 или IL-29, содержащего замены цистеина, и осуществляют концентрирование, мутантные белки IL-28 или IL-29, содержащие замены цистеина, с восстановленной складчатой структурой поглощают разбавленным буфером на катионообменной колонке и очищают методом хроматографии с гидрофобными взаимодействиями.
Согласно настоящему изобретению, подходящими хозяевами являются культивируемые клетки млекопитающих. Способы введения экзогенной ДНК в клетки-хозяева млекопитающих включают опосредованную фосфатом кальция трансфекцию (Wigler et al., Cell 14: 725, 1978; Corsaro and Pearson, Somatic Cell Genetics 7: 603, 1981; Graham and Van der Eb, Virology 52: 456, 1973), электропорацию (Neumann et al., EMBO J. 1: 841-5, 1982), трансфекцию с помощью DEAE-декстрана (Ausubel et al., там же), опосредованную липосомами трансфекцию (Hawley-Nelson et al., Focus 15: 73, 1993; Ciccarone et al., Focus 15: 80, 1993) и вирусные векторы (Miller and Rosman, BioTechniques 7: 980-90, 1989; Wang and Finer, Nature Med. 2: 714-6, 1996). Продукция рекомбинантных полипептидов в культивируемых клетках млекопитающих раскрывается, например, в Levinson et al., патент США № 4713339; Hagen et al., патент США № 4784950; Palmiter et al., патент США № 4579821; и Ringold, патент США № 4656134. Подходящие культивируемые клетки млекопитающих включают COS-1 (ATCC № CRL 1650), COS-7 (ATCC № CRL 1651), BHK (ATCC № CRL 1632), BHK 570 (ATCC № CRL 10314), 293 (ATCC № CRL 1573; Graham et al., J. Gen. Virol. 36: 59-72, 1977) и клеточную линию яичников китайского хомячка (в частности, СНО-К1; ATCC № CСL 61). Дополнительные клеточные линии известны из области техники и доступны из общедоступных депозитариев, таких как Американская коллекция типовых культур, Манассас, Виргиния. В общем случае предпочтительны сильные промоторы транскрипции, такие как промоторы из SV-40 или вируса цитомегалии. См., например, патент США № 4956288. Другие подходящие промоторы включают промоторы из генов металлотионеина (патенты США № 4579821 и 4601978) и аденовирусный главный поздний промотор.
Для отбора культивируемых клеток млекопитающих, в которые вставлена чужеродная ДНК, обычно используют селекцию с помощью лекарств. Подобные клетки обычно называют “трансфектантами”. Клетки, которые выращены в присутствии селективного агента и способны передавать представляющий интерес ген своему потомству, называют “стабильными трансфектантами”. Предпочтительным селектируемым маркером является ген, кодирующий устойчивость к антибиотику неомицину. Селекцию проводят в присутствии лекарства неомицинового типа, такого как G-418 или подобное лекарство. Системы селекции могут также использоваться для повышения уровня экспрессии представляющего интерес гена, и этот процесс называют “амплификацией”. Амплификацию проводят, выращивая трансфектанты в присутствии низкого уровня селективного агента, а затем повышая количество селективного агента, с целью селекции клеток, которые продуцируют высокие уровни продуктов введенного гена. Предпочтительным амплифицируемым селектируемым маркером является дигидрофолатредуктаза, которая придает устойчивость к метотрексату. Могут применяться другие устойчивые к лекарствам гены (в частности, придающие устойчивость к гидромицину, придающие множественную лекарственную устойчивость, пуромицинацетилтрансфераза). В качестве альтернативы, маркерам, которые вводят измененный фенотип, таким как зеленый флуоресцентный белок или белки клеточной поверхности, такие как CD4, CD8, MHC класса I, плацентарная щелочная фосфатаза, для фракционного разделения трансфицированных клеток от нетрансфицированных клеток, могут применяться такие методы, как FACS-сортинг или технология разделения с использованием магнитных бусинок.
В качестве хозяев могут также использоваться другие клетки высших эукариот, включая клетки растений, клетки насекомых и клетки птиц. Обзор использования Agrobacterium rhizogenes в качестве вектора приводится в Sinkar et al., J. Biosci. (Bangalore) 11: 47-58, 1987. Трансформация клеток насекомых и продукция в них чужеродных полипептидов описывается в Guarino et al., патент США № 5162222 и публикация WIPO WO 94/06463. Клетки насекомых можно инфицировать рекомбинантным бакуловирусом, обычно получаемым из Autographa californica nuclear polyhedrosis virus (AcNPV). См. King, L.A. and Possee, R.D., The Baculovirus Expression System: A Laboratory Guide, London, Chapman & Hall; O'Reilly, D.R. et al, Baculovirus Expression Vectors: A Laboratory Manual, New York, Oxford University Press., 1994; and, Richardson, C. D., Ed., Baculovirus Expression Protocols. Methods in Molecular Biology, Totowa, NJ, Humana Press, 1995. Во втором способе получения рекомбинантного бакуловируса используют систему на основе транспозона, описанную у Luckow (Luckow, V.A. et al., J. Virol. 67: 4566-79, 1993). Указанная система продается в виде набора реагентов Bac-to-Bac (Life Technologies, Рокквиль. Мэриленд). В указанной системе используют вектор переноса, pFastBac1™ (Life Technologies), включающий транспозон Tn7 для перемещения ДНК, кодирующей мутантный полипептид IL-28 или IL-29, который содержит замены цистеина, в геном бакуловируса, поддерживаемый в E. coli в виде большой плазмиды, получившей название “бакмида”. Вектор переноса pFastBac1™ использует полиэдриновый промотор AcNPV для активации экспрессии представляющего интерес гена, в данном случае мутантного IL-28 или IL-29, содержащего замены цистеина. Однако pFastBac1™ может быть существенно модифицирован. Полиэдриновый промотор можно удалить и заменить промотором основного белка бакуловируса (известного также как промотор Pcor, p6.9 или МР), который раньше экспрессировался при бакуловирусной инфекции и было показано, что он удобен для экспрессии секретируемых протеинов. См. Hill-Perkins, M.S. and Posse, R.D., J. Gen. Virol. 71: 971-6, 1990; Bonning, B.C. et al., J. Gen. Virol. 75: 1551-6, 1994; и Chazenbalk, G.D. and Rapoport, B., J. Biol. Chem. 270: 1543-9, 1995. В подобных генных конструкциях вектора переноса можно использовать длинную или короткую версию основного белка промотора. Более того, могут быть сконструированы векторы переноса, которые замещают секреторную сигнальную последовательность нативного IL-28 или IL-29 секреторной сигнальной последовательностью, полученной из белков насекомых. Например, секреторная сигнальная последовательность, полученная из экдистероид-глюкозилтрансферазы (EGT), мелиттина пчелы (Invitrogen, Карлсбад, Калифорния) или бакуловируса gp67 (PharMingen, Сан-Диего, Калифорния), могут применяться в генных конструкциях, с целью замены секреторной сигнальной последовательности нативного IL-28 или IL-29. Кроме того, векторы переноса могут включать слияние в рамке с ДНК, кодирующей эпитопную метку у С- или N-конца экспрессируемого мутантного полипептида IL-28 или IL-29, содержащего замены цистеина, например, эпитопную метку Glu-Glu (Grussenmeyer, T. et al., Proc. Natl. Acad. Sci. USA 82: 7952-4, 1985). С помощью известных из техники методов вектор переноса, включающий мутантный IL-28 или IL-29, который содержит замены цистеина, трансформируют в E. coli и проводят скрининг по бакмидам, которые содержат прерванный ген lacZ, указывающий на рекомбинантный бакуловирус. Используя известные методы, выделяют ДНК бакмиды, содержащую геном рекомбинантного бакуловируса, и используют для трансфекции клеток Spodoptera frugiperda, в частности, клеток Sf9. Затем продуцируют рекомбинантный вирус, который экспрессирует мутантный IL-28 или IL-29, содержащий замены цистеина. Запасы рекомбинантного вируса готовят, используя методы, известные из области техники.
Рекомбинантный вирус используют для инфицирования клеток-хозяев, как правило, клеток, полученных из ратных червей, Spodoptera frugiperda. Общие сведения см. Glick and Pasternak, Molecular Biotechnology: Principles and Applications of Recombinant DNA, ASM Press, Washington, D.C., 1994. Другой подходящей клеточной линией является клеточная линия High FiveO™ (Invitrogen), полученная из Trichoplusia ni (патент США № 5300435).
Согласно настоящему изобретению, могут также использоваться клетки грибов, включая дрожжевые клетки. В этом отношении представляющие наибольший интерес виды дрожжей включают Saccharomyces cerevisiae, Pichia pastoris и Pichia methanolica. Методы трансформирования клеток S. cerevisiae с помощью экзогенной ДНК и продуцирования из них рекомбинантных полипептидов раскрываются, например, в Kawasaki, патент США № 4599311; Kawasaki et al., патент США № 4931373; Brake, патент США № 4870008; Welch et al., патент США № 5037743; и Murray et al., патент США № 4845075. Трансформированные клетки отбирают по фенотипу, определяемому селектируемым маркером, обычно по устойчивости к лекарству или по способности расти в отсутствие конкретного нутриента (в частности, лейцина). Предпочтительной векторной системой для использования в Saccharomyces cerevisiae, является векторная система РОТ1, раскрытая Kawasaki et al. (патент США № 4931373), которая позволяет отобрать трансформированные клетки по росту в содержащих глюкозу питательных средах. Подходящие промоторы или терминаторы для использования с дрожжами включают промоторы и терминаторы из генов гликолитических ферментов (см., например, Kawasaki, патент США № 4599311; Kingsman et al., патент США № 4615974; и Bitter, патент США № 4977092) и из генов алкогольдегидрогеназы. См. также патенты США № 4990446, 5063154, 5139936 и 4661454. Из области техники известны системы трансформации для других дрожжей, включая Hansenula polymorpha, Schizosaccharomyces pombe, Kluyveromyces lactis, Kluyveromyces fragilis, Ustilago maydis, Pichia pastoris, Pichia methanolica, Pichia guillermondii и Candida maltosa. См., например, Gleeson et al., J.Gen. Microbiol. 132: 3459-65, 1986 и Cregg, патент США № 4882279. Согласно способам, изложенным McKnight et al., патент США № 4935349, могут использоваться клетки Aspergillus. Способы трансформирования Acremonium chrysogenum раскрывают Sumino et al., патент США № 5162228. Способы трансформирования Neurospora раскрывают Lambowitz, патент США № 4486533. Использование Pichia methanolica в качестве хозяина для продуцирования рекомбинантных белков раскрывается в патентах США № 5955349, 5888768 и 6001597 и патентах США № 5965389, 5736383 и 5854039.
Полипептиды и белки по настоящему изобретению предпочтительно очищают до степени чистоты ≥ 80%, более предпочтительно, до степени чистоты ≥ 90%, еще более предпочтительно, до степени чистоты ≥ 95%, и наиболее предпочтительно до фармацевтической чистоты, которая составляет более 99,9% по отношению к примесным макромолекулам, в частности, другим белкам и нуклеиновым кислотам, и они не содержат инфекционных и пирогенных агентов. Очищенный полипептид или белок преимущественно практически свободен от других полипептидов или белков, в частности полипептидов или белков животного происхождения.
Экспрессируемые рекомбинантные мутантные белки IL-28 или IL-29, содержащие замены цистеина (включая химерные полипептиды или мультимерные белки), очищают с помощью обычных способов, применяемых для очистки белков, как правило, с помощью комбинации хроматографических методов. Общие сведения см. Affinity Chromatography: Principles & Methods, Pharmacia LKB Biotechnology, Uppsala, Sweden, 1988; и Scopes, Protein Purification: Principles and Practice, Springer-Verlag, New York, 1994. Белки, содержащие полигистидиновую аффинную метку (обычно приблизительно 6 остатков гистидина), очищают аффинной хроматографией на полимере, содержащем хелаты никеля. См., например, Houchuli et al., Bio/Technol. 6: 1321-1325, 1988. Белки, содержащие метку glu-glu, могут быть очищены обычными образом с помощью иммуноаффинной хроматографии. См., например, Grussenmeyer et al., выше. Слитые белки, содержащие мальтозу, очищают на колонке с амилозой в соответствии с известными из области техники методами.
Мутантные полипептиды IL-28 или IL-29, содержащие замены цистеина, могут быть также получены химическим синтезом, известными из области техники методами, включая твердофазный синтез, частично твердофазные методы, конденсацию фрагментов или классический синтез в растворе. См., например, Merrifield, J. Am. Chem. Soc. 85: 2149, 1963; Stewart et al., Solid Phase Peptide Synthesis (2nd edition), Pierce Chemical Co., Rockford, IL, 1984; Bayer and Rapp, Chem. Pept. Prot. 3: 3, 1986; и Atherton et al., Solid Phase Peptide Synthesis: A Practical Approach, IRL Press, Oxford, 1989. Для получения небольших полипептидов особенно удобен метод in vitro синтеза.
С помощью известных из области техники методов мутантные белки IL-28 или IL-29, содержащие замены цистеина, можно получить в виде мономеров или мультимеров; в гликозилированном или негликозилированном виде; в пегилированном или непегилированом виде; в виде слитых белков; или же они могут включать или не включать концевой метионин в качестве остатка аминокислоты. Используемые в терапии конъюгаты мутантного IL-28 или IL-29, содержащего замены цистеина, могут включать фрагменты фармацевтически приемлемых водорастворимых полимеров. Было показано, что конъюгация интерферонов с водорастворимыми полимерами увеличивает полупериод циркуляции интерферона и снижает иммуногенность полипептида (см., например, Nieforth et al., Clin. Pharmacol. Ther. 59: 636 (1996) и Monkarsh et al., Anal. Biochem. 247: 434 (1997)).
Подходящие водорастворимые полимеры включают полиэтиленгликоль (PEG), монометокси-PEG, моно-(С1-С10)алкокси-PEG, арилокси-PEG, поли-(N-винилпирролидон)PEG, трезил-монометокси PEG, монометокси-PEG/пропионовый альдегид, PEG/пропионовый альдегид, PEG/бис-сукцинимидилкарбонат, гомополимеры пропиленгликоля, сополимер пропиленоксида/этиленоксида, полиоксиэтилированные полиолы (в частности, глицерин), монометокси-PEG/масляный альдегид, PEG/масляный альдегид, монометокси-PEG/ацетальдегид, PEG/ацетальдегид, метоксил PEG/сукцинимидилпропионат, метоксил PEG/сукцинимидилбутаноат, поливиниловый спирт, декстран, целлюлозу или другие полимеры на основе углеводов. Подходящие PEG могут иметь молекулярную массу от приблизительно 600 до приблизительно 60000, в том числе, например, 5000 дальтон, 12000 дальтон, 20000 дальтон, 30000 дальтон и 40000 дальтон, и могут быть линейными или разветвленными. Конъюгаты мутантного IL-28 или IL-29, содержащего замены цистеина, могут содержать смесь подобных водорастворимых полимеров.
Один пример конъюгата мутантного IL-28 или IL-29, содержащего замены цистеина, включает фрагмент мутантного IL-28 или IL-29, содержащего замены цистеина, и фрагмент полиалкилоксида, присоединенный к N-концу фрагмента мутантного IL-28 или IL-29, содержащего замены цистеина. Одним из подходящих полиалкилоксидов является PEG. В качестве иллюстрации мутантный IL-28 или IL-29, содержащий замены цистеина, может быть модифицирован с помощью PEG, и этот процесс называют “пегилированием”. Пегилирование мутантного IL-28 или IL-29, содержащего замены цистеина, может быть проведено с помощью любой из известных из области техники реакций пегилирования (см., например, ЕР 0154316, Delgado et al., Critical Reviews in Therapeutic Drug Carrier Systems 9: 249 (1992), Duncan and Spreafico, Clin. Pharmacokinet. 27: 290 (1994), и Francis et al., Int. J. Hematol. 68: 1 (1998)). Например, пегилирование можно осуществить по реакции ацилирования или по реакции алкилирования с реакционно-способной молекулой полиэтиленгликоля. В альтернативном подходе конъюгаты мутантного IL-28 или IL-29, содержащего замены цистеина, получают конденсацией активированного PEG, при которой концевая гидроксильная группа или аминогруппа в PEG заменена активированным линкером (см., например, Karasiewicz et al., патент США № 5382657).
Пегилирование путем ацилирования требует проведения реакции активного сложноэфирного производного PEG c мутантным полипептидом IL-28 или IL-29, содержащим замены цистеина. Примером активированного сложного эфира PEG является PEG, этерифицированный N-гидроксисукцинимидом. В настоящем описании термин “ацилирование” включает следующие типы связывания мутантного IL-28 или IL-29, содержащего замены цистеина, с водорастворимым полимером: амид, карбамат, уретан и т.п. Способы пегилированного мутантного IL-28 или IL-29, содержащего замены цистеина, путем ацилирования обычно включают стадии (а) взаимодействия мутантного полипептида IL-28 или IL-29, содержащего замены цистеина, с PEG (таким как реакционно-способный сложный эфир альдегидного производного PEG) в условиях, при которых одна или несколько групп PEG присоединяются к мутантному IL-28 или IL-29, содержащему замены цистеина, и (b) выделение продукта(ов) реакции. В общем случае оптимальные условия проведения реакции ацилирования определяют исходя из известных параметров и желаемых результатов. Например, чем больше отношение PEG : мутантный IL-28 или IL-29, содержащий замены цистеина, тем больше процент продукта пегилирования мутантного IL-28 или IL-29, содержащего замены цистеина.
Пегилирование путем алкилирования обычно включает взаимодействие концевого альдегидного производного PEG, полученного, в частности, из пропионового альдегида, масляного альдегида, ацетальдегида и т.п., с мутантным IL-28 или IL-29, содержащим замены цистеина, в присутствии восстановителя. Группы PEG предпочтительно присоединяются к полипептиду посредством группы -CH2-NH2.
Получение производных путем восстановительного алкилирования, с целью получения монопегилированного продукта, имеет то преимущество, что в этом случае можно использовать разницу в реакционно-способности различных типов первичных аминогрупп, доступных для дериватизации. Как правило, реакцию проводят при значении рН, которое позволяет использовать преимущества в разнице величин рКа между ε-аминогруппами остатков лизина и α-аминогруппой N-концевого остатка белка. Путем подобного селективного образования производных осуществляют контроль над присоединением к белку водорастворимого полимера, содержащего реакционно-способную группу, такую как альдегидная группа. Конъюгация с полимером проводится преимущественно по N-концу белка без существенной модификации других реакционно-способных групп, таких как аминогруппы в боковой цепи лизина.
Восстановительное алкилирование, с целью получения практически гомогенной популяции монополимерных молекул конъюгата мутантного IL-28 или IL-29, содержащего замены цистеина, может включать следующие стадии: (а) взаимодействие мутантного полипептида IL-28 или IL-29, содержащего замены цистеина, с реакционноспособным PEG в условиях восстановительного алкилирования при величине рН, которая позволяет осуществить селективную модификацию α-аминогруппы у аминового конца мутантного IL-28 или IL-29, содержащего замены цистеина, и (b) выделение продукта(ов) реакции. Восстановитель, который применяют при проведении восстановительного алкилирования, должен быть устойчив в водном растворе и предпочтительно должен быть способен восстанавливать только основание Шиффа, образующееся на ранней стадии восстановительного алкилирования. Предпочтительные восстановители включают боргидрид натрия, цианборгидрид натрия, диметиламинборан, триметиламинборан и комплекс пиридина с бораном.
С целью получения практически гомогенной популяции монополимерных конъюгатов мутантного IL-28 или IL-29, содержащего замены цистеина, условия проведения восстановительного алкилирования должны быть такими, чтобы они позволяли осуществить селективное присоединение фрагмента водорастворимого полимера к N-концу мутантного IL-28 или IL-29, содержащего замены цистеина. Подобные условия проведения реакции обычно обеспечивают разницу в величинах рКа между аминогруппами лизина и α-аминогруппы у N-конца. Значение рН оказывает влияние также на отношение используемого полимера и белка. В общем случае, если значение рН низкое, то желателен больший избыток полимера по отношению к белку, поскольку чем меньше реакционная способность N-концевой α-группы, тем больше полимера требуется для создания оптимальных условий. Если значение рН выше, то отношение полимер:мутантный IL-28 или IL-29, содержащий замены цистеина, не должно быть таким большим, поскольку доступны более реакционно-способные группы. Как правило, величина рН составляет в интервале 3-9, или 3-6. Другим фактором, который необходимо учитывать, является молекулярная масса водорастворимого полимера. В общем случае, чем больше молекулярная масса полимера, тем меньше количество молекул полимера, которые могут присоединиться к белку. Для реакций пегилирования типичная молекулярная масса составляет от приблизительно 2 кДа до приблизительно 100 кДа, от приблизительно 5 кДа до приблизительно 50 кДа, от приблизительно 12 кДа до приблизительно 40 кДа или от приблизительно 20 кДа до приблизительно 30 кДа. Молярное отношение водорастворимого полимера к мутантному IL-28 или IL-29, содержащему замены цистеина, обычно составляет в интервале от 1:1 до 100:1. Как правило, молярное отношение водорастворимого полимера к мутантному IL-28 или IL-29 содержащему замены цистеина, составляет от 1:1 до 20:1 для полипегилирования и от 1:1 до 5:1 для монопегилирования.
Общие способы получения конъюгатов, состоящих из интерферона и фрагментов водорастворимого полимера, известны из области техники. См., например, Karasiewicz et al., патент США № 5382657, Greenwald et al., патент США № 5738846, Nieforth et al., Clin. Pharmacol. Ther. 59: 636 (1996), Monkarsh et al., Anal. Biochem. 247: 434 (1997). Пегилированные производные могут быть отделены от непегилированных мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, с помощью обычных методов очистки, таких как диализ, ультрафильтрация, ионообменная хроматография, аффинная хроматография, эксклюзионная хроматография и т.п.
Молекулы мутантного IL-28 или IL-29, содержащего замены цистеина, по настоящему изобретению способны специфически связываться с рецептором IL-28 и/или действовать как антивирусное средство. Анализ связывания мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, с рецептором IL-28 можно осуществить с помощью общепринятых способов. Мутантный IL-28 или IL-29, содержащий замены цистеина, можно иодировать по методу Idobead (Pierce, Рокфорд, Иллинойс) в соответствии с рекомендациями производителя, а затем полученные 125I-IL-28 или 125I-IL-29 могут использоваться, как описано ниже.
В первом подходе пятьдесят нанограммов 125I-IL-28 или 125I-IL-29 можно смешать с 1000 нг слитого белка рецептора IL-28-IgG человека в присутствии или в отсутствие возможных конкурентов связывания, включая не имеющий метки мутантный IL-28, содержащий замены цистеина, мутантный IL-29, содержащий замены цистеина, IL-28 или IL-29. Те же самые реакции связывания можно осуществить, взяв в качестве контроля для определения специфичности другие слитые конструкции рецептор цитокина - IgG человека. После инкубирования при 4°С в реакционную смесь добавляют белок-G (Zymed, Сан-Франциско, Калифорния), с целью захвата слитых конструкций рецептор - IgG и любых связанных с ними белков, и реакционную смесь дополнительно инкубируют в течение часа при 4°С. Затем (белок-G)-сефарозу выделяют, промывают трижды забуференным фосфатом физиологическим раствором и проводят измерение связанных 125I-IL-28 или 125I-IL-29 с помощью счетчика гамма-излучения (Packard Instruments, Даунерс-Гроув, Иллинойс).
Во втором подходе можно провести анализ способности молекул ингибировать связывание 125I-IL-28 или 125I-IL-29 с иммобилизованными на планшете рецепторами. Фрагмент рецептора IL-28, представляющий собой внеклеточный домен связывания лиганда, можно адсорбировать на стенках 96-луночного планшета инкубированием в течение ночи со 100 мкл на лунку раствора рецептора с концентрацией 1 г/мл. В качестве второго варианта слитую конструкцию рецептор - IgG человека можно прикрепить к стенкам 96-луночного планшета, которые были покрыты антителом против той части в слитом белке, которая представляет собой IgG человека. После того, как лунка покроется рецептором, ее промывают, блокируют с помощью SUPERBLOCK (Pierce, Рокфорд, Иллинойс) и вновь промывают. Готовят растворы, содержащие фиксированные концентрации 125I-IL-28 или 125I-IL-29 в присутствии или в отсутствие повышающихся концентраций потенциальных конкурентов связывания, включая мутантный IL-28, содержащий замены цистеина, мутантный IL-29, содержащий замены цистеина, IL-28 или IL-29, и 100 мкл раствора добавляют в соответствующие ячейки на планшете. После инкубирования в течение одного часа при температуре 4°С планшеты промывают и количество связанного 125I-IL-28 или 125I-IL-29 определяют путем подсчета сигналов (Topcount, Packard Instruments, Даунерс-Гроув, Иллинойс). Специфичность связывания 125I-IL-28 или 125I-IL-29 можно определить с помощью молекул рецептора, используемых в указанных анализах на связывание, а также с помощью молекул, используемых в качестве ингибиторов.
Помимо пегилирования, с целью продления времени его полужизни, полипептид по настоящему изобретению можно генетически соединить с альбумином человека. Альбумин человека является наиболее распространенным нативным белком крови в системе кровообращения человека, который сохраняется в системе кровообращения в течение более двадцати дней. Исследования показали, что терапевтически полезные белки, которые генетически сливают с альбумином человека, имеют более длительные времена полужизни. Слитый белок IL-28-альбумин или IL-29-альбумин, подобно пегилированию, может предоставить пациентам возможность осуществить более продолжительное лечение, что позволит использовать более удобные схемы назначения лекарств, которые столь же эффективны или более эффективны и безопасны, чем существующие методы лечения (патент США № 6165470; Syed et al., Blood, 89(9): 3243-3253 (1997); Yeh et al., Proc. Natl. Acad. Sci. USA 89: 1904-1908 (1992); и Zeist et al. Horm. Res., 37: 5-13 (1992)).
Подобно указанным выше пегилированию и связыванию с альбумином человек, Fc часть молекулы IgG человека может быть слита с полипептидом по настоящему изобретению. Полученный слитый белок, благодаря фрагменту Fc, может обладать увеличенным временем полужизни в системе кровообращения (патент США № 5750375, патент США № 5843725, патент США № 6291646; Barouch et al., Journal of Immunology, 61: 1875-1882(1998); Barouch et al., Proc. Natl. Acad. Sci. USA, 97(8): 4192-4197 (April 11, 2000); и Kim et al., Transplant. Proc., 30(8): 4031-4036 (Dec. 1998)).
Методы определения и диагностики вирусных инфекций хорошо известны специалистам в данной области техники. Конкретный метод, который применяют для оценки ослабления вируса в ответ на введение молекул по настоящему изобретению, будет зависеть от видов вируса и от того, является ли инфекция in vitro или in vivo инфекцией. В случае in vivo инфекции измерение и обнаружение инфекции и изменений в уровнях инфекции может варьировать в зависимости от инфицированного субъекта, типа вирусной инфекции и т.д. Например, эти методы включают, но этим не ограничиваясь, определение изменений в количестве CD4 клеток, серологические испытания, определение вирусной ДНК и вирусной РНК анализом с помощью метода обычной и количественной в реальном времени полимеразной цепной реакции, определение индуцированных вирусом уровней антител, иммунофлуоресценцию и твердофазные иммуносорбентные анализы, цитопатические эффекты и гистологию.
Антивирусное действие может быть прямым и опосредованным. Примером прямого антивирусного действия является такой, в котором мутантный полипептид IL-28 или IL-29, содержащий замены цистеина, конкурирует с вирусным рецептором или корецептором, с целью блокировать вирусную инфекцию. Мутантный IL-28 или IL-29, содержащий замены цистеина, можно вводить парентерально, чтобы предотвратить вирусную инфекцию или снизить продолжающуюся репликацию вируса или повторную инфекцию (Gayowski, T. et al., Transplantation 64: 422-426, 1997). Примером опосредованного антивирусного действия является такой, в котором мутантный IL-28 или IL-29, содержащий замены цистеина, может связывать CD4 или другой рецептор лейкоцита и оказывает антивирусное действие за счет модулирования эффектов иммунного ответа.
Особый интерес представляет использование мутантного IL-28 или IL-29, содержащего замены цистеина, в качестве антивирусного средства против вирусной лейкемии (HTLV), СПИДа (ВИЧ) или желудочно-кишечных вирусных инфекций, вызываемых, например, ротавирусом, калицивирусом (в частности, Norwalk Agent) и определенными штаммами патогенных аденовирусов, вирусом гепатита В и С.
Дополнительные типы вирусных инфекций для мутантного IL-28 или IL-29, содержащего замены цистеина, включают, но этим не ограничиваясь, инфекции вызываемые: ДНК-вирусами (в частности, вирусами герпеса, такими как вирусы простого герпеса, вирус Эпштейна-Барр, цитомегаловирус; поксвирусами, такими как вирус натуральной оспы (небольшой поксвирус); гепаднавирусами (в частности, вирусом гепатита В); вирусами папилломы; аденовирусами); РНК-вирусами (в частности, ВИЧ I, II; HTLV I, II; вирусом полиомиелита; гепатитом А; короновирусами, такими как внезапный острый респираторный синдром (SARS); ортомиксовирусами (в частности, вирусами гриппа); парамиксовирусами (в частности, вирусом кори); вирусом бешенства; вирусом гепатита С), флавивирусами, вирусами гриппа; калицивирусами; вирусами бешенства, вирусом чумы рогатого скота, аренавирусом и т.п. Кроме того, примеры типов вызываемых вирусами заболеваний, для лечения которых может применяться мутантный IL-28 или IL-29, содержащий замены цистеина, включают, но этим не ограничиваясь, приобретенный иммунодефицит; тяжелый острый респираторный синдром (SARS); гепатит; гастроэнтерит; геморрагические заболевания; энтерит; кардит; энцефалит; паралич; брохиолит; заболевания верхних и нижних дыхательных путей; респираторный папилломатоз; артрит; диссеминированное заболевание, менингит, мононуклеоз. Кроме того, мутантный IL-28 или IL-29, содержащий замены цистеина, может найти различное применение в антивирусной иммунотерапии и в сочетании с другими цитокинами, другими белками или маленькими молекулами антивирусных средств, и т.п.
В клинических условиях диагностические испытания на HCV включают серологические анализы на антитела и молекулярные тесты на вирусные частицы. Ферментные иммуноанализы известны (Vrielink et al., Transfusion 37: 845-849, 1997), но может потребоваться подтверждение с использованием таких тестов как иммуноблоттинг (Pawlotsky et al., Hepatology 27: 1700-1702, 1998). Для проведения качественных и количественных анализов обычно используют методы полимеразной цепной реакции, и они являются предпочтительными для анализа вирусемии и ответной реакции на лечение (Poynard et al., Lancet 352: 1426-1432, 1998; McHutchinson et al., N. Engl. J. Med. 339: 1485-1492, 1998). Доступно несколько коммерческих тестов, таких как метод количественного RT-PCR (Amplicor HCV Monitor™, Roche Molecular Systems, Бранчбург, Нью-Джерси) и метод гибридизации с использованием разветвленных зондов ДНК (дезоксирибонуклеиновой кислоты) (Quantiplex™ HCV RNA Assay [bDNA], Chiron Corp., Эмеривиль, Калифорния). Неспецифичный лабораторный тест на HCV инфекцию, в котором определяют уровень аминотрансферазы аланина (ALT), недорог и легко доступен (National Institutes of Health Consensus Development Conference Panel, Hepatology 26 (Suppl. 1): 2S-10S, 1997). Гистологическая оценка биопсии печени обычно считается наиболее точным методом определения развития HCV (Yano et al., Hepatology 26: 1334-1340, 1996). Обзор клинических тестов на HCV см. Lauer et al., N. Engl. J. Med. 345: 41-52, 2001.
Существует несколько in vivo моделей для тестирования на HBV и HCV, которые известны специалистам. Что касается HCV, то модель HCV репликона представляет собой систему на основе клетки для исследования эффективности лекарства при подавлении репликации HCV (Blight et al., Science, 290 (5498): 1972-1974 (Dec. 8, 2000); и Lohmann et al., Science, 285 (5424): 110-113 (July 2, 1999)). Хорошо известную специалистам и признанную in vitro модель HBV, которая может использоваться для определения активности тестируемых молекул против HBV, приводят Korba et al., Antiviral Res., 19(1):55-70 (1992) и Korba et al., Antiviral Res., 15(3): 217-228 (1991).
Например, влияние мутантного IL-28 или IL-29, содержащего замены цистеина, на млекопитающих, инфицированных вирусом HBV, можно изучать на модели лесных сурков. Если кратко, то у хронически инфицированных вирусом гепатита сурков (WHV) развивается гепатит и печеночно-клеточный рак наподобие заболевания у людей, хронически инфицированных вирусом HBV. Указанную модель использовали для проведения предклинической оценки антивирусной активности. Получают устойчивую инфицированную линию WHV и новорожденным суркам вводят сыворотку, чтобы получить животных для изучения влияния определенных соединений с использованием указанной модели (для обзора см. Tannant et al., ILAR J. 42(2): 89-102, 2001). Для исследования влияния на HBV-инфицированных животных мутантного IL-28 или IL-29, содержащего замены цистеина, можно также использовать шимпанзе. Используя шимпанзе, провели определение параметров HBV, и проведенные исследования показали, что болезнь у шимпанзе весьма сходна с болезнью у людей (Barker et al., J. Infect. Dis. 132: 451-458, 1975 и Tabor et al., J. Infect. Dis. 147: 531-534, 1983). Модель шимпанзе использовали для оценки вакцин (Prince et al., In Vaccines 97, Cold Spring Harbor Laboratory Press, 1997). Терапевтические методы для HBV обычно тестируют на отличных от человека приматах, инфицированных обезьяньим вирусом иммунодефицита (для обзора см. Hirsch et al., Adv. Pharmacol. 49: 437-477, 2000 и Nathanson et al., AIDS 13 (suppl. A): S113-S120, 1999). Обзор использования отличных от человека приматов для исследования ВИЧ, гепатита, малярии, респираторно-синцитиального вируса и других заболеваний см. у Sibal et al., ILAR J. 42(2): 74-84, 2001. Разработанная недавно модель трансгенных мышей (Guidotti et al., Journal of Virology 69: 6158-6169, 1995) позволяет воспроизводить высокие уровни инфекционного HBV и ее использовали в качестве хемотерапевтической модели для инфекции HBV. Трансгенных мышей лечили антивирусными лекарствами и после лечения определяли уровни ДНК и РНК HBV в печени и сыворотке трансгенных мышей. После лечения можно также определить уровни белка HBV в сыворотке трансгенных мышей. Указанную модель использовали для оценки эффективности ламивудина и IFN-α для снижения вирусного титра HBV (Morrey et al., Antiviral Therapy 3: 59-68, 1998).
Более того, мутантные полипептиды и белки IL-28 или IL-29, содержащие замены цистеина, по настоящему изобретению можно охарактеризовать по их активности, т.е. по модулированию пролиферации, дифференцировки, миграции, адгезии, генной экспрессии или метаболизму соответствующих типов клеток. Биологическую активность мутантных полипептидов и белков IL-28 или IL-29, содержащих замены цистеина, анализируют с использованием in vitro и in vivo методов анализа, разработанных для установления пролиферации, дифференцировки, миграции и адгезии; или анализируют по изменению генной экспрессии или клеточного метаболизма (в частности, по продукции факторов роста или других макромолекул). Из области техники известно много подходящих методов анализа, и отдельные виды анализа приводятся в данном описании. Наиболее удобными для проведения скрининга являются анализы с использованием культивированных клеток, такие как методы определения влияния замен, делеций или вставок аминокислот.
Активность мутантных белков IL-28 или IL-29, содержащих замены цистеина, может быть определена in vitro с использованием выращенных клеток или in vivo путем введения заявляемых в настоящем изобретении молекул в подходящие животные модели. Анализы, в которых определяют пролиферацию или дифференцировку клеток, хорошо известны из области техники. Например, анализы, в которых измеряют пролиферацию, включают такие анализы, как хемочувствительность к красителю нейтральному красному (Cavanaugh et al., Investigational New Drugs 8: 347-354, 1990), включение меченных радиоактивной меткой нуклеотидов (описывается, например, в Raines and Ross, Methods Enzymol. 109: 749-773, 1985; Wahl et al., Mol. Cell Biol. 8: 5016-5025, 1988; и Cook et al., Analytical Biochem. 179: 1-7, 1989), включение 5-бром-2'-дезоксиуридина (BrdU) в ДНК пролиферирующих клеток (Porstmann et al., J. Immunol. Methods 82: 169-179, 1985) и использование солей тетразолия (Mosmann, J. Immunol. Methods 65: 55-63, 1983; Alley et al., Cancer Res. 48: 589-601, 1988; Marshall et al., Growth Reg. 5: 69-84, 1995; и Scudiero et al., Cancer Res. 48: 4827-4833, 1988). Дифференцировку можно анализировать, используя подходящие клетки-предшественники, которых можно заставить дифференцировать в более зрелый фенотип. Анализы, в которых измеряют дифференцировку, включают, например, определение маркеров на клеточной поверхности, связанных с фаза-зависимой экспрессией в ткани, ферментативной активности, функциональной активности или морфологических изменений (Watt, FASEB, 5: 281-284, 1991; Francis, Differentiation 57: 63-75, 1994; Raes, Adv. Anim. Cell Biol. Technol. Bioprocesses, 161-171, 1989; все они включены в данное описание посредством ссылки).
Активность мутантных белков IL-28 или IL-29, содержащих замены цистеина, можно также определить с помощью анализов, основанных на измерении IL-28-индуцируемой или IL-29-индуцируемой продукции одного или нескольких дополнительных факторов роста или других макромолекул. Было показано, что некоторые члены семейства белков, включая IL-28 или IL-29, увеличивают in vivo количество моноцитов в кровообращении. Активация моноцитов важна как для врожденного, так и для приобретенного иммунитета. Например, было показано, что моноциты активируют презентирование антигена посредством нескольких механизмов. Презентирование антигена способствует активации и пролиферации Т-клеток как цитотоксических, так и хелперных Т-клеток. Созревание и активация дендритных клеток также способствует активации Т-клеток, а также как врожденного, так и приобретенного иммунитета. Было также показано, что активированные моноциты и макрофаги усиливают цитолитичесую активность. Таким образом, мутантный IL-28 или IL-29, содержащий замены цистеина, пригоден в качестве антиинфекционного средства, усиливающего врожденный, опосредованный клетками и гуморальный ответ. Наблюдалось усиление окрашивания моноцитов CD14+ под действием ICAM, из чего можно заключить, что IL-28 или IL-29 играют определенную роль в активации моноцитов. Результаты показали, что члены этого семейства способствуют развитию антивирусного ответа на действие вирусов, однако, они, вероятно, могут также воздействовать на бактерии и паразиты.
Анализы активации моноцитов проводят, чтобы (1) оценить способность мутантных белков IL-28 или IL-29, содержащих замены цистеина, дополнительно стимулировать активацию моноцитов и (2) исследовать способность мутантных белков IL-28 или IL-29, содержащих замены цистеина, модулировать индуцированную присоединением или индуцированную эндотоксином активацию моноцитов (Fuhlbrigge et al., J. Immunol. 138: 3799-3802, 1987). Уровни IL-1α и TNF-α, продуцированных в ответ на активацию, определяют методом ELISA (Biosource, Inc., Камарилло, Калифорния). Клетки моноцитов/макрофагов, благодаря CD14 (рецептор LPS), особо чувствительны к действию эндотоксина, и белки с умеренным уровнем эндотоксиноподобной активности должны активировать указанные клетки.
Повышенные уровни моноцитов указывают на то, что мутантный IL-28 или IL-29, содержащий замены цистеина, оказывает прямое действие на миелоидные клетки-предшественники в костном мозге. Усиление дифференцировки миелоидных клетки-предшественников в моноциты имеет важнейшее значение для восстановления иммунокомпетентности, например, после химиотерапии. Таким образом, введение мутантного IL-28 или IL-29, содержащего замены цистеина, пациентам, проходящим курс химиотерапии, способствует их реабилитации и способности противостоять инфекциям, которые обычно сопутствуют химиотерапевтическим методам. Так, в настоящем изобретении предоставляются способы увеличения количества моноцитов или клеток-предшественников моноцитов культивированием либо костного мозга, либо клеток периферической крови вместе с молекулами по настоящему изобретению таким образом, чтобы увеличивалось количество моноцитов или клеток-предшественников моноцитов с тем, чтобы добиться указанного эффекта in vivo или ex vivo. В настоящем изобретении предлагается также способ in vivo введения молекул по настоящему изобретению млекопитающему, которое нуждается в увеличении количества моноцитов или клеток-предшественников моноцитов. Увеличение количества моноцитов или клеток-предшественников моноцитов можно определить с помощью методов, хорошо известных врачам в клиниках, практикующим врачам и другим специалистам. Клетки моноцитов включаются в миелоидную линию дифференцировки кроветворных клеток, и, таким образом, их влияние на другие клетки этой линии дифференцировки не может показаться необычным. Например, когда какой-либо фактор усиливает дифференцировку или пролиферацию одного типа клеток миелоидного или лимфоидного направления дифференцировки, то это может оказать влияние на продукцию других клеток, которые имеют общие клетки-предшественники или стволовые клетки.
Гемопоэтическая активность мутантных белков IL-28 или IL-29, содержащих замены цистеина, может быть определена на различных кроветворных клетках в культуре. Предпочтительные анализы включают анализ образования колоний в первичной культуре костного мозга и анализ линиеспецифического образования колоний в поздней культуре, которые известны из области техники (в частности, Holly et al., публикация WIPO WO 95/21920). Клетки костного мозга, нанесенные на подходящую полутвердую среду (например, 50%-ную метилцеллюлозу, содержащую 15% фетальной телячьей сыворотки, 10% бычьего сывороточного альбумина и 0,6% смеси антибиотиков PSN), выращивают в присутствии тестируемого полипептида, а затем исследуют под микроскопом образование колоний. В качестве контролей используют известные кроветворные факторы. Митогенную активность мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, по отношению к гемопоэтическим клеточным линиям можно определить, как указано выше.
Миграцию клеток анализируют по той же методике, что и описанная у Kдhler et al. (Arteriosclerosis, Thrombosis, and Vascular Biology 17: 932-939, 1997). Белок считается хемотактическим, если он индуцирует миграцию клеток из области с низкой концентрацией белка в область с высокой концентрацией белка. Типичный анализ проводят, используя модифицированные камеры Бойдена с полистирольными мембранами, разделяющими две камеры (Transwell; Corning Costar Corp.). Тестируемый образец, разведенный средой, которая содержит 1% BSA, помещают в нижнюю камеру Transwell с 24-ю лунками. После этого клетки помещают на вставку Transwell, которая предварительно обработана 0,2%-ным желатином. Миграцию клеток определяют после 4 час инкубирования при 37°С. Не мигрировавшие клетки вытирают с верхней части мембраны Transwell, а клетки, присоединившиеся к нижней поверхности мембраны, фиксируют и окрашивают 0,1%-ным кристаллическим фиолетовым. Окрашенные клетки затем экстрагируют 10%-ной уксусной кислотой и измеряют поглощение при 600 нм. После этого рассчитывают миграцию из стандартной калибровочной кривой. Миграцию клеток можно также измерить по методу матригеля, разработанному Grant et al. (“Angiogenesis as a component of epithelial-mesenchymal interactions” in Goldberg and Rosen, Epithelial-mesenchymal Interactions in Cancer, Birkhдuser Verlag, 1995, 235-248; Baatout, Anticancer Research 17: 451-456, 1997).
Адгезивную активность клеток анализируют главным образом по методу, приведенному LaFleur et al. (J. Biol. Chem. 272: 32798-32803, 1997). Если кратко, то планшеты для микротитрования покрывают тестируемым белком, неспецифичные сайты блокируют с помощью BSA и высевают клетки (такие как клетки гладких мышц, лейкоциты или клетки эндотелия) с плотностью приблизительно 104-105 клеток/ячейка. Лунки инкубируют при 37°С (обычно в течение 60 мин), затем не прикрепившиеся клетки удаляют осторожной промывкой. Количество прикрепившихся клеток оценивают обычными методами (в частности, окрашиванием кристаллическим фиолетовым, лизингом клеток и определением оптической плотности лизата). Контрольные лунки покрывают известным адгезивным белком, таким как фибронектин или витронектин.
Экспрессия мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, у животных предоставляет модель для дальнейшего изучения биологических эффектов сверхпродукции или ингибирования активности белка in vivo. Полинуклеотиды, кодирующие IL-28 или IL-29, и антисмысловые полинуклеотиды могут быть введены в тестируемых животных, таких как мыши, с помощью вирусных векторов или “голых” ДНК или же могут быть получены трансгенные животные.
В одном из in vivo подходов при анализе белков по настоящему изобретению используют вирусные системы доставки. Примеры вирусов для этой цели включают аденовирус, вирус герпеса, ретровирусы, вирус коровьей оспы и аденоассоциированный вирус (AAV). Аденовирус, вирус с двунитевой ДНК, в настоящее время является наиболее изученным вектором переноса гена для доставки гетерологичных нуклеиновых кислот. Для обзора см. Becker et al., Meth. Cell Biol. 43: 161-89, 1994; и Douglas and Curiel, Science & Medicine 4: 44-53, 1997. Аденовирусная система предоставляет несколько преимуществ. Аденовирус может (i) принимать относительно большие вставки в ДНК; (ii) быть выращен до больших титров; (iii) инфицировать широкий круг типов клеток млекопитающих; и (iv) использоваться со многими различными промоторами, включая убиквитарные, тканеспецифичные и регулируемые промоторы. Поскольку аденовирусы устойчивы в кровотоке, то их можно вводить внутривенной инъекцией. См. также Wu et al., J. Biol. Chem. 263: 14621-14624, 1988; Wu et al., J. Biol. Chem. 267: 963-967, 1992; и Johnson and Tang, Meth. Cell Biol. 43: 353-365, 1994.
Методами генной инженерии можно также произвести таких трансгенных мышей (Lowell et al., Nature 366: 740-742, 1993), которые способны экспрессировать мутантный ген IL-28 или IL-29, содержащий замены цистеина, или мышей, демонстрирующих полное отсутствие функции мутантного гена IL-28 или IL-29, содержащего замены цистеина, которых называют “мышами-нокаутами” (Snouwaert et al., Science 257: 1083, 1992). Указанных мышей можно использовать для изучения in vivo мутантного гена IL-28 или IL-29, содержащего замены цистеина, и кодируемого им белка. Предпочтительные промоторы для трансгенной экспрессии включают промоторы из генов металлотионеина и альбумина.
Большинство цитокинов, а также других белков, продуцируемых активированными лимфоцитами, играют важную биологическую роль в дифференцировке клеток, активации, рекрутменте и гомеостазе клеток во всем организме. Ожидается, что мутантные IL-28 или IL-29, содержащие замены цистеина, и ингибиторы их активности найдут широкое терапевтическое применение. Указанное терапевтическое применение включает лечение заболеваний, которые требуют иммунной регуляции, включая аутоиммунные заболевания, такие как ревматоидный артрит, рассеянный склероз, тяжелую псевдопаралитическую миастению, системную красную волчанку и диабет. IL-28 или IL-29 может оказаться важным для регуляции воспаления и поэтому может быть пригоден для лечения ревматоидного артрита, астмы и сепсиса. IL-28 или IL-29 может играть определенную роль в опосредовании онкогенеза, а потому антагонист мутантного IL-28 или IL-29, содержащего замены цистеина, может быть пригоден для лечения рака. IL-28 или IL-29 может быть пригоден для модулирования иммунной системы, а потому антагонисты мутантного IL-28 или IL-29, содержащего замены цистеина, могут применяться для ослабления отторжения трансплантатов, для болезни “трансплантат против хозяина”, для усиления иммунитета к инфекционным заболеваниям, для лечения пациентов с поражениями иммунной системы (в частности, ВИЧ+ пациентов) или для улучшения вакцин.
Было показано, что члены семейства белков по настоящему изобретению обладают антивирусным действием, которое напоминает антивирусное действие интерферона-α. Использование интерферонов одобрено в Соединенных Штатах для лечения аутоиммунных заболеваний, остроконечной кондиломы, хронического гепатита С, карциономы мочевого пузыря, цервикальной карциномы, папилломатоза гортани, грибовидного микоза, хронического гепатита В, саркомы Капоши у пациентов, инфицированных вирусом иммунодефицита человека, злокачественной меланомы, лейкемии “волосатых” клеток и рассеянного склероза. Кроме того, мутантный IL-28 или IL-29, содержащий замены цистеина, может использоваться для лечения форм артериосклероза, таких как атеросклероз, за счет ингибирования пролиферации клеток. Таким образом, настоящее изобретение охватывает использование мутантных белков IL-28 или IL-29, содержащих замены цистеина, мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, и пептидов, обладающих активностью IL-28 или IL-29, для лечения указанных состояний, а также для лечения ретинопатии. Настоящее изобретение охватывает также использование мутантных белков IL-28 или IL-29, содержащих замены цистеина, мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, и пептидов, обладающих активностью IL-28 или IL-29, для лечения лимфопролиферативных заболеваний, включая лимфому В-клеток, хронический лимфолейкоз, острый лимфолейкоз, не-ходжкинской лимфомы, множественную миелому, острый миелоцитоз, хронический миелоцитоз.
Было также показано, что интерфероны индуцируют экспрессию антигенов культивированными клетками (см., например, Auth et al., Hepatology 18: 546 (1993), Guаdagni et al., Int. J. Biol. Markers 9: 53 (1994), Girolomoni et al., Eur. J. Immunol. 25: 2163 (1995), и Maciejewski et al., Blood 85: 3183 (1995). Эта активность усиливает способность идентифицировать in vitro новые ассоциированные с опухолями антигены. Более того, способность интерферонов повышать уровень экспрессии антигенов опухолей человека указывает на то, что интерфероны могут применяться для адъювантного регулирования иммунотерапии или усиления иммуносцинтиграфии с использованием противоопухолевых антигенных антител (Guadagni et al., Cancer Immunol. Immunother. 26: 222 (1988); Guadagni et al., Int. J. Biol. Markers 9: 53 (1994)). Таким образом, настоящее изобретение включает использование мутантных белков IL-28 или IL-29, содержащих замены цистеина, мутантных полипептидов IL-28 или IL-29, содержащих замены цистеина, и пептидов, обладающих активностью IL-28 или IL-29, в качестве адъювантов для иммунотерапии или для улучшения иммуносцинтиграфии с использованием противоопухолевых антигенных антител.
Активность и влияние мутантного IL-28 или IL-29, содержащего замены цистеина, на развитие опухолей и метастазы может быть определена in vivo. Для изучения влияния полипептидов, соединений и других способов лечения на развитие опухолей было разработано несколько моделей сингенных мышей. В этих моделях опухолевые клетки после нескольких пересевов в культуральной среде имплантируют мышам той же линии, что и донор опухолей. У мышей-реципиентов клетки развиваются в опухоли, имеющие похожие характеристики, а в некоторых моделях развиваются и метастазы. Подходящие модели опухолей для проведенных авторами исследования включают, среди прочих, легочную карциному Льюиса (АТСС No. CRL-1642) и меланому В16 (АТСС No. CRL-6323). Обе они представляют обычно используемые опухолевые линии, сингенные по отношению к мышам C57BL6, которые легко вырастить и с которыми легко манипулировать in vitro. Опухоли, полученные имплантацией любой из указанных клеточных линий, способны метастазировать в легкие мышей C57BL6. Модель легочной карциномы Льюиса недавно была использована на мышах для идентификации ингибитора ангиогенеза (O'Reilly MS, et al., Cell 79: 315-328, 1994). Проводят обработку мышей C57BL6/J с помощью экспериментального средства либо путем ежедневных инъекций рекомбинантного белка, агониста или антагониста, либо путем однократной инъекции рекомбинантного аденовируса. Через три дня после обработки от 105 до 106 клеток имплантируют в кожу на спине. В качестве альтернативы, сами клетки до их имплантации могут быть инфицированы рекомбинантным аденовирусом, например, таким, который экспрессирует мутантный IL-28 или IL-29, содержащий замены цистеина, таким образом, что белок скорее синтезируется по месту нахождения опухоли или внутриклеточно, а не системно. У мышей различимые опухоли появляются в течение 5 дней. Опухолям дают возможность расти в течение вплоть до 3 недель, и за это время в обработанной контрольной группе они могут достичь размеров 1500-1800 мм3. В течение всего эксперимента размер опухоли и массу тела тщательно контролируют. Как только животных забивают, опухоли извлекают вместе с легкими и печенью и взвешивают. Установлено, что масса легкого коррелирует с метастатической опухолевой нагрузкой. В качестве дополнительного измерения рассчитывают пораженную метастазами поверхность легкого. Иссеченную опухоль, легкие и печень готовят для проведения гистологических исследований, иммуногистохимии и in situ гибридизации, используя методы, известные из области техники и приведенные в данном описании. Указанным образом можно исследовать влияние экспрессии рассматриваемого полипептида, в частности, мутантного IL-28 или IL-29, содержащего замены цистеина, на способность опухоли восстанавливать сосудистую сеть и метастазировать. Кроме того, помимо использования аденовирусов, имплантированные клетки могут быть временно трансфицированы мутантным IL-28 или IL-29, содержащим замены цистеина. Использование стабильных трансфектантов мутантного IL-28 или IL-29, содержащего замены цистеина, а также использование индуцибельных промоторов для активации экспрессии мутантного IL-28 или IL-29, содержащего замены цистеина, известны из области техники и могут применяться в данной системе для анализа активации метастазирования. Более того, очищенную кондиционированную среду, включающую мутантный IL-28 или IL-29, который содержит замены цистеина, можно непосредственно ввести с помощью инъекции в мышиную модель и, таким образом, использовать в данной системе. Общие сведения см. O'Reilly MS, et al., Cell 79: 315-328, 1994; и Rusciano D, et al., Murine Models of Liver Metastasis. Invasion Metastasis 14: 349-361, 1995.
Мутантные IL-28 или IL-29, содержащие замены цистеина, могут также использоваться для лечения миокардита, расстройства, которое возникает, когда сердце вовлекается в воспалительный процесс. Полагают, что результатом инфекции вируса, бактерии, гриба или паразита является инфильтрация лимфоцитов или миоцитолиз (см., например, Brodison et al., J. Infection 37: 99 (1998)). Для лечения инфекций, связанных с миокардитом, мутантный IL-28 или IL-29, содержащий замены цистеина, можно ввести внутривенно или подкожно. Мутантный IL-28 или IL-29, содержащий замены цистеина, можно также ввести внутривенно в качестве иммунорегуляторного цитокина при лечении аутоиммунного миокардита. Дозировки интерферона можно экстраполировать, используя аутоиммунную модель миокардита у мышей A/J (Donermeyer et al., J. Exp. Med. 182: 1291 (1995)).
Последние сообщения высветили роль интерферонов типа I в предотвращении вызываемого вирусами диабета за счет индуцирования сильного антивирусного статуса в бета-клетках поджелудочной железы на ранних стадиях вирусной инфекции (Flodstroem et al., Nature Immunology 3: 373-382 (2002)). Таким образом предотвращается потеря бета-клеток вследствие индуцированного вирусом отмирания клеток и сопровождающей его аутоиммунной реакции. Мутантный IL-28 или IL-29, содержащий замены цистеина, индуцирует также антивирусное состояние в клетках, которые экспрессируют рецептор IL-28. Рецептор IL-28 высоко экспрессируется в тканях поджелудочной железы, а потому мутантный IL-28 или IL-29, содержащий замены цистеина, может играть определенную роль в предотвращении вызываемого вирусами диабета и отмирания бета-клеток. Кроме того, роль интерферона типа I в предотвращении вызываемого вирусами диабета можно распространить на другие вызываемые вирусами аутоиммунные заболевания, и поэтому мутантный IL-28 или IL-29, содержащий замены цистеина, может сыграть роль в предотвращении других заболеваний, таких как мышечный склероз, волчанка и вызываемые вирусами аутоиммунные заболевания тканей, которые экспрессируют рецептор IL-28.
Мутантные полипептиды IL-28 или IL-29, содержащие замены цистеина, могут вводиться индивидуально или в комбинации с другими васкулогенными или ангиогенными средствами, включая VEGF. При использовании мутантного IL-28 или IL-29, содержащего замены цистеина, в комбинации с дополнительным средством оба соединения могут вводиться одновременно или раздельно в зависимости от конкретного излечиваемого состояния.
Мутантные IL-28 или IL-29, содержащие замены цистеина, пригодны при лечении онкогенеза, а потому могли бы использоваться для лечения рака. IL-28 может ингибировать опухолевые линий В-клеток, и, таким образом, может оказаться терапевтически полезным проводить лечение пациентов с помощью мутантного IL-28 или IL-29, содержащего замены цистеина, с целью перевести В-клетки опухолевых клеток в менее пролиферативное состояние. Лиганд можно вводить в комбинации с другими средствами, которые уже нашли практическое применение, включая обычные химиотерапевтические средства, а также иммуномодуляторы, такие как интерферон-альфа. Было показано, что альфа/бета-интерфероны эффективны при лечении некоторых типов лейкемий и животных моделях болезни, и ингибирующее действие интерферона-альфа и мутантного IL-28 или IL-29, содержащего замены цистеина, на рост может дополнять действие индуцированных опухолями клеточных линий В-клеток.
В соответствии с еще одним аспектом, настоящее изобретение предоставляет фармацевтическую композицию, содержащую изолированный пептид, который выбирают из группы, включающей SEQ ID NO: 2, 4, 6, 8, 10, 13, 15, 17, 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161, и фармацевтически приемлемый носитель.
Для целей фармацевтического применения мутантные белки IL-28 или IL-29, содержащие замены цистеина, готовят обычными способами в виде композиции для местного нанесения или парентерального, в частности, внутривенного или подкожного, введения. В общем случае, фармацевтические препараты включают мутантный полипептид IL-28 или IL-29, содержащий замены цистеина, в сочетании с фармацевтически приемлемым носителем, таким как физиологический раствор, забуференный физиологический раствор, 5%-ный раствор декстрозы в воде и т.п. Препараты могут, кроме того, включать одно или несколько вспомогательных средств, консервантов, солюбилизаторов, буферирующих добавок, альбумин для предотвращения потерь белка на стенках ампул и т.п. Способы приготовления препаратов хорошо известны из области техники и приводятся, например, в Remington: The Science and Practice of Pharmacy, Gennaro, ed., Mack Publishing Co., Easton, PA, 19th ed., 1995. Мутантный IL-28 или IL-29, содержащий замены цистеина, преимущественно используют с концентрацией приблизительно от 10 до 100 мкг/мл в общем объеме, хотя могут применяться концентрации в диапазоне от 1 нг/мл до 1000 мкг/мл. Для местного нанесения, например, с целью ускорения заживления ран, белок наносят в диапазоне 0,1-10 мкг на квадратный сантиметр площади раны, при этом точная доза определяется врачом на основании принятых стандартов с учетом природы и тяжести излечиваемого состояния, индивидуальных особенностей пациента и т.п. Определение дозы находится в пределах компетенции специалиста. Дозировку проводят ежедневно или делают перерывы в лечении. Внутривенное введение осуществляют путем инъекции болюсами или инфузией, как правило, в течение от одного до нескольких часов. Могут также применяться составы с пролонгированным высвобождением лекарства. В общем случае терапевтически эффективное количество мутантного IL-28 или IL-29, содержащего замены цистеина, представляет собой такое количество, которое достаточно для того, чтобы вызывать клинически значимое изменение в излечиваемом состоянии, такое как клинически значимое изменение в вирусной нагрузке или иммунной функции, клинически значимое снижение заболеваемости или клинически значимое повышение гистологического показателя.
В качестве иллюстрации, фармацевтические препараты могут быть представлены в виде набора, содержащего контейнер, в котором содержится полипептид IL-28 или IL-29 по настоящему изобретению. Имеющие терапевтическую ценность полипептиды могут быть представлены в виде раствора для инъекций для однократной или многократных доз или в виде стерильного порошка, который восстанавливают перед инъекцией. В качестве альтернативы, указанный набор может включать диспергатор для сухих порошков, генератор аэрозолей из жидкости или распылитель для введения терапевтического полипептида. Кроме того, указанный набор может включать отпечатанную в виде инструкцию информацию о показаниях и применении фармацевтической композиции. Более того, подобная информация может включать указание относительно того, что состав, содержащий полипептид IL-28 или IL-29 противопоказан пациентам с известной гиперчувствительностью к полипептиду IL-28 или IL-29.
В соответствии с другим аспектом, в настоящем изобретении предлагается способ получения антитела к полипептиду, который включает: вакцинацию животного полипептидом, выбранным из группы, включающей SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161, при этом полипептид вызывает у животного иммунный ответ, приводящий к продукции антитела; и выделение антитела из животного. В соответствии с другим аспектом, в настоящем изобретении предлагается антитело (в частности, нейтрализующее антитело), получаемое по указанному выше способу, при этом антитело связывается с полипептидом, выбранным из группы, включающей SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. В одном из вариантов осуществления настоящего изобретения раскрытое выше антитело специфически связывается с полипептидом, выбранным из группы, включающей SEQ ID NO: 19, 21, 23, 25, 27, 29, 36, 37, 38, 39, 40, 41, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159 и 161. В соответствии с другим аспектом, в настоящем изобретении предлагается антитело или фрагмент антитела, которое специфически связывается с полипептидом, как указывается в данном описании. В одном из вариантов осуществления настоящего изобретения антитело выбирают из группы, включающей поликлональное антитело, мышиное моноклональное антитело, гуманизированное антитело, полученное из мышиного моноклонального антитела, фрагмент антитела и моноклональное антитело человека. В одном из вариантов осуществления настоящего изобретения фрагмент антитела представляет собой приведенный в настоящем описании фрагмент антитела, при этом указанный фрагмент антитела выбирают из группы, включающей F(ab'), F(ab), Fab', Fab, Fv, scFv и минимальную распознавательную единицу.
В соответствии с другим аспектом, в настоящем изобретении предлагается антигенотипное антитело, которое специфически связывается с антителом, как указывается в данном описании.
В тексте настоящего описания термин “антитела” включает поликлональные антитела, моноклональные антитела, их антиген-связывающие фрагменты, такие как фрагменты F(ab')2 и Fab, одноцепочечные антитела и т.п., включая антитела, полученные методами генной инженерии. Отличные от человека антитела можно гуманизировать прививкой отличных от человека CDRs в скелетные и константные области антитела человека или включением отличных от человека вариабельных областей целиком (с необязательным “покрытием” их человекоподобной поверхностью за счет открытых остатков, при этом получают антитело со слоем “шпона”). В некоторых случаях гуманизированные антитела могут сохранять не присущие человеку остатки внутри вариабельных областей антитела человека, с целью усиления необходимых для связывания свойств. Посредством гуманизации антител биологический период полужизни может быть увеличен, а потенциал протекания вредных иммунных реакций снижен. Специалист может генерировать гуманизированные антитела, содержащие специфические и отличающиеся константные домены (например, различные субклассы Ig), с целью облегчить или ингибировать различные иммунные функции, связанные с конкретными константными участками антитела. Антитела определяют как специфически связывающиеся, если они связываются с мутантным полипептидом или белком IL-28 или IL-29, содержащим замены цистеина, с аффинностью, по меньшей мере, в 10 раз превышающей аффинность к контрольному (отличному от мутантного IL-28 или IL-29, содержащего замены цистеина) полипептиду или белку. Специалист может легко определить аффинность моноклонального антитела (см., например, Scatchard, Ann. NY Acad. Sci. 51: 660-672, 1949).
Способы получения поликлональных и моноклональных антител хорошо известны из области техники (см., например, Hurrell, J.G.R., Ed., Monoclonal Hybridoma Antibodies: Techniques and Applications, CRC Press, Inc., Boca Raton, FL, 1982; включена в настоящее описание посредством ссылки). Полипептидный иммуноген может представлять собой полную молекулу или ее часть. Если полипептидная часть является “гаптеноподобной”, то при проведении вакцинации указанную часть удобно соединить или связать с макромолекулярным носителем (таким как гемоцианин моллюска фиссуреллии (KLH), бычий сывороточный альбумин (BSA) или столбнячный анатоксин).
Для детектирования антител, которые специфически связываются с мутантными полипептидами IL-28 или IL-29, содержащими замены цистеина, может быть использовано большое количество известных специалистам аналитических методов. Примеры анализов подробно излагаются в Using Antibodies: A Laboratory Manual, Harlow and Lane (Eds.), Cold Spring Harbor Laboratory Press, 1999. Отдельные примеры подобных анализов включают: совместный иммуноэлектрофорез, радиоиммуноанализы, радиоиммуноосаждения, иммуноферментный твердофазный анализ (ELISA), дот-блоттинг, вестерн-блоттинг, ингибиторные и конкурентные анализы и сэндвич-анализы.
Для определенных применений, включая использование в in vitro и in vivo диагностических целях, удобно использовать содержащие метки антитела. Подходящими прямыми метками являются радионуклиды, ферменты, субстраты, кофакторы, ингибиторы, флуоресцентные маркеры, хемилюминесцентные маркеры, магнитные частицы и т.п.; функции непрямых меток могут выполнять биотин-авидин и другие пары комплемент/антикомплемент в качестве промежуточных соединений. Антитела по настоящему изобретению могут быть непосредственно или опосредованно связаны с лекарствами, токсинами, радионуклидами и т.д., а полученные конъюгаты могут применяться для in vivo диагностики или терапевтических применений (например, для угнетения клеточной пролиферации). Общую информацию см. Ramakrishnan et al., Cancer Res. 56: 1324-1330, 1996.
Настоящее изобретение далее поясняется следующими не ограничивающими изобретение примерами.
ПРИМЕРЫ
Пример 1
Экспрессионные плазмиды млекопитающих
Экспрессионную плазмиду, содержащую zcyto20 и zcyto21, конструируют посредством гомологической рекомбинации. Фрагменты кДНК zcyto20 и zcyto21 получают с помощью ПЦР-амплификации. В качестве праймеров для проведения ПЦР используют следующие:
zcyto20/pZMP21: zc40923 и zc43152 SEQ ID NO: 42 и 43, соответственно; и zcyto21/pZMP21: zc40922 и zc43153 SEQ ID NO: 2 и 73, соответственно.
Реакцию ПЦР проводят на 1%-ном агарозном геле и полосу, соответствующую размеру вставки, экстрагируют с помощью набора QIAquick™ Gel Extraction (Qiagen, Валенсия, Калифорния).
Плазмиду pZMP21, которую разрезают с помощью BglII, используют для рекомбинации с фрагментом вставки ПЦР. Плазмида pZMP21 представляет собой экспрессирующий вектор млекопитающего, содержащий полигенный экспрессирующий кластер с MPSV промотором и множественные сайты рестрикции для вставки кодирующих последовательностей; сайт инициации репликации из E. coli; блок селектируемого маркера экспрессии млекопитающего, включающий SV40 промотор, энхансер и сайт инициации репликации, ген DHFR и SV40 терминатор; и последовательности URA3 и CEN-ARS, необходимые для селекции и репликации в S. cerevisiae. Ее конструируют из pZP9 (депонирована в Американской коллекции типовых культур, 10801 University Boulevard, Manassas, VA 20110-2209, под номером 98668) с генетическими элементами дрожжевой системы, полученными из pRS316 (депонирована в Американской коллекции типовых культур, 10801 University Boulevard, Manassas, VA 20110-2209, под номером 77145), элементом сайта внутренней посадки рибосомы (IRES) из вируса полиомиелита и внеклеточным доменом из CD8, усеченным по С-концу трансмембранного домена.
Сто микролитров компетентных дрожжевых клеток (S. cerevisiae) независимо объединяют с 10 мкл ДНК-вставки и 100 нг разрезанного вектора pZMP21, указанного выше, и смесь помещают в кювету для электропорации с расстоянием между электродами 0,2 см. Смесь дрожжи/ДНК подвергают электропорации с помощью источника тока (BioRad Laboratories, Геркулес, Калифорния) с параметрами 0,75 кВ (5 кВ/см), ∞ Ом, 25 мкФ. В кювету добавляют шестьсот микролитров 1,2 М раствора сорбита и дрожжи помещают в виде аликвот объемом 100 мкл и 300 мкл в две чашки URA-D и инкубируют при 30°С. Через приблизительно 72 час трансформанты дрожжей Ura+ из одной чашки вновь суспендируют в 1 мл H2O и осторожно центрифугируют для получения осадка из дрожжевых клеток. Клеточную массу ресуспендируют в 0,5 мл буферного раствора для лизиса (2% Triton X-100, 1% SDS, 100 мМ NaCl, 10 мМ Трис, рН 8,0, 1 мМ ЭДТК). Пятьсот микролитров смеси для лизиса помещают в пробирку Эппендорфа, содержащую 250 мкл промытых кислотой стеклянных шариков и 300 мкл смеси фенол-хлороформ, и энергично перемешивают в течение 3 мин, а затем с максимальной скоростью вращают в течение 5 мин в центрифуге Эппендорфа. Триста микролитров водной фазы переносят в свежую пробирку и осаждают ДНК с помощью 600 мкл этанола (EtOH) и 30 мкл 3М раствора ацетата натрия, а затем центрифугируют с максимальной скоростью в течение 30 мин. Осадок ДНК ресуспендируют в 30 мкл ТЕ.
Трансформацию элекрокомпетентных E. coli клеток-хозяев (МС1061) проводят, используя 5 мкл препарата дрожжевой ДНК и 50 мкл клеток. Клетки подвергают электропорации с параметрами 2,0 кВ, 25 мкФ и 400 Ом. В процессе электропорации добавляют 1 мл SOC (2% бактотриптона (Difco, Детройт, Мичиган), 0,5% дрожжевого экстракта (Difco), 10 мМ NaCl, 2,5 мМ KCl, 10 мМ MgCl2, 10 мМ MgSO4, 20 мМ глюкозы) и клетки помещают в виде аликвот 50 мкл и 200 мкл в две чашки LB AMP (питательная среда LB (Lennox), 1,8% Bacto™ Agar (Difco), 100 мг/л ампициллина).
Вставки трех клонов для каждой генной конструкции секвенируют и отбирают один клон для каждой конструкции, содержащий правильную последовательность. Более масштабное выделение плазмидной ДНК проводят с помощью коммерчески доступного набора (QIAGEN Plasmid Mega Kit, Qiagen, Валенсия, Калифорния) в соответствии с рекомендациями производителя. Правильные конструкции называют zcyto20/pZMP21 и zcyto21/pZMP21.
Пример 2
Экспрессия конструкций млекопитающих в клетках СНО
200 мкг генетических конструкций zcyto20/pZMP21 и zcyto21/pZMP21 расщепляют с использованием 200 единиц PvuI при 37єС в течение трех часов, а затем осаждают изопропиловым спиртом и осадок отделяют центрифугированием в микропробирках емкостью 1,5 мл. Надосадочную жидкость декантируют с осадка и осадок промывают 1 мл 70%-ного раствора этанола и инкубируют в течение 5 мин при комнатной температуре. Пробирку для микроцентрифуги вращают в течение 10 мин со скоростью 14000 об/мин и надосадочную жидкость отделяют с помощью отсоса. Затем осадок ресуспендируют в 750 мкл среды PF-CHO в стерильных условиях и инкубируют при 60°С в течение 30 мин. Клетки СНО отделяют центрифугированием и ресуспендируют в растворе среды ДНК. Смесь ДНК/клетки помещают в кювету для электропорации и электропорируют в следующих условиях: 950 мкФ, высокая емкость и 300 В. Затем содержимое извлекают из кюветы, разбавляют с помощью 25 мл среды PF-CHO и помещают в колбу качалочной мешалки емкостью 125 мл. Колбу устанавливают в инкубатор на качалочной мешалке при 37°С, 6% СО2 и перемешивают со скоростью 120 об/мин.
Пример 3
Очистка и анализ белка zcyto20-CHO
А. Очистка белка zcyto20-CHO
Рекомбинантный белок zcyto20-CHO (IL-28A) выделяют из пула клеточных линий DXB11-CHO. Выращивают культуры, и питательную среду стерилизуют фильтрованием через фильтр с размерами пор 0,2 мкм.
Очистку белка zcyto20-CHO проводят последовательно с использованием колонки Poros HS 50 (Applied Biosystems, Фрамингэм, Массачусетс), колонки Monolithic WCX (Isco, Inc., Линкольн, Небраска), колонки ToyoPearl Butyl 650S (TosoH, Монтгомеривиль, Пенсильвания) и колонки Superdex 75 (Amersham Biosciences, Пискатауэй, Нью-Джерси). Перед помещением на колонку Poros HS 50 величину рН культуральной среды из DXB111-CHO доводят до 6,0. Колонку промывают раствором 50 мМ MES (2-морфолинэтансульфоновой кислоты), 100 мМ NaCl с рН 6 и связанный белок элюируют 10 объемами колонки (CV) в линейном градиенте до 60% 50 мМ MES, 2 М NaCl с рН 6. Выделенные элюированием фракции собирают и наличие белка zcyto20 подтверждают методом SDS-PAGE, используя окрашивание Кумасси. Указанные фракции, которые содержат белок zcyto20, объединяют, разбавляют бидистиллированной водой до электропроводности приблизительно 20 мСм и помещают на колонку Monolithic WCX. Колонку промывают 93% 50 мМ MES, 100 мМ NaCl с рН 6 и 7% 50 мМ MES, 2 М NaCl с рН 6. Связанный белок элюируют 25 объемами колонки в линейном градиенте от 7% до 50% 50 мМ MES, 2 М NaCl с рН 6. Выделенные элюированием фракции собирают и наличие белка zcyto20 подтверждают методом SDS-PAGE, используя окрашивание Кумасси. Фракции, которые содержат белок zcyto20, объединяют, доводят до 1 М сульфатом аммония и помещают на колонку ToyoPearl Butyl 650S. Zcyto20 элюируют в уменьшающемся градиенте сульфата аммония и фракции, содержащие очищенный zcyto20, объединяют и концентрируют перед инжекцией в колонку Superdex 75. Содержащие zcyto20 фракции, которые получают после колонки гель-фильтрации, объединяют, концентрируют, фильтруют через фильтр с размерами пор 0,2 мкм и замораживают при -80°С. Концентрацию конечного очищенного белка определяют анализом с помощью ВСА (Pierce Chemical Co., Рокфорд, Иллинойс) и аминокислотным ВЭЖХ-анализом.
B. SDS-PAGE и анализ по методу вестерн-блоттинга белка zcyto20-CHO
Рекомбинантный белок zcyto20 анализируют методом SDS-PAGE (Nupage 4-12% Bis-Tris, Invitrogen, Карлсбад, Калифорния) и по методу вестерн-блоттинга с использованием IgG кролика против zcyto21-CEE-BV в качестве основного антитела, которое перекрестно взаимодействует с белком zcyto20-CHO. Гель подвергают электрофорезу в мини-ячейке Xcell II компании Invitrogen (Карлсбад, Калифорния) и переносят на мембрану из нитроцеллюлозы с размерами пор 0,2 мкм (Bio-Rad Laboratories, Геркулес, Калифорния) с помощью модуля для блоттинга Xcell II компании Invitrogen в соответствии с инструкциями, прилагающимися к устройству. Указанный перенос осуществляют при 500 мА в течение 50 мин в буферном растворе, содержащем 25 мМ основания Трис, 200 мМ глицина и 20% метанола. Мембрану блокируют 10%-ным раствором обезжиренного сухого молока в 1х PBS в течение 10 мин, затем зондируют основным антителом в 1х PBS, содержащем 2,5% обезжиренного сухого молока. Реплику помечают в течение одного часа при комнатной температуре при встряхивании. Для введения метки второго антитела, реплику три раза по 10 мин каждый промывают раствором PBS и зондируют козьим антителом против IgG-HRP кролика (Pierce Chemical Co., Рокфорд, Иллинойс) в течение одного часа. Реплику промывают раствором 1х PBS три раза по 10 мин каждый и проявляют смесью 1:1 реагентов SuperSignal® ULTRA (Pierce Chemical Co., Рокфорд, Иллинойс) и сигнал регистрируют с помощью Lumi-Imager (Boehringer Mannheim GmbH, Германия).
C. Резюме по очистке и анализу белка
Очищенный белок zcyto20 в не восстановительных условиях преимущественно перемещается из среды СНО на 4-12% Bis-Tris гель в виде дублета с массой приблизительно 20 кДа и в меньшей степени в виде димера триплетов с массой приблизительно 38 кДа. В восстановительных условиях все они сжимаются в одну полосу 20 кДа. Картирование пептида методом масс-спектрометрии указывает на смесь двух изомеров относительно дисульфидного мостика и наличие О-связанного сайта гликозилирования.
Пример 4
Очистка и анализ белка zcyto21-CHO
А. Очистка белка zcyto21-CHO
Рекомбинантный zcyto21 получают из стабильных клеточных линий DXB11-CHO. Выращивают культуры и питательную среду стерилизуют фильтрованием через фильтр с размерами пор 0,2 мкм. Белки очищают из кондиционированной среды, начав с комбинации катионной и анионной обменной хроматографии, а затем хроматографией с гидрофобными взаимодействиями и эксклюзионной хроматографией. Перед помещением на колонку Poros HS 50 (Applied Biosystems, Фрамингэм, Массачусетс) величину рН культуральной среды DXB111-CHO доводят до 6,0. Колонку промывают с помощью 1х PBS с рН 6 и связанный белок элюируют с помощью 5х PBS с рН 8,4. Выделенные элюированием фракции собирают и наличие белка zcyto21 подтверждают методом SDS-PAGE, используя окрашивание Кумасси. Указанные фракции затем разбавляют до электропроводности 13 мСм, доводят рН до 8,4 и пропускают через колонку Poros 50 HQ (Applied Biosystems, Фрамингэм, Массачусетс). Фильтрат, содержащий белок zcyto21, доводят сульфатом аммония до электропроводности приблизительно 127 мСм и помещают на колонку Toyopearl Phenyl 650S (TosoH, Монтгомеривиль, Пенсильвания). Zcyto21 элюируют в уменьшающемся градиенте сульфата аммония и фракции, содержащие очищенный zcyto21, объединяют и концентрируют перед инжекцией в колонку Superdex 75 (Amersham Biosciences, Пискатауэй, Нью-Джерси). Концентрацию конечного очищенного белка определяют анализом с помощью ВСА (Pierce Chemical Co., Рокфорд, Иллинойс) и аминокислотным ВЭЖХ-анализом.
B. SDS-PAGE и вестерн-блоттинг анализ белка zcyto20-CHO
Рекомбинантный белок zcyto21 анализируют методом SDS-PAGE (Nupage 4-12% Bis-Tris, Invitrogen, Карлсбад, Калифорния) и методом вестерн-блоттинга с использованием IgG кролика против zcyto21-CEE-BV в качестве основного антитела. Гель подвергают электрофорезу в мини-ячейке Xcell II компании Invitrogen (Карлсбад, Калифорния) и переносят на мембрану из нитроцеллюлозы с размерами пор 0,2 мкм (Bio-Rad Laboratories, Геркулес, Калифорния) с помощью модуля для блоттинга Xcell II компании Invitrogen в соответствии с инструкциями, прилагающимися к устройству. Перенос осуществляют при 500 мА в течение 50 мин в буферном растворе, содержащем 25 мМ основания Tris, 200 мМ глицина и 20% метанола. Переместившееся пятно блокируют 10%-ным раствором обезжиренного сухого молока в 1х PBS в течение 10 мин, затем зондируют основным антителом в 1х PBS, содержащим 2,5% обезжиренного сухого молока. Реплику помечают в течение одного часа при комнатной температуре при встряхивании. Для введения метки второго антитела, реплику три раза по 10 мин каждый промывают раствором PBS и зондируют козьим антителом против IgG-HRP кролика (Pierce Chemical Co., Рокфорд, Иллинойс) в течение одного часа. Реплику промывают раствором 1х PBS три раза по 10 мин каждый и проявляют смесью 1:1 реагентов SuperSignal® ULTRA (Pierce Chemical Co., Рокфорд, Иллинойс) и сигнал регистрируют с помощью Lumi-Imager (Boehringer Mannheim GmbH, Германия).
C. Резюме по очистке и анализу белка
Очищенный белок zcyto21 как в восстановительных, так и невосстановительных условиях перемещается из среды СНО на 4-12% Bis-Tris гель в виде двух или нескольких полос с массой приблизительно 20 кДа. Картирование пептида методом масс-спектрометрии указывает на смесь двух изомеров относительно дисульфидного мостика и наличие N-связанного сайта гликозилирования и нескольких О-связанных сайтов гликозилирования.
Пример 5
Идентификация форм IL-29
Пики фракций из очищенных пулов IL-29 расщепляют в течение ночи при температуре 37°С с помощью трипсина (Roche Applied Science, Индианаполис, Индиана), чистота которого подходит для проведения секвенирования, в фосфатном буфере с рН приблизительно 6,3 таким образом, чтобы свести к минимуму перестройку дисульфидных связей. Продукт каждого расщепления анализируют методом ВЭЖХ с обращенной фазой (Agilent, Пало-Альто, Калифорния) на хроматографе, сопряженном с квадрупольным времяпролетным гибридным масс-спектрометром (Micromass, Милфорд, Массачусетс). Получают спектры, преобразуют величины массы в отношения заряда к массе и сравнивают со всеми теоретически возможными пептидами и комбинациями связанных дисульфидными мостиками пептидов, которые могут получиться при расщеплении IL-29 с помощью трипсина. Дисульфиды определяют путем сравнения спектров до и после сокращения с отнесением соответствующих масс к связанным дисульфидными мостиками пептидам в IL-29. Вещество из фракции #20 показывает дисульфидную структуру С15-С112 и С49-С145 с С171 наблюдаемым как S-глутатионил цистеин (все относятся к SEQ ID NO: 4). Вещество из фракции #51 показывает дисульфидную структуру С49-С145 и С112-С171 с С15 наблюдаемым как S-глутатионил цистеин (все относятся к SEQ ID NO: 4).
Пример 6
Экспрессионная плазмида E. coli
Конструирование экспрессирующего вектора, pTAP237
Плазмиду pTAP237 конструируют вставкой генерированного по методу ПЦР линкера в SmaI сайт pTAP186 по методу гомологичной рекомбинации. Плазмиду pTAP186 получают из плазмид pRS316 (“челночного” вектора Saccharomyces cerevisiae) и pMAL-c2, экспрессионной плазмиды E. coli, полученной из pKK223-3 и включающей tac промотор и rrnB терминатор. Плазмида pTAP186 содержит сайт устойчивости к канамицину, в котором сайт SmaI разрушен и содержит сайты NotI и SfiI, фланкирующие дрожжевые последовательности ARS-CEN6 и URA3, что облегчает их удаление из плазмиды под действием NotI. Генерированный по методу ПЦР линкер заменяет последовательность экспрессирующего линкера в pTAP186 на синтетическую последовательность RBS II. Ее получают из 100 пМ каждого из олигонуклеотидов zc29740 и zc29741, приведенных в SEQ ID NO: 44 и 45, соответственно, и приблизительно 5 пМ каждого из олигонуклеотидов zc29736 и zc29738, приведенных в SEQ ID NO: 46 и 47, соответственно. Указанные олигонуклеотиды объединяют методом ПЦР за десять циклов, включающих 94°С в течение 30 сек, 50°С в течение 30 сек и 72°С в течение 30 сек с последующим отжигом при 4°С. Полученные ПЦР-продукты концентрируют осаждением двумя порциями 100%-ного этанола. Таблетку ресуспендируют в 10 мкл воды и используют для повторного объединения с вектором реципиента pTAP186, расщепленного с помощью SmaI, и получают генную конструкцию, включающую синтетическую последовательность RBS II. Примерно 1 мкг полученного методом ПЦР линкера и 100 нг pTAP186, расщепленной с помощью SmaI, смешивают друг с другом и трансформируют в компетентные дрожжевые клетки (S. cerevisiae). Дрожжи затем помещают в чашки -URA D и оставляют при комнатной температуре приблизительно на 72 час. Затем Ura+ трансформанты из одной чашки ресуспендируют в 1 мл H2O и центрифугируют в течение короткого времени, чтобы получить осадок дрожжевых клеток. Таблетку из клеток ресуспендируют в 0,5 мл буферного раствора для лизиса. ДНК выделяют и трансформируют в E. coli МС1061. Клоны подвергают скринингу по методу ПЦР колоний, как указано выше, используя по 20 пМ каждого из олигонуклеотидов zc29740 и zc29741, приведенных в SEQ ID NO: 44 и 45, соответственно. Клоны, которые дают корректный размер полосы на агарозном геле, секвенируют. Правильную плазмиду называют pTAP237.
Пример 7
Оптимизация кодонов в мутантном IL-29, содержащем замены цистеина
А. Оптимизация кодонов при генерировании экспрессионной генной конструкции IL-29 дикого типа
Последовательность природного гена IL-29 человека плохо экспрессируется в штамме W3110 E. coli. Изучение кодонов, используемых в кодирующей последовательности IL-29, показывает, что она содержит избыток наименее часто используемых в E. coli кодонов, при этом величина CAI составляет 0,206. Значение CAI является статистической мерой синонимичного смещения кодонов и может быть использована для предсказания уровня продукции белка (Sharp et al., Nucleic Acid Res. 15(3): 1281-95, 1987). Гены, кодирующие высокоэкспрессируемые белки, проявляют тенденцию к большим значениям CAI (> 0,6), в то время как белки, кодируемые генами с низким значением CAI (≤ 0,2), обычно экспрессируются неэффективно. Это объясняет причину плохой продукции IL-29 в E. coli. Кроме того, редкие кодоны кластеризуются во второй части транскрипта, что приводит к высокой вероятности задержки трансляции, преждевременной терминации трансляции и ошибке в объединении аминокислот (Kane J.F., Curr. Opin. Biotechnol. 6(5): 494-500, 1995).
Было показано, что уровень экспрессии белков, гены которых содержат редкие кодоны, может быть значительно улучшен, когда у хозяина повышается уровень определенных редких молекул тРНК (Zdanovsky et al., Applied Enviromental Microb. 66: 3166-3173, 2000; You et al., Biotechniques 27: 950-954, 1999). Плазмида pRARE содержит гены, кодирующие тРНК для ряда кодонов, редко используемых E. coli (argU, argW, leuW, proL, ileX и glyТ). Указанные гены контролируются их нативными промоторами (Novy, там же). Коэкспрессия с pRARE усиливает продукцию IL-29 в E. coli и выход достигает приблизительно 200 мг/л. На основании этих данных можно сделать вывод, что повторный синтез гена, кодирующего IL-29, вместе с более правильным использованием кодонов предоставляет улучшенный вектор для экспрессии больших количеств IL-29.
Кодирующую IL-29 последовательность с оптимизированными кодонами конструируют из шестнадцати перекрывающихся олигонуклеотидов: zc44566 (SEQ ID NO: 48), zc44565 (SEQ ID NO: 49), zc44564 (SEQ ID NO: 50), zc44563 (SEQ ID NO: 51), zc44562 (SEQ ID NO: 52), zc44561 (SEQ ID NO: 53), zc44560 (SEQ ID NO: 54), zc44559 (SEQ ID NO: 55), zc44558 (SEQ ID NO: 56), zc44567 (SEQ ID NO: 57). Удлинение указанных олигонуклеотидов праймером с последующей ПЦР-амплификацией дает ген IL-29 полной длины с кодонами, оптимизированными для экспрессии в E. coli. Конечный ПЦР-продукт вставляют в экспрессирующий вектор pTAP237 с помощью гомологичной рекомбинацией в дрожжевой системе. Экспрессионную генетическую конструкцию экстрагируют из дрожжей и трансформируют в компетентный МС1061 E. coli. Устойчивость клонов к канамицину идентифицируют методом ПЦР колоний. Положительный клон подтверждают секвенированием и затем трансформируют в хозяин-продуцент штамм W3110. Экспрессирующий вектор с оптимизированной последовательностью IL-29 называют pSDH184. Полученный ген очень хорошо экспрессируется в E. coli. Уровни экспрессии с новой генной конструкцией возрастают приблизительно до 250 мг/л.
В. Приготовление экспрессионной конструкции zcyto21 C172S, содержащей мутацию по цистеину, с оптимизированными кодонами
Стратегия, используемая для приготовления zcyto21 C172S, содержащего мутацию по цистеину, основана на использовании набора реагентов для проведения сайтнаправленного мутагенеза QuickChange Site-Directed Mutagenesis (Stratagene). Праймеры для введения мутации С172S разрабатывают в соответствии с рекомендациями изготовителя. Указанные праймеры обозначают как ZG44340 (SEQ ID NO: 58) и ZG44341 (SEQ ID NO: 59). ПЦР для генерирования zcyto21 C172S, содержащего мутацию по цистеину, проводят в соответствии с инструкциями к набору реагентов QuickChange Mutagenesis. Проводят пять идентичных реакций в объеме 50 мкл. В каждой реакции используют по 2,5 мкл pSDH175 ДНК (не содержит каркасную последовательность дрожжевого вектора) в качестве матрицы. ПЦР-коктейль готовят, используя следующие количества реагентов: 30 мкл 10х ПЦР-буфера, 125 нг (27,42 мкл) ZG44340, 125 нг (9,18 мкл) ZG44341, 6 мкл dNTP, 6 мкл полимеразы Pfu Turbo (Stratagene, Ла-Джойла, Калифорния) и 206,4 мкл воды. В каждой реакции используют аликвоту 47,5 мкл коктейля. Условия проведения ПЦР следующие: 1 цикл при 95°С в течение 30 сек, а затем 16 циклов при 95°С в течение 30 сек, 55°С в течение 1 мин, 68°С в течение 7 мин, затем 1 цикл при 68°С в течение 7 мин и окончание с отжигом при 4°С. Все пять реакционных ПЦР-смесей объединяют в одной пробирке. В соответствии с рекомендациями производителя, к реакционной ПЦР-смеси добавляют 5 мкл рестриктазы DpnI и инкубируют при 37°С в течение 2 час. ДНК осаждают добавлением 10% 3-молярного раствора ацетата натрия и два объема 100%-ного этанола. Осаждение проводят при -20°С в течение 20 мин. ДНК отделяют центрифугированием со скоростью 14000 об/мин в течение 5 мин и осадок ускоренно сушат в вакууме. Таблетку ДНК ресуспендируют в 20 мкл воды. ДНК, полученную по методу ПЦР, трансформируют в штамм E. coli DH10B. 5 мкл ДНК смешивают с 40 мкл клеток ElectroMAX DH10B (Invitrogen). Смесь клеток и ДНК затем электропорируют в кювете с расстоянием между электродами 0,1 см (Bio-Rad) с помощью Bio-Rad Gene Pulser II™ и следующими параметрами: 1,75 кВ, 100 Ом и 25 мкФ. Электропорированные клетки растят при 37°С в течение 1 час. Смесь помещают в чашку на среду LB + 25 мкг/мл канамицина и инкубируют в течение ночи при температуре 37°С. Проводят скрининг десяти клонов на наличие вставки zcyto21 C172S. ДНК извлекают изо всех десяти клонов с помощью набора QIAprep™ Spin Miniprep (Qiagen, Валенсия, Калифорния) и анализируют на наличие вставки путем разрезания ферментами рестрикции XbaI и PstI. Девять клонов, которые содержат вставки, секвенируют для подтверждения введения мутации zcyto21 C172S. Клон проверяют секвенированием и обозначают его как pSDH188.
Пример 8
Экспрессионная генетическая конструкция E. coli IL-29
Фрагмент ДНК IL-29, содержащий последовательность дикого типа, выделяют методом ПЦР. В реакции используют праймеры zc41212 (SEQ ID NO: 60), содержащие 41 пару оснований (п.о.) фланкирующей последовательности вектора, и 24 п.о., соответствующие аминовому концу IL-29, и праймер zc41041 (SEQ ID NO: 61), содержащий 38 п.о., который соответствует 3'-концу вектора, содержащего вставку zcyto21. Условия проведения ПЦР следующие: 25 циклов при 94°С в течение 30 сек, 50°С в течение 30 сек и 72°С в течение 1 мин; с последующим отжигом при 4°С. Небольшой образец (2-4 мкл) ПЦР-образца, с целью анализа, прогоняют на 1%-ном агарозном геле с буфером 1Х ТВЕ и обнаруживают ожидаемую полосу, соответствующую фрагменту размером приблизительно 500 п.о. Оставшийся объем реакционной смеси, составляющий 100 мкл, осаждают с помощью 200 мкл абсолютного этанола. Полученный осадок ресуспендируют в 10 мкл воды перед использованием для проведения рекомбинации в вектор реципиента рТАР238, разрезанный с помощью SmaI, с целью получения, как указано выше, генной конструкции, кодирующей zcyto21. Клон с корректной последовательностью обозначают как pTAP377. Клон pTAP377 расщепляют с помощью Not1/Nco1 (10 мкл ДНК, 5 мл буферной смеси 3 New England BioLabs, 2 мкл Not1, 2 мкл Nco1, 31 мкл воды в течение 1 час при 37°) и вновь лигируют Т4 ДНК-лигазой в буферной смеси (7 мкл продукта предыдущей реакции расщепления, 2 мкл 5Х буфера, 1 мкл Т4 ДНК-лигазы). На этой стадии удаляют дрожжевую последовательность, CEN-ARS, чтобы спрямить вектор. pTAP377 ДНК в диагностических целях расщепляют с помощью Pvu2 и Pst1, чтобы подтвердить отсутствие дрожжевой последовательности. ДНК pTAР377 трансформируют в штамм E. coli W3110/pRARE, штамм-хозяин, содержащий дополнительные копии редких генов тРНК E. coli.
Пример 9
Экспрессионная генетическая конструкция E. coli IL-28А
Фрагмент ДНК, содержащий последовательность дикого типа zcyto20 (как указано в SEQ ID NO: 1), выделяют методом ПЦР. В реакции используют праймеры zc43431 (SEQ ID NO: 62), содержащие 41 п.о. фланкирующей последовательности вектора, и 24 п.о., соответствующие аминовому концу zcyto20, и праймер zc43437 (SEQ ID NO: 63), содержащий 38 п.о., которые соответствуют 3'-концу вектора, содержащего вставку zcyto20. Условия проведения ПЦР следующие: 25 циклов при 94°С в течение 30 сек, 50°С в течение 30 сек и 72°С в течение 1 мин; с последующим ожигом при 4°С. Небольшой образец (2-4 мкл) ПЦР-образца, с целью анализа, прогоняют на 1%-ном агарозном геле с буфером 1Х ТВЕ и обнаруживают ожидаемую полосу, соответствующую фрагменту размером приблизительно 500 п.о. Оставшийся объем реакционной смеси, составляющий 100 мкл, осаждают с помощью 200 мкл абсолютного этанола. Полученный осадок ресуспендируют в 10 мкл воды перед использованием для проведения рекомбинации в вектор реципиента рТАР238, разрезанный с помощью SmaI, с целью получения генной конструкции, кодирующей zcyto20, как указано выше. Клон с корректной последовательностью обозначают как pYEL7. Его расщепляют с помощью Not1/Nco1 (10 мкл ДНК, 5 мкл буферной смеси 3 New England BioLabs, 2 мкл Not1, 2 мкл Nco1, 31 мкл воды в течение 1 час при 37°) и вновь лигируют Т4 ДНК-лигазой в буферной смеси (7 мкл продукта предыдущей реакции расщепления, 2 мкл 5Х буфера, 1 мкл Т4 ДНК-лигазы). На этой стадии удаляют дрожжевую последовательность, CEN-ARS, чтобы спрямить вектор. Идентифицированную ДНК pYEL7 в диагностических целях расщепляют с помощью Pvu2 и Pst1, чтобы подтвердить отсутствие дрожжевой последовательности. ДНК pYEL7 трансформируют в штамм E. coli W3110/pRARE.
Пример 10
Экспрессионная генетическая конструкция zcyto21 C172S, содержащая мутацию по цистеину
Стратегия, используемая для приготовления zcyto21 C172S, содержащего мутацию по цистеину (SEQ ID NO: 28), основана на использовании набора реагентов для проведения сайтнаправленного мутагенеза QuikChange® Site-Directed Mutagenesis (Stratagene, Ла-Джойла, Калифорния). Праймеры для внесения мутации С172S разрабатывают в соответствии с рекомендациями изготовителя. Указанные праймеры обозначают как ZG44327 и ZG44328 (SEQ ID NO: 64 и 65, соответственно). ПЦР для генерирования zcyto21 C172S, содержащего мутацию по цистеину, проводят в соответствии с инструкциями к набору реагентов QuikChange Mutagenesis. Проводят пять идентичных реакций в объеме 50 мкл. В каждой реакции используют по 2,5 мкл ДНК pТАР377 (не содержит каркасную последовательность дрожжевого вектора) в качестве матрицы. ПЦР-коктейль готовят, используя следующие количества реагентов: 30 мкл 10х ПЦР-буфера, 125 нг (27,42 мкл) ZG44327 (SEQ ID NO: 64), 125 нг (9,18 мкл) ZG44328 (SEQ ID NO: 65), 6 мкл dNTP, 6 мкл полимеразы Pfu Turbo (Stratagene) и 206,4 мкл воды. В каждой реакции используют аликвоту 47,5 мкл коктейля. Условия проведения ПЦР следующие: 1 цикл при 95°С в течение 30 сек, а затем 16 циклов при 95°С в течение 30 сек, 55°С в течение 1 мин, 68°С в течение 7 мин, затем 1 цикл при 68°С в течение 7 мин и окончание с ожигом при 4°С. Все пять реакционных ПЦР-смесей объединяют в одной пробирке. В соответствии с рекомендациями производителя, к реакционной ПЦР-смеси добавляют 5 мкл рестриктазы DpnI и инкубируют при 37°С в течение 2 час. ДНК осаждают добавлением 10% 3-молярного раствора ацетата натрия и два объема 100%-ного этанола (Aaper Alcohol, Шелбивиль, Кентукки). Осаждение проводят при -20°С в течение 20 мин. ДНК отделяют центрифугированием со скоростью 14000 об/мин в течение 5 мин и осадок ускоренно сушат в вакууме. Осадок ДНК ресуспендируют в 20 мкл воды. ДНК, полученную по методу ПЦР, трансформируют в штамм E. coli DH10B. 5 мкл ДНК смешивают с 40 мкл клеток ElectroMAX DH10B (Invitrogen, Карлсбад, Калифорния). Смесь клеток и ДНК затем электропорируют в кювете с расстоянием между электродами 0,1 см (Bio-Rad, Геркулес, Калифорния) с помощью Bio-Rad Gene Pulser II™ и следующими параметрами: 1,75 кВ, 100 Ом и 25 мкФ. Электропорированные клетки растят при 37°С в течение 1 час. Смесь помещают в чашку на среду LB + 25 мкг/мл канамицина и инкубируют в течение ночи при температуре 37°С. Проводят скрининг десяти клонов на наличие вставки IL-29. ДНК выделяют изо всех десяти клонов с помощью набора QIAprep™ Spin Miniprep (Qiagen) и анализируют на наличие вставки путем разрезания ферментами рестрикции XbaI (Roche) и PstI (New England Biolabs). Девять клонов, которые содержат вставки, секвенируют для подтверждения введения мутации zcyto21 C172S. Клон проверяют секвенированием и обозначают его как pSDH171. Аналогичную стратегию можно применить для генерирования мутанта zcyto21 C15S.
Пример 11
Экспрессионная генетическая конструкция zcyto20 C49S, содержащая мутацию по цистеину
Последовательность, которая кодирует zcyto20 C49S, содержащий мутацию по цистеину, генерируют методом ПЦР по праймерам с перекрывающимися последовательностями (SEQ ID NO: 20). Первые 187 оснований последовательности IL-28A дикого типа (SEQ ID NO: 1) генерируют ПЦР-амплификацией с использованием pYEL7 (SEQ ID NO: 67) в качестве матрицы и олигонуклеотидных праймеров zc43431 (SEQ ID NO: 62) и zc45399 (SEQ ID NO: 66). Второй фрагмент ДНК от основания 105 до основания 531 генерируют ПЦР-амплификацией с использованием pYEL7 (SEQ ID NO: 67) в качестве матрицы и олигонуклеотидных праймеров zc45398 (SEQ ID NO: 68) и zc43437 (SEQ ID NO: 63). Праймеры zc45399 (SEQ ID NO: 66) и zc45398 (SEQ ID NO: 68) содержат специфически модифицированную последовательность, которая заменяет цистеин 49 на серин. Два указанных продукта ПЦР объединяют и ПЦР перекрывание амплифицируют с помощью олигонуклеотидных праймеров zc43431 (SEQ ID NO: 62) и zc43437 (SEQ ID NO: 63). Конечный продукт ПЦР вставляют в экспрессирующий вектор pTAP238 методом гомологичной рекомбинации в дрожжевой системе (Raymond et al., Biotechniques. Jan. 26(1): 134-8, 140-1, 1999). Экспрессионную генетическую конструкцию экстрагируют из дрожжей и трансформируют в компетентные E. coli DH10B. Проводят отбор устойчивых к канамицину клонов методом ПЦР колоний. Положительный клон подтверждают секвенированием и затем трансформируют в продуцирующий штамм-хозяин W3110/pRARE. Экспрессионную генетическую конструкцию zcyto20 C49S, содержащую мутацию по цистеину, называют pCHAN9.
Пример 12
Экспрессионная генетическая конструкция zcyto20, содержащая мутацию по цистеину C51S
Последовательность, которая кодирует zcyto20, содержащий мутацию по цистеину C51S, генерируют методом ПЦР по праймерам с перекрывающимися последовательностями (SEQ ID NO: 24). Первые 193 оснований последовательности IL-28A дикого типа генерируют ПЦР-амплификацией с использованием pYEL7 (SEQ ID NO: 67) в качестве матрицы и олигонуклеотидных праймеров zc43431 (SEQ ID NO: 62) и zc45397 (SEQ ID NO: 63). Второй фрагмент ДНК от основания 111 до основания 531 генерируют ПЦР-амплификацией с использованием pYEL7 (SEQ ID NO: 67) в качестве матрицы и олигонуклеотидных праймеров zc45396 (SEQ ID NO: 70) и zc43437 (SEQ ID NO: 63). Праймеры zc45397 (SEQ ID NO: 69) и zc45396 (SEQ ID NO: 70) содержат специфически модифицированную последовательность, которая заменяет цистеин 51 на серин. Два указанных продукта ПЦР объединяют и ПЦР перекрывание амплифицируют с помощью олигонуклеотидных праймеров zc43431 (SEQ ID NO: 62) и zc43437 (SEQ ID NO: 63). Конечный продукт ПЦР вставляют в разработанный авторами экспрессирующий вектор pTAP238 методом гомологичной рекомбинации в дрожжевой системе (Raymond et al., выше). Экспрессионную генетическую конструкцию экстрагируют из дрожжей и трансформируют в компетентные E. coli DH10B. Проводят отбор устойчивых к канамицину клонов методом ПЦР колоний. Положительный клон подтверждают секвенированием и затем трансформируют в продуцирующий штамм-хозяин W3110/pRARE. Экспрессионную генетическую конструкцию zcyto20 C50S, содержащую мутацию по цистеину, называют pCHAN10.
Пример 13
Экспрессия IL-28A, IL-29 и мутантных по цистеину E. coli, содержащих замены цистеина на серин
В отдельных экспериментах E. coli, трансформированные каждым из экспрессирующих векторов, описанных в Примерах 6-9, высевают в 100 мл питательной среды Superbroth II (Becton Dickinson, Сан-Диего, Калифорния) с 0,01% Antifoam 289 (Sigma Aldrich, Сент-Луис, Миссури), 30 мкг/мл канамицина, 35 мкг/мл хлорамфеникола и растят в течение ночи при 37°С. 5 мл посевного материала вносят в 500 мл той же самой среды, помещенной в колбу для выращивания емкостью 2 л, и встряхивают со скоростью 250 об/мин при 37°С до тех пор, пока оптическая плотность OD600 культуры не достигнет значения 4. Затем добавляют IPTG до конечной концентрации 1 мМ и встряхивание продолжают еще в течение 2,5 час. Клетки центрифугируют с ускорением 4000 x g в течение 10 мин при температуре 4°С. Осадок клеток замораживают при -80°С и хранят вплоть до дальнейшего использования.
Пример 14
Восстановление складчатой структуры и очистка IL-28
А. Приготовление телец включения
Человеческий IL-29 дикого типа, как указано выше, экспрессируется в штамме E. coli W3110 в виде телец включения. Биомассу бактерий, полученных непрерывной ферментацией с подпиткой, ресуспендируют в 50 мМ растворе Трис с рН 7,3. Суспензию трижды пропускают через гомогенизатор APV-Gaulin (Invensys APV, Тонаванда, Нью-Йорк) под давлением 8000 фунтов на квадратный дюйм. Нерастворимые вещества отделяют центрифугированием с ускорением 15000 g в течение 30 мин. Таблетку последовательно промывают 50 мМ Трис, 1% (об./об.) Triton X100 с рН 7,3 и 4 М раствором мочевины. Затем тельца включения диспергируют в 50 мМ Трис, 6 М гидрохлорида гуанидина, 5 мМ DTT при комнатной температуре в течение 1 час. После этого образец центрифугируют с ускорением 15000 g в течение 1 час. Жидкость над осадком, полученная на этой стадии, содержит восстановленный растворимый IL-29.
В. Восстановление складчатой структуры
Солюбилизованный IL-29 медленно при перемешивании разводят раствором 50 мМ Трис, с рН 8, 0,75 М аргинина, 0,05% PEG3350, 2 мМ MgCl2, 2 мМ CaCl2, 0,4 мМ KCl, 10 мМ NaCl, 4 мМ восстановленного глутатиона, 0,8 мМ окисленного глутатиона при комнатной температуре. Конечная концентрация IL-29 в восстанавливающей складчатую структуру буферной смеси составляет 0,1 мг/мл. Смесь для восстановления складчатой структуры оставляют на ночь при комнатной температуре. Для регулирования рН суспензии до величины 5 используют концентрированную уксусную кислоту. Затем суспензию отфильтровывают через фильтр с размерами пор 0,2 мкм. Анализ смеси для восстановления складчатой структуры методом ВЭЖХ с обращенной фазой показывает два пика.
С. Очистка
Смесь для восстановления складчатой структуры разбавляют (1:2) в протоке с помощью 50 мМ NaOAc с рН 5 и помещают на катионообменную колонку Pharmacia SP Sepharose Fast Flow (North Peapack, Нью-Джерси). Колонку промывают раствором 50 мМ NaOAc, 400 мМ NaCl с рН 5 в количестве 3 объема колонки. Связанный IL-29 элюируют раствором 50 мМ NaOAc, 1,4 М NaCl с рН 5. К объеденному пулу фракций, полученных элюированием на стадии с использованием катионообменной колонки, добавляют твердый (NH4)2SO4 до тех пор, пока конечная концентрация (NH4)2SO4 не составит 0,5 М. После этого вещество помещают на колонку ToyoPearl Phenyl 650S HIC (Tosoh Biosep, Монтгомеривиль, Пенсильвания). Затем колонку промывают тремя ее объемами раствором 50 мМ NaOAc, 1 М (NH4)2SO4 с рН 5. Линейный градиент в количестве 10 объемов колонки от 50 мМ NaOAc, 1 М (NH4)2SO4 с рН 5 до 50 мМ NaOAc с рН 5 используют для элюирования связанного zcyto21. Полученные элюированием фракции объединяют. На этой стадии наблюдают два пика. Проводят анализ элюированных фракций методом ВЭЖХ с обращенной фазой. После конечной замены буферирующего раствора на PBS получают два продукта, соответствующие двум изомерам относительно дисульфидной связи.
Пример 15
Восстановление складчатой структуры и очистка мутантного IL-29, содержащего замены цистеина
Как указано в Примере 3, очистка полученного IL-29 дает два изомера относительно дисульфидной связи. Для разделения указанных двух форм проводят стадию HIC FPLC. Разделение форм не удается полностью разрешить относительно базовой линии. Чтобы получить существенно очищенные изомеры (> 95%), необходимо провести значительную “обрезку пика”. Выход на этой стадии невелик и снижает сквозной выход всего процесса. Конечные выходы составляют 8% и 9% для формы С15-С112 и С12-С171, соответственно. IL-29 дикого типа, полученный из систем СНО и бакуловируса (BV), обладает аналогичными свойствами. Было установлено, что форма С15-С112 изомера гомологична по структуре дисульфидной связи интерферонам типа I. Кроме того, при проведении анализа ISRE (см. ниже) было установлено, что форма С15-С112 показывает в 30 раз большую биологическую активность, чем форма С112-С171.
Восстановление складчатой структуры и очистка мутеина zcyto21 Cys172Ser
Получение телец включения, восстановление складчатой структуры и очистку полипептида zcyto21 C172S (SEQ ID NO: 29) осуществляют аналогично тому, как указано для IL-29 дикого типа (SEQ ID NO: 4). ВЭЖХ с обращенной фазой смеси для восстановления складчатой структуры мутеина показывает только один заметный пик, соответствующий форме С15-С112 IL-29 дикого типа. Последующая хроматография с гидрофобными взаимодействиями показывает только один пик. Поэтому нет необходимости проводить значительную “обрезку пика”. Общий выход для всего способа близок к 50%. В анализе ISRE, приведенном в Примере 16, полипептид zcyto21 Cys172Ser (SEQ ID NO: 29) показывает биологическую активность, эквивалентную форме С15-С112 IL-29 дикого типа.
Пример 16
Антивирусная активность: эффект в клетках Hela и L929
Первичный функциональный анализ антивирусной активности проводят с использованием кондиционированной среды из временно трансфицированных клеток эмбриональной почки человека (НЕК). Полноразмерную кДНК для человеческих или мышиных IL-28А, IL-28В или IL-29 стандартными методами клонируют в вектор pzp7Z. Генные конструкции человеческих или мышиных IL-28А, IL-28В или IL-29 трансфицируют в клетки 293 НЕК. Если кратко, для каждой конструкции 700000 клеток на лунку (на 6-луночном планшете) помещают за 18 час до трансфекции на планшет с 2 мл DMEM + 10% фетальной телячьей сыворотки. Для каждой лунки 1,5 мкг человеческого или мышиного IL-28А, IL-28В или IL-29 ДНК и 0,5 мкг ДНК pIRES2-EGFP (Clontech) добавляют к 6 мкл реагента Fugene 6 (Roche Biochemicals) в общем объеме 100 мкл DMEM. 2 мкг индивидуальной ДНК pIRES2-EGFP используют в качестве негативного контроля. Указанные смеси для трансфекции по прошествии 30 мин добавляют к предварительно нанесенным на планшет клеткам 293. По прошествии 24 час клеточную среду удаляют и добавляют DMEM + 0,1% бычьего сывороточного альбумина. Кондиционированную среду собирают через 48 час, фильтруют через фильтр с размерами пор 0,45 мкм и используют в антивирусном и репортерном анализах.
Антивирусные анализы проводят с использованием клеток цервикальной карциномы человека (HeLa) и клеток фибробластов мыши (L929). В первый день кондиционированную среду, содержащую человеческий или мышиный IL-28А, IL-28В или IL-29, разбавляют и помещают вместе с 50000 клеток на 96-луночный планшет с плоским дном для микротитрования. После 24 час инкубирования при 37°С питательную среду удаляют и заменяют средой, содержащей вирус энцефаломиокардита с индексом множественности инфекции 0,1. Клетки вновь инкубируют в течение 24 час при 37°С. Лунки с культурой затем оценивают визуально по 4-балльной шкале на наличие цитопатического эффекта (СРЕ), который затем выражают в виде % СРЕ, как показано в Таблице 7. В качестве контролей включают кондиционированную среду из клеток, трансфицированных лишь с помощью GFP, и очищенный интерферон-а-2а человека или мышиный интерферон-альфа.
Определение цитопатического эффекта
В Таблице 8 показано, что кондиционированная среда, содержащая человеческий или мышиный IL-28А, IL-28В или IL-29, в зависимости от дозы подавляет вирусную инфекцию (% СРЕ) в клетках HeLa, в то время как контрольная кондиционированная среда GFP не способна в заметной степени блокировать проявление цитопатического эффекта. Как показано в Таблице 9, кондиционированная среда, содержащая человеческий или мышиный IL-28А, IL-28В или IL-29, не подавляет вирусную инфекцию в клетках L929. В обоих экспериментах очищенный интерферон показывает позитивную антивирусную активность.
Процент цитопатического эффекта человеческого или мышиного IL-28А, IL-28В или IL-29 в клетках HeLa с использованием кондиционированной среды (СМ, КС)
Процент цитопатического эффекта человеческого или мышиного IL-28А, IL-28В или IL-29 в клетках L929 с использованием кондиционированной среды (КС)
Пример 17
Передача сигнала по вызываемому интерфероном каскаду ответных реакций
Взаимодействие интерферонов типа 1 с их специфическим рецептором приводит к индукции ряда генов, ответственных за их антивирусную/антипролиферативную активность. Они включают 2'-5'-олигоаденилатсинтазу (2-5 OAS), зависимую от двунитевой ДНК Pkr-киназу (Pkr), фосфолипидскрамблазу и молекулу межклеточной адгезии-1 (ICAM-1). Также наблюдается индукция генов с еще неизвестными функциями, таких как активированный интерфероном генный продукт размером 56 кДа (ISG-56k). С целью определения того, индуцируются ли некоторые или все из указанных генов при обработке клеток с помощью IL-28A, человеческие лимфоидные клетки Дауди B обрабатывают в течение 72 час кондиционированной средой из клеток Sf9, инфицированных бакуловирусом, экспрессирующим IL-28A. В качестве негативного контроля используют кондиционированную среду из клеток Sf9, инфицированных бакуловирусом дикого типа. После обработки клетки собирают и подвергают лизингу, с целью выделения полной РНК. Один микрограмм полной РНК превращают в кДНК с помощью обратной транскриптазы и используют в качестве матрицы в ПЦР вместе с примерами, специфичными для активированных интерфероном человека генов, которые приведены выше. Олигонуклеотидные праймеры для глицерол-3-фосфатдегидрогеназы (G3PDH) человека используют в качестве не интерфероном активированных контрольных генов. Результаты показывают явную индукцию ISG-56k, Pkr, 2-5 OAS и фосфолипидстрамблазы после обработки клеток с помощью IL-28A. Никакой индукции не наблюдается для ICAM-1 или не интерфероном активированного генного контроля, G3PDH.
Пример 18
Репортерный анализ трансдукции сигнала
Репортерный анализ трансдукции сигнала может быть использован для установления функционального взаимодействия человеческого или мышиного IL-28 или IL-29 с рецептором IL-28. Клетки эмбриональной почки человека (НЕК) трансфицируют репортерной плазмидой, содержащей индуцированный интерфероном элемент ответа (ISRE), который вызывает транскрипцию репортерного гена люциферазы в присутствии или в отсутствие экспрессирующих векторов pZP7, содержащих кДНК для рецепторов цитокинов класса II (в том числе DIRS1, IFNαR1, IFNαR2 и рецептор IL-28). Активность люциферазы после активации трансфицированных клеток по отношению к лигандам класса II (включая IL-28А (SEQ ID NO: 2), IL-29 (SEQ ID NO: 4), IL-28В (SEQ ID NO: 6), zcyto10, huIL10 и huIFNa-2a) отражает взаимодействие лиганда с трансфицированными и нативными цитокиновыми рецепторами на поверхности клеток. Результаты и методики приводятся ниже.
Трансфекция клеток
Клетки 293 НЕК трансфицируют следующим образом: 700000 клеток 293 на лунку (на 6-луночном планшете) помещают за 18 час до трансфекции на планшет с 2 мл DMEM + 10% фетальной телячьей сыворотки. Для каждой лунки 1 мкг ДНК pISRE-люцифераза (Stratagene), 1 мкг ДНК цитокинового рецептора и 1 мкг ДНК pIRES2-EGFP (Clontech) добавляют к 9 мкл реагента Fugene 6 (Roche Biochemicals) в общем объеме 100 мкл DMEM. В том случае, если не используют ДНК цитокинового рецептора, то добавляют 2 мкг ДНК pIRES2-EGFP. Указанную смесь для трансфекции по прошествии 30 мин добавляют к предварительно нанесенным на планшет клеткам 293. По прошествии 24 час трансфицированные клетки удаляют с планшета с помощью смеси трипсин-ЭДТК и повторно наносят в количестве приблизительно 25000 клеток на лунку на 96 луночный планшет для микротитрования. Приблизительно за 18 час до активации лигандом среду меняют на DMEM + 0,5% фетальной телячьей сыворотки (FBS).
Репортерные анализы трансдукции сигнала
Репортерные анализы трансдукции сигнала проводят следующим образом: после инкубации в течение 18 час при 37°С в питательной среде DMEM + 0,5% FBS трансфицированные клетки активируют разбавлениями (в питательной среде DMEM + 0,5% FBS) следующих лигандов класса II; IL-28А, IL-29, IL-28В, zcyto10, huIL10 и huIFNa-2a. После 4-часового инкубирования при 37°С клетки подвергают лизису и после добавления субстрата люциферазы измеряют относительные световые единицы (RLU) с помощью люминометра. Полученные результаты представлены в виде кратности индуцирования RLU в экспериментальных образцах по отношению только к контрольной среде (RLU экспериментальных образцов/RLU контрольной среды = кратность индуцирования). Таблица 10 показывает, что IL-28А, IL-29 и IL-28В активируют передачу сигнала ISRE в клетках 293, трансфицированных ISRE-люциферазой, и дают от 15- до 17-кратное усиление активности люциферазы по сравнению с одной лишь питательной средой. Введение ДНК альфа-субъединицы рецептора IL-28 (SEQ ID NO: 11) в смесь для трансфекции с помощью эндогенного CRF2-4 (SEQ ID NO: 71) приводит к дальнейшему от 6- до 8-кратному усилению трансдукции сигнала ISRE под действием IL-28А, IL-29 и IL-28В, что дает общую активацию в интервале от 104 до 125 раз. Ни один из других трансфицированных ДНК рецепторов цитокинов класса II не приводит к усилению передачи сигнала ISRE. Полученные результаты указывают на то, что IL-28А, IL-29 и IL-28В функционально взаимодействуют с рецептором цитокина IL-28. Таблица 10 показывает также, что huIFNa-2a способен активировать передачу сигнала в трансфицированных ISRE-люциферазой клетках 293 и приводит к 205-кратному усилению активности люциферазы по сравнению с одной лишь питательной средой. Тем не менее, добавление ДНК рецептора IL-28 к трансфекциям приводит к 11-кратному снижению передачи сигнала ISRE (по сравнению с действием только ДНК ISRE-люциферазы), что позволяет сделать вывод о том, что сверхпродукция рецептора IL-28 оказывает отрицательное воздействие на передачу сигнала интерферона, в отличие от положительных эффектов, которые сверхпродукция рецептора IL-28 оказывает на передачу сигнала IL-28А, IL-29 и IL-28В.
Стимулированный интерфероном элемент ответа (ISRE) передачи сигнала трансфицированных клеток 293 после активации цитокином класса II (кратность активации)
Пример 19
Анализы трансдукции сигнала мутантным IL-29, содержащим замены цистеина
Трансфекция клеток
Для получения клеток 293 НЕК, в которых возможна устойчивая сверхпродукция рецептора IL-28, клетки 293 трансфицируют следующим образом: 300000 клеток 293 на лунку (на 6-луночном планшете) помещают за 6 час до трансфекции на планшет с 2 мл DMEM + 10% фетальной телячьей сыворотки. Для каждой лунки 2 мкг экспрессирующего вектора pZP7, содержащего ДНК альфа-субъединицы рецептора IL-28 человека (SEQ ID NO: 11), добавляют к 6 мкл реагента Fugene 6 (Roche Biochemicals) в общем объеме 100 мкл DMEM. Указанную смесь для трансфекции по прошествии 30 мин добавляют к предварительно нанесенным на планшет клеткам 293. По прошествии 48 час трансфицированные клетки подвергают селекции с использованием 2 мкг/мл пуромицина. Клетки, устойчивые к пуромицину, получают в виде популяции клеток.
Клетки 293 НЕК, избыточно продуцирующие рецептор IL-28 человека, трансфицируют следующим образом: 700000 клеток 293 на лунку (на 6-луночном планшете) помещают за 18 час до трансфекции на планшет с 2 мл DMEM + 10% фетальной телячьей сыворотки. Для каждой лунки 1 мкг KZ157, содержащей индуцированный интерфероном элемент ответа (ISRE), который вызывает транскрипцию репортерного гена люциферазы, добавляют к 3 мкл реагента Fugene 6 (Roche Biochemicals) в общем объеме 100 мкл DMEM. Указанную смесь для трансфекции по прошествии 30 мин добавляют к предварительно нанесенным на планшет клеткам 293 НЕК. По прошествии 48 час трансфицированные клетки удаляют с планшета с помощью трипсина-ЭДТК и вновь наносят вместе с раствором 500 мкг/мл G418 (Geneticin, Life Technologies). Клетки, устойчивые к пуромицину и G418, выделяют в виде популяции клеток.
Репортерные анализы трансдукции сигнала
Репортерные анализы трансдукции сигнала проводят следующим образом: клетки 293 НЕК, избыточно продуцирующие рецептор IL-28 человека и содержащие KZ157, обрабатывают трипсином-ЭДТК и вновь наносят в количестве приблизительно 25000 клеток на лунку на 96-луночные планшеты. Приблизительно после 18 час активации среду меняют на питательную среду DMED + 0,5% FBS.
Через 18 час инкубации при 37°С в питательной среде DMED + 0,5% FBS трансфицированные клетки активируют разбавлениями (в среде DMED + 0,5% FBS) различных форм zcyto21, полученного из E. coli, который включает различные типы связывания цистеина. Через 4 час инкубирования при 37°С клетки подвергают лизису и после добавления субстрата люциферазы измеряют относительные световые единицы (RLU) с помощью люминометра. Полученные результаты представлены в виде кратности индуцирования RLU в экспериментальных образцах по отношению только к контрольной среде (RLU экспериментальных образцов/RLU контрольной среды = кратность индуцирования).
Таблица 11 показывает, что форма С1-С3 (С16-С113) IL-29, полученного из E. coli дикого типа, обладает большей способностью индуцировать передачу сигнала ISRE, чем форма С3-С5 дикого типа (С113-С172) или смесь формы С1-С3 дикого типа и формы С3-С5 (С16-С113, С113-С172), которые все относятся к SEQ ID NO: 15.
Таблица 12 показывает, что форма С1-С3 (С16-С113) IL-29, полученного из E. coli дикого типа, и С1-С3 (С16-С113; SEQ ID NO: 15) содержащего мутацию по цистеину (C172S) IL-29 (SEQ ID NO: 29), полученного из E. coli, одинаково способны индуцировать передачу сигнала ISRE в клетках 293 НЕК, избыточно продуцирующих рецептор IL-28 человека.
Передача сигнала ISRE различными формами IL-29, полученного из E. coli (кратность активации)
Передача сигнала ISRE различными формами IL-29, полученного из E. coli (кратность активации)
Пример 20
Активация IL-28А, IL-29 и IL-28В под действием поли I:C и вирусной инфекции
Свежевыделенные мононуклеарные клетки периферической крови человека выращивают в присутствии полиинозиновой кислоты - полицитидиловой кислоты (поли I:C; 100 мкг/мл) (Sigma, Сент-Луис, Миссури), вируса энцефаломиокардита (EMCV) с величиной MOI, равной 0,1, или только в питательной среде. Через 15 час инкубирования полную РНК выделяют из клеток и обрабатывают ДНКазой, не содержащей РНКазу. 100 нг полной РНК используют в качестве матрицы в одностадийном методе RT-PCR вместе с Superscript One-Step RT-PCR, набором реагентов Platinum Taq и генспецифичными праймерами в соответствии с рекомендациями производителя (Invitrogen).
В необработанных клетках наблюдаются низкие, вплоть до значений ниже предела обнаружения, количества IL-28А, IL-28В и IL-29, РНК IFN-α и IFN-β. Напротив, количества РНК IL-28А, IL-29 и IL-28В увеличиваются как при обработке с помощью поли I:C, так и под действием вирусной инфекции, что наблюдается и для интерферонов типа I. Эти эксперименты показывают, что IL-28А, IL-28В и IL-29, как и интерфероны типа I, могут быть активированы двунитевой РНК или вирусной инфекцией.
Пример 21
Активность передачи сигнала для IL-28, IL-29 в сравнении с IFNα в клетках HepG2
А. Трансфекция клеток
Клетки HepG2 трансфицируют следующим образом: 700000 клеток HepG2 на лунку (на 6-луночном планшете) помещают за 18 час до трансфекции на планшет с 2 мл DMEM + 10% фетальной телячьей сыворотки. Для каждой лунки 1 мкг ДНК pISRE-люцифераза (Stratagene) и 1 мкг ДНК pIRES2-EGFP (Clontech) добавляют к 6 мкл реагента Fugene 6 (Roche Biochemicals) в общем объеме 100 мкл DMEM. Указанную смесь для трансфекции по прошествии 30 мин добавляют к предварительно нанесенным на планшет клеткам HepG2. Через 24 час трансфицированные клетки удаляют с планшета с помощью смеси трипсин-ЭДТК и повторно наносят в количестве приблизительно 25000 клеток на лунку на 96 луночные планшеты для микротитрования. Приблизительно за 18 час до активации лигандом среду меняют на DMEM + 0,5% FBS.
В. Репортерные анализы трансдукции сигнала
Репортерные анализы трансдукции сигнала проводят следующим образом: после инкубации в течение 18 час при 37°С в питательной среде DMEM + 0,5% FBS трансфицированные клетки активируют 100 нг/мл лигандов IL-28А, IL-29, IL-28В, zcyto24, zcyto25 и huIFN-α2a. После 4-часового инкубирования при 37°С клетки подвергают лизису и после добавления субстрата люциферазы измеряют относительные световые единицы (RLU) с помощью люминометра. Полученные результаты представлены в виде кратности активации RLU в экспериментальных образцах по отношению только к контрольной среде (RLU экспериментальных образцов/RLU контрольной среды = кратность индуцирования). Таблица 13 показывает, что IL-28А, IL-29, IL-28В, zcyto24 и zcyto25 активируют передачу сигнала ISRE в клетках HepG2 печени человека, трансфицированных ISRE-люциферазой.
Кратность активации зависимой от цитокина передачи сигнала ISRE
Пример 22
Антивирусная активность IL-29 в сравнении с IFNα в клетках HepG2
Антивирусные анализы адаптируют для EMCV (Американская коллекция типовых культур #VR-129B, Манассас, Виргиния) с клетками человека (Familletti, P. et al., Methods Enzym. 78: 387-394, 1981). Клетки вместе с цитокином помещают в чашку и инкубируют в течение 24 час перед тем, как ввести провокационную пробу EMCV с показателем множественности инфекции в интервале от 0,1 до 1. Клетки анализируют на жизнеспособность с помощью биоанализов на захват красителей через 24 час после инфицирования (Berg, K. et al., Apmis 98: 156-162, 1990). Клетки-мишени обрабатывают с помощью МТТ и инкубируют при 37°С в течение 2 час. Добавляют раствор солюбилизатора, инкубируют в течение ночи при 37°С и определяют оптическую плотность при 570 нм. Значение OD570 прямо пропорционально антивирусной активности.
Полученные результаты показывают антивирусную активность в том случае, когда IL-29 и IFN тестируют вместе с клетками HepG2: IL-29, IFN-β и IFNα-2а добавляют с различными концентрациями к клеткам HepG2 перед инфекцией EMCV и проведением анализа на захват красителя. Среднее значение и стандартное отклонение значения OD570 по трем ячейкам наносят на график. Величины OD570 пропорциональны антивирусной активности. Для IL-29 значение ЕС50 составляет 0,60 нг/мл; для IFNα-2а значение ЕС50 составляет 0,57 нг/мл; а для IFN-β значение ЕС50 составляет 0,46 нг/мл.
Пример 23
Экспрессия мРНК IL-28RA в печени и субпопуляции лимфоцитов
С целью дальнейшего изучения распределения мРНК для IL-28RA, проводят полуколичественный RT-PCR с использованием системы SDS 7900HT (Applied Biosystems, Калифорния). Одностадийный RT-PCR осуществляют, используя 100 нг полной РНК для каждого образца и генспецифичные праймеры. Для каждого набора праймеров с помощью РНК Bjab получают стандартную кривую и полученные для всех образцов значения нормируют относительно HPRT. Нормированные данные собраны в Таблицах 14-17. Приведены также нормированные данные для IFNAR2 и CRF2-4.
Таблица 14: В- и Т-клетки экспрессируют значительные количества мРНК IL-28RA. Низкие значения наблюдаются в дендритных клетках и в большинстве моноцитов.
Как видно из Таблицы 15, нормальные ткани печени и полученные из печени клеточные линии показывают значительные уровни мРНК IL-28RA и CRF2-4.
Как видно из Таблицы 16, основные эпителиальные клетки дыхательных путей содержат повышенные уровни IL-28RA и CRF2-4.
Как видно из Таблицы 17, IL-28RA присутствует в нормальных и больных образцах печени, при этом экспрессия повышена в образцах, инфицированных гепатитом С и гепатитом В.
Как показано в Таблицах 18-22, IL-28RA обнаруживается в нормальных В-клетках, В-клетках клеточной линии лимфомы, Т-клетках, Т-клетках клеточной линии лимфомы (клетках Jurkat), нормальных и трансформированных лимфоцитах (В-клетках и Т-клетках) и нормальных моноцитах человека.
средн.
средн.
норм.
норм.
норм.
станд. отклон.
станд. отклон.
Hprt
IFNAR2
IL-28RA
CRF
норм.
норм.
норм.
станд. откл.
станд. откл.
станд. откл.
станд. откл.
станд. откл.
станд. откл.
станд. откл.
Пример 24
Мышиный IL-28 не оказывает влияние на пролиферацию клеток Дауди
Человеческие клетки Дауди суспендируют в питательной среде RPMI + 10% FBS в количестве 50000 клеток/мл и 5000 клеток на лунку помещают на 96-луночный планшет. В каждую лунку добавляют IL-29-CEE (IL-29, конъюгированный с меткой glu), IFN-γ или IFN-α2а добавляют сериями с 2-кратным разведением. IL-29-CEE используют в диапазоне концентраций от 1000 нг/мл до 0,5 нг/мл. IFN-γ используют в диапазоне концентраций от 125 нг/мл до 0,06 нг/мл. IFN-α2а используют в диапазоне концентраций от 62 нг/мл до 0,03 нг/мл. Клетки инкубируют 72 час при температуре 37°С. Через 72 час добавляют Alamar Blue (Accumed, Чикаго, Иллинойс) в количестве 20 мкл на лунку. Планшеты дополнительно инкубируют в течение 24 час при 37°С в атмосфере 5% СО. Планшеты считывают на планшет-ридере Fmax™ (Molecular Devices, Саннивейл, Калифорния) с использованием программы SoftMax™ Pro на длине волны 544 (возбуждение) и 590 (излучение). Alamar Blue дает флуорометрический отклик в соответствии с метаболической активностью клеток и, таким образом, позволяет провести прямое измерение пролиферации клеток в сравнении с негативным контролем. Результаты показывают, что IL-29-CEE, в отличие от IFN-α2а, не оказывает заметного действия на пролиферацию клеток Дауди.
Пример 25
Мышиный IL-28 не оказывает антипролиферативного действия на мышиные В-клетки
Мышиные В-клетки выделяют из селезенки мышей 2 Balb/C (в возрасте 7 месяцев) элиминацией клеток CD43+ с помощью магнитных бусинок MACS. Очищенные В-клетки выращивают in vitro в присутствии LPS, моноклональных антител против IgM или против CD40. В культуры добавляют мышиный IL-28 или мышиный IFNα, через 48 час добавляют 3Н-тимидин и включение 3Н-тимидина в клетки измеряют через 72 час.
IFNα в концентрации 10 нг/мл ингибирует включение 3Н-тимидина мышиными В-клетками, активированными либо с помощью LPS, либо антителом против IgM. Однако мышиный IL-28 при любой из протестированных концентраций, вплоть до 1000 нг/мл, не ингибирует включение 3Н-тимидина. Напротив, как mIFNα, так и мышиный IL-28 повышают включение 3Н-тимидина мышиными В-клетками, активированными моноклональным антителом против CD40.
Полученные данные показывают, что мышиный IL-28, в отличие от IFNα, не проявляет антипролиферативную активность даже при высоких концентрациях. Кроме того, zcyto24 усиливает пролиферацию в присутствии моноклональных антител против CD40. Результаты показывают, что мышиный IL-28 отличается от IFNα тем, что мышиный IL-28 не проявляет антипролиферативную активность по отношению к В-клеткам даже при высоких концентрациях. Кроме того, мышиный IL-28 усиливает пролиферацию в присутствии моноклональных антител против CD40.
Пример 26
Размножение костного мозга
Здоровым мононуклеарным клеткам костного мозга (Poietic Technologies, Гетерсберг, Мэриленд) дают в течение 2 час прилипнуть к полимерной подложке в питательной среде αMEM, 10% FВS, 50 мМ β-меркаптоэтанола, 2 нг/мл FLT3L при температуре 37°С. Не прилипшие клетки затем переносят на планшеты (96-луночные планшеты для культивирования тканей) в количестве от 25000 до 45000 на лунку в питательной среде αMEM, 10% FВS, 50 мМ β-меркаптоэтанола, 2 нг/мл FLT3L в присутствии или в отсутствие 1000 нг/мл IL-29-CEE, 100 нг/мл IL-29-CEE, 10 нг/мл IL-29-CEE, 100 нг/мл IFN-α2а, 10 нг/мл IFN-α2а или 1 нг/мл IFN-α2а. Указанные клетки инкубируют с различными цитокинами, с целью изучения размножения или дифференцировки кроветворных клеток костного мозга (20 нг/мл IL-2, 2 нг/мл IL-3, 20 нг/мл IL-4, 20 нг/мл IL-5, 20 нг/мл IL-7, 20 нг/мл IL-10, 20 нг/мл IL-12, 20 нг/мл IL-15, 10 нг/мл IL-21 или без добавления цитокина). По прошествии от 8 до 12 дней добавляют Alamar Blue (Accumed, Чикаго, Иллинойс) в количестве 20 мкл на лунку. Планшеты дополнительно инкубируют в течение 24 час при 37°С в атмосфере 5% СО. Планшеты считывают на планшет-ридере Fmax™ (Molecular Devices, Саннивейл, Калифорния) при использовании программы SoftMax™ Pro на длине волны 544 (возбуждение) и 590 (испускание). Alamar Blue дает флуорометрический отклик в соответствии с метаболической активностью клеток и, таким образом, позволяет провести прямое измерение пролиферации клеток в сравнении с негативным контролем.
IFN-α2а вызывает значительное угнетающее действие на рост костного мозга при всех исследованных условиях. Напротив, IL-29 не оказывает значительного действия на размножение клеток костного мозга в присутствии IL-3, IL-4, IL-5, IL-7, IL-10, IL-12, IL-21 или без добавления цитокина. Небольшое угнетающее действие на рост костного мозга наблюдается в присутствии IL-2 и IL-15.
Пример 27
Ингибирование трансдукции сигнала IL-28 или IL-29 растворимым рецептором (zcytoR19/CFR2-4)
А. Репортерный анализ трансдукции сигнала
Репортерные анализы трансдукции сигнала может быть использован для выявления ингибирующих свойств гомодимерного zcytor19-Fc4 и гетеродимерного zcytor19-Fc/CRF2-4-Fc растворимых рецепторов на передачу сигнала zcyto20, zcyto21 и zcyto24. Клетки почки эмбриона человека (НЕК), избыточно продуцирующие рецептор zcytor19, трансфицируют репортерной плазмидой, содержащей индуцированный интерфероном элемент ответа (ISRE), который вызывает транскрипцию репортерного гена люциферазы. Активность люциферазы после активации трансфицированных клетками под действием лигандов (включая zcyto20 (SEQ ID NO: 2), zcyto21 (SEQ ID NO: 4), zcyto24 (SEQ ID NO: 8)) отражает взаимодействие лиганда с растворимым рецептором.
В. Трансфекция клеток
Клетки 293 НЕК, избыточно продуцирующие zcytor19, трансфицируют следующим образом: 700000 клеток 293 на лунку (на 6-луночном планшете) помещают за 18 час до трансфекции на планшет с 2 мл DMEM + 10% фетальной телячьей сыворотки. Для каждой лунки 1 мкг ДНК pISRE-люцифераза (Stratagene) и 1 мкг ДНК pIRES2-EGFP (Clontech) добавляют к 6 мкл реагента Fugene 6 (Roche Biochemicals) в общем объеме 100 мкл DMEM. Указанную смесь для трансфекции по прошествии 30 мин добавляют к предварительно нанесенным на планшет клеткам 293. По прошествии 24 час трансфицированные клетки удаляют с планшета с помощью смеси трипсин-ЭДТК и повторно наносят в количестве приблизительно 25000 клеток на лунку на 96 луночные планшеты для микротитрования. Приблизительно за 18 час до активации лигандом среду меняют на DMEM + 0,5% FBS.
С. Репортерные анализы трансдукции сигнала
Репортерные анализы трансдукции сигнала проводят следующим образом: после инкубации в течение 18 час при 37°С в питательной среде DMEM + 0,5% FBS трансфицированные клетки активируют с помощью 10 нг/мл zcyto20, zcyto21 или zcyto24 и 10 мкг/мл следующих растворимых рецепторов: гомодимерный zcyto19-Fc человека, гетеродимерный zcyto19-Fc человека/CRF2-4-Fc человека; гомодимерный CRF2-4-Fc человека; гомодимерный мышиный zcyto19-Ig. После 4-часового инкубирования при 37°С клетки подвергают лизису и после добавления субстрата люциферазы измеряют относительные световые единицы (RLU) с помощью люминометра. Полученные результаты представляют в виде процента ингибирования активированной лигандом передачи сигнала в присутствии растворимого рецептора, по сравнению с передачей сигнала в присутствии только PBS. Таблица 23 показывает, что гетеродимерный растворимый рецептор zcyto19-Fc человека/CRF2-4 человека способен в диапазоне от 16 до 45% ингибировать индуцируемую zcyto20, zcyto21 и zcyto24 передачу сигнала, по сравнению с контролем. Гомодимерный растворимый рецептор zcyto19-Fc человека также способен на 45% ингибировать индуцируемую zcyto21 передачу сигнала. Никаких заметных эффектов не обнаружено для гомодимерных растворимых рецепторов huCRF2-4-Fc или muzcytor19-Ig.
Процент ингибирования активированной лигандом передачи сигнала элементом ответа, индуцированного интерфероном (ISRE), под действием растворимых рецепторов
Пример 28
IL-28 и IL-29 ингибируют репликацию ВИЧ в здоровых PBMCs человека
Вирус иммунодефицита человека (ВИЧ) является патогенным ретровирусом, который инфицирует клетки иммунной системы. CD4 Т-клетки и моноциты представляют собой типы клеток, которые инфицируются в первую очередь. С целью исследовать способность IL-28 и IL-29 ингибировать репликацию ВИЧ in vitro, PBMCs, взятые от нормальных доноров, инфицируют вирусом ВИЧ в присутствии IL-28, IL-29 и MetIL-29C172S-PEG.
Здоровые мононуклеарные клетки периферической крови (PBMCs) человека выделяют из цельной крови, полученной от прошедших отбор доноров, имеющих серонегативную реакцию к ВИЧ и HBV. Клетки периферической крови 2-3 раза осаждают центрифугированием при малой скорости, ресуспендируют и промывают в PBS, с целью удаления загрязняющих их тромбоцитов. Промытые клетки крови разводят в соотношении 1:1 забуференным фосфатом физиологическим раствором Дульбекко (D-PBS) и помещают в 14 мл среды для разделения лимфоцитов ((LSM; Cellgro™ от компании Mediatech, Inc., Херндон, Виргиния); плотность 1,078 +/- 0,002 г/мл) в центрифужной пробирке емкостью 50 мл и центрифугируют в течение 30 мин с ускорением 600×g. Связанные PBMCs осторожно отсасывают с поверхности раздела и затем дважды промывают с помощью PBS и центрифугированием с малой скоростью. После окончательной промывки количество клеток подсчитывают исключением с помощью красителя трипанового синего и ресуспендируют в количестве 1×107 клеток/мл в питательной среде RPMI 1640, дополненной 15% фетальной телячьей сыворотки (FBS), 2 мМ L-глутамина, 4 мкг/мл PHA-P. Клетки инкубируют в течение 48-72 час при температуре 37°С. После инкубирования PBMCs центрифугируют и ресуспендируют в среде RPMI 1640 с 15% FBS, 2 мМ L-глутамина, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина, 10 мкг/мл гентамицина и 20 ед./мл рекомбинантного IL-2 человека. Концентрацию PBMCs поддерживают в питательной среде на уровне 1-2×106 клеток/мл и два раза в неделю проводят замену питательной среды до тех пор, пока клетки не используют в соответствии с методикой анализа. Моноциты очищают от культуры путем их адгезии к стенкам колбы с тканевой культурой.
Для проведения стандартного РВМС-анализа клетки, полученные, по меньшей мере, от двух доноров и активированные с помощью РНА-Р, объединяют, разводят свежей средой до конечной концентрации 1×106 клеток/мл и наносят на внутренние стенки 96-луночного микропланшета с круглодонными лунками в количестве 50 мкл на лунку (5×104 клеток на лунку). Тестируемые концентрации получают 2Х разведением в пробирках для микротитрования и 100 мкл смеси каждой концентрации помещают в соответствующие лунки в стандартном формате. IL-28, IL-29 и MetIL-29C172S-PEG добавляют с концентрациями в диапазоне 0-10 мкг/мл, обычно в виде полулогарифмических разведений. 50 мкл заранее заданного разведения маточного раствора вируса помещают в каждую тестируемую лунку (конечное значение MOI составляет 0,1). Лунки, в которые добавляют лишь клетки и вирус, используют для вирусного контроля. Отдельно с помощью аналитической системы MTS готовят планшеты без вируса, с целью изучения цитотоксичности лекарства. Культуры РВМС выдерживают в течение семи дней, после чего собирают образцы свободных от клеток надосадочных жидкостей и анализируют на активность обратной транскриптазы и уровней антигена р24.
Понижение активность обратной транскриптазы и уровней антигена р24 под действием IL-28, IL-29 и MetIL-29C172S-PEG служит индикатором антивирусной активности. Результаты показывают, что IL-28 и IL-29 могут обладать терапевтической ценностью при лечении ВИЧ и СПИДа.
Пример 29
IL-28 и IL-29 ингибируют репликацию GBV-B в клетках печени мартышки
HCV является членом семейства Flaviviridae РНК-вирусов. HCV с трудом реплицируется как в ex-vivo, так и in vitro культурах и поэтому не существует удовлетворительных систем для тестирования анти-HCV активности молекул in vitro. GB вирус В (GBV-B) является привлекательной суррогатной моделью для использования при разработке антивирусных средств против HCV, поскольку его последовательности имеют относительно высокую степень идентичности с последовательностью HCV и он является гепатотрофным вирусом. В настоящее время вирус может быть выращен только в первичных гепатоцитах некоторых отличных от человека приматах. Выращивание осуществляют либо изолированием гепатоцитов in vitro и инфицированием их с помощью GBV-B, либо выделением гепатоцитов из GBV-B-инфицированных мартышек и использованием их непосредственно с антивирусными соединениями.
Действие IL-28, IL-29 и MetIL-29C172S-PEG анализируют по внеклеточной продукции РНК в GBV-B с использованием TaqMan RT-PCR и по цитотоксичности с использованием реагента CellTiter96® (Promega, Мэдисон, Висконсин) тремя сериями по шесть полулогарифмических разведений полипептидов IL-28, IL-29 и MetIL-29C172S-PEG. Необработанные культуры служат в качестве клеточных и вирусных контролей. Как RIBAVIRIN® (с максимальной тестируемой концентрацией 200 мкг/мл), так и IFN-α (с максимальной тестируемой концентрацией 5000 международных единиц/мл) включены в качестве положительных контрольных соединений. Выделяют культуры первичных гепатоцитов и помещают на покрытые коллагеном чашки. На следующий день культуры обрабатывают тестируемыми соединениями (IL-28, IL-29, MetIL-29C172S-PEG, IFN-α или RIBAVIRIN®) за 24 час до воздействия вирионами GBV-B или непосредственно обрабатывают тестируемыми образцами, когда используют in vivo инфицированные гепатоциты. Тестируемые образцы и среды добавляют на следующий день и заменяют через три дня. Еще через три или четыре дня (на 6-7 день поле добавления тестируемого образца) собирают надосадочную жидкость и количество клеток подсчитывают с помощью реагента CellTiter96®. Вирусную РНК экстрагируют из надосадочной жидкости и тремя сериями количественно оценивают с помощью количественного анализа с помощью TaqMan RT-PCR с использованием in vitro транскрибированной РНК, содержащей RT-PCR мишень в качестве стандарта. Рассчитывают среднее значение для серий образцов. Ингибирование продукции вируса анализируют графически путем нанесения на график среднего значения количества РНК и количества клеток, полученного из трех серий образцов, в сравнении с необработанными вирусными и клеточными контролями. Ингибирующую концентрацию лекарства, приводящую к 50%-ному подавлению продукции РНК GBV-B (IC50), и токсическую концентрацию, приводящую к разрушению 50% количества клеток, по отношению с контрольными значениями (ТС50), рассчитывают интерполяцией из графиков, построенных на основании полученных данных.
Ингибирование продукции РНК GBV-B под действием IL-28 и IL-29, является индикатором антивирусных свойств IL-28 и IL-29 против указанного вируса, напоминающего вирус гепатита С, в гепатоцитах, главного объекта инфекции гепатита С, и положительные результаты указывают на то, что IL-28 или IL-29 могут использоваться при лечении инфекции HCV у людей.
Пример 30
IL-28, IL-29 и MetIL-29C172S-PEG ингибируют репликацию HBV в клетках WT10
Хронический гепатит В (HBV) является одной из самых распространенных и тяжелых вирусных инфекций у людей и принадлежит к семейству вирусов Hepadnaviridae. С целью исследования антивирусной активности IL-28 и IL-29 против HBV, IL-28, IL-29 и MetIL-29C172S-PEG тестируют против HBV в in vitro инфекционной системе, используя различные клеточные линии HepG2 человека. IL-28, IL-29 и MetIL-29C172S-PEG ингибируют репликацию вируса в указанной системе, и это указывает на их терапевтическую ценность при лечении HBV у людей.
Клетки WT10 являются производными линии клеток HepG2 2.2.15 человека. Клетки WT10 устойчиво трансфицируются геномом HBV, что обеспечивает стабильную экспрессию транскриптов HBV в указанной клеточной линии (Fu and Cheng, Antimicrobial Agents Chemother. 44(12): 3402-3407, 2000). В анализе с использованием клеток WT10 рассматриваемое лекарство и используемый в качестве контроля 3ТС испытывают каждый в пяти концентрациях, полученный сериями полулогарифмических разведений. Точками окончания являются результаты TaqMan PCR для внеклеточной ДНК HBV (IC50) и количество клеток, определяемое с помощью реагента CellTiter96 (ТС50). Методика анализа аналогична приведенной Korba et al., Antiviral Res. 15(3): 217-228, 1991 и Korba et al., Antiviral Res. 19(1): 55-70, 1992. Если кратко, то клетки WT10 помещают на 96-луночные планшеты для микротитрования. Через 16-24 час конфлюэнтный монослой клеток HepG2-2.2.15 промывают, среду заменяют полной питательной средой, содержащей различные концентрации тестируемых образцов, и проводят по три серии экспериментов. 3ТС используют в качестве положительного контроля, в то время как саму питательную среду добавляют к клеткам в качестве отрицательного контроля (вирусного контроля, VC). Через три для культуральную среду заменяют свежей питательной средой, содержащей соответствующим образом разбавленные тестируемые образцы. Через шесть дней после первоначального добавления тестируемых соединений собирают надосадочную жидкость над культурой, обрабатывают проназой и ДНКазой и используют для проведения количественного TaqMan PCR анализа в режиме реального времени. ПЦР-амплифицированную ДНК HBV детектируют в режиме реального времени путем мониторинга усиления сигналов флюоресценции, возникающей в результате экзонуклеолитической деградации захваченной флуоресцентной молекулы-зонда, которая гибридизуется с амплифицированной ДНК HBV. Для каждой ПЦР-амплификации одновременно строят стандартную кривую, используя разбавления очищенной ДНК HBV. Антивирусную активность рассчитывают по уменьшению уровней ДНК HBV (IC50). После этого для оценки жизнеспособности клеток применяют метод с захватом красителя, который используют для расчета цитотоксичности (ТС50). Терапевтический индекс (TI) вычисляют как отношение ТС50/IC50.
IL-28, IL-29 и MetIL-29C172S-PEG ингибируют репликацию вируса HepB в клетках WT10 со значением IC50 < 0,032 мкг/мл. Это доказывает антивирусную активность IL-28 и IL-29 против HBV, выращенных в клеточной линии печени, и указывает на терапевтическую ценность IL-28 и IL-29 при лечении инфекции HBV у людей.
Пример 31
IL-28, IL-29 и MetIL-29C172S-PEG ингибируют репликацию BVDV в клетках почки быка
HCV является членом семейства Flaviviridae РНК-вирусов. Другими вирусами, относящимися к этому семейству, являются вирус бычьей вирусной диареи (BVDV) и вирус желтой лихорадки (YFV). HCV с трудом реплицируется как в ex vivo, так и in vitro культурах, поэтому не существует системы для изучения in vitro активности против HCV. BVDV и YFV используют вместо в HCV качестве суррогатных вирусов для исследования антивирусной активности против семейства вирусов Flaviviridae.
Антивирусное действие IL-28, IL-29 и MetIL-29C172S-PEG изучают по ингибированию при проведении анализов на цитотоксический эффект (СРЕ). В этом анализе определяют отмирание клеток в клеточной линии Мадина-Дарби из бычьей почки (MDBK) после инфицирования цитопатическим вирусом BVDV и ингибирование отмирания клеток при введении IL-28, IL-29 и MetIL-29C172S-PEG. Клетки MDBK размножают в модифицированной по Дульбекко основной среде (DMEM), содержащей феноловый красный вместе с 10% сыворотки лошади, 1% глутамина и 1% пенициллина-стрептомицина. Анализ ингибирования СРЕ проводят в DMEM без фенолового красного в присутствии 2% FBS, 1% глутамина и 1% пенициллина-стрептомицина. За день до проведения анализа клетки обрабатывают трипсином (1% трипсин-ЭДТК), промывают, подсчитывают и помещают в количестве 104 клеток на лунку в 96-луночные планшеты BioCoat® (Fisher Scientific, Питтсбург, Пенсильвания) с плоским дном в объеме 100 мкл на лунку. На следующий день среду удаляют и к клеткам добавляют предварительно оттитрованные аликвоты вируса. Количество вируса соответствует максимальному разведению, которое приводит к полной смерти клеток (> 80%) ко времени полного развития СРЕ (7-й день для BVDV). Жизнеспособность клеток определяют с помощью реагента CellTiter96® (Promega), в соответствии с рекомендациями производителя, и планшет-ридера Vmax (Molecular Devices, Саннивэйл, Калифорния). Каждый тестируемый образец исследуют в шести концентрациях, получаемых полулогарифмическими разведениями с помощью среды для анализа. В качестве положительных контролей применяют IFNα и RIBAVIRIN®. Тестируемые образцы вводят вместе с вирусной инфекцией. Средний фон и скорректированные по окрашиванию образца данные для определения процента снижения СРЕ и процента жизнеспособности клеток для каждой концентрации определяют в сравнении с контролями и рассчитывают значение IC50 относительно ТС50.
IL-28, IL-29 и MetIL-29C172S-PEG подавляют отмирание клеток, индуцированное действием BVDV в клетках MDBK бычьей почки. IL-28 подавляет отмирание клеток со значением IC50, равным 0,02 мкг/мл, IL-29 подавляет отмирание клеток со значением IC50, равным 0,19 мкг/мл, а MetIL-29C172S-PEG подавляют отмирание клеток со значением IC50, равным 0,45 мкг/мл. Полученный результат доказывает, что IL-28 и IL-29 обладают антивирусной активностью против семейства вирусов Flaviviridae.
Пример 32
Индукция активированных интерфероном генов под действием IL-28 и IL-29
А. Мононуклеарные клетки периферической крови человека
Свежевыделенные мононуклеарные клетки периферической крови человека выращивают в присутствии IL-29 (20 нг/мл), IFNα2а (2 нг/мл) (PBL Biomedical Labs, Пискатауэй, Нью-Джерси) или только лишь питательной среды. Клетки выращивают в течение 6, 24, 48 или 72 час, а затем полную РНК изолируют и обрабатывают ДНКазой, не содержащей РНКазу. 100 нг полной РНК используют в качестве матрицы для проведения одностадийного полуколичественного метода RT-PCR вместе с реагентом Taqman One-Step RT-PCR Master Mix® и генспецифичными праймерами, в соответствии с рекомендациями производителя (Applied Biosystems, Бранчбург, Нью-Джерси). Полученные результаты нормируют относительно HPRT и представляют для каждой временной точки в виде кратности индукции по сравнению с одной лишь питательной средой, которую используют в качестве контроля. Таблица 24 показывает, что IL-29 во всех исследованных временных интервалах индуцирует активированную интерфероном экспрессию гена в мононуклеарных клетках периферической крови человека.
В. Активированные Т-клетки человека
Т-клетки человека выделяют методом отрицательной селекции из свежевыращенных мононуклеарных клеток периферической крови с помощью набора реагентов Pan T-cell Isolation®, в соответствии с рекомендациями изготовителя (Miltenyi, Аубурн, Калифорния). Затем Т-клетки активируют и размножают в течение 5 дней вместе с иммобилизованными на планшете анти-CD3, растворимыми анти-CD28 (0,5 мкг/мл) (Pharmingen, Сан-Диего, Калифорния) и интерлейкином 2 (IL-2; 100 ед./мл) (R&D Systems, Миннеаполис, Миннесота), промывают и размножают еще в течение 5 дней вместе с IL-2. После активации и размножения клетки стимулируют действием IL-28А (20 нг/мл), IL-29 (20 нг/мл) или одной лишь средой в течение 3, 6 или 18 час. Выделяют полную РНК и обрабатывают ДНКазой, не содержащей РНКазу. Осуществляют одностадийный полуколичественный метод RT-PCR®, как указано в предыдущем примере. Полученные результаты нормируют относительно HPRT и представляют для каждой временной точки в виде кратности индукции по сравнению с одной лишь питательной средой, которую используют в качестве контроля. Таблица 25 показывает, что IL-28 и IL-29 во всех исследованных временных интервалах индуцирует активированную интерфероном экспрессию гена в активированных Т-клетках человека.
С. Первичные гепатоциты человека
Свежевыделенные гепатоциты человека от двух различных доноров (Cambreax, Балтимор, Мэриленд и CellzDirect, Туссон, Аризона) активируют в течение 24 час с помощью IL-28А (50 нг/мл), IL-29 (50 нг/мл), IFNα2а (50 нг/мл) или только лишь питательной среды. После активации полную РНК выделяют и обрабатывают ДНКазой, не содержащей РНКазу. Одностадийный полуколичественный метод RT-PCR осуществляют, как указано в предыдущем примере. Результаты нормируют относительно HPRT и представляют для каждой временной точки в виде кратности индукции по сравнению с одной лишь питательной средой, которую используют в качестве контроля. Таблица 26 показывает, что после 24-часовой активации IL-28 и IL-29 индуцируют активированную интерфероном экспрессию гена в гепатоцитах человека.
D. HepG2 и HuH7: Клеточные линии гепатомы печени человека
Клетки HepG2 и HuH7 (АТСС №№ 8065, Манассас, Виргиния) активируют действием IL-28А (10 нг/мл), IL-29 (10 нг/мл), IFNα2а (10 нг/мл) IFNB (1 нг/мл) (PBL Biomedical, Labs, Пискатауэй, Нью-Джерси) или только лишь питательной среды в течение 24 или 48 час. В отдельной культуре клетки HepG2 активируют, как указано выше, действием 20 нг/мл MetIL-29C172S-PEG или MetIL-29-PEG. Выделяют полную РНК и обрабатывают ДНКазой, не содержащей РНКазу. 100 нг полной РНК используют в качестве матрицы для осуществления одностадийного полуколичественного метода RT-PCR, как указано ранее. Результаты нормируют относительно HPRT и представляют для каждой временной точки в виде кратности индукции по сравнению с одной лишь питательной средой, которую используют в качестве контроля. Таблица 27 показывает, что IL-28 и IL-29 индуцируют через 24 и 48 час экспрессию ISG в клетках HepG2 и HuH7 клеточных линий гепатомы печени.
Представлены данные для 20 нг/мл MetIL-29-PEG и MetIL-29C172S-PEG версий IL-29 после выращивания в течение 24 час.
Приведенные данные нормированы относительно HPRT и представлены в виде кратности индукции по сравнению с неактивированными клетками.
Пример 33
Антивирусная активность IL-28 и IL-29 в системе репликона HCV
Способность антивирусных лекарств ингибировать репликацию HCV может быть протестирована in vitro в системе репликона HCV. Система репликона состоит из клеток Huh7 клеточной линии гепатомы человека, трансфицированных субгеномными репликонами РНК, которые направляют конститутивную репликацию геномных молекул РНК HCV (Blight, K.J. et al., Science 290: 1972-1974, 2000). Обработка клонов репликона с помощью TNFα в количестве 10 междун. ед./мл снижает количество РНК HCV на 85%, по сравнению с необработанными контрольными клетками. Способность IL-28А и IL-29 снижать количество РНК HCV, продуцируемой через 72 час клонами репликона, указывает на то, что антивирусный статус, который придает клеткам Huh7 обработка с помощью IL-28А/IL-29, эффективно ингибирует репликацию репликона HCV и, таким образом, весьма вероятно эффективна для ингибирования репликации HCV.
Способность IL-28А и IL-29 ингибировать репликацию HCV, которую определяют с помощью набора реагентов Branched chain DNA фирмы Bayer, может быть проверена в следующих условиях:
1. IL28 индивидуально с возрастающими концентрациями (6)* вплоть до 1,0 мкг/мл
2. IL29 индивидуально с возрастающими концентрациями (6)* вплоть до 1,0 мкг/мл
3. PEGIL29 индивидуально с возрастающими концентрациями (6)* вплоть до 1,0 мкг/мл
4. IFNα2А индивидуально с концентрациями 0,3, 1,0 и 3,0 межд. ед./мл
5. Рибавирин индивидуально.
Положительным контролем является IFNα, а отрицательным контролем является рибавирин.
Для определения их жизнеспособности клетки через 72 час окрашивают с помощью Alomar Blue.
* Концентрации для условий 1-3 следующие:
1,0 мкг/мл, 0,32 мкг/мл, 0,10 мкг/мл, 0,032 мкг/мл, 0,010 мкг/мл, 0,0032 мкг/мл.
Клон репликона (ВВ7) обрабатывают 1Х в день в течение трех последовательных дней приведенной выше дозой. Полную РНК HCV определяют через 72 час.
Пример 34
IL-28 и IL-29 обладают антивирусной активностью против патогенных вирусов
Два метода используют для in vitro анализа антивирусной активности IL-28 и IL-29 против панели патогенных вирусов, включая среди прочих аденовирус, вирус парагриппа, респираторно-синцитиальный вирус, риновирус, вирус Коксаки, вирус гриппа, вирус коровьей оспы, вирус Западного Нила, вирус денге, вирус энцефаломиелита лошадей, вирус Pichinde и вирус полиомиелита. Указанными двумя методами являются подавление индуцированного вирусом цитопатического эффекта (CPE), который определяют визуальным (под микроскопом) наблюдением клеток, и усиление захвата клетками красителя нейтрального красного (NR). В методе на ингибирование СРЕ оценивают действие семи концентраций тестируемого лекарства (используют логарифмические разведения, такие как 1000, 100, 10, 1, 0,1, 0,01, 0,001 нг/мл) против каждого вируса в формате 96-луночных микропланшетов с плоским дном, содержащих клетки-хозяева. Соединения добавляют за 24 час до введения вируса, который используют, в зависимости от вируса, с концентрацией приблизительно от 5 до 100 инфицирующих клеточную культуру доз на лунку, что соответствует множественности инфекции (MOI) в диапазоне от 0,01 до 0,0001 инфекционных частиц на клетку. Тесты считывают после инкубирования при 37°С в течение заданного времени, достаточного для того, чтобы позволить развиться адекватному цитопатическому эффекту вируса. В анализе на захват, NR краситель (с концентрацией 0,34% в питательной среде) добавляют в тот же набор планшетов, чтобы провести визуальную оценку. Через 2 час интенсивность поглощенного клетками и затем элюированного из клеток красителя определяют с помощью ридера микропланшетов. Антивирусную активность выражают в виде 50%-ной эффективной (подавляющей вирус) концентрации (ЕС50), которую определяют графически нанесением данных на полулогарифмическую бумагу по зависимости концентрации от процента ингибирования. В некоторых случаях, с целью проведения регрессионного анализа, могут определяться значения EC50/IС50. В общем случае значения ЕС50, определяемые по методу анализа с использованием NR, в два раза превышают значения ЕС50, полученные по методу СРЕ.
Визуальный анализ
Анализ с использованием нейтрального красного
Пример 35
IL-28, IL-29, metIL-29-PEG и metIL-29C172S-PEG стимулируют индукцию ISG в клеточной линии AML-12 печени мышей
Активированные интерфероном гены (ISGs) являются генами, которые индуцируются интерферонами типа I (IFNs), а также молекулами семейства IL-28 и IL-29, указывая на то, что IFN и IL-28 и IL-29 индуцируют одинаковые пути, приводящие к антивирусной активности. Интерфероны типа I человека (IFNα1-4 и IFNβ) проявляют незначительную активность или не проявляют никакой активности по отношению к мышиным клеткам, что, как полагают, является следствием отсутствия кросс-видовой реакционноспособности. Для исследования, оказывают ли IL-28 и IL-29 эффект на мышиные клетки, индукцию ISG под действием IL-28 и IL-29 оценивают методом ПЦР в реальном времени на мышиных клетках, полученных из клеточной линии AML-12.
Клетки AML-12 наносят на 6-луночные планшеты в полной среде DMEM с концентрацией 2×106 клеток/лунку. Через 24 час после нанесения клеток в культуры добавляют IL-28 и IL-29 человека с концентрацией 20 нг/мл. В качестве контроля клетки активируют либо мышиным IFNα (положительный контроль), либо не активируют (отрицательный контроль). Клетки после добавления полученных из СНО IL-28А (SEQ ID NO: 2) или IL-29 (SEQ ID NO: 4) человека выращивают в течение 8, 24, 48 и 72 час. РНК выделяют из клеточной массы с помощью набора реагентов RNAEasy-kit® (Qiagen, Валенсия, Калифорния). РНК обрабатывают ДНКазой (Millipore, Биллерика, Массачусетс), чтобы очистить РНК от любых следов ДНК. кДНК генерируют с помощью смеси Perkin-Elmer RT. Индукцию генов ISG оценивают методом ПЦР в реальном времени с использованием праймеров и зондов, специфичных для мышиных OAS, Pkr и Мх1. Для получения количественных данных ПЦР HPRT в реальном времени редуплицируют с ПЦР ISG. Стандартную кривую получают, используя известные количества РНК из IFN-стимулированных мышиных РBLs. Все данные приведены в виде экспрессии относительно внутренней экспрессии HPRT.
IL-28А и IL-29 человека активируют индукцию ISG в гепатоцитах мышей клеточной линии AML-12, и результаты показывают, что в отличие от интерферонов типа I, семейство белков IL-28/29 проявляют кросс-видовую реакционноспособность.
Все данные представляют как кратность увеличения индукции по отношению к экспрессии гена HPRT:
нг мРНК HPRT
В качестве примера приведены данные для временной точки 48 час.
AML12's
Клетки активируют действием 20 нг/мл MetIL-29-PEG или MetIL-29C172S-PEG в течение 24 час.
Приведенные данные нормированы относительно HPRT и представлены в виде кратности индукции по отношению к неактивированным клеткам.
Пример 36
ISGs эффективно индуцируются в селезенке трансгенных мышей, экспрессирующих IL-29 человека
Готовят трансгенных (Tg) мышей, экспрессирующих IL-29 человека под управлением промотора Eu-lck. Для изучения, обладает ли IL-29 in vivo активностью у мышей, экспрессию ISG анализируют методом ПЦР в реальном времени с использованием селезенок трансгенных мышей IL-29 Eu-lck.
Трансгенных мышей (C3H/C57BL/6) готовят с помощью конструкции, которая экспрессирует ген IL-29 человека под управлением промотора Eu-lck. Указанный промотор активен в Т-клетках и В-клетках. Трансгенных мышей и их нетрансгенных однопометников (n=2/группа) забивают в возрасте приблизительно 10 недель. Извлекают селезенки мышей. РНК выделяют из клеточной массы с помощью набора реагентов RNAEasy-kit® (Qiagen). РНК обрабатывают ДНКазой, чтобы очистить РНК от любых следов ДНК. кДНК генерируют с помощью смеси Perkin-Elmer RT®. Генную индукцию ISG оценивают методом ПЦР в реальном времени с использованием праймеров и зондов (5' FAM, 3' NFQ), специфичных для мышиных OAS, Pkr и Мх1. Для получения количественных данных HPRT по методу ПЦР в реальном времени редуплицируют с ПЦР ISG. Кроме того, стандартную кривую получают, используя известные количества IFN-стимулированных мышиных PBLs. Все данные приведены в виде экспрессии относительно внутренней экспрессии HPRT.
Селезенки, выделенные из мышей IL-29 Tg, показывают высокую индукцию ISGs в OAS, Pkr и Мх1, по сравнению с нетрансгенными однопометными контролями, указывая на то, что IL-29 человека in vivo биологически активен в мышах.
Все данные представлены как кратность увеличения экспрессии по отношению к экспрессии гена HPRT. Средние значения экспрессии получены от двух мышей.
Пример 37
Белки IL-28 и IL-29 человека индуцируют генную экспрессию ISG в печени, селезенке и крови мышей
С целью определить, могут ли IL-28 и IL-29 человека индуцировать активированные интерфероном гены in vivo, полученные из СНО белки IL-28А и IL-29 человека вводят мышам в виде инъекции. Кроме того, в in vivo анализах тестируют также IL-29, полученный из E. coli, как указано выше, используя MetIL-29C172S-PEG и MetIL-29-PEG. В различные периоды времени и с различными дозами и определяют генную индукцию ISG в крови, селезенке и печени мышей.
Мышам C57BL/6 вводят внутрибрюшинные или внутривенные инъекции полученных из СНО IL-28А и IL-29 человека или MetIL-29C172S-PEG и MetIL-29-PEG в диапазоне доз (10 мкг - 250 мкг). Мышей забивают в разные периоды времени (1 час - 48 час). У мышей извлекают селезенку и печень и выделяют РНК. РНК выделяют также из клеток крови. Из клеток получают таблетки и выделяют из них РНК с помощью набора реагентов RNAEasy-kit® (Qiagen). РНК обрабатывают ДНКазой (Amicon), чтобы очистить РНК от любых остатков ДНК. кДНК генерируют с помощью смеси Perkin-Elmer RT (Perkin-Elmer). Генную индукцию ISG оценивают методом ПЦР в реальном времени с использованием праймеров и зондов, специфичных для мышиных OAS, Pkr и Мх1. Для получения количественных данных HPRT по методу ПЦР в реальном времени редуплицируют с ПЦР ISG. Стандартную кривую рассчитывают, используя известные количества IFN-стимулированных мышиных PBLs. Все данные приведены в виде экспрессии относительно внутренней экспрессии HPRT.
IL-29 человека в зависимости от дозы индуцирует генную экспрессию ISG (OAS, Pkr и Мх1) в печени, селезенке и крови мышей. Экспрессия ISG достигает максимальной величины в интервале 1-6 час после инъекции и показывает пролонгированную, по сравнению с контрольными мышами, экспрессию вплоть до 48 час. В этом эксперименте IL-28А человека не индуцирует генную экспрессию ISG.
Результаты представлены как кратность увеличения экспрессии по отношению к экспрессии гена HPRT. В качестве образца приведен пример для индукции в OAS под действием IL-29 в виде однократной внутрибрюшинной инъекции 250 мкг. Приведенные данные являются средними значениями экспрессии для 5 различных животных/групп.
Мышам внутривенно вводят 100 мкг белков. Данные представлены в виде кратности увеличения экспрессии, по сравнению с экспрессией HPRT печенью мышей. Аналогичные данные получены для селезенки и крови мышей.
Пример 38
IL-28 и IL-29 индуцируют белок ISG у мышей
С целью исследования эффекта IL-28 и IL-29 человека на индукцию белка ISG (OAS), сыворотку и плазму мышей, обработанных белками IL-28 и IL-29, тестируют на активность OAS.
Мышам C57BL/6 вводят внутривенные инъекции IL-28А и IL-29 человека в виде растворов в PBS в диапазоне концентраций (10 мкг - 250 мкг). У мышей берут сыворотку и плазму в различные периоды времени и определяют активность OAS с помощью набора для радимоиммуноанализа (RIA) OAS от компании Eiken Chemicals (Токио, Япония).
IL-28 и IL-29 индуцируют активность OAS в сыворотке и плазме мышей, указывая на то, что эти белки биологически активны in vivo.
Активность OAS приведена в пМ/дл в плазме для одной концентрации (250 мкг) IL-29 человека.
Пример 39
IL-28 и IL-29 подавляют аденовирусную патологию у мышей
С целью исследования антивирусной активности IL-28 и IL-29 против вирусов, которые инфицируют печень, тестируемые образцы были испытаны на мышах против инфекционных аденовирусных векторов, экспрессирующих внутренний ген зеленого флуоресцентного белка (GFP). При внутривенной инъекции указанные вирусы для генной экспрессии в первую очередь нацеливаются на печень. Аденовирусы не способны к репликации, но приводят к поражению печени, вызванному инфильтрацией воспалительных клеток, которую можно отслеживать по измерению в сыворотке уровней ферментов печени, таких как AST и ALT, или непосредственным наблюдением патологии печени.
Мышам C57BL/6 один раз ежедневно вводят внутрибрюшинно 50 мкг мышиного IL-28 (zcyto24 как указано в SEQ ID NO: 8) или MetIL-29C172S-PEG в течение 3 дней. Контрольным животным вводят инъекции PBS. Через час после введения 3-й дозы мышам в хвостовую вену вводят однократную в виде болюса инъекцию аденовирусного вектора, AdGFP (1×109 бляшкообразующих единиц (бое)). После этого ежедневно мышам вводят дополнительно 4 дозы PBS, мышиного IL-28 или MetIL-29C172S-PEG (обще количество 7 доз). Через час после введения последней дозы PBS, мышиного IL-28 или MetIL-29C172S-PEG у мышей последний раз берут кровь на анализ, после чего животных забивают. Анализируют сыворотку и ткани печени. Сыворотку анализируют на содержание ферментов печени AST и ALT. Извлекают печень и проводят анализ экспрессии GFP и гистологию. Для проведения гистологии образцы печени закрепляют в формалине, а затем парафинируют с последующим H&E окрашиванием. Срезы печени, которые темнеют при обработке, исследуют под оптическим микроскопом. Отмечают изменения и проводят подсчет в баллах по шкале, разработанной для оценки патологии печени и воспаления.
Мышиные IL-28 и IL-29 подавляют аденовирусную инфекцию и генную экспрессию, которую измеряют методом флуоресценции печени. У PBS-обработанных мышей (n=8) средняя относительная флюоресценции печени составляет 52,4 (в относительных единицах). Напротив, у IL-28-обработанных мышей (n=8) средняя относительная флюоресценции печени составляет 34,5, а у IL-29-обработанных мышей (n=8) средняя относительная флюоресценции печени составляет 38,9. Снижение аденовирусной инфекции и генной экспрессии приводит к уменьшению патологии печени, что определяют по уровням AST и ALT в сыворотке и гистологией. У PBS-обработанных мышей (n=8) среднее значение для AST в сыворотке составляет 234 ед./л, а значение для ALT в сыворотке составляет 250 ед./л. Напротив, у IL-28-обработанных мышей (n=8) среднее значение для AST в сыворотке составляет 193 ед./л, а значение для ALT в сыворотке составляет 216 ед./л; у IL-29-обработанных мышей (n=8) среднее значение для AST в сыворотке составляет 162 ед./л, а значение для ALT в сыворотке составляет 184 ед./л. Кроме того, гистология печени показывает, что мыши, которым вводили мышиный IL-28 или IL-29, имеют меньшие показатели патологии печени и воспаления, чем PBS-обработанная группа. В образцах печени из группы IL-29 наблюдаются также меньшая пролиферация синусоидальных клеток, меньшее количество фигур митоза и меньшие изменения в гепатоцитах (в частности, вакуолизация, наличие нескольких ядер, увеличение размеров гепатоцитов), чем PBS-обработанной группе. Эти данные показывают, что мышиные IL-28 или IL-29 обладают антивирусными свойствами против трофических вирусов печени.
Пример 40
Модели LCMV
Инфекции вируса лимфоцитарного хориоменингита (LCMV) у мышей являются превосходной моделью острой и хронической инфекции. Указанные модели используют для оценки влияния цитокинов на антивирусный иммунный ответ и эффекта, который IL-28 или IL-29 оказывают на вирусную нагрузку и антивирусный иммунный ответ. Двумя используемыми моделями являются: LCMV инфекция Армстронга (острая) и инфекция клона 13 LCMV. (См. в частности, Wherry et al., J. Virol. 77: 4911-4927, 2003; Blattman et al., Nature Med. 9(5): 540-547, 2003; Hoffman et al., J. Immunol. 170: 1339-1353, 2003.) Наблюдаются три стадии развития CD8 Т-клеток в ответ на вирус: 1) размножение, 2) сокращение и 3) память (острая модель). Инъекции IL-28 или IL-29 вводят на каждой стадии как острой, так и хронической модели. В хронической модели инфекции IL-28 или IL-29 вводят в течение 60 дней после инфекции, чтобы проанализировать эффект IL-28 или IL-29 на персистирующую вирусную нагрузку. IL-28 или IL-29 вводят как в острой, так и хронической моделях и исследуют вирусную нагрузку в крови, селезенке и печени. Другие параметры, которые могут изучаться, включают: окрашивание тетрамера в потоке, с целью подсчета количества LCMV-специфичных CD8+ Т-клеток; способность тетрамера + клеток продуцировать цитокины при активировании их родственным антигеном LCMV; и способность LCMV-специфичных CD8+ Т-клеток пролиферировать в ответ на их родственный антиген LCMV. Фенотип LCMV-специфичных Т-клеток определяют методом проточной цитометрии, с целью анализа активации клеток и статуса дифференцировки. Кроме того, изучают способность LCMV-специфичных CTL подвергать лизису клетки-мишени, несущие их родственный антиген LCMV. Анализируют также количество и функцию LCMV-специфичных CD4+ Т-клеток.
Определяют снижение вирусной нагрузки после лечения с помощью IL-28 или IL-29. Значимой является 50%-ное снижение вирусной нагрузки в любом органе, в частности, печени. Для мышей, обработанных с помощью IL-28 или IL-29, значимым считается также 20%-ное увеличение процентного содержания тетрамерных положительных Т-клеток, которые пролиферируют, дают цитокины или проявляют зрелый фенотип, по сравнению с не подвергавшимися обработке мышами.
Инъекции IL-28 или IL-29, которые приводят к снижению вирусной нагрузки, являются результатом более эффективного контролирования вирусной инфекции, особенно в хронической модели, где в отсутствие обработки лекарствами вирусные титры остаются повышенными в течение длительного периода времени. Значимым считается двукратное снижение вирусного титра, по сравнению с не подвергавшимися обработке мышами.
Пример 41
Модель гриппа для острой вирусной инфекции
А. Предварительные эксперименты по исследованию антивирусной активности
С целью определения антивирусной активности IL-28 или IL-29 по отношению к острой инфекции вирусом гриппа, проводят in vivo исследование инфицированных гриппом мышей c57B1/6 по следующему протоколу:
Животные: 148 самок мышей BALB/c (Charles River) в возрасте 6 недель, 30 на группу.
Группы:
(1) Абсолютная контрольная группа (не инфицированные животные) для параллельного исследования титра антител и гистопатологии (2 животных в группе)
(2) Носитель (внутрибрюшинно) физиологический контроль
(3) Амантадин (положительный контроль) 10 мг/день в течение 5 дней (внутрь), вводят за 2 час до инфекции
(4) Животные, обработанные с помощью IL-28 или IL-29 (5 мкг, внутрибрюшинно, вводят через 2 час после инфекции)
(5) Животные, обработанные с помощью IL-28 или IL-29 (25 мкг, внутрибрюшинно, вводят через 2 час после инфекции)
(6) Животные, обработанные с помощью IL-28 или IL-29 (125 мкг, внутрибрюшинно, вводят через 2 час после инфекции)
День 0 - За исключением абсолютных контролей, всех животных инфицируют вирусом гриппа
Для вирусной нагрузки (10 для LD50)
Для иммунологической тренировки (LD30)
День 0-9 - Ежедневные инъекции IL-28 или IL-29 (внутрибрюшинно)
Регистрируют массу тела и общее состояние (3 раза в неделю)
День 3 - Умерщвляют по 8 животных в каждой группе
Вирусная нагрузка в правом легком (TCID50)
Гистопатология левого легкого
Образцы крови для титрования антител
День 10 - Забивают всех выживших животных, проводят отбор проб крови для титрования антител, выделение легочных лимфоцитов (4 пула из 3) для прямого CTL анализа (во всех 5 группах) и количественное определение иммунного фенотипа для следующих маркеров: CD3/CD4, CD3/CD8, CD3/CD8/CD11b, CD8/CD44/CD62L, CD3/DX5, GR-1/F480 и CD19.
Исследование № 2
Изучение эффективности действия IL-28 или IL-29 у мышей C57B1/6, инфицированных адаптированным к мышам вирусом, проводят на самках мышей C57B1/6 (Charles River) в возрасте 8 недель.
Группа 1: Носитель (внутрибрюшинно)
Группа 2: Положительный контроль: нейтрализующее антитело против гриппа (A/USSR (H1N1) козла против гриппа) (Chemicon International, Темекула, Калифорния); 40 мкг/мышь через 2 и 4 час после инфекции (10 мкл интраназально)
Группа 3: IL-28 или IL-29 (5 мкг, внутрибрюшинно)
Группа 4: IL-28 или IL-29 (25 мкг, внутрибрюшинно)
Группа 5: IL-28 или IL-29 (125 мкг, внутрибрюшинно)
После наблюдений при жизни и иммунологической тренировки получают:
День 0 - Всех животных инфицируют вирусом гриппа (доза определена в эксперименте 2)
День 0-9 - Ежедневные инъекции IL-28 или IL-29 (внутрибрюшинно)
Раз в два дня регистрируют массу тела и общее состояние
День 10 - Умерщвляют выживших животных и проводят анализ вирусов для определения вирусной нагрузки в легком.
Выделение легочных лимфоцитов (для прямого CTL анализа в легких с использованием EL-4 в качестве мишеней при различном отношении Е:Т (на основании лучших результатов из экспериментов 1 и 2).
Окрашивание тетрамера: При использовании комплексов MHC класса I с вирусными пептидами: FLU-NP366-374/Db (ASNENMETM), (LMCV пептид/Db) исследуют количество CD8+ Т-клеток, связывающих тетрамеры MHC класса I, которые содержат эпитоп нуклеопротеина (NP) гриппа А.
Количественное определение иммунофенотипа для: CD8, тетрамер, внутриклеточный IFNγ, NK1.1, CD8, тетрамер, CD62L, CD44, CD3 (+ или -), NK1.1(+), внутриклеточный IFNγ, CD4, CD8, NK1.1, DX5, CD3 (+ или -), NK1.1, DX5, тетрамер, одноцветные образцы для калибровки цитометра.
Выживание/Исследование с повторным введением провокационной пробы
День 30: Изучение выживаемости на мышах проводят в течение 9 дней с различными дозами IL-28 или IL-29 или с положительным контролем антитела против гриппа. Определяет массу тела и продукцию антител против гриппа в индивидуальных образцах сыворотки (полную, IgG1, IgG2a, IgG2b).
Исследование с повторным введением провокационной пробы
День 0: Обе группы инфицируют вирусом A/PR (1LD30)
Группу 6 не подвергают лечению
Группу 7 подвергают лечению в течение 9 дней дозой 125 мкг IL-28 или IL-29.
День 30: Исследуют выживаемость.
Измеряют массу тела и продукцию в индивидуальных образцах сыворотки (полный, IgG1, IgG2a, IgG2b).
День 60: Проводят исследование с повторным введением провокационной пробы.
Выживших в каждой группе животных делят на 2 подгруппы.
В группе 6А и 7А вводят повторную провокационную пробу вируса A/PR (1 LD30).
В группе 6В и 7В вводят повторную провокационную пробу вируса A/PR (1 LD30).
Проводят наблюдение за обеими группами и определяют день, когда животных умерщвляют. Измеряют массу тела и определяют продукцию антител в индивидуальных образцах сыворотки (полную, IgG1, IgG2a, IgG2b).
Пример 42
IL-28 и IL-29 обладают in vivo антивирусной активностью против вируса гепатита В (HBV)
Модель трансгенных мышей (Guidotti et al., J. Virology 69: 6158-6169, 1995) поддерживает репликацию высоких уровней инфекционного HBV и ее используют в качестве химиотерапевтической модели для инфекции HBV. Трансгенных мышей лечат антивирусными лекарствами и после эксперимента определяют уровни ДНК и РНК HBV в печени и сыворотке трансгенных мышей. После эксперимента можно также определить уровни белка HBV у трансгенных мышей. Указанную модель использовали для оценки эффективности ламивудина и TNF-α для снижения вирусных титров HBV.
Самцам мышей HBV TG ежедневно в течение 14 дней вводят внутрибрюшинно инъекции 2,5, 25 или 250 мкг IL-28 или IL-29 (всего 8 доз). У мышей берут кровь для анализа сыворотки в день начала лечения (день 0) и на 7 день. Через 1 час после того, как была взята последняя проба крови на анализ IL-29, животных умерщвляют. Сыворотку и печень анализируют на ДНК HBV в печени, РНК HBV в печени, ДНК HBV в сыворотке, НВс в печени, НВе в сыворотке и HBs в сыворотке.
Уменьшение количества ДНК HBV в печени, РНК HBV в печени, ДНК HBV в сыворотке, НВс в печени, НВе в сыворотке и HBs в сыворотке в ответ на действие IL-28 или IL-29 отражает антивирусную активность указанных соединений против HBV.
Пример 43
IL-28 и IL-29 ингибируют репликацию вируса герпеса-8 (HHV-8) человека в клетках BCBL-1
Антивирусную активность IL-28 и IL-29 против HHV-8 исследуют в in vitro инфекционной системе с использованием В-лимфоидной клеточной линии, BCBL-1.
В HHV-8 анализе тестируемое соединение и ганцикловир, который применяют в качестве контроля, исследуют каждое в пяти концентрациях, получаемых в виде серии полулогарифмических разбавлений. Точками окончания являются результаты TaqMan PCR для внеклеточной ДНК HHV-8 (IC50) и количество клеток при использовании реагента CellTiter96® (T50; Promega, Мэдисон, Висконсин). Если кратко, клетки BCBL-1 наносят на 96-луночные планшеты для микротитрования. Через 16-24 час клетки промывают и среду заменяют полной питательной средой, содержащей различные концентрации тестируемых соединений; проводят три серии экспериментов. Ганцикловир используют в качестве положительного контроля, а сама питательная среда служит отрицательным контролем (вирусный контроль, VC). Через три дня культуральную среду заменяют свежей питательной средой, содержащей соответствующим образом разбавленное тестируемое соединение. Через шесть дней после первоначального введения тестируемого соединения собирают надосадочную жидкость над культурой, обрабатывают проназой и ДНКазой и затем используют для проведения количественного анализа с помощью TaqMan PCR в режиме реального времени. ПЦР-амплифицированную ДНК HHV-8 детектируют в режиме реального времени путем мониторинга усиления сигналов флуоресценции, возникающей в результате экзонуклеолитической деградации захваченной флуоресцентной молекулы-зонда, которая гибридизуется с амплифицированной ДНК HHV-8. Для каждой ПЦР-амплификации одновременно строят стандартную кривую, используя разбавления очищенной ДНК HHV-8. Антивирусную активность рассчитывают по уменьшению уровней ДНК HHV-8 (IC50). После этого для оценки жизнеспособности клеток применяют другой метод с захватом красителя, который используют для расчета цитотоксичности (ТС50). Терапевтический показатель (TI) вычисляют как отношение ТС50/IC50.
IL-28 и IL-29 ингибируют репликацию вируса HHV-8 в клетках BCBL-1. Величина IC50 для IL-28А составляет 1 мкг/мл, а величина ТС50 составляет >10 мкг/мл (TI > 10). Величина IC50 для IL-29 составляет 6,5 мкг/мл, а величина ТС50 составляет >10 мкг/мл (TI > 1,85). Величина IC50 для MetIL-29C172S-PEG составляет 0,14 мкг/мл, а величина ТС50 составляет >10 мкг/мл (TI > 100).
Пример 44
IL-28 и IL-29 обладают антивирусной активностью против вируса Эпштейна-Барр (EBV)
Антивирусную активность IL-28 или IL-29 против EBV исследуют в in vitro инфекционной системе с использованием В-лимфоидной клеточной линии, P3HR-1. В EBV анализе тестируемое и контрольное соединение исследуют каждое в пяти концентрациях, получаемых в виде серии полулогарифмических разбавлений. Точками окончания являются TaqMan PCR для внеклеточной ДНК EBV (IC50) и количество клеток при использовании реагента CellTiter96® (T50; Promega). Если кратко, клетки P3HR-1 наносят на 96-луночные планшеты для микротитрования. Через 16-24 час клетки промывают и среду заменяют полной питательной средой, содержащей различные концентрации тестируемых соединений; проводят три серии экспериментов. Помимо положительного контроля саму питательную среду добавляют к клеткам в качестве отрицательного контроля (вирусный контроль, VC). Через три дня культуральную среду заменяют свежей питательной средой, содержащей соответствующим образом разбавленное тестируемое соединение. Через шесть дней после первоначального введения тестируемого соединения собирают надосадочную жидкость над культурой, обрабатывают проназой и ДНКазой и затем используют для проведения количественного анализа с помощью TaqMan PCR в режиме реального времени. ПЦР-амплифицированную ДНК EBV детектируют в режиме реального времени путем мониторинга усиления сигналов флюоресценции, возникающей в результате экзонуклеолитической деградации захваченной флуоресцентной молекулы-зонда, которая гибридизуется с амплифицированной ДНК EBV. Для каждой ПЦР-амплификации одновременно строят стандартную кривую, используя разбавления очищенной ДНК EBV. Антивирусную активность рассчитывают по уменьшению уровней ДНК EBV (IC50). После этого для оценки жизнеспособности клеток применяют другой метод с захватом красителя, который используют для расчета цитотоксичности (ТС50). Терапевтический показатель (TI) вычисляют как отношение ТС50/IC50.
Пример 45
Антивирусная активность IL-28 и IL-29 против вируса простого герпеса-2 (HSV-2)
Антивирусную активность IL-28 и IL-29 против HSV-2 исследуют в in vitro инфекционной системе в клетках Vero. Антивирусное действие IL-28 и IL-29 исследуют по анализу ингибирования цитотоксического эффекта (СРЕ). Указанный анализ включает отмирание клеток Vero под действием цитопатического вируса HSV-2 и ингибирование отмирания клеток под действием IL-28 и IL-29. Клетки Vero размножают в модифицированной по Дульбекко основной среде (DMEM), содержащей феноловый красный вместе с 10% сыворотки лошади, 1% глутамина и 1% пенициллина-стрептомицина, а анализ ингибирования СРЕ проводят в среде DMEM без фенолового красного в присутствии 2% FBS, 1% глутамина и 1% пенициллина-стрептомицина. За день до проведения анализа клетки обрабатывают трипсином (1% трипсин-ЭДТК), промывают, подсчитывают и помещают в количестве 104 клеток на лунку в 96-луночные планшеты BioCoat® (Fisher Scientific, Питтсбург, Пенсильвания) с плоским дном в объеме 100 мкл на лунку. На следующее утро среду удаляют и к клеткам добавляют предварительно оттитрованные аликвоты вируса. Используемое количество вируса соответствует максимальному разведению, которое приводит к полной смерти клеток (> 80%) ко времени максимального развития СРЕ. Жизнеспособность клеток определяют с помощью реагента CellTiter96® (Promega), в соответствии с рекомендациями производителя, и планшет-ридера Vmax (Molecular Devices, Саннивэйл, Калифорния). Каждый тестируемый образец исследуют в шести концентрациях, получаемых полулогарифмическими разведениями с помощью среды для анализа. В качестве положительного контроля применяют ацикловир. Соединения вводят вместе с вирусной инфекцией. Средний фон и скорректированные по окрашиванию образца данные для определения процента снижения СРЕ и процента жизнеспособности клеток для каждой концентрации определяют в сравнении с контролями и рассчитывают значение IC50 относительно ТС50.
В данном анализе IL-28, IL-29 и MetIL-29C172S-PEG не ингибируют отмирание клеток (IC50 > 10 мкг/мл). IFNα в этом анализе также не проявляет антивирусную активность.
Полное описание патентов, патентных заявок и публикаций, а также находящихся в свободном доступе электронных материалов (например, депоненты аминокислотных и нуклеотидных последовательностей в базе данных GenBank), приведенные в данном описании, включены в него посредством ссылки. Приведенное выше подробное описание и примеры представлены лишь для того, чтобы облегчить понимание изобретения. Они никак не ограничивают настоящее изобретение. Изобретение не ограничивается конкретными приведенными и описанными деталями, поскольку в него должны быть включены очевидные для специалистов вариации, которые определены в приведенной ниже формуле изобретения.
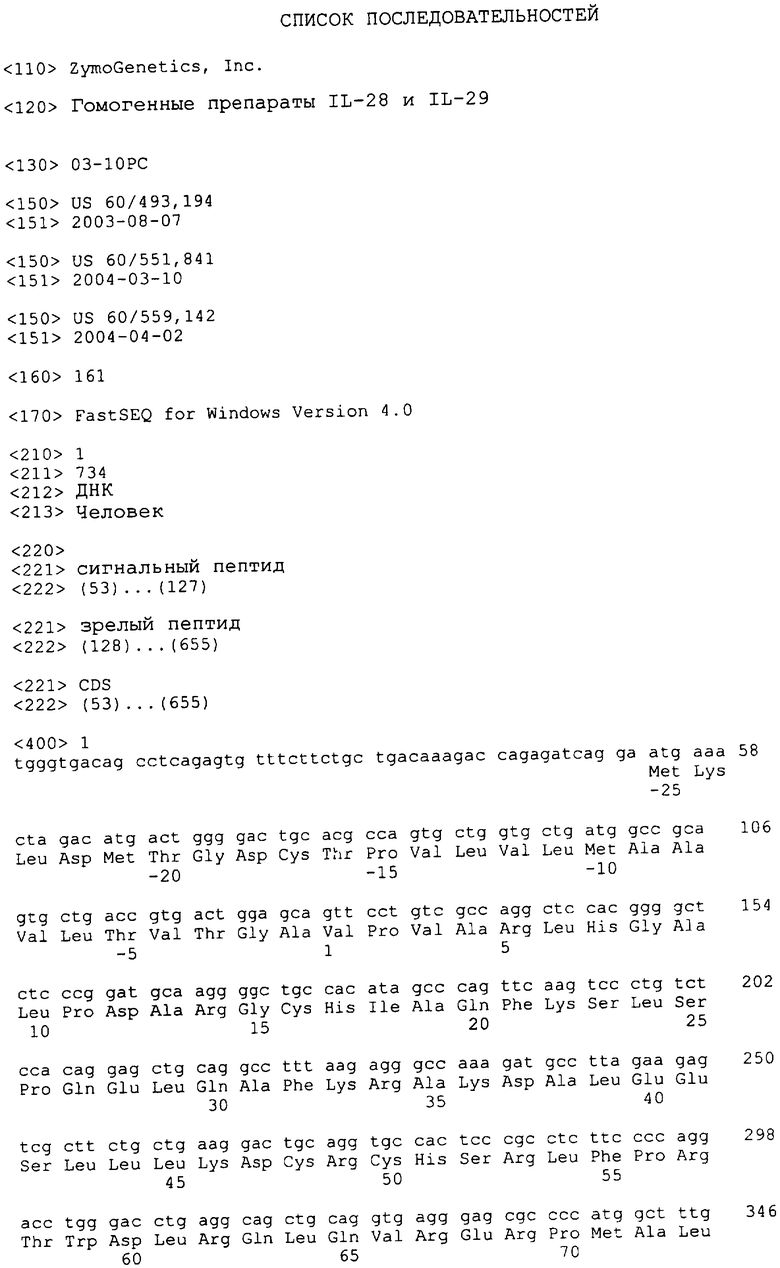

































































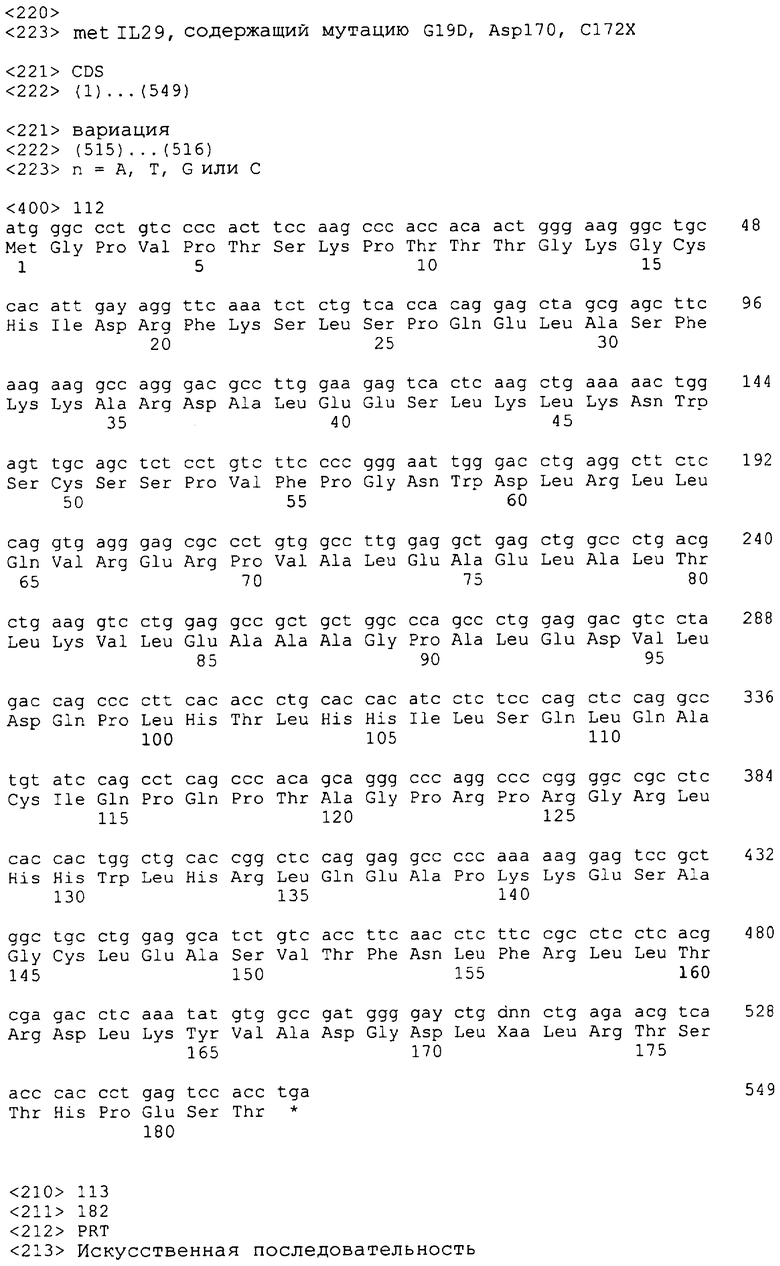









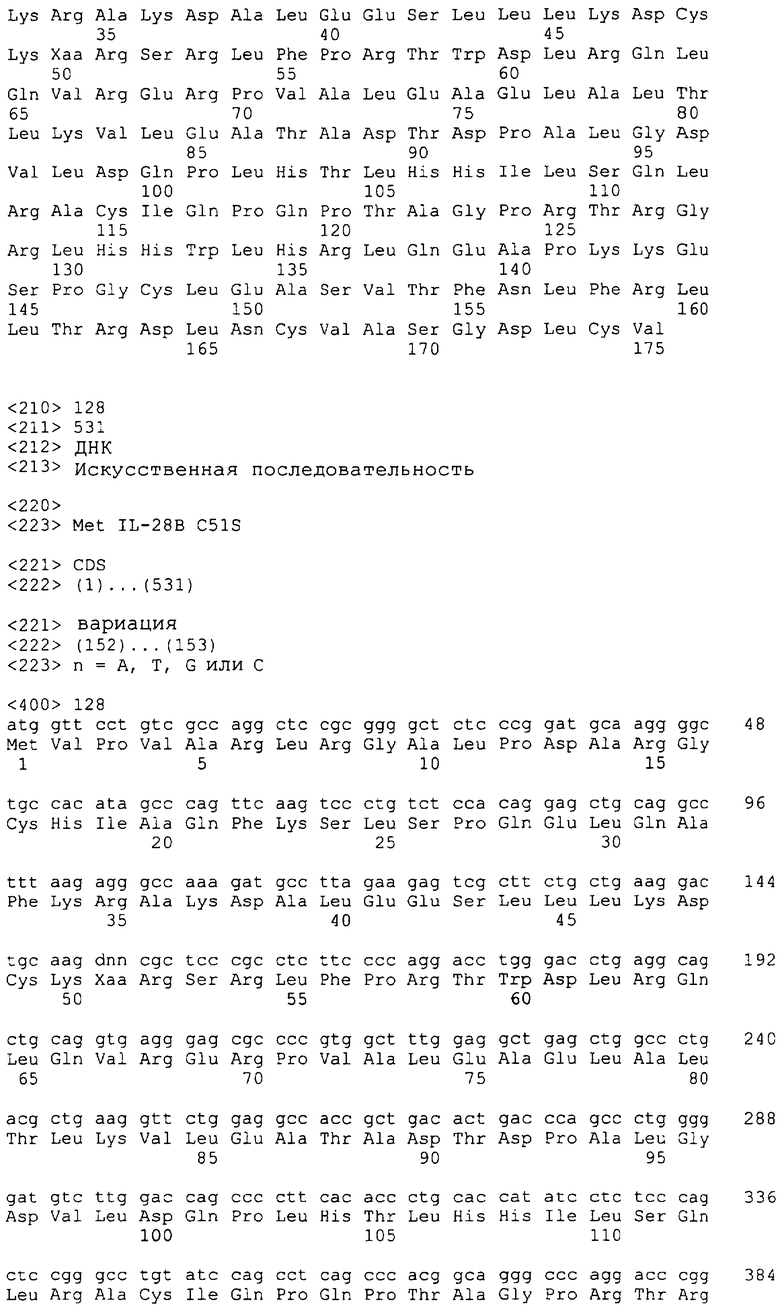



























| название | год | авторы | номер документа |
|---|---|---|---|
| ГОМОГЕННЫЕ ПРЕПАРАТЫ IL-28 И IL-29 | 2004 |
|
RU2518324C2 |
| ИНТЕРФЕРОН-ПОДОБНЫЙ БЕЛОК ZCYTO21 | 2001 |
|
RU2292394C2 |
| ПРИМЕНЕНИЕ ПЭГИЛИРОВАННЫХ ИНТЕРФЕРОНОВ ТИПА III ДЛЯ ЛЕЧЕНИЯ ГЕПАТИТА С | 2009 |
|
RU2496514C2 |
| КОМПОЗИЦИЯ ДЛЯ ИММУНИЗАЦИИ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ АЛЛЕРГИЧЕСКИХ ЭОЗИНОФИЛЬНЫХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2319503C2 |
| КОНЪЮГАТЫ ПЕПТИДА Melan-A, АНАЛОГА ВИРУСОПОДОБНОЙ ЧАСТИЦЫ | 2004 |
|
RU2351362C2 |
| НОВЫЕ РАСТВОРИМЫЕ ПОЛИПЕПТИДЫ CD83, КОМПОЗИЦИИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2009 |
|
RU2535340C2 |
| МУТАНТНЫЕ ПОЛИПЕПТИДЫ СУАА И ПРОИЗВОДНЫЕ ПОЛИПЕПТИДОВ, ПОДХОДЯЩИЕ ДЛЯ ДОСТАВКИ ИММУНОГЕННЫХ МОЛЕКУЛ В КЛЕТКУ | 2010 |
|
RU2585216C2 |
| РЕКОМБИНАНТНАЯ ВАКЦИНА ВИРУСА ЛЕЙКЕМИИ КОШЕК, СОДЕРЖАЩАЯ ОПТИМИЗИРОВАННЫЙ ГЕН ОБОЛОЧКИ ВИРУСА ЛЕЙКЕМИИ КОШЕК | 2012 |
|
RU2591817C2 |
| ИММУНОСУПРЕССОРНЫЕ ПОЛИПЕПТИДЫ И НУКЛЕИНОВЫЕ КИСЛОТЫ | 2008 |
|
RU2506275C2 |
| ВЫДЕЛЕННЫЙ РАСТВОРИМЫЙ IL-20 РЕЦЕПТОР (ВАРИАНТЫ) | 2000 |
|
RU2279441C2 |
Изобретение относится к области биотехнологии, в частности к генной инженерии, и может быть использовано в медикобиологической промышленности для получения активных препаратов интерлейкина-29 (IL-29). Предложены мутантные формы IL-29 (SEQ ID NO: 27, 29, 40, 41, 149 и 159) с заменой цистеинового остатка в положении, соответствующем положению 171 аминокислотной последовательности зрелого белка дикого типа, которые характеризуются корректным образованием внутримолекулярных дисульфидных связей и, соответственно, обеспечивают при экспрессии в гетерологичной системе получение полипептидов с антивирусной активностью в виде гомогенных препаратов. Описаны векторные конструкции и трансформированные этими конструкциями клетки-хозяева для экспрессии новых вариантов IL-29. 7 с. и 8 з.п. ф-лы, 37 табл.
1. Выделенный полипептид с антивирусной активностью, который характеризуется аминокислотной последовательностью, выбранной из группы, включающей SEQ ID NO: 27, 29, 40, 41, 149 и 159.
2. Полипептид по п.1, отличающийся тем, что полипептид обладает активностью против гепатита.
3. Полипептид по п.1, отличающийся тем, что полипептид обладает активностью против гепатита В.
4. Полипептид по п.1, отличающийся тем, что полипептид обладает активностью против гепатита С.
5. Производное полипептида по п.1, характеризующееся тем, что оно состоит из полипептида по п.1 и полиэтиленгликолевой группы, ковалентно присоединенной к N-концу полипептида.
6. Производное полипептида по п.5, отличающееся тем, что полиэтиленгликолевой группой является mPEG/пропионовый альдегид.
7. Производное полипептида по п.6, отличающееся тем, что mPEG/пропионовый альдегид имеет молекулярную массу приблизительно 20 кДа.
8. Производное полипептида по п.6, отличающееся тем, что mPEG/пропионовый альдегид является линейным.
9. Выделенный полинуклеотид, кодирующий полипептид с антивирусной активностью и характеризующийся нуклеотидной последовательностью, которая определяет аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO: 27, 29, 40, 41, 149 и 159.
10. Выделенный полинуклеотид по п.9, отличающийся тем, что кодируемый полипептид обладает активностью против гепатита В.
11. Выделенный полинуклеотид по п.9, отличающийся тем, что кодируемый полипептид обладает активностью против гепатита С.
12. Экспрессирующий вектор, который включает следующие операбельно связанные элементы:
промотор транскрипции;
сегмент ДИК, по существу соответствующий выделенному полину клеотиду по п.9; и
терминатор транскрипции.
13. Культивируемая клетка, в которую введен экспрессирующий вектор по п.12 и которая экспрессирует полипептид с антивирусной активностью.
14. Способ получения полипептида с антивирусной активностью, включающий:
культивирование клетки по п.13 в подходящих для экспрессии указанного полипептида условиях и выделение экспрессированного полипептида.
15. Композиция с антивирусной активностью, содержащая терапевтически эффективное количество полипептида, обладающего указанной активностью, и фармацевтически приемлемый носитель, отличающаяся тем, что полипептид выбран из группы, включающей SEQ ID NO: 27, 29, 40, 41, 149 и 159.
Приоритет по пунктам и признакам:
07.08.2003 по пп.1-15, SEQ ID NO: 27, 29, 40, 41;
09.08.2004 по пп.1-15, SEQ ID NO: 149, 159.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| RAJARATHNAM К | |||
| ЕТ AL., Biochemistry, 38, no | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| WO 2004037995 A, 06.05.2004. | |||
Авторы
Даты
2009-11-10—Публикация
2004-08-09—Подача