Настоящее изобретение относится к промежуточным продуктам для нового и эффективного синтеза конечных продуктов, в которых фармакофоры хинолона и оксазолидинона соединены между собой химически стабильным линкером. Конечные продукты подобного типа, описанные в WO 03/032962, отличаются высокой эффективностью по отношению к бактериям в организме человека и животных. Настоящее изобретение относится далее к новому и эффективному синтезу этих промежуточных продуктов, а также конечных продуктов.
Настоящее изобретение относится к соединениям формулы (ZP)
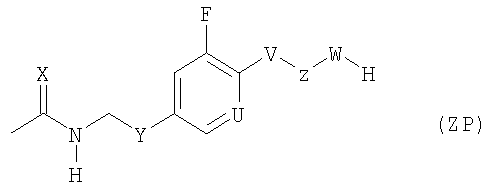 ,
,
в которой U обозначает атом азота или группу СН,
V обозначает атом кислорода, атом серы или группу формулы CR6R7,
W обозначает связь, атом кислорода, атом серы, группу формулы NR8, необязательно замещенную циклоалкиленовую, гетероциклоалкиленовую, алкилциклоалкиленовую, гетероалкилциклоалкиленовую, ариленовую, гетероариленовую, аралкиленовую или гетероаралкиленовую группу,
Х обозначает атом кислорода или атом серы,
Y выбран из группы, включающей
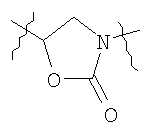 ,
, 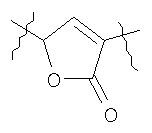 ,
, 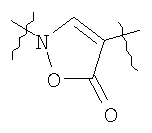 ,
,
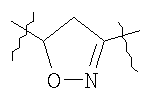 ,
, 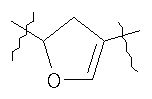 ,
, 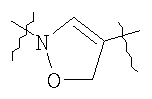 ,
,
Z обозначает необязательно замещенную алкиленовую, алкениленовую, алкиниленовую, гетероалкиленовую, циклоалкиленовую, гетероциклоалкиленовую, алкилциклоалкиленовую, гетероалкилциклоалкиленовую, ариленовую, гетероариленовую, аралкиленовую или гетероаралкиленовую группу, остатки R6 и R7 независимо друг от друга представляют собой атом водорода, атом галогена, гидрокси-, амино-, нитро- или тиоловую группу, необязательно замещенный алкильный, алкенильный, алкинильный, гетероалкильный, арильный, гетероарильный, циклоалкильный, алкилциклоалкильный, гетероалкилциклоалкильный, гетероциклоалкильный, аралкильный или гетероаралкильный остаток,
R8 представляет собой атом водорода, необязательно замещенный алкильный, алкенильный, алкинильный, гетероалкильный, арильный, гетероарильный, циклоалкильный, алкилциклоалкильный, гетероалкилциклоалкильный, гетероциклоалкильный, аралкильный или гетероаралкильный остаток.
Под понятием "алкил" подразумевается насыщенная прямоцепочечная либо разветвленная углеводородная группа, содержащая 1-20, предпочтительно 1-12, особенно предпочтительно 1-6, атомов углерода, например метильная, этильная, пропильная, изопропильная, н-бутильная, изобутильная, трет-бутильная, н-пентильная, н-гексильная или 2,2-диметилбутильная группа.
Под понятиями "алкенил" и "алкинил" подразумеваются по меньшей мере частично ненасыщенные прямоцепочечные либо разветвленные углеводородные группы, содержащие 2-20, предпочтительно 2-12, особенно предпочтительно 2-6, атомов углерода, например этенильная, аллильная, ацетиленильная, пропаргильная, изопренильная или гекс-2-енильная группа. Предпочтительно алкенильные группы содержат одну или две (особенно предпочтительно одну) двойные связи, а алкинильные группы содержат одну или две (особенно предпочтительно одну) тройные связи.
Под понятиями "алкил", "алкенил" и "алкинил" подразумеваются, кроме того, группы, в которых один либо несколько атомов водорода независимо друг от друга заменен(ы) на атом(ы) галогена (предпочтительно F или Cl), такие, например, группы, как 2,2,2-трихлорэтильная или трифторметильная группа.
Под понятием "гетероалкил" подразумевается алкильная, алкенильная или алкинильная группа (например, гетероалкенильная, соответственно гетероалкинильная), в которой один либо несколько атомов углерода (предпочтительно 1, 2 или 3) независимо друг от друга заменен(ы) на атом(ы) кислорода, азота, фосфора, бора, селена, кремния или серы (предпочтительно кислорода, серы или азота). Под понятием "гетероалкил" подразумевается, кроме того, карбоновая кислота или группа - производное карбоновой кислоты, такая, например, как ацил, ацилалкил, алкоксикарбонил, ацилоксигруппа, ацилоксиалкил, карбоксиалкиламид или алкоксикарбонилоксигруппа.
В качестве примеров гетероалкильных групп можно назвать группы формул Ra-О-Ya-, Ra-S-Ya-, Ra-N(Rb)-Ya-, Ra-СО-Ya-, Ra-O-CO-Ya-, Ra-СО-О-Ya-, Ra-СО-N(Rb)-Ya-, Ra-N(Rb)-СО-Ya-, Ra-О-СО-N(Rb)-Ya-, Ra-N(Rb)-CO-O-Ya-, Ra-N(Rb)-CO-N(Rc)-Ya-, Ra-О-СО-О-Ya-, Ra-N(Rb)-C(=NRd)-N(Rc)-Ya-, Ra-CS-Ya-, Ra-O-CS-Ya-, Ra-CS-O-Ya-, Ra-CS-N(Rb)-Ya-, Ra-N(Rb)-CS-Ya-, Ra-О-CS-N(Rb)-Ya-, Ra-N(Rb)-CS-О-Ya-, Ra-N(Rb)-CS-N(Rc)-Ya-, Ra-O-CS-O-Ya-, Ra-S-CO-Ya-, Ra-CO-S-Ya-, Ra-S-CO-N(Rb)-Ya-, Ra-N(Rb)-CO-S-Ya-, Ra-S-CO-O-Ya-, Ra-O-CO-S-Ya-, Ra-S-CO-S-Ya-, Ra-S-CS-Ya-, Ra-CS-S-Ya-, Ra-S-CS-N(Rb)-Ya-, Ra-N(Rb)-CS-S-Ya-, Ra-S-CS-O-Ya-, Ra-O-CS-S-Ya-, где Ra обозначает атом водорода, C1-С6алкильную, С2-С6алкенильную или С2-С6алкинильную группу, Rb обозначает атом водорода, C1-С6алкильную, С2-С6алкенильную или С2-С6алкинильную группу, Rc обозначает атом водорода, C1-С6алкильную, С2-С6алкенильную или С2-С6алкинильную группу, Rd обозначает атом водорода, C1-С6алкильную, С2-С6алкенильную или С2-С6алкинильную группу, a Y3 обозначает прямую связь, C1-С6алкиленовую, С2-С6алкениленовую или С2-С6алкиниленовую группу, при этом каждая гетероалкильная группа содержит по меньшей мере один атом углерода и один либо несколько атомов водорода может(гут) быть заменен(ы) на атом(ы) фтора или хлора. Конкретно в качестве гетероалкильных групп можно назвать среди прочих метокси-, трифторметокси-, этокси-, н-пропилокси-, изопропилокси-, трет-бутилоксигруппу, метоксиметил, этоксиметил, метоксиэтил, метиламино-, этиламино-, диметиламино-, диэтиламино-, изопропилэтиламиногруппу, метиламинометил, этиламинометил, диизопропиламиноэтил, простой енольный эфир, диметиламинометил, диметиламиноэтил, ацетил, пропионил, бутирилокси-, ацетилоксигруппу, метоксикарбонил, этоксикарбонил, N-этил-N-метилкарбамоил или N-метилкарбамоил. В качестве других примеров гетероалкильных групп можно назвать нитрильные, изонитрильные, цианатные, тиоцианатные, изоцианатные, изотиоцианатные и алкилнитрильные группы. Одним из примеров гетероалкиленовой группы является группа формулы -СН2СН(ОН)-.
Под понятием "циклоалкил" подразумевается насыщенная либо частично ненасыщенная (например, циклическая группа, содержащая одну, две или несколько двойных связей, такая как циклоалкенильная группа) циклическая группа с одним либо несколькими циклами (предпочтительно 1 или 2), содержащими 3-14 атомов углерода в цикле, предпочтительно 3-10 (прежде всего 3, 4, 5, 6 или 7), атомов углерода в цикле. Под понятием "циклоалкил" подразумеваются также соответствующие группы, в которых один либо несколько атомов водорода независимо друг от друга заменен(ы) на атом(ы) фтора, хлора, брома либо иода или на группу(ы) ОН, =O, SH, =S, NH2, =NH либо NO2, т.е., например, циклические кетоны, такие как циклогексанон, 2-циклогексанон или циклопентанон. В качестве других конкретных циклоалкильных групп можно назвать, например, циклопропильную, циклобутильную, циклопентильную, спиро[4,5]деканильную, норборнильную, циклогексильную, циклопентенильную, циклогексадиенильную, декалинильную, бицикло[4.3.0]нонильную, тетралинильную, циклопентилциклогексильную, фторциклогексильную или циклогекс-2-енильную группу.
Под понятием "гетероциклоалкил" подразумевается циклоалкильная группа из числа вышеназванных, в которой один либо несколько (предпочтительно 1, 2 или 3) атомов углерода в цикле независимо друг от друга заменен(ы) на атом(ы) кислорода, азота, кремния, селена, фосфора или серы (предпочтительно кислорода, серы или азота). Предпочтительно гетероциклоалкильная группа содержит 1 или 2 цикла с 3-10 (прежде всего 3, 4, 5, 6 или 7) атомами в цикле. Под понятием "гетероциклоалкил" подразумеваются, кроме того, группы, в которых один либо несколько атомов водорода независимо друг от друга заменен(ы) на атом(ы) фтора, хлора, брома либо иода или на группу(ы) ОН, =O, SH, =S, NH2, =NH или NO2. В качестве примеров можно назвать пиперидильную, пиперазинильную, морфолинильную, уротропинильную, пирролидинильную, тетрагидротиофенильную, тетрагидропиранильную, тетрагидрофурильную или 2-пиразолинильную группу, а также лактамы, лактоны, циклические имиды и циклические ангидриды.
Под понятием "алкилциклоалкил" подразумеваются группы, которые в соответствии с раскрытыми выше значениями содержат как циклоалкильные, так и алкильные, алкенильные или алкинильные группы, например алкилциклоалкильные, циклоалкилалкильные, алкилциклоалкенильные, алкенилциклоалкильные и алкинилциклоалкильные группы. Предпочтительно алкилциклоалкильная группа содержит циклоалкильную группу с одной либо двумя циклическими системами, содержащими 3-10 (прежде всего 3, 4, 5, 6 или 7) атомов углерода и одну либо две алкильные, алкенильные или алкинильные группы с 1 или 2-6 атомами углерода.
Под понятием "гетероалкилциклоалкил" подразумеваются алкилциклоалкильные группы из числа вышеназванных, в которых один либо несколько (предпочтительно 1, 2 или 3) атомов углерода независимо друг от друга заменен(ы) на атом(ы) кислорода, азота, кремния, селена, фосфора или серы (предпочтительно кислорода, серы или азота). Предпочтительно гетероалкилциклоалкильная группа содержит 1 либо 2 циклические системы с 3-10 (прежде всего 3, 4, 5, 6 или 7) атомами в цикле и одну либо две алкильные, алкенильные, алкинильные или гетероалкильные группы с 1 или 2-6 атомами углерода. В качестве примеров подобных групп можно назвать алкилгетероциклоалкил, алкилгетероциклоалкенил, алкенилгетероциклоалкил, алкинилгетероциклоалкил, гетероалкилциклоалкил, гетероалкилгетероциклоалкил и гетероалкилгетероциклоалкенил, при этом циклические группы являются насыщенными либо одно-, дву- или трехкратно ненасыщенными.
Под понятием "арил" (краткое обозначение Ar) подразумевается ароматическая группа, содержащая один либо несколько циклов с 6-14 атомами углерода, предпочтительно 6-10 (прежде всего 6) атомами углерода в цикле. Под понятием "арил" (Ar) подразумеваются, кроме того, группы, в которых один либо несколько атомов водорода независимо друг от друга заменен(ы) на атом(ы) фтора, хлора, брома либо иода или на группу(ы) ОН, SH, NH2 или NO2. В качестве примеров можно назвать фенильную, нафтильную, бифенильную, 2-фторфенильную, анилиновую, 3-нитрофенильную или 4-гидроксифенильную группу.
Под понятием "гетероарил" подразумевается ароматическая группа, содержащая один либо несколько циклов с 5-14, предпочтительно 5-10 (прежде всего 5 или 6), атомами в цикле и одним либо несколькими (предпочтительно 1, 2, 3 или 4) атомами кислорода, азота, фосфора или серы в цикле (предпочтительно О, S или N). Под понятием "гетероарил" подразумеваются, кроме того, группы, в которых один либо несколько атомов водорода независимо друг от друга заменен(ы) на атом(ы) фтора, хлора, брома либо иода или на группу(ы) ОН, SH, NH2 либо NO2. В качестве примеров можно назвать 4-пиридильную, 2-имидазолильную, 3-фенилпирролильную, тиазолильную, оксазолильную, триазолильную, тетразолильную, изоксазолильную, индазолильную, индолильную, бензимидазолильную, пиридазинильную, хинолинильную, пуринильную, карбазолильную, акридинильную, пиримидильную, 2,3'-бифурильную, 3-пиразолильную и изохинолинильную группы.
Под понятием "аралкил" подразумеваются группы, которые в соответствии с раскрытыми выше значениями содержат как арильные, так и алкильные, алкенильные, алкинильные и/или циклоалкильные группы, такие, например, как арилалкильные, арилалкенильные, арилалкинильные, арилциклоалкильные, арилциклоалкенильные, алкиларилциклоалкильные и алкиларилциклоалкенильные группы. Конкретно в качестве аралкилов можно назвать, например, толуол, ксилол, мезитилен, стирол, бензилхлорид, о-фтортолуол, 1H-инден, тетралин, дигидронафталин, инданон, фенилциклопентил, кумол, циклогексилфенил, флуорен и индан. Предпочтительно аралкильная группа содержит одну либо две ароматические циклические системы (1 или 2 цикла) с 6-10 атомами углерода и одну либо две алкильные, алкенильные и/или алкинильные группы с 1 или 2-6 атомами углерода и/или циклоалкильную группу с 5 или 6 атомами углерода в цикле.
Под понятием "гетероаралкил" подразумевается аралкильная группа из числа выше названных, в которой один либо несколько (предпочтительно 1, 2, 3 или 4) атомов углерода независимо друг от друга заменен(ы) на атом(ы) кислорода, азота, кремния, селена, фосфора, бора или серы (предпочтительно кислорода, серы или азота), т.е. подразумеваются группы, которые в соответствии с раскрытыми выше значениями содержат как арильные, соответственно гетероарильные, так и алкильные, алкенильные, алкинильные и/или гетероалкильные, и/или циклоалкильные, и/или гетероциклоалкильные группы. Предпочтительно гетероаралкильная группа содержит одну либо две ароматические системы (1 или 2 цикла) с 5 или 6-10 атомами углерода в цикле и одну либо две алкильные, алкенильные и/или алкинильные группы с 1 или 2-6 атомами углерода, и/или одну циклоалкильную группу с 5 или 6 атомами углерода в цикле, при этом 1, 2, 3 или 4 таких атомов углерода независимо друг от друга заменен(ы) на атом(ы) кислорода, серы или азота.
В качестве примеров можно назвать арилгетероалкильные, арилгетероциклоалкильные, арилгетероциклоалкенильные, арилалкилгетероциклоалкильные, арилалкенилгетероциклоалкильные, арилалкинилгетероциклоалкильные, арилалкилгетероциклоалкенильные, гетероарилалкильные, гетероарилалкенильные, гетероарилалкинильные, гетероарилгетероалкильные, гетероарилциклоалкильные, гетероарилциклоалкенильные, гетероарилгетероциклоалкильные, гетероарилгетероциклоалкенильные, гетероарилалкилциклоалкильные, гетероарилалкилгетероциклоалкенильные, гетероарилгетероалкилциклоалкильные, гетероарилгетероалкилциклоалкенильные и гетероарилгетероалкилгетероциклоалкильные группы, при этом циклические группы являются насыщенными либо одно-, дву- или трехкратно ненасыщенными. Конкретно в качестве примеров можно назвать тетрагидроизохинолинильную, бензоильную, 2- либо 3-этилиндолильную, 4-метилпиридино-, 2-, 3- либо 4-метоксифенильную, 4-этоксифенильную, 2-, 3-либо 4-карбоксифенилалкильную группу.
Под понятиями "алкил", "алкенил", "алкинил", "гетероалкил", "циклоалкил", "гетероциклоалкил", "алкилциклоалкил", "гетероалкилциклоалкил", "арил", "гетероарил", "аралкил" и "гетероаралкил" подразумеваются также группы, в которых один либо несколько атомов водорода независимо друг от друга заменен(ы) на атом(ы) фтора, хлора, брома либо иода или на группу(ы) ОН, =O, SH, =S, NH2, =NH либо NO2.
Под понятием "необязательно замещенные" имеются в виду группы, в которых один либо несколько атомов водорода независимо друг от друга заменен(ы) на атом(ы) фтора, хлора, брома либо иода или на группу(ы) ОН, =O, SH, =S, NH2, =NH либо NO2. Указанное понятие относится далее к группам, которые замещены незамещенными C1-С6алкильными, С2-С6алкенильными, С2-С6алкинильными, C1-С6гетероалкильными, С3-С10циклоалкильными, С2-С9гетероциклоалкильными,
С6-С10арильными, С1-С9гетероарильными, С7-С12аралкильными или С2-С11гетероаралкильными группами.
Описанные в настоящей заявке соединения благодаря схеме своего замещения могут содержать один или несколько хиральных центров. В объем настоящего изобретения включены в соответствии с этим как все чистые энантиомеры и все чистые диастереомеры, так и их смеси в любом соотношении данных компонентов. В объем настоящего изобретения включены также все цис- и транс-изомеры соединений общей формулы (I), равно как и их смеси. В объем настоящего изобретения включены далее все таутомерные формы описанных соединений
Предпочтительно U обозначает группу СН. Также предпочтительно R6 и R7 представляют собой атомы водорода. Предпочтительно далее V обозначает атом кислорода. Предпочтительно также Y обозначает структурный фрагмент следующей формулы:
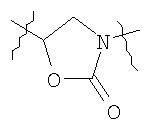 .
.
Предпочтительно далее W обозначает атом кислорода, атом серы, группу формулы NR8, необязательно замещенную гетероциклоалкиленовую, гетероалкилциклоалкиленовую, гетероариленовую или гетероаралкиленовую группу, при этом связанный с группой W Н-атом предпочтительно связан с атомом кислорода, атомом серы или атомом азота.
W, кроме того, предпочтительно обозначает необязательно замещенную гетероциклоалкиленовую группу, содержащую цикл с 4, 5, 6 или 7 атомами в цикле, прежде всего W замещена ОН-группой.
Предпочтительно далее Z обозначает необязательно замещенную С1-С4алкиленовую группу. Особенно предпочтительно Z обозначает группу СН2 или группу СН2СН2.
Предпочтительным значением W помимо указанных является пиперидинильная или пирролидинильная группа, причем эти группы необязательно могут быть замещены группами ОН, ОРО3Н2, OSO3H либо гетероалкильной группой, которая несет по меньшей мере одну ОН-, NH2-, SO3H-, РО3Н2- или СООН-группу (прежде всего ОН-группу).
Особенно предпочтительно Z и W совместно образуют группу формулы:
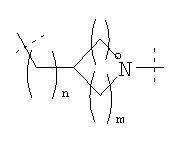 .
.
где n обозначает 1 или 2, m обозначает 1 или 2 и о обозначает 1 или 2, при этом данная группа необязательно может быть замещена группой ОН, ОРО3Н2, OSO3H либо гетероалкильной группой, которая несет по меньшей мере одну ОН-, NH2-, SO3H-, РО3Н2- или СООН-группу.
Особенно предпочтительно W имеет следующую структурную формулу:
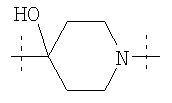 или
или 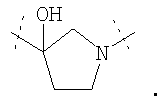
Соединения формулы (ZP) могут использоваться при синтезе соединений формулы (I)
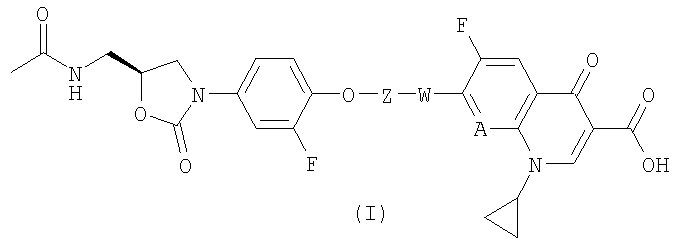
где Z обозначает необязательно замещенную С1-С4алкиленовую группу, А обозначает атом азота или группу СН и W обозначает необязательно замещенную гетероциклоалкиленовую группу, содержащую по меньшей мере один атом азота, и при этом хинолиновый остаток связан с указанным атомом азота.
Соединения формулы (I) можно получать следующим образом:
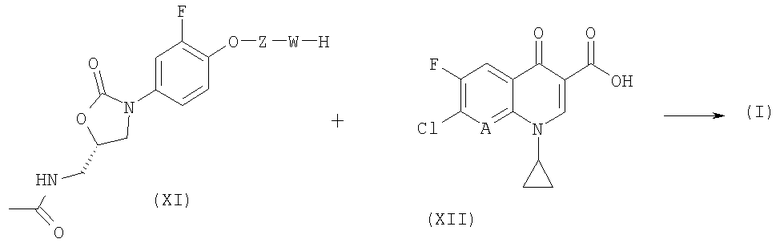
при этом соединение формулы (XI) представляет собой соединение, предлагаемое в настоящем изобретении, а соединение формулы (XII) предпочтительно использовать в виде комплексного соединения бора (например, в виде бордиацетатного комплекса).
При осуществлении этой реакции предпочтительны условия, где предусматривается использовать N-метилпирролидон, триметилсилилхлорид, основание Хюнига или К2СО3, а температура составляет 80°С.
Предлагаемые в изобретении соединения можно синтезировать, например, следующим путем:
Стадия 1:
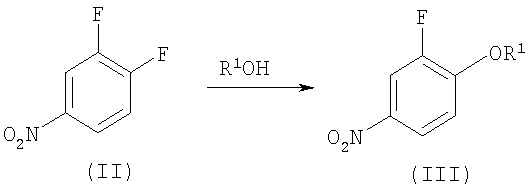
Стадия 2:
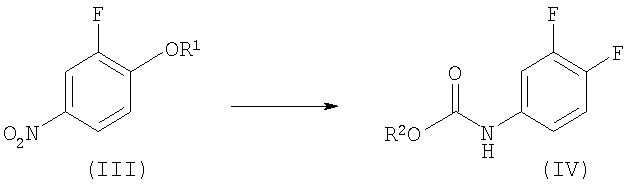
Стадия 3:
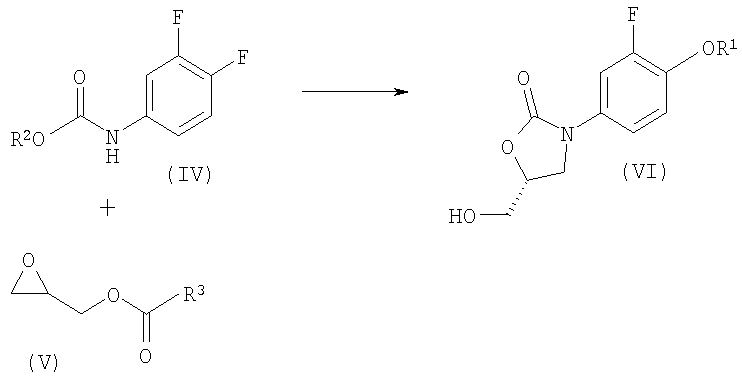
Стадия 4:
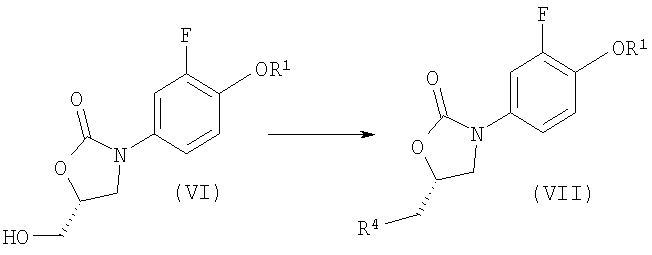
Стадия 5:
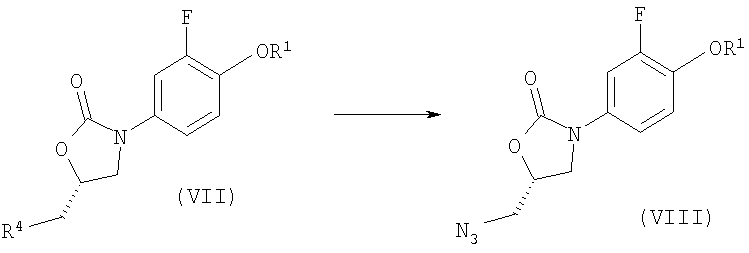
Стадия 6:
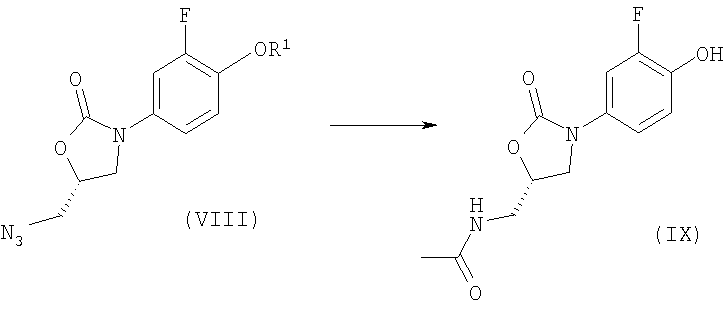
Стадия 7:
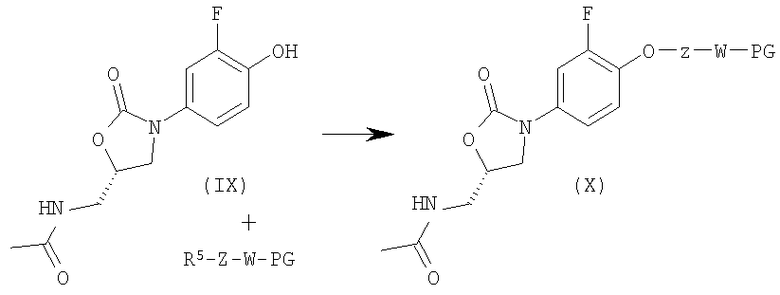
Стадия 8:
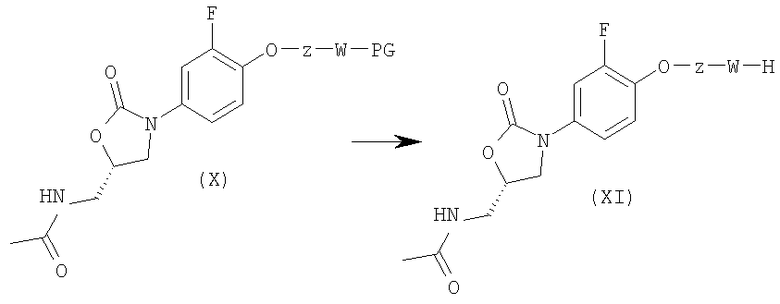
Согласно другому варианту соединения формулы (ZP), соответственно формулы (XI) можно синтезировать следующим путем:
Стадия 1:
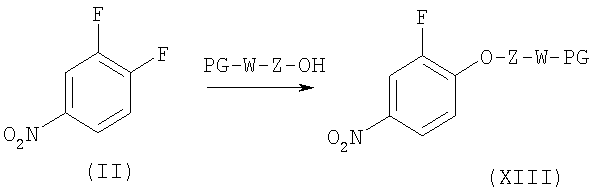
Стадия 2:
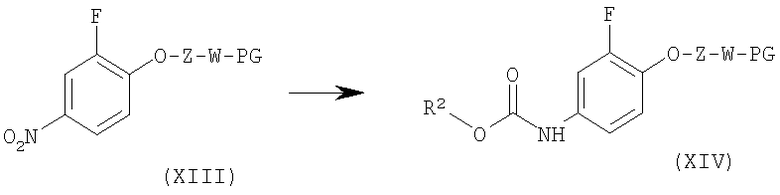
Стадия 3:
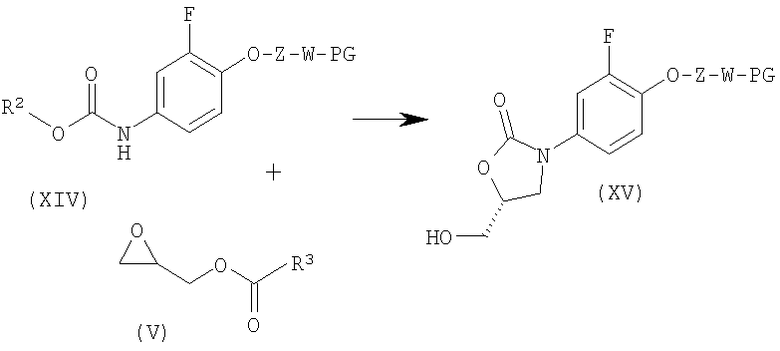
Стадия 4:
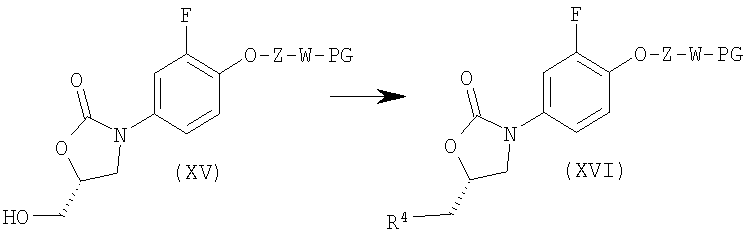
Стадия 5:
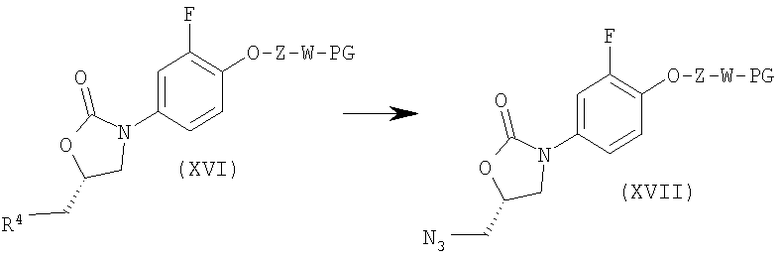
Стадия 6:
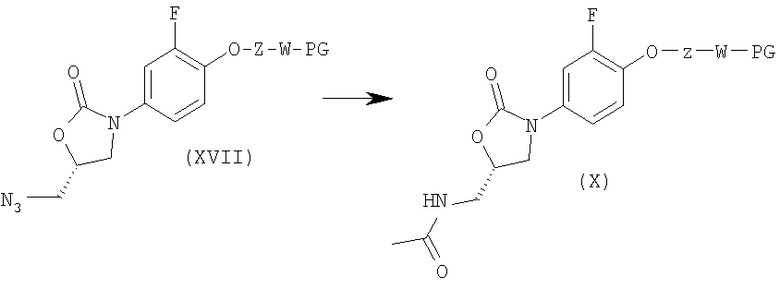
Стадия 7:
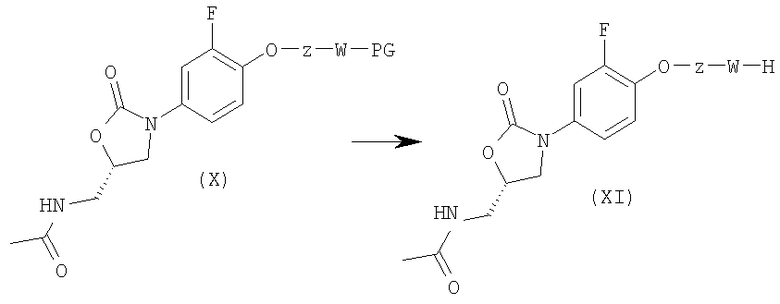
Если в этом варианте синтеза в качестве защитной группы PG выбирать защитную группу Cbz, то необходимость в проведении стадии 7 отпадает, поскольку в данном случае соединение формулы (XI) непосредственно образуется на стадии 6.
При этом PG представляет собой обычную защитную группу для аминов, прежде всего бензилоксикарбонильную (Cbz) группу,
R1 представляет собой необязательно замещенную бензильную (например, n-метоксибензильную) или аллильную группу,
R2 представляет собой С1-С4алкильную, аллильную или бензильную группу,
R3 представляет собой С1-С4алкильную группу,
R4 представляет собой мезилокси-, тозилокси-, трифлилокси- либо тексилоксигруппу или атом хлора, брома либо иода и
R5 представляет собой мезилокси-, тозилокси-, трифлилокси- либо тексилоксигруппу или атом хлора, брома либо иода.
Защитные группы специалисту в данной области известны и описаны, например, у P.J.Kocienski в "Protecting Groups", изд-во Georg Thieme Verlag, Stuttgart, 1994, а также у T.W.Greene, P.G.M. Wuts в "Protective Groups in Organic Synthesis", изд-во John Wiley & Sons, New York, 1999. В качестве обычно используемых аминозащитных групп можно назвать, например, трет-бутилоксикарбонильную (Boc), бензилоксикарбонильную (Cbz, Z), бензильную (Bn), бензоильную (Bz), флуоренилметилоксикарбонильную (Fmoc), аллилоксикарбонильную (Alloc), трихлорэтоилксикарбонильную (Troc), ацетильную или трифторацетильную группы.
Предпочтительно R1 представляет собой бензильную группу.
Предпочтительно R2 представляет собой бензильную группу.
Предпочтительно R3 представляет собой н-пропильную группу.
Предпочтительно R4 представляет собой мезилоксигруппу.
Предпочтительно R5 представляет собой мезилоксигруппу.
При осуществлении синтеза согласно первому варианту предпочтительно работать при соблюдении следующих условий с использованием указанных компонентов.
На стадии 1: CH2Cl2, гидроксид калия, комнатная температура.
На стадии 2: водород/Pt/C, затем Cbz-Cl, NaHCO3, ацетон/вода, и то, и другое при комнатной температуре.
На стадии 3: (R)-глицидилбутират (V), н-бутиллитий, -60°С, соответственно ДАЛ (диизопропиламид лития), -15°С.
На стадии 4: метилсульфонилхлорид, триэтиламин, CH2Cl2.
На стадии 5: NaN3 в ДМФ, каталитические количества Bu4NI, 90°C.
На стадии 6: водород/Pd(ОН)2, ТГФ, МеОН, затем АсОН, Ас2О, и то, и другое при комнатной температуре.
На стадии 7: диметилформамид (ДМФ), гидрид натрия, 70°С.
На стадии 8: H2/Pd(OH)2, ТГФ, метанол, комнатная температура.
При осуществлении синтеза согласно второму варианту предпочтительно работать при соблюдении следующих условий с использованием указанных компонентов.
На стадии 1: реакция Мицунобу или основание (например, NaH), ДМФ, тозилат PG-W-Z-OH.
На стадии 2: водород/Pt/C, затем Cbz-Cl, NaHCO3, ацетон/вода, и то, и другое при комнатной температуре или Sn, HCl.
На стадии 3: (R)-глицидилбутират (V), н-бутиллитий, -60°С, соответственно ДАЛ (диизопропиламид лития), -15°С.
На стадии 4: метилсульфонилхлорид, триэтиламин, CH2Cl2.
На стадии 5: NaN3 в ДМФ, каталитические количества Bu4NI, 90°С.
На стадии 6: водород/Pd(ОН)2, ТГФ, МеОН, затем АсОН, Ас2О, и то, и другое при комнатной температуре.
В представленных далее примерах более подробно описывается синтез соединений формулы (ZP), а также их применение для синтеза соединений формулы (I).
Примеры
Пример 1
7-(4-{4-[(5S)-5-(Ацетиламинометил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота
Стадия 1: бензиловый эфир (4-бензилокси-3-фторфенил)карбаминовой кислоты
Смесь из 34,9 г 1-бензилокси-2-фтор-4-нитробензола (WO 03064413) (мол. масса 247,28, 141 ммоль) и 340 мг платины (5%-ной на активированном угле) в 350 мл этилацетата перемешивали в атмосфере водорода при комнатной температуре (КТ) и нормальном давлении. Течение реакции отслеживали с помощью ЖХВР (жидкостной хроматографии высокого разрешения), и по истечении 20 ч реакция завершалась. Катализатор отфильтровывали и фильтрат при пониженном давлении концентрировали досуха центрифугированием. Маслянистый остаток растворяли в 500 мл ацетона и смешивали с 250 мл насыщенного раствора гидрокарбоната натрия и 17,5 г гидрокарбоната натрия (мол. масса 84,01, 208 ммолей). Затем смесь охлаждали до 5°С и к ней по каплям добавляли 26,08 г бензилхлорформиата (мол. масса 170,59, 152 ммоля). После этого смесь в течение 2 ч перемешивали при КТ и течение реакции отслеживали с помощью ТХ (тонкослойной хроматографии) (гексан/этилацетат в соотношении 3:1). Ацетон удаляли при пониженном давлении, остаток смешивали с 500 мл воды и твердое вещество отфильтровывали.
Образовавшиеся кристаллы промывали 500 мл воды и сушили. Выход 48,05 г, 95,8%. МС: 352,5 (М+Н)+, 350,8 (М-Н)-. Метод: ESI+, ESI-.
Стадия 2: (5R)-3-(4-бензилокси-3-фторфенил)-5-гидроксиметилоксазолидин-2-он
Перемешанный раствор 17,5 г бензилового эфира (4-бензилокси-3-фторфенил)карбаминовой кислоты (мол. масса 351,38, 50 ммолей) в 30 мл сухого тетрагидрофурана охлаждали с помощью ванны из сухого льда и ацетона до -78°С. Затем по каплям добавляли 22,8 мл 2,3-молярного раствора н-бутиллития в н-гексане (52,5 ммоля) и смесь при -78°С перемешивали в течение 15 мин. Далее добавляли 7,92 г R(-)-глицидилбутирата (мол. масса 144,17, 60 ммолей) и реакционную смесь нагревали до КТ. Реакцию отслеживали с помощью ЖХВР, затем ее добавлением насыщенного раствора хлорида аммония прекращали и смесь разбавляли 100 мл этилацетата. Органическую фазу промывали 200 мл воды и 200 мл насыщенного раствора поваренной соли. Органическую фазу сушили над сульфатом магния, фильтровали и фильтрат концентрировали при пониженном давлении. Остаток кристаллизовали из 200 мл этилацетата/гексана (в соотношении 1:1). Полученное твердое вещество перекристаллизовывали из 150 мл этилацетата/дихлорметана (в соотношении 9:1). Бесцветные кристаллы собирали и сушили. Выход 10,4 г, 65,5%. МС: 318,1 (М+Н)+. Метод: ESI+.
Стадия 3: (5S)-5-азидометил-3-(4-бензилокси-3-фторфенил)оксазолидин-2-он
Смесь из 10 г (5R)-3-(4-бензилокси-3-фторфенил)-5-гидроксиметилоксазолидин-2-она (мол. масса 317,32, 31,51 ммоля) и 4,78 г триэтиламина (мол. масса 101,19, 47,26 ммоля) в 300 мл дихлорметана смешивали при 10°С при перемешивании с 4,32 г метансульфонилхлорида (мол. масса 114,55, 37,82 ммоля). Реакционную смесь перемешивали при КТ в течение 1 ч и течение реакции отслеживали с помощью ТХ (этилацетат/гексан в соотношении 1:1). Реакцию прекращали добавлением 100 мл воды и органическую фазу промывали 100 мл насыщенного раствора поваренной соли. Затем органическую фазу сушили над сульфатом магния, фильтровали и фильтрат концентрировали при пониженном давлении. Образовавшийся остаток растворяли в 100 мл диметилформамида и к раствору добавляли 5,12 г азида натрия (мол. масса 65,01, 78,7 ммоля) и каталитическое количество иодида тетрабутиламмония. Суспензию перемешивали в течение ночи при 90°С. Течение реакции отслеживали с помощью ЖХВР. Диметилформамид при пониженном давлении удаляли центрифугированием, остаток растворяли в 200 мл дихлорметана и органическую фазу последовательно промывали 100 мл воды и 100 мл насыщенного раствора поваренной соли. Дихлорметановый раствор сушили над сульфатом магния, фильтровали и фильтрат концентрировали при пониженном давлении. Остаток кристаллизовали из 150 мл этилацетата/гексана (в соотношении 1:1). Выход 10,4 г, 97%. МС: 343,1 (М+Н)+. Метод: ESI+.
Стадия 4: N-[(5S)-{3-(3-фтор-4-гидроксифенил)}-2-оксооксазолидин-5-илметил]ацетамид
Суспензию 10,4 г (5S)-5-азидометил-3-(4-бензилокси-3-фторфенил)оксазолидин-2-она (мол. масса 342,33, 30,38 ммоля) и 1,5 г палладия (10%-ного на активированном угле) в 400 мл смеси метанола и этилацетата в соотношении 1:1 перемешивали при комнатной температуре в атмосфере водорода в течение двух дней. Затем катализатор отфильтровывали и фильтрат упаривали при пониженном давлении. Остаток растворяли в 100 мл уксусной кислоты и смешивали с 3,72 г ангидрида уксусной кислоты (мол. масса 102,09, 36,45 ммоля). Растворитель при пониженном давлении выпаривали и остаток перекристаллизовывали из смеси этилацетата и гексана (в соотношении 1:1). Выход 6,76 г, 83%. МС: 269,4 (М+Н)+, 267,3 (М-Н)-. Метод: ESI+, ESI-.
Стадия 5: бензиловый эфир 4-{4-[(5S)-5-(ацетиламинометил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-карбоновой кислоты
Суспензию 22,72 г бензилового эфира 1-окса-6-азаспиро[2,5]октан-6-карбоновой кислоты (WO 9803507) (мол. масса 247,29, 92 ммоля), 21,45 г N-[(5S)-{3-(3-фтор-4-гидроксифенил)}-2-оксооксазолидин-5-илметил]ацетамида (мол. масса 268,246, 80 ммолей) и 16,58 г карбоната калия (мол. масса 138,20, 120 ммолей) в 150 мл диметилформамида перемешивали при 100°С в течение 7 ч. Течение реакции отслеживали с помощью ТХ (дихлорметан/метанол в соотношении 9:1). Диметилформамид при пониженном давлении выпаривали и остаток растворяли в 600 мл смеси дихлорметана и метанола в соотношении 9:1.
Органическую фазу промывали 400 мл воды и 400 мл насыщенного раствора поваренной соли, сушили с помощью сульфата магния, фильтровали и фильтрат разбавляли 250 мл этилацетата. Затем смесь концентрировали при пониженном давлении до конечного объема 400 мл. Далее смесь в течение ночи перемешивали при КТ. Образовавшиеся кристаллы отфильтровывали и последовательно промывали 150 мл этилацетата и 100 мл пентана. Выход 31,65 г, 76,7%. МС: 516,8 (М+Н)+. Метод: ESI+.
Стадия 6: N-[{(5S)-3-[3-фтор-4-(4-гидроксипиперидин-4-илметокси)фенил]-2-оксооксазолидин-5-илметил}]ацетамид
Суспензию 31 г бензилового эфира 4-{4-[(5S)-5-(ацетиламинометил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-карбоновой кислоты (мол. масса 515,54, 60,13 ммоля) и 2,5 г палладия (10%-ного на активированном угле) в 310 мл метанола и 150 мл этилацетата перемешивали в течение 4 ч в атмосфере водорода. Течение реакции отслеживали с помощью ТХ (с использованием этилацетата). Затем суспензию разбавляли 300 мл метанола, нагревали до 40°С и катализатор отфильтровывали через стекловолокнистую фильтровальную бумагу. Фильтрат концентрировали до объема 150 мл, разбавляли 300 мл этилацетата и повторно концентрировали до объема 200 мл. Далее добавляли 200 мл диэтилового эфира и суспензию охлаждали при перемешивании до 0°С. Твердое вещество собирали и сушили. Выход 21,6 г, 94,3%. МС: 382,6 (М+Н)+. Метод: ESI+.
Стадия 7:
7-(4-{4-[(5S)-5-(ацетиламинометил)-2-оксооксазолидин-3-ил]-2-фторфеноксиметил}-4-гидроксипиперидин-1-ил)-1-циклопропил-6-фтор-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота
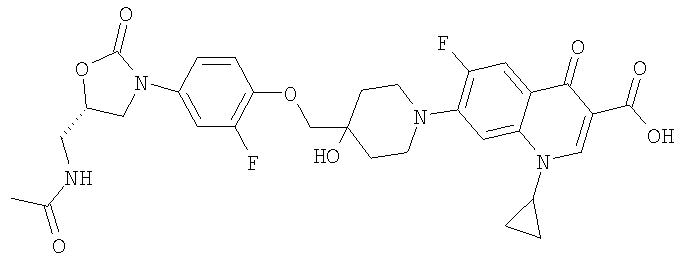
Раствор 60 г N-[{(5S)-3-[3-фтор-4-(4-гидроксипиперидин-4-илметокси)фенил]-2-оксооксазолидин-5-илметил}]ацетамида (C18H24FN3O5, мол. масса 381,40, 0,157 моля) и 26,87 мл этилдиизопропиламина (мол. масса 129,25, 0,157 моля) в 300 мл N-метилпирролидин-2-она смешивали с 67,81 г комплекса 7-хлор-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновой кислоты и диацетата бора (мол. масса 410,57, 0,165 моля) и смесь в течение 5 ч перемешивали при 80°С. N-Метилпирролидин-2-он отделяли при пониженном давлении центрифугированием и остаток растворяли в 300 мл метанола. Через этот раствор в течение 30 мин при 10°С пропускали поток сухого хлористого водорода. Далее раствор перемешивали при КТ, при этом в осадок выпадало твердое вещество желтого цвета. Превращение борсодержащего комплекса в свободную кислоту отслеживали с помощью ЖХВР. Смесь разбавляли 300 мл этилацетата. Твердое вещество отфильтровывали и промывали 100 мл этилацетата/метанола (в соотношении 8:2) и 100 мл этилацетата. Твердое вещество желтого цвета сушили, получив в результате 86,4 г такого желтого вещества. Затем это твердое вещество растворяли в 200 мл диметилсульфоксида при 40°С и желтый раствор сливали при перемешивании в 1000 мл воды. Желтое твердое вещество собирали, промывали водой и сушили. Выход 73 г, 74,5%. МС: 627,8 (M+H)+, 625,8 (М+Н)-. Метод: ESI+, ESI-.
Пример 2
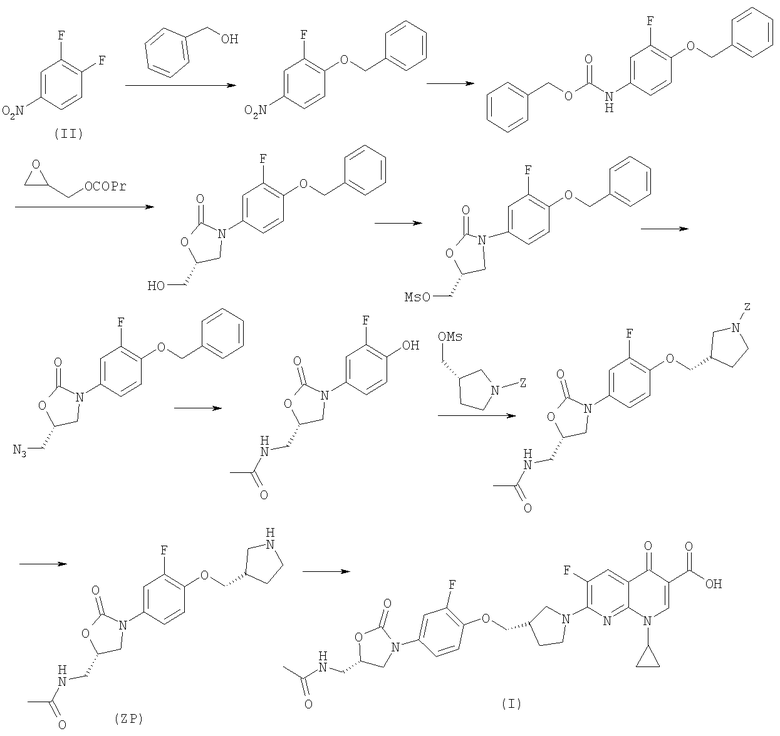
Условия реакции и используемые компоненты
Стадия 1: CH2Cl2, КОН (50%), 3 ч, КТ, 97%.
Стадия 2: H2, Pt/C, 20 ч, КТ, затем Cbz-Cl, ацетон/вода, NaHCO3, 12 ч, КТ, 98%.
Стадия 3: н-BuLi, -60°C, 24 ч, 80%.
Стадия 4: MsCl, ТЭА, CH2Cl2, 100%.
Стадия 5: NaN3 в ДМФ, 90°С, кат. Bu4NI, 5 ч, 90%.
Стадия 6: H2, Pd(OH)2, ТГФ, МеОН, 24 ч, затем АсОН, Ас2О, КТ, 2 ч, 70%.
Стадия 7: ДМФ, NaH, 70°C, 12 ч, 75%.
Стадия 8: Н2, Pd(OH)2, МеОН, ТГФ, 24 ч, КТ, 100%.
Стадия 9: N-метилпирролидон, 1-циклопропил-7-хлор-6-фтор-1,4-дигидро-4-оксо-1,8-нафтидрин-3-карбоновая кислота (коммерчески доступный продукт), ТМСХ (триметилсилилхлорид), основание Хюнига или К2СО3, 80°С, 5 ч, 80%.
При проведении всех этих стадий хроматографическое разделение не требуется.
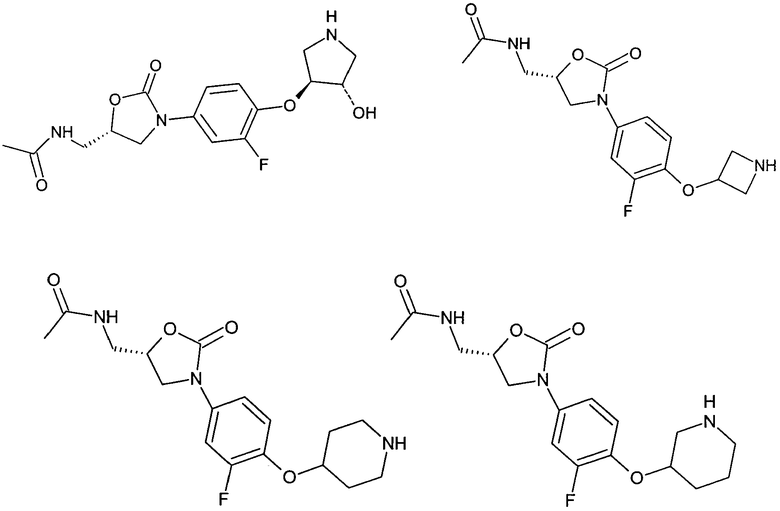
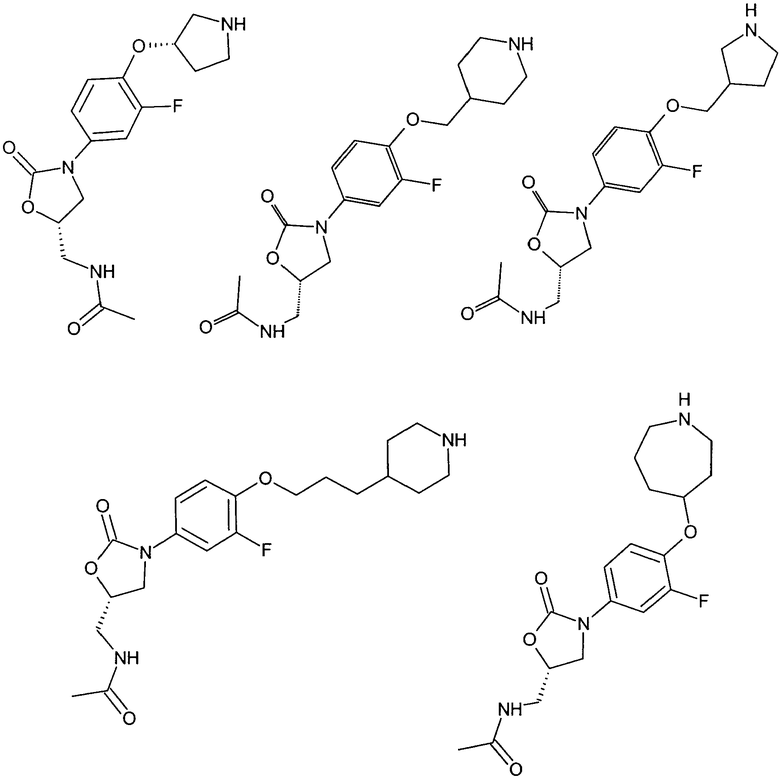
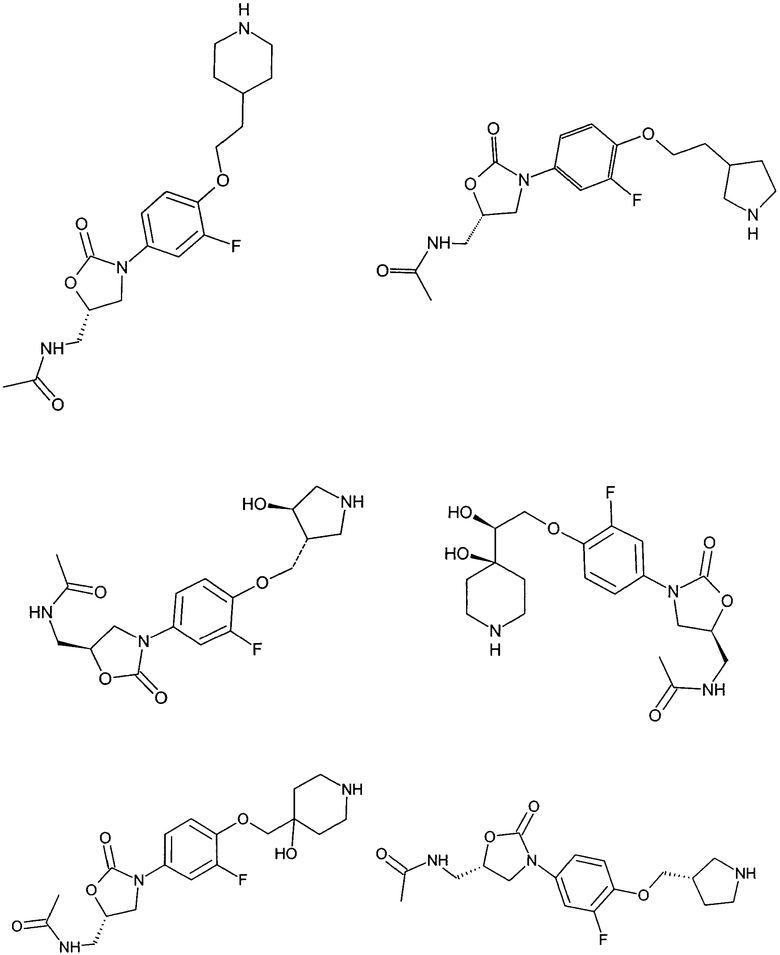
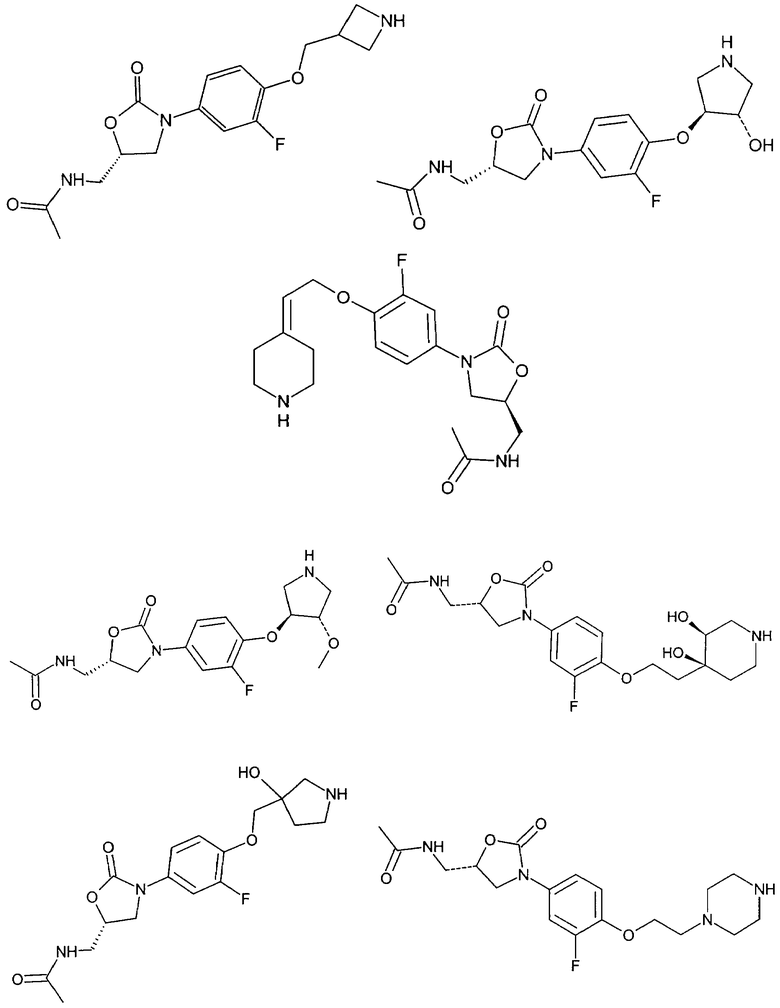
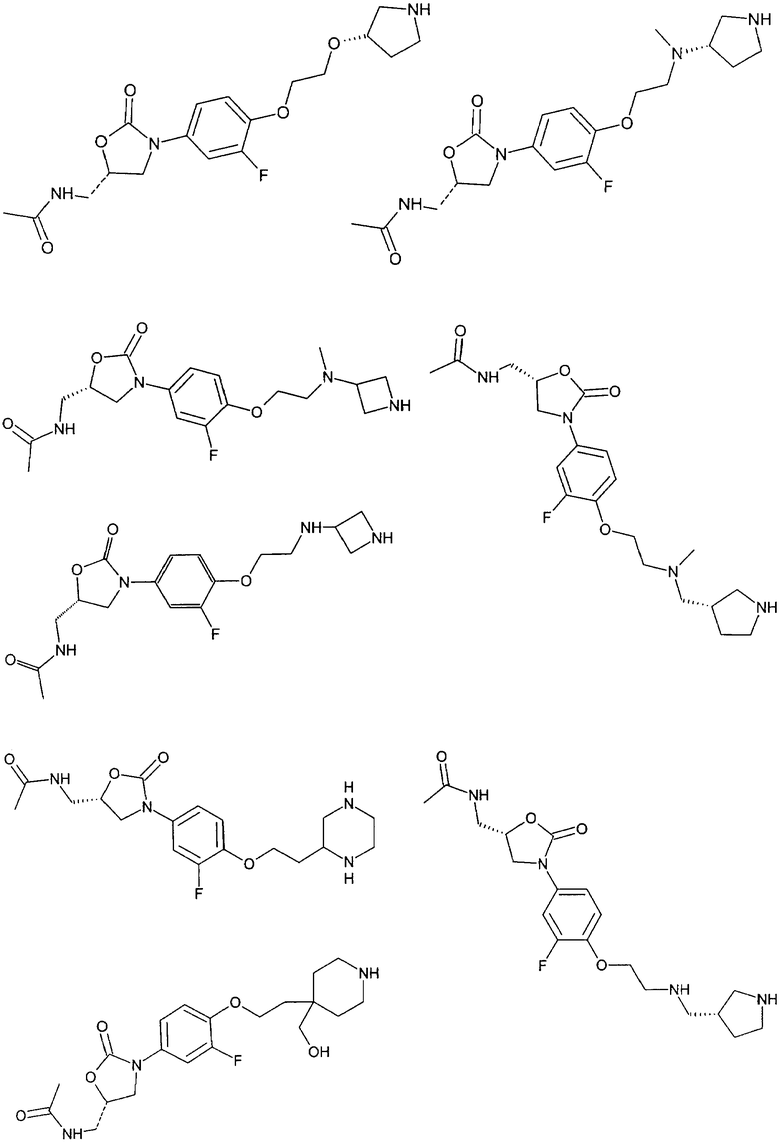
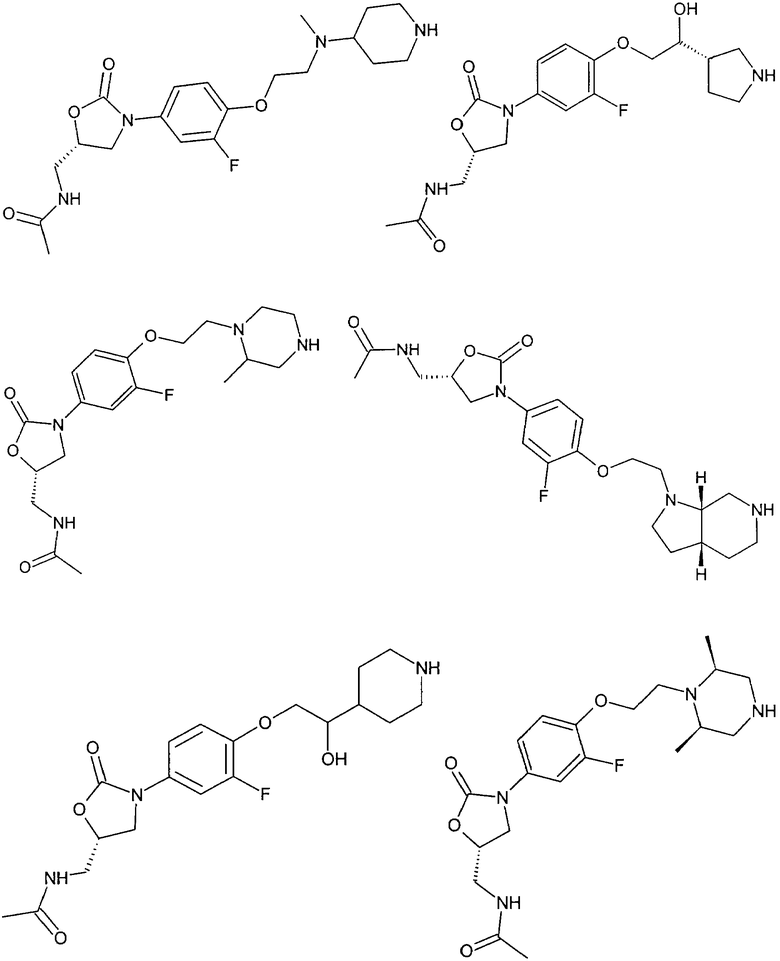
Ниже представлены соединения формулы (ZP), соответственно формулы (X), полученные по способам, аналогичным вышеописанным, с использованием соответствующих исходных материалов. При использовании соединений, содержащих свободные ОН-группы, получали также соединения, в которых эти ОН-группы были защищены защитными группами (такими, например, как ацетат, бензоат, МОМ-эфир (метилоксиметиловый эфир) или изопропилиден).
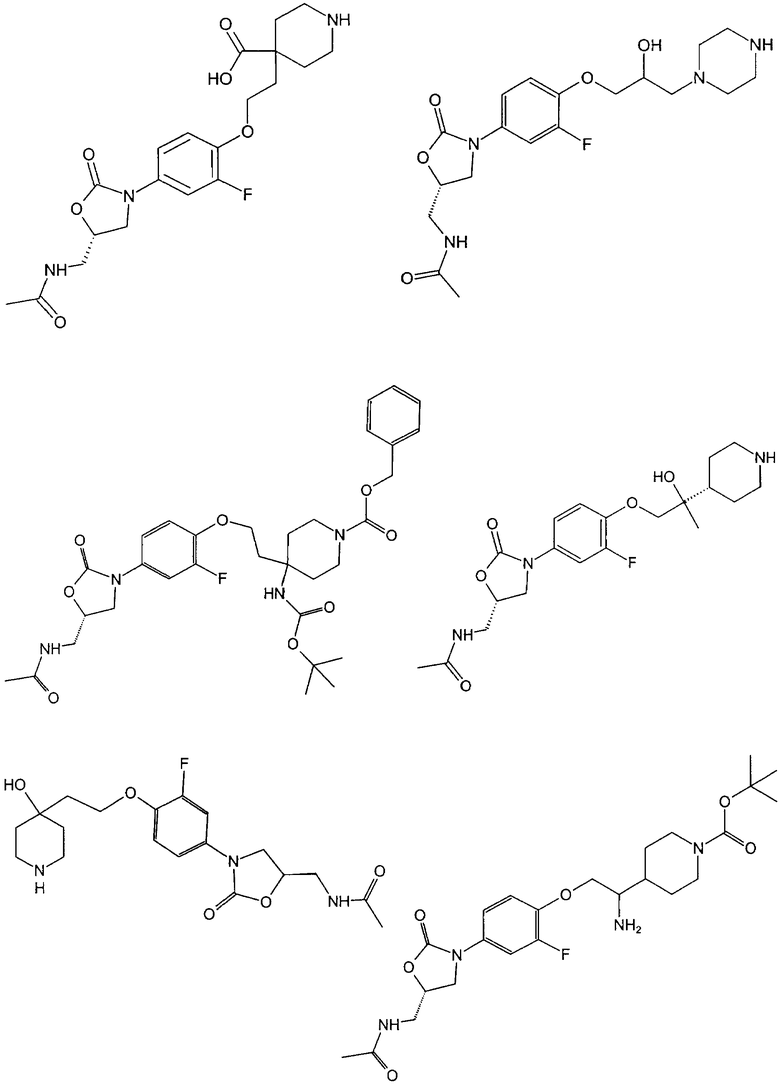
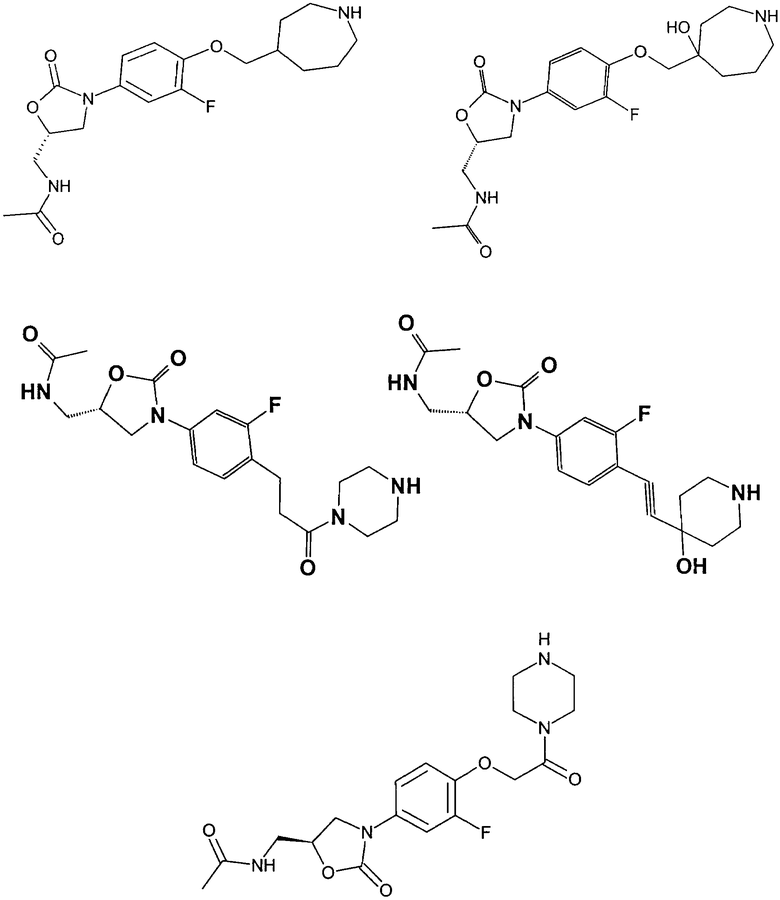
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ СОЕДИНЕНИЯ С АНТИБАКТЕРИАЛЬНЫМ ДЕЙСТВИЕМ | 2004 |
|
RU2397982C2 |
| НОВЫЕ БИОИЗОСТЕРЫ АКТИНОНИНА | 2004 |
|
RU2379284C2 |
| ПРИМЕНЕНИЕ ОКСАЗОЛИДИНОН-ХИНОЛИНОВЫХ ГИБРИДНЫХ АНТИБИОТИКОВ ДЛЯ ЛЕЧЕНИЯ СИБИРСКОЙ ЯЗВЫ И ДРУГИХ ИНФЕКЦИЙ | 2004 |
|
RU2351335C2 |
| ИМИДАЗО[1,2-a]ПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ, КОТОРЫЕ МОЖНО ИСПОЛЬЗОВАТЬ В КАЧЕСТВЕ ИНГИБИТОРОВ ПЕПТИДДЕФОРМИЛАЗЫ (ПДФ) | 2006 |
|
RU2409575C2 |
| ОКСАЗОЛИДИНОН-ХИНОЛОНГИБРИДНЫЕ АНТИБИОТИКИ | 2004 |
|
RU2371443C2 |
| ПОКРЫТОЕ МОЛЕКУЛЯРНОЕ СИТО | 2007 |
|
RU2458735C2 |
| МЕТАБОЛИЧЕСКИ УСТОЙЧИВЫЕ АНАЛОГИ CYP-ЭЙКОЗАНОИДОВ ДЛЯ ЛЕЧЕНИЯ КАРДИОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2016 |
|
RU2761438C2 |
| ПРОИЗВОДНЫЕ ЗАМЕЩЕННОЙ МОЧЕВИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ, ОБЛАДАЮЩИЕ РЕТИНОИДНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2303027C2 |
| ПРОИЗВОДНЫЕ ЭФИРА ГЕТЕРОАРИЛКАРБОНОВОЙ КИСЛОТЫ | 2013 |
|
RU2664544C2 |
| БЕНЗОПИРАНЫ И БЕНЗОКСЕПИНЫ, СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 1999 |
|
RU2228333C2 |
Настоящее изобретение относится к соединениям формулы (ZP)
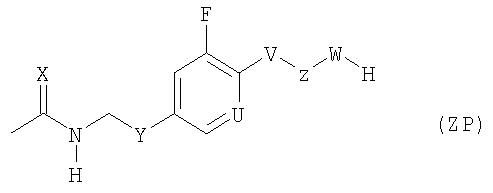
в которой U обозначает группу СН, V обозначает атом кислорода, W обозначает замещенную гидроксилом гетероциклоалкиленовую группу, содержащую от 5 до 7 атомов в цикле, включая атом N в качестве гетероатома, Х обозначает атом кислорода, Y представляет собой 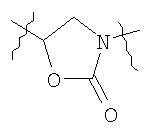 , Z обозначает C1-С6-алкиленовую группу. Изобретение также относится к применению соединений изобретения для получения соединения формулы (I)
, Z обозначает C1-С6-алкиленовую группу. Изобретение также относится к применению соединений изобретения для получения соединения формулы (I)
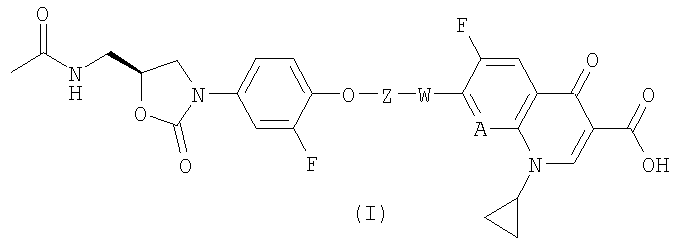
в которой А обозначает атом азота или группу СН. 2 н. и 4 з.п. ф-лы.
1. Соединения формулы (ZP)

в которой U обозначает группу СН;
V обозначает атом кислорода;
W обозначает замещенную гидроксилом гетероциклоалкиленовую группу, содержащую от 5 до 7 атомов в цикле, включая атом N в качестве гетероатома;
Х обозначает атом кислорода;
Y представляет собой
 ,
,
Z обозначает C1-С6-алкиленовую группу.
2. Соединения по п.1, где Z обозначает С1-С4-алкиленовую группу.
3. Соединения по п.1, где Z обозначает группу СН2 или группу СН2СН3.
4. Соединения по п.1, где Z и W совместно образуют группу формулы
 ,
,
где n обозначает 1 или 2, m обозначает 1 или 2 и о обозначает 1 или 2, при этом m и о одновременно не означают 1.
5. Соединения по п.1, где W имеет следующую структурную формулу
 или
или 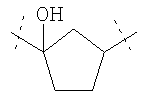 .
.
6. Применение соединения по п.1 для получения соединения формулы (I)
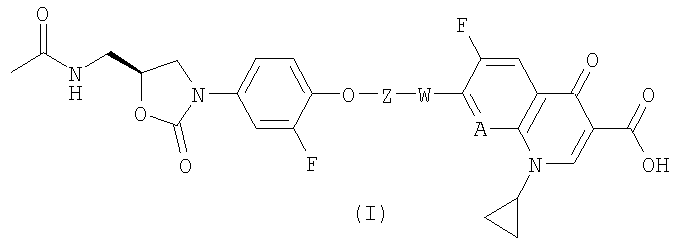 ,
,
в которой А обозначает атом азота или группу СН, а остальные остатки имеют указанные в п.1 значения.
| ПРОИЗВОДНОЕ ОКСАЗОЛИДИНОНА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, СПОСОБ ЛЕЧЕНИЯ МИКРОБНЫХ ИНФЕКЦИЙ У ТЕПЛОКРОВНЫХ ЖИВОТНЫХ | 1993 |
|
RU2105003C1 |
| WO 03032962 A2, 24.04.2003 | |||
| Реверсивная резьбонарезная головка | 1961 |
|
SU146164A1 |
| Электромеханический датчик | 1956 |
|
SU109107A1 |
| Аппарат для отмеривания, отрезывания и наматывания тканей | 1927 |
|
SU10566A1 |
Авторы
Даты
2009-11-20—Публикация
2004-09-03—Подача