Данная заявка является продолжением заявки на выдачу патента США №10/322312, поданной 16 декабря 2002 года, которая отчасти является продолжением заявки на выдачу патента США №10/131961, поданной 25 апреля 2002 года, каждая из которых включена в данное описание посредством ссылки во всей ее полноте.
1. ВВЕДЕНИЕ
Данное изобретение имеет отношение к способам улучшения терапевтического эффекта, предусматривающим введение препарата белка теплового шока (HSP) или препарата α-2-макроглобулина (α2М) вместе с невакцинным лечебным воздействием. В частности, препарат HSP или препарат α2М вводят вместе с невакцинным лечебным воздействием для лечения злокачественных опухолей или инфекционных заболеваний. При практическом применении изобретения препарат, содержащий HSP, такие как hsp70, hsp90 и gp96, но не ограничиваясь перечисленным, отдельно или в комбинации друг с другом, нековалентно или ковалентно связанные с антигенными молекулами, или α2М, нековалентно или ковалентно связанный с антигенными молекулами, вводят вместе с невакцинным лечебным воздействием.
2. ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Цитирование и обсуждение ссылок в описании не следует рассматривать как признание того, что указанные ссылки являются предшествующим для данного изобретения уровнем техники.
2.1 ИММУННЫЕ ОТВЕТЫ
Иммунная система организма реагирует на патогены или другие вредные агенты двумя типами ответов - гуморальным ответом или клеточно-опосредованным ответом (См. Alberts, B. et al., 1994, Molecular Biology of the Cell. 1195-96). Если покоящиеся В-клетки активируют антигеном для пролиферации и созревания в антитело-секретирующие клетки, они продуцируют и секретируют антитела с единственным антиген-связывающим участком. Указанная реакция секреции антител известна как гуморальный ответ. С другой стороны, разнообразные ответы Т-клеток совокупно называют клеточно-опосредованными иммунными реакциями. Существует два основных класса Т-клеток - цитотоксические Т-клетки и хелперные Т-клетки. Цитотоксические Т-клетки непосредственно убивают клетки, которые инфицированы вирусом или некоторыми другими внутриклеточными микроорганизмами. В противоположность им хелперные Т-клетки помогают стимулировать ответы других клеток: они способствуют активации макрофагов, дендритных клеток и В-клеток (см. Alberts, B. et al., 1994, Molecular Biology of the Cell. 1228). Как цитотоксические Т-клетки, так и хелперные Т-клетки распознают антиген в виде пептидных фрагментов, которые образуются в результате деградации чужеродных белковых антигенов в клетке-мишени, и поэтому оба типа клеток зависят от молекул главного комплекса гистосовместимости (MHC), которые связывают указанные пептидные фрагменты, перенося их на клеточную поверхность, и присутствия их на Т-клетках (см. Alberts, B. et al., 1994, Molecular Biology of the Cell. 1228). Обычно молекулы MHC обнаруживают в большом количестве на антигенпрезентирующих клетках (APC).
2.2. ХРОНИЧЕСКИЙ МИЕЛОИДНЫЙ ЛЕЙКОЗ
Хронический миелоидный (миелогенный, миелоцитарный, гранулоцитарный) лейкоз (“CML”) представляет собой злокачественную опухоль системы крови и костного мозга, характеризующуюся сверхпродукцией лейкоцитов. CML характеризуется хронической фазой со средней продолжительностью от 3 до 5 лет при лечении общепринятыми средствами и ускоренной или острой фазой продолжительностью приблизительно от 3 до 6 месяцев, неизбежно завершающейся летально. В начальной стадии хроническая фаза характеризуется отсутствием или небольшим количеством симптомов и признаков. Однако в большинстве случаев, в конце концов, появляются органические симптомы и аномальные физические показатели, включая экстрамедуллярные нарушения, такие как миелобластомы.
CML составляет от 7% до 20% всех лейкозов и поражает приблизительно от 1 до 2/100000 человек от всего населения. American Cancer Society сообщает, что каждый год в Соединенных Штатах возникает 4400 новых случаев CML.
CML вызывается определенным цитогенетическим нарушением в Philadelphia-(“Ph+”)-хромосоме, которое приводит к клональному миелопролиферативному нарушению плюрипотентных кроветворных стволовых клеток (Faderl et al., 1999, New England J. Med. 341(3): 164-172). Ph+-хромосома является результатом сбалансированной транслокации между длинными плечами хромосом 9 и 22, приводящей к возникновению химерного гена bcr/abl, который экспрессирует аномальный слитый белок с измененной тирозинкиназной активностью.
На сегодняшний день выбор лечения для пациентов в хронической фазе CML включает бисульфан (BUS), гидроксимочевину (HU), схемы лечения на основе интерферона (IFN), специфический ингибитор киназы для bcr/abl или трансплантации костного мозга/стволовых клеток (ВМТ) (Silver et al., 1999, Blood 94(5): 1517-1536). Еще несколько лет назад аллогенная ВМТ было лечением выбора для всех подходящих пациентов, так как она была единственным лечением, которое, как казалось, изменяет естественное течение заболевания. Исследования показали, что, по крайней мере, половина пациентов, которым производили трансплантацию, оставались в живых от 5 до 10 лет после лечения. Однако этот способ все же осложняется отсутствием доноров и значительными связанными с трансплантацией осложнениями, такими как реакция «трансплантат против хозяина» и инфекции. Схемы лечения на основе IFN также оказывают влияние на естественное течение CML. Однако схемы лечения только на основе IFN обеспечивают повышение продолжительности выживания в среднем приблизительно на 20 месяцев (Chronic Myeloid Leukemia Trialists' Collaborative Group, 1997, J. Natl. Cancer Inst. 89(21): 1616-20).
Показано, что специфический ингибитор bcr/abl Gleevec™ (иматиниба мезилат, Novartis™) позволял получить обнадеживающие результаты клинических испытаний фазы I, Drucker and Lydon, 2000, J. Clin. Invest. 105(1): 3-7; Dazzi et al., 2000, Leukemia 14:419-426; см. также Hellman, Principles of Cancer Management: 6th edition, 2001, DeVita et al., J.B.Lippencott Company, Philadelphia, которая включена в данное описание посредством ссылки во всей ее полноте, pp.2443-2444. Gleevec™ (иматиниба мезилат) также известен как ингибитор передачи сигнала 571, STI-571 и CGP-57148. На основании исследований фазы II (Druker et al., 2001, New England J. Med. 344(14): 1031-1037, и Druker et al., 2001, New England J. Med. 344(14): 1038-1042) FDA одобрило применение Gleevec™ для лечения следующих трех фаз CML: хронической фазы при отсутствии какого-либо ответа на стандартную терапию интерфероном; ускоренной фазы и миелоидного бластного криза. Однако долгосрочная эффективность и токсичность остаются не установленными. Кроме того, наблюдали побочные эффекты у пациентов, которых подвергали лечению Gleevec™, включающие отек, гепатотоксичность и гематологическую токсичность. Physician's Desk Reference (56th ed., 2002). Кроме того, уже описана резистентность к Gleevec™. Le Coutre et al., 2000, Blood 95(5): 1758-1766. Таким образом, в данной области существует потребность в улучшенных способах лечения CML.
2.3. БЕЛКИ ТЕПЛОВОГО ШОКА
Белки теплового шока (HSP), которые также в описании взаимозаменяемо называют стрессовыми белками, можно выбрать среди любых клеточных белков, которые удовлетворяют следующим критериям. Указанный белок представляет собой белок, внутриклеточная концентрация которого возрастает, когда клетку подвергают воздействию стрессовых раздражителей, белок, способный связывать другие белки или пептиды, белок, способный высвобождать связанные белки или пептиды в присутствии аденозинтрифосфата (АТФ) или при низком pH, и белок, являющийся белком, обладающим, по крайней мере, 35% гомологией с любым клеточным белком, характеризующимся любым из вышеприведенных свойств. HSP включают конститутивно экспрессируемые, консервативные клеточные гомологи белков, индуцируемые стрессом. Поэтому предполагают, что стрессовые белки/HSP включают другие белки, мутеины, аналоги и их варианты, имеющие, по крайней мере, от 35% до 55%, предпочтительно от 55% до 75% и наиболее предпочтительно от 75% до 85% аминокислотной идентичности с представителями трех семейств с указанными выше свойствами.
Первыми стрессовыми белками, которые были идентифицированы, являются HSP. Как подразумевает их название, HSP синтезируются в ответ на тепловой шок. В настоящее время три главных семейства HSP идентифицированы на основании молекулярной массы. Семейства были названы hsp60, hsp70 и hsp90, где число отражает приблизительную молекулярную массу стрессовых белков в килодальтонах. Впоследствии было обнаружено, что большинство представителей указанных семейств индуцируются в ответ на другие стрессовые стимулы, включающие в себя недостаточность питания, метаболическое нарушение, кислородные радикалы и инфекции внутриклеточными патогенными микроорганизмами, не ограничиваясь указанным (см. Welch, May 1993, Scientific American 56-64; Young, 1990, Annu. Rev. Immunol. 8:401-420; Craig, 1993, Science 260: 1902-1903; Gething, et al., 1992, Nature 355: 33-45; и Lindquist, et al., 1988, Annu. Rev. Genetics 22: 631-677), содержание которых включено в данное описание посредством ссылки. Полагают, что HSP/стрессовые белки, принадлежащие ко всем из указанных трех семейств, можно использовать при практическом применении данного изобретения.
HSP являются внутриклеточными молекулами, которые присутствуют в большом количестве, являются растворимыми и высококонсервативными. Как внутриклеточные шапероны, HSP участвуют во многих биохимических, метаболических путях созревания белков и активно функционируют во время периодов стресса и нормального клеточного гомеостаза. Большинство стрессов может нарушать трехмерную структуру, или укладку, клеточных белков. Оставаясь денатурированными, неправильно уложенные белки образуют агрегаты, которые со временем могут убить клетку. HSP связывают описанные поврежденные белки, помогая им ренатурироваться в надлежащие конформации. В нормальном (нестрессовом) клеточном гомеостазе HSP необходимы для клеточного метаболизма. HSP помогают вновь синтезированным полипептидам укладываться и, таким образом, предупреждают преждевременные взаимодействия с другими белками. Также HSP способствуют транспорту белков в различных клеточных компартментах.
Главные HSP могут накапливаться в очень высоких концентрациях в клетках, подвергшихся стрессу, но они встречаются в низких или средних концентрациях в клетках, которые не подвергались стрессу. Например, высокоиндуцибельный hsp70 млекопитающих едва определяется при нормальных температурах, но становится одним из наиболее активно синтезируемых белков в клетке при тепловом шоке (Welch et al., 1985, J. Cell Biol. 101: 1198-1211). В противоположность этому, белки hsp90 и hsp60 имеются в большом количестве при нормальных температурах в большинстве, но не всех, клетках млекопитающих и, кроме того, индуцируются нагреванием (Lai et al., 1984, Mol. Cell Biol. 4: 2802-2810; van Bergen en Henegouwen et al., 1987, Genes Dev. 1: 525-531).
Обнаружено, что HSP обладают иммунными и антигенными свойствами. Иммунизация мышей gp96 или p84/86, выделенными из определенной опухоли, развивает у мышей иммунитет к данной опухоли, но не к антигенно-различным опухолям (Srivastava, P.K. et al., 1988, Immunogenetics 28: 205-207; Srivastava, P.K. et al., 1991, Curr. Top. Microbiol. Immunol. 167: 109-123). Кроме того, показано, что hsp70 вызывает иммунитет к опухоли, из которой он был выделен, но не к антигенно-различным опухолям. Однако установлено, что hsp70 без пептидов теряют свою специфическую иммуногенную активность (Udono, M., and Srivastava, P.K., 1993, J. Exp. Med. 178: 1391-1396). Представленные наблюдения позволили предположить, что белки теплового шока не являются антигенными сами по себе, но образуют нековалентные комплексы с антигенными пептидами, и комплексы могут вызывать специфический иммунитет к антигенным пептидам (Srivastava, P.K., 1993, Adv. Cancer Res. 62: 153-177; Udono, H. et al., 1994, J. Immunol., 152: 5398-5403; Suto, R. et al., 1995, Science, 269: 1585-1588). Недавно было показано, что hsp60 и hsp70 стимулируют продукцию провоспалительных цитокинов, таких как TNFα и IL-6, моноцитами, макрофагами или цитотоксическими Т-клетками (Breloer et al., 1999, J. Immunol. 162: 3141-3147; Chen et al., 1999, J. Immunol. 162: 3212-3219; Ohashi et al., 2000, J. Immunol. 164: 558-561; Asea et al., 2000, Nature Medicine, 6: 435-442; Todryk et al., 1999, J. Immunol. 163: 1398-1408). Hsp70 также обнаружен в незрелых дендритных клетках-мишенях и он делает их более способными захватывать антигены (Todryk et al., 1999, J. Immunol. 163: 1398-1408). Высказано предположение, что высвобождение hsp60 и hsp70 или индукция экспрессии hsp60 и hsp70, например, вследствие клеточной гибели может служить сигналом, что должна индуцироваться иммунная реакция (Chen et al., 1999, J. Immunol. 162: 3212-3219; Ohashi et al., 2000, J. Immunol. 164: 558-561; Todryk et al., 1999, J. Immunol. 163: 1398-1408).
Применение нековалентных комплексов HSP и пептида, выделенного из злокачественных клеток, для лечения и профилактики злокачественных опухолей раскрыто в патентах США №5750119, 5837251 и 6017540.
Применение комплексов HSP-пептид для сенсибилизации антигенпрезентирующих клеток in vitro для использования в адоптивной иммунотерапии раскрыто в патентах Соединенных Штатов №5985270 и 5830464.
Комплексы HSP-пептид также можно выделять из клеток, инфицированных патогенными микроорганизмами, и использовать для лечения и профилактики инфекции, вызываемой патогенами, такими как вирусы и другие внутриклеточные патогены, включая бактерии, простейшие, грибы и паразиты; см. патент Соединенных Штатов №5961979 и 6048530.
Иммуногенные комплексы HSP-пептид также можно получать путем образования in vitro комплексов HSP и антигенных пептидов, использование таких комплексов для лечения и профилактики злокачественных опухолей и инфекционных заболеваний раскрыто в патентах Соединенных Штатов №5935576 и 6030618. Применение белка теплового шока вместе с определенным антигеном для лечения злокачественных опухолей и инфекционных заболеваний также описано в публикации РСТ WO97/06821, датированной 27 февраля 1997.
Ранее было раскрыто выделение комплексов HSP-пептид из лизатов клеток; см., например, патенты Соединенных Штатов №5750119 и 5997873.
2.4. α2-МАКРОГЛОБУЛИН
α-Макроглобулины являются представителями белкового семейства структурно родственных белков, которое также включает компоненты комплемента С3, С4 и С5. Белок плазмы человека, альфа(2)макроглобулин (α2М) является гомотетрамерным белком 720 кДа, известным, главным образом, как ингибитор протеиназ и молекула-сборщик протеиназ плазмы и воспалительной жидкости (для ознакомления см. Chu and Pizzo, 1994, Lab. Invest. 71: 792). Альфа(2)макроглобулин синтезируется в виде предшественника из 1474 аминокислот, первые 23 из которых функционируют как сигнальная последовательность, которая отщепляется с образованием зрелого белка из 1451 аминокислот (Kan et al., 1985, Proc. Natl. Acad. Sci. U.S.A. 82: 2282-2286).
Альфа(2)макроглобулин беспорядочно связывает белки и пептиды с нуклеофильными аминокислотными боковыми цепями ковалентным способом (Chu et al., 1994, Ann. N.Y. Acad. Sci 737: 291-307) и направляет их в клетки, которые экспрессируют рецептор α2М (α2MR) (Chu and Pizzo, 1993, J. Immunol. 150: 48). Связывание α2М с α2MR опосредуется С-концевой частью белка α2М (Holtet et al., 1994, FEBS Lett. 344: 242-246), и ключевые остатки идентифицированы (Nielsen et al., 1996, J. Biol. Chem. 271: 12909-12912).
Общеизвестно, что благодаря ингибирующей протеазной активности α2М связывает целый ряд протеаз по многочисленным связывающим участкам (см., например, Hall et al., 1981, Biochem. Biophys. Res. Commun. 100(1): 8-16). Взаимодействие протеаз с α2М приводит к сложной структурной реаранжировке, называемой трансформацией, которая приводит к расщеплению в области «байта» α2М после того, как протеиназа становится «захваченной» сложными тиоэфирами. Конформационное изменение экспонирует остатки, требуемые для рецепторного связывания, позволяя комплексу α2М-протеиназа связываться с α2MR. Метиламин может индуцировать подобные конформационные изменения и расщепление, как изменения, вызываемые протеиназами. Нерасщепленную форму α2М, которую не распознают рецепторы, часто называют «медленной» формой (s-α2M). Расщепленную форму называют «быстрой» формой (f-α2M) (рассматриваемая Chu et al., 1994, Ann. N.Y. Acad. Sci. 737: 291-307).
Исследования показали, что помимо его протеиназа-ингибиторных функций α2М, когда образует комплексы с антигенами, может повышать антигенную способность, чтобы поглощаться антигенпрезентирующими клетками, такими как макрофаги, и присутствовать в Т-клеточных гибридомах in vitro, вплоть до величин на два порядка более высоких (Chu and Pizzo, 1994, Lab. Invest. 71: 792), и индуцирует Т-клеточную пролиферацию (Osada et al., 1987, Biochem. Biophys. Res. Commun. 146: 26-31). Кроме того, данные позволяют предположить, что образование комплекса антигена с α2М повышает продукцию антител неочищенными клетками селезенки in vitro (Osada et al., 1988, Biochem. Biophys. Res. Commun. 150: 883) и вызывает in vivo ответы антител у экспериментальных кроликов (Chu et al., 1994, J. Immunol. 152: 1538-1545) и мышей (Mitsuda et al., 1993, Biochem. Biophys. Res. Commun. 101: 1326-1331). Однако ни в одном из описанных исследований не показано, способны ли комплексы α2М-антиген вызывать ответы цитотоксических Т-клеток in vivo.
α2М может образовывать комплексы с антигенами, которые поглощаются антигенпрезентирующими клетками (“APC”) с помощью α2MR, также известные как LDL (липопротеин низкой плотности), рецептор-связанный белок (“LRP”) или CD91 (см. PCT/US01/18047, которая включена в данное описание посредством ссылки во всей ее полноте). α2М непосредственно конкурирует за связывание белка теплового шока gp96 с α2MR, что указывает на то, что α2М и HSP могут связывать общий сайт узнавания на α2MR (Binder et al., 2000, Nature Immunology 1(2), 151-154). Кроме того, комплексы α2М-антигенный пептид, полученные in vitro, можно вводить животным, чтобы генерировать ответ цитотоксических Т-клеток, специфический для антигенных молекул (Binder et al., 2001, J. Immunol. 166: 4968-72). Таким образом, так как HSP и α2М имеют целый ряд общих функциональных свойств, таких как способность связывать пептид, распознавание и поглощение посредством α2MR и стимуляция ответа цитотоксических Т-клеток, α2М можно использовать для иммунотерапии против злокачественных опухолей и инфекционных заболеваний.
3. КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение отчасти базируется на признании того, что препарат HSP может повышать или улучшать терапевтическое действие невакцинных лечебных воздействий или терапевтических воздействий для лечения злокачественных опухолей или инфекционных заболеваний. Таким образом, данное изобретение охватывает способы и композиции, которые включают введение препарата HSP в комбинации с невакцинным лечебным воздействием. Также изобретение рассматривает способы и композиции, которые включают введение препарата α2М в комбинации с невакцинным лечебным воздействием. В частности, изобретение рассматривает способы и композиции для лечения и композиции, которые обеспечивают лучший терапевтический эффект, чем эффект препарата HSP или препарата α2М, вводимых отдельно, или невакцинное лечебное воздействие, осуществленное отдельно. Источником HSP или α2М предпочтительно являются эукариоты, и наиболее предпочтительно млекопитающие. Субъектом, подвергающимся лечению, предпочтительно являются млекопитающие, включающие, но не ограничиваясь перечисленным, домашних животных, таких как кошки и собаки, диких животных, таких как лисы и еноты, домашний скот и домашнюю птицу, таких как лошади, крупный рогатый скот, овцы, индюки и куры, а также любых грызунов. Наиболее предпочтительно субъектом является человек.
Изобретение касается способов улучшения терапевтического эффекта невакцинного лечебного воздействия, включающих введение или препарата HSP, или препарата α2М, предпочтительно препарата очищенного HSP или препарата очищенного α2М, вместе с проведением невакцинного лечебного воздействия. Или препарат HSP, или препарат α2М можно вводить в течение периода времени, который может предшествовать, перекрывать и/или следовать за схемой лечения невакцинным лечебным воздействием. Препарат HSP или препарат α2М можно вводить одновременно, до или после применения лечебного воздействия. Примеры лечебных воздействий включают, но не ограничиваясь перечисленным, антибиотики, противовирусные, противогрибковые соединения, противораковые лечебные средства, такие как химиотерапевтические средства и облучение, а также биологические терапевтические средства и иммунотерапевтические средства. В предпочтительных аспектах лечебное воздействие используют для лечения или профилактики злокачественных опухолей. В особо предпочтительных аспектах лечебное воздействие используют для лечения или профилактики хронического миелоидного лейкоза или сарком мягких тканей, включая, но не ограничиваясь перечисленным, желудочно-кишечные стромальные опухоли. В другом предпочтительном аспекте лечебным воздействием является Gleevec™.
В одном аспекте изобретение представляет способы лечения, которые обеспечивают лучшие терапевтические показатели, чем применение лечебного воздействия или только препарата HSP. В другом аспекте изобретение касается способов лечения, которые обеспечивают лучшие терапевтические показатели, чем применение одного лечебного воздействия или только препарата α2М. Изобретение представляет способы, при которых применение лечебного воздействия с препаратом HSP или препаратом α2М оказывает аддитивное действие или аддитивный терапевтический эффект. Изобретение также касается синергического действия, при котором терапевтическая эффективность оказывается выше, чем аддитивная. Предпочтительно такое применение лечебного воздействия с препаратом HSP или препаратом α2М также снижает или устраняет нежелательные или побочные эффекты. В некоторых аспектах благодаря изобретению дозы невакцинного лечебного воздействия могут быть снижены или их можно вводить менее часто, предпочтительно повышая податливость пациента, улучшая терапию и/или снижая нежелательные или побочные эффекты. В особом аспекте применяют более низкие или менее часто назначаемые дозы химиотерапии или лучевой терапии вводят, чтобы снизить или устранить нежелательные эффекты. Альтернативно дозы препарата HSP и дозы препарата α2М можно снижать или вводить менее часто, если применяют вместе с лечебным воздействием.
В другом аспекте данное изобретение обеспечивает способ улучшения результата лечения у субъекта, получающего лечебное воздействие, которое является невакцинным. Способ включает введение или препарата белка теплового шока, предпочтительно препарат очищенного HSP, или препарата α2М, предпочтительно препарата очищенного α2М, субъекту до, одновременно с или после применения лечебного воздействия. В особом аспекте препарат HSP или препарат α2М может увеличивать терапевтический эффект лечебного воздействия и улучшить результат лечения. Без связи с какой-либо теорией или механизмом, введение препарата HSP млекопитающего или препарата α2М субъекту может повышать реактивность неспецифических иммунных механизмов субъекта, например, посредством увеличения количества природных клеток-киллеров (NK) и/или ускорения созревания дендритных клеток, и/или также может повышать реактивность специфических иммунных механизмов, например, увеличивая количество Т-клеток CD4+ и CD8+. В предпочтительном особом аспекте препарат HSP вводят до применения лечебного воздействия. В другом предпочтительном особом аспекте препарат α2М вводят до применения лечебного воздействия.
В следующем аспекте данное изобретение обеспечивает способ улучшения результата лечения у субъекта, получающего препарат HSP, предпочтительно препарат очищенного HSP, посредством назначения невакцинного лечебного воздействия субъекту до, одновременно с или после введения препарата HSP. В особом аспекте невакцинное лечебное воздействие может усилить терапевтический эффект препарата HSP и улучшить результат лечения.
В другом аспекте данное изобретение предусматривает способ улучшения результата лечения у субъекта, получающего препарат α2М, предпочтительно препарат очищенного α2М, назначением невакцинного лечебного воздействия субъекту до, одновременно с или после введения препарата α2М. В специальном аспекте невакцинное лечебное воздействие может усилить терапевтический эффект препарата α2М и улучшить результат лечения.
В некоторых аспектах введение препарата HSP/α2М без применения лечебного воздействия или применение лечебного воздействия без введения препарата HSP/α2М не является терапевтически эффективным. В особом аспекте количество препарата HSP/α2М или лечебное воздействие назначают в количестве, недостаточном, чтобы оказаться терапевтически эффективным, когда применяют отдельно. В альтернативных аспектах оба или, по крайней мере, один из препарата HSP/α2М или лечебного воздействия является терапевтически эффективным, когда назначают отдельно.
В различных аспектах способы включают введение препарата HSP, предпочтительно препарата очищенного HSP, субъекту, получающему лечебное воздействие для лечения злокачественных опухолей или инфекционных заболеваний. Предпочтительно препарат HSP включает комплексы HSP-пептид, проявляющие антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака или антигена инфекционного агента, то есть белков теплового шока, образующих комплексы с антигенными пептидами злокачественных клеток или инфицированных клеток, из которых получены комплексы. Соответственно, в одном аспекте специфическая иммуногенность препарата HSP происходит от пептида, образующего комплекс с HSP. В предпочтительных аспектах комплексы HSP-пептид выделяют из источника антигена, такого как злокачественные ткани, злокачественные клетки или инфицированные ткани. При практическом применении изобретения такие комплексы HSP-пептид предпочтительно являются аутогенными индивидуальному субъекту, то есть получают из тканей субъекта, которому вводят препарат HSP или применяют лечебное воздействие, но необязательно (то есть аллогенным индивидуальному субъекту).
В разных других аспектах способы включают введение препарата α2М, предпочтительно препарата очищенного α2М, субъекту, получающему лечебное воздействие для лечения злокачественных опухолей или инфекционных заболеваний. Предпочтительно препарат α2М включает комплексы α2М-пептид, проявляющие антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака или антигена инфекционного агента, то есть α2М, образующего комплексы с антигенными пептидами злокачественных клеток или инфицированных клеток, из которых получены комплексы. Соответственно, в одном аспекте специфическая иммуногенность препарата α2М происходит от пептида, образующего комплекс с α2М. В предпочтительных аспектах комплексы α2М-пептид выделяют из источника антигенов, таких как злокачественные ткани, злокачественные клетки или инфицированные ткани. При практическом применении изобретения предпочтительно такие комплексы α2М-пептид являются аутогенными индивидуальному субъекту, то есть полученными из тканей субъекта, которому вводят препарат α2М и проводят лечебное воздействие, но не обязательно (то есть аллогенные для индивидуального субъекта).
В одном аспекте способы включают введение препарата HSP или препарата α2М, предпочтительно препарата очищенного HSP или препарата очищенного α2М, субъекту, которому проводят лечебное воздействие для лечения инфекционного заболевания. Такие лечебные воздействия известны в данной области и включают, но не ограничиваясь ими, антибиотики, противовирусные средства, противогрибковые средства, а также биологические и иммунотерапевтические средства. Предпочтительно препарат HSP содержит комплексы HSP-пептид, которые проявляют антигенность агента, вызвавшего инфекционного заболевания. Предпочтительно препарат α2М содержит комплексы α2М-пептид, которые проявляют антигенность агента инфекционного заболевания. В специальном аспекте результат лечения типа инфекционного заболевания у субъекта, которому проводят невакцинное лечебное воздействие, улучшается при введении комплексов HSP-пептид, содержащих HSP, образующий комплекс с пептидом, проявляющим антигенность антигена агента указанного типа инфекционного заболевания. Предпочтительно комплексы HSP-пептид не присутствуют в смеси с HSP или α2М, который не образует комплекс с пептидом, проявляющим антигенность антигена агента указанного инфекционного заболевания (см. Международную заявку №PCT/US01/28840, поданную 15 сентября 2001, включенную в данное описание посредством ссылки во всей своей полноте). В одном аспекте препарат HSP вводят до проведения лечебного воздействия. В другом аспекте лечебное воздействие проводят до введения препарата HSP. В другом специальном аспекте результат лечения типа инфекционного заболевания у субъекта, которому проводят невакцинное лечебное воздействие, улучшают введением комплексов α2М-пептид, содержащих α2М, образующий комплекс с пептидом, проявляющим антигенность антигена агента указанного типа инфекционного заболевания. Предпочтительно комплексы α2М-пептид не присутствуют в смеси с HSP или α2М, которые не образуют комплекс с пептидом, проявляющим антигенность антигена агента того же инфекционного заболевания. В одном аспекте препарат α2М вводят до проведения лечебного воздействия. В другом аспекте лечебное воздействие проводят до введения препарата α2М.
В другом аспекте способы включают введение или препарата HSP, или препарата α2М, предпочтительно препарата очищенного HSP или препарата очищенного α2М, субъекту, которому проводят лечебное воздействие для лечения злокачественных опухолей. Такие лечебные воздействия включают, но, не ограничиваясь ими, химиотерапию и лучевую терапию, а также гормональную терапию, биологическую терапию и иммунотерапию. Предпочтительно препарат HSP или препарат α2М вводят субъекту, получающему химиотерапию или лучевую терапию для лечения злокачественных опухолей. Предпочтительно препарат HSP содержит комплексы HSP-пептид, которые проявляют антигенность типа рака, который лечат. Предпочтительно, когда препарат является препаратом α2М, препарат α2М содержит комплексы α2М-пептид, которые проявляют антигенность типа рака, который лечат. Соответственно, в предпочтительных аспектах изобретение предусматривает способы улучшения результата лечения злокачественных опухолей у субъекта, которому проводят лечебное воздействие, которое является невакцинным, используя комплексы HSP-пептид, содержащие HSP, образующий комплекс с пептидом, проявляющим антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака, или используя комплексы α2М-пептид, содержащие α2М, образующий комплекс с пептидом, проявляющим антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака. В некоторых предпочтительных аспектах, такие комплексы HSP-пептид и комплексы α2М-пептид не разводят ни HSP, ни α2М, образующие комплекс с пептидом, проявляющим антигенность антигена того же типа рака. В одном аспекте препарат HSP или препарат α2М вводят до проведения лечебного воздействия. В другом аспекте лечебное воздействие проводят до введения препарата HSP или препарата α2М.
В различных аспектах препарат HSP или препарат α2М вводят с противораковым средством, которое может представлять собой, но не ограничиваясь перечисленным, цитотоксический агент, противомитотическое средство, средство, стабилизирующее тубулин, средство, ингибирующее образование микротрубок, ингибиторы топоизомеразы, алкилирующий агент, взаимодействующее с ДНК средство, антиметаболит, антиметаболит РНК/ДНК, антиметаболит ДНК. В особом аспекте противораковое средство является химиотерапевтическим.
В специальном аспекте препарат HSP вводят пациенту, получающему химиотерапевтическое средство для лечения злокачественных опухолей. В другом предпочтительном аспекте препарат α2М вводят субъекту, получающему химиотерапевтическое средство для лечения злокачественных опухолей. Такие химиотерапевтические средства известны в данной области и включают, но не ограничиваясь перечисленным: метотрексат, таксол, меркаптопурин, тиогуанин, гидроксимочевину, цитарабин, циклофосфамид, ифосфамид, нитрозомочевины, цисплатин, карбоплатин, митомицин, дакарбазин, прокарбизин, этопозид, кампатецины, блеомицин, доксорубицин, идарибицин, даунорубицин, дактиномицин, пликамицин, митоксантрон, аспарагиназу, винбластин, винкристин, винорелбин, паклитаксел и доцетаксел, доксорубицин, эпирубицин, 5-фторурацил, таксаны, такие как доцетаксел и паклитаксел, леуковорин, левамисол, иринотекан, эстрамустин, этопозид, источники азота, такие как кармустин и ломустин, алкалоиды барвинки, соединения платины, митомицин, гемцитабин, гексаметилмеланин, топотекан, ингибиторы тирозинкиназы, тирфостины, STI-571 или Gleevec™ (иматиниба мезилат), гербимицин А, генистейн, эрбстатин и лавендустин А.
В предпочтительных аспектах каждый из способов включает введение или препарата HSP, или препарата α2М, предпочтительно препарата очищенного HSP или препарата очищенного α2М, субъекту, получающему лекарственное средство класса 2-фениламинопиримидина для лечения злокачественных опухолей. Более предпочтительно субъект получает Gleevec™ (то есть иматиниба мезилат) для лечения злокачественных опухолей.
В другом специальном аспекте препарат HSP или препарат α2М вводят субъекту, получающему лучевую терапию для лечения злокачественных опухолей. Для лечения лучевой терапией излучение может быть гамма-излучением или рентгеновским излучением. Способы охватывают лечение злокачественных опухолей, включая лучевую терапию, такую как внешняя дистанционная лучевая терапия, интерстициальная имплантация радиоактивных изотопов (I-125, палладия, иридия), радиоактивные изотопы, такие как стронций-89, торакальная лучевая терапия, внутрибрюшинная лучевая терапия Р-32, и/или общая абдоминальная и тазовая лучевая терапия. Для общего ознакомления с лучевой терапией см. Hellman, Chapter 16: Principles of Cancer Management: Radiation Therapy, 6th edition, 2001, DeVita et al., eds., J.B.Lippencott Company, Philadelphia. В предпочтительных аспектах лучевую терапию проводят в виде внешней дистанционной лучевой терапии или телетерапии, при которой излучение направлено из дистанционного источника. В различных предпочтительных аспектах лучевую терапию проводят в виде внутренней терапии или брахитерапии, при которой радиоактивный источник помещают в теле вблизи злокачественных клеток или массы опухоли.
В другом аспекте каждый из вышеприведенных способов включает введение препарата HSP, предпочтительно препарата очищенного HSP, субъекту, которому проводят комбинацию лечебных воздействий для лечения злокачественных опухолей. В другом аспекте каждый из вышеприведенных способов включает введение препарата α2М, предпочтительно препарата очищенного α2М, субъекту, которому проводят комбинацию лечебных воздействий для лечения злокачественных опухолей. Предпочтительно препарат HSP и препарат α2М, каждый содержит комплексы HSP-пептид и комплексы α2М-пептид соответственно, которые проявляют антигенность типа рака, который лечат. В одном таком аспекте препарат HSP вводят субъекту, получающему химиотерапию в комбинации с биологической терапией, предпочтительно цитокином. В другом таком аспекте препарат α2М вводят субъекту, получающему химиотерапию в комбинации с биологической терапией, предпочтительно цитокином. В различных аспектах цитокин выбирают из группы, состоящей из IL-1α, IL-1β, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IFNα, IFNβ, IFNγ, TNFα, TNFβ, G-CSF, GM-CSF, TGF-β, IL-15, IL-18, GM-CSF, INF-γ, INF-α, SLC, эндотелиального моноцит-активирующего белка-2 (EMAP2), MIP-3α, MIP-3β или ген МНС, такой как HLA-B7. Кроме того, другие типичные цитокины включают других представителей семейства TNF, включая TNF-α-родственный индуцирующий апоптоз лиганд (TRAIL), TNF-α-родственный вызывающий активацию цитокин (TRANCE), TNF-α-родственный слабый индуктор апоптоза (TWEAK), лиганд CD40 (CD40L), LT-α, LT-β, OX40L, CD40L, FasL, CD27L, CD30L, 4-1BBL, APRIL, LIGHT, TL1, TNFSF16, TNFSF17 и AITR-L или их функциональные части. См., например, Kwon et al., 1999, Curr. Opin. Immunol. 11: 340-345, для общего ознакомления с семейством TNF. В одном аспекте препарат HSP вводят до лечебных воздействий. В другом аспекте лечебное воздействие проводят до введения препарата HSP.
В предпочтительном аспекте препарат очищенного HSP вводят субъекту, получающему циклофосамид в комбинации с IL-12 для лечения злокачественных опухолей. В другом предпочтительном аспекте препарат очищенного α2М вводят субъекту, получающему циклофосамид в комбинации с IL-12 для лечения злокачественных опухолей.
В другом аспекте описанные выше способы используют для профилактики злокачественных опухолей или инфекционных заболеваний. В особом аспекте препарат HSP вводят вместе с невакцинным лечебным воздействием субъекту, чтобы снизить риск развития типа рака или инфекционного заболевания. В других специальных аспектах способы заключаются во введении препарата HSP с проведением невакцинного лечебного воздействия в виде предупредительного мероприятия субъекту, имеющему генетическое или негенетическое предрасположение к злокачественным опухолям или инфекционному заболеванию, или субъекту, сталкивающемуся с действием агента инфекционного заболевания. В следующих аспектах изобретение также предусматривает возможность применения каждого из предшествующих аспектов, причем препарат α2М вводят вместе с невакцинным лечебным воздействием.
Способы и композиции изобретения используют не только для не подвергавшихся лечению пациентов, но также используют при лечении пациентов частично или полностью нечувствительных к лечебному воздействию в отсутствии препарата HSP/α2М или к препарату HSP/α2М в отсутствии лечебного воздействия. В различных аспектах изобретение предусматривает способы и композиции, используемые для лечения или профилактики заболеваний и нарушений у пациентов, которые, как было показано, являются или могут быть резистентными или нечувствительными к терапиям, предусматривающим применение любого или обоих препарата HSP/α2М или лечебного воздействия. Изобретение также предусматривает способы и композиции, предусматривающие применение препарата HSP/α2М и лечебного воздействия пациентам, которые ранее получали и/или одновременно получают другие формы лечебной терапии.
Препарат HSP, используемый в способах и композициях изобретения, предпочтительно очищают и он может включать свободный HSP, не связанный с какой-либо молекулой, и молекулярные комплексы HSP с другой молекулой, такой как пептид. Комплекс HSP-пептид содержит HSP, ковалентно или нековалентно присоединенный к пептиду. Способы изобретения могут требовать или могут не требовать ковалентного или нековалентного прикрепления HSP к любому специальному антигену или антигенным пептидам до введения субъекту. Хотя пептид(ы) может быть не связан с инфекционным заболеванием или нарушением или определенными злокачественными опухолями, которые лечат, в предпочтительных аспектах препарат HSP содержит комплексы, которые проявляют антигенность антигена агента инфекционного заболевания или опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака, который лечат, соответственно. Более предпочтительно для лечения инфекционного заболевания препарат HSP содержит нековалентные комплексы HSP-пептид, выделенные из клеток, инфицированных инфекционным агентом (или неинфекционным его вариантом, проявляющим его антигенность), который вызывает инфекционное заболевание. Более предпочтительно для лечения типа рака препарат HSP содержит нековалентные комплексы HSP-пептид, выделенные из злокачественной ткани указанного типа рака или его метастаза, которые могут быть от пациента (аутогенные) или нет (аллогенные). Соответственно, для целей данного изобретения, препарат HSP представляет собой композицию, содержащую HSP, или не связанные, или связанные с другими молекулами (например, пептидами). Предпочтительно HSP очищают. Препарат HSP может включать неочищенный клеточный лизат, содержащий HSP, количество лизата, соответствующее диапазону от 100 до 108 клеточных эквивалентов. HSP можно подходящим образом выделять из многих клеточных источников в виде популяции комплексов различных пептидов, нековалентно связанных с HSP. HSP могут быть отделены от нековалентно связанных пептидов при экспозиции при низком рН и/или с аденозинтрифосфатом, или с помощью способов, известных в данной области.
Препарат α2М, используемый в способах и композициях изобретения, предпочтительно очищают и он может включать свободный α2М, не связанный с какой-либо молекулой, и молекулярные комплексы α2М с другой молекулой, такой как пептид. Комплекс α2М-пептид содержит α2М, ковалентно или нековалентно присоединенный к пептиду. Способы изобретения могут требовать или не требовать ковалентного или нековалентного прикрепления α2М к любым специфическим антигенам или антигенным пептидам до введения субъекту. Хотя пептид(ы) может быть не связан с инфекционным заболеванием или нарушением или определенными злокачественными опухолями, которые лечат, в предпочтительных аспектах препарат α2М содержит комплексы, которые проявляют антигенность антигена агента инфекционного заболевания или опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака, который лечат, соответственно. Более предпочтительно для лечения инфекционного заболевания препарат α2М содержит нековалентные комплексы α2М-пептид, выделенные из клеток, инфицированных инфекционным агентом (или неинфекционным его вариантом, проявляющим его антигенность), который вызывает инфекционное заболевание. Более предпочтительно для лечения типа рака препарат α2М содержит нековалентные комплексы α2М-пептид, выделенные из злокачественной ткани указанного типа рака или его метастаза, которые могут быть от пациента (аутогенная) или нет (аллогенная). Соответственно, для целей данного изобретения препарат α2М представляет собой композицию, содержащую α2М, или не связанный, или связанный с другими молекулами (например, пептидами). Предпочтительно α2М очищают. Препарат α2М может включать неочищенный клеточный лизат, содержащий α2М, количество лизата соответствует диапазону от 100 до 108 клеточных эквивалентов. α2М может быть выделен общепринятыми способами из многих клеточных источников в виде популяции комплексов различных пептидов, нековалентно связанных с α2Ms. α2М можно отделить от нековалентно связанных пептидов экспозицией при низком pH и/или с аденозинтрифосфатом, или другими способами, известными в данной области.
В различных аспектах источником HSP и α2М предпочтительно являются эукариоты, более предпочтительно млекопитающие и наиболее предпочтительно человек. Соответственно, препарат HSP, используемый в способах изобретения, включает эукариотические HSP, HSP млекопитающих и HSP человека. Препарат α2М включает эукариотический α2М, α2М млекопитающих и α2М человека. Эукариотический источник, из которого получают препарат HSP или препарат α2М, и субъект, которому назначают препарат HSP или препарат α2М, предпочтительно относятся к одному и тому же виду.
В одном аспекте специфическая иммуногенность препарата HSP происходит от пептида, образующего комплекс с белком теплового шока. Соответственно, в разных аспектах препарат HSP содержит комплексы белок теплового шока-пептид, в которых белки теплового шока образуют комплексы с пептидами, полученными из специального антигенного источника. В предпочтительном аспекте белковый препарат HSP содержит комплексы белок теплового шока-пептид, которые являются аутогенными. В другом предпочтительном аспекте препарат HSP содержит белки теплового шока, образующие комплексы с антигенными пептидами злокачественных клеток, из которых они происходят.В специальных аспектах антиген представляет собой опухолеспецифический антиген (то есть экспрессированный только в опухолевых клетках). В других специальных аспектах антиген является ассоциированным с опухолью антигеном (то есть относительно сверхэкспрессированный в опухолевых клетках). В еще одном предпочтительном аспекте препарат HSP содержит белки теплового шока, образующие комплексы с антигенными пептидами инфицированных клеток, из которых они происходят.
В другом аспекте специфическая иммуногенность препарата α2М происходит от пептида, образующего комплекс с α2М. Соответственно, в разных аспектах препарат α2М содержит комплексы α2М-пептид, в которых α2М образует комплекс с пептидами, полученными из специального антигенного источника. В предпочтительном аспекте белковый препарат α2М содержит комплексы α2М-пептид, которые являются аутогенными. В другом предпочтительном аспекте препарат α2М содержит α2М, образующий комплексы с антигенными пептидами злокачественных клеток, из которых их получают. В других специальных аспектах антиген представляет собой ассоциированный с опухолью антиген (то есть относительно сверхэкспрессированный в опухолевых клетках). В еще одном предпочтительном аспекте препарат α2М содержит α2М, образующий комплексы с антигенными пептидами инфицированных клеток, из которых их получают.
Также изобретение касается способов лечения и доставки, фармацевтических композиций и составов, предусматривающих применение, по крайней мере, одного невакцинного лечебного воздействия и препарата HSP или препарата α2М, и наборот, содержащих такие фармацевтические композиции.
4. ОПИСАНИЕ ЧЕРТЕЖА
Краткий обзор клинического протокола, описанного в разделе 7, ниже. Краткий обзор включает все физические исследования, обследование крови, рентгеновское исследование и исследования костного мозга, которые проводили до, во время и после вакцинации комплексом HSP-пептид.
5. ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение отчасти основано на признании того, что препарат HSP может повышать или улучшать терапевтический эффект невакцинных лечебных воздействий или терапевтических воздействий для лечения злокачественных опухолей или инфекционных заболеваний. Таким образом, данное изобретение охватывает способы и композиции, которые включают введение препарата HSP вместе с невакцинным лечебным воздействием. Также изобретение касается способов и композиций, которые включают введение препарат α2М вместе с невакцинным лечебным воздействием. В частности, изобретение касается способов лечения и композиции, которые обеспечивают лучшие терапевтические показатели, чем показатели, полученные при введении только препарата HSP или препарата α2М или при проведении только невакцинного лечебного воздействия. Источником HSP или α2М предпочтительно являются эукариоты и наиболее предпочтительно млекопитающие. Субъектом, получающим лечение, предпочтительно являются млекопитающие, включая, но не ограничиваясь перечисленным, домашних животных, таких как кошки и собаки, диких животных, таких как лисы и еноты, домашний скот и птиц, таких как лошади, крупный рогатый скот, индюки и куры, а также любых грызунов. Наиболее предпочтительно субъектом является человек.
Изобретение предусматривает способы улучшения терапевтического эффекта невакцинного лечебного воздействия, предусматривающие введение или препарата HSP, или препарата α2М, предпочтительно препарата очищенного HSP или препарата очищенного α2М, вместе с проведением лечебного воздействия. Или препарат HSP, или препарат α2М можно вводить в течение периода времени, который может предшествовать, совпадать и/или следовать за схемой лечения невакцинным лечебным воздействием. Препарат HSP или препарат α2М можно вводить одновременно, до или после проведения лечебного воздействия. Примеры лечебных воздействий включают антибиотики, противовирусные, противогрибковые соединения, противораковую терапию, такую как химиотерапевтические средства и лучевая терапия, а также биологические терапевтические средства и иммунотерапевтические средства. В предпочтительных аспектах лечебное воздействие полезно для лечения или профилактики злокачественных опухолей. В другом предпочтительном аспекте способом воздействия является Gleevec™.
В одном аспекте изобретение касается способов лечения, которые обеспечивают лучшие терапевтические показатели, чем показатели, полученные при проведении только лечебного воздействия или при введении только препарата HSP. В другом аспекте изобретение касается способов лечения, которые обеспечивают лучшие терапевтические показатели, чем показатели, полученные при проведении только лечебного воздействия или при введении только препарата α2М. Изобретение охватывает способы, при которых проведение лечебного воздействия вместе с препаратом HSP или препаратом α2М оказывает аддитивное действие или аддитивный терапевтический эффект. Изобретение также относится к синергическим результатам, при которых терапевтическая эффективность оказывается более высокой, чем аддитивная. Предпочтительно такое проведение лечебного воздействия вместе с препаратом HSP или с препаратом α2М также снижает или устраняет нежелательные или побочные эффекты. Благодаря изобретению, в некоторых аспектах, дозы невакцинного лечебного воздействия можно снизить или вводить менее часто, предпочтительно увеличивая чувствительность пациента, улучшая терапию и/или снижая нежелательные или побочные эффекты. В специальном аспекте более низкие и реже применяемые дозы химиотерапии или лучевой терапии вводят, чтобы снизить или устранить нежелательные эффекты. Альтернативно дозы препарата HSP или дозы препарата α2М можно снижать или вводить менее часто, если их вводят вместе с лечебным воздействием.
В одном аспекте данное изобретение предусматривает способ улучшения результата лечения субъекта, которому проводят лечебное воздействие, которое является невакцинным. Способ заключается во введении или препарата белка теплового шока, предпочтительно препарата очищенного HSP, или препарата α2М, предпочтительно препарата очищенного α2М, субъекту до, одновременно с или после проведения лечебного воздействия. В специальном аспекте препарат HSP или препарат α2М может усилить терапевтический эффект лечебного воздействия и улучшить результат лечения. Без связи с какой-либо теорией или механизмом, введение препарата HSP или препарата α2М млекопитающего субъекту может повысить реактивность неспецифических иммунных механизмов субъекта, например, посредством увеличения количества природных клеток-киллеров (NK) и/или ускорения созревания дендритных клеток, и/или также может повысить реактивность специфических иммунных механизмов, например, посредством увеличения количества Т-клеток CD4+ и CD8+. В специальном аспекте препарат HSP вводят до проведения лечебного воздействия. В другом специальном аспекте лечебное воздействие проводят до введения препарата HSP. В особом аспекте препарат α2М вводят до проведения лечебного воздействия. В другом специальном аспекте лечебное воздействие осуществляют до введения препарата α2М.
В другом аспекте данное изобретение предусматривает способ улучшения результата лечения субъекта, получающего препарат HSP, предпочтительно препарат очищенного HSP, проведением невакцинного лечебного воздействия субъекту до, одновременно с или после введения препарата HSP. В специальном аспекте невакцинное лечебное воздействие может усилить терапевтический эффект препарата HSP и улучшить результат лечения.
В другом аспекте данное изобретение предусматривает способ улучшения результата лечения у субъекта, получающего препарат α2М, предпочтительно препарат очищенного α2М, проведением невакцинного лечебного воздействия субъекту до, одновременно с или после введения препарата α2М. В специальном аспекте, невакцинное лечебное воздействие может усилить терапевтический эффект препарата α2М и улучшить результат лечения.
В некоторых аспектах введение препарата HSP/α2М без проведения лечебного воздействия или проведение лечебного воздействия без введения препарата HSP/α2М не является терапевтически эффективным. В специальном аспекте количество препарата HSP/α2М или лечебного воздействия применяют в количестве, недостаточном, чтобы они были терапевтически эффективны отдельно. В альтернативных аспектах оба или, по крайней мере, один препарат HSP/α2М или одно лечебное воздействие оказываются терапевтически эффективными, если их применяют отдельно.
В различных аспектах способы включают введение препарата HSP, предпочтительно препарата очищенного HSP, субъекту, которому проводят лечебное воздействие для лечения злокачественных опухолей или инфекционных заболеваний. Предпочтительно препарат HSP содержит комплексы HSP-пептид, проявляющие антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака или антигена инфекционного агента, то есть белков теплового шока, образующих комплексы с антигенными пептидами злокачественных клеток или инфицированных клеток, из которых получают комплексы. Соответственно, в одном аспекте специфическая иммуногенность препарата HSP происходит от пептида, образующего комплекс с HSP. В предпочтительных аспектах комплексы HSP-пептид выделяют из источника антигена, такого как злокачественные ткани или инфицированные ткани. При практическом применении изобретения, такие комплексы HSP-пептид предпочтительно являются аутогенными для индивидуального субъекта, то есть получены из тканей субъекта, которому вводят препарат HSP или проводят лечебное воздействие, но не обязательно (то есть аллогенны для индивидуального субъекта).
В различных аспектах способы включают введение препарата α2М, предпочтительно очищенного препарата α2М, субъекту, которому проводят лечебное воздействие для лечения злокачественных опухолей или инфекционных заболеваний. Предпочтительно препарат α2М содержит комплексы α2М-пептид, проявляющие антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака или антигена инфекционного агента, то есть α2М, образующего комплекс с антигенными пептидами злокачественных клеток или инфицированных клеток, из которых получают комплексы. Соответственно, в одном аспекте специфическая иммуногенность препарата α2М происходит от пептида, образующего комплекс с α2М. В предпочтительных аспектах комплексы α2М-пептид выделяют из источника антигена, такого как злокачественные ткани или инфицированные ткани. При практическом применении изобретения, такие комплексы α2М-пептид предпочтительно являются аутогенными для индивидуального субъекта, то есть получают из тканей субъекта, которому вводят препарат α2М и проводят лечебное воздействие, но необязательно (то есть аллогенные для индивидуального субъекта).
В одном аспекте способы включают введение препарата HSP или препарата α2М, предпочтительно препарата очищенного HSP или препарата очищенного α2М, субъекту, которому проводят лечебное воздействие для лечения инфекционного заболевания. Такие лечебные воздействия известны в данной области и включают, но не ограничиваясь перечисленным, антибиотики, противовирусные средства, противогрибковые средства, а также биологические и иммунотерапевтические средства. Предпочтительно препарат HSP содержит комплексы HSP-пептид, которые проявляют антигенность агента инфекционного заболевания. Предпочтительно препарат α2М содержит комплексы α2М-пептид, которые проявляют антигенность агента инфекционного заболевания. В специальном аспекте результат лечения типа инфекционного заболевания у субъекта, которому проводят невакцинное лечебное воздействие, улучшают введением комплексов HSP-пептид, содержащих HSP, образующий комплекс с пептидом, проявляющим антигенность антигена агента указанного типа инфекционного заболевания. Предпочтительно комплексы HSP-пептид не присутствуют в смеси с HSP или α2М, которые не образуют комплексы с пептидом, проявляющим антигенность антигена агента того же инфекционного заболевания (см. Международную заявку №PCT/US01/28840, поданную 15 сентября 2001). В одном аспекте препарат HSP вводят до проведения лечебного воздействия. В другом аспекте лечебное воздействие проводят до введения препарата HSP. В другом специальном аспекте результат лечения типа инфекционного заболевания у субъекта, которому проводят невакцинное лечебное воздействие, улучшают введением комплексов α2М-пептид, содержащих α2М, образующий комплекс с пептидом, проявляющим антигенность антигена агента указанного типа инфекционного заболевания. Предпочтительно комплексы α2М-пептид не присутствуют в смеси с HSP или α2М, которые не образуют комплексы с пептидом, проявляющим антигенность антигена агента указанного инфекционного заболевания. Предпочтительно препарат α2М вводят до проведения лечебного воздействия.
В другом аспекте способы включают введение или препарата HSP, или препарата α2М, предпочтительно препарата очищенного HSP или препарата очищенного α2М, субъекту, которому проводят лечебное воздействие для лечения злокачественных опухолей. Такое лечебное воздействие включает, но не ограничиваясь перечисленным, противораковые терапии, такие как химиотерапия и лучевая терапия, а также гормональную терапию, биологическую терапию и иммунотерапию, не ограничиваясь перечисленным. В способах изобретения противораковые средства, которые можно использовать, включают цитотоксические средства, антимитогенные средства, средства, стабилизирующие тубулин, агенты, ингибирующие образование микротрубок, средства, активирующие топоизомеразу, алкилирующие агенты, вещества, взаимодействующие с ДНК, антиметаболиты, антиметаболиты РНК/ДНК и антиметаболиты ДНК. Предпочтительно противораковым средством является химиотерапевтическое средство. Предпочтительно препарат HSP или препарат α2М вводят субъекту, которому проводят химиотерапию или лучевую терапию для лечения злокачественных опухолей. Предпочтительно препарат HSP содержит комплексы HSP-пептид, которые проявляют антигенность типа рака, который лечат. Предпочтительно, когда препаратом является препарат α2М, препарат α2М содержит комплексы α2М-пептид, которые проявляют антигенность типа рака, который лечат. Соответственно, в предпочтительных аспектах изобретение предусматривает способы улучшения результата лечения злокачественных опухолей у субъекта, которому проводят лечебное воздействие, которое является невакцинным, используя комплексы HSP-пептид, содержащие HSP, образующий комплекс с пептидом, проявляющим антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака, или используя комплексы α2М-пептид, содержащие α2М, образующий комплекс с пептидом, проявляющим антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака. В некоторых предпочтительных аспектах такие комплексы HSP-пептид и комплексы α2М-пептид не разбавляют ни HSP, ни α2М, которые не образуют комплексы с пептидом, проявляющим антигенность антигена того же типа рака. Предпочтительно препарат HSP или препарат α2М вводят до проведения лечебного воздействия.
В особом аспекте препарат HSP вводят субъекту, получающему химиотерапевтическое средство для лечения злокачественных опухолей. В другом предпочтительном аспекте препарат α2М вводят субъекту, получающему химиотерапевтическое средство для лечения злокачественных опухолей. Такие химиотерапевтические средства известны в данной области и включают, но не ограничиваясь ими, метотрексат, таксол, меркаптопурин, тиогуанин, гидроксимочевину, цитарабин, циклофосфамид, ифосфамид, нитрозомочевины, цисплатин, карбоплатин, митомицин, дакарбазин, прокарбазин, этопозид, кампатецины, блеомицин, доксорубицин, ибарубицин, даунорубицин, дактиномицин, пликамицин, митоксантрон, аспарагиназу, винбластин, винкристин, винорелбин, паклитаксел и доцетаксел, доксорубицин, эпирубицин, 5-фторурацил, таксаны, такие как доцетаксел и паклитаксел, леуковорин, левамисол, иринотекан, эстрамистин, этопозид, нитрозомочевины, такие как кармустин и ломустин, алкалоиды барвинки, соединения платины, митомуцин, гемцитабин, гексаметилмеламин, топотекан, ингибиторы тирозинкиназы, тирпостины, Gleevec™ (иматиниба мезилат), гербимицин А, генистейн, эрбстатин и лавендустин А. В предпочтительном аспекте химиотерапевтическим агентом является Gleevec™ (иматиниба мезилат).
В других аспектах подходящие химиотерапевтические средства включают, но не ограничиваясь ими, метротрексат, таксол, L-аспарагиназу, меркаптопурин, тиогуанин, гидроксимочевину, цитарабин, циклофосфамид, ифосфамид, нитрозомочевины, цисплатин, карбоплатин, митомицин, дакарбазин, прокарбазин, топотекан, азотистые иприты, цитоксан, этопозид, 5-фторурацил, BCNU, иринотекан, камптотецины, блеомицин, доксорубицин, идарубицин, даунорубицин, дактиномицин, пликамицин, митоксантрон, аспарагиназу, винбластин, винкристин, винорелбин, паклитаксел и доцетаксел. В предпочтительном аспекте противораковым средством может быть, но не ограничиваясь перечисленным, лекарственное средство, приведенное в табл. 1.







Дополнительные противораковые средства, которые можно использовать в способах данного изобретения, включают, но не ограничиваясь ими, ацивицин, акларубицин, акодазол гидрохлорид, акринин, адозелесин, алдеслеукин, альтретамин, амбомицин, аметантрон ацетат, аминоглутетимид, амсакрин, анастрозол, антрамицин, аспарагиназу, асперлин, азацитидин, азетепа, азотомицин, батимастат, бензодепа, бикалутамид, бисантрен гидрохлорид, биснафид димезилат, бизелесин, блеомицин сульфат, брехинар натрий, бропиримин, бусульфан, кактиномицин, калустерон, карацемид, карбетимер, карбоплатин, кармустин, карубицин гидрохлорид, карзелесин, цедефингол, хлорамбуцил, циролемицин, цисплатин, кладрибин, криснатол мезилат, хлорфосфамид, цитарабин, дакарбазин, дактиномицин, даурорубицин гидрохлорид, децитабин, дезоксирмаплатин, дезагуанин, дезагуанин мезилат, диазихион, доцетаксел, доксорубицин, доксорубицин гидрохлорид, дролоксифен, дролоксифен цитрат, дромостанолон пропионат, дуазомицин, эдатрексат, эфлорпитин гидрохлорид, элсамитруцин, энлоплатин, энпромат, эпипропидин, эпирубицин гидрохлорид, эрбулозол, эзорубицин гидрохлорид, эстрамустин, эстрамустин фосфат натрия, этанидазол, этопозид, этопозид фосфат, этоприн, фадрозол гидрохлорид, фаразабин, фенретинид, флоксуридин, флударабин фосфат, фторурацил, фторцитабин, фосхидон, фостриецин натрий, гемцитабин, гемцитабин гидрохлорид, гидроксимочевина, идарубицин гидрохлорид, ифосфамид, илмофозин, интерлейкин II (включая рекомбинантный интерлейкин II или rIL2), интерферон альфа-2а, интерферон альфа-2b, интерферон альфа-n1, интерферон альфа-n3, интерферон бета-Ia, интерферон гамма-Ib, ипроплатин, иринотекан гидрохлорид, ланреотид ацетат, летрозол, леупролид ацетат, лиарозол гидрохлорид, лометрексол натрий, ломустин, лозоксантрон гидрохлорид, мазопрокол, майтанзин, мехлоретамин гидрохлорид, мегестрол ацетат, меленгестрол ацетат, мелфалан, меногарил, меркаптопурин, метотрексат, метротрексат натрия, меоприн, метуредепа, митиндомид, митокарцин, митокромин, митогиллин, митомальцин, митомицин, митоспер, митотан, митоксантрон гидрохлорид, микофенолнвая кислота, нокодазол, ногаламицин, ормаплатин, оксисуран, паклитаксел, пегаспаргазу, пелиомицин, пентамустин, пепломицин сульфат, перфосфамид, пироброман, пипосульфан, пироксантрон гидрохлорид, пликамицин, пломестан, порфимер натрия, порфиромицин, преднимустин, прокарбазин гидрохлорид, пуромицин, пуромицин гидрохлорид, пиразофурин, рибоприн, роглетимид, сафингол, сафингол гидрохлорид, семистин, симтразен, спарфосат натрия, спарсомицин, спирогерманий гидрохлорид, спиромустин, спироплатин, стрептонигрин, стрептозоцин, сулофенир, талисомицин, текогалан натрия, тегафур, телоксантрон гидрохлорид, темопорфин, тенипозид, тероксирон, тестолактон, тиамиприн, тиогуанин, тиотепа, тиазофурин, тирапазамин, торемифен цитрат, трестолон ацетат, трицирибин фосфат, триметрексат, триметрексат глукуронат, трипторелин, тубулозол гидрохлорид, урацил иприт, уредепа, вапреотид, вертепорфин, винбластин сульфат, винкристин сульфат, виндезин, виндезин сульфат, винепидин сульфат, винглицинат сульфат, винлеурозин сульфат, винзолидин сульфат, винорелбин тартрат, винрозидин сульфат, ворозол, зениплатин, зиностатин, зорубицин гидрохлорид.
Другие противораковые лекарственные средства, которые можно использовать включают, но не ограничиваясь ими, 20-эпи-1,25 дигидроксивитамин D3, 5-этинилурацил, абиратерон, акларубицин, ацилфульвен, адеципенол, адозелезин, альдеслеукин, антагонисты ALL-TK, альтретамин, амбамустин, амидокс, амифостин, аминолевулиновая кислота, амрубицин, амсакрин, анагрелид, анастрозол, андрографолид, ингибиторы ангиогенеза, антагонист D, антагонист G, антареликс, антидорзализирующий морфогенетический белок-1, антиандроген, карцинома простаты, антиэстроген, антинеопластон, антисмысловые олигонуклеотиды, афидиколин глицинат, модуляторы апоптозного гена, регуляторы апоптоза, апуриновая кислота, аrа-CDP-DL-PTBA, аргининдеаминазу, асулакрин, атаместан, атримустин, аксинастатин 1, аксинастатин 2, аксинастатин 3, азасетрон, азатоксин, азатирозин, производные баккатина III, баланол, батимастат, антагонисты BCR/ABL, бензохлорины, бензоилстауроспорин, производные бета-лактама, бета-алетин, бетакламицин В, бетулиновая кислота, ингибитор bFGF, бикалутамид, бисантрен, бисазиридинилспермин, биснафид, бистратен А, бизелезин, брефлат, бропиримин, будотитан, бутионин сульфоксимин, кальципотриол, калфостин С, производные камптотецина, канарипокс IL-2, капецитабин, карбоксамид-амино-триазол, карбоксиамидотриазол, CaRest M3, CARN 700, ингибитор, полученный из хряща, карзелезин, ингибиторы казеинкиназы (ICOS), кастаноспермин, цекропин В, цетрореликс, хлорины, хлорхиноксалин сульфонамид, цикапрост, цис-порфирин, кладрибин, аналоги кломифена, клотримазол, коллимицин А, коллимицин В, комбретастатин А4, аналог комбретастатин, конагенин, крамбесцидин 816, криснатол, криптофицин 8, производные криптофицина А, курацин А, циклопентантрахиноны, циклоплатам, ципемицин, цитарабин окфосфат, цитолитический фактор, цитостатин, дакликсимаб, децитабин, дегидродидемнин В, деслорелин, дексаметазон, дексифосфамид, дексразоксан, дексверапамил, диазихион, дидемнин В, дидокс, диэтилнорспермин, дигидро-5-азацитидин, дигидротаксол 9-, диоксамицин, дифенилспиромустин, доцетаксел, докозанол, долазетрон, доксифлуридин, дролоксифен, дронабинол, дуокармицин SA, эбселен, экомустин, эделфозин, эдреколомаб, эфлорнитин, элемен, эмитефур, эпирубицин, эпристерид, аналог эстрамустина, агонисты эстрогена, антагонисты эстрогена, этанидазол, этопозид фосфат, эксеместан, фадрозол, фазарабин, фенретинид, филграстим, финастерид, флавопиридол, флезеластин, флуастерон, флударабин, фтордауноруницин гидрохлорид, форфенимекс, форместан, фостриецин, фотемустин, гадолиний тексафирин, галлий нитрат, галоцитабин, ганиреликс, ингибиторы желатиназы, гемцитабин, ингибиторы глутитиона, гепсульфам, герегилин, гексаметилен бисацетамид, гиперицин, ибандроновая кислота, идарубицин, идоксифен, идрамантон, илмофозин, иломастат, имидозоакридоны, имихимод, иммуностимулирующие пептиды, ингибитор рецептора инсулин-подобного фактора роста-1, агонисты интерферона, интерфероны, интерлейкины, иобенгуан, иододоксорубицин, ипомеанол 4-, ироплакт, ирсогладин, изобенгазол, изогомогаликондрин В, итасетрон, джасплакинолид, кагалалид F, ламелларин-N триацетат, ланреотид, леинамицин, ленограстим, лентинан сульфат, лептостатин, летрозол, ингибирующий лейкоз фактор, лейкоцитарный альфа-интерферон, лейпролид + эстроген + прогестерон, лейпрорелин, левамизол, лиарозол, линейный аналог полиамина, липофильный дисахаридный пептид, липофильные соединения платины, лиссоклинамид 7, лобаплатин, ломбрицин, лометрексол, линидамин, лозоксантрон, ловастатин, локсорибин, луртотекан, литий тексафирин, лизофиллин, литические пептиды, маитазин, манностатин А, маримастат, мазопрокол, маспин, ингибиторы матрилизинов, ингибиторы матриксных металлопротеиназ, меногарил, мербарон, метерелин, метиониназу, метоклопрамид, ингибитор MIF, мифепристон, милтефозин, миримостин, несоответствующая двухнитевая РНК, митогуазон, митолактол, аналоги митомицина, митонафид, митотоксин, сапорин-фактор роста фибробластов, митоксантрон, мофаротен, молграмостин, моноклональные антитела, хорионический гонадотропин человека, монофосфорил липид А+клеточная стенка миобактерий sk, мопидамол, ингибитор гена мультилекарственной резистентности, политерапия на основе опухолевого супрессора-1, ипритное противораковое вещество, микапероксид В, экстракт клеточной стенки микобактерий, мириапорон, N-ацетилдиналин, N-замещенные бензамиды, нафарелин, нагрестип, налоксон + пентазоцин, напавин, нафтерпин, нартограстим, недаплатин, неморубицин, неридроновую кислоту, нейтральную эндопептидазу, нилутамид, низамицин, модуляторы оксида азота, нитроксидный антиоксидант, нитруллин, О6-бензилгуанин, октреотид, окиценон, олигонуклеотиды, онапристон, ондансетрон, ондансетрон, орацин, аппарат для перорального введения цитокинов, ормаплатин, озатерон, оксалиплатин, оксауномицин, паклитаксел, аналоги паклитакселя, производные паклитакселя, палауамин, пальмитоилгизоксин, памидроновую кислоту, панакситриол, паномифен, парабактин, пазеллиптин, пегаспарагазу, пелдезин, пентосан полисульфат натрия, пентостатин, пентрозол, перфлуброн, перфосфамид, периллиловый спирт, феназиномицин, фенилацетат, ингибиторы фосфатазы, пицибанил, пилокарпин гидрохлорид, пирарубицин, пиритрексим, плацетин А, плацетин В, ингибитор активатора плазминогена, платиновый комплекс, соединения платины, комплекс платина-триамин, порфимер натрия, порфиромицин, преднизолон, пролил-бис-акридон, простагландин J2, ингибиторы протеасом, иммунный модулятор на основе белка А, ингибитор протеинкиназы С, ингибиторы протеинкиназы С, микроалгал, белковые ингибиторы тирозинфосфатазы, ингибиторы пириннуклеозидфосфорилазы, пурпурины, пиразолоакридин, пиридоксилированный конъюгат гемоглобин-полиоксиэтилен, антагонисты raf, ралтитрексед, рамосетрон, ингибиторы ras-фарнезил-протеинтрансферазы, ингибиторы ras, ингибитор ras-GAP, деметилированный ретеллиптин, рений Re 186 этидронат, ризоксин, ризозимы, ретинамид RII, роглетимид, рогитукин, ромуртид, рохинимекс, рубигинон В1, рубоксил, сафингол, саинтопин, SarCNU, саркофитол А, сарграмостим, миметики Sdi 1, семустин, ингибитор 1 старения, смысловые олигонуклеотиды, ингибиторы сигнальной трансдукции, модуляторы сигнальной трансдукции, одноцепочечный антигенсвязывающий белок, сизофиран, собузоксан, борокаптат натрия, фенилацетат натрия, солверол, соматомедин-связывающий белок, сонермин, спарфозивую кислоту, спикамицин D, спиромустин, спленопентин, спонгистатин 1, свкалмин, ингибитор стволовых клеток, ингибиторы деления стволовых клеток, стипиамид, ингибиторы стромелизина, сульфинозин, сверхактивный антагонист вазоактивного интестинального пептида, сурадиста, сурамин, сваинсонин, синтетические глюкозамингликаны, таллимустин, тамоксифен метиодид, тауромустин, тазаротен, текогалан натрий, тегафур, теллурапирилий, ингибиторы теломеразы, темопорфин, темозоломид, тенипозид, тетрахлордекаоксид, тетразомин, талибластин, тиокаралин, тромбопоэтин, тромбопоэтин-миметик, тималфазин, агонист рецептора тимопоэтина, тимотринан, тироид-стимулирующий гормон, тин-этил-этиопурпурин, тирапазамин, титаносен бихлорид, топсентин, торемифен, тотипотентный фактор стволовых клеток, ингибиторы трансляции, третиноин, триацетилуридин, трицирибин, триметрексат, триптогелин, трописетрон, туростерид, ингибиторы тирозинкиназы, тирфостины, ингибиторы UBC, убенимекс, ингибиторный фактор роста мочеполового синуса, антагонисты рецептора урокиназы, вапреотид, вариолин В, векторную систему, эритроцитную генную терапию, веларезол, верамин, вердины, вертепорфин, винорелбин, винксалтин, витаксин, ворозол, занотерен, зениплатин, зиласкорб и зиностатин стималамер. Предпочтительные химиотерапевтические средства изобретения включают Gleevec™ (иматиниба мезилат) и другие ингибиторы тирозинкиназы.
В предпочтительных аспектах каждый из описанных выше способов включает введение или препарата HSP, или препарата α2М, предпочтительно препарата очищенного HSP или препарата очищенного α2М, субъекту, получающему лекарственное средство класса 2-фениламинопиримидина для лечения злокачественных опухолей. Более предпочтительно субъект получает Gleevec™ (то есть иматиниба мезилат) для лечения злокачественных опухолей.
В другом предпочтительном аспекте препарат HSP или препарат α2М вводят субъекту, получающему лучевую терапию для лечения злокачественных опухолей. Что касается лучевой терапии, излучением может быть гамма-излучение или рентгеновское излучение. Способы охватывают лечение злокачественных опухолей, включающее лучевую терапию, такую как внешне-дистанционная лучевая терапия, интерстициальная имплантация радиоактивных изотопов (I-125, палладий, иридий), радиоизотопы, такие как стронций-89, теракальная лучевая терапия, внутрибрюшинная лучевая терапия Р-32 и/или общая абдоминальная и лучевая терапия мочеполового синуса. Для общего ознакомления с лучевой терапией см. Hellman, Chapter 16: Principles of Cancer Management: Radiation Therapy, 6th edition, 2001, DeVita et al., eds., J.B.Lippencott Company, Philadelphia. В предпочтительных аспектах лучевую терапию применяют в виде внешнего дистанционного излучения или телетерапии, при которых излучение направляют из дистанционного источника. В различных предпочтительных аспектах лучевую терапию осуществляют в виде внутренней терапии или брахитерапии, при которой радиоактивный источник помещают внутри организма вблизи злокачественных клеток или опухолевой массы.
В другом аспекте каждый из описанных выше способов включает введение препарата HSP, предпочтительно препарата очищенного HSP, субъекту, получающему комбинацию лечебных воздействий для лечения злокачественных опухолей. В другом аспекте каждый из приведенных выше способов включает введение препарата α2М, предпочтительно препарата очищенного α2М, субъекту получающему комбинацию лечебных воздействий для лечения злокачественных опухолей. Предпочтительно препарат HSP и препарат α2М, каждый содержит комплексы HSP-пептид и комплексы α2М-пептид соответственно, которые проявляют антигенность типа рака, который лечат. В одном таком аспекте препарат HSP вводят субъекту, получающему химиотерапию в комбинации с биологической терапией, предпочтительно с цитокином. В другом таком аспекте препарат α2М вводят субъекту, получающему химиотерапию в комбинации с биологической терапией, предпочтительно с цитокином. В различных аспектах цитокин выбирают из группы, состоящей из IL-1α, IL-1β, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IFNα, IFNβ, IFNγ, TNFα, TNFβ, G-CSE, GM-CSE, TGF-β, IL-15, IL-18, GM-CSE, IFN-γ, INF-α, SLC, эндотелиального моноцит-активирующего белка-2 (EMAP2), MIP-3α, MIP-3β или гена MHC, такого как HLA-B7. Кроме того, другие характерные цитокины включают другие представители семейства TNF, включающего, но не ограничиваясь перечисленным, TNF-α-родственный апоптоз-индуцирующий лиганд (TRAIL), TNF-α-родственный, индуцированный активацией цитокин (TRANCE), TNF-α-родственный слабый индуктор апоптоза (TWEAK), лиганд CD40 (CD40L), LT-α, LT-β, OX40L, CD40L, FasL, CD27L, CD30L, 4-1BBL, APRIL, LIGHT, TL1, THFSF16, TNFSF17 и AITR-L или их функциональные части. См., например, Kwon et al., 1999, Curr. Opin. Immunol. 11: 340-345 для общего рассмотрения семейства TNF. Предпочтительно препарат HSP вводят до лечебных воздействий.
В специальном аспекте препарат очищенного HSP вводят субъекту, получающему циклофосфамид в комбинации с IL-12 для лечения злокачественных опухолей. В другом специальном аспекте препарат очищенного α2М вводят субъекту, получающему циклофосфамид в сочетании с IL-12 для лечения злокачественных опухолей.
В другом специальном аспекте химиотерапевтическим средством является ингибитор тирозинкиназы, препарат HSP получают от больного со злокачественной опухолью, которую лечат, а химиотерапию проводят до введения препарата HSP. В следующем специальном аспекте противораковым средством является химиотерапевтический Gleevec™ (иматиниба мезилат), препарат HSP содержит hsp70, полученный от пациента со злокачественной опухолью, которую лечат, и химиотерапевтическое средство применяют до введения препарата HSP. В другом особом аспекте препарат HSP содержит комплексы hsp70-пептид, полученные от больного со злокачественной опухолью, которую лечат. Другой особый аспект охватывает способ лечения CML у субъекта, получающего приблизительно от 400 мг до 800 мг иматиниба мезилата ежедневно, включающий введение препарата белка теплового шока указанному субъекту, причем указанный препарат белка теплового шока содержит комплексы hsp70-пептид. В предпочтительных аспектах препарат белка теплового шока вводят один раз в неделю, и препарат белка теплового шока содержит комплексы hsp70-пептид, полученные от указанного субъекта.
В некоторых специальных аспектах препарат HSP вводят субъекту, уже получающему Gleevec™ (например, 400-800 мг ежедневно в капсульной форме, дозы 400-600 мг вводят раз в день, или дозу 800 мг вводят в двух дозах по 400 мг каждая). В таких аспектах препарат HSP/α2М в начальной стадии вводят субъекту, который уже получал Gleevec™ в отсутствие препарата HSP/α2М 2 дня, 2 дня в неделю, 1 неделю в месяц, 1 месяц из 6 месяцев, 6 месяцев в 1 году до введения препарата HSP/α2М кроме Gleevec™. В особом аспекте препарат HSP/α2М вводят субъекту, когда субъект проявляет резистентность к лечению только Gleevec™.
В других аспектах препарат HSP/α2М сначала вводят субъекту одновременно с начальным введением Gleevec™.
В еще следующих специальных аспектах Gleevec™ (например, 400-800 мг ежедневно в капсульной форме) вводят субъекту, уже получающему лечение, включающее введение препарата HSP/α2М. В таких аспектах Gleevec™ сначала вводят субъекту, который уже получал препарат HSP/α2М в отсутствие Gleevec™ 2 дня, 2 дня в неделю, 1 неделю в 1 месяц, 1 месяц из 6 месяцев, 6 месяцев в 1 году до назначения Gleevec™ помимо введения препарата HSP/α2М.
В специальном аспекте Gleevec™ вводят перорально. В другом особом аспекте препарат HSP вводят внутрикожно.
В каждом из способов, рассматриваемых выше, пациент, в качестве примера, получает от 50 мг до 100 мг, от 100 мг до 200 мг, от 200 мг до 300 мг, от 300 мг до 400 мг, от 400 мг до 500 мг, от 500 мг до 600 мг, от 600 мг до 700 мг, от 700 мг до 800 мг, от 800 мг до 900 мг или от 900 мг до 1000 мг Gleevec™ ежедневно. В некоторых аспектах общую ежедневную дозу вводят субъекту в виде двух ежедневных доз от 25 мг до 50 мг, от 50 мг до 100 мг, от 100 мг до 200 мг, от 200 мг до 300 мг, от 300 мг до 400 мг или 400 мг до 500 мг.
Другие рассматриваемые лечебные воздействия включают, но не ограничиваясь ими, противовирусные средства, известные в данной области. Такие противовирусные средства включают, но не ограничиваясь перечисленным, рибаварин, рифампицин, AZT, ddI, ddC, ацикловир и ганцикловир.
Также изобретение охватывает лечебные воздействия, которые представляют собой антибиотики, известные в данной области, включающие, но не ограничиваясь перечисленным, аминогликозидазные антибиотики (например, апрамицин, арбекацин, бамбермицины, бутирозин, дибекацин, неомицин, неомицин, ундециленат, нетилмицин, паромомицин, рибостамицин, сизомицин и спектиномицин), антибиотики, производные амфеникола (например, азидамфеникол, хлорамфеникол, флорфеникол и тиамфеникол), анзамициновые антибиотики (например, рифамид и рифампин), карбацефемы (например, лоракарбеф), карбапенемы (например, биапенем и имипенем), цефалоспорины (например, цефаклор, цефадроксил, цефамандол, цефатризин, цефазедон, цефозопран, цефпимизол, цефпирамид и цефпиром), цефамицины (например, цефбуперазон, цефметазол и цефминокс), монобактамы (например, азтреонам, карумонам и тигемонам), оксацефемы (например, фломоксеф и моксаластам), пенициллины (например, амдиноциллин, амдиноциллин пивоксил, амоксициллин, бакампициллин, бензилпенициллиновая кислота, бензилпенициллин натрий, эпициллин, фенбеннициллин, флоксациллин, пенамкцмллин, пенетамат гидрохлорид, пенициллин о-бенетамин, пенициллин О, пенициллин V, пенициллин V бензатин, пенициллин V гидрабамин, пенимепициклин и фенцигициллин калий), линкозамиды (например, клиндамицин и линкомицин), макролиды (например, азитромицин, карбомицин, кларитомицин, диритромицин, эритромицин и эритромицин ацистрат), амфомицин, бацитрацин, капреомицин, колистин, эндурацидин, энвиомицин, тетрациклины (например, апициклин, хлортетрациклин, хломоциклин и демеклоциклин), 2,4-диаминопиримидины (например, бродимоприм), нитрофураны (например, фуралтадон и фуразолий хлорид), хинолоны и их аналоги (например, циноксацин, ципрофлоксацин, клинафлоксацин, флумехин и грепаглоксацин), сульфонамиды (например, ацетил-сульфаметоксипиразин, бензилсульфамид, ноприлсульфамид, фталилсульфацетамид, сульфахризоидин и сульфацитин), сульфоны (например, диатимосульфон, глюкосульфон натрий и соласульфон), циклосерин, мупироцин и туберин.
Также изобретение охватывает лечебные воздействия, которые представляют собой противогрибковые средства, известные в данной области и включающие, но не ограничиваясь перечисленным, полиены (например, амфотерицин b, кандицидин, мепартрицин, натамицин и нистатин), аллиламины (например, бутенафин и нафтифин), имидазолы (например, бифоназолы, бутоконазолы, хлордантоин, флутримазол, изоконазол, кетоконазол и ланоконазол), тиокарбаматы (например, толциклат, толиндат и толнафтат), триазолы (например, флуконазол, итраконазол, саперконазол и терконазол), бромсалицилхлоранилид, буклозамид, кальций пропионат, хлорфенезин, циклопирокс, азазерин, гризеофульвин, олигомицины, неомицин ундециленат, пирролнитрин, сикканин, туберцидин и виридин.
В другом аспекте вышеприведенные способы полезны для профилактики злокачественных опухолей или инфекционного заболевания. В особом аспекте препарат HSP вводят в комбинации с невакцинным лечебным воздействием субъекту, чтобы снизить риск появления типа рака или инфекционного заболевания. В других специальных аспектах способы заключаются во введении препарата HSP с проведением невакцинного лечебного воздействия как предупредительной меры субъекту, имеющему генетическую или негенетическую предрасположенность к злокачественным опухолям или инфекционному заболеванию, или субъекту, подвергшемуся воздействию агента инфекционного заболевания. В следующих аспектах изобретение также предусматривает каждый из предшествующих аспектов, который также можно применять, когда препарат α2М вводят в комбинации с невакцинным лечебным воздействием.
Способы и композиции изобретения полезны не только для не подвергавшихся лечению пациентов, но они также полезны для лечения пациентов частично или полностью не чувствительных к лечебному воздействию в отсутствие препарата HSP/α2М или к препарату HSP/α2М в отсутствие лечебного воздействия. В различных аспектах изобретение предусматривает способы и композиции, полезные для лечения или профилактики заболеваний или нарушений у пациентов, которые, как было показано, являются или могут быть резистентными или нечувствительными к терапиям, включающим применение или одного или обоих препаратов HSP/α2М или лечебного воздействия. Изобретение также включает способы и композиции, предусматривающие применение препарата HSP/α2М и лечебного воздействия пациенту, который ранее получал и/или одновременно получает другие формы медикаментозной терапии.
Препарат HSP, используемый в способах и композициях изобретения, предпочтительно очищают и он может содержать свободный HSP, не связанный с какой-либо молекулой, и молекулярные комплексы HSP с другой молекулой, такой как пептид. Комплекс HSP-пептид содержит HSP, ковалентно или нековалентно присоединенный к пептиду. Способы изобретения могут требовать или могут не требовать ковалентного или нековалентного прикрепления HSP к каким-либо определенным антигенам или антигенным пептидам до введения субъекту. Хотя пептид(ы) могут быть не связаны с инфекционным заболеванием или нарушением или особыми злокачественными опухолями, которые лечат, в предпочтительных аспектах препарат HSP содержит комплексы, которые проявляют антигенность к антигену агента инфекционного заболевания или опухолеспецифическому антигену или ассоциированному с опухолью антигену типа рака, который лечат, соответственно. Более предпочтительно для лечения инфекционного заболевания препарат HSP содержит нековалентные комплексы HSP-пептид, выделенные из клеток, инфицированных инфекционным агентом (или его неинфекционным вариантом, проявляющим его антигенность), который вызывает инфекционное заболевание. Более предпочтительно для лечения типа рака препарат HSP содержит нековалентные комплексы HSP-пептид, выделенные из злокачественной ткани указанного типа рака или его метастаза, которые могут быть от пациента (аутогенные) или нет (аллогенные). Соответственно, для целей данного изобретения препарат HSP представляет собой композицию, содержащую HSP, или не связанные, или связанные с другими молекулами (например, пептидами). Предпочтительно HSP очищают. Препарат HSP может заключать в себе неочищенный клеточный лизат, содержащий HSP, количество лизата соответствует диапазону от 100 до 108 клеточных эквивалентов. HSP обычно можно выделять из многих клеточных источников, в которых популяции комплексов различных пептидов нековалентно связаны с HSP. HSP можно отделять от нековалентно связанных пептидов, подвергая воздействию низкого pH и/или аденозинтрифосфата, или другими способами, известными в данной области.
Препарат α2М, используемый в способах и композициях изобретения, предпочтительно очищают и он может включать свободный α2М, не связанный с какой-либо молекулой, и молекулярные комплексы α2М с другой молекулой, такой как пептид. Комплекс α2М-пептид содержит α2М, ковалентно или нековалентно присоединенный к пептиду. Способы изобретения могут требовать или могут не требовать ковалентного или нековалентного прикрепления α2М к каким-либо определенным антигенам или антигенным пептидам до введения субъекту. Хотя пептид(ы) могут быть не связанными с инфекционным заболеванием или нарушением или определенными злокачественными опухолями, которые лечат, в предпочтительных аспектах препарат α2М содержит комплексы, которые проявляют антигенность антигена агента инфекционного заболевания или опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака, который лечат, соответственно. Более предпочтительно для лечения инфекционного заболевания препарат α2М содержит нековалентные комплексы α2М-пептид, выделенные из клеток, инфицированных инфекционным агентом (или его неинфекционным вариантом, проявляющим его антигенность), который вызывает инфекционное заболевание. Более предпочтительно для лечения злокачественных опухолей препарат α2М содержит нековалентные комплексы α2М-пептид, выделенные из злокачественной ткани указанного типа рака или его метастаза, которые могут быть от пациента (аутогенные) или нет (аллогенные). Соответственно, для целей данного изобретения препарат α2М представляет собой композицию, содержащую α2М, или не связанный, или связанный с другими молекулами (например, пептидами). Предпочтительно α2М очищают. Препарат α2М может включать неочищенный клеточный лизат, содержащий α2М, количество лизата соответствует диапазону от 100 до 108 клеточных эквивалентов. α2М обычно можно выделить из многих клеточных источников, в которых популяция комплексов различных пептидов нековалентно связана с α2М. α2М можно отделять от нековалентно связанных пептидов в результате экспозиции при низком pH и/или с аденозинтрофосфатом или другими способами, известными в данной области.
В различных аспектах источником HSP и α2М предпочтительно являются эукариоты, более предпочтительно млекопитающие и наиболее предпочтительно человек. Соответственно, препарат HSP, используемый в способах изобретения, включает эукариотические HSP, HSP млекопитающих и HSP человека. Препарат α2М включает эукариотический α2М, α2М млекопитающих и α2М человека. Эукариотический источник, из которого получают препарат HSP или препарат α2М, и субъект, получающий препарат HSP или препарат α2М, соответственно, предпочтительно принадлежат к одному и тому же виду.
В одном аспекте специфическая иммуногенность препарата HSP происходит от пептида, образующего комплекс с белком теплового шока. Соответственно, в различных аспектах препарат HSP содержит комплексы белок теплового шока-пептид, в которых белки теплового шока образуют комплексы с пептидами, полученными из специального антигенного источника. В предпочтительном аспекте белковый препарат HSP содержит комплексы белок теплового шока-пептид, которые являются аутогенными. В другом предпочтительном аспекте препарат HSP содержит белки теплового шока, образующие комплексы с антигенными пептидами злокачественных клеток, из которых их получают. В специальных аспектах антиген является опухолеспецифическим антигеном (то есть экспрессируется только в опухолевых клетках). В других специальных аспектах антиген представляет собой ассоциированный с опухолью антиген (то есть относительно сверхэкспрессируется в опухолевых клетках). В еще одном предпочтительном аспекте препарат HSP содержит белки теплового шока, образующие комплексы с антигенными пептидами инфицированных клеток, из которых их получают.
В другом аспекте специфическая иммуногенность препарата α2М происходит от пептида, образующего комплекс с α2М. Таким образом, в различных аспектах препарат α2М содержит комплексы α2М-пептид, в которых α2М образует комплексы с пептидами, полученными из определенного антигенного источника. В предпочтительном аспекте белковый препарат α2М содержит комплексы α2М-пептид, которые являются аутогенными. В другом предпочтительном аспекте препарат α2М содержит α2М, образующий комплексы с антигенными пептидами злокачественных клеток, из которых их получают. В других специальных аспектах антиген представляет собой ассоциированный с опухолью антиген (то есть относительно сверхэкспрессированный в опухолевых клетках). В еще одном предпочтительном аспекте препарат α2М содержит α2М, образующий комплексы с антигенными пептидами инфицированных клеток, из которых их получают.
В различных специальных аспектах описанные выше способы включают введение препарата HSP или препарата α2М субъекту, которого подвергают лечебному воздействию, причем проводимое отдельно лечебное воздействие не является клинически достаточным, чтобы лечить субъекта так, чтобы субъект не нуждался в дополнительной эффективной терапии, например, субъект является нечувствительным к лечебному воздействию без введения препарата HSP или препарата α2М. Такие аспекты охватывают способы, предусматривающие введение препарата HSP или препарата α2М субъекту, получающему лечебное воздействие, причем указанный субъект, который оказывается восприимчивым к терапии, еще страдает от побочных эффектов, рецидива и развития резистентности и так далее. Такой субъект может быть нечувствительным или резистентным к лечению только лечебным воздействием. В аспектах предусматривают, что способы изобретения, включающие введение препарата HSP субъекту, резистентному к одному лечебному воздействию, могут улучшить терапевтическую эффективность лечебного воздействия, если вводят, как рекомендуют по способам изобретения. Способы изобретения, предусматривающие введение препарата α2М субъекту, резистентному к лечебному воздействию, проводимому отдельно, также могут улучшить терапевтическую эффективность лечебного воздействия, если вводят, как рекомендуют по способам изобретения.
В специальном аспекте препарат HSP вводят субъекту, которому проводят лечебное воздействие для лечения злокачественных опухолей, причем субъект может быть нечувствительным к лечению только лечебным воздействием, то есть, по крайней мере, некоторая значительная часть злокачественных клеток не погибает или их клеточное деление не останавливается. Определение эффективности лечебного воздействия можно исследовать in vivo или in vitro, используя способы, известные в данной области. Признанное в данной области значение резистентности хорошо известно в контексте злокачественных опухолей. В одном аспекте злокачественная опухоль является резистентной или нечувствительной, когда количество злокачественных клеток не снижается значительно или увеличивается. В предпочтительном аспекте, препарат HSP, который проявляет антигенность типа рака, вводят субъекту, нечувствительному к проведению одного лечебного воздействия, при этом введение препарата HSP повышает эффективность лечебного воздействия. В числе субъектов, которых лечат, имеются субъекты, которым проводят химиотерапию или лучевую терапию.
В особом аспекте препарат α2М вводят субъекту, получающему лечебное воздействие для лечения злокачественных опухолей, при этом субъект может быть нечувствительным или резистентным к лечению одним лечебным воздействием, то есть, по крайней мере, некоторая значительная часть злокачественных клеток не погибает или их деление не останавливается. Определение эффективности лечебного воздействия можно исследовать in vivo или in vitro, используя способы, известные в данной области. Признанное в данной области значение резистентности хорошо известно в контексте злокачественных опухолей. В одном аспекте злокачественная опухоль является резистентной или нечувствительной, когда количество злокачественных клеток не снижается значительно или увеличивается. В предпочтительном аспекте препарат α2М, который проявляет антигенность типа рака, вводят субъекту, нечувствительному к проведению одного лечебного воздействия, причем введение препарата α2М повышает эффективность лечебного воздействия. В числе субъектов, которых лечат, имеются субъекты, которым проводят химиотерапию или лучевую терапию.
В специальном аспекте препарат HSP вводят субъекту, получающему лечебное воздействие для лечения злокачественных опухолей, при этом субъект может испытывать нежелательные или побочные эффекты на лечение одним лечебным воздействием, например, проводимое отдельно лечебное воздействие может быть токсичным или вредным при его эффективной дозе. Благодаря изобретению препарат HSP может улучшить терапевтический эффект лечебного воздействия так, что дозировку или частоту введения лечебного воздействия можно снизить, когда вводят вместе с препаратом HSP. В предпочтительном аспекте препарат HSP, который проявляет антигенность типа рака, вводят субъекту, чтобы снизить или устранить нежелательные или побочные эффекты одного лечебного воздействия, при этом введение препарата HSP предусматривает более низкие и/или менее часто вводимые дозы лечебного воздействия. В числе субъектов, которых лечат, имеются субъекты, которым проводят химиотерапию или лучевую терапию.
В особом аспекте препарат α2М вводят субъекту, получающему лечебное воздействие для лечения злокачественных опухолей, при котором субъект может испытывать нежелательный или побочный эффект лечения одним лечебным воздействием, например, проводимое одно лечебное воздействие может быть токсичным или вредным при его эффективной дозе. Благодаря изобретению препарат α2М может улучшить терапевтическое действие лечебного воздействия так, что дозировка или частота проведения лечебного воздействия может быть снижена, когда вводят вместе с препаратом α2М. В предпочтительном аспекте препарат α2М, который проявляет антигенность типа рака, вводят субъекту, чтобы снизить или устранить нежелательные или побочные эффекты одного лечебного воздействия, при этом введение препарата α2М позволяет применять более низкие и/или менее часто вводимые дозы лечебного воздействия. В числе субъектов, которых лечат, имеются субъекты, которым проводят химиотерапию или лучевую терапию.
В специальном аспекте препарат HSP вводят в субоптимальном количестве, например, в количестве, которое не оказывает очевидного определяемого терапевтического эффекта, когда вводят в отсутствие лечебного воздействия, которое оценивают по способам, известным в данной области. В таких способах введение такого субоптимального количества препарата HSP субъекту, которому проводят лечебное воздействие, приводит к общему улучшению эффективности лечения. В другом особом аспекте препарат α2М вводят в субоптимальном количестве. В таких способах введение такого субоптимального количества препарата α2М субъекту, которому проводят лечебное воздействие, приводит к общему улучшению в эффективности лечения.
В предпочтительном аспекте препарат HSP вводят в количестве, которое не приводит к регрессии опухоли или злокачественной ремиссии, или в количестве, которое не снижает значительно злокачественные клетки или увеличивает, когда указанный препарат HSP вводят в отсутствие лечебного воздействия. Предпочтительно препарат HSP содержит комплексы HSP-пептид, проявляющие антигенность типа рака, который лечат. В предпочтительном аспекте субоптимальное количество препарата HSP вводят субъекту, которому проводят лечебное воздействие, при этом общая эффективность лечения повышается. В другом предпочтительном аспекте препарат α2М вводят в количестве, которое не приводит к регрессии опухоли или злокачественной ремиссии, или в количестве, которое значительно не снижает злокачественные клетки или увеличивает их, когда указанный препарат α2М вводят в отсутствие лечебного воздействия. Предпочтительно препарат α2М содержит комплексы α2М-пептид, проявляющие антигенность типа рака, который лечат. В предпочтительном аспекте субоптимальное количество препарата α2М вводят субъекту, которому проводят лечебное воздействие, при этом повышают общую эффективность лечения. В числе субъектов, которых лечат препаратом HSP или препаратом α2М, имеются субъекты, которым проводят химиотерапию или лучевую терапию. Субоптимальное количество может быть определено с помощью соответствующих исследований на животных. Такое субоптимальное количество для человека можно установить экстраполяцией из экспериментов на животных.
Препарат HSP или препарат α2М можно вводить до, одновременно с или после проведения невакцинного лечебного воздействия. В одном аспекте введение препарата HSP и лечебное воздействие проводят точно в одно время. В другом аспекте введение препарата α2М и лечебное воздействие осуществляют точно в одно и то же время. В следующем аспекте или введение препарата HSP, или препарата α2М и лечебное воздействие проводят один за другим и в пределах интервала времени с тем, чтобы препарат HSP и лечебное воздействие могли действовать вместе, чтобы обеспечить более сильное действие, чем если бы их проводили отдельно, или с тем, чтобы препарат α2М и лечебное воздействие могли действовать вместе с тем, чтобы обеспечить более сильный эффект, чем если бы их проводили отдельно. В другом аспекте введение препарата HSP и лечебное воздействие осуществляют достаточно близко по времени с тем, чтобы обеспечить требуемый терапевтический эффект. В следующем аспекте введение препарата α2М и лечебное воздействие осуществляют достаточно близко по времени с тем, чтобы обеспечить требуемый терапевтический эффект. Введение препарата HSP или α2М и лечебное воздействие можно проводить одновременно или отдельно в любой подходящей форме или любым соответствующим способом. В одном аспекте препарат HSP и лечебное воздействие проводят с помощью различных способов введения. В альтернативном аспекте каждый вводят одним и тем же способом введения. Препарат HSP можно вводить в тот же самый или разные участки, например в руку или ногу. В другом аспекте препарат α2М и лечебное воздействие проводят с помощью различных способов введения. Альтернативно каждый может быть введен одним и тем же способом. Кроме того, каждый можно вводить в тот же самый участок или разные участки.
В различных аспектах, таких как описано выше, введение препарата HSP и лечебное воздействие проводят с интервалом менее 1 часа, с интервалом приблизительно 1 час, с интервалом от 1 часа до 2 часов, 2-3 часа, 3-4 часа, 4-5 часов, с интервалом от 5 часов до 6 часов, 6-7 часов, 7-8 часов, 8-9 часов, 9-10 часов, 10-11 часов, 11-12 часов, с интервалом не более 24 часов или с интервалом не более 48 часов, или не более 1 недели или 2 недель, или с интервалом 1 месяц или 3 месяца. В других аспектах введение препарата HSP и лечебное воздействие проводят с интервалом от 2 до 4 дней, 4-6 дней, с интервалом 1 неделя, от 1 до 2 недель, от 2 до 4 недель, с интервалом один месяц, от 1 до 2 месяцев или с интервалом 2 или более месяцев. В предпочтительных аспектах введение препарата HSP и лечебное воздействие проводят во временных рамках, когда оба еще активны. Специалисты в данной области смогут установить такие временные рамки определением периода полувыведения каждого введенного компонента. В отдельном или в предшествующих аспектах введение препарата HSP и лечебное воздействие проводят с интервалом менее 2 недель, один месяц, шесть месяцев, 1 год или 5 лет. Предпочтительно препарат HSP вводят до лечебного воздействия. В других аспектах введение препарата α2М и лечебное воздействие проводят с временными интервалами и во временных рамках, описанных в каждом из приведенных выше аспектах. Предпочтительно препарат α2М вводят до лечебного воздействия. Предпочтительно в каждом из вышеприведенных аспектов лечебное воздействие представляет собой сочетание химиотерапии и лечения цитокином.
В одном аспекте, лечебное воздействие проводят ежедневно, и препарат HSP или препарат α2М вводят один раз в неделю в течение первых 4 недель и затем один раз через неделю. В одном аспекте, лечебное воздействие проводят ежедневно, и препарат HSP или препарат α2М вводят один раз в неделю в течение первых 8 недель и затем один раз через неделю.
В одном аспекте два или более компонентов вводят во время одного и того же визита пациента. В еще одном аспекте препарат α2М вводят до проведения лечебного воздействия. В альтернативном аспекте препарат α2М вводят после введения лечебного воздействия. В одном аспекте препарат α2М вводят до проведения лечебного воздействия. В альтернативном аспекте препарат HSP вводят после проведения лечебного воздействия.
В некоторых аспектах введение препарата HSP или препарата α2М и невакцинное лечебное воздействие проводят пациенту циклически. Циклическая терапия включает введение препарата HSP в течение периода времени, за которым следует проведение лечебного воздействия в течение периода времени, и повторение данного последовательного введения. Альтернативно циклическая терапия может включать введение препарата α2М в течение периода времени, за которым следует проведение лечебного воздействия в течение периода времени, и повторение данного последовательного введения. Циклическая терапия может снизить развитие резистентности к одной или более терапиям, устранить или уменьшить побочные эффекты одной из терапий, и/или улучшить эффективность лечения. В таких аспектах изобретение рассматривает переменное введение препарата HSP с последующим проведением лечебного воздействия спустя 4-6 дней, предпочтительно спустя 2-4 дня, более предпочтительно спустя 1-2 дня, причем такой цикл можно повторять столько раз, сколько требуется. Изобретение также рассматривает переменное введение препарата α2М с последующим проведением лечебного воздействия спустя 4-6 дней, предпочтительно спустя 2-4 дня, более предпочтительно спустя 1-2 дня, причем такой цикл можно повторять столько раз, сколько требуется.
В некоторых аспектах введение препарата HSP и лечебное воздействие проводят переменно с циклом менее 3 недель, один раз в две недели, один раз в 10 дней или один раз в неделю. В других аспектах введение препарата α2М и лечебное воздействие альтернативно проводят с циклом менее 3 недель, один раз в две недели, один раз в 10 дней или один раз в неделю. В специальном аспекте изобретения один цикл может включать проведение химиотерапии с помощью вливания в течение 90 минут каждого цикла, 1 часа каждого цикла или 45 минут каждого цикла. Каждый цикл может включать, по крайней мере, 1 неделю отдыха, по крайней мере, 2 недели отдыха, по крайней мере, 3 недели отдыха. В аспекте количество проводимых циклов составляет от 1 до 12 циклов, более типично 2-10 циклов и наиболее типично 2-8 циклов.
В предпочтительном аспекте препарат HSP, проявляющий антигенность опухолеспецифического или ассоциированного с опухолью антигена типа рака, вводят субъекту в количестве, не эффективном для лечения указанного рака в течение приблизительно от 2 недель до 1 месяца до проведения комбинации химиотерапии с лечением цитокином, при этом эффективность оказывается выше, чем эффективность препарата HSP или комбинации химиотерапии с лечением цитокином, проводимых отдельно. Предпочтительно субъектом является человек. В предпочтительном аспекте субъект оказывается нечувствительным к комбинации химиотерапии с цитокиновой терапией до введения препарата HSP. В другом предпочтительном аспекте химиотерапией является циклофосфамид, цитокином является IL-12, и препарат HSP содержит комплексы gp96-пептид, полученные из злокачественной ткани субъекта.
В особо предпочтительном аспекте препарат α2М, проявляющий антигенность опухолеспецифического антигена или ассоциированного с опухолью антигена типа рака, вводят субъекту в количестве, не эффективном для лечения указанного рака приблизительно от 2 недель до 1 месяца до проведения комбинации химиотерапии и терапии цитокином, при этом эффективность оказывается выше, чем эффективность препарата α2М или комбинации химиотерапии с цитокиновой терапией, проводимых отдельно. Предпочтительно субъектом является человек. В предпочтительном аспекте субъект оказывается нечувствительным к комбинации химиотерапии и терапии цитокином до введения препарата α2М. В другом предпочтительном аспекте химиотерапией является циклофосфамид, цитокином является IL-12, и препарат α2М содержит комплексы α2М-пептид, полученные из злокачественной ткани субъекта.
В специальных аспектах описанные выше способы включают введение Gleevec™ (иматиниба мезилат) для лечения злокачественных опухолей. В предпочтительном аспекте злокачественная опухоль представляет собой CML, химиотерапевтическим средством является Gleevec™ (иматиниба мезилат), и препарат HSP содержит комплексы hsp70-пептид, полученные из злокачественной ткани субъекта, которого лечат.
Также изобретение касается способов лечения и доставки фармацевтических композиций и составов, предусматривающих применение, по крайней мере, одного невакцинного лечебного воздействия и препарата HSP или препарата α2М, и наборот, содержащих такие фармацевтические композиции.
5.1. ПРЕПАРАТЫ БЕЛКОВ ТЕПЛОВОГО ШОКА
Три главных семейства HSP были идентифицированы на основании молекулярной массы. Семейства названы hsp60, hsp70 и hsp90, где числа отражают приблизительную молекулярную массу стрессовых белков в килодальтонах. Впоследствии было установлено, что большинство представителей указанных семейств индуцируются в ответ на другие стрессовые стимулы, предусматривающие, но не ограничиваясь перечисленным, недостаточность питания, нарушение метаболизма, кислородные радикалы и инфекцию внутриклеточными патогенными микроорганизмами (см. Welch, May 1993, Scientific American 56-64; Young, 1990, Annu. Rev. Immunol. 8: 401-420; Craig, 1993, Science 260: 1902-1903; Gething, et al., 1992, Nature 355: 33-45; и Lindquist, et al., 1988, Annu. Rev. Genetics 22: 631-677). Полагают, что целый ряд белков, которые вовлечены в шаперонные функции, являются резидентами полости эндоплазматического ретикулума (ER) и включают, но не ограничиваясь ими, например, протеин-дисульфидизомеразу (PDI; Gething et al., 1992, Nature 355: 33-45), калретикулин (Herbert et al., 1997, J. Cell Biol. 139: 613-623), Grp94 или ERp99 (Sorter & Pelham, 1987, J. Mol. Biol. 194: (2) 341-4), которые связаны с hsp90, и Grp78 или BiP, которые связаны с hsp70 (Munro et al., 1986, Cell 46: 291-300; Haas & Welb, 1983, Nature 306: 387-389). Полагают, что HSP, принадлежащие ко всем из приведенных трех семейств, включая фрагменты таких HSP, можно использовать при практическом применении данного изобретения. Также отмечено, что HSP включают конститутивно экспрессируемые консервативные клеточные гомологи белков, индуцированных стрессом.
HSP также взаимозаменяемо называют в описании стрессовыми белками, и они могут быть выбраны из числа любых клеточных белков, которые удовлетворяют следующим критериям. Указанный белок является белком, чья внутриклеточная концентрация увеличивается, когда клетку подвергают действию стрессовых стимулов, указанный белок способен связывать другие белки или пептиды, способен высвобождать связанные белки или пептиды в присутствии аденозинтрифосфата (АТФ) или при низком pH, и указанный белок является белком, демонстрирующим, по крайней мере, 35% гомологию с любым клеточным белком, характеризующимся любыми из описанных выше свойств.
Белки теплового шока относятся к числу наиболее высококонсервативных белков, существующих в природе. Например, DnaK, hsp70 из E. coli имеют приблизительно 50% идентичность аминокислотной последовательности с белками hsp70 из ссадин (Bardwell, et al., 1984, Proc. Natl. Acad. Sci. 81: 848-852). Аналогично семейства hsp60 и hsp90 также проявляют высокие уровни консерватизма внутри семейств (Hickey, et al., 1989, Vol.Cell. Biol. 9: 2615-2626; Jindal, 1989, Vol. Cell. Biol. 9: 2279-2283). Кроме того, обнаружено, что семейства hsp60, hsp70 и hsp90 состоят из белков, которые являются родственными стрессовым белкам по последовательности, например, обладающим более 35% аминокислотной идентичностью, но уровни экспрессии которых не изменяются при стрессе. Поэтому предполагают, что стрессовые белки/HSP включают другие белки, мутеины, аналоги и их варианты, характеризующиеся, по крайней мере, 35-55%, предпочтительно 55-75% и наиболее предпочтительно 75-85% аминокислотной идентичностью с представителями трех семейств, уровни экспрессии которых в клетке повышаются в ответ на стрессовый стимул. Очистка стрессовых белков, принадлежащих к указанным трем семействам, описана ниже.
Кроме того, обнаружено, что HSP проявляют иммунологические и антигенные свойства. В настоящее время понимают, что HSP играют важную роль в иммунной регуляции. Например, предшествующими экспериментами продемонстрировано, что HSP стимулируют сильные и длительно продолжающиеся специфические иммунные ответы против антигенных пептидов, которые ковалентно или нековалентно присоединены к HSP. При использовании специфического пептида генерированный иммунный ответ оказывается “специфическим” для такого пептида или таргетированным на такой пептид.
Когда комплексы HSP-пептид используют вместе с проведением невакцинного лечебного воздействия, предпочтительно, чтобы пептиды являлись антигенными или относящимися к состоянию. В особенно предпочтительных аспектах предполагают, что терапевтический эффект лечебного воздействия, проводимого субъекту с определенным типом рака, улучшается при введении комплекса HSP-пептид, в котором пептид проявляет антигенность антигена такого типа рака.
В данном изобретении препарат HSP может включать несвязанный hsp70, hsp90, gp96, калрекулин, hsp110 или grp170 или их нековалентные или ковалентные комплексы, образованные с пептидом.
5.2 ПОЛУЧЕНИЕ БЕЛКОВ ТЕПЛОВОГО ШОКА И α2М
В данном изобретении используют очищенные несвязанные HSP, HSP ковалентно или нековалентно связанные со специфическими пептидами или неспецифическими пептидами (в описании собирательно называемые “комплексы HSP-пептид”) и их комбинации. Очистка HSP, в комплексных формах или некомплексных формах, описана в следующих подразделах. Кроме того, специалисты в данной области могут синтезировать HSP методом рекомбинантной экспрессии или пептидного синтеза, которые также описаны ниже.
Также в данном изобретении используют очищенные несвязанный α2М, α2М, ковалентно или нековалентно связанный со специфическими пептидами или неспецифическими пептидами (в описании совокупно называемые “комплексы α2М-пептид”) и их комбинации. Очистка α2М в комплексных формах или некомплексных формах описана в следующих подразделах. Кроме того, специалисты в данной области могут синтезировать α2М методом рекомбинантной экспрессии или пептидного синтеза, которые также описаны ниже.
5.2.1 Получение и очистка Hsp70 или комплексов Hsp70-пептид
Очистка нековалентно связанных, продуцируемых клеткой комплексов hsp70-пептид была описана ранее, см., например, Udono et al., 1993, J. Exp. Med. 178: 1391-1396. Представленный в качестве примера способ, который может быть использован, но без ограничения, заключается в следующем.
Сначала клетки человека или млекопитающего суспендируют в 3 объемах буфера для лизиса 1Х, состоящего из 5 мМ натрий фосфатного буфера (pH 7), 150 мМ NaCl, 2 мМ CaCl2, 2 мМ MgCl2 и 1 мМ фенилметилсульфонилфторида (PMSF). Затем осадок обрабатывают ультразвуком на льду до тех пор, пока >99% клеток не будет подвергнуто лизису, что устанавливают при микроскопическом исследовании. Как альтернатива разрушению ультразвуком, клетки можно лизировать механическим фрагментированием и при таком подходе клетки обычно повторно суспендируют в 30 мМ бикарбонате натрия (pH 7,5), 1 мМ PMSF, инкубируют на льду в течение 20 минут и затем гомогенизируют в гомогенизаторе Dounce до тех пор, пока >95% клеток не будет подвергнуто лизису.
Затем лизат центрифугируют при 1000 g в течение 10 минут, чтобы удалить неразрушенные клетки, ядра и другой клеточный дебрис. Полученный супернатант повторно центрифугируют при 100000 g в течение 90 минут, супернатант собирают и затем смешивают с Con A Sepharose™, уравновешенной забуференным фосфатом физиологическим раствором (PBS), содержащим 2 мМ Ca2+ и 2 мМ Mg2+. Когда клетки лизируют механической фрагментацией, супернатант разводят равным объемом буфера для лизиса 2Х до смешивания с Con A Sepharose™. Затем супернатант оставляют для связывания с Con A Sepharose™ в течение 2-3 часов при 4°С. Материал, который не удалось связать, собирают и диализуют в течение 36 часов (три раза, 100 объемов каждый раз) против 10 мМ трис-ацетата (pH 7,5), 0,1 мМ EDTA, 10 мМ NaCl, 1 мМ PMSF. Затем диализат центрифугируют при 17000 оборотов в минуту (ротор Sorvall SS34) в течение 20 минут. Затем полученный супернатант собирают и наносят на ионообменную хроматографическую колонку Mono Q FPLC™ (Pharmacia), уравновешенную 20 мМ трис-ацетатом (рН 7,5), 20 мМ NaCl, 0,1 мМ EDTA и 15 мМ 2-меркаптоэтанолом. Затем колонку обрабатывают градиентом от 20 мМ до 500 мМ NaCl и затем элюированные фракции фракционируют с помощью гелевого электрофореза в полиакриламине в присутствии додецилсульфата натрия (SDS-PAGE) и характеризуют с помощью иммуноблоттинга, используя подходящие анти-hsp70-антитела (например, из клона N27F3-4 от StressGen).
Фракции, проявляющие сильную иммунореактивность с анти-hsp70-антителами, объединяют и комплексы hsp70-пептид осаждают сульфатом аммония; точнее фракцией 50-70% насыщения сульфатом аммония. Полученный осадок затем собирают центрифугированием при 17000 оборотов в минуту (ротор Sorvall SS34) и промывают 70% сульфатом аммония. Промытый осадок затем растворяют и любой остаточный сульфат аммония удаляют гель-фильтрацией на колонке с сефадексомR G-25 (Pharmacia). Если необходимо, полученный таким образом препарат hsp70 можно повторно очистить на ионообменной хроматографической колонке Mono Q FPLC™ (Pharmacia), как описано выше.
Комплекс hsp70-пептид можно очистить до явной гомогенности, используя описанный способ. Обычно 1 мг комплекса hsp70-пептид можно выделить из 1 г клеток/ткани.
Улучшенный способ выделения комплексов hsp70-пептид включает контактирование клеточных белков с АДФ или негидролизуемым аналогом АТФ, прикрепленным к твердому субстрату, с тем чтобы hsp70 в лизате мог связываться с АДФ или негидролизуемым аналогом АТФ, и элюирование связанного hsp70. В предпочтительном способе используют колоночную хроматографию с АДФ, прикрепленным к твердому субстрату (например, АДФ-агароза). Полученные препараты hsp70 характеризуются более высокой чистотой и отсутствием загрязняющих пептидов. Выходы комплекса hsp70 также оказываются значительно увеличенными, приблизительно в 10 раз. Альтернативно хроматография с негидролизуемыми аналогами АТФ, вместо АДФ, можно использовать для очистки комплексов hsp70-пептид. В качестве примера, но без ограничения, очистку комплексов hsp70-пептид хроматографией на АДФ-агарозе можно проводить следующим образом.
Клетки саркомы Meth A (500 миллион клеток) гомогенизируют в гипотоническом буфере и лизат центрифугируют при 100000 g в течение 90 минут при 4°С. Супернатант наносят на колонку с АДФ-агарозой. Колонку промывают буфером и элюируют 5 колоночными объемами 3 мМ АДФ. Комплексы hsp70-пептид элюируются во фракциях с 2 по 10 из общих 15 фракций, которые элюируются. Элюированные фракции исследуют с помощью SDS-PAGE. Комплексы hsp70-пептид можно очищать до явной гомогенности, используя описанный способ.
Выделение HSP из комплекса hsp70-пептид можно проводить в присутствии АТФ или при низком pH. Указанные оба способа можно использовать, чтобы элюировать пептид из комплекса hsp70-пептид. Первый подход включает инкубацию препарата комплекса hsp70-пептид в присутствии АТФ. Другой подход включает инкубацию препарата комплекса hsp70-пептид в буфере с низким pH. Описанные способы и любые другие способы, известные в данной области, можно применять, чтобы выделить HSP и пептид из комплекса hsp-пептид.
5.2.2 Получение и очистка Hsp90 или нековалентных, продуцируемых клеткой комплексов Hsp90-пептид
Представленный в качестве примера способ, который можно использовать, но без ограничения, заключается в следующем.
Сначала клетки человека или млекопитающего суспендируют в 3 объемах буфера для лизиса 1Х, состоящего из 5 мМ натрий фосфатного буфера (pH 7), 150 мМ NaCl, 2 мМ CaCl2, 2 мМ MgCl2 и 1 мМ фенилметилсульфонилфторида (PMSF). Затем осадок обрабатывают ультразвуком на льду до тех пор, пока >99% клеток не будет подвергнуто лизису, что устанавливают при микроскопическом исследовании. Как альтернатива разрушению ультразвуком, клетки можно лизировать механическим фрагментированием и при таком подходе клетки обычно повторно суспендируют в 30 мМ бикарбонате натрия (pH 7,5), 1 мМ PMSF, инкубируют на льду в течение 20 минут и затем гомогенизируют в гомогенизаторе Dounce до тех пор, пока >95% клеток не будет подвергнуто лизису.
Затем лизат центрифугируют при 1000 g в течение 10 минут, чтобы удалить неразрушенные клетки, ядра и другой клеточный дебрис. Полученный супернатант повторно центрифугируют при 100000 g в течение 90 минут, супернатант собирают и затем смешивают с Con A Sepharose™, уравновешенной PBS, содержащим 2 мМ Ca2+ и 2 мМ Mg2+. Когда клетки лизируют механической фрагментацией, супернатант разводят равным объемом буфера для лизиса 2Х до смешивания с Con A Sepharose™. Затем супернатант оставляют для связывания с Con A Sepharose™ в течение 2-3 часов при 4°С. Материал, который не удалось связать, собирают и диализуют в течение 36 часов (три раза, 100 объемов каждый раз) против 10 мМ трис-ацетата (pH 7,5), 0,1 мМ EDTA, 10 мМ NaCl, 1 мМ PMSF. Затем диализат центрифугируют при 17000 оборотов в минуту (ротор Sorvall SS34) в течение 20 минут. Затем полученный супернатант собирают и наносят на ионообменную хроматографическую колонку Mono Q FPLC™ (Pharmacia), уравновешенную буфером для лизиса. Затем белки элюируют градиентом NaCl от 200 мМ до 600 мМ.
Элюированные фракции фракционируют с помощью SDS-PAGE и фракции, содержащие комплексы hsp90-пептид, идентифицируют с помощью иммуноблоттинга, используя подходящие анти-hsp90-антитела, такие как 3G3 (Affinity Bioreagents). Комплексы hsp90-пептид можно очищать до явной гомогенности, используя описанный способ. Обычно 150-200 мкг комплекса hsp90-пептид можно выделить из 1 г клеток/ткани.
Выделение HSP их комплекса hsp90-пептид можно проводить в присутствии АТФ или при низком рН. Указанные оба способа можно использовать, чтобы элюировать пептид из комплекса hsp90-пептид. Первый подход включает инкубацию препарата комплекса hsp90-пептид в присутствии АТФ. Другой подход включает инкубацию препарата комплекса hsp90-пептид в буфере с низким рН. Описанные способы и любые другие способы, известные в данной области, можно применять, чтобы выделить HSP и пептид из комплекса hsp-пептид.
5.2.3 Получение и очистка Gp96 или нековалентных, продуцируемых клеткой комплексов Gp96-пептид
Представленный в качестве примера способ, который можно использовать, но без ограничения, заключается в следующем.
Осадок клеток человека или млекопитающего повторно суспендируют в 3 объемах буфера, состоящего из 30 мМ натрий-бикарбонатного буфера (pH 7,5) и 1 мМ PMSF, и клетки оставляют для набухания на льду на 20 минут. Затем клеточный осадок гомогенизируют в гомогенизаторе Dounce (соответствующее разрешение гомогенизатора изменяют в соответствии с каждым типом клеток) на льду до тех пор, пока >95% клеток не будет подвергнуто лизису.
Лизат центрифугируют при 1000 g в течение 10 минут, чтобы удалить неразрушенные клетки, ядра и другой дебрис. Супернатант с описанной стадии центрифугирования затем повторно центрифугируют при 100000 g в течение 90 минут. Комплекс gp96-пептид можно выделить или из осадка, полученного при 100000 g, или из супернатанта.
Когда выделяют из супернатанта, супернатант разводят равным объемом буфера для лизиса 2Х и супернатант смешивают в течение 2-3 часов при 4°С с Con A Sepharose™, уравновешенной PBS, содержащим 2 мМ Ca2+ и 2 мМ Mg2+. Затем суспензию заполняют в колонку и промывают буфером для лизиса 1Х до тех пор, пока OD280 не упадет до базового значения. Затем колонку промывают 1/3 колоночного объема 10% α-метилманнозидом (α-ММ), растворенным в PBS, содержащим 2 мМ Ca2+ и 2 мМ Mg2+, колонку герметически закрывают парафином и инкубируют при 37°С в течение 15 минут. Затем колонку охлаждают до комнатной температуры и парафин удаляют со дна колонки. Пять колоночных объемов буфера α-ММ наносят на колонку и элюат анализируют с помощью SDS-PAGE. Обычно полученный материал имеет приблизительно 60-95% чистоты, однако чистота зависит от типа клеток и используемого соотношения ткани к буферу для лизиса. Затем образец наносят на ионообменную хроматографическую колонку Mono Q FPLC™ (Pharmacia), уравновешенную буфером, содержащим 5 мМ фосфата натрия (pH 7). Затем белки элюируют с колонки градиентом 0-1 М NaCl и фракцию gp96 элюируют между 400 мМ и 550 мМ NaCl.
Однако способ можно модифицировать с помощью двух дополнительных стадий, применяемых или отдельно, или в комбинации, чтобы последовательно получить явно гомогенные комплексы gp96-пептид. Одна возможная стадия включает осаждение сульфатом аммония до стадии очистки на Con A и другая возможная стадия включает очистку на DEAE-Sepharose™ после стадии очистки на Con A, но до стадии на Mono Q FPLC™.
На первой возможной стадии, описанной в качестве примера следующим образом, супернатант, полученный на стадии центрифугирования при 100000 g, приводят к конечной концентрации 50% насыщения сульфатом аммония добавлением сульфата аммония. Сульфат аммония добавляют медленно при осторожном перемешивании раствора в стакане, помещенном на лоток с охлажденной льдом водой. Раствор перемешивают приблизительно от 1/2 до 12 часов при 4°С и полученный раствор центрифугируют при 6000 оборотов в минуту (ротор Sorvall SS34). Полученный на описанной стадии раствор удаляют, приводят к 70% насыщения сульфатом аммония добавлением раствора сульфата аммония и центрифугируют при 6000 оборотов в минуту (ротор Sorvall SS34). Полученный на описанной стадии осадок собирают и суспендируют в PBS, содержащем 70% сульфата аммония, чтобы промыть осадок. Полученную смесь центрифугируют при 6000 оборотов в минуту (ротор Sorvall SS34) и осадок растворяют в PBS, содержащем 2 мМ Ca2+ и Mg2+. Нерастворенный материал удаляют кратким центрифугированием при 15000 оборотов в минуту (ротор Sorvall SS34). Затем раствор смешивают с Con A Sepharose™ и способ осуществляют как раньше.
На второй возможной стадии, описанной в качестве примера как следующее, содержащие gp96 фракции, элюированные из колонки Con A, объединяют и буфер заменяют 5 мМ натрий-фосфатным буфером (pH 7), 300 мМ NaCl диализом или, предпочтительно, заменой буфера на колонке с сефадексом G-25. После замены буфера раствор смешивают с DEAE-Sepharose™, предварительно уравновешенной 5 мМ натрий-фосфатным буфером (pH 7), 300 мМ NaCl. Белковый раствор и гранулы осторожно смешивают в течение 1 часа и вливают в колонку. Затем колонку промывают 5 мМ натрий-фосфатным буфером (pH 7), 300 мМ NaCl до тех пор, пока оптическая плотность при 280 нм не упадет до базового значения. Затем связанный белок элюируют из колонки пятью объемами 5 мМ натрий-фосфатного буфера (pH 7), 700 мМ NaCl. Содержащие белок фракции объединяют и разводят 5 мМ натрий-фосфатным буфером (pH 7), чтобы снизить концентрацию соли до 175 мМ. Затем полученный материал наносят на ионообменную хроматографическую колонку Mono Q FPLC™ (Pharmacia), уравновешенную 5 мМ натрий-фосфатным буфером (рН 7), и белок, который связывается на ионообменной хроматографической колонке Mono Q FPLC™ (Pharmacia), элюируют, как описано выше.
Однако следует отдать должное, специалисты в данной области стандартным экспериментированием могут оценить пользу от введения второй возможной стадии в протокол очистки. Кроме того, следует заметить, что полезный эффект от добавления каждой из возможных стадий зависит от источника исходного материала.
Когда фракцию gp96 выделяют из осадка, полученного при 100000 g, осадок суспендируют в 5 объемах PBS, содержащего или 1% дезоксихолат натрия, или 1% окстилглюкопиранозид (но без Mg2+ и Ca2+), и инкубируют на льду в течение 1 часа. Суспензию центрифугируют при 20000 g в течение 30 минут и полученный супернатант диализуют против нескольких смен PBS (также без Mg2+ и Ca2+), чтобы удалить детергент. Диализат центрифугируют при 100000 g в течение 90 минут, супернатант собирают и в супернатант добавляют кальций и магний, чтобы получить конечные концентрации 2 мМ, соответственно. Затем образец очищают по или немодифицированному или модифицированному способу выделения комплекса gp96-пептид из супернатанта, полученного при 100000 g, см. выше.
Комплексы gp96-пептид можно очищать до явной гомогенности, используя описанный способ. Приблизительно 10-20 мкг gp96 можно выделить из 1 г клеток/ткани.
Выделение HSP из комплекса gp96-пептид можно проводить в присутствии АТФ или при низком pH. Описанные два способа можно использовать, чтобы элюировать пептид из комплекса gp96-пептид. Первый подход включает инкубацию препарата комплекса gp96-пептид в присутствии АТФ. Другой подход включает инкубацию препарата комплекса gp96-пептид в буфере с низким значением рН. Указанные способы и другие способы, известные в данной области, можно применять, чтобы выделить HSP и пептид из комплекса hsp-пептид.
5.2.4 Получение и очистка нековалентных, продуцируемых клеткой комплексов Hsp110-пептид
Представленный в качестве примера способ, описанный Wang et al., 2001, J. Immunol. 166(1): 490-7, который можно использовать, но без ограничения, заключается в следующем.
Осадок (40-60 мл) клеток или ткани, например ткани опухолевых клеток, гомогенизируют в 5 объемах гипотонического буфера (30 мМ бикарбонат натрия, pH 7,2 и ингибиторы протеаз) в гомогенизаторе Dounce. Лизат центрифугируют при 4500 g и затем при 100000 g в течение 2 часов. Если клетки или ткани происходят из печени, полученный супернатант сначала наносят на колонку с голубой Sepharose (Pharmacia), чтобы удалить альбумин. Или же полученный супернатант наносят на колонку с Con A-Sepharose (Pharmacia Biotech, Piscataway, NJ), предварительно уравновешенную буфером для связывания (20 мМ трис-HCl, pH 7,5; 100 мМ NaCl; 1 мМ MgCl2; 1 мМ CaCl2; 1 мМ MnCl2 и 15 мМ 2-МЕ). Связанные белки элюируют буфером для связывания, содержащим 15% α-D-o-метиламаннозид (Sigma, St. Louis, MO).
Не связанный с Con A-Sepharose материал сначала диализуют против раствора 20 мМ трис-HCl, pH 7,5; 100 мМ NaCl и 15 мМ 2-МЕ, затем наносят на колонку с DEAE-Sepharose и элюируют градиентом соли от 100 до 500 мМ NaCl. Фракции, содержащие hsp110, собирают, диализуют и наносят на колонку Mono Q (Pharmacia) 10/10, уравновешенную 20 мМ трис-HCl, рН 7,5; 200 мМ NaCl; и 15 мМ 2-МЕ. Связанные белки элюируют градиентом 200-500 мМ NaCl. Фракции анализируют с помощью SDS-PAGE с последующим иммуноблоттингом с Ab для hsp110, как описано Wang et al., 1999, J. Immunol. 162: 3378. Объединенные фракции, содержащие hsp110, концентрируют на установке Centriplus (Amicon, Beverly, MA) и наносят на колонку с суперозой 12 (Pharmacia). Белки элюируют 40 мМ трис-HCl, pH 8,0; 150 мМ NaCl и 15 мМ 2-МЕ со скоростью 0,2 мл/мин.
5.2.5. Получение и очистка нековалентных, продуцируемых клеткой комплексов Grp170-пептид
Представленный в качестве примера способ, описанный Wang et al., 2001, J. Immunol. 166(1): 490-7, который можно использовать, но без ограничения, заключается в следующем.
Осадок (40-60 мл) клеток или ткани, например ткани опухолевых клеток, гомогенизируют в 5 объемах гипотонического буфера (30 мМ бикарбонат натрия, рН 7,2 и ингибиторы протеаз) гомогенизацией в гомогенизаторе Dounce. Лизат центрифугируют при 4500 g и затем при 100000 g в течение 2 часов. Если клетки или ткани происходят из печени, полученный супернатант сначала наносят на колонку с голубой Sepharose (Pharmacia), чтобы удалить альбумин. Или же полученный супернатант наносят на колонку с Con A-Sepharose (Pharmacia Biotech, Piscataway, NJ), предварительно уравновешенную буфером для связывания (20 мМ трис-HCl, рН 7,5; 100 мМ NaCl; 1 мМ MgCl2; 1 мМ CaCl2; 1 мМ MnCl2 и 15 мМ 2-МЕ). Связанные белки элюируют буфером для связывания, содержащим 15% α-D-o-метиламаннозид (Sigma, St. Louis, MO).
Связанный с Con A-Sepharose материал сначала диализуют против раствора 20 мМ трис-HCl, рН 7,5; 150 мМ NaCl, затем наносят на колонку Mono Q и элюируют градиентом 150-400 мМ NaCl. Объединенные фракции концентрируют и наносят на колонку с суперозой 12 (Pharmacia). Фракции, содержащие гомогенный grp170, собирают.
5.2.6 Комплексы α2М-антигенная молекула
Эндогенные комплексы α2М-антигенная молекула можно получать по следующим способам, не ограничиваясь ими.
Альфа-2-макроглобулин можно приобретать из коммерческих источников или получать в результате очистки из крови человека. Для выделения α2М из крови можно использовать следующую, не ограничивающую методику.
Кровь берут у субъекта и оставляют для свертывания. Затем кровь центрифугируют в течение 30 минут при 14000×g, чтобы получить сыворотку, которую затем наносят на гель-фильтрационную колонку (Sephacryl S-100R), уравновешенную 0,04М трис-буфером, pH 7,6 плюс 0,3 М NaCl. Колонку 65 мл используют приблизительно для 10 мл сыворотки. Собирают фракции по три мл и каждую фракцию тестируют относительно присутствия α2М с помощью дот-блоттинга, используя специфические для α2М антитела. α2М-Позитивные фракции объединяют и наносят на колонку PD10, чтобы заменить буфер 0.01 М натрий-фосфатным буфером, рН 7,5, с PMSF. Объединенные фракции затем наносят на колонку с Con A (10 мл), уравновешенную фосфатным буфером. Колонку промывают и белок элюируют 5% метилманноза-пиранозидом. Элюент пропускают через колонку PD10, чтобы заменить буфер натрий-ацетатным буфером (0,05 М; pH 6,0). Затем колонку с DEAE уравновешивают ацетатным буфером и образец наносят на колонку с DEAE. Колонку промывают и белок элюируют 0,13 М ацетатом натрия. Затем фракции с α2М объединяют.
5.2.7 Рекомбинантная экспрессия HSP и α2М и антигенных пептидов
Известные в данной области способы можно использовать, чтобы рекомбинантно получать HSP и α2М. Последовательность нуклеиновой кислоты, кодирующей белок теплового шока или кодирующей α2М, можно вставить в экспрессирующий вектор для размножения и экспрессии в клетках хозяина.
Используемая в изобретении экспрессирующая конструкция имеет отношение к нуклеотидной последовательности, кодирующей HSP или α2М, действенно ассоциирована с одной или более регуляторных областей, что облегчает экспрессию HSP или α2М в соответствующей клетке хозяина. Термин «действенно ассоциирована» имеет отношение к ассоциации, в которой регуляторные области и последовательность HSP или α2М, которые должны экспрессироваться, соединяются и располагаются таким образом, чтобы допустить транскрипцию и, в конце концов, трансляцию.
Регуляторные области, необходимые для транскрипции HSP или α2М, могут быть обеспечены экспрессирующим вектором. Инициирующий трансляцию кодон (ATG) также может быть обеспечен, если в генной последовательности HSP или α2М отсутствует родственный инициирующий кодон, который должен экспрессироваться. В совместимой системе хозяин-конструкция клеточные факторы транскрипции, такие как РНК-полимераза, будут связываться с регуляторными областями на экспрессирующей конструкции, чтобы осуществить транскрипцию модифицированной последовательности HSP или α2М в организме хозяина. Определенная природа регуляторных областей, требуемая для генной экспрессии, может изменяться от клетки хозяина к клетке хозяина. Обычно требуется промотор, который способен связывать РНК-полимеразу и стимулировать транскрипцию действенно-ассоциированной последовательности нуклеиновых кислот. Такие регуляторные области могут включать области некодирующих последовательностей 5', вовлеченных в инициацию транскрипции и трансляции, такие как TATA box, кэппинг-последовательности, последовательности CAAT и подобные. Некодирующая область 3' в кодирующей последовательности может содержать транскрипционные терминационные регуляторные последовательности, такие как терминаторы и участки полиаденилирования.
Для того чтобы последовательности ДНК с регуляторными функциями, такими как промоторы, связать с генной последовательностью HSP или α2М или вставить генную последовательность HSP или α2М в клонирующий участок вектора, линкеры и адапторы, обеспечивающие соответствующие совместимые сайты рестрикции, могут быть лигированы по концам кДНК по способам, хорошо известным в данной области (Wu et al., 1987, Methods in Enzymol 152: 343-349). Расщепление рестрикционным ферментом можно проводить по модификации, чтобы дефосфолировать концы в результате переваривания или накопления концов одноцепочечной ДНК до лигирования. Альтернативно требуемый сайт рестрикционного фермента может быть введен во фрагмент ДНК амплификацией ДНК при применении PCR (ПЦР) с праймерами, содержащими требуемый сайт рестрикционного фермента.
Экспрессирующая конструкция, содержащая последовательность HSP или α2М, действенно ассоциированную с регуляторными областями, можно непосредственно вводить в подходящие клетки хозяина для экспрессии и продукции комплексов HSP-пептид и комплексов α2М-пептид без дальнейшего клонирования. См., например, патент США №5580859. Экспрессирующие конструкции также могут содержать последовательности ДНК, которые способствуют интеграции последовательности HSP или α2М в геном клеток хозяина, например через гомологичную рекомбинацию. В этом случае необходимо использовать экспрессирующий вектор, содержащий точку репликации, подходящую для соответствующих клеток хозяина, для размножения и экспрессии HSP или α2М в клетках хозяина.
Можно применять целый ряд экспрессирующих векторов, включающих, но не ограничиваясь перечисленным, плазмиды, космиды, фаги, фагемиды или модифицированные вирусы. Обычно такие экспрессирующие векторы содержат функциональную точку репликации для размножения вектора в соответствующей клетке хозяина, один или более рестрикционных эндонуклеазных сайтов для вставки генной последовательности HSP или α2М и один или более маркеров селекции. Экспрессирующий вектор следует использовать с совместимой клеткой хозяина, которая может происходить из прокариотического или эукариотического организма, включая, но не ограничиваясь перечисленным, бактерии, дрожжи, насекомых, млекопитающих и человека.
Для длительного периода времени оказывается предпочтительной продукция с высоким выходом соответственно обработанных комплексов HSP/α2М или HSP-пептид/α2М-пептид, стабильная экспрессия в клетках млекопитающих. Клеточные линии, которые стабильно экспрессируют комплексы HSP/α2М или HSP-пептид/α2М-пептид, могут быть созданы инженерно с использованием вектора, который содержит селектированный маркер. В качестве примера, но без ограничения, после введения экспрессирующих конструкций, инженерные клетки могут быть оставлены для роста в течение 1-2 дней в обогащенной среде и затем переведены на избирательные среды. Селектированный маркер в экспрессирующей конструкции придает резистентность к селекции и оптимально позволяет клеткам стабильно интегрировать экспрессирующую конструкцию в их хромосомы и расти в культуре и развиваться в клеточные линии. Такие клетки можно культивировать в течение длительного периода времени, так как HSP/α2М экспрессируются непрерывно.
Рекомбинантные клетки можно культивировать в стандартных условиях температуры, времени инкубации, оптической плотности и составе среды. Однако условия для роста рекомбинантных клеток могут отличаться от условий экспрессии HSP/α2М и антигенных пептидов. Модифицированные культуральные условия и среды также можно использовать, чтобы повысить продукцию HSP/α2М. Например, рекомбинантные клетки, содержащие HSP с их родственными промоторами, можно подвергать действию теплового стресса или другого стресса окружающей среды, или химическому стрессу. Любые способы, известные в данной области, можно применять, чтобы установить оптимальные условия для продукции комплексов HSP/α2М или HSP-пептид/α2М-пептид.
Клетки могут происходить из целого ряда источников, включающих, но не ограничиваясь ими, клетки, инфицированные инфекционным агентом, и злокачественные клетки, и включать, но не ограничиваясь ими, эпителиальные клетки, эндотелиальные клетки, кератиноциты, фибробласты, мышечные клетки, гепатоциты; клетки крови, такие как Т-лимфоциты, В-лимфоциты, моноциты, макрофаги, нейтрофилы, эозинофилы, мегакариоциты, гранулоциты; различные стволовые клетки или клетки-предшественники, в частности кроветворные стволовые или предшественники клетки, например, которые получены из костного мозга, пуповинной крови, периферической крови, печени эмбриона и так далее. Выбор типа клеток зависит от типа опухоли или инфекционного заболевания, которое лечат или предупреждают, и может быть установлен специалистом в данной области. В специальном аспекте экспрессирующую конструкцию, содержащую последовательность нуклеиновых кислот, кодирующую полипептид HSP/α2М, вводят в антигенную клетку. В случае изобретения антигенные клетки могут включать клетки, которые инфицированы инфекционным агентом или патогенным микроорганизмом, клетки, инфицированные неинфекционными или непатогенными формами инфекционного агента или патогенного микроорганизма (например, при применении хелпер инфекционного агента), клетки, инфицированные или созданные инженерно, чтобы экспрессировать ослабленную форму инфекционного агента или непатогенного или репликация-дефицитного варианта патогенного микроорганизма, пренеопластические клетки, которые инфицированы вызывающим злокачественную опухоль инфекционным агентом, таким как вирус, но который еще не является неопластическим; или антигенные клетки, которые были подвергнуты действию мутагена или вызывающего злокачественную опухоль агента, такого как, например, ДНК-повреждающие агенты, излучение и так далее. Другие клетки, которые можно использовать, представляют собой пренеопластические клетки, которые находятся в переходном состоянии от нормальной к неопластической форме, которые отличаются по морфологии, физиологическим или биохимическим функциям. Предпочтительно злокачественные клетки и пренеопластические клетки, используемые в способах изобретения, происходят от млекопитающих. Рассматриваемые в этом аспекте изобретения млекопитающие включают человека, животных-компаньонов (например, собак и кошек), домашних животных (например, овец, крупный рогатый скот, коз, свиней и лошадей), лабораторных животных (например, мышей, крыс и кроликов) и плененных или свободных диких животных.
В различных аспектах любую злокачественную клетку, предпочтительно раковую клетку человека, можно использовать в данном изобретении для продукции пептид-комплексов. Злокачественные клетки дают антигенные пептиды, которые становятся ковалентно или нековалентно ассоциированными с экспрессированным полипептидом HSP/α2М. Затем пептид-комплексы очищают из клеток и применяют, чтобы лечить такие злокачественные заболевания. Злокачественные опухоли, которые можно лечить или предупреждать иммуногенными композициями, приготовленными по способам данного изобретения, включают, но не ограничиваясь ими, опухоли, такие как саркомы и карциномы. Соответственно, любые ткани и клетки, выделенные из пренеопластического повреждения, злокачественной опухоли, включая рак, который метастазировал в многочисленные отдаленные участки, можно использовать в данном способе. Например, можно использовать клетки, обнаруженные в аномально растущей ткани, циркулирующие лейкозные клетки, метастатические поражения, а также ткань солидных опухолей.
В другом аспекте клеточные линии, происходящие из пренеопластического поражения, злокачественных тканей или злокачественных клеток также можно использовать при условии, что клетки клеточной линии имеют, по крайней мере, одну или более антигенных детерминант подобно антигенам на злокачественных клетках-мишенях. Предпочтительными являются злокачественные ткани, злокачественные клетки, клетки, инфицированные вызывающим злокачественную опухоль агентом, другие пренеопластические клетки и клеточные линии человеческого происхождения.
Злокачественные и пренеопластические клетки можно идентифицировать по способу, известному в данной области. Например, злокачественные клетки можно идентифицировать по морфологии, ферментному анализу, исследованию пролиферации, цитогенетической характеристике, картированию ДНК, секвенированию ДНК, присутствию вызывающего злокачественную опухоль вируса или истории воздействия мутагена или вызывающего злокачественную опухоль агента, визуализации и так далее. Злокачественные клетки также можно получать при хирургическом вмешательстве, эндоскопии или другом способе биопсии. Если некоторые отличительные характеристики злокачественных клеток известны, клетки также можно получать и очищать с помощью любых биохимических или иммунологических способов, известных в данной области, таких как аффинная хроматография и флуоресцентная сортировка активированных клеток (например, флуоресцентно меченые антитела против антигена, экспрессированного злокачественными клетками).
Злокачественные ткани, злокачественные клетки или клеточные линии можно получать от одного индивидуума или объединять от нескольких индивидуумов. Не является существенным, что используют клональные, гомогенные или очищенные популяции злокачественных клеток. Также не является важным использование клеток конечной цели in vivo (например, клеток из опухоли предполагаемого реципиента), поскольку, по крайней мере, одна или более антигенных детерминант на злокачественных клетках-мишенях присутствуют на клетках, используемых для экспрессии полипептида HSP/α2М. Кроме того, клетки, происходящие из отдаленных метастазов, можно использовать, чтобы получить иммуногенную композицию против первичного рака. Смесь клеток можно использовать при условии, что значительное количество клеток в смеси являются злокачественными клетками и имеют, по крайней мере, одну совместную антигенную детерминанту с раковой клеткой-мишенью. В специальном аспекте очищают злокачественные клетки, которые должны использовать при экспрессии полипептида HSP/α2М.
5.2.8 Пептидный синтез
Альтернативой продукции HSP/α2М рекомбинатными способами является пептидный синтез. Например, целый HSP/α2М или пептид, соответствующий части HSP/α2М, можно синтезировать, применяя пептидный синтезатор. Можно использовать общепринятый способ пептидного синтеза или другие методики синтеза, хорошо известные в данной области.
Пептиды, имеющие аминокислотную последовательность HSP/α2М или его части, можно синтезировать с помощью способа твердофазного пептидного синтеза, используя методики, подобно описанным Merrifield, 1963, J. Am. Chem. Soc., 85: 2149. Во время синтеза N-α-защищенные аминокислоты, имеющие защищенные боковые цепи, ступенчато добавляют к растущей полипептидной цепи, присоединяющиеся своим С-концом, и к нерастворимому полимерному носителю, то есть полистирольным гранулам. Пептиды синтезируют путем связывания аминогруппы N-α-лишенной защиты аминокислоты с α-карбоксильной группой N-α-защищенной аминокислоты, которая активирована реактивированием ее реагентом, таким как дихлоргексилкарбодиимид. Присоединение свободной аминогруппы к активированному карбоксилу приводит к образованию пептидной связи. Обычно наиболее используемые N-α-защищенные группы включают Boc, которая является кислотолабильной, и Fmoc, которая является щелочнолабильной. Детали относительно соответствующей химии, смол, защитных групп, защищенных аминокислот и реагентов хорошо известны в данной области и поэтому подробно не обсуждаются в данном описании (см. Atherton, et al., 1989, Solid Phase Peptide Synthesis: A Practical Approach, IRL Press, and Bodanszky, 1993, Peptide Chemistry, A Practical Textbook, 2nd Ed., Springer-Verlag).
Очистку полученного HSP/α2М осуществляют с применением общепринятых способов, таких как препаративная ВЭЖХ, использующая гельпроникающую, распределительную и/или ионообменную хроматографию. Выбор подходящих носителей и буферов хорошо известен в данной области и поэтому не рассматривается в данном описании подробно.
5.3 АНТИГЕННЫЕ МОЛЕКУЛЫ
В следующих подразделах рассматриваются пептиды, которые используют как антигенные/иммуногенные компоненты комплексов HSP/α2М-пептид изобретения, и как такие пептиды могут быть идентифицированы, например, для применения в рекомбинантной экспрессии пептидов для образования комплексов HSP/α2М и антигенных молекул in vitro. Однако при практическом применении данного изобретения требуется идентификация антигенной молекулы(ул) комплекса HSP/α2М-пептид, которая не известна(ны), например, когда комплекс HSP/α2М выделяют непосредственно из злокачественной клетки или из ткани, инфицированной патогенным микроорганизмом.
5.3.1 Выделение антигенных/иммуногенных компонентов
Обнаружено, что антигенные пептиды и/или компоненты можно элюировать из комплексов HSP/α2М или в присутствии АТФ или при низком рН. Описанные экспериментальные условия можно использовать, чтобы выделить пептиды и/или антигенные компоненты из клеток, которые могут содержать потенциально полезные антигенные детерминанты. Аминокислотную последовательность каждого антигенного пептида можно определить непосредственно посла выделения, используя общепринятую методологию аминокислотного секвенирования. Затем такие антигенные молекулы могут быть получены по способам химического синтеза или рекомбинантными способами, очищены и они могут образовывать комплексы с HSP in vitro, чтобы образовать комплексы HSP изобретения.
Аналогично обнаружено, что потенциально иммуногенные пептиды можно элюировать из комплексов МНС-пептид, используя способы, хорошо известные в данной области (Falk, K. et al., 1990 Nature 348: 248-251; Elliot, T., et al., 1990, Nature 348: 195-197; Falk, K., et al., 1991, Nature 351: 290-296).
Таким образом, потенциально иммуногенные или антигенные пептиды можно выделять из или эндогенных комплексов стрессовый белок-пептид, или эндогенных комплексов МНС-пептид для применения впоследствии в качестве антигенных молекул посредством комплексообразования in vitro с HSP/α2М, чтобы образовать комплексы HSP/α2М изобретения. Показательные протоколы выделения пептидов и/или антигенных компонентов из любых из указанных комплексов, известные в данной области, описаны ниже.
5.3.2 Пептиды из комплексов стрессовый белок-пептид
Два способа можно использовать, чтобы элюировать пептид из комплекса стрессовый белок/пептид.
Один подход включает инкубацию комплекса стрессовый белок/пептид в присутствии АТФ. Другой подход включает инкубацию комплексов в буфере с низким значением pH.
Кратко, представляющий интерес комплекс центрифугируют на установке Centricon 10 (Millipore), чтобы удалить любой низкомолекулярный материал, свободно ассоциированный с комплексом. Высокомолекулярную фракцию можно удалить и исследовать с помощью SDS-PAGE, тогда как низкомолекулярную фракцию можно анализировать с помощью ВЭЖХ, как описано ниже. По протоколу инкубации в присутствии АТФ комплекс стрессовый белок-пептид в высокомолекулярной фракции инкубируют с 10 мМ АТФ в течение 30 минут при комнатной температуре. По протоколу с применением низкого pH, уксусную кислоту или трифторуксусную кислоту (TFA) добавляют к комплексу стрессовый белок-пептид, чтобы получить конечную концентрацию 10% (об./об.), и смесь инкубируют при комнатной температуре или на кипящей водяной бане, или при любой температуре в диапазоне между указанными температурами в течение 10 минут (см. Van Bleek, et al., 1990, Nature 348: 213-216; и Li, et al., 1993, EMBO Journal 12: 3143-3151).
Полученные образцы центрифугируют на установке Centricon 10, как описано выше. Получают высокомолекулярные и низкомолекулярные фракции. Оставшиеся высокомолекулярные комплексы стрессовый белок-пептид можно повторно инкубировать с АТФ или при низком pH, чтобы удалить любые оставшиеся пептиды.
Полученные низкомолекулярные фракции объединяют, концентрируют выпариванием и растворяют в 0,1% TFA. Растворенный материал затем фракционируют методом ОФ-ВЭЖХ, используя, например, колонку с обращенной фазой VYDAC C18, уравновешенную 0,1% TFA. HSP/α2М Связанный материал затем элюируют при объемной скорости приблизительно 0,8 мл/мин при работе колонки с линейным градиентом от 0 до 80% ацетонитрила в 0,1% TFA. За элюированием пептидов можно следить по OD210 и собирать фракции, содержащие пептиды.
5.3.3 Пептиды из комплексов МНС-пептид
Способ отделения потенциально иммуногенных пептидов от молекул МНС хорошо известен в данной области и поэтому в изобретении не описывается подробно (см. Falk, et al., 1990, Nature 348:248-251; Rotzsche, et al., 1990, Nature 348: 252-254; Elliott, et al., 1990, Nature 348: 191-197; Falk, et al., 1991, Nature 351: 290-296; Demotz, et al., 1989, Nature 343:682-684: Rotzsche, et al., 1990, Science 249: 283-287), данные из которых включены в описание посредством ссылки.
Кратко, комплексы МНС-пептид можно выделять по общепринятому иммуноаффинному способу. Затем пептиды можно элюировать из комплекса инкубацией комплексов в присутствии приблизительно 0,1% TFA в ацетонитриле. Элюированные пептиды можно фракционировать и очищать с помощью ОФ-ВЭЖХ, как описано ранее.
Аминокислотные последовательности элюированных пептидов можно определять по способам или ручного, или автоматического аминокислотного секвенирования, хорошо известным в данной области. Как только аминокислотная последовательность необязательно защищенного пептида определена, пептид можно синтезировать в любом требуемом количестве, используя общепринятый пептидный синтез или другие протоколы, хорошо известные в данной области.
Пептиды, имеющие одинаковые аминокислотные последовательности, как пептиды, выделенные выше, можно синтезировать по способу твердофазного пептидного синтеза, используя методики, подобно описанным Merrifield, 1963, J. Am. Chem. Soc., 85: 2149. Во время синтеза N-α-защищенные аминокислоты, имеющие защищенные боковые цепи, ступенчато добавляют к растущей полипептидной цепи, присоединяющиеся своим С-концом, и к нерастворимому полимерному носителю, то есть полистирольным гранулам. Пептиды синтезируют путем связывания аминогруппы N-α-лишенной защиты аминокислоты с α-карбоксильной группе N-α-защищенной аминокислоты, которая активирована реактивированием ее реагентом, таким как дихлоргексилкарбодиимид. Присоединение свободной аминогруппы к активированному карбоксилу приводит к образованию пептидной связи. Обычно наиболее используемые N-α-защищенные группы включают Boc, которая является кислотолабильной, и Fmoc, которая является щелочнолабильной.
Кратко, С-концевую N-α-защищенную аминокислоту сначала присоединяют к полистироловым гранулам. Затем N-α-защитную группу удаляют. Лишенную защиты α-аминогруппу связывают с активированной α-карбоксилатной группой следующей N-α-защищенной аминокислоты. Процесс повторяют до тех пор, пока не будет синтезирован требуемый пептид. Полученные пептиды затем отделяют от нерастворимого полимерного носителя и снимают защиту аминокислотных боковых цепей. Более длинные пептиды можно получать конденсацией защищенных пептидных фрагментов. Подробности относительно соответствующей химии, смол, защитных групп, защищенных аминокислот и реагентов хорошо известны в данной области и поэтому подробно не обсуждаются в данном описании (см. Atherton, et al., 1989, Solid Phase Peptide Synthesis: A Practical Approach, IRL Press, and Bodanszky, 1993, Peptide Chemistry, A Practical Textbook, 2nd Ed., Springer-Verlag).
Очистку полученных пептидов осуществляют, применяя общепринятые методики, такие как препаративная ВЭЖХ, использующая гельпроникающую, разделительную и/или ионообменную хроматографию. Выбор подходящих носителей и буферов хорошо известен в данной области и поэтому подробно не описывается.
5.3.4 Экзогенные антигенные молекулы
Молекулы, которые проявляют антигенность известного антигена патогенного микроорганизма или опухолеспецифического или ассоциированного с опухолью антигена типа рака, например антигены или их антигенные части, можно выбирать для применения в качестве антигенных молекул для образования комплексов с HSP/α2М среди молекул, известных в данной области, или молекул, которые по данным иммуноанализа способны связываться с антителом или молекулами МНС (антигенность), или генерировать иммунный ответ (иммуногенность). Для установления иммуногенности или антгенности посредством определения связывания с антителом, можно использовать различные иммуноанализы, известные в данной области, включающие, но не ограничивающиеся ими, конкурентные и неконкурентные системы анализа, использующие методы, такие как радиоиммуноанализ, ELISA (твердофазный иммуноферментный анализ), иммуноферментный сэндвич-анализ, иммунорадиометрический анализ, гельдиффузионные реакции с преципитином, иммунодиффузионные анализы, иммуноанализы in vivo (например, использующие коллоидное золото, ферментные или радиоактивные изотопные метки), вестерн-блоттинг, реакции иммунопреципитации, исследования агглютинации (например, гельагглютинационные анализы, гемагглютинационные анализы), анализ фиксации комплемента, иммунофлуоресцентные анализы, анализ с протеином А и иммуноэлектрофорез и так далее. В одном аспекте связывание антител определяют посредством определения метки на первичном антителе. В другом аспекте первичное антитело определяют посредством определения связывания вторичного антитела или реагента с первичным антителом. В следующем аспекте метят вторичное антитело. Большинство способов для определения связывания в иммуноанализе известны в данной области и доступны для применения. В еще одном аспекте для определения иммуногенности опосредованные Т-клетками ответы можно исследовать с помощью стандартных методов, например с помощью цитотоксического анализа in vitro или анализа гиперчувствительности замедленного типа in vivo.
Потенциально полезные антигены или их производные для применения в качестве антигенных молекул также можно идентифицировать по различным критериям, таким как антигенное вовлечение в нейтрализацию инфекционности патогенного микроорганизма (причем желательно лечить или предупреждать инфекцию таким патогенным микроорганизмом) (Norrby, 1985, Summary, in Vaccines 85, Lerner, et al., (eds.), Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, pp.388-389), тип или группа специфичности, узнавание антисывороткой или иммунными клетками пациента и/или демонстрация защитного действия антисыворотки или иммунных клеток, специфичных в отношении антигена. Кроме того, желательно, чтобы лечить или предупреждать заболевание, вызванное патогенным микроорганизмом, эпитоп, кодированный антигеном, предпочтительно должен проявлять в небольшой степени антигенную изменчивость или не проявлять никакой изменчивости со временем или среди различных изолятов того же патогенного микроорганизма.
Предпочтительно, в случае когда требуется лечить или предупреждать злокачественные опухоли, используют известные, опухолеспецифические (то есть экспрессируемые в опухолевых клетках) или ассоциированные с опухолью антигены (то есть относительно сверхэкспрессируемые в опухолевых клетках), или их фрагменты или производные. Например, такие опухолеспецифические или ассоциированные с опухолью антигены включают, но не ограничиваясь ими, антиген пан-карциномы KS ј (Perez and Walker, 1990, J. Immunol. 142: 3662-3667; Bumal, 1988, Hybridoma 7(4): 407-415); антиген карциномы яичника (CA125) (Yu, et al., 1991, Cancer Res. 51(2): 468-475); кислый фосфат простаты (Tailer, et al., 1990, Nucl. Acids Res. 18(16): 4928); специфический антиген простаты (Henttu and Vihko, 1989, Biochem. Biophys. Res. Comm. 160(2): 903-910; Israeli, et al., 1993, Cancer Res. 53: 227-230); ассоциированный с меланомой антиген p97 (Estin, et al., 1989, J. Natl. Cancer Inst. 81(6): 445-446); антиген меланомы gp75 (Vijayasardahl, et al., 1990, J. Exp.Med. 171(4): 1375-1380); высокомолекулярный антиген меланомы (Natali, et al., 1987, Cancer 59: 55-63) и специфический мембранный антиген простаты. Другие экзогенные антигены, которые могут образовывать комплексы с HSP/α2М, включают порции или белки, которые мутируют с высокой частотой в злокачественных клетках, такие как онкогены (например, ras, особенно мутанты ras с активирующими мутациями, которые происходят только в четырех аминокислотных остатках (12, 13, 59 или 61) (Gedde-Dahl et al., 1994, Eur. J. Immunol. 24(2): 410-414) и гены супрессоров опухолей (например, p53), для которых целый ряд мутантных или полиморфных пептидных р53 антигенов, способных стимулировать ответ цитотоксических Т-клеток, был идентифицирован (Gnjatic et al., 1995, Eur. J. Immunol. 25(6): 1638-1642).
В специальном аспекте антиген или его фрагмент или производное, специфичный к определенной опухоли, выбирают для комплексообразования с HSP/α2М, чтобы образовать комплекс HSP/α2М для введения пациенту, имеющему опухоль.
Предпочтительно, когда требуется лечить или предупреждать вирусные заболевания, используют молекулы, содержащие эпитопы известных вирусов. Например, такие антигенные эпитопы можно получать из вирусов, включающих, но не ограничивающихся ими, вирус гепатита типа А, гепатита типа В, гепатита типа С, гриппа, ветряной оспы, аденоассоциированный вирус, вирус герпеса типа I (HSV-1), герпеса типа II (HSV-II), вирус rinderpest, риновирус, echo-вирус, ротавирус, респираторно-синцитиальный вирус, вирус папилломы, папова-вирус, цитомегаловирус, эхиновирус, арбовирус, гунтавирус, вирус Коксаки, вирус паротита, вирус кори, вирус краснухи, вирус полиомиелита, вирус иммунодефицита человека типа I (HIV-I) и вирус иммунодефицита человека типа II (HIV-II). Предпочтительно, когда требуется лечить или предупреждать бактериальные инфекции, используют молекулы, содержащие эпитопы известных бактерий. Например, такие антигенные эпитопы можно получать из бактерий, включающих, но не ограничиваясь перечисленным, микобактерии, риккетсии, микоплазму, нейссерии и легионеллу.
Предпочтительно, когда требуется лечить или предупреждать протозойные инфекции, используют молекулы, содержащие эпитопы известных простейших. Например, такие антигенные эпитопы можно получать от простейших, включающих, но не ограничиваясь перечисленным, лейшмании, кокзидии и трипаносомы.
Предпочтительно, когда требуется лечить или предупреждать паразитарные инфекции, используют молекулы, содержащие эпитопы известных паразитов. Например, такие антигенные эпитопы могут быть от паразитов, включая, но не ограничиваясь перечисленным, хламидии и риккеттсии.
5.4 IN VITRO ПРОДУКЦИЯ НЕКОВАЛЕНТНЫХ КОМПЛЕКСОВ HSP/α2М
В аспекте, в котором HSP/α2М и пептиды, с которыми они эндогенно ассоциированы in vivo, не применяют, комплексы HSP/α2М с антигенными молекулами получают in vitro. Специалистам в данной области будет очевидно, что пептиды, или выделенные указанными выше способами или химически синтезированные, или рекомбинантно полученные, могут распознаваться целым рядом очищенных природных или рекомбинантных стрессовых белков in vitro, чтобы генерировать иммуногенные нековалентные комплексы стрессовый белок-антигенная молекула. Альтернативно экзогенные антигены или их антигенные или иммуногенные фрагменты или производные могут образовывать комплексы со стрессовыми белками. Предпочтительный показательный протокол комплексообразования стрессового белка и антигенной молекулы in vitro описан ниже.
В способе, по которому получают нековалентные комплексы HSP-антигенная молекула и комплексы α2М-антигенная молекула, комплекс получают в соответствии со способом, описанным Blachere et al., 1997 J. Exp. Med. 186(8): 1315-22, включенным в данное описание посредством ссылки во всей ее полноте. Blachere рассматривает in vitro комплексообразование HSP c антигенной молекулой. Описанный Blachere протокол можно модифицировать так, чтобы компонент hsp замещался α2М. Binder et al. (2001, J. Immunol. 166: 4968-72) демонстрирует, что способ Blachere дает комплексы α2М, связанного с антигенными молекулами.
До образования комплексов, HSP/α2М предварительно обрабатывают АТФ или при низком рН, чтобы удалить любые пептиды, которые могут быть ассоциированы с представляющим интерес HSP/α2М. Когда используют АТФ-методику, избыток АТФ удаляют из препарата добавлением апираназы, как описано Levy, et al., 1991, Cell 67: 265-274. Когда используют методику с низким рН, буфер повторно доводят до нейтрального pH добавлением реагентов, модифицирующих рН.
Антигенные молекулы и предварительно обработанные HSP/α2М смешивают, чтобы получить молярное соотношение приблизительно 5 антигенных молекул:1 стрессовый белок. Затем смесь инкубируют в течение от 15 минут до 3 часов при от 4°С до 45°С в подходящем буфере для связывания, таком как буфер, содержащий 20 мМ фосфат натрия, рН 7,2, 350 мМ NaCl, 3 мМ MgCl2 и 1 мМ фенилметилсульфонилфторида (PMSF). Препараты центрифугируют на установке Centricon 10 (Millipore), чтобы удалить любой несвязанный пептид. Ассоциацию пептидов со стрессовыми белками можно анализировать с помощью SDS-PAGE. Это является предпочтительным способом для комплексообразования in vitro пептидов, выделенных из комплексов МНС-пептид, пептидов, диссоциировавших из эндогенных комплексов HSP-пептид.
В альтернативном аспекте изобретения предпочтительно для продукции комплексов hsp70 с экзогенными антигенными молекулами, такими как белки, 5-10 микрограмм очищенного HSP инкубируют с эквимолярными количествами антигенной молекулы в 20 мМ натрий-фосфатном буфере, pH 7,5, 0,5 М NaCl, 3 мМ MgCl2 и 1 мМ АДФ в объеме 100 микролитров при 37°С в течение 1 часа. Указанную инкубационную смесь в дальнейшем разводят до 1 мл забуференным фосфатом физиологическим раствором.
В альтернативном аспекте изобретения предпочтительно для продукции комплексов gp96 или hsp90 с пептидами, 5-10 микрограмм очищенного gp96 или hsp90 инкубируют с эквимолярными или избыточными количествами антигенного пептида в подходящем буфере, таком как 20 мМ натрий-фосфатном буфере, pH 7,5, 0,5 М NaCl, 3 нМ MgCl2 при 60-65°С в течение 15-20 минут. Указанную инкубационную смесь оставляют для охлаждения до комнатной температуры и центрифугируют один или более раз, если необходимо, на установке Centricon 10 (Millipore), чтобы удалить любой несвязанный пептид.
Антигенные молекулы можно выделять из различных источников, химически синтезировать или получать рекомбинантно. Такие способы можно легко адаптировать для среды или продукции большого масштаба иммунотерапевтических или профилактических вакцин.
После комплексообразования иммуногенные комплексы антигенных молекул необязательно можно исследовать in vitro, используя, например, смешанный анализ лимфоцитарных клеток-мишеней (MLTC), описанный ниже. Как только иммуногенные комплексы выделены, их необязательно можно далее характеризовать на животных моделях, используя предпочтительные протоколы введения и эксципиенты, обсуждаемые ниже.
5.5 ОБРАЗОВАНИЕ КОВАЛЕНТНЫХ КОМПЛЕКСОВ HSP/α2М
Как альтернатива нековалентным комплексам HSP/α2М и антигенным молекулам, антигенные молекулы могут быть ковалентно присоединены к HSP/α2М. Комплексы HSP/α2М-пептид предпочтительно поперечно сшивают после их выделения из клеток или тканей. Ковалентно связанные комплексы являются комплексами выбора, когда требуется ответ В-клеток.
В одном аспекте HSP/α2М ковалентно связывают с антигенными молекулами химическим сшиванием. Способы химического сшивания хорошо известны в данной области. Например, в предпочтительном аспекте можно использовать глутаральдегидное сшивание. Глутаральдегидное сшивание использовали для образования ковалентных комплексов пептидов и HSP (см. Barrios et al., 1992, Eur. J. Immunol. 22: 1365-1372). Предпочтительно 1-2 мг комплекса HSP-пептид сшивают в присутствии 0,002% глутаральдегида в течение 2 часов. Глутаральдегид удаляют диализом против забуференного фосфатом физиологического раствора (PBS) в течение ночи (Lussow et al., 1991, Eur. J. Immunol. 21: 2297-2302). В одном аспекте используют следующий протокол. Необязательно, HSP можно предварительно обработать АТФ или при низком pH до комплексообразования, чтобы удалить любые пептиды, которые могут быть ассоциированы с полипептидом HSP. Предпочтительно 1 мг HSP сшивают с 1 мг пептида в присутствии 0,002% глутаральдегида в течение 2 часов. Глутаральдегид удаляют диализом против забуференного фосфатом физиологического раствора (PBS) в течение ночи (Lussow et al., 1991, Eur. J. Immunol. 21: 2297-2302).
Также можно использовать другие способы для химического сшивания, кроме того, другие способы для ковалентного присоединения белков, такие как фотосшивание (см. Current Protocol in Molecular Biology, Ausubel et al., (eds.), Greene Publishing Associates and Wiley Interscience, New York).
В другом аспекте HSP и специфический антиген(ы) сшивают по способу ультрафиолетового (УФ) сшивания.
В одном аспекте HSP ковалентно сшивают с пептидными фрагментами по способу химического сшивания. Способы химического сшивания хорошо известны в данной области. Например, в предпочтительном аспекте можно использовать глутаральдегидное сшивание. Глутаральдегидное сшивание применяли для образования ковалентных комплексов пептидов и HSP (см. Barrios et al., 1992, Eur. J. Immunol. 22: 1265-1372). Предпочтительно 1-2 мг комплекса HSP-пептид сшивают в присутствии 0,002% глутаральдегида в течение 2 часов. Глутаральдегид удаляют диализом против забуференного фосфатом физиологического раствора (PBS) в течение ночи (Lussow et al., 1991, Eur. J. Immunol. 21: 2297-2302). Альтернативно HSP и популяцию пептидов можно сшивать по способу ультрафиолетового (УФ) сшивания в условиях, известных в данной области.
В другом аспекте изобретения популяция пептидов может образовывать комплексы с α2М при инкубации пептидных фрагментов с α2М при молярном соотношении 50:1, и смесь инкубируют при 50°С в течение 10 минут с последующей 30 минутной инкубацией при 25°С. Свободные (некомплексные) пептиды затем удаляют при вытеснительном фильтровании по размеру. Комплексы белок-пептид предпочтительно определяют с помощью сцинтилляционного счетчика, чтобы убедиться, как на каждую молярную основу каждый наблюдаемый белок связан с эквивалентным количеством пептида (приблизительно 0,1% исходного количества пептида). Для подробностей см. Binder, 2001, J. Immunol. 166(8): 4968-72, включенную в данное описание посредством ссылки во всей своей полноте.
Альтернативно популяция антигенных пептидов может ковалентно образовывать комплексы с α2М по способам, которые описаны в публикациях PCT WO 94/14976 и WO 99/50303 для комплексообразования пептида α2М, которые включены в данное описание посредством ссылки во всей своей полноте. Ковалентное сшивание популяции антигенных пептидов с α2М можно проводить, используя бифункциональный сшивающий агент. Такие сшивающие агенты и способы их применения также хорошо известны в данной области.
Вообще, когда α2М смешивают с протеазой, происходит расщепление “байт”-области α2М, протеиназа становится “захваченной” сложными тиоэфирами и имеет место конформационное изменение, которое допускает связывание комплекса α2М с рецептором α2М. Во время протеолитической активации α2М непротеолитические лиганды могут становиться ковалентно связанными с активированными сложными тиоэфирами. Непротеолитические лиганды также могут быть включены в активированную молекулу α2М с помощью аммиака или метиламина во время реверсирования нуклеофильной активации, использующего тепло (Gron and Pizzo, 1998, Biochemistry, 37: 6009-6014). Такие условия, которые допускают случайный захват пептидов посредством α2М, используют, чтобы получить комплексы α2М-антигенная молекула для применения в изобретении. Способы для такого ковалентного связывания были описаны ранее (Osada et al., 1987, Biochem. Biophys. Res. Commun. 146: 26-31; Osada et al., 1988, Biochem. Biophys. Res. Commun. 150: 883; Chu and Pizzo, 1993, J. Immunol. 150: 48; Chu et al., 1994, Ann. N.Y. Acad. Sci. 737: 291-307; Mitsuda et al., 1993, Biochem. Biophys. Res. Commun. 101: 1326-1331). Таким образом, в одном аспекте комплекс α2М-антигенная молекула можно получать, как описано Gron and Pizzo, 1998, Biochemistry, 37: 6009-6014. По способу Gron и Pizzo получают комплексы α2М, которые ковалентно связаны с антигенными молекулами.
Например, полипептид α2М смешивают с антигенной молекулой в присутствии протеазы, аммиака или другого небольшого аминного нуклеофила, такого как метиламин или этиламин. Не ограничивающие примеры протеаз, которые можно использовать, включают трипсин, панкреатическую эластазу свиньи (PEP), эластазу нейтрофиллов человека, катепсин G, протеиназу V-8 S. aureus, трипсин, α-химотрипсин, протеазу V-8, папаин и протеиназу К (см. Ausubel et al., eds., in “Current Protocols in Molecular Biology”, Greene Publishing Associates and Wiley Interscience, New York, 17.4.6-17.4.8). Предпочтительным показательным протоколом для образования комплекса полипептида α2М и антигенной молекулы in vitro является следующее. Антигенные молекулы (1 мкг-20 мг) и полипептид α2М (1 мкг-20 мг) смешивают вместе в забуференном фосфатом физиологическом растворе (PBS) (100 мкл-5 мл) в присутствии протеазы, такой как трипсин (0,92 мг трипсина приблизительно в 500 мкл PBS), чтобы получить молярное соотношение 5:1 антигенная молекула:полипептид α2М. Затем смесь инкубируют в течение 5-15 минут при 37°С. п-Афенилметилсульфонилфторид (p-APMSF), 500 мкл 4 мг/мл, добавляют к раствору, чтобы ингибировать активность трипсина, и инкубируют в течение 2 часов при 25°С. Препараты можно центрифугировать на установке Centricon 10 (Millipore), чтобы удалить любой несвязанный пептид. Альтернативно свободная антигенная молекула может быть удалена при прохождении через гельпроникающую колонку. Ассоциацию пептидов с полипептидом α2М можно исследовать методом SDS-PAGE. Это является предпочтительным способом для образования in vitro комплекса антигенных молекул, выделенных из комплексов МНС-антигенная молекула, или пептидов, диссоциировавших из эндогенных комплексов α2М-антигенная молекула. Вышеприведенные способы можно быстро использовать, чтобы образовать комплексы HSP-пептид.
5.6 СЛИТЫЕ БЕЛКИ, СОДЕРЖАЩИЕ HSP ИЛИ α2М
В некоторых аспектах изобретения комплекс HSP/α2М-антигенная молекула представляет собой рекомбинантные слитые белки. Такие рекомбинантные слитые белки, содержащие последовательности HSP/α2М, связанные с последовательностями антигенных молекул, можно использовать в способах данного изобретения. Чтобы получить такой рекомбинантный слитый белок, экспрессирующий вектор конструируют, используя последовательности нуклеиновых кислот, кодирующие HSP/α2М, слитые с последовательностями, кодирующими антигенную молекулу, используя рекомбинантные способы, известные в данной области (см. Suzue et al., 1997, Proc. Natl. Acad. Sci. USA. 94: 13146-51). Затем образованный слиянием HSP/α2М-антигенный пептид экспрессируют и выделяют. Согласно специфическому конструированию антигенной пептидной части молекулы такие слитые белки можно использовать, чтобы выявить иммунный ответ, и в иммунотерапии против таргетированных злокачественных опухолей и инфекционных заболеваний.
5.7 НАБОРЫ, СХЕМЫ ПРИЕМА ЛЕКАРСТВЕННОГО СРЕДСТВА, ВВЕДЕНИЕ И СОСТАВ
Также предусмотрены наборы для осуществления терапевтических способов данного изобретения. В одном аспекте набор включает первый контейнер, содержащий очищенный препарат HSP или препарат α2М, и второй контейнер, содержащий невакцинный лечебный препарат для лечения злокачественных опухолей. Предпочтительно злокачественные опухоли представляют собой CML, препарат HSP содержит комплексы hsp70-пептид, и терапевтическим препаратом является Gleevec™. В специальном аспекте второй контейнер содержит иматиниба мезилат. В другом специальном аспекте иматиниба мезилат очищают. В особом аспекте набор содержит первый контейнер, содержащий препарат очищенного HSP или препарат α2М в количестве недостаточном, чтобы лечить заболевание или нарушение, когда вводят отдельно; и второй контейнер, содержащий невакцинный лечебный препарат в количестве, которое, когда вводят до, одновременно с или после введения препарата HSP или препарата α2М из первого контейнера, оказывается эффективным, чтобы улучшить общую эффективность лечения по сравнению с эффективностью при введении каждого компонента отдельно. В другом специальном аспекте набор содержит первый контейнер, содержащий препарат очищенного HSP или препарат α2М в количестве, не эффективном, чтобы лечить заболевание или нарушение, когда вводят отдельно; и второй контейнер, содержащий один или более невакцинных лечебных препаратов для воздействия в количестве, которое, когда вводят до, одновременно с или после введения препарата HSP или препарата α2М из первого контейнера, оказывается эффективным, чтобы улучшить общую эффективность лечения по сравнению с эффективностью введения препарата HSP или препарата α2М, вводимых отдельно, или лечебных воздействий, проводимых отдельно. В еще одном специальном аспекте первый контейнер содержит препарат очищенного HSP или препарат α2М в количестве недостаточном, чтобы лечить заболевание или нарушение, когда вводят отдельно; и второй и третий контейнеры, каждый из которых содержит невакцинный лечебный препарат в количестве, которое, когда вводят до, одновременно с или после введения препарата HSP или препарата α2М из первого контейнера, оказывается эффективным, чтобы улучшить общую эффективность лечения по сравнению с эффективностью введения препарата HSP или препарата α2М, вводимых отдельно, или лечебных воздействий, применяемых отдельно. В предпочтительном специальном аспекте изобретение предусматривает набор, содержащий в первом контейнере препарат очищенного HSP или α2М, содержащий популяцию нековалентных комплексов HSP-пептид и комплексов α2М-пептид, полученных из злокачественной ткани млекопитающего; во втором контейнере композицию, содержащую очищенное раковое химиотерапевтическое средство; и в третьем контейнере композицию, содержащую очищенный цитокин. В специальном аспекте второй контейнер содержащий иматиниба мезилат, содержит очищенный иматиниба мезилат.
Дозировки препарата HSP или препарата α2М, которые вводят, зависят в большой степени от состояния и размера субъекта, которого лечат, а также количества проводимого невакцинного лечебного воздействия, частоты лечения и способа введения. Схемы для продолжительной терапии, включая участок, дозу и частоту, могут быть выбраны по первоначальному ответу и клинической оценке.
В зависимости от способа введения и типа HSP в препарате HSP, количество HSP в препарате HSP может колебаться, например, от 0,1 до 1000 мкг на введение. Предпочтительные количества gp96 или hsp70 составляют диапазон от 10 до 600 мкг на введение и от 0,1 до 1000 мкг, если препарат HSP вводят внутрикожно. Особо предпочтительное количество hsp70 составляет приблизительно 50 мкг на введение, если вводят внутрикожно. Для hsp90 предпочтительные количества составляют приблизительно от 50 до 1000 мкг на введение и приблизительно от 5 до 50 мкг для внутрикожного введения. Количество вводимого α2М может колебаться от 2 до 1000 мкг, предпочтительно от 20 до 500 мкг, наиболее предпочтительно приблизительно от 25 до 250 мкг, назначаемого один раз еженедельно в течение приблизительно 4-6 недель внутрикожно с участком введения, изменяемом впоследствии.
Так как в некоторых аспектах способы изобретения используют введение препарата HSP в субоптимальных количествах, полагают, что в зависимости от способа введения и типа HSP в препарате HSP, количество HSP в препарате HSP может быть меньше, чем количество, составляющее диапазон от 0,1 до 1000 мкг на введение. Соответственно, предпочтительные количества gp96 или hsp70 составляют количества меньше, чем диапазон от 10 до 600 мкг на введение, и меньше, чем диапазон от 0,1 до 10 мкг, если препарат HSP вводят внутрикожно. Для hsp90 предпочтительные количества составляют меньше, чем область от 50 до 1000 мкг на введение и меньше, чем диапазон от 5 до 50 мкг для внутрикожного введения. Количество вводимого α2М может колебаться в диапазоне, более низком, чем от 2 до 1000 мкг, предпочтительно менее чем от 20 до 500 мкг, наиболее предпочтительно в диапазоне менее чем от 25 до 250 мкг, вводимых один раз еженедельно в течение приблизительно 4-6 недель внутрикожно с участком введения, изменяемом впоследствии.
Растворимость и участок применения лечебного воздействия являются факторами, которые следует учитывать при выборе способа введения препарата HSP изобретения. Способ введения может быть разнообразным, предусматривающим, но без ограничения, например, подкожное, внутривенное, внутрибрюшинное, внутримышечное, внутрикожное и чресслизистое введение. Способы введения через слизистые могут далее принимать формы перорального, ректального и назального введения. Принимая во внимание вышеприведенные факторы, может быть предпочтительным введение HSP в участок, который является тем же самым или проксимальным к участку применения лечебного воздействия.
В аспекте изобретения HSP/α2М можно вводить, используя любой требуемый способ введения. Преимущества внутрикожного введения включают применение более низких доз и быстрое всасывание соответственно. Преимущества подкожного или внутримышечного введения заключаются в пригодности для некоторых нерастворимых суспензий и маслянистых суспензий соответственно. Способы введения через слизистые включают, но не ограничиваясь ими, пероральное, ректальное и назальное введение. Препараты для введения через слизистые подходят для различных составов, которые описаны ниже.
Если препарат HSP/α2М является растворимым в воде, тогда он может быть приготовлен в подходящем буфере, например забуференном фосфатом физиологическом растворе или других физиологически совместимых растворах, предпочтительно стерильных. Альтернативно, если полученный комплекс плохо растворим в водных растворителях, тогда он может быть приготовлен с неионным поверхностно-активным веществом, таким как твин или полиэтиленгликоль. Таким образом, соединения и их физиологически приемлемые сольваты могут быть приготовлены для введения с помощью ингаляции или вдувания (или через рот, или нос) или перорального, щечного, парентерального или ректального введения, или, в случае опухоли, непосредственного введения в солидную опухоль.
Для перорального введения фармацевтический препарат может быть в жидкой форме, например в виде растворов, сиропов или суспензий, или может быть представлен в виде лекарственного средства для воссоздания с водой или другим подходящим наполнителем перед применением. Такой жидкий препарат можно приготовить по общепринятым способам с фармацевтически приемлемыми добавками, такими как суспендирующие вещества (например, сироп сорбита, производные целлюлозы или гидрогенизированные годные в пищу жиры), эмульгаторы (например, лецитин или аравийская камедь), неводные наполнители (например, миндальное масло, маслянистые сложные эфиры или гидрогенизированные растительные масла), и консерванты (например, метил или пропил-п-гидроксибензоаты или сорбиновая кислота). Фармацевтические препараты могут быть в виде, например, таблеток или капсул, приготовленных общепринятыми способами с фармацевтически приемлемыми эксципиентами, такими как связующие вещества (например, предварительно желатинизированный маисовый крахмал, поливинилпирролидон или гидроксипропилметилцеллюлоза), наполнители (например, лактоза, микрокристаллическая целлюлоза или вторичный кислый фосфат кальция), смазки (например, стеарат магния, тальк или диоксид кремния), дезинтегранты (например, картофельный крахмал или натрия гликолят крахмал) или смачивающие вещества (например, лаурилсульфат натрия). Таблетки могут быть покрыты способом, хорошо известным в данной области.
Препарат HSP/α2М для перорального введения может быть приготовлен таким образом, чтобы обеспечить контролируемое высвобождение активного соединения.
Для щечного введения препарат может быть в виде таблеток или лепешек, приготовленных общепринятым способом.
Препарат можно готовить для парентерального введения посредством инъекции, например инъекции ударной дозы вещества или непрерывного вливания. Препараты для инъекции могут представлять собой единичную дозированную форму, например, в ампулах или в мультидозовых контейнерах, с добавленным консервантом. Препарат может быть в таких формах, как суспензии, растворы или эмульсии в маслянистом или водном наполнителе, и может содержать фармацевтические средства, такие как суспендирующие, стабилизирующие и/или диспергирующие вещества. Альтернативно активный ингредиент может быть в виде порошка для составления перед применением с подходящим наполнителем, например стерильной апирогенной водой.
Препарат может быть приготовлен в виде ректального препарата, такого как суппозитории или удерживающая клизма, например, содержащие суппозиторные основы, такие как масло какао или другие глицериды.
Помимо описанных выше составов, препарат также может быть приготовлен в виде препарата замедленного всасывания. Такие длительно действующие препараты можно вводить имплантацией (например, подкожно или внутримышечно) или посредством внутримышечной инъекции. Таким образом, например, препарат может быть приготовлен с подходящими полимерными или гидрофобными материалами (например, в виде эмульсии в подходящем масле) или с ионообменными смолами, или в виде постепенно растворимых производных, например, в виде постепенно растворимой соли. Липосомы и эмульсии являются хорошо известными примерами наполнителей или носителей для гидрофильных лекарственных средств.
Для введения с помощью ингаляции препарат для применения в соответствии с данным изобретением обычно выпускают в форме подачи аэрозольного спрея из герметизированных упаковок или распылителя с применением метательного вещества, например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа. В случае поддерживающего повышенное давление аэрозоля дозировку можно устанавливать с помощью вентиля, чтобы поставить назначенное количество. Капсулы и картриджи, например, из желатина для применения в ингаляторе или инсуффляторе могут быть приготовлены с содержанием порошкообразной смеси соединения и подходящей порошковой основы, такой как лактоза или крахмал.
Препарат, если требуется, может находиться в упаковке или распределительном устройстве, которое может содержать одну или более единичных дозированных форм, содержащих препарат HSP или препарат α2М. Упаковка, например, может содержать металлическую или пластиковую пленку, такую как блистер-упаковку. Упаковка или распределительное устройство могут сопровождаться инструкциями для введения.
Соответствующие или рекомендуемые дозы, составы и способы введения лечебных препаратов, таких как химиотерапевтические средства, лучевая терапия и биологические/иммунотерапевтические средства, такие как цитокины, известны в данной области и описаны в такой литературе, как Physician's Desk Reference (56th ed., 2002). В особых аспектах данное изобретение включает введение противоракового средства, такого как любое из средств, описанных ниже в таблице 2, предпочтительно для лечения злокачественных опухолей молочной железы, яичников, меланомы, рака простаты, прямой кишки или легкого, CML или сарком мягких тканей, включая, но не ограничиваясь указанным, желудочно-кишечные стромальные опухоли, которые описаны ниже в разделе 5.11.
Так как в некоторых аспектах способы изобретения включают применение субоптимальных количеств лечебного воздействия, полагают, что дозировки каждого лечебного воздействия могут быть меньше, чем дозировки, используемые при стандартной терапии или известные в данной области.
В одном аспекте Gleevec™ вводят от 50 мг до 100 мг, от 100 мг до 200 мг, от 200 мг до 300 мг, от 300 мг до 400 мг, от 400 мг до 500 мг, от 500 мг до 600 мг, от 600 мг до 700 мг, от 700 мг до 800 мг, от 800 мг до 900 мг или от 900 мг до 1000 мг ежедневно. В некоторых аспектах общую ежедневную дозу вводят субъекту в виде двух ежедневных доз от 25 мг до 50 мг, от 50 мг до 100 мг, от 100 мг до 200 мг, от 200 мг до 300 мг, от 300 мг до 400 мг или от 400 мг до 500 мг. Gleevec™ вводят перорально в дозах от 100 мг до 1000 мг, предпочтительно от 200 мг до 900 мг, более предпочтительно от 300 мг до 800 мг, наиболее предпочтительно от 400 мг до 600 мг. В специальном аспекте Gleevec™ вводят перорально в субоптимальной ежедневной дозе. В предпочтительных аспектах субоптимальная ежедневная дозировка перорально вводимого Gleevec™ составляет приблизительно от 10 мг до 600 мг, приблизительно от 50 мг до 400 мг, приблизительно от 100 мг до 300 мг или приблизительно 200 мг. В других аспектах Gleevec™ вводят перорально каждый второй день, каждый третий день, каждый четвертый день, каждый пятый день, каждый шестой день или один раз в неделю в дозе от 100 мг до 800 мг, от 200 мг до 600 мг, от 300 мг до 500 мг или 400 мг.




5.8 ЛЕЧЕНИЕ И ПРЕДУПРЕЖДЕНИЕ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ
Инфекционные заболевания, которые можно лечить, используя способы данного изобретения, вызываются инфекционными агентами, включающими, но не ограничиваясь перечисленным, вирусы, бактерии, грибки, простейшие и паразитов.
Возбудители инфекционных заболеваний, которые можно лечить в соответствии с изобретением, включают, но не ограничиваясь ими, вирусы, бактерии, грибы и возбудителей протозойного заболевания.
Вирусные заболевания, которые можно лечить или предупреждать, используя способы данного изобретения, включают, но не ограничиваясь ими, заболевания, вызванные вирусом гепатита типа А, гепатита типа В, гепатита типа С, вирусом гриппа, ветряной оспы, аденовирусом, вирусом герпеса тип I (HSV-I), герпеса тип II (HSV-II), вирусом rinderpest, риновирусом, Echo-вирусом, ротавирусом, респираторно-синцитиальным вирусом, вирусом папилломы, папова-вирусом, цитомегаловирусом, эхиновирусом, арбовирусом, гунтаривирусом, вирусом Коксаки, вирусом паротита, вирусом кори, вирусом краснухи, полио-вирусом, малым поксвирусом, вирусом Эпштейна-Барра, вирусом иммунодефицита человека тип I (HIV-I), вирусом иммунодефицита человека тип II (HIV-II) и возбудителями вирусных заболеваний, таких как менингит, энцефалит, лихорадка денге и ветряная оспа.
Бактериальные заболевания, которые можно лечить или предупреждать с использованием способов данного изобретения, вызываются бактериями, включающими, но не ограничиваясь ими, микобактерии, риккеттсии, микоплазму, нейссерии, S. pneumonia, Borrelia burgdorferi (болезнь Лайма), Bacillus antracis (сибирская язва), tetanus, streptococcus, staphylococcus, mycobacterum, tetanus, pertissus, cholera, plague, diptheria, chlamydia, S. aureus и legionella.
Протозойные заболевания, которые можно лечить или предупреждать применением иммунореактивного реагента вместе со способами данного изобретения, вызываются простейшими, включающими, но не ограничиваясь ими, лейшмании, кокзидиоа, трипаносомы или возбудителя малярии.
Паразитарные заболевания, которые можно лечить или предупреждать с применением способов данного изобретения, вызываются паразитами, включающими, но не ограничиваясь ими, хламидии и риккеттсии.
5.9 ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ
Целый ряд невакцинных злокачественных лечебных воздействий в настоящее время проходят клинические испытания и хорошо известны в данной области. Препарат HSP/α2М можно использовать вместе с такими невакцинными злокачественными лечебными воздействиями для лечения и профилактики соответствующих типов злокачественных заболеваний. Специалист в данной области сможет определить экспериментальные и стандартные противораковые терапии и курс лечения, которые следует использовать в соответствии со способами данного изобретения.
Злокачественные заболевания, которые можно лечить, используя способы данного изобретения включают, но не ограничиваясь ими, саркомы человека и карциномы, например фибросаркому, мукосаркому, липосаркому, хондросаркому, остеогенную саркому, хондрому, ангиосаркому, эндотелиосаркому, лимфоангиосаркому, лимфангиоэндотелиосаркому, синовиому, мезотелиому, опухоль Юинга, лейомиосаркому, рабдомиосаркому, карциному прямой кишки, рак поджелудочной железы, рак молочной железы, рак яичников, рак простаты, плоскоклеточную карциному, базально-клеточный рак, аденокарциному, карциному потовых желез, карциному сальных желез, папиллокарциному, аденокарциному, цистаденокарциному, карциному мозга, бронхогенный рак, рак почки, гепатому, карциному желчного протока, хориокарциному, семиному, эмбриональную карциному, опухоль Вильма, рак шейки матки, опухоль яичка, карциному легкого, мелкоклеточный рак легкого, карциному мочевого пузыря, эпительальную карциному, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, акустическую невриному, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому, лейкозы, острый лимфолейкоз, острый миелолейкоз, миелобластный лейкоз, промиелолейкоз, миеломоноцитарный лейкоз, моноцитарный лейкоз, эритролейкоз, хронический лейкоз, хронический миелоидный лейкоз, хронический миелогенный лейкоз, хронический миелоцитарный лейкоз, хронический гранулоцитарный лейкоз, хронический лимфолейкоз, полицитемию истинную, лимфому, лимофогранулематоз Ходжкина, лимофогранулематоз не-Ходжкина, множественную миелому, болезнь Вальденстрема, болезнь тяжелой цепи, саркомы мягких тканей, желудочно-кишечные стромальные опухоли и глиобастомы.
6. ПРИМЕРЫ: ОПУХОЛИ, НЕЧУВСТВИТЕЛЬНЫЕ К ХИМИОТЕРАПИИ/ЛЕЧЕНИЮ ЦИТОКИНОМ, ОТВЕЧАЮТ ПОСЛЕ ВВЕДЕНИЯ КОМПЛЕКСА HSP-ПЕПТИД
Мыши, имеющие опухоли, такие как LLC (D122) и B16, не отвечали на лечение циклофосфамидом (Cy) в сочетании с интерлейкином-12 (IL-12). В эксперименте с двойным имплантатом мышам инъецировали MCA207 (опухоли, которые, как известно, отвечают на лечение Cy IL-12) и D122 на двух противоположных сторонах и опухоли оставляли расти до значительного размера (10×10 мм), затем мышей лечили Cy+IL-12. Большие опухоли MCA207 быстро регрессировали, тогда как опухоли D122 продолжали расти на противоположной стороне того же самого животного. Результаты продемонстрировали, что определенные опухоли, например D122, не отвечали на лечение Cy+IL-12, даже если наблюдали сильный ответ против другой опухоли у того же самого животного.
Оказалось, что опухоли, которые отвечали на лечение, являются иммуногенными, тогда как другие опухоли, которые не отвечали, все характеризовались низкой иммуногенностью. Чтобы исследовать, приведет ли происходящее от хозяина иммунное узнавание опухоли в формах Т-клеточного примирования до лечения Cy+IL-12 к опухолевому ответу на лечение, проводили следующие эксперименты. Следующие результаты продемонстрировали, что, если мышь, несущая опухоль D122, которая не отвечает на лечение только Cy+IL-12, получала иммунологическую память опухоли, отторжение опухоли происходило у мыши после лечения Cy+IL-12.
Комплексы белок теплового шока - пептид - использовали для выявления ясного ответа Т-клеток, который вовлекает Т-клетки как CD4+, так и CD8+у мышей.
6.1 МАТЕРИАЛЫ И СПОСОБЫ
Нативных мышей или не иммунизировали или иммунизировали один раз в 0-день 5 мкг и 20 мкг комплексами gp96-пептид, происходящими из D122, вводимыми подкожно, или 2 мкг комплексами gp96-пептид, происходящими из D122, вводимыми внутрикожно. В качестве негативного контроля другую группу мышей иммунизировали комплексами gp96-пептид, происходящими из печени. Комплексы gp96-пептид, происходящие из D122, представляли собой комплексы HSP-пептид, эндогенные в отношении клеток опухоли D122 и выделенные из клеток опухоли D122. Комплексы gp96-пептид, происходящие из печени, представляют собой комплексы HSP-пептид, эндогенные относительно клеток печени и выделенные из клеток печени. Через две недели после иммунизации (14 дней) мышам проводили контрольное заражение подкожно 200000 клеток D122. Иммунизация была субоптимальной относительно опухолевого отторжения в соответствии с предварительным экспериментом и опухоли D122 росли у всех мышей. Когда размер опухолей достигал 10 мм или больше в диаметре (32-34 день), мышей лечили Cy+IL-12 (Cy, 3 мг интрапарентеральным введением; IL-12, 200 нг, интрапарентеральным введением в течение 5 дней).
6.2 РЕЗУЛЬТАТЫ
(# общая)
Как суммировано в таблице выше, при антиген-специфической иммунологической стимуляции аутогенными комплексами gp96-пептид, происходящими из опухоли, нечувствительная опухоль D122 становилась респондером на лечение Cy+IL-12. В группах, не иммунизированных и иммунизированных комплексами gp96-пептид, происходящими из печени, только у мышей, несущих наименьшие опухоли (менее 10-12 мм в диаметре) происходила регрессия опухолей после лечения Cy+IL-12. В противоположность этому у мышей, которых иммунизировали комплексами gp96-пептид, происходящими из D122, большие опухоли D122, такие как опухоли 22 мм в диаметре, которые обычно резистентны к любому виду иммунотерапевтических подходов, отвечали, полностью регрессировали после лечения Cy+IL-12. Кроме того, иммуногистохимический анализ целого ряда опухолевых образцов, собранных у каждой группы, показал 1) отсутствие какого-либо признака Т-клеточной инфильтрации в опухолях, удаленных у мышей, которые не были иммунизированы или были иммунизированы комплексами gp96-пептид, происходящими из печени, до или после лечения Cy+IL-12; 2) в противоположность этому некоторую Т-клеточную инфильтрацию (как CD4+, так и CD8+) наблюдали в опухолях, полученных от мышей, иммунизированных комплексами gp96-пептид, происходящими из D122, через 12 дней, но не 6 дней после того, как начали лечение Cy+IL-12.
7. ПРИМЕР: ПОЛНАЯ ЭЛИМИНАЦИЯ ЛЕЙКОЗНЫХ КЛЕТОК У ПАЦИЕНТОВ В ХРОНИЧЕСКОЙ ФАЗЕ CML ПОСЛЕ ВВЕДЕНИЯ КОМБИНАЦИИ GLEEVECТМ И КОМПЛЕКСА HSP/α2М
Чтобы исследовать возможность иммунизации аутогенными комплексами hsp7-пептид, происходящими из опухоли, чтобы лечить пациентов в хронической фазе CML, использовали следующий протокол (см. чертеж). Клинический протокол, суммированный на чертеже, включает все физические показатели, обследование крови, рентгеновское исследование и исследование костного мозга, которое проводили до, во время и после вакцинации препаратом HSP. До включения в исследование диагноз пациента CML подтверждали молекулярным типированием bcr/abl периферической крови или костного мозга, полученных от субъекта, используя полимеразно-цепную реакцию (ПЦР), чтобы установить присутствие или отсутствие химерных белков или транскриптов bcr/abl.
7.1 МАТЕРИАЛЫ И СПОСОБЫ
Участвующие субъекты удовлетворяли следующим критериям: субъект показывал коэффициент Западной кооперированной онкологической научно-исследовательской группы (Eastern Cooperative Oncology Group (ECOG)) менее 2; возраст субъекта составлял, по крайней мере, 18 лет и субъект был способен уведомить о согласии; менее одного года прошло с тех пор, как поставлен первоначальный диагноз хромосома-Philadelphia-позитивный CML в хронической фазе; у субъекта нет цитогенетической ремиссии; субъекту не производили трансплантацию костного мозга или стволовых клеток в пределах около шести месяцев, пока такую терапию не счел необходимой лечащий врач вследствие развития заболевания; субъекту позволили продолжить сопутствующее стандартное лечение гидроксимочевиной, Ara-c/день в течение 10 дней или Gleevec™ (иматиниба мезилат); у субъекта отсутствовало любое серьезное заболевание, такое, что состояние здоровья может подвергнуться опасности в результате участия в исследовании; у субъекта установлена адекватная почечная функция, которую оценивали по уровням сывороточного креатинина менее 2,0 и адекватная функция печени, которую оценивали по билирубину и трансаминазе менее чем в 2,0 раза выше верхней нормальной границы; субъект не получал кортикостероидной терапии или другого иммуносупрессивного медикаментозного лечения; и субъект не проявлял отсутствия толерантности, что продемонстривано адекватным ответом гиперчувствительности замедленного типа (DHT), по крайней мере, на 1 из 3 антигенов при кожном тестировании с Candida, эпидемическим паротитом и PPD, то есть затвердение было больше 0,5 см через 48 часов после размещения.
Субъектов исключали, если субъект показывал коэффициент ECOG ≥2; у субъекта прошло более 3 лет от установления первоначального диагноза хромосома-Philadelphia-позитивный лейкоз в хронической фазе; субъект был на лечении IFN; у субъекта имелась значительная анемия, то есть гемоглобин был менее 10 г/дл, или тромбоцитопения, то есть количество тромбоцитов составляло менее 20000/мкл, что требовало переливания крови; у субъекта обнаружено количество периферических бластных клеток свыше 10%; у субъекта оказался позитивным тест мочи и крови на беременность; у субъекта установлена нарушенная функция почек, то есть сывороточный креатинин выше или равен 2,0, или нарушенная функция печени, то есть билирубин или трансаминаза более чем в 2,0 раза выше верхнего нормального предела; у субъекта имелась значительная активная инфекция, требующая госпитализации в период вербовки; у субъекта наблюдали значительные поведенческие или психологические проблемы, которые препятствовали адекватному последующему наблюдению.
Субъект прерывал исследование по любой из следующих причин: субъект просил отвод по какой-либо причине; доказанный эффективный терапевтический подход становился доступным и оказывался предпочтительным для субъекта (например, одобрение другой исследовательской лекарственной терапии официальным агентством, идентификация идентичного лейкоцитарного антигена человека (HLA) совместимого донора), субъект лишился врачебного наблюдения; у субъекта наблюдали четкое доказательство усиления заболевания несмотря на сопутствующую терапию, что подтверждалось следующими признаками и симптомами: периферические бластные клетки 10% или более, периферическая бластная клетка плюс промиелоциты 30% или более; периферические базофилы 20% или более; тромбоцитопения менее 100000/мм3, не регулируемая терапией; нейтропения менее 1000/мм3, не регулируемая терапией, бластные клетки костного мозга 10% или более; значительный фиброз костного мозга; прогрессирующая спленомегалия, нечувствительная к терапии; триада WBC выше 50000/мм3, гематокрит менее 25% и тромбоцитов менее 100000/мм3, не регулируемые терапией; стойкая необъяснимая лихорадка; и цитогенетическая клональная эволюция; экстрамедуллярное заболевание с локализованными незрелыми бластными клетками, такое как хлорома; любые другие причины, которые, по мнению исследователя, должны защитить интересы субъекта.
До введения их первого препарата HSP субъекты получали лечение Gleevec™ (400-800 мг ежедневно в виде капсул, 400-600 ежедневные дозы вводили один раз в день или 800 мг в двух ежедневных дозах по 400 мг каждая) в течение 2 дней, 5 месяцев, 9 месяцев, 10 месяцев и 1 года соответственно. Субъектам, удовлетворяющим приведенным выше критериям, позволяли продолжать лечение Gleevec™ на протяжении всего исследования. Субъектам впоследствии проводили аферез, используя периферическую вену, доступную для сбора периферических мононуклеарных клеток. Большинство образцов использовали для очистки комплексов hsp70-пептид. Затем аутогенные комплексы hsp70-пептид очищали, используя протокол с АДФ-агарозой, по существу, как описано в разделе 5.3.1 выше. Небольшую фракцию собранного материала использовали как мишени для анализа CTL. Субъектам производили внутрикожную инъекцию 50 мг комплексов hsp70-пептид в кожу предплечья еженедельно в течение периода двух месяцев всего из 8 инъекций помимо лечения Gleevec™ (400-800 мг ежедневно в капсульной форме, 400-600 мг ежедневная доза, вводимая один раз в день, 800 мг дозы, вводимые дважды в день). Образцы крови брали три раза, чтобы оценить статус иммунной системы. Кровь брали до вакцинации, во время вакцинации и через 1-2 недели после 8-й вакцинации (см. чертеж). В конце лечения всем субъектам проводили полное гематологическое и цитогенетическое определение стадии заболевания по костному мозгу (см. Silver et al., 1999, Blood, 94(5):1517-1536).
Кроме того, чтобы сделать вывод о выполнимости исследования и токсических данных, оценивали формирование противоопухолевого иммунитета по способам, известным в данной области, таким как: (1) увеличение в периферической крови IFN-g-продуцирующих Т-лимфоцитов CD8+, которые реагируют с аутогенными bcr/abl-позитивными периферическими мононуклеарными клетками (см. например, Janetzki et al., 2000, Int. J. Cancer 88:232-238); (2) увеличение PR-1-специфических CTL по тетрамерным способам PR1-HLA-A2 у пациентов, которые оказались HLA-A2-позитивными (см., например, Clark et al., 2001, Blood 98(10): 2887-2893 и Molldrem et al., 1999, Cancer Research 59: 2675-2681); (3) изменение иммунофенотипа периферических лимфоцитов (см., например, Akel et al., 2002, Clin. Lab. Haem. 24: 362-367); и (4) цитогенетическая ремиссия хромосомы Philadelphia из костного мозга (см., например, Wang et al., 2002, British J. Haematology 118: 771-777).
Комбинированное лечение у пяти оцениваемых субъектов приводило к полной элиминации лейкозных клеток, что определяли по анализу ОФ-ПЦР, определяющему присутствие или отсутствие транскриптов bcr/abl в периферической крови или костном мозге, взятых от леченных пациентов (см., например, Merx et al., 2002, Leukemia 16: 1579-1583; Wang et al., 2002, British Journal of Haematology 118: 771-777; и Stentoft et al., 2001, Eur. J. Haemotol. 67: 302-308); цитогенетическому ответу, один из критериев, использованных при одобрении Gleevec™ (см. Silver et al., 1999, Blood 94(5): 1517-1536); или по комбинации ОФ-ПЦР и цитогенетическому ответу. На основании предыдущих сообщений менее 10 процентов пациентов, подвергнутых лечению одним Gleevec™, достигали ответов, по тем же приведенным выше критериям. См. Druker et al., 2002, Hematology (Am. Soc. Hematol. Educ. Program): 111-135, at 114-115.
Все ссылки, цитируемые в описании, включены в данное описание посредством ссылки во всей своей полноте и для всех целей в одинаковой степени, как если бы каждая индивидуальная публикация или патент, или заявка на патент специально и индивидуально свидетельствовали о необходимости быть включенными в описание посредством ссылки во всей своей полноте для всех целей.
Множество модификаций и изменений данного изобретения может быть осуществлено без отступления от сущности и объема, что очевидно специалистам в данной области. Специальные аспекты, описанные в изобретении, представлены только в качестве примеров и изобретение не ограничено с точки зрения прилагаемой формулы изобретения наряду с полным объемом эквивалентов, к которым такая формула изобретения имеет отношение.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ БЕЛКОВ ТЕПЛОВОГО ШОКА ДЛЯ УЛУЧШЕНИЯ ТЕРАПЕВТИЧЕСКОГО ЭФФЕКТА НЕВАКЦИОННОГО ЛЕЧЕБНОГО ВОЗДЕЙСТВИЯ | 2009 |
|
RU2573380C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ, ВКЛЮЧАЮЩИХ ХИТШОКОВЫЕ БЕЛКИ ИЛИ АЛЬФА-2-МАКРОГЛОБУЛИН, ПРИГОДНЫХ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ И ИНФЕКЦИОННОГО ЗАБОЛЕВАНИЯ | 2002 |
|
RU2335295C2 |
| ИСПОЛЬЗОВАНИЕ ЛЕКТИНОВ ДЛЯ АКТИВАЦИИ ОЛИГОМЕРИЗАЦИИ ГЛИКОПРОТЕИДОВ И АНТИГЕННЫХ МОЛЕКУЛ | 2004 |
|
RU2399381C2 |
| ИСПОЛЬЗОВАНИЕ БЕЛКОВ ТЕПЛОВОГО ШОКА ДЛЯ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ТЕРАПИЙ АНТИТЕЛАМИ | 2003 |
|
RU2375077C2 |
| ВАКЦИННЫЕ КОМПОЗИЦИИ, СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ МЕЛАНОМЫ И ГЕНЕТИЧЕСКИЕ КОНСТРУКЦИИ ДЛЯ ПОЛУЧЕНИЯ ДЕЙСТВУЮЩИХ КОМПОНЕНТОВ КОМПОЗИЦИИ | 2006 |
|
RU2333767C2 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2008 |
|
RU2379055C1 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК, ОБЕСПЕЧИВАЮЩАЯ СИНТЕЗ ГИБРИДНОГО БЕЛКА, СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2316342C1 |
| БЕЛКОВОПЕПТИДНЫЙ ПРОТИВООПУХОЛЕВЫЙ КОМПОЗИТ, КЛЕТОЧНЫЙ ПРЕПАРАТ, АКТИВИРОВАННЫЙ ЭТИМ КОМПОЗИТОМ, И СПОСОБ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2004 |
|
RU2283129C1 |
| СПОСОБ ТЕРАПИИ ОПУХОЛЕВЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2597414C2 |
| ЛЕЧЕНИЕ ИНФЕКЦИИ, ВЫЗЫВАЕМОЙ ВИРУСОМ ПАПИЛЛОМЫ ЧЕЛОВЕКА | 2001 |
|
RU2282461C2 |
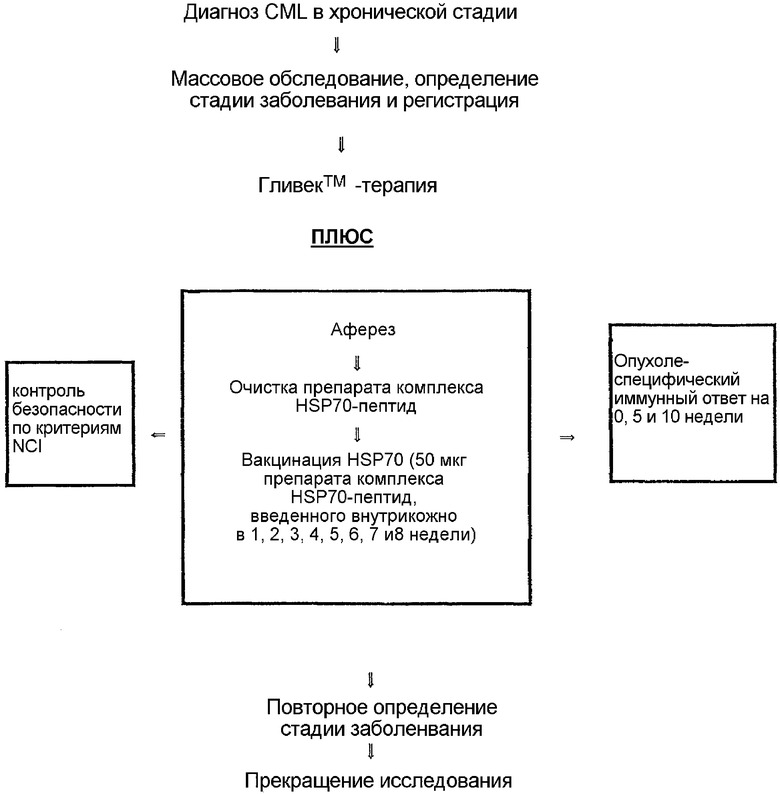
Группа изобретений относится к медицине, а именно к онкологии, и может быть использована для лечения злокачественных опухолей. Варианты способа по изобретению включают введение комплекса белок теплового шока-антигенный пептид опухоли и ингибитора тирозинкиназы или ретиноида. Набор по изобретению включает контейнер с комплексом белок теплового шока-антигенный пептид опухоли и контейнер с ингибитором тирозинкиназы или ретиноидом. Изобретение позволяет усилить иммунный ответ на опухоль, уменьшить ее массу за счет синергического эффекта комплексов белок теплового шока-антигенный пептид опухоли и ингибитора тирозинкиназы или ретиноида. 2 н. и 52 з.п. ф-лы, 2 табл., 1 ил.
1. Способ лечения злокачественной опухоли у субъекта, предусматривающий: (а) назначение субъекту, по крайней мере, одного лечебного воздействия, причем указанное, по крайней мере, одно лечебное воздействие включает (i) ингибитор тирозинкиназы, или (ii) ретиноид; и (b) введение препарата очищенного белка теплового шока, содержащего комплекс белок теплового шока-пептид, содержащий белок теплового шока, ковалентно или нековалентно присоединенный к антигенному пептиду, где указанный антигенный пептид проявляет антигенность антигена указанной злокачественной опухоли.
2. Способ по п.1, при котором злокачественная опухоль представляет собой хронический миелоидный лейкоз.
3. Способ по п.2, при котором злокачественная опухоль находится в хронической фазе.
4. Способ по п.1, при котором злокачественная опухоль представляет собой саркому мягкой ткани.
5. Способ по п.1, при котором злокачественная опухоль представляет собой желудочно-кишечную стромальную опухоль, экспрессирующую рецептор тирозинкиназы c-kit.
6. Способ по п.1, при котором указанное, по крайней мере, одно лечебное воздействие содержит ингибитор тирозинкиназы.
7. Способ по п.6, при котором ингибитор тирозинкиназы представляет собой тирфостин.
8. Способ по п.6, при котором ингибитор тирозинкиназы выбран из группы, состоящей из иматиниба мезилата, гербимицина А, генистейна, эрбстатина, SU 11248 и лавендустина А.
9. Способ по п.6, при котором ингибитор тирозинкиназы представляет собой иматиниба мезилат.
10. Способ по любому из пп.1-9, при котором субъект ранее проявлял нечувствительность к лечению, по крайней мере, одним лечебным воздействием в отсутствии препарата очищенного белка теплового шока.
11. Способ по любому из пп.1-9, при котором препарат очищенного белка теплового шока содержит комплексы белок теплового шока-пептид, которые содержат один или несколько из hsp60, hsp70, hsp90, hsp110, gp96, grp170 или калретикулина.
12. Способ по любому из пп.1-9, при котором препарат очищенного белка теплового шока содержит комплексы hsp70-пептид.
13. Способ по любому из пп.1-9, при котором препарат очищенного белка теплового шока является аутогенным субъекту.
14. Способ по любому из пп.1-9, при котором субъектом является человек.
15. Способ по любому из пп.1-9, при котором указанное, по крайней мере, одно, лечебное воздействие назначают до первоначального введения препарата очищенного белка теплового шока.
16. Способ по любому из пп.1-9, при котором указанное, по крайней мере, одно, лечебное воздействие назначают одновременно с введением препарата очищенного белка теплового шока.
17. Способ по любому из пп.1-9, при котором указанное, по крайней мере, одно, лечебное воздействие назначают после первоначального введения препарата очищенного белка теплового шока.
18. Способ по п.2, при котором указанное, по крайней мере, одно лечебное воздействие включает ингибитор тирозинкиназы и при котором указанный ингибитор тирозинкиназы представляет собой иматиниба мезилат.
19. Способ по п.18, при котором субъектом является человек.
20. Способ по п.18 или 19, при котором указанный иматиниба мезилат вводят ежедневно в дозе от 200 мг до 800 мг.
21. Способ по п.18, при котором препарат очищенного белка теплового шока содержит комплексы белок теплового шока-пептид, которые содержат один или несколько из hsp60, hsp70, hsp90, hsp110, gp96, grp170 или калретикулина.
22. Способ по п.18, при котором препарат очищенного белка теплового шока содержит комплексы белок теплового шока-пептид, которые содержат hsp70.
23. Способ по п.18, при котором указанный иматиниба мезилат вводят до первоначального введения субъекту препарата очищенного белка теплового шока.
24. Способ по п.18, при котором указанный иматиниба мезилат вводят одновременно с указанным введением препарата очищенного белка теплового шока.
25. Способ по п.18, при котором указанный иматиниба мезилат вводят после первоначального введения субъекту препарата очищенного белка теплового шока.
26. Способ по п.18 или 19, при котором указанный препарат очищенного белка теплового шока является аутогенным субъекту.
27. Способ по п.1, при котором указанное, по крайней мере, одно лечебное воздействие содержит ретиноид.
28. Способ по п.27, при котором ретиноид представляет собой ретиноевую кислоту в трансположении.
29. Способ по пп.1, 6, 27 или 28, при котором указанная злокачественная опухоль представляет собой саркому, карциному, фибросаркому, миксосаркому, липосаркому, хондросаркому, остеогенную саркому, хордому, ангиосаркому, эндотелиосаркому, лимфоангиосаркому, лимфангиоэндотелиосаркому, синовиому, мезотелиому, опухоль Юинга, лейомиосаркому, рабдомиосаркому, карциному прямой кишки, рак поджелудочной железы, рак молочной железы, рак яичников, рак простаты, плоскоклеточную карциному, базально-клеточный рак, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярные аденокарциномы, цистаденокарциному, медуллярный рак, бронхогенный рак, рак почки, гепатому, карциному желчного протока, хориокарциному, семиному, эмбриональную карциному, опухоль Вильма, рак шейки матки, опухоль яичка, карциному легкого, мелкоклеточный рак легкого, карциному мочевого пузыря, эпителиальную карциному, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, акустическую неврому, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому, лейкозы, острый лимфолейкоз, острый миелолейкоз, миелобластный лейкоз, промиелолейкоз, миеломоноцитарный лейкоз, моноцитарный лейкоз, эритролейкоз, хронический лейкоз, хронический миелоидный лейкоз, хронический миелогенный лейкоз, хронический миелоцитарный лейкоз, хронический гранулоцитарный лейкоз, хронический лимфолейкоз, полицитемию истинную, лимфому, лимофогранулематоз Ходжкина, лимофогранулематоз не-Ходжкина, множественную миелому, болезнь Вальденстрема, болезнь тяжелой цепи, саркомы мягких тканей, желудочно-кишечные стромальные опухоли и глиобластому.
30. Способ по п.27 или 28, при котором злокачественная опухоль представляет собой рак почки.
31. Способ по п.27 или 28, при котором злокачественная опухоль представляет собой меланому.
32. Способ по п.27, при котором ретиноид представляет собой производное витамина А.
33. Способ по п.27, при котором ретиноид выбран из группы, состоящей из цисретиноевой кислоты или ретиноевой кислоты в трансположении.
34. Способ по п.27, при котором субъект ранее проявлял нечувствительность к лечению указанным ретиноидом в отсутствии препарата очищенного белка теплового шока.
35. Способ по п.27 или 28, при котором препарат очищенного белка теплового шока содержит комплексы белок теплового шока-пептид, которые содержат один или несколько из hsp60, hsp70, hsp90, hsp110, gp96, grp170 или калретикулина.
36. Способ по п.27 или 28, при котором препарат очищенного белка теплового шока содержит комплексы белок теплового шока-пептид, которые содержат hsp70.
37. Способ по п.27 или 28, при котором препарат очищенного белка теплового шока содержит комплексы белок теплового шока-пептид, которые содержат gp96.
38. Способ по п.27 или 28, при котором препарат очищенного белка теплового шока является аутогенным субъекту.
39. Способ по п.27 или 28, при котором субъектом является человек.
40. Способ по п.27 или 28, при котором указанное, по крайней мере, одно лечебное воздействие назначают до первоначального введения препарата очищенного белка теплового шока.
41. Способ по п.27 или 28, при котором указанное, по крайней мере, одно лечебное воздействие назначают одновременно с введением препарата очищенного белка теплового шока.
42. Способ по п.27 или 28, при котором указанное, по крайней мере, одно лечебное воздействие назначают после первоначального введения препарата очищенного белка теплового шока.
43. Способ по п.28, при котором ретиноевая кислота в трансположении представляет собой ATRA-IV.
44. Способ по п.1, при котором препарат очищенного белка теплового шока содержит комплексы белок теплового шока-пептид, содержащие белки теплового шока, нековалентно присоединенные к антигенным пептидам.
45. Способ по п.1, при котором препарат очищенного белка теплового шока содержит комплексы белок теплового шока-пептид, выделенные из клеток указанной злокачественной опухоли.
46. Способ по п.1, при котором указанный антигенный пептид проявляет антигенность опухолеспецифического антигена или опухолеассоциированного антигена указанной злокачественной опухоли у указанного субъекта.
47. Набор, содержащий первый контейнер, включающий препарат очищенного белка теплового шока, содержащий комплекс белок теплового шока-пептид, содержащий белок теплового шока, ковалентно или нековалентно присоединенный к антигенному пептиду, где указанный антигенный пептид проявляет антигенность антигена указанной злокачественной опухоли, и второй контейнер, включающий (i) ингибитор тирозинкиназы или (ii) ретиноид.
48. Набор по п.47, в котором указанный второй контейнер включает ингибитор тирозинкиназы.
49. Набор по п.48, в котором указанный ингибитор тирозинкиназы представляет собой иматиниба мезилат.
50. Набор по п.47, в котором указанный второй контейнер включает ретиноид.
51. Набор по п.50, в котором указанный ретиноид представляет собой ретиноевую кислоту в трансположении.
52. Набор по п.51, в котором ретиноевая кислота в трансположении представляет собой ATRA-IV.
53. Набор по любому из пп.47-52, в котором указанный препарат очищенного белка теплового шока содержит комплексы hsp70-пептид.
54. Набор по любому из пп.47-52, в котором указанный препарат очищенного белка теплового шока содержит комплексы gp96-пептид.
| US 5837251, 17.11.1998 | |||
| ВАКЦИНА ДЛЯ СТИМУЛЯЦИИ ПРОТИВООПУХОЛЕВОГО ИММУНИТЕТА | 2000 |
|
RU2192884C2 |
| US 6136315, 24.10.2000, см | |||
| примеры | |||
| ДЕВИТ В.Т | |||
| и др | |||
| Биологические методы лечения онкологических заболеваний | |||
| - М.: Медицина, 2002, с.690 | |||
| DRUKER B.J | |||
| et al | |||
| Activity of a specific inhibitor of the DCR-ABL tyrosine kinase in the blast crisis of chronic myeloid leukemia and acute lymphoblastic | |||
Авторы
Даты
2009-12-20—Публикация
2003-04-25—Подача