Изобретение относится к новым биологически активным химическим соединениям, обладающим противовирусной активностью, может применяться в медицине для лечения и профилактики заболеваний, вызываемых патогенными для человека и животных вирусами, в частности ортопоксвирусами.
Наиболее опасными для человеческой популяции из-за чрезвычайно высокой патогенности, многообразия и эпидемиологических показателей являются вирусы группы оспы. В последние годы неожиданную остроту и актуальность приобрела проблема человеческой оспы, поскольку вакцинация населения с 1980 г. не проводится, появилась значительная часть населения без иммунитета или с ослабленным иммунитетом и отсутствуют гарантии полного исчезновения возбуждающих это заболевание вирусов, а также несанкционированной утечки вирусного материала из мест его официального хранения. Более того, в условиях постоянного роста категорий населения с иммунодефицитными состояниями сама идея вакцинации живым вирусом осповакцины становится проблематичной, и важное значение приобретает задача успешного купирования поствакцинальных осложнений, а также вспышек заболеваний вызванных ортопоксвирусами с помощью высокоэффективных химиотерапевтических препаратов. Кроме того, следует отметить и высокую патогенность вирусов оспы обезьян, коров, относящихся к тому же роду Orthopoxvirus, способных вызывать заболевание и у людей со смертельным исходом. Так, в последнее время в Африке, особенно в районах с высоким процентом ВИЧ-инфицированных, отмечаются вспышки оспы обезьян (летальность достигает 10-20%). Кроме того, существует реальная возможность генетической модификации вирусов оспы животных, что может привести к повышению их патогенности для человека.
Известно, что производные адамантана являются потенциальными источниками веществ с противовирусными свойствами. В частности, ингибиторы вируса осповакцины выявлены в ряду адамантоил-1-гидразинов (Гужова С.В., Даниленко Г.И., Коробченко Л.В., Денисова Л.В., Андреева О.Т., Бореко Е.И., Даниленко В.Ф., Баклан В.Ф. Ингибиторы вируса вакцины в ряду адамантоил-1-гидразинов // Физиол, Активн. В-ва. Киев: Наукова думка. 1986, вып.18. С.24). Изомерные 1-(аминобензоил)аминоадамантаны наряду с действием на различные типы вирусов проявляют умеренную активность в отношении вируса осповакцины (Вотяков В.И., Андреева О.Т., Кицара М.С. и др. // В сб.: Физиологически активные вещества. Киев. 1978. Вып.10. С.88). Опубликованы данные о выраженном ингибирующем действии на размножение вирусов осповакцины замещенных аминоацетиладамантиламинов, аминоалкоксиацетиладамантиламинов и тромантадина (May G., Peteri D. // Arzneimitt.- Forsch. 1973. Bd.23. N.5. S.718). Широкий ряд гидрокси-, азотсодержащих и серусодержащих функциональных производных адамантанового ряда проявил слабую и умеренную степень активности против вируса осповакцины (Климочкин Ю.Н., Леонова М.В., Коржев И.Р., Моисеев И.К., Владыко Г.В., Коробченко Л.В., Бореко Е.И., Николаева С.Н. // Хим.-фарм. журнал. 1992. №7-8. С.58; Климочкин Ю.Н., Моисеев И.К., Владыко Г.В., Коробченко Л.В., Бореко Е.И. // Хим.-фарм. журнал. 1991. Т.25. №7. С.46; Климочкин Ю.Н., Моисеев И.К., Абрамов О.В., Владыко Г.В., Коробченко Л.В., Бореко Е.И. // Хим.-фарм. ж. 1991. Т.25. №7. С.49).
Недостатком вышеперечисленных аналогов является невысокая активность соединений в отношении вируса осповакцины.
Среди производных адамантана известно биологически активное соединение 1-адамантаноилгидразон α-азидометил(1-адамантил)кетона (прототип), обладающее противовирусной активностью в отношении вируса осповакцины (А.с. 1568481 СССР, 1990). Однако указанное соединение не изучалось на предмет противовирусной активности в отношении вируса оспы коров, вируса оспы обезьян и вируса эктромелии. К недостаткам прототипа следует отнести также и недостаточно высокую эффективность в отношении вируса осповакцины.
Кроме того, в научно-технической и патентной литературе нет других сведений о производных адамантана, обладающих противовирусным действием в отношении широкого ряда ортопоксвирусов.
В настоящее время практически нет средств специфической профилактики и лечения заболеваний, вызываемых вирусами группы оспы, поэтому разработка высокоэффективных противовирусных препаратов, обладающих высокой активностью, низкой токсичностью и продолжительным действием в отношении ортопоксвирусов является важной задачей для обеспечения безопасности здоровья и жизни людей.
Технический результат предлагаемого изобретения - изыскание новых химических соединений с высоким индексом селективности в ряду азидокетонов алициклического и алифатического ряда, обладающих противовирусным действием, в отношении широкого ряда ортопоксвирусов, патогенных для человека и животных.
Технический результат достигается введением в молекулу исследуемого вещества азидокетонов алициклического и алифатического ряда.
Гидразоны азидокетонов общей формулы получают из α-азидометил-R1-кетонов и гидразидов R2-карбоновых кислот в присутствии ледяной уксусной кислоты.
Пример 1.
3-Гидрокси-1-адамантоилгидразон α-азидометил-(1-адамантил)кетона (соединение I)
В 50 мл абсолютного метанола последовательно растворяют α-азидометил-(1-адамантил)кетон (20 ммоль) и гидразид 3-гидрокси-1-адамантанкарбоновой кислоты (25 ммоль), добавляют 4-5 капель ледяной уксусной кислоты и выдерживают 35-40 ч при комнатной температуре. Выпавшие кристаллы отфильтровывают, промывают холодным метанолом, отфильтровывают и сушат. Выход 71%. Т.пл. 176°С (разл.).
ИК спектр, ν, см-1: 3250 (NH, ОН), 2900 (СН), 2100 (N3), 1650 (С=O), 1520 (NH), 1435 (СН).
Найдено, %: С 66,93; Н 8,31; N 16,86. C23H33N5O2. Вычислено, %: С 67,13; Н 8,08; N 17,02.
Масс-спектр (ЭИ): m/z 355 (100%) [М-СН2N3]+, 204 (9%), 176 (10%), 151 (39%), 135 (22%) [Ad]+.
Пример 2.
3-(4-Толил)-1-адамантоилгидразон α-азидометил(1-адамантил)-кетона (соединение II)
Получен аналогично из α-азидометил-(1-адамантил)-кетона и гидразида 3-(4-толил)-1-адамантанкарбоновой кислоты.
Выход 68%. Т. пл. 166-167°С (разл.).
ИК спектр, ν, см-1: 3300 (NH), 2900 (СН), 2050 (N3), 1680 (С=O), 1520 (N-H), 1450 (СН).
Найдено, %: С 73,89; Н 7.81; N 14,96. C30H39N5O. Вычислено, %: С 74,19; Н 8.09; N 14.42.
Масс-спектр (ЭИ): m/z 428 (100%) [М-CH2N3]+, 251 (18%), 225 (82%), 169 (47%), 135 (17%) [Ad]+.
Пример 3.
2-Адамантоилгидразон α-азидометил-(1-адамантил)-кетона (соединение III)
Получен аналогично из α-азидометил-(1-адамантил)-кетона и гидразида 2-адамантанкарбоновой кислоты.
Выход 52%, Т. пл. 133-134°С (разл.).
ИК спектр, ν, см-1: 3200 (NH), 2900 (CH), 2100 (N3), 1680 (С=O), 1530 (N-H), 1460 (CH).
Найдено, %: С 69,73; Н 8,52; N 17,46. С23Н33N5O. Вычислено, %: С 69,84; Н 8,41; N 17,71.
Масс-спектр (ЭИ): m/z 338 (9%) [М-СН2N3]+, 204 (10%), 162 (16%), 135 (100%) [Ad]+.
Пример 4.
Формилгидразон α-азидометил(1-адамантил)кетона (соединение IV)
Получен аналогично из α-азидометил-(1-адамантил)-кетона и гидразида муравьиной кислоты.
Выход 51%, Т. пл. 121°С (разл.).
ИК спектр, ν, см-1: 3100 (NH), 2900 (CH), 2100 (N3), 1690 (C=O), 1620 (N-H), 1450 (CH).
Найдено, %: С 69,73; Н 8,51; N 17,46. С13Н19N5О. Вычислено, %: С 59,75; Н 7,33; N 26,80.
Масс-спектр (ЭИ): m/z 204 (13%) [M-CH2N3]+, 162 (36%), 135 (100%) [Ad]+.
Пример 5.
n-Толуилгидразон α-азидометил(1-адамантил)кетона (соединение V)
Получен аналогично из α-азидометил-(1-адамантил)-кетона и гидразида n-толуиловой кислоты.
Выход 65%, Т. пл. 146°С (разл.).
ИК спектр, ν, см-1: 3300 (NH), 2900 (CH), 2100 (N3), 1680 (C=O), 1520 (N-H), 1450 (CH).
Найдено, %: С 68,11; Н 16,92; N 19,46. C20H25N5O. Вычислено, %: С 68,35; Н 17,17; N 19,93.
Пример 6.
4-Бромбензоилгидразон α-азидометил(1-адамантил)кетона (соединение VI)
Получен аналогично из α-азидометил-(1-адамантил)кетона и гидразида n-бромбензойной кислоты.
Выход 69%, Т. пл. 148°С (разл.).
ИК спектр, ν, см-1: 3200 (NH), 2900 (СН), 2150 (N3), 1650 (С=О), 1580 (NH).
Найдено, %: С 54,23; Н 5,76; N 16,36. C19H22BrN5O. Вычислено, %: С 54,82; Н 5,98; N 16,82.
Масс-спектр (ЭИ): m/z 358 (94%) [М-СH2N3]+, 281 (9%), 182 (69%), 135 (67%) [Ad]+.
Пример 7.
4-Гидроксибензоилгидразон 1-адамантил(азидометил)кетона (соединение VII)
Получен аналогично из α-азидометил-(1-адамантил)кетона и гидразида 4-гидроксибензойной кислоты.
Выход 57%, Т. пл. 127-128°С (разл.).
ИК спектр, ν, см-1: 3200 (NH), 2900 (СН), 2100 (N3), 1640 (C=O), 1580 (N-H), 1450 (СН).
Найдено, %: С 64,23; Н 6,97; N 19,46. C19H23N5O2. Вычислено, %: С 64,57; Н 6,56; N 19,82.
Масс-спектр (ЭИ): m/z 296 (100%) [M-CH2N3]+, 177 (11%), 161 (12%), 135 (32%) [Ad]+.
Пример 8.
4-Метоксибензоилгидразон α-азидометил-(1-адамантил)кетона (соединение VIII)
Получен аналогично из α-азидометил-(1-адамантил)-кетона и гидразида 4-метоксибензойной кислоты.
Выход 72%, Т. пл. 138°С (разл.).
ИК спектр, ν, см-1: 3180 (NH), 2900 (СН), 2080 (N3), 1650 (C=O), 1530 (N-H), 1440 (СН).
Найдено, %: С 65,12; Н 7,08; N 18,86. C20H25N5O2. Вычислено, %: С 65,37; Н 6,86; N 19,06.
Масс-спектр (ЭИ): m/z 311 (59%) [М-СН2N3]+, 191 (14%), 176 (8%), 135 (100%) [Ad]+.
Пример 9.
1-Адамантоилгидразон α-азидометил-(3-бром-1 -адамантил)кетона (соединение IX)
Получен аналогично из α-азидометил-(3-бром-1-адамантил)кетона и гидразида 1-адамантанкарбоновой кислоты.
Выход 65%. Т. пл. 140°С (разл.).
ИК спектр, ν, см-1: 3300 (NH), 2900 (СН), 2150 (N3), 1680 (С=O), 1520 (N-H+δNH), 1400 (CH).
Найдено, %: С 57,89; Н 7,21; N 14,42. C23H32BrN5O. Вычислено, %: С 58,23; Н 6,80; N 14,76.
Масс-спектр (ЭИ): m/z 417 (33%) [М-CH2N3]+, 337 (4%), 135 (100%) [Ad]+.
Пример 10.
1-Адамантоилгидразон α-азидометил(третбутил)кетона (соединение X)
Получен аналогично из α-азидометил(третбутил)кетона и гидразида 1-адамантанкарбоновой кислоты.
Выход 73%, Т. пл. 130°С (разл.).
ИК спектр, ν, см-1: 3200 (NH), 2900 (СН), 2100 (N3), 1650 (С=О), 1520 (N-H), 1450 (СН).
Найдено, %: С 64,19; Н 8,71; N 21,86. C17H27N5O. Вычислено, %: С 64,32; Н 8,57; N 22,06.
Масс-спектр (ЭИ): m/z 261 (93%) [М-СН2N3]+, 243 (19%), 228 (12%), 135 (100%) [Ad]+.
Пример 11.
Семикарбазон α-азидометил-(3-бром-1-адамантил)кетона (соединение XI)
В 30 мл этилового спирта и 10 мл воды растворяют α-азидометил-(3-бром-1-адамантил)кетон (4 ммоль) и гидрохлорид семикарбазида (5,2 ммоль), добавляют 0,6 г ацетата натрия и выдерживают 48 ч при комнатной температуре. Выпавшие кристаллы отфильтровывают, промывают этанолом и сушат.
Выход 70%. Т. пл. 153-155°С (разл.).
ИК спектр, ν, см-1: 3380 (NH), 3100 (NH), 2900 (CH), 2100 (N3), 1700 (C=O), 1580 (N-H+δNH), 1460 (CH).
Найдено, %: С 43,25; Н 5,48; N 23,96. C13H19BrN6O. Вычислено, %: С 43,95; Н 5,39; N 23,66.
Масс-спектр (ЭИ): m/z 297 (97%) [М-СH2N3]+, 282 (18%), 213 (22%), 202 (36%), 160 (81%), 133 (45%).
Пример 12. Исследование противовирусной активности заявляемых соединений.
Для оценки противовирусного действия заявляемых соединений, полученных в соответствии с примерами 1-11, использовали следующую методику. Монослой культуры клеток Vero или МК-2 выращивали в лунках плоскодонных 96-луночных планшетов. В культуральную среду добавляли серийные разведения исследуемых соединений и соответствующий вирус. После инкубирования в течение 3-5 суток монослой клеток прокрашивали витальным красителем нейтральным красным, после удаления красителя и отмывки избытка красителя вносили лизирующий раствор и количество красителя, включенного в монослой клеток, учитывали на планшетном спектрофотометре при длине волны 490 нм. В качестве контролей использовали лунки планшета, в которые вирус не вносили (контроль токсичности соединений), в которые вносили вирус без соединений (контроль вируса), и лунки, в которые не вносили ни вирус, ни соединения (контроль культуры клеток). Результаты анализировали с помощью программы SoftMax (версия 4.0, Molecular Devices, Menlo Park, USA). Данная методика основана на способности тестируемых соединений предотвращать репродукцию вируса и его распространение от клетки к клетке, в связи с чем клетки не погибают и сохраняют способность фагоцитировать нейтральный красный.
В качестве исследуемых вирусов использовали ортопоксвирусы оспы коров (штамм Гришак) и оспы обезьян (штамм Zair 599), патогенные для человека. Кроме того, использовали вирус осповакцины (штамм ЛИВП), используемый для вакцинации населения. Помимо ортопоксвирусов, патогенных для человека, для оценки противовирусной активности использовали вирус эктромелии (оспы мышей), штамм К-1.
Результаты изучения противовирусного действия соединений I-XI приведены в таблицах 1-8.
Противовирусная активность соединений I-XI в отношении вируса осповакцины (штамм вируса ЛИВП) на культуре клеток Vero
Противовирусная активность соединений I, IX в отношении вируса осповакцины (штамм вируса ЛИВП) на культуре клеток МК-2
Противовирусная активность соединений I, IX в отношении вируса оспы коров (штамм Гришак) на культуре клеток Vero
Противовирусная активность соединений I, IX в отношении вируса оспы коров (штамм Гришак) на культуре клеток МК-2
Противовирусная активность соединений I, IX в отношении вируса оспы обезьян (штамм вируса Zaire 599) на культуре клеток Vero
Противовирусная активность соединений I, IX в отношении вируса оспы обезьян (штамм вируса Zaire 599) на культуре клеток МК-2
Противовирусная активность соединений I, IX в отношении вируса эктромелии (штамм вируса К-1) на культуре клеток Vero
Противовирусная активность соединений I, IX в отношении вируса эктромелии (штамм вируса К-1) на культуре клеток МК-2
Анализ полученных данных наглядно показывает, что заявляемый ряд соединений обладает противовирусным действием, в частности в отношении ортопоксвирусов, патогенных для человека.
Как видно из данных таблиц 1-8, все исследованные соединения эффективно подавляют размножение ортопоксвирусов в культуре клеток. Так, соединения I, III, V, VI, VIII, Х ингибируют размножение вируса осповакцины в концентрациях 0.87, 0.93, 0.24, 0.78, 0.12 и 0.2 мкг/мл (соответственно), значения которых по величине существенно превосходят препарат сравнения (1-адамантаноилгидразон α-азидометил(1-адамантил)кетона), активная концентрация которого составляет 2.6 мкг/мл. Наиболее высокую противовирусную активность имеют соединения I, V, IX, Х, индекс селективности которых в отношении вируса осповакцины составляет 71.7, 237.5, 234 и 189 (соответственно). Несколько менее он выражен у соединений III, IV, VI и VIII (28.5, >21, 51.3 и 41 соответственно). Индекс селективности большинства исследованных соединений по величине значительно превосходит индекс селективности препарата сравнения 1-адамантаноилгидразон α-азидометил(1-адамантил)кетона.
Изобретение может быть использовано в медицине, ветеринарии, лечебных учреждениях.
| название | год | авторы | номер документа |
|---|---|---|---|
| 7-[N'-(4-ТРИФТОРМЕТИЛБЕНЗОИЛ)-ГИДРАЗИНОКАРБОНИЛ]-ТРИЦИКЛО[3.2.2.0]НОН-8-ЕН-6-КАРБОНОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2412160C1 |
| ГИДРАТ N-{3,5-ДИОКСО-4-АЗАТЕТРАЦИКЛО[5.3.2.0.0]ДОДЕЦ-11-ЕН-4-ИЛ}-2-ГИДРОКСИБЕНЗАМИДА, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ОРТОПОКСВИРУСОВ | 2009 |
|
RU2412168C1 |
| Амиды, содержащие адамантановые и ароматические фрагменты, используемые в качестве ингибиторов репродукции ортопоксвирусов | 2021 |
|
RU2798665C2 |
| N-{3,5-ДИОКСО-4-АЗАТЕТРАЦИКЛО[5.3.2.0.0]ДОДЕЦ-11-ЕН-4-ИЛ}-4-ГИДРОКСИБЕНЗАМИД, ПРОТИВОВИРУСНЫЙ ПРЕПАРАТ, ИНГИБИРУЮЩИЙ РЕПЛИКАЦИЮ РАЗЛИЧНЫХ ВИДОВ ОРТОПОКСВИРУСОВ | 2010 |
|
RU2424800C1 |
| МЕТИЛ, ХЛОР И НИТРОПРОИЗВОДНЫЕ N-{3, 5-ДИОКСО-4-АЗАТЕТРАЦИКЛО[5.3.2.0.0]ДОДЕЦ-11-ЕН-4-ИЛ}-2-ГИДРОКСИБЕНЗАМИДА-ПРОТИВОВИРУСНЫЕ ПРЕПАРАТЫ, ИНГИБИРУЮЩИЕ РЕПЛИКАЦИЮ РАЗЛИЧНЫХ ВИДОВ ОРТОПОКСВИРУСОВ | 2010 |
|
RU2440983C1 |
| {3,5-ДИОКСО-4-АЗАТЕТРАЦИКЛО[5.3.2.0.0]ДОДЕЦ-11-ЕН-4-ИЛ}ТИОМОЧЕВИНА, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ОРТОПОКСВИРУСОВ | 2009 |
|
RU2412167C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО | 2009 |
|
RU2423359C1 |
| АМИНОПРОИЗВОДНЫЕ АДАМАНТАНА, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСА ГРИППА | 2008 |
|
RU2401263C2 |
| Амиды, сочетающие адамантановый и монотерпеновый фрагменты, используемые в качестве ингибиторов ортопоксвирусов | 2019 |
|
RU2712135C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО ПРОТИВ ВИРУСА НАТУРАЛЬНОЙ ОСПЫ И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2013 |
|
RU2543338C1 |
Изобретение относится к новым гидразонам азидокетонов алициклического и алифатического ряда, обладающим активностью против ортопоксвирусов, общей формулы
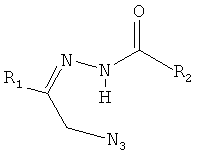
где R1=1-Ad, R2=3-R-1-Ad (R=OH, 4-толил), 2-Ad, Н, 4-толил, 4-бромфенил, 4-гидроксифенил, 4-метоксифенил; R1=3-Br-1-Ad, R2=1-Ad, NH2; R1=третбутил, R2=1-Ad, где Ad - адамантил. 8 табл.
Гидразоны азидокетонов алициклического и алифатического ряда общей формулы

где R1=1-Ad, R2=3-R-1-Ad (R=OH, 4-толил), 2-Ad, H, 4-толил, 4-бромфенил, 4-гидроксифенил, 4-метоксифенил; R1=3-Br-1-Ad, R2=1-Ad, NH2; R1=третбутил, R2=1-Ad, где Ad-адамантил, обладающие активностью против ортопоксвирусов.
| Производные адамантана, проявляющие противовирусную активность | 1988 |
|
SU1568481A1 |
| STN on the Web, БД Registry, RN 125011-71-4, RN 120511-72-5, на основании статьи «Термолиз ацилгидразонов α-азидокетонов-новый путь к 1,2,4-триазинам», Матвеев А.И., Моисеев И.К | |||
| «Химия Гетероциклических Соединений», 1989, №2, с.275-276 | |||
| STN on the Web, БД Registry, RN 871897-38-0, на основании | |||
Авторы
Даты
2009-12-20—Публикация
2007-10-10—Подача