Настоящее изобретение относится к новым рекомбинантным молекулам лубрицина и к их использованию в качестве смазывающих веществ, антиадгезивных агентов и/или внутрисуставных добавок, например, для введения в синовиальные соединения, мениск, сухожилия, брюшину, перикард и в плевру.
Предшествующий уровень техники
Для оптимального функционирования синовиальных соединений, коэффициенты трения между суставными тканями должны быть крайне низкими. Обычно, суставный хрящ имеет хорошо смазанную поверхность. Однако, при остеоартрите (ОА), снижение уровня суставной “смазки” может приводить к разрушению хрящевого матрикса и к фибрилляции, что, в свою очередь, может приводить к нарушению функции суставов и к болям. Уменьшение суставной смазки также приводит к нарушению функции суставов и к болям при других формах артрита, включая ревматоидный артрит (РА).
Что касается других тканей (например, сухожилий), то смазанная поверхность также может придавать этим тканям определенные оптимальные функциональные свойства. Сухожилию, для его нормального функционирования, помимо необходимой смазанной поверхности также требуется предотвращение прилипания клеток к поверхностям сухожилий. При поражении и восстановлении сгибательной мышцы сухожилия наиболее распространенным осложнением является, например, образование спаек между сухожилиями.
Природный белок лубрицин представляет собой белок, родственный белку-предшественнику фактора стимуляции мегакариоцитов (MSF). PRG4 (протеогликан 4) обозначается аббревиатурой MSF, которая имеется в базе данных по номенклатуре человеческих генов UCL/HGNC/HUGO. Белок PRG4 (т.е., белок-предшественник MSF) описан в патенте США № 6433142 и в заявке на патент США № 20020137894 (все патенты и патентные заявки, цитируемые в этом документе, во всей своей полноте вводятся в настоящее описание посредством ссылки). Полипептид, кодируемый экзоном 6 гена PRG4, является в высокой степени гликозилированным и, очевидно, его присутствие необходимо для того, чтобы PRG4-родственный белок служил в качестве смазки, например, между поверхностями суставного хряща.
Исследования показали, что гликопротеин PRG4 также синтезируется внутренними синовиоцитами, которые выстилают влагалище сухожилия, при этом наиболее вероятно, что этот гликопротеин также происходит от теноцитов (Rees et al., 2002). Указанный гликопротеин присутствует, в основном, в области волокнистой хрящевой ткани сухожилия. Данный гликопротеин, помимо того, что он обладает функцией синовиальной жидкости, может играть в сухожилии важную цитопротективную роль, заключающуюся в предупреждении прилипания клеток к поверхностям сухожилия, а также в обеспечении “смазки” в процессе нормального функционирования сухожилия.
Экзон 6 гена PRG4 (также называемый “лубрицином”) кодирует приблизительно 76-78 повторов КЕРАРТТ-подобных последовательностей и 6 повторов ХХТТТХ-подобных последовательностей. В соответствии с настоящим изобретением изменение числа сравнимых последовательностей-повторов в рекомбинантных белках лубрицина может быть положено в основу разработки улучшенных биотерапевтических средств в целях увеличения уровня смазывания суставов и для предотвращения нежелательных спаек между тканями.
Описание сущности изобретения
Настоящее изобретение относится к новым рекомбинантным молекулам лубрицина и к их использованию в качестве смазывающих веществ, антиадгезивных средств и/или внутрисуставных добавок.
Для оптимизации параметров экспрессии и исследования функциональной необходимости использования всех приблизительно 76-78 повторов КЕРАРТТ-подобных последовательностей были сконструированы конструкции для экспрессии лубрицина, которые обеспечивают синтез рекомбинантных белков лубрицина с различной степенью О-связанных олигосахаридных замещений. Это может быть достигнуто путем включения различного числа КЕРАРТТ-подобных последовательностей в “коровую” кДНК-конструкцию, состоящую из экзонов 1 - 5, 5'- и 3'-фланкирующих областей экзона 6 и экзонов 7-12. Введение повторяющихся вставок в “синтетические кДНК-кластеры”, кодирующие множество КЕРАРТТ-подобных последовательностей, облегчает генерирование рекомбинантных конструкций лубрицина различного размера. Исходным объектом этих исследований была конструкция PRG4-Lub:1 (содержащая ДНК “синтетического кДНК-кластера-1” (SEQ ID NO:1), кодирующего четыре последовательности КЕРАРТТ).
Рекомбинантные белки лубрицина настоящего изобретения имеют общую первичную структуру с несколькими изоформами нативного человеческого лубрицина (см. US6743774, US20040072741 и WO0064930). Каждая из охарактеризованных изоформ отличается по составу экзонов гена PRG4, которые кодируют первичную структуру изоформ. Так, например, экзоны 1-12 гена PRG4 кодируют изоформу V0, которая представляет собой полноразмерную изоформу, а экзоны 1-4 и 6-12 кодируют изоформу V1, в которой отсутствует только сегмент, кодируемый экзоном 5. Экзоны 1-3 и 6-12 кодируют изоформу V2, в которой отсутствуют сегменты, кодируемые экзонами 4 и 5. И наконец, экзоны 1, 3 и 6-12 кодируют изоформу V3, в которой отсутствуют сегменты, кодируемые экзонами 2, 4 и 5. При этом, вероятно, существуют и другие изоформы, и некоторые родственные мутантные белки были описаны ранее (см. US20020086824).
В частности, настоящее изобретение относится к рекомбинантному белку лубрицину, содержащему повторяющиеся КЕРАРТТ-подобные последовательности. В своих предпочтительных вариантах настоящее изобретение относится к выделенному белку, содержащему последовательности SEQ ID NO:9, 13, 17, 21 или 25. Настоящее изобретение также относится к родственным вариантам выделенного белка, содержащего последовательности SEQ ID NO:7, 11, 15, 19 или 23. В других родственных вариантах настоящее изобретение относится к выделенному полинуклеотиду, содержащему последовательность нуклеиновой кислоты, кодирующую рекомбинантный белок лубрицин. В предпочтительных вариантах настоящее изобретение относится к выделенному полинуклеотиду, содержащему последовательность нуклеиновой кислоты, кодирующую белок. В других родственных вариантах настоящее изобретение относится к выделенному полинуклеотиду, последовательность которого по всей его длине по крайней мере на 80%, 85%, 90%, 95%, 97%, 98% или на 99% идентична последовательности SEQ ID NO:6, 10, 14, 18 или 22.
В родственных аспектах настоящее изобретение также относится к выделенному белку, содержащему последовательность SEQ ID NO:26, присоединенную к последовательности (N-2) повтора(ов) SEQ ID NO:27, где N равно целому числу от 3 до 200. В других родственных вариантах настоящее изобретение относится к выделенному белку, содержащему последовательность SEQ ID NO:26 + SEQ ID NO:28 + [(N-2) повтора(ов) SEQ ID NO:27] + SEQ ID NO:29, где N равно целому числу от 3 до 200. В других вариантах родственных аспектов настоящего изобретения, описанных в этом параграфе, более предпочтительно, чтобы N было равно целому числу от 5 до 50, и еще более предпочтительно, чтобы N было равно целому числу от 10 до 30.
Идентификация последовательностей, имеющих идентификационные номера
В родственных вариантах настоящее изобретение также относится к композиции, содержащей терапевтически эффективное количество рекомбинантного белка лубрицина в фармацевтически приемлемом носителе. В некоторых вариантах изобретения указанная композиция дополнительно содержит гиалуронан или гилан.
Настоящее изобретение также относится к способу лечения индивидуума, предусматривающему: получение композиции, содержащей рекомбинантный белок лубрицин, и введение указанной композиции в ткань данного индивидуума. В родственных вариантах применения указанного способа настоящего изобретения ткань выбирают из группы, состоящей из хряща, синовиальной жидкости, мениска, сухожилия, брюшины, перикарда и плевры. В других родственных вариантах способа настоящего изобретения указанный способ, кроме того, включает стадию, выбранную из группы, состоящей из: введения индивидууму анестетика; введения индивидууму противовоспалительного лекарственного средства; введения индивидууму антибиотика; отсасывания у индивидуума жидкости; промывки ткани индивидуума и визуализации ткани указанного индивидуума. В других родственных вариантах изобретения указанный индивидуум выбран из группы, состоящей из мышей, кошек, собак, лошадей и человека.
В других своих вариантах, настоящее изобретение также относится к экспрессионному вектору, содержащему полинуклеотид, кодирующий рекомбинантный белок лубрицин, где указанный полинуклеотид функционально присоединен к последовательности регуляции экспрессии. В своих родственных вариантах настоящее изобретение относится к способу получения рекомбинантного белка лубрицина, предусматривающему: культивирование клеток, трансформированных экспрессирующим вектором в жидкой культуральной среде, и сбор рекомбинантного белка лубрицина из данной среды. Стадия сбора белка может также включать: концентрирование белка путем фильтрации данной среды через мембрану; сбор оставшегося белка из указанной мембраны, и солюбилизацию собранного белка в забуференном солевом растворе, содержащем гидрохлорид L-аргинина в концентрации от 0,1 до 2,0 М.
В другом родственном варианте настоящее изобретение относится к выделенному антителу, специфичному к рекомбинантному белку лубрицину.
Другие отличительные признаки и преимущества настоящего изобретения будут очевидны из нижеследующего описания предпочтительных вариантов изобретения и из формулы изобретения.
Подробное описание изобретения
Основная ДНК-конструкция, используемая для генерирования рекомбинантных белков лубрицина, может включать последовательности 5'- и 3'-экзона 6 гена PRG4 в различном порядке. Так, например, основная ДНК-конструкция может включать последовательности, кодирующие домены, подобные доменам соматомедина В, (экзоны 2-4) или гемопексин-подобные домены (экзоны 7-9) в различном порядке.
Вариантами основной ДНК-конструкции, имеющей последовательности 3'-экзона 6 в различном порядке, могут быть основные ДНК-конструкции, которые включают только отдельные экзоны 7, 8, 9, 10, 11 или 12, или пары экзонов (7 и 8), (7 и 9), (7 и 10), (7 и 11), (7 и 12), (8 и 9), (8 и 10), (8 и 11), (8 и 12), (9 и 10), (9 и 11), (9 и 12), (10 и 11), (10 и 12) или (11 и 12), или триплеты экзонов (7, 8 и 9), (7, 8 и 10), (7, 8 и 11), (7, 8 и 12), (7, 9 и 10), (7, 9 и 11), (7, 9 и 12), (7, 10 и 11), (7, 10 и 12), (7, 11 и 12), (8, 9 и 10), (8, 9 и 11), (8, 9 и 12), (8, 10 и 11), (8, 10 и 12), (8, 11 и 12), (9, 10 и 11), (9, 10 и 12), (9, 11 и 12) или (10, 11 и 12), или квадруплеты экзонов (7, 8, 9 и 10), (7, 8, 9 и 11), (7, 8, 9 и 12), (7, 8, 10 и 11), (7, 8, 10 и 12), (7, 8, 11 и 12), (7, 9, 10 и 11), (7, 9, 10 и 12), (7, 9, 11 и 12), (7, 10, 11 и 12), (8, 9, 10 и 11), (8, 9, 10 и 12), (8, 9, 11 и 12), (8, 10, 11 и 12) или (9, 10, 11 и 12), или квинтеты экзонов (7, 8, 9, 10 и 11), (7, 8, 9, 10 и 12), (7, 8, 9, 11 и 12), (7, 8, 10, 11 и 12), (7, 9, 10, 11 и 12) или (8, 9, 10, 11 и 12) или секстет экзонов (7, 8, 9, 10, 11 и 12).
Кроме того, вариантами основной ДНК-конструкции, имеющей последовательности 5'-экзона 6 в различном порядке, могут быть основные ДНК-конструкции, которые включают только отдельные экзоны 1, 2, 3, 4 или 5, или пары экзонов (1 и 2), (1 и 3), (1 и 4), (1 и 5), (2 и 3), (2 и 4), (2 и 5), (3 и 4), (3 и 5) или (4 и 5), или триплеты экзонов (1, 2 и 3), (1, 2 и 4), (1, 2 и 5), (1, 3 и 4), (1, 3 и 5), (1, 4 и 5), (2, 3 и 4), (2, 3 и 5), (2, 4 и 5) или (3, 4 и 5), или квадруплеты экзонов (1, 2, 3 и 4), (1, 2, 3 и 5), (1, 2, 4 и 5), (1, 3, 4 и 5) или (2, 3, 4 и 5), или квинтеты экзонов (1, 2, 3, 4 и 5).
Настоящее изобретение также охватывает белки, кодируемые основными ДНК-конструкциями, то есть белки, в которых часть полипептида или весь полипептид, кодируемые последовательностью экзона 6, делетированы, и в которых отсутствуют аминокислоты, кодируемые вставками, происходящими от синтетических кДНК-кластеров.
Настоящее изобретение также охватывает полинуклеотиды, гомологичные полинуклеотидам конкретных описанных здесь вариантов, например полинуклеотиды, имеющие последовательности, которые по крайней мере на 80%, 85%, 90%, 95%, 97%, 98% или 99% идентичны конкретным ДНК-последовательностям. Настоящее изобретение также включает полинуклеотиды, имеющие последовательность нуклеиновой кислоты, способную гибридизоваться с комплементом конкретных ДНК-последовательностей по всей длине функционального домена в условиях высокой жесткости. Настоящее изобретение также включает белки, кодируемые этими гомологичными или гибридизующимися полинуклеотидами.
Для лучшего понимания вариантов настоящего изобретения ниже приводятся определения встречающихся здесь терминов.
Определения
Выражение “повторяющаяся КЕРАРТТ-подобная последовательность” означает аминокислотную последовательность, которая по крайней мере на 90%, 93%, 95%, 96%, 97%, 98%, 99% или более: (а) идентична последовательности “APTTPКЕРАРТТTKSAPTTКЕРАРТТTKEPAPTTPКЕРАРТТТK” (SEQ ID NO:26; 45 аминокислот) и имеет по крайней мере одно замещение по О-связи; (b) идентичная последовательности “КЕРАРТТTКЕРАРТТTKSAPTTPКЕРАРТТP” (SEQ ID NO:27; 31 аминокислота) и имеет по крайней мере одно замещение по О-связи; или (с) идентична последовательности “ЕРАРТТTKSAPTTPКЕРАРТТP” (SEQ ID NO:28; 22 аминокислоты) и которая имеет по крайней мере одно замещение по О-связи. Повторяющаяся КЕРАРТТ-подобная последовательность может иметь, предпочтительно, две, три, четыре или более замещений по О-связи.
Существует ряд методов определения идентичности между двумя полинуклеотидными или полипептидными последовательностями, и термин “идентичность” хорошо известен специалистам и имеет определенное значение в зависимости от конкретно применяемого метода. Описанную здесь идентичность последовательностей определяют с использованием компьютерной программы BLAST 2 SEQUENCES, имеющейся в NCBI (http://www.ncbi.nlm.nih.gov/blast/, см. также Tatusova & Madden (1999)). Для аминокислотных последовательностей используются следующие параметры: ожидаемая величина = 1000; длина слова = 2; команда фильтр = отсутствует, а другие параметры используются по умолчанию. Для последовательностей нуклеиновых кислот используются те же самые параметры, за исключением, того, что длина слова = 8. Для сравнения аминокислотных последовательностей используются следующие параметры по умолчанию: матрица = BLOSUM62; штраф за пробел-пропуск = 11; штраф за пробел-удлинение = 1 и пробел х исключение = 50. Для сравнения последовательностей нуклеиновых кислот используются следующие параметры по умолчанию: “премия” за совпадение = 1; штраф за ошибочное спаривание = -2; выбор цепи = обе цепи; штраф за пробел-пропуск = 5; штраф за пробел-удлинение = 2 и пробел х исключение = 50.
Замещением по О-связи в рекомбинантном лубрицине может быть замещение смазывающим олигосахаридом β-(1-3)-Gal-GalNac, или другими молекулами, включая искусственные или природные углеводные молекулы (такие как сульфат кератина или сульфат хондротина). В некоторых вариантах изобретения, замещением по О-связи может быть замещение молекулами, которые способствуют функционированию рекомбинантного лубрицина как носителя поверхностно-активного фосфолипида (SALP) или других поверхностно-активных веществ (Hills, 2002). Процент гликозилирования или замещения определяют по массе (сухой массе).
Условия высокой жесткости, используемые для гибридизации ДНК:ДНК, означают условия, эквивалентные условиям связывания или гибридизации при 42єС в растворе, состоящем из 5х SSPE (43,8 г/л NaCl, 6,9 г/л NaH2PO4 · H2O и 1,85 г/л EDTA, рН, доведенный до 7,4 путем добавления NaOH), 0,5% ДСН, 5х реагент Денхардта и 100 мкг/мл денатурированной ДНК спермы лосося, с последующей промывкой в растворе, содержащем 0,1х SSPE, 1,0% ДСН, при 42°С, при использовании зонда длиной примерно 500 нуклеотидов.
Говорят, что полипептиды или другие описанные здесь соединения являются “выделенными”, если они присутствуют в препаратах, которые содержат по крайней мере 50 мас.% (по сухой массе) представляющего интерес соединения. Говорят, что полипептиды или другие описанные здесь соединения являются “по существу, чистыми”, если они присутствуют в препаратах, которые содержат по крайней мере 80 мас.% (по сухой массе) представляющего интерес соединения. Говорят, что полипептиды или другие описанные здесь соединения являются “гомогенными”, если они присутствуют в препаратах, которые содержат по крайней мере 95 мас.%, а предпочтительно, 99 мас.% (по сухой массе) представляющего интерес соединения. Чистоту измеряют путем электрофореза в восстанавливающем полиакриламидном геле и интенсивного окрашивания кумасси синим с последующим мониторингом оптической плотности полос (то есть, где чистота белка определяется путем оптической денситометрии).
Термин “апирогенный” означает “не содержащий примесей, вызывающих лихорадку, включая эндотоксин”. Определение наличия примесей осуществляют с помощью серии стандартных тестов, разрешенных Управлением по контролем за качеством пищевых продуктов, медикаментов и косметических средств (США).
Используемый здесь термин “терапевтически эффективное количество” означает общее количество каждого активного компонента, используемого в соответствующей фармацевтической композиции или в соответствующем способе, которое является достаточным для продуцирования у пациента положительного эффекта лечения и для излечения, предупреждения или улучшения соответствующего клинического состояния, а также для ускорения продуцирования у пациента положительного эффекта лечения и для ускорения излечения, предупреждения или улучшения такого состояния. При применении конкретного активного ингредиента, вводимого отдельно, этот термин относится лишь к одному ингредиенту. При применении комбинации ингредиентов этот термин означает комбинированное количество активных ингредиентов, которое дает терапевтический эффект независимо от того, вводятся ли эти ингредиенты в комбинации последовательно или одновременно.
В некоторых вариантах настоящего изобретения могут быть использованы внутрисуставные добавки. Такими добавками являются внутрисуставные добавки, которые содержат соединения, не происходящие от лубрицина, и которые используются в качестве терапевтических средств для лечения суставов. Так, например, для устранения ОА-ассоциированной боли в коленях использовали клинически приемлемые “добавки, повышающие вязкость” с полимерным гиауронаном (НА) и высокомолекулярными гиланами (такими как упруговязкая жидкость SYNVISC® “Hylan G-F 20”, распространяемая фирмой WYETH® Pharmaceuticals). Было показано, что эта повышающая вязкость добавка имеет высокую терапевтическую ценность, особенно для устранения боли в суставах у пациентов, вызываемые нагрузкой под действием массы тела (Wobig et al., 1998).
Гилан G-F 20 образуется при сшивании нескольких молекул НА, выделенных из петушиных или куриных гребешков. Добавка, повышающая вязкость и содержащая гилан G-F 20, может быть гораздо более эффективной для ослабления боли, чем добавка, содержащая НА с более низкой молекулярной массой (Wobig et al., 1999). Кроме того, использование повышающей вязкость и облегчающей боль добавки с гиланом G-F20, может оказаться более предпочтительной при введении НСПВС тем пациентам, которые страдают непереносимостью НСПВС (например, пациентам с высоким риском возникновения осложнений желудочно-кишечного заболевания; Espallargues & Pons, 2003). Хотя введение повышающей вязкость добавки с гиланом G-F 20 является безопасной и хорошо переносимой терапией, которая приводит к кратковременному (то есть, до 3-6 месяцев после лечения) ослаблению болевых симптомов и улучшению функции суставов, однако такая терапия пока не может дать надежную гарантию того, что в дальнейшем не потребуется протезирование колена у пациентов с ОА (Espallargues & Pons, 2003).
Пример 1: Клонирование рекомбинантного лубрицина
Конструкции. В некоторых вариантах изобретения, основная ДНК-конструкция для генерирования рекомбинантных молекул лубрицина состоит из последовательности, простирающейся от кодона Met (ATG) до (включительно) рестрикционного BssHII-сайта (G^CGCGC) SEQ ID NO:6 (т.е., нуклеотиды 1-1123), и из последовательности, простирающейся от рестрикционного BspE1-сайта (T^CCGGA) до (включительно) стоп-кодона (ТАА) SEQ ID NO:6 (т.е., нуклеотиды 1269-2946). Эти последовательности, т.е., нуклеотиды 1-1123 и 1269-2946 SEQ ID NO:6, кодируют аминокислоты М1-S373 (кодируемые экзонами 1-5 и приблизительно 174 фланкирующими 5'-кодонами экзона 6) и Е848-Р1404 (кодируемые приблизительно 293 фланкирующими 3'-кодонами экзона 6 и экзонами 7-14) природного полноразмерного лубрицина (т.е., PRG4). Часть экзона 6, удаленная из основной ДНК-конструкции, соответствует ДНК-последовательности, кодирующей аминокислоты А374-Р847 нативного PRG4 (т.е., приблизительно из 940 аминокислот, кодируемых экзоном 6, были удалены 474 аминокислоты). Такая отсутствующая аминокислотная последовательность обогащена КЕРАРТТ-подобными последовательностями.
ДНК-последовательность синтетического кДНК-кластера-1 (SEQ ID NO:1) была добавлена посредством BssHII/BspEI к основной конструкции с получением рекомбинантной кДНК-конструкции PRG4-Lub:1 (SEQ ID NO:6). Последовательность SEQ ID NO:6 состоит из ДНК-вставки Lub:1 (SEQ ID NO:8, которая кодирует 51 аминокислоту SEQ ID NO:9 с ее четырьмя последовательностями КЕРАРТТ), расположенной между ДНК, кодирующей аминокислоты М1-S373, и ДНК, кодирующей аминокислоты Е848-Р1404 нативного PRG4. Другими словами, вместо А374-Р847 (474 аминокислоты) нативного PRG4, рекомбинантный лубрицин PRG4-LUB:1 включает 51 аминокислоту, которые образуют четыре полноразмерные последовательности КЕРАРТТ и приблизительно три неполных последовательности КЕРАРТТ.
ДНК-последовательность синтетического кДНК-кластера-1 (SEQ ID NO:1) была добавлена посредством BsuHII/BspEI к конструкции PRG4-Lub:1 с получением кДНК-конструкции “PRG4-Lub:2” (SEQ ID NO:10). кДНК-конструкция PRG4-Lub:1 имеет один рестрикционный Bsu36I-сайт (CC^TNAGG, т.е., CC^TAAGG, нуклеотиды №№ 1225-1231 SEQ ID NO:6). При добавлении синтетического кДНК-кластера-2 к кДНК-конструкции PRG4-Lub:1, этот Bsu36I-сайт был разрушен, однако синтетический кластер-2 содержит другой внутренний рестрикционный Bsu36I-сайт (CC^TNAGG, т.е., CC^TAAGG; нуклеотиды 92-98 SEQ ID NO:3). Затем может быть получена конструкция PRG4-Lub:N+1 путем присоединения Bsu36I/BspEI-фрагмента синтетического кДНК-кластера-2 к описанной ранее конструкции PRG4-Lub:N в этом внутреннем рестрикционном Bsu36I-сайте, который обеспечивается синтетическим кДНК-кластером-2.
кДНК-кластеры синтезировали в виде одноцепочечных олигонуклеотидов и гибридизовали вместе для продуцирования фрагмента двухцепочечной ДНК с липкими концами. Поэтому концевые BssHII-, Bsu36I- и BspEI-сайты являются неполными. В синтетическом кДНК-кластере-1 (SEQ ID NO:1) последовательность, ограниченная остаточными фланкирующими рестрикционными сайтами BssHII-(G^CGCGC) и BspEI-(T^CCGGA), включает внутренний рестрикционный Bsu36I-сайт (CC^TNAGG, то есть, CC^TAAGG), и эти рестрикционные сайты в указанных ниже последовательностях подчеркнуты.

SEQ ID NO:2, которая образуется в результате трансляции последовательности SEQ ID NO:1, включает четыре последовательности КЕРАРТТ, имеющие абсолютные соответствия (подчеркнуты снизу):
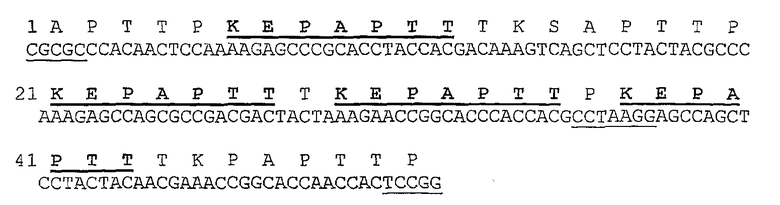
Аналогичным образом, синтетический кДНК-кластер-2 (SEQ ID NO:3) имеет остаточный 5'-концевой рестрикционный Bsu36I-сайт (то есть, CC^TNAGG, представленный только последовательностью ТАА), 3'-концевой остаточный рестрикционный BspEI-сайт (T^CCGGA) и внутренний рестрикционный Bsu36I-сайт (CC^TNAGG); эти рестрикционные сайты в указанных ниже последовательностях подчеркнуты.
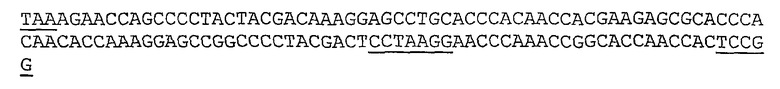
SEQ ID NO:4, которая образуется в результате трансляции последовательности SEQ ID NO:3, включает три последовательности КЕРАРТТ, имеющие абсолютные соответствия (подчеркнуты снизу):
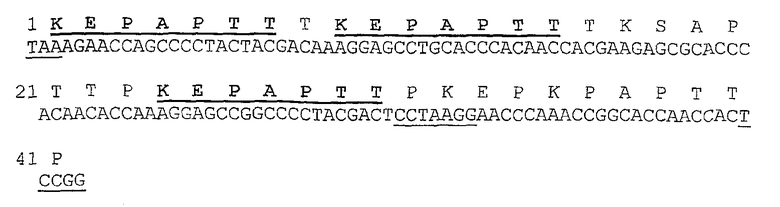
Рекомбинантная кДНК-конструкция PRG4-Lub:1 (SEQ ID NO:6) в векторе рTmed2 (конструкция + вектор составляют последовательность SEQ ID NO:5) фланкирована рестрикционным Sall-сайтом (G^TCGAC; нуклеотиды 1027-1032 SEQ ID NO:5) и рестрикционным NotI-сайтом (GC^GGCCGC; нуклеотиды 3984-3991 SEQ ID NO:5). Sall-сайт вводит модифицированную последовательность инициации трансляции Козака (СССАСС; нуклеотиды 1032-1037 SEQ ID NO:5) перед кодоном инициации трансляции АТG (нуклеотиды 1038-1040 SEQ ID NO:5). Между рестрикционным BssHII-сайтом (G^CGCGC; нуклеотиды 2155-2160 SEQ ID NO:5) и BspEI-сайтом (T^CCGGA; нуклеотиды 2306-2311 SEQ ID NO:5) находится внутренний клонирующий Bsu36I-сайт (CC^TNAGG, то есть, CC^TАAGG; нуклеотиды 2262-2268 SEQ ID NO:5).
кДНК-конструкция PRG4-Lub:1 (SEQ ID NO:6) транслируется в белок PRG4-LUB:1 (SEQ ID NO:7). Вставка между S373 и Е425 (то есть, Е848 нативного PRG4) целого белка PRG4-LUB:1 (SEQ ID NO:7) представляет собой последовательность SEQ ID NO:9, состоящую из 51 аминокислоты. Эта последовательность транслируется из ДНК-вставки Lub:1 (SEQ ID NO:8) и включает четыре полноразмерных последовательностей КЕРАРТТ. Между рестрикционным BssHII-сайтом (G^CGCGC; нуклеотиды 1118-1123 SEQ ID NO:6) и рестрикционным BspEI-сайтом (T^CCGGA; нуклеотиды 1269-1274 SEQ ID NO:6) находится внутренний клонирующий Bsu36I-сайт (CC^TNAGG, то есть, CC^TАAGG; нуклеотиды 1225-1231 SEQ ID NO:6).
Как и в рекомбинантной конструкции PRG4-Lub:1 в векторе рTmed2, рекомбинантная кДНК-конструкция PRG4-Lub:2 (SEQ ID NO:10) в векторе рTmed2 фланкирована рестрикционным Sall-сайтом (G^TCGAC) и рестрикционным NotI-сайтом (GC^GGCCGC), где Sall-сайт вводит модифицированную последовательность инициации трансляции Козака (СССАСС) перед кодоном инициации трансляции АТG (нуклеотиды 1-3 SEQ ID NO:10). И аналогичным образом, каждая из рекомбинантных кДНК-конструкций PRG4-Lub:3 (SEQ ID NO:14), PRG4-Lub:4 (SEQ ID NO:18) и PRG4-Lub:5 (SEQ ID NO:22) в векторе рTmed2 фланкирована рестрикционным Sall-сайтом (G^TCGAC) и рестрикционным NotI-сайтом (GC^GGCCGC), где Sall-сайт вводит модифицированную последовательность инициации трансляции Козака (СССАСС) перед кодоном инициации трансляции АТG (нуклеотиды 1-3 SEQ ID NO:14, 18 и 22, соответственно).
В кДНК-конструкции “PRG4-Lub:2” внутренний клонирующий Bsu36I-сайт (CC^TNAGG, то есть, CC^TАAGG; нуклеотиды 1318-1324 SEQ ID NO:10) находится между рестрикционным BssHII-сайтом (G^CGCGC; нуклеотиды 1118-1123) и рестрикционным BspEI-сайтом (T^CCGGA; нуклеотиды 1347-1352). Конструкция PRG4-Lub:2 (SEQ ID NO:10) транслируется в белок PRG4-LUB:2 (SEQ ID NO:11). Вставка между S373 и Е451 (то есть, Е848 нативного PRG4) целого белка PRG4-LUB:2 (SEQ ID NO:11) представляет собой последовательность SEQ ID NO:13, состоящую из 77 аминокислот. Эта последовательность транслируется из ДНК-вставки Lub:2 (SEQ ID NO:12). Вместо А374-Р847 (474 аминокислоты) нативного PRG4, 77 аминокислот рекомбинантного лубрицина PRG4-LUB:2 образуют шесть полноразмерных последовательностей КЕРАРТТ и примерно четыре неполных последовательности КЕРАРТТ.
В кДНК-конструкции “PRG4-Lub:3” внутренний клонирующий Bsu36I-сайт (CC^TNAGG, то есть, CC^TАAGG; нуклеотиды 1411-1417 SEQ ID NO:14) находится между рестрикционным BssHII-сайтом (G^CGCGC; нуклеотиды 1118-1123) и рестрикционным BspEI-сайтом (T^CCGGA; нуклеотиды 1440-1445). Конструкция PRG4-Lub:3 (SEQ ID NO:14) транслируется в белок PRG4-LUB:3 (SEQ ID NO:15). Вставка между S373 и Е482 (то есть, Е848 нативного PRG4) целого белка PRG4-LUB:3 (SEQ ID NO:15) представляет собой последовательность SEQ ID NO:17, состоящую из 108 аминокислот. Эта последовательность транслируется из ДНК-вставки Lub:3 (SEQ ID NO:16). Вместо А374-Р847 (474 аминокислоты) нативного PRG4, 108 аминокислот рекомбинантного лубрицина PRG4-LUB:3 образуют девять полноразмерных последовательностей КЕРАРТТ и примерно пять неполных последовательностей КЕРАРТТ.
В кДНК-конструкции “PRG4-Lub:4” внутренний клонирующий Bsu36I-сайт (CC^TNAGG, то есть, CC^TАAGG; нуклеотиды 1504-1510 SEQ ID NO:18) находится между рестрикционным BssHII-сайтом (G^CGCGC; нуклеотиды 1118-1123) и рестрикционным BspEI-сайтом (T^CCGGA; нуклеотиды 1533-1538). Конструкция PRG4-Lub:4 (SEQ ID NO:18) транслируется в белок PRG4-LUB:4 (SEQ ID NO:19). Вставка между S373 и Е513 (то есть, Е848 нативного PRG4) целого белка PRG4-LUB:4 (SEQ ID NO:19) представляет собой последовательность SEQ ID NO:21, состоящую из 139 аминокислот. Эта последовательность транслируется из ДНК-вставки Lub:4 (SEQ ID NO:20). Вместо А374-Р847 (474 аминокислоты) нативного PRG4, 139 аминокислот рекомбинантного лубрицина PRG4-LUB:4 образуют двенадцать полноразмерных последовательностей КЕРАРТТ и примерно шесть неполных последовательностей КЕРАРТТ.
В кДНК-конструкции “PRG4-Lub:5” внутренний клонирующий Bsu36I-сайт (CC^TNAGG, то есть, CC^TАAGG; нуклеотиды 1597-1603 SEQ ID NO:22) находится между рестрикционным BssHII-сайтом (G^CGCGC; нуклеотиды 1118-1123) и рестрикционным BspEI-сайтом (T^CCGGA; нуклеотиды 1626-1631). Конструкция PRG4-Lub:5 (SEQ ID NO:22) транслируется в белок PRG4-LUB:5 (SEQ ID NO:23). Вставка между S373 и Е544 (то есть, Е848 нативного PRG4) целого белка PRG4-LUB:5 (SEQ ID NO:23) представляет собой последовательность SEQ ID NO:25, состоящую из 170 аминокислот. Эта последовательность транслируется из ДНК-вставки Lub:5 (SEQ ID NO:24). Вместо А374-Р847 (474 аминокислоты) нативного PRG4, 170 аминокислот рекомбинантного лубрицина PRG4-LUB:5 образуют пятнадцать полноразмерных последовательностей КЕРАРТТ и примерно семь неполных последовательностей КЕРАРТТ.
Важно отметить, что процесс встраивания синтетического кДНК-кластера-2 может повторяться бесконечно. Каждая итерация приводит к добавлению трех полноразмерных последовательностей КЕРАРТТ. Рекомбинантные лубрицины PRG4-LUB:6 - PRG4-LUB:N конструировали так же как и рекомбинантные лубрицины PRG4-LUB:2 - PRG4-LUB:5, которые были сконструированы вышеописанным способом с использованием последовательностей-вставок. В таблице 2 в систематизированном виде приводятся последовательности BssHII/BspEI-вставки.
Таблица 2. Последовательности BssHII/BspEI-вставки


Хотя авторами была проиллюстрирована основная ДНК-конструкция с полноразмерным PRG4, содержащим все 12 экзонов (без центральной части экзона 6), однако, могут быть также использованы варианты сплайсинга PRG44 в зависимости от желаемых активностей и нужной длины. Кроме того, могут быть использованы и другие рестриктирующие ферменты в аналогичной стратегии при условии, что они будут иметь подходящую локализацию в последовательности нуклеиновой кислоты, кодирующей белок PRG4. В других вариантах изобретения основная ДНК-конструкция не содержит нативной последовательности экзона 6, но включает одну или несколько последовательностей от экзона 1 до экзона 5, включительно, или последовательностей от экзона 7 до экзона 12, включительно, нативного гена PRG4. В других вариантах изобретения, основная ДНК-конструкция идентична рекомбинантным последовательностям МSF, описанным в US6433142 или US20020137894, за исключением того, что в ней отсутствует вся последовательность экзона 6 или ее часть.
В своем предпочтительном варианте настоящее изобретение относится к кДНК-конструкции, кодирующей рекомбинантные лубрицины, которые были клонированы в рестрикционный Sall-сайт (G^TCGAC; нуклеотиды 1027-1032 SEQ ID NO:5) и рестрикционный NotI-сайт (GC^GGCCGC; нуклеотиды 3984-3991 SEQ ID NO:5) в эукариотическом экспрессионном векторе рTmed2 (например, рекомбинантная кДНК-конструкция PRG4-Lub:1 (SEQ ID NO:10) в экспрессионном векторе рTmed2, локализована в SEQ ID NO:5 в положениях нуклеотидов 1038-3983). Sall-сайт вводит первый нуклеотид модифицированной последовательности инициации трансляции Козака (СССАСС; нуклеотид 1032 SEQ ID NO:5) перед инициирующим кодоном метионина (АТG; нуклеотиды 1038-1040 SEQ ID NO:5). Другие варианты настоящего изобретения включают другие комбинации рестрикционных сайтов и другие экспрессионные векторы.
В предпочтительном варианте изобретения, описанный итеративный процесс предусматривает использование синтетического кДНК-кластера-1 (SEQ ID NO:1) в экспрессионном векторе рTmed2, который фланкирован рестрикционными BssHII-сайтом (G^CGCGC) и рестрикционным BspEI-сайтом (T^CCGGA), и синтетического кДНК-кластера-1, который включает внутренний рестрикционный Bsu36I-сайт (CC^TNAGG, то есть, CC^TАAGG; нуклеотиды 107-113 SEQ ID NO:1). В этом предпочтительном варианте для итеративного генерирования рекомбинантных конструкций лубрицина, содержащих КЕРАРТТ-подобные последовательности, синтетический кДНК-кластер-2 (SEQ ID NO:3) был встроен между Bsu36I- и BspEI-сайтами указанной рекомбинантной конструкции. Синтетический кДНК-кластер-2 (SEQ ID NO:3) фланкирован модифицированным остаточным Bsu36I-сайтом (TAAAG) и остаточным BspEI-сайтом (ACTCCGG). Он также включает внутренний Bsu36I-сайт (CC^TNAGG, то есть, CC^TАAGG; нуклеотиды 92-98 SEQ ID NO:3). После клонирования синтетического кДНК-кластера-2 в Bsu36I- и BspEI-сайты рекомбинантной конструкции лубрицина, клонирующий Bsu36I-сайт исходной конструкции разрушался, в результате чего оставался один уникальный клонирующий Bsu36I-сайт в новой конструкции.
В этом предпочтительном варианте изобретения аминокислотная последовательность, “APTTPKEPAPTTTKSAPTTPKEPAPTTTKEPAPTTPKEPAPTTTK” (SEQ ID NO:26; 45 аминокислот) сохраняет часть каждого из белков PRG4-LUB:N (где N = целому числу 1 или более). Кроме того, аминокислотная последовательность “KEPAPTTTKEPAPTTTKSAPTTPKEPAPTTP” (SEQ ID NO:27; 31 аминокислота) кодируется ДНК-вставкой, которая становится частью каждой из кДНК-конструкций PRG4-LUB:N+1 в результате присоединения синтетического Bsu36I/BspEI-кДНК-кластера-2 к кДНК-конструкции PRG4-LUB:N. Что касается белка PRG4-LUB:N, где N равно целому числу ≥ 3, то в предпочтительных вариантах изобретения аминокислотная последовательность“EPAPTTTKEPAPTTTKSAPTTPKEPAPTTP” (SEQ ID NO:28; 22 аминокислоты), соединяет SEQ ID NO:26 с повторами (N-2) SEQ ID NO:27. Кроме того, в предпочтительных вариантах изобретения за аминокислотной последовательностью “KEPKPAPTTP” (SEQ ID NO:29, 10 аминокислот) непосредственно следует последняя повторяющаяся вставка SEQ ID NO:27 белка PRG4-LUB:N, где N ≥ 2.
Поскольку они образуют по крайней мере две последовательности КЕРАРТТ, то каждая из описанных здесь последовательностей SEQ ID NO:26, SEQ ID NO:27 и SEQ ID NO:28 представляют собой “повторяющуюся КЕРАРТТ-подобную последовательность” (N-конец SEQ ID NO:28 связан с остатком К, в результате чего SEQ ID NO:28 образует две последовательности КЕРАРТТ в белках PRG4-LUB:N).
Поэтому, в предпочтительном варианте настоящего изобретения, рекомбинантный белок лубрицина PRG4-LUB:N (где N равно целому числу 1 или более) включает SEQ ID NO:26. Кроме того, в предпочтительном варианте настоящего изобретения рекомбинантный белок лубрицина PRG4-LUB:N (где N равно целому числу 2 или более) также включает SEQ ID NO:27. В этих предпочтительных вариантах в каждом из белков PRG4-LUB:N, последовательность SEQ ID NO:27 повторяется N-1 раз. В PRG4-LUB:2, SEQ ID NO:26 и SEQ ID NO:27 перекрываются (то есть, они имеют общую последовательность КЕРАРТТ).
В других предпочтительных вариантах изобретения, где N равно целому числу ≥ 3 (например, где N равно целому числу 3-200, или, в более предпочтительных вариантах, где N равно целому числу 5-50, или, в еще более предпочтительных вариантах, где N равно целому числу 10-30), рекомбинантный белок лубрицин содержит последовательность SEQ ID NO:28, состоящую из 22 аминокислот и соединяющую N-концевые 45 аминокислот SEQ ID NO:26 с повтором(ами) (N-2) SEQ ID NO:27, состоящим(и) из 31 аминокислоты, где 10 аминокислот SEQ ID NO:29 находятся со стороны С-конца по отношению к последнему повтору SEQ ID NO:27, состоящему из 31 аминокислоты.
Частота встречаемости последовательностей в предпочтительных белках PRG4-LUB
--
--
С-концевая вставка
В предпочтительных вариантах осуществления изобретения, белки PRG4-LUB:N, в основном, имеют 3 х N повторов последовательности КЕРАРТТ, где N равно числу повторяющихся КЕРАРТТ-подобных последовательностей. Рекомбинантный лубрицин PRG4-LUB:5 (имеющий 3×N = 3×5 = 15 копий последовательности КЕРАРТТ в предпочтительных вариантах изобретения) является самым крупным рекомбинантным лубрицином PRG4-LUB:N, последовательность которого подробно описана в настоящей заявке. Однако, в рекомбинантном лубрицине настоящего изобретения, N может составлять более 5, например, 7, 10, 12, 15, 20, 25, 30, 40, 50, 100, 150, 200 или более.
В частности, белки PRG4-LUB:1, PRG4-LUB:2, PRG4-LUB:3, PRG4-LUB:4 и PRG4-LUB:5, имеющие 4, 6, 9, 12 и 15 полноразмерных последовательностей КЕРАРТТ, соответственно, подробно описаны в настоящей заявке. Однако может быть присоединено и большее число последовательностей КЕРАРТТ путем проведения дополнительных описанных здесь итеративных процедур встраивания Lub:N. Авторами настоящей заявки представлено подробное описание рекомбинантных лубрицинов PRG4-LUB:N с относительно небольшим числом последовательностей КЕРАРТТ или КЕРАРТТ-подобных последовательностей по сравнению с нативным белком PRG4/лубрицином, поскольку более мелкие белки легче синтезировать и модифицировать.
Может также оказаться желательным увеличение числа КЕРАРТТ-подобных последовательностей по сравнению с нативным белком PRG4. Это может быть осуществлено либо путем проведения дополнительных описанных здесь итеративных процедур встраивания Lub:N так, чтобы в рекомбинантном белке лубрицине PRG4-LUB:N присутствовало более, чем 78 КЕРАРТТ-подобных последовательностей, либо это может быть осуществлено путем использования интактной кДНК PRG4, вместо кДНК PRG4 с делетированным экзоном 6, или варианта кДНК PRG4 с усеченным экзоном 6. Таким образом, любая из добавленных КЕРАРТТ-подобных последовательностей может присутствовать в избыточном количестве, превышающем количество, обнаруживаемое в нативном белке PRG4. Процедуры встраивания вставки, осуществляемые для генерирования более крупных рекомбинантных белков лубрицина из интактной кДНК PRG4, а также процедуры встраивания вставки, предусматривающие использование варианта кДНК PRG4 с делетированным экзоном 6 или варианта кДНК PRG4 с усеченным экзоном 6, также входят в объем настоящего изобретения.
Пример 2: Экспрессия и очистка белка “LUB”
кДНК-конструкцию PRG4-Lub:1 (SEQ ID NO:6, содержащую последовательность синтетического кДНК-кластера 1) экспрессировали в стабильно трансфицированной и предварительно адаптированной клеточной линии СНО DUKX, затем выделяли из кондиционированной среды, и солюбилизировали в PBS, содержащем 500 мМ гидрохлорида L-аргинина, как описано ниже.
кДНК-конструкцию PRG4-Lub:1 экспрессировали в стабильно трансфицированной клеточной линии СНО DUKX, и кондиционированную среду собирали. Затем двухлитровый объем этой кондиционированной среды концентрировали путем фильтрации в сжатом газообразном азоте (40 фунт/кв.дюйм) с использованием фильтра AMICON® M2000ТМ, снабженного дисковой мембраной PALL FILTRON® OMEGATM с отсечкой номинальной молекулярной массы (NMWL) либо 10 кДа, либо 30 кДа, либо 100 кДа. Среду концентрировали до объема приблизительно 100 мл, а затем ее отсасывали из дисковой мембраны. После этого, дисковую мембрану удаляли из фильтра AMICON® M2000ТМ. “Слизеобразный” ретентат, который аккумулировался на поверхности дисковой мембраны, собирали с помощью скребка для соскоба клеток и переносили в микроцентрифужные пробирки. Образцы в микроцентрифужных пробирках центрифугировали приблизительно при 12000 х g в течение 10 минут, и водный супернатант удаляли. “Богатый лубрицином” осадок растворяли в забуференном фосфатом физиологическом растворе (PBS), содержащем 500 мМ гидрохлорида L-аргинина. Концентрация гидрохлорида L-аргинина может составлять в пределах от 100 мМ до 2,0 М.
В соответствии с вышеуказанной процедурой гликопротеины PRG4-LUB:2 - PRG4-LUB:5 (и белки PRG4-LUB:N, где N = неотрицательное целое число 6 или более, а также другие гликопротеины, содержащие КЕРАРТТ-подобные последовательности) собирали непосредственно из дисковых мембран, т.е. без очистки концентрата, находящегося поверх дисковых мембран. То есть, эти рекомбинантные гликопротеины лубрицина выделяли непосредственно из дисковых мембран фильтра PALL FILTRON® OMEGATM с NMWL = 10 кДа, 30 кДа или 100 кДа. В некоторых случаях такие гликопротеины могут быть также очищены от концентрата, находящегося поверх дисковых мембран, хроматографическими методами или электрофоретическими методами, либо обоими методами. Рекомбинантные белки и гликопротеины лубрицина могут быть также очищены с помощью хроматографии и другими известными методами (например, описанными в US6433142 для белков MSF; см. также Deutscher, 1990 & Scopes, 1994).
Пример 3: Иммуногистохимия
Клеточный источник лубрицина в нормальных суставах и в суставах, пораженных остеоартритом, дополнительно исследовали иммуногистохимическими методами. Кроме того, оценку на присутствие лубрицина на других поверхностях ткани, включая плевру, перикард, брюшину и оболочки головного мозга, проводили нижеследующими методами.
Хрящ и синовиальную жидкость у пациентов с остеоартритом брали с их информированного согласия при проведении хирургической операции по протезированию колена. Другими проанализированными тканями были нормальная синовиальная жидкость человека и нормальные синовиальная жидкость, хрящ, плевра, перикард, брюшина, оболочки головного мозга, головной мозг, сухожилие и связки нормального примата, не относящегося к человеку (NНР), а также нормальные и пораженные остеоартритом мениск, хрящ, синовиальная жидкость, связки и сухожилия собак. Полученные ткани фиксировали в 4% параформальдегиде сразу после сбора или после 24-часового инкубирования в среде с добавленным монензином (5 мкМ) и без него. Для проведения иммуногистохимических исследований, ткани фиксировали в 4% параформальдегиде в течение 24 часов и получали 6-8-микронные парафиновые срезы. Субсерию тканей замораживали в соединении, используемом для заморозки, в целях проведения оптической когерентной томографии (OCT) и разрезали через интервалы 5-10 микрон, а затем фиксировали ацетоном.
Иммуногистохимические и иммунофлуоресцентные анализы проводили с использованием очищенного поликлонального кроличьего антитела против человеческого лубрицина (Ab 06A10), генерированного путем иммунизации усеченной формой рекомбинантного лубрицина и его очистки на колонке с белком А. Антитело против CD16 (NEOMARKERS®, Fremont CA) использовали для идентификации макрофагов (рецептор III Fcy). Антитело против CD106/VCAM-1 (NEOMARKERS®) использовали для мечения фибробластов в криостатных срезах. Затем для контрольных срезов использовали эквивалентные концентрации RIgG (VECTOR
LABSTM, CA), MIgG1 (DAKO®) и MIgG2a (DAKO®). Для визуализации связывания с антителом применяли технологию с использованием декстрановой системы (ENVISOION+TM; DAKO®), и срезы подвергали контрастному окрашиванию квасцами-гематоксилином Мейера. Иммунофлуоресценцию осуществляли с использованием вышеуказанных “первых” антител и зондировали “вторыми” антителами (Alexa Dyes - MOLECULAR PROBESTM, Oregon), а именно козьим антикроличьим антителом Alexa dye при 546 нм и козьим антимышиным антителом Alexa dye при 488 нм. Флуоресцентное связывание с антителом детектировали на флуоресцентном микроскопе NIKON®.
Лубрицин детектировали по всей поверхности нормальных и пораженных остеоартритом суставного хряща и синовиальной жидкости человека. Фибриллированная поверхность, пораженная остеоартритом, была полностью покрыта толстым слоем лубрицина. Иммунофлуоресценция CD106 обнаруживала сильное окрашивание клеточных мембран внутренних фибробластов синовиальной жидкости; при этом белок лубрицин также визуализировали по окрашиванию в синовиальных клетках. Двойное иммуноокрашивание на CD106+лубрицин явно указывало на их совместную локализацию во внутренних фибробластах синовиальной жидкости. Окрашивание синовиальных макрофагов на CD16 продемонстрировало присутствие этих клеток во всех слоях синовиальной жидкости, но не выявило совместной локализации с лубрицином.
Окрашивание суставных тканей приматов (NНР) и собак (нормальных и пораженных ОА) антителом против лубрицина обнаруживало лубрицин, покрывающий поверхностный слой синовиальной жидкости, хряща, мениска и сухожилия. Хрящ здоровых приматов (NНР) также обнаруживал сильную иммунореактивность не только в клетках поверхностной зоны, но также и в клетках переходной зоны без добавления монензина, осуществляемого для увеличения запаса внутриклеточного гликопротеина. Клетки, выстилающие брюшину, перикард и плевру, также обнаруживали экспрессию лубрицина, однако в оболочке головного мозга или в головном мозге не наблюдалось.
В целом, нормальные и пораженные остеоратритом синовиальная жидкость, сухожилие, мениск и хрящ были покрыты значительным слоем лубрицина. На тканях в суставах, пораженных ОА, явно обнаруживалось присутствие гликопротеина. Двойное иммунофлуоресцентное окрашивания синовиальной жидкости человека, страдающего остеоартритом (ОА), продемонстрировало, что внутренние фибробластные синовиоциты ответственны за синтез лубрицина.
Локализация белка лубрицина вне суставной ткани не была описана ранее. Присутствие поверхностного слоя лубрицина было явно продемонстрировано на плевре легких, перикарде и в брюшине. Считается, что лубрицин обладает смазывающей функцией внутри синовиального сустава, но он может также выполнять и множество других функций, включая, но не ограничиваясь ими, смазывающую и антиадгезивную функцию в других тканях. Пополнение этих других тканей лубрицином представляет собой биотерапию, которая входит в объем настоящего изобретения.
Пример 4: Рекомбинантный лубрицин, используемый в качестве механической смазки
В общих чертах, рекомбинантный лубрицин может быть использован в качестве смазки, например, вместе с уплотняющим материалом и носителем и т.п. Так, например, в патенте США 3973781, озаглавленном “Self-lubricating seal”, в патенте США 4491331, озаглавленном “Grooved mechanical face seal”, в патенте США 4560174, озаглавленном “Multi lip seal”, и в патенте США 4973068, озаглавленном “Differential surface roughness dynamic seals and bearings”, в каждом из которых описаны уплотнители различных конструкций. Рекомбинантный лубрицин может быть использован в качестве смазки с указанными носителями.
В частности, рекомбинантный лубрицин может быть использован в качестве смазки для медицинских инструментов, протезов и имплантатов, особенно когда требуется биосовместимая смазка. Кроме того, он может быть использован не только в медицинских целях, а также для предотвращения негативного воздействия окружающей среды, то есть в том случае, когда может потребоваться биологически совместимая смазка.
Пример 5: Композиции, содержащие рекомбинантный лубрицин
Рекомбинантный лубрицин настоящего изобретения может быть использован в фармацевтической композиции в комбинации с фармацевтически приемлемым носителем. Такая композиция может также содержать (помимо белка и носителя) разбавители, наполнители, соли, буферы, стабилизаторы, солюбилизаторы и другие материалы, хорошо известные специалистам. Термин “фармацевтически приемлемый” относится к нетоксичному материалу, который не оказывает влияния на эффективность биологической активности активного(ых) ингредиента(ов). Свойства носителя будут зависеть от способа введения. Фармацевтическая композиция настоящего изобретения может также содержать цитокины, лимфокины или другие гемопоэтические факторы, такие как M-CSF, GM-CSF, TNF, IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IL-13, IL-14, IL-15, TNF1, TNF2, G-CSF, Meg-CSF, тромбопоэтин, фактор стволовых клеток и эритропоэтин. Фармацевтическая композиция может также содержать и другие агенты, которые являются либо усилителями активности белка или активности его комплемента, либо терапевтическими агентами. Такие дополнительные факторы и/или агенты могут быть включены в фармацевтическую композицию для продуцирования синергического эффекта с белком настоящего изобретения или для минимизации побочных эффектов. И наоборот, белки настоящего изобретения могут быть включены в композиции, содержащие конкретный цитокин, лимфокин, другой гемопоэтический фактор, тромболитический или антитромботический фактор, или противовоспалительного средства для минимизации побочных эффектов.
Особенно предпочтительным является использование рекомбинантного белка лубрицина для введения вовнутрь сустава в комбинации с ранее описанным полимерным гиалуронаном (НА) и гиланами с более высокой молекулярной массой. Другими предпочтительными комбинациями для их использования в качестве внутрисуставных добавок являются комбинации рекомбинантного белка лубрицина с анестетиками (например, лидокаином), со стероидами (например, гексацетонидом триамцинолона) или с радиоизотопами (например, с иттрием). Другими предпочтительными комбинациями для их использования в качестве внутрисуставных добавок могут быть аутологичные или гетерологичные клеточные препараты (например, состоящие из культивированных хондроцитов, синовиоцитов или стволовых клеток, независимо от того, являются ли они аутологичными или гетерологичными).
Рекомбинантный лубрицин настоящего изобретения может быть активным в мультимерах (например, гетеродимерах или гомодимерах) или комплексах с самим собой или с другими белками. Следовательно, фармацевтическая композиция настоящего изобретения может содержать белок настоящего изобретения в указанной мультимерной или в комплексной форме.
Фармацевтическая композиция настоящего изобретения может быть получена в форме комплекса рекомбинантного(ых) белка(ов) лубрицина настоящего изобретения вместе с белковыми или пептидными антигенами. Белковый и/или пептидный антиген может передавать стимулирующий сигнал В- и Т-лимфоцитам. В-лимфоциты будут отвечать на антиген благодаря присутствию на их поверхности иммуноглобулинового рецептора. Т-лимфоциты будут отвечать на антиген благодаря присутствию Т-клеточного рецептора (ТСR) после презентации антигена белками МНС. МНС и структурно родственные белки, включая белки, кодируемые генами МНС класса I и класса II на клетках-хозяевах, будут служить для презентации пептидного(ых) антигена(ов) Т-лимфоцитам. Антигенные компоненты могут также поставляться как очищенные комплексы МНС-пептид отдельно или вместе с ко-стимулирующими молекулами, которые могут передавать сигнал непосредственно Т-клеткам. Альтернативно, антитела, способные связываться с поверхностным иммуноглобулином и с другими молекулами на В-клетках, а также данные антитела, способные связываться с ТСR и другими молекулами на Т-клетках, могут быть объединены с фармацевтической композицией настоящего изобретения.
Фармацевтическая композиция настоящего изобретения может быть получена в форме липосомы, в которой белок настоящего изобретения объединен, помимо других фармацевтически приемлемых носителей, с амфипатическими агентами, такими как липиды, которые существуют в агрегированной форме, такой как мицеллы, нерастворимые монослои, жидкие кристаллы или ламеллярные слои в водном растворе. Подходящими липидами для липосомной композиции являются, но не ограничиваются ими, моноглицериды, диглицериды, сульфатиды, лизолецитин, фосфолипиды, сапонин, желчные кислоты и т.п. Получение таких липосомных композиций может быть осуществлено любым специалистом и описано в патентах США №№ 4235871, 4501728, 4837028 и 4737323.
При осуществлении способа лечения или другого применения в соответствии с настоящим изобретением терапевтически эффективное количество белка настоящего изобретения вводят индивидууму (например, млекопитающему), страдающему данным состоянием. Белок настоящего изобретения может быть введен в соответствии со способом настоящего изобретения либо отдельно, либо в комбинации с другими агентами, применяемыми в других способах лечения, предусматривающих использование цитокинов, лимфокинов, других гемопоэтических факторов или клеточных добавок. В случае совместного введения с одним или несколькими цитокинами, лимфокинами, другими гемопоэтическими факторами или клеточными добавками, белок настоящего изобретения вводят либо одновременно с указанными цитокинами, лимфокинами, другими гемопоэтическими факторами, тромболитическими или антитромботическими факторами или клеточными добавками, либо последовательно. При последовательном введении соответствующую схему введения белка настоящего изобретения в комбинации с указанными цитокинами, лимфокинами, другими гемопоэтическими факторами, тромболитическими или антитромботическими факторами или клеточными добавками может назначить лечащий врач.
Введение белка настоящего изобретения, используемого в фармацевтической композиции или для реализации способа настоящего изобретения, может быть осуществлено различными путями, например путем чрескожной, подкожной, внутрибрюшинной, парентеральной или внутривенной инъекции, или, в некоторых случаях, путем перорального введения, ингаляции или местного применения. При этом предпочтительным введением обычно является инъекция в суставную ткань пациента (Schumacher, 2003).
При пероральном введении терапевтически эффективного количества белка настоящего изобретения этот белок может быть приготовлен в форме таблетки, капсулы, порошка раствора или эликсира. При введении в форме таблетки, фармацевтическая композиция настоящего изобретения может дополнительно содержать твердый носитель, такой как желатин или адъювант. Таблетки, капсула и порошок содержат примерно 5-95%, а предпочтительно, примерно 25-95% белка настоящего изобретения. При введении в жидкой форме в жидкий носитель, такой как вода, могут быть добавлены вазелиновое масло, масло животного или растительного происхождения, такое как арахисовое масло, минеральное масло, соевое масло или кунжутное масло, или синтетическое масло. Фармацевтическая композиция в жидкой форме может также содержать физиологический раствор, раствор декстрозы или растворы других сахаридов, либо гликоли, такие как этиленгликоль, пропиленгликоль или полиэтиленгликоль. При введении в жидкой форме фармацевтическая композиция содержит примерно от 0,5 до 90 мас.%, а предпочтительно примерно от 1 до 50% белка настоящего изобретения.
Если терапевтически эффективное количество белка настоящего изобретения вводят путем внутривенной, чрескожной или подкожной инъекции, белок настоящего изобретения может быть приготовлен в форме апирогенного, парентерально приемлемого водного раствора. Такие парентерально приемлемые растворы белка, имеющие соответствующие рН, изотоничность, стабильность и т.п., могут быть получены каждым специалистом. Предпочтительная фармацевтическая композиция для внутривенной, чрескожной или подкожной инъекции помимо белка настоящего изобретения может содержать изотонический носитель для инъекций, такой как инъекционный раствор хлорида натрия, инъекционный раствор Рингера, инъекционный раствор декстрозы, инъекционный раствор декстрозы и хлорида натрия, лактатсодержащий инъекционный раствор Рингера или другой носитель, известный специалистам. Фармацевтическая композиция настоящего изобретения может также содержать стабилизаторы, консерванты, буферы, антиоксиданты или другие добавки, известные специалистам. Так, например, настоящее изобретение также предусматривает введение инъекции в сочетании или в комбинации с лидокаином или с другими местными анестетиками, стероидами или адренокортикоидами, НА и/или гиланами, или с радиоизотопами.
Количество белка настоящего изобретения в фармацевтической композиции настоящего изобретения зависит от природы и тяжести состояния, подвергаемого лечению, и от типа лечения, которое данный пациент проходил ранее. В конечном счете, количество белка настоящего изобретения, которое требуется для введения каждому конкретному пациенту, назначается лечащим врачом. Сначала лечащий врач назначает низкие дозы белка настоящего изобретения и наблюдает ответную реакцию у пациента. Затем доза белка настоящего изобретения может быть увеличена вплоть до достижения оптимального терапевтического эффекта у пациента, и с этого момента дозу больше не увеличивают. При этом считается, что различные фармацевтические композиции, используемые для осуществления способа настоящего изобретения, должны содержать примерно от 0,01 мкг до 100 мг (предпочтительно, примерно от 0,1 мкг до 10 мг, а более предпочтительно, примерно от 0,1 мкг до 1 мг) белка настоящего изобретения на один кг массы тела в зависимости от способа введения и назначенной терапевтической схемы лечения.
При внутривенном введении продолжительность внутривенной терапии с использованием фармацевтической композиции, содержащей рекомбинантный лубрицин настоящего изобретения, может варьироваться в зависимости от тяжести заболевания, подвергаемого лечению, а также от состояния и от потенциального идиосинкратического ответа каждого отдельного пациента. При этом считается, что продолжительность каждой процедуры по введению белка настоящего изобретения может составлять порядка 12-24 часов непрерывного внутривенного введения. В конечном счете, продолжительность внутривенной терапии с использованием фармацевтической композиции настоящего изобретения определяется лечащим врачом.
Что касается композиций настоящего изобретения, которые могут быть использованы для лечения поражений костей, хряща, сухожилий или связок, то применяемый терапевтический способ предусматривает местное, системное или локальное введение данной композиции в виде имплантата или устройства. Совершенно очевидно, что вводимая терапевтическая композиция, используемая в целях настоящего изобретения, должна быть апирогенной и фармацевтически приемлемой. Кроме того, может оказаться желательным, чтобы данная композиция была получена в инкапсулированной или инъецируемой вязкой форме для доставки в пораженный участок кости, хряща или ткани. Для заживления ран и репарации ткани может оказаться подходящим местное применение композиции. В способах настоящего изобретения в композицию, описанную выше, альтернативно или дополнительно могут быть, также, но необязательно, включены терапевтически эффективные агенты, которые могут быть введены одновременно или последовательно вместе с композицией, содержащей рекомбинантный белок лубрицин настоящего изобретения. Предпочтительно, чтобы указанная композиция включала матрицу, которая была бы способна доставлять белоксодержащую композицию на пораженный участок кости и/или хряща, и была бы способна создавать структуру для развития кости и хряща, а также могла бы оптимально поглощаться организмом пациента. Такие матрицы могут быть получены из материалов, применяемых в настоящее время для других клинических процедур по имплантации.
При использовании матрицы выбор материала для матрицы должен быть осуществлен исходя их биологической совместимости, биологической разлагаемости, механических свойств, косметических свойств и межфазных свойств. Конкретное применение данных композиций будет определять соответствующий состав препарата. Потенциальными матрицами для данных композиций могут быть биологически разлагаемые материалы определенной химической структуры, такие как сульфат кальция, трикальцийфосфат, гидроксиапатит, полимолочная кислота, полигликолевая кислота и полиангидриды. Другими потенциальными материалами являются биологически разлагаемые и хорошо известные биологические соединения, такие как коллаген костей или кожи. Другие матрицы состоят из чистых белков или компонентов внеклеточного матрикса. Другими подходящими матрицами являются биологически неразлагаемые материалы определенной химической структуры, такие как агрегированный гидроксиапатит, биологическое стекло, алюминаты или другие керамические соединения. Матрицы могут состоять из комбинации материалов любого из вышеуказанных типов, таких как полиакриловая кислота и гидроксиапатит или коллаген и трикальцийфосфат. Биокерамические материалы могут быть модифицированы по своему составу, например по соотношению калиция-алюмината-фосфата, и эти материалы могут быть соответствующим образом обработаны для изменения размера пор, размера частиц, формы частиц и биологической разлагаемости.
В других композициях белки настоящего изобретения могут быть объединены с другими терапевтически эффективными агентами, используемыми для лечения повреждения и ран костей и/или хряща или нужных тканей. Такими агентами являются различные факторы роста, такие как эпидермальный фактор роста (ЕGF), тромбоцитарный фактор роста (PDGF), трансформирующие факторы роста (ТGF-α и ТGF-β) и инсулиноподобный фактор роста (IGF).
Терапевтические композиции могут также с успехом применяться в ветеринарии. Помимо человека особенно подходящими субъектами или пациентами для лечения рекомбинантными белками лубрицина настоящего изобретения являются, в частности, домашние животные, такие как кошки и собаки, лабораторные животные, такие как мыши и крысы, а также лошади.
Схема введения доз белоксодержащей фармацевтической композиции, используемой для регенерации ткани, может быть определена лечащим врачом с учетом различных факторов, которые модифицируют действие белков, например, таких как количество, необходимое для образования тканевой массы, участок повреждения, состояние пораженной ткани, размер раны, тип пораженной ткани (например, хряща или сухожилия), возраст, пол и режим питания пациента, тяжесть инфекции, если она имеется, время введения и другие клинические факторы. Доза может варьироваться в зависимости от типа матрицы, используемой для восстановления ткани, и от включения в фармацевтическую композицию других белков. Так, например, эффект от введения дозы может быть также достигнут путем добавления в конечную композицию других известных факторов роста, таких как IGF-1 (инсулиноподобный фактор роста I). Мониторинг положительного эффекта лечения может быть осуществлен путем периодической оценки образования/или репарации ткани/кости, например, путем рентгеновского анализа, гистоморфометрического анализа и мечения тетрациклином.
Полинуклеотиды настоящего изобретения могут быть также использованы для генной терапии. Такие полинуклеотиды либо могут быть введены in vivo, либо ex vivo в клетки для экспрессии у индивидуума (например, у млекопитающего). Полинуклеотиды настоящего изобретения могут быть также введены другими известными методами, используемыми для введения нуклеиновых кислот в клетку или в организм (включая, но не ограничиваясь ими, нуклеиновые кислоты в форме вирусных векторов или “оголенной” ДНК).
Клетки могут быть также культивированы ex vivo в присутствии нуклеиновых кислот или белков настоящего изобретения для пролиферации или для достижения нужного воздействия на активность или продуцирования нужной активности в таких клетках. Обработанные клетки могут быть затем введены in vivo в терапевтических целях.
Пример 6: Антитела против лубрицина
Рекомбинантный белок лубрицина настоящего изобретения может быть также использован в целях иммунизации животных для вырабатывания у них поликлональных и моноклональных антител, которые специфически реагируют с белками, или, в некоторых вариантах изобретения, с их природными аналогами. Такие антитела могут быть получены с использованием любого полноразмерного рекомбинантного белка лубрицина или его фрагментов в качестве иммуногена. Пептидные иммуногены могут, кроме того, содержать цистеиновый остаток у карбокси-конца и могут быть конъюгированы с гаптеном, таким как гемоцианин лимфы улитки (КLH). Методы синтеза таких пептидов известны специалистам (например, методы, описанные Merrifield, 1963 и Krstenansky et al., 1987). Моноклональные антитела, связывающиеся с рекомбинантным белком лубрицина настоящего изобретения, могут быть ценными диагностическими агентами для иммунодетекции родственных белков. Нейтрализующие моноклональные антитела, связывающиеся с этими родственными белками, могут быть также ценными терапевтическими агентами для лечения ассоциированных с лубрицином состояний, или, в некоторых случаях, для лечения некоторых форм рака, где может наблюдаться аномальная экспрессия лубрицина (например, в синовиомах).
Помимо антител, направленных против полипептидной коровой части рекомбинантного белка лубрицина, может оказаться желательным использование антитела, направленного против сахарной части или гликопротеинового комплекса рекомбинантного белка лубрицина. Для генерирования антител, связывающиеся с гликозилированным рекомбинантным лубрицином (но не с лубрицином в негликозилированной форме), предпочтительным иммуногеном является гликопептид, аминокислотная последовательность которого охватывает высокогликозилированную часть рекомбинантного лубрицина, например, повторяющуюся КЕРАРТТ-подобную последовательность. В качестве иммуногенов также используются более короткие полипептиды, например, длиной в 8-15 аминокислот, в той же самой высокогликозилированной области. Методы генерирования антител против высокогликозилированных биомолекул известны специалистам (например, как описано Schneerson et al., 1980).
Пример 7: Доставка рекомбинантного лубрицина
Для доставки рекомбинантного лубрицина применяются стандартные методы. Для внутрисуставного введения, рекомбинантный лубрицин доставляют в синовиальную полость при концентрации 20-500 мкг/мл в объеме приблизительно 0,1-2 мл на инъекцию. Так, например, 1 мл рекомбинантного лубрицина в концентрации 200-300 мкг/мл инъецируют в коленный сустав с помощью тонкой иглы (например, калибром 14-30, а предпочтительно, 18-26). Композиции настоящего изобретения могут быть также использованы для парентерального введения, такого как внутривенное, подкожное, внутримышечное или внутрибрюшинное введение, а в предпочтительных вариантах изобретения они могут быть использованы для нанесения на поверхность брюшины, перикарда или плевры.
Правильное положение иглы является решающим фактором для эффективной доставки рекомбинантного белка лубрицина путем инъекции, осуществляемой для лечения суставов (Schumacher, 2003). Правильное положение иглы может быть осуществлено благодаря применению ультразвуковой технологии. Успешная инъекция чаще всего достигается после успешной аспирации жидкости. Предполагается, что наиболее надежный доступ в пространство коленного сустава может быть достигнут путем супралатеральной инъекции в наднадколенниковую сумку. Помимо введения рекомбинантного лубрицина в синовиальную полость путем внутрисуставной инъекции могут быть введены нуклеиновые кислоты, кодирующие рекомбинантный лубрицин (например, при применении генной терапии).
Для предупреждения образования хирургических спаек, описанные здесь рекомбинантные лубрицины вводят в форме геля, пены, волокна или ткани. Рекомбинантный лубрицин, приготовленный таким способом, наносят на пораженные или обнаженные ткани или на границы раздела пораженных или обнаженных тканей для предупреждения образования спаек между противоположными поверхностями. Для большей эффективности на этом участке должны оставаться гель или пленка, которые будут предотвращать контакты между тканями в течение длительного периода времени, достаточного для того, чтобы ткани, при окончательном диспергировании геля и его контактировании с этими тканями, больше не прилипали друг к другу. Препарат рекомбинантного лубрицина, полученный в целях ингибирования или предотвращения образования спаек (например, полученный в форме мембраны, текстильного материала, пены или геля), был проанализирован на его способность предотвращать возникновение спаек у крыс-моделей после хирургической операции по удалению слепой кишки (Goldberg et al., 1993). Композиции наносили крысам на участок в области хирургического удаления слепой кишки и сравнивали с необработанным контролем (то есть, с животными, которым была удалена слепая кишка, но которые не получали какого-либо лечения). Снижение степени образования спаек у крысиной модели в присутствии композиции рекомбинантного лубрицина по сравнению с образованием спаек в отсутствие такой композиции указывало на то, что данная композиция является клинически эффективной для уменьшения образования спаек между тканями. Однако если образование спаек между тканями (например, при заживлении хрящевых трещин) является желательным, то в этом случае не следует использовать рекомбинантный лубрицин. Смазка хрящевых поверхностей предотвращает срастание хрящей друг с другом (Schaefer et al., 2004).
Рекомбинантные лубрицины также использовали для покрытия искусственных конечностей и суставов перед их имплантацией млекопитающему. Так, например, эти протезы могут быть погружены или залиты в раствор рекомбинантного лубрицина, например, методами, описанными в патентах США №№ 57009020 или 5702456. Однако при использовании in vivo рекомбинантного лубрицина для обеспечения смазки в области протеза должны соблюдаться меры предосторожности. Сообщалось, что заметное повышение уровня экспрессии гена PRG4 (т.е., экспрессии гена MSF) ассоциируется с расшатыванием протеза, при этом лубрицин может нарушать тесное взаимодействие между костями и протезом и тем самым способствовать расшатыванию протеза (Morawirtz et al., 2003).
Пример 8: Модель с ОА
Для оценки эффективности внутрисуставного введения препаратов лубрицина получали мышиную модель с остеоартритом/эрозией хряща. Для хирургического индуцирования остеоартрита мышей анестезировали 250 мг/кг путем внутрибрюшинного введения трибромэтанола (SIGMA® Chemical), и колени подготавливали для проведения хирургической процедуры в условиях асептики. Затем делали продольный разрез, медиальный по отношению к связке надколенника, суставную капсулу вскрывали и находили мениско-большеберцовую связку (прикрепляющую медиальный мениск к плато большеберцовой кости). Животных одной из подгрупп не подвергали никакой дополнительной обработке, и эта группа рассматривалась как группа, подвергнутая ложной хирургической операции. Животным экспериментальной группы делали медиальный разрез мениско-большеберцовой связки, что приводило к дестабилизации медиального мениска (DMM). У ложнооперированных и у ДММ-животных суставную капсулу и подкожный слой по отдельности зашивали и рану на коже закрывали путем нанесения тканевого клея NEXABAND® S/C (Abbott, North Chicago, IL). До и после проведения хирургической операции вводили бупренорфин (BUPRENEX®; Reckitt & Coleman, Kingston-upon-Hull, UK).
Препараты рекомбинантного лубрицина вводили путем внутрисуставной инъекции с использованием иглы калибра 30. Инъекции 5-10 микролитров на колено вводили в течение недели после хирургической операции. Могут быть также введены, но необязательно, дополнительные еженедельные инъекции. Затем через 4 недели и через 8 недель после операции животных умерщвляли с использованием диоксида углерода.
Для анализа на прогрессирование и тяжесть остеоартрита интактные коленные суставы помещали на 24 часа в 4% параформальдегид, а затем декальцифицировали в EDTA/поливинилпирролидоне в течение пяти дней. Суставы заливали в парафин и получали фронтальные 6 мкм-срезы по всему суставу. Покровные стекла окрашивали сафраниновым быстрым зеленым (Safronin О-fast) и проводили анализ всего сустава через интервалы в 70-мкм с использованием модифицированной семибальной шкалы оценок (Chambers et al., 2001), где “0” = нормальный хрящ; “0,5” = отсутствие окраски сафранином О без структурных изменений; “1” = неровная поверхность сустава и небольшая фибрилляция; “2” = фибрилляция захватывает слой, лежащий непосредственно ниже поверхностного слоя, и частичное отсутствие поверхностного слоя; “3” = небольшая (<20%); “5” = умеренная (20-80%); и “6” = значительная (>80%) утрата некальцифицированного хряща. Оценка “4” (эрозия кости) не является характерным признаком этой модели. Все квадранты этого сустава (плато медиальной большеберцовой кости, мыщелок медиальной бедренной кости, плато латеральной большеберцовой кости и мыщелок латеральной бедренной кости) были проанализированы отдельно. Для каждого коленного сустава слепым методом было проанализировано минимум 12 уровней. Оценки представляют собой максимальную гистологическую оценку для каждого отдельного сустава или как суммированные гистологические оценки. Суммированные гистологические оценки представляют собой сумму оценок для каждого квадранта на каждом гистологическом срезе по всему суставу. Этот метод анализа позволяет оценивать тяжесть поражений, а также площадь поверхности хряща, пораженного ОА-подобным заболеванием (Glasson et al., 2004).
Пример 9: Введение лубрицина препятствует развитию остеоратрита на модели у крыс
Введение
Хондропротективный гликопротеин лубрицин обеспечивает существенную защиту против патологического старения и дегенерации суставного хряща24'25. На этом основании было сделано предположение, что местное введение рекомбинантного лубрицина может иметь значительный эффект в качестве модифицирующего заболевание лечения при остеоартрите суставов. Был разработан новый белок лубрицина, «LUB:1», и оценена его терапевтическая эффективность после внутрисуставного введения на экспериментальной модели остеоартрита (АО) у крыс (остеоартрит индуцирован за счет разрыва мениска). Введение LUB:1, которое начинали через неделю после хирургического вмешательства, значительно снижало множественные параметры развития остеоартрита в течение последующих 4 недель, что доказывает возможное применение рекомбинантного лубрицина для лечения дегенеративных заболеваний суставов.
Способы
Получение конструкции рекомбинантного лубрицина. LUB:1
кДНК лубрицина человека26 обрабатывали рестрикционными ферментами, расщепляющими уникальные сайты экзона 6, которые фланкируют последовательность, кодирующую Аlа374-Pro847 (474 аминокислоты). Эту область заменяли короткой синтезированной кассетой кДНК, кодирующей 7 «КЕРАРТТ-подобных» повторяющихся элементов. Полученная конструкция, содержащая экзоны 1-5 природного лубрицина человека (кодирующие сигнальный пептид и N-концевые домены) и экзоны 7-12 (кодирующие С-концевые домены), была обозначена как «LUB:1». Экспрессию конструкции LUB:1 осуществляли в стабильно-трансфицированной клеточной линии СНО и продукт экспрессии выделяли из среды.
Оценка эффективности LUB:1 на модели ОА у крыс
Основная методика эксперимента и использование животных было одобрено IACUC. Односторонний коленный ОА индуцировали у самцов крыс Lewis (n=20) животных/обрабатываемая группа) путем трансекции медиальной коллатеральной связки и мениска (модель разрыва мениска). Начиная с первой недели после проведения хирургической операции осуществляли внутрисуставные инъекции LUB:1 (20 мкг/40 мкл) или физиологического раствора с фосфатным буфером (РВС) в качестве носителя (40 мкл) три раза в неделю в течение четырех недель. В конце эксперимента срезы тканей каждого обработанного коленного сустава анализировали под микроскопом и оценивали множественные патологические параметры ОА27. Статистический анализ осуществляли используя двусторонний t-тест Студента со значимостью р≤0,5.
Результаты
Конструкция рекомбинантного белка лубрицина, LUB:1, эффективно экспрессировалась в клетках СНО и была выделена из культуральной среды СНО. Было показано, что LUB:1 является функционально активным in vitro, так как он способен предотвращать клеточную адгезию и рост на культуральных плашках, покрытых тканью, в отличие от эквимолярных количеств контрольного белка (бычий альбумин сыворотки).
На модели ОА мениска у крысы степень дегенерации тибиального хряща была на 22% ниже при обработке животных LUB:1 по сравнению с PBS (фиг.1), значение остеофитов и суммарные баллы сустава также были значительно снижены, на 14% и 15%, соответственно (фиг.1В и 1C). Поразительно, что видимое и серьезное поражение коллагена в медиальном тибиальном плато, области, отображающей дегенерацию хряща, в котором потеря коллагена составляла более 50% толщины хряща, было значительно компенсировано, до 83%, в ответ на LUB:1 (фиг.ID). У животных, получавших PBS, частота такого поражения составляла 10/20 (50%), а у животных, получавших LUB:1, составляла 5/20 (25%). Субхондральные изменения кости у экспериментальных групп не имели существенных различий, что указывает на одинаковую нагрузку сустава у всех животных. Кроме того, вес медиальной капсулы значительно не различался в экспериментальных группах, что указывает на то, что фиброплазия синовиальной оболочки не была главным фактором модификации ОА при введении LUB:1.
Обсуждение
В настоящем исследовании авторы проанализировали эффективность внутрисуставного введения лубрицина в отношении прогрессирования заболевания на модели ОА у крыс. Лубрицин представляет собой сложный гликопротеин, содержащий большой муцино-подобный домен (кодируемый экзоном 6) с множественными повторами 'КЕРАРТТ-подобных' элементов, несущими сайты присоединения O-связанных олигосахаридов, обеспечивающих смазывающую активность [28, 9]. Авторы значительно оптимизировали экспрессию рекомбинантного лубрицина человека заменой большинства этих повторяющихся последовательностей синтезированной 'кассетой' с получением новой конструкции белка лубрицина, “LUB:1”. По сравнению с полноразмерным лубрицином человека последовательность LUB:1 содержит приблизительно 1/3 от числа 'КЕРАРТТ-подобных' элементов, расположенных в муцино-подобном домене.
Местное введение LUB:1 было терапевтически эффективным для профилактики дегенерации хряща на модели хирургически индуцированного ОА у крыс (остеоартрит индуцирован за счет разрыва мениска). Таким образом, коленные суставы животных, получавших LUB:1, были значительно менее серьезно поражены по сравнению с коленными суставами животных, получавших PBS (носитель). Снижение баллов дегенерации хряща (общая патология) и ингибирование потери матрикса также указывает на благоприятный эффект в отношении защиты всей хрящевой ткани.
Кроме оценки применимости для лечения ОА, также могут быть рассмотрены другие возможные варианты терапевтического применения лубрицина, например, для уменьшения патологических адгезивных образований после повреждения/восстановления связки или абдоминальной хирургии. Кроме того, стратегия синтезированной кассеты, использованная для экспрессии LUB:1, упрощает многократные повторы числа 'КЕРАРТТ-подобных' последовательностей в области, кодируемой экзоном 6 [4]. Разработка и характеристика таких конструкций может служить для дальнейшей оптимизации эффективности рекомбинантных молекул лубрицина.
Источники информации
1. Chambers et al., 2001, Arthritis Rheum. 44: 1455-65.
2. Deutscher, 1990, Methods in Enzymology, Vol.182: Guide to Protein Purification, Academic Press.
3. Espallargues and Pons, 2003, Int'l J. Tech. Assess. Health Care 19: 41-56.
4. Flannery et al., 1999, Biochem. Biophys. Res. Comm. 254: 535-41.
5. Glasson et al., 2004, Arthritis Rheum. 50: 2547-58.
6. Goldberg et al., 1993, In: Gynecologic Surgery and Adhesion Prevention, Willey-Liss, pp.191-204.
7. Hills, 2002, J. Rheumatology 29: 200-01.
8. Ikegawa et al., 2000, Cytogenet. Cell Genet. 90: 291-297.
9. Jay et al., 2001, J. Orthopaedic Research 19: 677-87.
10. Jay et al., 2002, Glycoconjugate Journal 18: 807-15.
11. Krstenansky et al., 1987, FEES Lett. 211: 10-16.
12. Marcelino et al., 1999, Nature Genetics 23: 319-322.
13. Merberg et al., 1993, Biology of Vitronectins and their Receptors, Pressner et al. (eds.): Elsevier Science Publishers, pp.45-53.
14. Merrifield, 1963, J. Amer. Chem. Soc. 85: 2149-54.
15. Morawietz et al., 2003, Virchows Arch. 443: 57-66.
16. Rees et al., 2002, Matrix Biology 21:593-602.
17. Schneerson et al., 1980, J. Exp. Mod. 152:361-76.
18. Scopes, 1994, Protein Purlfication: Principles and Practice (3rd edition), Springer Verlag.
19. Schaefer et al., 2004, Biorheology 41:503-508.
20. Schumacher, 2003, Arthritis & Rheumatism 49:413-20.
21. Tatusova and Madden, 1999, FEMS Microbiol Lett. 174:
247-50.
22. Wobig et al., 1998, Gin. Tlier. 20:410-23.
23. Wobig et al., 1999, Gin. Ther. 21:1549-62.
24. Rhee DK, et al. 2005. J Clin Invest 115:622-31.
25. Jay GD, et al. 2007. Proc Nati Acad Sci USA 104:6194-9.
26. Jones ARC, et al. 2007. J Orthop Res 25:283-92.
27. Flannery CR, et al. 2005. PCT WO 2005/01630 A2.
28. Bendele AM. 2001. J Musculoskel Neuron Interact 1:363-76.












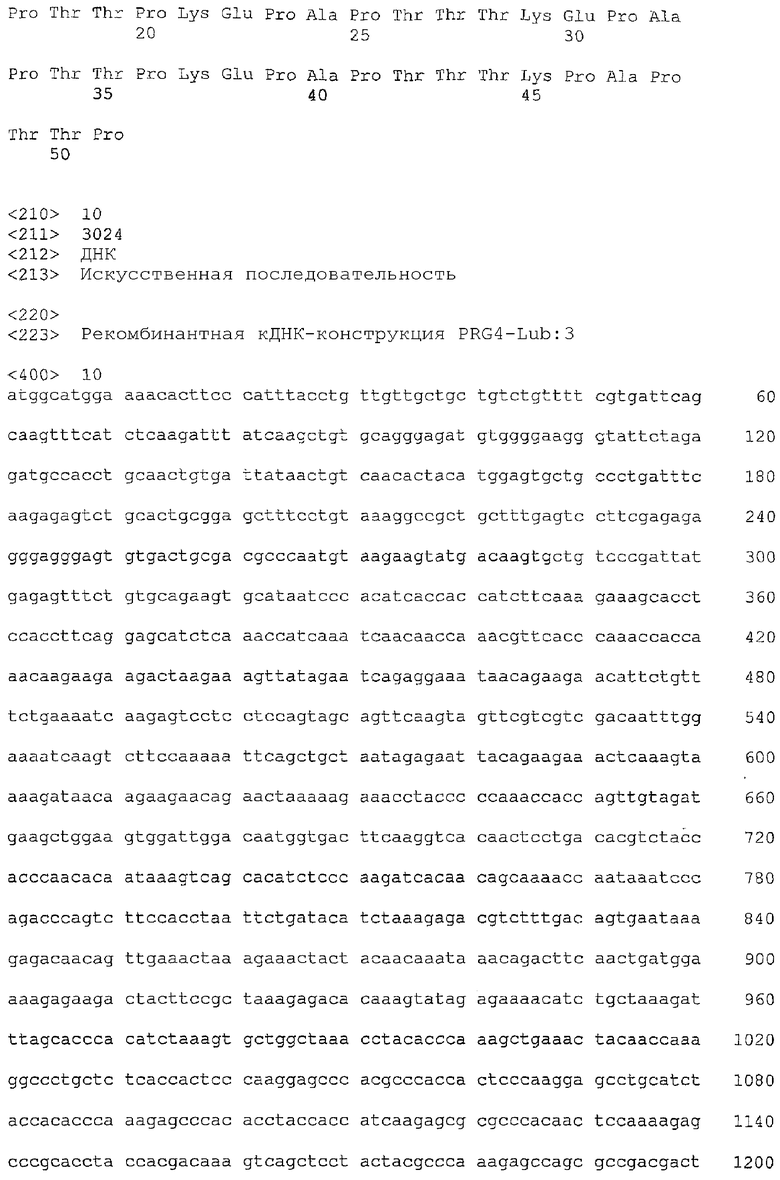


























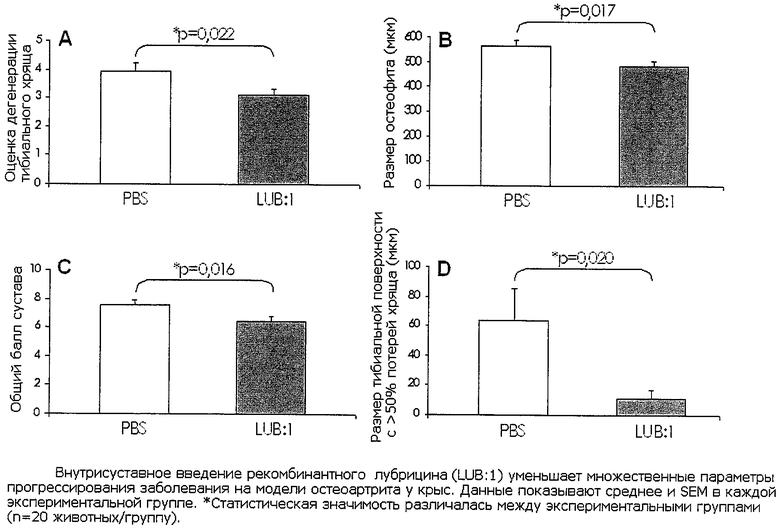
Изобретение относится к области биотехнологии и может быть использовано в медико-биологической промышленности при получении препаратов, используемых в качестве смазывающих веществ, антиадгезивных средств и/или внутрисуставных добавок. В результате замены части кодируемой экзоном 6 аминокислотной последовательности человеческого белка PRG-4 искусственным полипептидом, включающим 4-15 последовательностей КЕРАРТТ или КЕРАРТТ-подобных последовательностей, получены рекомбинантные белки с существенно меньшим, чем у природного лубрицина, числом гликозилируемых повторов, которые сохраняют при этом его смазывающие свойства. Предлагается использование новых рекомбинантных белков в составе фармацевтических композиций и в способах лечения, где традиционно применяется природный лубрицин. Применение настоящего изобретения в медицинских целях имеет ряд преимуществ, связанных с упрощением, по сравнению с нативным белком, как синтеза рекомбинантных лубрицинов, так и манипуляций с ними. 15 н. и 13 з.п. ф-лы, 1 ил., 3 табл.
1. Выделенный рекомбинантный белок, обладающий смазывающими свойствами лубрицина, характеризующийся последовательностью нативного белка человека PRG-4, в которой часть аминокислотной последовательности, кодируемой экзоном 6, от Ala в положении 374 до Pro в положении 847 заменена искусственным полипептидом с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 9, 13, 17, 21 и 25.
2. Выделенный рекомбинантный белок, обладающий смазывающими свойствами лубрицина, аминокислотная последовательность которого характеризуется SEQ ID NO:7, 11, 15, 19 или 23.
3. Белок по п.1 или 2, который связан O-связью с β-(l-3)-Gal-GalNac.
4. Выделенный полинуклеотид, кодирующий рекомбинантный белок, с последовательностью, по существу, соответствующей последовательности нуклеиновой кислоты, которая определяет аминокислотную последовательность рекомбинантного белка по п.1 или 2.
5. Полинуклеотид по п.4, где последовательность полинуклеотида, по существу, соответствует последовательности SEQ ID NO:6, 10, 14, 18 или 22.
6. Выделенный полинуклеотид, по существу, соответствующий полинуклеотиду, который по всей своей длине по крайней мере на 80% идентичен последовательности SEQ ID NO:6, 10, 14, 18 или 22 и при этом кодирует рекомбинантный лубрицин с аминокислотной последовательностью SEQ ID NO:7, 11, 15, 19 или 23 соответственно.
7. Полинуклеотид по п.6, идентичность которого составляет по крайней мере 90%.
8. Полинуклеотид по п.6, идентичность которого составляет по крайней мере 95%.
9. Полинуклеотид по п.6, идентичность которого составляет по крайней мере 99%.
10. Фармацевтическая композиция, обладающая смазывающими свойствами лубрицина, содержащая терапевтически эффективное количество белка по п.1 или 2 в фармацевтически приемлемом носителе.
11. Фармацевтическая композиция со свойствами синовиальной жидкости, содержащая терапевтически эффективное количество белка по п.1 или 2 в фармацевтически приемлемом носителе.
12. Фармацевтическая композиция для покрытия искусственных конечностей и суставов, содержащая терапевтически эффективное количество белка по п.1 или 2 в фармацевтически приемлемом носителе.
13. Фармацевтическая композиция для снижения эрозии хряща у индивида, содержащая терапевтически эффективное количество белка по п.1 или 2 в фармацевтически приемлемом носителе.
14. Композиция по любому из пп.10-13, дополнительно содержащая гиалуронан или гилан.
15. Способ улучшения смазывания сустава у индивида, страдающего остеоартритом, включающий:
получение композиции по п.10 и введение указанной композиции в сустав индивида.
16. Способ улучшения смазывания хряща у индивида, страдающего остеоартритом, включающий:
получение композиции по п.10 и введение указанной композиции в хрящ индивида.
17. Способ по п.15, дополнительно включающей стадию, выбранную из группы, состоящей из: введения индивиду анестетика; введения индивиду противовоспалительного лекарственного средства; введения индивиду антибиотика; отсасывание у индивида жидкости; промывку ткани индивида и визуализацию ткани индивида.
18. Способ по п.15, где индивид выбран из группы, состоящей из мыши, крысы, кошки, собаки, лошади и человека.
19. Способ по п.18, где индивидом является человек.
20. Способ лечения индивида, у которого нарушено оптимальное функционирование синовиальных соединений в результате снижения смазывания сустава, включающий:
получение композиции по п.10 или 11 и
введение указанной композиции индивиду.
21. Способ снижения боли в суставах у индивида, вызываемой нагрузкой под действием массы и опосредованной остеоартритом, включающий:
получение композиции по п.10 и введение указанной композиции индивиду.
22. Вектор экспрессии, содержащий полинуклеотид по п.4, функционально связанный с последовательностью, регулирующей экспрессию.
23. Способ получения рекомбинантного белка лубрицина, включающий:
культивирование клеток млекопитающих, трансформированных подходящим экспрессионным вектором по п.22, в жидкой культуральной среде и выделение рекомбинантного белка из среды.
24. Способ по п.23, где указанное выделение белка включает:
концентрирование белка путем фильтрации среды через мембрану;
сбор оставшегося белка из указанной мембраны и
солюбилизацию собранного белка в забуференном солевом растворе, содержащем гидрохлорид L-аргинина в концентрации от 0,1 до 2,0 М.
25. Способ по п.23, где клетками являются клетки китайского хомячка.
26. Способ по п.25, где клетками китайского хомячка являются клетки DUKX СНО.
27. Способ по п.24, где концентрация гидрохлорида L-аргинина составляет 0,5 М.
28. Способ лечения остеоартрита у пациента, включающий:
получение композиции по п.10 и
введение указанной композиции индивиду.
Приоритет по пунктам:
14.08.2003 по пп.1-28.
| JAY G | |||
| ET AL, J Reumatol, 27(3), 594-600, 2000 | |||
| JAY G | |||
| ET AL., Glycoconj | |||
| J., 18(10), 807-815, 2001 | |||
| WO 00/64930 A2, 02.11.2000. |
Авторы
Даты
2009-12-20—Публикация
2004-08-13—Подача