Изобретение относится к новым гексафторизопропанолзамещенным производным циклогексана формулы (I)

где R1 обозначает водород, низший алкил, фтор-низший алкил, низший алкил-карбонил, фтор-низший алкил-карбонил, арил-низший алкил, циклоалкил-низший алкил, циклоалкил-карбонил или циклоалкил-низший алкил-карбонил;
R2 обозначает водород или низший алкил;
R3 обозначает низший алкил, арил-низший алкил, гетероциклил-низший алкил или низшую алкоксигруппу-карбонил, или, если Х не обозначает простую связь, или, если Х обозначает простую связь и m не равен 0, R3 может быть также гидроксигруппой;
R4 обозначает арил или гетероциклил;
R5 обозначает водород, низший алкил, арил, гетероциклил, арил-низший алкил или гетероциклил-низший алкил;
Х обозначает простую связь, SO2, СО, С(O)O или C(O)N(R5);
m обозначает 0, 1, 2 или 3;
n обозначает 0 или 1;
и их фармацевтически приемлемым солям и сложным эфирам.
Кроме того, изобретение относится к способу получения названных выше соединений, фармацевтическим препаратам, содержащим такие соединения, а также к применению этих соединений для получения фармацевтических препаратов.
Х-рецепторы печени (LXRs) являются членами семейства ядерных гормональных рецепторов. LXRs активируются посредством эндогенных оксистеролов и регулируют транскрипционный контроль многочисленных путей метаболизма. Описаны два подтипа, LXRα и LXRβ (Willy et al., Genes Dev. 1995, 9:1033-45; Song et al., Proc Natl Acad Sci USA.1994, 91:10809-13). LXRβ экспрессирует посредством убиквитинизации, в то время, как LXRα предпочтительно экспрессирует в тканях, метабилизирующих холестерин, таких как ткани печени, жира, кишечника и макрофага. LXRs модулируют различные физиологические ответы, включающие регуляцию холестериновой абсорбции, элиминирование холестерина (синтез желчной кислоты) и транспорт холестерина из периферических тканей через плазму липопротеинов в печень. LXRs включены также в метаболизм глюкозы, холестериновый метаболизм в мозгу, клеточную дифференциацию и воспалительный процесс.
В настоящее время приблизительно половина всех пациентов с коронарно-артериальной болезнью имеют низкие концентрации холестерина ЛВП (липопротеины высокой плотности) в плазме. Атеропротекторная функция ЛВП впервые привлекла внимание почти 25 лет назад и стимулировала привлечение генетических и экологических факторов, влияющих на ЛВП уровни (Miller N.E., Lipids, 1978, 13^ 914-9). Защитная функция ЛВП вытекает из их роли в процессе, связанном с обратным транспортом холестерина. ЛВП опосредуют удаление холестерина из клеток в периферических тканях, включая пенные клетки макрофага в атеросклеротически поврежденных стенках артерий. ЛВП доставляют затем этот холестерин в печень и стерин-метаболизирующие органы для превращения в желчь и удаления из организма. Исследования показали, что ЛВП-Х уровни предопределяют риск коронарно-артериальной болезни независимо от уровней холестерина ЛНП (липопротеины низкой плотности) (Gordon et al., Am. J. Med. 1977, 62, 707-714).
Проведенное в настоящее время исследование среди американцев в возрасте от 20 лет и старше показало, что доля имеющих ЛВП-Х менее 35 мг/дл, составляет 16% (у мужчин) и 5,7% (у женщин). Существенное увеличение ЛВП-Х достигается посредством лечения ниацином в различных композициях. Однако существенные нежелательные побочные эффекты ограничивают терапевтическую эффективность этого метода.
Было установлено, что до 90% из 14 млн. пациентов с диагнозом диабет типа 2 в США имеют излишек веса или ожирение, и высокая доля пациентов с диабетом 2 типа имеет аномальные концентрации липопротеинов. Исследование показало, что преобладание общего холестерина >240 мг/дл обнаружено у 37% диабетиков-мужчин и 44% у диабетиков-женщин. Соответствующие показатели для ЛНП-Х >160 мг/дл составляют 31% и 44% соответственно, показатели ЛВП-Х <35 мг/дл составляют 28% и 11% у диабетиков-мужчин и диабетиков-женщин соответственно. Диабет является болезнью, при которой способность пациента контролировать уровни глюкозы в крови уменьшается из-за частичного нарушения ответа на воздействие инсулина. Диабет типа 2 (Т2Д), называемый также инсулиннезависимый сахарный диабет (NIDDM), поражает 80-90% больных диабетом пациентов в развитых странах. При Т2Д островки Лангерганса поджелудочной железы продолжают продуцировать инсулин. Однако органы-мишени, на которые направлено действие инсулина, главным образом, мышцы, печень и жировые ткани, проявляют полную резистентность к инсулиновой стимуляции. Чтобы компенсировать кажущийся недостаток инсулина, организм продолжает вырабатывать нефизиологически высокие уровни инсулина, которые в конце концов уменьшаются на последней стадии болезни из-за истощения и неспособности поджелудочной железы вырабатывать инсулин. Таким образом, Т2Д представляет собой сердечно-сосудистым метаболический синдром, ассоциированный со множеством сопутствующих заболеваний, включающих инсулиновую резистентность, дислипидемию, гипертензию, эндотелиальную дисфункцию и воспалительный атеросклероз.
Первая стадия лечения дислипидемии и диабета в настоящее время обычно включает пониженные жировую и глюкозовую диеты, физические упражнения и снижение веса. Однако результаты лечения могут быть умеренными и по мере прогрессирования болезни становится необходимым лечение различных метаболических дефицитных состояний, например, липид-модулирующими агентами такими, как статины и фибраты для дислипидемии, и гипогликемическими лекарствами, например, сульфонилуреазой, метформином или сенсибилизирующими агентами, относящимися к тиазолидиндионовому (TZD) классу PPARγ-агонистов в случае инсулиновой резистенции. Проведенные недавно исследования предоставили доказательство того, что модуляторы LXRs могут привести к соединениям с усиленным терапевтическим потенциалом и вследствие этого модуляторы LXRs должны улучшать плазменный липидный профиль и повышать ЛВП-Х-уровни (Lund et al., Arterioscler. Thromb. Vase. Biol. 2003, 23:1169-77). Известно также, что LXRs контролируют отток холестерина из пенных клеток макрофага в атеросклеротически поврежденнных стенках артерий, и агонисты LXRs, как было показано, проявляют атеропротекторные свойства (Joseph and Tontonoz, Curr. Opin. Pharmacol. 2003, 3:192-7). Таким образом, модуляторы LXRs должны быть эффективными в лечении атеросклеротической болезни, которая вызывает сердечно-сосудистую патологию и смертность от инсульта и болезни сердца. Недавно проведенные исследования позволили предположить, что существует независимый LXR, вызывающий воздействие на инсулиновую сенсибилизацию в дополнение к его роли при атерозащите (Cao et al., J Biol Chem. 2003, 278:1131-6). Таким образом, LXR модуляторы могут проявлять значительную терапевтическую эффективность при повышении ЛВП и атерозащите с дополнительным воздействием на диабет, сравнимым со стандартной терапией.
Новые соединения по настоящему изобретению, как было установлено, одновременно и очень эффективно связаны как с селективной активностью LXRα и LXRβ, так и с совместной активностью LXRα и LXRβ. Следовательно, происходит снижение абсорбции холестерина, увеличение ЛВП-холестерина, снижение воспалительного атеросклероза. Так как многочисленные случаи комбинированного гомеостаза дислипидемии и холестерина относятся к LXR модуляторам, новые соединения по настоящему изобретению обладают повышенным терапевтическим потенциалом по сравнению с соединениями, уже известными из уровня техники. Вследствие этого они могут быть применены при профилактике и лечении болезней, опосредованных LXRα и/или LXRβ агонистами. Такие болезни включают повышенные липидный и холестериновый уровни, в частности низкий ЛВП-холестерин, высокий ЛНП-холестерин, атеросклеротические болезни, диабет, особенно инсулиннезависимый сахарный диабет, метаболический синдром, дислипидемию, болезнь Альцгеймера, сепсис и воспалительные заболевания, например, колит, панкреатит, холестаз-фиброз печени, псориаз и другие воспалительные заболевания кожи, и болезни, имеющие воспалительный компонент такие, как болезнь Альцгеймера или ухудшение когнитивной функции. Кроме того, новые соединения по настоящему изобретению могут быть использованы для лечения и профилактики возрастной и наследственной (например, болезнь Старгардта) макуларной дегенерации.
Другие соединения, которые связаны и активируют LXRα и LXRβ, были предложены ранее (например, в WO 03/099769). Однако еще существует потребность в новых соединениях с улучшенными свойствами. Настоящее изобретение предлагает новые соединения формулы (I), которые связаны с LXRα и/или LXRβ. Соединения по настоящему изобретению неожиданно обнаружили улучшенные фармакологические свойства по сравнению с соединениями, уже известными из уровня техники, в отношении, например, метаболической стабильности, биодоступности и активности.
Если не указано особо, следующие определения приводятся, чтобы проиллюстрировать и определить значение и объем различных терминов, используемых для описания настоящего изобретения.
В настоящем описании термин "низший" используется для обозначения группы, включающей от одного до семи, предпочтительно, от одного до четырех, атомов углерода.
Термин "галоген" относится к фтору, хлору, брому и йоду, при этом фтор, хлор и бром являются предпочтительными.
Термин "алкил", один или в комбинации с другими группами, относится к разветвленному или прямолинейному моновалентному, насыщенному алифатическому углеводородному радикалу, содержащему от одного до двадцати атомов углерода, предпочтительно от одного до шестнадцати атомов углерода, более предпочтительно от одного до десяти атомов углерода. Низшие алкильные группы, описанные ниже, также являются предпочтительными алкильными группами.
Термин "низший алкил", один или в комбинации с другими группами, относится к разветвленному или прямолинейному моновалентному алкильному радикалу, содержащему от одного до семи атомов углерода, предпочтительно от одного до четырех атомов углерода. Этот термин далее иллюстрируется такими радикалами, как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил и подобные им.
Термин "фтор-низший алкил" относится к низшей алкильной группе, которая моно- или многократно замещена фтором. Примерами фтор-низшей алкильной группы являются CFH2, CF2H, CF3, CF3CH2, CF3(CH2)2, (CF3)2СН и CF2H-CF2.
Термин "аминогруппа", одна или в комбинации с другими группами, означает первичную, вторичную или третичную группу, связанную через атом азота, с вторичной аминогруппой, имеющей алкильный или циклоалкильный заместитель, и третичной аминогруппой, имеющей два одинаковых или различных алкильных или циклоалкильных заместителя, или два азотных заместителя, образующих вместе цикл, например, -NH2, метиламиногруппу, этиламиногруппу, диметиламиногруппу, диэтиламиногруппу, метилэтиламиногруппу, пирролидин-1-ил или пиперидиновую группу и т.п.
Термин "циклоалкил" относится к моновалентному карбоциклическому радикалу, содержащему от 3 до 10, предпочтительно от 3 до 6, атомов углерода, такому как циклопропил, циклобутил, циклопентил или циклогексил.
Термин "алкоксигруппа" относится к группе R'-O-, где R' обозначает алкил. Термин "низшая алкоксигруппа" относится к группе R'-O-, где R' обозначает низший алкил.
Термин "фтор-низшая алкоксигруппа" относится к группе R''-O-, где R'' обозначает фтор-низший алкил. Примерами фтор-низшая алкоксигруппа являются CFH2-O, CF2H-О, CF3-О, CF3CH2-О, CF3(СН2)2-O, (CF3)2CH-O и CF2H-CF2-O.
Термин "алкилен" относится к прямолинейной или разветвленной дивалентной насыщенной алифатической углеводородной группе, содержащей от 1 до 20 атомов углерода, предпочтительно от 1 до 16 атомов углерода, более предпочтительно до 10 атомов углерода. Низшие алкиленовые группы, как описано ниже, также являются предпочтительными алкиленовыми группами. Термин "низший алкилен" относится к прямолинейной или разветвленной дивалентной насыщенной алифатической углеводородной группе, содержащей от 1 до 7 атомов углерода, предпочтительно от 1 до 6 или от 3 до 6 атомов углерода. Прямолинейные алкиленовые или низшие алкиленовые группы являются предпочтительными.
Термин "арил", один или в комбинации с другими группами, относится к фенильной или нафтильной группе, предпочтительно к фенильной группе, которая может быть необязательно замещена от 1 до 5, предпочтительно от 1 до 3, заместителями, независимо выбранными из группы, включающей низший алкил, низшую алкоксигруппу, галоген, гидроксигруппу, CN, CF3, аминогруппу, аминокарбонил, карбоксильную группу, NO2, диоксогруппу-низший алкилен (образующий, например, бензодиоксильную группу), низший алкилсульфонил, аминосульфонил, низший алкилкарбонил, низшую алкилкарбонилоксигруппу, низший алкилкарбонил-NH, низший алкоксикарбонил, фтор-низший алкил, фтор-низшую алкоксигруппу, циклоалкил и и фенилоксигруппу. Предпочтительными заместителями являются галоген, низший алкил, фтор-низший алкил, CN и низший алкоксикарбонил.
Термин "гетероциклил", один или в комбинации с другими группами, означает насыщенную, частично ненасыщенную или ароматическую 5-10-членную, моно- или бициклическую гетероциклическую группу, содержащую один или более гетероатомов, предпочтительно от одного до трех, выбранных из азота, кислорода и серы. При необходимости он может быть замещен при одном или более углеродном атоме, например, галогеном, низшим алкилом, низшей алкоксигруппой, оксогруппой и т.п. и/или при вторичном атоме азота (например, -NH-) низшим алкилом, циклоалкилом, фенил-низшим алкоксикарбонилом, низшим алкилкарбонилом, фенилом или фенил-низшим алкилом, или при третичном атоме азота (например, =N-) оксидной группой, при этом предпочтительными являются галоген и низший алкил. Примерами таких гетероциклических групп являются пирролидинил, пирролил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, пиразолил, тиазолил, тетразолил, изотиазолил, имидазолил (например, имидазолил-4-ил и 1-бензилоксикарбонил-4-ил), бензоимидазолил, пиразолил, пиридинил, пиразинил, пиридазинил, пиримидинил, гексагидропиримидинил, фурил, тиенил, тиазолил, оксазолил, изооксазолил, индолил (например, 2-индолил), индазолил, хинолил (например, 2-хинолил, 3-хинолил и 1-оксидо-2-хинолил), изохинолил (например, 1-изохинолил и 3-изохинолил), тетрагидрохинолил (например, 1,2,3,4-тетрагидро-2-хинолил), 1,2,3,4-тетрагидроизохинолил (например, 1,2,3,4-тетрагидро-1-оксогидроизохинолил), тетрагидропиранил, хиноксалинил, оксопирролидинил и бензо[b]тиофенил. Предпочтительными являются тиазолил, имидазолил и пиразолил. Гетероциклическая группа может также иметь структуру замещения, описанную ранее в связи с термином "арил". Ароматические гетероциклические группы являются предпочтительными.
Термин "отщепляемая группа" относится к группе, которая может быть заменена посредством нуклеофильного замещения (например, вторичный амин). Типичными отщепляемыми группами являются, например: Cl, Br, I, O-SO2 - низший алкил (где O-SO2-СН3 = OMs), O-SO2-фтор-низший алкил (где O-SO2-CF3 = OTf), O-SO2-арил (где О-SO2-п-толил = OTs), О- (п-нитрофенил).
Термин "защитная группа" относится к группам, которые временно используются для защиты функциональных групп, в частности гидроксильных групп. Примерами защитных групп являются бензил, п-метоксибензил, трет-бутилдиметилсилил, триэтилсилил, триизопропилсилил и трет-бутилдифенилсилил.
Соединения формулы (I) могут образовывать фармацевтически приемлемые кислотно-аддитивные соли. Примерами таких фармацевтически приемлемых солей являются соли соединений формулы (I) с физиологически совместимыми минеральными кислотами такими, как хлористоводородная кислота, серная кислота, сернистая кислота или фосфорная кислота; или органическими кислотами такими, как метансульфоновая кислота, п-толуолсульфоновая кислота, уксусная кислота, молочная кислота, трифторуксусная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, винная кислота, янтарная кислота или салициловая кислота. Термин "фармацевтически приемлемые соли" относится к таким солям. Соединения формулы (I) могут, кроме того, образовывать соли с основаниями. Примерами таких солей являются щелочные, щелочно-земельные и аммонийные соли такие, как, например,
Na-, K-, Са- и триметиламмонийные соли. Термин "фармацевтически приемлемые
соли" также относится к таким солям. Соли, образующиеся посредством присоединения основания, являются предпочтительными.
Термин "фармацевтически приемлемые сложные эфиры" включает производные соединений формулы (I), в которых карбоксильная группа превращена в сложно-эфирную. Низший алкил, гидроксигруппа-низший алкил, низшая алкоксигруппа-низший алкил, аминогруппа-низший алкил, моно- или ди-низший алкил-аминогруппа-низший алкил, морфолино-низший алкил, пирролидино-низший алкил, пиперидино-низший алкил, пиперазино-низший алкил, низший алкил-пиперазино-низший алкил и аралкил сложные эфиры являются примерами подобных эфиров. Метиловый, этиловый, пропиловый, бутиловый и бензиловый эфиры являются предпочтительными сложными эфирами. Термин "фармацевтически приемлемые сложные эфиры" включает, кроме того, производные соединений формулы (I), в которых гидроксильные группы могут быть превращены в соответствующие сложно-эфирные группы при помощи неорганических или органических кислот таких, как азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, яблочная кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и им подобных, которые нетоксичны по отношению к живому организму.
Конкретно, настоящее изобретение относится к соединениям формулы (I)

где R1 обозначает водород, низший алкил, фтор-низший алкил, низший алкил-карбонил, фтор-низший алкил-карбонил, арил-низший алкил, циклоалкил-низший алкил, циклоалкил-карбонил или циклоалкил-низший алкил-карбонил;
R2 обозначает водород или низший алкил;
R3 обозначает низший алкил, арил-низший алкил, гетероциклил-низший алкил или низшую алкоксигруппу-карбонил, или, если Х не обозначает простую связь, или, если Х обозначает простую связь и m не равно 0, R3 может быть также гидроксигруппой;
R4 обозначает арил или гетероциклил;
R5 обозначает водород, низший алкил, арил, гетероциклил, арил-низший алкил или гетероциклил-низший алкил;
Х обозначает простую связь, SO2, CO, С(O)O или C(O)N(R5);
m обозначает 0, 1, 2 или 3;
n обозначает 0 или 1;
и их фармацевтически приемлемым солям и сложным эфирам.
Соединения формулы (I) по отдельности являются предпочтительными и их физиологически приемлемые соли по отдельности являются предпочтительными и их фармацевтически приемлемые сложные эфиры по отдельности являются предпочтительными, при этом особенно предпочтительными являются соединения формулы (I).
Соединения формулы (I) имеют два или более ассиметричных атома углерода, и могут поэтому существовать в виде энантиомерной смеси, смеси стереоизомеров или в виде оптически чистых соединений.
Предпочтительными соединениями по настоящему изобретению являются транс-соединения. Предпочтительные соединения формулы (I) описаны выше и характеризуются следующей формулой (IA)
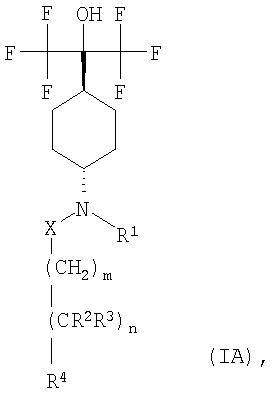
где R1, R2, R3, R4, X, m и n описаны выше, и их фармацевтически приемлемыми солями и сложными эфирами.
Предпочтительными соединениями формулы (I) по описанию выше, являются соединения, где R1 обозначает водород, низший алкил, фтор-низший алкил, низший алкил-карбонил, фтор-низший алкил-карбонил, арил-низший алкил, циклоалкил-низший алкил или циклоалкил-карбонил. Предпочтительно, R1 обозначает фтор-низший алкил, арил-низший алкил или циклоалкил-низший алкил. Более предпочтительно, R1 обозначает 2,2,2-трифторэтил, бензил или циклопропилэтил.
Другими предпочтительными соединениями формулы (I) по описанию выше являются соединения, где n обозначает 1, R2 обозначает водород или низший
алкил, и R3 обозначает низший алкил, арил-низший алкил или низшую алкоксигруппу-карбонил, или, если Х не обозначает простую связь, или, если Х обозначает простую связь и m не равно 0, R3 может быть также гидроксильной группой. Предпочтительно, R2 обозначает низший алкил. Более предпочтительно, R2 обозначает метил. Другими предпочтительными соединениями являются такие, где R3 обозначает низший алкил, в частности где R3 обозначает метил.
Другой предпочтительный вариант по настоящему изобретению относится к соединениям формулы (I) по описанию выше, где R4 обозначает арил или гетероциклил, выбранный из группы, включающей тиазолил, имидазолил и пиразолил, при этом тиазолил, имидазолил и пиразолил необязательно замещены от 1 до 3 заместителями, независимо выбранными из группы, включающей низший алкил и галоген. Соединения, где R4 обозначает арил, являются предпочтительными, особенно предпочтительными являются соединения, где R4 обозначает фенил.
Другими предпочтительными соединениями формулы (I) по описанию выше являются такие соединения, где m=0 или 1. Соединения, где m=0, и соединения, где m=1, по отдельности представляют предпочтительные варианты по настоящему изобретению. Предпочтительно, m=0. Другой предпочтительный вариант по настоящему изобретению относится к соединениям формулы (I) по описанию выше, где n=0.
Следующий предпочтительный вариант по настоящему изобретению относится к соединениям формулы (I) по описанию выше, где Х обозначает простую связь, SO2, СО или С(O)O. Предпочтительно, Х обозначает SO2.
В частности, предпочтительными соединениями являются соединения формулы (I), описанные в примерах в качестве индивидуальных соединений, а также в качестве их фармацевтически приемлемых солей и в качестве их фармацевтически приемлемых сложных эфиров.
Предпочтительными соединениями формулы (I) являются соединения, выбранные из группы, включающей:
транс-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-бензил-2,2,2-трифтор-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамид, этиловый эфир
транс-фенил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексиламино]уксусной кислоты,
транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамид,
транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2,4-диметилтиазол-5-сульфоновой кислоты,
[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты,
этил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты,
этил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-4-метил-2-пропилтиазол-5-сульфоновой кислоты,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2,4-диметилтиазол-5-сульфоновой кислоты,
циклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2,4-диметилтиазол-5-сульфоновой кислоты,
этил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2,4-диметилтиазол-5-сульфоновой кислоты,
транс-N-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-этил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты,
[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты,
транс-2-[4-(бензилэтиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол,
транс-2-[4-(бензилпропиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол,
транс-2-[4-(бензилциклопропилметиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол,
транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]пропионамид,
бензил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)гексил]амид транс-циклопропанкарбоновой кислоты,
транс-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензамид,
транс-N-циклопропилметил-2-фенил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамид, фениловый эфир
транс-циклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]карбаминовой кислоты, бензиловый эфир
транс-циклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]карбаминовой кислоты,
(рап)-транс-2-{4-[циклопропилметил-(2-гидрокси-2-фенилэтил)амино]циклогексил}-1,1,1,3,3,3-гексафторпропан-2-ол,
транс-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]-сульфонамид,
транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид(рац)-транс-1-фенилэтансульфоновой кислоты,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2-фенилпропан-2-сульфоновой кислоты,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид(рац)-транс-1,2-дифенилэтансульфоновой кислоты, метиловый эфир
(рац)-транс-3-(2-фенил-2-{(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфамоил}этил)бензойной кислоты, и цис-N-этил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид, и их фармацевтически приемлемые соли и сложные эфиры.
Особенно предпочтительными соединениями формулы (I) являются соединения, выбранные из группы, включающей:
транс-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид и
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2-фенилпропан-2-сульфоновой кислоты, и их фармацевтически приемлемые соли и сложные эфиры.
Понятно, что соединения общей формулы (I) по настоящему изобретению могут быть превращены по функциональным группам в производные, которые способны превращаться в исходные соединения в условиях in vivo.
Изобретение относится далее к способу получения соединений формулы (I) по определению выше, включающему
а) реакцию соединения формулы (II)
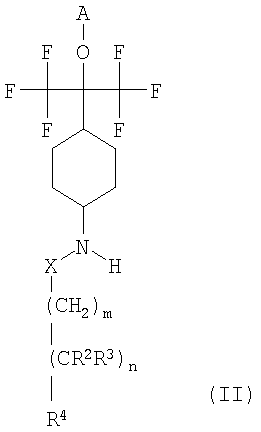
с соединением LG-R1,
где R1, R2, R3, R4, X, m и n определены выше, А обозначает водород или защитную группу, LG обозначает отщепляемую группу (такую, например, как I, Br, Cl, трифлат, мезилат, тозилат),
или
б) реакцию соединения формулы (III)
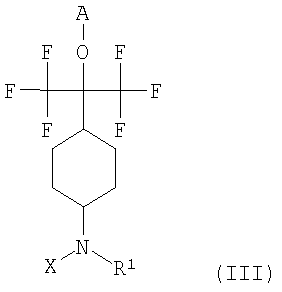
с соединением LG-Х-(СН2)m(CR2R3)n-R4,
где R1, R2, R3, R4, X, m и n определены выше, А обозначает водород или защитную группу и LG обозначает отщепляемую группу (такую, как, например I, Br, Cl, или, если Х обозначает простую связь, LG может также обозначать трифлат, мезилат, тозилат),
и удаление защитной группы А.
Реакция соединения формулы (II) с соединением LG-R1 и удаление защитной группы А при необходимости могут быть проведены в условиях, известных специалистам в данной области техники. Такие реакции соединения формулы (II) стандартно проводят путем обработки сильным основанием таким, как бис(триметилсилил)амид лития, или в некоторых случаях в присутствии основания такого, как ДВУ в растворителе таком, как, например, ТГФ или ДМФ при соответствующей температуре. Реакция соединения формулы (II) с соединением LG-X-(CH2)m(CR2R3)n-R4 и удаление защитной группы А при необходимости могут быть проведены в условиях, известных специалистам в данной области техники. Такие реакции соединения формулы (III) могут быть стандартно проведены в присутствии основания такого, как, например NEt3, в растворителе типа дихлорметана или тетрагидрофурана при соответствующей температуре. Защитную группу удаляют с использованием стандартных методов, в общем известных из уровня техники, например, таких, как десилилирование с использованием тетрабутиламмонийфторида (ТБАФ).
Настоящее изобретение относится также к соединениям формулы (I) по определению выше, полученным способом, описанным выше.
Соединения формулы (I) могут быть получены методами, известными из уровня техники или методами, описанными выше. Если не указано иначе, заместители R1, R2, R3, R4, R5, X, m и n описаны выше.
Получение производных, в которых R1 обозначает водород, проводят в соответствии с приведенной ниже схемой 1.
Схема 1
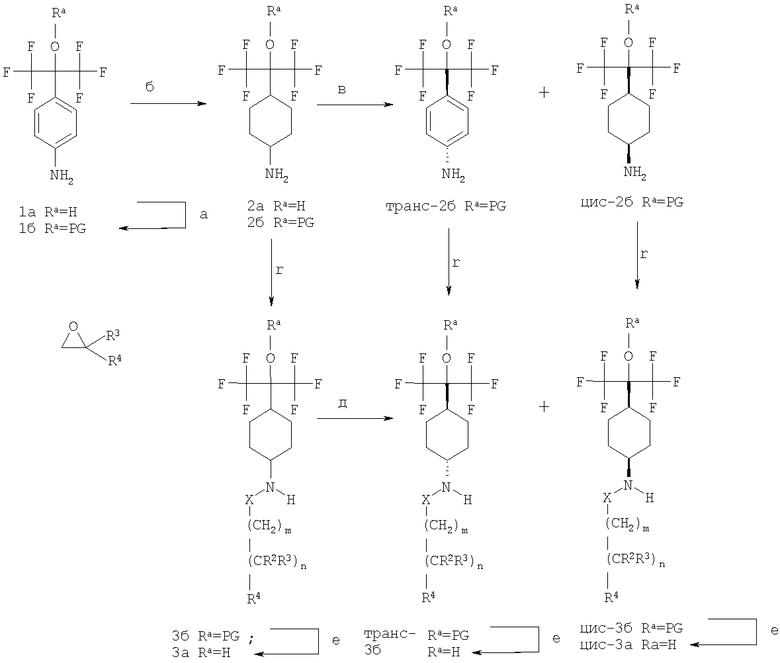
Анилин 1а может быть O-защищен с образованием соединения 1б (стадия а) с помощью соответствующей защитной группы «PG», например, такой, как триэтилсилильная или трет-бутилдиметилсилильная группа, посредством обработки силилирующим агентом (например, триэтилсилилхлоридом или трет-бутилдиметилсилилхлоридом соответственно) в присутствии подходящего основания (например, ДВУ, имидазол). Незащищенный анилин 1а или защищенный анилин 1б могут быть превращены в смесь транс-/цис-циклогексанов 2а и 2б в соотношении 1:1, соответственно, гидрированием в соответствующем растворителе таком, как АсОН, метанол или этанол, в присутствии катализатора, например, Pt на угле или PtO2, в кислых условиях (стадия б). Фильтрование и выпаривание растворителя приводит к соединениям 2а или 2б в форме их аммонийных солей с депротонизацией кислоты в виде противоиона. Свободные амины могут быть получены щелочной обработкой (например, распределением между водным раствором NaOH и AcOEt). Свободные амины транс- и цис-изомеров транс-2б и цис-2б могут быть разделены с помощью хроматографии (стадия в).
Введение «Х-(CH2)m-CR2R3)nR4»-фрагмента (стадия г), приводящая к производным 3а, 3б или транс-3б или цис-3б, может быть проведено одним из методов, описанных ниже. Чтобы получить соединения 3а, 3б, транс-3б или цис-3б, в которых Х обозначает простую связь, 2а, 2б, транс-2б или цис-2б обрабатывают альдегидом CHO-(CH2)m-1-(CR2R3)n-R4 (где m=1-3) в присутствии восстановительного агента такого, как NaBCNH3, в соответствующем растворителе таком, как, например, этанол или метанол. Использование кетона R3-СО-R4 вместо CHO-(CH2)m-1-(CR2-R3)n-R4 приводит к производным, в которых Х обозначает простую связь, m=0, n=1 и R2 обозначает водород. Альтернативно, соединение 2а, предпочтительно 2б, транс-2б, или цис-2б может быть обработано алкилирующим агентом LG-(CH2)m-(CR2R3)n-R4, где LG обозначает отщепляемую группу такую, например, как Cl, Br, I, OSO2арил, OSO2CH3, OSO3CF3. Такое алкилирование проводят предпочтительно в присутствии основания (например, К2СО3) в подходящем растворителе типа ацетонитрила, ДМФ, ДМА или ТГФ. Чтобы получить соединения 3а, 3b, транс-3б или цис-3б, в котором Х обозначает СО, COO, CONR5 или SO2, 2а, 2б, транс-2б или цис-2б могут быть введены в реакцию с хлоридом Cl-X-(CH2)m-(CR2R3)n-R4 в присутствии соответствующего основания такого, например, как ДИПЭА, NEt3 или N-метилморфолин. Когда Х обозначает СО и SO2, 3а, 3б, транс-3б или цис-3б могут быть получены введением в реакцию с карбоновой кислотой HOCO-(CH2)m-(CR2R3)n-R4 или сульфоновой кислоты HOSO2-(CH2)m-(CR2R3)n-R4 в присутствии обычного пептидного конденсирующего реагента такого, например, как этилендихлорид или N,N-дициклогексилкарбодиимид (если необходимо, в комбинации с 1-гидроксибензотриазолом), в подходящем растворителе (например, дихлорметане, ТГФ или ДМФ). Соединения 3а, 3б, транс-3б или цис-3б, в котором Х обозначает CONH, могут быть также получены введением в реакцию 2а, 2б, транс-2б или цис-2б с изоцианатом O=C=N-(CH2)m-(CR2R3)n-R4. Производные, в которых R3 обозначает гидроксигруппу, Х обозначает простую связь, и m=1, могут быть получены обработкой 2а, 2б, транс-2б или цис-2 оксираном (4).
Транс-3а, транс-3б и соответствующие цис-аналоги могут быть получены, при необходимости, из соединений 3а и 3б соответственно, с помощью хроматографии (стадия д). Удаление защитной группы (стадия е) проводят в соответствии с известными стандартными методиками такими, например, которые описаны в разделе «Protective groups in organic chemistry» by T.W. Greene and P.G.M.Wutts, 2nd Ed., 1991, N.Y. (например, десилилированием с использованием тетрабутиламмонийфторида).
Получение производных, в которых R1 обозначает низший алкил, фтор-низший алкил, низший алкил-карбонил, фтор-низший алкил-карбонил, арил-низший алкил, циклоалкил-низший алкил, циклоалкил-карбонил, циклоалкил-низший алкил-карбонил, проводят одним из методов, описанных ниже на схеме 2.
Схема 2
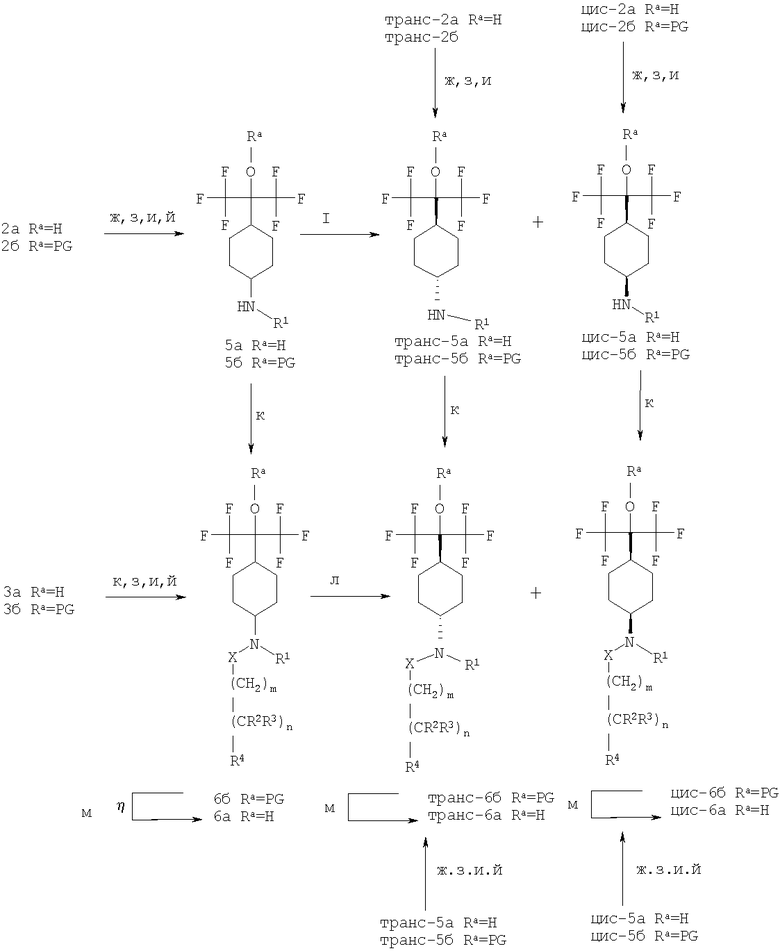
Обработка 2а, 2б, транс-2а, транс-2б, цис-2а или цис-2б ацилирующим агентом таким, как, например, ацетилхлорид R1-Cl или ангидрид уксусной кислоты (R1)2O, где
R1 обозначает низший алкил-карбонил, фтор-низший алкил-карбонил, циклоалкил-карбонил, циклоалкил-низший алкил-карбонил, в присутствии основания такого, как ДИПЭА, NEt3 или N-метилморфолин в растворителе типа дихлорметана, ТГФ или ДМФ приводит к производным 5а, 5б, транс-5а, транс-5б, цис-5а или цис-5б (стадия ж). Альтернативно, такое ацилирование может быть проведено с использованием карбоновой кислоты в присутствии обычного пептидного конденсирующего реагента такого, например, как этилендихлорид или дициклокарбодиимид (если необходимо, в комбинации с 1-гидроксибензотриазолом) в подходящем растворителе (например, дихлорметане, ТГФ или ДМФ).
Карбонильная группа необязательно может быть впоследствии удалена обработкой восстанавливающим реагентом таким, например, как ВНз в растворителе таком, как ТГФ, что приводит к 5а, 5б, транс-5а, транс-5б, цис-5а или цис-5б, где R1 обозначает низший алкил, фтор-низший алкил, циклоалкил-низший алкил (стадия з). Последние производные могут быть также получены обработкой 2а, 2б, транс-2а, транс-5б, цис-5а или цис-5б подходящим альдегидом или кетоном в присутствии восстанавливающего реагента такого, например, как NaBCNHa (стадия и) или обработкой алкилирующим реагентом таким, например, как низший алкил-LG, фтор-низший алкил-LG, арил-низший алкил-LG, циклоалкил-низший алкил-LG, где LG обозначает отщепляемую группу такую, например, как Cl, Br, I, OSO2арил, OSO2CH3, OSO2CF3 (стадия и). Обработка алкилирующим реагентом проводится предпочтительно в присутствии основания (например, ДБУ, К2СО3), или после депротонизации 2а, 2б, транс-2а, транс-2б, цис-2а, цис-2б, сильным основанием (например, бис(триметилсилил)амидом лития или диизопропиламидом лития). Те же самые методы (ж-й) могут быть использованы для превращения 3а, 3б, транс-3а, транс-3б, цис-3а, цис-3б в 6а, 6б, транс-6а, транс-6б, цис-6а, цис-6б соответственно. Для производных 5а, 5б, транс-5а, транс-5б, цис-5а или цис-5б, в которых R1 ограничивается R1, обозначающим низший алкил, фтор-низший алкил, арил-низший алкил, циклоалкил-низший алкил, Х-(CH2)m-(CR2R3)n-R4фрагмент может быть введен одним из методов, описанных на стадии г схемы 1 (стадия к).
Депротонизация производных 6б, транс-6б или цис-6б, где Х обозначает SO2, CO, m=1 и n=0, сильным основанием, например, бис(триметилсилил)амидом лития или диизопропиламидом лития, и последующая обработка кислородом низшего алкил-LG, арил-низший алкил-LG, гетероциклил-низший алкил-LG (где LG обозначает отщепляемую группу такую, например, как Cl, Br, I, OSO2арил, OSO2CH3, OSO2CF3) приводит к производным 6б, транс-6б или цис-6б с R3, обозначающим гидроксигруппу, низший алкил, арил-низший алкил, гетероциклил-низший алкил, соответственно, и где Х обозначает SO2, CO, m=0 и n=1.
Производные 6 (транс-6б или цис-6б), где Х обозначает SO2, СО, m=0 и n=1, могут быть депротонизированы сильным основанием, например, бис (триметилсилил) амидом лития или диизопропиламидом лития, и последовательно обработаны «низшим алкил-LG» (где LG обозначает отщепляемую группу такую, например, как Cl, Br, I, OSO2арил, OSO2CH3, OSO2CF3), с получением производных 6 (транс-6б или цис-6б), где Х обозначает SO2, СО, m=0, n=1 и R2 обозначает низший алкил.
Транс-5а, транс-5б, транс-6а, транс-6б и соответствующие цис-аналоги могут быть получены при необходимости из 3а и 3б, соответственно, с помощью хроматографии (стадия м). Удаление защитной группы (стадия м) проводят в соответствии с известными стандартными методиками такими, например, которые описаны в разделе «Protective groups in organic chemistry» by T.W.Greene and P.G.M.Wutts, 2nd Ed., 1991, N.Y. (например, десилилированием с использованием тетрабутиламмонийфторида).
Большое число соединений Cl-X-(CH2)m-(CR2R3)n-R4, CHO-(CH2)m-1-(CR2R3)n-R4, LG-(CH2)m-(CR2R3)n-R4 являются коммерчески доступными. Они могут быть получены также из родственных коммерчески доступных исходных веществ таких, например, как сложный эфир алкилОСО-(СН2)m-1-(CR2R3)n-R4, карбоновой кислоты HOCO-(CH2)m-1(CR2R3)n-R4, спирта HO-(CH2)m-(CR2R3)n-R4 или в случае, когда Х обозначает SO2, из сульфоновой кислоты HOSO2-(CH2)m-(CR2R3)n-R4 в соответствии со стандартными литературными методами, известными специалистам в области техники. В качестве типичных примеров таких превращений выбраны три примера: 1) превращение карбоновой кислоты НОСО(СН2)m-1-(CR2R3)n-R4 в соответствующий хлорангидрид карбоновой кислоты Cl-CO(CH2)m-1-(CR2R3)n-R4 обработкой. SOCl2 или POCl3 в соответствующем растворителе, например дихлорметане; 2) окисление спирта HO-(CH2)m-(CR2R3)n-R4 n, в альдегид CHO(CH2)m-1-(CR2R3)n-R4 (например, окислением по Шверну); 3) превращение спирта HO-(CH2)m-(CR2R3)n-R4 в производное LG-(CH2)m-(CR2R3)n-R4, с использованием, например, PBr3 с получением производного, в котором LG обозначает Br, или с использованием, например, метансульфонилхлорида (в присутствии основания такого, например, как NEt3) с получением производного, в котором LG обозначает OSO2CH3.
Эпоксиды 4, если они недоступны коммерчески, могут быть получены эпоксидированием алкенов CH2=CR3R4 с помощью обычно используемого эпоксидирующего агента такого, например, как м-хлорбензойная кислота, в соответствующем растворителе таком, например, как дихлорметан.
Если 3а, 3б, 6а, 6б, транс-3а, транс-3б, транс-6а, транс-6б, цис-3а, цис-3б, цис-6а или цис-6б содержат функциональную группу, не совместимую с одним из транс-соединений, описанных выше, эта функциональная группа может быть соответственно замещена до проведения превращения(ий) и депротонизирована снова на более поздней стадии. Такую защиту и депротонизацию проводят в соответствии с известными стандартными методиками такими, например, которые описаны в разделе "Protective groups in organic chemistry" by T.W.Greene and P.G.M.Wutts, 2nd Ed., 1991, N.Y.", и известны специалистам в данной области техники.
Превращение соединений формулы (I) в фармацевтически приемлемые соли может быть проведено путем обработки данного соединения неорганической кислотой, например, галогенводородной кислотой, такой, как, хлористоводородная кислота или бромистоводородная кислота, или неорганическими кислотами такими, как серная кислота, азотная кислота, форсфорная кислота и т.д., или органической кислотой такой, как, например, уксусная кислота, лимонная кислота, яблочная кислота, фумаровая кислота, винная кислота, метансульфоновая кислота или п-толуолсульфоновая кислота. Одним из методов образования таких солей является добавление 1/n эквивалентов кислоты, где n = числу протонов кислоты, к раствору соединения в соответствующем растворителе (например, этаноле, смеси этанол-вода, смеси тетрагидрофуран-вода) и удаление растворителя выпариванием или лиофилизацией. Соединения формулы (I) могут, кроме того, образовывать соли с физиологически совместимыми основаниями. Примерами таких солей являются щелочные, щелочно-земельные и аммонийные соли такие, например, как. Na-, К-, Са- и триметиламмонийные соли. Одним из методов образования такой соли является добавление 1/n эквивалентов основной соли такой, например, как М(ОН)n, где М обозначает катион металла или аммония и n = числу гидроксидных катионов, к раствору соединения в соответствующем растворителе (например, этаноле, смеси этанол-вода, смеси тетрагидрофуран-вода) и удаление растворителя выпариванием или лиофилизацией.
Превращение соединениий формулы (I) в фармацевтически приемлемые эфиры может быть проведено, например, обработкой соответствующей аминогруппы или гидроксигруппы, присутствующих в молекулах, карбоновой кислотой такой, как уксусная кислота, конденсирующими реагентами такими, как гексафторфосфат бензотриазол-1-илокси-трис(диметиламино)фосфония (ВОР), N,N-дициклогексилкарбодиимид (DCC), гидрохлорид N-(3-диметиламинопропил)-N'-этилкарбодиимида (EDCI) или тетрафторборат O-(1,2-дигидро-2-оксо-1-пиридил)-N,N,N,N-тетраметилурония (TPTU), с образованием сложного эфира или амида. Фармацевтически приемлемые эфиры могут быть получены обработкой соответствующих карбоксильных групп, присутствующих в молекулах, соответствующим спиртом с использованием одного из конденсирующих агентов, отмеченных выше.
В случае, если получение не описано в примерах, соединения формулы (I), а также все промежуточные продукты могут быть получены аналогичными методами или методами, соответствующими методам, представленным выше. Исходные соединения являются коммерчески доступными или известны из уровня техники.
Как отмечено выше, новые соединения по настоящему изобретению, как установлено, одновременно и очень эффективно связаны как с селективной активностью LXRα и LXRβ, так и с совместной активностью LXRα и LXRβ. Это приводит к снижению абсорбции холестерина, увеличению ЛВП-холестерина, снижению воспалительного атеросклероза. Так как многочисленные случаи комбинированного гомеостаза дислипидемии и холестерина относятся к LXR модуляторам, новые соединения по настоящему изобретению обладают повышенным терапевтическим потенциалом по сравнению с соединениями, уже известными из уровня техники. Вследствие этого они могут быть применены при профилактике и лечении болезней, модулируемых LXRα и/или LXRβ агонистами. Такие болезни включают повышенные липидный и холестериновый уровни, в частности низкий уровень ЛВП-холестерина, высокий уровень ЛНП-холестерина, атеросклеротические болезни, диабет, особенно инсулиннезависимый сахарный диабет, метаболический синдром, дислипидемию, болезнь Альцгеймера, сепсис и воспалительные заболевания, например, колит, панкреатит, холестаз-фиброз печени, псориаз и другие воспалительные заболевания кожи, и болезни, включающие воспалительный компонент такие, как болезнь Альцгеймера или ухудшенная/улучшаемая когнитивная функция. Кроме того, новые соединения по настоящему изобретению могут быть использованы для лечения и профилактики возрастной и наследственной (например, болезнь Старгардта) макулярной дегенерации.
Изобретение вследствие этого относится также к фармацевтическим композициям, включающим соединение по определению выше и фармацевтически приемлемый носитель и/или адъювант.
Кроме того, изобретение включает соединения по определению выше для применения в качестве терапевтически активных субстанций, в частности в качестве терапевтически активных субстанций для лечения и/или профилактики болезней, модулируемых LXRα и/или LXRβ агонистами, в частности в качестве терапевтически активных субстанций для лечения и/или профилактики повышенных липидных уровней, повышенных уровней холестерина, низкого ЛВП-холестерина, высокого ЛНП-холестерина, атеросклеротических болезней, диабета, инсулиннезависимого сахарного диабета, метаболического синдрома, дислипидемии, сепсиса, воспалительных заболеваний, кожных болезней, колита, панкреатита, холестаза печени, фиброза печени, макулярной дегенерации и/или болезни Альцгеймера.
В другом предпочтительном варианте изобретение относится к способу терапевтического и/или профилактического лечения болезней, модулируемых LXRα и/или LXRβ агонистами, в частности в качестве терапевтически активных субстанций для лечения и/или профилактики повышенных липидных уровней, повышенных уровней холестерина, низкого ЛВП-холестерина, высокого ЛНП-холестерина, атеросклеротических болезней, диабета, инсулиннезависимого сахарного диабета, метаболического синдрома, дислипидемии, сепсиса, воспалительных заболеваний, кожных болезней, колита, панкреатита, холестаза печени, фиброза печени, макулярной дегенерации и/или болезни Альцгеймера, включающему введение соединения по определению выше человеку или животному.
Изобретение включает также применение соединений по определению выше для терапевтического и/или профилактического лечения болезней, модулируемых LXRα и/или LXRβ агонистами, в частности в качестве терапевтически активных субстанций, для лечения и/или профилактики повышенных липидных уровней, повышенных уровней холестерина, низкого ЛВП-холестерина, высокого ЛНП-холестерина, атеросклеротических болезней, диабета, инсулиннезависимого сахарного диабета, метаболического синдрома, дислипидемии, сепсиса, воспалительных заболеваний, кожных болезней, колита, панкреатита, холестаза печени, фиброза печени, макулярной дегенерации и/или болезни Альцгеймера.
Изобретение относится также к применению соединений по определению выше для получения лекарственных средств для терапевтического и/или профилактического лечения болезней, модулируемых LXRα и/или LXRβ агонистами, в частности в качестве терапевтически активных субстанций для терапевтического и/или профилактического лечения повышенных липидных уровней, повышенных уровней холестерина, низкого ЛВП-холестерина, высокого ЛНП-холестерина, атеросклеротических болезней, диабета, инсулиннезависимого сахарного диабета, метаболического синдрома, дислипидемии, сепсиса, воспалительных заболеваний, кожных болезней, колита, панкреатита, холестаза печени, фиброза печени, макулярной дегенерации и/или болезни Альцгеймера. Такие лекарственные средства включают соединение по определению выше.
Профилактика и/или лечение повышенных липидных уровней, повышенных холистериновых уровней, атеросклеротических болезней, дислипидемии или диабета является предпочтительным показанием, в частности, предпочтительны профилактика и/или лечение повышенных липидных уровней, повышенных уровней холестерина, атеросклеротических болезней или дислипидемии, особенно предпочтительны профилактика и/или лечение атеросклеротических болезней или дислипидемии. Диабет, в частности инсулиннезависимый сахарный диабет, является другой предпочтительной болезнью.
Для определения активности соединений по настоящему изобретению проведены описанные ниже тесты. Основная информация по проведению анализов может быть найдена в: Nichols J.S. et al. "Development of а scintillation proximity assay for peroxisome proliferator-activated receptor gamma ligand binding domain". Anal. Biochem. 1998, 257: 112-119.
Векторы экспрессии млекопитающих были сконструированы, чтобы продуцировать полноразмерные человеческие LXRα и LXRβ. Векторы экспрессии бактерий и млекопитающих сконструированы таким образом, чтобы продуцировалась глутатион-s-трансфераза (GST), гибридизированная с лиганд-связывающими доменами (LBD) человеческого LXRα (аа 164 до 447) и человеческого LXRβ (аа 155 до 460). Чтобы достичь этого, участки клонированных последовательностей, кодирующих LBDs, были амплифицированы из полноразмерных клонов посредством ПЦР и затем субклонированы в векторы плазмид. Конечные клоны были верифицированы с помощью анализа последовательности ДНК (Willy et al., Genes Dev. 1995, 9:1033-45; Song et al., Proc. Natl. Acad. Sci. USA.1994, 91:10809-13).
Индукцию, экспрессию и очистку GST-LBD гибридизированных белков осуществляют в Е.coli линии BL21(pLysS) клетках стандартными методами (Ref: Current Protocols в Molecular Biology, Wiley Press, edited by Ausubel et al).
Анализ радиолигандного связывания
Связывание LXRα и LXRβ рецепторов анализируют в буфере, состоящем из 50 мМ HEPES, рН 7,4, 10 мМ NaCl, 5 мМ MgCl2. В каждой реакционной лунке 96-луночного планшета 500 нг GST-LXRα-LBD или 700 нг GST-LXRβ-LBD гибридных белков связывают с 80 мкг или 40 мкг SPA гранул (Pharmacia Amersham), соответственно, с конечным объемом 50 мкл посредством встряхивания. Образовавшуюся суспензию инкубируют в течение 1 ч при КТ и центрифугируют в течение 2 мин при 1300 г. Супернатант, содержащий несвязанный белок, удаляют и полусухой осадок, содержащий покрытые рецептором гранулы, вновь суспендируют в 50 мкл буфера. Добавляют радиолиганд (например, 100,000 распадов/мин N-(2,2,2-трифтофенил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)фенил]бензолсульфонамида)), реакцию инкубируют при КТ в течение 1 ч, и отсчет гранул, пропитанных сцинциллятором, осуществляют в присутствии тестируемых соединений. Все анализы связывания проводят в 96-луночных планшетах и количество связанного лиганда измеряют на Packard TopCount, используя OptiPlates (Packard). Кривые эффекта дозы представлены в области концентраций от 10-4 М.
Анализ с использованием транскрипционного репортерного гена люциферазы
Клетки почки детеныша хомячка (ВНК21 АТСС CCL10) выращивают в DMEM среде, содержащей 10% FBS, при 37°С в атмосфере 95%O2:5%CO2. Клетки высеивают в 6-луночный планшет с плотностью 105 клеток/лунку и затем партиями трансфецируют либо с полноразмерным-LXRα, либо с полноразмерным-LXRβ экспрессионными плазмидами с добавлением репортерной плазмиды, экспрессирующей люциферазу под контролем элементов LXR ответа. Трансфекция завершалась с помощью Fugene 6 реагента (Roche Molecular Biochemicals) согласно принятому протоколу. Через 6 ч после трансфекции клетки были харвестированы посредством трипсинизации и высеяны в 96-луночный планшет с плотностью 104 клеток/лунку. После 24 ч, предусмотренных для связывания клеток, среду удаляют и замещают 100 мкл не имеющей красной окраски фенольной среды, содержащей тестируемые субстанции или контрольные лиганды (конечная концентрация ДМСО: 0,1%). Вслед за инкубацией клеток с субстанциями в течение 24 ч отбрасывают 50 мкл супернатанта, а затем добавляют 50 мкл Luciferase Constant-Light Reagent (Roche Molecular Biochemicals) для лизирования клеток и инициации реакции люциферазы. Люминесценцию, как меру активности люциферазы, детектируют в Packard TopCount. Транскрипционная активация в присутствии тестируемой субстанции выражается возведенной в степень величиной активации по сравнению с клетками, инкубированными в отсутствие субстанции. ЕС50 величины были рассчитаны с использованием XLfit программы (ID Business Solutions Ltd. UK).
Соединения формулы (I) имеют активность по крайней мере по одному из выше проведенных анализов (EC50 или IC50) от 1 нМ до 100 мкМ, предпочтительно от 1 нМ до 10 мкМ, более предпочтительно от 1 нМ до 1 мкМ.
Например, указанные соединения имеют следующие IC50 величины в анализе связывания:
IC50 [мкмол/л]
IC50 [мкмол/л]
Данные результаты получены с помощью вышеприведенных тестов.
Соединения формулы (I) и их фармацевтически приемлемые соли могут быть применены в качестве лекарственных препаратов, например, в виде фармацевтических препаратов для энтерального, парентерального или местного введения. Они могут быть введены, например, перорально, например, в форме таблеток, таблеток в оболочке, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий; ректально, например, в форме суппозиториев, парентерально, например, в виде инъекционных или инфузионных растворов, местно, например, в виде мазей, кремов или масел. Оральное введение является предпочтительным.
Изготовление фармацевтических препаратов может быть осуществлено с использованием методов, известных любому специалисту в данной области техники, путем внесения требуемых соединений формулы (I) и их фармацевтически приемлемых производных в лекарственную форму для введения вместе с подходящими, нетоксичными, инертными, терапевтически совместимыми твердыми или жидкими носителями и, если желательно, обычными фармацевтическими адъювантами.
Подходящими носителями являются не только неорганические носители, но также и органические носители. Так, например, лактоза, кукурузный крахмал или их производные, тальк, стеариновая кислота или ее соли могут быть использованы в качестве материалов для таблеток, таблеток в оболочке, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры и полутвердые и жидкие полиолы (в зависимости от природы активного ингредиента никаких носителей, однако, не требуется в случае мягких желатиновых капсул). Подходящими носителями для приготовления растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар и подобные им. Подходящими носителями для инъекционных растворов являются, например, вода, спирты, полиолы, глицерин и растительные масла. Подходящими носителями для суппозиториев являются, например, натуральные и отвержденные масла, воски, жиры и полутвердые и жидкие полиолы. Подходящими носителями для местных препаратов являются глицериды, полусинтетические и синтетические глицериды, гидрогенизированные масла, жидкие воски, жидкие парафины, жидкие жирные спирты, стеролы, полиэтиленгликоли и производные целлюлозы.
Обычные стабилизаторы, консерванты, смачивающие и эмульсионные агенты, улучшители консистенции, улучшители вкуса, соли для регулировки осмотического давления, буферные субстанции, растворители, красители и маскировочные агенты и антиоксиданты рассматриваются в качестве фармацевтических адъювантов.
Дозировка соединений формулы (I) может варьироваться в широких пределах в зависимости от подлежащей контролю болезни, возраста и индивидуального состояния пациента и способа введения и, конечно, должна соответствовать индивидуальным требованиям в каждом отдельном случае. Для взрослых пациентов рассматривается суточная доза, составляющая приблизительно от 1 мг до 2000 мг, в частности, приблизительно от 1 мг до 500 мг. В зависимости от тяжести болезни и точного фармакокинетического профиля соединение может быть введено в виде одной или нескольких дозированных единиц в день, например, от 1 до 3 дозированных единиц.
Фармацевтические препараты стандартно содержат около 1-500 мг, предпочтительно 1-200 мг, соединения формулы (I).
Следующие примеры иллюстрируют настоящее изобретение более подробно, ни в коей мере не ограничивая, однако, его объема.
Примеры
Аббревиатуры:
АсОН = уксусная кислота, н-BuLi = н-бутиллитий, CH2Cl2 = дихлорметан, ДБУ = 1,8-диазабицикло[5.4.0]ундец-7-ен, ДИПЭА = N-этилдиизопропиламин, ДМФ = диметилформамид, EtOAc = этилацетат, EtOH = этанол, Et2O = диэтиловый эфир, гептан = н-гептан, i.v. = в вакууме, МеОН = метанол, ТБАФ = тетрабутиламмонийфторид, ТЭХС = триэтилхлорсилан, ТФК = трифторуксусная кислота, ТГФ = тетрагидрофуран, RT = комнатная температура.
Общие замечания
Все реакции проведены в атмосфере аргона.
Пример 1: транс-N-(2,2,2-трифторэткл}-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид
1.1. Раствор 10 г (38,6 ммолей) 2-(4-аминофенил)-1,1,1,3,3,3-гексафторпропан-2-ола в 100 мл ДМФ обрабатывают 6,3 мл (42,4 ммолей) ДБУ, а затем по каплям добавляют 6,5 мл (38,6 ммолей) ТЭСХ. После перемешивания смеси при КТ в течение ночи растворитель частично удаляют в вакууме. Распределение сырой смеси между разбавленным водным раствором NaOH и Et2O и высушивание объединенной органической фазы над Na2SO4 приводит к 13 г (90%) 4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)фениламина в виде бесцветного масла, МС: 374 (М+Н)+.
1.2. Раствор 5 г (13,4 ммолей) 4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)фениламина в 150 мл АсОН обрабатывают 2,5 г Pt/C (10%-ный) и гидрируют в течение 72 ч при атмосферном давлении при интенсивном перемешивании. Фильтрование и выпаривание растворителя дает желтое полутвердое вещество, которое распределяют между 1-молярным водным раствором NaOH и этилацетатом. Объединенные органические фазы высушивают над Na2SO4 и выпаривают, получая 4 г сырого продукта. Хроматография на силикагеле с использованием EtOAc, а затем EtOAc/MeOH в соотношении 10:1, дает около 1,9 г (37%) цис-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина и около 1,9 г (37%) транс-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина в виде слегка желтого масла, МС: 380 (M+H)+.
1.3. Раствор 0,71 г (1,87 ммолей) транс-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина в 5 мл CH2Cl2 обрабатывают 0,64 мл (3,74 ммолей) ДИПЭА и 0,24 мл (1,87 ммолей) бензолсульфонилхлорида и перемешивают при комнатной температуре в течение 3 ч. Распределение сырой смеси между разбавленным водным раствором HCl и эфиром, высушивание объединенной органической фазы над Na2SO4 и хроматография на силикагеле с использованием смеси EtOAc/гептан в соотношении 1:1 дает 0,9 г (93%) транс-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]бензолсульфонамида в виде слегка желтого полутвердого вещества, МС: 518 (М-Н)-.
1.4. Раствор 0,45 г (0,87 ммолей) транс-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]бензолсульфонамида в 5 мл сухого ТГФ охлаждают до -78°С и прибавляют к нему по каплям 0,7 мл (1,13 ммолей) 1,6-молярного раствора н-BuLi в гексане. Раствор нагревают до -40°С, обрабатывают 1,0 г (4,33 ммолей) 2,2,2-трифторэтилового эфира трифторметансульфоновой кислоты и оставляют нагреваться до комнатной температуры. Смесь перемешивают в течение 30 мин при КТ, а затем нагревают с обратным холодильником в течение 2 ч. Растворитель выпаривают, а остаток растворяют в 2 мл ТГФ и обрабатывают избытком фторидом тетрабутиламмония. Распределение между водным раствором NH4Cl и Et2O, высушивание объединенной органической фазы и хроматография на силикагеле с использованием смеси гептан/EtOAc в соотношении 2:1 дает 0,17 г (40%) транс-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамида в виде слегка желтого масла, МС: 486 (М-Н)-.
Пример 2: транс-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид
2.1. Раствор 350 мг (0,135 ммолей) 2-(4-аминофенил)-1,1,1,3,3,3-гексафторпропан-2-ола в 10 мл уксусной кислоты обрабатывают 100 мг Pt/C (10%-ной) и гидрируют при атмосферном давлении при интенсивном перемешивании в течение 24 ч. Фильтрование и выпаривание растворителя дает 400 мг (91%) ацетата 2-(4-аминоциклогексил)-1,1,1,3,3,3-гексафтор-пропан-2-ола в виде слегка коричневого твердого вещества, МС: 266 (М+Н)+.
2.2: Раствор 100 мг (0,37 ммолей) ацетата 2-(4-аминоциклогексил)-1,1,1,3,3,3-гексафторпропан-2-ола в 5 мл ДМФ обрабатывают 0,2 мл (1,16 ммолей) ДИПЭА и 0,144 мл (1,1 ммолей) бензолсульфонилхлорида. Смесь перемешивают в течение 1 ч и распределяют между разбавленным водным раствором HCl и диэтиловым эфиром. Объединенные органические фазы высушивают над Na2SO4 и растворителя выпаривают. Колоночная хроматография на силикагеле с использованием смеси EtOAc/гептан в соотношении 1:1 дает 90 мг (72%) N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил] бензолсульфонамида в виде розового твердого вещества, МС: 404 (М-Н)-.
2.3: Хроматография 50 мг (0,12 ммоля) N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамида на силикагеле с использованием смеси EtOAc/гептан в соотношении 2:1 дает около 19 мг (38%) цис-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамида и около 20 мг (40%) транс-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамида в виде бесцветного полутвердого вещества, МС: 404 (М-Н)-.
Пример 3: транс-N-бензил-2,2,2-трифтор-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил-1-ацетамид
3.1. Раствор 17 г (78, 23 ммолей) ацетата 2-(4-аминоциклогексил)-1,1,1,3,3,3-гексафторпропан-2-ола (пример 2.1) в 250 мл этанола обрабатывают 27,2 мл (196 ммолей) триэтиламина и 8,75 мл (86,1 ммолей) бензальдегида. Смесь перемешивают в течение ночи при комнатной температуре, и растворители выпаривают в вакууме. Полученное коричневое масло растворяют в 120 мл ДМФ и обрабатывают 8,76 мл (58,7 ммолей) ДБУ, а затем добавляют по каплям 9,85 мл (58,7 ммолей) триэтилхлорсилана. Смесь перемешивают в течение 4 ч при КТ и распределяют между насыщенным водным раствором NH4Cl и Et2O. Сырой продукт, полученный после высушивания объединенных органических фаз над Na2SO4 и выпаривания растворителя, растворяют в 250 мл этанола, по порциям обрабатывают 2,2 г (58,7 ммолей) NaBH4 и перемешивают в течение 2 ч при КТ. Выпаривание растворителя, распределение между этиловым эфиром и водным раствором NaOH, высушивания объединенной органической фазы над Na2SO4 и хроматография на силикагеле с использованием смеси гептан/EtOAc (градиент в соотношении от 6:1 до 2:1) дает 3,3 г (14%) цис-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина и 4,7 г (20%) транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина в виде желтого масла, МС: 470 (М+Н)+.
3.2. Раствор 100 мг (0,28 ммолей) транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 2) в 2 мл CH2Cl2 обрабатывают 0,1 мл (1,24 ммолей) пиридина и 0,1 мл (0,72 ммолей) ангидрида трифторуксусной кислоты и перемешивают при КТ в течение ночи. Обработка избытком ТБАФ, перемешивание в течение 30 мин и распределение смеси между разбавленным водным раствором HCl и этиловым эфиром, высушивание объединенной органической фазы над Na2SO4 и выпаривание дает приблизительно 100 мг (79%) транс-N-бензил-2,2,2-трифтор-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамида в виде желтого масла, МС: 452 (М+Н)+.
Пример 4: этиловый эфир транс-фенил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексиламино]уксусной кислоты
Раствор 300 мг (1,0 ммоль) ацетата 2-(4-аминоциклогексил)-1,1,1,3,3,3-гексафторпропан-2-ола (пример 2.1) в 5 мл этанола обрабатывают 227 мг (1,0 ммоль) этилового эфира оксофенилуксусной кислоты и 87 мг (1,0 ммоля) цианборгидрида натрия. Смесь перемешивают в течение ночи при КТ и распределяют между насыщенным водным раствором Na2HCO3 и этиловым эфиром. Высушивание объединенной органической фазы над Na2SO4 и хроматография на силикагеле смесью гептан/EtOAc в соотношении 4:1 дает приблизительно 100 мг (25%) этилового эфира цис-фенил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексиламино] уксусной кислоты и приблизительно 100 мг (25%) этилового эфира транс-фенил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексиламино]уксусной кислоты в виде бесцветного масла, МС: 428 (М+Н)+.
Пример 5: транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамид
Раствор 50 мг (0,11 ммоля) транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 3.1) в 1 мл CH2Cl2 обрабатывают 0,1 мл триэтиламина, охлаждают до 0°С и обрабатывают 0,14 мл (1,97 ммолей) ацетилхлорида. Смесь перемешивают в течение 30 мин и распределяют между насыщенным водным раствором NH4Cl и этиловым эфиром. Сырой продукт, полученный после высушивания объединенных органических фаз над Na2SO4 и выпаривания растворителя, растворяют в 1 мл ТГФ, обрабатывают избытком ТБАФ и оставляют при перемешивании в течение 1 ч. Распределение между насыщенным водным раствором NH4Cl и этиловым эфиром, высушивание объединенной органической фазы над Na2SO4, выпаривание растворителя и хроматография на силикагеле с использованием смеси EtOAc/гептан в соотношении 1:1 дает 50 мг (95%) транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамида в виде бесцветного вязкого масла, МС: 398 (М+Н)+.
Пример 6: транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид
По аналогии с примером 5 из транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 3.1) и бензолсульфонилхлорида получают транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид в виде бесцветного масла, МС: 494 (М-Н)-.
Пример 7: [4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амидтранс-2,4-диметилтиазол-5-сульфоновой кислоты
По аналогии с примером 5 из транс-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина (пример 1, 2) и 2,4-диметил-1,3-тиазол-5-сульфонилхлорида получают [4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амидтранс-2, 4-диметилтиазол-5-сульфоновой кислоты в виде желтого масла, МС: 441 (М+Н)+
Пример 8: [4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты
По аналогии с примером 5, из транс-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина (пример 1, 2) и 1,2-диметил-1Н-имидазол-4-сульфонилхлорида получают [4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты в виде светлого твердого вещества, МС: 424 (М+Н)+.
Пример 9: (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты
9.1. По аналогии с примером 1.3 из транс-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина и 1,2-диметил-N-имидазол-4-сульфонилхлорида получают [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты в виде белого твердого вещества, МС: 538 (М+Н)+.
9.2. По аналогии с примером 1, 4 из [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты и 2,2,2-трифторэтилового эфира трифторметансульфоновой кислоты получают (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты в виде слегка коричневого твердого вещества, МС: 506 (М+Н)+.
Пример 10: этил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)диклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты
10.1. Раствор 150 мг (0,28 ммоля) [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты (пример 9.1) в 1 мл ДМФ обрабатывают 0,66 мл (0,44 ммолей) ДБУ, перемешивают в течение 15 мин и обрабатывают 0,9 мл (0,58 ммоля) этилйодида. Смесь перемешивают при 60°С в течение 4 ч и распределяют между насыщенным водным раствором NH4Cl и этиловым эфиром. Высушивание объединенной органической фазы над Na2SO4 и выпаривание растворителя дает 150 мг (95%) этил[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида транс-1,2-диметил-N-имидазол-4-сульфоновой кислоты в виде слегка желтой жидкости, МС: 566 (М+Н)+.
10.2. Раствор 130 мг (0,23 ммоля) этил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты в 2 мл ТГФ обрабатывают избытком фторида тетрабутиламмония и перемешивают в течение 2 ч при комнатной температуре. Распределение между насыщенным водным раствором NH4Cl и Et2O, высушивание объединенной органической фазы, выпаривание растворителя и колоночная хроматография на силикагеле смесью EtOAc/гептан в соотношении 1:1 дает 42 мг (25%) этил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амида транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты в виде желтого бесцветного масла, МС: 452 (М+Н)+.
Пример 11: этил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-4-метил-2-пропилтиазол-5-сульфоновой кислоты
11.1. По аналогии с примером 1.3 из транс-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина (пример 1.2) и 2,4-диметил-1,3-тиазол-5-сульфонилхлорида получают [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амидтранс-2,4-диметилтиазол-5-сульфоновой кислоты в виде белого твердого вещества, МС: 555 (М+Н)+.
11.2. Раствор 200 мг (0,36 ммолей) [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амидатранс-2,4-диметилтиазол-5-сульфоновой кислоты в 5 мл ТГФ охлаждают до -78°С и по каплям прибавляют 0,25 мл 1,6-молярного раствора н-BuLi в гексане. Раствор нагревают до -30°С, обрабатывают 1 мл (1,2 ммолей) этилйодида, оставляют нагреваться до КТ, а затем нагревают с обратным холодильником в течение 2 ч. Распределение между насыщенным водным раствором NH4Cl и Et2O, высушивание объединенной органической фазы над Na2SO4 и выпаривание растворителя дают остаток, который растворяют в ТГФ и обрабатывают избытком ТБАФ. Распределение между насыщенным водным раствором NH4Cl и этиловым эфиром, высушивание объединенной органической фазы над Na2SO4, выпаривание растворителя и хроматография на силикагеле смесью гептан/EtOAc в соотношении 2:1 дает 20 мг (11%) этил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амидатранс-4-метил-2-пропилтиазол-5-сульфоновой кислоты в виде желтого масла, МС: 497 (М+Н)+.
Пример 12: (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил1амид транс-2,4-диметилтиазол-5-сульфоновой кислоты
По аналогии с примером 1, 4 из [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида транс-2,4-диметилтиазол-5-сульфоновой кислоты (пример 11.1) и 2,2,2-трифторэтилового эфира трифторметансульфоновой кислоты получают (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-N-имидазол-4-сульфоновой кислоты в виде желтого вязкого масла, МС: 523 (М+Н)+.
Пример 13: циклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)диклогексил]амидтранс-2,4-диметилтиазол-5-сульфоновой кислоты
По аналогии с примером 10 из [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амидатранс-2,4-диметилтиазол-5-сульфоновой кислоты (пример 11.1) и бромметилциклопропана получают циклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2,4-диметилтиазол-5-сульфоновой кислоты в виде желтой смолы, МС: 495(M+H)+.
Пример 14: этил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амидтранс-2,4-диметилтиазол-5-сульфоновой кислоты
По аналогии с примером 10 из [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амидатранс-2,4-диметилтиазол-5-сульфоновой кислоты (пример 11.1) и этилйодида получают этил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амидтранс-2,4-диметилтиазол-5-сульфоновой кислоты в виде желтого масла, МС: 469 (M+H)+.
Пример 15: транс-N-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид
Раствор 500 мг (0,89 ммоля) транс-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]бензолсульфонамида (пример 1.3) в 10 мл ТГФ охлаждают до -78°С и по каплям прибавляют 0,72 мл 1,6-молярного раствора н-BuLi в гексане. Раствор нагревают до -40°С в течение 30 мин, обрабатывают 0,43 мл (4,45 ммолей) бромметилциклопропана, оставляют нагреваться до комнатной температуры, а затем нагревают с обратным холодильником в течение ночи. Добавляют избыток ТБАФ и смесь дополнительно перемешивают в течение часа. Распределение сырой смеси между насыщенным водным раствором NH4Cl и Et2O, высушивание объединенной органической фазы над Na2SO4, выпаривание и хроматография на силикагеле с помощью дихлорметана дают 200 мг (49%) транс-N-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамида в виде бесцветного вязкого масла, МС: 460 (M+H)+.
Пример 16: транс-N-этил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид
По аналогии с примером 10 из транс-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]бензолсульфонамида (пример 1.3) и этилйодида получают транс-этил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид в виде бесцветного масла, МС: 434 (М+Н)+.
Пример 17: (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты
17.1. По аналогии с примером 1.3 из транс-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина и 5-хлор-1,3-диметилпиразол-4-сульфонилхлорида получают [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1H-пиразол-3-сульфоновой кислоты в виде светлого аморфного твердого вещества, МС: 528 (М+Н)+.
17.2. По аналогии с примером 10 из [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты и 2,2,2-трифторэтилового эфира трифторметансульфоновой кислоты получают (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1H-пиразол-3-сульфоновой кислоты в виде слегка желтого масла, МС: 540 ((М+Н)+ 1Cl).
Пример 18: [4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты
По аналогии с примером 10.2 из [4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты (пример 17.1) получают [4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты в виде полутвердого вещества, МС: 458 ((М+Н)+ 1 Cl)
Пример 19: транс-2-[4-(бензилэтиламино)циклогексил]-1,1,1,3,3,3-гексафтор-пропан-2-ол
Раствор 200 мг (0,43 ммоля) транс-бензил[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 3.1) в 2 мл пиридина обрабатывают 0,05 мл ангидрида уксусной кислоты (0,51 ммоля), перемешивают в течение ночи при КТ и распределяют между насыщенным водным раствором NH4Cl и Et2O. После высушивания объединенной органической фазы над Na2SO4 и выпаривания растворителя осадок растворяют в 3,5 мл ТГФ и обрабатывают 0,86 мл 1-молярного раствора ВН3 в ТГФ. Смесь перемешивают при комнатной температуре в течение 2 ч, и растворитель выпаривают. Остаток растворяют в ТГФ, обрабатывают избытком фторида тетрабутиламмония и перемешивают в течение 2 ч. Выпаривание растворителя и хроматография на силикагеле смесью гексан/EtOAc в соотношении 4:1 дает 64 мг (39%) транс-2-[4-(бензилэтиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ола в виде слегка желтого масла, МС: 384 (М+Н)+.
Пример 20: транс-2-[4-(бензилпропиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол
По аналогии с примером 19 из транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 3.1) и пропионилхлорида получают транс-2-[4-(бензилпропиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол в виде бесцветного масла, МС: 398 (М+Н)+.
Пример 21: транс-2-[4-(бензилциклопропилметиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол
По аналогии с примером 19 из транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 3.1) и циклопропилкарбонилхлорида получают транс-2-[4-(бензилциклопропилметиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол в виде бесцветного масла, МС: 310 (M+H)+.
Пример 22: транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]пропионамид
По аналогии с примером 5 из транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 3.1) и пропионилхлорида получают транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]пропионамид в виде слегка желтого масла, МС: 412 (M+H)+.
Пример 23: бензил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-циклопропанкарбоновой кислоты
По аналогии с примером 5 из транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 3.1) и циклопропилкарбонилхлорида получают бензил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-циклопропанкарбоновой кислоты в виде слегка желтого масла, МС: 424 (M+H)+.
Пример 24: транс-N-циклопропилметил-]-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил-1-бензамид
24.1. Раствор 930 мг (1,73 ммолей) транс-бензил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 3.1) в 2 мл CH2Cl2 обрабатывают 0,6 мл (3,5 ммолей) ДИПЭА и 0,23 мл (2,56 ммолей) циклопропилкарбонилхлорида. Смесь перемешивают при комнатной температуре в течение ночи и распределяют между насыщенным водным раствором NH4Cl и Et2O. Объединенные органические фазы высушивают над Na2SO4, а растворитель выпаривают. Сырой полученный продукт растворяют в 10 мл ТГФ, обрабатывают 3,46 мл 1-молярного раствора ВН3 в ТГФ и нагревают с обратным холодильником в течение 6 ч. Распределение между разбавленным водным раствором NaOH и Et2O, высушивание объединенной органической фазы над Na2SO4 и выпаривание растворителя дают 1 г сырого транс-бензилциклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина в виде желтого масла, МС: 524 (М+Н)+.
24.2. 1 г (около 2,0 ммолей) сырого транс-бензилциклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина растворяют в 50 мл уксусной кислоты, вносят 300 мг Pd/C (10%-ный) и гидрируют в течение ночи при атмосферном давлении при интенсивном перемешивании. Фильтрование и выпаривание растворителя дают 775 мг (около 82%) сырого транс-циклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина в виде желтого масла, МС: 434 (М+Н)+
24.3. Раствор 50 мг (0,12 ммоля) транс-циклопропилметил[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина в 3 мл смеси (в соотношении 1:2) ТГФ и 1,2-дихлорэтана обрабатывают 0,03 мл (0,23 ммолей) триэтиламина и 0,02 мл (0,4 ммолей) бензоилхлорида. Смесь перемешивают при КТ в течение 2 ч и распределяют между насыщенным водным раствором NH4Cl и Et2O. После высушивания объединенной органической фазы над Na2SO4 и выпаривания растворителя остаток растворяют 2 мл ТГФ, обрабатывают избытком фторида тетрабутиламмония и распределяют между насыщенным водным
раствором NH4Cl и Et2O. Высушивание объединенной органической фазы над Na2SO4 и колоночная хроматография на силикагеле смесью гептан/этилацетат в соотношении 2:1 дают 35 мг (72%) транс-N-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензамида в виде белого твердого вещества, МС: 424, (М+Н)+.
Пример 25: транс-N-циклопропилметил-2-фенил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамид
По аналогии с примером 24.3 из транс-циклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 24.2) и фенилацетилхлорида получают транс-N-циклопропилметил-2-фенил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил] ацетамид в виде слегка коричневого масла, МС: 438 (М+Н)+.
Пример 26: фениловый эфир транс-диклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]карбаминовой кислоты
По аналогии с примером 24.3 из транс-циклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 24.2) и фенилхлорформиата получают фениловый эфир транс-циклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]карбаминовой кислоты в виде слегка коричневого масла, МС: 440 (М+Н)+.
Пример 27: бензиловый эфир транс-циклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]карбаминовой кислоты
По аналогии с примером 24.3 из транс-циклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 24.2) и бензилхлорформиата получают бензиловый эфир транс-циклопропилметил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]карбаминовой кислоты в виде слегка коричневого масла, МС: 454 (М+Н)+.
Пример 28: (рац)-транс-2-{4-[циклопропилметил-(2-гидрокси-2-фенилэтил)амино]циклогексил}-1,1,1,3,3,3-гексафторпропан-2-ол
28.1. Раствор 100 мг (0,23 ммоля) транс-циклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амина (пример 24.2) в 0,5 мл ацетонитрила обрабатывают 41 мг (0,38 ммолей) литийперхлората и 46 мг (0,38 ммолей) (рац)-фенилэтиленоксида. Смесь перемешивают в запаянной трубке при 80°С в течение 6 ч и распределяют между насыщенным водным раствором NH4Cl и Et2O. Высушивание объединенной органической фазы над Na2SO4, выпаривание растворителя и колоночная хроматография на силикагеле смесью гептан/этилацетат в соотношении 1:1 дают 52 мг (49%) (рац) транс-2-{циклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амино}-1-фенилэтанола в виде бесцветного масла, МС: 554 (М+Н)+.
28.2. По аналогии с примером 10.2 из (рац)-транс-2-{циклопропилметил-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амино}-1-фенилэтанола получают (рац)-транс-2-{4-[циклопропилметил-(2-гидрокси-2-фенилэтил)амино]циклогексил}-1,1,1,3,3,3-гексафторпропан-2-ол в виде слегка желтого полутвердого вещества, МС: 440 (М+Н)+.
Пример 29: транс-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид
29.1. По аналогии с примером 1.3 из транс-4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина и фенилметансульфонилхлорида получают транс-бензил-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]сульфонамид в виде желтого твердого вещества, МС: 534 (М+Н)+.
29.2. По аналогии с примером 10.2 из транс-бензил-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]сульфонамида получают транс-бензил-1-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид, в виде слегка коричневой смолы, МС: 420 (М+Н)+.
Пример 30: транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид
30.1. Раствор 200 мг (0,37 ммоля) транс-бензил-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]сульфонамида (пример 29.1) в 2 мл ТГФ охлаждают до -78°С и по каплям обрабатывают 0,4 мл 1-молярного раствора бис-(триметилсилил)амида лития в ТГФ. Смесь нагревают до -40°С, обрабатывают 609 мг (2,6 ммолей) 2,2,2-трифторэтилового эфира трифторметансульфоновой кислоты и оставляют нагреваться до комнатной температуры. Затем после 4 ч нагревания с обратным холодильником смесь охлаждают до комнатной температуры и распределяют между насыщенным водным раствором NH4Cl и Et2O. Объединенные органические фазы высушивают над Na2SO4, а растворитель выпаривают. Хроматография на силикагеле смесью гептан/этилацетат в соотношении 9:1 дает 140 мг (61%) транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]сульфонамида в виде слегка желтого масла, МС: 614 (М-Н)-.
30.2. По аналогии с примером 10.2 из транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]сульфонамида получают транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид в виде слегка окрашенной пены, МС: 502 (М+Н)+.
Пример 31: (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид (рац) транс-1-фенилэтансульфоновой кислоты
31.1. Раствор 128 мг (0.21 ммолей) транс-бензил-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]сульфонамида (пример 30.1) в 2 мл ТГФ охлаждают до -78°С, обрабатывают по каплям 0,42 мл 1-молярного раствора бис-(триметилсилил)амида лития в ТГФ и оставляют нагреваться до -40°С. После добавления 0,13 мл (2,1 ммолей) йодметана смесь перемешивают при комнатной температуре в течение 4 ч и распределяют между насыщенным водным раствором NH4Cl и Et2O. Объединенные органические фазы высушивают над Na2SO4, а растворитель выпаривают, получая 130 мг (98%) сырого (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида (рац)-транс-1-фенилэтансульфоновой кислоты в виде слегка желтого масла, МС: 648 (M+NH4)+.
31.2. Раствор 30 мг (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида в метаноле обрабатывают 0,12 мл 2-молярного раствора NaOMe в метаноле. Распределение между насыщенным водным раствором NH4Cl и Et2O и колоночная хроматография смесью гептан/этилацетат в соотношении 2:1 дают 18 мг (73%) (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амида (рац)-транс-1-фенилэтансульфоновой кислоты в виде бесцветного масла, МС: 514 (М-Н)-.
Пример 32: (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)диклогексил]амид транс-2-фенилпропан-2-сульфоновой кислоты
Раствор 100 мг (0,16 ммолей) (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]амида 1-фенилэтансульфоновой кислоты (пример 31.1) в ТГФ охлаждают до -78°С и по каплям обрабатывают 0,17 мл 1-молярного раствора бис-(триметилсилил)амида лития вТГФ. Смесь нагревают до 0°С и обрабатывают 0,22 мл (0,35 ммоля) йодметана, оставляют нагреваться до комнатной температуры, а затем нагревают с обратным холодильником в течение 4 ч. Распределение смеси между насыщенным водным раствором NH4Cl и этиловым эфиром, высушивание объединенной органической фазы над Na2SO4 и выпаривание растворителя дают остаток, который растворяют в 2 мл МеОН и обрабатывают 0,5 мл 2-молярного раствора NaOMe. Распределение этого раствора между насыщенным водным раствором NH4Cl и этиловым эфиром, высушивание объединенной органической фазы над Na2SO4, выпаривание и колоночная хроматография на силикагеле смесью дихлорметан/гептан в соотношении 1:2 дают 6 мг (7%) (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амида транс-2-фенилпропан-2-сульфоновой кислоты в виде белой смолы, МС: 528 (М-Н)-.
Пример 33: (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид (рац)-транс-1,2-дифенилэтансульфоновой кислоты
Раствор 50 мг (0,08 ммолей) транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]сульфонамида (пример 30.1) в 0,5 мл ТГФ охлаждают до -78°С и обрабатывают 0,11 мл 1-молярного раствора бис-(триметилсилил)амида лития в ТГФ. Смесь оставляют нагреваться до приблизительно -5°С в течение 30 мин и обрабатывают 0,11 мл (0,1 ммоля) бензилбромида. Смесь перемешивают в течение ночи и распределяют между разбавленным водным раствором HCl и Et2O. Объединенные органические фазы высушивают над Na2SO4 и растворитель выпаривают. Остаток растворяют в метаноле и обрабатывают 0,5 мл 2-молярного раствора NaOMe в метаноле. Распределение этого раствора между насыщенным водным раствором NH4Cl и El2O, высушивание объединенной органической фазы над Na2SO4, выпаривание и колоночная хроматография на силикагеле смесью гептан/этилацетат в соотношении 4:1 дают 50 мг (76%) (2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амида (рац)-транс-1,2-дифенилэтансульфоновой кислоты в виде бесцветной пены, МС: 590 (М-Н)-.
Пример 34: метиловый эфир (рац)-транс-3-(2-фенил-2-{(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфамоил}этил)бензойной кислоты
По аналогии с примером 33 из бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]сульфонамида (пример 30.1) и метил-3-(бромметил)бензоата вместо бензилбромида получают метиловый эфир (рац)-транс-3-(2-фенил-2-{(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфамоил}этил)бензойной кислоты в виде бесцветного масла, МС: 648 (М-Н)-.
Пример 35: цис-N-этил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил-1-бензолсульфонамид
35.1. По аналогии с примером 1.3 из цис 4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексиламина (пример 1.2) получают цис-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]бензолсульфонамид в виде бесцветного масла, МС:518(М-Н)-
35.2. По аналогии с примером 10 из цис-N-[4-(2,2,2-трифтор-1-триэтилсиланилокси-1-трифторметилэтил)циклогексил]бензолсульфонамида и этилйодида получают цис-N-этил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид в виде слегка желтого вязкого масла, МС: 434 (М+Н)+
Пример А
Таблетки, покрытые оболочкой, содержащие следующие ингредиенты, могут быть получены стандартным методом:
Активные ингредиенты просеивают, смешивают с микрокристаллической целлюлозой и гранулируют смесь в растворе поливинилпирролидона в воде. Гранулят смешивают с щелочным гликолятом крахмала и стеаратом магния и прессуют, получая сердцевину таблеток массой 120 или 350 мг соответственно. Сердцевину лакируют с помощью водного раствора/суспензии упомянутой выше пленочной оболочки.
Пример Б
Капсулы, содержащие следующие ингредиенты, могут быть получены стандартным методом:
Компоненты просеивают, смешивают и вносят в капсулу размера 2.
Пример В
Инъекционные растворы могут иметь следующий состав:
Активный ингредиент растворяют в смеси полиэтиленгликоля 400 и воды для инъекций, используя ее часть. Доводят рН до 5,0 с помощью уксусной кислоты. Объем доводят до 1,0 мл добавлением оставшегося количества воды. Раствор отфильтровывают, заполняют в пузырьки, используя соответствующее устройство, и стерилизуют.
Пример Г
Мягкие желатиновые капсулы, содержащие следующие ингредиенты, могут быть получены стандартным методом:
Ингредиенты
Содержание капсулы
Желатиновая капсула
Активный ингредиент растворяют в теплом расплаве других ингредиентов и смесью заполняют мягкие желатиновые капсулы соответствующего размера. Заполненные мягкие желатиновые капсулы обрабатывают с использованием обычных методов.
Пример Д
Облатки, содержащие следующие ингредиенты, могут быть получены стандартным методом:
Ингредиенты
(AVICELPH 102)
Ингредиенты
Активный ингредиент смешивают с лактозой, микрокристаллической целлюлозой и натрийкарбоксиметилцеллюлозой, а затем гранулируют со смесью поливинилпирролидона в воде. Гранулят смешивают со стеаратом магния и вкусовыми добавками и вносят в облатки.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПРОИЗВОДНЫЕ ГЕКСАФТОРИЗОПРОПАНОЛА | 2005 |
|
RU2389718C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ АРИЛСУЛЬФОНЫ, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, КОТОРЫЕ ОТВЕЧАЮТ НА МОДУЛИРОВАНИЕ 5HT РЕЦЕПТОРОВ | 2007 |
|
RU2451012C2 |
| ПРОИЗВОДНЫЕ ИНДАЗОЛОНА В КАЧЕСТВЕ ИНГИБИТОРОВ 11B-HSD1 | 2005 |
|
RU2392272C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛПИРИМИДИНА | 2005 |
|
RU2378277C2 |
| ПРОИЗВОДНЫЕ НИТРИЛОВ β-АМИНОКИСЛОТ | 2001 |
|
RU2245871C2 |
| АМИНОТЕТРАЛИНОВЫЕ ПРОИЗВОДНЫЕ, СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ В ТЕРАПИИ | 2010 |
|
RU2546649C2 |
| НОВЫЕ АЗАЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2011 |
|
RU2603263C2 |
| ДВОЙНЫЕ МОДУЛЯТОРЫ 5-HT И D-РЕЦЕПТОРОВ | 2008 |
|
RU2480466C2 |
| ЦИКЛОАЛКИЛНИТРИЛПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ЯНУС-КИНАЗЫ | 2014 |
|
RU2655380C2 |
| ГЕМИНАЛЬНО-ЗАМЕЩЕННЫЕ ЦИАНОЭТИЛПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ JANUS КИНАЗ | 2014 |
|
RU2664533C2 |
Изобретение относится к новым гексафторизопропанолзамещенным производным циклогексана формулы (I), обладающим свойствами модулирования LXRα- и/или LXRβ агонистов, а также к их фармацевтически приемлемым солям. В формуле (I)
R1 обозначает водород, низший алкил, фтор-низший алкил, низший алкил-карбонил, фтор-низший алкил-карбонил, фенил-низший алкил, С3-С6-циклоалкил-низший алкил, С3-С6-циклоалкилкарбонил или С3-С6-циклоалкил-низший алкил-карбонил; R2 обозначает водород или низший алкил; R3 обозначает низший алкил, фенил-низший алкил, где фенил возможно замещен низшим алкоксикарбонилом, низший алкоксикарбонил, или, если Х обозначает простую связь и m не равен 0, R3 может также обозначать гидроксигруппу; R4 обозначает фенил или гетероциклил, где гетероциклил представляет собой пятичленное ароматическое гетероциклическое кольцо, содержащее два гетероатома, выбранных из азота и серы, необязательно замещенное от 1 до 3 заместителями, независимо выбранными из группы, включающей низший алкил и галоген; Х обозначает простую связь, SO2, СО или С(O)O; m обозначает 0, 1, 2 или 3; n обозначает 0 или 1. Изобретение относится также к фармацевтической композиции, включающей соединение формулы (I). 2 н. и 18 з.п. ф-лы.
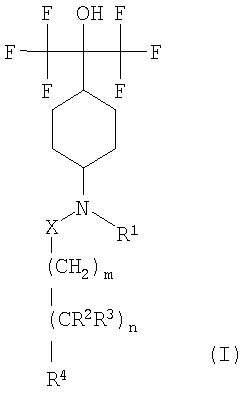
1. Соединения формулы (I)
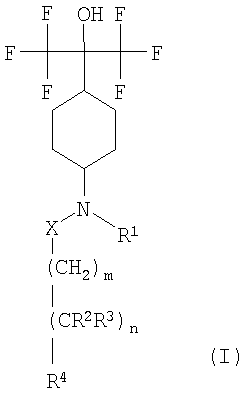
где R1 обозначает водород, низший алкил, фтор-низший алкил, низший алкил-карбонил, фтор-низший алкил-карбонил, фенил-низший алкил, С3-С6-циклоалкил-низший алкил, С3-С6-циклоалкилкарбонил или С3-С6-циклоалкил-низший алкил-карбонил;
R2 обозначает водород или низший алкил;
R3 обозначает низший алкил, фенил-низший алкил, где фенил возможно замещен низшим алкоксикарбонилом, низший алкоксикарбонил, или, если Х обозначает простую связь и m не равен 0, R3 может также обозначать гидроксигруппу;
R4 обозначает фенил или гетероциклил, где гетероциклил представляет собой пятичленное ароматическое гетероциклическое кольцо, содержащее два гетероатома, выбранных из азота и серы, необязательно замещенное от 1 до 3 заместителями, независимо выбранными из группы, включающей низший алкил и галоген;
Х обозначает простую связь, SO2, СО или С(O)O;
m обозначает 0, 1, 2 или 3;
n обозначает 0 или 1;
в виде рацематов, цис- или транс-изомеров или их смеси, и их фармацевтически приемлемые соли.
2. Соединения по п.1, характеризующиеся формулой (IA)

где R1, R2, R3, R4, X, m и n определены в п.1, и их фармацевтически приемлемые соли.
3. Соединения по п.1, где R1 обозначает фтор-низший алкил, фенил-низший алкил или С3-С6-циклоалкил-низший алкил.
4. Соединения по п.1, где R1 обозначает 2,2,2-трифторэтил, бензил или циклопропилметил.
5. Соединения по п.1, где n=1, R2 обозначает водород или низший алкил и R3 обозначает низший алкил, фенил-низший алкил или низший алкоксикарбонил, или, если Х не обозначает простую связь, или, если Х обозначает простую связь и m не равен 0, R3 может обозначать также гидроксильную группу.
6. Соединения по п.5, где R2 обозначает низший алкил.
7. Соединения по п.6, где R2 обозначает метил.
8. Соединения по п.1 или п.2, где R3 обозначает низший алкил.
9. Соединения по п.5, где R3 обозначает метил.
10. Соединения по п.1, где R обозначает фенил или гетероциклил, выбранный из группы, включающей тиазолил, имидазолил и пиразолил, при этом тиазолил, имидазолил и пиразолил необязательно замещены от 1 до 3 заместителями, независимо выбранными из группы, включающей низший алкил и галоген.
11. Соединения по п.1, где R4 обозначает фенил.
12. Соединения по п.1, где m обозначает 0 или 1.
13. Соединения по п.1, где m обозначает 0.
14. Соединения по п.13, где n обозначает 0.
15. Соединения по п.1, где Х обозначает SO2.
16. Соединения по п.10, выбранные из группы, включающей
транс-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-бензил-2,2,2-трифтор-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамид,
этиловый эфир транс-фенил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексиламино]уксусной кислоты,
транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамид,
транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2,4-диметилтиазол-5-сульфоновой кислоты,
[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты,
этил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-1,2-диметил-1Н-имидазол-4-сульфоновой кислоты,
этил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-4-метил-2-пропилтиазол-5-сульфоновой кислоты,
(2,2,2-трифторэтил)[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амидтранс-2,4-диметилтиазол-5-сульфоновой кислоты,
циклопропилметил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амидтранс-2,4-диметилтиазол-5-сульфоновой кислоты,
этил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2,4-диметилтиазол-5-сульфоновой кислоты,
транс-N-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-этил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты,
[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-5-хлор-1,4-диметил-1Н-пиразол-3-сульфоновой кислоты,
транс-2-[4-(бензилэтиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол,
транс-2-[4-(бензилпропиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол,
транс-2-[4-(бензилциклопропилметиламино)циклогексил]-1,1,1,3,3,3-гексафторпропан-2-ол,
транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]пропионамид,
бензил-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-циклопропанкарбоновой кислоты,
транс-N-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензамид,
транс-N-циклопропилметил-2-фенил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]ацетамид,
фениловый эфир транс-циклопропилметил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]карбаминовой кислоты,
бензиловый эфир транс-циклопропилметил[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)пиклогексил]карбаминовой кислоты,
(рац)-транс-2-{4-[циклопропилметил-(2-гидрокси-2-фенилэтил)амино]циклогексил}-1,1,1,3,3,3-гексафторпропан-2-ол,
транс-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид,
транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид(рац)-транс-1-фенилэтансульфоновой кислоты,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид транс-2-фенилпропан-2-сульфоновой кислоты,
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]амид (рац)-транс-1,2-дифенилэтансульфоновой кислоты,
метиловый эфир (рац)-транс-3-(2-фенил-2-{(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфамоил}этил)бензойной кислоты, и цис N-этил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
и их фармацевтически приемлемые соли.
17. Соединения по п.12, выбранные из группы, включающей
транс-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-бензил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-N-циклопропилметил-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]бензолсульфонамид,
транс-бензил-N-(2,2,2-трифторэтил)-N-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил]сульфонамид и
(2,2,2-трифторэтил)-[4-(2,2,2-трифтор-1-гидрокси-1-трифторметилэтил)циклогексил] амид транс-2-фенилпропан-2-сульфоновой кислоты,
и их фармацевтически приемлемые соли.
18. Фармацевтическая композиция, обладающая свойствами модулирования LXRα- и/или LXRβ агонистов, включающая соединение по п.1 и фармацевтически приемлемый носитель и/или адъювант.
19. Соединения по п.1, обладающие свойствами модулирования LXRα- и/или LXRβ агонистов.
20. Соединения по п.1 в качестве терапевтически активных веществ для получения лекарственных средств для лечения и/или профилактики болезней, модулируемых LXRα и/или LXRβ агонистами.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| N-[4-2'-ГИДРОКСИГЕКСАФТОРИЗОПРОПИЛ)ФЕНИЛ] -N-ЭТИЛ-N'-ФЕНИЛМОЧЕВИНА, ОБЛАДАЮЩАЯ РОСТРЕГУЛИРУЮЩИМ И АНТИДОТНЫМ ДЕЙСТВИЕМ | 1990 |
|
RU1743153C |
Авторы
Даты
2010-02-20—Публикация
2005-12-14—Подача