Область изобретения
Данное изобретение относится к новым хромен-2-оновым производным, полезным в качестве ингибиторов обратного захвата моноаминовых нейромедиаторов.
В других аспектах изобретение относится к применению этих соединений в способе терапии и к фармацевтическим композициям, содержащим соединения по изобретению.
Предшествующий уровень техники
В настоящее время селективные ингибиторы обратного захвата серотонина (SSRIs) обеспечивают эффективность лечения некоторых расстройств центральной нервной системы (ЦНС), включая депрессию и паническое расстройство. Психиатры и врачи первой медицинской помощи обычно воспринимают SSRIs как эффективные, хорошо переносимые и легкие во введении. Однако им сопутствует ряд нежелательных свойств.
Таким образом, до сих пор имеется сильная потребность в соединениях с оптимальным фармакологическим профилем в отношении активности обратного захвата моноаминовых нейромедиаторов серотонина, дофамина и норадреналина, таком как соотношение активности обратного захвата серотонина к активности обратного захвата норадреналина и дофамина.
В Bioorganic & Medicinal Chemistry (Jackson, Sharon A. et al., 13 (2005) 2723-2739) рассмотрены строение, синтез и характеристики нового класса ингибиторов, основанных на кумарине, или индуцибельной синтазы оксида азота. К числу раскрытых соединений относится соль трифторуксусной кислоты и 6-бром-4-(пиперидин-4-илокси)-1-бензопиран-2-она. Такое же соединение раскрыто в WO 2005/026143.
Краткое описание сущности изобретения
В первом аспекте изобретения предлагается соединение формулы I
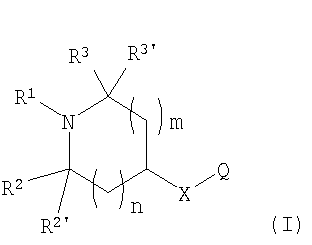
или любой из его изомеров, или любая смесь его изомеров, или его фармацевтически приемлемая соль,
где R1, R2, R2, R3, R3', m, n, X и Q определены ниже.
Во втором аспекте изобретения предлагается фармацевтическая композиция, содержащая терапевтически эффективное количество соединения по изобретению или любого из его изомеров, или любой смеси его изомеров, или его фармацевтически приемлемой соли вместе с по меньшей мере одним фармацевтически приемлемым носителем, эксципиентом или разбавителем.
В дополнительном аспекте изобретения предлагается применение соединения по изобретению или любого из его изомеров, или любой смеси его изомеров, или его фармацевтически приемлемой соли для изготовления фармацевтической композиции для лечения, предупреждения или облегчения заболевания или расстройства, или состояния млекопитающего, включая человека, причем заболевание, расстройство или состояние чувствительно к ингибированию обратного захвата моноаминовых нейромедиаторов в центральной нервной системе.
В еще одном дополнительном аспекте изобретение относится к способу лечения, предупреждения или облегчения заболевания или расстройства, или состояния живого организма животного, включая человека, причем заболевание, расстройство или состояние чувствительно к ингибированию обратного захвата моноаминовых нейромедиаторов в центральной нервной системе, и этот способ включает стадию введения такому нуждающемуся в нем живому организму животному терапевтически эффективного количества соединения по изобретению или любого из его изомеров, или любой смеси его изомеров, или его фармацевтически приемлемой соли.
Другие объекты изобретения будут очевидны для специалиста в данной области техники из следующего ниже подробного описания и примеров.
Подробное описание изобретения
Хромен-2-оновые производные
В первом аспекте настоящего изобретения предлагается соединение формулы I

или любой из его изомеров, или любая смесь его изомеров,
или его фармацевтически приемлемая соль,
где
R1 представляет собой водород или алкил;
где алкил возможно замещен одним или более заместителями, независимо выбранными из группы, состоящей из: галогено, трифторметила, трифторметокси, циано, гидрокси, амино, нитро, алкокси, циклоалкокси, алкила, циклоалкила, циклоалкилалкила, алкенила и алкинила;
каждый из R2, R2', R3 и R3' независимо друг от друга представляет собой водород или алкил; или R2 и R3 вместе образуют -(СН2)р, и R2' и R3' независимо друг от друга представляют собой водород или алкил; где р равен 1, 2 или 3;
m равен 0, 1 или 2;
n равен 0, 1 или 2;
X представляет собой -О- или -NR4-;
где R4 представляет собой водород, алкил, -C(=O)R5 или -SO2R5;
где R5 представляет собой водород или алкил; и
Q представляет собой хромен-2-оновую группу, которая возможно замещена одним или более заместителями, независимо выбранными из группы, состоящей из галогено, трифторметила, трифторметокси, циано, гидрокси, амино, нитро, алкокси, циклоалкокси, алкила, циклоалкила, циклоалкилалкила, алкенила и алкинила.
В одном воплощении R1 представляет собой водород. Во втором воплощении R1 представляет собой алкил.
В дополнительном воплощении R2 и R3 вместе образуют -(CH2)p-. В еще одном дополнительном воплощении R2 и R3 вместе образуют -(CH2)p-, и R2' и R3' каждый представляет собой водород. В конкретном воплощении R2 и R3 вместе образуют
-(CH2)2 -. В дополнительном конкретном воплощении R2 и R3 вместе образуют -(СН2)2-,
и R2' и R3' представляют собой водород.
В еще одном дополнительном воплощении R2, R2', R3 и R3' каждый представляет собой алкил. В конкретном воплощении R2, R2', R3 и R3' каждый представляет собой метил. В дополнительном воплощении R2, R2', R3 и R3' каждый представляет собой водород.
В дополнительном воплощении m равен 1. В еще одном дополнительном воплощении n равен 1. В конкретном воплощении m равен 1 и n равен 1.
В дополнительном воплощении Х представляет собой -О-.
В еще одном дополнительном воплощении R2, R2', R3 и R3' каждый представляет собой алкил, такой как метил, m равен 1 и n равен 1.
В дополнительном воплощении R2, R2', R3 и R3' каждый представляет собой водород, m равен 1 и n равен 1.
В дополнительном воплощении R2 и R3 вместе образуют -(СН2)2-, R2' и R3' представляют собой водород, m равен 1 и n равен 1.
В еще одном дополнительном воплощении Q представляет собой хромен-2-он-4-ил, хромен-2-он-6-ил или хромен-2-он-7-ил. В конкретном воплощении Q представляет собой хромен-2-он-4-ил. В дополнительном воплощении Q представляет собой хромен-2-он-6-ил. В еще одном дополнительном воплощении Q представляет собой хромен-2-он-7-ил. В дополнительном воплощении Q представляет собой хромен-2-он, замещенный алкилом, таким как метил. В конкретном воплощении Q представляет собой 4-метил-хромен-2-он-6-ил.
В конкретном воплощении химическим соединением по изобретению не является 6-бром-4-(пиперидин-4-илокси)-1-бензопиран-2-он.
В конкретном воплощении химическим соединением по изобретению является
экзо-7-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-он;
экзо-4-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-он;
экзо-6-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-4-метил-хромен-2-он;
экзо-6-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-он;
7-(1-метил-пиперидин-4-илокси)-хромен-2-он;
7-(1,2,2,6,6-пентаметил-пиперидин-4-илокси)-хромен-2-он;
7-(2,2,6,6-тетраметил-пиперидин-4-илокси)-хромен-2-он;
экзо-7-(8-Н-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-он;
экзо-6-(8-Н-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-он;
или их фармацевтически приемлемая соль.
Любая комбинация двух или более описанных выше воплощений рассматривается в объеме настоящего изобретения.
Определение заместителей
В контексте данного изобретения галогено представляет собой фторо, хлоро, бромо или йодо.
В контексте данного изобретения алкильная группа означает одновалентную насыщенную неразветвленную или разветвленную углеводородную цепь. Углеводородная цепь предпочтительно содержит от одного до шести атомов углерода (C1-6-алкил), включая пентил, изопентил, неопентил, третичный пентил, гексил и изогексил. В предпочтительном воплощении алкил представляет собой C1-4-алкильную группу, включая бутил, изобутил, вторичный бутил и третичный бутил. В другом предпочтительном воплощении данного изобретения алкил представляет собой C1-3-алкильную группу, которая может быть, в частности, метилом, этилом, пропилом или изопропилом.
В контексте данного изобретения алкенильная группа означает углеродную цепь, содержащую одну или более двойных связей, включая диены, триены и полиены. В предпочтительном воплощении алкенильная группа по изобретению содержит от двух до шести атомов углерода (С2-6-алкенил) вместе с по меньшей мере одной двойной связью. В наиболее предпочтительном воплощении алкенильная группа по изобретению является этенилом; 1- или 2-пропенилом; 1-, 2- или 3-бутенилом или 1,3-бутадиенилом; 1-, 2-, 3-, 4- или 5-гексенилом или 1,3-гексадиенилом, или 1,3,5-гексатриенилом.
В контексте данного изобретения алкинильная группа означает углеродную цепь, содержащую одну или более тройных связей, включая диины, триины и полиины. В предпочтительном воплощении алкинильная группа по изобретению содержит от двух до шести атомов углерода (С2-6-алкинил) вместе с по меньшей мере одной тройной связью. В своем наиболее предпочтительном воплощении алкинильная группа по изобретению является этинилом; 1- или 2-пропинилом; 1-, 2- или 3-бутинилом или 1,3-бутадиинилом; 1-, 2-, 3-, 4-пентинилом или 1,3-пентадиинилом; 1-, 2-, 3-, 4- или 5-гексинилом или 1,3-гексадиинилом, или 1,3,5-гексатриинилом.
В контексте данного изобретения циклоалкильная группа означает циклическую алкильную группу, предпочтительно содержащую от трех до семи атомов углерода (С3-7-циклоалкил), включая циклопропил, циклобутил, циклопентил, циклогексил и циклогептил.
Алкокси представляет собой О-алкил, где алкил определен выше.
Циклоалкокси означает О-циклоалкил, где циклоалкил определен выше.
Циклоалкилалкил означает указанный выше циклоалкил и указанный выше алкил; например, означает циклопропилметил.
Амино представляет собой NH2, или NH-алкил, или N-(алкил)2, где алкил определен выше.
В контексте данного изобретения арильная группа означает карбоциклическую ароматическую кольцевую систему, такую как фенил, нафтил (1-нафтил или 2-нафтил) или флуоренил.
Фармацевтически приемлемые соли
Химическое соединение по изобретению может быть представлено в любой форме, подходящей для назначенного введения. Подходящие формы включают фармацевтически (то есть физиологически) приемлемые соли и пре- или пролекарственные формы химического соединения по изобретению.
Примеры фармацевтически приемлемых солей присоединения включают, без ограничения, нетоксичные соли присоединения неорганических и органических кислот, такие как гидрохлорид, гидробромид, нитрат, перхлорат, фосфат, сульфат, формиат, ацетат, аконат (aconate), аскорбат, бензолсульфонат, бензоат, циннамат, цитрат, эмбонат, энантат, фумарат, глутамат, гликолят, лактат, малеат, малонат, манделат, метансульфонат, производное нафталин-2-сульфоната, фталат, салицилат, сорбат, стеарат, сукцинат, тартрат, толуол-п-сульфонат и тому подобное. Такие соли могут быть образованы по хорошо известным и описанным в данной области техники методикам.
Примеры фармацевтически приемлемых катионных солей химического соединения по изобретению включают, без ограничения, натриевую, калиевую, кальциевую, магниевую, цинковую, алюминиевую, литиевую, соль холина, соль лизина и аммониевую соль (и тому подобную) химического соединения по изобретению, содержащего анионную группу. Такие катионные соли могут быть образованы по хорошо известным и описанным в данной области техники методикам.
В контексте данного изобретения "ониевые соли" N-содержащих соединений также предусмотрены в качестве фармацевтически приемлемых солей. Предпочтительные "ониевые соли" включают алкил-ониевые соли, циклоалкил-ониевые соли и циклоалкилалкил-ониевые соли.
Примеры пре- и пролекарственных форм химического соединения по изобретению включают примеры подходящих пролекарств веществ по изобретению, включают соединения, модифицированные по одной или более чем одной реакционно-способной или способной к дериватизации группе исходного соединения. Особый интерес представляют соединения, модифицированные по карбоксильной группе, гидроксильной группе или аминогруппе. Примерами подходящих производных являются сложные эфиры или амиды.
Химическое соединение по изобретению может быть представлено в растворимой или нерастворимой формах вместе с фармацевтически приемлемым растворителем, таким как вода, этанол и тому подобное. Растворимые формы могут также включать гидратированные формы, такие как моногидрат, дигидрат, гемигидрат, тригидрат, тетрагидрат и тому подобное. В общем, для целей данного изобретения растворимые формы признаются эквивалентными нерастворимым формам.
Пространственные изомеры
Специалистам в данной области техники будет понятно, что соединения по настоящему изобретению могут содержать один или более хиральных центров и что такие соединения существуют в форме изомеров.
Также некоторые химические соединения по изобретению, имеющие -С=С- двойную связь, могут существовать в двух формах, син- и анти-форме (Z- и Е-форме), в зависимости от расположения заместителей около двойной связи. Химическое соединение по настоящему изобретению может таким образом быть в син- или анти-форме или может представлять собой их смесь.
Более того, химические соединения по настоящему изобретению могут существовать в виде энантиомеров в (+) и (-) формах, а также в рацемических формах (±).
Изобретение включает все такие изомеры и любые их смеси, включая рацемические смеси.
Рацемические формы могут быть разделены на оптические антиподы известными методами и способами. Одним из путей разделения изомерных солей является применение оптически активной кислоты и выделение оптически активного аминного соединения путем обработки основанием. Другой способ разделения рацематов на оптические антиподы основан на хроматографии на оптически активной матрице. Рацемические соединения по настоящему изобретению таким образом могут быть разделены на их оптические антиподы, например, фракционной кристаллизацией d- или l-солей (тартраты, манделаты или камфорсульфонат), например.
Химические соединения по настоящему изобретению также могут быть разделены путем образования диастереомерных амидов в результате реакции химических соединений по настоящему изобретению с оптически активной активированной карбоновой кислотой, такой как производное от (+) или (-) фенилаланина, (+) или (-) фенилглицина, (+) или (-) камфановой кислоты, или путем образования диастереомерных карбаматов в результате реакции химического соединения по настоящему изобретению с оптически активным хлороформиатом или тому подобным.
Дополнительные способы разделения оптических изомеров известны в данной области техники. Такие способы включают в себя описанные Jaques J, Collet A & Wilen S в "Enantiomers, Racemates, and Resolutions" (John Wiley and Sons, New York (1981)).
Оптически активные соединения также могут быть приготовлены из оптически активных исходных материалов.
Меченые соединения
Соединения по изобретению можно применять в их меченой или немеченой форме. В контексте данного изобретения меченое соединение имеет один или более чем один атом, замененный атомом, имеющим атомную массу или массовое число, отличающееся от атомной массы или массового числа, которые обычно встречаются в природе. Метка обеспечивает возможность легкого количественного определения указанного соединения.
Меченые соединения по изобретению можно применять в качестве диагностических средств, радиоактивных индикаторов или контрольного агента в различных диагностических методах и для визуализации рецепторов in vivo.
Меченый изомер по изобретению предпочтительно содержит по меньшей мере один радионуклид в качестве метки. Все позитрон-излучающие радионуклиды являются кандидатами на применение. В контексте данного изобретения радионуклид предпочтительно выбран из 2H (дейтерия), 3H (трития), 13С, 14С, 131I, 125I, 123I и 18F.
Физический способ обнаружения меченого изомера по настоящему изобретению может быть выбран из позитронной эмиссионной томографии (PET), однофотонной визуализирующей компьютерной томографии (SPECT), магнитно-резонансной спектроскопии (MRS), магнитно-резонансной визуализации (MRI) и компьютерной аксиальной рентгеновской томографии (CAT) или их комбинаций.
Способы получения
Химические соединения по изобретению могут быть получены общепринятыми способами химического синтеза, например, описанными в рабочих примерах. Исходные материалы для способов, описанных в настоящей заявке, являются известными или могут быть легко получены общепринятыми способами из имеющихся в продаже химических веществ.
Также одно соединение по изобретению может быть превращено в другое соединение по изобретению с использованием общепринятых способов.
Конечные продукты описанных здесь реакций могут быть выделены по общепринятым методикам, например, экстракцией, кристаллизацией, дистилляцией, хроматографией и так далее.
Биологическая активность
Соединения по изобретению могут быть испытаны на их способность ингибировать обратный захват моноаминов дофамина, норадреналина и серотонина в синаптосомах, например, так, как описано в WO 97/30997 (NeuroSearch A/S). Основываясь на сбалансированной активности, наблюдавшейся в этих испытаниях, соединение по изобретению рассматривается полезным для лечения, предупреждения или облегчения заболевания, или расстройства, или состояния млекопитающего, включая человека, которое чувствительно к ингибированию обратного захвата моноаминовых нейромедиаторов в центральной нервной системе.
В конкретном воплощении соединения по изобретению рассматриваются полезными для лечения, предупреждения или облегчения: расстройства настроения, депрессии, атипичной депрессии, вторичной депрессии из-за боли, глубокого депрессивного расстройства, дистимического расстройства, биполярного расстройства, биполярного расстройства I, биполярного расстройства II, циклотимического расстройства, расстройства настроения вследствие общего медицинского состояния, расстройства настроения, вызванного веществами, псевдодеменции, синдрома Ганзера, обсессивно-компульсивного расстройства, панического расстройства, панического расстройства без агорафобии, панического расстройства с агорафобией, агорафобии без панического расстройства в анамнезе, острого тревожного состояние с реакцией паники, дефицитов памяти, потери памяти, синдрома дефицита внимания с гиперактивностью, ожирения, тревоги, расстройства генерализованной тревоги, расстройства приема пищи, болезни Паркинсона, паркинсонизма, деменции, старческой деменции, сенильной деменции, болезни Альцгеймера, комплекса деменции и синдрома приобретенного иммунодефицита, старческой дисфункции памяти, специфической фобии, социальной фобии, посттравматического стрессового расстройства, острого стрессового расстройства, лекарственного привыкания, лекарственного злоупотребления, кокаинового злоупотребления, никотинового злоупотребления, табачного злоупотребления, хронического алкоголизма, алкоголизма, боли, хронической боли, воспалительной боли, невропатической боли, мигреневой боли, головной боли напряженного типа, головной боли хронического типа, боли, связанной с депрессией, фибромиалгии, артрита, остеоартрита, ревматоидного артрита, боли в спине, раковой боли, боли при раздраженном кишечнике, синдрома раздраженного кишечника, послеоперационной боли, постмастэктомического болевого синдрома (PMPS), боли после удара, невропатии, вызванной лекарственным средством, диабетической невропатии, симпатически поддерживаемой боли, невралгии тройничного нерва, зубной боли, миофасциальной боли, фантомной боли, булимии, предменструального синдрома, синдрома поздней лютеиновой фазы, посттравматического синдрома, синдрома хронической усталости, недержания мочи, стрессового недержания, неудержания, ночного недержания, сексуальной дисфункции, преждевременной эякуляции, эректильного затруднения, эректильной дисфункции, преждевременного женского оргазма, синдрома "беспокойных ног", расстройств приема пищи, нервно-психической анорексии, расстройств сна, глубоких расстройств развития, аутизма, синдрома Аспергера, синдрома Ретта, дезинтегративного расстройства детского возраста, необучаемостей, расстройств двигательных навыков, мутизма, трихотилломании, нарколепсии, депрессии после удара, повреждения мозга, вызванного ударом, нейронального повреждения, вызванного ударом, или болезнью Жиль де ля Туретта. В предпочтительном воплощении соединения рассматриваются полезными для лечения, предупреждения или облегчения депрессии.
Настоящим предусмотрено, что подходящей дозировкой активного фармацевтического ингредиента (API) является диапазон от приблизительно 0,1 до приблизительно 1000 мг API в сутки, более предпочтительно от приблизительно 10 до приблизительно 500 мг API в сутки, наиболее предпочтительно от приблизительно 30 до приблизительно 100 мг API в сутки, в зависимости, однако, от правильного пути введения, формы введения, рассматриваемых показаний, субъекта и, в частности, массы тела затрагиваемого субъекта и, кроме того, предпочтения и опыта лечащего врача или ветеринара.
Предпочтительные соединения по изобретению проявляют биологическую активность в субмикромолярном и микромолярном диапазоне, то есть ниже 1 до приблизительно 100 мкМ.
Фармацевтические композиции
В другом аспекте изобретения предлагаются новые фармацевтические композиции, содержащие терапевтически эффективное количество химического соединения по изобретению,
Хотя химическое соединение по изобретению для применения в терапии можно вводить в форме необработанного химического соединения, предпочтительным является внесение активного ингредиента, возможно в форме физиологически приемлемой соли, в фармацевтическую композицию вместе с одним или более адъювантами, эксципиентами, носителями, буферами, разбавителями и/или другими обычными фармацевтическими добавками.
В предпочтительном воплощении изобретения предлагаются фармацевтические композиции, содержащие химическое соединение по изобретению или его фармацевтически приемлемые соль или производное вместе с одним или более фармацевтически приемлемыми носителями и, возможно, другими терапевтическими и/или профилактическими ингредиентами, известными и применяемыми в данной области техники. Носитель(и) должен(ны) быть "приемлемым(и)" в смысле совместимости с другими ингредиентами композиции и безвредности для реципиента.
Фармацевтические композиции по изобретению могут быть подходящими для перорального, ректального, бронхиального, назального, пульмонального, местного (включая трансбуккальное и подъязычное), трансдермального, вагинального или парентерального (включая кожную, подкожную, внутримышечную, внутрибрюшинную, внутривенную, внутриартериальную, внутрицеребральную, внутриглазную инъекцию или инфузию) введения или быть в форме, подходящей для введения путем ингаляции или инсуффляции, включая порошки и жидкое аэрозольное введение, или системами замедленного высвобождения. Подходящие примеры систем замедленного высвобождения включают полупроницаемые матрицы твердых гидрофобных полимеров, содержащих соединение по изобретению, которые (матрицы) могут быть в виде частиц определенной формы, например пленок или микрокапсул.
Так, химическое соединение по изобретению вместе с общепринятым адъювантом, носителем или разбавителем могут быть помещены в форму фармацевтических композиций и их стандартные лекарственные формы. Такие формы включают твердые вещества, в частности таблетки, капсулы с наполнителем, порошковые формы и формы гранул, и жидкости, в частности водные и неводные растворы, суспензии, эмульсии, эликсиры и заполненные тем же капсулы, все для перорального применения, суппозитории для ректального введения и стерильные растворы для инъекций для парентерального применения. Такие фармацевтические композиции и их стандартные лекарственные формы могут содержать общепринятые ингредиенты в общепринятых пропорциях с или без дополнительных активных соединений или действующих начал, и такие стандартные лекарственные формы могут содержать любое подходящее эффективное количество активного ингредиента, соразмерное с планируемым суточным диапазоном дозы для употребления.
Химическое соединение по настоящему изобретению можно вводить в широком множестве пероральных и парентеральных лекарственных форм. Для специалистов в данной области техники будет очевидно, что следующие лекарственные формы могут содержать в качестве активного компонента или химическое соединение по изобретению, или фармацевтически приемлемую соль химического соединения по изобретению.
Для приготовления фармацевтических композиций из химического соединения по настоящему изобретению фармацевтически приемлемые носители могут быть или твердыми, или жидкими. Препараты в твердой форме включают порошки, таблетки, пилюли, капсулы, облатки, суппозитории и дисперсные гранулы. Твердый носитель может быть одним или более веществами, которые также могут действовать в качестве разбавителей, корригентов, солюбилизаторов, смазывающих веществ, суспендирующих агентов, связующих веществ, консервантов, разрыхлителей таблеток или инкапсулирующего материала.
В порошках носитель представляет собой мелкоизмельченное твердое вещество, которое находится в смеси с мелкоизмельченным активным компонентом.
В таблетках активный компонент в подходящих пропорциях смешан с носителем, имеющим необходимую связывающую способность, и спрессован до желаемых формы и размера.
Порошки и таблетки предпочтительно содержат от пяти или десяти до приблизительно семидесяти процентов активного соединения. Подходящими носителями являются карбонат магния, стеарат магния, тальк, сахар, лактоза, пектин, декстрин, крахмал, желатин, трагакант, метил целлюлоза, натриевая карбоксиметилцеллюлоза, низкоплавкий воск, масло какао и тому подобное. Термин "препарат" подразумевает включение композиции активного соединения с инкапсулирующим материалом в качестве носителя, обеспечивающей капсулу, в которой активный компонент, с носителями или без них, окружен носителем, который таким образом связан с ним. Похожим образом включены облатки и лепешки. Таблетки, порошки, капсулы, пилюли, облатки и лепешки можно применять в виде твердых форм, подходящих для перорального введения.
Для приготовления суппозиториев сначала плавят низкоплавкий воск, такой как смесь глицерида жирной кислоты или масло какао, и там гомогенно распределяют активный компонент, например, путем перемешивания. Расплавленную гомогенную смесь затем вливают в формы с общепринятыми размерами, оставляют охладиться и тем самым затвердеть.
Композиции, подходящие для вагинального введения, могут быть представлены пессариями, тампонами, кремами, гелями, пастами, пенами или спреями, содержащими в добавление к активному ингредиенту такие носители, про которые в данной области техники известно, что они являются подходящими.
Жидкие препараты включают растворы, суспензии и эмульсии, например водные или водно-пропиленгликолевые растворы. Например, жидкие препараты для парентеральных инъекций могут быть приготовлены в виде растворов в водном растворе полиэтиленгликоля.
Химическое соединение по настоящему изобретению может быть таким образом приготовлено для парентерального введения (например, инъекцией, например, болюсной инъекцией или длительной инфузией) и может быть представлено в стандартной лекарственной форме в ампулах, предзаполненных шприцах, инфузии малых объемов или в мультидозовых контейнерах с добавленным консервантом. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных и водных растворителях, и могут содержать формирующие агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Альтернативно, активный ингредиент может быть в форме порошка, полученного асептической изоляцией стерильного твердого вещества или лиофилизацией из раствора, для объединения с подходящим растворителем, например стерильной апирогенной водой, перед применением.
Водные растворы, подходящие для перорального применения, могут быть получены растворением активного компонента в воде и добавлением подходящих красителей, корригентов, стабилизирующих агентов и загустителей, по желанию.
Водные суспензии, подходящие для перорального применения, могут быть получены диспергированием мелкоизмельченного активного компонента в воде с вязким материалом, таким как натуральные или синтетические смолы, полимеры, метилцеллюлоза, натриевая карбоксиметилцеллюлоза или другие широко известные суспендирующие агенты.
Включены также препараты в твердой форме, предназначенные для быстрого превращения перед применением в препараты в жидкой форме для перорального введения. Такие жидкие формы включают растворы, суспензии и эмульсии. В добавление к активному компоненту такие препараты могут содержать красители, корригенты, стабилизаторы, буферы, искусственные и натуральные подсластители, диспергирующие агенты, загустители, солюбилизирующие агенты и тому подобное.
Для местного введения в эпидермис химическое соединение по изобретению может быть приготовлено в виде мазей, кремов или лосьонов или трансдермального пластыря. Мази и кремы могут быть приготовлены, например, на водной или масляной основе с добавлением подходящих загустителей и/или гелеобразующих агентов. Лосьоны могут быть приготовлены на водной или масляной основе и обычно также содержат один или более чем один эмульгатор, стабилизирующий агент, диспергирующий агент, суспендирующий агент, загуститель или краситель.
Композиции, подходящие для местного введения в рот, включают лепешки, содержащие активный агент на вкусовой основе, обычно сахарозе и гуммиарабике или траганте; пастилки, содержащие активный ингредиент на инертной основе, такой как желатин и глицерин или сахароза и гуммиарабик; и жидкости для полоскания полости рта, содержащие активный ингредиент в подходящем жидком носителе.
Непосредственно в полости носа растворы или суспензии применяются при помощи традиционных средств, например, с капельницей, пипеткой или спреем. Композиции могут быть предоставлены в одиночной или мультидозовой форме.
Введение в дыхательные пути также может быть достигнуто посредством аэрозольного препарата, в котором активный ингредиент предоставляется в упаковке под давлением с подходящим пропеллентом, таким как хлорфторуглерод (CFC), например дихлордифторметан, трихлорфторметан или дихлортетрафторэтан, диоксид углерода или другой подходящий газ. Аэрозоль также может традиционно содержать поверхностно-активное вещество, такое как лецитин. Доза лекарства может контролироваться посредством обеспечения дозирующим клапаном.
Альтернативно, активные ингредиенты могут быть предоставлены в форме сухого порошка, например порошковой смеси соединения на подходящей порошковой основе, такой как лактоза, крахмал, крахмальные производные, такие как гидроксипропилметилцеллюлоза и поливинилпирролидон (PVP). Порошковый носитель традиционно образует гель в полости носа. Порошковая композиция может быть представлена в стандартной лекарственной форме, например в капсулах или картриджах из, например, желатина, или блистерных упаковках, из которых порошок может быть введен посредством ингалятора.
В композициях, предназначенных для введения в дыхательные пути, включая интраназальные композиции, соединение обычно будет иметь небольшой размер частиц, например порядка 5 микрон или менее. Такой размер частиц может быть получен способами, которые известны в данной области техники, например микронизацией.
При необходимости могут применяться композиции, адаптированные для замедленного высвобождения активного ингредиента.
Фармацевтические препараты предпочтительно находятся в стандартных лекарственных формах. В такой форме препарат разделен на стандартные дозы, содержащие подходящие количества активного компонента. Стандартная лекарственная форма может быть упакованным препаратом, где упаковка содержит дискретные количества препарата, такие как упакованные таблетки, капсулы и порошки в пузырьках или ампулах. Также стандартная лекарственная форма сама может быть капсулой, таблеткой, облаткой или лепешкой или может представлять собой соответствующее количество любого из них в упакованной форме.
Предпочтительными композициями являются таблетки или капсулы для перорального введения и жидкости для внутривенного введения и длительной инфузии.
Дополнительные подробности способов приготовления и введения можно найти в последнем издании Remington's Pharmaceutical Sciences (Maack Publishing Co., Easton, PA).
Терапевтически эффективная доза относится к такому количеству активного ингредиента, которое улучшает симптомы или состояние. Терапевтическая эффективность и токсичность, например ED50 и LD50, могут быть определены стандартными фармакологическими процедурами на клеточных культурах или экспериментальных животных. Дозовое соотношение между терапевтическими и токсическими эффектами является терапевтическим индексом и может быть выражено соотношением LD50/ED50. Фармацевтические композиции, проявляющие высокие терапевтические индексы, являются предпочтительными.
Доза для введения, конечно, должна быть тщательно выверена по возрасту, массе и состоянию человека, находящегося на лечении, также как по способу введения, лекарственной форме и режиму, а желаемый результат и точная дозировка должна, конечно, определяться практикующим врачом.
Фактическая дозировка зависит от природы и тяжести заболевания, которое лечат, и остается на усмотрение врача, и может изменяться титрованием дозы по отношению к конкретным случаям данного изобретения для получения желаемого терапевтического эффекта. Настоящим, однако, предусмотрено, что подходящими для терапевтического лечения являются фармацевтические композиции, содержащие от приблизительно 0,1 до приблизительно 500 мг активного ингредиента в индивидуальной дозе, предпочтительно от приблизительно 2 до приблизительно 100 мг, наиболее предпочтительно от приблизительно 1 до приблизительно 10 мг.
Активный ингредиент можно вводить в одной или в нескольких дозах в сутки. В отдельных случаях удовлетворительный результат может быть получен уже при дозе 0,1 мкг/кг внутривенно (в.в.) и 1 мкг/кг перорально (п.о.). Верхней границей диапазона дозы в настоящее время считается приблизительно 10 мг/кг в.в. и 100 мг/кг п.о. Предпочтительными диапазонами являются от приблизительно 0,1 мкг/кг до приблизительно 10 мг/кг/сутки в.в. и от приблизительно 1 мкг/кг до приблизительно 100 мг/кг/сутки п.о.
Способы лечения
В другом аспекте изобретения предлагается способ лечения, предупреждения или облегчения заболевания, или расстройства, или состояния живого организма животного, включая человека, причем заболевание, расстройство или состояние чувствительно к ингибированию обратного захвата моноаминовых нейромедиаторов в центральной нервной системе, и этот способ включает введение такому нуждающемуся в нем живому организму животного, включая человека, эффективного количества химического соединения по изобретению.
Настоящим предусмотрено, что подходящими диапазонами дозировки являются от 0,1 до 1000 миллиграммов в сутки, 10-500 миллиграммов в сутки и особенно 30-100 миллиграммов в сутки, в зависимости, как обычно, от правильного пути введения, формы введения, показания для назначения введения, затрагиваемого субъекта и массы тела затрагиваемого субъекта и, кроме того, предпочтения и опыта ответственного лечащего врача или ветеринара.
Примеры
Далее изобретение проиллюстрировано ссылкой на следующие ниже примеры, которые не предназначены для какого-либо ограничения объема заявленного изобретения.
Общие положения: Все реакции, в которых участвовали чувствительные к воздуху реагенты или промежуточные соединения, проводили в атмосфере азота и в безводных растворителях. В качестве осушающего агента в рабочих методиках использовали сульфат магния, растворители выпаривали при пониженном давлении.
Способ А
Экзо-7-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-оновая соль фумаровой кислоты
Смесь трифенилфосфина (17,6 г, 67 ммоль) и диоксана (150 мл) перемешивали и охлаждали до 8°С, после чего медленно добавляли диэтилазодикарбоксилат (10,4 мл, 67 ммоль) при температуре ниже 15°С. Охлаждение удаляли, добавляли тропин (7,9 г, 56 ммоль) и 7-гидрокси-кумарин (10 г, 62 ммоль) и реакционную смесь оставляли перемешиваться в течение 15 часов. Реакционную смесь перемешивали при 65°С в течение 5 часов. Добавляли водный гидроксид натрия (100 мл, 1 М) и экстрагировали диэтиловым эфиром (2×100 мл). Фазу диэтилового эфира промывали водой (50 мл). Хроматография сырой смеси на силикагеле с дихлорметаном, метанолом и концентрированным аммиаком (96:3:1) дала указанное в заголовке соединение в форме свободного основания в виде масла. Выход 2,0 г (13%). Соответствующую соль получали путем добавления смеси диэтилового эфира и метанола (9:1), насыщенной фумаровой кислотой. Т.пл. (температура плавления) 252°С.
Экзо-4-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-оновое свободное основание
Получали из 4-гидроксикумарина согласно способу А. Т.пл. 143,5-146,5°С.
Экзо-6-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-4-метил-хромен-2-оновая соль соляной кислоты
Получали из 6-гидрокси-4-метилкумарина согласно способу А. Т.пл. >250°С (разл.).
Экзо-7-(8-трет-бутоксикарбонил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-оновое свободное основание (промежуточное соединение)
Получали в виде масла согласно способу А.
Экзо-6-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-оновая соль соляной кислоты
Получали из 6-гидроксикумарина согласно способу А. Т.пл. 278°С.
7-(1-Метил-пиперидин-4-илокси)-хромен-2-оновая соль фумаровой кислоты
Получали из 7-гидроксикумарина и 4-гидрокси-1-метилпиперидина согласно способу А. Т.пл. 205-210°С.
Способ Б
7-(1,2,2,6,6-Пентаметил-пиперидин-4-илокси)-хромен-2-оновая соль соляной кислоты
Смесь трифенилфосфина (9,4 г, 36 ммолъ) и диоксана (100 мл) перемешивали при комнатной температуре, после чего медленно добавляли диэтилазодикарбоксилат (5,6 мл, 36 ммоль). Добавляли 4-гидрокси-1,2,2,6,6-пентаметил-пиперидин (5,1 г, 30 ммоль) (полученный из 1,2,2,6,6-пентаметил-пиперидин-4-она путем восстановления борогидридом натрия) и 7-гидроксикумарин (5,2 г, 32 ммоль) и реакционную смесь оставляли перемешиваться в течение 15 часов при комнатной температуре, после чего перемешивали при 40°С в течение 4 часов. Добавляли водный гидроксид натрия (100 мл, 1 М) и диэтиловым эфиром (2×50 мл) экстрагировали смесь. Фазу диэтилового эфира промывали водой (50 мл). Объем эфирной фазы уменьшали до 30 мл и отфильтровывали кристаллический оксид трифенилфосфина. Фильтрат смешивали с соляной кислотой (30 мл, 1 М) и два раза промывали диэтиловым эфиром (2×50 мл). Водную смесь доводили до щелочного состояния путем добавления концентрированного аммиака. Продукт выпадал в осадок в виде свободного основания, и его собирали фильтрованием. Свободное основание растворяли в этилацетате (40 мл) и добавляли соляную кислоту (2 мл, 3 М). Продукт выпадал в осадок в виде соли соляной кислоты, и его отфильтровывали. Продукт подвергали перекристаллизации из изопропилового спирта (50 мл). Выход 1,05 г (10%). Т.пл. 273°С.
Способ В
7-(2,2,6,6-Тетраметил-пиперидин-4-илокси)-хромен-2-оновая соль соляной кислоты
Смесь 7-(1,2,2,6,6-пентаметил-пиперидин-4-илокси)-хромен-2-она (0,69 г, 2,2 ммоль), диэтилазодикарбоксилата (1,0 мл, 6,6 мл) и толуола (50 мл) перемешивали при 115°С в течение 15 часов. К смеси добавляли соляную кислоту (10 мл, 2н.) и кипятили с обратным холодильником в течение 1 часа. Смесь охлаждали, и продукт выпадал в осадок в виде соли соляной кислоты. Выход 0,26 г (37%). Т.пл. >300°С.
Способ Г
Экзо-7-(8-Н-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-оновая соль соляной кислоты
Смесь экзо-7-(8-трет-бутоксикарбонил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-она (0,60 г, 1,6 ммоль) и соляной кислоты (10 мл, 1 М) в уксусной кислоте перемешивали в течение 1 часа. Добавляли диэтиловый эфир, осадок отфильтровывали и промывали диэтиловым эфиром (10 мл). Выход 0,28 г (57%). Т.пл. >300°С.
Способ Д
Экзо-6-(8-Н-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-оновая соль соляной кислоты
Смесь экзо-6-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-она (0,90 г, 3,15 ммоль), 2,2-трихлорэтил-хлорформиата (2,00 г, 9,4 ммоль) и толуола (20 мл) перемешивали при нагревании с обратным холодильником в течение 15 часов. Добавляли воду (20 мл), органическую фазу отделяли и промывали водой (20 мл). Толуоловую фазу упаривали. Добавляли уксусную кислоту (5 мл), воду (5 мл) и цинковый порошок (1,03 г, 15,77 ммоль) и перемешивали в течение 70 часов. Добавляли водный гидроксид натрия (10 мл, 1 М) и диэтиловым эфиром (2×30 мл) экстрагировали смесь. Выделяли свободное основание, выход 0,86 г (94%). Осаждали соль соляной кислоты. Т.пл. >280°С.
In vitro ингибирование обратного захвата 3 H-дофамина ( 3 H-DA) в стриарных синаптосомах
Получение тканевых препаратов: Получение тканевых препаратов выполняли при 0-4°С, если не указано иное. Полосатое тело из самцов крысы Wistar (150-200 г) гомогенезировали в течение 5-10 секунд в 100 объемах охлажденного во льду 0,32 М раствора сахарозы, содержащего 1 мМ паргилина, с использованием гомогенизатора Ultra-Turrax. Активность моноаминоксидазы ингибируется в присутствии паргилина. Гомогенат центрифугируют при 1000×g в течение 10 минут. Полученный супернатант затем центрифугируют при 27000×g в течение 50 минут и супернатант отбрасывают. Остаток после центрифугирования (Р2) ресуспендируют в оксигенированном (уравновешенном в атмосфере 96% О2: 4% СО2 в течение по меньшей мере 30 минут) инкубационном буфере Кребса-Рингера (8000 мл на г первоначальной ткани) при рН 7,2, содержащем 122 мМ NaCl, 0,16 mM ЭДТА (этилендиаминтетрауксусная кислота), 4,8 мМ KCl, 12,7 мМ Na2HPO4, 3,0 мМ NaH2PO4, 1,2 мМ MgSO4, 1 мМ CaCl2, 10 мМ глюкозы и 1 мМ аскорбиновой кислоты.
Анализ: Аликвоты 4,0 мл тканевой суспензии добавляют к 100 мкл тестируемого раствора и 100 мкл 3H-DA (1 нМ, конечная концентрация), смешивают и инкубируют в течение 25 минут при 37°С. Неспецифический обратный захват определяют с использованием бензотропина (10 мкМ, конечная концентрация). После инкубации образцы выливают прямо на стекловолокнистые фильтры Whatman GF/C под разрежением. Эти фильтры затем промывают три раза 5 мл охлажденного во льду 0,9% (мас./об.) раствора NaCl. Количество радиоактивности на фильтрах определяют общепринятым методом регистрации жидкостной сцинтилляции. Специфический обратный захват вычисляют как разницу между общим обратным захватом и неспецифическим обратным захватом.
Должно быть достигнуто 25-75% ингибирование специфического связывания, после чего производят вычисление IC50.
Тестируемое значение приводится как IC50 (концентрация (мкМ) тестируемого вещества, которое ингибирует специфическое связывание 3H-DA на 50%).
In vitro ингибирование обратного захвата 3 H-норадреналина ( 3 H-NA) в гиппокампальных синаптосомах
Получение тканевых препаратов: Получение тканевых препаратов выполняли при 0-4°С, если не указано иное. Гиппокампы из самцов крысы Wistar (150-200 г) гомогенизировали в течение 5-10 секунд в 100 объемах охлажденного во льду 0,32М раствора сахарозы, содержащего 1 мМ паргилина, с использованием гомогенизатора Ultra-Turrax. Активность моноаминоксидазы ингибируется в присутствии паргилина. Гомогенат цетрифугируют при 1000×g в течение 10 минут. Полученный супернатант затем центрифугируют при 27000×g в течение 50 минут и супернатант отбрасывают. Остаток после центрифугирования (Р2) ресуспендируют в оксигенированном (уравновешенном в атмосфере 96% O2: 4% CO2 в течение по меньшей мере 30 минут) инкубационном буфере Кребса-Рингера (2000 мл на г первоначальной ткани) при рН 7,2, содержащем 122 мМ NaCl, 0,16 mM ЭДТА, 4,8 мМ KCl, 12,7 мМ Na2HPO4, 3,0 мМ NaH2PO4, 1,2 мМ MgSO4, 1 мМ CaCl2, 10 мМ глюкозы и 1 мМ аскорбиновой кислоты.
Анализ: Аликвоты 4,0 мл суспензии ткани добавляют к 100 мкл тестируемого раствора и 100 мкл 3H-NA (1 нМ, конечная концентрация), смешивают и инкубируют в течение 90 минут при 37°С. Неспецифический обратный захват определяют с использованием дезипрамина (10 мкМ, конечная концентрация). После инкубации образцы выливают прямо на стекловолокнистые фильтры Whatman GF/C под разрежением. Эти фильтры затем промывают три раза 5 мл охлажденного во льду 0,9% (мас./об.) раствора NaCl. Количество радиоактивности на фильтрах определяют общепринятым методом регистрации жидкостной сцинтилляции. Специфический обратный захват вычисляют как разницу между общим обратным захватом и неспецифическим обратным захватом.
Должно быть достигнуто 25-75% ингибирование специфического связывания, после чего производят вычисление IC50.
Тестируемое значение приводится как IC50 (концентрация (мкМ) тестируемого вещества, которое ингибирует специфическое связывание 3H-NA на 50%).
In vitro ингибирование обратного захвата 3 H-5-гидрокситриптамина ( 3 H-S-HT, серотонин) в кортикальных синаптосомах
Получение тканевых препаратов: Получение тканевых препаратов выполняли при 0-4°С, если не указано иное. Кору головного мозга из самцов крысы Wistar (150-200 г) гомогенизировали в течение 5-10 секунд в 100 объемах охлажденного во льду 0,32 М раствора сахарозы, содержащего 1 мМ паргилина, с использованием гомогенизатора Ultra-Turrax. Активность моноаминоксидазы ингибируется в присутствии паргилина. Гомогенат цетрифугируют при 1000×g в течение 10 минут. Полученный супернатант затем центрифугируют при 27000×g в течение 50 минут и супернатант отбрасывают. Остаток после центрифугирования (Р2) ресуспендируют в оксигенированном (уравновешенном в атмосфере 96% О2: 4% СО2 в течение по меньшей мере 30 минут) инкубационном буфере Кребса-Рингера (1000 мл на г первоначальной ткани) при рН 7,2, содержащем 122 мМ NaCl, 0,16 mM ЭДТА (этилендиаминтетрауксусная кислота), 4,8 мМ KCl, 12,7 мМ Na2HPO4, 3,0 мМ NaH2PO4, 1,2 мМ MgSO4, 1 мМ CaCl2, 10 мМ глюкозы и 1 мМ аскорбиновой кислоты.
Анализ: Аликвоты 4,0 мл суспензии ткани добавляют к 100 мкл тестируемого раствора и 100 мкл 3Н-5-1-НТ (1 нМ, конечная концентрация), смешивают и инкубируют в течение 30 минут при 37°С. Неспецифический обратный захват определяют с использованием циталопрама (10 мкМ, конечная концентрация). После инкубации образцы выливают прямо на стекловолокнистые фильтры Whatman GF/C под разрежением. Эти фильтры затем промывают три раза 5 мл охлажденного во льду 0,9% (мас./об.) раствора NaCl. Количество радиоактивности на фильтрах определяют общепринятым методом регистрации жидкостной сцинтилляции. Специфический обратный захват вычисляют как разницу между общим обратным захватом и неспецифическим обратным захватом.
Должно быть достигнуто 25-75% ингибирование специфического связывания, после чего производят вычисление IC50.
Тестируемое значение приводится как IC50 (концентрация (мкМ) тестируемого вещества, которое ингибирует специфическое связывание 3H-5-НТ на 50%).
Полученные результаты тестирования соединений по настоящему изобретению приведены в следующей далее таблице.
Представленные в таблице результаты показывают, что соединения по изобретению эффективно ингибируют обратный захват дофамина, норадреналина и серотонина в синаптосомах.
Изобретение относится к новым соединениям формулы I
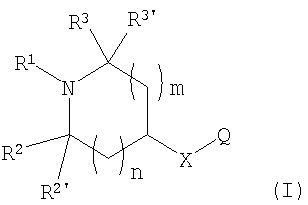
или к любому его изомеру, или любой смеси его изомеров,
или к его фармацевтически приемлемой соли,
где
R1 представляет собой водород или алкил;
R2 и R3 вместе образуют -(СН2)2-, и R2' и R3' представляют собой водород;
m равно 1;
n равно 1;
Х представляет собой -O-; и
Q представляет собой хромен-2-он-7-ил, который возможно замещен одним или более заместителями, независимо выбранными из группы, состоящей из галогено, трифторметила, трифторметокси, циано, гидрокси, амино, нитро, алкокси, циклоалкокси, алкила, циклоалкила, циклоалкилалкила, алкенила и алкинила. Изобретение также относится к фармацевтической композиции, а также к применению химического соединения по любому из пп.1-4. Технический результат - получение новых биологически активных соединений, обладающих активностью ингибиторов обратного захвата моноаминовых нейромедиаторов. 3 н. и 5 з.п. ф-лы, 1 табл.
1. Соединение формулы I
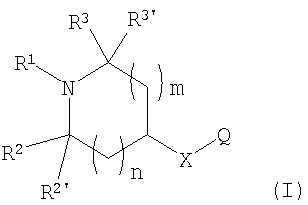
или любой из его изомеров, или любая смесь его изомеров,
или его фармацевтически приемлемая соль,
где R1 представляет собой водород или алкил;
R2 и R3 вместе образуют -(CH2)2-, и R2' и R3' представляют собой водород;
m равно 1;
n равно 1;
Х представляет собой -O-; и
Q представляет собой хромен-2-он-7-ил, который возможно замещен одним или более заместителями, независимо выбранными из группы, состоящей из галогено, трифторметила, трифторметокси, пиано, гидрокси, амино, нитро, алкокси, циклоалкокси, алкила, циклоалкила, циклоалкилалкила, алкенила и алкинила.
2. Химическое соединение по п.1, где R1 представляет собой водород.
3. Химическое соединение по п.1, где R1 представляет собой алкил.
4. Химическое соединение по п.1, которое представляет собой
экзо-7-(8-метил-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-он;
экзо-7-(8-Н-8-аза-бицикло[3.2.1]окт-3-илокси)-хромен-2-он;
или его фармацевтически приемлемая соль.
5. Фармацевтическая композиция, обладающая активностью ингибиторов обратного захвата моноаминовых нейромедиаторов, содержащая терапевтически эффективное количество соединения по любому из пп.1-4 или любого из его изомеров, или любой смеси его изомеров, или его фармацевтически приемлемой соли, вместе с по меньшей мере одним фармацевтически приемлемым носителем, эксципиентом или разбавителем.
6. Применение химического соединения по любому из пп.1-4 или любого из его изомеров, или любой смеси его изомеров, или его фармацевтически приемлемой соли для изготовления лекарства, проявляющего активность ингибиторов обратного захвата моноаминовых нейромедиаторов.
7. Применение по п.6 для изготовления фармацевтической композиции для лечения, предупреждения или облегчения заболевания или расстройства, или состояния млекопитающего, включая человека, причем заболевание, расстройство или состояние чувствительно к ингибированию обратного захвата моноаминовых нейромедиаторов в центральной нервной системе.
8. Применение по п.7, где заболевание, расстройство или состояние является расстройством настроения, депрессией, атипичной депрессией, вторичной депрессией из-за боли, глубоким депрессивным расстройством, дистимическим расстройством, биполярным расстройством, биполярным расстройством I, биполярным расстройством II, циклотимическим расстройством, расстройством настроения вследствие общего медицинского состояния, расстройством настроения, вызванным веществами, псевдодеменцией, синдромом Ганзера, обсессивно-компульсивным расстройством, паническим расстройством, паническим расстройством без агорафобии, паническим расстройством с агорафобией, агорафобией без панического расстройства в анамнезе, острым тревожным состоянием с реакцией паники, дефицитами памяти, потерей памяти, синдромом дефицита внимания с гиперактивностью, ожирением, тревогой, расстройством генерализованной тревоги, расстройством приема пищи, болезнью Паркинсона, паркинсонизмом, деменцией, старческой деменцией, сенильной деменцией, болезнью Альцгеймера, комплексом деменции и синдрома приобретенного иммунодефицита, старческой дисфункцией памяти, специфической фобией, социальной фобией, посттравматическим стрессовым расстройством, острым стрессовым расстройством, лекарственным привыканием, лекарственным злоупотреблением, кокаиновым злоупотреблением, никотиновым злоупотреблением, табачным злоупотреблением, хроническим алкоголизмом, алкоголизмом, болью, хронической болью, воспалительной болью, невропатической болью, мигреневой болью, головной болью напряженного типа, головной болью хронического типа, болью, связанной с депрессией, фибромиалгией, артритом, остеоартритом, ревматоидным артритом, болью в спине, раковой болью, болью при раздраженном кишечнике, синдромом раздраженного кишечника, послеоперационной болью, постмастэктомическим болевым синдромом (PMPS), болью после удара, невропатией, вызванной лекарственным средством, диабетической невропатией, симпатически поддерживаемой болью, невралгией тройничного нерва, зубной болью, миофасциальной болью, фантомной болью, булимией, предменструальным синдромом, синдромом поздней лютеиновой фазы, посттравматическим синдромом, синдромом хронической усталости, недержанием мочи, стрессовым недержанием, неудержанием, ночным недержанием, сексуальной дисфункцией, преждевременной эякуляцией, эректильным затруднением, эректильной дисфункцией, преждевременным женским оргазмом, синдромом "беспокойных ног", расстройствами приема пищи, нервно-психической анорексией, расстройствами сна, глубокими расстройствами развития, аутизмом, синдромом Аспергера, синдромом Ретта, дезинтегративным расстройством детского возраста, необучаемостями, расстройствами двигательных навыков, мутизмом, трихотилломанией, нарколепсией, депрессией после удара, повреждением мозга, вызванным ударом, нейрональным повреждением, вызванным ударом, или болезнью Жиль де ля Туретта.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| EP 1130020 A, 05.09.2001 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| RU 98105169 A, 20.12.1999. | |||
Авторы
Даты
2010-02-20—Публикация
2005-09-28—Подача