Предпосылки изобретения
1. Область техники, к которой относится настоящее изобретение
Настоящее изобретение относится к химии биологически активных соединений, а именно к новому способу получения водорастворимых моно-ПЭГилированных производных тетрапиррола, в частности производных хлорина, бактериохлорина, феофорбида и бактериофеофорбида типов 1, 2 и 3. Соединения настоящего изобретения могут использоваться в качестве фотосенсибилизаторов для фотодинамической терапии рака, инфекций и других заболеваний, а также для лечения световым облучением в некоторых других случаях.
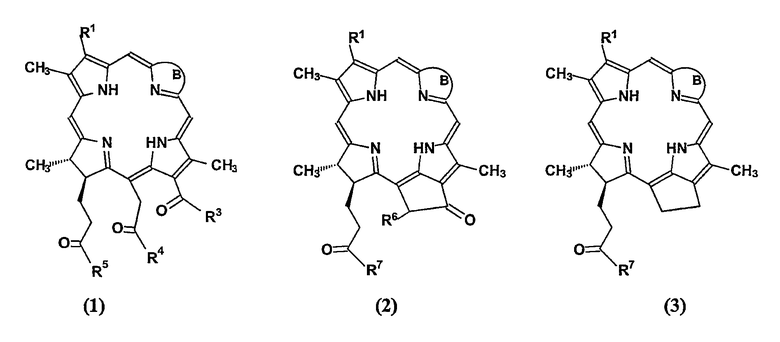
где В представляет собой цикл, имеющий структуру
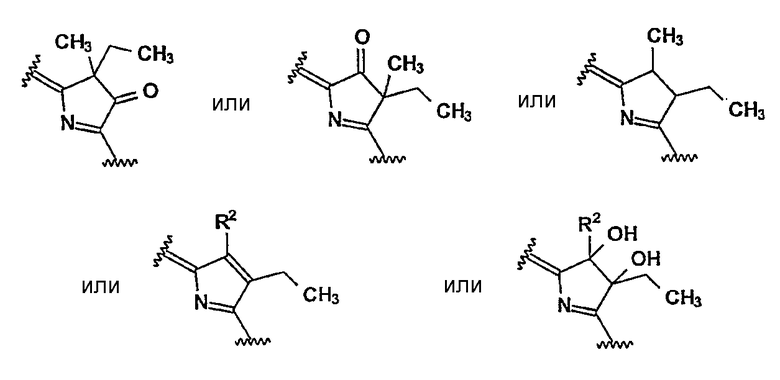
где
R1 = -CH=CH2, -CH(OAlk)CH3, -CHO, -C(O)CH3, -CH2CH3, -CH(Alk)CH(COAlk)2, -CH2CH(COAlk)2, -CH(Alk)CH2COAlk, -CH(Alk)CH2CH(OH)CH3 и -CH2CH2CH(OH)CH3;
R2 = -CH3, -CHO, -CH(OH)Alk, -CH=CHAlk, CH2OH и CH2OAlk;
R3 = -OH, -OAlk, -NH-Alk, -NR8-R9-R10, -NH(CH2)m-R11-R9-R10;
R4 = -OH, -OAlk, -NH-Alk, -NR8-R9-R10, -NH(CH2)m-R11-R9-R10;
R5 = OH, -OAlk, -NH-Alk, -NR8-R9-R10, -NH(CH2)m-R11-R9-R10;
R6 = H и -COOAlk;
R7 = NR8-R9-R10, -NH(CH2)m-R11-R9-R10;
R8 =H и -Alk;
R9 = -(CH2CH2O)nCH2CH2-;
R10 = -OH, -OAlk, -NH2, -NHAlk, -NHAcyl, -NAcyl2, -NR12R13, -COR14, -OCH2COR14;
R11 = -CH2CONR8-, -NHCOO-;
R12 = H и -Alk;
R13 = H и -Alk и
R14 = -OH, -OAlk, -NR12R13,
где:
m=2-12;
n=8-500 и
Alk = алкильный заместитель.
2. Уровень техники
Фотодинамическая терапия (photodynamic therapy - PDT) является одним из наиболее перспективных новых способов, выявленных в настоящее время для применения в различных медицинских областях, и, в частности, является широко признанным способом лечения с целью разрушения опухолей (E.D. Sternberg et al. Porphyrin based photosensitizers for Use in Photodynamic Therapy. Tetrahedron 54 (1998) 4151-4202).
Разработаны критерии, которым должно удовлетворять соединение, по меньшей мере, в некоторой степени для того, чтобы успешно применяться в PDT (R. Bonnett. Photodynamic Therapy in Historical Perspective. Rev.Contemp. Pharmacother. 1999, 10, 1-17). Такими критерии являются следующие:
1. высокий количественный выход реакционноспособных частиц, таких как синглетный кислород или радикалы;
2. относительно низкая токсичность для субъекта;
3. способность активироваться излучением с длинами волн дальнего диапазона (предпочтительно в красной или ближней инфракрасной области спектра), которое способно проникать более глубоко в ткани, чем излучение с меньшими длинами волн;
4. селективное аккумулирование клетками, которые ответственны за данное патологическое состояние, и быстрое выведение из тканей, которые не подвержены патологическому состоянию;
5. возможность сочетания с макромолекулярными носителями при сохранении характеристик фотосенсибилизационной эффективности,
6. растворимость в подходящих растворителях для облегчения введения пациенту и физиологического поглощения и транспорта в организме пациента.
Тетрапирролы представляют собой соединения, широко используемые в PDT. Основной проблемой в фармацевтическом применении тетрапирролов является их низкая растворимость в физиологических растворах. Это затрудняет получение эффективных фармацевтических растворов для инъекции для применения в PDT и других областях.
Способы получения водорастворимых производных тетрапиррола для PDT известны в данной области техники. В Патенте США № 5330741 (Smith et al.) описывается способ получения тринатриевой соли лизилхлорина р6, включающий взаимодействие между метиловым эфиром пурпурина 18, полученным в результате трансформации метилфеофорбида а, и водным лизином в метиленхлориде в присутствии пиридина. Смесь перемешивается при комнатной температуре в течение 12 часов с последующим удалением растворителей в высоком вакууме. Полученный таким образом сырой продукт очищают высокоэффективной жидкостной хроматографией (ВЭЖХ) с обращенной фазой и затем лиофилизуют. Для получения раствора для инъекций для PDT рака препарат сначала растворяют в фосфатно-буферном растворе и затем к нему добавляют 0,1 н. гидроксид натрия. Значение рН раствора доводят до 7,35 с помощью 0,1 н. HCl с последующей стерильной фильтрацией через микропористый фильтр. Недостатки описанного выше способа включают отсутствие воспроизводимости и трудность обработки и использования токсичных реагентов, что делает данный способ плохо приемлемым для фармацевтического производства. Кроме того, полученный целевой водорастворимый продукт является стабильным в водном растворе при отсутствии освещения при 4°С только в течение 24 часов, а в твердой форме в темноте при 4°С - в течение до 4 месяцев [M.W. Leach, R.J. Higgins, J.E. Boggan, S.-J. Lee, S. Autry, K.M. Smith. Effectiveness of a Lysylchlorin p6/Chlorin p6 mixture in Photodynamic Therapy of the Subcutaneous 9L Glioma in the Rat. Cancer Res., 1992, 52, 1235-1239; Патент США № 5330741].
Способ получения водорастворимой натриевой соли феофорбида а (4) описан в Патенте США № 5378835 (Nakazato). Согласно указанному изобретению феофорбид а (5) растворяют в диэтиловом эфире и к полученному раствору медленно по каплям добавляют очень разбавленный раствор щелочи в н-пропаноле, изопропаноле или в их смеси. Реакцию осуществляют до полного осаждения соли феофорбида а (4), которую собирают центрифугированием и сушат в вакууме. Затем продукт растворяют в воде с получением раствора с концентрацией 0,5% и значением рН в интервале от 9,2 до 9,5, который затем разбавляют фосфатным буфером с рН в интервале от 7,4 до 7,8. Недостатком данного способа, описанного Nakazato, является то, что с помощью описанного способа нельзя получить концентрированный (>1%) водный раствор феофорбида а для инъекций. Кроме того, авторы настоящего изобретения наблюдали химическую нестабильность таких солей при хранении в сухом состоянии и невозможность их полного растворения в воде после хранения в сухом состоянии.
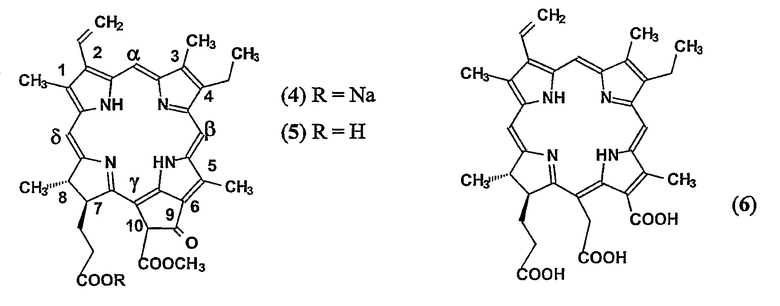
В Патенте России № 2144538 (Г.В. Пономарев и др.) описан способ получения водорастворимых комплексов хлорина е6 (6) с различными органическими аминами, включая N-метил-D-глюкозамин, многостадийной последовательностью прямых химических реакций, включая получение хлорофилла а из биомассы цианобактерии Spirulina Platensis, последующее превращение в хлорин е6 в соответствии со стандартными методиками [S. Lötjönen, P.H. Hynninen. An improved method for the preparation of (10R)- and (10S)-pheophytins a and b. Synthesis. 1983, 705-708; P.H. Hynninen, S. Lötjönen. Preparation of phorbin derivatives from chlorophyll mixture utilizing the principle of selective hydrolysis. Synthesis, 1980, 539-541; S. Lötjönen, P.H. Hynninen. A convenient method for the preparation of wet chlorin e6 and rhodin g7 trimethyl esters. Synthesis, 1980,
541-543] при общем выходе более 50% после осаждения хлорина е6 (6) методом постепенного добавления воды к его ацетоновому раствору с последующим выделением центрифугированием, троекратной промывкой водой и последовательной обработкой влажного хлорина е6 водным раствором 2 г-экв. определенного органического амина. К сожалению, образцы водорастворимых солей хлорина е6, полученные в соответствии с описанным выше способом, содержат различные примеси нететрапиррольного и тетрапиррольного типов, которые нельзя отделить от целевого хлорина е6, используя стандартные методики.
Существует способ получения фармацевтических водорастворимых производных тетрапиррола высокой чистоты, включающий следующие стадии: одно- или двухстадийный прямой кислотный алкоголиз биологического исходного вещества с получением кристаллического алкилфеофорбида, превращение полученного алкилфеофорбида в феофорбид и взаимодействие последнего с гидрофильным органическим амином в среде, выбранной из группы, включающей воду и водный органический раствор (Заявка на Патент США № 10/151764, Nefantiev et al.). Гидрофильный органический амин выбирается из группы, включающей N-метил-D-глюкамин, аминоалкилгликозиды, трис(гидроксиметил)аминометан (“TRIS”) и его производные, аминокислоты и олигопептиды.
Получение водорастворимых соединений для фармацевтического применения посредством так называемого ПЭГилирования, то есть прямым или непрямым (через линкер) присоединением полиэтиленгликольных цепей (ПЭГ), известно в данной области техники. ПЭГ нетоксичен, он повышает растворимость в воде терапевтически активных молекул и изменяет биораспределение, что приводит к благоприятному фармакокинетическому профилю (Международная заявка № WO 01/66550, Bradley et al.).
Водорастворимые ПЭГилированные соединения для PDT описаны в Патенте США № 5622685 (Sinn et al.), где указанные соединения содержат, по меньшей мере, две фенольные гидроксильные и/или аминогруппы, по меньшей мере, одну алифатическую аминогруппу или, по меньшей мере, одну фенольную гидроксильную и/или аминогруппу и, по меньшей мере, одну алифатическую аминогруппу, и указанные группы замещены полиэтиленгликольными цепями, в которых степень полимеризации n находится в интервале от 5 до 250 и концевая гидроксильная группа замещена группой С1-С12 алкилового сложного или простого эфира, причем каждое соединение замещено, по меньшей мере, двумя такими полиэтиленгликольными цепями. В Патенте США № 5622685 описаны также соединения, содержащие ПЭГ-цепи, присоединенные через линкер, где полиэтиленгликольные цепи присоединены посредством не способных подвергаться биологическому гидролизу или слабо биологически гидролизуемых линкеров.
Ближайшим аналогом настоящего изобретения является способ, описанный в Патенте США № 6147207 (Sinn et al.), озаглавленном “Method for productiong chlorins and bacteriochlorins containing polyether”. Способ включает связывание простого полиэфира с порфирином и превращение порфирина, содержащего простой полиэфир, под действием восстановителя. В предпочтительном варианте осуществления указанного изобретения простой полиэфир представляет собой полиэтиленгликоль (ПЭГ). Основным недостатком способа является то, что очень ограниченное количество соединений может быть получено вследствие химических особенностей способа. Кроме того, заявка (как и другие заявки Sinn et al.) раскрывает бис-, трис- или тетра-ПЭГилированные соединения, но не моно-ПЭГилированные соединения. На практике можно получить лишь сложную смесь изомеров и олигомеров соединений, содержащих ПЭГ-остаток. Этот факт делает практически невозможным проведение достоверного количественного анализа и качественного контроля, которые обязательны при получении фармацевтических продуктов. Кроме того, в Патенте США № 6147207 описывается получение продуктов, в которых ПЭГ-цепи могли заканчиваться только ОН и ОМе группами, что ограничивает практическое применение полученных соединений.
Таким образом, существует потребность в получении новых водорастворимых моно-ПЭГилированных производных тетрапиррола для фотодинамической терапии, а также в простом и эффективном способе получения таких водорастворимых моно-ПЭГилированных соединений.
Цели и сущность изобретения
Целью данного изобретения является предоставление улучшенного фотосенсибилизатора для применения в фотодинамической терапии (PDT) рака, инфекций и других заболеваний.
Другой целью данного изобретения является предоставление водорастворимых производных тетрапиррола, которые могут использоваться в качестве фотосенсибилизаторов в PDT и стабильны в течение длительных периодов времени.
Еще одной целью данного изобретения является предоставление воспроизводимого и эффективного способа получения улучшенных водорастворимых производных тетрапиррола для применения в PDT.
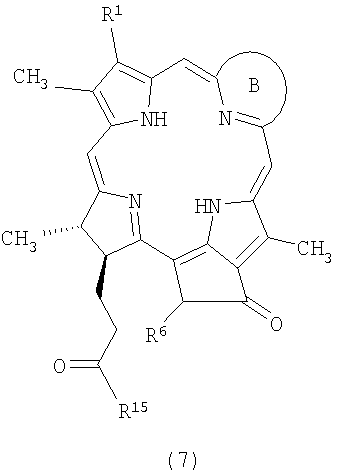
Формулируя кратко, данное изобретение предоставляет способ получения водорастворимых моно-ПЭГилированных производных тетрапиррола (1)-(3), включающий взаимодействия одного из соединений (7)-(10) с аминополиэтиленгликолем, содержащим функционализованный концевой фрагмент. Соединения (7)-(10) представлены ниже:
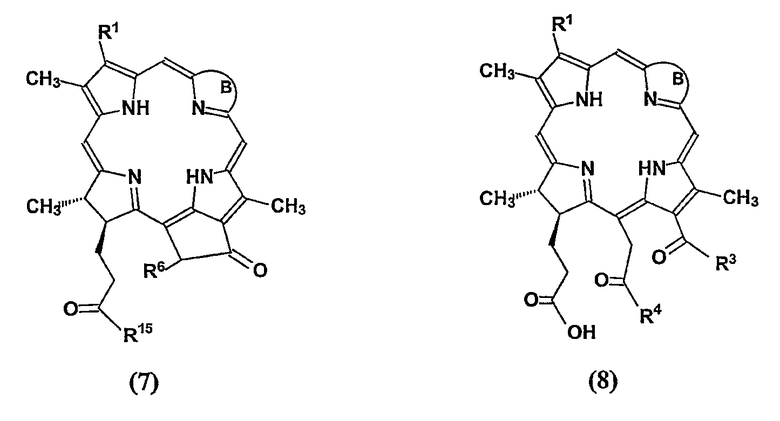
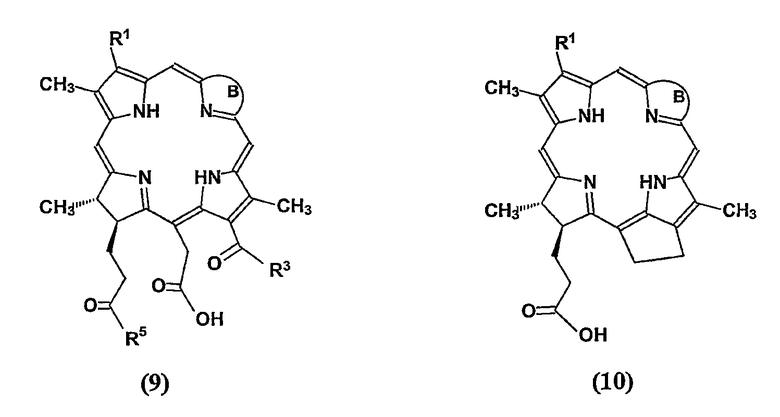
где В представляет собой цикл, имеющий структуру

где
R1 = -CH=CH2, -CH(OAlk)CH3, -CHO, -C(O)CH3, -CH2CH3, -CH(Alk)CH(COAlk)2, -CH2CH(COAlk)2, -CH(Alk)CH2COAlk, -CH(Alk)CH2CH(OH)CH3 и -CH2CH2CH(OH)CH3;
R2 = -CH3, -CHO, -CH(OH)Alk, -CH=CHAlk, CH2OH и CH2OAlk;
R3 = -OH, -OAlk, -NH-Alk;
R4 = -OH, -OAlk, -NH-Alk;
R5 = -OH, -OAlk, -NH-Alk;
R6 = H и -COOAlk;
R15 = -OH, -NH(СН2)m-R16;
R16 = -COOH, -NH2;
где:
m=2-12 и
Alk = алкильный заместитель.
Функционализованный концевой фрагмент (показанный как R10 (см. формулы (1)-(3))) предпочтительно выбран из группы, включающей:
R10 = -OH, -OAlk, -NH2, -NHAlk, -NHAcyl, -NAcyl2, -NR12R13, -COR14, -OCH2COR14, где
R12 = H и -Alk;
R13 =H и -Alk;
R14 = -OH, -OAlk, -NR12R13 и
Alk = алкильный заместитель. OAlk предпочтительно представляет собой ОМе. Молекулярная масса аминополиэтиленгликоля, содержащего функционализованный концевой фрагмент, составляет 500-30000.
Изобретение предоставляет также водорастворимое моно-ПЭГилированное производное тетрапиррола, выбранное из группы, включающей:
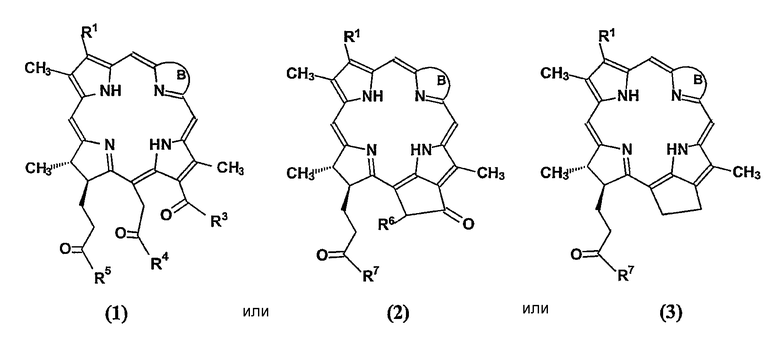
где В представляет собой цикл структуры:

где
R1 = -CH=CH2, -CH(OAlk)CH3, -CHO, -C(O)CH3, -CH2CH3, -CH(Alk)CH(COAlk)2, -CH2CH(COAlk)2, -CH(Alk)CH2COAlk, -CH(Alk)CH2CH(OH)CH3 и -CH2CH2CH(OH)CH3;
R2 = -CH3, -CHO, -CH(OH)Alk, -CH=CHAlk, CH2OH и CH2OAlk;
R3 = -OH, -OAlk, -NH-Alk, NR8-R9-R10, -NH(CH2)m-R11-R9-R10;
R4 = -OH, -OAlk, -NH-Alk, NR8-R9-R10, -NH(CH2)m-R11-R9-R10;
R5 = -OH, -OAlk, -NH-Alk, NR8-R9-R10, -NH(CH2)m-R11-R9-R10;
R6 = H и -COOAlk;
R7 = -NR8-R9-R10, -NH(CH2)m-R11-R9-R10;
R8 = H и -Alk;
R9 = -(CH2CH2O)nCH2CH2-;
R10 = -OH, -OAlk, -NH2, -NHAlk, -NHAcyl, -NAcyl2, -NR12R13, -COR14, -OCH2COR14;
R11 = -CH2CONR8-, -NHCOO-;
R12 = H и -Alk;
R13 = H и -Alk;
R14 = -OH, -OAlk, -NR12R13;
где:
m=2-12;
n=8-500 и
Alk = алкильный заместитель,
полученное способом, указанным выше.
Согласно дополнительному аспекту данного изобретения предоставлено применение указанных водорастворимых моно-ПЭГилированных производных тетрапиррола в качестве фотосенсибилизаторов в фотодинамической терапии.
Описанные выше и другие цели, отличительные признаки и преимущества настоящего изобретения станут понятными из приведенного далее описания.
Подробное описание предпочтительных вариантов осуществления настоящего изобретения
За исключением случаев, оговоренных особо, все технические и научные термины, используемые в описании, имеют значения, которые общеизвестны для специалистов области техники, к которой относится настоящее изобретение.
Тетрапирролы представляют собой макроциклические соединения с мостиками из одного атома углерода, соединяющими четыре пиррольных структурных элемента, или их модифицированные производные. Существует множество различных классов тетрапирролов, включая классы, содержащие дигидропиррольные структурные элементы. В настоящем описании термин «тетрапиррол» относится к феофорбидам, бактериофеофорбидам, хлоринам, бактериохлоринам и их производным, подходящим для фотодинамической терапии (PDT) и фармацевтическим препаратам.
Термин «ПЭГ», используемый в данном описании, относится к полиэтиленгликольной цепи. Моно-ПЭГилированное тетрапиррольное производное данного изобретения представляет собой соединение, содержащее полиэтиленгликольную цепь и полученное взаимодействием тетрапиррола с аминополиэтиленгликолем, содержащим функционализованный концевой фрагмент (functionalized terminal fragment - FTF) (11-13). Такой аминополиэтиленгликоль известен как ПЭГамин-производное.
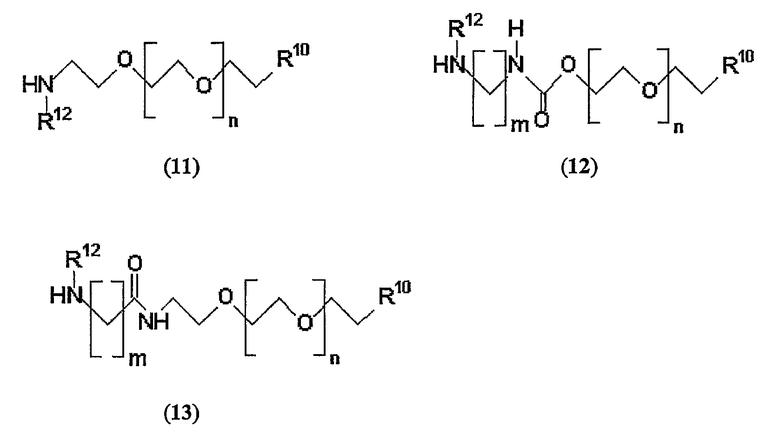
где
R10 = -OH, -OAlk, -NH2, -NHAlk, -NHAcyl, -NAcyl2, -NR12R13, -COR14, -OCH2COR14;
R12 = H и -Alk;
R13 = H и -Alk;
R14 = -OH, -OAlk, -NR12R13;
m=2-12;
n=8-500 и
Alk = алкильный заместитель.
Получение продуктов, которые представляют собой объект настоящего изобретения, осуществляется связыванием ПЭГ-амин-производных типа (11)-(13) с соответствующим исходным тетрапирролом. Для этой цели могут использоваться традиционные способы присоединения органических первичных и вторичных аминов к соединениям, содержащим свободную или активированную карбоксильную(ые) группу(ы), а также любые другие удобные способы образования амидной связи. В случаях когда исходный тетрапиррол представляет собой производное феофорбида, может использоваться также присоединение амина (11)-(13) посредством раскрытия циклопетанонового цикла, как показано в примерах 3 и 6.
Аминополиэтиленгликоль (11)-(13), используемый в настоящем изобретении, может содержать одну исходную ОН группу, присутствующую в исходных полиэтиленгликолях, или другие функционализованные концевые фрагменты (FTF, R10), расположенные на конце аминополиэтиленгликольной цепи. Предпочтительные FTF выбраны из группы, включающей OAlk, NH2, NAlk2, COOH, OCH2COOH, NHAcyl, NAcyl2 (включая фталимидо, малеидо и другие циклические имидогруппы). OAlk предпочтительно представляет собой ОМе.
В случаях когда R10 представляет собой группу, которая может быть реакционноспособной в условиях, используемых для осуществления связывания тетрапиррола с аминополиэтиленгликолем, выбираются подходящие селективно модифицированные аналоги соединения (11)-(13), которые могут содержать в R10 временные блокирующие группы для защиты тетрапиррольных структурных единиц от связывания вместе. В частности, при применении диаминов типа (11)-(13) (R10 = NH2) необходимо применять избыток диамина для предотвращения присоединения двух тетрапиррольных структурных единиц к диамину. Это неудобно ввиду трудности хроматографического разделения избытка диамина и целевого продукта его конъюгации с тетрапирролом. Следовательно, в случаях когда R10 содержит первичную или вторичную аминогруппы, применение временно N-замещенных производных с трет-бутилоксикарбонильной, бензилоксикарбонильной, трихлорацетильной и другими подходящими временными N-блокирующими группами является предпочтительным.
Аналогично, получение соединений данного изобретения из ПЭГ-амин-производных (11)-(13), содержащих карбоксильную группу в заместителе R10, могло бы осуществляться с применением производных (11)-(13), содержащих свободную карбоксильную группу, карбоксильную группу в солевой форме или временно защищенную карбоксильную группу в форме сложного алкилового эфира, такого как метиловый, этиловый, трет-бутиловый и другие группы, традиционно используемые для защиты функциональной карбоксильной группы.
Моно-ПЭГилированные соединения настоящего изобретения являются не только высокорастворимыми в воде, они также обладают хорошей растворимостью в традиционных органических растворителях. Это дает возможность осуществлять их качественную очистку колоночной хроматографией или хроматографией других типов и анализ ВЭЖХ и ТСХ. Предпочтительные органические растворители для хроматографии продуктов настоящего изобретения включают хлорированные углеводороды, простые эфиры, сложные эфиры, ацетонитрил, толуол, ацетон, спирты и их сочетания, традиционно используемые для очистки и анализа органических соединений и, особенно, фармацевтических продуктов.
Присутствие подходящего FTF, присоединенного к полиэтиленгликолевой цепи, позволяет осуществлять дополнительные химические модификации, включая легкое сопряжение через соответствующий FTF с метками, носителями, белками, молекулярными векторами и другими молекулами. В частности, в примере 6 описывается синтез водорастворимого моно-ПЭГилированного сложноэфирного соединения и его дальнейшее превращение в соответствующее кислотное производное омылением.
Настоящее изобретение предоставляет также способ применения водорастворимых моно-ПЭГилированных производных тетрапиррола, полученных согласно настоящему изобретению, в фотодинамической терапии (PDT) рака и других гиперпролиферативных заболеваний и инфекций. PDT осуществляется введением производных в фармацевтически приемлемый разбавитель для доставки в сайт специфической обработки. В одном примере осуществления настоящего изобретения, в частности для лечения рака кожи и других дерматологических заболеваний, разбавитель может быть в форме крема, геля или в некоторых случаях диспергируемого жидкого аэрозоля. После доставки производных в разбавителе к области обработки предоставляется достаточное время для того, чтобы позволить тетрапиррольным производным предпочтительно аккумулироваться в больной ткани. И, наконец, область обработки облучается светом достаточной мощности с конкретной длиной волны для активации тетрапиррольных производных с целью некроза клеток больной ткани. Определение токсичности в отсутствие освещения (описанное в примере 7) и фототоксичности (описанное в примере 8) показывает прекрасные свойства соединений настоящего изобретения для применения в PDT.
Настоящее изобретение дополнительно проиллюстрировано приведенными далее примерами, не ограничивающими данное изобретение. Приведенные примеры предназначены только для иллюстрации настоящего изобретения, а не для его ограничения. Все полученные соединения имеют точные МС-спектры (CI-МС) и являются однородно чистыми в соответствии с ВЭЖХ с обращенной фазой.
ПРИМЕР 1
Получение бактериофеофорбида а (14)
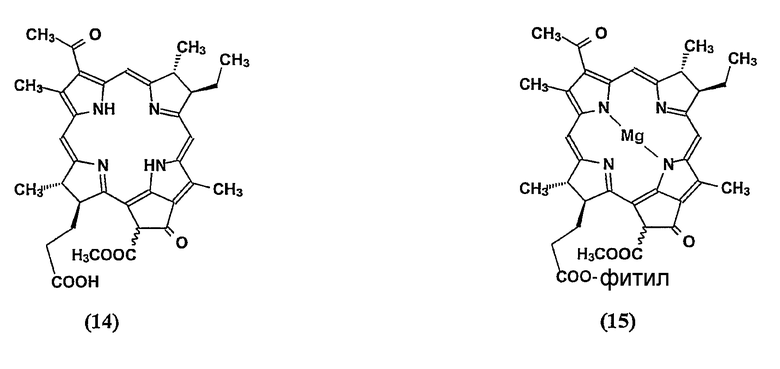
Раствор бактериохлорофилла a (15) (45 мг, 0,05 ммоль, продукт Sigma-Aldrich Corp.) в смеси трифторуксусной кислоты (1,2 мл) и воды (0,3 мл) выдерживают при комнатной температуре в течение 3 часов, концентрируют в вакууме (~20 мм Hg) при комнатной температуре, разбавляют водой и экстрагируют дихлорметаном. Экстракты промывают водой, сушат, концентрируют и очищают на силикагеле смесью 5% MeOH-CHCl3, получая 31 мг (98%) бактериофеофорбида a (14).
ПРИМЕР 2
Получение пиробактериофеофорбида a (16)
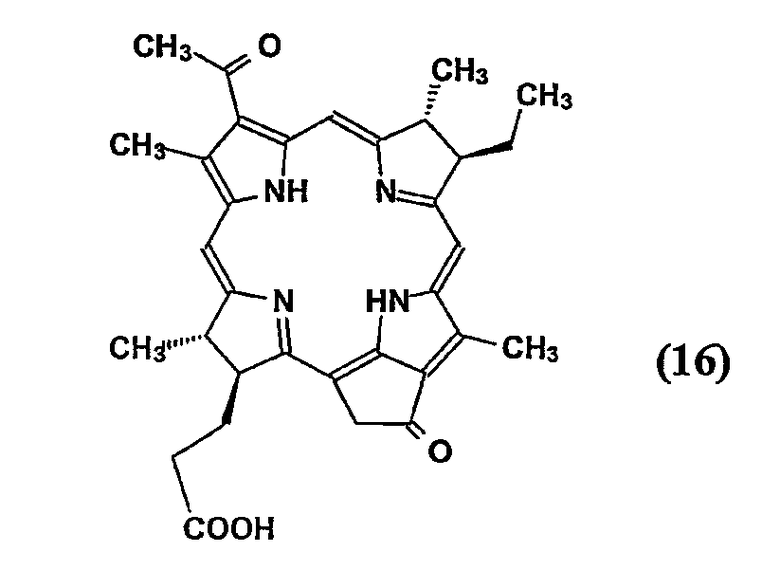
Смесь бактериофеофорбида a (14) (65 мг, 0,11 ммоль) и пиридина (4 мл) кипятят с обратным холодильником в течение 12 часов, охлаждают, упаривают досуха, разбавляют водой и экстрагируют дихлорметаном. Экстракты промывают 1 н. соляной кислотой, водой, сушат, концентрируют и очищают на силикагеле смесью 5%
MeOH-CHCl3, получая 59 мг (94%) пиробактериофеофорбида a (16).
ПРИМЕР 3
Получение водорастворимых моно-ПЭГилированных производных хлорина e 6 (17-18)
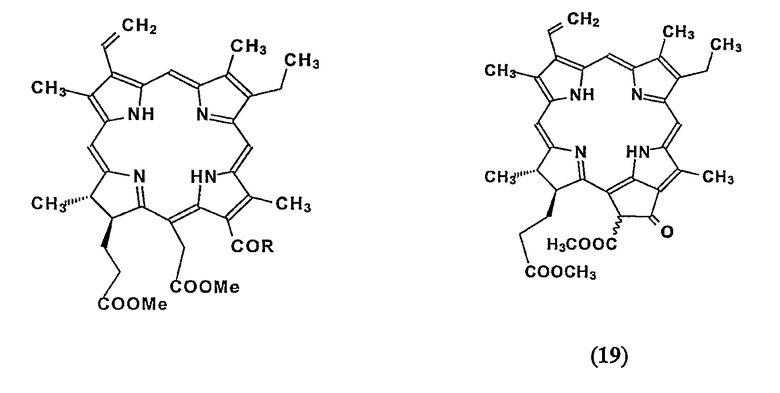
(17) R = NH-PEG750-OMe
(18) R = NH-PEG2000-OMe
Смесь метилфеофорбида a (19) (10 мг, 0,017 ммоль) и MeO-PEG750-NH2 или MeO-PEG2000-NH2 (0,068 ммоль, 4 экв.) (продукт RAPP Polymere GmbH) в тетрагидрофуране (0,5 мл) выдерживают при комнатной температуре в течение 3 дней, разбавляют дихлорметаном, промывают 0,5 н. водным раствором HCl, водой, сушат, концентрируют и очищают на силикагеле с использованием 5%MeOH-CHCl3. Полученный раствор (17) или (18) упаривают досуха, остаток снова растворяют в воде (2 мл), фильтруют через 45 мкм фильтр и сушат вымораживанием, получая 60-70% водорастворимого соединения (17) или (18) соответственно.
ПРИМЕР 4
Общая методика получения водорастворимых моно-ПЭГилированных производных мезопирофеофорбида a (20)-(25), феофорбида a (26) и (27), бактериофеофорбида (28) и пиробактериофеофорбида a (29).
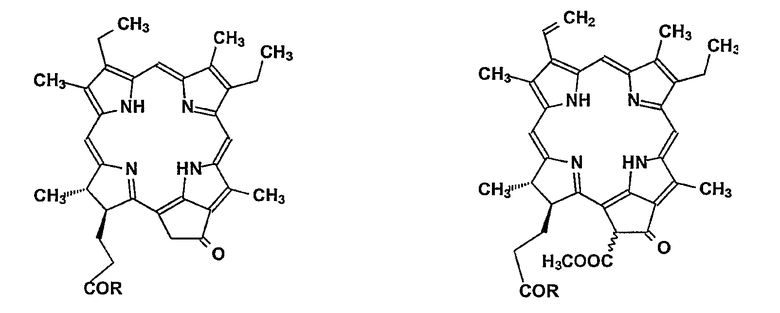
(21) R = NH-PEG2000-OMe
(22) R = NH-PEG5000-OMe
(23) R = NH-PEG10000-OMe
(24) R = NH-PEG20000-OMe
(25) R = NH-PEG3000-OCH2COOH
(30) R = OH
(31) R = пентафторфенокси
(27) R = NH-PEG2000-OMe
(32) R = пентафторфенокси
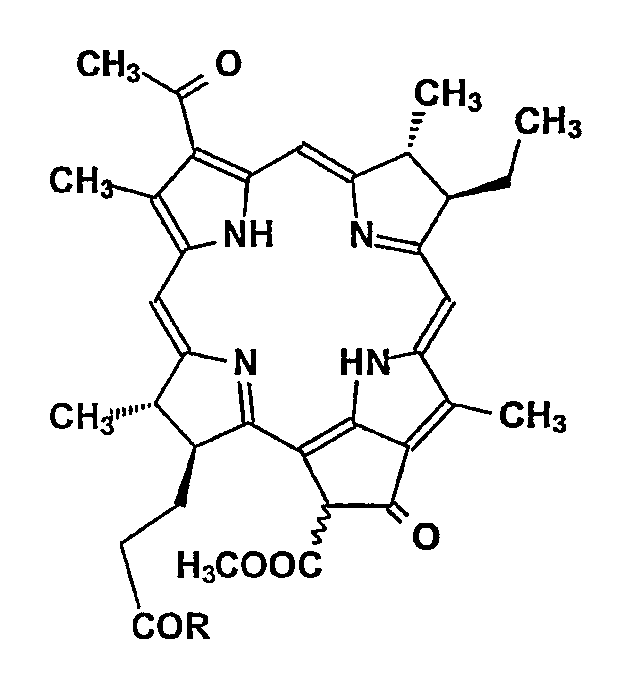
(33) R = пентафторфенокси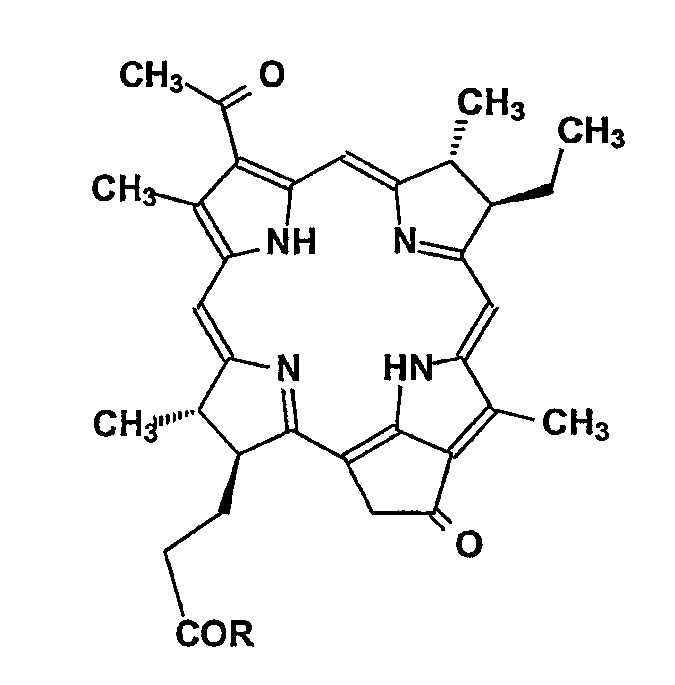
(34) R = пентафторфенокси
Мезопирофеофорбид a (30), феофорбид a (5), бактериофеофорбид a (14) или пиробактериофеофорбид (16) (0,03 ммоль) растворяют в дихлорметане (2 мл), затем добавляют 0,05 мл триэтиламинас последующим добавлением 0,01 мл (0,058 ммоль, 1,9 экв.) трифторацетата пентафторфенила. Смесь перемешивают при комнатной температуре в течение 10 минут для получения соединения (31), (32), (33) или (34) соответственно, разбавляют дихлорметаном, промывают водой, сушат и полученный раствор добавляют к раствору подходящего MeO-PEG-NH2 с ММ 750, 2000, 5000, 10000 или 20000 (продукты RAPP Polymere GmbH) или HOOCCH2O-PEG3000-NH2 (0,039 ммоль, 1,5 экв. (продукт GlycoSense AG)) в дихлорметане (1,0 мл). Смесь перемешивают в течение 0,5-10 часов при комнатной температуре, разбавляют дихлорметаном и затем промывают 0,5 н. водным раствором HCl. После этого смесь промывают водой, сушат, концентрируют и очищают на силикагеле с использованием смеси 5% MeOH-CHCl3. Полученный раствор соответствующего ПЭГ-амида упаривают досуха, снова растворяют в воде (2-5 мл), фильтруют через 45 мкм фильтр и сушат вымораживанием, получая чистое водорастворимое соединение (20)-(29) с общими выходами 70-99%.
ПРИМЕР 5
Получение водорастворимых моно-ПЭГилированных производных мезопирофеофорбида a (35), содержащих гептаметилендиаминовый спейсер между тетрапирролом и ПЭГ 2000 частями.
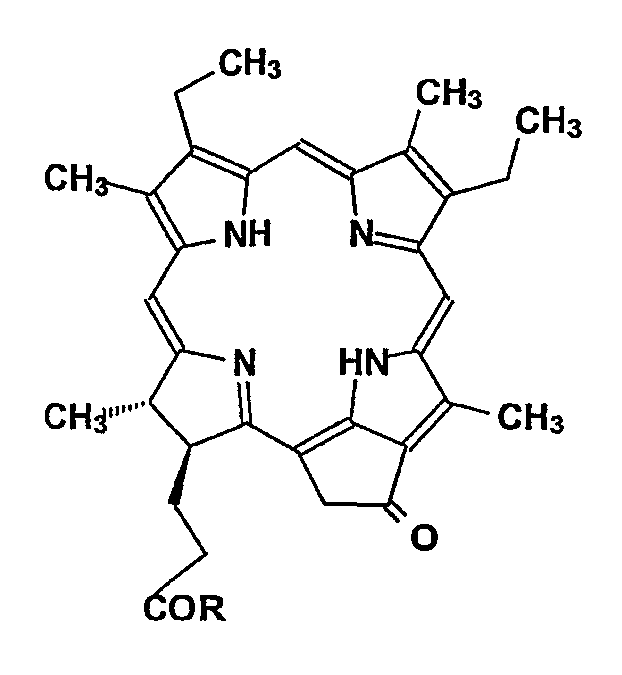
1,1'-карбонилдиимидазол (25 мг, 0,15 ммоль, 3 экв.) добавляют к раствору MeO-PEG2000-OH (100 мг, 0,05 ммоль (продукт RAPP Polymere GmbH)) в тетрагидрофуране (2,0 мл). Раствор выдерживают в течение 10 минут при комнатной температуре, после чего добавляют раствор 1,7-диаминогептана (33 мг, 0,25 ммоль, 5 экв.) в тетрагидрофуране (1,0 мл). Смесь выдерживают при комнатной температуре в течение 30 минут и продукт осаждают добавлением простого эфира. Полученный продукт растворяют в дихлорметане (2 мл) и полученный раствор добавляют к раствору (31) [полученному из 15 мг (0,026 ммоль) мезопирофеофорбида a (30) в соответствии с методикой примера 6] в дихлорметане (2 мл). Смесь выдерживают при комнатной температуре в течение 30 минут, разбавляют дихлорметаном и промывают 0,5 н. водным раствором HCl. После этого смесь промывают водой, сушат, концентрируют и очищают на силикагеле с использованием смеси
5% MeOH-CHCl3. Полученный раствор (35) упаривают досуха, снова растворяют в воде (2,0 мл), фильтруют через 45 мкм фильтр и сушат вымораживанием, получая 60 мг (85%) водорастворимого соединения (35).
ПРИМЕР 6
Получение водорастворимых моно-ПЭГилированных производных хлорина e 6 (36) и (37)
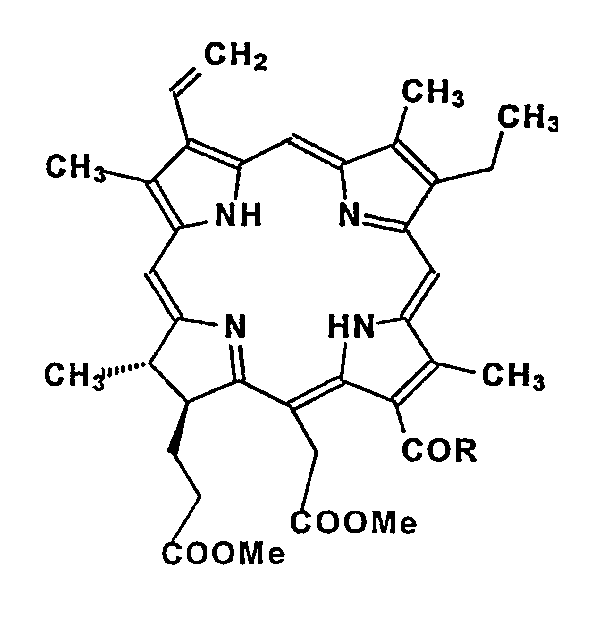
(37) R = NH-PEG3000-OCH2COOH
Смесь метилфеофорбида a (20) (10 мг, 0,017 ммоль) и MeOOCCH2O-PEG3000-NH2 (215 мг, 0,068 ммоль, 4 экв.) (продукт GlycoSense AG) в тетрагидрофуране (0,5 мл) выдерживают при комнатной температуре в течение 3 дней, разбавляют дихлорметаном, промывают 0,5 н. водным раствором HCl, затем водой, сушат, концентрируют и очищают на силикагеле с использованием смеси
5% MeOH-CHCl3. Полученный раствор (36) упаривают досуха, растворяют в диоксане (2 мл), добавляют 6 н. водный раствор гидроксида натрия (0,01 мл) и реакционную смесь кипятят с обратным холодильником в течение 10 минут. После этого смесь охлаждают, разбавляют дихлорметаном, промывают 0,5 н. водным раствором HCl, затем водой, сушат, концентрируют досуха, снова растворяют в воде (2 мл) и затем фильтруют через 45 мкм фильтр и сушат вымораживанием, получая 42 мг (70%) водорастворимого соединения (37).
ПРИМЕР 7
Определение токсичности (цитотоксичности) водорастворимого моно-ПЭГилированного феофорбида a (35) и водорастворимой соли феофорбида a (5) N-метил-D-глюкамином в клетках HeLa при отсутствии освещения
Для определения токсичности в условиях отсутствия освещения водорастворимого производного (35) и водорастворимой соли феофорбида a (5) с N-метил-D-глюкамином (полученной в соответствии с методикой, описанной в заявке на Патент США № 10/151764) в клетках HeLa (клетки цервикальной карциномы человека) монослойные клеточные культуры инкубируют в 96-луночных микропланшетах (плотность высева: 7000 клеток на лунку в модифицированной по Дульбеко основной среде (DMEM) c 10% фетальной телячьей сывороткой) при повышающихся концентрациях фотосенсибилизатора в интервале от 2 до 500 мкг/мл и инкубируют в течение 48 часов.
Клетки промывают чистой DMEM и обрабатывают 10% формалином в течение 15 минут при комнатной температуре. Клетки дважды промывают водой, инкубируют в течение 15 минут с 0,1% раствором кристаллического фиолетового (50 мкл/лунка), затем промывают водой и обрабатывают этанолом (100 мкл/лунка). Оптические плотности полученных этанольных растворов определяют с помощью спектрофотометра Specord 100 (Analytik Jena AG, Германия) spectrophotometer при 594 нм для контроля выживания клеток.
Значения выражают в виде процентов от неинкубированного контроля. Для каждой инкубационной концентрации проводят восемь опытов. Данные экспериментов, представленные в таблице 1, показывают значения IC50 и IC80.
ПРИМЕР 8
Определения фототоксичности водорастворимого моно-ПЭГилированного производного феофорбида a (35) и водорастворимой соли феофорбида a (5) с N-метил-D-глюкамином в клетках HeLa при облучении светом с длиной волны 662 нм
Для определении фототоксичности водорастворимое производное (35) или водорастворимую соль феофорбида a (5) с N-метил-D-глюкамином (полученную в соответствии с методикой заявки на Патент США № 10/151764) и монослойную культуру клеток HeLa (клетки цервикальной карциномы человека) инкубируют в 96-луночных микропланшетах (плотность высева: 30000 клеток на лунку в DMEM с 10% фетальной телячьей сыворотки) с возрастающими концентрациями фотосенсибилизатора в интервале от 0,01 до 40 мкг/мл. Освещение осуществляют при 662 нм (Ceralas PDT laser, BioLitec AG, Germany; 150 мВ/см2, 5-20 Дж/см2) после инкубирования в течение 30 минут. Количество выживших клеток определяют с использованием MTT-опыта. Значения выражают в виде процентов от освещенного, но неинкубированного контроля. Эксперименты проводят восьмикратно. Данные экспериментов, представленные в таблице 2, показывают значения IC50 и IC90, наблюдаемые после облучения 10 Дж/см2.
(Пример 8)
Располагая описаниями предпочтительных вариантов осуществления данного изобретения, следует представлять, что изобретение не ограничивается указанными вариантами осуществления и что квалифицированными специалистами в данной области техники могут осуществляться различные изменения и модификации без выделения их из области или существа настоящего изобретения, которые определены в прилагаемой формуле изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ХЛОРИНОВ | 1998 |
|
RU2144538C1 |
| ФОТОСЕНСИБИЛИЗАТОРЫ НА ОСНОВЕ (БАКТЕРИО)ХЛОРОФИЛЛА ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ ЗАБОЛЕВАНИЙ И РАССТРОЙСТВ | 2012 |
|
RU2632439C2 |
| ВОДОРАСТВОРИМЫЕ АНИОНСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ БАКТЕРИОХЛОРОФИЛЛА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2353624C2 |
| КАТИОННЫЕ ПРОИЗВОДНЫЕ БАКТЕРИОХЛОРОФИЛЛА И ИХ ПРИМЕНЕНИЕ | 2005 |
|
RU2397172C2 |
| СПОСОБ ТРАНСЭТЕРИФИКАЦИИ ДЛЯ ПОЛУЧЕНИЯ СИНТЕТИЧЕСКОГО ПРОИЗВОДНОГО ХЛОРОФИЛЛА ИЛИ БАКТЕРИОХЛОРОФИЛЛА | 2000 |
|
RU2250905C2 |
| ВОДОРАСТВОРИМЫЕ АНАЛОГИ СС-1065 И ИХ КОНЪЮГАТЫ | 2007 |
|
RU2489423C2 |
| НОВЫЕ АНАЛОГИ СС-1065 И ИХ КОНЪЮГАТЫ | 2009 |
|
RU2562232C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИНА e6 | 2006 |
|
RU2330037C1 |
| НОВЫЕ АНАЛОГИ СС-1065 И ИХ КОНЪЮГАТЫ | 2009 |
|
RU2628069C2 |
| 9А-АЗАЛИДНЫЕ ФРАГМЕНТЫ МАКРОЛИДНЫХ АНТИБИОТИКОВ КЛАССА АЗАЛИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2130936C1 |
Описываются новые водорастворимые моно-ПЭГилированные производные тетрапиррола формул (1А) или (2) (значения радикалов Y,B,R1,R4-R6 приведены в формуле изобретения),
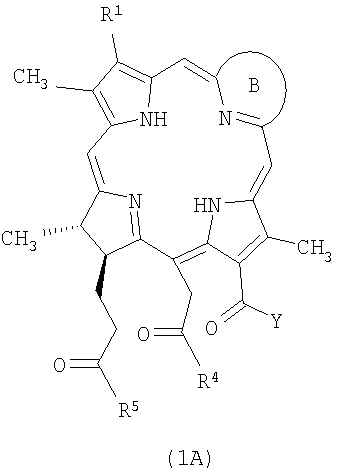
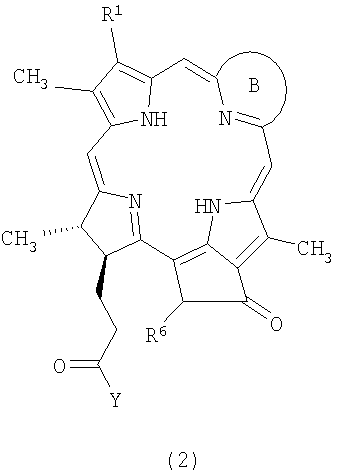
фармацевтическая композиция, их содержащая, способ получения соединения (2), включающий взаимодействие соответствующего тетрапиррола общей формулы (7) с аминополиэтиленгликолем формулы Н-Y, содержащим функционализованный концевой фрагмент, и применение новых соединений в качестве фотосенсибилизаторов при фотодинамической терапии. 4 н. и 1 з.п. ф-лы, 2 табл.
1. Водорастворимое моно-ПЭГилированное производное тетрапиррола, выбранное из группы, включающей соединения формулы 1А и 2:

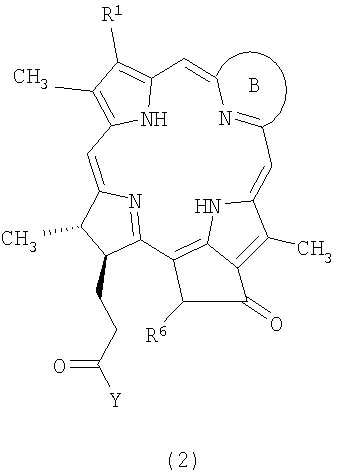
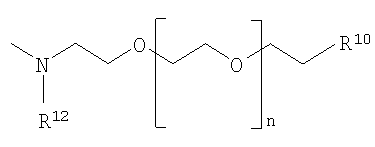
где Y представляет собой остаток функционализованного аминополиэтиленгликоля H-Y, где Y выбран из группы, включающей структуры
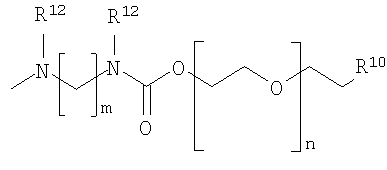
где В представляет собой цикл, имеющий структуру
или 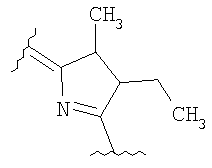
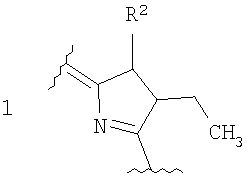
где R1=-СН=СН2, -С(O)СН3, -СН2СН3;
R2=-СН3;
R4=-OMe;
R5 -ОМе;
R6=Н или -СООМе;
R10= -ОМе или -OCH2COR14;
R12=H;
R14= -OH или -ОМе,
где m=2-12;
n=8-500.
2. Способ получения водорастворимого моно-ПЭГилированного производного тетрапиррола общей формулы 2 по п.1, заключающийся в том, что тетрапиррол общей формулы 7:
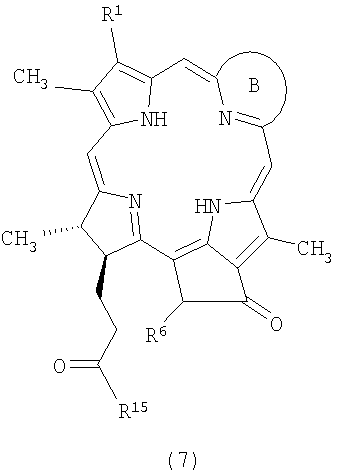
где В представляет собой цикл, имеющий структуру
или 
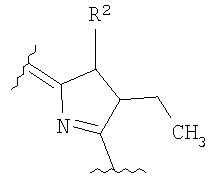
где R1=-СН-СН2, -С(O)СН3, -СН2СН3;
R2=-СН3;
R4= -ОМе;
R5= -ОМе;
R6=Н и -СООМе;
R15= -OH
подвергают взаимодействию с аминополиэтиленгликолем общей формулы H-Y, где Y выбран из группы, включающей


где R10= -OMe или -OCH2COR14;
R12=H;
R14= -OH или -ОМе;
m=2-12;
n=8-500.
3. Способ по п.2, где молекулярная масса указанного аминополиэтиленгликоля H-Y находится в интервале от 500 до 30000.
4. Применение водорастворимого моно-ПЭГилированного производного тетрапиррола по п.1 в фотодинамической терапии, включающей стадии:
введение указанного моно-ПЭГаминотетрапиррола в фармацевтически приемлемый разбавитель для получения препарата для доставки в больные ткани на специфическом сайте обработки;
доставку указанного препарата моно-ПЭГаминотетрапиррол-разбавитель к указанному специфическому сайту обработки;
предоставление возможности указанному препарату моно-ПЭГаминотетрапиррол-разбавитель предпочтительно аккумулироваться в указанных больных тканях;
облучение указанного сайта обработки светом достаточной мощности и длины волны для активации указанного моно-ПЭГаминотетрапиррола.
5. Фармацевтическая композиция, обладающая свойствами фотосенсибилизатора, содержащая указанный моно-ПЭГилированный тетрапиррол по п.1 в виде водного раствора.
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ХЛОРИНОВ | 1998 |
|
RU2144538C1 |
| US 5002962 A, 26.03.1991 | |||
| US 5378835 A, 03.01.1995 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2010-02-27—Публикация
2004-03-19—Подача