Изобретение относится к синтетическим, химическим биологически активным веществам из ряда гетероциклических соединений формулы 1-2
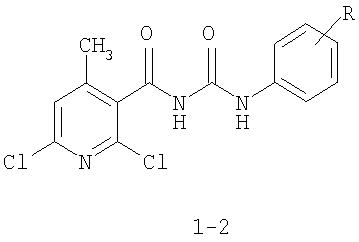
1 R=4-ОСН3;
2 R=2-СООСН3
защищающим растения подсолнечника от фитотоксического действия гербицида 2,4-дихлорорфеноксиуксусной кислоты (антидотам).
Соединение 1 известно (Каталог Chemical Library Suhhlier: Chemical Block Ltd, Registry Number 893778-02-4, 17.07.2006), однако его антидотные свойства выявлены впервые. Соединение 2 является новым.
Как известно, подсолнечник является чрезвычайно чувствительной культурой к гербицидам группы 2,4-Д, и, в случаях непреднамеренного попадания гербицида на его посевы, потери могут составлять, в зависимости от дозы, до 100% [Д.И.Чкаников, М.С.Соколов. Гербицидное действие 2,4-Д и других галоидфеноксикислот, М.: Наука, 1973].
До сих пор защита вегетирующих растений подсолнечника от повреждающего действия 2,4-Д остается актуальной и нерешенной.
К наиболее близким аналогам по структуре заявляемых соединений может быть отнесен N-(4-фторфенил)-N'-(4-метил-2,6-дихлорникотиноил)мочевина 3 [Л.В.Дядюченко, И.Г.Дмитриева, С.Н.Михайличенко, В.Н.Заплишный. Синтез, свойства и особенности фрагментации под электронным ударом N-замещенных никотиноилмочевин./ ХГС / 2005, №5, с.705-712].

В качестве аналога по свойствам известен Сульфален [«Антидот гербицидов гормонального действия 2,4-дихлорфеноксиуксусной кислоты и 4-амино-3,5,6-трихлорпи-колиновой кислот» [пат. РФ №2043021 от 10.09.95, заявка №5042089 от 14.05.92] 4:
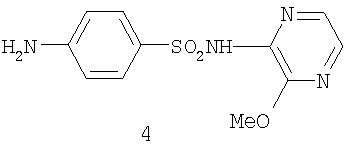
Сульфален формулы 4 используется в качестве средства снижения негативного действия гербицида 2,4-Д, он в дозе 200 г/га применяется по поврежденным вегетирующим растениям. В то же время Сульфален широко применяется в качестве антибактериального средства в медицинской практике, его синтез описан в литературе [В.Г.Беликов. Фармацевтическая химия. - М.: Высшая школа, 1985, с.383, 768]. Однако антидотная активность Сульфалена является недостаточно высокой.
Задачей настоящего изобретения является расширение арсенала биологически активных веществ, полученных синтетическим путем, для применения их в сельском хозяйстве в качестве антидотов.
Это достигается применением N-замещенных 4-метил-2,6-дихлорникотиноилмочевин 1-2 на вегетирующих растениях подсолнечника.
Заявляемые соединения получали известным методом - взаимодействием 4-метил-2,6-дихлорникотиноилизоцианата с ароматическими аминами в растворе безводного бензола при комнатной температуре [Л.В.Дядюченко, И.Г.Дмитриева, С.Н.Михайличенко, В.Н.Заплишный. Синтез, свойства и особенности фрагментации под электронным ударом N-замещенных никотиноилмочевин./ ХГС / 2005, №5, c.705-712].
Исходный 4-метил-2,6-дихлорникотиноилизоцианат синтезирован реакцией 4-метил-2,6-дихлорникотинамида с оксалилхлоридом в среде безводного диоксана [Л.В.Дядюченко, И.Г.Дмитриева, С.Н.Михайличенко, В.Н.Заплишный. Синтез и свойства некоторых новых никотиноилизоцианатов и их фрагментация под электронным ударом. /Л ХГС/ 2005, №4, с.549-553].
Использованные растворители бензол и диоксан абсолютировали известным способом [А.Вайсбергер, Э.Проскауэр, Дж.Риддик, Э.Тупс. Органические растворители. М.: Иностр. литература. 1958. С.518].
Изобретение иллюстрируется следующими примерами.
Пример 1. N-(4-метоксифенил)-N'-(4-диметил-2,6-дихлорникотиноил)-мочевина (соединение 1).
К раствору 1,46 г (6,3 ммоль) 4-метил-2,6-дихлорникотиноилизоцианата в 20 мл абсолютного бензола прибавляют раствор 0,85 г (6,9 ммоль) п-низидина в 10 мл абсолютного бензола и перемешивают при комнатной температуре в течение 5 ч. Выделившийся осадок отфильтровывают, промывают бензолом, сушат. После перекристаллизации из смеси этанол : ДМФА=4:1 получают 1,75 г (78%) целевого продукта 1 в виде кристаллов с т.пл. 220-222°С.
Найдено, %: С 50,64; Н 3,52; N 11,98; С15H13Сl2N3О3;
Вычислено, %: С 50,86; Н 3,71; N 11,87.
Спектр ЯМР 1Н, δ, м.д. (группа): 2,35 (с, 3Н, 4-СН3 Ру); 3,75 (с, 3Н, ОСН3); 6,88…7,50 (м, 4Н, Аr); 7,65 (с, 1Н, 5-Н Ру); 10, 16 и 11,40 (уш. с, 1H, NH).
Пример 2. N-(2-метоксикарбонилфенил)-N'-(4-диметил-2,6-дихлорникотиноил)мочевина (соединение 2).
К раствору 1,46 г (6,3 ммоль) 4-метил-2,6-дихлорникотиноилизоцианата в 20 мл абсолютного бензола прибавляют раствор 1,05 г (6,9 ммоль) метил-2-аминобензоата в 10 мл абсолютного бензола и перемешивают при комнатной температуре в течение 7 ч. Выделившийся осадок отфильтровывают, промывают бензолом, сушат. После перекристаллизации из смеси этанол : ДМФА=3:1 получают 1,93 г (80%) целевого продукта 2 в виде кристаллов с т.пл. 258-260°С.
Найдено, %: С 50,42; Н 3,19; N 11,28; С16Н13Сl2N3O4;
Вычислено, %: С 50,27; Н 3,44; N 11,00.
Спектр ЯМР 1H δ, м.д. (группа): 2,35 (с, 3Н, 4-СН3 Ру); 3,90 (с, 3Н, СООСН3); 7,22…8,46 (м, 4Н, Аr); 7,64 (с, 1Н, 5-Н Ру); 11,46 и 11,98 (уш. с, 1Н, NH).
Пример 3. N-(4-фтopфeнил)-N'-(4-мeтил-2,6-диxлopникoтинoил)мoчeвинa 3.
К раствору 1,13 г (4,9 ммоль) 4-метил-2,6-дихлорникотиноилизоцианата в 20 мл абсолютного бензола прибавляют раствор 0,50 г (5,0 ммоль) 4-фторанилина перемешивают при комнатной температуре в течение 2 ч. Выделившийся осадок отфильтровывают, промывают бензолом, сушат. Маточный раствор упаривают досуха, остаток объединяют с основным осадком, после перекристаллизации из этанола получают 1,25 г (75%) целевого продукта 3 в виде белых кристаллов с т.пл. 223-224°С.
Найдено, %: С 49,34; Н 2,64; N 12,39; С14Н10Сl2FN3O2;
Вычислено, %: С 49,12; Н 2, 81; N 12,28.
Спектр ЯМР 1Н, 5, м.д. (группа): 2,39 (с, 3Н, 4-СН3 Ру); 7,10…7,28 (м, 4Н, Аr); 7,53 (с, 1Н, 5-Н Ру); 9,92 и 10,16 (уш. с, 1Н, NH).
Пример 4. Оценка соединений 1-4 на антидотную активность на растениях подсолнечника в условиях полевого опыта.
Оценку антидотной активности соединений 1-4 осуществляли на экспериментальном поле ВНИИБЗР. Испытания проводили по следующей методике.
В полевых условиях растения подсолнечника сорта ВНИИМК 8883 в фазу 10-16 листьев обрабатывали бутиловым эфиром 2,4-дихлорфеноксиуксусной кислоты в дозе 18 г/га и через 5 суток наносили раствор антидота в дозе 200 г/га с нормой расхода рабочей жидкости 500 л/га.
В опыте предусмотрены следующие варианты:
- контроль - необработанные растения;
- «гербицид» (эталон) - растения, обработанные гербицидом;
- «гербицид+антидот» - растения, обработанные гербицидом и антидотом.
Опыты проводили на делянках площадью 2,8 м2, повторность пятикратная. Уборку урожая подсолнечника проводили в момент полного созревания семян.
Антидотный эффект определяли по абсолютной величине прибавки урожая к гербицидному эталону и в процентах по формуле
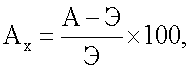
Ax - антидотный эффект, %;
А - урожай в варианте антидот+гербицид;
Э - урожай в варианте эталон (гербицид).
Полученные данные статистически обработаны с использованием t-критерия Стьюдента.
Результаты испытаний представлены в таблице.
Различия между вариантами достоверны при Р=0.90.
Таким образом, применение заявляемых N-замещенные 4-метил-2,6-дихлорникотиноилмочевин 1-2 в качестве антидотов позволяет обеспечить антидотный эффект на уровне 28-33% против 21% у прототипа, а также расширить ассортимент известных антидотов. Структурный аналог 3 проявляет слабую антидотную активность.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-ЗАМЕЩЕННЫЕ НИКОТИНОИЛМОЧЕВИНЫ, ПРОЯВЛЯЮЩИЕ РОСТРЕГУЛИРУЮЩУЮ АКТИВНОСТЬ НА ПРОРОСТКАХ ПОДСОЛНЕЧНИКА | 2010 |
|
RU2432742C1 |
| 4,6-ДИМЕТИЛ-2-ХЛОР-3-(5-Х-1,2,4-ОКСАДИАЗОЛИЛ-3)-ПИРИДИНЫ В КАЧЕСТВЕ АНТИДОТОВ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ | 2008 |
|
RU2356900C1 |
| N-ЭТИЛ-(3`-ЦИАНО-4`-МЕТИЛ-6-ХЛОРПИРИДИЛ-2`)ЭТОКСИГИДРАЗОН В КАЧЕСТВЕ АНТИДОТА | 2005 |
|
RU2276664C1 |
| О-(4-трет-бутилфенил)карбонил-4,6-диметил-2-хлорпиридил-3-амидоксим в качестве антидота 2,4-Д на подсолнечнике | 2018 |
|
RU2672881C1 |
| N-АЦИЛИРОВАННЫЕ 3-АМИНО-4,6-ДИМЕТИЛТИЕНО[2,3-b]ПИРИДИН-2-КАРБОКСАМИДЫ В КАЧЕСТВЕ АНТИДОТОВ 2,4-Д НА ПОДСОЛНЕЧНИКЕ | 2011 |
|
RU2475490C1 |
| 3-[(3,5-ДИНИТРОФЕНИЛ)КАРБОКСАМИДО]-1,4,6-ТРИМЕТИЛ-5-ХЛОРПИРАЗОЛО[3,4-b]ПИРИДИН В КАЧЕСТВЕ АНТИДОТА 2,4-Д НА ПОДСОЛНЕЧНИКЕ | 2008 |
|
RU2358973C1 |
| СПОСОБ ЗАЩИТЫ ВЕГЕТИРУЮЩИХ РАСТЕНИЙ ПОДСОЛНЕЧНИКА ОТ ПОВРЕЖДАЮЩЕГО ДЕЙСТВИЯ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ | 2014 |
|
RU2567515C1 |
| 7',9'-ДИМЕТИЛ-3'-АРИЛ-1'-СПИРО[ИНДЕН-2,2'-ПИРИДО[3',2':4,5]ТИЕНО]3,2-D]ПИРИМИДИН]-1,3,4'(3'H)ТРИОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИДОТОВ 2,4-Д НА ПОДСОЛНЕЧНИКЕ | 2020 |
|
RU2754220C1 |
| АНТИДОТ ГЕРБИЦИДА 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ НА ПОДСОЛНЕЧНИКЕ | 2014 |
|
RU2557550C1 |
| ПРИМЕНЕНИЕ 3[(ЗАМЕЩЕННЫЙ ФЕНИЛ) КАРБОКСАМИДО]-1,4,6-ТРИМЕТИЛ-5-R ПИРАЗОЛО [4,5-b]ПИРИДИНОВ В КАЧЕСТВЕ АНТИДОТОВ 2,4-Д | 2005 |
|
RU2287275C1 |
Изобретение относится к химическим биологически активным веществам. В качестве веществ, снижающих отрицательное воздействие гербицида 2,4-дихлорфеноксиуксусной кислоты на растения подсолнечника, предложены N-замещенные 4-метил-2,6-дихлорникотиноилмочевины формулы 1-2. Задачей настоящего изобретения является расширение ряда биологически активных веществ, полученных синтетическим путем, для их применения в сельском хозяйстве в качестве антидотов 2,4-Д. Это достигается применением N-замещенных 4-метил-2,6-дихлорникотиноилмочевин путем обработки поврежденных растений подсолнечника через 5 суток после нанесения гербицида. 1 табл.

Антидоты гербицида 2,4-дихлорфеноксиуксусной кислоты на подсолнечнике, представляющие собой N-замещенные 4-метил-2,6-дихлорникотиноилмочевины формулы 1-2:

1 R - 4-ОСН3;
2 R - 2-СООСН3,
в дозе 200 г/га.
| Каталог Chemical Library Supplier: Chemical Block Ltd, Registry Number 893778-02-4, 17.07.2006 | |||
| Дядюченко Л.В | |||
| и др | |||
| Синтез, свойства и особенности фрагментации под электронным ударом N-замещенных никотиноилмочевин | |||
| Химия гетероциклических соединений, 2005, №5, с.705-712 | |||
| 2-ТИОАЛКИЛПИРИДИНЫ И ТИЕНО[2,3-B]ПИРИДИНЫ-АНТИДОТЫ ГЕРБИЦИДА ГОРМОНАЛЬНОГО ДЕЙСТВИЯ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ | 2003 |
|
RU2232762C1 |
| US 4405552, 20.09.1983. | |||
Авторы
Даты
2010-03-20—Публикация
2008-02-11—Подача