Область техники
Данное изобретение относится к гелеобразованию пектина в растворимых твердых веществах (РТВ) в концентрации менее 30%. Пектин обладает свойствами, которые позволяют образовывать застывающие среды с низкой концентрацией ионов кальция и низкой концентрацией растворимых твердых веществ (% РТВ).
Уровень техники
Патент US 5929051 Ni et al. описывает пектин как компонент стенки растительной клетки. Клеточная стенка состоит из трех слоев: срединного слоя, первичной и вторичной клеточной стенки. Срединный слой более всего обогащен пектином. Пектины продуцируются и накапливаются в течение роста клеточной стенки. Особенно много пектина находится в мягких растительных тканях в условиях быстрого роста и высокого содержания влаги. В клеточных стенках пектин присутствует в виде комплекса с кальцием. Наличие перекрестного связывания с кальцием подтверждено фактом, что хелатообразующие агенты облегчают высвобождение пектина из клеточных стенок, как раскрыто Nanji (US 1634879) и Maclay (US 2375376).
Пектин является сложным полисахаридом, связанным с растительной клеточной стенкой. Он состоит из остова альфа 1,4-связанной полигалактуроновой кислоты, в который включены остатки рамнозы и который модифицирован боковыми цепями нейтральных сахаров и несахарными компонентами, такими, как ацетил, метил, и группами феруловой кислоты.
Боковые цепи нейтральных сахаров, которые включают арабинан и арабиногалактаны, присоединены к остаткам рамнозы в составе остова. Остатки рамнозы имеют тенденцию образовывать кластеры внутри остова. Таким образом, вместе с присоединенными боковыми цепями данный участок является ворсистым и остальная часть остова называется, следовательно, гладким участком.
Традиционно пектин используют в качестве пищевых добавок. Однако его применение распространилось также и на фармацевтические области. Пектин уже давно используют как противодиарейный препарат, и он может улучшать работу кишечного тракта. Считается, что противодиарейное действие частично обусловлено противомикробной активностью пектина.
Пектин также является эффективным против желудочно-кишечных язв и энтероколита. Пектин также влияет на пролиферацию клеток в кишечнике. Он также обладает эффектом снижения уровня холестерина в крови и проявляет ингибирование атеросклероза. Такой эффект является результатом взаимодействия пектина с солями желчных кислот.Также было показано, что пектин воздействует на фибриновую сеть у пациентов с гиперхолестеринемией.
Способность взаимодействовать с различными ионами двухвалентных металлов делает пектин сильным детоксифицирующим агентом.
Устойчивость пектина к разложению в верхнем отделе желудочно-кишечного тракта и его полное разложение в толстой кишке делают пектин очень удобным средством доставки непосредственно в толстую кишку. Коацервация с желатином делает возможным образование микроглобул, пригодных для получения продуктов контролируемого высвобождения. Более того, пектин используется при получении таблеток.
Согласно Dumitriu, S.: Polysaccharides, Structural diversity and functional versatility, Marcel Dekker, Inc., New York, 1998, 416-419 пектин применяется в ряде продуктов питания.
Исторически сложилось, что пектин использовался главным образом в качестве гелеобразующего агента для джема или похожих фруктосодержащих продуктов или продуктов с фруктовым ароматом, обогащенных сахаром. Примерами являются традиционные джемы, джемы со сниженным содержанием сахара, прозрачные желе, кондитерские желе с фруктовым ароматом, кондитерские желе без фруктового аромата, термообратимая глазурь для хлебопечения, термоустойчивые джемы для хлебопечения, фруктовые добавки для мороженого и фруктовые заправки для йогурта.
На сегодняшний день основная часть пектина используется для стабилизации молочных напитков с низким значением рН, включая ферментированные напитки и смеси фруктового сока и молока.
В последнее время было обнаружено, что пектин является эффективным при лечении изжоги, вызванной попаданием кислоты в пищевод.
Остатки галактуроновой кислоты в пектине частично этерифицированы и находятся в виде метилового эфира. Степень этерификации определяют как процентное содержание этерифицированных карбоксильных групп. Пектин со степенью этерификации («СЭ») более 50% называется высокометилированным («ВМ») пектином или высокоэтерифицированным пектином, и пектин со СЭ ниже 50% называется низкометилированным («НМ») пектином или низкоэтерифицированным пектином. Большинство пектинов в фруктах и овощах являются ВМ пектинами. Ацетатные сложноэфирные группы могут дополнительно присутствовать у атомов углерода в положениях 2 или 3 остатков галактуроновой кислоты. Степень ацетилирования («САц») определяют как процентное содержание остатков галактуроновой кислоты, содержащих ацетатную сложноэфирную группу. Большинство природных пектинов имеет низкую САц, за исключением пектина сахарной свеклы. Подобным образом степень амидирования (СА) определяют как процентное содержание остатков галактуроновой кислоты, содержащих амидную группу, и количество свободных кислот вычисляется как 100-(СЭ+СА).
В WO2004005352 Christensen раскрывается пектин, который деэтерифицируют сначала биокатализатором, а затем химическими реагентами. Подобные пектины отличаются более высокой молекулярной массой, чем традиционные низкоэтерифицированные пектины, что приводит к образованию гелей более высокой прочности, чем гели традиционных низкоэтерифицированных пектинов.
WO 2005/016027 A1 раскрывает способ получения пищевого продукта с использованием деполимеризованных пектинов в качестве стабилизатора. Указанные деполимеризованные пектины имеют цепи не более чем из 250 звеньев и вязкость в 5% растворе при 25°С от 15 сП до 400 сП.
В области производства джемов и желе низкая калорийность означает низкое содержание растворимых твердых веществ. Обычно растворимые твердые вещества являются сахарами, такими, как сиропы сахарозы и глюкозы, но могут также быть другими соединениями, такими, как декстроза, сорбит или другие сахарные спирты, и менее усвояемыми соединениями, например, такими, как глицерин и/или полидекстроза.
Для получения геля, имеющего низкое содержание растворимых твердых веществ, в литературе описана модель, которая содержит в относительно высоких концентрациях различные виды смол. При получении гелей с пектином важным является вид пектинового геля, который будет получен. Для высокого содержания растворимых твердых веществ El-Nawawi и Heikal: Factors affecting gelation of high-ester citrus pectin: Process Biochemistry, v.32, p.381-385, 1997 описывает условия, такие, как рН от 3,1 до 3,5 и содержание растворимых твердых веществ более 65%. Пектин, который образует гель в этих условиях, является высокоэтерифицированным пектином или высокометилированным пектином. Гель состоит, главным образом, из водородных связей, как описано Nielsen и Rolin: Pectin: Polysaccharides, Structural Drivers Functional Versatility, 1998, p.377-431, и, таким образом, концентрация растворимых твердых веществ должна быть высокой, низкая активность воды предохраняет пектин от образования водородных связей с водой. Следовательно, водородные связи образуются между пектином и пектином, и получается гелевая структура.
В системе с низкой концентрацией растворимых твердых веществ необходимо ввести другую гелеобразующую систему. НМ-пектин со СЭ ниже 50 образует гели не через образование водородных связей, а через ионные связи с ионами кальция, как обсуждено Padival, Ranganna и Manjrekar: Mechanism of gel formation by low methoxyl pectins, Journal of Food Technology, v.14, p.277-287, 1979. Для низкоэтерифицированных пектинов гелеобразование имеет место в диапазоне рН 3,0-3,6 и при концентрации растворимых твердых веществ выше 20%, как описано Rolin и de Vries: Pectin, в Harris (ed), Food Gels: London, Elsevier Applied Science, p.401-435, 1990.
При более низких концентрациях растворимых твердых веществ должны быть использованы другие, отличные от пектина, смолы, для того чтобы предотвратить выделение воды из геля. В Padival, Ranganna и Manjrekar: Mechanism of gel formation by low methoxyl pectins, Journal of Food Technology, v.14, p.277-287, 1979 описана смесь смолы бобов рожкового дерева (LBG) и пектина, и использование каппа-каррагенана и смолы камеди рожкового дерева вместе с НМ-пектином описано в Soler et al.; Development of formulations for a low-sugar guava preserve using LM-pectin and kappa-carrageenan combined with locust bean gum (LBG), изданной Phillips, Williams и Wedlock: Wrexham UK, IRL Press. Gums and Stabiliseres for the Food Industry 8, 257-266, 1995, описывает смесь НМ-пектина, каппа-каррагенана и LBG. Комбинации пектина и каррагенана описаны Gajar и Badrie: Processing and quality evaluation of low-calorie christophene jam (Sechium edule (Jacq.)) Swartz, Journal of Food Science 67 [1], 341-346, 2002. Суммарная концентрация камеди, которая включает пектин и/или другие смолы, составляет вплоть до 2,03% для предотвращения синерезиса и достижения требуемой текстуры.
Основная вкусовая проблема, связанная с низким содержанием растворимых твердых веществ и непектиновыми полисахаридами, такими, как камедь плодов рожкового дерева, гуаровая камедь, крахмал и каррагенан, заключается в появлении запаха. К тому же некоторые непектиновые полисахариды, такие, как камедь плодов рожкового дерева, гуаровая камедь и крахмал, придают ощущение клейкости во время поедания джема или желе, содержащих подобные полисахариды. Более того, непектиновые полисахариды являются менее стабильными, чем пектин, при низких значениях рН, предпочтительных из-за вкуса фруктов.
Существует необходимость приготовления гелеобразующей системы, основанной только на пектине, которая используется в низкокалорийных джемах и желе. Подобные джемы и желе являются важными для ограничения потребления простых углеводов по причине пользы для здоровья и для улучшения вкуса и питательной ценности, благодаря увеличению потребления фруктовых продуктов.
Гелеобразующая система, полностью состоящая из пектина, могла бы позволить заменить простые углеводы, такие, как сахароза, кукурузный сироп и концентрированный сироп фруктозы, водой, сильными подсластителями и, при желании, сложными полисахаридами, поддерживая в то же время качество ощущения и применения.
К тому же, при использовании гелеобразующей системы, полностью состоящей из пектина, и с низким содержанием растворимых твердых веществ, возможно избавиться от запаха.
Более того, гелеобразующая система, полностью состоящая из пектина, имеет улучшенную стабильность при низких значениях рН. Это означает, что при использовании гелеобразующей системы, полностью состоящей из пектина, процесс производства, в частности, время и температурные условия, становятся для достижения желаемой гелеобразной и/или пастообразной текстуры джема или желе менее критическими.
Более того, гелеобразующая система, полностью состоящая из пектина, могла бы обеспечить чистое, неклейкое ощущение и меньший синерезис джемов и желе как в банке, так и после того, как джем или желе будут механически разрушены, например, в процессе использования.
Другие преимущества гелеобразующей системы, полностью состоящей из пектина, включают хорошо определенное значение выхода или образования геля, которое обеспечивается при температуре чуть ниже температуры заполнения джема или желе. Это обеспечивает улучшенное распределение фруктовых компонентов; стабильность и низкую вязкость гелеобразующей системы при температуре и рН пастеризации; минимальное повреждение нагреванием фруктовых ароматизаторов и фруктовых красителей при данном содержании растворимых твердых веществ посредством улучшенной теплопередачи при температурах пастеризации.
Неожиданно было обнаружено, что гелеобразующая система, полностью состоящая из пектина, способна образовывать гели с менее чем примерно 30% растворимых твердых веществ без отделения неприемлемого количества воды, тем самым снижая потребность в использовании непектиновых смол, чтобы связывать воду.
Раскрытие изобретения
Настоящее изобретение относится к гелеобразующей системе, отличающейся тем, что она является комбинацией первого пектина и, по меньшей мере, одного второго пектина, в которой указанный первый пектин имеет содержание свободных кислотных остатков (Количество Свободных Кислот, КСК) в диапазоне 50-80% и в которой комбинация включает, по меньшей мере, 5 мас.% указанного второго пектина.
Настоящее изобретение также относится к применению гелеобразующей системы, соответствующей изобретению, в продуктах с низким содержанием растворимых твердых веществ.
Более того, изобретение относится к джему или желейным продуктам, включающим гелеобразующую систему в соответствии с настоящим изобретением.
Не ограничиваясь теорией, полагают, что содержание свободных кислотных остатков в компоненте первого пектина является важной характеристикой, поскольку содержание свободных кислотных остатков в пектине определяет количество центров, в которых такие двухвалентные катионы, как ионы кальция, могут связывать между собой две цепи молекул пектина с образованием трехмерной сети - геля. Однако если содержание свободных кислотных остатков становится слишком велико, то взаимодействия между цепями молекул пектина и двухвалентными катионами становятся настолько сильными, что образующаяся трехмерная сеть становится неспособной удерживать водную фазу внутри трехмерной сети. Это приводит к высвобождению воды, которое традиционно называется синерезисом.
Изобретение описано более детально со ссылкой на чертежи и раскрытия предпочтительных воплощений.
Краткое описание чертежей
Ниже изобретение объяснено детально со ссылками на чертежи, на которых
фиг.1 показывает устройство для измерения синерезиса геля,
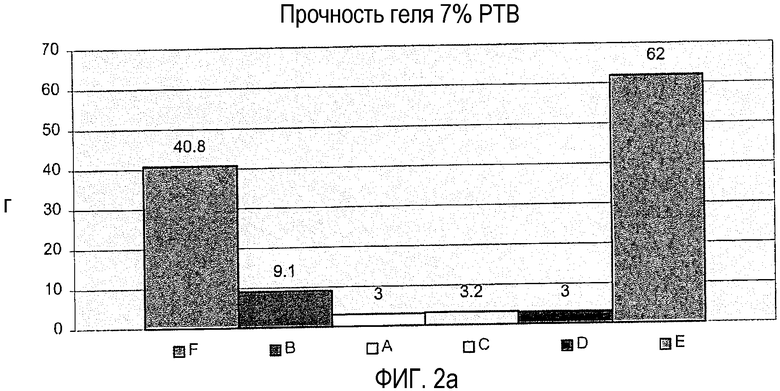
фиг.2а показывает прочность гелей, полученных с различными пектинами, при 7% растворимых твердых веществ,
фиг.2b показывает прочность гелей, полученных с различными пектинами, при 15% растворимых твердых веществ,
фиг.2с показывает прочность гелей, полученных с различными пектинами, при 20% растворимых твердых веществ,
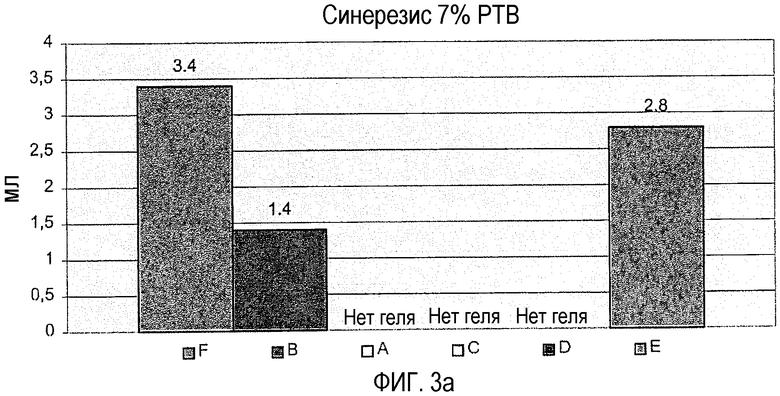
фиг.3а показывает синерезис гелей, полученных с различными пектинами, при 7% растворимых твердых веществ,
фиг.3b показывает синерезис гелей, полученных с различными пектинами, при 15% растворимых твердых веществ,
фиг.3с показывает синерезис гелей, полученных с различными пектинами, при 20% растворимых твердых веществ,
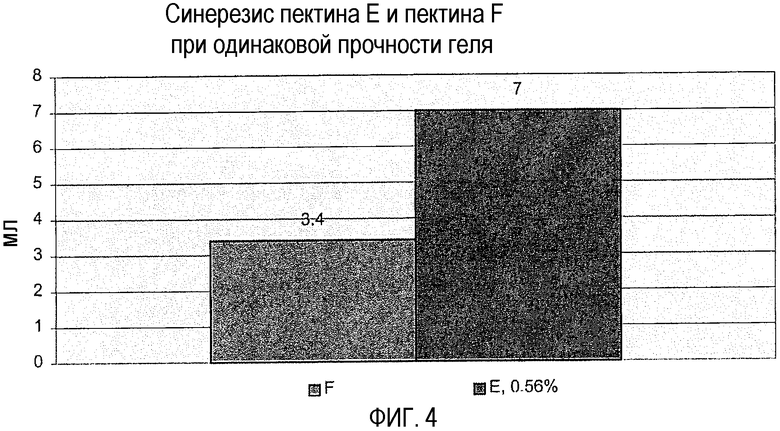
фиг.4 показывает синерезис гелей, полученных с различными пектинами, одинаковой прочности, но при различных уровнях нагрузки.
Наилучшие способы осуществления изобретения
В соответствии с изобретением в предпочтительном воплощении первый пектин имеет содержание свободных кислотных остатков, КСК, в диапазоне 55-75%, более конкретно, в диапазоне 60-70%. В предпочтительном воплощении указанный первый пектин дополнительно имеет степень амидирования, СА, в диапазоне 3-30%, более конкретно, 10-20%, еще более конкретно, 14-18%. Пример раскрытия первого пектина и его получения может быть найден в WO 2004005352. Пример первого пектина продается под торговой маркой пектин GENU® типа Х-602-03.
В соответствии с настоящим изобретением второй пектин для использования в гелеобразующей системе является обычным амидированным или неамидированным пектином, имеющим степень этерификации, СЭ, в диапазоне 10-75. В наиболее предпочтительном воплощении указанный второй пектин является пектином с низкой СЭ, более конкретно, в диапазоне 20-50%, еще более конкретно, в диапазоне 30-40%.
Соответственно степень амидирования, СА, указанного второго пектина находится в диапазоне 0-30%, более конкретно, в диапазоне 5-25%, и, главным образом, в диапазоне 12-18%. Подобные пектины являются, в том числе, коммерчески доступными от СР Keico, Lille Skensved, Дания, под торговыми марками пектин GENU® типа 101AS, пектин GENU® типа 102AS, пектин GENU® типа 104AS, пектин GENU® типа LM 12 CG и GENU® пектин типа LM 5CS или могут быть получены обычными способами получения пектинов.
Было обнаружено, что комбинация вышеупомянутых первого и второго пектинов в соотношении 25-95:5-75 приводит к великолепным гелеобразующим свойствам продуктов с низким содержанием растворимых твердых веществ. Предпочтительными соотношениями являются 50-75:25-50, и более предпочтительным является соотношение примерно 67% указанного первого пектина и примерно 33% указанного второго пектина. Подобная комбинация приводит к оптимальным характеристикам, с точки зрения прочности и синерезиса, как показано в примерах ниже.
В соответствии с изобретением гелеобразующая система особенно хорошо подходит для продуктов с низким содержанием растворимых твердых веществ, главным образом, продуктов, имеющих содержание растворимых твердых веществ (% РТВ) в диапазоне 5-30%, более конкретно, в диапазоне 7-20%. Сегодня продукты с низким содержанием растворимых твердых веществ являются более востребованными, с точки зрения здоровья. Благодаря гелеобразующей системе в соответствии с настоящим изобретением стало возможным получить джемы или желе, имеющие достаточное сопротивление разрушению, одновременно поддерживая низкий уровень синерезиса.
Более того, гелеобразующая система по настоящему изобретению достигает требуемого уровня сопротивления разрушению при значительно более низких уровнях нагрузки, чем гелеобразующие системы предшествующего уровня техники, не полностью состоящие из пектина. Таким образом, предусмотрен уровень нагрузки в диапазоне 0,3-1,1 мас.%. Более конкретно, предусмотрен уровень нагрузки в диапазоне 0,5-0,9, конкретно уровень нагрузки в диапазоне 0,6-0,8.
Материалы и методы
Определение степени этерификации (СЭ), амидирования (СА) и галактуроновой кислоты (ГК) в пектине
Принцип:
Данный способ является модификацией способа FAO/WHO определения % СЭ, % СА и % ГК в пектине (FCC, Food Chemicals Codex (1996), Committee on Food Chemicals Codex/ Food and Nutrition Board, Institute of Medicine, National Academy of Sciences, 4th edition, National Academy Press, Washington DC, USA).
Материалы:
Магнитная мешалка, IKA-Werke RO-10 Power, Bie & Bernsten A/S Avedøre, Дания
Подкисленный спирт: 100 мл 60% ИПС+5 мл дымящей 37% HCl, Prolabo, VWR International Aps, Albertslund, Дания
Автотитратор, Metrohm, 730 с устройством для смены образцов, 2600 Glostrup, Дания
Дозатор: 685 Dosimat, Metrohm, 2600 Glostrup, Дания
0,1 N NaOH, Prolabo, VWR International Aps, Albertslund, Дания
0,1 N HCl Bie & Bernsten A/S Avedøre, Дания
0,5 N NaoH Bie & Bernsten A/S Avedøre, Дания
0,5 N HCl Bie & Bernsten A/S Avedøre, Дания
Дистилляционный аппарат: Kjeltec™ 2200, Foss, Дания
4% борная кислота с индикатором, Bie & Bernsten A/S Avedøre, Дания
32,5% NaOH для определения N, Bie & Bernsten A/S Avedøre, Дания
Порядок определения % СЭ, % СА и % ГК:
1. Взвешивают 2,000 г пектина в стеклянном стакане на 250 мл.
2. Добавляют 100 мл подкисленного спирта и перемешивают в течение 10 мин на магнитной мешалке.
3. Отфильтровывают в сухой, взвешенный стеклянный фильтровальный тигель (размер 1).
4. Полностью промывают стакан 6×15 мл подкисленного спирта.
5. Промывают 60% ИПС до тех пор, пока фильтрат не станет свободным от хлора (приблизительно 500 мл).
6. Промывают 20 мл 100% ИПС.
7. Высушивают образец в течение двух часов при 105°С.
8. Взвешивают тигель после высушивания и охлаждения в эксикаторе.
9. Точно взвешивают приблизительно 0,2000 г образца в пластиковой пробирке на 120 мл.
10. Взвешивают два образца для двойного определения.
11. Смачивают пектин приблизительно 2 мл 100% ИПС и добавляют приблизительно 50 мл деионизированной воды, свободной от диоксида углерода при перемешивании магнитной мешалкой в течение, по меньшей мере, 10 мин.
12. Готовят три слепых контрольных опыта. Каждая пластиковая пробирка на 120 мл содержит 50 мл деионизированной воды, не содержащей диоксида углерода.
*(Тест на хлор: переносят приблизительно 10 мл фильтрата в пробирку, добавляют приблизительно 3 мл 3 N HNO3 и добавляют несколько капель AgNO3. Если раствор прозрачный, то фильтрат не содержит хлора, иначе появится осадок хлорида серебра).
После промывания кислотой образцы готовы для титрования.
Автотитратор программируют следующим образом.
1. Титрование 0,1N NaOH до достижения точки эквивалентности (рН равен приблизительно 8,5). Объем титрования обозначается как V1.
2. Добавляют 10 мл 0,5 N NaOH.
3. Смесь выдерживают в течение 15 мин.
4. Добавляют 10 мл 0,5 N HCl.
5. Титрование 0,1 N NaOH до достижения точки эквивалентности (рН равен приблизительно 8,5). Объем титрования обозначается как V2 для образцов и B1 для контрольных слепых опытов.
Для неамидированного пектина вычисляют % СЭ и % ГК.
Вычисление:
Vt=V1+(V2-B1)
% СЭ (Степень этерификации)=((V2-B1)×100)/Vt
% КСК (Количество свободной кислоты)=100-% СЭ
% ГК* (Количество галактуроновой кислоты)=(194,1×Vt×N×100)/200
*На обеззоленное и безводное основание
194,1: Молекулярная масса (г/моль) галактуроновой кислоты
N: Исправленная нормальность 0,1 N NaOH, использованного для титрования (например, 0,01002 N)
200: Масса в мг промытого и высушенного образца для титрования
% Чистого пектина=количество пектина, промытого кислотой и высушенного, (100/взвешенное количество пектина)
Для амидированного пектина дистилляция амидных групп проводится на устройстве Kjeltec:
1. Образец переносят количественно в пробирку для разрушения промыванием стакана суммарно 50 мл воды, свободной от диоксида углерода в три стадии.
2. Помещают в устройство приемную колбу, содержащую 10,00 мл 4% борной кислоты с индикатором.
3. Kjeltec программируют на добавление 30 мл 32,5% NaOH в пробирку для разрушения, содержащую образец.
4. Устанавливают время дистилляции, равное 4 минутам и 40 секундам.
5. Титруют дистиллят в автотитраторе 0,1 N HCl до достижения точки эквивалентности (рН примерно 4,8). Объем титрования обозначают как V3.
Образец слепого контрольного опыта дистиллируют и титруют как образец. Объем титрования обозначают как B2.
Вычисление:
Vt=V1+(V2-B1)+(V3-B2)
% СЭ (Степень этерификации)=((V2-B1)×*100)/Vt
% СА (Степень амидирования)=((V3-B2)×100)/Vt
% КСК (Количество свободной кислоты)=100-% СЭ-% СА
% ГК* (Количество галактуроновой кислоты)=(194,1×Vt×N×100)/200
*На обеззоленное и безводное основание
194,1: Молекулярная масса (г/моль) галактуроновой кислоты
N: Исправленная нормальность 0,1 N NaOH, использованного для титрования, (например, 0,01002 N)
200: Масса в мг промытого и высушенного образца для титрования
% Чистого пектина=количество пектина, промытого кислотой и высушенного,*100/взвешенное количество пектина
Реологические измерения малиновых синтетических гелей
Материалы:
Смеситель и режущая пластина: Silverson L4RT с распадающейся головкой (d-3,5 см) Silverson Machines Limited, Waterside, Chesham, HP5 IPQ Bucks, Англия
Электрическая нагревающая плитка: Buch & Holm A/S, DK-2730 Herlev, Дания
Электрическая лопастная мешалка: RW 20, Janke & Kunkel, IKA-Werk, Bie & Berntsen A/S, Rødovre, Дания
Весы: Mettler PJ 6000 Instruments, Greifensee-Zurich, Switzerland.
Водяная баня: Haake EK - Julabo MD.
4 кристаллизационных стакана, диаметр: 70 мм, высота: 40 мм.
Чистая, чувствительная к давлению клейкая лента
Деревянная стойка для измерения синерезиса (см. фиг.1)
Фильтр (размер сита 180 мкм и диаметр 95 мм) (см. фиг.1)
Пластиковая воронка (диаметр 95 мм) (см. фиг.1)
Мерный цилиндр 10 мл
Анализатор структуры TA - XT2, Stable Micro Systems, GU71YL Surrey, Англия.
Кислый сок малины: Sur Hindbær Saft, изготовленный Rynkeby Foods A/S, Ringe 5750, Дания
Столовый сахар
Бензоат натрия 20% мас./об.
Сорбат калия 20% мас./об.
Лимонная кислота 50% мас./об.
Способ:
Синтетические малиновые гели получают, как раскрыто в примерах. Сразу после их получения проверяют массу (1000 г) и температуру (95°С) раствора до заполнения четырех кристаллизационных стаканов, которые помещены в водяную баню при 20°С на 24 часа, после которых измеряют синерезис и прочность геля. Проверяют % РТВ (±1%)и рН (3,1-3,3). Синерезис измеряют, помещая гель на фильтр (размер сита 180 мкм и диаметр 95 мм) и собирая через два часа отделенную жидкость (фиг.1).
Прочность геля, которая определяется как груз, требуемый для сжатия геля на 4 мм, измеряется на TA-XT2, снабженном однодюймовым поршнем. Другие настройки включают:
Скорость до испытания: 2,0 мм/с
Скорость во время испытаний: 0,5 мм/с
Скорость после испытаний: 10,00 мм/с
Скорость разрыва во время испытаний: 1 мм/с
Расстояние: 24,0 мм/с
Сила: 40 г
Время: 0,09 г
Счет: 5
Тип: Авто
Сила триггера: 0,5 г
Примеры
Следующие пектины были использованы в синтетических малиновых гелях, описанных ниже.
Пектины А, B, C и D являются коммерческими пектинами, производимыми CP Kelco ApS и используемыми для приготовления восстановленных джемов и желе, продаваемых под торговыми марками пектин GENU® типа 101AS, пектин GENU® типа 104AS, пектин GENU® типа LM 12 CG, пектин GENU® LM 5CS и пектин GENU® типа X-602-03 соответственно. Пектины А и В являются амидированными низкоэтерифицированными пектинами, в то время как пектины С и D являются неамидированными низкоэтерифицированными пектинами. Пектин Е относится к амидированным низкоэтерифицированным пектинам, как раскрыто в WO2004005352, и продается под торговой маркой пектин GENU® типа X-602-03.
*Вязкость была измерена следующим образом:
Для приготовления 5% раствора 25,00 граммов стабилизатора растворили в примерно 500 мл деминерализованной воды при 80°С во взвешенном стакане. Затем раствор стабилизатора охладили до 25°С и довели рН добавлением 1 N хлороводородной кислоты или 20% раствором карбоната натрия до 3,5±0,2. Суммарный вес раствора довели до 500,0 граммов, добавляя деминерализованную воду. Вязкость измерили на Brookfield Viscosimeter модель DV-II со шпинделем №61 (в случае более высоких вязкостей шпиндели №62 или №63) при 25°С при 60 оборотах в минуту.
Получение малиновых синтетических гелей
Были получены малиновые синтетические гели следующих составов.
Распределение растворимых твердых веществ (% РТВ)
(20% мас./об.
Пектин диспергируют в 200 г горячей воды при 90°С при перемешивании Silverson L4RT в течение 5 мин. при 5000 оборотов в минуту. 300 г кислого сока малины, сахар в соответствии с желаемой концентрацией растворимых твердых веществ и деионизированную воду смешивают для приготовления 500 г. Эту смесь нагревают в сосуде на 1 литр до точки кипения при перемешивании электрической лопастной мешалкой при 500 оборотах в минуту. Когда весь сахар растворится и смесь закипит, добавляют горячий раствор пектина, и раствор поддерживают кипящим в течение 2 мин при перемешивании. До добавления 2 мл бензоата натрия (20% мас./об.) и 2 мл сорбата калия (20% мас./об.) раствор доводят горячей деионизированной водой до 1000 г. В заключение добавляют 6 мл лимонной кислоты (50% мас./об.). При добавлении консервантов и кислоты раствор поддерживают при 95°С при перемешивании.
Прочность геля и уровень синерезиса вышеуказанных пектинов измеряют, как описано выше.
Прочность геля и синерезис гелей
*2 гелеобразующая система в соответствии с изобретением, включающая комбинацию 33% пектина А и 67% пектина Е
Пектины A, C и D не вызывают гелеобразования, и, таким образом, синерезис не может быть определен. При прочности геля менее 5 г гель является слишком слабым, чтобы обеспечить какую-либо видимую структуру.
фиг.2 показывает, что пектин Е явно обеспечивает наибольшую прочность геля. Фактически данная прочность геля слишком высока, что означает, что образующийся гель является чрезмерно жестким, тугим и ломким. Пектин В обеспечивает гораздо более слабый гель. Фактически данная прочность геля является слишком малой, чтобы обеспечивать приемлемый гель. Также показано, что пектины A, C и D не образуют гелей.
фиг.3 показывает, что оба пектина В и Е демонстрируют синерезис, при этом пектин В является единственным, который производит наименьшее количество синерезиса. Таким образом, пектины предшествующего уровня техники являются либо слишком прочными, либо слишком слабыми.
Однако комбинация гелеобразующей системы F по настоящему изобретению обеспечивает прочный гель, который является сенсориально приемлемым. Достаточно обеспечить необходимую растекаемость без течения. К тому же уровень синерезиса является достаточно низким, чтобы гарантировать, что гель останется явно сухим и не приведет к видимой воде, пока гель будет находиться в контейнере, например в стеклянной банке.
Сравнение пектина E и пектина F
Таблица 3 показывает, что пектин Е обеспечивает прочность геля, которая является органолептически неприемлемой. Данная прочность геля может быть уменьшена до уровня, соответствующего прочности геля пектина F, соответствующего изобретению, уменьшением концентрации пектина Е до 0,56%. Однако при данном значении концентрации образующийся гель характеризуется слишком большим синерезисом. Различие в синерезисе показано на фиг.4.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ (КМЦ) В ПРОДУКТАХ НА ФРУКТОВОЙ ОСНОВЕ | 2003 |
|
RU2322085C2 |
| ГЕЛЕВАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2584162C2 |
| УЛУЧШЕННЫЙ СПОСОБ ОБРАБОТКИ РАСТИТЕЛЬНОГО МАТЕРИАЛА, СОДЕРЖАЩЕГО ПЕКТИН | 2003 |
|
RU2336280C2 |
| КИСЛОМОЛОЧНЫЙ ПРОДУКТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2599442C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФРУКТОВО-ЯГОДНОГО ЖЕЛЕЙНОГО ПИЩЕВОГО ПРОДУКТА | 2020 |
|
RU2748802C1 |
| ЭМУЛЬСИИ "МАСЛО-В-ВОДЕ", СОДЕРЖАЩИЕ СМЕСЬ БИОПОЛИМЕРОВ | 2002 |
|
RU2311789C2 |
| МОЛОЧНЫЙ ПУДИНГ | 2013 |
|
RU2562116C2 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО ПЕКТИНА | 2010 |
|
RU2441025C1 |
| КОМПОЗИЦИЯ С РЕГУЛИРУЕМОЙ ЩЕЛОЧНОСТЬЮ ДЛЯ ЗАЩИТЫ КОЖИ И ЕЕ ПРИМЕНЕНИЕ | 2005 |
|
RU2358713C2 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО ПЕКТИНА | 2010 |
|
RU2441024C1 |





Изобретение относится к пищевой промышленности. Гелеобразующая система отличается тем, что она является комбинацией первого пектина и, по меньшей мере, одного второго пектина. Первичный пектин имеет содержание свободных кислотных остатков в диапазоне 50-80%. Указанный второй пектин содержится в комбинации в количестве по меньшей мере 5 мас.% и имеет степень этерификации в диапазоне 20-50%. Гелеобразующая система является пригодной для гелеобразования джемов и желе с содержанием растворимых твердых веществ менее 30%. Изобретение позволило получить джемы и желе с низким содержанием растворимых твердых веществ, обладающие улучшенными органолептическими показателями без ощущения клейкости и стабильностью, исключить использование непектиновых полисахаридов при производстве и уменьшить синерезис продукта в процессе хранения и использования. 3 н. и 16 з.п. ф-лы, 8 ил., 4 табл.
1. Гелеобразующая система, отличающаяся тем, что она является комбинацией первого пектина и, по меньшей мере, одного второго пектина, в которой указанный первый пектин имеет содержание свободных кислотных остатков (количество свободных кислот, КСК) в диапазоне 50-80%, и в которой указанная комбинация включает, по меньшей мере, 5 мас.% указанного второго пектина, имеющего СЭ в диапазоне 20-50%.
2. Гелеобразующая система по п.1, в которой указанный первый пектин имеет КСК в диапазоне 55-75%.
3. Гелеобразующая система по п.1 или 2, в которой КСК указанного первого пектина находится в диапазоне 60-70%.
4. Гелеобразующая система по п.1, в которой указанный первый пектин имеет степень амидирования, СА, в диапазоне 3-30%.
5. Гелеобразующая система по п.4, в которой СА указанного первого пектина находится в диапазоне 10-20%.
6. Гелеобразующая система по п.5, в которой СА указанного первого пектина находится в диапазоне 14-18%.
7. Гелеобразующая система по п.1, в которой СЭ указанного второго пектина находится в диапазоне 30-40%.
8. Гелеобразующая система по п.1, в которой указанный второй пектин имеет степень амидирования, СА, в диапазоне 0-30%.
9. Гелеобразующая система по п.8, в которой СА указанного второго пектина находится в диапазоне 5-25%.
10. Гелеобразующая система по п.8 или 9, в которой СА указанного второго пектина находится в диапазоне 12-18%.
11. Гелеобразующая система по п.1, включающая примерно 25-95% указанного первого пектина и примерно 5-75% указанного второго пектина.
12. Гелеобразующая система по п.11, включающая примерно 50-75% указанного первого пектина и примерно 25-50% указанного второго пектина.
13. Гелеобразующая система по п.12, включающая примерно 67% указанного первого пектина и примерно 33% указанного второго пектина.
14. Применение гелеобразующей системы в соответствии с любым из пп.1-13 в продуктах с содержанием растворимых твердых веществ в диапазоне 5-30%.
15. Применение по п.14, в котором содержание растворимых твердых веществ находится в диапазоне 7-20%.
16. Джем или желе, включающие гелеобразующую систему в соответствии с любым из пп.1-13.
17. Джем или желе по п.16, включающие примерно 0,3-1,1 мас.% указанной гелеобразующей системы.
18. Джем или желе по п.16 или 17, включающие примерно 0,5-0,9 мас.% указанной гелеобразующей системы.
19. Джем или желе по п.18, включающие примерно 0,6-0,8 мас.% указанной гелеобразующей системы.
| Дезинфекционная камера | 1977 |
|
SU639555A1 |
| ПРОИЗВОДНЫЕ ПИРИДОНА | 1992 |
|
RU2078082C1 |
| US 4532143 А, 30.07.1985. | |||
Авторы
Даты
2010-04-10—Публикация
2005-10-12—Подача