Область техники
Настоящее изобретение относится к новому способу посттрансляционной конъюгации пептидов, где трансглутаминазу используют для включения в пептид места присоединения, к которому может быть избирательно присоединена другая группа. Указанные конъюгированные пептиды обладают измененными характеристиками и могут, следовательно, иметь применение в терапевтических целях либо они могут облегчить анализ или выделение и очистку указанных пептидов.
Предшествующий уровень техники
Хорошо известно, что свойства и характеристики пептидов можно модифицировать путем присоединения к этим пептидам групп, которые должным образом изменяют свойства пептида. Для такой конъюгации обычно необходимо, чтобы некоторая функциональная группа в пептиде взаимодействовала с другой функциональной группой с образованием конъюгирующей группы. Как правило, аминогруппы, такие как N-концевая аминогруппа или ε-аминогруппа в лизинах, использовали в сочетании с подходящим ацилирующим реагентом. Часто желательно или даже необходимо уметь регулировать реакцию конъюгации, то есть контролировать, где присоединяются конъюгирующие соединения и сколько конъюгирующих групп присоединяется. Это часто называют специфичностью.
Задачей настоящего изобретения является разработка способа, с помощью которого пептиды можно конъюгировать с высокой степенью специфичности. В общих чертах в этом способе используют фермент, например трансглутаминазу, способный к включению соединения, содержащего подходящую функциональную группу, в пептид, где указанную функциональную группу затем используют в качестве места присоединения, где происходит конъюгация.
Конъюгация пептидов известна на протяжении длительного времени, и более 20 лет назад в US 4179337 раскрыты пептиды, конъюгированные с полиэтилен- или полипропиленгликолями.
Раскрыты различные типы химических реакций, которые эффективны для образования связи между пептидом и фрагментом, который конъюгируют с этим пептидом. В ЕР 605963 раскрыта графт-полимеризация водных полимеров, которые образуют оксимную связь с альдегидной группой на белке. Ни одна из природных аминокислот не содержит альдегидную группу, поэтому в процессе конъюгации сначала нужно окислить гидроксильную группу. В WO 96/41813 раскрыты полимеры, которые содержат группу, образующую оксим амино-окси, полезный в реакциях конъюгации. В WO 98/05363 раскрыто соединение, содержащее пептид и растворимый в воде полимер, где эти два соединения ковалентно связаны посредством оксимной связи при N-концевом аминокислотном остатке.
Кроме того, известно использование ферментов для обеспечения более специфичной конъюгации пептидов. В ЕР 243929 раскрыто использование протеолитических ферментов, таких как карбоксипептидаза, для включения соединения с функциональной группой в С-конец пептида, где указанную функциональную группу можно затем использовать в качестве места, к которому присоединяют цитотоксические группы, другие пептиды или репортерные группы, используемые для облегчения анализа пептида, такие как, например, флуоресцентные группы. Эта методика, однако, ограничивает выбор места присоединения С-концевым аминокислотным остатком, что является жестким ограничением, если этот С-концевой остаток является существенным для активности пептида.
Трансглутаминазу ранее использовали для изменения свойств пептидов. В пищевой промышленности и, в частности, в молочной промышленности, существует много методик, например, для структурированных пептидов, с использованием трансглутаминаз. В других документах раскрыто использование трансглутаминазы для изменения свойств физиологически активных пептидов. В ЕР 950665, ЕР 785276 и Sato, Adv. Drug Delivery Rev., 54, 487-504, 2002, раскрыта прямая реакция между пептидами, содержащими по меньшей мере один Gln, и аминированным ПЭГ или подобными лигандами в присутствии трансглутаминазы, и авторами Wada в Biotech. Lett., 23, 1367-1372, 2001, раскрыта прямая конъюгация β-лактоглобулина с жирными кислотами с помощью трансглутаминазы.
Краткое изложение сущности изобретения
Авторы настоящего изобретения неожиданно обнаружили, что ферменты, такие как, например, трансглутаминаза, можно использовать для включения в пептид одной или более чем одной функциональной группы, не доступные в данном пептиде, с образованием функционализированного пептида, и что этот функционализированный пептид можно затем подвергать взаимодействию с другим соединением, содержащим конъюгирующую группу и одну или более чем одну функциональную группу, способную взаимодействовать с функциональной группой или группами, включенными, таким образом, в пептид, но не взаимодействовать с другими функциональными группами, присутствующими в этом пептиде.
Такой способ обеспечивает высокую степень специфичности в связи с тем, что трансглутаминаза может катализировать включение соединений только при аминокислотных остатках, которые являются субстратами для трансглутаминазы, и в связи с тем, что функциональные группы выбраны таким образом, что они могут взаимодействовать друг с другом, но не взаимодействовать с другими функциональными группами, содержащимися в этом пептиде. Таким образом, конъюгирующая группа присоединяется только в контролируемом локусе или локусах, и путем выбора функциональных групп можно регулировать число конъюгированных групп.
Соответственно, в одном варианте изобретения предложен способ конъюгации пептидов, включающий
i) взаимодействие в одну или более чем одну стадию пептида с первым соединением, содержащим одну или более чем одну функциональную группу или скрытую функциональную группу, которая не доступна ни в одном из аминокислотных остатков, составляющих указанный пептид, в присутствии трансглутаминазы, способной катализировать включение указанного первого соединения в пептид с образованием функционализированного пептида,
ii) возможную активацию указанной скрытой функциональной группы и
iii) взаимодействие в одну или более чем одну стадию функционализированного пептида со вторым соединением, содержащим одну или более чем одну функциональную группу, где указанная функциональная группа или группы не взаимодействуют с функциональными группами, доступными в аминокислотных остатках, составляющих указанный пептид, причем функциональная группа или группы во втором соединении способны взаимодействовать с функциональной группой или группами в первом соединении с образованием ковалентной связи между функционализированным пептидом и вторым соединением.
Задачей настоящего изобретения также является разработка пептидов, конъюгированных способом согласно настоящему изобретению.
Следующей задачей настоящего изобретения также является разработка пептидов, которые модифицированы таким образом, чтобы сделать их более пригодными для способа согласно настоящему изобретению.
Следующей задачей настоящего изобретения является разработка реагентов и ферментов, пригодных для использования в способах согласно настоящему изобретению.
Следующей задачей настоящего изобретения является разработка композиций, например фармацевтических композиций, содержащих пептиды, конъюгированные способом согласно настоящему изобретению.
Следующей задачей настоящего изобретения является разработка пептидов, конъюгированных способами согласно настоящему изобретению, для применения в терапии.
Следующей задачей настоящего изобретения является разработка терапевтических способов для лечения заболеваний, при которых вводят конъюгированные пептиды, полученные способами согласно настоящему изобретению.
Следующей задачей настоящего изобретения является разработка применения конъюгированных пептидов, полученных способами согласно настоящему изобретению, в для изготовления лекарственных средств.
Следующей задачей настоящего изобретения является разработка способа улучшения фармакологических свойств пептида путем конъюгации указанного пептида способами согласно настоящему изобретению.
Определения
В настоящем контексте "трансаминирование" или подобный термин предназначен для обозначения реакции, где атом азота в боковой цепи глутамина обменивается с атомом азота от другого соединения, в частности с атомом азота от другого азотсодержащего нуклеофила.
В настоящем контексте термин "не доступный" означает, что что-либо отсутствует или отсутствует de facto в том смысле, что что-либо не достижимо. Когда указано, что функциональные группы не доступны в пептиде, который конъюгируют, это должно означать, что указанная функциональная группа отсутствует в пептиде или, если присутствует, то каким-либо образом предотвращено ее участие в реакциях. Например, указанная функциональная группа может быть углублена в структуру пептида таким образом, что она защищена от участия в реакции, либо она может быть расположена в таком участке пептида, где ограниченная гибкость пептидной цепи предотвращает участие этой функциональной группы в реакциях. Понятно, что доступность или недоступность функциональной группы зависит от условий реакции. Можно рассматривать, что в присутствии денатурирующих агентов или при повышенных температурах пептид может развертываться с обнажением не доступных в других условиях функциональных групп. Должно быть понятно, что "не доступный" означает "не доступный при условиях реакции, выбранных для конкретной интересующей реакции".
В настоящем контексте термин "оксимная связь" означает группу формулы -С=N-O-.
В настоящем контексте термин "гидразонная связь" означает группу формулы -C=N-N-.
В настоящем контексте термин "фенилгидразонная связь" означает группу формулы
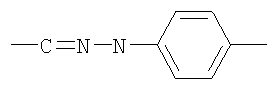
В настоящем контексте термин "семикарбазонная связь" означает группу формулы -C=N-N-C(O)-N-.
Термин "алкан" означает насыщенный, нормальный, разветвленный и/или циклический углеводород. Если при нем не указано иное число атомов, этим термин означает углеводороды с числом атомов углерода от 1 до 30 (оба включительно), как, например, от 1 до 20 (оба включительно), как, например, от 1 до 10 (оба включительно), например, от 1 до 5 (оба включительно) или от 15 до 30 атомов углерода (оба включительно).
Термин "алкен" означает насыщенный, нормальный, разветвленный и/или циклический углеводород, содержащий по меньшей мере одну двойную связь углерод-углерод. Если при нем не указано иное число атомов, этим термин означает углеводороды с числом атомов углерода от 2 до 30 (оба включительно), как, например, от 2 до 20 (оба включительно), как, например, от 2 до 10 (оба включительно), например, от 2 до 5 (оба включительно) или от 15 до 30 атомов углерода (оба включительно).
Термин "алкин" означает насыщенный, нормальный, разветвленный и/или циклический углеводород, содержащий по меньшей мере одну тройную связь углерод-углерод. Если при нем не указано иное число атомов, этим термин означает углеводороды с числом атомов углерода от 2 до 30 (оба включительно), как, например, от 2 до 20 (оба включительно), как, например, от 2 до 10 (оба включительно), например, от 2 до 5 (оба включительно) или от 15 до 30 атомов углерода (оба включительно).
Термин "гомоциклическое ароматическое соединение" означает ароматические углеводороды, такие как бензол и нафталин.
Термин "гетероциклическое соединение" означает циклическое соединение, содержащее 5, 6 или 7 кольцевых атомов, из которых 1, 2, 3 или 4 представляют собой гетероатомы, выбранные из N, О и/или S. Примеры гетероциклических ароматических соединений включает тиофен, фуран, пиран, пиррол, имидазол, пиразол, изотиазол, изоксазол, пиридин, пиразин, пиримидин, пиридазин, а также их частично или полностью гидрогенизированные эквиваленты, такие как пиперидин, пиразолидин, пирролидин, пирролин, имидазолидин, имидазолин, пиперазин и морфолин.
Термины "гетероалкан", "гетероалкен" и "гетероалкин" обозначают алканы, алкены и алкины, как определено выше, в котором один или более чем один гетероатом или группа включена в структуру указанных групп. Примеры гетерогрупп и гетероатомов включают -О-, -S-, -S(O)-, -S(O)2-, -C(O)- -C(S)- и -N(R*)-, где R* представляет собой водород или C1-C6-алкил. Примеры гетероалканов включают:
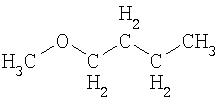 ,
, 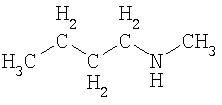 ,
, 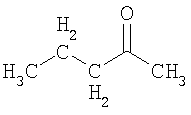 ,
,
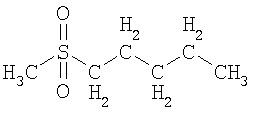 ,
, 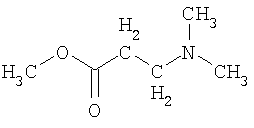 и
и 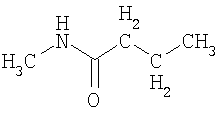
Термин "радикал" или "бирадикал" означает соединение, из которого один или два, соответственно, атома водорода удалены. Когда конкретно указано, радикал может также означать группу, образованную путем удаления из соединения большей группы атомов, например, гидроксила.
Термин "галоген" означает члены седьмой группы главной подгруппы периодической таблицы, например. F, Cl, Br и I.
Термин "ПЭГ означает полиэтиленгликоль молекулярной массы между примерно 100 и примерно 1000000 Да, включая его аналоги, где, например, концевая ОН-группа замещена группой алкокси, такой как, например, группа метокси, группа этокси или группа пропокси. В частности, ПЭГ, где концевая группа -ОН замещена метокси, называют мПЭГ.
Термин "мПЭГ" (или более правильно "мПЭГил") означает полидисперсный или монодисперсный радикал структуры
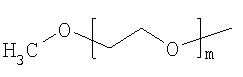
где m представляет собой целое число больше 1. Таким образом, мПЭГ, где m равно 90, имеет молекулярную массу 3991 Да, то есть примерно 4 кДа. Подобным образом, мПЭГ со средней молекулярной массой 20 кДа имеет среднее m 454. В результате способа получения мПЭГ эти молекулы часто имеют распределение молекулярных масс. Это распределение описывают индексом полидисперсности.
Термин "индекс полидисперсности" означает отношение между средней молекулярной массой и среднечисловой молекулярной массой, как известно в области химии полимеров (см., например, "Polymer Synthesis and Characterization", J.A. Nairn, University of Utah, 2003). Индекс полидисперсности представляет собой число, которое выше или равно единице, и его можно оценить на основании данных гель-проникающей хроматографии. Когда индекс полидисперсности равен 1, продукт является монодисперсным и, таким образом, состоит из соединений с единой молекулярной массой. Когда индекс полидисперсности выше 1, он является мерой полидисперсности этого полимера, то есть того, насколько широким является распределение полимеров с различными молекулярными массами.
Использование, например, выражения "мПЭГ20000" в формулах, названиях соединений или в молекулярных структурах означает остаток мПЭГ, где мПЭГ является полидисперсным и имеет молекулярную массу примерно 20 кДа.
Индекс полидисперсности, как правило, повышается с повышением молекулярной массы ПЭГ или мПЭГ. Когда делают ссылку на 20 кДа ПЭГ и, в частности, 20 кДа мПЭГ, она предназначена для указания соединения (или в действительности смеси соединений) с индексом полидисперсности ниже 1,06, таким как ниже 1,05, таким как ниже 1,04, таким как ниже 1,03, таким как между 1,02 и 1,03. Когда делают ссылку на 30 кДа ПЭГ и, в частности, 30 кДа мПЭГ, она предназначена для указания соединения (или в действительности смеси соединений) с индексом полидисперсности ниже 1,06, таким как ниже 1,05, таким как ниже 1,04, таким как ниже 1,03, таким как между 1,02 и 1,03. Когда делают ссылку на 40 кДа ПЭГ и, в частности, 40 кДа мПЭГ, она предназначена для указания соединения (или в действительности смеси соединений) с индексом полидисперсности ниже 1,06, таким как ниже 1,05, таким как ниже 1,04, таким как ниже 1,03, таким как между 1,02 и 1,03.
В настоящем контексте слова "пептид" и "белок" используют взаимозаменяемо, и они должны обозначать одно и то же. Термин "пептид" означает соединение с двумя или более чем двумя аминокислотными остатками, связанными пептидной связью. Аминокислоты могут быть природными или неприродными. В этот термин также следует включать указанные соединения, замещенные другими пептидами, сахаридами, липидами или другим органическим соединением, а также соединения, где один или более чем один аминокислотный остаток химически модифицирован. В этот термин также следует включать пептиды, к которым присоединены простетические группы. В частности, пептид проявляет физиологическую активность, такую как, например, терапевтическая активность.
В настоящем контексте термин "арил" означает гомоциклический ароматический кольцевой радикал или радикал, представляющий собой конденсированную гомоциклическую кольцевую систему, где по меньшей мере одно из колец является ароматическим. Типичные арильные группы включают фенил, дифенил, нафтил, тетралинил и тому подобное.
Термин "гетероарил", как его используют здесь, один или в комбинации, относится к ароматическому кольцевому радикалу с числом кольцевых атомов, например, от 5 до 7, или к радикалу, представляющему собой конденсированную ароматическую кольцевую систему с числом кольцевых атомов, например, от 7 до 18, где по меньшей мере одно из колец является ароматическим и содержит один или более чем один гетероатом в виде кольцевых атомов, выбранный из гетероатомов азота, кислорода или серы, где N-оксиды, а также монооксиды серы и диоксиды серы являются допустимыми гетероароматическими замещениями. Примеры включают фуранил, тиенил, тиофенил, пирролил, имидазолил, пиразолил, триазолил, тетразолил, тиазолил, оксазолил, изоксазолил, оксадиазолил, тиадиазолил, изотиазолил, пиридинил, пиридазинил, пиразинил, пиримидинил, хинолинил, изохинолинил, бензофуранил, бензотиофенил, индолил и индазолил и тому подобное.
Термин "конъюгат" в виде существительного означает модифицированный пептид, то есть пептид с группой, связанной с ним для модификации свойств указанного пептида. В виде глагола термин "конъюгировать" означает процесс связывания группы с пептидом для модификации свойств указанного пептида.
Термин "пролекарство", как его используют здесь, означает соединение, которое не обладает или не обязательно обладает терапевтической активностью, но которое после введения превращается в терапевтически активное соединение посредством реакции, происходящей в организме. Как правило, такие реакции представляют собой гидролиз, например, посредством эстераз или окисления. Примеры пролекарств включают биологически гидролизуемые амиды и биологически гидролизуемые эфиры, а также охватывают а) соединения, в которых биологически гидролизуемая функциональная группа в таком пролекарстве включена в соединение согласно настоящему изобретению, и б) соединения, которые могут окисляться или восстанавливаться биологически при данной функциональной группе с образованием лекарственных веществ согласно настоящему изобретению. Примеры этих функциональных групп включают 1,4-дигидропиридин, N-алкилкарбонил-1,4-дигидропиридин, 1,4-циклогексадиен, трет-бутил и тому подобное.
В данном описании термин "биологически гидролизуемый эфир" означает эфир лекарственного вещества (в данном случае соединение по изобретению), который либо а) не препятствует биологической активности исходного вещества, но придает этому веществу преимущественные свойства in vivo, такие как продолжительность действия, начало действия и тому подобное, либо б) является биологически неактивным, но легко превращается in vivo субъектом в биологически активное действующее вещество. Преимущество состоит, например, в повышенной растворимости или в том, что биологически гидролизуемый эфир после перорального введения всасывается из пищеварительного тракта и превращается в соединение согласно настоящему изобретению в плазме. Множество таких примеров известно в данной области техники и включает, например, низшие алкиловые эфиры (например, C1-C4), низшие ацилоксиалкиловые эфиры, низшие алкоксиацилоксиалкиловые эфиры, алкоксиацилоксиэфиры, алкилациламиноалкиловые эфиры и холиновые эфиры.
В данном описании термин "биологически гидролизуемый амид" означает амид лекарственного вещества (в данном случае соединение по изобретению), который либо а) не препятствует биологической активности исходного вещества, но придает этому веществу преимущественные свойства in vivo, такие как продолжительность действия, начало действия и тому подобное, либо б) является биологически неактивным, но легко превращается in vivo субъектом в биологически активное действующее вещество. Преимущество состоит, например, в повышенной растворимости или в том, что биологически гидролизуемый амид после перорального введения всасывается из пищеварительного тракта и превращается в соединение согласно настоящему изобретению в плазме. Множество таких примеров известно в данной области техники и включает, например, низшие алкиламиды, амиды α-аминокислот, алкоксиациламиды и алкиламиноалкилкарбониламиды.
В настоящем контексте термин "фармацевтически приемлемая соль" означает соли, которые не являются вредными для пациента. Такие соли включают соли присоединения фармацевтически приемлемой кислоты, фармацевтически приемлемые соли металлов, соли аммония и алкилированного аммония. Соли присоединения кислоты включают соли как неорганических кислот, так и органических кислот. Репрезентативные примеры пригодных неорганических кислот включают соляную, бромистоводородную, йодистоводородную, фосфорную, серную, азотную кислоты и тому подобное. Репрезентативные примеры пригодных органических кислот включают муравьиную, уксусную, трихлоруксусную, трифторуксусную, пропионовую, бензойную, коричную, лимонную, фумаровую, гликолевую, молочную, малеиновую, яблочную, малоновую, миндальную, щавелевую, пикриновую, пировиноградную, салициловую, янтарную, метансульфоновую, этансульфоновую, винную, аскорбиновую, памовую, бисметиленсалициловую, этандисульфоновую, глюконовую, цитраконовую, аспарагиновую, стеариновую, пальмитиновую, ЭДТА, гликолевую, пара-аминобензойную, глутаминовую, бензолсульфоновую, пара-толуолсульфоновую кислоты и тому подобное. Дополнительные примеры фармацевтически приемлемых солей присоединения неорганической или органической кислоты включают фармацевтически приемлемые соли, перечисленные в J. Pharm. Sci. 1977, 66, 2, который включен в данное описание посредством ссылки. Примеры солей металлов включают соли лития, натрия, калия, магния и тому подобное. Примеры солей аммония и алкилированного аммония включают соли аммония, метиламмония, диметиламмония, триметиламмония, этиламмония, гидроксиэтиламмония, диэтиламмония, бутиламмония, тетраметиламмония и тому подобное.
Термин "терапевтически эффективное количество" соединения означает количество, достаточное для лечения, облегчения или частичного прекращения клинических проявлений данного заболевания и его осложнений. Количество, достаточное для осуществления этого, определяют как "терапевтически эффективное количество". Эффективные количества для каждой цели будут зависеть как от тяжести заболевания или повреждения, так и от массы и общего состояния субъекта. Должно быть понятно, что определение подходящей дозировки может быть достигнуто с использованием рутинных экспериментов путем построения матрицы значений и тестирования различных точек на этой матрице, что находится в пределах обычной компетенции практикующего врача или ветеринара.
Термины "лечение" и "лечить", как их используют в данном описании, означают оказание помощи и уход за пациентом для борьбы с состоянием, таким как заболевание или расстройство. В этот термин следует включать весь спектр терапий для данного состояния, которым страдает пациент, таких как введение активного соединения, для облегчения симптомов или осложнений, для замедления прогрессирования заболевания, расстройства или состояния, для облегчения или ослабления симптомов и осложнений и/или для лечения или элиминации заболевания, расстройства или состояния, а также для предупреждения этого состояния, где предупреждение следует понимать как оказание помощи и уход за пациентом для борьбы с заболеванием, состоянием или расстройством и включает введение активных соединений для предупреждения появления симптомов или осложнений. Пациент, подлежащий лечению, предпочтительно представляет собой млекопитающее, в частности человека, но также может включать животных, таких как собаки, кошки, коровы, овцы и свиньи.
Раскрытие изобретения
Трансглутаминаза (Е.С.2.3.2.13), также известная как белок - глутамин-γ-глутамилтрансфераза, катализирует общую реакцию

В одном варианте осуществления изобретения Q-C(O)-NH2 (акцептор амина) представляет собой глутаминсодержащий пептид и Q′-NH2 (донор амина) представляет собой первое соединение, как указано выше, либо Q-С(O)-NH2 представляет собой первое соединение, как указано выше, и Q′-NH2 тогда представляет собой лизинсодержащий пептид. В конкретном варианте осуществления изобретения, однако, Q-C(O)-NH2 представляет собой глутаминсодержащий пептид и Q′-NH2 представляет собой первое соединение, как указано выше.
Общий донор амина in vivo представляет собой лизин, связанный пептидной связью, и тогда приведенная выше реакция дает образование поперечных связей пептидов. Фактор свертывания крови фактор XIII представляет собой трансглутаминазу, которая осуществляет свертывание крови при повреждениях. Различные трансглутаминазы отличаются друг от друга, например, тем, что аминокислотные остатки вокруг Gln требуются этому белку в качестве субстрата, то есть различные трансглутаминазы будут иметь различные Gln-содержащие пептиды в качестве субстратов в зависимости от того, какие аминокислотные остатки являются соседними с остатком Gln. Данный аспект может быть использован, если пептид, подлежащий модификации, содержит более чем один остаток Gln. Если желательно избирательно конъюгировать пептид только при некоторых из присутствующих остатков Gln, эта избирательность может быть получена путем отбора трансглутаминазы, которая принимает только релевантный(е) остаток(ки) Gln в качестве субстрата. Альтернативно один или более чем один аминокислотный остаток, близкий к Gln, может быть изменен, например, методами генной инженерии, в сторону модификации активности данной трансглутаминазы в отношении указанного остатка Gln.
Известно, что, является ли соединение субстратом для данного фермента, в принципе зависит от условий реакции, например временных рамок. При достаточном времени многие соединения, обычно не рассматриваемые в качестве субстратов, в действительности являются субстратами. Когда выше указано, что для данной трансглутаминазы некоторые остатки Gln могут являться субстратами, тогда как другие не являются, это должно указывать на то, что "другие не являются" до той степени, где желаемая избирательность все же может быть достигнута. Если один или более чем один остаток Gln, для которого желательно, чтобы он остался не конъюгированным, в действительности является субстратом для трансглутаминазы, однако, только если он находится в контакте с трансглутаминазой в течение продолжительного периода времени, избирательность может быть достигнута путем удаления или инактивации трансглутаминазы спустя подходящее время.
Примеры полезных трансглутаминаз включают микробные трансглутаминазы, такие как, например, из Streptomyces mobaraense, Streptomyces cinnamoneum и Streptomyces griseocarneum (все раскрыты в US 5156956, который включен в данное описание посредством ссылки) и Streptomyces lavendulae (раскрыта в US 5252469, который включен в данное описание посредством ссылки), а также Streptomyces ladakanum (JP2003199569, который включен в данное описание посредством ссылки). Следует отметить, что члены вышеуказанного рода Streptoverticillium в настоящее время включены в род Streptomyces [Kaempfer, J. Gen. Microbiol., 137, 1831-1892, 1991]. Другие полезные микробные трансглутаминазы были выделены из Bacillus subtilis (раскрыты в US 5731183, который включен в данное описание посредством ссылки) и из различных Myxomycetes. Другими примерами полезных микробных трансглутаминаз являются те, которые раскрыты в WO 96/06931 (например, трансглутаминаза из Bacilus lydicus) и WO 96/22366, обе из которых включены в данное описание посредством ссылки. Полезные не микробные трансглутаминазы включают трансглутаминазу печени морской свинки и трансглутаминазу из различных морских источников, таких как камбала Pagrus major (раскрыта в ЕР-0555649, которая включена в данное описание посредством ссылки), и японская устрица Crassostrea gigas (раскрыта в US 5736356, который включен в данное описание посредством ссылки).
В одном варианте осуществления изобретения Q′-NH2, то есть первое соединение, как указано выше, представляет собой азотсодержащий нуклеофил, где нуклеофил понимают как основное, богатое электронами соединение, которое имеет тенденцию атаковать ядро атома углерода. Азотсодержащий нуклеофил может представлять собой, например, амин или оксипроизводное амина.
В одном варианте осуществления изобретения изобретение относится к способу конъюгации пептидов, где пептид, содержащий остаток Gln, представленный формулой
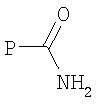
подвергают взаимодействию в одну или более чем одну стадию с азотсодержащим нуклеофильным соединением (первым соединением), представленным формулой
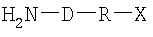
в присутствии трансглутаминазы с образованием трансаминированного пептида формулы
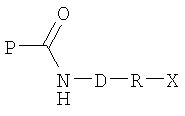
затем, при желании, указанную скрытую функциональную группу в Х активируют,
полученный трансаминированный пептид подвергают дальнейшему взаимодействию со вторым соединением формулы
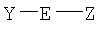
с образованием конъюгированного пептида формулы
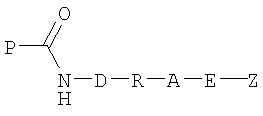
где D представляет собой связь или кислород;
R представляет собой линкер или связь;
Х представляет собой радикал, содержащий одну или более чем одну функциональную группу или скрытую функциональную группу, недоступную в аминокислотных остатках, составляющих пептид P-C(O)-NH2;
Y представляет собой радикал, содержащий одну или более чем одну функциональную группу, причем эти группы взаимодействуют с функциональными группами, присутствующими в X, и не взаимодействуют с функциональными группами, доступными в пептиде Р-С(O)-NH2;
Е представляет собой линкер или связь;
А представляет собой группу, образованную путем взаимодействия между парой функциональных групп, содержащихся в Х и Y, и
Z представляет собой группу, которую нужно конъюгировать с пептидом.
После конъюгации конъюгированный пептид можно выделить и очистить с помощью методик, хорошо известных в данной области техники. Конъюгированный пептид можно также превратить в фармацевтически приемлемую соль или пролекарство, если необходимо.
В частности, указанный способ может также включать стадию, где препарат полученного в результате конъюгированного пептида готовят в виде фармацевтической композиции.
Группа А, образованная при взаимодействии между функциональными группами Х и Y, может в принципе иметь любой вид в зависимости от того, какие свойства конечного конъюгированного пептида желательны. В некоторых ситуациях может быть желательным иметь лабильную связь, которую можно расщепить на какой-либо более поздней стадии, например, под действием какого-либо фермента или путем фотолиза. В некоторых ситуациях может быть желательным иметь стабильную связь, так чтобы получить стабильный конъюгированный пептид. Конкретно упомянуты типы групп, образованных в результате взаимодействий между производными амина и карбонильными группами, такие как оксим-, гидразон-, фенилгидразон- и семикарбазоновые группы.
В одном варианте осуществления изобретения функциональные группы Х и Y выбраны среди карбонильных групп, таких как кето- и альдегидные группы, и аминопроизводных, таких как
Должно быть понятно, что, если функциональная группа, содержащаяся в X, представляет собой карбонильную группу, то функциональная группа, содержащаяся в Y, представляет собой производное амина, и наоборот. Считают, что благодаря наличию групп -NH2 в большинстве пептидов лучшая избирательность получается, если Х содержит кето- или альдегидную функциональную группу.
Другим примером подходящей пары функциональных групп, присутствующих в Х и Y, являются производные азида (-N3) и алкины, которые взаимодействуют с образованием триазольной группы. Еще одним другим примером подходящей пары является алкин и нитрилоксид, которые взаимодействуют с образованием изооксазолидиновой группы.
Должно быть понятно, что функциональная группа, содержащаяся в X, может быть скрытой в том смысле, что ее нужно активировать перед взаимодействием с Y-E-Z. Например, Х может содержать группу, которая при взаимодействии с подходящим реагентом превращается в альдегид или кетон. Примеры таких групп включают
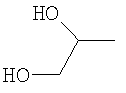
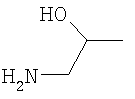
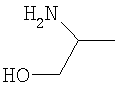
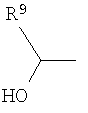
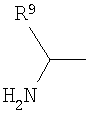
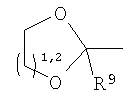
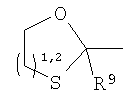
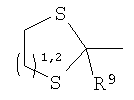
где R9 представляет собой Н, C1-6алкил, арил или гетероарил. Конкретные примеры включают метил, этил и пропил. Указанные группы можно превращать в альдегид или кетон путем окисления подходящим агентом, таким как, например, периодат, или путем гидролиза водной кислотой, возможно в присутствии катализатора, такого как соли меди, серебра или ртути.
В частности, соединение формулы (первое соединение),
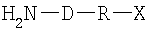
может быть выбрано из 4-(аминометил)фенилэтанона, 4-(2-аминоэтил)фенилэтанона, N-(4-ацетилфенил)-2-аминоацетамида, 1-[4-(2-аминоэтокси)фенил]этанона, 1-[3-(2-аминоэтокси)фенил]этанона, 1,4-бис(аминокси)бутана, 3-оксапентан-1,5-диоксиамина, 1,8-диаминокси-3,6-диоксаоктана, 1,3-бис(аминокси)пропан-2-ола, 1,11-бис(аминокси)-3,6,9-триоксаундекана, 1,3-диамино-2-пропанола, 1,2-бис(аминокси)этана и 1,3-бис(аминокси)пропана.
Как соединение для трансаминирования (первое соединение), так и соединение для взаимодействия с трансаминированным пептидом (второе соединение) содержит линкер, R и Е, соответственно. Эти линкеры, которые являются независимыми друг от друга, могут отсутствовать или могут быть выбраны среди бирадикалов алкана, алкена или алкина и бирадикалов гетероалкана, гетероалкена и гетероалкина, где один или более чем один возможно замещенный ароматический гомоциклический бирадикал или бирадикал гетероциклического соединения, например бирадикал фенилена или пиперидина, может быть встроен между вышеупомянутыми бирадикалами. Должно быть понятно, что указанные линкеры могут также содержать заместители, выбранные из гидроксила, галогена, нитро, циано, карбоксила, арила, алкила и гетероарила.
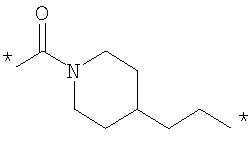
Как Е, так и R представляют собой связи или линкеры, и в настоящем контексте термин "линкер" означает группу, функционирующую как средство для отделения Y от Z и Х от NH2-D- соответственно. Одной из функций линкеров Е и R может быть обеспечение адекватной подвижности в связи между пептидом и конъюгированной группировкой Z. Типичные примеры Е и R включают нормальный, разветвленный и/или циклический С1-10алкилен, С2-10алкенилен, С2-10алкинилен, С2-10гетероалкилен, С2-10гетероалкенилен, С2-10гетероалкинилен, где может быть встроен один или более чем один гомоциклический бирадикал ароматического соединения или бирадикал гетероциклического соединения. Конкретные примеры Е и R включают
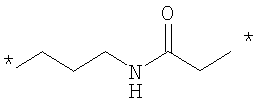 ,
,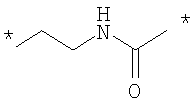 ,
,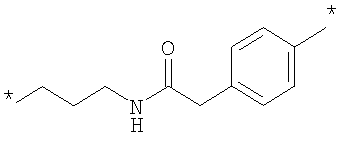 ,
,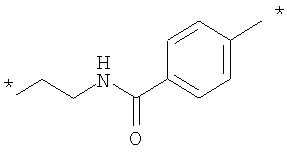 ,
,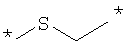 ,
,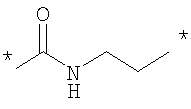 ,
,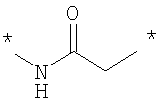 ,
,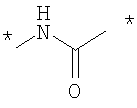 ,
,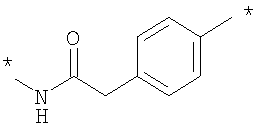 ,
,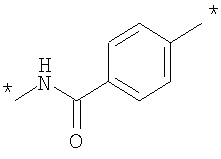 ,
,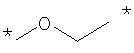 ,
,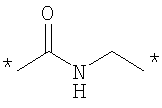 ,
,

 ,
,  ,
,
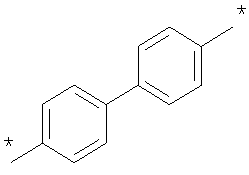 ,
,
где * означает точки присоединения.
Необходимость в модификации пептидов может возникнуть по целому ряду причин, что также отражено в тех видах соединений, которые могут быть конъюгированы с пептидами согласно способам согласно настоящему изобретению. Конъюгировать пептиды может быть желательно, чтобы изменить физико-химические свойства пептида, как, например, чтобы повысить (или снизить) растворимость, чтобы модифицировать биологическую доступность терапевтических пептидов. В другом варианте осуществления изобретения может быть желательно модифицировать клиренс (скорость очищения организма) путем конъюгации с пептидом соединений, которые связываются с белками плазмы, такими как, например, альбумин, или которые увеличивают размер пептида для предотвращения или замедления выделения через почки. Конъюгация может также изменить и, в частности, уменьшить чувствительность пептида к гидролизу, такому как, например, протеолиз in vivo. В другом варианте осуществления изобретения может быть желательно конъюгировать метку, чтобы облегчить анализ пептида. Примеры такой метки включают радиоактивные изотопы, флуоресцентные маркеры и субстраты ферментов. Еще в одном варианте осуществления изобретения соединение конъюгируют с пептидом для облегчения выделения этого пептида. Например, соединение со специфичным аффинитетом к конкретному материалу колонки можно конъюгировать с пептидом. Может быть также желательно модифицировать иммуногенность пептида, например, путем конъюгации пептида таким образом, чтобы скрыть, замаскировать или заслонить один или более чем один иммуногенный эпитоп при этом пептиде.
В одном варианте осуществления изобретения предложен способ улучшения фармакологических свойств пептидов. Это улучшение представляет собой улучшение относительно соответствующего не конъюгированного пептида. Примеры таких фармакологических свойств включают полупериод существования in vivo, иммуногенность, почечную фильтрацию, защиту от протеаз и связывание альбумина.
Термин “полупериод существования in vivo” используют в его обычном значении, то есть периода времени, за который 50% биологической активности пептида или конъюгированного пептида еще присутствует в организме/органе-мишени, или период времени, за который активность пептида или конъюгированного пептида составляет 50% от ее исходного значения. Как альтернативу определения полупериода существования in vivo можно определить “период полувыведения из плазмы in vivo”, то есть период времени, за который 50% пептида или пептидного конъюгата циркулирует в плазме или кровотоке до клиренса. Определение периода полувыведения из плазмы часто является более простым, чем определение полупериода существования, и величина периода полувыведения из плазмы часто является хорошим показателем величины полупериода существования in vivo. Термины, альтернативные периоду полувыведения из плазмы, включают период полувыведения из сыворотки, полупериод циркуляции, период полувыведения из кровообращения, клиренс из сыворотки, клиренс из плазмы и полупериод клиренса.
Термин "повышенный", в связи с полупериодом существования in vivo или периодом полувыведения из плазмы, используют для обозначения того, что релевантный период полувыведения пептидного конъюгата статистически значимо повышен относительно этого периода не конъюгированного (исходного) пептида, как определено в сравнимых условиях. Например, релевантный период полувыведения может быть повышен по меньшей мере примерно на 25%, как, например, по меньшей мере на 50%, например, по меньшей мере на 100%, 150%, 200%, 250% или 500%. В одном варианте осуществления изобретения соединения согласно настоящему изобретению проявляют повышение периода полувыведения по меньшей мере примерно на 5 ч, предпочтительно по меньшей мере примерно на 24 ч, более предпочтительно по меньшей мере примерно на 72 ч и наиболее предпочтительно по меньшей мере примерно на 7 суток по сравнению с периодом полувыведения исходного пептида.
Измерение периода полувыведения из плазмы in vivo можно осуществить с помощью целого ряда способов, описанных в литературе. Повышение периода полувыведения из плазмы in vivo можно определить количественно как снижение клиренса (CL) или как повышение среднего времени существования (mean residence time, MRT). Конъюгированные пептиды согласно настоящему изобретению, для которых CL снижен до значения менее чем 70%, как, например, менее чем 50%, как, например, менее чем 20%, как, например, менее чем 10% от CL исходного пептида, как определено в подходящем анализе, считают обладающими повышенным периодом полувыведения из плазмы in vivo. Конъюгированные пептиды согласно настоящему изобретению, для которых MRT повышен до значения более чем 130%, как, например, более чем 150%, как, например, более чем 200%, как, например, более чем 500% от MRT исходного пептида в подходящем анализе, считают обладающими повышенным периодом полувыведения из плазмы in vivo. Клиренс и среднее время существования можно оценить в стандартных фармакокинетических исследованиях, используя подходящих подопытных животных. В пределах компетенции специалиста в данной области техники находится выбор подходящего подопытного животного для данного белка. Испытания на человеке, конечно, являются последним тестом. Как правило и в качестве примера, мышам, крысам, собакам, обезьянам или свиньям инъецируют интересующее соединение. Инъецируемое количество зависит от подопытного животного. Затем берут образцы крови в течение периода от одних до пяти суток, как пригодно для оценки CL и MRT. Эти образцы крови удобно анализировать с помощью методик ELISA (твердофазного иммуноферментного анализа).
Термин "иммуногенность" соединения относится к способности соединения, когда его вводят человеку, вызывать вредный иммунный ответ, либо гуморальный, либо клеточный, либо оба. В любой группе населения могут существовать индивидуумы, которые проявляют чувствительность к конкретным вводимым белкам. Иммуногенность можно измерить путем количественного определения присутствия антител к гормону роста и/или реактивных к гормону роста Т-клеток у чувствительного индивидуума, используя общепринятые способы, известные в данной области техники. В одном варианте осуществления изобретения конъюгированный пептид согласно настоящему изобретению проявляет снижение иммуногенности у чувствительного индивидуума по меньшей мере примерно 10%, предпочтительно по меньшей мере примерно 25%, более предпочтительно по меньшей мере примерно 40% и наиболее предпочтительно по меньшей мере примерно 50% относительно иммуногенности исходного пептида для этого индивидуума.
Термин "защита от протеаз" или "защищенный от протеаз", как его используют здесь, означает, что конъюгированный пептид согласно настоящему изобретению является более устойчивым к пептидазе или к протеазам плазмы, чем исходный пептид. Известно, что ферменты протеазы и пептидазы, присутствующие в плазме, вовлечены в расщепление циркулирующих белков.
Устойчивость белка к расщеплению, например, дипептидиламинопептидазы IV (DPPIV) определяют путем приведенного ниже анализа расщепления. Аликвоты белка (5 нмоль) инкубируют при 37°С с 1 мкл очищенной дипептидиламинопептидазы IV, что соответствует ферментативной активности 5 mU, в течение 10-180 минут в 100 мкл буфера 0,1 М триэтиламин-HCl, pH 7,4. Ферментативные реакции останавливают добавлением 5 мкл 10% трифторуксусной кислоты, продукты расщепления белка разделяют и определяют количественно, используя анализ ВЭЖХ. Один из способов проведения этого анализа: смеси наносят на колонку с широкими порами Vydac C18 (поры 30 нм, частицы 5 мкм) 250×4,6 мм и элюируют при скорости тока 1 мл/мин линейными ступенчатыми градиентами ацетонитрила в 0,1% трифторуксусной кислоте (0% ацетонитрил в течение 3 мин, 0-24% ацетонитрил в течение 17 мин, 24-48% ацетонитрил в течение 1 мин) согласно Siegel et al., Regul. Pept. 1999; 79:93-102, и Mentlein et al. Eur. J. Biochem. 1993; 214: 829-35. Мониторинг белков и продуктов их расщепления можно проводить на основании их поглощения при 220 нм (пептидные связи) или 280 нм (ароматические аминокислоты) и определять количественно путем интегрирования их пиковых областей относительно областей стандартов. Скорость гидролиза белка дипептидиламинопептидазой IV оценивают как периоды инкубации, в результате которых гидролизуется менее чем 10% пептида. В одном варианте осуществления изобретения скорость гидролиза пептидного конъюгата составляет менее чем 70%, как, например, менее чем 40%, как, например, менее чем 10% скорости гидролиза исходного пептида.
Наиболее часто встречающимся белковым компонентом в циркулирующей крови млекопитающих является сывороточный альбумин, который в норме присутствует при концентрации примерно от 3 до 4,5 граммов на 100 миллилитров цельной крови. Сывороточный альбумин представляет собой белок крови с молекулярной массой примерно 70000 дальтон, который обладает несколькими важными функциями в системе кровообращения. Он функционирует в качестве переносчика ряда органических молекул, находящихся в крови, в качестве главного переносчика различных метаболитов, таких как жирные кислоты и билирубин, через кровь, а также, благодаря его обилию, в качестве осмотического регулятора циркулирующей крови. Сывороточный альбумин имеет период полувыведения более чем одну неделю, и один из подходов к повышению периода полувыведения белков из плазмы состоял в конъюгации с белком группы, которая связывается с сывороточным альбумином. Свойство связывания альбумина можно определить, как описано в статье J. Med. Chem, 43, 2000, 1986-1992, которая включена в данное описание посредством ссылки.
Конкретные примеры Z включают радикалы, содержащие одну или более чем одну метку, такую как флуоресцентные маркеры, такие как радикал флуоресцеина, радикал родамина, радикал Texas Red® и радикал белка фикобиллина; субстраты ферментов, такие как радикал пара-нитрофенолацетата, и радиоактивные изотопы, такие как Cu-64, Ga-67, Ga-68, Zr-89, Ru-97, Tc-99, Rh-105, Pd-109, In-111, I-123, I-125, I-131, Re-186, Re-188, Au-198, Pb-203, At-211, Pb-212 и Bi-212; органические молекулы, такие как радикалы ПЭГ или мПЭГ и их аминопроизводные (включая нормальные и разветвленные радикалы ПЭГ и мПЭГ); нормальный, разветвленный и/или циклический С1-22алкил, С2-22алкенил, С2-22алкинил, С1-22гетероалкил, С2-22гетероалкенил, С2-22гетероалкинил, где может быть встроен один или более чем один гомоциклический бирадикал ароматического соединения или бирадикал гетероциклического соединения и где указанные радикалы С1-С22 или С2-С22 могут быть возможно замещены одним или более чем одним заместителем, выбранным из гидроксила, галогена, карбоксила, гетероарила и арила, где указанный арил или гетероарил может быть возможно дополнительно замещен одним или более чем одним заместителем, выбранным из гидроксила, галогена и карбоксила; стероидные радикалы; липидные радикалы; полисахаридные радикалы, например декстраны; полиамидные радикалы, например, радикалы полиаминокислоты; радикалы ПВП; радикалы ПВА; поли(1,3-диоксалан); поли(1,3,6-триоксан); полимер этилена/малеинового ангидрида; красители типа цибакрона, такие как цибакрон синий (Cibacron Blue 3GA); полиамидные цепи определенной длины, как описано в WO 00/12587, которая включена в данное описание посредством ссылки; и гидроксиалкилкрахмал, такой как, например, гидроксиэтилкрахмал, такой, как описан в WO 03/074087 и WO 02/80979, обе из которых включены в данное описание посредством ссылки.
Конкретные примеры включают С10-20алкил, такой как C15 и C17, и, в частности, нормальный C15 и C17, а также производные бензофенона формулы
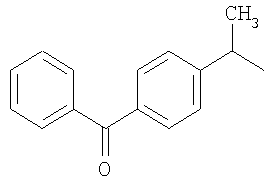
Конкретным примером является Z, содержащий радикал цибакронил, как показано ниже
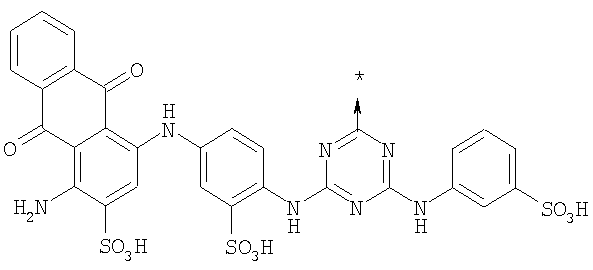
ПЭГ или мПЭГ, конъюгированные с пептидом согласно настоящему изобретению, могут иметь любую молекулярную массу. В частности, молекулярная масса может составлять между 500 и 1000000 Да, как, например, между 500 и 500000 Да, как, например, между 500 и 100000 Да, как, например, между 500 и 60000 Да, как, например, между 1000 и 40000 Да, как, например, между 5000 и 40000 Да. В частности, можно использовать ПЭГ с молекулярными массами между 10000 Да и 40000 Да, как, например, между 20000 Да и 40000 Да, как, например, между 20000 и 30000 Да или между 30000 и 40000 Да. Конкретно упомянуты ПЭГ или мПЭГ с молекулярной массой 10000, 20000, 30000 или 40000 Да.
Z может быть разветвленным и может содержать более чем одну из вышеупомянутых меток или радикалов. Например, мПЭГ40К, как правило, получают в виде разветвленного мПЭГ с двумя плечами, каждое из которых содержит МПЭГ20К.
В одном варианте осуществления изобретения Z содержит одну или более чем одну группу, которая, как известно, связывается с белками плазмы, такими как, например, альбумин. Способность соединения к связыванию с альбумином можно определить, как описано в статье J. Med. Chem, 43, 2000, 1986-1992, которая включена в данное описание посредством ссылки. В данном контексте соединение определяют как связывающееся с альбумином, если Ru/Da выше 0,05, как, например, выше 0,10, как, например, выше 0,12 или даже выше 0,15.
В другом варианте осуществления изобретения группа, связывающая альбумин, представляет собой пептид, такой как пептид, содержащий менее 40 аминокислотных остатков. Ряд малых пептидов, которые являются связывающими альбумин фрагментами, раскрыт в статье J. Biol. Chem. 277, 38 (2002) 35035-35043, которая включена в данное описание посредством ссылки.
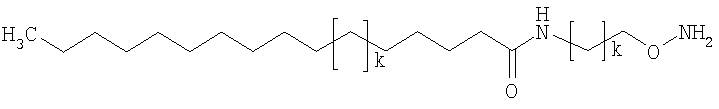
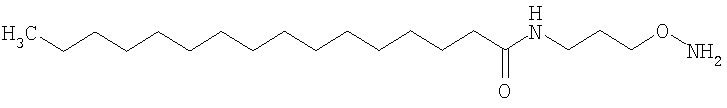
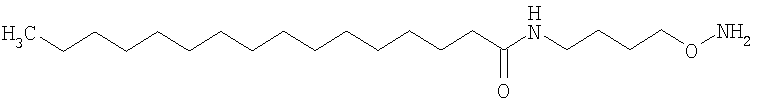
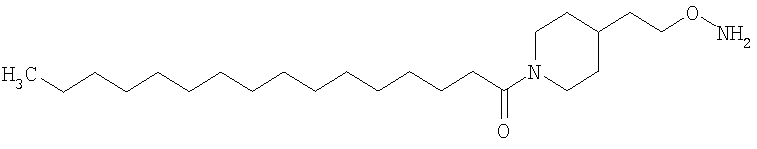
Конкретные примеры соединений формулы Y-E-Z включают
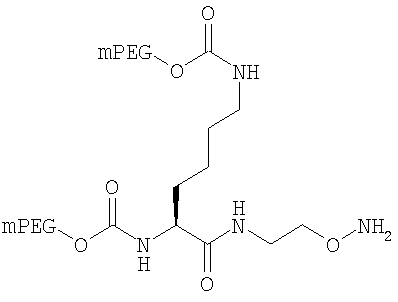 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
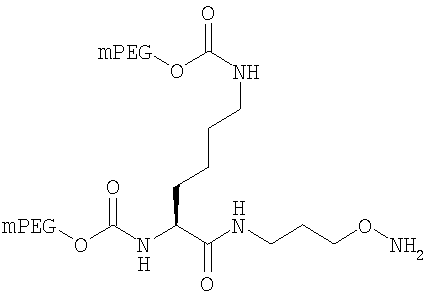 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
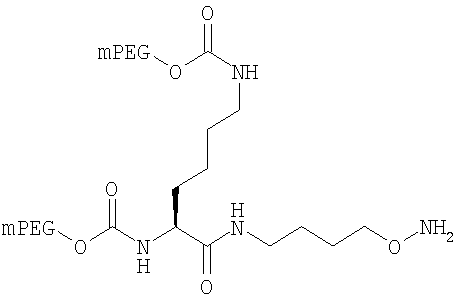 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
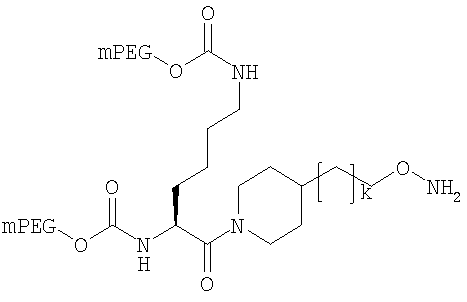 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
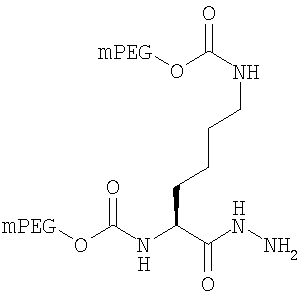 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
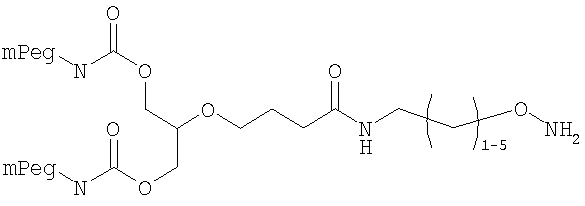 ,
,
где мПЭГ имеет молекулярную массу 20 кДа или 30 кДа,
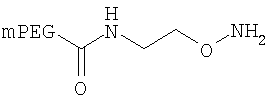 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
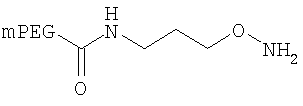 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
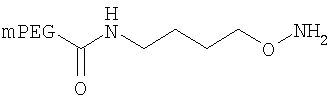 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
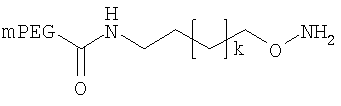 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
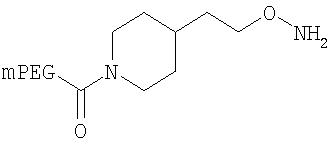 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
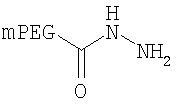 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
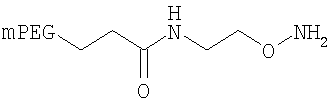 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
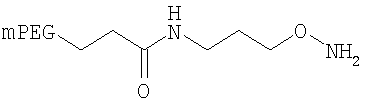 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
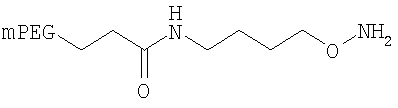 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
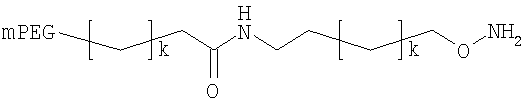 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
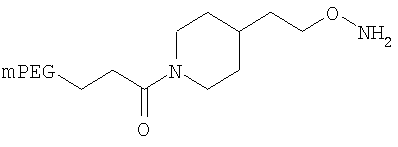 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
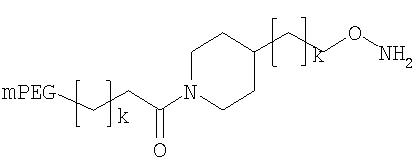 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
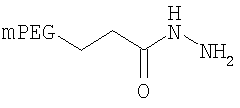 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
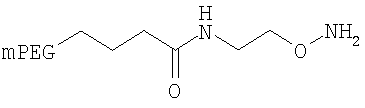 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
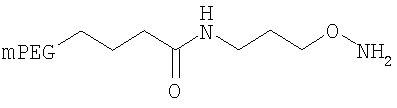 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
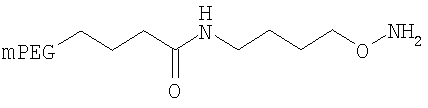 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
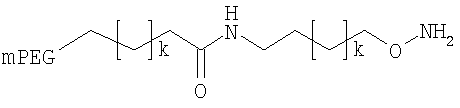
где мПЭГ имеет молекулярную массу 20 кДа,
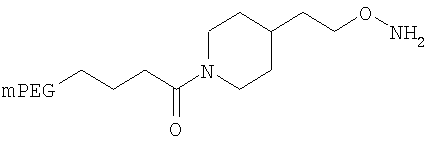 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
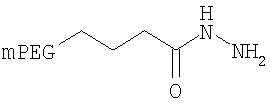 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
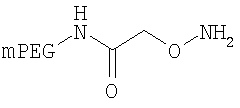 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
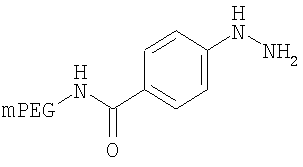 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
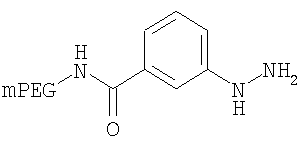 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
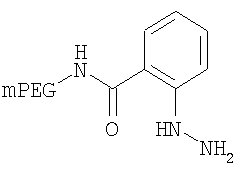
где мПЭГ имеет молекулярную массу 20 кДа,
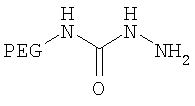 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
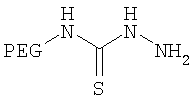 ,
,
где мПЭГ имеет молекулярную массу 20 кДа,
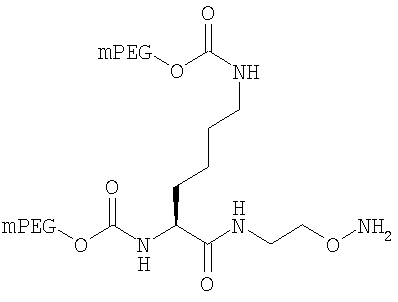 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
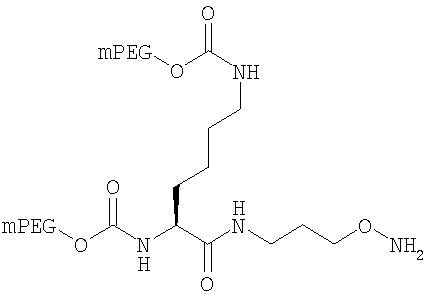 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
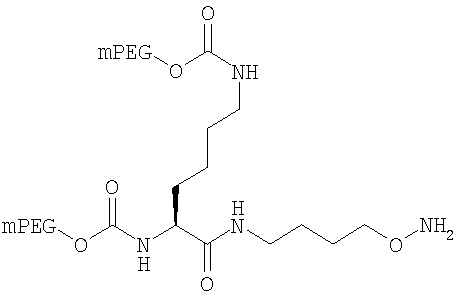 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
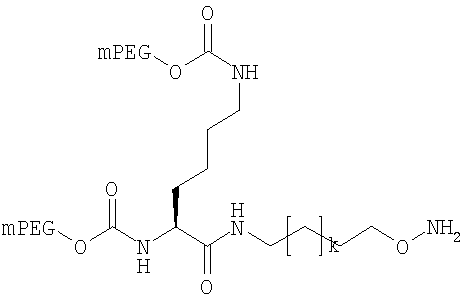
где мПЭГ имеет молекулярную массу 10 кДа,
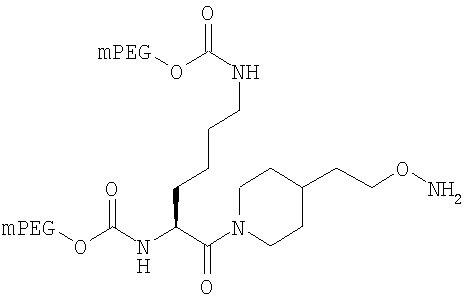 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
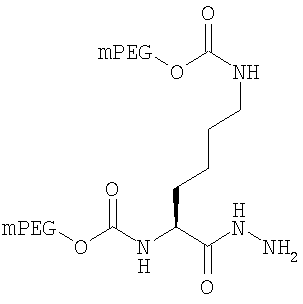 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
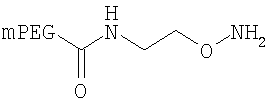 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
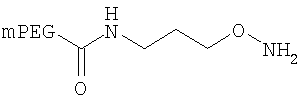 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
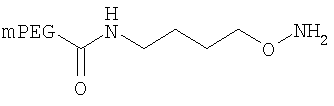 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
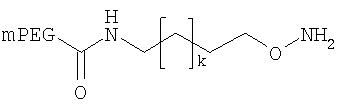 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
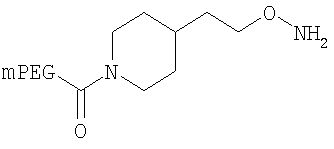 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
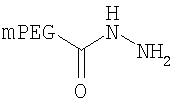 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
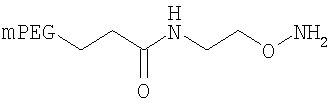 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
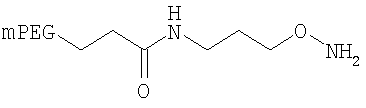 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
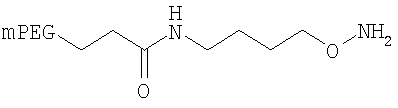 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
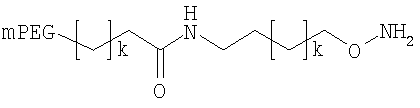 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
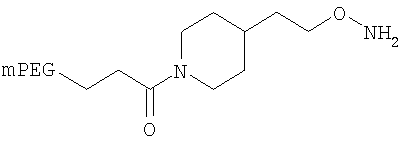 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
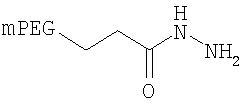 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
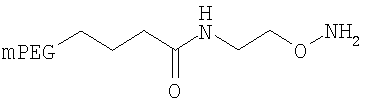 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
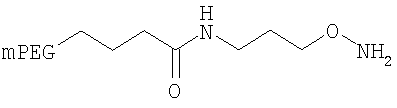 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
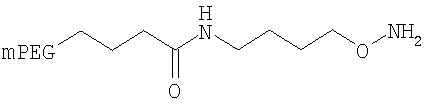 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
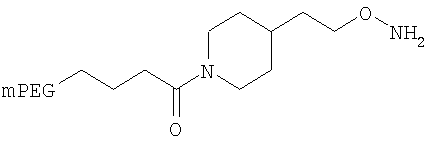 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
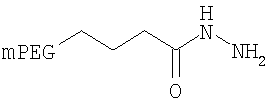 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
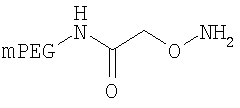 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
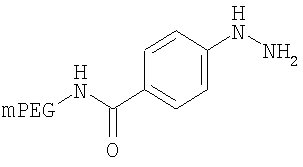 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
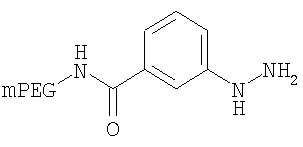 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
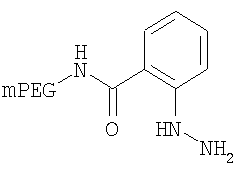 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
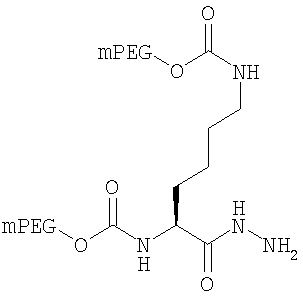 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
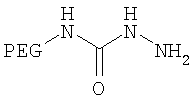 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
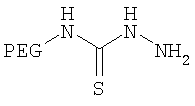 ,
,
где мПЭГ имеет молекулярную массу 10 кДа,
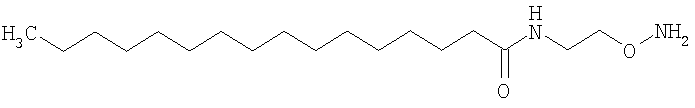 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
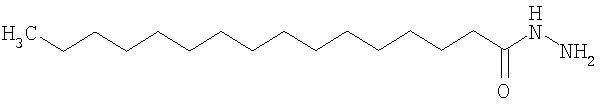 ,
,
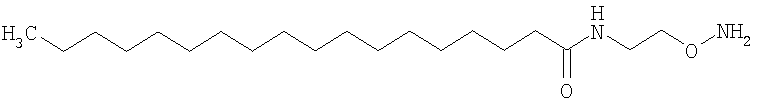 ,
,
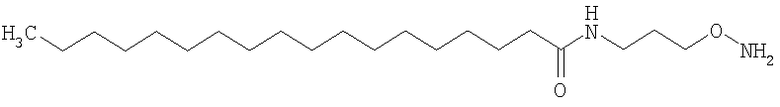 ,
,
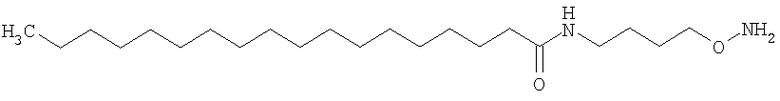 ,
,
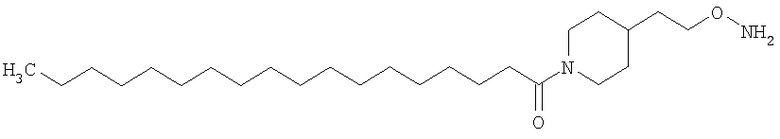
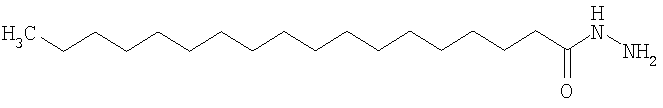 ,
,
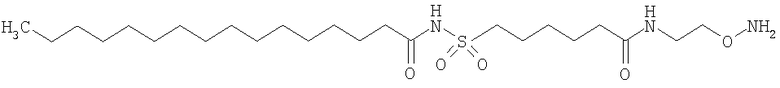
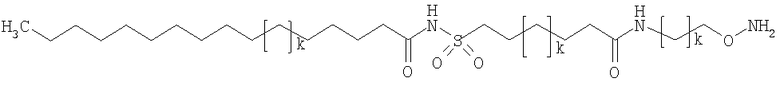 ,
,
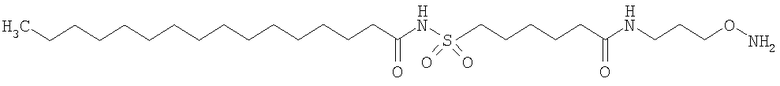
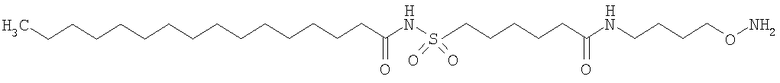 ,
,
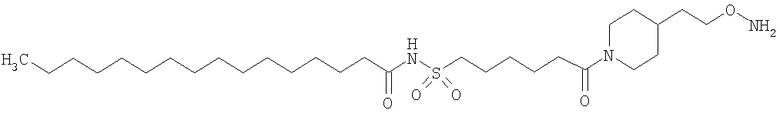 ,
,
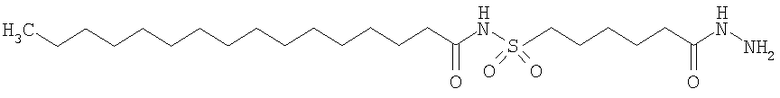 ,
,
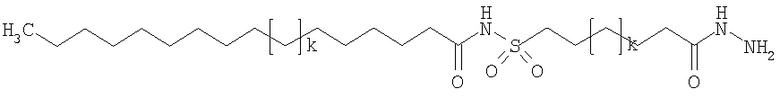 ,
,
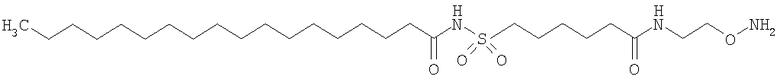 ,
,
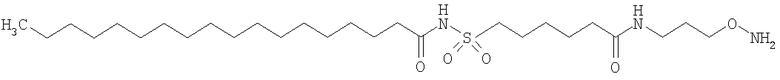
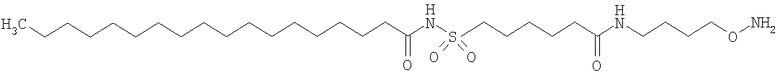 ,
,
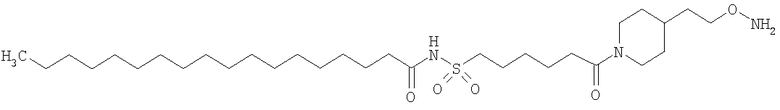
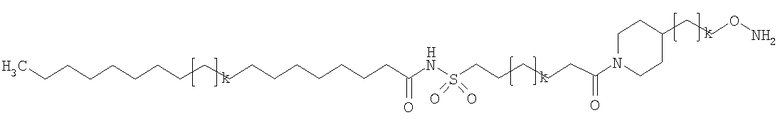
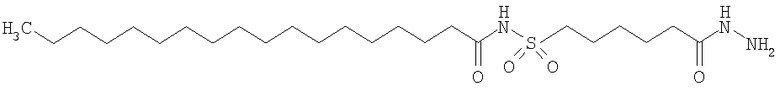
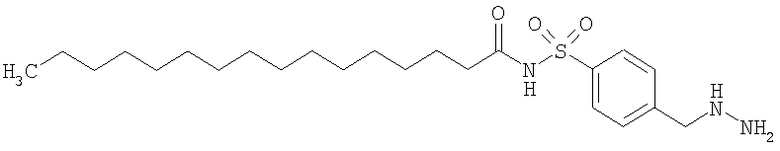 ,
,
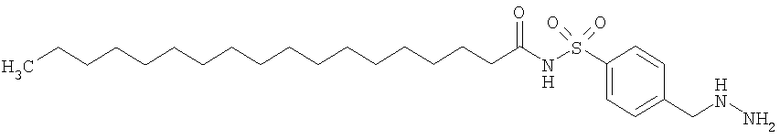 ,
,
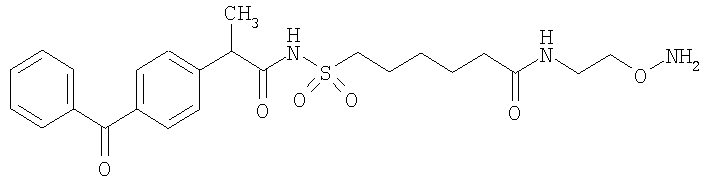 ,
,
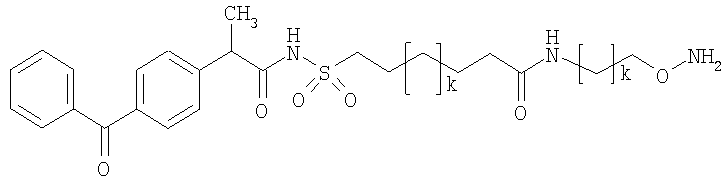 ,
,
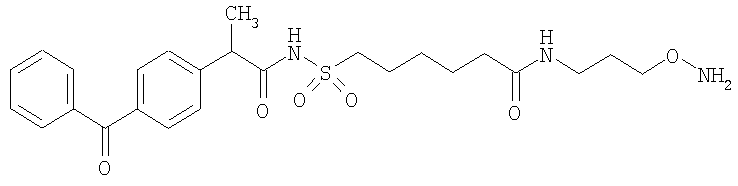 ,
,
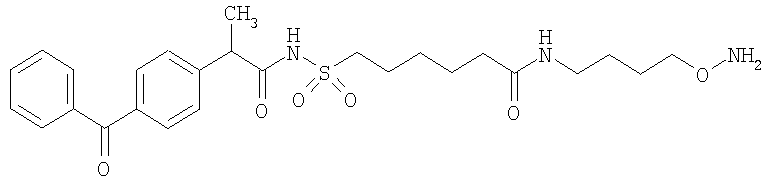 ,
,
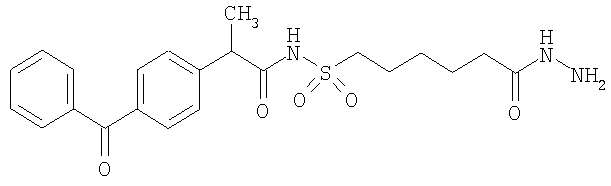 ,
,
где каждый k в приведенных выше формулах независимо представляет собой целое число от 0 до 5, то есть 0, 1, 2, 3, 4 или 5.
Как обсуждено в разделе "Предшествующий уровень техники", известна прямая конъюгация, например, функционализированных амином ПЭГ или жирных кислот с пептидами, содержащими Gln. Однако на основании примеров, раскрытых, например, в ЕР 950665, ЕР 785276, Sato, Adv. Drug Delivery Rev., 54, 459-476, 2002, и Wada, Biotech. Lett., 23, 1367-1372, 2001, ясно, что для прохождения этой реакции необходим значительный избыток (вплоть до 100-1000-кратного) соединения, которое нужно конъюгировать с пептидом. Такой избыток создает ограничение применимости этой реакции в техническом или большом масштабе. Например, мПЭГ с малым индексом полидисперсности является очень дорогостоящим, и требование к его большому избытку на практике запрещено. Кроме того, для конъюгации групп большого размера, таких как, например, ПЭГ 10 кДа или ПЭГ 20 кДа, избыток реагента порядка 100-1000-кратного неосуществим вследствие молекулярной массы таких соединений. Также хорошо известно, что при наличии больших количеств ПЭГ вероятно осаждение пептидов, то есть и пептида, который нужно конъюгировать, и трансглутаминазы. В противоположность этому настоящий двухстадийный способ дает преимущество в том, что реагент, который необходим на ферментативной стадии в большом избытке, представляет собой малую молекулу, которую легко использовать даже в большом избытке. При правильном выборе связи, которая должна образоваться на второй стадии, не требуется большого избытка, поскольку, например, образование оксима происходит при почти эквимолярных количествах функциональных амино- и кето-групп.
Дополнительным преимуществом является возможность получения пептидов, "готовых к конъюгации". Пептид можно подвергнуть взаимодействию с подходящим нуклеофилом (H2N-D-R-X) в присутствии трансглутаминазы с образованием функционализированного пептида. Указанный функционализированный пептид можно хранить, сколько необходимо, чтобы позже подвергать его взаимодействию с одним или более чем одним вторым соединением (Y-E-Z) с образованием различных по-разному конъюгированных пептидов. Это дает возможность использования одного функционализированного пептида для образования множества конъюгированных пептидов. Таким образом, можно избежать различных оптимизаций для подбора подходящих условий реакции.
Пептид должен представлять собой субстрат для трансглутаминазы в способах согласно настоящему изобретению. Следовательно, необходимо, чтобы этот пептид содержал остаток Gln или Lys, в частности остаток Gln. Если данный пептид не является субстратом для трансглутаминазы, возможно вставить один или более чем один остаток Gln или Lys, и, в частности, остатки Gln в пептидную последовательность, чтобы сделать этот пептид субстратом для трансглутаминазы. В принципе такой остаток Gln или Lys можно вставить в любое положение в последовательности, однако, предпочтительно вставлять его в том положении, где физиологическая, такая как, например, терапевтическая активность, этого пептида не подвергалась воздействию до той степени, при которой этот пептид более не будет полезным, например, при терапевтическом вмешательстве. Вставки аминокислотных остатков в пептиды можно осуществить с помощью стандартных методик, известных специалистам в данной области техники, таких как посттрансляционная химическая модификация или трансгенные методики.
Любые пептиды, которые являются субстратами для трансглутаминазы, можно конъюгировать способами согласно настоящему изобретению, такие как, например, ферменты, пептидные гормоны, факторы роста, антитела, цитокины, рецепторы, лимфокины и вакцинные антигены, и, в частности, следует упомянуть терапевтические пептиды, такие как инсулин, глюкагоноподобный пептид 1 (GLP-1), глюкагоноподобный пептид 2 (GLP-2), гормон роста, цитокины, пептидов трилистникого фактора (TFF - trefoil factor family, пептиды-модификаторы рецептора меланокортина и соединения фактора VII.
Конкретный приемлемый инсулин представляет собой человеческий инсулин. В настоящем контексте термин "человеческий инсулин" относится к продуцируемому в природе инсулину или инсулину, продуцируемому рекомбинантным путем. Рекомбинантный человеческий инсулин можно продуцировать в любой подходящей клетке-хозяине, например клетки-хозяева могут представлять собой бактериальные, грибные (включая дрожжевые), клетки насекомых, растительные или животные клетки. Множество соединений инсулина раскрыто в литературе, и они также являются особенно полезными в способах согласно настоящему изобретению. Под "соединением инсулина" (и родственными выражениями) понимают человеческий инсулин, в котором одна или более чем одна аминокислота делетирована и/или заменена другими аминокислотами, включая некодируемые аминокислоты, и/или человеческий инсулин, содержащий дополнительные аминокислоты, то есть более чем 51 аминокислоту, и/или человеческий инсулин, в котором по меньшей мере один органический заместитель связан с одной или более чем одной аминокислотой.
В приведенных ниже патентных документах раскрыты соединения инсулина, конкретно применимые в способах, предложенных настоящим изобретением.
В WO 97/31022 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина с пролонгированным профилем активности, в которых аминогруппа N-концевой аминокислоты В-цепи и/или ε-аминогруппа LysB29 имеет карбоновую кислоту, содержащую липофильный заместитель. Конкретно упомянуты NεB29-(CO-(CH2)14-COOH) человеческий инсулин; NεB29-(CO-(CH2)16-COOH) человеческий инсулин; NεB29-(CO-(CH2)18-СООН) человеческий инсулин; NεB29-(CO-(CH2)20-СООН) человеческий инсулин; NεB29-(СО-(CH2)22-СООН) человеческий инсулин; NεB29-(СО-(СН2)14-СООН)AspB28-человеческий инсулин; NεB29-(СО-(СН2)16-СООН)AspB28-человеческий инсулин; NεB29-(CO-(CH2)18-СООН)AspB28-человеческий инсулин; NεB29-(CO-(CH2)20-COOH)AspB28-человеческий инсулин; NεB29-(CO-(CH2)22-COOH)AspB28-человеческий инсулин; NεB30-(CO-(CH2)14-СООН)ThrB29LysB30-человеческий инсулин; NεB30-(CO-(CH2)16-COOH)ThrB29LysB30-человеческий инсулин; NεB30-(CO-(CH2)18-COOH)ThrB29LysB30-человеческий инсулин; NεB30-(CO-(СН2)20-СООН)ThrB29LysB30-человеческий инсулин; NεB30-(CO-(CH2)22-COOH)ThrB29LysB30-человеческий инсулин; NεB28-(CO-(CH2)14-СООН)LysB28ProB29-человеческий инсулин; NεB28-(CO-(CH2)16-COOH)LysB28ProB29-человеческий инсулин; NεB28-(CO-(CH2)18-COOH)LysB28ProB29-человеческий инсулин; NεB28-(CO-(CH2)20-СООН)LysB28ProB29-человеческий инсулин; NεB28-(CO-(CH2)22-COOH)LysB28ProB29-человеческий инсулин; NεB29-(CO-(CH2)14-COOH)дезВ30 человеческий инсулин; NεB29-(СО-(СН2)16-СООН)дезВ30 человеческий инсулин; NεB29-(CO-(CH2)18-COOH)дезВ30 человеческий инсулин; NεB29-(CO-(CH2)20-COOH)дезВ30 человеческий инсулин и NεB29-(CO-(CH2)22COOH)дезВ30 человеческий инсулин.
В WO 96/29344 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина с пролонгированным профилем активности, в которых либо к аминогруппе N-концевой аминокислоты В-цепи присоединен липофильный заместитель, содержащий от 12 до 40 атомов углерода, либо в которых к группе карбоновой кислоты С-концевой аминокислоты В-цепи присоединен липофильный заместитель, содержащий от 12 до 40 атомов углерода.
В WO 95/07931 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина с пролонгированным профилем активности, в которых ε-аминогруппа LysB29 имеет липофильный заместитель. Конкретно упомянуты NεB29-тридеканоил дез(В30) человеческий инсулин, NεB29-тетрадеканоил дез(В30) человеческий инсулин, NεB29-деканоил дез(В30) человеческий инсулин, NεB29-додеканоил дез(В30) человеческий инсулин, NεB29-тридеканоил GlyA21 дез(В30) человеческий инсулин, NεB29-тетрадеканоил GlyA21 дез(В30) человеческий инсулин, NεB29-деканоил GlyA21 дез(В30) человеческий инсулин, NεB29-додеканоил GlyA21 дез(В30) человеческий инсулин, NεB29-тридеканоил GlyA21 GlnB3 дез(В30) человеческий инсулин, NεB29-тетрадеканоил GlyA21 GlnB3 дез(В30) человеческий инсулин, NεB29-деканоил GlyA21 GlnB3 дез(В30) человеческий инсулин, NεB29-додеканоил GlyA21 GlnB3 дез(В30) человеческий инсулин, NεB29-тридеканоил AlaA21 дез(В30) человеческий инсулин, NεB29-тетрадеканоил AlaA21 дез(В30) человеческий инсулин, NεB29-деканоил AlaA21 дез(В30) человеческий инсулин, NεB29-додеканоил AlaA21 дез(В30) человеческий инсулин, NεB29-тридеканоил AlaA21 GlnB3 дез(В30) человеческий инсулин, NεB29-тетрадеканоил AlaA21 GlnB3 дез(В30) человеческий инсулин, NεB29-деканоил AlaA21 GlnВ3 дез(В30) человеческий инсулин, NεB29-додеканоил AlaA21 GlnB3 дез(В30) человеческий инсулин, NεB29-тридеканоил GlnB3 дез(В30) человеческий инсулин, NεB29-тетрадеканоил GlnB3 дез(В30) человеческий инсулин, NεB29-деканоил GlnB3 дез(В30) человеческий инсулин, NεB29-додеканоил GlnB3 дез(В30) человеческий инсулин, NεB29-тридеканоил GlyA21 человеческий инсулин, NεB29-тетрадеканоил GlyA21 человеческий инсулин, NεB29-деканоил GlyA21 человеческий инсулин, NεB29-додеканоил GlyA21 человеческий инсулин, NεB29-тридеканоил GlyA21 GlnB3 человеческий инсулин, NεB29-тетрадеканоил GlyA21 GlnB3 человеческий инсулин, NεB29-деканоил GlyA21 GlnB3 человеческий инсулин, NεB29-додеканоил GlyA21 GlnB3 человеческий инсулин, NεB29-тридеканоил AlaA21 человеческий инсулин, NεB29-тетрадеканоил AlaA21 человеческий инсулин, NεB29-деканоил AlaA21 человеческий инсулин, NεB29-додеканоил AlaA21 человеческий инсулин, NεB29-тридеканоил AlaA21 GlnB3 человеческий инсулин, NεB29-тетрадеканоил AlaA21 GlnB3 человеческий инсулин, NεB29-деканоил AlaA21 GlnB3 человеческий инсулин, NεB29-додеканоил AlaA21 GlnB3 человеческий инсулин, NεB29-тридеканоил GlnB3 человеческий инсулин, NεB29-тетрадеканоил GlnB3 человеческий инсулин, NεB29-деканоил GlnB3 человеческий инсулин, NεB29-додеканоил GlnB3 человеческий инсулин, NεB29-тридеканоил GluB30 человеческий инсулин, NεB29-тетрадеканоил GluB30 человеческий инсулин, NεB29-деканоил GluB30 человеческий инсулин, NεB29-додеканоил GluB30 человеческий инсулин, NεB29-тридеканоил GlyA21 GluB30 человеческий инсулин, NεB29-тетрадеканоил GlyA21 GluB30 человеческий инсулин, NεB29-деканоил GlyA21 GluB30 человеческий инсулин, NεB29-додеканоил GlyA21 GluB30 человеческий инсулин, NεB29-тридеканоил GlyA21 GlnB3 GluB30 человеческий инсулин, NεB29-тетрадеканоил GlyA21 GlnB3 GluB30 человеческий инсулин, NεB29-деканоил GlyA21 GlnB3 GluB30 человеческий инсулин, NεB29-додеканоил GlyA21 GlnB3 GluB30 человеческий инсулин, NεB29-тридеканоил AlaA21 GluB30 человеческий инсулин, NεB29-тетрадеканоил AlaA21 GluB30 человеческий инсулин, NεB29-деканоил AlaA21 GluB30 человеческий инсулин, NεB29-додеканоил AlaA21 GluB30 человеческий инсулин, NεB29-тридеканоил AlaA21 GlnB3 GluB30 человеческий инсулин, NεB29-тетрадеканоил AlaA21 GlnB3 GluB30 человеческий инсулин, NεB29-деканоил AlaA21 GlnB3 GluB30 человеческий инсулин, NεB29-додеканоил AlaA21 GlnB3 GluB30 человеческий инсулин, NεB29-тридеканоил GlnB3 GluB30 человеческий инсулин, NεB29-тетрадеканоил GlnB3 GluB30 человеческий инсулин, NεB29-деканоил GlnB3 GluB30 человеческий инсулин и NεB29-додеканоил GlnB3 GluB30 человеческий инсулин.
В WO 97/02043 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты гормонально неактивные соединения инсулина, которые полезны при инсулиновой профилактике, и, в частности, такие аналоги человеческого инсулина, выбранные среди дезА1 человеческого инсулина; дез(А1-А2) человеческого инсулина; дез(А1-А3) человеческого инсулина; дезА21 человеческого инсулина; дез(В1-В5) человеческого инсулина; дез(В1-В6) человеческого инсулина; дез(В23-В30) человеческого инсулина; дез(В24-В30) человеческого инсулина; дез(В25-В30) человеческого инсулина; GlyA2 человеческого инсулина; AlaA2 человеческого инсулина; NIeA2 человеческого инсулина; ThrA2 человеческого инсулина; ProA2 человеческого инсулина; D-алло-IIeA2 человеческого инсулина; NvaA3 человеческого инсулина; NIeA3 человеческого инсулина; LeuA3 человеческого инсулина; ValA2,IIeA3 человеческого инсулина; AbuA2,AbuA3 человеческого инсулина; GlyA2,GlyA3 человеческого инсулина; D-CysA6 человеческого инсулина; D-CysA6,D-CysA11 человеческого инсулина; SerA6,SerA11, дез(А8-А10) человеческого инсулина; D-CysA7 человеческого инсулина; D-CysA11 человеческого инсулина; LeuA19 человеческого инсулина; GlyB6 человеческого инсулина; GluB12 человеческого инсулина; AsnB12 человеческого инсулина; PheB12 человеческого инсулина; D-AlaB12 человеческого инсулина и AspB25 человеческого инсулина, применимы в способах согласно настоящему изобретению.
В WO 92/15611 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты аналоги человеческого инсулина с высокими константами скорости ассоциации в процессе связывания с рецептором инсулина, которые характеризуются содержанием тирозина в положении А13 и/или фенилаланина, триптофана или тирозина в положении В17. В частности, такие аналоги выбраны среди TyrA13 человеческого инсулина, PheB17 человеческого инсулина, TrpB17 человеческого инсулина, TyrB17 человеческого инсулина, TyrA13,PheB17 человеческого инсулина, TyrA13, TrpB17 человеческого инсулина, TyrA13,TyrB17 человеческого инсулина, PheA13, PheB17 человеческого инсулина, PheA13,TrpB17 человеческого инсулина, PheA13, TyrB17 человеческого инсулина, TrpA13, PheB17 человеческого инсулина, TrpA13, Trp17 человеческого инсулина и TrpA13,TyrB17 человеческого инсулина.
В WO 92/00322 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты аналоги человеческого инсулина, которые способны направляться к конкретным тканям-мишеням и которые характеризуются наличием в положении А13 и/или в положении В17 в молекуле инсулина природного аминокислотного остатка, отличного от лейцина, и/или наличием в положении В18 в молекуле инсулина природного аминокислотного остатка, отличного от валина. В частности, такие аналоги выбраны среди AlaB17 человеческого инсулина, AlaB18 человеческого инсулина, AsnA13 человеческого инсулина, AsnA13, AlaB17 человеческого инсулина, AsnA13,AspB17 человеческого инсулина, AsnA13, GluB17 человеческого инсулина, AsnB18 человеческого инсулина, AspA13 человеческого инсулина, AspA13, AlaB17 человеческого инсулина, AspA13, AspB17 человеческого инсулина, AspA13, GluB17 человеческого инсулина, AspB18 человеческого инсулина, GlnA13 человеческого инсулина, GlnA13, AlaB17 человеческого инсулина, GlnA13, Asp B17 человеческого инсулина, GlnB18 человеческого инсулина, GluA13 человеческого инсулина, GluA13, AlaB17 человеческого инсулина, GluA13, AspB17 человеческого инсулина, GluA13, GluB17 человеческого инсулина, GluB18 человеческого инсулина, GlyA13 человеческого инсулина, GlyA13, AlaB17 человеческого инсулина, GlyA13,AsnB17 человеческого инсулина, GlyA13, AspB17 человеческого инсулина, GlyA13, GluB17 человеческого инсулина, GlyB18 человеческого инсулина, SerA13 человеческого инсулина, SerA13, GlnA17, CluB10, GlnB17-дез(ThrБ30) человеческого инсулина, SerA13, AlaB17 человеческого инсулина, SerA13,AsnB17 человеческого инсулина, SerA13, AspB17 человеческого инсулина, SerA13, GlnB17 человеческого инсулина, SerA13, GluB17 человеческого инсулина, SerA13, ТhrB17 человеческого инсулина, SerB14, AspB17 человеческого инсулина, SerB18 человеческого инсулина, ThrA13 человеческого инсулина или ThrB18 человеческого инсулина.
В WO 90/01038 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты аналоги человеческого инсулина с высокой биологической активностью, характеризующиеся тем, что PheB25 заменен His или Tyr, наличием замен в одном или более чем одном из положений А4, А8, А17, А21, В9, В10, В12, В13, В21, В26, В27, В28 и В30 и возможным отсутствием аминокислотного остатка в положении В30. В частности, такие аналоги выбраны среди ТуrB25 человеческого инсулина, TyrB25, AspB28 человеческого инсулина, HisB25 человеческого инсулина, HisB25, AspB28 человеческого инсулина, TyrB25 человеческого инсулина-В30-амида и HisB25 человеческого инсулина-В30-амида.
В WO 86/05496 (Nordisk Gentofte) раскрыты аналоги человеческого инсулина с пролонгированным действием, характеризующиеся тем, что карбоксильная группа В30 блокирована, и наличием от одной до четырех блокированных карбоксильных групп в аминокислотных остатках в положениях А4, А17, А21, В13 и В21. В частности, такие аналоги выбраны среди инсулин-В30-октилового эфира, инсулин-В30-додециламида, инсулин-В30-гексадециламида, инсулин-(В21,В30)-диметилового эфира, инсулин-(В17,В30)-диметилового эфира, инсулин-(А4,В30)-диамида, инсулин-А17амид-В30-октилового эфира, инсулин-(А4,В13)-диамид-В30-гексиламида, инсулин-(А4,А17,В21,В30)-тетраамида, инсулин-(А17,В30)-диамида, А4-Ala-инсулин-В30-амида и В30-Leu-инсулин-(А4,В30)-диамида.
В WO 86/05497(Nordisk Gentofte), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина, в которых один или более чем один из четырех аминокислотных остатков в положениях А4, А17, В13 и В21 содержит незаряженную боковую цепь. Конкретно упомянуты человеческий инсулин A17-Gln, человеческий инсулин A4-Gln, свиной инсулин B21-Gln, человеческий инсулин B13-Gln, человеческий инсулин (A17,B21)-Gln, человеческий инсулин А4-Ala, человеческий инсулин B21-Thr, человеческий инсулин B13-Val, человеческий инсулин-Thr-А17-Gln, человеческий инсулин В21-метиловый эфир и человеческий инсулин А17-метиловый эфир.
В WO 92/00321 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина с пролонгированной активностью, в которые введен положительный заряд в N-конце В-цепи. Конкретно упомянуты ArgB5, SerA21, ThrB30-NH2 человеческий инсулин, ArgB5, ProB6, SerA21, ThrB30-NH2 человеческий инсулин, ArgB5, GlyA21, ThrB30-NH2 человеческий инсулин, ArgB5, ProB6, GlyA21, ThrB30-NH2 человеческий инсулин, ArgB2, SerA21, ThrB30-NH2 человеческий инсулин, ArgB2, ProB3, SerA21, ThrB30-NH2 человеческий инсулин, ArgB2,GlyA21,ThrB30-NH2 человеческий инсулин, ArgB2, ProB3, GlyA21, ThrB30-NH2 человеческий инсулин, ArgB2, ArgB3, SerA21, ThrB30-NH2 человеческий инсулин, ArgB2, ArgB3, SerA21 человеческий инсулин, ArgB4, ProB5, SerA21, ThrB30-NH2 человеческий инсулин, ArgB4, ArgB5, ProB6, GlyA21, ThrB30 человеческий инсулин, ArgB3, GlyA21, ThrB30-NH2 человеческий инсулин, ArgB3,SerA21,ThrB30-NH2 человеческий инсулин, ArgB4, GlyA21, ThrB30-NH2 человеческий инсулин, ArgB4, SerA21, ThrB30-NH2 человеческий инсулин и ArgB1, ProB2, GlyA21, ThrB30-NH2 человеческий инсулин.
В WO 90/07522 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина, проявляющие низкую способность к ассоциации в растворе, в которых есть положительно заряженный аминокислотный остаток, то есть Lys или Arg, в положении В28. Конкретно упомянуты дез[PheB25]-человеческий инсулин, дез[PheB26]-человеческий инсулин, дез{TyrB27]-человеческий инсулин, дез[ProB28]-человеческий инсулин, дез[PheB25]-свиной инсулин, дез[ProB28]-свиной инсулин, дез[ProB28]-кроличий инсулин, дез[PheB25],дез[ThrB30]-человеческий инсулин, дез[TyrB26],дез[ThrB30]-человеческий инсулин, [SerA21]-дез[ProB28]-человеческий инсулин, [GlyA21]-дез[ProB28]-человеческий инсулин, [GlyA21]-дез[PheB25]-человеческий инсулин, [AspA21]-дез[PheB25]-человеческий инсулин, [HisB25]-дез[TyrB26],дез[ThrB30]-человеческий инсулин, [AsnB25]-дез[TyrB26],дез[ThrB30]-человеческий инсулин, [AspA21]-дез[PheB25],дез[ThrB30]-человеческий инсулин, [AspB28]-дез[PheB25]- человеческий инсулин, [AspB3]-дез[PheB25]-человеческий инсулин, [LysB28]-человеческий инсулин, [LysB28,ThrB29]-человеческий инсулин и [ArgB28]-дез[LysB29]-человеческий инсулин.
В WO 90/11290 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина с пролонгированной активностью. Конкретно упомянуты [ArgA0]-человеческий инсулин-(В30-амид), [ArgA0,GlnB13]-человеческий инсулин-(В30-амид), [ArgA0,GlnA4,AspA21]-человеческий инсулин-(В30-амид), [ArgA0,SerA21]-человеческий инсулин-(В30-амид) и [ArgA0,ArgB27]-дез[ThrB30]-человеческий инсулин.
В WO 90/10645 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты гликозилированные инсулины. Конкретно упомянуты Phe(B1)-глюкоза-человеческий инсулин, Phe(В1)-манноза-человеческий инсулин, Gly(А1)-манноза-человеческий инсулин, Lys(В29)-манноза-человеческий инсулин, Phe(B1)-галактоза-человеческий инсулин, Gly(A1)-галактоза-человеческий инсулин, Lys(В29)-галактоза-человеческий инсулин, Phe(В1)-мальтоза-человеческий инсулин, Phe(B1)-лактоза-человеческий инсулин, Gly(А1)-глюкоза-человеческий инсулин, Gly(А1)-мальтоза-человеческий инсулин, Cly(А1)-лактоза-человеческий инсулин, Lys(В29)-глюкоза-человеческий инсулин, Lys(В29)-мальтоза-человеческий инсулин, Lys(В29)-лактоза-человеческий инсулин, Gly(А1), Phe(В1)-диглюкоза-человеческий инсулин, Gly(А1), Lys(В29)-диглюкоза-человеческий инсулин, Phe(B1), Lys(B29)-диглюкоза-человеческий инсулин, Phe(В1)-изомальтоза-человеческий инсулин, Gly(A1)-изомальтоза-человеческий инсулин, Lys(В29)-изомальтоза-человеческий инсулин, Phe(В1)-мальтотриоза-человеческий инсулин, Gly(А1)-мальтотриоза-человеческий инсулин, Lys(В29)-мальтотриоза-человеческий инсулин, Gly(A1),Phe(B1)-димальтоза-человеческий инсулин, Gly(A1), Lys(В29)-димальтоза-человеческий инсулин, Phe(В1), Lys(В29)-димальтоза-человеческий инсулин, Gly(A1), Phe(B1)-дилактоза-человеческий инсулин, Gly(А1), Lys(В29)-дилактоза-человеческий инсулин, Phe(В1),Lys(В29)-дилактоза-человеческий инсулин, Gly(А1), Phe(В1)-димальтотриоза-человеческий инсулин, Gly(А1), Lys(В29)-димальтотриоза-человеческий инсулин, Phe(B1), Lys(В29)-димальтотриоза-человеческий инсулин, Phe(B1), Gly(A1)-диманноза-человеческий инсулин, Phe(В1), Lys(В29)-диманноза-человеческий инсулин, Gly(А1), Lys(В29)-диманноза-человеческий инсулин, Phe(В1), Gly(А1)-дигалактоза-человеческий инсулин, Phe(В1), Lys(В29)-дигалактоза-человеческий инсулин, Gly(A1), Lys(В29)-дигалактоза-человеческий инсулин, Phe(B1), Gly(A1)-диизомальтоза-человеческий инсулин, Phe(В1), Lys(В29)-диизомальтоза-человеческий инсулин, Gly(A1), Lys(В29)-диизомальтоза-человеческий инсулин, Phe(B1)глюкоза[AspB10]человеческий инсулин и Gly(A1), Phe(B1)диглюкоза[AspB10]человеческий инсулин.
В WO 88/065999 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты стабилизированные соединения инсулина, в которых Ans21A заменен другими аминокислотными остатками. Конкретно упомянуты GlyA21 человеческий инсулин, AlaA21 человеческий инсулин, SerA21 человеческий инсулин, ThrA21 человеческий инсулин и hSerA21 человеческий инсулин.
В ЕР 254516 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина с пролонгированным действием, в которых основные аминокислотные остатки заменены нейтральными аминокислотными остатками. Конкретно упомянуты GlyA21, LysB27, ThrB30-NH2 человеческий инсулин, SerA21, LysB27, ThrB30-NH2 человеческий инсулин, ThrA21, LysB27, ThrB30-NH2 человеческий инсулин, AlaB21, LysB27, ThrB30-NH2 человеческий инсулин, HisA21, LysB27, ThrB30-NH2 человеческий инсулин, AspB21, LysB27, ThrB30-NH2 человеческий инсулин, GlyA21, ArgB21, ThrB30-NH2 человеческий инсулин, SerA21, ArgB27, ThrB30-NH2 человеческий инсулин, ThrA21, ArgB27, ThrB30-NH2 человеческий инсулин, AlaB21, ArgB27, ThrB30-NH2 человеческий инсулин, HisA21, ArgB27, ThrB30-NH2 человеческий инсулин, AspB21, ArgB27, ThrB30-NH2 человеческий инсулин, GlnB13, GlyA21, ArgB27, ThrB30-NH2 человеческий инсулин, GlnB13, SerA21, ThrB30-NH2 человеческий инсулин, GlnB13, SerA21, ArgB27, ThrB30-NH2 человеческий инсулин, GlnB13, ThrA21, ArgB27, ThrB30-NH2 человеческий инсулин, GlnB13, AlaA21, ArgB27, ThrB30-NH2 человеческий инсулин, GlnB13,HisA21,ArgB27, ThrB30-NH2 человеческий инсулин, GlnB13,AspA21, ArgB27, ThrB30-NH2 человеческий инсулин, GlnB13, GlyA21, LysB27, ThrB30-NH2 человеческий инсулин, GlnB13, SerA21, LysB27, ThrB30-NH2 человеческий инсулин, GlnB13, ThrA21, LysB27, ThrB30-NH2 человеческий инсулин, GlnB13, AlaA21, LysB27, ThrB30-NH2 человеческий инсулин, GlnB13,HisA21,LysB27, ThrB30-NH2 человеческий инсулин, GlnB13, AspA21, LysB27, ThrB30-NH2 человеческий инсулин, AsnA21, LysB27 человеческий инсулин, SerA21, LysB27 человеческий инсулин, ThrA21, LysB27 человеческий инсулин, AlaA21, LysB27 человеческий инсулин, HisA21, LysB27 человеческий инсулин, AspA21, LysB27 человеческий инсулин, GlyA21, LysB27 человеческий инсулин, AsnA21, ArgB27 человеческий инсулин, SerA21, ArgB27 человеческий инсулин, ThrA21, ArgB27 человеческий инсулин, AlaA21, ArgB27 человеческий инсулин, HisA21, ArgB27 человеческий инсулин, AspA21, ArgB27 человеческий инсулин, GlyA21, ArgB27 человеческий инсулин, GlnA17, AsnA21, ArgB27 человеческий инсулин, GlnA17, SerA21, ArgB27 человеческий инсулин, GlnA17, ThrA21, ArgB27 человеческий инсулин, GlnA17, AlaA21, ArgB27 человеческий инсулин, GlnA17, HisA21, ArgB27 человеческий инсулин, GlnA17, AspA21, ArgB27 человеческий инсулин, GlnA17, GlyA21, ArgB27 человеческий инсулин, GlnA17, AsnA21, GlnB13 человеческий инсулин, GlnA17, SerA21, GlnB13 человеческий инсулин, GlnA17, ThrA21, GlnB13 человеческий инсулин, GlnA17, AlaA21, GlnB13 человеческий инсулин, GlnA17, HisA21, GlnB13 человеческий инсулин, GlnA17, AspA21, GlnB13 человеческий инсулин, GlnA17, GlyA21, GlnB13 человеческий инсулин, ArgA27, AsnA21, GlnB13 человеческий инсулин, ArgA27, SerA21, GlnB13 человеческий инсулин, ArgA27, ThrA21, GlnB13 человеческий инсулин, ArgA27, AlaA21, GlnB13 человеческий инсулин, ArgA27, HisA21, GlnB13 человеческий инсулин, ArgA27, AspA21, GlnB13 человеческий инсулин, ArgA27, GlyA21, GlnB13 человеческий инсулин, GlnA17, AsnA21, LysB27 человеческий инсулин, GlnA17, SerA21, LysB27 человеческий инсулин, GlnA17, ThrA21, LysB27 человеческий инсулин, GlnA17, AlaA21, LysB27 человеческий инсулин, GlnA17, HisA21, LysB27 человеческий инсулин, GlnA17, AspA21, LysB27 человеческий инсулин, GlnA17, GlyA21, LysB27 человеческий инсулин, GlnB13, AsnA21, LysB27 человеческий инсулин, GlnB13, SerA21, LysB27 человеческий инсулин, GlnB13, ThrA21, LysB27 человеческий инсулин, GlnB13, AlaA21, LysB27 человеческий инсулин, GlnB13, HisA21, LysB27 человеческий инсулин, GlnB13, AspA21, LysB27 человеческий инсулин и GlnB13, GlyA21, LysB27 человеческий инсулин.
В ЕР 214826 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина с быстрым началом действия.
В ЕР 194864 (Novo Nordisk), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина с пролонгированным действием, в которых основные аминокислотные остатки заменены нейтральными аминокислотными остатками. Конкретно упомянуты GlnA17, ArgB27, ThrB30-NH2 человеческий инсулин, GlnA17, GlnB13, ThrB30-NH2 человеческий инсулин, GlnA17, LysB27, ThrB30-NH2 человеческий инсулин, GlnA17, LysB27-NH2 человеческий инсулин, GlnA17, GlnA17, ThrB30-NH2 человеческий инсулин, GlnB13, ArgB27, ThrB30-NH2 человеческий инсулин, GlnB13, LysB27, ThrB30-NH2 человеческий инсулин, GlnB13, LysB30-NH2 человеческий инсулин, GlnB13, ThrB30-NH2 человеческий инсулин, ArgB27, ArgB30-NH2 человеческий инсулин, ArgB27, LysB30-NH2 человеческий инсулин, ArgB27, ThrB30-NH2 человеческий инсулин, LysB27, ArgB30-NH2 человеческий инсулин, LysB27, LysB30-NH2 человеческий инсулин, LysB27, ThrB30-NH2 человеческий инсулин, LysB29-NH2,дез-(В30)человеческий инсулин, ThrB30-NH2 человеческий инсулин, LysB30-NH2 человеческий инсулин, LysB30(Lau)-NH2 человеческий инсулин, LysB30, ArgB31-NH2 человеческий инсулин, LysB30, LysB31-NH2 человеческий инсулин, ArgB30-NH2 человеческий инсулин, ArgB30, ArgB31-NH2 человеческий инсулин и ArgB30, LysB31-NH2 человеческий инсулин.
В патенте США №3528960 (Eli Lilly), который включен в данное описание посредством ссылки, раскрыты N-карбоксиароильные соединения инсулина, в которых одна, две или три первичные аминогруппы молекулы инсулина имеют карбоксиароильную группу.
В патенте GB №1492997 (Nat. Res. Dev. Corp.), который включен в данное описание посредством ссылки, раскрыты соединения инсулина с карбамильным замещением при NεB29 с улучшенным профилем гипогликемического эффекта.
В выложенной патентной заявке JP №1-254699 (Kodama Co., Ltd.), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина, в которых алканоильная группа связана либо с аминогруппой PheB1, либо с ε-аминогруппой LysB29, либо с ними обеими.
В выложенной патентной заявке JP №57-067548 (Shionogi), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина, в которых в положении ВЗО находится аминокислота, имеющая по меньшей мере пять атомов углерода, которая необязательно может кодироваться триплетом нуклеотидов.
В WO 03/053339 (Eli Lilly), которая включена в данное описание посредством ссылки, раскрыты соединения инсулина, в которых А - цепь в N-конце удлинена двумя аминокислотными остатками, А-1 и А0, где В - цепь удлинена при N-конце двумя аминокислотными остатками, В-1 и В0, где аминокислотные остатки в положениях В28, В29 и В39 могут быть заменены и где ε-аминогруппа Lys в положении В28 или В29 ковалентно связана с α-карбоксильной группой положительно заряженной аминокислоты с образованием Lys-Nε-аминокислотного производного. Конкретно упомянуты указанные аналоги, где А-1 и В-1 оба отсутствуют и где А0 представляет собой Arg, а В0 представляет собой Arg или отсутствует.
Соединения инсулина, выбранные из группы, состоящей из
i. аналога, где в положении В28 содержится Asp, Lys, Leu, Val или Ala и в положении В29 содержится Lys или Pro, и
ii. дез(В28-В30), дез(В27) или дез(В30) человеческого инсулина,
также применимы для способов согласно настоящему изобретению, и, в частности, соединение инсулина, где в положении В28 содержится Asp или Lys, а в положении В29 содержится Lys или Pro.
Дез(В30)-человеческий инсулин также применим в способах согласно настоящему изобретению.
Другие применимые соединения инсулина выбраны из группы, состоящей из B29-Nε-миристоил-дез(B30) человеческого инсулина, B29-Nε-пальмитоил-дез(B30) человеческого инсулина, B29-Nε-миристоил человеческого инсулина, B29-Nε-пальмитоил человеческого инсулина, B28-Nε-миристоил LysB28 ProB29 человеческого инсулина, B28-Nε-пальмитоил LysB28 ProB29 человеческого инсулина, B30-Nε-миристоил-ThrB29LysB30 человеческого инсулина, B30-Nε-пальмитоил-ThrB29LysB30 человеческого инсулина, B29-Nε-(N-пальмитоил-γ-глутамил)-дез(B30) человеческого инсулина, В29-Nε-(N-литохолил-γ-глутамил)-дез(В30) человеческого инсулина, В29-Nε-(ω-карбоксигептадеканоил)-дез(B30) человеческого инсулина, B29-Nε-(ω-карбоксигептадеканоил) человеческого инсулина и B29-Nε-миристоил-дез(B30) человеческого инсулина.
Примеры GLP-1, применимого в способах согласно настоящему изобретению, включают человеческий GLP-1 и соединения GLP-1. Человеческий GLP-1 представляет собой пептид из 37 аминокислотных остатков, образующийся из препроглюкагона, который синтезируется среди прочего в L-клетках в терминальной подвздошной кишке, в поджелудочной железе и в головном мозге. GLP-1 является важным кишечным гормоном с регуляторной функцией в метаболизме глюкозы, а также в желудочно-кишечной секреции и метаболизме. Процессинг препроглюкагона с образованием GLP-1(7-36)-амида, GLP-1(7-37) и GLP-2 происходит, в основном, в L-клетках. Фрагменты GLP-1(7-36)-амид и GLP-1(7-37) оба являются глюкозозависимыми инсулинотропными агентами. В последние десятилетия ряд структурных аналогов GLP-1 был выделен из яда ящериц ядозубов (Heloderma suspectum и Heloderma horridum}. Экзендин-4 представляет собой пептид из 39 аминокислотных остатков, выделенный из яда Heloderma horridum, и этот пептид имеет 52% гомологии с GLP-1. Экзендин-4 является сильным агонистом рецептора GLP-1, который, как показано, стимулирует высвобождение инсулина и обеспечивает снижение уровня глюкозы в крови при инъекции собакам. GLP-1(1-37) и экзендин-4(1-39), а также некоторые их фрагменты, аналоги и производные (здесь обозначенные как соединения GLP-1) являются эффективными инсулинотропными агентами, и все они применимы в способе согласно настоящему изобретению. Инсулинотропные фрагменты GLP-1(1-37) являются инсулинотропными пептидами, полноразмерную последовательность которых можно найти в последовательности GLP-1(1-37), и где по меньшей мере одна концевая аминокислота делетирована. Примерами инсулинотропных фрагментов GLP-1 (1-37) являются GLP-1 (7-37), где аминокислотные остатки в положениях 1-6 GLP-1(1-37) делетированы, и GLP-1(7-36), где аминокислотные остатки в положениях 1-6 и 37 GLP-1(1-37) делетированы. Примерами инсулинотропных фрагментов экзендина-4(1-39) являются экзендин-4(1-38) и экзендин-4(1-31). Инсулинотропное свойство соединения можно определить с помощью анализов in vivo или in vitro, хорошо известных в данной области техники. Например, это соединение можно ввести животному и проводить мониторинг концентрации инсулина по времени. Инсулинотропные аналоги GLP-1(1-37) и экзендина-4(1-39) - это соответствующие молекулы, в которых один или более чем один аминокислотный остаток заменен другими аминокислотными остатками и/или из которых один или более чем один аминокислотный остаток делетирован и/или в которых один или более чем один аминокислотный остаток добавлен, при условии, что такой аналог либо является инсулинотропным, либо является пролекарством инсулинотропного соединения. Примерами инсулинотропных аналогов GLP-1(1-37) являются, например, Met8-GLP-1(7-37), где аланин в положении 8 заменен метионином и аминокислотные остатки в положении 1-6 делетированы, и Arg34-GLP-1(7-37), где валин в положении 34 заменен аргинином и аминокислотные остатки в положениях 1-6 делетированы. Примером инсулинотропного аналога экзендина-4(1-39) является Ser2Asp3-экзендин-4(1-39), где аминокислотные остатки в положении 2 и 3 заменены серином и аспарагиновой кислотой, соответственно (данный конкретный аналог также известен в данной области техники как экзендин-3). Инсулинотропными производными GLP-1(1-37), экзендина-4(1-39) и их аналогов являются те, которые специалисты в данной области техники считают производными данных пептидов, то есть имеющие по меньшей мере один заместитель, который не присутствует в молекуле исходного пептида, при условии, что указанное производное либо является инсулинотропным, либо является пролекарством инсулинотропного соединения. Примерами заместителей являются амиды, углеводы, алкильные группы и липофильные заместители. Примерами инсулинотропных производных GLP-1(1-37), экзендина-4(1-39) и их аналогов являются СL-Р-1(7-36)-амид, Arg34, Lys26(Nε-(γ-Glu(Nα-гексадеканоил)))-GLP-1(7-37) и Tyr31-экзендин-4(1-31)-амид. Дополнительные примеры GLP-1(1-37), экзендина-4(1-39), их инсулинотропных фрагментов, их инсулинотропных аналогов и их инсулинотропных производных описаны в WO 98/08871, WO 99/43706, US 5424286 и WO 00/09666, которые все включены в данное описание посредством ссылки.
GLP-2 и соединения GLP-2 могут быть также модифицированы способами, предложенными в настоящем изобретении. В настоящем контексте соединение GLP-2 связывается с рецептором GLP-2, предпочтительно с константой аффинности (связывания) (KD) или эффективностью (EC50) ниже 1 мкМ, например ниже 100 нМ. Термин "соединение GLP-2" означает человеческий GLP-2, в котором один или более чем один аминокислотный остаток делетирован и/или заменен другим аминокислотным остатком, природным или неприродным, и/или человеческий GLP-2, содержащий дополнительные аминокислотные остатки, и/или человеческий GLP-2, в котором по меньшей мере один органический заместитель связан с одним или более чем одним аминокислотным остатком. В частности, рассматривают те пептиды, аминокислотная последовательность которых содержит в любой последовательности из 33 последовательных аминокислот более чем 60% аминокислотной последовательности человеческого GLP-2. Также рассматривают те пептиды, аминокислотная последовательность которых содержит в любой последовательности из 37 последовательных аминокислот более чем 60% аминокислотной последовательности человеческого GLP-2, когда вплоть до четырех аминокислот делетированы из этой аминокислотной последовательности. Также рассматривают те пептиды, аминокислотная последовательность которых содержит в любой последовательности из 31 последовательных аминокислот более чем 60% аминокислотной последовательности человеческого GLP-2, когда вплоть до двух аминокислот добавлены в его аминокислотную последовательность. В термин "соединения GLP" также включают природные аллельные варианты, которые могут существовать и появляться от одного индивидуума к другому. Также степень и локализация гликозилирования или других посттрансляционных модификаций может варьировать в зависимости от выбранных клеток-хозяев и от природы клеточного окружения хозяина.
Соединения-кандидаты GLP-2, которые можно использовать согласно настоящему изобретению, включают соединения GLP-2, описанные в WO 96/32414, WO 97/39031, WO 98/03547, WO 96/29342, WO 97/31943, WO 98/08872, которые все включены в данное описание посредством ссылки.
В частности, приведенные ниже соединения GLP-2 применимы в способах согласно настоящему изобретению: A2G-GLP-2(1-33); K30R-GLP-2(1-33); S5K-GLP-2(1-33); S7K-GLP-2(1-33); D8K-GLP-2(1-33); E9K-GLP-2(1-33); M10K-GLP-2(1-33); N11K-GLP-2(1-33); T12K-GLP-2(1-33); I13K-GLP-2(1-33); L14K-GLP-2(1-33); D15K-GLP-2(1-33); N16K-GLP-2(1-33); L17K-GLP-2(1-33); A18K-GLP-2(1-33); D21K-GLP-2(1-33); N24K-GLP-2(1-33); Q28K-GLP-2(1-33); S5K/K30R-GLP-2(1-33); S7K/K30R-GLP-2(1-33); D8K/K30R-GLP-2(1-33); E9K/K30R-GLP-2(1-33); M10K/K30R-GLP-2(1-33); N11K/K30R-GLP-2(1-33); T12K/K30R-GLP-2(1-33); 113K/K30R-GLP-2(1-33); L14K/K30R-GLP-2(1-33); D15K/K30R-GLP-2(1-33); N16K/K30R-GLP-2(1-33); L17K/K30R-GLP-2(1-33); A18K/K30R-GLP-2(1-33); D21K/K30R-GLP-2(1-33); N24K/K30R-GLP-2(1-33); Q28K/K30R-GLP-2(1-33); K30R/D33K-GLP-2(1-33); D3E/K30R/D33E-GLP-2(1-33); D3E/S5K/K30R/D33E-GLP-2(1-33); D3E/S7K/K30R/D33E-GLP-2(1-33); D3E/D8K/K30R/D33E-GLP-2(1-33); D3E/E9K/K30R/D33E-GLP-2(1-33); D3E/M10K/K30R/D33E-GLP-2(1-33); D3E/N11K/K30R/D33E-GLP-2(1-33); D3E/T12K/K30R/D33E-GLP-2(1-33); D3E/I13K/K30R/D33E-GLP-2(1-33); D3E/L14K/K30R/D33E-GLP-2(1-33); D3E/D15K/K30R/D33E-GLP-2(1-33); D3E/N16K/K30R/D33E-GLP-2(1-33); D3E/L17K/K30R/D33E-GLP-2(1-33); D3E/A18K/K30R/D33E-GLP-2(1-33); D3E/D21K/K30R/D33E-GLP-2(1-33); D3E/N24K/K30R/D33E-GLP-2(1-33) и D3E/Q28K/K30R/D33E-GLP-2(1-33).
Производные GLP-2 только с одним липофильным заместителем, присоединенным к пептиду GLP-2, также применимы в способах согласно настоящему изобретению, как, например, производные GLP-2, где липофильный заместитель содержит от 4 до 40 атомов углерода, как, например, от 8 до 25 атомов углерода, например, от 12 до 20 атомов углерода.
Липофильный заместитель может быть присоединен к аминокислотному остатку таким образом, чтобы карбоксильная группа липофильного заместителя образовала амидную связь с аминогруппой аминокислотного остатка.
Для примера липофильный заместитель присоединен к остатку Lys.
Липофильный заместитель может быть присоединен к аминокислотному остатку таким образом, чтобы аминогруппа липофильного заместителя образовала амидную связь с карбоксильной группой аминокислотного остатка.
Липофильный заместитель может быть также присоединен к пептиду GLP-2 с помощью спейсера, и указанный спейсер может быть выбран из β-аланина, гамма-аминомасляной кислоты (ГАМК), γ-глутаминовой кислоты, Lys, Asp, Glu, дипептида, содержащего Asp, дипептида, содержащего Glu, или дипептида, содержащего Lys. В одном варианте осуществления изобретения спейсер представляет собой β-аланин.
Карбоксильная группа исходного пептида GLP-2 может также образовать амидную связь с аминогруппой спейсера, а карбоксильная группа аминокислотного или дипептидного спейсера образует амидную связь с аминогруппой липофильного заместителя.
Аминогруппа исходного пептида GLP-2 может также образовать амидную связь с карбоксильной группой спейсера, а аминогруппа спейсера образует амидную связь с карбоксильной группой липофильного заместителя.
В одном варианте осуществления изобретения липофильный заместитель представляет собой прямоцепочечную или разветвленную алкильную группу. В одном варианте осуществления изобретения липофильный заместитель представляет собой ацильную группу прямоцепочечной или разветвленной жирной кислоты.
В одном варианте осуществления изобретения липофильный заместитель представляет собой ацильную группу прямоцепочечной или разветвленной алкан-α,ω-дикарбоновой кислоты.
В одном варианте осуществления изобретения производное GLP-2 имеет один липофильный заместитель. В одном варианте осуществления изобретения производное GLP-2 имеет два липофильных заместителя. В одном варианте осуществления изобретения производное GLP-2 имеет три липофильных заместителя. В одном варианте осуществления изобретения производное GLP-2 имеет четыре липофильных заместителя.
Приведенный ниже перечень содержит производные GLP-2, которые являются конкретно применимыми в способах согласно настоящему изобретению.






Соединения фактора VII, применимые в способах согласно настоящему изобретению, охватывают фактор VII дикого типа (то есть полипептид, имеющий аминокислотную последовательность, раскрытую в патенте США №4784950), а также варианты фактора VII, проявляющие по существу такую же или улучшенную биоилогическую активность относительно фактора VII дикого типа, полипептиды, родственные фактору VII, а также производные фактора VII и конъюгаты фактора VII. В термин "соединения фактора VII" следует включать полипептиды фактора VII в их нерасщепленной (зимогенной) форме, а также те, которые подверглись протеолитическому процессингу с образованием их соответствующих биологически активных форм, которые могут быть обозначены как фактор VIIa. Как правило, фактор VII расщепляется между остатками 152 и 153 с образованием фактора VIIa. Такие варианты фактора VII могут проявлять свойства, отличные от человеческого фактора VII, включая стабильность, связывание фосфолипида, измененную специфичную активность и тому подобное.
Как используют здесь, "полипептиды, родственные фактору VII", охватывают полипептиды, включая варианты, в которых биологическая активность фактора VIIa существенно модифицирована или снижена относительно активности фактора VIIa дикого типа. Эти полипептиды включают без ограничения фактор VII или фактор VIIa, в который были введены специфичные изменения аминокислотной последовательности, которые модифицируют или нарушают биологическую активность полипептида.
Термин "производное фактора VII", как его используют здесь, означает фактор VII дикого типа, варианты фактора VII, проявляющие по существу такую же или улучшенную биологическую активность относительно фактора VII дикого типа, и полипептиды, родственные фактору VII, в которых одна или более чем одна аминокислота исходного пептида химически модифицирована, например, путем алкилирования, ПЭГилирования, ацилирования, образования эфира или амида и т.п. Они включают, но не ограничены ими, ПЭГилированный человеческий фактор VIIa, цистеин-ПЭГилированный человеческий фактор VIIa и его варианты.
Термин "ПЭГилированный человеческий фактор VIIa" означает человеческий фактор VIIa, имеющий молекулу ПЭГ, конъюгированную с полипептидом человеческого фактора VIIa. Должно быть понятно, что молекула ПЭГ может быть присоединена к любому участку полипептида фактора VIIa, включая любой аминокислотный остаток или углеводную группу полипептида фактора VIIa. Термин "цистеин-ПЭГилированный человеческий фактор VIIa" означает человеческий фактор VIIa, имеющий молекулу ПЭГ, конъюгированную с сульфгидрильной группой цистеина, введенного в человеческий фактор VIIa.
Биологическая активность фактора VIIa при свертывании крови является результатом его способности (i) связываться с тканевым фактором (TF) и (ii) катализировать протеолитическое расщепление фактора IX или фактора Х с получением активированного фактора IX или Х (фактора IXa или Ха соответственно). Для целей изобретения биологическую активность фактора VIIa можно определить количественно путем измерения способности препарата стимулировать свертывание крови, используя фактор VII-зависимую плазму и тромбопластин, как описано, например, в патенте США №5997864. В данном анализе биологическую активность выражают в виде уменьшения времени свертывания крови относительно контрольного образца и превращают в "единицы фактора VII" путем сравнения со стандартом объединенной человеческой сыворотки, содержащей 1 единицу/мл активности фактора VII. Альтернативно биологическую активность фактора VIIa можно определить количественно путем (i) измерения способности фактора VIIa продуцировать фактор Ха в системе, содержащей TF, заключенный в липидную мембрану, и фактор X. (Persson et al., J. Biol. Chem. 272: 19919-19924, 1997); (ii) измерения гидролиза фактора Х в водной системе; (iii) измерения его физического связывания с TF, используя прибор, основанный на поверхностном плазменном резонансе (Persson, FEBS Letts. 413: 359-363, 1997) и (iv) измерения гидролиза синтетического субстрата.
Варианты фактора VII, обладающие по существу такой же или улучшенной биологической активностью относительно фактора VIIa дикого типа, охватывают те, которые проявляют по меньшей мере примерно 25%, предпочтительно по меньшей мере примерно 50%, более предпочтительно по меньшей мере примерно 75% и наиболее предпочтительно по меньшей мере примерно 90% специфичной активности фактора VIIa, который продуцирован в том же типе клеток, при тестировании в одном или более чем одном анализе свертывания, анализе протеолиза или анализе связывания TF, как описано выше. Вариантами фактора VII, обладающими существенно сниженной биологической активностью относительно фактора VIIa дикого типа, являются те, которые проявляют менее чем примерно 25%, предпочтительно менее чем примерно 10%, более предпочтительно менее чем примерно 5% и наиболее предпочтительно менее чем примерно 1% специфичной активности фактора VIIa дикого типа, который продуцирован в том же типе клеток, при тестировании в одном или более чем одном анализе свертывания, анализе протеолиза или анализе связывания TF, как описано выше. Вариантами фактора VII, обладающими существенно модифицированной биологической активностью относительно фактора VII дикого типа, являются без ограничения варианты фактора VII, которые проявляют TF-независимую протеолитическую активность фактора Х и те, которые связываются с TF, но не расщепляют фактор X.
Варианты фактора VII, либо проявляющие по существу такую же или лучшую биологическую активность, чем фактор VII дикого типа, либо альтернативно проявляющие существенно модифицированную или сниженную биологическую активность относительно фактора VII дикого типа, включают без ограничения полипептиды, имеющие аминокислотную последовательность, которая отличается от последовательности фактора VII дикого типа вставкой, делецией или заменой одной или более чем одной аминокислоты.
Терминами "вариант" или "варианты", как используют здесь, обозначают фактор VII, имеющий последовательность фактора VII дикого типа, где одна или более чем одна аминокислота исходного белка заменена другой аминокислотой и/или где одна или более чем одна аминокислота исходного белка делетирована и/или где одна или более чем одна аминокислота вставлена в белок и/или где одна или более чем одна аминокислота добавлена к исходному белку. Такое добавление может иметь место либо при N-конце, либо при С-конце исходного белка, либо при обоих концах. "Вариант" или "варианты" в пределах данного определения все же обладают активностью фактора FVII в его активированной форме. В одном варианте осуществления изобретения вариант является на 70% идентичным последовательности фактора VII дикого типа. В одном варианте осуществления изобретения вариант является на 80% идентичным последовательности фактора VII дикого типа. В другом варианте осуществления изобретения вариант является на 90% идентичным последовательности фактора VII дикого типа. В следующем варианте осуществления изобретения вариант является на 95% идентичным последовательности фактора VII дикого типа.
Не ограничивающие примеры вариантов фактора VII, обладающих по существу такой же биологической активностью, как фактор VII дикого типа, включают S52A-FVIIa, S60А-FVIIa (Lino et al., Arch. Biochem. Biophys. 352: 182-192, 1998); варианты FVIIa, проявляющие повышенную протеолитическую стабильность, как раскрыто в патенте США №5580560; фактор VIIa, который был подвергнут протеолитическому расщеплению между остатками 290 и 291 или между остатками 315 и 316 (Mollerup et al., Biotechnol. Bioeng. 48: 501-505, 1995); окисленные формы фактора VIIa (Kornfelt et al., Arch. Biochem. Biophys. 363: 43-54, 1999); варианты FVII, как раскрыто в PCT/DK02/00189; и варианты FVII, проявляющие повышенную протеолитическую стабильность, как раскрыто в WO 02/38162 (Scripps Research Institute); варианты FVII, имеющие модифицированный Gla-домен и проявляющие усиленное связывание с мембраной, как раскрыто в WO 99/20767 (University of Minnesota); и варианты FVII, как раскрыто в WO 01/58935 (Maxygen ApS), все из которых включены в данное описание посредством ссылки.
Конкретно упомянуты варианты FVII, обладающие повышенной биологической активностью по сравнению с FVIIa дикого типа, включают варианты FVII, как раскрыто в WO 01/83725, WO 02/22776, WO 02/077218, PCT/DK02/00635, Датской патентной заявке PA 2002 01423, Датской патентной заявке PA 2001 01627; WO 02/38162 (Scripps Research Institute) и варианты FVIIa с повышенной активностью, как раскрыто в JP 2001061479 (Chemo-Sero-Therapeutic Res Inst.), все из которых включены в данное описание посредством ссылки.
Примеры вариантов фактора VII, обладающих существенно сниженной или модифицированной биологической активностью относительно фактора VII дикого типа, включают R152E-FVIIa (Wildgoose et al., Biochem 29: 3413-3420, 1990), S344A-FVIIa (Kazama et al., J. Biol. Chem. 270:66-72, 1995), FFR-FVIIa (Holst et al., Eur. J. Vasc. Endovasc. Surg. 15:515-520, 1998) и фактор VIIa, у которого отсутствует домен Gla (Nicolaisen et al., FEBS Letts. 317: 245-249, 1993), все из которых включены в данное описание посредством ссылки.




Гормон роста (GH), применимый в способах согласно настоящему изобретению, включает человеческий гормон роста (hGH), последовательность и характеристики которого изложены, например, в Hormone Drugs, Gueriguian, U.S.P. Covention, Rockvill, 1982, и соединения гормона роста. Термин "соединение гормона роста" означает человеческий гормон роста (hGH), в котором один или более чем один аминокислотный остаток делетирован и/или заменен другими аминокислотными остатками, природными или неприродными, и/или hGH, содержащий добавления аминокислотных остатков, природных или неприродных, и/или hGH, в котором присутствует по меньшей мере один органический заместитель, связанный с аминокислотным остатком. Конкретно упомянута последовательность из 191 природных аминокислот (соматотропин) и виды последовательности из 192 аминокислот с N-концевым метионином (соматрем).
Другие примеры соединения гормона роста, применимого в настоящем изобретении, включают те, где группа аминокислот 172, 174, 176 и 178 заменена одной из приведенных ниже групп аминокислот (R, S, F, R); (R, A, Y, R), (К, Т, Y, К); (R, S, Y, R); (К, А, Y, R); (R, F, F, R); (К, Q, Y, R); (R, Т, Y, H); (Q, R, Y, R); (К, К, Y, К); (R, S, F, S) или (К, S, N, R), как раскрыто в WO 92/09690 (Genentech), которая включена в данное описание посредством ссылки.
Другие примеры соединения гормона роста, применимого в настоящем изобретении, включают hGH со следующими заменами G120R, G120K, G120Y, G120F и G120E, как раскрыто в US 6004931 (Genentech), который включен в данное описание посредством ссылки.
Другие примеры соединения гормона роста, применимого в настоящем изобретении, включают hGH со следующей серией замен R167N, D171S, E174S, F176Y и I179T; R176E, D171S, E174S и F176Y; F10A, M14W, H18D и H21N; F10A, M14W, H18D, H21N, R167N, D171S, E174S, F176Y, I179T; F10A, M14W, H18D, H21N, R167N, D171A, E174S, F176Y, I179Т; F10H, M14G, H18N и H21N; F10A, M14W, H18D, H21N, R167N, D171A, Т175Т и I179Т; и F10I, M14Q, Н18Е, R167N, D171S и 1I79Т, как имтраскрыто в US 6143523 (Genentech), который включен в данное описание посредством ссылки.
Другие примеры соединения гормона роста, применимого в настоящем изобретении, включают hGH со следующей серией замен Н18А, Q22A, F25A, D26A, Q29A, Е65А, К168А, Е174А и G120K, как раскрыто в US 6136536 (Genentech), который включен в данное описание посредством ссылки.
Другие примеры соединения гормона роста, применимого в настоящем изобретении, включают hGH со следующей серией замен H18D, H21N, R167N, K168A, D171S, K172R, E174S, I179Т, и где G120 дополнительно заменен любой из R, К, W, Y, F или Е, как раскрыто в US 6057292 (Genentech), который включен в данное описание посредством ссылки.
Другие примеры соединения гормона роста, применимого в настоящем изобретении, включают hGH со следующей серией замен H18D, H21N, R167N, K168A, D171S, K172R, E174S и I179Т, как раскрыто в US 5849535 (Genentech), который включен в данное описание посредством ссылки.
Другие примеры соединения гормона роста, применимого в настоящем изобретении, включают hGH со следующей серией замен H18D, H21D, R167N, K168A, D171S, K172R, E174S и I179T; и Н18А, Q22A, F25A, D26A, Q29A, Е65А, K168A и Е174А, как раскрыто в WO 97/11178 (Genentech), которая включена в данное описание посредством ссылки.
Другие примеры соединения гормона роста, применимого в настоящем изобретении, включают hGH со следующей серией замен К168А и Е174А; R178N и I179M; К172А и F176A; и H54F, S56E, L58I, E62S, D63N и Q66E, как раскрыто в WO 90/04788 (Genentech), которая включена в данное описание посредством ссылки.
Примеры цитокинов, которые можно модифицировать, используя способ согласно настоящему изобретению, включают эритропоэтин (ЕРО), тромбопоэтин, INF-α, IFN-β, IFN-γ, TNF-α, интерлейкин-1β (IL-1-β), IL-3, IL-4, IL-5, IL-10, IL-12, IL-15, IL-18, IL-19, IL-20, IL-21 IL-24, гранулоцитарный колониестимулирующий фактор (G-CSF), GM-CSF и хемокины, такие как воспалительный белок макрофагов-1 (МIР-1), белок, индуцируемый гамма-интерфероном, и монокины, индуцируемые IFNγ(MIG).
Конкретные примеры IL-19, применимого в способах согласно настоящему изобретению, включают те, которые раскрыты в WO 98/08870 (Human Genome Science), которая включена в данное описание посредством ссылки. Конкретно упомянут пептид, раскрытый как SEQ ID NO:2 в WO 98/08870.
Конкретные примеры применимого IL-20 включают те, которые раскрыты в WO 99/27103 (Zymogenetics), которая включена в данное описание посредством ссылки. В настоящем контексте IL-20 означает как сам IL-20 и его фрагменты, так и полипептиды, которые являются по меньшей мере на 90% идентичными IL-20 или его фрагментам. Белки, конкретно применимые в способах согласно настоящему изобретению, включают те, которые раскрыты в WO 99/27103 как SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:8, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:16, SEQ ID NO:17, SEQ ID NO:18, SEQ ID NO:19, SEQ ID NO:20, SEQ ID NO:21, SEQ ID NO:22, SEQ ID NO:23, SEQ ID NO:24, SEQ ID NO:25, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:28, SEQ ID NO:29, SEQ ID NO:30, SEQ ID NO:31, SEQ ID NO:32, SEQ ID NO:33, SEQ ID NO:34 и SEQ ID NO:35.
Примеры IL-21, применимого в способах согласно настоящему изобретению, включают те, которые раскрыты в WO 00/53761 (Zymogenetics), которая включена в данное описание посредством ссылки. Конкретно упомянут пептид, раскрытый как SEQ ID NO:2 в WO 00/53761.
TFF применим в способах согласно настоящему изобретению. Пептиды TFF представляют собой семейство пептидов, обнаруживаемых, в основном, в связи с желудочно-кишечным трактом. Конкретно упомянут пептид pS2, связанный с раком молочной железы (TFF-1), который известен у человека, мыши и крысы, спазмолитический полипептид (TFF-2), который известен у человека, свиньи, крысы и мыши, и кишечный фактор (TFF-3), который известен у человека, крысы и мыши.
Другие пептиды из семейства TFF, применимые в способах согласно настоящему изобретению, включают те, которые раскрыты в WO 02/46226 (Novo Nordisk), которая включена в данное описание посредством ссылки. Конкретно упомянут пептид TFF-2, где пептид TFF-2 с аминокислотной последовательностью SEQ ID NO:1 содержит дисульфидные мостики между Cys6-Cys104, Cys8-Cys35, Cys19-Cys34, Cys29-Cys46, Cys58-Cys84, Cys68-Cys83 и Cys78-Cys95 и где группа X независимо выбрана из остатков сахара, и олигосахариды ковалентно присоединены к Asn15.
Другие пептиды семейства TFF включают димеры TFF-1 и TFF-3, такие как раскрыты в WO 96/06861 (Novo Nordisk), которая включена в данное описание посредством ссылки.
Известно несколько рецепторов меланокортина, и конкретно упомянутые пептиды, применимые для способов согласно настоящему изобретению, представляют собой пептидные агонисты рецептора меланокортина-4, которые, как известно, обладают эффектом подавления аппетита. Конкретно упомянуты пептиды или белки, раскрытые в приведенных ниже патентных документах, которые все включены в данное описание посредством ссылки: US 6054556 (Hruby), WO 00/05263 (William Harvey Research), WO 00/35952 (Melacure), WO 00/35952 (Melacure), WO 00/58361 (Procter & Gamble), WO 01/52880 (Merck), WO 02/26774 (Procter & Gamble), WO 03/06620 (Palatin), WO 98/27113 (Rudolf Magnus Institute) и WO 99/21571 (Trega).
Другие классы пептидов или белков, которые применимы в способах согласно настоящему изобретению, включают ферменты. Многие ферменты используют в различных промышленных целях, и конкретно упомянуты гидролазы (протеазы, липазы, целлюлазы, эстеразы), оксидоредуктазы (лакказы, пероксидазы, каталазы, супероксиддисмутазы, липоксигеназы), трансферазы и изомеразы.
Другие классы пептидов или белков, которые применимы в способах согласно настоящему изобретению, включают АКТГ, фактор, высвобождающий кортикотропин, ангиотензин, кальцитонин, инсулин и его фрагменты и аналоги, глюкагон, IGF-1, IGF-2, энтерогастрин, гастрин, тетрагастрин, пентагастрин, урогастрин, эпидермальный ростовой фактор, секретин, фактор роста нервов, гормон, высвобождающий тиреотропин, соматостатин, гормон, высвобождающий гормон роста, соматомедин, паратиреоидный гормон, тромбопоэтин, эритропоэтин, гипоталамические высвобождающие факторы, пролактин, гормоны, стимулирующие щитовидную железу, эндорфины, энкефалины, вазопрессин, окситоцин, опиоиды и их аналоги, аспарагиназу, аргиназу, аргининдезаминазу, аденозиндезаминазу и рибонуклеазу.
Пептиды для модификации согласно способам согласно настоящему изобретению могут быть либо выделены из природных источников (например, растений, животных или микроорганизмов, таких как дрожжи, бактерии, грибы или вирусы), либо синтезированы. Пептиды из природных источников также включают пептиды из трансгенных источников, например из источников, которые были генетически модифицированы для экспрессии или повышенной экспрессии пептида, где указанный пептид может быть "природным" в том смысле, что он существует в природе, или "неприродным" в том смысле, что он существует только благодаря вмешательству человека. Пептиды, выделенные из природных источников, могут быть также подвергнуты синтетической модификации перед конъюгацией согласно настоящему изобретению.
В одном варианте осуществления изобретения изобретение относится к конъюгированным пептидам, которые можно получить, например, согласно способам согласно настоящему изобретению. Если конъюгированный пептид, который можно получить, например, согласно способам согласно настоящему изобретению, представляет собой терапевтический пептид, в изобретении также предложено применение таких соединений в терапии и фармацевтические композиции, содержащие такие соединения.
В одном варианте осуществления изобретения предложены конъюгированные пептиды формулы
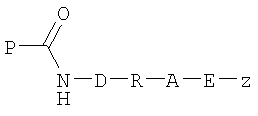
где Р, R, A, D, Е и Z являются такими, как определено выше, и где группа
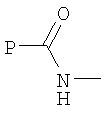
представляет собой пептидный радикал, полученный путем удаления атома водорода из -NH2 в боковой цепи остатка Gln, и их фармацевтически приемлемые соли, сольваты и пролекарства.
В частности, соединение формулы 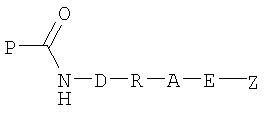 представляет собой человеческий гормон роста, который конъюгирован при положении 141, и, в частности, исключительно в данном положении.
представляет собой человеческий гормон роста, который конъюгирован при положении 141, и, в частности, исключительно в данном положении.
Конкретные примеры таких соединений включают
Nε141[2-(4-(4-(мПЭГ(20k)илбутаноил)аминобутилоксиимино)этил]hGH,
Nε141-[2-(1-(гексадеканоил)пиперидин-4-ил)этилоксиимино)этил]hGH,
Nε141(2-(4-(4-(1,3-бис(мПЭГ(20k)иламинокарбонилокси)проп-2-илокси)бутириламино)бутилоксиимино)этил)hGH,
Nε141(2-(4-(2,6-бис(мПЭГ(20k)илоксикарбониламино)гексаноиламино)бутилоксиимино)этил)hGH,
Nε141(2-(4-(4-(мПЭГ(30k)илокси)бутириламино)бутилоксиимино)этил)hGH,
Nε141(2-(4-(4-(мПЭГ(20k)илокси)бутириламино)бутилоксиимино)этил)hGH и
Nε141(2-(4-(3-(мПЭГ(30k)илокси)пропаноиламино)бутилоксиимино)этил)hGH
и их фармацевтически приемлемые соли, сольваты и пролекарства.
Как обсуждено выше, мПЭГ(20k)ил, упомянутый в приведенном выше перечне, должен обозначать мПЭГ(20k)ил с индексом полидисперсности ниже 1,06, как, например, ниже 1,05, как, например, ниже 1,04, как, например, ниже 1,03, как, например, между 1,02 и 1,03. Подобным образом, мПЭГ(30k)ил, упомянутый в приведенном выше перечне, должен обозначать мПЭГ(30k)ил с индексом полидисперсности ниже 1,06, как, например, ниже 1,05, как, например, ниже 1,04, как, например, ниже 1,03, как, например, между 1,02 и 1,03.
Как обсуждено выше, пептид может содержать более чем один Gln-остаток, в котором этот пептид можно конъюгировать. В данном случае приведенная выше формула должна также обозначать пептид, который конъюгирован более чем при одном сайте.
В той степени, в какой неконъюгированный пептид (P-C(O)-NH2) представляет собой терапевтический пептид, изобретение также относится к применению конъюгированных пептидов в терапии, и, в частности, к фармацевтическим композициям, содержащим указанные конъюгированные пептиды.
Инсулин применяют для лечения или предупреждения диабета, и, таким образом, в одном варианте осуществления изобретения предложен способ лечения диабета типа 1 или типа 2, при котором субъекту, нуждающемуся в этом, вводят терапевтически эффективное количество конъюгата инсулина или соединения инсулина согласно настоящему изобретению.
В другом варианте осуществления изобретения предложено применение конъюгата инсулина или соединения инсулина согласно настоящему изобретению для изготовления лекарственного средства, применяемого при лечении диабета типа 1 или типа 2.
GLP-1 можно применять при лечении гипергликемии, диабета типа 2, нарушенной толерантности к глюкозе, диабета типа 1, ожирения, гипертензии, синдрома X, дислипидемии, апоптоза β-клеток, дефицита β-кпеток, воспалительного кишечного синдрома, диспепсии, когнитивных расстройств, например, усиления познавательной способности, нейропротекции, атеросклероза, коронарной болезни сердца и других сердечно-сосудистых расстройств. В одном варианте осуществления изобретения, таким образом, предложен способ лечения вышеуказанных заболеваний, при котором субъекту, нуждающемуся в этом, вводят терапевтически эффективное количество конъюгата GLP-1 или соединения GLP-1 согласно настоящему изобретению.
В другом варианте осуществления изобретения предложено применение конъюгата GLP-1 или соединения GLP-1 согласно настоящему изобретению для изготовления лекарственного средства, применяемого при лечении вышеупомянутых заболеваний.
GLP-2 можно применять при лечении кишечного расстройства, приводящего к недостаточности всасывания нутриентов в кишечнике, и, в частности, GLP-2 можно применять при лечении синдрома укороченной тонкой кишки, воспалительного кишечного синдрома, болезни Крона, колита, включая коллагеновый колит, колит, вызванный облучением, атрофии после облучения, глютеновой болезни (непереносимости глютена) и тропической спру, поврежденной ткани после закупорки сосудов или травмы, диареи туристов, обезвоживания, бактериемии, сепсиса, нервной анорексии, поврежденной ткани после химиотерапии, недоношенных детей, склеродермы, гастрита, включая атрофический гастрит, атрофический гастрит после антректомии и гастрит, вызванный Helicobacter pylori, язвенной болезни, энтерита, слепого мешка, лимфатической обструкции, сосудистого заболевания и реакции «трансплантат против хозяина», заживления после хирургических процедур, атрофии после облучения и химиотерапии и остеопороза. Следовательно, задачей настоящего изобретения является разработка способов лечения вышеуказанных заболеваний, при котором субъекту, нуждающемуся в этом, вводят терапевтически эффективное количество конъюгата GLP-2 или соединения GLP-2 согласно данному изобретению.
В другом варианте осуществления изобретения предложено применение конъюгата GLP-2 или соединения GLP-2 согласно данному изобретению для изготовления лекарственного средства, применяемого при лечении вышеупомянутых заболеваний.
Гормон роста можно применять при лечении дефицита гормона роста (growth hormone deficiency, GHD); синдрома Тернера; синдрома Прадера-Вилли (ПВС); синдрома Нунан; синдрома Дауна; хронического заболевания почек, ювенильного ревматоидного артрита; муковисцидоза, ВИЧ-инфекции у детей, получающих высокоэффективную противоретровирусную терапию HAART (детей с ВИЧ-ассоциированным синдромом липодистрофии - детей с HIV/HALS); детей маленького роста, рожденных с маленьким ростом для гестационного возраста (SGA, short gestational age); детей маленького роста, рожденных с очень низкой массой для гестационного возраста (VLBW, very low birth weight), кроме маленького роста для гестационного возраста (SGA); скелетной дисплазии; гипохондроплазии; ахондроплазии; идиопатического маленького роста (ISS, idiopathic short stature); GHD у взрослых; переломов длинных костей, таких как большеберцовая кость, малоберцовая кость, бедренная кость, плечевая кость, лучевая кость, локтевая кость, ключица, пястная кость, плюсневая кость и палец; переломов губчатых костей, таких как череп, основание головы и основание стопы; пациентов после операции на сухожилиях или связках, например, в руке, колене или плече; пациентов, перенесших или переносящих вытяжение кости; пациентов после вправления диска или тазобедренного сустава, исправления мениска, артродеза позвонков или фиксации протеза, как, например, в колене, бедре, плече, локте, запястье или челюсти; пациентов, у которых закреплен материал остеосинтеза, такой как штифты, винты и пластинки; пациентов с несращением или неправильным сращением переломов; пациентов после остеатомии, например, из голени или первого пальца стопы; пациентов после имплантации трансплантата; хрящевого перерождения коленного сустава, вызванного травмой или артритом; остеопороза у пациентов с синдромом Тернера; остеопороза у мужчин; взрослых пациентов на хроническом диализе (ВПХД); сердечно-сосудистого заболевания, связанного с нарушением питания, у ВПХД; восстановления кахексии у ВПХД; рака у ВПХД; хронической обструктивной болезни легких у ВПХД; ВИЧ у ВПХД; старения у ВПХД; хронического заболевания печени у ВПХД, синдрома усталости у ВПХД; болезни Крона; нарушения функции печени; мужчин с ВИЧ-инфекциями; синдрома укороченной тонкой кишки; центрального ожирения; синдрома липодистрофии, связанного с ВИЧ (HALS, HIV-associated lipodystrophy syndrome); мужского бесплодия; пациентов после обширного оперативного вмешательства, алкогольной/лекарственной детоксикации или неврологической травмы; старения; хрупкости костей у пожилых; остеоартрита; травматически поврежденного хряща; эректильной дисфункции; фибромиалгии; расстройств памяти; деперессии; травматического повреждения головного мозга; субарахноидального кровоизлияния; очень низкой массы при рождении; метаболического синдрома; миопатии, вызванной глюкокортикоидами; или маленького роста у детей вследствие лечения глюкокортикоидами, для ускорения заживления мышечной ткани, нервной ткани или ран; ускорения или улучшения кровотока к поврежденной ткани или уменьшения вероятности инфицирования поврежденной ткани. Способ лечения согласно изобретению включает введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы I. В настоящем изобретении, таким образом, предложен способ лечения указанных заболеваний или состояний, при котором пациенту, нуждающемуся в этом, вводят терапевтически эффективное количество конъюгата гормона роста или соединения гормона роста согласно настоящему изобретению.
Как правило, количество вводимого конъюгированного гормона роста находится в интервале 10-7-10-3 г/кг массы тела, как, например, 10-6-10-4 г/кг массы тела, как, например, 10-5-10-4 г/кг массы тела.
В другом варианте осуществления изобретения предложено применение конъюгата гормона роста или соединения гормона роста для изготовления лекарственного средства, применяемого при лечении вышеупомянутых заболеваний или состояний.
Цитокины играют роль в этиологии множества заболеваний, в которые вовлечена иммунная система. В частности, известно, что IL-20 может быть вовлечен в псориаз и его лечение, a IL-21 вовлечен в рак и может составлять терапию при данном заболевании. В одном варианте осуществления изобретения предложен способ лечения псориаза, при котором пациенту вводят терапевтически эффективное количество конъюгата IL-20 согласно настоящему изобретению. В другом варианте осуществления изобретения изобретение относится к применению конъюгата IL-20 согласно настоящему изобретению для изготовления лекарственного средства, применяемого при лечении псориаза.
В другом варианте осуществления изобретения настоящее изобретение относится к способу лечения рака, при котором субъекту, нуждающемуся в этом, вводят терапевтически эффективное количество конъюгата IL-21 согласно настоящему изобретению.
В другом варианте осуществления изобретения изобретение относится к применению конъюгата IL-21 согласно настоящему изобретению для изготовления лекарственного средства, применяемого при лечении рака.
Пептиды TFF можно применять для увеличения вязкости слизистых слоев у субъекта, для уменьшения секреции слюны, например, где увеличение секреции слюны вызвано лучевой терапией, лечением антихолинергическими агентами или синдромом Шегрена, для лечения аллергического ринита, вызванных стрессом язв желудка, вторичных по отношению к травме, шоку, обширным операциям, заболеваниям почек или печени, лечению НСПВЛ (нестероидными противовоспалительными лекарствами), например, аспирином, стероидами или алкоголю. Пептиды TFF можно также применять для лечения болезни Крона, неспецифического язвенного колита, кератоконъюнктивита, хронических инфекций мочевого пузыря, интерстициального цистита, папиллом и рака мочевого пузыря. В одном варианте осуществления изобретения, таким образом, изобретение относится к способу лечения вышеупомянутых заболеваний или состояний, при котором пациенту, нуждающемуся в этом, вводят терапевтически эффективное количество конъюгата TFF согласно настоящему изобретению.
В другом аспекте изобретение относится к применению конъюгата TFF согласно настоящему изобретению для изготовления лекарственного средства для лечения вышеупомянутых заболеваний или состояний.
Модификаторы рецепторов меланокортина, и, в частности, агонисты рецептора меланокортина 4, играют роль при лечении и предупреждении ожирения и родственных заболеваний. В одном варианте осуществления изобретения предложен способ предупреждения или замедления прогрессирования нарушенной толерантности к глюкозе (НТГ) до инсулиннезависимого диабета типа 2, предупреждения или замедления прогрессирования инсулиннезависимого диабета типа 2 до инсулинозависимого диабета, лечения ожирения и регуляции аппетита. Агонисты рецептора меланокортина 4 также вовлечены в лечение заболеваний, выбранных из атеросклероза, гипертензии, диабета, диабета типа 2, нарушенной толерантности к глюкозе (НТГ), дислипидемии, коронарной болезни сердца, болезни желчного пузыря, камней желчного пузыря, остеоартрита, рака, половой дисфункции и риска преждевременной смерти. В одном варианте осуществления изобретения, таким образом, предложен способ лечения вышеупомянутых заболеваний или состояний, при котором субъекту, нуждающемуся в этом, вводят терапевтически эффективное количество конъюгата агониста рецептора меланокортина 4 согласно настоящему изобретению.
Еще в одном аспекте изобретение относится к применению конъюгата агониста рецептора меланокортина 4 согласно настоящему изобретению для изготовления лекарственного средства для лечения вышеупомянутых заболеваний или состояний.
Соединения фактора VII полезны при лечении заболевания, связанного со свертыванием крови, и биологически активные соединения фактора VII, в частности, полезны при лечении больных гемофилиями, больных гемофилиями с ингибиторами факторов VIII и IX, пациентов с тромбоцитопенией, пациентов с тромбоцитопатиями, такими как тромбастения Гланцманна, нарушение высвобождения тромбоцитов и дефекты пула хранения (форма врожденного функционального дефекта тромбоцитов, приводящего к увеличению времени кровотечения), пациентов с болезнью Виллебранда, пациентов с заболеванием печени и проблемами кровотечения, связанными с травмами или с операцией. Биологически неактивные соединения фактора VII полезны при лечении пациентов, находящихся в состоянии гиперкоагуляции, таких как пациенты с сепсисом, тромбозом глубоких вен, пациентов с риском инфаркта миокарда или тромботического шока, легочной эмболии, пациентов с острыми коронарными синдромами, пациентов, перенесших коронарное шунтирование, предупреждения инфарктов и рестеноза у пациента, перенесшего пластическую операцию на сосудах, пациентов с периферическими сосудистыми заболеваниями и острым респираторным дистресс-синдромом. В одном варианте осуществления изобретения, таким образом, предложен способ лечения вышеупомянутых заболеваний или состояний, при котором субъекту, нуждающемуся в этом, вводят терапевтически эффективное количество конъюгата соединения фактора VII согласно настоящему изобретению.
В другом варианте осуществления изобретения предложено применение конъюгата соединения фактора VII согласно настоящему изобретению для изготовления лекарственного средства, применяемого при лечении вышеупомянутых заболеваний или состояний.
Многие заболевания лечат, применяя более чем одно лекарство при лечении, которые вводят либо одновременно, либо последовательно. Следовательно, в пределах объема настоящего изобретения находится применение пептидных конъюгатов согласно настоящему изобретению в терапевтических способах для лечения одного или более чем одного из вышеупомянутых заболеваний в комбинации с одним или более чем одним другим терапевтически активным соединением, обычно применяемым при лечении указанного заболевания. По аналогии также в пределах объема настоящего изобретения находится применение пептидных конъюгатов согласно настоящему изобретению в комбинации с другими терапевтически активными соединениями, обычно применяемыми при лечении одного или более чем одного из вышеупомянутых заболеваний, для изготовления лекарственного средства для лечения указанного заболевания.
Как обсуждено выше, терапевтические пептиды, конъюгированные согласно способам согласно настоящему изобретению, можно применять в терапии, и это также составляет воплощение настоящего изобретения.
В другом варианте осуществления изобретения предложено применение конъюгированных пептидов согласно настоящему изобретению в диагностике.
ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
Другой задачей является разработка фармацевтической композиции, содержащей конъюгированный пептид, такой как конъюгированный гормон роста (GH) согласно настоящему изобретению, в концентрации от 10-15 мг/мл до 200 мг/мл, как, например, от 10-10 мг/мл до 5 мг/мл, и где указанная композиция имеет pH от 2,0 до 10,0. Эта композиция может дополнительно содержать буферную систему, консервант(ы), тонический(е) агент(ы), хелатирующий(е) агент(ы), стабилизаторы и сурфактанты. В одном варианте осуществления изобретения фармацевтическая композиция представляет собой водную композицию, то есть композицию, содержащую воду. Такая композиция, как правило, представляет собой раствор или суспензию. В следующем варианте осуществления изобретения фармацевтическая композиция представляет собой водный раствор. Термин "водная композиция" означает композицию, содержащую по меньшей мере 50 мас.% воды. Подобным образом термин "водный раствор" означает раствор, содержащий по меньшей мере 50 мас.% воды, а термин "водная суспензия" определяют как суспензию, содержащую по меньшей мере 50 мас.% воды.
В другом варианте осуществления изобретения фармацевтическая композиция представляет собой лиофилизированную композицию, в которую врач или пациент добавляет растворители и/или разбавители перед применением.
В другом варианте осуществления изобретения фармацевтическая композиция представляет собой высушенную композицию (например, лиофилизированную или высушенную распылительной сушкой), готовую к применению без какого-либо предварительного растворения.
В следующем варианте осуществления изобретения изобретение относится к фармацевтической композиции, содержащей водный раствор пептидного конъюгата, такого как, например, конъюгат GH, и буфер, где указанный пептидный конъюгат, такой как, например, конъюгат GH, присутствует в концентрации от 0,1-100 мг/мл или выше и где указанная композиция имеет рН от примерно 2,0 до примерно 10,0.
В другом варианте осуществления изобретения pH композиции выбран из перечня, состоящего из 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3,0, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4,0, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9, 5,0, 5,1, 5,2, 5,3, 5,4, 5,5, 5,6, 5,7, 5,8, 5,9, 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9, 7,0, 7,1, 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8, 7,9, 8,0, 8,1, 8,2, 8,3, 8,4, 8,5, 8,6, 8,7, 8,8, 8,9, 9,0, 9,1, 9,2, 9,3, 9,4, 9,5, 9,6, 9,7, 9,8, 9,9 и 10,0.
В следующем варианте осуществления изобретения буфер выбран из группы, состоящей из ацетата натрия, карбоната натрия, цитрата, глицилглицина, гистидина, глицина, лизина, аргинина, дигидрофосфата натрия, динатрия гидрофосфата, фосфата натрия и трис(гидроксиметил)аминометана, бицина, трицина, яблочной кислоты, сукцината, малеиновой кислоты, фумаровой кислоты, винной кислоты, аспарагиновой кислоты или их смесей. Каждый из этих конкретных буферов составляет альтернативный вариант изобретения.
В следующем варианте осуществления изобретения композиция дополнительно содержит фармацевтически приемлемый консервант. В следующем варианте осуществления изобретения консервант выбран из группы, состоящей из фенола, орто-крезола, мета-крезола, пара-крезола, метил-пара-гидроксибензоата, пропил-пара-гидроксибензоата, 2-феноксиэтанола, бутил-пара-гидроксибензоата, 2-фенилэтанола, бензилового спирта, хлорбутанола и тиомеросала, бронопола, бензойной кислоты, имидмочевины, хлоргексидина, дегидроацетата натрия, хлоркрезола, этил-пара-гидроксибензоата, бензетония хлорида, хлорфенезина (3-пара-хлорфеноксипропан-1,2-диола) или их смесей. В следующем варианте осуществления изобретения консервант присутствует в концентрации от 0,1 мг/мл до 20 мг/мл. В следующем варианте осуществления изобретения консервант присутствует в концентрации от 0,1 мг/мл до 5 мг/мл. В следующем варианте осуществления изобретения консервант присутствует в концентрации от 5 мг/мл до 10 мг/мл. В следующем варианте осуществления изобретения консервант присутствует в концентрации от 10 мг/мл до 20 мг/мл. Каждый из этих конкретных консервантов составляет альтернативный вариант изобретения. Применение консерванта в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделана ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
В следующем варианте осуществления изобретения композиция дополнительно содержит изотонический агент. В следующем варианте осуществления изобретения изотонический агент выбран из группы, состоящей из соли (например, хлорида натрия), сахара или сахарного спирта, аминокислоты (например, L-глицина, L-гистидина, аргинина, лизина, изолейцина, аспарагиновой кислоты, триптофана, треонина), альдита (например, глицерола (глицерина), 1,2-пропандиола (пропиленгликоля), 1,3-пропандиола, 1,3-бутандиола), полиэтиленгликоля (например, ПЭГ400) или их смесей. Можно использовать любой сахар, такой как моно-, ди- или полисахариды или растворимые в воде глюканы, включая, например, фруктозу, глюкозу, маннозу, сорбозу, ксилозу, мальтозу, лактозу, сахарозу, трегалозу, декстран, пуллулан, декстрин, циклодекстрин, растворимый крахмал, гидроксиэтилкрахмал и карбоксиметилцеллюлоза Na. В одном варианте осуществления изобретения сахарная добавка представляет собой сахарозу. Сахарный спирт определен как С4-С8 углеводород, имеющий по меньшей мере одну группу -ОН, и включает, например, маннит, сорбит, инозит, галактит, дульцит, ксилит и арабит. В одном варианте осуществления изобретения добавка сахарного спирта представляет собой маннит. Сахара или сахарные спирты, упомянутые выше, можно использовать индивидуально или в комбинации. Не существует фиксированного предела используемого количества до тех пор, пока сахар или сахарный спирт растворим в жидком препарате и не оказывает вредного воздействия на стабилизирующие эффекты, полученные при использовании способов по изобретению. В одном варианте осуществления изобретения концентрация сахара или сахарного спирта составляет между примерно 1 мг/мл и примерно 150 мг/мл. В следующем варианте осуществления изобретения изотонический агент присутствует в концентрации от 1 мг/мл до 50 мг/мл. В следующем варианте осуществления изобретения изотонический агент присутствует в концентрации от 1 мг/мл до 7 мг/мл. В следующем варианте осуществления изобретения изотонический агент присутствует в концентрации от 8 мг/мл до 24 мг/мл. В следующем варианте осуществления изобретения изотонический агент присутствует в концентрации от 25 мг/мл до 50 мг/мл. Каждый из этих конкретных изотонических агентов составляет альтернативный вариант изобретения. Применение изотонического агента в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделана ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
В следующем варианте осуществления изобретения композиция дополнительно содержит хелатирующий агент. В следующем варианте осуществления изобретения хелатирующий агент выбран из группы, состоящей из солей этилендиаминтетрауксусной кислоты (ЭДТА), лимонной кислоты и аспарагиновой кислоты и их смесей. В следующем варианте осуществления изобретения хелатирующий агент присутствует в концентрации от 0,1 мг/мл до 5 мг/мл. В следующем варианте осуществления изобретения хелатирующий агент присутствует в концентрации от 0,1 мг/мл до 2 мг/мл. В следующем варианте осуществления изобретения хелатирующий агент присутствует в концентрации от 2 мг/мл до 5 мг/мл. Каждый из этих конкретных хелатирующих агентов составляет альтернативный вариант изобретения. Применение хелатирующего агента в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделана ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
В следующем варианте осуществления изобретения композиция дополнительно содержит стабилизатор. Применение стабилизатора в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделена ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
Более конкретно композиции по изобретению представляют собой стабилизированные жидкие фармацевтические композиции, терапевтически активные компоненты которых включают белок, который может образовывать агрегаты в процессе хранения в жидких фармацевтических композициях. Под "образованием агрегатов" понимают физическое взаимодействие между молекулами белка, результатом которого является образование олигомеров, которые могут оставаться растворимыми, или больших видимых агрегатов, которые осаждаются из раствора. Под "процессом хранения" подразумевают, что жидкую фармацевтическую композицию или композицию, как только она изготовлена, не сразу вводят субъекту. Вероятно, после изготовления ее упаковывают для хранения либо в жидкой форме, либо в замороженном состоянии, либо в высушенной форме для последующего восстановления до жидкой формы или другой формы, пригодной для введения субъекту. Под "высушенной формой" подразумевают, что жидкую фармацевтическую композицию или композицию высушивают либо путем сушки вымораживанием (то есть лиофилизации; см., например, Williams and Polli (1984) J. Parenteral Sci. Technol. 38:48-59), либо распылительной сушки (см. Masters (1991) в Spray-Drying Handbook (5th ed; Longman Scientific and Technical, Essez, U.K.), pp.491-676; Broadhead et al. (1992) Drug Devel. Ind. Pharm. 18:1169-1206; и Mumenthaler et al. (1994) Pharm. Res. 11:12-20), либо сушки на воздухе (Carpenter and Crowe (1988) Cryobiology 25: 459-470, и Roser (1991) Biopharm. 4:47-53). Образование агрегатов белком в процессе хранения жидкой фармацевтической композиции может оказывать вредное воздействие на биологическую активность этого белка, что приводит в результате к потере терапевтической эффективности фармацевтической композиции. Кроме того, образование агрегатов может вызвать другие проблемы, такие как закупорка трубок, мембран или насосов, когда фармацевтическую композицию, содержащую белок, вводят с использованием инфузионной системы.
Фармацевтические композиции по изобретению могут дополнительно содержать количество аминокислотного основания, достаточное для уменьшения образования агрегатов белком в процессе хранения композиции. Под "аминокислотным основанием" подразумевают аминокислоту или комбинацию аминокислот, где любая данная аминокислота присутствует либо в ее форме свободного основания, либо в форме ее соли. Где используют комбинацию аминокислот, все аминокислоты могут присутствовать в их форме свободного основания, все могут присутствовать в их солевых формах либо некоторые могут присутствовать в их формах свободного основания, тогда как другие присутствуют в их солевых формах. В одном варианте осуществления изобретения аминокислоты для использования при изготовлении композиций по изобретению представляет собой аминокислоты, несущие заряженную боковую цепь, такие как аргинин, лизин, аспарагиновая кислота и глутаминовая кислота. Любой стереоизомер (то есть L или D изомер или их смеси) конкретной аминокислоты (метионина, гистидина, аргинина, лизина, изолейцина, аспарагиновой кислоты, триптофана, треонина и их смесей), либо комбинации этих стереоизомеров, либо глицин, либо органическое основание, такое как, но не ограниченное им, имидазол, может присутствовать в фармацевтических композициях по изобретению, пока конкретная аминокислота или органическое основание присутствует либо в его форме свободного основания, либо в его солевой форме. В одном варианте осуществления изобретения используют L-стереоизомер аминокислоты. В одном варианте осуществления изобретения используют L-стереоизомер. Препараты композиций по изобретению можно также готовить с аналогами этих аминокислот. Под "аналогом аминокислоты" подразумевают производное встречающейся в природе аминокислоты, которое производит желаемый эффект уменьшения образования агрегатов белком в процессе хранения жидких фармацевтических композиций по изобретению. Подходящие аналоги аргинина включают, например, аминогуанидин, орнитин и N-моноэтил-L-аргинин, подходящие аналоги метионина включают этионин и бутионин и подходящие аналоги цистеина включают S-метил-L-цистеин. Что касается других аминокислот, аналоги этих аминокислот включают в композиции либо в их форме свободного основания, либо в их солевой форме. В следующем варианте осуществления изобретения аминокислоты или аналоги аминокислот используют в концентрации, которая является достаточной для предотвращения или замедления агрегации белка.
В следующем варианте осуществления изобретения метионин (или другие серосодержащие аминокислоты или аналоги аминокислот) можно добавлять для ингибирования окисления метиониновых остатков до метионинсульфоксида, когда белок, действующий в качестве терапевтического агента, представляет собой белок, содержащий по меньшей мере один остаток метионина, чувствительный к такому окислению. Под "ингибированием" подразумевают минимальное накопление продуктов окисления метионина с течением времени. Ингибирование окисления метионина приводит в результате к более длительному сохранению белка в его правильной молекулярной форме. Можно использовать любой стереоизомер метионина (L или D изомер) или любые их комбинации. Количество, которое нужно добавлять, должно составлять достаточное количество для ингибирования окисления остатков метионина, так чтобы количество метионинсульфоксида было приемлемым для регламентирующих ведомств. Как правило, это означает, что композиция содержит не более чем от примерно 10% до примерно 30% метионинсульфоксида. Как правило, этого можно достичь путем добавления метионина, так чтобы отношение добавленного метионина к остаткам метионина находилось в интервале от примерно 1:1 до примерно 1000:1, как, например, от 10:1 до примерно 100:1.
В следующем варианте осуществления изобретения композиция дополнительно содержит стабилизатор, выбранный из группы, состоящей из высокомолекулярных полимеров или низкомолекулярных соединений. В следующем варианте осуществления изобретения стабилизатор выбран из полиэтиленгликоля (например, ПЭГ3350), поливинилового спирта (ПВС), поливинилпирролидона, карбокси/гидроксицеллюлозы или ее производных (например, НРС, HPC-SL, HPC-L и НРМС), циклодекстринов, серосодержащих веществ, таких как монотиоглицерин, тиогликолевая кислота и 2-метилтиоэтанол, и различных солей (например, хлорида натрия). Каждый из этих конкретных стабилизаторов составляет альтернативный вариант изобретения.
Фармацевтические композиции могут также содержать дополнительные стабилизирующие агенты, которые дополнительно усиливают стабильность терапевтически активного белка в них. Стабилизирующие агенты, представляющие особый интерес для настоящего изобретения, включают, но не ограничены ими, метионин и ЭДТА, которые защищают белок от окисления метионина, и неионный сурфактант, который защищает белок от агрегации, связанной с замораживанием-оттаиванием или с механическим сдвигом.
В следующем варианте осуществления изобретения композиция дополнительно содержит сурфактант. В следующем варианте осуществления изобретения сурфактант выбран из детергента, этоксилированного касторового масла, полигликозилированных глицеридов, ацетилированных моноглицеридов, сорбитановых эфиров жирных кислот, блоксополимеров полиоксипропилена-полиоксиэтилена (например, полоксамеров, таких как Pluronic® F68, полоксамер 188 и 407, тритон Х-100), полиоксиэтиленсорбитановых эфиров жирных кислот, производных полиоксиэтилена и полиэтилена, таких как алкилированные и алкоксилированные производные (твины, например, твин-20, твин-40, твин-80 и Brij-35), моноглицеридов или их этоксилированных производных, диглицеридов или их полиоксиэтиленовых производных, спиртов, глицерина, пектинов и фосфолипидов (например, фосфатидилсерина, фосфатидилхолина, фосфатидилэтаноламина, фосфатидилинозита, дифосфатидилглицерина и сфингомиелина), производных фосфолипидов (например, дипальмитоилфосфатидной кислоты) и лизофосфолипидов (например, пальмитоил-лизофосфатидил-L-серина и 1-ацил-sn-глицеро-3-фосфатных эфиров этаноламина, холина, серина или треонина) и алкил-, алкоксил(алкиловый эфир)-, алкокси(алкиловый эфир)производных лизофосфатидил- и фосфатидилхолинов, например, лауроил- и миристоилпроизводных лизофосфатидилхолина, дипальмитоилфосфатидилхолина и модификаций главной полярной группы, то есть холинов, этаноламинов, фосфатидной кислоты, серинов, треонинов, глицерина, инозита и положительно заряженных DODAC, DOTMA, DCP, BISHOP, лизофосфатидилсерина и лизофосфатидилтреонина, и глицерофосфолипидов (например, кефалинов), глицерогликолипидов (например, галактопиранозида), сфингогликолипидов (например, церамидов, ганглиозидов), додецилфосфохолина, лизолецитина куриного яйца, производных фусидовой кислоты (например, тауро-дигидрофусидата натрия), длинноцепочечных жирных кислот и их солей C6-C12 (например, олеиновой кислоты и каприловой кислоты), ацилкарнитинов и их производных, Nα-ацилированных производных лизина, аргинина или гистидина или ацилированных по боковой цепи производных лизина или аргинина, Nα-ацилированных производных дипептидов, содержащих любую комбинацию лизина, аргинина или гистидина и нейтральной или кислой аминокислоты, Nα-ацилированного производного трипептида, содержащего любую комбинацию нейтральной аминокислоты и двух заряженных аминокислот, DSS (докузата натрия, регистрационный №CAS[577-11-7]), докузата кальция, регистрационный №CAS[128-49-4]), докузата калия, регистрационный №CAS[7491-09-0]), ДСН (додецилсульфата натрия или лаурилсульфата натрия), каприлата натрия, холевой кислоты или ее производных, желчных кислот и их солей и конъюгатов глицина или таурина, урсодезоксихолевой кислоты, холата натрия, дезоксихолата натрия, таурохолата натрия, гликохолата натрия, N-гексадецил-N,N-диметил-3-аммонио-1-пропансульфоната, анионных (алкил-арил-сульфонаты) одновалентных сурфактантов, цвиттерионных сурфактантов (например, N-алкил-N,N-диметиламмонио-1-пропансульфонатов, 3-холамидо-1-пропилдиметиламмонио-1-пропансульфоната, катионных сурфактантов (оснований четвертичного аммония) (например, цетил-триметиламмония бромида, цетилпиридиния хлорида), неионных сурфактантов (например, додецил-β-D-гликопиранозида), полоксаминов (например, Tetronic), которые представляют собой тетрафункциональные блоксополимеры, полученные путем последовательного добавления пропиленоксида и этиленоксида к этилендиамину, либо сурфактант может быть выбран из группы производных имидазолина и их смесей. Каждый из этих конкретных сурфактантов составляет альтернативный вариант изобретения.
Применение сурфактанта в фармацевтических композициях хорошо известно специалистам в данной области техники. Для удобства сделена ссылка на Remington: The Science and Practice of Pharmacy, 20th edition, 2000.
Возможно, что в фармацевтической композиции согласно настоящему изобретению могут присутствовать другие ингредиенты. Такие дополнительные ингредиенты могут включать увлажняющие агенты, эмульгаторы, антиоксиданты, сыпучие агенты, модификаторы тоничности, хелатирующие агенты, ионы металлов, маслянистые наполнители, белки (например, человеческий сывороточный альбумин, желатин или белки) и цвиттерион (например, аминокислоту, такую как бетаин, таурин, аргинин, глицин, лизин и гистидин). Такие дополнительные ингредиенты, конечно, не должны оказывать вредное влияние на общую стабильность фармацевтической композиции согласно настоящему изобретению.
Фармацевтические композиции, содержащие пептидный конъюгат, такой как, например, конъюгат GH согласно настоящему изобретению, можно вводить пациенту, нуждающемуся в таком лечении, местно, например на кожу и слизистую, в органы, где исключено всасывание, например в артерию, в вену, в сердце, и в органы, где происходит всасывание, например в кожу, под кожу, в мышцу или в брюшину.
Введение фармацевтических композиций согласно изобретению пациентам, нуждающимся в таком лечении, можно осуществлять посредством нескольких путей введения, например язычного, подъязычного, трансбуккального, в рот, перорального, в желудок и кишечник, назального, легочного, например через бронхиолы и альвеолы или их сочетанием, эпидермального, кожного, чрескожного, вагинального, ректального, глазного, например через конъюнктиву, уретрального и парентерального.
Композиции согласно настоящему изобретению можно вводить в нескольких лекарственных формах, например в виде растворов, суспензий, эмульсий, микроэмульсий, многослойной эмульсии, пенок, мазей, паст, пластырей, твердых мазей, таблеток, покрытых таблеток, полосканий, капсул, например твердых желатиновых капсул и мягких желатиновых капсул, суппозиториев, ректальных капсул, капель, гелей, спреев, порошков, аэрозолей, ингаляторов, глазных капель, глазных мазей, глазных полосканий, вагинальных пессариев, вагинальных колец, вагинальных мазей, инъекционного раствора, растворов, превращающихся in situ, например образующих гель in situ, выпадающих в осадок in situ, осаждающихся in situ, кристаллизующихся in situ, в виде инфузионного раствора и имплантатов.
Композиции по изобретению можно дополнительно компаундировать или соединять, например, посредством ковалентных, гидрофобных и электростатических взаимодействий, с носителем лекарства, системой доставки лекарства и усовершенствованной системой доставки лекарства с задачей дополнительного усиления стабильности конъюгата GH, повышения биологической доступности, повышения растворимости, уменьшения вредных эффектов, достижения хронотерапии, хорошо известной специалистам в данной области техники, и улучшения соблюдения пациентом режима и схемы лечения, либо любого сочетания этих целей. Примеры носителей, систем доставки лекарства и усовершенствованных систем доставки лекарства включают, но не ограничены ими, полимеры, например, целлюлозу и ее производные, полисахариды, например декстран и производные, крахмал и производные, поливиниловый спирт) полимеры акрилата и метакрилата, полимолочной и полигликолевой кислоты и их блоксополимеры, полиэтиленгликоли, белки-носители, например альбумин, гели, например, системы термогелеобразования, например, блоксополимерные системы, хорошо известные специалистам в данной области техники, мицеллы, липосомы, микросферы, наночастицы, жидкие кристаллы и их дисперсии, L2 фазу и ее дисперсию, хорошо известную специалистам в области поведения фаз в липидно-водных системах, полимерные мицеллы, многослойные эмульсии, самоэмульгирующие, самомикроэмульгирующие, циклодекстрины и их производные, и дендримеры.
Композиции согласно настоящему изобретению полезны при составлении твердых веществ, полутвердых веществ, порошка и растворов для легочного введения пептидного конъюгата, такого как, например, конъюгат GH, используя, например, ингалятор с дозатором, ингалятор сухого порошка и небулайзер, причем все они представляют собой устройства, хорошо известные специалистам в данной области техники.
Композиции согласно настоящему изобретению особенно полезны при составлении систем доставки лекарств регулируемого, ограниченного, пролонгированного, запаздывающего и медленного высвобождения. Более конкретно, но не ограничиваясь этим, композиции полезны при составлении систем парентерально регулируемого высвобождения и ограниченного высвобождения (обе системы приводят к многократному снижению числа введений), хорошо известных специалистам в данной области техники. Даже более предпочтительными являются системы регулируемого высвобождения и ограниченного высвобождения, вводимые подкожно. Без ограничения объема изобретения примерами полезных систем и композиций регулируемого высвобождения являются гидрогели, масляные гели, жидкие кристаллы, полимерные мицеллы, микросферы, наночастицы.
Способы получения систем регулируемого высвобождения, полезных для композиций согласно настоящему изобретению, включают, но не ограничены ими, кристаллизацию, конденсацию, совместную кристаллизацию, осаждение, соосаждение, эмульгирование, дисперсию, гомогенизацию высокого давления, инкапсулирование, распылительную сушку, микроинкапсулирование, коацервацию, разделение фаз, выпаривание растворителя с получением микросфер, экструзию и сверхкритические процессы с псевдоожиженным материалом. Общая ссылка сделана на Handbook of Pharmaceutical Controlled Release (Wise, D.L., ed. Marcel Dekker, New York, 2000) и Drug and the Pharmaceutical Sciences vol.99: Protein Composition and Delivery (MacNally, E.J., ed. Marcel Dekker, New York, 2000).
Парентеральное введение можно осуществлять путем подкожной, внутримышечной, внутрибрюшинной или внутривенной инъекции с помощью шприца, возможно шприца карандашного типа. Альтернативно парентеральное введение можно осуществлять с помощью инфузионного насоса. Дополнительной возможностью является композиция, которая может представлять собой раствор или суспензию для введения пептидного конъюгата, такого как, например, конъюгат GH, в форме назального или легочного спрея. В качестве еще одной дополнительной возможности фармацевтические композиции, содержащие пептидный конъюгат, такой как, например, конъюгат GH, по изобретению, можно также адаптировать для чрескожного введения, например, путем безыгольной инъекции или из пластыря, возможно ионофоретического пластыря, или введения через слизистую оболочку, например, трансбуккального.
Термин "стабилизированная композиция" относится к композиции с повышенной физической стабильностью, повышенной химической стабильностью или повышенной физической и химической стабильностью.
Термин "физическая стабильность" белковой композиции, как его используют здесь, относится к склонности белка к образованию биологически неактивных и/или нерастворимых агрегатов белка в результате термо-механических напряжений и/или взаимодействия с границами раздела и поверхностями, которые являются дестабилизирующими, такими как гидрофобные поверхности и границы раздела. Физическую стабильность водных белковых композиций оценивают с помощью визуальной проверки и/или измерений мутности после воздействия на композицию, заполненную в подходящие контейнеры (например, картриджи или флаконы), механической/физической нагрузки (например, перемешивания) при различных температурах в течение различных периодов времени. Визуальную проверку композиций осуществляют в контрастном сфокусированном свете при темном фоне. Мутность композиции характеризуют с помощью визуальной оценки, оценивая степень мутности, например, по шкале от 0 до 3 (композиция, не проявляющая мутности, соответствует визуальному баллу 0, а композиция, проявляющая визуальную мутность при дневном свете, соответствует визуальному баллу 3). Композицию классифицируют как физически нестабильную в отношении агрегации белка, когда она проявляет визуальную мутность при дневном свете. Альтернативно мутность композиции можно оценить с помощью простых измерений мутности, хорошо известных специалистам в данной области техники. Физическую стабильность водных белковых композиций можно также оценить путем использования спектроскопического агента или зонда конформационного состояния белка. Этот зонд предпочтительно представляет собой малую молекулу, которая преимущественно связывается с ненативным конформером белка. Одним из примеров низкомолекулярного спектроскопического зонда структуры белка является тиофлавин Т. Тиофлавин Т представляет собой флуоресцентный краситель, который широко использовался для обнаружения амилоидных фибрилл. В присутствии фибрилл а также, возможно, других конфигураций белка тиофлавин Т образует новый максимум возбуждения примерно при 450 нм и усиленную эмиссию примерно при 482 нм, когда он связывается с фибриллярной формой белка. Несвязанный тиофлавин Т является по существу не флуоресцентным при этих длинах волн.
Другие малые молекулы можно использовать в качестве зондов изменений в структуре белка от нативных до не нативных состояний, например, зонды "гидрофобный пэтч", которые преимущественно связываются с обнаженными гидрофобными пэтчами белка. Эти гидрофобные пэтчи обычно углублены внутри третичной структуры белка в его нативном состоянии, но становятся обнаженными, когда белок начинает развертываться или денатурировать. Примерами этих низкомолекулярных спектроскопических зондов являются ароматические, гидрофобные красители, такие как антрацен, акридин, фенантролин или подобные. Другие спектроскопические зонды представляют собой комплексы металл-аминокислота, такие как комплексы металла кобальта и гидрофобных аминокислот, таких как фенилаланин, лейцин, изолейцин, метионин или валин, или тому подобных.
Термин "химическая стабильность" белковой композиции, как его используют здесь, относится к химическим ковалентным изменениям в структуре белка, приводящим к образованию продуктов химического разрушения с потенциальной меньшей биологической эффективностью и/или потенциальными повышенными иммунологическими свойствами по сравнению с нативной структурой белка. Различные продукты химического разрушения могут образоваться в зависимости от типа и природы нативного белка и окружения, воздействию которого подвергается этот белок. Скорее всего трудно полностью исключить химическое разрушение белка, и в процессе хранения и применения белковой композиции часто возрастает количество продуктов химического разрушения, как хорошо известно специалистам в данной области техники. Большинство белков склонно к деамидированию, процессу, при котором амидная группа боковой цепи в остатках глутаминила или аспарагинила гидролизуется с образованием свободной карбоновой кислоты. Другие пути разрушения включают образование высокомолекулярных продуктов превращения, где две или более чем две молекулы белка ковалентно связываются друг с другом посредством трансамидирования и/или дисульфидных взаимодействий, приводящих к образованию ковалентно связанных димерных, олигомерных и полимерных продуктов разрушения (Stability of Protein Pharmaceuticals, Ahern. T.J. & Manning M.C., Plenum Press, New York 1992). Окисление (например, остатков метионина) можно упомянуть как другой вариант химического разрушения. Химическую стабильность белковой композиции можно оценить путем измерения продуктов химического разрушения в различные моменты времени при воздействии различных окружающих условий (образование продуктов расщепления можно часто ускорить, например, путем повышения температуры). Количество каждого индивидуального продукта разрушения часто определяют путем разделения продуктов разрушения в зависимости от размера молекулы и/или заряда, используя различные хроматографические методики (например, эксклюзионной ВЭЖХ по размеру и/или ВЭЖХ с обращенной фазой).
Следовательно, как изложено выше, "стабилизированная композиция" относится к композиции с повышенной физической стабильностью, повышенной химической стабильностью или повышенной физической и химической стабильностью. В целом композиция должна быть стабильной в процессе применения и хранения (при соблюдении рекомендованных условий применения и хранения) вплоть до истечения срока годности.
В одном варианте осуществления изобретения фармацевтическая композиция, содержащая конъюгат GH, стабильна в течение более чем 6 недель применения и в течение более 3 лет хранения.
В другом варианте осуществления изобретения фармацевтическая композиция, содержащая конъюгат GH, стабильна в течение более чем 4 недель применения и в течение более 3 лет хранения.
В следующем варианте осуществления изобретения фармацевтическая композиция, содержащая конъюгат GH, стабильна в течение более чем 4 недель применения и в течение более двух лет хранения.
Еще в одном следующем варианте осуществления изобретения фармацевтическая композиция, содержащая конъюгат GH, стабильна в течение более чем 2 недель применения и в течение более двух лет хранения.
Все цитируемые ссылки, включая публикации, патентные заявки и патенты, включены в данное описание посредством ссылки в их полном объеме и в той степени, как если бы каждая ссылка была индивидуально и конкретно включена и изложена здесь в полном объеме (до максимальной степени, разрешенной законом).
Все заголовки и подзаголовки использованы здесь только для удобства и не должны рассматриваться как ограничивающие изобретение каким-либо образом.
Использование любого примера и всех примеров или примерного языка (например, "такой как"), приведенных здесь, предназначено исключительно для лучшего освещения изобретения и не налагает ограничений на объем изобретения, если не заявлено иное. Никакие выражения описания не должны рассматриваться как указывающие на какой-либо не заявленный элемент как на существенный для практики изобретения.
Цитирование и включение патентных документов здесь сделано только для удобства и не отражает никакую точку зрения на действительность, патентоспособность и/или практическую применимость таких патентных документов.
Данное изобретение включает все модификации и эквиваленты сущности изобретения, заявленной в прилагаемой формуле изобретения, как разрешено соответствующим патентным законодательством.
ПРИМЕРЫ
Пептид, который нужно конъюгировать, растворенный в подходящем растворителе, таком как, например, вода, смешивают с первым соединением (как обсуждено выше) в 5-1000-кратном избытке и добавляют трансглутаминазу. Подходящими трансглутаминазами являются, например, те, которые выделены из Streptomyces mobaraenese, Streptomyces lyticus или печени морских свинок. Количество трансглутаминазы, которое нужно добавить, зависит от желаемой скорости реакции. Чем больше добавить фермента, тем быстрее будет идти реакция. Температура может быть равна температуре окружающей среды или несколько повышена примерно до 40°С. Когда реакция достигает желаемой точки, то есть точки, где желаемая фракция пептида, который нужно конъюгировать, функционализирована, добавляют второе соединение (как обсуждено выше) с получением конъюгированного пептида. Затем этот конъюгированный пептид можно очистить, например, с помощью колоночных методик. Одну или более чем одну дополнительную стадию очистки можно также включить раньше в последовательности реакций, например, для удаления избытка первого соединения или для удаления фермента. На второй стадии температуру можно повысить для повышения скорости реакции, поскольку эта стадия не зависит от ферментативной активности. Типичные условия реакции можно найти в Biochem., 35, 13072-13080, 1996, Bioconjugate Chem., 11, 502-509, 2000, и Bioconjugate Chem., 12, 701-710, 1991.
Сокращения
ТGаза: Микробная трансглутаминаза из Streptoverticillium mobaraenae согласно US 5156956 или из Streptomyces Lydicus согласно WO 9606931-А1.
Аналитические методы
Maldi-TOF масс-спектрометрия (времяпролетная масс-спектрометрия с лазерной ионизацией путем десорбции из матрицы).
Молекулярные массы определяли, используя прибор Autoflex Maldi-Tof (Bruker). Образцы готовили согласно сэндвич-методу. Матрица 1 представляла собой раствор 10 мг альфа-циано-4-гидроксикоричной кислоты в 1 мл ацетона. Матрица 2 представляла собой раствор 10 мг альфа-циано-4-гидроксикоричной кислоты в 1 мл 50% ацетонитрила в воде. Образцы готовили на the garget путем последовательного нанесения 1 мкл матрицы 1, сушки на воздухе, нанесения 1 мкп 3% трифторуксусной кислоты, нанесения 1 мкл образца, нанесения 1 мкл матрицы 2, сушки на воздухе, промывки путем орошения планшета водой и, наконец, сушки на воздухе. Спектры получали, используя 20% мощность лазера и стандартный метод для диапазона 3-20 кДа, который поставляется с прибором.
ВЭЖХ с обращенной фазой.
Анализ ОФ-ВЭЖХ проводили на Waters 2690 Separation Module, оборудованном цифровым диодным детектором Waters 996. Использовали колонку силикагеля Vydac 218TP54 4,6 мм × 250 мм 5 мкм С-18 (The Separations Group, Hesperia), и обнаружение проводили с помощью УФ при 214 нм, 254 нм, 280 нм и 301 нм. Колонку уравновешивали 0,1% трифторуксусной кислотой/Н2О и элюировали градиентом от 0 до 90% ацетонитрила против 0,1% трифторуксусной кислоты/Н2О в течение 50 мин при 42°С при скорости тока 0,5 мл/мин.
ЖХ-МС (жидкостная хроматография - масс-спектрометрия)
Анализ ЖХ-МС проводили на масс-спектрометре PE-Sciex API 100, оборудованном двумя микронасосами Perkin Elmer Series 200, автоматическим сэмплером Perkin Elmer Series 200, УФ-детектором Applied Biosystems 785A и детектором испарительного светорассеяния Sedex 75. Колонку силикагеля Waters Xterra 3,0 мм × 50 мм 5 мкм С-18 элюировали при 1,5 мл/мин при комнатной температуре. Ее уравновешивали 5% ацетонитрилом/0,1% трифторуксусной кислотой/Н2О и элюировали в течение 1,0 мин 5% ацетонитрилом/0,1% трифторуксусной кислотой/Н2О, а затем линейным градиентом до 90% ацетонитрила/0,1% трифторуксусной кислоты/Н2О в течение 7 мин. Обнаружение проводили с помощью УФ-детектора при 214 нм и испарительного светорассеяния. Фракцию элюата колонки вводили на границу ионизации распылением масс-спектрометра PE-Sciex API 100. Диапазон массы 300-2000 amu сканировали каждые 2 секунды во время пробега.
Секвенирование по Эдману
Аминокислотные последовательности определяли с помощью автоматизированных расщеплений Эдмана, используя секвенатор белков Applied Biosystem Model 494, по существу как описано фирмой-производителем. Как правило, 50 пмоль пептида использовали для анализа. ПЭГилированный или преобразованный жирной кислотой аминокислотный остаток показыват пустой цикл Эдмана.
Количественное определение белка
Концентрации белка оценивали путем измерения поглощения при 280 нм, используя УФ-спектрофотометр. Использовали коэффициент молярной экстинкции 16170 М-1 см-1. Количества вычисляли на основании объемов и концентраций.
Ферментативное картирование пептидов для определения сайта(ов) преобразования
Пептидное картирование проводили, используя ферментативный гидролиз Asp-N восстановленного и алкилированного белка. Сначала белок обрабатывали ДТТ (дитиотрейтолом) и йодоацетамидом в соответствии со стандартными методиками. Алкилированный продукт очищали, используя ВЭЖХ. Затем алкилированный очищенный продукт подвергали ферментативному гидролизу в течение ночи эндопептидазой Asp-N (Boehringer) при соотношении ферменгсубстрат 1:100. Продукты расщепления разделяли на ВЭЖХ, используя колонку С-18 и стандартную буферную систему трифторуксусная кислота/ацетонитрил. Полученную в результате пептидную карту сравнивали с картой не преобразованного DGH и фракции с различным временем удерживания собирали и анализировали далее, используя Maldi-tof масс-спектрометрию.
Электрофорез в ДСН-ПААГ
Электрофорез в ДСН-полиакриламидном геле проводили, используя NuPAGE 4%-12% Бис-Трис гели (Invitrogen NP0321BOX). Гели окрашивали серебром (Invitrogen LC6100) или красителем Кумасси (Invitrogen LC6065) и, где это релевантно, также окрашивали на ПЭГ йодидом бария, как описано М. М. Kurfurst в Anal. Biochem. 200 (2): 244-248, 1992.
Иллюстративная схема конъюгации hGH с мПЭГ или с липофильной группировкой

I. hGH, человеческий гормон роста
II. Nε141-(2-гидрокси-3-аминопропил)hGH
III. Nε141-(2-оксоэтил)hGH
IV. Nε141-[2-(4-(4-(мПЭГил)бутаноил)аминобутилоксиимино)этил]hGH
V. Nε141-[2-(1-(гексадеканоил)пиперидин-4-ил)этилоксиимино)этил]hGH
Пример 1. Трансаминирование hGH (I.) с получением Nε141-(2-гидрокси-3-аминопропил)hGH (II.)
hGH (I.) (200 мг) растворяли в фосфатном буфере (50 мМ, рН 8,0, 14 мл). Этот раствор смешивали с раствором 1,3-диаминопропан-2-ола (378 мг), растворенного в фосфатном буфере (50 мМ, 1 мл, pH 8,0, pH доводили до 8,0 разбавленной соляной кислотой после растворения 1,3-диаминопропан-2-ола).
Наконец, добавляли раствор ТGазы (18 мг ~ 40 U), растворенного в фосфатном буфере (50 мМ, pH 8,0, 1 мл), и объем доводили до 10 мл добавлением фосфатного буфера (50 мМ, pH 8) с получением концентрации 1,3-диаминопропан-2-ола 0,2 М. Объединенную смесь инкубировали в течение 4 часов при 37°С.
Температуру понижали до комнатной температуры и добавляли N-этилмалеимид до конечной концентрации 1 мМ.
Еще через 1 час смесь разбавляли 10 объемами Трис-буфера (50 мМ, pH 8,5).
Пример 2. Ионообменная хроматография Nε141-(2-гидрокси-3-аминопропил) hGH (II.)
Раствор, полученный в примере 1, наносили на колонку MonoQ 10/100 GL (Amersham Biosciences cat. No. 17-5167-01), предварительно уравновешенную буфером А (50 мМ Трис, рН 8,5). Затем ее элюировали при скорости тока 2 мл/мин градиентом от 3% до 6% буфера В (50 мМ Трис, 2 М NaCl, pH 8,5) в буфере А в течение 40 мин. Фракции собирали на основании УФ-поглощения при 280 нм и проводили анализ Maldi-Tof на отобранных фракциях. Фракции, соответствующие самому большому пику, дающему ожидаемую молекулярную массу согласно масс-спектрометрии Maldi-Tof, объединяли.
Пример 3. Характеристика Nε141-(2-гидрокси-3-аминопропил)hGH (II.)
Пептидное картирование пула, собранного в примере 2, показало, что Asp-N выявлено увеличение массы фрагмента АА 130-146 на 73 единицы атомной массы, соответствующее добавлению аминоспирта в боковую цепь остатка глутамина. Этот пептид был единственным, у которого было изменено время удерживания на карте ВЭЖХ по сравнению с временем удерживания нативного hGH. Этот фрагмент содержит два остатка глутамина. Пептид подвергали секвенированию по Эдману, и Gln-137 обнаружили при ожидаемом выходе, тогда как Gln-141 показал пустой цикл Эдмана. Был сделан вывод, что дериватизация имела место избирательно при Gln-141.
Пример 4. Синтез N-(4-аминооксибутил)-4-мПЭГилбутирамида, где мПЭГил является полидисперсным и имеет молекулярную массу примерно 20 кДа.
Стадия 1: 2-(4-(трет-бутоксикарбониламинокси)бутил)изоиндол-1,3-дион
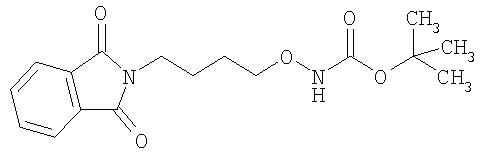
К смеси имеющегося в продаже N-(4-бромбутил)фталимида (2,82 г, 10 ммоль) и N-Вос-гидроксиламина (2,08 г, 15,6 ммоль) добавляли ацетонитрил (2 мл), а затем 1,8-диазабицикло[5.4.0]ундек-7-ен (2,25 мл, 15 ммоль). Эту реакционную смесь перемешивали при комнатной температуре в течение 30 мин, а затем при 50°С в течение 2 суток. Ее разбавляли смесью воды (30 мл) и 1 н. соляной кислоты (20 мл). Эту смесь экстрагировали этилацетатом (2×100 мл). Органическую фазу промывали рассолом (50 мл) и высушивали над сульфатом магния. Сырой продукт очищали хроматографией на силикагеле (60 г), используя градиент гептан/этилацетат от 1:0 до 0:1 в качестве элюента, с получением 2,08 г 2-(4-(трет-бутоксикарбониламинокси)бутил)изоиндол-1,3-диона.
Стадия 2: трет-бутиловый эфир N-(4-аминобутокси)карбаминовой кислоты
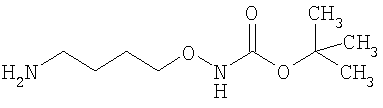
Гидрат гидразина (1,0 мл, 20 ммоль) добавляли к раствору 2-(4-(трет-бутоксикарбониламинокси)бутил)изоиндол-1,3-диона (2,08 г, 6,22 ммоль) в этаноле (8,0 мл). Эту реакционную смесь перемешивали при 80°С в течение 65 ч. Растворитель удаляли в вакууме. Остаток растворяли в толуоле (10 мл) и растворитель удаляли в вакууме. Остаток суспендировали в 1 н. соляной кислоте (10 мл). Осадок удаляли фильтрованием и промывали водой (2 мл). Фильтрат и промывные жидкости объединяли и подщелачивали карбонатом калия. Этот раствор экстрагировали дихлорметаном (4×20 мл). Органический слой высушивали над сульфатом магния. Растворитель удаляли в вакууме с получением 0,39 г трет-бутилового эфира N-(4-аминобутокси)карбаминовой кислоты. Карбонат калия (3 г) добавляли к водной фазе, которую экстрагировали дихлорметаном (3×20 мл). Эти объединенные органические слои высушивали над сульфатом магния. Растворитель удаляли в вакууме с получением еще 0,39 г трет-бутилового эфира N-(4-аминобутокси)карбаминовой кислоты.
Стадия 3: трет-бутиловый эфир N-(4-(4-(мПЭГ20000ил)бутаноиламино)бутокси)карбаминовой кислоты
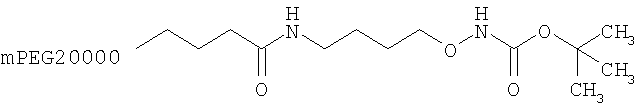
Имеющийся в продаже N-гидроксисукцинимидный эфир мПЭГ2000илбутановой кислоты (Nektar "mPEG-SBA", #2M450P01, 3 г, 0,15 ммоль) растворяли в дихлорметане (25 мл). Добавляли трет-бутиловый эфир N-(4-аминобутокси)карбаминовой кислоты (0,12 г, 0,59 ммоль). Реакционную смесь встряхивали при комнатной температуре. Добавляли диэтиловый эфир до получения осадка. Этот осадок выделяли фильтрованием. Вещество высушивали в вакууме с получением 2,39 г трет-бутилового эфира N-(4-(4-(мПЭГ20000ил)бутаноиламино)бутокси)карбаминовой кислоты.
Стадия 4: N-(4-аминоксибутил)-4-(мПЭГ20000ил)бутаноиламид
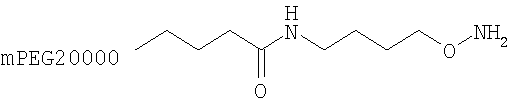
Трифторуксусную кислоту (20 мл) добавляли к раствору трет-бутилового эфира N-(4-(4-(мПЭГ20000ил)бутаноиламино)бутокси)карбаминовой кислоты (2,39 г, 0,12 ммоль) в дихлорметане (20 мл). Реакционную смесь встряхивали в тчеение 30 мин. Добавляли диэтиловый эфир (100 мл). Образовавшийся осадок выделяли фильтрованием. Его промывали диэтиловым эфиром (2×100 мл) и высушивали в вакууме с получением 1,96 г N-(4-аминоксибутил)-4-(мПЭГ20000ил)бутаноиламида.
Пример 5. Окисление Nε141-(2-гидрокси-3-аминопропил)hGH (II.) с получением Nε141-(2-оксоэтил)hGH (III.)
Буфер объединенных фракций из примера 2, содержащий 48,7 мг (II.), заменяли четыре раза 15 мМ триэтаноламинным буфером, pH 8,5 (доведенным 1 н. соляной кислотой), используя устройство для ультрафильтрации Amicon Ultra-15 (Millipore). Наконец, раствор концентрировали до 2 мл. К этому раствору добавляли 2 мл 100 мМ раствора метионина в 15 мМ триэтаноламинном буфере при pH 8,5. Наконец, добавляли 0,4 мл 25 мМ периодата натрия в воде и смесь инкубировали в течение 30 мин при комнатной температуре. Затем ее охлаждали во льду и добавляли 1,6 охлажденного во льду N,N-диметилформамида.
Пример 6. Оксимирование Nε141-(2-оксоэтил)hGH (III.) N-(4-аминооксибутил)-4-мПЭГилбутирамидом с получением Nε141-[2-(4-(4-(мПЭГил)бутаноил)аминобутилоксиимино)этил]hGH (IV.), где мПЭГил является полидисперсным и имеет молекулярную массу примерно 20 кДа
380 мг N-(4-аминооксибутил)-4-мПЭГилбутирамида растворяли в 4 мл воды и доводили pH до 6,0 1 н. соляной кислотой. Затем медленно добавляли смесь, полученную в примере 5, при мягком перемешивании и реакции давали протекать при комнатной температуре в течение 72 ч.
Пример 7. Ионообменная хроматография Nε141-[2-(4-(4-(мПЭГил)бутаноил)аминобутилоксиимино)этил]hGH (IV.), где мПЭГил является полидисперсным и имеет молекулярную массу примерно 20 кДа
Раствор, полученный в примере 6, наносили на колонку MonoQ 10/100 GL (Amersham Biosciences cat. No.17-5167-01), предварительно уравновешенную буфером А (50 мМ Трис, pH 8,5). Затем его элюировали при скорости тока 0,5 мл/мин градиентом от 0% до 7% буфера (50 мМ Трис, 2 М NaCl, pH 8,5) в буфере А в течение 1120 мин. Фракции объединяли на основании УФ-поглощения при 280 нм и проводили анализ Maldi-Tof на отобранных фракциях. Фракции, соответствующие самому большому пику, дающему ожидаемую молекулярную массу согласно масс-спектрометрии Maldi-Tof, объединяли. В результате анализа Maldi-Tof получили широкий пик с центром около 43130 Да в соответствии с полидисперсной природой мПЭГ. Электрофорез в ДСН-ПААГ показал единственную полосу с примерной молекулярной массой 60 кДа. Эта полоса окрашивалась как серебром, так и йодидом бария, что подтвердило белок, модифицированный мПЭГ. Результаты этого анализа подтвердили, что соединение выделенного продукта представляет собой монопэгилированное производное hGH.
Пример 8. Синтез 1-[4-(2-(аминоокси)этил)пиперидин-1-ил]гексадекан-1-она
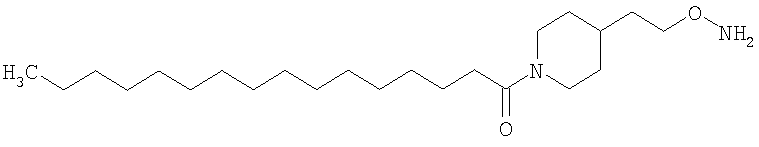
Стадия 1:
трет-бутиловый эфир 4-[2-(толуол-4-сульфонилокси)этил]пиперидин-1-карбоновой кислоты
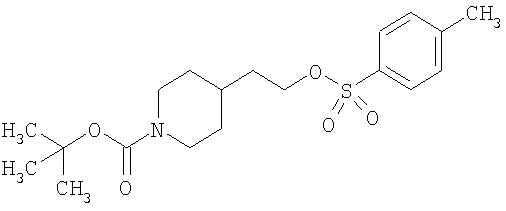
Тозилхлорид (4,16 г, 21,8 ммоль) добавляли к раствору имеющегося в продаже трет-бутилового эфира 4-(2-гидроксиэтил)пиперидин-1-карбоновой кислоты (например, Aldrich 54,724-7, 5,0 г, 21,8 ммоль) и триэтиламина (4,25 мл, 30,5 ммоль) в дихлорметане (100 мл). Реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Ее разбавляли этилацетатом (300 мл) и промывали 10% водным раствором гидросульфата натрия (200 мл). Водную фазу экстрагировали этилацетатом (150 мл). Объединенные органические слои промывали насыщенным водным раствором гидрокарбоната натрия (250 мл) и высушивали над сульфатом магния. Растворитель удаляли в вакууме. Сырой продукт очищали флэш-хроматографией на силикагеле (80 г), используя этилацетат/гептан сначала 1:2, затем 1:1 в качестве элюента, с получением 6,04 г трет-бутилового эфира 4-[2-(толуол-4-сульфонилокси)этил]пиперидин-1 -карбоновой кислоты.
1Н-ЯМР (CDCl3): δ 1.05 (m, 2H); 1.45 (s, 9H); 1.55 (m, 5H); 2.50 (s, 3H); 2.65 (t, 10 2H); 4.05 (m, 4H); 7.35 (d, 2H); 7.80 (d, 2H).
Стадия 2:
трет-бутиловый эфир 4-[2-(1,3-диоксо-1,3-дигидроизоиндол-2-илокси)этил]пиперидин-1-карбоновой кислоты
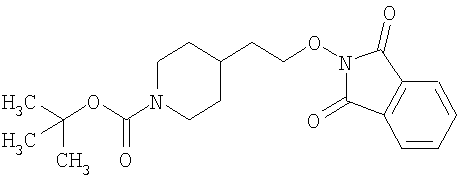
При 0°С 60% суспензию гидрида натрия в минеральном масле (0,69 г, 17,2 ммоль) добавляли к раствору N-гидроксифталимида (2,80 г, 17,2 ммоль) в N,N-диметилформамиде (20 мл). Реакционную смесь перемешивали в течение 45 мин при 0°С. Последовательно добавляли раствор трет-бутилового эфира 4-[2-(толуол-4-сульфонилокси)этил]пиперидин-1-карбоновой кислоты (5,99 г, 15,6 ммоль) в N,N-диметилформамиде (15 мл) и тетрабутиламмония йодида (0,17 г, 0,47 ммоль). Реакционную смесь нагревали до 60°С в течение 2 суток и охлаждали до комнатной температуры. Осторожно добавляли воду (5 мл). Реакционную смесь разбавляли этилацетатом (250 мл) и промывали 10% водным раствором гидросульфата натрия (200 мл). Водную фазу экстрагировали этилацетатом (200 мл). Объединенные органические слои промывали насыщенным водным раствором гидрокарбоната натрия (150 мл) и высушивали над сульфатом магния. Растворитель удаляли в вакууме. Сырой продукт очищали флэш-хроматографией на силикагеле (80 г), используя этилацетат/гептан 1:1 в качестве элюента, с получением 4,36 г трет-бутилового эфира 4-[2-(1,3-диоксо-1,3-дигидроизоиндол-2-илокси)этил]пиперидин-1-карбоновой кислоты.
1H-ЯМР (CDCl3): δ 1.15 (m, 2H); 1.50 (s, 9H); 1.75 (m, 5H); 2.75 (m, 2H); 4.10 (m, 2H); 4.30 (t, 2H); 7.80 (m, 4H).
Стадия 3:
2-(2-(пиперидин-4-ил)этокси)изоиндол-1,3-дион
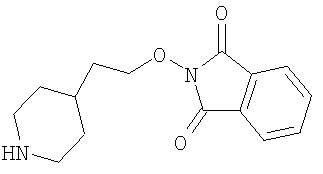
Трифторуксусную кислоту (20 мл) добавляли к раствору трет-бутилового эфира 4-[2-(1,3-диоксо-1,3-дигидроизоиндол-2-илокси)этил]пиперидин-1 -карбоновой кислоты (4,26 г, 11,4 ммоль) в дихлорметане (20 мл). Реакционную смесь перемешивали при комнатной температуре в течение 50 мин. Растворитель удаляли в вакууме. Остаток растворяли в дихлорметане (50 мл) и растворитель удаляли в вакууме. Последнюю процедуру повторяли дважды с получением 6,46 г сырой соли трифторацетат 2-(2-(пиперидин-4-ил)этокси)изоиндол-1,3-диона.
МС: m/z=275[M+1+].
1H-ЯМР (ДМСО-d6): δ 1.30 (m, 2Н); 1.65 (m, 2Н); 1.90 (m, 3Н); 2.90 (q, 2H); 3.30 (d, 2H); 4.20 (t, 2H); 7.90 (s, 4Н); 8.30 (br, 1H); 8.65 (br, 1H).
Стадия 4:
2-[2-(1-(гексадеканоил)пиперидин-4-ил)этокси]изоиндол-1,3-дион
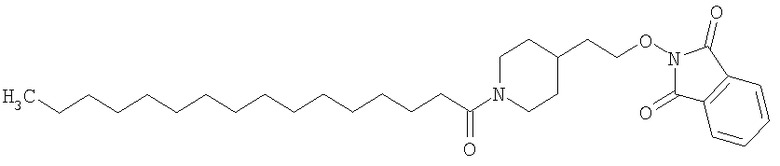
При 0°С гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (1,04 г, 5,44 ммоль) добавляли к раствору пальмитиновой кислоты (1,40 г, 5,44 ммоль) и 3,4-дигидро-3-гидрокси-4-оксо-1,2,3-бензотриазола (0,89 г, 5,44 ммоль) в N,N-диметилформамиде (20 мл) и дихлорметане (20 мл). Реакционную смесь перемешивали при 0°С в течение 20 мин. Последовательно добавляли раствор соли трифторацетат 2-(2-(пиперидин-4-ил)этокси)изоиндол-1,3-диона (2,11 г, 5,44 ммоль) в N,N-диметилформамиде (5 мл) и этилдиизопропиламин (6,19 мл, 38,1 ммоль). Реакционную смесь перемешивали в течение 16 ч, в то время как она нагрелась до комнатной температуры. Смесь разбавляли этилацетатом (150 мл) и промывали 10% водным раствором гидросульфата натрия (150 мл). Водную фазу экстрагировали этилацетатом. Объединенные органические слои промывали смесью воды (50 мл) и насыщенного водного раствора гидрокарбоната натрия (50 мл) и высушивали над сульфатом магния. Сырой продукт очищали флэш-хроматографией на силикагеле (40 г), используя этилацетат/гептан 1:1 в качестве элюента, с получением 1,52 г 2-[2-(1-(гексадеканоил)пиперидин-4-ил)этокси]изоиндол-1,3-диона.
МС: m/z=513[M+1+].
1H-ЯМР (ДМСО-d6): δ 0.90 (t, 3H); 1.10 (m, 2H); 1.25 (m, 26H); 1.45 (m, 2H); 1.65 (m, 1Н); 1.80 (m, 2Н); 2.30 (t, 2Н); 2.95 (t, 1Н); 3.85 (m, 3Н); 4.20 (t, 2Н); 4.40 (d, 1H); 7.90 (s, 4H).
Стадия 5:
гидрат гидразина (0,14 мл, 2,96 ммоль) добавляли к раствору 2-[2-(1-(гексадеканоил)пиперидин-4-ил)этокси]изоиндол-1,3-диона (1,52 г, 2,96 ммоль) в этаноле (30 мл), реакционную смесь нагревали до образования флегмы в течение 75 мин и охлаждали до комнатной температуры. Образовавшийся осадок удаляли фильтрованием. Растворитель фильтрата удаляли в вакууме. Сырой продукт очищали флэш-хроматографией на силикагеле (30 г), используя смесь дихлорметан/метанол/25% водный аммиак (100:10:1) в качестве элюента, с получением 800 мг 1-[4-(2-(аминоокси)этил)пиперидин-1-ил]гексадекан-1-она.
МС: m/z=383[М+1+].
1Н-ЯМР (CDCl3): δ 0.80 (t, 3Н); 1.25 (m, 2H); 1.60 (m, 26H); 1.70 (m, 4H); 1.65 (m, 3Н); 2.70 (8t, 2H); 2.60 (t, 1H); 3.05 (t, 1H); 3.80 (m, 3Н); 4.60 (d, 1H).
Пример 9. Трансаминирование Z-Gln-Gly с получением [4-(3-амино-2-гидроксипропилкарбамоил)-2-бензилоксикарбониламинобутириламино]уксусной кислоты
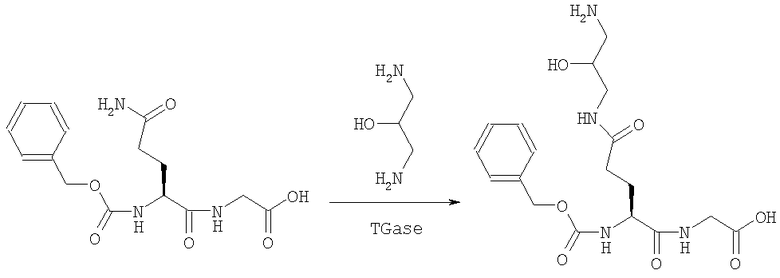
30 мг Z-Gln-Gly (Bachem C1635) растворяли в фосфатном буфере (50 мМ, рН 8,0, 2 мл).
К этому раствору добавляли раствор 1,3-диаминопропан-2-ола (9 мг) в фосфатном буфере (50 мМ, pH 8,0, pH доведен до 8,0 после растворения 1,3-диаминопропан-2-ола, 0,9 мл). Наконец, добавляли раствор ТGазы (0,9 мг ~ 2 U), растворенной в фосфатном буфере (50 мМ, рН 8,0, 0,1 мл) и эту объединенную смесь инкубировали в течение 4 часов при 37°С. Температуру снижали до комнатной температуры и добавляли N-этилмалеимид до конечной концентрации 1 мМ. Еще через 1 час смесь разбавляли 10 объемами воды. Продукт выделяли из этого раствора с помощью полупрепаративной ВЭЖХ за один пробег на колонке 25 мм × 250 мм, набитой силикагелем 7 мкм С-18. Колонку элюировали градиентом от 10 до 30% ацетонитрила в 0,1% трифторуксусной кислоте/Н2О при 10 мл/мин при температуре 40°С в течение 50 мин. Фракции, содержащие пептид, соответствующий основному пику, собирали, разбавляли до 30 мл примерно 3 объемами Н2О и лиофилизировали. Полученный конечный продукт характеризовали с помощью ОФ-ВЭЖХ, где он имел время удерживания 12,75 мин, и с помощью ЖХ-МС, где время удерживания 1,9 мин имело пик массы, соответствующий М+H+ 411,5 единиц атомной массы, что соответствует ожидаемой структуре.
Пример 10. Окисление [4-(3-амино-2-гидроксипропилкарбамоил)-2-бензилоксикарбониламинобутириламино]уксусной кислоты с получением [2-бензилоксикарбониламино-4-(2-оксоэтилкарбамоил)бутириламино]уксусной кислоты
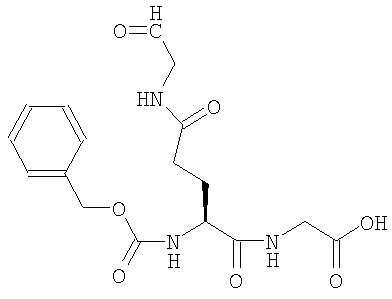
0,8 мг [4-(3-амино-2-гидроксипропилкарбамоил)-2-бензилоксикарбониламинобутириламино]уксусной кислоты растворяли в 4 мл 15 мМ триэтаноламинного буфера, pH 8,5 (доведенного 1 н. соляной кислотой). К этому раствору добавляли 1 мл 173 мМ раствора метионина в воде. Наконец, добавляли 0,5 мл 24 мМ периодата натрия в воде и смесь инкубировали в течение 10 мин при 0°С.
Пример 11. Оксимирование [2-бензилоксикарбониламино-4-(2-оксоэтилкарбамоил)бутириламино]уксусной кислоты с получением (2-бензилоксикарбониламино-4-{2-[2-(1-гексадеканоилпиперидин-4-ил)этоксиимино]этилкарбамоил}бутириламино)уксусной кислоты
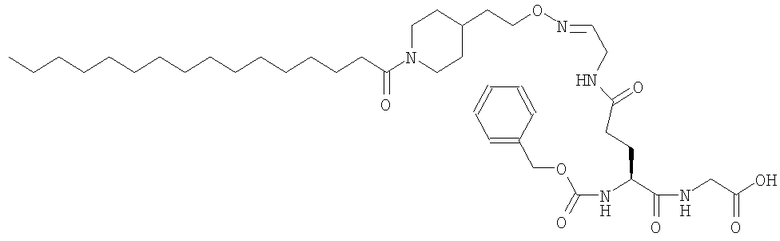
2 мг 1-[4-(2-(аминоокси)этил)пиперидин-1-ил]гексадекан-1-она растворяли в 3 мл N,N-диметилформамида и этот раствор охлаждали на льду. К 0,53 мл этого раствора добавляли 1,38 мл реакционной смеси из примера 10 и этой смеси давали взаимодействовать при 0°С в течение ночи. ОФ-ВЭЖХ подтвердила образование нового продукта. Этот продукт выделяли с помощью ОФ-ВЭЖХ в аналитическом масштабе и подвергали масс-спектрометрии Maldi-TOF, которая дала пик, соответствующий М+H+: 744,7 единиц атомной массы в соответствии с ожидаемой структурой.
Пример 12. Окисление Nε141-гидрокси-3-аминопропил)hGH (II.) с получением Nε141-оксоэтил)hGH (III.)
5 мг Nε141-(2-гидрокси-3-аминопропил) hGH (II.) растворяли в 0,5 мл 15 мМ триэтаноламинного буфера, pH 8,5 (доведенного 1 н. соляной кислотой). К этому раствору добавляли 0,13 мл 173 мМ раствор метионина в воде. Наконец, добавляли 0,06 мл 24 мМ периодата натрия в воде и смесь инкубировали в течение 10 мин при 0°С.
Пример 13. Оксимирование Nε141-(2-оксоэтил)hGH (III.) 1-[4-(2-(аминоокси)этил)пиперидин-1-ил]гексадекан-1-оном с получением Nε141-[2-(1-(гексадеканоил)пиперидин-4-ил)этилоксиимино)этил]hGH (V.)
2 мг 1-[4-(2-(аминоокси)этил)пиперидин-1-ил]гексадекан-1-она растворяли в 3 мл N,N-диметилформамида и этот раствор охлаждали на льду. Добавляли 0,14 мл реакционной смеси из примера 12 и этой смеси давали взаимодействовать при 0°С в течение ночи.
Пример 14. Характеристика Nε141-[2-(1-(гексадеканоил)пиперидин-4-ил)этилоксиимино)этил]hGH (V.)
Аликвоту сырой реакционной смеси из примера 13 фракционировали с помощью ОФ-ВЭЖХ в аналитическом масштабе и проводили масс-спектрометрию Maldi-TOF на фракциях. Фракцию, дающую ожидаемую молекулярную массу для ожидаемой структуры продукта, подвергали пептидному картированию. Карта показала, что выявлено увеличение массы Asp-N фрагмента АА 130-146 на 407 единиц атомной массы, что соответствует добавлению 2-(1-(гексадеканоил)пиперидин-4-ил)этилоксиимино)этила к боковой цепи остатка глутамина. Этот пептид был единственным, у которого изменилось время удерживания на карте ВЭЖХ по сравнению с временем удерживания нативного hGH. Этот фрагмент содержит два остатка глутамина. Пептид подвергали секвенированию по Эдману, и Gln-137 был обнаружен при ожидаемом выходе, тогда как Gln-141 показал пустой цикл Эдмана. Был сделан вывод, что дериватизация имела место избирательно при Gln-141.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНОЕ ИНСУЛИНА, РАСТВОРИМАЯ ПРОЛОНГИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПРОЛОНГИРОВАНИЯ ГИПОГЛИКЕМИЧЕСКОГО ДЕЙСТВИЯ ПРИ ЛЕЧЕНИИ ДИАБЕТА | 1994 |
|
RU2164520C2 |
| ПРОИЗВОДНЫЕ ИНСУЛИНА | 2004 |
|
RU2352581C2 |
| ЛЕЧЕНИЕ САХАРНОГО ДИАБЕТА С ИСПОЛЬЗОВАНИЕМ ИНЪЕКЦИЙ ИНСУЛИНА С ЧАСТОТОЙ МЕНЕЕ ОДНОГО РАЗА В ДЕНЬ | 2009 |
|
RU2540922C2 |
| ПРОИЗВОДНЫЕ ИНСУЛИНА | 2004 |
|
RU2518460C2 |
| ПЕПТИДНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОПИЛЕНГЛИКОЛЬ, ЯВЛЯЮЩАЯСЯ ОПТИМАЛЬНОЙ ДЛЯ ИЗГОТОВЛЕНИЯ И ПРИМЕНЕНИЯ В ИНЪЕКЦИОННЫХ УСТРОЙСТВАХ | 2004 |
|
RU2421238C2 |
| ПЕПТИДНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОПИЛЕНГЛИКОЛЬ, ЯВЛЯЮЩАЯСЯ ОПТИМАЛЬНОЙ ДЛЯ ИЗГОТОВЛЕНИЯ И ПРИМЕНЕНИЯ В ИНЪЕКЦИОННЫХ УСТРОЙСТВАХ | 2004 |
|
RU2831321C2 |
| ОЧИСТКА ИНСУЛИНА | 2012 |
|
RU2603752C2 |
| СТАБИЛЬНЫЕ НЕВОДНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2008 |
|
RU2472492C2 |
| РЕГЕНЕРАЦИЯ ХРОМАТОГРАФИЧЕСКОЙ СТАЦИОНАРНОЙ ФАЗЫ | 2004 |
|
RU2350945C2 |
| КОНЪЮГИРОВАННЫЕ БЕЛКИ С ПРОЛОНГИРОВАННЫМ ДЕЙСТВИЕМ IN VIVO | 2009 |
|
RU2526804C2 |
Предложены конъюгаты человеческого гормона роста, полученные путем удаления атома водорода из -NH2 в боковой цепи Gln, который образован от человеческого гормона роста или соединения человеческого гормона роста. 3 н. и 3 з.п. ф-лы.
1. Соединение формулы
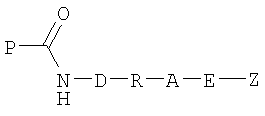
где P-C(O)-NH- представляет собой пептидный радикал, полученный путем удаления атома водорода из -NH2 в боковой цепи Gln, который образован от человеческого гормона роста или соединения человеческого гормона роста;
D представляет собой связь или кислород;
R представляет собой линкер, выбранный из С1-10алкилена, или связь;
Е представляет собой линкер, выбранный из
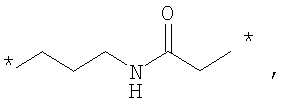
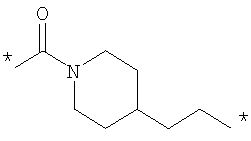 и
и 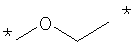 ,
,
или связь;
А представляет собой оксим- и
Z выбран среди радикалов ПЭГ или мПЭГ и их аминопроизводных,
включая нормальные и разветвленные радикалы ПЭГ и мПЭГ,
и его фармацевтически приемлемые соли, биологически гидролизуемые амиды и биологически гидролизуемые эфиры.
2. Соединение по п.1, которое конъюгировано в положении, соответствующем положению 141 в человеческом гормоне роста.
3. Соединение по п.1, выбранное из
Nε141-[2-(4-(4-(мПЭГ(20k)илбутаноил)аминобутилоксиимино)-этил]hGH,
Nε141(2-(4-(4-(1,3-бис(мПЭГ(20k)иламинокарбонилокси)проп-2-илокси)бутириламино)бутилоксиимино)этил)hGH,
Nε141(2-(4-(2,6-бис(мПЭГ(20k)илоксикарбониламино)гексаноиламино)бутилоксиимино)-этил)hGH,
Nε141(2-(4-(4-(мПЭГ(30k)илокси)бутириламино)бутилоксиимино)этил)hGH,
Nεl41(2-(4-(4-(мПЭГ(20k)илокси)бутириламино)бутилоксиимино)этил)hGH и
Nε141(2-(4-(3-(мПЭГ(30k)илокси)пропаноиламино)бутилоксиимино)этил)hGH и их фармацевтически приемлемых солей, биологически гидролизуемых амидов и биологически гидролизуемых эфиров,
где мПЭГ(20k)ил и мПЭГ(30k)ил означает соответственно мПЭГ(20k)ил и мПЭГ(30k)ил с индексом полидисперсности ниже 1,06.
4. Фармацевтическая композиция, обладающая активностью гормона роста, содержащая терапевтически эффективное количество соединения по любому из пп.1-3 и фармацевтически приемлемые добавки.
5. Соединение по любому из пп.1-3 для использования в лечении заболеваний, при которых показана активность гормона роста.
6. Применение соединения по любому из пп.1-3 для лечения заболеваний, при которых показана активность гормона роста.
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| GORMAN J | |||
| J | |||
| et al | |||
| Transglutaminase Amine Substrates for Photochemical Labeling and Cleavable Cross-linking of Proteins | |||
| Journal of biological chemistry | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| THUMSHIRN G | |||
| et al | |||
| Multimeric cyclic RGD peptides as potential tools | |||
Авторы
Даты
2010-04-10—Публикация
2005-01-18—Подача