Область изобретения
Данное изобретение относится к хроматографическому способу выделения белковых компонентов раствора, содержащего белок, в частности выделения инсулинового пептида с учетом родственных примесей.
Уровень техники
Очистка рекомбинантных белков и пептидов для фармацевтического применения в основном проводится с использованием способов жидкостной хроматографии. Хроматографические способы характеризуются признаками их стационарной фазы, например хроматографии с обращенной фазой для гидрофобных хроматографических смол, тем не менее на разделение влияет целый ряд параметров, например состав подвижной фазы. Ионообменная хроматография (IEC) характеризуется заряженной поверхностью неподвижной фазы и применением буферов, солей и контролем pH подвижной фазы. IEC оказалась очень эффективной в разделении родственных и неродственных примесей, тем не менее некоторые примеси могут быть очень трудно удалимыми, например, если имеется один и тот же заряд целевого полипептида и примеси.
GB 694530 и GB 729670 описывают кристаллизацию инсулина в присутствии хинолина или акридин-подобных веществ и веществ фенольной природы, соответственно, а также в присутствии цинка.
US 5504188 описывает приготовление кристаллов аналога инсулина (LysPro) при pH 5,5-6,5 в присутствии (среди прочих) ионов цинка.
WO 98/34953 описывает кристаллизацию белка с лизиновой боковой цепью, несущей липофильный заместитель (инсулин детемир), в растворе, содержащем ионы цинка, при этом кристаллизация достигается путем подведения pH раствора от кислого до pH 7-10.
US 3907676 раскрывает способ снижения антигенности инсулина, извлеченного из поджелудочных желез домашних млекопитающих, в частности свиных и бычьих поджелудочных желез, и содержащего антигенные инсулин-подобные вещества с молекулярной массой примерно 6000 вместе с некоторыми антигенными белками, полученными из поджелудочной железы, с молекулярной массой более 6000. Снижение антигенности получают, проводя инсулин через хроматографическую колонку с анионообменной смолой, которая предпочтительно является сильным основанием, при этом в качестве элюента используют водосодержащий алифатический одноатомный спирт и собирают фракции элюата, содержащие инсулин, свободный или по существу свободный от упомянутых примесей.
EP 1071703 показывает, что добавление ионов кальция к подвижной фазе обеспечивает повышенную селективность между гликозилированными и негликозилированными видами (в частности, для инсулина) по сравнению с традиционными RPC-способами (использующими одновалентные ионы).
US 3649456 в основном описывает замену буфера полипептида на RPC-подобной неподвижной фазе из водного раствора на раствор, содержащий органический растворитель, в присутствии различных солей, включая хлорид кальция.
US 5633350 описывает отделение витамин K-зависимых белков от витамин K-независимых белков в присутствии ионов кальция на ионообменных смолах.
GB 2173503 A описывает способ очистки инсулина с использованием слабокислого катионного обменника, предпочтительно с предоставлением гидрофобной матрицы. Фракционирование инсулина проводят путем поэтапного или непрерывного изменения концентрации растворителя в кислом диапазоне pH.
US 4129560 описывает способ очистки высокомолекулярных пептидов, которые имеют тенденцию к ассоциации, с помощью ионообменной хроматографии в водных буферных растворителях на кислотных или основных ионообменниках, при этом способ включает растворение неионных детергнетов в буферизованных растворителях.
US 2005-080000A раскрывает способ хроматографической очистки препроинсулинов, в котором вещества с большей молекулярной массой удаляют из водного раствора препроинсулина при первой хроматографии на анионообменной смоле в проточном режиме и при последующей второй хроматографии на катионном обменнике в режиме адсорбции, а также способ получения инсулинов, который включает способ получения препроинсулинов.
US 2006-167221 A раскрывает извлечение и изоляцию инсулинов из рекомбинантных источников, в частности тех, которые экспрессируются и секретируются дрожжами. Органические растворители использовали для извлечения форм инсулинового пептида, связанных с хозяйской поверхностью. Кроме того, раскрыты процедуры поэтапной очистки среды, экстракции растворителем и хроматографии для осуществления одновременного выделения и очистки растворимых и мембраносвязанных форм инсулина.
US 5278284 описывает способ удаления нужного белка из сложного раствора и извлечения нужного белка в очищенном виде, который заключается в добавлении сорбента силикагеля с размером пор, приблизительно равным размеру молекулы белка, к раствору, содержащему белок, позволяя белку сорбироваться на сорбенте, выделении сорбента из раствора и последующем выделении белка из сорбента.
US 6451987 раскрывает способ ионообменной хроматографии для выделения пептида из смеси, содержащей пептид и родственные примеси, а также промышленный способ, включающий такой способ ионообменной хроматографии.
Некоторые из них (часто родственные) примеси часто являются трудными для устранения или уменьшения в связи с формой пика, например, примеси, которые элюируются на передней или задней границе пика. Таким образом, результатом может быть недостаточная чистота белка, представляющего интерес.
Сущность изобретения
Данное изобретение предусматривает средства для контроля формы хроматографического пика для улучшенного удаления примесей, например, родственных примесей, которые в противном случае трудно удалить при высокой нагрузке белком, представляющим интерес, колонки с хроматографическим твердофазным материалом. Форма пика контролируется путем присутствия ди- или поливалентных ионов металлов в белоксодержащем растворе, наносимом на хроматографическую колонку (т.е. загружаемом в нее), в сочетании с подведением pH элюента, например, в отношении изоэлектрической точки (pI) для белка, представляющего интерес, и это делает возможным сбор очень концентрированного пула белка, представляющего интерес, в очищенной форме.
Автором (авторами) данного изобретения было обнаружено, что контролируемая форма пика может позволить повысить нагрузку белком, представляющим интерес, и, следовательно, повысить мощность и снизить число циклов для данного количества белка, которое нужно очистить, так что можно получить пулы с более высокими концентрациями.
Таким образом, в первом аспекте данное изобретение относится к хроматографическому способу выделения белковых компонентов белоксодержащего раствора, при этом указанный раствор содержит инсулиновый пептид и один или более чем один ди- или поливалентный ион металл, и указанный инсулиновый пептид способен к самоассоциации и/или структурному изменению в присутствии ди- или поливалентных ионов металлов, причем способ включает следующие этапы:
а. нанесение белоксодержащего раствора на колонку с хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом составляет по меньшей мере 6,0 г на литр объема колонки (g/LCV, г/лCV); и
б. элюция инсулинового пептида из указанного твердофазного материала с помощью элюента с pH максимум 8,5; и сбор пула инсулинового пептида, соответствующего по меньшей мере 75% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а).
Во втором аспекте данное изобретение относится к хроматографическому способу выделения белковых компонентов инсулинсодержащего раствора, при этом указанный раствор, содержащий инсулиновый пептид, способен к самоассоциации и/или структурному изменению в присутствии цинка и двухвалентных ионов цинка, причем указанный способ включает следующие этапы:
а. нанесение инсулинсодержащего раствора на колонку с анионообменным хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом, представляющим интерес, составляет по меньшей мере 6,0 г на литр объема колонки (г/лCV); и
б. элюция инсулинового пептида, представляющего интерес, из указанного твердофазного материала с помощью элюента с pH максимум 6,8; и сбор пула представляющего интерес инсулинового пептида, соответствующего по меньшей мере 90% по весу представляющему интерес инсулиновому пептиду, нанесенному на колонку на этапе (а).
В третьем аспекте данное изобретение относится к способу контроля формы пика при ионообменной хроматографии инсулиновых пептидов, способных к самоассоциации и/или структурному изменению в присутствии ди- или поливалентных ионов металлов с использованием
а. ди- или поливалентных ионов металлов для получения оптимального разделения инсулинового пептида и родственных примесей, при котором двухвалентные ионы металлов были добавлены, чтобы закрепить форму передней части пика инсулинового пептида, где родственные примеси элюируют перед инсулиновым пептидом.
Краткое описание графических материалов
Фиг.1-3: Изменение профиля инсулинового пика от растянутого заднего пика при высоких значениях pH (тонкая пунктирная кривая на фиг.3, рН=7,2), который соответствует нормальному профилю Ленгмюра расширенного пика при заданном значении pH (сплошная тонкая кривая на фиг.2, pH 6,8), к профилю с растянутым передним краем пика при низком значении pH (толстая пунктирная кривая фиг.1, pH 6,4) в присутствии Zn2+ в подвижной фазе, т.е. в белоксодержащем растворе.
Фиг.4. Хроматограмма эксперимента с Zn-балансом.
Подробное описание изобретения
Как упоминалось выше, данное изобретение относится к хроматографическому способу выделения белковых компонентов белоксодержащего раствора. В частности, целью данного изобретения является применимый в промышленности способ, при котором белок, представляющий интерес, можно отделять от родственных примесей, в то же время получая высокое извлечение белка, представляющего интерес. Такие родственные примеси, как правило, являются неантигенными.
В одном аспекте предусмотрен хроматографический способ выделения белковых компонентов белоксодержащего раствора, при этом указанный раствор содержит инсулиновый пептид и один или более чем один ди- или поливалентный ион металлов, указанный инсулиновый пептид способен к самоассоциации и/или структурному изменению в присутствии ди- или поливалентных ионов металла, причем указанный способ включает следующие этапы:
а. нанесение белоксодержащего раствора на колонку с хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом, представляющим интерес, составляет по меньшей мере 6,0 г на литр объема колонки (г/лCV); и
б. элюция инсулинового пептида из указанного твердофазного материала с помощью элюента с pH максимум 8,5; и сбор пула инсулинового пептида, соответствующего по меньшей мере 75% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а).
В другом аспекте предусмотрен хроматографический способ выделения белковых компонентов инсулинсодержащего раствора, при этом указанный раствор содержит инсулиновый пептид, который способен к самоассоциации и/или структурному изменению в присутствии цинка или двухвалентных ионов цинка, причем указанный способ включает следующие этапы:
а. нанесение инсулинсодержащего раствора на колонку с анионообменным хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом, представляющим интерес, составляет по меньшей мере 6,0 г на литр объема колонки (г/лCV); и
б. элюция инсулинового пептида, представляющего интерес, из указанного твердофазного материала с помощью элюента с pH максимум 6,8; и сбор пула инсулинового пептида, представляющего интерес, соответствующего по меньшей мере 90% по весу представляющему интерес инсулиновому пептиду, нанесенному на колонку на этапе (а).
В другом аспекте предусмотрен способ контроля формы пика при ионообменной хроматографии инсулиновых пептидов, способных к самоассоциации и/или структурному изменению в присутствии ди- или поливалентных ионов металлов, с использованием
а. ди- или поливалентных ионов металлов для получения оптимального разделения инсулинового пептида и родственных примесей, где двухвалентные ионы металлов были добавлены, чтобы закрепить форму переднего края пика инсулинового пептида, где родственные примеси элюируются перед инсулиновым пептидом.
Белки могут происходить из экспрессионных систем дрожжей. В способе производства белков применение хроматографической очистки широко распространено. Белки, как правило, подвергают химическим модификациям и серии этапов хроматографической очистки, в частности колоночной хроматографии, включая высокоэффективную жидкостную хроматографию (или жидкостную хроматографию высокого давления, ВЭЖХ), например, обращенно-фазовую хроматографию (RPC), хроматографию гидрофобного взаимодействия (HIC) и ионообменную хроматографию (IEC) (например, анионообменную хроматографию (AIEC) или катионообменную хроматографию (CIEC)), аффинную хроматографию, эксклюзионную хроматографию, металл-хелатную хроматографию, псевдоаффинную хроматографию и/или хроматографию смешанного режима.
Принцип очистки белков с применением колоночной хроматографии основан на различиях в равновесии между неподвижной и подвижной фазами белков, которые нужно разделить. С помощью соответствующей комбинации неподвижной и подвижной фаз белки покидают колонку через разные интервалы времени. В контексте данного изобретения было обнаружено, что модификация подвижной фазы, изначально загруженной в колонку, посредством ди- или поливалентных ионов металлов обеспечивает усовершенствование формы пика по сравнению с контролем и тем самым обеспечивает отделение белка, представляющего интерес, от близкородственных примесей.
Важным параметром хроматографической очистки является емкость колонки, определенная как количество (целевого) белка, которое может связаться с колонкой. Емкость колонки зависит от концентрации белка в подвижной фазе, и изображение концентрации белка на стационарной фазе в зависимости от концентрации белка в подвижной фазе называют изотермами связывания. Изотермы связывания могут быть вогнутыми (хроматографические пики впереди) или выпуклыми (хроматографические пики позади) [J.M. Mollerup, Chem. Eng. Technol. 31 (2008) 864-874]. В редких случаях получаются s-образные изотермы, когда пики идут впереди при низко концентрированной подвижной фазе и позади при более высоко концентрированной подвижной фазе [J.M. Mollerup et al., J. Liq. Chromatogr. Rel. Technol. 32 (2009) 1577-1597].
Mollerup (J.M. Mollerup, Chem. Eng. Technol. 31 (2008) 864-874) ранее показали, что кооперативность, когда адсорбция одной молекулы способствует адсорбции другой молекулы, может привести к фронтальным хроматограммам.
В хроматографии привлекательно иметь наклон до высоких концентраций, близкий к начальному наклону изотермы, для получения небольшого объема пула и высокой концентрации пула.
Были определены некоторые существенные параметры:
- ди- или поливалентные ионы металлов (например, Zn2+) пытаются придать восходящее направление кривой изотермы, (dq/dc растет - q является концентрацией белка, связанного с твердофазным материалом, а с является концентрацией белка в растворе).
- Повышенная нагрузка на смолу придает нисходящее направление кривой (dq/dc уменьшается).
- при pH, близком к изоэлектрической точке, суммарный заряд мал, и силы отталкивания между белками малы.
- при приближении к изоэлектрической точке растворимость белка, как правило, уменьшается. Тем не менее, самоассоциация может привести к явному повышению растворимости вблизи изоэлектрической точки.
Белок, представляющий интерес
Термин «белок» предназначен для охвата белков, полипептидов и пептидов, состоящих по меньшей мере из десяти составных аминокислотных остатков, соединенных пептидными связями. Составные аминокислоты могут быть выбраны из группы аминокислот, кодируемых генетическим кодом, и они могут быть природными аминокислотами, которые не кодируются генетическим кодом, а также синтетическими аминокислотами.
В данном описании термин «аминокислотный остаток» означает аминокислоту, в которой формально гидроксильная группа удалена из карбоксигруппы, и/или в которой формально атом водорода удален из аминогруппы.
Природными аминокислотами, которые не кодируются генетическим кодом, являются, например, γ-карбоксиглутамат, орнитин, фосфосерин, D-аланин и D-глутамин. Синтетические аминокислоты включают аминокислоты, полученные путем химического синтеза, т.е. D-изомеры аминокислот, кодируемых генетическим кодом, такие как D-аланин и D-лейцин, Aib (α-аминоизомасляную кислоту), Abu (α-аминомасляную кислоту), TLE (трет-бутилглицин), β-аланин, 3-аминометилбензойную кислоту, антраниловую кислоту.
22 протеогенные аминокислоты представляют собой: аланин, аргинин, аспарагин, аспарагиновую кислоту, цистеин, цистин, глутамин, глутаминовую кислоту, глицин, гистидин, гидроксипролин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин и валин.
Таким образом, непротеогенная аминокислота представляет собой группировку, которая может быть включена в пептид через пептидные связи, но не является протеогенной аминокислотой. Примерами являются (но не ограничиваясь ими) γ-карбоксиглутамат, орнитин, фосфосерин, D-аминокислоты, такие как D-аланин и D-глутамин. Синтетические непротеогенные аминокислоты включают аминокислоты, полученные путем химического синтеза, т.е. D-изомеры аминокислот, кодируемых генетическим кодом, такие как D-аланин и D-лейцин, Aib (α-аминоизомасляную кислоту), Abu (α-аминомасляную кислоту), Tle (трет-бутилглицин), 3-аминометилбензойную кислоту, антраниловую кислоту, дезаминогистидин, бета-аналоги аминокислот, такие как β-аланин и т.д., D-гистидин, дезаминогистидин, 2-аминогистидин, β-гидроксигистидин, гомогистидин, Nα-ацетилгистидин, α-фторметилгистидин, α-метилгистидин, 3-пиридилаланин, 2-пиридилаланин или 4-пиридилаланин, (1-аминоциклопропил)карбоновую кислоту, (1-аминоциклобутил)карбоновую кислоту, (1-аминоциклопентил)карбоновую кислоту, (1-аминоциклогексил)карбоновую кислоту, (1-аминоциклогептил)карбоновую кислоту или (1-аминоциклооктил)карбоновую кислоту, α-метилпролин, 1-метилгистидин, 3-метилгистидин и 4,5,6,7-тетрагидро-1Н-имидазо-[4,5-с]-пиридин-6-карбоновой кислоты β-(1,2,4-триазол-1-ил)-аланин.
В данном описании термин «белок, представляющий интерес» означает белок (или белки), который желательно получить в изолированной, концентрированной или очищенной форме по сравнению с белком, присутствующем в белоксодержащем растворе (см. ниже). В некоторых случаях белок, представляющий интерес, может претерпевать некоторые четко определенные изменения в способе хроматографического процесса; конечно, следует понимать, что в таких случаях белок, представляющий интерес, в белоксодержащем растворе и в полученной форме может не быть химически или структурно одинаковым.
Считается, что хроматографический способ особенно пригоден для белков, которые способны к самоассоциации и/или структурным изменениям в присутствии ди- или поливалентных ионов металлов. Примерами таких белков являются инсулиновые пептиды, глюкагон-подобные пептиды, эксендины, глюкагон, hGH (человеческий гормон роста), апротинин, инсулин-подобный фактор роста-1, инсулин-подобный фактор роста-2, желудочный ингибирующий пептид, рилизинг-фактор гормона роста, пептид, активирующий аденилатциклазу гипофиза, секретин, энтерогастрин, соматостатин, соматотропин, соматомедин, паратгормон, тромбопоэтин, эритропоэтин, гипоталамические рилизинг-факторы, пролактин, тиреотропные гормоны, эндорфины, энкефалины, вазопрессин, окситоцин, опиоиды, GIP (желудочный ингибиторный полипептид), амид пептида гистидин-метионин, хелоспектины, гелодермин, пептид, связанный с пептидом, активирующим аденилатциклазу гипофиза, вазоактивный кишечный полипептид, в том числе его варианты (см. ниже).
Наиболее интересные в настоящее время белки выбраны среди инсулиновых пептидов, глюкагон-подобных пептидов и эксендинов, включая их варианты.
В некоторых особенно интересных воплощениях белок, представляющий интерес, выбран из инсулиновых полипептидов, включая их варианты.
Особенно интересной группой белков является та, которая представлена белками, способными к самоассоциации в присутствии ионов двухвалентных металлов, таких как Zn2+.
Термин «вариант», используемый в данном документе по отношению к белку, означает модифицированный белок, который является аналогом родительского белка, производным родительского белка (включая DPP-IV-защищенные формы) или производным аналога родительского белка (включая DPP-IV-защищенные формы).
Термин «аналог», используемый в данном документе по отношению к белку, означает модифицированный белок, в котором один или более чем один аминокислотный остаток белка замещен другим аминокислотным остатком, и/или в котором один или более чем один аминокислотный остаток удален из белка, и/или в котором один или более чем один аминокислотный добавлен к белку. Такое добавление или удаление аминокислотных остатков может иметь место на М-конце белка и/или на С-конце белка. Две различные и простые системы часто используются для описания аналогов: например, Arg34-GLP-1 (7-37) или K34R-GLP-1 (7-37) обозначают аналог GLP-1, в котором природный лизин в позиции 34 заменен аргинином (стандартные однобуквенные аббревиатуры для аминокислот используются в соответствии с номенклатурой IUPAC-IUB).
Термин «производное», используемый в данном документе по отношению к родительскому белку, означает химически модифицированный родительский белок или его аналог, в котором по меньшей мере один заместитель не присутствует в родительском белке или его аналоге, т.е. родительский белок, который подвергся ковалентной модификации. Типичными модификациями являются амиды, углеводы, алкильные группы, ацильные группы, сложные эфиры, пегилирование и т.п. Примером производного GLP-1 (7-37) является Arg34, Lys26(Nε-(γ-Glu(Nα-гексадеканоил)))-GLP-1(7-37). Производные также включают DPP-IV-защищенные формы изучаемого белка.
Термин «DPP-IV-защищенный», используемый в данном документе по отношению к белку, означает белок, который был химически модифицирован для того, чтобы сделать указанное соединение устойчивым к плазматической пептидазе дипептидиламинопептидазе-4 (DPP-IV). Фермент DPP-IV в плазме, как известно, участвует в разрушении некоторых белков (например, пептидных гормонов), например, GLP-1, GLP-2, эксендина-4 и т.д. Таким образом, нужно приложить значительные усилия, чтобы разработать аналоги и производные белков, чувствительные к DPP-IV-опосредованному гидролизу, с тем чтобы уменьшить скорость деградации посредством DPP-IV. В одном воплощении DPP-IV-защищенный белок является более устойчивым к DPP-IV, чем GLP-1 (7-37) или эксендин-4(1-39).
Термин «человеческий инсулин», используемый в данном документе, обозначает человеческий гормон инсулин, структура и свойства которого хорошо известны. Человеческий инсулин состоит из двух полипептидных цепей, называемых A-цепью и B-цепью. A-цепь является 21-аминокислотным пептидом, а B-цепь является 30-аминокислотным пептидом, при этом две цепи соединены дисульфидными мостиками: первый мостик между цистеином в позиции 7 A-цепи и цистеином в позиции 7 B-цепи, и второй между цистеином в позиции 20 A-цепи и цистеином в позиции 19 B-цепи. Третий мостик находится между цистеинами в позициях 6 и 11 A-цепи.
В человеческом организме гормон синтезируется в виде одноцепочечного предшественника проинсулина (препроинсулина), состоящего из препептида из 24 аминокислот, за которым следует проинсулин, содержащий 86 аминокислот в следующей конфигурации: препептид-B-Arg Arg-C-Lys Arg-A, где C представляет собой связывающий пептид из 31 аминокислоты. Arg-Arg и Lys-Arg являются сайтами расщепления для отщепления связывающего пептида от A- и B-цепей.
Под «инсулином» в данном документе понимается человеческий инсулин или инсулин от других видов, такой как свиной или бычий инсулин.
Термин «инсулиновый пептид», используемый в данном документе, обозначает пептид (белок), который является инсулином или его аналогом или производным с инсулиновой активностью, т.е. активирует инсулиновый рецептор.
Термин «инсулиновый аналог», используемый в данном документе, означает модифицированный инсулин, в котором один или более чем один аминокислотный остаток инсулина замещен другим аминокислотным остатком, и/или в котором один или более чем один аминокислотный остаток удален из инсулина, и/или в котором один или более чем один аминокислотный добавлен к инсулину. Аминокислоты предпочтительно представляют собой аминокислоты, которые могут быть кодированы триплетом («кодоном») нуклеотидов, см. генную инженерию. В данном документе аминокислоты могут быть предоставлены их стандартными трехбуквенными кодами, предпочтительно: Gly, Pro, Ala, Val, Leu, Ile, Met, Cys, Phe, Tyr, Trp, His, Lys, Arg, Gin, Asn, Glu, Asp, Ser и Thr. Альтернативно, могут быть использованы однобуквенные коды.
В одном воплощении инсулиновый аналог содержит менее 8 модификаций (замен, делеций, добавлений (включая инсерции) и любых их комбинаций) по сравнению с родительским инсулином, альтернативно менее 7 модификаций по сравнению с родительским инсулином, альтернативно менее 6 модификаций по сравнению с родительским инсулином, альтернативно менее 5 модификаций по сравнению с родительским инсулином, альтернативно менее 4 модификаций по сравнению с родительским инсулином, альтернативно менее 3 модификаций по сравнению с родительским инсулином, альтернативно менее 2 модификаций по сравнению с родительским инсулином.
Модификации в молекуле инсулина обозначают с указанием цепи (A или B), позиции и одно- или трехбуквенного кода для аминокислотного остатка, заменяющего остаток природной аминокислоты.
Под «соединительным пептидом» или «C-пептидом» понимается соединяющая группировка «C» полипептидной последовательности B-C-A одноцепочечной проинсулиновой молекулы. В цепи человеческого инсулина C-пептид соединяет позицию 30 B-цепи и позицию 1 A-цепи и имеет 35 аминокислотных остатков в длину. Связывающий пептид включает две концевых двухосновных аминокислотных последовательности, например, Arg-Arg и Lys-Arg, которые выступают в качестве сайтов рестрикции для отщепления соединительного пептида от A- и B-цепей, чтобы сформировать двуцепочечную молекулу инсулина.
Под «desB30» или «B(1-29)» понимается природная инсулиновая B-цепь или ее аналог, в котором отсутствует аминокислотный остаток B30, а под «A(1-21)» понимается природная A-цепь инсулина. Таким образом, например, человеческий инсулин A21Gly, B28Asp, desB30 представляет собой аналог человеческого инсулина, в котором аминокислота в позиции 21 A-цепи замещена глицином, аминокислота в позиции 28 в B-цепи замещена аспарагиновой кислотой, а аминокислота в позиции 30 B-цепи удалена.
В данном документе такие термины как «A1», «A2», «A3» и т.д. показывают, соответственно, позиции 1, 2 и 3 в A-цепи инсулина (считая с N-конца). Аналогичным образом такие термины как «B1», «B2», «B3» и т.д. показывают, соответственно, позиции 1, 2 и 3 в В-цепи инсулина (считая с N-конца). При использовании однобуквенных кодов аминокислот такие термины, как «A21A», «A21G» и «A21Q» обозначают, что аминокислота в позиции A21 представляет собой A, G и Q, соответственно. При использовании трехбуквенных кодов аминокислот соответствующие выражения представляют собой A21Ala, A21Gly и A21Gin, соответственно.
В данном документе термины «A(0)» или «B(0)» указывают на позиции аминокислот, соседних с N-конца по отношению к A1 или B1, соответственно. Термины «A(-1)» или «B(-1)» указывают на позиции первых аминокислот с N-конца от A(0) или B(0), соответственно. Таким образом, «A(-2)» и «B(-2)» указывают на аминокислотные позиции, N-концевые по отношению к A(-1) и B(-1), соответственно, A(-3) и B(-3) указывают на аминокислотные позиции, N-концевые по отношению к A(-2) и B(-2), соответственно, и т.д.
В данном документе термины «A(0)» или «B(0)» указывают на позиции аминокислот, соседних с N-конца по отношению к A1 или B1, соответственно. Термины «A(-1)» или «В(-1)» указывают на позиции первых аминокислот с N-конца от A(0) или B(0), соответственно. Таким образом, «А(-2)» и «В(-2)» указывают на аминокислотные позиции, N-концевые по отношению к A(-1) и B(-1), соответственно, «А(-3)» и «В(-3)» указывают на аминокислотные позиции, N-концевые по отношению к A(-2) и B(-2), соответственно, и т.д. Термины «A22» или «B31» указывают на позиции аминокислот, C-концевых по отношению к А21 или B30, соответственно. Термины «A23» или «B32» указывают на позиции первых аминокислот, C-концевых по отношению к A22 или B31, соответственно. Таким образом, A24 и B33 указывают на позиции аминокислот, C-концевых по отношению к A23 и B32, соответственно, и т.д.
Примерами инсулиновых аналогов являются такие, в которых Pro в позиции 28 B-цепи заменен на Asp, Lys, Leu, Val или Ala, и/или Lys в позиции B29 заменен на Pro, Glu или Asp. Кроме того, Asn в позиции B3 может быть заменен на Thr, Lys, Gin, Glu или Asp. Аминокислотный остаток в позиции A21 может быть заменен на Gly. Также одна или более чем одна аминокислота может быть добавлена к C-концу A-цепи и/или B-цепи, например, Lys. Аминокислота в позиции В1 может быть заменена на Glu. Аминокислота в позиции B16 может быть заменена на Glu или His. Другими примерами инсулиновых аналогов являются аналоги с делециями, например аналоги, в которых аминокислота B30 человеческого инсулина удалена (человеческий инсулин des(B30)), инсулиновые аналоги, в которых аминокислота B1 человеческого инсулина удалена (человеческий инсулин des(B1)), человеческий инсулин des(B28-B30) и человеческий инсулин des(B27). Также примерами инсулиновых аналогов являются инсулиновые аналоги, в которых A-цепь и/или B-цепь имеют N-концевое удлинение, и инсулиновые аналоги, в которых A-цепь и/или B-цепь имеют C-концевое удлинение, например два остатка аргинина, добавленные к C-концу B-цепи. Другими примерами являются инсулиновые аналоги, содержащие комбинации упомянутых мутаций. Другими примерами инсулиновых аналогов являются инсулиновые аналоги, в которых аминокислота в позиции A14 является Asn, Gin, Glu, Arg, Asp, Gly или His, аминокислота в позиции B25 является His, и которые также, возможно, включают одну или более чем одну дополнительную мутацию. Также примерами инсулиновых аналогов являются инсулиновые аналоги человеческого инсулина, где аминокислотный остаток в позиции A21 является Gly, и где инсулиновый аналог также удлинен на C-конце двумя остатками аргинина.
Другие примеры аналогов инсулина включают, но не ограничиваясь ими: человеческий инсулин desB30; человеческий инсулин AspB28; человеческий инсулин AspB28, desB30; человеческий инсулин LysB3, GluB29; человеческий инсулин LysB28, ProB29; человеческий инсулин GlyA21, ArgB31, ArgB32; человеческий инсулин GluA14, HisB25; человеческий инсулин HisA14, HisB25; человеческий инсулин GluA14, HisB25, desB30; человеческий инсулин HisA14, HisB25, desB30; человеческий инсулин GluA14, HisB25, desB27, desB28, desB29, desB30; человеческий инсулин GluA14, HisB25, GluB27, desB30; человеческий инсулин GluA14, HisB16, HisB25, desB30; человеческий инсулин HisA14, HisB16, HisB25, desB30; человеческий инсулин HisA8, GluA14, HisB25, GluB27, desB30; человеческий инсулин HisA8, GluA14, GluB1, GluB16, HisB25, GluB27, desB30 и человеческий инсулин HisA8, GluA14, GluB16, HisB25, desB30.
Термин «производное инсулина», используемый в данном документе, означает химически модифицированный родительский белок или его аналог, в котором модификация(и) находится в форме амидов, углеводородов, алкильных групп, ацильных групп, сложных эфиров, пегилирования и т.п. Примерами производных человеческого инсулина являются метиловый эфир треонина человеческого инсулина ВЗО, человеческий инсулин GlyA21, ArgB31, Arg-амидB32, человеческий инсулин NεB29-тетрадеканоил desB30, человеческий инсулин NεB29-тетрадеканоил, человеческий инсулин NεB29-деканоил desB30, человеческий инсулин NεB29-додеканоил desB30, человеческий NεB29-3-(2-{2-(2-метокси-этокси)-этокси}-этокси)-пропионил-инсулин, человеческий инсулин LysB29(Nε-гексадекандиол-γ-Glu)des(B30)); человеческий инсулин NεB29-(Nα-(Sar-OC(CH2)13CO)-γ-Glu)desB30, человеческий инсулин NεB29-ω-карбокси-пентадеканоил-γ-L-глутамиламид desB30, человеческий инсулин NεB29-гексадекандиол-γ-амино-бутаноил desB30, инсулин NεB29-гексадекандиол-γ-L-Glu-амид desB30.
Термин «глюкагон-подобный пептид», используемый в данном документе, относится к гомологичным пептидам глюкагон-подобному пептиду 1 (GLP-1), глюкагон-подобному пептиду 2 (GLP-2) и оксинтомодулину (ОХМ), полученным из гена препроглюкагона, эксендинам, а также к их аналогам и производным. Эксендины, которые найдены у Gila monster, гомологичны GLP-1, а также оказывают инсулинотропный эффект. Примерами эксендинов являются эксендин-4 и эксендин-3.
Термин «пептид GLP-1», используемый в данном документе, обозначает GLP-1 (7-37), амид GLP-1 (7-36), а также их аналоги и производные, которые можно получить с помощью обычных методик рекомбинантной ДНК, а также обычных синтетических способов. Такие GLP-1-пептиды включают, но не ограничиваясь ими, нативный глюкагон-подобный пептид-1, например, такие пептидные фрагменты, которые включают GLP-1 (7-37) и их функциональные производные, описанные в WO 87/06941; такие пептидные фрагменты, которые включают GLP-1 (7-36) и их функциональные производные, описанные в WO 90/11296; такие аналоги активных GLP-1-пептидов 7-34, 7-35, 7-36 и 7-37, описанные в WO 91/11457; такие производные GLP-1, в которых липофильный заместитель присоединен по меньшей мере к одному аминокислотному остатку, как описано в WO 98/08871; такие усеченные с М-конца фрагменты GLP-1, которые описаны в EP 0699686-А2; и такие аналоги и производные GLP-1, которые содержат N-концевую группу имидазола, как описано в EP 0708179-А2.
Термин «пептид GLP-2», используемый в данном документе, обозначает GLP-2 (1-35), GLP-2 (1-34), GLP-2 (1-33), а также их аналоги и производные, которые можно получить с помощью обычных методик рекомбинантной ДНК, а также обычных синтетических способов. Такие GLP-2-пептиды включают, но не ограничиваясь ими, нативный глюкагон-подобный пептид-2, производные GLP-2, в которых липофильный заместитель присоединен по меньшей мере к одному аминокислотному остатку, как описано в WO 98/08872, человеческий глюкагон-подобный пептид-2 (hGLP-2), GLP-2(1-30); GLP-2(1-31); GLP-2(1-32); GLP-2(1-33); GLP-2(1-34), GLP-2(1-35), Lys20GLP-2(1-33), Lys20Arg30GLP-2(1-33), Arg30Lys34GLP-2(1-34), Arg30Lys35GLP-2(1-35), Arg30,35Lys20GLP-2(1-35), Arg35GLP-2(1-35), Lys20(Nε-тетрадеканоил)GLP-2(1-33); Lys20,30-бис(Nε-тетрадеканоил)GLP-2(1-33); Lys20(Nε-тетрадеканоил)Arg30GLP-2(1-33); Arg30Lys35(Nε-тетрадеканоил)GLP-2(1-35); Arg30,35Lys20(Nε-тетрадеканоил)GLP-2(1-35); Arg35Lys30(Nε-тетрадеканоил)GLP-2(1-35); Arg30Lys34(Nε-тетрадеканоил)GLP-2(1-34); Lys20(Nε-(ω-карбоксинонадеканоил))GLP-2(1-33); Lys20,30-бис(Nε-(ω-карбоксинонадеканоил))GLP-2(1-33); Lys20(Nε-(ω-карбоксинонадеканоил))-Arg30GLP-2(1-33); Arg30Lys35(Nε-(ω-карбоксинонадеканоил))GLP-2(1-35); Lys30(Nε-(γ-глутамил(Nα-тетрадеканоил)))hGLP-2, Lys30(Nε-(γ-глутамил(Nα-гексадеканоил)))hGLP-2, Arg30,35Lys20(Nε-(ω-карбоксинонадеканоил))GLP-2(1-35); Arg30Lys34(Nε-(ω-карбоксинонадеканоил))GLP-2(1-35); и Arg30Lys34(Nε-(ω-карбоксинонадеканоил))GLP-2(1-34).
Термин «эксендин», используемый в данном документе, обозначает эксендин, а также его аналоги, производные и фрагменты, например, эксендин-3 и -4. Эксендин, а также его аналоги, производные и фрагменты описаны, например, в WO 99/43708, содержание которого включено в данное описание посредством ссылки во всей его полноте.
Одной из целей данного изобретения является разработка способа удаления одной или более чем одной родственной примеси в отношении белка, представляющего интерес.
Термин «родственная примесь» при использовании в данном документе означает примесь, которая обладает структурным сходством с белком, представляющим интерес. Родственная примесь имеет химическую или физическую структуру, отличную от белка, представляющего интерес, например усеченную форму, удлиненную форму (дополнительные аминокислоты, различные производные и т.д.), дезамидированную форму, неправильно свернутую форму, форму с нежелательным (например, избыточным, неверным или недостаточным) гликозилированием, включая сиалилирование, окисленные формы, формы, полученные при рацемизации, формы, в которых ацилирование имеет место на другом остатке, чем было нужно, и другие.
В одном воплощении такие родственные примеси элюируются перед белком, представляющим интерес.
Из этого следует, что термин «неродственные примеси», используемые в данном документе, обозначает примеси, которые отличаются от родственных примесей.
В отличие от родственных примесей неродственные примеси могут быть антигенными.
Белоксодержащий раствор
Исходным материалом для хроматографического процесса может быть любой белоксодержащий раствор, который содержит белок, представляющий интерес, такой как белок, выбранный среди инсулиновых пептидов, глюкагон-подобных пептидов и эксендинов, включая их варианты (см. выше). В качестве исходного материала может выступать среда, полученная непосредственно из экспрессионной системы дрожжей или непосредственно путем химического синтеза, либо исходный материал может быть подвергнут нескольким этапам очистки или химической модификации перед способом в соответствии с изобретением.
В некоторых интересных воплощениях белоксодержащий раствор содержит один или более чем один ди- или поливалентный ион металла. Без связи с какой-либо конкретной теорией, в настоящее время считается, что такие ди- или поливалентные ионы металлов способствуют самоассоциации и/или структурным модификациям белка, представляющего интерес, при которых форма пика в хроматографическом процессе будет изменена таким образом, что близкородственные примеси, в частности те, которые элюируются перед белком, представляющим интерес, могут быть отделены от белка, представляющего интерес.
Отличительным свойством инсулина является его способность ассоциировать в гексамеры, в форме которых гормон защищен от химической и физической деградации в процессе биосинтеза и хранения. Рентгеноструктурные исследования инсулина показывают, что гексамер состоит из трех димеров, связанных по трем осям вращения. Эти димеры тесно связаны посредством взаимодействия двух ионов цинка в их центральной части, расположенной на 3 осях.
Подходящими примерами ди- или поливалентных ионов металлов, в том числе ионов переходных металлов, являются те, которые выбраны среди Zn2+, Ca2+, Mg2+, Ni2+, Cu2+, Ba2+, предпочтительно Zn2+. В белоксодержащем растворе могут присутствовать два или более двух типов ди- или поливалентных ионов металлов, или только один тип.
Концентрация ди- или поливалентных ионов металла в белоксодержащем растворе обычно находится в диапазоне 0,01-200 мМ, например 0,1-100 мМ, например, 0,5-75 мМ.
Соотношение эквивалентов заряда ди- или поливалентных ионов металлов и белка, представляющего интерес, (т.е. эквивалентный заряд на молекулу белка, представляющего интерес) обычно составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например, от 0,4:1 до 15:1 или от 0,5:1 до 10:1.
В тех случаях, когда белок, представляющий интерес, представляет собой инсулиновый пептид, соотношение между эквивалентами заряда ди- или поливалентных ионов металлов, например, ионов Zn2+, и инсулинового пептида обычно составляет от 1:6 до 20:6, например, от 2:6 до 15:6, например, от 3:6 до 10:6, или от 3:6 до 5:6, или от 7:6 до 9:6. В качестве иллюстративного примера, два иона цинка на одну молекулу инсулина понимается как отношение между эквивалентами заряда ди- или поливалентных ионов металлов (Zn2+) и инсулина 4:1 (т.е. (2 цинка * 2 заряда на каждый цинк): 1). В присутствии Zn2+ инсулин способен к самоассоциации путем формирования гексамеров, дигексамеров или даже больших комплексов инсулинового пептида, которые все еще являются растворимыми, которые используются в кристаллизации инсулина. Следовательно, в некоторых воплощениях белоксодержащий раствор получают из инсулинового пептида, кристаллизованного с цинком.
Кроме того, может быть желательным или необходимым регулировка концентрации любых растворителей или уменьшение ионной силы путем добавления воды к белоксодержащему раствору. Значение pH может быть отрегулировано с помощью подходящего буфера, и можно добавить растворитель, например этанол, чтобы увеличить растворимость белка, представляющего интерес. Таким образом, белоксодержащий раствор также может содержать растворители, соли, буферы, модификаторы/эксципиенты (органические или неорганические). Органический растворитель может представлять собой, но не ограничиваясь этим, какой-либо одноатомный алифатический спирт (метанол, этанол, пропанолы и бутанолы), например, метанол, этанол, 2-пропанол, 1-пропанол и гексиленгликоль. Дополнительные солевые компоненты для любой части хроматографической очистки могут представлять собой любую соль, включая, но не ограничиваясь ими: NaCl, KCl, NK4Cl, ацетат натрия, ацетат калия, ацетат аммония и т.д. Может быть использован любой буферный компонент, включая, но не ограничиваясь ими: цитратные буферы, фосфатные буферы, Tris-буферы, боратные буферы, карбонатные буферы, ацетатные буферы, аммонийные буферы, глициновые буферы и т.д. В одном воплощении растворитель pH-буферизован в диапазоне от pH 5 до pH 9.
Ионная сила, указанная как проводимость белоксодержащего раствора при 25°C, также может играть роль. Таким образом, в некоторых воплощениях проводимость белоксодержащего раствора находится в диапазоне 0-100 мСм/см, например, 0-50 мСм/см, например, 0-30 мСм/см или 0,01-100 мСм/см, например, 0,05-50 мСм, например, 0,1-30 мСм/см.
Значение pH белоксодержащего раствора обычно поддерживают в интервале 0-14, 1-13, 2-12, 3-11 или 4-10. Тем не менее, во многих случаях значение pH белоксодержащего раствора является примерно таким же, как величина pH элюента.
Хроматографический процесс
Целью хроматографического процесса является отделение белка, представляющего интерес, от других компонентов белоксодержащего раствора, или получение белка, представляющего интерес, с более высокой степенью чистоты, или по меньшей мере уменьшение присутствия одной или более чем одной примеси, родственной белку, представляющему интерес.
Хроматографический процесс будет подробно описан далее.
Этап (а)
На первом этапе процесса в соответствии с изобретением белоксодержащий раствор наносят на колонку с хроматографическим твердофазным материалом.
Твердофазный материал выбирают в соответствии с типом хроматографического процесса, например, обращенно-фазовой хроматографии (RPC), ионообменной хроматографии (IEC), такой как анионообменная хроматография (AIEC) или катионообменная хроматография (CIEC), хроматографии гидрофобного взаимодействия (HIC), аффинной хроматографии, эксклюзионной хроматографии, металл-хелатной хроматографии, псевдоаффинной хроматографии, хроматографии смешанного режима и т.д. Предпочтительно используется ионообменный Хроматографический материал, в частности анионообменный Хроматографический материал.
Поскольку ионообменный Хроматографический процесс является желательным, твердофазный материал может быть выбран в зависимости от конкретного пептида, который нужно очистить, и от используемых условий, таких как pH, буфер, ионная сила и т.д., которые известны специалистам в данной области (т.е., как правило, pH ниже изоэлектрической точки (pI) пептида для катионообменных смол и pH выше изоэлектрической точки пептида для анионообменных смол, достаточная сила буфера для поддержания нужного pH и достаточно низкая ионная сила, возможно вызванная концентрацией соли). Неограничивающие примеры подходящих твердофазных материалов включают смолы Sepharose, смолы Sephadex, смолы Streamline и смолы Source от Amersham-Pharmacia Biotech, смолы HyperD, смолы Trisacryl и смолы Spherosil от BioSepra, смолы TSKgel и смолы Toyoperal от TosoHaas, смолы Fractogel EMD от Merck, смолы Poros от Perseptive Biosystems, смолы Macro-Prep от BioRAD, смолы Express-ion от Whatman и т.д.
Для обращенно-фазового хроматографического процесса твердофазный материал может представлять собой любой выбор обращенно-фазовой хроматографической смолы, возможно с любым замещением, включая, но не ограничиваясь этим: смолы на основе оксида кремния, такие как Kromasil 100 C18, смолы на основе полимеров, такие как Source от Amersham Biosciences, материалы Poros от Applied Biosystems, например, обращенно-фазовые смолы Poros R1, R2 и R3, смолы на керамической основе от Cipherge, смолы на основе оксидов металлов и другие. Предпочтительно используется смола на основе оксида кремния. Раствор для уравновешивания (раствор для уравновешивания твердофазных материалов перед этапом (а)) и белковый раствор для нанесения могут содержать или не содержать органический растворитель. Органический растворитель может представлять собой, но не ограничиваясь ими, какой-либо одноатомный алифатический спирт (метанол, этанол, пропанолы и бутанолы), например, метанол, этанол, 2-пропанол, 1-пропанол и гексиленгликоль. Дополнительные солевые компоненты для любого раздела хроматографической очистки могут представлять собой любую соль, включая, но не ограничиваясь ими: NaCl, KCl, NH4Cl, CaCl2, ацетат натрия, ацетат калия, ацетат аммония и т.д. Может быть использован любой буферный компонент, включая, но не ограничиваясь ими: цитратные буферы, фосфатные буферы, Tris-буферы, боратные буферы, карбонатные буферы, ацетатные буферы, аммонийные буферы, глициновые буферы и т.д. В одном воплощении растворитель pH-буферизован в диапазоне от pH 5 до pH 9.
В одном воплощении процесс обращенно-фазовой высокоэффективной жидкостной хроматографии выполняется с использованием хроматографической смолы на основе диоксида кремния, например, замещенного силикагеля, такого как C4-, C6-, C8-, C12-, C16-, C18-, C20-, фенил- или бензолзамещенного силикагеля. В другом воплощении процесс обращенно-фазовой высокоэффективной жидкостной хроматографии выполняется с использованием хроматографической смолы, которая представляет собой материал на основе полимера.
Для хроматографии гидрофобного взаимодействия твердофазный материал является матрицей, замещенной гидрофобными лигандами, такими как этил-, бутил, фенил- или гексил- (которые, по-видимому, ответственны за связывание белка). Предпочтительными материалами являются материалы, замещенные бутил- и/или фенил-лигандами.
Используемый твердофазный материал наиболее часто представлен в форме шариков, например, материала в виде частиц со средним диаметром в диапазоне 0,1-1000 мкм, например, в диапазоне 1-100 мкм. Твердофазный материал соответствующим образом расположен в ВЭЖХ-колонке, собранной с насосами и т.д., что будет очевидно специалисту.
Нанесение белоксодержащего раствора на колонку с хроматографическим твердофазным материалом обычно проводят в соответствии со стандартными протоколами, т.е. концентрация, температура, ионная сила и т.д. белоксодержащего раствора могут быть обычными (с изменениями, предложенными в данном документе), и хроматографический материал гидрофобного взаимодействия может быть промыт и уравновешен до применения, как обычно.
Было обнаружено, что нагрузка белком, представляющим интерес, может быть достаточно высокой, например, по меньшей мере 6,0 г белка, представляющего интерес, на литр объема колонки (г/лCV), а также за счет улучшения формы пика в процессе объем пула будет несколько уменьшен по сравнению с обычными процессами. В некоторых воплощениях нагрузка белком, представляющим интерес, составляет по меньшей мере 7,0 г/лCV, или по меньшей мере, 8,0 г/лCV, или по меньшей мере 8,5 г/лCV, или 6,0-50 г/лCV, или 7,0-40 г/лCV, или 8,0-30 г/лCV, например 8,5-25 г/лCV, например 9,0-20 г/лCV или 9,5-15 г/лCV. Нагрузка белком, представляющим интерес, максимально может быть нагрузкой до емкости колонны. Объем колонки обычно соответствует объему упакованного набухшего хроматографического твердофазного материала.
Хотя не ограничиваясь этим, способ данного изобретения особенно возможен для применения в «крупномасштабных» (или «промышленных») целях. Таким образом, в некоторых важных воплощениях процесс является крупномасштабным процессом, при котором объем колонки составляет по меньшей мере 1 л, или по меньшей мере 10 л, или по меньшей мере 20 л, или по меньшей мере 50 л, или по меньшей мере 100 л, например, по меньшей мере 500 л, например, по меньшей мере 1000 л или по меньшей мере 5000 л.
Хотя это не очень критично, но может быть желательной регулировка температуры колонки и белоксодержащего раствора, чтобы сделать еще лучше форму пика. Как правило, температура составляет 0-70°C, 0-50°C, например, 2-30°C. Температуру колонки можно поддерживать в пределах указанного диапазона с помощью охлаждающей рубашки и растворов с контролируемой температурой.
Этап (б)
На втором этапе процесса, который обычно проводится без прерывания общего процесса, представляющий интерес белок элюируют из твердофазного материала с помощью элюента.
Типичный принцип элюции при ионообменной хроматографии в процессах промышленных очистки заключается в применении градиентов солевого компонента в водном буферном растворе при постоянном значении pH, либо поэтапных, либо линейных градиентов. Также возможно изократическое элюирование. К элюенту могут быть добавлены органические растворители или модификаторы для поддержания белка в нужной форме или просто в растворе. Кроме того, изменение pH иногда может быть использовано для элюции белка, представляющего интерес.
В процессе хроматографии гидрофобного взаимодействия тип элюции не является особенно критичным, таким образом, например, можно проводить элюцию с помощью буфера для элюции, содержащего ступенчато уменьшающийся градиент соли и/или цвиттерионов, элюировать с линейно уменьшающийся градиентом соли (или профиль градиент-задержка-градиент, или другие варианты), или использовать градиент pH или градиент температуры или комбинацию всего вышеупомянутого. Кроме того, в качестве буфера для элюции может быть использован градиент кальций-хелатирующего соединения (например, EDTA, цитрата, малоната и т.д.) или растворитель, менее полярный, чем вода (например, водные растворы, содержащие этанол, полиэтиленгликоль, 2-пропанол и т.п.). В одном воплощении элюирующий буфер содержит соль в начальной концентрации в диапазоне 0,7-2,2 М. Таким образом, в одном воплощении элюирующий буфер является градиентным буфером в отношении соли аммония, при этом начальная концентрация соли аммония в градиентном буфере находится в диапазоне 1,7-2,2 М, конечная концентрация соли аммония в градиентном буфере находится в диапазоне 0,0-1,6 М. Проводимость конечного буфера для элюции предпочтительно является более низкой, чем проводимость белоксодержащего раствора на этапе (а). Во многих случаях элюирующий буфер на этапе (б) имеет такой же pH, как на этапе (а).
Для процесса обращенно-фазовой высокоэффективной жидкостной хроматографии используемый растворитель для элюции, как правило, является pH-буферизованным в диапазоне от pH 4 до pH 10. Элюент может содержать спирт в концентрации от 10% вес/вес до 80% вес/вес. Белок, представляющий интерес, и примеси можно элюировать и разделять путем ступенчатого, асимптотического или линейного изменения градиента или изократически в органическом растворителе, или при их комбинации. Градиент компонента органического растворителя будет идти от более низкой к более высокой концентрации. Элюция также возможна путем изменения рН и/или температуры в элюирующем разделе.
Выбор исходного pH, буфера и ионной силы осуществляется в соответствии с известными методиками, такими как обычные способы «в пробирке», см., например, справочники от Amersham-Pharmacia Biotech или Fundamentals of preparative and nonlinear chromatography, Georges Guiochon, Dean G. Shirazi, Attila Felinger, Anita M. Katti, Academic Press, 2006.
В одном воплощении элюент содержит солевой компонент, выбранный среди любых органических или неорганических солей, предпочтительно NaCl, KCl, NH4Cl, CaCl2, ацетата натрия, ацетата калия, ацетата аммония, цитрата натрия, цитрата калия, цитрата аммония, сульфата натрия, сульфата калия, сульфата аммония, ацетата кальция или их смесей, наиболее предпочтительно ацетата натрия, ацетата калия, ацетата аммония, NaCl, NH4Cl, KCl.
Солевой компонент обычно присутствует в концентрации от 0,1 мМ до 3000 мМ, предпочтительно от 1 мМ до 1000 мМ, более предпочтительно от 5 мМ до 500 мМ, наиболее предпочтительно от 20 мМ до 300 мМ.
Элюент также может содержать буфер, например, выбранный среди цитратных буферов, фосфатных буферов, Tris-буферов, боратных буферов, лактатных буферов, глицилглициновых буферов, аргининовых буферов, карбонатных буферов, ацетатных буферов, глутаматных буферов, аммонийных буферов, глициновых буферов, алкиламиновых буферов, аминоэтилспиртовых буферов, этилендиаминовых буферов, триэтаноламиновых буферов, имидазольных буферов, пиридиновых буферов и барбитуратных буферов и их смесей, предпочтительно лимонной кислоты, цитрата натрия, фосфата натрия, фосфорной кислоты, глутаминовой кислоты, глутамата натрия, глицина, карбоната натрия, цитрата калия, фосфата калия, глутамата калия, карбоната калия, трисгидроксиметиламинометана и борной кислоты и их смесей.
Буфер обычно присутствует в концентрации от 0,1 мМ до 500 мМ, предпочтительно от 1 мМ до 200 мМ, более предпочтительно от 5 мМ до 100 мМ, наиболее предпочтительно от 10 до 50 мМ.
Значение pH элюента, как правило, составляет максимум 8,5, например, максимум 8,0, или максимум 7,5, или максимум 7,0, или максимум 6,9, или по меньшей мере 6,8, или по меньшей мере 6,7, или по меньшей мере 6,6, или по меньшей мере 6,5, например, в диапазоне 4,5-8,5, или 4,5-8,0, или 4,5-7,5, или 4,5-7,0, например, 4,6-8,0, или 4,6-7,5, или 4,6-7,0, или 4,6-6,9, или 4,7-7,5, или 4,7-7,0, или 4,7-6,7 или 4,8-7,5, или 4,8-7,0, или 4,8-6,6, или 4,9-6,5, или 5,0-6,4.
Было обнаружено, что этот процесс может быть еще улучшен, если pH элюента имеет максимальное значение на 2,1 единицы выше pI белка, представляющего интерес, например, максимум на 1,9 единиц выше, например, максимум на 1,7 единиц выше.
Термин «pI» или «изоэлектрическая точка», используемый в данном документе, означает величину pH, при которой общий суммарный заряд белка равен нулю.
В некоторых воплощениях растворитель также может содержать один или более чем один ди- или поливалентный ион металла, такой как указанные выше для белоксодержащего раствора.
Без связи с какой-либо конкретной теорией, в настоящее время считается, что такие ди- или поливалентные ионы металлов в элюенте способствуют самоассоциации и/или структурным модификациям белка, представляющего интерес, индуцированным на этапе (а), при которых форма пика в хроматографическом процессе будет изменена таким образом, что близкородственные примеси, в частности те, которые элюируются перед белком, представляющим интерес, могут быть отделены от белка, представляющего интерес.
Подходящими примерами ди- или поливалентных ионов металлов, в том числе ионов переходных металлов, являются те, которые выбраны среди Zn2+, Ca2+, Mg2+, Ni2+, Cu2+, Ba2+, предпочтительно Zn2+. В элюенте могут присутствовать два или более двух типов ди- или поливалентных ионов металлов или только один тип.
Концентрация ди- или поливалентных ионов металла в элюенте обычно находится в диапазоне 0,1-200 мМ, например 0,5-100 мМ или 1,0-60 мМ.
В одном конкретном воплощении элюент содержит ионы Zn2+, например, в концентрации в диапазоне 0,01-200 мМ, например 0,1-100 мМ, например, 0,5-75 мМ.
Соотношение эквивалентов заряда ди- или поливалентных ионов металлов и белка, представляющего интерес, (т.е. эквивалентный заряд на молекулу белка, представляющего интерес) обычно составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например, от 0,4:1 до 15:1 или от 0,5:1 до 10:1.
В тех случаях, когда белок, представляющий интерес, представляет собой инсулиновый пептид, соотношение между эквивалентами заряда ди- или поливалентных ионов металлов, например, ионов Zn2+, и инсулинового пептида обычно составляет от 1:6 до 20:6, например, от 2:6 до 15:6, например, от 3:6 до 10:6 или от 3:6 до 5:6, или от 7:6 до 9:6.
В связи с элюцией собирают белок, представляющий интерес. Следовательно, особенностью изобретения является сбор пула белка, представляющего интерес, соответствующего по меньшей мере 75% по весу белку, представляющему интерес, нанесенному на колонку на этапе (а). В некоторых воплощениях пул белка, представляющего интерес, собранный на этапе (б), соответствует по меньшей мере 80% по весу, например, по меньшей мере 85% по весу, или по меньшей мере 90% по весу, или по меньшей мере 91% по весу, или по меньшей мере 92% по весу, или по меньшей мере 93% по весу, или по меньшей мере 94% по весу, или по меньшей мере 95% по весу, или по меньшей мере 96% по весу белку, представляющему интерес, нанесенному на колонку на этапе (а).
С помощью процесса данного изобретения желательно исключить из пула белка, представляющего интерес, любые близкородственные белки.
Следует понимать, что может быть желательным включить после этапа (а), но до этапа (б) этап промывки с использованием промывочного буфера перед этапом элюции (этап (б)). Промывочный буфер, как правило, представляет собой водный раствор, содержащий буферный агент, как правило, буферный агент, содержащий по меньшей мере один компонент, выбранный из группы, состоящей из кислот и солей MES, PIPES, ACES, BES, TES, HEPES, TRIS, гистидина, имидазола, глицина, глицилглицина, глицинамида, фосфорной кислоты, уксусной кислоты (например, ацетата натрия), молочной кислоты, глутаровой кислоты, лимонной кислоты, винной кислоты, яблочной кислоты, малеиновой кислоты и янтарной кислоты. Следует понимать, что буферный агент может включать смесь двух или более компонентов, где смесь способна обеспечить значение pH в указанном диапазоне. В качестве примеров можно назвать уксусную кислоту и ацетат натрия и т.п. Кроме того, должно быть понятно, что этап промывки (б) может быть проведен с применением одного, двух или более различных промывочных буферов или с применением градиентного промывочного буфера. Следует также отметить, что этап промывки и элюции не должны быть дискретными этапами, но могут быть объединены, в частности, если на этапе элюции используется градиентный элюирующий буфер.
Продукт, полученный в процессе согласно изобретению (этапы (а) и (б)), может при желании подвергаться другим стандартным этапам очистки и выделения.
Предпочтительные воплощения данного изобретения в настоящее время В одном предпочтительном в настоящее время воплощении данное изобретение предусматривает процесс хроматографического разделения белковых компонентов инсулинсодержащего раствора, при этом указанный раствор, содержащий инсулиновый пептид, способен самоассоциации и/или структурным изменениям в присутствии цинка и двухвалентных ионов цинка, причем указанный процесс включает следующие этапы:
а. нанесение инсулинсодержащего раствора на колонку с анионообменным хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом, представляющим интерес, составляет по меньшей мере 6,0 г на литр объема колонки (г/лCV); и
б. элюция инсулинового пептида, представляющего интерес, из указанного твердофазного материала с помощью элюента с pH максимум 6,8; и сбор пула представляющего интерес инсулинового пептида, который соответствует по меньшей мере 90% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а).
В одном воплощении, приведенном выше, соотношение между эквивалентами заряда ди- или поливалентных ионов металлов, например, ионов Zn2+, и инсулинового пептида обычно составляет от 1:6 до 20:6, например, от 2:6 до 15:6, например, от 3:6 до 10:6, или от 3:6 до 5:6, или от 7:6 до 9:6.
Изобретение подытожено в следующих пунктах:
1. Хроматографический способ выделения белковых компонентов белоксодержащего раствора, при этом указанный раствор содержит инсулиновый пептид и один или более чем один ди- или поливалентный ион металла, указанный инсулин пептид способен к самоассоциации и/или структурным изменениям в присутствии ди- или поливалентных ионов металлов, причем способ включает следующие этапы:
а. нанесение белкового раствора на колонку с хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом составляет по меньшей мере 6,0 г на литр объема колонки (г/лCV); и
б. элюция инсулинового пептида из указанного твердофазного материала с помощью элюента с pH максимум 8,5; и сбор пула инсулинового пептида, соответствующего по меньшей мере 75% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а).
2. Способ по п.1, в котором ди- или поливалентные ионы металлов выбраны среди Zn2+, Ca2+, Mg2+, Ni2+, Cu2+, Ba2+, предпочтительно Zn2+.
3. Способ по любому из предыдущих пп., в котором концентрация ди- или поливалентных ионов металла в растворе находится в диапазоне 0,01-200 мМ, например 0,1-100 мМ, например 0,5-75 мМ.
4. Способ по любому из предыдущих пунктов, в котором соотношение эквивалентов заряда ди- или поливалентных ионов металлов и инсулинового пептида обычно составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например, от 0,4:1 до 15:1 или от 0,5:1 до 10:1.
5. Способ по любому из предыдущих пунктов, в котором проводимость белоксодержащего раствора находится в диапазоне 0-100 мСм/см, например, 0-50 мСм/см, например, 0-30 мСм/см или 0,01-100 мСм/см, например, 0,05-50 мСм, например, 0,1-30 мСм/см.
6. Способ по любому из предыдущих пунктов, в котором твердофазный материал выбран среди ионообменного хроматографического материала (IEC), обращенно-фазового хроматографического материала (RPC), хроматографического материала гидрофобного взаимодействия (HIC), такого как ионообменный хроматографический материал, в частности анионообменный хроматографический материал.
7. Способ по любому из предыдущих пуктов, в котором нагрузка инсулиновым пептидом составляет по меньшей мере 7,0 г/лCV, или по меньшей мере 8,0 г/лCV, или по меньшей мере 8,5 г/лCV, или 6,0-50 г/лCV, или 7,0-40 г/лCV, или 8,0-30 г/лCV, например 8,5-25 г/лCV, например 9,0-20 г/лCV или 9,5-15 г/лCV.
8. Способ по любому из предыдущих пунктов, в котором pH элюента составляет максимум 8,5, например максимум 8,0, или максимум 7,5, или максимум 7,0, или максимум 6,9, или по меньшей мере 6,8, или по меньшей мере 6,7, или по меньшей мере 6,6, или по меньшей мере 6,5, например, в диапазоне 4,5-8,5, или 4,5-8,0, или 4,5-7,5, или 4,5-7,0, например, 4,6-8,0, или 4,6-7,5, или 4,6-7,0, или 4,6-6,9, или 4,7-7,5, или 4,7-7,0, или 4,7-6,7 или 4,8-7,5, или 4,8-7,0, или 4,8-6,6, или 4,9-6,5, или 5,0-6,4.
9. Способ по любому из предыдущих пунктов, в котором pH элюента имеет максимальное значение на 2,1 единицы выше pI инсулинового пептида, например, максимум на 1,9 единиц выше, например, максимум на 1,7 единиц выше.
10. Способ по любому из предыдущих пунктов, в котором пул инсулинового пептида, собранного на этапе (б), соответствует по меньшей мере 80% по весу, например, по меньшей мере 85% по весу, или по меньшей мере 90% по весу, или по меньшей мере 91% по весу, или по меньшей мере 92% по весу, или по меньшей мере 93% по весу, или по меньшей мере 94% по весу, или по меньшей мере 95% по весу, или по меньшей мере 96% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а).
11. Способ по любому из предыдущих пунктов, в котором концентрация ди- или поливалентных ионов металлов в элюенте находится в диапазоне 0,1-200 мМ, например 0,5-100 мМ или 1,0-60 мМ.
12. Способ по любому из предыдущих пунктов, в котором соотношение эквивалентов заряда ди- или поливалентных ионов металлов в элюенте и инсулинового пептида составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например от 0,4:1 до 15:1 или от 0,5:1 до 10:1
13. Способ по любому из предыдущих пунктов, в котором элюент содержит ионы Zn2+, например, в концентрациях в диапазоне 0,01-200 мМ, например 0,1-100 мМ, например, 0,5-75 мМ.
14. Способ по любому из предыдущих пунктов, в котором инсулиновый пептид выбран среди инсулиновых пептидов, глюкагон-подобных пептидов и эксендинов, включая их варианты, в частности инсулиновых пептидов, включая их варианты.
15. Способ по любому из предыдущих пунктов, в котором белоксодержащий раствор получают из инсулинового пептида, кристаллизованного с цинком.
16. Способ по любому из предыдущих пунктов, который является крупномасштабным способом, в котором объем колонки составляет по меньшей мере 1 л, или по меньшей мере 10 л, или по меньшей мере 20 л, или по меньшей мере 50 л, или по меньшей мере 100 л, например, по меньшей мере 500 л, например, по меньшей мере 1000 л или по меньшей мере 5000 л.
17. Способ по любому из предыдущих пунктов, в котором инсулиновый пептид выбран среди инсулиновых производных, которые являются природным инсулином или его аналогом с боковой цепью, присоединенной к α-аминогруппе N-концевого аминокислотного остатка В-цепи или к ε-аминогруппе остатка Lys, присутствующего в В-цепи родительского инсулина, при этом боковая цепь имеет общую формулу:
-W-X-Y-Z,
где W представляет собой:
- α-аминокислотный остаток с карбоксильной группой в боковой цепи, который формирует через одну из его карбоксильных групп амидную группу вместе с α-аминогруппой N-концевого аминокислотного остатка B-цепи или вместе с ε-аминогруппой остатка Lys, присутствующего в B-цепи родительского инсулина;
- цепь, состоящую из двух, трех или четырех α-аминокислотных остатков, связанных друг с другом посредством амидных связей, которая через амидную связь связана с α-аминогруппой N-концевого аминокислотного остатка B-цепи или с ε-аминогруппой остатка Lys, присутствующего в В-цепи родительского инсулина, при этом аминокислотные остатки W выбраны из группы аминокислотных остатков с нейтральной боковой цепью и аминокислотных остатков с карбоксильной группой в боковую цепи, так что W имеет по меньшей мере один аминокислотный остаток с карбоксильной группой в боковой цепи; либо
- ковалентную связь от Х к α-аминогруппе N-концевого аминокислотного остатка B-цепи или к ε-аминогруппе остатка Lys, присутствующего в B-цепи родительского инсулина;
X представляет собой
- -CO-;
- -СН(COOH)CO-;
- -N(СН2СООН)CH2 CO-;
- -N(CH2COOH)CH2CON(CH2COOH)CH2 CO-;
- -N(CH2CH2COOH)CH2CH2 CO-;
- -N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2CO-;
- -NHCH(COOH)(CH2)4NHCO-;
- -N(CH2CH2COOH)CH2CO-; или
- -N(CH2COOH)CH2CH2CO-.
что
а) когда W представляет собой аминокислотный остаток или цепь аминокислотных остатков, он через связь с подчеркнутым карбонильным углеродом образует амидную связь с аминогруппой в W, или
б) когда W представляет собой ковалентную связь, он через связь с подчеркнутым карбонильным углеродом образует амидную связь с N-концевой α-аминогруппой в B-цепи или с ε-аминогруппой остатка Lys, присутствующего в B-цепи родительского инсулина;
Y представляет собой:
- -(CH2)m-, где m представляет собой целое число в диапазоне от 6 до 32;
- двухвалентную углеводородную цепь, содержащую 1, 2 или 3 группы -CH=CH-, и число групп -CH2-, достаточное, чтобы дать общее число атомов углерода в цепи в диапазоне от 10 до 32;
- двухвалентную углеводородную цепь формулы -(CH2)vC6H4(CH2)w-, где v и w являются целыми числами или один из них равен нулю, так что сумма v и w находится в диапазоне от 6 до 30; а также
Z представляет собой:
- -COOH;
- -CO-Asp;
- -CO-Glu;
- -CO-Gly;
- -CO-Sar;
- -CH(COOH)2;
- -N(CH2COOH)2;
- -SO3H; или
- PO3H;
и любых их комплексов с Zn2+.
18. Способ по любому из предыдущих пунктов, в котором инсулиновый пептид представляет собой человеческий инсулин LysB29(Nε-гексадекандиол-γ-Glu) des(B30).
19. Способ по любому из пп.1-16, в котором инсулиновый пептид представляет собой производное инсулина, имеющее формулу:

где Ins представляет собой фрагмент родительского инсулина, а
Q1-Q2-[CH2]n-X1-[CH2]n-Q3-[CH2]n-X2-[CH2]n-Q4-[CH2]n-X3-[CH2]n-Q5-[CH2]n-Z представляет собой заместитель, и где Ins присоединен к заместителю через амидную связь между α-аминогруппой N-концевого аминокислотного остатка из B-цепи Ins или ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, и CO-группой в Q1 или Q2 заместителя;
каждый n независимо представляет собой 0, 1, 2, 3, 4, 5 или 6;
Q1 является:
- амидом аминокислоты с карбоксильной кислотой в боковой цепи или аминокислоты с незаряженной боковой цепью, остаток которой через его карбоксильную группу формирует амидную группу вместе с α-аминогруппой N-концевого аминокислотного остатка из В-цепи Ins или вместе с ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, либо
- цепью, состоящей из двух, трех или четырех амидов α-аминокислот или аминокислотных остатков, как указано выше, связанных друг с другом с помощью амидной связи, при этом цепь через амидную связь связана с α-аминогруппой N-концевого аминокислотного остатка В-цепи Ins или с ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, либо
- связью.
Q2 представляет собой:
- -COCH(CONH2)-
- -COCH2N(CH2CONH2)-
- -COCH2N(CH2CONH2)COCH2N(CH2CONH2)
- -COCH2CH2N(CH2CH2CONH2)-
- -COCH2CH2N(CH2CH2CONH2)-COCH2CH2N(CH2CH2CONH2)-
- -COCH2N(CH2CH2CONH2)-
- -COCH2CH2N(CH2CONH2)-
- -COCH2OCH2CONH-
- -CO-((CR5R6)1-6-NH-CO)1-4-;
- -СО-((CR5R6)1-6-CO-NH)1-4- где R5 независимо может быть H, -CH3, -(CH2)1-6CH3 или -CONH2, а R6 независимо может представлять собой H, -CH3, -(CH2)1-6CH3; или
- связь
при условии, что
- по меньшей мере один из Q1 или Q2 не является связью, и
- что Q2 не является -СО-(СН2)2-CO-NH- где n составляет 0 или 1, X1 представляет собой связь, а Q3 представляет собой (CH2CH2O)2-, (CH2CH2O)3- или (CH2CH2OCH2CH2CH2CH2O)- и
- что если амин в Q1 или Q2 образует связь с остальной частью заместителя, амин должен быть связан с остальной частью заместителя через карбонильную группу;
Q3, Q4 и Q5 каждый независимо друг от друга может представлять собой
- -(CH2)m-, где m представляет собой целое число в диапазоне от 6 до 32;
- двухвалентную углеводородную цепь, содержащую 1, 2 или 3 группы -CH=СН- и число групп -CH2-, достаточное, чтобы дать общее число атомов углерода в цепи в диапазоне от 4 до 32;
- -CO-((CR5R6)1-6-NH-CO)-;
- -(CO-(CR5R6)1-6-CO-NH)1-4-, где R5 независимо может быть H, -CH3, -(CH2)1-6CH3 или -CONH2, а R6 независимо может быть H, -CH3, -(CH2)1-6CH3;
- -CO-(CH2)0-3-Ar-(CH2)0-3-, где Ar может быть ариленом или гетероариленом, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из -CH3, -(CH)1-6-CH3, -CONR1R2 или -SO2NR1R2, где R1 и R2 независимо друг от друга могут быть H, -CH3 или -(CH)1-6-CH3;
- (CH2CH2O)y-; (CH2CH2CH2O)y- (CH2CH2CH2CH2O)y-(CH2CH2OCH2CH2CH2CH2O)y- или (CH2CH2CH2OCH2CH2CH2CH2O)y- -(CH2OCH2)y- где y составляет 1-20;
- арилен или гетероарилен, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из -CH3, -(CH)1-6-CH3, -CONR1R2 или -SO2NR1R2, где R1 и R2 независимо друг от друга может быть H, -CH3 или -(CH)1-6-СН3;
- цепь с формулой
-(CH2)s-Y1-(Ar)v1-Y2-(CH2)w-Y3-(Ar)v2-Y4-(CH2)t-Y5-(Ar)v3-Y6-(CH2)z-,
где Ar имеет вышеуказанное значение, Y1-Y6 независимо друг от друга могут быть О, S, S=O, SO2 или связью; где s, w, t и z независимо друг от друга составляют ноль или целое число от 1 до 10, так что сумма s, w, t и z находится в диапазоне от 4 до 30, a v1, v2, и v3 независимо друг от друга могут быть равны нулю или 1, при условии, что Y1-Y6 не связаны друг с другом, и что структура -O-(CH2)1-O- не происходит; либо
- связь;
при условии, что по меньшей мере один из Q3-Q5 не является связью;
X1, X2 и X3 независимо друг от друга представляют собой
- О;
- -C=O
- связь;
- NCOR1, где R1 может быть H, -CH3 или -(CH)1-6-CH3; или
-
- 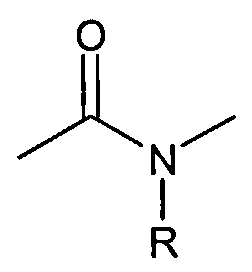 или
или 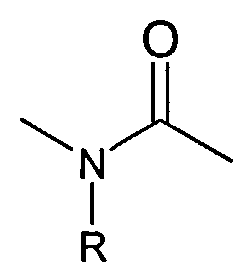
где R представляет собой водород, C1-3-алкин, C2-3-алкенил или C2-3-алкинил;
с условием, что
- X1, X2 и X3 не могут быть связаны с Z, и
- если X1, X2 и X3 представляют собой O, то X1, X2 и X3 не связаны напрямую с О в Q3, Q4 и Q5
и
Z представляет собой: -COOH; -CO-Asp; -CO-Glu; -CO-Gly; -CO-Sar; -CH(COOH)2; -N(CH2COOH)2; -SO3H; -OSO3H; -OPO3H2; -PO3H2; -тетразол-5-ил или -O-W1,
где W1 представляет собой арилен или гетероарилен, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из тетразо-5-лил, -COOH, -SO3H, -(CH2)1-6-SO3H, -(CH2)1-6-O-PO3H2, -CONR3R4 или -SO2NR3R4, где R3 и R4, независимо друг от друга могут быть H, -(СН2)1-6-SO3H, или -(CH2)1-6-O-PO3H2; при условии, что если Z представляет собой -O-W1, то Q1 должен присутствовать; и любой его Zn2+-комплекс.
20. Способ по любому из пп.1-16 и 19, где инсулиновый пептид выбран из группы, состоящей из:
NεB29-ω-карбокси-пентадеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-тетрадеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-тридеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-β-аланил desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-γ-L-аспартиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-ε-аминогексаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-α-аминопентаноил desB30 человеческого инсулина,
NεB29-10-(4-карбоксифенокси)-деканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-4-[11-(карбоксифенил)ундеканоиламино]бутирил desB30 человеческого инсулина,
NεB29-(3-(3-{4[3-(7-карбоксигептаноиламино)пропокси]бутокси}пропилкарбамоил)-пропионил-γ-глутамиламид) desB30 человеческого инсулина,
NεB29-ω-карбокси-тридеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-ундеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-тетрадеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-{4-[10-(4-карбокси-фенокси)-деканоиламино3-бутирил} desB30 инсулина,
NεB29-{4-[(14-карбокси-тетрадеканоиламино)-метил]-бензоил} desB30 инсулина,
NεB29-[16-(4-карбокси-фенокси)гексадеканоил] desB30 инсулина,
NεB29-{4-[(15-карбоксипентадеканоиламино)бензоил]-desB30 человеческого инсулина и NεB29-{4-[(15-карбокси-пентадеканоиламино)-метил]-бензоил}-desB30 инсулина.
21. Хроматографический способ выделения белковых компонентов инсулинсодержащего раствора, при этом указанный раствор содержит инсулиновый пептид, способный к самоассоциации и/или структурным изменениям в присутствии цинка и двухвалентных ионов цинка, причем указанный способ включает следующие этапы:
а. нанесение инсулинсодержащего раствора на колонку с аниообменным хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом, представляющим интерес, составляет по меньшей мере 6,0 г на литр объема колонки (г/лCV); и
б. элюция инсулинового пептида, представляющего интерес, из указанного твердофазного материала с помощью элюента с pH максимум 6,8; и сбор пула инсулинового пептида, представляющего интерес, соответствующего по меньшей мере 90% по весу инсулиновому пептиду, представляющему интерес, нанесенному на колонку на этапе (а).
22. Способ по п.21, в котором концентрация ионов цинка в растворе находится в диапазоне 0,01-200 мМ, например 0,1-100 мМ, например, 0,5-75 мМ.
23. Способ по любому из пп.21-22, в котором соотношение эквивалентов заряда ионов цинка и инсулинового пептида обычно составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например, от 0,4:1 до 15:1 или от 0,5:1 до 10:1.
24. Способ по любому из пп.21-23, в котором проводимость инсулинсодержащего раствора находится в диапазоне 0-100 мСм/см, например 0-50 мСм/см, например 0-30 мСм/см или 0,01-100 мСм/см, например 0,05-50 мСм, например 0,1-30 мСм/см.
25. Способ по любому из пп.21-24, в котором нагрузка инсулиновым пептидом составляет по меньшей мере 7,0 г/лCV, или по меньшей мере, 8,0 г/лCV, или по меньшей мере 8,5 г/лCV или 6,0-50 г/лCV или 7,0-40 г/лCV или 8,0-30 г/лCV, например 8,5-25 г/лCV, например 9,0-20 г/лCV или 9,5-15 г/лCV.
26. Способ по любому из пп.21-25, в котором pH элюента составляет максимум 6,8, например максимум 6,6, или максимум 6,4, или максимум 6,2, или максимум 6,0, или по меньшей мере 4,0, или по меньшей мере 4,4, или по меньшей мере 4,8, или по меньшей мере 5,0, например, в диапазоне 4,0-6,8, или 4,4-6,8, или 4,8-6,8, или 4,0-6,8, или 4,0-6,6, или 4,0-6,4, или 4,0-6,2, или 4,0-6,0, или 4,4-6,8, или 4,4-6,6, или 4,4-6,4, или 4,8-6,8, или 4,8-6,6, или 4,8-6,2, или 5,0-6,8, или 5,0-6,6.
27. Способ по любому из предыдущих пп.21-26, в котором pH элюента имеет максимальное значение на 2,1 единицы выше pI белка, представляющего интерес, например, максимум на 1,9 единиц выше, например, максимум на 1,7 единиц выше.
28. Способ по любому из предыдущих пп.21-27, в котором пул инсулинового пептида, собранного на этапе (б), соответствует по меньшей мере 91% по весу, или по меньшей мере 92% по весу, или по меньшей мере 93% по весу, или по меньшей мере 94% по весу, или по меньшей мере 95% по весу, или по меньшей мере 96% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а).
29. Способ по любому из предыдущих пп.21-28, в котором концентрация ионов цинка в элюенте находится в диапазоне 0,1-200 мМ, например 0,5-100 мМ или 1,0-60 мМ.
30. Способ по любому из предыдущих пп.21-29, в котором соотношение эквивалентов заряда ионов цинка в элюенте и инсулинового пептида составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например, от 0,4:1 до 15:1 или от 0,5:1 до 10:1.
31. Способ по любому из предыдущих пп.21-30, в котором элюент содержит ионы Zn2+, например, в концентрациях в диапазоне 0,01-200 мМ, например 0,1-100 мМ, например 0,5-75 мМ.
32. Способ по любому из предыдущих пп.21-31, который является крупномасштабным способом, в котором объем колонки составляет по меньшей мере 1 л, или по меньшей мере 10 л, или по меньшей мере 20 л, или по меньшей мере 50 л, или по меньшей мере 100 л, например, по меньшей мере 500 л, например, по меньшей мере 1000 л или по меньшей мере 5000 л.
33. Способ по любому из предыдущих пп.21-32, в который включен этап промывки после этапа (а), но до этапа (б) с применением одного, двух или более промывочных буферов.
34. Способ по любому из предыдущих пп.21-33, в котором промывочный буфер представляет собой водный раствор, содержащий буферный агент по меньшей мере с одним компонентом, выбранным из группы, состоящей из кислот и солей MES, PIPES, ACES, BES, TES, HEPES, TRIS, гистидина, имидазола, глицина, глицилглицина, глицинамида, фосфорной кислоты, уксусной кислоты (например, ацетата натрия), молочной кислоты, глутаровой кислоты, лимонной кислоты, винной кислоты, яблочной кислоты, малеиновой кислоты и янтарной кислоты.
35. Способ по любому из предыдущих пп.21-34, в котором буферный агент содержит смесь двух или более компонентов, где смесь способна обеспечить значение pH в указанном диапазоне, например, смесь уксусной кислоты и/или ацетата натрия.
36. Способ по любому из предыдущих пп.21-35, в котором инсулиновый пептид выбран среди инсулиновых производных, которые являются природным инсулином или его аналогом с боковой цепью, присоединенной к α-аминогруппе N-концевого аминокислотного остатка В-цепи или к ε-аминогруппе остатка Lys, присутствующего в B-цепи родительского инсулина, при этом боковая цепь имеет общую формулу:
-W-X-Y-Z,
где W представляет собой:
- α-аминокислотный остаток с карбоксильной группой в боковой цепи, который формирует через одну из его карбоксильных групп амидную группу вместе с α-аминогруппой N-концевого аминокислотного остатка В-цепи или вместе с ε-аминогруппой остатка Lys, присутствующего в В-цепи родительского инсулина;
- цепь, состоящую из двух, трех или четырех α-аминокислотных остатков, связанных друг с другом посредством амидных связей, которая через амидную связь связана с α-аминогруппой N-концевого аминокислотного остатка В-цепи или с ε-аминогруппой остатка Lys, присутствующего в В-цепи родительского инсулина, при этом аминокислотные остатки W выбраны из группы аминокислотных остатков с нейтральной боковой цепью и аминокислотных остатков с карбоксильной группой в боковой цепи, так что W имеет по меньшей мере один аминокислотный остаток с карбоксильной группой в боковой цепи; либо
- ковалентную связь от X к α-аминогруппе N-концевого аминокислотного остатка В-цепи или к ε-аминогруппе остатка Lys, присутствующего в В-цепи родительского инсулина;
X представляет собой
- -CO-;
- -CH(COOH)СО-
- -N(СН2СООН)CH2 CO-;
- -N(CH2COOH)CH2CON(CH2COOH)CH2 CO-;
- -N(СН2СН2СООН)СН2СН2 СО-;
- -N(СН2СН2СООН)CH2CH2CON(СН2СН2СООН)СН2СН2 СО-;
- -NHCH(COOH)(CH2)4NHCO-;
- -N(CH2CH2COOH)СН2 СО-; или
- -N(CH2COOH)СН2СН2 СО-.
что
а) когда W представляет собой аминокислотный остаток или цепь аминокислотных остатков, он через связь с подчеркнутым карбонильным углеродом образует амидную связь с аминогруппой в W, или
б) когда W представляет собой ковалентную связь, он через связь с подчеркнутым карбонильным углеродом образует амидную связь с N-концевой α-аминогруппой в B-цепи или с ε-аминогруппой остатка Lys, присутствующего в B-цепи родительского инсулина;
Y представляет собой:
- -(CH2)m- где m представляет собой целое число в диапазоне от 6 до 32;
- двухвалентную углеводородную цепь, содержащую 1, 2 или 3 -CH=CH-группы, и число групп -CH2-, достаточное, чтобы дать общее число атомов углерода в цепи в диапазоне от 10 до 32;
- двухвалентную углеводородную цепь формулы -(CH2)vC6H4(CH2)w-, где v и w являются целыми числами или один из них равен нулю, так что сумма v и w находится в диапазоне от 6 до 30; а также
Z представляет собой:
- -COOH;
- -CO-Asp;
- -CO-Glu;
- -CO-Gly;
- -CO-Sar;
- -CH(COOH)2;
- -N(CH2COOH)2;
- -SO3H; или
- -PO3H;
и любых их комплексов с Zn2+.
37 Способ по любому из предыдущих пп.21-36, в котором инсулиновый пептид представляет собой человеческий инсулин LysB29(Nε-гексадекандиол-γ-Glu) des(B30).
38. Хроматографический способ по любому из предыдущих пп.21-37 для выделения белковых компонентов инсулинсодержащего раствора, при этом указанный раствор содержит человеческий инсулин LysB29(Nε-гексадекандиол-γ-Glu) des(B30) и двухвалентные ионы цинка, а указанный способ включает следующие этапы:
а. нанесение инсулинсодержащего раствора на колонку с анионообменным хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом, представляющим интерес, составляет по меньшей мере 6,0 г на литр объема колонки (г/лCV); и
б. элюцию инсулинового пептида, представляющего интерес, из указанного твердофазного материала с помощью элюента с pH в диапазоне от 6,4 до 6,8; и сбор пула человеческого инсулина 1-LysB29(Nε-гексадекандиол-γ-Glu) des(B30), соответствующего по меньшей мере 90% по весу человеческому инсулину LysB29(Nε-гексадекандиол-γ-Glu) des(B30), нанесенному на колонку на этапе (а).
39. Способ по любому из пп.1 и 38, в который включен этап промывки после этапа (а), но до этапа (б) с применением промывочного буфера, содержащего этанол и триэтаноламин.
40. Способ по любому из пп.21-35, в котором инсулиновый пептид представляет собой производное инсулина, имеющее формулу:

где Ins представляет собой фрагмент родительского инсулина, а Q1-Q2-[CH2]n-X1-[CH2]n-Q3-[CH2]n-X2-[CH2]n-Q4-[CH2]n-Х3-[СН2]n-Q5-[CH2]n-Z представляет собой заместитель, и где Ins присоединен к заместителю через амидную связь между α-аминогруппой N-концевого аминокислотного остатка В-цепи Ins или ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, и CO-группой в Q1 или Q2 заместителя;
каждый n независимо представляет собой 0, 1, 2, 3, 4, 5 или 6;
Q1 является:
- амидом аминокислоты с карбоксильной кислотой в боковой цепи или аминокислоты с незаряженной боковой цепью, остаток которой через его карбоксильную группу формирует амидную группу вместе с α-аминогруппой N-концевого аминокислотного остатка B-цепи Ins или вместе с ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, либо
- цепью, состоящей из двух, трех или четырех амидов α-аминокислот или аминокислотных остатков, как указано выше, связанных друг с другом с помощью амидной связи, при этом цепь через амидную связь связана с α-аминогруппой N-концевого аминокислотного остатка B-цепи Ins или с ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, либо
- связью.
Q2 представляет собой:
- -COCH(CONH2)-
- -COCH2N(CH2CONH2)-
- -COCH2N(CH2CONH2)COCH2N(CH2CONH2)
- -COCH2CH2N(CH2CH2CONH2)-
- -COCH2CH2N(CH2CH2CONH2)-COCH2CH2N(CH2CH2CONH2)-
- -COCH2N(CH2CH2CONH2)-
- -COCH2CH2N(CH2CONH2)-
- -COCH2OCH2CONH-
- -CO-((CR5R6)1-6-NH-CO)1-4-;
-CO-((CR5R6)1-6-CO-NH)1-4-, где R5 независимо может быть H, -CH3, -(CH2)1-6CH3 или -CONH2, а R6 независимо может представлять собой H, -CH3, -(CH2)1-6CH3; или
- связь
при условии, что
- по меньшей мере один из Q1 или Q2 не является связью, и
- что Q2 не является -CO-(CH2)2-CO-NH-, где n составляет 0 или 1, X1 представляет собой связь, а Q3 представляет собой (CH2CH2O)2-, (CH2CH2O)3- или (CH2CH2OCH2CH2CH2CH2O)- и
- что если амин в Q1 или Q2 образует связь с остальной частью заместителя, амин должен быть связан с остальной частью заместителя через карбонильную группу;
Q3, Q4 и Q5 каждый независимо друг от друга могут представлять собой
- -(CH2)m-, где m представляет собой целое число в диапазоне от 6 до 32;
- двухвалентную углеводородную цепь, содержащую 1, 2 или 3 -CH=СН- группы и число -CH2- групп, достаточное, чтобы дать общее число атомов углерода в цепи в диапазоне от 4 до 32;
- -CO-((CR5R6)1-6-NH-CO)-;
- -(CO-(CR5R6)1-6-CO-NH)1-4- где R5 независимо может быть H, -CH3, -(СН2)1-6CH3 или -CONH2, а R6 независимо может быть Н, -CH3, -(CH2)1-6CH3;
- -CO-(СН2)0-3-Ar-(СН2)0-3-, где Ar может быть ариленом или гетероариленом, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из -CH3, -(CH)1-6-CH3, -CONR1R2 или -SO2NR1R2, где R1 и R2 независимо друг от друга могут быть H, -CH3 или -(СН)1-6-CH3;
- (CH2CH2O)y-; (CH2CH2CH2O)y-; (CH2CH2CH2CH2O)y-(CH2CH2OCH2CH2CH2CH2O)y- или (CH2CH2CH2OCH2CH2CH2CH2O)y-; -(CH2OCH2)y-, где y составляет 1-20;
- арилен или гетероарилен, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из -CH3, -(СН)1-6-CH3, -CONR1R2 или -SO2NR1R2, где R1 и R2 независимо друг от друга могут быть Н, -CH3 или -(CH)1-6-CH3;
- цепь с формулой
-(CH2)s-Y1-(Ar)v1-Y2-(СН2)w-Y3-(Ar)v2-Y4-(CH2)t-Y5-(Ar)v3-Y6-(СН2)z-,
где Ar имеет вышеуказанное значение, Y1-Y6 независимо друг от друга могут быть О, S, S=O, SO2 или связью; где s, w, t и z независимо друг от друга составляют ноль или целое число от 1 до 10, так что сумма s, w, t и z находится в диапазоне от 4 до 30, a v1, v2, и v3 независимо друг от друга могут быть равны нулю или 1, при условии, что Y1-Y6 не связаны друг с другом, и что структура -O-(CH2)1-O- не происходит; либо
- связь;
при условии, что по меньшей мере один из Q3-Q5 не является связью;
X1, X2 и X3 независимо друг от друга представляют собой
- O;
- -C=O
- связь;
- NCOR1, где R1 может быть Н, -CH3 или -(CH)1-6-CH3; или
-  или
или 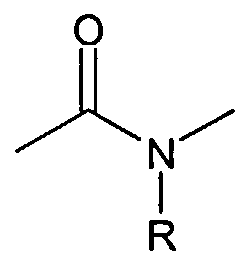
где R представляет собой водород, C1-3-алкин, C2-3-алкенил или C2-3-алкинил;
при условии, что
- X1, X2 и X3 не могут быть связаны с Z, и
- если X1, X2 и X3 представляют собой О, то X1, X2 и X3 не связаны напрямую с О в Q3, Q4 и Q5
и
Z представляет собой: -COOH; -CO-Asp; -CO-Glu; -CO-Gly; -CO-Sar; -CH(COOH)2; -N(CH2COOH)2; -SO3H; -OSO3H; -OPO3H2; -PO3H2; -тетразол-5-ил или-O-W1,
где W1 представляет собой арилен или гетероарилен, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из тетразо-5-лил, -COOH, -SO3H, -(СН2)1-6-SO3H, -(CH2)1-6-O-PO3H2, -CONR3R4 или -SO2NR3R4, где R3 и R4, независимо друг от друга могут быть H, -(СН2)1-6-SO3H, или -(СН2)1-6-O-PO3H2; при условии, что если Z представляет собой -O-W1, то Q1 должен присутствовать, и любой их Zn2+-комплекс.
41. Способ по пп.21-35 и 40, где инсулиновый пептид выбран из группы, состоящей из:
NεB29-ω-карбокси-пентадеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-γ-амино-бутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-тетрадеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-тридеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-β-аланил desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-γ-L-аспартиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-ε-аминогексаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-δ-аминопентаноил desB30 человеческого инсулина,
NεB29-10-(4-карбоксифенокси)-деканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-4-[11-карбоксифенил)ундеканоиламино]бутирил desB30 человеческого инсулина,
NεB29-(3-(3-{4-[3-(7-карбоксигептаноиламино)пропокси]бутокси}пропилкарбамоил)-пропионил-γ-глутамиламид) desB30 человеческого инсулина,
NεB29-ω-карбокси-тридеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-ундеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-тетрадеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-{4-[10-(4-карбокси-фенокси)-деканоиламино]-бутирил} desB30 инсулина,
NεB29-{4-[(14-карбокси-тетрадеканоиламино)-метил]-бензоил} desB30 инсулина,
NεB29-[16(4-карбокси-фенокси)-гексадеканоил] desB30 инсулина,
NεB29-{4-[(15-карбоксипентадеканоиламино)бензоил]-desB30 человеческого инсулина и
NεB29-{4-[(15-карбокси-пентадеканоиламино)-метил]-бензоил}-desB30 инсулина.
42. Способ контроля формы пика при ионообменной хроматографии инсулиновых пептидов, способных к самоассоциации и/или структурному изменению в присутствии ди- или поливалентных ионов металлов с использованием
а. ди- или поливалентных ионов металлов для получения оптимального разделения инсулинового пептида и родственных примесей, где двухвалентные ионы металлов были добавлены, чтобы закрепить форму передней части пика инсулинового пептида, где родственные примеси элюируются перед инсулиновым пептидом.
43. Способ по пп.42, в котором ди- или поливалентные ионы металлов выбраны среди Zn2+, Ca2+, Mg2+, Ni2+, Cu2+, Ba2+, предпочтительно Zn2+.
44. Способ по пп.42-43, в котором инсулиновый пептид элюируют с помощью элюента, pH которого составляет максимум 6,8, например максимум 6,6, или максимум 6,4, или максимум 6,2, или максимум 6,0, или по меньшей мере 4,0, или по меньшей мере 4,4, или по меньшей мере 4,8, или по меньшей мере 5,0, например, в диапазоне 4,0-6,8, или 4,4-6,8, или 4,8-6,8, или 4,0-6,8, или 4,0-6,6, или 4,0-6,4, или 4,0-6,2, или 4,0-6,0, или 4,4-6,8, или 4,4-6,6, или 4,4-6,4, или 4,8-6,8, или 4,8-6,6, или 4,8-6,2, или 5,0-6,8, или 5,0-6,6.
45. Способ по любому из предыдущих пп.42-44, в котором число ди- или поливалентных ионов металлов составляет более 4 ионов металла на шесть молекул инсулинового пептида.
46. Способ по любому из предыдущих пп.42-45, в котором число ди- или поливалентных ионов металлов более 4,5 ионов металла на шесть молекул инсулинового пептида.
47. Способ по любому из предыдущих пп.42-46, в котором число ди- или поливалентных ионов металлов составляет более 5 ионов металла на 6 молекул инсулинового пептида, более 5,5 ионов металла на 6 молекул инсулинового пептида, более 6 ионов металлов на 6 молекул инсулинового пептида или более 6,5 ионов металла на 6 молекул инсулинового пептида.
48. Способ по любому из предыдущих пп.42-47, в котором число ди- или поливалентных ионов металлов составляет до 12 ионов металла на 6 молекул инсулинового пептида.
49. Способ по любому из предыдущих пп.42-48, в котором соотношение эквивалентов заряда ди- или поливалентных ионов металлов и инсулинового пептида обычно составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например, от 0,4:1 до 15:1 или от 0,5:1 до 10:1.
50. Способ по любому из предыдущих пп.42-49, в котором проводимость инсулинсодержащего раствора находится в диапазоне 0-100 мСм/см, например 0-50 мСм/см, например 0-30 мСм/см или 0,01-100 мСм/см, например 0,05-50 мСм, например 0,1-30 мСм/см.
51. Способ по любому из предыдущих пп.42-50, в котором pH элюента имеет максимальное значение на 2,1 единицы выше pI белка, представляющего интерес, например, максимум на 1,9 единиц выше, например, максимум на 1,7 единиц выше.
52. Способ по любому из предыдущих пп.42-51, в котором форма передней части пика инсулинового пептида контролируется таким образом, что по меньшей мере 90% по весу, или по меньшей мере 91% по весу, или по меньшей мере 92% по весу, или по меньшей мере 93% по весу, или по меньшей мере 94% по весу, или по меньшей мере 95% по весу, или по меньшей мере 96% по весу инсулинового пептида отделяется от родственных примесей.
53. Способ по любому из предыдущих пп.42-52, в котором концентрация ди- или поливалентных ионов металлов в элюенте находится в диапазоне 0,1-200 мМ, например 0,5-100 мМ или 1,0-60 мМ.
54. Способ по любому из предыдущих пп.42-53, в котором соотношение эквивалентов заряда ди- или поливалентных ионов металлов в элюенте и инсулинового пептида, представляющего интерес, составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например от 0,4:1 до 15:1 или от 0,5:1 до 10:1
55. Способ по любому из предыдущих пп.42-54, в котором элюент содержит ионы Zn2+, например, в концентрациях в диапазоне 0,01-200 мМ, например 0,1-100 мМ, например 0,5-75 мМ.
56. Способ по любому из предыдущих пп.42-55, в котором инсулиновый пептид самоассоциируется с ионами цинка.
57. Способ по любому из предыдущих пп.42-56, в котором инсулиновый пептид выбран среди инсулиновых производных, которые являются природным инсулином или его аналогом с боковой цепью, присоединенной к α-аминогруппе N-концевого аминокислотного остатка В-цепи или к ε-аминогруппе остатка Lys, присутствующего в В-цепи родительского инсулина, при этом боковая цепь имеет общую формулу:
-W-X-Y-Z,
где W представляет собой:
- α-аминокислотный остаток с карбоксильной группой в боковой цепи, который формирует через одну из его карбоксильных групп амидную группу вместе с α-аминогруппой N-концевого аминокислотного остатка В-цепи или вместе с ε-аминогруппой остатка Lys, присутствующего в В-цепи родительского инсулина;
- цепь, состоящую из двух, трех или четырех α-аминокислотных остатков, связанных друг с другом посредством амидных связей, которая через амидную связь связана с α-аминогруппой N-концевого аминокислотного остатка В-цепи или с ε-аминогруппой остатка Lys, присутствующего в В-цепи родительского инсулина, при этом аминокислотные остатки W выбраны из группы аминокислотных остатков с нейтральной боковой цепью и аминокислотных остатков с карбоксильной группой в боковой цепи, так что W имеет по меньшей мере один аминокислотный остаток с карбоксильной группой в боковой цепи; либо
- ковалентную связь от Х к α-аминогруппе N-концевого аминокислотного остатка В-цепи или к ε-аминогруппе остатка Lys, присутствующего в В-цепи родительского инсулина;
Х представляет собой
- -СО-;
- -CH(СООН)СО-;
- -N(CH2COOH)СН2 СО-;
- -N(CH2COOH)CH2CON(CH2COOH)CH2 CO-;
- -N(CH2CH2COOH)CH2CH2 CO-;
- -N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2 CO-;
- -NHCH(COOH)(CH2)4NHCO-;
- -N(СН2СН2СООН)СН2 СО-; или
- -N(CH2COOH)CH2CH2 CO,
что
а) когда W представляет собой аминокислотный остаток или цепь аминокислотных остатков, он через связь с подчеркнутым карбонильным углеродом образует амидную связь с аминогруппой в W, или
б) когда W представляет собой ковалентную связь, он через связь с подчеркнутым карбонильным углеродом образует амидную связь с N-концевой α-аминогруппой в В-цепи или с ε-аминогруппой остатка Lys, присутствующего в В-цепи родительского инсулина;
Y представляет собой:
- -(CH2)m- где m представляет собой целое число в диапазоне от 6 до 32;
- двухвалентную углеводородную цепь, содержащую 1, 2 или 3 -CH=CH -группы, и число групп -СН2-, достаточное, чтобы дать общее число атомов углерода в цепи в диапазоне от 10 до 32;
- двухвалентную углеводородную цепь формулы -(CH2)vC6H4(CH2)w-, где v и w являются целыми числами или один из них равен нулю, так что сумма v и w находится в диапазоне от 6 до 30; а также
Z представляет собой:
- -COOH;
- -CO-Asp;
- -CO-Glu;
- -CO-Gly;
- -CO-Sar;
- -CH(COOH)2;
- -N(CH2COOH)2;
- -SO3H; или
- -PO3H;
и любых их комплексов с Zn2+.
58. Способ по любому из предыдущих пп.42-57, в котором инсулиновый пептид представляет собой человеческий инсулин LysB29(Nε-гексадекандиол-γ-Glu) des(B30).
59. Способ по любому из пп.42-56, в котором инсулиновый пептид представляет собой производное инсулина, имеющее формулу:

где Ins представляет собой фрагмент родительского инсулина, а Q1-Q2-[CH2]n-X1-[CH2]n-Q3-[СН2]n-X2-[CH2]n-Q4-[CH2]n-X3-[СН2]n-Q5-[CH2]n-Z представляет собой заместитель, и где Ins присоединен к заместителю через амидную связь между α-аминогруппой N-концевого аминокислотного остатка В-цепи Ins или ε-аминогруппой остатка Lys, присутствующего в А- или В-цепи Ins, и CO-группой в Q1 или Q2 заместителя;
каждый n независимо представляет собой 0, 1, 2, 3, 4, 5 или 6;
Q1 является:
- амидом аминокислоты с карбоксильной кислотой в боковой цепи или аминокислоты с незаряженной боковой цепью, остаток которой через его карбоксильную группу формирует амидную группу вместе с α-аминогруппой N-концевого аминокислотного остатка B-цепи Ins или вместе с ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, либо
- цепью, состоящей из двух, трех или четырех амидов α-аминокислот или аминокислотных остатков, как указано выше, связанных друг с другом с помощью амидной связи, при этом цепь через амидную связь связана с α-аминогруппой N-концевого аминокислотного остатка В-цепи Ins или с ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, либо
- связью.
Q2 представляет собой:
- -COCH(CONH2)-
- -COCH2N(CH2CONH2)-
- -COCH2N(CH2CONH2)COCH2N(CH2CONH2)
- -COCH2CH2N(CH2CH2CONH2)-
- -COCH2CH2N(CH2CH2CONH2)-COCH2CH2N(CH2CH2CONH2)-
- -COCH2N(CH2CH2CONH2)-
- -COCH2CH2N(CH2CONH2)-
- -COCH2OCH2CONH-
- -СО-((CR5R6)1-6-NH-CO)1-4-
-СО-((CR5R6)1-6-CO-NH)1-4- где R5 независимо может быть H, -СН3, -(СН2)1-6CH3 или -CONH2, а R6 независимо может представлять собой H, -CH3, -(СН2)1-6СН3; или
- связь,
при условии, что
- по меньшей мере один из Q1 или Q2 не является связью, и
- что Q2 не является -СО-(СН2)2-CO-NH- где n составляет 0 или 1, X1 представляет собой связь, а Q3 представляет собой (CH2CH2O)2-, (CH2CH2O)3- или (CH2CH2OCH2CH2CH2CH2O)- и
- что если амин в Q1 или Q2 образует связь с остальной частью заместителя, амин должен быть связан с остальной частью заместителя через карбонильную группу;
Q3, Q4 и Q5 каждый независимо друг от друга могут представлять собой
- -(СН2)m-, где m представляет собой целое число в диапазоне от 6 до 32;
- двухвалентную углеводородную цепь, содержащую 1, 2 или 3 группы -CH=СН- и число групп -СН2-, достаточное, чтобы дать общее число атомов углерода в цепи в диапазоне от 4 до 32;
- -СО-((CR5R6)1-6-NH-CO)-;
- -(CO-(CR5R6)1-6-CO-NH)1-4- где R5 независимо может быть H, -CH3, -(СН2)1-6CH3 или -CONH2, а R6 независимо может быть Н, -CH3, -(CH2)1-6CH3;
- -СО-(СН2)0-3-Ar-(СН2)0-3-, где Ar может быть ариленом или гетероариленом, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из -CH3, -(CH)1-6-СН3, -CONR1R2 или -SO2NR1R2, где R1 и R2 независимо друг от друга могут быть H, -CH3 или -(СН)1-6-CH3;
- (CH2CH2O)y-; (CH2CH2CH2O)y-; (CH2CH2CH2CH2O)y-; (CH2CH2OCH2CH2CH2CH2O)y- или (CH2CH2CH2OCH2CH2CH2CH2O)y-; -(CH2OCH2)y-, где y составляет 1-20;
- арилен или гетероарилен, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из -CH3, -(СН)1-6-CH3, -CONR1R2 или -SO2NR1R2, где R1 и R2 независимо друг от друга могут быть H, -CH3 или -(CH)1-6-CH3;
- цепь с формулой
-(CH2)s-Y1-(Ar)v1-Y2-(СН2)w-Y3-(Ar)v2-Y4-(CH2)t-Y5-(Ar)v3-Y6-(CH2)z-,
где Ar имеет вышеуказанное значение, Y1-Y6 независимо друг от друга могут быть О, S, S=O, SO2 или связью; где s, w, t и z независимо друг от друга составляют ноль или целое число от 1 до 10, так что сумма s, w, t и z находится в диапазоне от 4 до 30, a v1, v2, и v3 независимо друг от друга могут быть равны нулю или 1, при условии, что Y1-Y6 не связаны друг с другом, и что структура -O-(CH2)1-O- не происходит; либо
- связь;
при условии, что по меньшей мере один из Q3-Q5 не является связью;
X1, X2 и X3 независимо друг от друга представляют собой
- O;
- -С=O
- связь;
- NCOR1, где R1 может быть H, -CH3 или -(СН)1-6-CH3; или
- 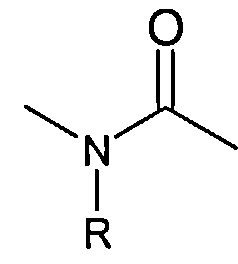 или
или 
где R представляет собой водород, C1-3-алкин, C2-3-алкенил или C2-3-алкинил;
при условии, что
- X1, X2 и X3 не могут быть связаны с Z, и
- если X1, X2 и X3 представляют собой О, то X1, X2 и X3 не связаны напрямую с О в Q3, Q4 и Q5
и
Z представляет собой: -COOH; -CO-Asp; -CO-Glu; -CO-Gly; -CO-Sar; -CH(COOH)2; -N(CH2COOH)2; -SO3H; -OSO3H; -OPO3H2; -PO3H2; -тетразол-5-ил или -O-W1,
где W1 представляет собой арилен или гетероарилен, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из тетразо-5-лила, -COOH, -SO3H, -(CH2)1-6-SO3H, -(CH2)1-6-O-PO3H2-CONR3R4 или -SO2NR3R4, где R3 и R4 независимо друг от друга могут быть Н, -(CH2)1-6-SO3H или -(CH2)1-6-O-PO3H2; при условии, что если Z представляет собой -O-W1, то Q1 должен присутствовать, и любой их Zn2+-комплекс.
60. Способ по пп.42-56 и 59, где инсулиновый пептид выбран из группы, состоящей из:
NεB29-ω-карбокси-пентадеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-γ-амино-бутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-тетрадеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-тридеканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-β-аланил desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-γ-L-аспартиламид desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-ε-аминогексаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-пентадеканоил-δ-аминопентаноил desB30 человеческого инсулина,
NεB29-10-(4-карбоксифенокси)-деканоил-γ-L-глутамиламид desB30 человеческого инсулина,
NεB29-4-[11-(4-карбоксифенил)ундеканоиламино]бутирил desB30 человеческого инсулина,
NεB29-(3-(3-{4-[3-(7-карбоксигептаноиламино)пропокси]бутокси}пропилкарбамоил)-пропионил-γ-глутамиламид) desB30 человеческого инсулина,
NεB29-ω-карбокси-тридеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-ундеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-ω-карбокси-тетрадеканоил-γ-аминобутаноил desB30 человеческого инсулина,
NεB29-{4-[10-(4-карбокси-фенокси)-деканоиламино]-бутирил} desB30 инсулина,
NεB29-{4-[(14-карбокси-тетрадеканоиламино)-метил]-бензоил} desB30 инсулина,
NεB29-[16-(4-карбокси-фенокси)-гексадеканоил] desB30 инсулина,
NεB29-{4-[(15-карбоксипентадеканоиламино)бензоил]-desB30 человеческого инсулина и
NεB29-{4-[(15-карбокси-пентадеканоиламино)-метил]-бензоил}-desB30 инсулина.
61. Очищенный инсулиновый пептид, полученный в процессе или способом в соответствии с любым из предыдущих пунктов.
Пример 1
Колонка с размерами d=1 см и L=25 см упакована с Source 30Q от GE Healthcare.
Белоксодержащий раствор с 12 г/л инсулинового пептида (человеческий инсулин LysB29(Nε-гексадекандиол-γ-Glu) des(B30)) (pI=4,7)) в 30% этаноле при pH=7,5 с проводимостью <3 мСм/см, наносили на колонку с нагрузкой 8, 10 и 12 г/лCV. Белоксодержащий раствор содержит Zn-ионы в количестве двух атомов цинка на шесть молекул инсулина.
Для элюции использовали два буфера с 42,5% этанола и 20 мМ триэтаноламина при pH=6,4, 6,8 и 7,2, содержащих 0 мМ и 300 мМ NH4Ac (ацетата аммония). После нанесения белоксодержащего раствора колонку промывали с помощью одного объема колонки растворителя, содержащего 0 мМ NH4Ac, и затем белок элюировали градиентом соли от 30 мМ до 180 мМ NH4Ac более чем 15 объемами колонки (см. фиг.1). Выход для всех экспериментов составлял более 90%.
Результат показан на фиг.1-3 и поясняется ниже.
Фиг.1: При pH 6,4 примеси, которые элюируются перед основным пиком (при V-VReg≈-80 мл), четко отделяются от основного пика и при низкой, и при высокой нагрузке (8 и 12 г/л). Объемы собранных пулов от примерно -70 и -60 мл до 0 мл малы, и концентрация продукта в пуле высокая.
Фиг.2: При рН 6,8 примеси, которые элюируются перед основным пиком (при V-VReg≈-80 мл), отделяются от основного пика при нагрузке 10 г/л. Объемы собранных пулов от примерно -80 больше, а концентрация продукта меньше, чем при pH 6,4.
Фиг.3: При рН 7,2 примеси элюируются перед основным пиком (при V-VReg≈-85 мл) при низкой нагрузке, 8 г/л, но без базального разделения, которое видно при pH 6,4 при низкой нагрузке. Когда нагрузка увеличивается до 12 г/л, примеси больше не отделяются от продукта, но смещаются относительно продукта (при V-VReg≈-120 мл). Объем пула является большим, а концентрация пула, следовательно, меньшей, чем наблюдаемая при более низких значениях pH
Пример 2
Был проведен эксперимент, в котором были взяты образцы для анализа содержания Zn2+ в каждой из фракций (см. фиг.4). Эти образцы показывают, что Zn элюируется вместе с продуктом.
Номера фракций в приведенной выше таблице соответствуют фракциям, показанным на фиг.4.
Хорошо видно, что Zn2+ элюируется вместе с продуктом.
Образцы, взятые из хроматографического способа (образец 1-4), в котором Zn2+ присутствовал в материале, но не в элюентах, показывают, что Zn2+ присутствует в значительно более высокой концентрации в пуле, содержащем продукт, где концентрация аналога инсулина самая высокая по сравнению с образцами, взятыми вокруг пула. Это свидетельствует о сильном взаимодействии/кооперативности между инсулином и Zn2+.
При сравнении хроматограммы на фиг.4 с традиционной хроматограммой Ленгмюра видно, что задняя часть хроматограммы выгнута вниз, в то время как традиционная хроматограмма Ленгмюра выгнута вверх. Это означает, что также при этих значениях pH форма пика зависит от Zn2+.
Наличие ди- или поливалентного иона металла в белоксодержащем растворе в сочетании с регулированием pH в элюенте, чтобы сбалансировать силы притяжения и отталкивания, и тем самым получить изотерму, которая является линейной на более высоких концентрациях, приводит к небольшой объему пула и высокой концентрации в пуле.
Кооперативность может быть видна на хроматограмме, где основной пик будет иметь растянутый передний край и отдаляться от примеси, которая элюируется перед основным пиком.
Изменение профилей инсулинового пика от растянутого заднего края пика при высоких значениях pH (тонкая пунктирная кривая на фиг.3, pH=7,2), аналогично профилю Ленгмюра задней части при заданном значении pH (сплошная тонкая кривая на фиг.2, pH=6,8), к профилю с растянутым передним краем пика при низком значении pH (толстая пунктирная кривая фиг.1, pH=6,4) в присутствии Zn2+ в подвижной фазе, т.е. в белоксодержащем растворе (фиг.1-3).
Были проведены эксперименты с высоким и низким pH при высокой и низкой нагрузке, которая может быть видна из площади под кривыми, в то время как эксперименты при pH=6,8 были проведены при нагрузке между нагрузкой в других экспериментах. Все эксперименты были повторены для подтверждения результатов, и все хроматограммы приведены в соответствии с концом сбора пула, чтобы сделать их более удобными для сравнения. Критическая примесь, подлежащая извлечению, элюируется перед основным пиком, например, при pH=6,8 она элюируется около -90 мл. Видно, что при этом значении pH и при высоком pH пики являются четко растянутыми в задней части (крутой передний край и плоский задний). При высоком pH расстояние между продуктом и примесью выглядит очень небольшим, особенно при высокой нагрузке, когда перед основным пиком не наблюдается элюция четкого пика. При низком pH пики являются растянутыми в передней части (плоский передний край и крутой задний), и между примесью и пиком продукта видно базальное разделение. Эта фронтальная часть имеет ряд преимуществ в данном случае: (а) пик продукта отдаляется от примеси; (б) концентрация пула выше, что может быть видно из более сильного УФ-сигнала; и (в) можно увеличить нагрузку на колонку, по-прежнему удаляя примесь.
Пример 3
Анализ самоассоциации инсулина с помощью SEC:
Способность инсулиновых пептидов к самоассоциации может быть проанализирована с помощью способа SEC. Анализ с помощью эксклюзионной хроматографии (SEC) на колонке Superose 6 PC (0,32*30 см) с использованием изотонического 10 мМ Tris-буферного солевого раствора, возможно с добавлением 2 мМ фенола, при 37°C и pH 7,3, вводимым объемом 20 мкл, скоростью потока 0,05 мл/мин, временем выполнения 130 мин. Первый сигнал от декстрана голубого (»5 МДа, KAV 0,0), тиреоглобулина (669 кДа, KAV 0,28), ферритина (440 кДа, KAV 0,39), овальбумина (44,5 кДа, KAV 0,56), рибонуклеазы (13,7 кДа, KAV 0,69), и второй сигнал от альбумина (66 кД, KAV 0,53), Co(III)-инсулин-гексамера (35 кДа, KAV 0,61) и мономерного инсулина Х2 (6 кДа, KAV 0,73). Время удерживания декстрана голубого составило 17,9 мин (t0) и 0,74 мин без колонки (tD), и время удерживания альбумина (HSA) составила примерно 34,1 мин,
KAV=(t-t0)/(V/f+td-t0), где
t: время удерживания (мин)
t0: время удерживания декстрана голубого (эксклюзионный предел)
td: время удерживания декстрана голубого без колонки (объем пустот колонки)
Vt: общий объем колонки (мл)
f: поток (мл/мин)
Формат данных:
Площадь KAV пика 1 измеряется от KAV=0 до KAV=0,46 (32 мин) как относительная площадь % от общей площади для KAV<0,46, соответствующей самоассоциации, большей, чем у альбумина. Для KAV пика 1 примерно 0,56 (размер альбумина) срез интеграции находится между размером альбумина и размером гексамера инсулина.
Пример 4
Анализ связывания рецептора инсулина
Аффинность инсулинового пептида к рецептору человеческого инсулина определяли с помощью анализа SPA (анализа сцинтилляционного приближения) в микротитровальных планшетах с антителами захвата. SPA-PVT-шарики, связывающие антитела, противомышиный реагент (Amersham Biosciences, кат. № PRNQ0017) смешивали с 25 мл связывающего буфера (100 мМ HEPES pH 7,8; 100 мМ хлорида натрия, 10 мМ MgSO4, 0,025% Tween-20). Смесь реагентов для одного планшета Packard Optiplate (Packard №6005190) состояла из 2,4 мкл 1:5000 разведенного очищенного рекомбинантного человеческого рецептора инсулина - экзона 11, количества исходного раствора А14 Tyr [125I]-инсулина человека, соответствующего 5000 имп/мин на 100 мкл смеси реагентов, 12 мкл разбавленного в соотношении 1:1000 антитела F12, 3 мл SPA-шариков и связывающего буфера до общего объема 12 мл. Затем добавляли в общей сложности 100 мкл и готовили серию разведении из соответствующих образцов. Затем к серии разведений добавляли 100 мкл смеси реагентов, и образцы инкубировали в течение 16 часов, осторожно встряхивая. Затем фазы разделяли центрифугированием в течение 1 мин, и планшеты оценивали в Topcounter. Данные связывания оценивали с помощью нелинейного регрессионного алгоритма в GraphPad Prism 2.01 (GraphPad Software, Сан-Диего, Калифорния, США).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОНЪЮГАЦИИ ПЕПТИДОВ, ОПОСРЕДОВАННОЙ ТРАНСГЛУТАМИНАЗОЙ | 2005 |
|
RU2385879C2 |
| ПРОИЗВОДНОЕ ИНСУЛИНА, РАСТВОРИМАЯ ПРОЛОНГИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПРОЛОНГИРОВАНИЯ ГИПОГЛИКЕМИЧЕСКОГО ДЕЙСТВИЯ ПРИ ЛЕЧЕНИИ ДИАБЕТА | 1994 |
|
RU2164520C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ИНСУЛИНА И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2015 |
|
RU2684456C2 |
| ПРОИЗВОДНЫЕ ИНСУЛИНА | 2004 |
|
RU2352581C2 |
| ПРОИЗВОДНЫЕ ИНСУЛИНА | 2004 |
|
RU2518460C2 |
| ПРОИЗВОДНЫЕ ИНСУЛИНА, СОДЕРЖАЩИЕ ДОПОЛНИТЕЛЬНЫЕ ДИСУЛЬФИДНЫЕ СВЯЗИ | 2011 |
|
RU2598273C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2013 |
|
RU2670106C2 |
| АНАЛОГИ ИНСУЛИНА, УСТОЙЧИВЫЕ К ПРОТЕАЗАМ | 2007 |
|
RU2524150C2 |
| СТАБИЛИЗИРОВАННЫЕ ПО ОТНОШЕНИЮ К ПРОТЕАЗАМ АЦИЛИРОВАННЫЕ АНАЛОГИ ИНСУЛИНА | 2009 |
|
RU2571857C2 |
| ЛЕЧЕНИЕ САХАРНОГО ДИАБЕТА С ИСПОЛЬЗОВАНИЕМ ИНЪЕКЦИЙ ИНСУЛИНА С ЧАСТОТОЙ МЕНЕЕ ОДНОГО РАЗА В ДЕНЬ | 2009 |
|
RU2540922C2 |
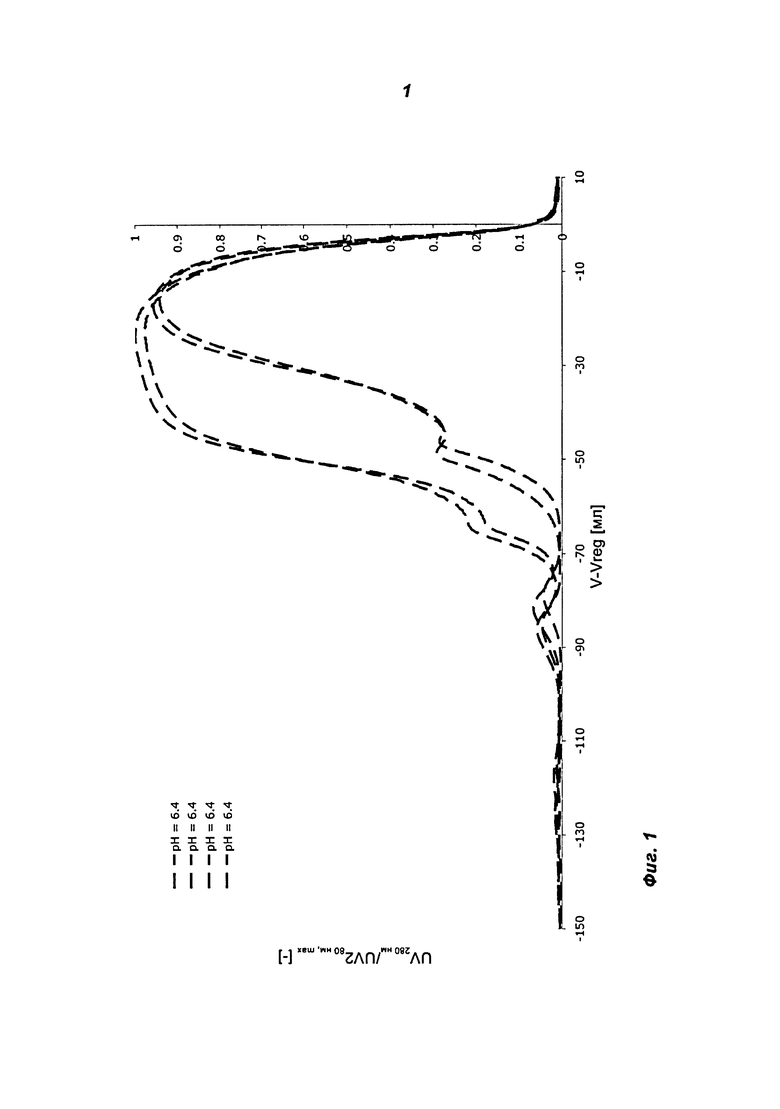


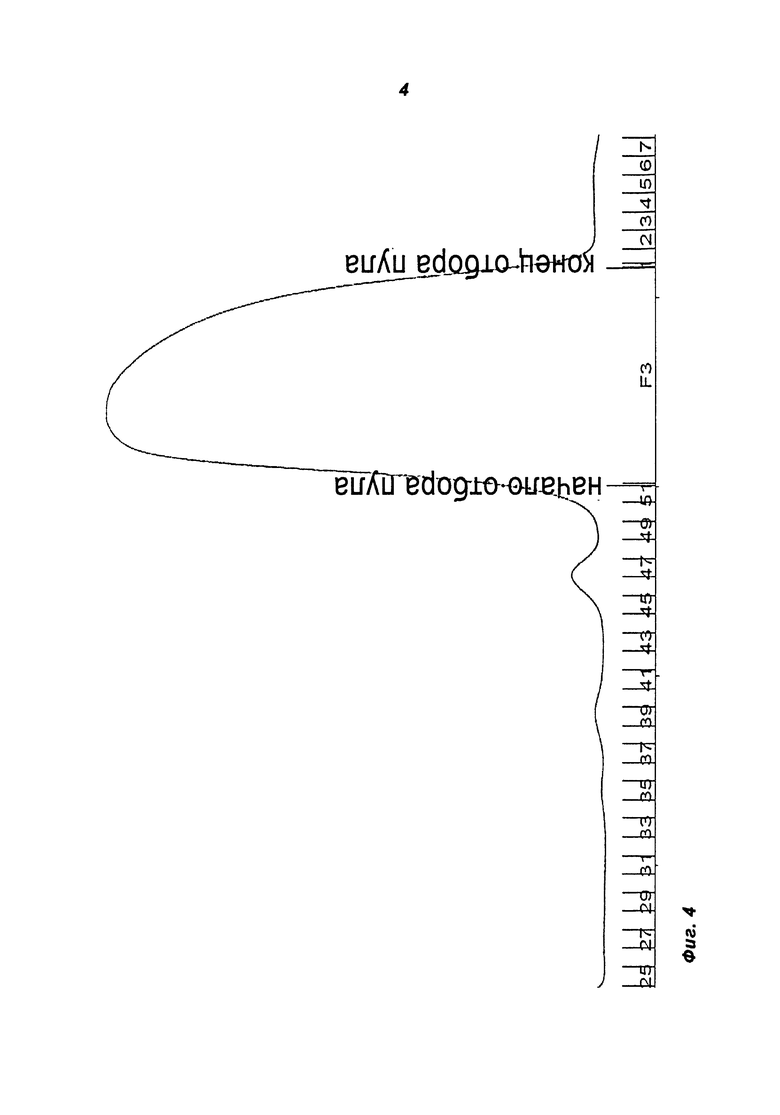
Изобретения относятся к области биохимии. Описана группа изобретений, включающая хроматографический способ выделения белковых компонентов белоксодержащего раствора, при этом указанный раствор содержит инсулиновый пептид и ионы цинка, указанный инсулиновый пептид способен к самоассоциации в присутствии ионов цинка (варианты). В одном варианте способ включает в себе этапы: а) нанесение белоксодержащего раствора на колонку с хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом находится в диапазоне 8-30 г на литр объема колонки (г/лCV); и б) элюция инсулинового пептида из указанного твердофазного материала с помощью элюента с pH максимум 7,0; и сбор пула инсулинового пептида, соответствующего по меньшей мере 75% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а). Изобретение расширяет арсенал хроматографических способов выделения белковых компонентов. 2 н. и 10 з.п. ф-лы, 4 ил., 4 пр.
1. Хроматографический способ выделения белковых компонентов белоксодержащего раствора, при этом указанный раствор содержит инсулиновый пептид и ионы цинка, указанный инсулиновый пептид способен к самоассоциации в присутствии ионов цинка, причем указанный способ включает следующие этапы:
а) нанесение белоксодержащего раствора на колонку с хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом находится в диапазоне 8-30 г на литр объема колонки (г/лCV); и
б) элюция инсулинового пептида из указанного твердофазного материала с помощью элюента с pH максимум 7,0; и сбор пула инсулинового пептида, соответствующего по меньшей мере 75% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а).
2. Хроматографический способ выделения белковых компонентов инсулинсодержащего раствора, при этом указанный раствор содержит инсулиновый пептид, способный к самоассоциации в присутствии цинка и двухвалентных ионов цинка, причем указанный способ включает следующие этапы:
а) нанесение инсулинсодержащего раствора на колонку с анионообменным хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом, представляющим интерес, находится в диапазоне 8-30 г на литр объема колонки (г/лCV); и
б) элюция инсулинового пептида, представляющего интерес, из указанного твердофазного материала с помощью элюента с pH максимум 6,8; и сбор пула инсулинового пептида, представляющего интерес, соответствующего по меньшей мере 90% по весу инсулиновому пептиду, представляющему интерес, нанесенному на колонку на этапе (а).
3. Способ по п.1 или 2, в котором ионы цинка представляют собой Zn2+ и концентрация ионов цинка в растворе находится в диапазоне 0,01-200 мМ, например 0,1-100 мМ, например 0,5-75 мМ.
4. Способ по п.1 или 2, в котором соотношение эквивалентов заряда ионов цинка и инсулинового пептида обычно составляет от 0,1:1 до 50:1, например от 0,3:1 до 20:1, например от 0,4:1 до 15:1 или от 0,5:1 до 10:1.
5. Способ по п.1 или 2, в котором pH элюента составляет максимум 6,8, например, максимум 6,6, или максимум 6,4, или максимум 6,2, или максимум 6,0, или по меньшей мере 4,0, или по меньшей мере 4,4, или по меньшей мере 4,8, или по меньшей мере 5,0, например, в диапазоне 4,0-6,8, или 4,4-6,8, или 4,8-6,8, или 4,0-6,8, таком как 4,0-6,6, или 4,0-6,4, или 4,0-6,2, или 4,0-6,0, или 4,4-6,8, или 4,4-6,6, или 4,4-6,4, или 4,8-6,8, или 4,8-6,6, или 4,8-6,2, или 5,0-6,8, или 5,0-6,6.
6. Способ по п.1 или 2, в котором пул инсулинового пептида, собранного на этапе (б), соответствует по меньшей мере 91% по весу, или по меньшей мере 92% по весу, или по меньшей мере 93% по весу, или по меньшей мере 94% по весу, или по меньшей мере 95% по весу, или по меньшей мере 96% по весу инсулиновому пептиду, нанесенному на колонку на этапе (а).
7. Способ по п.1 или 2, в котором инсулиновый пептид выбран среди инсулиновых производных, которые являются природным инсулином или его аналогом с боковой цепью, присоединенной к α-аминогруппе N-концевого аминокислотного остатка B-цепи или к ε-аминогруппе остатка Lys, присутствующего в B-цепи родительского инсулина, при этом боковая цепь имеет общую формулу:
- W-X-Y-Z,
где W представляет собой:
• α-аминокислотный остаток с карбоксильной группой в боковой цепи, который формирует через одну из его карбоксильных групп амидную группу вместе с α-аминогруппой N-концевого аминокислотного остатка B-цепи или вместе с ε-аминогруппой остатка Lys, присутствующего в B-цепи родительского инсулина;
• цепь, состоящую из двух, трех или четырех α-аминокислотных остатков, связанных друг с другом посредством амидных связей, которая через амидную связь связана с α-аминогруппой N-концевого аминокислотного остатка B-цепи или с ε-аминогруппой остатка Lys, присутствующего в B-цепи родительского инсулина, при этом аминокислотные остатки W выбраны из группы аминокислотных остатков с нейтральной боковой цепью и аминокислотных остатков с карбоксильной группой в боковой цепи, так что W имеет по меньшей мере один аминокислотный остаток с карбоксильной группой в боковой цепи; либо
• ковалентную связь от Х к α-аминогруппе N-концевого аминокислотного остатка B-цепи или к ε-аминогруппе остатка Lys, присутствующего в B-цепи родительского инсулина;
X представляет собой
• -CO-;
• -СН(COOH)CO-;
• -N(СН2СООН)CH2
CO-;
• -N(CH2COOH)CH2CON(CH2COOH)CH2
CO-;
• -N(CH2CH2COOH)CH2CH2
CO-;
• -N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2
CO-;
• -NHCH(COOH)(CH2)4NHCO-;
• -N(CH2CH2COOH)CH2
CO-; или
• -N(CH2COOH)CH2CH2
CO-;
что
а) когда W представляет собой аминокислотный остаток или цепь аминокислотных остатков, он через связь с подчеркнутым карбонильным углеродом образует амидную связь с аминогруппой в W, или
б) когда W представляет собой ковалентную связь, он через связь с подчеркнутым карбонильным углеродом образует амидную связь с N-концевой α-аминогруппой в B-цепи или с ε-аминогруппой остатка Lys, присутствующего в B-цепи родительского инсулина;
Y представляет собой:
• -(CH2)m-, где m представляет собой целое число в диапазоне от 6 до 32;
• двухвалентную углеводородную цепь, содержащую 1, 2 или 3 -CH=CH- группы, и число групп -CH2-, достаточное, чтобы дать общее число атомов углерода в цепи в диапазоне от 10 до 32;
• двухвалентную углеводородную цепь формулы -(CH2)vC6H4(CH2)w-, где v и w являются целыми числами или один из них равен нулю, так что сумма v и w находится в диапазоне от 6 до 30; а также
Z представляет собой:
• -COOH;
• -CO-Asp;
• -CO-Glu;
• -CO-Gly;
• -CO-Sar;
• -CH(COOH)2;
• -N(CH2COOH)2;
• -SO3H; или
• -PO3H;
и любым их комплексом с Zn2+.
8. Способ по п.1 или 2, в котором инсулиновый пептид представляет собой человеческий инсулин LysB29(Nε-гексадекандиол-γ-Glu) des(B30).
9. Способ по п.1 или 2 для выделения белковых компонентов инсулинсодержащего раствора, при этом указанный раствор содержит человеческий инсулин LysB29(Nε-гексадекандиол-γ-Glu) des(B30) и двухвалентные ионы цинка, а указанный способ включает следующие этапы:
а) нанесение инсулинсодержащего раствора на колонку с анионообменным хроматографическим твердофазным материалом, где нагрузка инсулиновым пептидом, представляющим интерес, находится в диапазоне 8-30 г на литр объема колонки (г/лCV); и
б) элюция инсулинового пептида, представляющего интерес, из указанного твердофазного материала с помощью элюента с pH в диапазоне от 6,4 до 6,8; и сбор пула человеческого инсулина LysB29(Nε-гексадекандиол-γ-Glu) des(B30), соответствующего по меньшей мере 90% по весу человеческому инсулину LysB29(Nε-гексадекандиол-γ-Glu) des(B30), нанесенному на колонку на этапе (а).
10. Способ по п.1 или 2, в который включен этап промывки после этапа (а), но до этапа (б) с применением промывочного буфера, содержащего этанол и триэтаноламин.
11. Способ по п.1 или 2, в котором инсулиновый пептид представляет собой производное инсулина, имеющее формулу:

где Ins представляет собой фрагмент родительского инсулина, а
Q1-Q2-[CH2]n-X1-[CH2]n-Q3-[CH2]n-X2-[CH2]n-Q4-[CH2]n-X3-[CH2]n-Q5-[CH2]n-Z представляет собой заместитель, и где Ins присоединен к заместителю через амидную связь между α-аминогруппой N-концевого аминокислотного остатка из B-цепи Ins или ε-аминогруппой остатка Lys, присутствующего в A- или B-цепи Ins, и CO-группой в Q1 или Q2 заместителя;
каждый n независимо представляет собой 0, 1, 2, 3, 4, 5 или 6;
Q1 является:
• амидом аминокислоты с карбоксильной кислотой в боковой цепи или аминокислоты с незаряженной боковой цепью, остаток которой через его карбоксильную группу формирует амидную группу вместе с α-аминогруппой N-концевого аминокислотного остатка из B-цепи Ins или вместе с ε-аминогруппой остатка Lys, присутствующего в А- или B-цепи Ins, либо
• цепью, состоящей из двух, трех или четырех амидов α-аминокислот или аминокислотных остатков, как указано выше, связанных друг с другом с помощью амидной связи, при этом цепь через амидную связь связана с α-аминогруппой N-концевого аминокислотного остатка B-цепи Ins или с ε-аминогруппой остатка Lys, присутствующего в А- или B-цепи Ins, или
• связью;
Q2 представляет собой:
• -COCH(CONH2)-
• -COCH2N(CH2CONH2)-
• -COCH2N(CH2CONH2)COCH2N(CH2CONH2)
• -COCH2CH2N(CH2CH2CONH2)-
• -COCH2CH2N(CH2CH2CONH2)-COCH2CH2N(CH2CH2CONH2)-
• -COCH2N(CH2CH2CONH2)-
• -COCH2CH2N(CH2CONH2)-
• -COCH2OCH2CONH-
• -CO-((CR5R6)1-6-NH-CO)1-4-;
• - -СО-((CR5R6)1-6-CO-NH)1-4- где R5 независимо может быть H, -CH3, -(CH2)1-6CH3 или -CONH2, а R6 независимо может представлять собой H, -CH3, -(CH2)1-6CH3; или
• - связь
при условии, что
• по меньшей мере один из Q1 или Q2 не является связью, и
• что Q2 не является -CO-(СН2)2-CO-NH-, где n составляет 0 или 1, X1 представляет собой связь, a Q3 представляет собой (CH2CH2O)2- (CH2CH2O)3- или (CH2CH2OCH2CH2CH2CH2O)- и
• что, если амин в Q1 или Q2 образует связь с остальной частью заместителя, амин должен быть связан с остальной частью заместителя через карбонильную группу;
Q3, Q4 и Q5 каждый независимо друг от друга может представлять собой
• -(CH2)m-, где m представляет собой целое число в диапазоне от 6 до 32;
• двухвалентную углеводородную цепь, содержащую 1, 2 или 3 -СН=СН- группы и число -CH2- групп, достаточное, чтобы дать общее число атомов углерода в цепи в диапазоне от 4 до 32;
• -СО-((CR5R6)1-6-NH-CO)-;
• -(СО-(CR5R6)1-6-CO-NH)1-4-, где R5 независимо может быть H, -CH3, -(СН2)1-6СН3 или -CONH2, а R6 независимо может быть Н, -CH3, -(СН2)1-6СН3;
• -СО-(СН2)0-3-Ar-(СН2)0-3-, где Ar может быть ариленом или гетероариленом, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из -CH3, -(CH)1-6-СН3, -CONR1R2 или -SO2NR1R2, где R1 и R2 независимо друг от друга могут быть H, -CH3 или -(CH)1-6-CH3;
• (CH2CH2O)y- (CH2CH2CH2O)y-; (CH2CH2CH2CH2O)y-; (CH2CH2OCH2CH2CH2CH2O)y- или (CH2CH2CH2OCH2CH2CH2CH2O)y-; -(CH2OCH2)y- где y составляет 1-20;
• арилен или гетероарилен, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из -CH3, -(CH)1-6-СН3, -CONR1R2 или -SO2NR1R2, где R1 и R2 независимо друг от друга может быть Н, -CH3 или -(CH)1-6-СН3;
• цепь формулы
-(CH2)s-Y1-(Ar)v1-Y2-(CH2)w-Y3-(Ar)v2-Y4-(CH2)t-Y5-(Ar)v3-Y6-(CH2)z-,
где Ar имеет вышеуказанное значение, Y1-Y6 независимо друг от друга могут быть О, S, S=O, SO2 или связью; где s, w, t и z независимо друг от друга составляют ноль или целое число от 1 до 10, так что сумма s, w, t и z находится в диапазоне от 4 до 30, a v1, v2, и v3 независимо друг от друга могут быть равны нулю или 1, при условии, что Y1-Y6 не связаны друг с другом, и что не образуется структура -O-(CH2)1-O-; либо
• связь;
при условии, что по меньшей мере один из Q3-Q5 не является связью;
X1, X2 и X3 независимо друг от друга представляют собой
• О;
• -С=O
• связь;
• NCOR1, где R1 может быть H, -CH3 или -(CH)1-6-CH3; или
•  или
или 
где R представляет собой водород, C1-3-алкин, C2-3-алкенил или C2-3-алкинил;
с условием, что
• X1, X2 и X3 не могут быть связаны с Z, и
• если X1, X2 и X3 представляют собой О, то X1, X2 и X3 не связаны напрямую с О в Q3, Q4 и Q5
и
Z представляет собой: -COOH; -CO-Asp; -CO-Glu; -CO-Gly; -CO-Sar; -CH(COOH)2, -N(CH2COOH)2; -SO3H; -OSO3H; -OPO3H2; -PO3H2; -тетразол-5-ил или -O-W1,
где W1 представляет собой арилен или гетероарилен, который может быть заменен одной или двумя группами, выбранными из группы, состоящей из тетразо-5-лил, -COOH, -SO3H, -(СН2)1-6-SO3H, -(CH2)1-6-О-PO3H2-CONR3R4 или -SO2NR3R4, где R3 и R4, независимо друг от друга могут быть H, -(CH2)1-6-SO3H, или -(СН2)1-6-O-PO3H2; при условии, что если Z представляет собой -O-W1, то Q1 должен присутствовать, и любой их Zn2+-комплекс.
12. Способ по любому из пп. 1 или 2, где двухвалентные ионы цинка были добавлены, чтобы закрепить форму передней части пика инсулинового пептида, где родственные примеси элюируются перед инсулиновым пептидом.
| RU 2010110805 A, 27.09.2011 | |||
| WO 2007108955 A1, 27.09.2007 | |||
| Блочек для обуви | 1989 |
|
SU1666048A1 |
| Способ определения величины зазораВ РАбОчЕй пАРЕ плуНжЕР-цилиНдРСКВАжиННОгО шТАНгОВОгО HACOCA | 1978 |
|
SU832121A1 |
Авторы
Даты
2016-11-27—Публикация
2012-02-01—Подача