Настоящее изобретение относится к новым 3-замещенным производным 6-пиперазинилпиридина, к их получению, к фармацевтическим композициям, содержащим эти соединения, и к их применению в качестве лекарственных средств. Биологически активные соединения согласно настоящему изобретению можно использовать для лечения ожирения и других нарушений и расстройств.
В частности, настоящее изобретение относится к соединениям общей формулы:
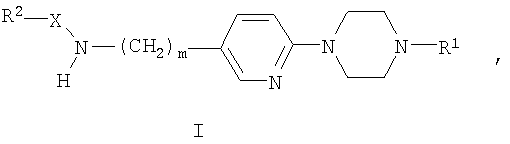
где
R1 выбирают из группы, состоящей из водорода, низшего алкила, С3-С7-алкенила,
С3-С7-алкинила, низшего галогеналкила, низшего гидроксиалкила, низшего алкоксиалкила, С3-С7-циклоалкила и низшего С3-С7-циклоалкилалкила;
Х представляет собой С(O) или SO2;
m означает 0 или 1;
R2 выбирают из группы, состоящей из низшего алкила, С3-С7-алкенила, С3-С7-алкинила,
низшего галогеналкила, низшего гидроксиалкила, низшего алкоксиалкила,
незамещенного С3-С7-циклоалкила или С3-С7-циклоалкила, замещенного фенилом,
низшего С3-С7-циклоалкилалкила,
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом,
незамещенного пиридила или пиридила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и
-NR3R4,
или в том случае, когда Х представляет собой С(O), R2 также может представлять собой низший алкокси или низший алкоксиалкокси,
или в том случае, когда m означает 1, R2 также может представлять собой незамещенный фенил или фенил, моно- или дизамещенный низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, R3 представляет собой водород или низший алкил
R4 выбирают из группы, состоящей из низшего алкила, С3-С7-алкенила, С3-С7-алкинила,
низшего алкоксиалкила,
С3-С7-циклоалкила,
С3-С7-циклоалкила, замещенного фенилом,
низшего С3-С7-циклоалкилалкила,
незамещенного фенила или фенила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом; или
R3 и R4 вместе с атомом азота, к которому они присоединены, образует 4-, 5-, 6- или 7-членную гетероциклическую кольцевую систему, необязательно содержащую еще один гетероатом, выбранный из азота, кислорода или серы, причем указанная гетероциклическая кольцевая система является незамещенной или замещенной одной, двумя или тремя группами, независимо выбранными из низшего алкила, низшего алкокси, низшего алкоксикарбонила, оксо, галогена и галогеналкила, или является конденсированной (сопряженной) с С5-С6-циклоалкильным кольцом или с фенильным кольцом, указанное циклоалкильное кольцо или фенильное кольцо является незамещенным или замещенным одной, двумя или тремя группами, независимо выбранными из низшего алкила, низшего алкокси, галогена и галогеналкила;
и фармацевтически приемлемым солям этих соединений;
за исключением 2,2-диметил-N-[6-(4-метилпиперазин-1-ил)пиридин-3-ил]пропионамида.
2,2-Диметил-N-[6-(4-метилпиперазин-1-ил)пиридин-3-ил]пропионамид описан в ЕР 1035115 A1 (F.Hoffmann - La Roche AG) в качестве промежуточного соединения для синтеза производных 4-фенилпиридина, которые могут быть использованы в качестве антагонистов NK-1 рецептора.
Было обнаружено, что соединения формулы I являются антагонистами и/или обратными агонистами гистаминового 3 рецептора (Н3 рецептора).
Гистамин (2-(4-имидазолил) этиламин) относится к аминергическим нейротрансмиттерам, которые широко представлены в организме человека, например, в желудочно-кишечном тракте (Burks 1994 in Johnson L.R. ed., Physiology of the Gastrointestinal Tract, Raven Press, NY, pp.211-242). Гистамин является регулятором множества патофизиологических пищеварительных процессов, таких как секреция кислоты желудочного сока, перистальтика кишечника (Leurs et al., Br J. Pharmacol. 1991, 102, pp 179-185), вазомоторная реакция, воспалительные реакции кишечника и аллергические реакции (Raithel et al., Int. Arch. Allergy Immunol. 1995, 108, 127-133). В мозге млекопитающих гистамин синтезируется в гистаминергических протопластах, которые обнаружены в основном в сосцевидных отростках ядер заднего базального отдела гипоталамуса. По этим данным, протопласты располагаются в различных областях мозга (Panula et al., Proc. Natl. Acad. Sci. USA 1984, 81, 2572-2576; Inagaki et al., J. Comp. Neurol 1988, 273, 283-300).
В соответствии с последними данными гистамин является медиатором различных функций как центральной, так и периферической нервной системы, с участием четырех различных гистаминовых рецепторов, а именно, гистаминовых рецепторов H1, Н2, Н3 и Н4.
Гистаминовые Н3 рецепторы преимущественно локализируются в центральной нервной системе (ЦНС). В качестве авторецепторов гистаминовые H3 рецепторы конститутивно ингибируют синтез и секрецию гистамина гистаминергическими нейронами (Arrang et al., Nature 1983, 302, 832-837; Arrang et al., Neuroscience 1987, 23, 149-157). В качестве гетерорецепторов гистаминовые H3 рецепторы также модулируют высвобождение других нейротрансмиттеров, таких как ацетилхолин, допамин, серотонин и норадреналин (норэпинефрин) как в центральной системе, так и в периферических органах, таких как легкие, сердечно-сосудистая система и желудочно-кишечный тракт (Clapham & Kilpatrik, Br. J. Pharmacol. 1982, 107, 919-923; Blandina et al. in The Hystamine H3 Receptor (Leurs RL, Timmermann H eds, 1998, pp 27-40, Elsevier, Amsterdam, The Netherlands). Гистаминовые H3 рецепторы являются конститутивно активными, что означает, что даже без экзогенного гистамина рецептор является тонически активированным. В случае ингибирующего рецептора, например, такого как Н3 рецептор, такая собственная активность вызывает тоническое ингибирование высвобождения нейротрансмиттера. Таким образом, может быть существенным, что H3R антагонист также может видоизменять агонистическую активность как в отношении блокирования экзогенных эффектов гистамина, так и в отношении перехода рецептора из конститутивно активной (ингибирующей) формы в нейтральное состояние.
Широкое распространение Н3 рецепторов в ЦНС млекопитающих свидетельствуют о физиологической роли этого рецептора. Таким образом, можно предполагать наличие у этих соединений терапевтического потенциала в качестве нового лекарственного средства, которое можно использовать при разнообразных показаниях.
Введение H3R лигандов - в качестве антагонистов, обратных агонистов, агонистов или частичных агонистов - может оказывать воздействие на уровень гистамина или выделение нейротрансмиттеров в мозг и периферические системы, и таким образом может быть полезно для лечения некоторых нарушений и расстройств. Такие нарушения и расстройства включают ожирение, (Masaki et al; Endocrinol. 2003, 144, 2741-2748; Hancock et al., European J. of Pharmacol. 2004, 487, 183-197), сердечно-сосудистые заболевания, такие как острый инфаркт миокарда, деменция, когнитивные расстройства, такие как синдром дефицита внимания и гиперактивности (ADHD) и болезнь Альцгеймера, неврологические нарушения и расстройства, такие как шизофрения, депрессия, эпилепсия, болезнь Паркинсона и эпилептические припадки или судороги, расстройства сна, нарколепсия, боль, желудочно-кишечные заболевания, вестибулярная дисфункция, такая как болезнь Меньера (эндолимфатическая водянка), токсикомания и укачивание в транспорте (Timmermann, J. Med. Chem. 1990, 33, 4-11).
Таким образом, целью настоящего изобретения является получение селективных, антагонистов, соответственно, обратных агонистов Н3 рецепторов прямого действия. Такие антагонисты / обратные агонисты могут быть использованы в качестве терапевтически активных соединений, в частности, при лечении и/или профилактике заболеваний, которые связаны с модулированием гистаминовых Н3 рецепторов.
В описании настоящего изобретения термин "алкил", по отдельности или в комбинации с другими группами, относится к моновалентному насыщенному алифатическому углеводородному радикалу с линейной или разветвленной цепью, содержащему от одного до двадцати атомов углерода, предпочтительно, от одного до шестнадцати атомов углерода, более предпочтительно, от одного до десяти атомов углерода.
Термин "низший алкил" или "С1-С8-алкил", по отдельности или в комбинации, означает алкильную группу с линейной или разветвленной цепью, содержащую от 1 до 8 атомов углерода, предпочтительно, алкильную группу с линейной или разветвленной цепью, содержащую от 1 до 6 атомов углерода и особенно предпочтительно, алкильную группу с линейной или разветвленной цепью, содержащую от 1 до 4 атомов углерода Примерами C1-C8 алкильной группы с линейной или разветвленной цепью являются метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, изомерные пентилы, изомерные гексилы, изомерные гептилы и изомерные октилы, предпочтительно, метил, этил и изопропил, и наиболее предпочтительно, метил и этил.
Термин "низший алкенил" или "С3-С8-алкенил", по отдельности или в комбинации, означает алкильную группу с линейной или разветвленной цепью, включающую олефиновую связь и до 8, предпочтительно, до 6, особенно предпочтительно, до 4 атомов углерода. Примерами алкенильных групп являются 1-пропенил, 2-пропенил, изопропенил, 1-бутенил, 2-бутенил, 3-бутенил и изобутенил. Предпочтительным примером является 2-пропенил.
Термин "низший алкинил" или "С3-С8-алкинил", по отдельности или в комбинации, означает алкильную группу с линейной или разветвленной цепью, включающую тройную связь и до 8, предпочтительно до 6, особенно предпочтительно до 4 атомов углерода. Примеры алкинильных групп включают 2-пропинил (пропаргил), 1-метил-2-пропинил, 2-бутинил, 3-бутинил, 2-пентинил и 1-пентин-3-ил.
Термин "алкокси" относится к группе R'-O-, где R' представляет собой алкил. Термин "низший алкокси" относится к группе R'-O-, где R' представляет собой низший алкил, и термин "низший алкил" имеет ранее указанное значение ("C1-C8-алкокси"). Примерами низших алкоксигрупп являются, например, метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси и трет-бутокси, предпочтительно, метокси и этокси, и наиболее предпочтительно, метокси.
Термин "низший алкоксиалкил" или "С1-С8-алкокси-С1-С8-алкил" относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен алкоксигруппой, как указано выше. К числу предпочтительных низших алкоксиалкильных групп относятся метоксиметил, метоксиэтил и этоксиметил, причем метоксиметил является особенно предпочтительным.
Термин "низший алкоксиалкокси" или "C1-C8-алкокси-C1-C8-алкокси" относится к низшим алкоксигруппам, как определено выше, где по меньшей мере один из атомов водорода низшей алкоксигруппы замещен алкоксигруппой, которая определена выше. К числу предпочтительных низших алкоксиалкоксигрупп относятся метоксиэтокси, метоксипропилокси и этоксиэтокси, причем метоксиэтокси является особенно предпочтительным.
Термин "галоген" относится к фтору, хлору, брому и иоду, причем фтор, хлор и бром являются предпочтительными.
Термин "низший галогеналкил" или "галоген-С1-С8-алкил" относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы является замещенным атомом галогена, предпочтительно, фтором или хлором, наиболее предпочтительно, фтором. К числу предпочтительных галогенированных низших алкильных групп относятся трифторметил, дифторметил, фторметил и хлорметил, причем трифторметил является особенно предпочтительным.
Термин "низший гидроксиалкил" или "гидрокси-С1-С8-алкил" относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен гидроксигруппой. Примерами низших гидроксиалкильных групп являются гидроксиметил или гидроксиэтил.
Термин "циклоалкил" или "С3-С7-циклоалкил" означает циклоалкильную кольцевую систему, содержащую от 3 до 7 атомов углерода, такую как циклопропил, циклобутил, циклопентил, циклогексил или циклогептил. Циклоалкильная кольцевая система может быть замещенной таким образом, как определено в тексте настоящей заявки. Особенно предпочтительными являются циклопропил или циклопентил.
Термин "низший циклоалкилалкил" или "С3-С7-циклоалкил-С1-С8-алкил" относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен циклоалкильной группой, которая указана выше. Примерами предпочтительных низших циклоалкилалкильных групп являются циклопропилметил или циклопропилметил.
Термин "низший фенилалкил" или "фенил-С1-С8-алкил" относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен фенильной группой. Фенильное кольцо может быть замещенным таким образом, как определено в тексте настоящей заявки. Примерами предпочтительных низших фенилалкильных групп являются бензил, 4-метилбензил, 4-фторбензил, 3-метоксибензил и 3,4-диметоксибензил.
Термин "образуют 4-, 5-, 6- или 7-членную насыщенную гетероциклическую кольцевую систему, необязательно содержащую дополнительный гетероатом, выбранный из азота, кислорода или серы" относится к насыщенным N-гетероциклическим кольцевым системам, которые могут необязательно содержать дополнительный атом азота, кислорода или серы, например, к таким системам как азетидинил, пирролидинил, имидазолидинил, пиразолидинил, оксазолидинил, изоксазолидинил, тиазолидинил, изотиазолидинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил или азепенил. Гетероциклическая кольцевая система может быть незамещенной или замещенной одной, двумя или тремя группами, независимо выбранными из низшего алкила, низшего алкокси, оксо, галогена и галогеналкила. Гетероциклическая кольцевая система может быть также сопряженной (конденсированной) с С5-С6-циклоалкильным кольцом или фенильным кольцом, причем указанное циклоалкильное кольцо или фенильное кольцо могут быть незамещенными или замещенными одной, двумя или тремя группами, независимо выбранными из низшего алкила, низшего алкокси, галогена и галогеналкила. Примерами таких конденсированных гетероциклических кольцевых систем являются 3,4-дигидро-1H-изохинолин, 1,3-дигидроизоиндол и октагидрохинолин.
Термин "фармацевтически приемлемые соли" относится к таким солям, которые сохраняют биологическую эффективность и свойства свободных оснований или свободных кислот, и которые не являются нежелательными ни в биологическом, ни в каком-либо другом отношении. Эти соли образованы с неорганическими кислотами, такими как хлороводородная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., предпочтительно, с хлороводородной кислотой, и с органическими кислотами, такими как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, малеиновая кислота, малоновая кислота, салициловая кислота, янтарная кислота (бутандикислота), фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная (β-фенилакриловая) кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота, N-ацетилцистеин и т.п. Дополнительно эти соли могут быть получены при присоединении неорганического основания или органического основания к свободной кислоте. Соли - производные неорганического основания - включают, но не ограничиваются указанным, соли натрия, калия, лития, аммония, кальция, магния и т.п. Соли - производные органического основания - включают, но не ограничиваются указанным, соли первичных, вторичных и третичных аминов, замещенных аминов, включая природные соединения - замещенные амины, циклические амины и основные ионообменные смолы, такие как смолы на основе изопропиламина, триметиламина, диэтиламина, триэтиламина, трипропиламина, этаноламина, лизина, аргинина, N-этилпиперидина, пиперидина, полииминовые смолы и т.п. Соединение формулы I также может быть представлено в виде цвиттерионов. Особенно предпочтительными фармацевтически приемлемыми солями соединений формулы I являются соли - гидрохлориды.
Соединения формулы I также могут быть сольватированными, например гидратированными. Сольватация может осуществляться в процессе получения соединения или может происходить, например, вследствие гигроскопичности первоначально безводного соединения формулы I (гидратация). Термин фармацевтически приемлемые соли также включает физиологически приемлемые сольваты.
"Изомеры" представляют собой соединения, которые имеют одинаковую молекулярную формулу, но различаются по природе и порядку присоединения входящих в них атомов или по последовательности присоединения атомов, или по расположению атомов в пространстве. Изомеры, которые отличаются по расположению атомов в пространстве, называют "стереоизомерами". Стереоизомеры, которые не являются зеркальными отображениями друг друга, называют "диастереоизомерами", и стереоизомеры, которые не являются накладываемыми зеркальными отображениями, обозначают как "энантиомеры", или иногда как оптические изомеры. Атом углерода, у которого имеется четыре различных заместителя, называют "хиральным центром".
Более подробно, настоящее изобретение относится к соединениям общей формулы:
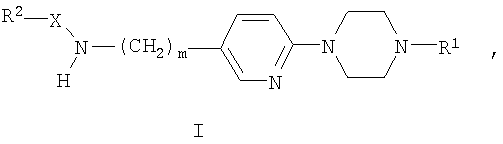
где
R1 выбирают из группы, состоящей из водорода, низшего алкила, С3-С7-алкенила,
С3-С7-алкинила, низшего галогеналкила, низшего гидроксиалкила, низшего алкоксиалкила, С3-С7-циклоалкила и низшего С3-С7-циклоалкилалкила;
Х представляет собой С(O) или SO2;
m означает 0 или 1;
R2 выбирают из группы, состоящей из низшего алкила, С3-С7-алкенила, С3-С7-алкинила,
низшего галогеналкила, низшего гидроксиалкила, низшего алкоксиалкила,
незамещенного С3-С7-циклоалкила или С3-С7-циклоалкила, замещенного фенилом,
низшего С3-С7-циклоалкилалкила,
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом,
незамещенного пиридила или пиридила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом и
-NR3R4,
или в том случае, когда Х представляет собой С(O), R2 также может представлять собой низший алкокси или низший алкоксиалкокси,
или в том случае, когда m означает 1, R2 также может означать незамещенный фенил или фенил, моно- или дизамещенный низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом,
R3 представляет собой водород или низший алкил;
R4 выбирают из группы, состоящей из низшего алкила, С3-С7-алкенила, С3-С7-алкинила,
низшего алкоксиалкила,
С3-С7-циклоалкила,
С3-С7-циклоалкила, замещенного фенилом,
низшего С3-С7-циклоалкилалкила,
незамещенного фенила или фенила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом; или
R3 и R4 вместе с атомом азота, к которому они присоединены, образует 4-, 5-, 6- или 7-членную гетероциклическую кольцевую систему, необязательно содержащую еще один гетероатом, выбранный из азота, кислорода или серы, причем указанная гетероциклическая кольцевая система является незамещенной или замещенной одной, двумя или тремя группами независимо выбранными из низшего алкила, низшего алкокси, низшего алкоксикарбонила, оксо, галогена и галогеналкила, или является конденсированной (сопряженной) с С5-С6-циклоалкильным кольцом или фенильным кольцом, причем указанное циклоалкильное кольцо или фенильное кольцо является незамещенным или замещенным одной, двумя или тремя группами, независимо выбранными из низшего алкила, низшего алкокси, галогена и галогеналкила;
и к фармацевтически приемлемым солям этих соединений;
за исключением 2,2-диметил-N-[6-(4-метилпиперазин-1-ил)пиридин-3-ил]пропионамида.
Таким образом, заместитель R1 выбирают из группы, состоящей из водорода, низшего алкила, С3-С7-алкенила, С3-С7-алкинила, низшего галогеналкила, низшего гидроксиалкила, низшего алкоксиалкила, С3-С7-циклоалкила и низшего С3-С7-циклоалкилалкила. Предпочтительными соединениями формулы I согласно настоящему изобретению являются такие соединения, где R1 представляет собой низший алкил или С3-С7-циклоалкил, причем предпочтительными являются такие соединения, где R1 представляет собой С3-С7-циклоалкил, а соединения, где R1 представляет собой циклопентил, являются наиболее предпочтительными. Соединения формулы I, где R1 представляет собой этил или изопропил, также весьма предпочтительны.
Показатель m означает целое число, равное 0 или 1. Особенно предпочтительными являются такие соединения формулы I, где m означает 1. Однако соединения формулы I, где m означает 0, также представляют предпочтительный вариант осуществления настоящего изобретения.
Кроме того, предпочтительными являются соединения формулы I согласно настоящему изобретению, где R2 выбирают из группы, состоящей из следующих заместителей:
низший алкил, С3-С7-алкенил, С3-С7-алкинил,
низший галогеналкил, низший гидроксиалкил, низший алкоксиалкил,
незамещенный С3-С7-циклоалкил или С3-С7-циклоалкил, замещенный фенилом,
низший С3-С7-циклоалкилалкил,
низший фенилалкил, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом,
незамещенный пиридил или пиридил, моно- или дизамещенный низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом и
-NR3R4,
или в том случае, когда Х представляет собой С(O), R2 также может представлять собой низший алкокси или низший алкоксиалкокси.
В этой группе предпочтительными являются соединения формулы I, где R2 выбирают из группы, состоящей из низшего алкила, С3-С7-циклоалкила и С3-С7-циклоалкила, замещенного фенилом.
Кроме того, предпочтительными являются соединения формулы I, где R2 представляет собой низший фенилалкил, причем фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом.
Также предпочтительными являются соединения формулы I согласно настоящему изобретению, где R2 представляет собой группу -NR3R4.
Более предпочтительными являются такие соединения формулы I, где R2 представляет собой группу-NR3R4 и R3 представляет собой водород или низший алкил;
R4 выбирают из группы, состоящей из низшего алкила, С3-С7-алкенил, С3-С7-алкинила,
С3-С7-циклоалкила,
С3-С7-циклоалкила, замещенного фенилом,
низшего С3-С7-циклоалкилалкила,
незамещенного фенила или фенила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом; или
R3 и R4 вместе с атомом азота, к которому они присоединены, образует 4-, 5-, 6- или 7-членную гетероциклическую кольцевую систему, необязательно содержащую еще один гетероатом, выбранный из азота, кислорода или серы, причем указанная гетероциклическая кольцевая система является незамещенной или замещенной одной, двумя или тремя группами, независимо выбранными из низшего алкила, низшего алкокси, оксо, галогена и галогеналкила, или является конденсированной (сопряженной) с фенильным кольцом, указанное фенильное кольцо является незамещенным или замещенным одной, двумя или тремя группами, независимо выбранными из низшего алкила, низшего алкокси, галогена и галогеналкила.
Наиболее предпочтительными являются такие соединения формулы I, где R3 и R4 представляют собой низший алкил.
Другую группу предпочтительных соединений формулы I представляют такие соединения, где R2 представляет собой группу -NR3R4, R3 представляет собой водород, и R4 выбирают из группы, состоящей из
низшего алкила, С3-С7-алкенила, С3-С7-алкинила,
С3-С7-циклоалкила, С3-С7-циклоалкила, замещенного фенилом,
низшего С3-С7-циклоалкилалкила,
незамещенного фенила или фенила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом.
Указанные соединения, где R3 представляет собой водород и R4 представляет собой низший фенилалкил, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, являются особенно предпочтительными.
Кроме того, являются предпочтительными соединения формулы I согласно настоящему изобретению, где m означает 1, и R2 представляет собой незамещенный фенил или фенил, моно- или дизамещенный низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом.
Предпочтительную группу соединений формулы I представляют такие соединения, где Х представляет собой SO2. Эти соединения соответствуют формуле:
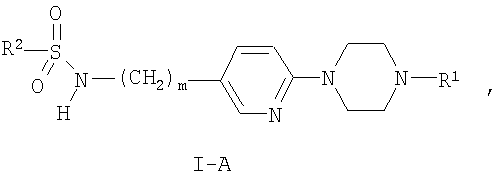
где R1, R2 и m являются такими, как указано выше в тексте настоящей заявки.
Кроме того, являются предпочтительными соединения формулы I, где Х представляет собой С(O). Эти соединения соответствуют формуле:
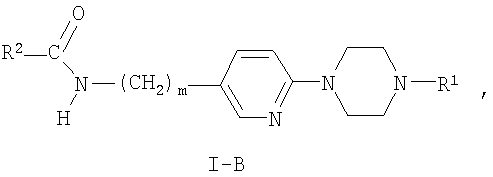
где R1, R2 и m являются такими, как указано выше в тексте настоящей заявки.
В этой группе особенно предпочтительными являются такие соединения, где Х представляет собой С(O) и R2 представляет собой -NR3R4, т.е. соединения формулы:
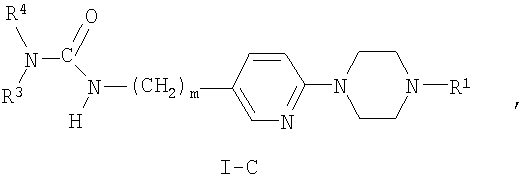
где R1, R3, R4 и m являются такими, как указано выше в тексте настоящей заявки.
Примерами предпочтительных соединений формулы I являются следующие соединения:
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-пропилмочевина,
1-циклогексил-3-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-бензил-3-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-п-толилмочевина,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-((1R,2S)-2-фенил-циклопропил)мочевина,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-(3-метоксифенил)мочевина,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-(4-фторфенил)мочевина,
1-циклогексил-3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-бензил-3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-3-(4-метилбензил)-мочевина,
1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-3-((1R,2S)-2-фенил-циклопропил)мочевина,
1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-3-(4-фторфенил)-мочевина,
1-циклогексил-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-фенилмочевина,
1-бензил-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-о-толилмочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-м-толилмочевина,
1-(2-хлорфенил)-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-(4-метилбензил)-мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-((1R,2S)-2-фенил-циклопропил)мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-(3-метокси-фенил)мочевина,
1-(4-фторфенил)-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-пропилмочевина,
1-циклогексил-3-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-бензил-3-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-м-толилмочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-п-толилмочевина,
1-(2-хлорфенил)-3-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-(4-метилбензил)мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-((1R,2S)-2-фенил-циклопропил)мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-(3-метокси-фенил)мочевина,
1-(4-фторфенил)-3-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]мочевина,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-диметиламиносульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-диметиламиносульфонамид,
N-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-диметиламиносульфонамид,
[6-(4-этилпиперазин-1-ил)пиридин-3-ил]амид циклогексанкарбоновой кислоты,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-2-фенилацетамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-2-(4-фторфенил)ацетамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-2-(3-метоксифенил)ацетамид,
2-(3,4-диметокси-фенил)-N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]ацетамид,
2-метоксиэтиловый эфир [6-(4-этилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
изобутиловый эфир [6-(4-этилпиперазин-1-ил)пиридин-3-ил]карбаминовой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид циклопропанкарбоновой кислоты,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]бутирамид,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид циклобутанкарбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид циклопентанкарбоновой кислоты,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-этилбутирамид,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид циклогексанкарбоновой кислоты,
2-хлор-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]никотинамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-фенилацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-(4-фторфенил)-ацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-(3-метоксифенил)-ацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-(3,4-диметокси-фенил)ацетамид,
этиловый эфир [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
2-метоксиэтиловый эфир [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
изобутиловый эфир [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]амид циклогексанкарбоновой кислоты,
2-(3,4-диметокси-фенил)-N-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]ацетамид,
этиловый эфир [6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
изобутиловый эфир [6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]бутирамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-3-метокси-бензамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-2-фенилацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-2-(4-фторфенил)-ацетамид,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]амид этансульфоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]амид пропан-1-сульфоновой кислоты,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]диметил-аминосульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-бензолсульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-С-фенил-метансульфонамид,
С-(4-хлорфенил)-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]метансульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-2-фтор-бензолсульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-3-фтор-бензолсульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-4-фтор-бензолсульфонамид,
2-хлор-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]бензолсульфонамид,
4-хлор-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]бензолсульфонамид,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-3-(4-фтор-бензил)мочевина,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-3-метоксибензамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-2-фенилацетамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-2-(4-фторфенил)ацетамид,
[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]амид этансульфоновой кислоты,
[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]амид пропан-1-сульфоновой кислоты,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-диметил-аминосульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]бензолсульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-С-фенил-метансульфонамид,
С-(4-хлорфенил)-N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-метансульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-2-фтор-бензол-сульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-3-фтор-бензолсульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-4-фтор-бензол-сульфонамид,
2-хлор-N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-бензолсульфонамид,
4-хлор-N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-бензолсульфонамид,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид 4-метилпиперидин-1-карбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид 2,6-диметил-пиперидин-1-карбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид 4-трифтор-метилпиперидин-1-карбоновой кислоты,
этиловый эфир 1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илкарбамоил]пиперидин-4-карбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид октагидрохинолин-1-карбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид октагидроизохинолин-2-карбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид 2-трифторметилпирролидин-1-карбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид 2-изопропилпирролидин-1-карбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид 1,3-дигидроизоиндол-2-карбоновой кислоты,
3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-1-изопропил-1-(2-метоксиэтил)мочевина,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид азепан-1-карбоновой кислоты,
3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-1-этил-1-фенилмочевина,
3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-1-(4-метокси-фенил)-1-метилмочевина,
3,4-дигидро-2N-хинолин-1-карбоновой кислоты [6-(4-этилпиперазин-1-ил)пиридин-3-ил]амид,
3,4-дигидро-2N-хинолин-1-карбоновой кислоты [6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]амид,
и фармацевтически приемлемые соли этих соединений.
Особенно предпочтительными соединениями формулы I согласно настоящему изобретению являются следующие соединения:
1-бензил-3-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-бензил-3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-3-(4-метилбензил)мочевина,
1-бензил-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]диметиламино-сульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-(3,4-диметокси-фенил)ацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-3-метокси-бензамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-2-фенилацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-
диметиламиносульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-С-фенил-
метансульфонамид,
С-(4-хлорфенил)-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]
метансульфонамид,
2,6-диметилпиперидин-1-карбоновой кислоты [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид,
и фармацевтически приемлемые соли этих соединений.
Кроме того, фармацевтически приемлемые соли соединения формулы I и фармацевтически приемлемые сложные эфиры соединения формулы I по отдельности являются предпочтительными вариантами осуществления настоящего изобретения.
Соединения формулы I могут образовывать аддитивные соли с кислотами, такими как общеизвестные фармацевтически приемлемые соли, например гидрохлорид, гидробромид, фосфат, ацетат, фумарат малеат, салицилат, сульфат, пируват, цитрат, лактат, соль миндальной кислоты, тартрат и метансульфонат. Предпочтительными являются соли гидрохлориды. Частью настоящего изобретения также являются сольваты и гидраты соединений формулы I и их соли.
Кроме того, N-атом пиридинового кольца может быть представлен как N-оксидная группа. Такие N-оксиды соединений формулы I также составляют часть настоящего изобретения.
Соединения формулы I могут содержать один или более асимметрический атом и могут существовать в виде оптически чистых энантиомеров, смесей энантиомеров, например, в виде рацематов, оптически чистых диастереоизомеров, смесей диастереоизомеров, диастереоизомерных рацематов или смесей диастереоизомерных рацематов. Оптически активные формы могут быть получены, например, посредством разделения рацематов, асимметрическим синтезом или асимметрической хроматографией (хроматография с хиральным адсорбентом или элюентом). Настоящее изобретение включает все такие формы.
Необходимо отметить, что соединения общей формулы I согласно настоящему изобретению могут быть модифицированы по функциональной группе с получением при этом производных, которые способны к обратному превращению в материнское соединение in vivo. Физиологически приемлемые и метаболически лабильные производные, которые способны к превращению в исходные соединения общей формулы I in vivo, также входят в объем настоящего изобретения.
Еще один аспект настоящего изобретения относится к способу получения соединений формулы I, как указано выше, указанный способ включает:
а) взаимодействие соединения формулы II:
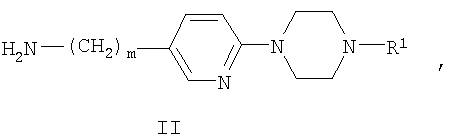
где R1 и m являются такими, как определено выше в тексте настоящей заявки, с сульфонилхлоридом или сульфамоилхлоридом формулы III:
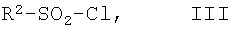
где R2 является таким, как определено выше в тексте настоящей заявки, с образованием при этом соединения формулы I-A:
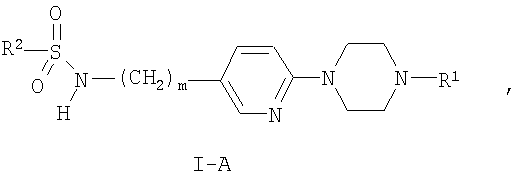
где R1, R2 и m являются такими, как определено выше в тексте настоящей заявки, или
б) взаимодействие соединения формулы II:
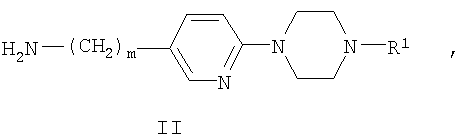
где R1 и m являются такими, как определено выше в тексте настоящей заявки, с хлорангидридом формулы IV:
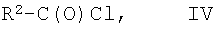
где R2 является таким, как определено выше в тексте настоящей заявки, с образованием при этом соединения формулы I-B:
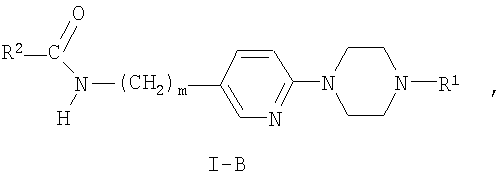
где R1, R2 и m являются такими, как определено выше в тексте настоящей заявки, или
в) взаимодействие соединения формулы II
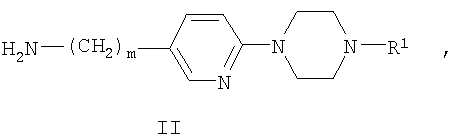
где R1 и m являются такими, как определено выше в тексте настоящей заявки,
с изоцианатом формулы V:
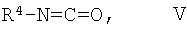
где R4 является таким, как определено выше в тексте настоящей заявки, с образованием при этом соединения формулы I-C:
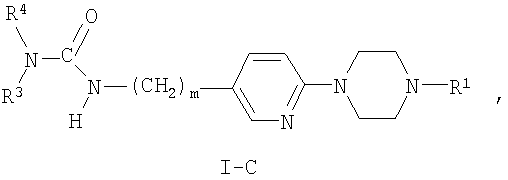
где R3 представляет собой водород и R1, R4 и m являются такими, как определено выше в тексте настоящей заявки,
и если необходимо, превращение соединения формулы I-A, I-B или I-C в фармацевтически приемлемую соль.
Более конкретно, соединения формулы I могут быть получены в соответствии со способами, приведенными ниже, в соответствии со способами, описанными в примерах или аналогичными способами. Подходящие условия проведения отдельных стадий реакции известны специалисту в данной области. Исходные вещества являются либо коммерчески доступными, или могут быть получены с использованием методик, аналогичных методикам, приведенным ниже, или с использованием способов, описанных в ссылках, приведенных ниже в тексте настоящей заявки, или в примерах, или в соответствии с методиками, известными из предшествующего уровня техники.
Получение соединений формулы I согласно настоящему изобретению можно осуществлять, используя последовательные или непрерывные методы синтеза. Синтез согласно настоящему изобретению показан на приведенных ниже схемах. Методики, необходимые для проведения реакций и очистки получаемых продуктов, известны из предшествующего уровня техники. Заместители и численные показатели, используемые далее при описании способов, имеют значения, указанные выше в тексте настоящей заявки, если не указано иное.
Соединения общей формулы I могут быть получены в соответствии со схемой 1 следующим образом.
а) Конденсация хлорзамещенных производных пиридина с пиперазинами подробно описана в литературе и соответствующие методики известны специалистам в данной области техники (условия проведения реакций описаны, например, в: Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition, Richard C. Larock. John Wiley & Sons, New York, NY. 1999). 2-Хлор-5-цианопиридин (соединение VI) или 2-хлор-5-нитропиридин (соединение IX) можно удобным образом превратить в соответствующее производное пиридина VIII или Х посредством взаимодействия с производным пиперазина VII (это соединение либо является коммерчески доступным или может быть получено согласно методикам, описанным в приведенных ссылках, или в соответствии с методиками, известными из предшествующего уровня техники; как целесообразно). Взаимодействие можно проводить в присутствии или в отсутствие растворителя и в присутствии или в отсутствие основания. Авторы настоящего изобретения обнаружили, что удобно проводить взаимодействие в среде такого растворителя, как вода и/или диметилформамид (ДМФ), и в присутствии такого основания как диизопропилэтиламин (ДИПЭА).
Схема 1
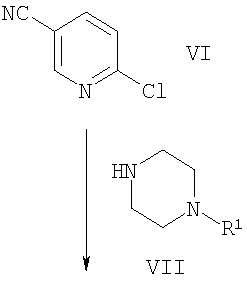

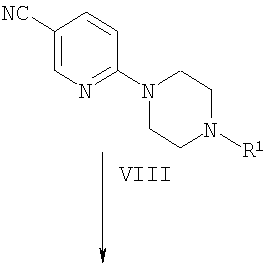
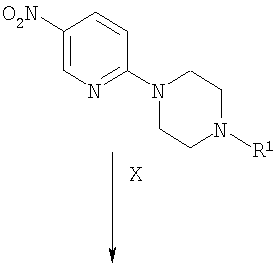
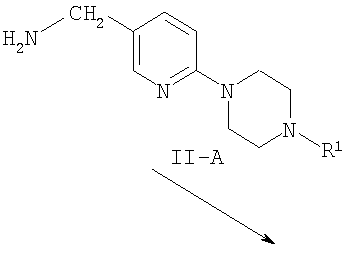
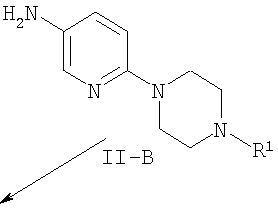
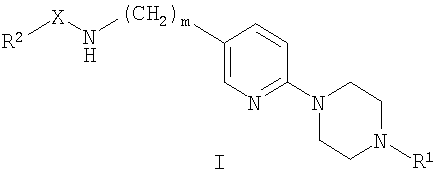
Нет особенных причин для ограничения использования растворителей различной химической природы, при условии, что они не оказывают отрицательное воздействие на ход реакции или на используемые реагенты, и при условии, что в этом растворителе растворяются реагенты, по меньшей мере, в некоторой степени. Примеры подходящих растворителей включают ДМФ, дихлорметан (ДХМ), диоксан, тетрагидрофуран (ТГФ) и подобные растворители. Нет особенных ограничений для использования оснований различной химической природы, и может быть использовано любое основание, обычно используемое для проведения реакций такого типа. Примеры таких оснований включают триэтиламин и диизопропилэтиламин, а также подобные основания. Взаимодействие можно проводить в широком диапазоне температуры, и точное значение температуры проведения реакции не является критичным для осуществления настоящего изобретения. Авторы настоящего изобретения обнаружили, что удобно проводить это взаимодействие при нагревании от температуры окружающей среды до температуры флегмообразования растворителя. Время проведения взаимодействия также может широко варьироваться, в зависимости от множества факторов, главным образом, в зависимости от температуры проведения взаимодействия и химической природы реагентов. Для получения производных пиридина VIII или Х обычно достаточен период времени от 0,5 часа до нескольких дней.
Однако в том случае, когда целевые производные пиперазина не являются легко доступными, может быть использован альтернативный способ получения производных пиридина VIII или X. Пиперазин (VII; R1=Н) подвергают взаимодействию с 2-хлор-5-цианопиридином (соединение VI) или с 2-хлор-5-нитропиридином (соединение IX) с получением при этом соответствующего производного пиридина VIII или Х (R1=Н). Взаимодействие можно проводить в присутствии или в отсутствие растворителя и в присутствии или в отсутствие основания. Авторы настоящего изобретения обнаружили, что удобно проводить это взаимодействие в среде такого растворителя как вода и/или диметилформамид (ДМФ) и в присутствии такого основания как триэтиламин. Нет особенных ограничений для использования растворителей различной химической природы, при условии, что они не оказывают отрицательное воздействие на ход реакции или на используемые реагенты, и при условии, что в этом растворителе растворяются реагенты, по меньшей мере, в некоторой степени. Примеры подходящих растворителей включают: ДМФ, дихлорметан (ДХМ), диоксан, ТГФ и подобные растворители. Нет особенных ограничений для использования на этой стадии оснований различной химической природы, и в этом случае может быть использовано любое основание, которое обычно используют для проведения реакций такого типа. Примеры таких оснований включают триэтиламин и диизопропилэтиламин, и подобные основания. Взаимодействие можно проводить в широком диапазоне температуры, и точное значение температуры проведения реакции не является критичным для осуществления настоящего изобретения. Авторы настоящего изобретения обнаружили, что удобно проводить это взаимодействие при нагревании от температуры окружающей среды до температуры флегмообразования. Время проведения взаимодействия также может широко варьироваться, в зависимости от множества факторов, главным образом в зависимости от температуры проведения взаимодействия и химической природы реагентов. Однако период времени от 0,5 часа до нескольких дней обычно достаточен для получения производных пиридина VIII или X. Затем для получения производных пиридина VIII или Х (R1≠H) промежуточное соединение помещают в условия проведения восстановительного аминирования с использованием соответствующих альдегидов или в условия проведения алкилирования с использованием соответствующих алкилирующих реагентов. Условия проведения этих реакций подробно описаны в литературе, а методики проведения взаимодействия известны специалисту в данной области техники (влияние условий проведения взаимодействия на ход реакции описано, например, в: Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition, Richard C. Larock. John Wiley & Sons, New York, NY. 1999).
б) Восстановление функциональной цианогруппы или нитрогруппы соединения VIII или X, соответственно, может быть осуществлено в различных условиях с получением при этом аминометильных производных пиридина II-A (соединения формулы II, где m означает 1) или производных аминопиридина II-B (соединения формулы II, где m означает 0). Условия проведения этих реакций подробно описаны в литературе и методики проведения взаимодействия известны специалисту в данной области техники (влияние условий проведения взаимодействия на ход реакции описано, например, в: Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition, Richard C. Larock. John Wiley & Sons, New York, NY. 1999). Авторы настоящего изобретения обнаружили, что удобно проводить гидрирование соединения VIII или соединения Х с использованием никеля Ренея или системы палладий/активированный уголь (Pd/C) в среде растворителя и в присутствии или в отсутствие кислоты. Авторы настоящего изобретения обнаружили, что удобно проводить это взаимодействие в среде такого растворителя как метанол или этилацетат. Нет особенных ограничений для использования растворителей различной химической природы, при условии, что они не оказывают отрицательное воздействие на ход реакции или на используемые реагенты, и при условии, что в этом растворителе растворяются реагенты, по меньшей мере, в некоторой степени. Примеры подходящих растворителей включают: метанол, этанол, этилацетат и подобные растворители. Нет особенных ограничений для использования на этой стадии кислоты различной химической природы, и в этом случае может быть использовано любое основание, которое обычно используют для проведения реакций такого типа. Примеры таких кислот включают уксусную кислоту или НСl, и подобные кислоты. Восстановление может быть осуществлено с использованием водорода, однако могут быть использованы и любые другие восстановители, которые применяют для проведения таких взаимодействий. Ни конкретное значение давления водорода, ни температура проведения реакции не являются критичными для осуществления этой реакции. Взаимодействие можно проводить в широком диапазоне температуры, и в широком диапазоне давления водорода. Авторы настоящего изобретения обнаружили, что удобно проводить это взаимодействие при нагревании от температуры окружающей среды до температуры флегмообразования. Время проведения взаимодействия также может широко варьироваться, в зависимости от множества факторов, главным образом от температуры проведения взаимодействия и химической природы реагентов. Однако обычно период времени от 0,5 часа до нескольких дней является достаточным для получения производных пиридина II-A (т означает 1).
в) Сульфонамиды, амиды, карбаматы и мочевины могут быть получены из соответствующих исходных соединений в соответствии с методиками, известными из предшествующего уровня техники. Превращение аминных фрагментов в соединениях II-A или II-B с получением при этом сульфонамидных, амидных, карбаматных фрагментов и фрагментов мочевины может быть выполнено согласно методикам, описанным в литературе. Например превращение аминопроизводных II с получением при этом соединений общей формулы I осуществляют посредством взаимодействия соединения II с подходящими сульфонилхлоридами или сульфамоилхлоридами (соединения формулы III) или хлорангидридами, хлорформиатами или сложными эфирами - карбонатами (соединения формулы IV, как указано выше в тексте настоящей заявки) или с изоцианатами (соединения формулы V), соответственно, в среде такого растворителя как дихлорметан и в присутствии или в отсутствие основания. Соединения формулы III, IV или V являются известными соединениями или могут быть получены согласно известным методикам. Нет особенных ограничений для использования растворителей различной химической природы, при условии, что они не оказывают отрицательное воздействие на ход реакции или на используемые реагенты, и при условии, что в этом растворителе растворяются реагенты, по меньшей мере, в некоторой степени. Примеры подходящих растворителей включают: хлороформ, или диоксан, ТГФ и подобные растворители. Нет особенных ограничений для использования на этой стадии оснований различной химической природы, и в этом случае в равной степени может быть использовано любое основание, которое обычно используют для проведения реакций такого типа. Примеры таких оснований включают триэтиламин и диизопропилэтиламин, и подобные основания. Взаимодействие можно проводить в широком диапазоне температуры, и точное значение температуры проведения реакции не является критичным для осуществления настоящего изобретения. Авторы настоящего изобретения обнаружили, что удобно проводить это взаимодействие при нагревании от температуры окружающей среды до температуры флегмообразования. Время проведения взаимодействия также может широко варьироваться, в зависимости от множества факторов, главным образом от температуры проведения и химической природы реагентов. Однако обычно период времени от 0,5 часа до нескольких дней является достаточным для получения производных пиридина I. Влияние условий проведения взаимодействия на ход реакции описано в литературе, например, в: Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition, Richard C. Larock. John Wiley & Sons, New York, NY. 1999.
Как описано выше, соединения формулы I согласно настоящему изобретению могут быть использованы в качестве лекарственных средств для лечения и/или профилактики заболеваний, которые связаны с модулированием гистаминовых H3 рецепторов. Примерами таких заболеваний являются ожирение, метаболический синдром (синдром X), неврологические заболевания, включая болезнь Альцгеймера, деменцию, связанное с возрастом расстройство памяти, умеренные нарушения познавательных способностей, когнитивные расстройства, синдром дефицита внимания и гиперактивности, эпилепсию, невропатическую боль, боль при воспалении, мигрень, болезнь Паркинсона, рассеянный склероз, нарушение мозгового кровообращения, головокружение, шизофрению, депрессию, зависимость от лекарственных средств, наркотиков и других веществ, укачивание в транспорте и расстройства сна, включая нарколепсию, а также другие заболевания, включая астму, аллергию, вызванное аллергией раздражение дыхательных путей, конгестию (застой), хроническое обструктивное заболевание легких и желудочно-кишечные заболевания. Предпочтительным является применения в качестве лекарственного средства для лечения и/или профилактики ожирения.
Таким образом, настоящее изобретение также относится к фармацевтическим композициям, включающим соединение, которое определено выше, и фармацевтически приемлемый носитель и/или вспомогательное вещество.
Кроме того, настоящее изобретение относится к соединениям как определено выше, для применения в качестве терапевтически активных соединений, в частности, в качестве терапевтически активных соединений для лечения и/или профилактики заболеваний, которые связаны с модулированием гистаминовых Н3 рецепторов. Примерами таких заболеваний являются ожирение, метаболический синдром (синдром X), неврологические заболевания, включая болезнь Альцгеймера, деменция, связанное с возрастом расстройство памяти, умеренные нарушения познавательных способностей, когнитивные расстройства, синдром дефицита внимания и гиперактивности, эпилепсия, невропатическая боль, боль при воспалении, мигрень, болезнь Паркинсона, рассеянный склероз, инсульт или внезапный приступ, головокружение, шизофрения, депрессия, зависимость от лекарственных средств, наркотиков и других веществ, укачивание в транспорте и расстройства сна, включая нарколепсию, и другие заболевания, включая астму, аллергию, вызванное аллергией раздражение дыхательных путей, конгестию (застой), хроническое обструктивное заболевание легких и желудочно-кишечные заболевания.
В соответствии с другим вариантом осуществления настоящее изобретение относится к способу лечения и/или профилактики заболеваний, которые связаны с модулированием гистаминовых Н3 рецепторов. Примерами таких заболеваний являются ожирение, метаболический синдром (синдром X), неврологические заболевания, включая болезнь Альцгеймера, деменцию, связанное с возрастом расстройство памяти, умеренные нарушения познавательных способностей, когнитивные расстройства, синдром дефицита внимания и гиперактивности, эпилепсию, невропатическую боль, боль при воспалении, мигрень, болезнь Паркинсона, рассеянный склероз, нарушение мозгового кровообращения, головокружение, шизофрения, депрессия, зависимость от лекарственных средств, наркотиков и других веществ, укачивание в транспорте и расстройства сна, включая нарколепсию, а также другие заболевания, включая астму, аллергию, вызванное аллергией раздражение дыхательных путей, конгестию (застой), хроническое обструктивное заболевание легких и желудочно-кишечные заболевания. Производным является способ лечения и/или профилактики ожирения.
Настоящее изобретение также относится к применению соединений формулы I, как определено выше, для лечения и/или профилактики заболеваний, которые связаны с модулированием гистаминовых Н3 рецепторов. Примерами таких заболеваний являются ожирение, метаболический синдром (синдром X), неврологические заболевания, включая болезнь Альцгеймера, деменцию, связанное с возрастом расстройство памяти, умеренные нарушения познавательных способностей, когнитивные расстройства, синдром дефицита внимания и гиперактивности, эпилепсию, невропатическую боль, боль при воспалении, мигрень, болезнь Паркинсона, рассеянный склероз, нарушение мозгового кровообращения, головокружение, шизофрению, депрессию, зависимость от лекарственных средств, наркотиков и других веществ, укачивание в транспорте и расстройства сна, включая нарколепсию, а также другие заболевания, включая астму, аллергию, вызванное аллергией раздражение дыхательных путей, конгестию (застой), хроническое обструктивное заболевание легких и желудочно-кишечные заболевания. Применение соединений формулы I как определено выше, для лечения и/или профилактики ожирения является предпочтительным.
Дополнительно, настоящее изобретение относится к применению соединений формулы I, как определено выше, для получения лекарственных средств для лечения и/или профилактики заболеваний, которые связаны с модулированием гистаминовых H3 рецепторов. Примерами таких заболеваний являются ожирение, метаболический синдром (синдром X), неврологические заболевания, включая болезнь Альцгеймера, деменцию, связанное с возрастом расстройство памяти, умеренные нарушения познавательных способностей, когнитивные расстройства, синдром дефицита внимания и гиперактивности, эпилепсию, невропатическую боль, боль при воспалении, мигрень, болезнь Паркинсона, рассеянный склероз, нарушение мозгового кровообращения, головокружение, шизофрению, депрессию, зависимость от лекарственных средств, наркотиков и других веществ, укачивание в транспорте и расстройства сна, включая нарколепсию, а также другие заболевания, включая астму, аллергию, вызванное аллергией раздражение дыхательных путей, конгестию (застой), хроническое обструктивное заболевание легких и желудочно-кишечные заболевания. Применение соединений формулы I как определено выше, для получения лекарственных средств для лечения и/или профилактики ожирения является предпочтительным.
Соединения формулы I и их фармацевтически приемлемые соли обладают ценными фармакологическими свойствами. В частности, было обнаружено, что соединения согласно настоящему изобретению являются успешными антагонистами и/или обратными агонистами гистаминового 3 рецептора (H3R).
Для оценки активности соединений формулы (I) проводятся следующие тесты.
Исследование связывания с 3H-(R)α-метилгистамином
Эксперименты в отношении связывания при насыщении проводят с использованием HR3-CHO мембран, приготовленных таким образом, как описано в статье: Takahashi, К, Tokita, S., Kotani, H. (2003) J. Pharmacol. Exp. Therapeutics 307, 213-218.
Соответствующее количество мембран (от 60 до 80 мкг белка на лунку) инкубируют с возрастающим количеством (концентрацией) дигидрохлорида 3H(R)α-метилгистамина (от 0,10 до 10 нМ). Неспецифическое связывание определяют, используя 200-кратный избыток холодного дигидробромида (R)α-метилгистамина (конечная концентрация 500 нМ). Инкубирование осуществляют при комнатной температуре (в планшетах с глубокими лунками при встряхивании в течение трех часов). Конечный объем в каждой лунке составляет 250 мкл. После инкубирования проводят быструю фильтрацию на фильтрах GF/B (предварительно смоченных с использованием 100 мкл 0,5% PEI в Трис 50 мМ, при встряхивании при 200 об/мин в течение двух часов). Фильтрацию выполняют, используя харвестер, и затем фильтровальные пластины промывают пять раз холодным промывочным буфером, содержащим 0,5 М NaCl. После сбора клеток планшеты высушивают при 55°С в течение 60 минут, затем добавляют сцинтилляционную жидкость (Microscint 40, по 40 микролитров в каждую лунку) и определяют величину радиоактивности планшетов, используя счетчик радиоактивности «Packard top-counter» после встряхивания в течение двух часов при 200 об/мин при комнатной температуре.
Буфер для оценки связывания: 50 мМ Трис-HCl, pH 7,4 и 5 мМ MgCl2×6Н2О, pH 7,4. Промывочный буфер: 50 мМ Трис-НСl pH 7,4 и 5 мМ MgCl2×6H2O и 0,5 М NaCl, pH 7,4.
Косвенное измерение сродства H3R обратных агонистов: выбранные соединения в повышающейся в двенадцать раз концентрации (изменяется от 10 мкМ до 0,3 нМ) тестируют в условиях конкурентного связывания, используя мембраны с линией клеток человека HR3-CHO. Соответствующее количество белка, например, приблизительно 500 сигн./мин (срm) связывания для RAMH при Kd, инкубируют в течение 1 часа при комнатной температуре при конечном объеме, составляющем 250 мкл в 96-луночных планшетах в присутствии 3Н(R)α-метилгистамина (конечная концентрация 1 нМ = Kd). Неспецифическое связывание определяют, используя 200-кратный избыток холодного дигидробромида (R)α-метилгистамина.
Все соединения тестируют для одной концентрации в двух параллельных опытах. Соединения, для которых ингибирование [3H]-RAMH составляет более чем 50%, тестируют еще раз для того, чтобы определить величину IC50 в эксперименте с серийным разбавлением. Значения Ki вычисляют по значениям IC50, используя уравнение Ченга - Прусоффа (Cheng, Y, Prusoff, WH (1973) Biochem Pharmacol 22, 3099-3108).
Соединения согласно настоящему изобретению характеризуются значениями Кi, которые находятся в интервале от приблизительно 1 нМ до приблизительно 1000 нМ, предпочтительно, в интервале от приблизительно 1 нМ до приблизительно 100 нМ, и более предпочтительно, в интервале от приблизительно 1 нМ до приблизительно 30 нМ. В приведенной ниже таблице указаны значения для некоторых соединений согласно настоящему изобретению.
Соединения формулы (I) и их фармацевтически приемлемые соли и сложные эфиры могут быть использованы в качестве лекарственных средств, например, в виде фармацевтических препаратов для энтерального, парентерального или местного ведения. Эти соединения могут быть введены, например, перорально, в частности, виде таблеток, таблеток с оболочкой, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий, ректально, например, в виде суппозиториев, парентерально, например, в виде растворов для инъекций или растворов для инфузии, или местно, например, в виде мазей, кремов или масел.
Получение фармацевтических композиций может быть осуществлено с использованием способов, которые известны любому специалисту в данной области, посредством введения описанных соединений формулы (I) и их фармацевтически приемлемых солей, необязательно в комбинации с другими терапевтически значимыми соединениями, в состав фармацевтического препарата вместе с подходящим нетоксичным, инертным, терапевтически совместимым твердым или жидким носителем и, если необходимо, с обычными фармацевтическими вспомогательными веществами.
Подходящие носители представляют собой не только неорганические носители, но также и носители органической природы. Таким образом, например, в качестве носителей для таблеток, таблеток с оболочкой, драже и твердых желатиновых капсул могут быть использованы лактоза, кукурузный крахмал или его производные, тальк, стеариновые кислоты или их соли. Подходящие носители для мягких желатиновых капсул представляют собой, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п. Однако в зависимости от природы активного соединения в случае мягких желатиновых капсул носитель может и не потребоваться. Подходящие носители для получения растворов и сиропов представляют собой, например, воду, полиолы, сахарозу, инвертированный сахар и т.п. Подходящие носители для получения растворов для инъекций представляют собой, например, воду, спирты, полиолы, глицерин и растительные масла. Подходящие носители для суппозиториев представляют собой, например, природные или отвержденные масла, воски, жиры, полутвердые и жидкие полиолы. Подходящие носители для получения препаратов для местного использования включают глицериды, полусинтетические и синтетические глицериды, гидрогенизированные масла, жидкие воски, жидкие парафины, жидкие жирные спирты, стерины, полиэтиленгликоли и производные целлюлозы.
В качестве фармацевтически пригодных вспомогательных веществ следует рассматривать обычные стабилизаторы, консерванты, смачивающие и эмульгирующие агенты, агенты, улучшающие консистенцию, агенты, улучшающие вкус и запах, соли для регулирования осмотического давления, буферные вещества, солюбилизаторы, подкрашивающие вещества, маскирующие агенты и антиоксиданты.
Дозировка соединений формулы I может варьироваться в широких пределах в зависимости от заболевания, которое подлежит контролю, возраста и конкретного состояния пациента и способа введения, и безусловно, должна соответствовать индивидуальным потребностям в каждом отдельном случае. Для взрослых пациентов следует рассматривать дневные дозировки, которые составляют приблизительно от 1 мг до приблизительно 1000 мг, в частности, приблизительно от 1 мг до приблизительно 100 мг. В зависимости от дозировки может быть удобным вводить дневную дозировку в виде нескольких единичных дозированных форм.
Удобно, когда фармацевтические композиции содержат приблизительно 0,1-500 мг, предпочтительно, 0,5-100 мг соединения формулы (I).
Приведенные ниже примеры иллюстрируют настоящее изобретение, но не ограничивают его объем.
Примеры
Промежуточное соединение 1
1-Этил-4-(5-нитропиридин-2-ил)пиперазин
Смесь 2 г (13 ммоль) 2-хлор-5-нитропиридина и 0,76 г (6 ммоль) N,N-диизопропилэтиламина в 21 мл воды и 4 мл ДМФ нагревают до 80°С. В течение 2 минут добавляют 1,73 г (15 ммоль) N-этилпиперазина и полученную смесь выдерживают дополнительно в течение часа при 80°С. Желтый осадок отфильтровывают и промывают три раза, используя 4 мл воды, после чего высушивают в течение 16 часов в вакууме, получая при этом 2,48 г (выход 83%) указанного в заголовке соединения в виде желтых кристаллов. Масс-спектр, (m/е): 237,1 (МН+; выход 100%).
Промежуточное соединение 2
6-(4-Этилпиперазин-1-ил)пиридин-3-иламин
Смесь 2,47 г (10 ммоль) 1-этил-4-(5-нитропиридин-2-ил)пиперазина и 0,247 г Pd/C (10%) в 25 мл метанола обрабатывают водородом при давлении 1 бар при комнатной температуре в течение 2 часов. После фильтрации полученную смесь упаривают досуха, получая при этом 2,12 г (выход 98%) указанного в заголовке соединения в виде бесцветного твердого вещества. Масс-спектр, (m/е): 207,3 (МН+; выход 100%).
Промежуточное соединение 3
1-Изопропил-4-(5-нитропиридин-2-ил)пиперазин
В соответствии с методикой, которая описана для синтеза промежуточного соединения 1, 1-изопропил-4-(5-нитропиридин-2-ил)пиперазин получают из 2-хлор-5-нитропиридина и N-изопропилпиперазина, получая при этом с выходом 97% указанное в заголовке соединение в виде желтых кристаллов. Масс-спектр, (m/е): 251,1 (МН+; выход 100%).
Промежуточное соединение 4
6-(4-Изопропилпиперазин-1-ил)пиридин-3-иламин
В соответствии с методикой, которая описана для синтеза промежуточного соединения 2, 6-(4-изопропилпиперазин-1-ил)пиридин-3-иламин получают из 1-изопропил-4-(5-нитропиридин-2-ил)пиперазина посредством гидрирования, получая при этом указанное в заголовке соединение, которое используют на следующей стадии без дополнительной очистки. Масс-спектр, (m/е): 221,1 (МН+; выход 100%).
Промежуточное соединение 5
1-Циклопентил-4-(5-нитропиридин-2-ил)пиперазин
В соответствии с методикой, которая описана для синтеза промежуточного соединения 1, 1-циклопентил-4-(5-нитропиридин-2-ил)пиперазин получают из 2-хлор-5-нитропиридина и N-циклопентилпиперазина, получая при этом с выходом 87% указанное в заголовке соединение в виде желтых кристаллов. Масс-спектр, (m/е): 277,1 (МН+; выход 100%).
Промежуточное соединение 6
6-(4-Циклопентилпиперазин-1-ил)пиридин-3-иламин
В соответствии с методикой, которая описана для синтеза промежуточного соединения 2, 6-(4-циклопентилпиперазин-1-ил)пиридин-3-иламин получают из 1-циклопентил-4-(5-нитропиридин-2-ил)пиперазина посредством гидрирования, получая при этом указанное в заголовке соединение с выходом 98% в виде бесцветных кристаллов. Масс-спектр, (m/е): 247,1 (МН+; выход 100%).
Промежуточное соединение 7
1-Изобутил-4-(5-нитропиридин-2-ил)пиперазин
Смесь 7 г (34 ммоль) 1-(5-нитропиридин-2-ил)пиперазина (коммерчески доступен), 3,15 г (44 ммоль) изобутиральдегида, 10,7 г (50 ммоль) трисацетоксиборгидрида натрия в 140 мл ТГФ и 3 мл уксусной кислоты перемешивают при комнатной температуре в течение 16 часов. После добавления 50 мл воды, ТГФ удаляют в вакууме. Остаток переносят в 300 мл воды и 400 мл этилацетата и подщелачивают добавлением 2 М водного раствора Nа2СО3. Затем полученную смесь экстрагируют два раза, используя каждый раз 300 мл этилацетата. Объединенные органические экстракты промывают два раза, используя каждый раз 200 мл воды, высушивают над MgSO4 и упаривают досуха. Остаток используют без дополнительной очистки для синтеза промежуточного соединения 9. Масс-спектр, (m/е): 265,0 (МН+; выход 100%).
Промежуточное соединение 8
6-(4-Изобутилпиперазин-1-ил)пиридин-3-иламин
Смесь 2,48 г 1-изобутил-4-(5-нитропиридин-2-ил)пиперазина (промежуточное соединение 7) и 0,8 г Pd/C (10%) в 30 мл метанола обрабатывают водородом при давлении 1 бар при комнатной температуре в течение 2 часов. После фильтрации полученную смесь упаривают досуха, получая при этом 2,09 г (выход 95%) указанного в заголовке соединения в виде бесцветного твердого вещества. Масс-спектр, (m/е): 235,0 (МН+; выход 100%).
Пример 1
1-[6-(4-Этилпиперазин-1-ил)пиридин-3-ил]-3-пропилмочевина
Смесь 20 мг (0,1 ммоль) 6-(4-изобутилпиперазин-1-ил)пиридин-3-иламина, 15 мг (0,15 ммоль) триэтиламина и 9,4 мг (0,11 ммоль) 1-изоцианатопропана в 1 мл ДХМ перемешивают при комнатной температуре в течение 16 часов. После упаривания остаток переносят в 1 мл смеси метанол/ацетонитрил в соотношении 1/1 и подвергают очистке обращенно-фазовой препаративной ЖХВР, элюируя градиентом ацетонитрил / вода (0,05% триэтиламин). Объединенные фракции продукта упаривают досуха, получая при этом 15,5 мг (выход 53%) указанного в заголовке соединения. Масс-спектр, (m/е): 292,3 (МН+; выход 100%).
В соответствии с методикой синтеза, описанной в примере 1, другие производные пиридина синтезируют из промежуточных соединений 2, 4, 6 и 8, соответственно, и коммерчески доступных реагентов, указанных в таблице 1. Примеры приведены в таблице 1 и включают примеры 2-60.
карбаминовой кислоты
карбаминовой кислоты
Промежуточное соединение 9
6-(4-Этилпиперазин-1-ил)никотинонитрил
Смесь 2 г (14 ммоль) 6-хлорникотинонитрила (коммерчески доступен) и 0,88 г (7 ммоль) N,N-диизопропилэтиламина в 20 мл воды и 4 мл ДМФ нагревают до 80°С. В течение 2 минут добавляют 1,98 г (17 ммоль) N-этил-пиперазина и перемешивают при 80°С в течение 1 часа. Добавляют 100 мл 1 М водного раствора Nа2СО3 и затем полученную смесь экстрагируют три раза, используя каждый раз по 100 мл этилацетата. Объединенные органические экстракты промывают два раза, используя каждый раз по 100 мл насыщенного раствора соли, и затем высушивают над MgSO4. После упаривания остаток очищают экспресс-хроматографией с использованием системы «Alox», элюируя градиентом этилацетат / гептан, получая при этом 1,4 г (выход 45%) указанного в заголовке соединения в виде светло-желтых кристаллов. Масс-спектр, (m/е): 21702 (МН+; выход 100%).
Промежуточное соединение 10
С-[6-(4-Этилпиперазин-1-ил)пиридин-3-ил]метиламин
Смесь 2 г (8 ммоль) 6-(4-этилпиперазин-1-ил)никотинонитрила, 1,3 г никеля Ренея (B113Z, Degussa) в 25 мл метанола, 15 мл этилацетата и 5 мл водного раствора аммиака (приблизительно 25%-ного) обрабатывают водородом при давлении 1 бар при 30-35°С в течение 4 часов. Полученную смесь фильтруют и затем остаток промывают три раза, используя каждый раз по 20 мл этилацетата, после чего объединенные органические экстракты упаривают досуха, получая при этом 1,83 г (выход 97%) указанного в заголовке соединения в виде белых кристаллов. Масс-спектр, (m/е): 261,1 (МH+; выход 100%).
Промежуточное соединение 11
6-(4-Циклопентилпиперазин-1-ил)никотинонитрил
Смесь 2 г (14 ммоль) 6-хлорникотинонитрила (коммерчески доступен) 2,45 г (16 ммоль) N-циклопентилпиперазина (коммерчески доступен) и 1,86 г (14 ммоль) N,N-диизопропилэтиламина в 5 мл воды и 15 мл ДМФ нагревают до 90°С в течение 24 часов. После добавления 250 мл 1 М водного раствора NaHCO3 полученную смесь экстрагируют три раза, используя каждый раз 250 мл этилацетата. Объединенные органические экстракты промывают два раза, используя каждый раз 150 мл насыщенного раствора соли, высушивают и упаривают досуха. После перекристаллизации из этилацетата получают первую партию - 2,83 г белых кристаллов. Дополнительную партию выделяют из фильтрата и суммарно получают 3,14 г (выход 85%) указанного в заголовке соединения в виде белых кристаллов. Масс-спектр, (m/е): 257,1 (МН+; выход 100%).
Промежуточное соединение 12
С-[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]метиламин
В соответствии с методикой, которая описана для синтеза промежуточного соединения 10 С-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]метиламин синтезируют из 6-(4-циклопентилпиперазин-1-ил)никотинонитрила посредством гидрирования на никеле Ренея. Получают 1,99 г (выход 98%) указанного в заголовке соединения в виде белых кристаллов. Масс-спектр, (m/е): 261,1 (МН+; выход 100%).
Пример 61
N-[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-илметил]бутирамид
Смесь 26 мг (0,1 ммоль) С-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]метиламина, 20 мг (0,2 ммоль) триэтиламина и 12 мг (0,11 ммоль) бутирил-хлорида в ДХМ перемешивают при комнатной температуре. После упаривания добавляют ацетонитрил / ДМФ и затем полученную смесь подвергают очистке обращенно-фазовой препаративной ЖХВР, элюируя градиентом ацетонитрил / вода (0,05% триэтиламина). Объединенные фракции продукта упаривают досуха, получая при этом 20,3 мг (выход 61%) указанного в заголовке соединения. Масс-спектр, (m/е): 331,3.
В соответствии с методикой синтеза, описанной в примере 73, другие производные пиридина, синтезированные из С-[6-(4-этилпиперазин-1-ил)пиридин-3-ил] метиламина и С-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]метиламина и соответствующих коммерчески доступных реагентов, указаны в таблице 2. Эти примеры приведены в таблице 2 и включают примеры 62-90.
метансульфонамид
пиридин-3-илметил]метансульфонамид
сульфонамид
Пример 91
[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]амид 4-метилпиперидин-1-карбоновой кислоты
Смесь 29 мг (0,08 ммоль) фенилового эфира [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты (промежуточное соединение, полученное из промежуточного соединения 6 и фенилхлорформиата) и 12 мг (0,12 ммоль) 4-метилпиперидина (коммерчески доступен) в 1 мл ДХМ и 0,1 мл ДМФ перемешивают при комнатной температуре в течение 16 часов. После упаривания остаток переносят в смесь метанол/ДМФ и подвергают очистке обращенно-фазовой препаративной ЖХВР, элюируя градиентом ацетонитрил / вода (0,05% триэтиламин). Объединенные фракции продукта упаривают досуха, получая при этом 13,6 мг (выход 46%) указанного в заголовке соединения. Масс-спектр, (m/е): 372,3 (МН+; выход 100%).
Пример 92
[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил] амид 2,6-диметил-пиперидин-1-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91, [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид 2,6-диметилпиперидин-1-карбоновой кислоты синтезируют из промежуточного соединения 6 и 2,6-диметилпиперидина (коммерчески доступен). Масс-спектр, (m/е): 372,3 (МН+; выход 100%).
Пример 93
[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]амид 4-трифторметилпиперидин-1-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91,
[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]амид 4-трифтор-метилпиперидин-1-карбоновой кислоты синтезируют из промежуточного соединения 6 и 4-трифторметилпиперидина (коммерчески доступен). Масс-спектр, (m/е): 426,3 (МН+; выход 100%).
Пример 94
Этиловый эфир 1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илкарбамоил]пиперидин-4-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91, этиловый эфир 1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илкарбамоил]пиперидин-4-карбоновой кислоты синтезируют из промежуточного соединения 6 и этилового эфира пиперидин-4-карбоновой кислоты (коммерчески доступен). Масс-спектр, (m/е): 430,4 (МН+; выход 100%).
Пример 95
[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]амид октагидрохинолин-1-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91, октагидрохинолин-1-карбоновой кислоты [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид синтезируют из промежуточного соединения 6 и 2,6-диметилпиперидина (коммерчески доступен). Масс-спектр, (m/е): 412,5 (МН+; выход 100%).
Пример 96
[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]амид октагидроизохинолин-2-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91, [6-(4-цикло-пентилпиперазин-1-ил)пиридин-3-ил]амид октагидроизохинолин-2-карбоновой кислоты синтезируют из промежуточного соединения 6 и октагидроизохинолина (коммерчески доступен). Масс-спектр, (m/е): 412,5 (МН+; выход 100%).
Пример 97
[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]амид2-трифтор-метилпирролидин-1-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91, [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил] амид 2-трифторметил-пирролидин-1-карбоновой кислоты синтезируют из промежуточного соединения 6 и 2-трифторметилпирролидина (коммерчески доступен). Масс-спектр, (m/е): 412,4 (МН+; выход 100%).
Пример 98
2-Изопропилпирролидин-1-карбоновой кислоты [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид
В соответствии с методикой синтеза, описанной в примере 91, [6-(4-цикло-пентилпиперазин-1-ил)пиридин-3-ил]амид 2-изопропилпирролидин-1-карбоновой кислоты синтезируют из промежуточного соединения 6 и 2-изопропилпирролидина (коммерчески доступен). Масс-спектр, (m/е): 386,3 (МН+; выход 100%).
Пример 99
1,3-Дигидроизоиндол-2-карбоновой кислоты [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид
В соответствии с методикой синтеза, описанной в примере 91, [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид 1,3-дигидроизоиндол-2-карбоновой кислоты синтезируют из промежуточного соединения 6 и 1,3-дигидроизоиндола (коммерчески доступен). Масс-спектр, (m/е): 392,2 (МН+; выход 100%).
Пример 100
3-[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]-1-изопропил-1-(2-метоксиэтил)мочевина
В соответствии с методикой синтеза, описанной в примере 91, 3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-1-изопропил-1-(2-метоксиэтил)мочевину синтезируют из промежуточного соединения 6 и изопропил-2-метоксиэтиламина (коммерчески доступен). Масс-спектр, (m/е):
390,4(МН+; выход 100%).
Пример 101
[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]амид азепан-1-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91, [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид азепан-1-карбоновой кислоты синтезируют из промежуточного соединения 6 и азепина (коммерчески доступен). Масс-спектр, (m/е): 372,3 (МН+; выход 100%).
Пример 102
3-[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]-1-этил-1-фенилмочевина
В соответствии с методикой синтеза, описанной в примере 91, 3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-1-этил-1-фенилмочевину синтезируют из промежуточного соединения 6 и этилфениламина (коммерчески доступен). Масс-спектр, (m/е): 394,4 (МН+; выход 100%).
Пример 103
3-[6-(4-Циклопентилпиперазин-1-ил)пиридин-3-ил]-1-(4-метокси-фенил)-1-метилмочевина
В соответствии с методикой синтеза, описанной в примере 91, 3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-1-(4-метокси-фенил)-1-метилмочевину синтезируют из промежуточного соединения 6 и (4-метоксифенил)метиламина (коммерчески доступен). Масс-спектр, (m/е): 410,4 (МН+; выход 100%).
Пример 104
[6-(4-Этилпиперазин-1-ил)пиридин-3-ил]амид 3,4-дигидро-2N-хинолин-1-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91, [6-(4-этилпиперазин-1-ил)пиридин-3-ил]амид 3,4-дигидро-2N-хинолин-1-карбоновой кислоты синтезируют из промежуточного соединения 2 и 3,4-дигидро-2N-хинолина (коммерчески доступен). Масс-спектр, (m/е): 366,3 (МН+; выход 100%).
Пример 105
[6-(4-Изопропилпиперазин-1-ил)пиридин-3-ил]амид 3,4-дигидро-2N-хинолин-1-карбоновой кислоты
В соответствии с методикой синтеза, описанной в примере 91, [6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]амид 3,4-дигидро-2N-хинолин-1-карбоновой кислоты синтезируют из промежуточного соединения 4 и 3,4-дигидро-2N-хинолина (коммерчески доступен). Масс-спектр, (m/е): 380,3 (МН+; выход 100%).
Пример А
Таблетки с пленочным покрытием, содержащие указанные ниже ингредиенты, могут быть получены общепринятым способом:
Активный ингредиент просеивают и смешивают с микрокристаллической целлюлозой, затем полученную смесь гранулируют с использованием раствора поливинилпирролидона в воде. Полученные гранулы смешивают с натриевой солью гликолята крахмала и стеаратом магния, затем прессуют, получая при этом ядра таблеток массой 120 или 350 мг соответственно. На ядра таблеток наносят покрытие, используя водный раствор / суспензию вышеуказанных компонентов для получения пленочной оболочки.
Пример Б
Капсулы, содержащие приведенные ниже ингредиенты, могут быть получены общепринятым способом:
Компоненты просеивают, смешивают и помещают в капсулы размера 2.
Пример В
Приготавливают растворы для инъекций следующего состава:
Пример Г
Мягкие желатиновые капсулы
Активный ингредиент растворяют в теплой размягченной массе, включающей остальные ингредиенты, после чего полученной смесью заполняют мягкие желатиновые капсулы соответствующего размера. Заполненные желатиновые капсулы используют для проведения лечения в соответствии с общепринятыми методиками.
Пример Д
Пакетики (саше), содержащие указанные ниже ингредиенты, могут быть получены общепринятым способом.
Активный ингредиент смешивают с лактозой, микрокристаллической целлюлозой и натриевой солью карбоксиметилцеллюлозы и затем подвергают гранулированию, используя смесь поливинилпирролидона и воды. Полученный гранулированный продукт смешивают со стеаратом магния и добавками, придающими вкус и запах, после чего помещают в пакетики (саше).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНИЛПИРИДИНА В КАЧЕСТВЕ АГЕНТОВ ПРОТИВ ОЖИРЕНИЯ | 2005 |
|
RU2386618C2 |
| 2-ЦИАНО-4-АМИНОПИРИМИДИНОВЫЕ СОЕДИНЕНИЯ С ИНГИБИРУЮЩИМ ДЕЙСТВИЕМ НА КАТЕПСИН К, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2002 |
|
RU2326119C2 |
| СУЛЬФОНАМИДТИАЗОЛПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ КАК АКТИВАТОРЫ ГЛЮКОКИНАЗЫ, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА ТИПА 2 | 2005 |
|
RU2412192C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2006 |
|
RU2368602C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2005 |
|
RU2401265C2 |
| ПРОИЗВОДНОЕ ПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРА PI3K И ЕГО ПРИМЕНЕНИЕ | 2007 |
|
RU2448109C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ АНТАГОНИСТОВ CCR2B | 2005 |
|
RU2423349C2 |
| ПРОИЗВОДНЫЕ НАФТАЛИНА, ПРИГОДНЫЕ В КАЧЕСТВЕ ЛИГАНДОВ РЕЦЕПТОРОВ 3 ГИСТАМИНА | 2005 |
|
RU2387638C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНТИРОЗИНКИНАЗЫ | 2006 |
|
RU2386630C2 |
| ПРОИЗВОДНЫЕ N-ФЕНИЛ-2-ПИРИМИДИНАМИНА | 2003 |
|
RU2370493C2 |
Изобретение относится к новым соединениям формулы I: 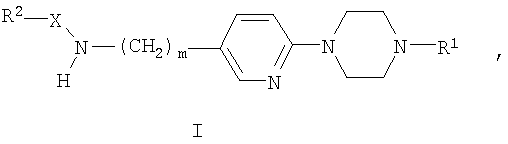 где R1 представляет собой низший алкил или С3-С7-циклоалкил; Х представляет собой C(O) или SO2; m означает 0 или 1; R2 выбирают из группы, состоящей из низшего алкила, низшего галогеналкила, низшего алкоксиалкила, незамещенного C3-C7-циклоалкила, низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, незамещенного пиридила или пиридила, моно- или дизамещенного низшим алкилом, галогеном или низшим галогеналкилом, и -NR3R4, или в том случае, когда Х представляет собой C(O),
где R1 представляет собой низший алкил или С3-С7-циклоалкил; Х представляет собой C(O) или SO2; m означает 0 или 1; R2 выбирают из группы, состоящей из низшего алкила, низшего галогеналкила, низшего алкоксиалкила, незамещенного C3-C7-циклоалкила, низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, незамещенного пиридила или пиридила, моно- или дизамещенного низшим алкилом, галогеном или низшим галогеналкилом, и -NR3R4, или в том случае, когда Х представляет собой C(O),
R2 также может представлять собой низший алкокси или низший алкоксиалкокси, или в том случае, когда m означает 1, R2 также может представлять собой незамещенный фенил или фенил, моно- или дизамещенный низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, R3 представляет собой водород или низший алкил; R4 выбирают из группы, состоящей из низшего алкила, С3-С7-циклоалкила, С3-С7-циклоалкила, замещенного фенилом, низшего С3-С7-циклоалкилалкила, незамещенного фенила или фенила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом; или R3 и R4 вместе с атомом азота, к которому они присоединены, образуют 4-, 5-, 6- или 7-членную гетероциклическую кольцевую систему, необязательно содержащую еще один гетероатом, выбранный из азота, причем указанная гетероциклическая кольцевая система является незамещенной или замещенной одной, двумя или тремя группами, независимо выбранными из низшего алкила, галогена и галогеналкила; и фармацевтически приемлемым солям этих соединений; за исключением 2,2-диметил-N-[6-(4-метилпиперазин-1-ил)пиридин-3-ил]
пропионамида. Кроме того, изобретение относится к фармацевтической композиции для лечения заболеваний, которые связаны с модулированием гистаминовых НЗ рецепторов, на основе соединений формулы I. Технический результат: получены и описаны новые соединения, которые могут быть использованы для лечения и/или профилактики заболеваний, которые связаны с модулированием гистаминовых Н3 рецепторов. 2 н. и 19 з.п., ф-лы, 2 табл.
1. Соединения общей формулы:
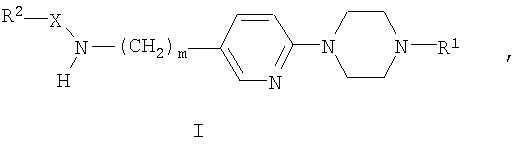
где R1 представляет собой низший алкил или C3-C7-циклоалкил;
Х представляет собой C(O) или SO2;
m означает 0 или 1;
R2 выбирают из группы, состоящей из низшего алкила, низшего галогеналкила, низшего алкоксиалкила,
незамещенного C3-C7-циклоалкила,
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, незамещенного пиридила или пиридила, моно- или дизамещенного низшим алкилом, галогеном или низшим галогеналкилом, и -NR3R4,
или в том случае, когда Х представляет собой C(O), R2 также может представлять собой низший алкокси или низший алкоксиалкокси,
или в том случае, когда m означает 1, R2 также может представлять собой незамещенный фенил или фенил, моно- или дизамещенный низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом,
R3 представляет собой водород или низший алкил;
R4 выбирают из группы, состоящей из низшего алкила,
C3-C7-циклоалкила,
C3-C7-циклоалкила, замещенного фенилом,
низшего C3-C7-циклоалкилалкила,
незамещенного фенила или фенила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом; или
R3 и R4 вместе с атомом азота, к которому они присоединены, образуют 4-, 5-, 6- или 7-членную гетероциклическую кольцевую систему, необязательно содержащую еще один гетероатом, выбранный из азота, причем указанная гетероциклическая кольцевая система является незамещенной или замещенной одной, двумя или тремя группами,
независимо выбранными из низшего алкила, галогена и галогеналкила;
и фармацевтически приемлемые соли этих соединений;
за исключением 2,2-диметил-N-[6-(4-метилпиперазин-1-ил)пиридин-3-ил]пропионамида.
2. Соединения формулы I по п.1, где R1 представляет собой C3-С7-циклоалкил.
3. Соединения формулы I по п.1 или 2, где R1 представляет собой этил или изопропил.
4. Соединения формулы I по п.1 или 2, где m означает 1.
5. Соединения формулы I по п.1 или 2, где m означает 0.
6. Соединения формулы I по п.1 или 2, где R2 выбирают из группы, состоящей из:
низшего алкила, низшего галогеналкила, низшего алкоксиалкила,
незамещенного C3-C7-циклоалкила,
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом,
незамещенного пиридила или пиридила, моно- или дизамещенного низшим алкилом, галогеном или низшим галогеналкилом, и -NR3R4,
или в том случае, когда Х представляет собой C(O), R2 также может представлять собой низший алкокси или низший алкоксиалкокси.
7. Соединения формулы I по п.1 или 2, где R2 выбирают из группы, состоящей из низшего алкила и C3-C7-циклоалкила.
8. Соединения формулы I по п.1 или 2, где R2 представляет собой низший фенилалкил, где фенил является незамещенным или моно- или дизамещенным низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом.
9. Соединения формулы I по п.1 или 2, где R2 представляет собой -NR3R4, а R3 и R4 являются такими, как указано в п.1.
10. Соединения формулы I по п.1 или 2, где
R3 представляет собой водород или низший алкил;
R4 выбирают из группы, состоящей из низшего алкила,
C3-C7-циклоалкила,
C3-C7-циклоалкила, замещенного фенилом,
низшего C3-C7-циклоалкилалкила,
незамещенного фенила или фенила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и
низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом; или
R3 и R4 вместе с атомом азота, к которому они присоединены, образуют 4-, 5-, 6- или 7-членную гетероциклическую кольцевую систему, необязательно содержащую еще один гетероатом, выбранный из азота, причем указанная гетероциклическая кольцевая система является незамещенной или замещенной одной, двумя или тремя группами, независимо выбранными из низшего алкила, галогена и галогеналкила.
11. Соединения формулы I по п.9, где R3 и R4 представляют собой низший алкил.
12. Соединения формулы I по п.9, где R3 представляет собой водород и R4 выбирают из группы, состоящей из:
низшего алкила,
C3-C7-циклоалкила,
C3-C7-циклоалкила, замещенного фенилом,
низшего C3-C7-циклоалкилалкила,
незамещенного фенила или фенила, моно- или дизамещенного низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом, и низшего фенилалкила, где фенил является незамещенным или моно- или дизамещенным низшим алкилом.
13. Соединения формулы I по п.9, где R3 представляет собой водород и R4 представляет собой низший фенилалкил, в котором фенил является незамещенным или моно- или дизамещенным низшим алкилом.
14. Соединения формулы I по п.1 или 2, где m означает 1, и R2 представляет собой незамещенный фенил или фенил, моно- или дизамещенный низшим алкилом, низшим алкокси, галогеном или низшим галогеналкилом.
15. Соединения формулы I по п.1 или 2, где Х представляет собой SO2.
16. Соединения формулы I по п.1 или 2, где Х представляет собой C(O).
17. Соединения формулы I по п.1 или 2, где Х представляет собой C(O) и R2 представляет собой -NR3R4.
18. Соединения формулы I по п.1, которые выбирают из группы, состоящей из следующих соединений:
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-пропилмочевина,
1-циклогексил-3-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-бензил-3-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-n-толилмочевина,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-((1R,2S)-2-фенил-циклопропил)мочевина,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-(3-метоксифенил)мочевина,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-3-(4-фторфенил)мочевина,
1-циклогексил-3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-бензил-3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-3-(4-метилбензил)мочевина,
1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-3-((1R,2S)-2-фенил-циклопропил)мочевина,
1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-3-(4-фторфенил)мочевина,
1-циклогексил-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-фенилмочевина,
1-бензил-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-о-толилмочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-м-толилмочевина,
1-(2-хлорфенил)-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-(4-метилбензил)мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-((1R,2S)-2-фенил-циклопропил)мочевина,
1-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-3-(3-метокси-фенил)мочевина,
1-(4-фторфенил)-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил] мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-пропилмочевина,
1-циклогексил-3-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-бензил-3-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-м-толилмочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-п-толилмочевина,
1-(2-хлорфенил)-3-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-(4-метилбензил)мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-((1R,2S)-2-фенил-циклопропил)мочевина,
1-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]-3-(3-метокси-фенил)мочевина,
1-(4-фторфенил)-3-[6-(4-изобутилпиперазин-1-ил)пиридин-3-ил]мочевина,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]диметиламиносульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]диметиламино-сульфонамид,
N-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]диметиламино-сульфонамид,
[6-(4-этилпиперазин-1-ил)пиридин-3-ил]амид циклогексанкарбоновой кислоты,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-2-фенилацетамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-2-(4-фторфенил)ацетамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]-2-(3-метокси-фенил)ацетамид,
2-(3,4-диметокси-фенил)-N-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]ацетамид,
2-метоксиэтиловый эфир [6-(4-этилпиперазин-1-ил)пиридин-3-ил]карбаминовой кислоты,
изобутиловый эфир [6-(4-этилпиперазин-1-ил)пиридин-3-ил]карбаминовой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид циклопропанкарбоновой кислоты,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]бутирамид,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид циклобутанкарбоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амид циклопентанкарбоновой кислоты,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-этилбутирамид,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]амидциклогексанкарбоновой кислоты,
2-хлор-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]никотинамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-фенилацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-(4-фторфенил)-ацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-(3-метокси-фенил)ацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-(3,4-диметокси-фенил)ацетамид,
этиловый эфир [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
2-метоксиэтиловый эфир [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
изобутиловый эфир [6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]амид циклогексанкарбоновой кислоты,
2-(3,4-диметоксифенил)-N-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]ацетамид,
этиловый эфир [6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
изобутиловый эфир [6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]-карбаминовой кислоты,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]бутирамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-3-метокси-бензамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-2-фенилацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-2-(4-фтор-фенил)ацетамид,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]амид этансульфоновой кислоты,
[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]амид пропан-1-сульфоновой кислоты,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-диметиламиносульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-бензолсульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-С-фенил-метансульфонамид,
С-(4-хлорфенил)-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]метансульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-2-фтор-бензолсульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-3-фтор-бензолсульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-4-фтор-бензолсульфонамид,
2-хлор-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-бензолсульфонамид,
4-хлор-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-бензолсульфонамид,
1-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-3-(4-фтор-бензил)мочевина,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-3-метоксибензамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-2-фенилацетамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-2-(4-фторфенил)ацетамид,
[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]амид этансульфоновой кислоты,
[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]амид пропан-1-сульфоновой кислоты,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]диметиламино-сульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]бензолсульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-С-фенил-метан-сульфонамид,
С-(4-хлорфенил)-N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-метансульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-2-фтор-бензол-сульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-3-фтор-бензолсульфонамид,
N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]-4-фтор-бензолсульфонамид,
2-хлор-N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]бензолсульфонамид,
4-хлор-N-[6-(4-этилпиперазин-1-ил)пиридин-3-илметил]бензолсульфонамид, и фармацевтически приемлемые соли этих соединений.
19. Соединения формулы I по п.1, которые выбирают из группы, состоящей из следующих соединений:
1-бензил-3-[6-(4-этилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-бензил-3-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]мочевина,
1-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-3-(4-метилбензил)мочевина,
1-бензил-3-[6-(4-изопропилпиперазин-1-ил)пиридин-3-ил]мочевина,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-диметиламиносульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-ил]-2-(3,4-диметокси-фенил)ацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-3-метокси-бензамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-2-фенилацетамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]диметиламиносульфонамид,
N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]-С-фенил-метансульфонамид,
С-(4-хлорфенил)-N-[6-(4-циклопентилпиперазин-1-ил)пиридин-3-илметил]метансульфонамид,
и фармацевтически приемлемые соли этих соединений.
20. Соединения по п.1 или 2, предназначенные для использования в качестве терапевтически активных соединений для лечения и/или профилактики заболеваний, которые связаны с модулированием гистаминовых Н3 рецепторов.
21. Фармацевтическая композиция для лечения и/или профилактики заболеваний, которые связаны с модулированием гистаминовых Н3 рецепторов, включающая соединение по любому из пп.1-19 и фармацевтически приемлемый носитель и/или вспомогательное вещество.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| RU 2000103449 A, 10.12.2001. | |||
Авторы
Даты
2010-05-20—Публикация
2005-11-24—Подача