Область, к которой относится изобретение
Данное изобретение относится к антагонисту рецепторов мутеина IL-4, присоединенному к небелковому полимеру, такому как полиэтиленгликоль. Кроме того, в нем предусмотрены составы, дозированные формы и способы их введения для терапевтических целей. Эти модифицированные антагонисты рецептора мутеина IL-4 и композиции и способы, их использующие, пригодны для лечения индивидуумов, страдающих от тяжелой астмы, хронического обструктивного легочного заболевания и связанных с ними состояний легких.
Предпосылки создания изобретения
Астма характеризуется изменчивой, обратимой обструкцией дыхательных путей и гиперответом дыхательных путей (AHR), связанными с инфильтрацией слизистой оболочки бронхов активированными Т-лимфоцитами (Т-клетками) и эозинофилами. Эти клетки вместе с резидентными тучными клетками дыхательных путей секретируют различные цитокины и медиаторы, которые играют главную роль в патогенезе болезни. Клетки CD4+Th2 за счет выделения специфических цитокинов (IL-4, IL-5, IL-9 и IL-13) управляют развитием болезни. В частности, Th2 цитокины, IL-4 и IL-13, как полагают, являются главными в развитии и сохранении воспаления дыхательных путей и гиперответа дыхательных путей.
В ряде in vivo исследований также поддерживается мнение об основной роли IL-4 и IL-13 в патогенезе астмы. При использовании животных с дефицитом цитокина или реагентов, которые нейтрализуют функцию или IL-4, или IL-13, наблюдается важная роль этих цитокинов в регулировании первичного и вторичного иммунного ответа, приводящего к воспалению дыхательных путей и гиперответу дыхательных путей (3, 4). Взятые вместе, эти данные позволяют предположить, что IL-4 и IL-13 оба могут играть перекрывающиеся и независимые роли в аллергическом ответе дыхательных путей и что нацеливание на оба цитокина может иметь значительное дополнительное преимущество по сравнению с нацеливанием на любой один цитокин.
Антагонисты IL-4 описаны в литературе. Мутанты IL-4, которые действуют как антагонисты, включают мутеин IL-4, IL-4/Y124D (Kruse N., Tony H.P., Sebald W., Conversion of human interleukin-4 into a high affinity antagonist by a single amino acid replacement, Embo J. 11:3237-41, 1992) и двойной мутеин IL-4 [R121D/Y124D] Tony H. et al., Design of Human Inerieukin-4 Antagonist in Inhibiting hierleukin-4-dependent and Inerleukin-13-dependent responses in T-cells and B-cells with high efficiency, Eur. J. Biochem. 225: 659-664 (1994)). Единичный мутеин представляет собой тирозин, замещенный аспартовой кислотой в положении 124 в D-спирали. Двойной мутеин представляет собой аргинин, замещенный аспартовой кислотой в положении 121, и тирозин, замещенный аспартовой кислотой в положении 124 в D-спирали. Изменения в этой части D-спирали хорошо коррелируются с изменениями во взаимодействиях на втором участке связывания.
Варианты мутантов IL-4, проявляющие агонизм или антагонизм IL-4 дикого типа, могут быть полезными при лечении состояний, связанных с одним из плейотропных эффектов IL-4. Например, антагонисты IL-4 будут пригодны для лечения состояний, обострившихся при продуцировании IL-4, таких как астма, аллергия или другие воспалительные состояния-ответы. Агонисты IL-4 могут быть полезны для лечения состояний, при которых наличие IL-4 связано с улучшением состояния или ослаблением болезни, например, аутоиммунных болезней, таких как ревматоидный артрит, рассеянный склероз, инсулинзависимый сахарный диабет и т.д. Эти аутоиммунные болезни характеризуются поляризацией при продуцировании популяций Т-клеток-помощников (хелперов), типов 1 и 2 (Th1, Th2). Незараженные СD4+Т-клетки дифференцируют на субпопуляции Th1 или Th2 в зависимости от цитокина, содержащегося во время стимулирования. Агонист IL-4 будет идеально сдвигать продуцирование в сторону Т-клеток-хелперов, а именно, в сторону образования Th2, оказывая тем самым терапевтическое действие.
В заявке PCT/US93/03613 описан вариант IL-4, содержащий Phe-Leu или Туг-Leu последовательность в альфа-области спирали и отрицательно заряженную аминокислоту среди двух аминокислот в 3'-5'-направлении или 5'-3'-направлении от последовательности Phe-Leu или Tyr-Leu, причем этот вариант имеет повышенное сродство к рецептору IL-4 благодаря нейтральной аминокислоте, замещающей отрицательно заряженную аминокислоту. В этой заявке указано также, что специфическое замещение Trp-Leu или Phe-Leu в а-спирали IL-4 в 2-остатках отрицательно заряженного остатка приводит к повышенному сродству. Вариант является IL-4 слитым белком (с дифтерийным токсином).
Рекомбинантный мутеин (IL-4RA), являющийся производным IL-4 человека, мутированным в двух положениях его аминокислотной последовательности, описан в патентах США 6028176 и 6313272. IL-4RA связывается с высоким сродством с альфа-цепью рецептора IL-4 человека, важным функциональным сигнальным компонентом обоих комплексов рецепторов IL-4 и IL-13. Этот мутеин не обладает активностью агониста и действует как сильнодействующий конкурентный антагонист рецепторов IL-4 и IL-13 in vitro (см. патенты США 6028176 и 613272). Значительный недостаток применения IL-4RA состоит в его довольно коротком периоде полураспада (примерно 3-6 часов). Фармакокинетическое/фармакодинамическое моделирование IL-4RA в модели астмы у приматов показывает, что эффективная средняя стабильная концентрация при достижении оптимального терапевтического эффекта составляет около 60 нг/мл.
Одним из подходов к преодолению короткого периода полураспада является частое введение мутеина IL-4RA пациенту, однако, частое введение (обычно путем инъекции или интубации в трахею) создает значительные препятствия переносимости терапии пациентом и проведению терапии в клинических условиях.
Сущность изобретения
Изобретение предусматривает мутеины IL-4RA с более длинным периодом полураспада, чем у ранее описанных мутеинов. Данное изобретение также предусматривает реагенты и способы ингибирования иммунных ответов, опосредованных IL-4 и IL-13. Этот и другие аспекты настоящего изобретения предусмотрены в одном или нескольких вариантах изобретения, указанных ниже.
Согласно одному варианту данное изобретение предусматривает очищенный препарат модифицированного антагониста рецептора мутеина IL-4, включающий антагонист рецептора мутеина IL-4, присоединенный к небелковому полимеру, выбранному из группы, состоящей из полиэтиленгликоля, полипропиленгликоля и полиоксиалкиленов. Согласно одному аспекту изобретения очищенный препарат содержит модифицированный полипептидный антагонист рецептора мутеина IL-4, который кодирован нуклеотидной последовательностью, указанной далее в SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7 или SEQ ID NO:8. Согласно другому аспекту полипептид включает аминокислотную последовательность, указанную ниже в SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15 или SEQ ID NO:16.
Согласно одному варианту модифицированный полипептидный антагонист рецептора мутеина IL-4 может быть сопряжен с небелковым полимером в аминокислотном остатке в положении 28, 36, 37, 38, 104, 105 или 106 IL-4. Эти положения пронумерованы согласно аминокислотной последовательности IL-4 дикого типа (то есть интерлейкина-4 человека). Согласно одному аспекту этого варианта аминокислотный остаток в положениях 28, 36, 37, 38, 104, 105 или 106 представляет собой цистеин.
Согласно еще одному варианту модифицированный антагонист рецептора мутеина по изобретению связывается с альфа-цепью рецептора IL-4 с Кd около 0,1 нМ - 10 мкМ, примерно 0,5 нМ - 1 мкМ или примерно 1,0 нМ - 100 нМ.
Согласно другому варианту модифицированный антагонист рецептора мутеина IL-4 ингибирует пролиферативный ответ TF-1-клеток на IL-4 с IC50, равной примерно 0,1 нМ - 10 мкМ, примерно 0,5 нМ - 1 мкМ или примерно 1,0 нМ - 100 нМ.
Согласно еще одному варианту модифицированный антагонист рецептора мутеина IL-4 ингибирует пролиферативный ответ TF-1-клеток на IL-13 с IС50, выбранной из интервалов примерно 0,1 нМ - 10 мкМ, примерно 0,5 нМ - 1 мкМ или примерно 1,0 нМ - 100 нМ.
Согласно дальнейшему варианту модифицированный антагонист рецептора мутеина IL-4 ингибирует пролиферативный ответ В-клеток человека на IL-4 с IС50, выбранной из интервалов примерно 0,1 нМ - 10 мкМ, примерно 0,5 нМ - 1 мкМ или примерно 1,0 нМ - 100 нМ.
Согласно еще одному варианту модифицированный антагонист рецептора мутеина IL-4 ингибирует пролиферативный ответ Т-клеток человека на IL-4 с IС50, выбранной из интервалов примерно 0,1 нМ - 10 мкМ, примерно 0,5 нМ - 1 мкМ или примерно 1,0 нМ - 100 нМ.
Согласно еще одному варианту модифицированный антагонист рецептора мутеина IL-4 по изобретению имеет период полураспада в плазме, который, по меньшей мере, в 2-10 раз больше периода полураспада в плазме не модифицированного антагониста рецептора мутеина IL-4.
Данное изобретение предусматривает также фармацевтические композиции, содержащие: (а) модифицированный антагонист рецептора мутеина IL-4, который связывается с рецептором IL-4 человека, и (б) фармацевтически приемлемый носитель. Изобретение также предусматривает очищенный полинуклеотид, содержащий (а) нуклеотидную последовательность, показанную ниже в SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7 или SEQ ID NO:8, или (б) нуклеотидную последовательность, кодирующую полипептид, содержащий аминокислотную последовательность, показанную ниже в SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15 или SEQ ID NO:16.
Настоящее изобретение предусматривает также векторы экспрессии, содержащие полинуклеотид по изобретению и клетки-хозяева, содержащие вектор экспрессии по изобретению.
Кроме того, данное изобретение предусматривает способы получения модифицированного антагониста рецептора мутеина IL-4, включающий стадии: (а) культивирования клетки-хозяина, описанной выше, в условиях, при которых происходит экспрессия антагониста, и (б) очистки антагониста от культуры клеток-хозяев. Согласно конкретному аспекту антагонист, полученный способом по изобретению, может ингибировать активность, опосредованную IL-4 и IL-13, и сочетается с небелковым полимером, выбранным из группы, состоящей из полиэтиленгликоля, полипропиленгликоля и полиоксиалкиленов.
Изобретение предусматривает также способы лечения нарушения у людей, связанного с повышенной активностью IL-4 и IL-13, включающие стадии: (а) подбора человека с состоянием, при котором увеличена активность IL-4 и IL-13, и (б) введения этому человеку эффективного количества модифицированного антагониста рецептора мутеина IL-4 по изобретению или фармацевтической композиции по изобретению. Согласно одному аспекту это нарушение представляет собой астму, хроническое обструктивное легочное заболевание (такое как эмфизема или хронический бронхит) или связанные с этим легочные нарушения.
Данное изобретение предусматривает также способ получения модифицированного антагониста рецептора мутеина IL-4 в активной форме, антагонисты, полученные этим способом, композиции, содержащие такие антагонисты, и способ лечения расстройств у людей, включающий введение таких антагонистов и фармацевтических композиций, содержащих такие антагонисты. Этот способ включает стадии: (а) культивирования клетки-хозяина, как описано выше, в условиях, при которых происходит экспрессия антагониста; (б) осуществления повторного складывания антагониста в присутствии дитиотреитола и (в) очистки антагониста от культуры клетки-хозяина. Согласно одному варианту способ включает также стадии: (г) сочетания антагониста с небелковым полимером и (д) очистки антагониста, присоединенного к небелковому полимеру.
Конкретные предпочтительные варианты данного изобретения станут очевидны из нижеследующего более подробного описания некоторых аспектов и из формулы изобретения.
На чертеже показана схема протекания реакции пэгилирования.
Подробное описание изобретения
Данное изобретение относится к модифицированным антагонистам рецептора мутеина IL-4, содержащим рецептор мутеина IL-4, присоединенный к небелковому полимеру, предпочтительно, к молекуле полиэтиленгликоля.
Если иное не требуется по контексту, термины в единственном числе включают множественное число и термины во множественном числе включают единственное число.
Определения
Термины «полинуклеотид» или «последовательность нуклеиновой кислоты» или «молекула нуклеиновой кислоты» относятся к последовательности ДНК или РНК. Эти термины охватывают молекулы, образовавшиеся из любого из известных основных аналогов ДНК или РНК, таких как, без ограничения, 4-ацетилцистеин, 8-гидрокси-N6-метиладенозин, азиридинилцитозин, псевдоизоцитозин, 5-(карбоксигидроксиметил)урацил, 5-фторурацил, 5-карбоксиметиламинометил-2-тиоурацил, 5-карбоксиметиламинометилурацил, дигидроурацил, инозин, N6-изо-пентениладенин, 1-метиладенин, 1-метилпсевдоурацил, 1-метилгуанин, 1-метил-инозин, 2,2-диметилгуанин, 2-метиладенил, 2-метилгуанин, 3-метилцитозин, 5-метилцитозин, N6-метиладенин, 7-метилгуанин, 5-метиламинометилурацил, 5-метоксиаминометил-2-тиоурацил, бета-D-маннозилквеозин, 5'-метоксикарбонилметилурацил, 5-метоксиурацил, 2-метилтио-N6-изопентениладенин, урацил-5-оксиуксусной кислоты метиловый эфир, урацил-5-оксиуксусная кислота, оксибутоксозин, псевдоурацил, квеозин, 2-тиоцитозин, 5-метил-2-тиоурацил, 2-тиоурацил, 4-тиоурацил, 5-метилурацил, N-урацил-5-оксиуксусной кислоты метиловый эфир, урацил-5-оксиуксусная кислота, псевдоурацил, квеозин, 2-тиоцитозин и 2,6-диаминопурин.
Термин «очищенный» или «выделенный» полинуклеотид относится к нуклеиновой кислоте по изобретению, которая (1) была отделена от, по меньшей мере, примерно 50% белков, липидов, углеводов или других материалов, с которыми она содержится, когда общая нуклеиновая кислота выделена из клеток источника, (2) не связана со всем или с частью полинуклеотида, с которым «выделенная нуклеиновая кислота» связана в природе, (3) связана с полинуклеотидом, с которым она не связана в природе, или (4) не встречается в природе как часть более длинной полинуклеотидной последовательности.
Предпочтительно, чтобы выделенная нуклеиновая кислота по изобретению практически не содержала любых других примесных нуклеиновых кислот или других загрязнений, которые обнаружены в ее среде, которые будут участвовать при ее использовании при получении полипептида или при ее терапевтическом, диагностическом, профилактическом применении или применении для исследовательских целей.
Под «нумерацией согласно IL-4 дикого типа» подразумевается идентификация выбранной аминокислоты со ссылкой на положение, в котором эта аминокислота обычно находится в IL-4 дикого типа.
Термин «вектор» относится к любой молекуле (например, нуклеиновой кислоте, плазмиде или вирусу), используемой для передачи кодирующей информации клетке-хозяину.
Термин «вектор экспрессии» относится к вектору, который пригоден для трансформации клетки-хозяина и содержит последовательности нуклеиновой кислоты, которые направляют и/или регулируют экспрессию вставленных последовательностей гетерологичных нуклеиновых кислот. Экспрессия включает, но не ограничивается, такие процессы, как транскрипция, трансляция и сплайсинг РНК, если имеются интроны.
Термин «клетка-хозяин» используется для обозначения клетки, которая была трансформирована или которая способна трансформироваться при помощи последовательности нуклеиновой кислоты и затем к экспрессии выбранного гена. Термин включает потомство родительской клетки, независимо от того, является ли это потомство идентичным по морфологии или организации генетического материала первоначальному родителю, до тех пор, пока имеется выбранный ген.
Термин «трансдукция» обозначает передачу генов от одной бактерии к другой, обычно при помощи фага. «Трансдукция» относится также к приобретению и передаче эукариотных клеточных последовательностей ретровирусами.
Термин «трансфекция» обозначает поглощение инородной или экзогенной ДНК клеткой, и клетка «трансфецирована», когда экзогенная ДНК была введена в клеточную мембрану. Ряд методов трансфекции хорошо известен и описан в уровне техники. См., например, Graham et al., 1973, Virology 52:456; Sambrook et al., Molecular Cloning, A Laboratory Manual (Cold Spring Harbor Laboratories, 1989); Davis et al.. Basic Methods in Molecular Biology (Elsevier, 1986); и Chu et al., 1981, Gene 13:197. Такие методы можно применять для введения одного или более фрагментов экзогенной ДНК в подходящие клетки-хозяева.
Термин «трансформация» относится к изменению генетических характеристик клетки, клетка является трансформированной, когда она была модифицирована и содержит новую ДНК. Например, клетка считается трансформированной, когда она генетически модифицирована в своем естественном состоянии. Вслед за трансфекцией и трансдукцией трансформирующая ДНК может рекомбинироваться с ДНК клетки путем физической интеграции в хромосому клетки, может сохраняться временно в виде эписомального элемента без воспроизводства или может воспроизводиться независимо как плазмида. Считается, что клетка трансформирована стабильно, когда ДНК воспроизведена с делением клетки.
Термин «идентичность», как известно из уровня техники, относится к отношению между последовательностями двух или более молекул полипептида или двух или более молекул нуклеиновой кислоты, что определяется сравнением последовательностей. В уровне техники «идентичность» означает также степень родства последовательностей между молекулами нуклеиновой кислоты или полипептидов, как это может быть и определяется совпадением между нитями двух или более нуклеотидов или двух или более аминокислотных последовательностей. «Идентичность» измеряется в процентном количестве идентичных совпадений между меньшей из двух или более последовательностей с выравниванием гэпов (если они есть) при помощи конкретной математической модели или компьютерной программы (то есть «алгоритмов»).
Термин «подобие» является родственным понятием, но по контрасту с «идентичностью» «подобие» относится к мере родства, которое включает как идентичные совпадения, так и пары консервативного замещения. Если две полипептидных последовательности имеют, например, 10/20 идентичных аминокислот, а остальные все представляют собой неконсервативные замещения, тогда величины степеней идентичности и подобия обе будут равны 50%. Если в том же примере имеется еще пять положений, где содержатся консервативные замещения, тогда величина степени идентичности остается равной 50%, а величина степени подобия будет составлять 75% (15/20). Следовательно, в случаях, когда имеются консервативные замещения, величина степени подобия двух полипептидов будет больше, чем величина степени идентичности этих двух полипептидов.
Степени идентичности и подобия родственных нуклеиновых кислот и полипептидов могут быть легко определены известными методами. Такие методы включают, но не ограничиваются, описанные в COMPUTATIONAL MOLECULAR BIOLOGY (Lesk, A. M., ed.), 1988, Oxford University Press, New York; BIOCOMPUTING: INFORMATICS AND GENOME PROJECTS (Smith, D. W., ed.), 1993, Academic Press, New York; COMPUTER ANALYSIS OF SEQENCE DATA, Part 1 (Griffin, A. M., and Griffin, H. G., eds.), 1994; Humana Press, New Jersey; von Heinje, G., SEQENCE ANALYSIS IN MOLECULAR BIOLOGY, 1987, Academic Press; SEQENCE ANALYSIS PRIMER (Gribskov, M. and Devereux, J., eds.), 1991, M. Stockton Press, New York; Carillo et al., 1988, SIAM J. Applied Math., 48:1073 и Durbin et al., 1998, BIOLOGICAL SEQENCE ANALYSIS, Cambridge University Press.
Предпочтительные методы определения степени идентичности разработаны так, чтобы обеспечить наибольшее совпадение между испытуемыми последовательностями. Методы определения степени идентичности описаны в доступных компьютерных программах. Предпочтительные методы определения степени идентичности двух последовательностей с помощью компьютерных программ включают, не ограничиваясь этим, пакет программ GCG, включая GAP (Devereux, et al., 1984, Nucl. Acid. Res., 12:387; Genetics Computer Group, University of Wisconsin, Madison, WI), BLASTP, BLASTN и FASTA (Altschul et al.. 1990, J. Mol. Biol, 215:403-410. Программа BLASTX общедоступна в Национальном центре информации в области биотехнологии (NCBI) и в других источниках (BLAST Manual, Altschul et al., NCB/NLM/NIH Bethesda MD 20894; Altschul et al., 1990, supra). Для определения степени идентичности можно также применять хорошо известный алгоритм Smith Waterman.
Некоторые схемы выравнивания последовательностей двух аминокислот могут привести к совпадению только короткого участка двух последовательностей, и этот небольшой участок может иметь очень высокую степень идентичности последовательностей, даже хотя нет значительной взаимосвязи между двумя последовательностями с полной длиной. Соответственно, в некоторых вариантах выбранный метод выравнивания (программа GAP) приводит к выравниванию, которое включает, по меньшей мере, 50 смежных аминокислот целевого полипептида.
Например, используя компьютерный алгоритм GAP (Genetics Computer Group, University of Wisconsin, Madison, WI), два полипептида, для которых должна быть определена степень идентичности последовательностей, выравнивают для оптимального совпадения их соответственных аминокислот («совпадающий участок», как определяется алгоритмом). Согласно некоторым вариантам в сочетании с алгоритмом используют штраф за открытие гэпа (который рассчитывается как тройная величина средней диагонали; где «средняя диагональ» является средней величиной диагонали используемой матрицы сравнения; «диагональ» означает балл или число, присвоенное каждому полному совпадению аминокислот при помощи конкретной матрицы сравнения) и штраф за расширение гэпа (который обычно равен 1/10 от штрафа за открытие гэпа), а также матрицу сравнения, такую как РАМ250 или BLOSUM62. Согласно некоторым вариантам в алгоритме используют также стандартную матрицу сравнения (cM.Dayhoff et al., 1978, Atlas of Protein Sequence and Structure, 5:345-352 for the РАМ 250 comparison matrix; Henikoffet al., 1992, Proc. Natl. Acad. Sci. USA, 89:10915-10919 for the BLOSUM 62 comparison matrix).
В некоторых вариантах параметры для сравнения полипептидных последовательностей включают следующие:
Алгоритм: Needleman et al., 1970, J. Mol. Biol., 48:443-453;
Матрица сравнения: BLOSUM 62Henikoff et al., 1992, supra;
Штраф за гэп: 12;
Штраф за удлинение гэпа: 4;
Порог подобия: 0.
С указанными параметрами может быть использована программа GAP. В некоторых вариантах вышеуказанные параметры являются параметрами по умолчанию для сравнения полипептидов (вместе с отсутствием штрафа за концевые гэпы) при использовании алгоритма GAP.
В данной заявке используются общепринятые двадцать обычных аминокислот и их аббревиатуры. См. IMMUNOLOGY - A SYNTHESIS. 2nd Edition (E.S.Golub and D.R.Gren, Eds.), Sinauer Associates: Sunderland, MA, 1991, эта публикация включена в данную заявку в качестве ссылки. Подходящими компонентами для полипептидов по изобретению могут также быть стереоизомеры (например, D-аминокислоты) двадцати обычных аминокислот, неприродные аминокислоты, такие как α-, α-дизамещенные аминокислоты, N-алкиламинокислоты, молочная кислота и другие необычные аминокислоты. Примеры необычных аминокислот включают 4-гидроксипролин, γ-карбоксиглутамат, ε-N,N,N-триметиллизин, ε-N-ацетиллизин, σ-фосфосерин, N-ацетилсерин, N-формилметионин, 3-метил-гистидин, 5-гидроксилизин, σ-N-метиларгинин и другие подобные иминокислоты (например, 4-гидроксипролин). В системе обозначений полипептидов, используемой в данной заявке, левое направление - это направление к N-концу с аминогруппой и правое направление - это направление к С-концу, несущему карбоксильную группу, это стандартные обозначения. Остатки природного происхождения можно разделить на следующие классы на основе общих свойств боковых цепей:
1) гидрофобные: норлейцин (Nor), Met, Ala, Val, Leu, Ile;
2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
3) кислые: Asp, Glu;
4) основные: His, Lys, Arg;
5) остатки, которые влияют на ориентацию цепей: Gly, Pro; и
6) ароматические: Trp, Tyr, Phe.
Консервативные замещения аминокислот могут вовлекать обмен члена одного из этих классов на другой член того же класса. Консервативные замещения могут охватывать остатки аминокислот неприродного происхождения, которые обычно вводятся путем химического синтеза пептидов, а не синтезом в биологических системах. Они включают пептидомиметики и другие обратимые или инвертированные формы аминокислот.
Неконсервативные замещения могут включать обмен члена одного из этих классов на член другого класса. Такие замещенные остатки могут быть введены в участки человеческого белка, которые являются гомологами нечеловеческих белков, или в негомологичные участки молекулы.
При осуществлении таких изменений согласно некоторым вариантам можно рассмотреть гидропатический индекс аминокислот. Каждой аминокислоте был присвоен гидропатический индекс на основе ее гидрофобности и характеристик зарядов. Эти аминокислоты: изолейцин (+4,5); валин (+4,2); лейцин (+3,8); фенилаланин (+2,8); цистеин/цистин (+2,5); метионин (+1,9); аланин (+1,8); глицин (-0,4); треонин (-0,7); серин (-0,8); триптофан (-0,9); тирозин (-1,3); пролин (-1,6); гистидин (-3,2); глутамат (-3,5); глутамин (-3,5); аспартат (-3,5); аспарагин (-3,5); лизин (-3,9) и аргинин (-4,5).
Важная роль гидропатического индекса аминокислот при сравнении интерактивной функции белка отмечена в уровне техники (см., например, Kyte et al., 1982, J. Mol. Biol. 157:105-131). Известно, что некоторые аминокислоты могут замещать другие аминокислоты, имеющие сходный гидропатический индекс или балл, и все еще сохранять похожую биологическую активность. При осуществлении изменений на основе гидропатического индекса согласно некоторым вариантам проводят замещение аминокислот, чьи гидропатические индексы равны ±2. Согласно некоторым вариантам используют аминокислоты с величиной указанного индекса ±1 и согласно другим вариантам - с величиной указанного индекса ±0,5.
Из уровня техники известно, что замещение подобных аминокислот можно осуществить эффективно на основе гидрофильности, особенно когда получаемый при этом биологически функциональный белок или пептид предназначен для применения в иммунологии, как описано в данной заявке.
Согласно некоторым вариантам самая большая локальная средняя гидрофильность белка, регулируемая гидрофильностью соседних аминокислот, коррелирует с его иммуногенностью и антигенностью, то есть с биологическим свойством белка.
Остаткам этих аминокислот присвоены следующие величины гидрофильности: аргинин (+3,0); лизин (+3,0); аспартат (+3,0±1); глутамат (+3,0±1); серин (+0,3); аспарагин (+0,2); глутамин (+0,2); глицин (0); треонин (-0,4); пролин (-0,5±1); аланин (-0,5); гистидин (-0,5); цистеин (-1,0); метионин (-1,3); валин (-1,5); лейцин (-1,8); изолейцин (-1,8); тирозин (-2,3); фенилаланин (-2,5) и триптофан (-3,4).
При осуществлении изменений на основе похожих величин гидрофильности согласно некоторым вариантам проводят замещение аминокислот, величина гидрофильности которых составляет ± 2, согласно некоторым вариантам эта величина равна ± 1 и согласно другим вариантам эта величина равна ± 0,5. Можно также на основе гидрофильности идентифицировать эпитопы из последовательностей первичных аминокислот. Эти участки называются также «эпитопными кор-участками».
Примеры замещений аминокислот приведены в Таблице 1.
Специалист в данной области способен определить подходящие варианты полипептида, что описано ниже с применением хорошо известных методов. Согласно некоторым вариантам специалист может определить подходящие участки молекулы, которые могут быть изменены без уничтожения активности нацеленными участками, которые не считаются важными для активности. Согласно другим вариантам специалист может идентифицировать остатки и части молекул, которые сохраняются среди подобных полипептидов. Согласно другим вариантам даже те области, которые могут быть важны для биологической активности или для структуры, могут подвергаться консервативным замещениям аминокислот без уничтожения биологической активности или без вредного влияния на структуру полипептидов.
Кроме того, специалист может изучить работы по изучению структуры-функции, в которых идентифицированы остатки в подобных полипептидах, которые важны для активности или структуры. С учетом такого сравнения специалист может предсказать значение остатков аминокислот в белке, которые соответствуют остаткам аминокислот, важным для активности или структуры в подобных белках. Специалист может выбрать химически подобные заместители для аминокислот в случае таких предсказанных важных остатков аминокислот.
Специалист может также проанализировать трехмерную структуру и аминокислотную последовательность в связи со структурой в подобных полипептидах. Располагая такой информацией, специалист может предсказать выравнивание остатков аминокислот полипептида по отношению к его трехмерной структуре. Согласно некоторым вариантам специалист может решить не осуществлять радикальных изменений остатков аминокислот, которые, как предсказано, находятся на поверхности белка, так как такие остатки могут участвовать в важных реакциях взаимодействий с другими молекулами. Более того, специалист может генерировать опытные варианты, содержащие одно замещение в аминокислотах в каждом желательном остатке аминокислоты. Эти варианты затем можно подвергнуть скринингу, применяя методы определения активности, известные специалистам. Такие варианты можно использовать для сбора информации о подходящих вариантах. Например, если обнаружено, что изменение в конкретном остатке аминокислоты привело к исчезновению, нежелательному снижению активности или появлению неподходящей активности, таких вариантов с такими изменениями нужно избегать. Другими словами, основываясь на информации, полученной из таких рутинных экспериментов, специалист может легко определить аминокислоты, дальнейшего замещения в которых нужно избегать самого по себе или в сочетании с другими мутациями.
Ряд научных публикаций был посвящен предсказанию вторичной структуры. См. Moult, 1996, Curr. Op. in Biotech. 7:422-427; Chou et al., 1974, Biochemistry 13:222-245; Chou et al., 1978, Adv. Enzymol. Relat. Areas Mol. Biol. 47:45-148; Chou et al., 1979, Ann. Rev. Biochem. 47:251-276 и Chou et al., 1979, Biophys. J. 26:367-384. Более того, в настоящее время доступны компьютерные программы, помогающие предсказать вторичную структуру. Один из методов предсказания вторичной структуры основан на моделировании гомологии. Например, два полипептида или белка, у которых степень идентичности равна более 30% или степень подобия более 40%, часто имеют похожие структурные топологии. Расширение базы структурных данных о белках (PDB) в последнее время обеспечило улучшенную предсказуемость вторичной структуры, включая потенциальное число складок в структуре полипептида или белка. См. Holm et al., 1999, Nucl. Acid. Res. 27:244-247. Было высказано предположение, что существует ограниченное число складок в данном полипептиде или белке и что, как только критическое число структур определяется, резко повышается точность предсказания структуры.
Дополнительные методы предсказания вторичной структуры включают «образование нитей» (Jones, 1997, Curr. Opin. Struct. Biol. 7:377-87; Sippi et al., 1996, Structure 4:15-19), «анализ профиля» (Bowie et al., 1991, Science 253: 164-170; Gribskov et al., 1990, Meth. Enzym. 183:146-159; Gribskov et al., 1987, Proc. Nat. Acad. Sci. 84:4355-4358) и «эволюционные связи» (см. Holm, 1999, supra и Brenner, 1997, supra).
В некоторых случаях варианты белков включают варианты гликозилирования, в которых число и/или тип сайтов гликозилирования были изменены по сравнению с аминокислотными последовательностями родительских форм полипептида. В других случаях варианты белка включают большее или меньшее количество N-связанных сайтов гликозилирования, чем нативный белок. N-связанный сайт гликозилирования характеризуется последовательностью Asn-X-Ser или Asn-X-Thr, где остаток аминокислоты, обозначенный X, может быть любым остатком аминокислоты, кроме пролина. Замещение остатков аминокислот для получения этой последовательности обеспечивает потенциальный новый сайт для добавления N-связанной углеводной цепи. Или же замещения, которые удаляют эту последовательность, будут удалять существующую N-связанную углеводную цепь. Предусмотрена также перестройка N-связанных углеводных цепей, когда один или более N-связанных сайтов гликозилирования (обычно те, которые имеют природное происхождение) удаляются и создаются один или более новых N-связанных сайтов. Дополнительные предпочтительные варианты включают цистеиновые варианты, в которых один или более цистеиновых остатков делецированы или замещены на другую аминокислоту (например, серин) по сравнению с последовательностью родительской формы аминокислоты. Цистеиновые варианты могут быть полезны, когда должен осуществиться рефолдинг белков для получения биологически активной конформации, такой как возникающая после выделения нерастворимых тел включения. Цистеиновые варианты обычно содержат меньше цистеиновых остатков, чем нативный белок, и обычно содержат то же число для минимизации взаимодействий, возникающих из-за не спаренных цистеинов. Согласно дополнительным аспектам варианты белков могут включать мутации, такие как замещения, присоединения, делеции или любая их комбинация, и обычно получаются путем сайтнаправленного мутагенеза с использованием одного или более мутагенных олигонуклеотидов в соответствии с методами, описанными в данной заявке, а также методами, известными из уровня техники (см., например, Sambrook et al., MOLECULAR CLONING: A LABORATORY MANUAL, 3rd Ed, 2001, Cold Spring Harbor. N.Y. and Berger and Kimmel, METHODS IN ENZYMOLOGY, Volume 152, Guide to Molecular Cloning Techniques, 1987, Academic Press, Inc., San Diego, CA., которые включены в данную заявку в качестве ссылок).
Согласно некоторым вариантам замещения аминокислоты включают такие, которые (1) уменьшают восприимчивость к протеолизу, (2) уменьшают восприимчивость к окислению, (3) изменяют сродство к связыванию при образовании белковых комплексов, (4) изменяют сродство к связыванию и/или (5) придают или модифицируют другие физико-химические или функциональные свойства таких полипептидов.
Согласно другим вариантам единичное или множественное замещения аминокислот (в некоторых вариантах консервативные замещения аминокислот) могут осуществляться в последовательности природного происхождения (в некоторых вариантах, в части полипептида, которая находится вне домена(-ов), формирующего (-их) внутримолекулярные контакты). Согласно предпочтительным вариантам консервативное замещение аминокислот обычно незначительно изменяет структурные характеристики родительской последовательности (например, замещение аминокислотой не имеет тенденции к разрушению спирали, которая возникает в родительской последовательности, или к разрыву других типов вторичной структуры, которые характеризуют родительскую последовательность). Примеры известных вторичных и третичных структур полипептидов описаны в PROTEINS, STRUCTURES AND MOLECULAR PRINCIPLES (Creighton, Ed.), 1984, W. H. Freeman and Company, New York; INTRODUCTION TO PROTEIN STRUCTURE (C. Branden and J. Tooze, eds.), 1991, Garland Publishing, New York, N.Y. и Thornton et al., 1991, Nature 354:105, причем каждая из этих публикаций включена в данную заявку в качестве ссылки.
Аналоги пептидов обычно применяются в фармацевтической промышленности как непептидные лекарства со свойствами, аналогичными свойствам пептидного темплата. Эти типы непептидного соединения называются «пептидными миметиками» или «пептидомиметиками». См. Fauchere, 1986, Adv. Drug Res. 15:29; Veber & Freidinger, 1985, TINS p.392 и Evans et al., 1987, J. Med. Chem. 30:1299, которые включены в данную заявку в качестве ссылок для любой цели. Такие соединения часто создают при помощи компьютерного молекулярного моделирования. Пептидные миметики, которые структурно похожи на терапевтически применяемые пептиды, могут быть использованы для получения подобного терапевтического или профилактического эффекта. Обычно пептидомиметики структурно подобны эталонному полипептиду (то есть полипептиду, который имеет биохимическое свойство или фармакологическую активность), такому как человеческое антитело, но содержат одну или более пептидных связей, возможно замещенных связью, выбранной из -CH2-NH-, -CH2-S, -CH2CH2-, -СН=СН- (цис- и транс-), -СОСН2-, -СН(ОН)СН2- и -CH2SO-, введенные хорошо известными методами. Систематическое замещение одной или более аминокислот в консенсусной последовательности D-аминокислотой того же типа (например, D-лизином вместо L-лизина) можно использовать в некоторых вариантах для получения более стабильных пептидов. Кроме того, малоподвижные белки, включающие консенсусную последовательность или в основном идентичный вариант консенсусной последовательности, могут быть получены известными способами (Rizo and Gierasch, 1992, Ann. Rev. Biochem. 61:387, включена в данную заявку в качестве ссылок для любой цели), например, путем добавления внутренних цистеиновых остатков, способных образовать внутримолекулярные дисульфидные мостики, которые циклизуют полипептид.
(а) Характеристики модифицированных антагонистов рецептора мутеина IL-4.
«Модифицированные антагонисты рецептора мутеина IL-4" в данной заявке включают мутеин IL-4RA, описанный в патентах США 6028176 и 6 313 272 (включены в данную заявку в качестве ссылок) с дополнительными замещениями аминокислот, причем указанные замещения способствуют сайтспецифичному сочетанию (присоединению), по меньшей мере, одного небелкового полимера, такого как полипропиленгликоль, полиоксиалкилен или полиэтиленгликоль (ПЭГ) с мутеином. Сайтспецифичное присоединение ПЭГ, например, позволяет получить модифицированный мутеин, который обладает преимуществами полиэтилен-гликозилированного (ПЭГилигированного) соединения, а именно, более длинным периодом полураспада в плазме и пониженной иммуногенностью при сохранении более высокой активности по сравнению с неспецифичными методами ПЭГилигирования, такими как N-концевое ПЭГилигирование или ПЭГилигирование в боковой цепи лизина. Для данного изобретения является также неотъемлемым выбор специфического сайта в заместителе аминокислоты, который способствует надлежащему фолдингу молекулы вслед за экспрессией. Модифицированные антагонисты рецептора мутеина IL-4 связываются с IL-4 и IL-13 с потерей сродства не более чем в 10 раз по сравнению с IL-4RA. Модифицированные антагонисты рецептора мутеина IL-4 ингибируют опосредованную IL-4 и IL-13 активность с потерей активности не более чем десятикратной, по сравнению с активностью IL-4RA. Кроме того, модифицированные антагонисты рецептора мутеина IL-4 характеризуются величиной полураспада в плазме, которая, по меньшей мере, в 2-10 раз больше, чем для не модифицированного IL-4RA.
Мутеины IL-4 по изобретению могут также характеризоваться вставками, делециями, замещениями и модификациями аминокислот в месте одного или более сайтов или в других остатках полипептидной цепи нативного IL-4. Согласно данному изобретению любые такие вставки, делеции, замещения и модификации обеспечивают получение мутеина IL-4, который сохраняет активность, связанную с IL-4.
Дополнительным аспектом настоящего изобретения является способ, согласно которому происходят экспрессия и рефолдинг, как описано в Примере 2. Мутеин IL-4 должен быть надлежащим образом очищен, чтобы можно было осуществить эффективное ПЭГилирование. Метод очистки описан, например, ниже в Примере 2. Когда происходит рефолдинг мутеина в присутствии сульфгидрильного защитного агента, такого как бета-меркаптоэтанол, глютатион или цистеин, очищенный мутеин не может быть ПЭГилигирован, так как активный сульфгидрил в цистеине, введенном в IL-4, инактивируется окисленным защитным агентом. Между свободным цистеином мутеина IL-4 и защитным агентом образуется ковалентная дисульфидная связь. В противоположность этому, применение сульфгидрильного защитного агента дитиотреитола (DTT), который окисляется с образованием стабильной дисульфидной связи, не будет образовывать ковалентную связь со свободным цистеином мутеина IL-4, что оставляет его сульфгидрильную группу свободной для реакции с ПЭГмальимидным реагентом. Мутеины IL-4, очищенные после рефолдинга в присутствии бета-меркаптоэтанола, глютатиона или цистеина, могут реагировать с ПЭГ, если они обработаны DTT, но образуется смесь моноПЭГилированных и муьтиПЭГилированных продуктов, что предполагает также ПЭГилигирование существующих цистеинов IL-4. ПЭГилигирование имеющихся цистеинов приведет к неправильному сворачиванию с образованием продуктов, которые являются неактивными.
Кd модифицированных антагонистов рецептора мутеина IL-4 к рецептору IL-4 можно определить любым известным методом, включая такие методики, как Bimolecular interaction Analysis (BIA) (анализ бимолекулярного взаимодействия) в реальном времени, описанный в Примере 4. BIA представляет собой методику для изучения биоспецифических взаимодействий в реальном времени без мечения любого из реагентов (например, BIAcore™). Изменения в оптическом резонансе поверхностного плазмона (SPR) могут быть использованы для индикации реакций между биологическими молекулами в реальном времени.
Способность модифицированных антагонистов рецепторов мутеина IL-4 ингибировать пролиферативный ответ иммунных клеток можно оценить, используя метод пролиферативного анализа, описанный в Примере 5, эта способность выражается в виде ингибирующей на 50% концентрации (IС50).
В методе BIAcore™ модифицированные антагонисты рецепторов мутеина IL-4 по изобретению связываются специфически с рецептором человеческого IL-4 с предпочтительной величиной Кd в пределах от примерно 1,0 нМ до примерно 100 нМ. Согласно более предпочтительным вариантам данного изобретения эти антагонисты связываются с рецептором человеческого IL-4 с Кd, равной примерно от 0,5 нМ до 1,0 мкМ. Согласно еще более предпочтительным вариантам эти антагонисты связываются с рецептором человеческого IL-4 с Кd, равной примерно от 0,1 нМ до 10 мкМ.
Кроме того, модифицированные антагонисты рецепторов мутеина IL-4 по изобретению будут связываться с рецептором человеческого IL-4 и нейтрализовать его способность промотировать пролиферацию клеток иммунной системы с предпочтительной величиной IС50 в пределах от примерно 1,0 нМ до примерно 100 нМ. Более предпочтительные антагонисты человека связывают рецептор IL-4 и нейтрализуют его способность к пролиферации клеток иммунной системы с величиной IС50 в пределах от примерно от 0,5 нМ до 1,0 мкМ, а наиболее предпочтительные антагонисты по изобретению - с величиной IС50 в пределах от примерно 0,1 нМ до примерно 10 мкМ.
Варианты модифицированных антагонистов рецепторов мутеина IL-4 по изобретению характеризуются также величиной периода полураспада в плазме, которая предпочтительно, по меньшей мере, в 2-10 раз больше, чем у не модифицированного IL-4RA, а наиболее предпочтительные варианты по изобретению имеют величину периода полураспада в плазме, которая в 10-100 раз больше, чем у не модифицированного IL-4RA (см. Пример 7).
Ряд модифицированных антагонистов рецепторов мутеина IL-4 с характеристиками, описанными выше, были идентифицированы путем скрининга с применением указанных выше методов анализа. Антагонисты согласно данному изобретению содержат полипептидные последовательности, приведенные в Таблице 2 (SEQ ID NO: 10-16).
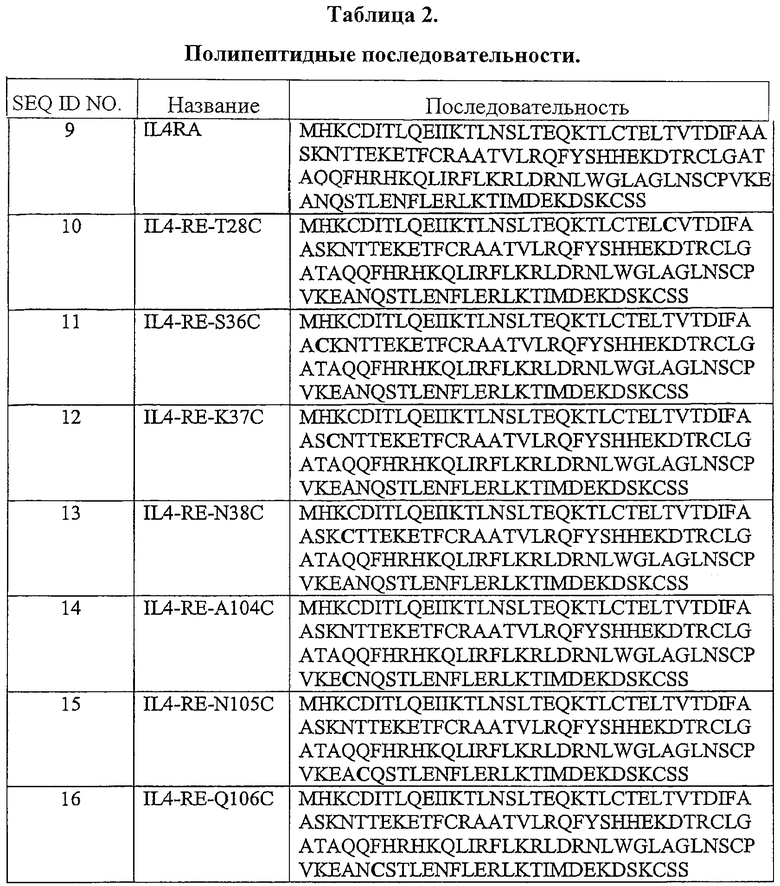
(б) Полинуклеотиды, кодирующие модифицированные антагонисты рецептора мутеина IL-4.
Данное изобретение предусматривает также полинуклеотиды, кодирующие модифицированные антагонисты рецептора мутеина IL-4. Эти полинуклеотиды можно применять, например, для количественного получения антагонистов по изобретению. Полинуклеотид по изобретению может быть легко получен разными способами, включая, без ограничения, химический синтез, скрининг кДНК или библиотеки геномов, скрининг библиотеки экспрессии и/или амплификацию кДНК по полимеразной цепной реакции (PCR).
Рекомбинация ДНК, описанная в данной заявке, осуществляется обычно методами, описанными в Sambrook et al., Molecular Cloning: A Laboratory Manual (Cold Spring Harbor Laboratory Press, 1989) и/или Current Protocols in Molecular Biology (Ausubel et al., eds., Green Publishers Inc. and Wiley and Sons 1994). Данное изобретение предусматривает нуклеиновые кислоты и способы их получения, описанные в данной заявке.
Один способ получения подходящей последовательности нуклеиновой кислоты представляет собой полимеразную цепную реакцию (PCR). Согласно этому способу кДНК получается из поли(А)+РНК или РНК с применением обратной транскрипазы. Два праймера, обычно комплиментарные двум отдельным фрагментам кДНК модифицированного антагониста рецептора мутеина IL-4, добавляются к кДНК вместе с полимеразой, такой как Taq-полимераза, и полимераза амплифицирует фрагмент кДНК между двумя праймерами.
Другим средством получения нуклеиновой кислоты по изобретению является химический синтез с применением методов, которые хорошо известны специалисту, например, описанных Engels et al., 1989, Angew. Chem. Intl. Ed. 28:716-34. Наряду с другими эти методы включают способы синтеза нуклеиновой кислоты с применением фосфотриэфира, фосфорамидита и Н-фосфоната. Предпочтительный метод такого химического синтеза представляет собой синтез на полимерном носителе с применением стандартной методики с фосфорамидитом. Обычно ДНК содержит несколько сотен нуклеотидных звеньев. Нуклеиновые кислоты, содержащие более примерно 100 нуклеотидных звеньев, могут быть синтезированы в виде нескольких фрагментов с применением этих методов. Затем эти фрагменты могут быть лигированы вместе. Можно использовать и другие методы, известные специалистам.
Полинуклеотиды по изобретению, которые можно применять для кодирования модифицированных антагонистов рецепторов мутеина IL-4, показаны в Таблице 3 (SEQ ID NO:2-8).


Изобретение предусматривает также векторы экспрессии, включающие полинуклеотид по изобретению, и клетки-хозяева, содержащие вектор экспрессии по изобретению.
Полинуклеотид по изобретению может быть вставлен в подходящий вектор экспрессии с применением стандартных методов дотирования. Обычно выбирают вектор, который является функциональным в конкретной используемой клетке-хозяине (то есть вектор совместим с процессами, происходящими в клетке-хозяине, и поэтому может возникнуть амплификация гена и/или экспрессия гена). Полинуклеотид по изобретению может экспрессироваться в прокариотные, дрожжевые клетки-хозяева, в хозяйские клетки насекомых и/или эукариотные клетки-хозяева. Выбор клеток-хозяев будет зависеть от разных факторов, таких как желательная степень экспрессии. Обзор векторов экспрессии см. в Meth. Enz. Vol.185 (D.V.Goeddel, ed., Academic Press, 1990).
Обычно векторы экспрессии, применяемые в клетке-хозяине, содержат последовательности для сохранения плазмид и для клонирования и экспрессии экзогенных нуклеотидных последовательностей. Такие последовательности, называемые «фланкирующими последовательностями», в некоторых случаях обычно включают одну или более следующих нуклеотидных последовательностей: промотор, одна или более последовательностей энхансера (усилителя), источник репликации, транскрипционная, терминальная (концевая) последовательность, полная интронная последовательность, содержащая донор- и акцептор-сайт сплайсинга, последовательность, кодирующая основную последовательность для секреции полипептида, сайт связывания рибосом, полиаденилирующая последовательность, участок полилинкера для вставки нуклеиновой кислоты, кодирующей полипептид, который должен экспрессироваться, и выбираемый элемент маркера. Каждая из этих последовательностей обсуждается ниже.
Фланкирующие последовательности могут быть гомологичными (то есть из тех же фрагментов и/или того же штамма, что и хозяйские клетки), гетерологичными (то есть из фрагментов, отличающихся от фрагментов хозяйских клеток или штамма), гибридными (то есть являются комбинацией фланкирующих последовательностей из более чем одного источника) или синтетическими, или фланкирующие последовательности могут быть нативными последовательностями, которые нормально функционируют, регулируя экспрессию антагониста рецептора мутеина IL-4. Как таковой источник фланкирующей последовательности может быть любым прокариотным или эукариотным организмом, любым организмом позвоночного или непозвоночного, или любым растением, при условии, что фланкирующая последовательность является функциональной в процессах, протекающих в клетке-хозяине, и может ими активироваться.
Фланкирующие последовательности, используемые в векторах согласно изобретению, могут быть получены любым из методов, хорошо известных из уровня техники. Обычно используемые по изобретению фланкирующие последовательности, другие, чем фланкирующие последовательности генов антагониста рецептора мутеина IL-4, должны были быть предварительно идентифицированы путем составления карты или путем переваривания рестрикционной эндонуклеазой, и могли быть, таким образом, изолированы из подходящего тканевого источника с применением соответствующих рестрикционных эндонуклеаз. В некоторых случаях полная нуклеотидная последовательность фланкирующей последовательности может быть известна. В данной заявке фланкирующая последовательность может быть синтезирована методами, описанными для синтеза или клонирования нуклеиновой кислоты, описанными в данной заявке.
Если вся или только часть фланкирующей последовательности известна, она может быть получена путем PCR и/или путем скрининга геномной библиотеки при помощи подходящего олигонуклеотида и/или фрагмента фланкирующей последовательности из того же или другого вида. Если фланкирующая последовательность неизвестна, фрагмент ДНК, содержащий фланкирующую последовательность, может быть выделен из большего участка ДНК, который может содержать, например, кодирующую последовательность или даже другой(-ие) ген или гены. Выделение может быть осуществлено путем переваривания рестрикционной эндонуклеазой с получением нужного фрагмента ДНК с последующей изоляцией путем очистки с применением геля агарозы, Qiagen® хроматография на колонке (Chatsworth, CA), или другими методами, известными специалисту. Выбор подходящих ферментов для достижения этой цели очевиден для специалиста в данной области.
Репликатор обычно представляет собой часть прокариотных векторов экспрессии, доступную коммерчески, и способствует амплификации вектора в клетке-хозяине. Если выбранный вектор не содержит источник сайта репликации, его можно синтезировать на основе известной последовательности химическим путем и лигировать в вектор. Например, репликатор из плазмиды pBR322 (New England Biolabs, Beverly, MA) пригоден для большинства грам-отрицательных бактерий, а различные источники (например, SV40, полиома, аденовирус, вирус везикулярного стоматита (VSV) или вирусы папилломы, такие как HPV или BPV) подходят для клонирования векторов в клетках млекопитающих. Обычно репликатор не нуждается в векторах экспрессии млекопитающих (например, SV40 часто используется только потому, что он содержит ранний промотор).
Транскрипционная терминальная последовательность обычно расположена в положении 3' конца кодирующего участка полипептида и служит для терминации транскрипции. Обычно транскрипционная терминальная последовательность в прокариотных клетках представляет собой обогащенный G-C фрагмент с последующей поли-Т-последовательностью. Хотя последовательность легко клонируется из библиотеки и даже может быть куплена как часть вектора, ее можно легко синтезировать, используя способы синтеза нуклеиновой кислоты, такие как описаны в данной заявке.
Селективный маркерный ген кодирует белок, который необходим для выживания и роста клетки-хозяина, выращиваемой в селективной культуральной среде. Типичные селективные маркерные гены кодируют белки, которые (а) придают резистентность к антибиотикам и другим токсинам; (б) дополняют ауксотрофные дефекты клетки; или (в) снабжают необходимыми питательными веществами, которые недоступны из сложной среды. Предпочтительными селективными маркерами являются ген, резистентный к канамицину, ген, резистентный к ампициллину, и ген, резистентный к тетрациклину. Ген, резистентный к неомицину, также можно использовать для селекции в прокариотных и эукариотных клетках-хозяевах.
Другие селективные гены могут быть применены для амплификации гена, который будет экспрессироваться. Амплификация представляет собой процесс, в котором гены, которые очень необходимы для продуцирования белка, критического для роста, повторяются в тандеме с хромосомами последующих поколений рекомбинантных клеток. Примеры подходящих селективных маркеров для человеческих клеток включают дигидрофолатредуктазу (DHFR) и тимидинкиназу. Трансформанты человеческих клеток помещают в условия действия давления отбора, причем только трансформанты адаптируются к выживанию за счет селективного гена, содержащегося в векторе. Давление отбора создается путем культивирования трансформированных клеток при условиях, в которых концентрация агента отбора в среде последовательно изменяется, что приводит к амплификации, как селективного гена, так и ДНК, которая кодирует модифицированный антагонист рецептора мутеина IL-4. В результате из амплифицированной ДНК синтезируются повышенные количества модифицированного антагониста рецептора мутеина IL-4.
Сайт связывания рибосомы обычно необходим для инициирования трансляции мРНК и характеризуется последовательностью Шайна-Далгарно (прокариоты) или последовательностью Козака (эукариоты). Этот элемент обычно расположен на конце 3' по отношению к промотору и 5' - к кодирующей последовательности модифицированного антагониста рецептора мутеина IL-4. Последовательность Шайна-Далгарно изменена, но обычно является полипурином (то есть имеет высокое содержание А-G). Многие последовательности Шайна-Далгарно были идентифицированы, каждая из них может быть легко синтезирована с применением методов, описанных в данной заявке, и используется в прокариотном векторе.
Лидирующая, или сигнальная, последовательность может быть использована для направления модифицированного антагониста рецептора мутеина IL-4 из клетки-хозяина. Обычно нуклеотидная последовательность, кодирующая сигнальную последовательность, расположена на кодирующем участке молекулы нуклеиновой кислоты модифицированного антагониста рецептора мутеина IL-4 или непосредственно на 5' конце кодирующего участка модифицированного антагониста рецептора мутеина IL-4. Многие сигнальные последовательности были идентифицированы, и любая из них, которая действует в выбранной клетке-хозяине, может быть применена в сочетании с молекулой нуклеиновой кислоты модифицированного антагониста рецептора мутеина IL-4. Следовательно, сигнальная последовательность может быть гомологичной (естественного происхождения) или гетерологичной по отношению к молекуле нуклеиновой кислоты модифицированного антагониста рецептора мутеина IL-4. Дополнительно, сигнальная последовательность может быть синтезирована химическими способами, описанными в данной заявке. В большинстве случаев секреция модифицированного антагониста рецептора мутеина IL-4 из клетки-хозяина благодаря наличию сигнального пептида приведет к удалению сигнального пептида из выделенного модифицированного антагониста рецептора мутеина IL-4. Сигнальная последовательность может быть компонентом вектора, или она может быть частью молекулы модифицированного антагониста рецептора мутеина IL-4, которая инсертирована в вектор.
Во многих случаях транскрипция молекулы нуклеиновой кислоты увеличивается за счет присутствия одного или более интронов в векторе; это особенно справедливо, когда полипептид продуцируется в эукариотных клетках-хозяевах, особенно в клетках-хозяевах млекопитающего. Использованные интроны могут быть естественного происхождения в гене модифицированного антагониста рецептора мутеина IL-4, особенно, когда используемый ген является последовательностью полного генома или ее фрагментом. Если интрон не является интроном естественного происхождения в гене, он может быть получен из другого источника. Положение интрона по отношению к фланкирующим последовательностям и гену модифицированного антагониста рецептора мутеина IL-4 обычно является важным, так как интрон для придания эффективности должен быть транскрибирован. Таким образом, когда молекула нуклеиновой кислоты по изобретению транскрибируется, предпочтительным положением интрона является положение 3' к сайту начала транскрипции и положение 5' к поли-А-транскрипционной терминальной последовательности. Предпочтительно, чтобы интрон или интроны были расположены на одной стороне или на другой стороне (то есть 5' или 3') кДНК, так чтобы он (они) не прерывал кодирующую последовательность. Любой интрон из любого источника, включая вирусные, прокариотные и эукариотные (растительные или животные) организмы, может быть использован в практике данного изобретения, при условии, что он совместим с клеткой-хозяином, в которую он инсертируется. Используются также синтетические интроны. В векторе может быть применен более чем один интрон.
Векторы экспрессии и клонирования по изобретению обычно содержат промотор, который распознается организмом хозяина и который связан с молекулой нуклеиновой кислоты по изобретению. Промоторы являются нетранскрибированными последовательностями, расположенными в направлении апстрим (а именно, к 5') к исходному кодону структурного гена (обычно 100-1000 пар оснований), которые контролируют транскрипцию структурного гена. Промоторы обычно относят к одному из двух классов: индуцибельным промоторам и конститутивным промоторам. Индуцибельные промоторы повышают степень транскрипции из ДНК под их контролем в ответ на некоторые изменения в условиях культивирования, такие как наличие или отсутствие питательной среды или изменение температуры. С другой стороны, конститутивные промоторы инициируют непрерывное продуцирование генного продукта, то есть происходит незначительный контроль экспрессии гена или его нет совсем. Большое число промоторов, признаваемых различными потенциальными клетками-хозяевами, хорошо известно. Подходящий промотор может быть связан с молекулой нуклеиновой кислоты по изобретению путем удаления промотора из источника ДНК при переваривании рестрикционным ферментом и инсертирования желательной последовательности промотора в вектор. Последовательность промотора антагониста рецептора мутеина нативного IL-4 можно применять для управления амплификацией и/или экспрессией нуклеиновой кислоты по изобретению. Гетерологичный промотор является предпочтительным, однако, только если он обеспечивает большую степень транскрипции и более высокие выходы экспрессированного белка по сравнению с нативным промотором и если он совместим с системой клетки-хозяина, которая была отобрана.
Промоторы, подходящие для использования с прокариотными хозяевами, включают бета-лактамазу и системы лактозных промоторов; щелочную фосфатазу, систему триптофанового (trp) промотора и гибридные промоторы, такие как tac-промотор. Подходящими являются также другие известные бактериальные промоторы. Их последовательности опубликованы, что дает возможность специалисту лигировать их желательной последовательностью ДНК с применением линкеров и адаптеров, необходимых для создания подходящих сайтов рестрикции.
Подходящие для применения с дрожжевыми клетками-хозяевами промоторы также хорошо известны из уровня техники. Дрожжевые энхансеры предпочтительно использовать с дрожжевыми промоторами. Подходящие промоторы для клеток-хозяев млекопитающего хорошо известны и включают, без ограничения, промоторы, полученные из геномов вирусов, таких как вирус полиомы, fowlpox вирус, аденовирус (такой как аденовирус 2), вирус папилломы крупного рогатого скота, вирус саркомы птиц, цитомегаловирус, ретровирусы, вирус гепатита В и, наиболее предпочтительно, вакуолизирующий обезьяний вирус 40 (SV40). Другие подходящие промоторы включают гетерологичные промоторы млекопитающих, например, хитшоковые промоторы (промоторы теплового шока) и актиновый промотор.
Другие промоторы, представляющие интерес для контролирования экспрессии генов, включают, без ограничения, область раннего промотора SV40 (Bernoist and Chambon, 1981, Nature, 290:304-10), промотор CMV, промотор, содержащийся в положении 3' длинного трминального повтора вируса саркомы Рауса (Yamamoto et al., Cell 22:787-97), промотор тимидинкиназы герпеса (Wagner et al., 1981, Proc. Natl. Acad. Sci. USA, 78:1444-45), регуляторные последовательности гена металлотионина (Brinster et al., 1982, Nature, 296:39-42), прокариотные векторы экспрессии, такие как промотор бета-лактамазы (Vella-Kamaroff et al., 1978, Proc. Natl. Acad. Sci. USA, 75:3727-31) или tac-промотор (DeBoer et al., 1983, Proc. Natl. Acad. Sci. USA, 80:21-25). Представляют также интерес следующие области контроля транскрипции у животных, которые проявляют тканевую специфичность и были использованы в трансгенных животных: область контроля гена эластазы I, которая активна в панкреатических ацинарных клетках (Swift et al., 1984, Cell 38:639-46; Ornitz et al., 1986, Cold Spring Harbor Symp. Quant. Biol. 50:399-409 (1986); MacDonald, 1987, Hepatology 7:425-515); область контроля инсулинового гена, которая активна в панкреатических бета-клетках (Hanahan, 1985, Nature 315:115-22); область контроля гена иммуноглобулина, которая активна в лимфоидных клетках (Grosscheld et al., 1984, Cell 38:647-58, Adames et al., 1985, Nature 318:533-38; Alexander et al, 1987, Mol. Cell. Biol, 7:1436-44); область контроля вируса Биттнера, которая активна в тестикулярных клетках, клетках молочной железы, лимфоидных и тучных клетках (Leder et al, 1986, Cell, 45:485-95); область контроля альбуминового гена, которая активна в печени (Pinkert et al, 1987, Genes and Devel. 1:268-76); область контроля гена альфа-фетопротеина, которая активна в печени (Krumlauf et al, 1985, Mol. Cell. Biol., 5:1639-48; Hammer et al., 1987, Science, 235:53-58); область контроля гена альфа-1-антитрипсина, которая активна в печени (Kelsey et al. Genes and Devel. 1:161-71); область контроля гена бета-глобина, которая активна в миелоидных клетках (Mogram et al., 1985, Nature, 315:338-40; Kollias et al., 1986, Cell, 46:89-94); область контроля гена основного белка миелина, которая активна в олигодендроцитных клетках мозга (Readhead et al., 1987, Cell 48:703-12); область контроля гена легкой цепи-2 миозина, которая активна в скелетных мышцах (Sani, 1985, Nature, 314:283-86) и область контроля гена гормона, выделяющего гонадотропин, которая активна в гипоталамусе (Mason et al., 1986, Science, 234:1372-78).
Энхансерная последовательность может быть инсертирована в вектор для увеличения транскрипции нуклеиновой кислоты по изобретению высшими эукариотами. Энхансеры являются цис-действующими элементами ДНК, обычно длиной примерно 10-300 пар оснований, которые действуют на промотор для увеличения транскрипции. Энхансеры довольно независимы от ориентации и положения. Было установлено, что они находятся в положении 5' и 3' к единице транскрипции. Несколько последовательностей энхансеров, доступные из генов млекопитающих, известны (например, глобулин, эластаза, альбумин, альфа-фетопротеин и инсулин). Однако обычно используют энхансер вируса. Энхансер SV40, энхансер раннего промотора цитомегаловируса, энхансер, полиомы и энхансеры аденовирусов являются примерами усилителей для активации эукариотных промоторов. Хотя энхансер может быть сплайсирован в вектор в положении 5' или 3' по отношению к молекуле нуклеиновой кислоты по изобретению, он обычно расположен на сайте 5' от промотора.
Векторы экспрессии по изобретению могут быть получены из исходного вектора, например, коммерчески доступного. Такие векторы могут или не могут содержать все из желательных фланкирующих последовательностей. Если одна или более фланкирующих последовательностей, описанных в данной заявке, еще не присутствует в векторе, они могут быть индивидуально получены и лигированы в векторе. Способы, используемые для получения каждой из фланкирующих последовательностей, хорошо известны специалисту.
Предпочтительные векторы в практике данного изобретения должны быть совместимыми с бактериальными клетками-хозяевами, клетками-хозяевами насекомых и млекопитающих. Такие векторы, наряду с другими, включают pCRII, pCR3 и pcDNA3.l (Invitrogen, San Diego, CA), pBSII (Stratagene, La Jolla, CA), pET15 (Novagen, Madison, WI), pGEX (Phannacia Biotech, Piscataway, NJ), pEGFP-N2 (Clontech, Palo Alto, CA), pETL (BlueBacII, Invitrogen), pDSR-alpha (WO 90/14363) и pFastBacDual (Gibco-BRL, Grand Island, NJ).
Другие подходящие векторы включают, без ограничения, космиды, плазмиды или модифицированные вирусы, при этом специалисту очевидно, что векторная система должна быть совместимой с выбранной клеткой-хозяином. Такие векторы включают, без ограничения, плазмиды, такие как производные плазмиды Bluescript® (фагмида на основе ColEl с большим числом копий, Stratagene Cloning Systems, La Jolla CA), PCR клонирующие плазмиды для клонирования Tag-амплифицированных продуктов PCR (например, производные плазмиды ТОРО™ ТА Cloning® Kit, PCR2.1®, Invitrogen, Carlsbad, CA) и векторы млекопитающих, дрожжей или вирусов, такие как система экспрессии бакуловируса (производные плазмиды рВасРАК, Clontech, Palo Alto, CA).
После создания вектора и инсерции нуклеиновой кислоты по изобретению в надлежащий сайт вектора готовый вектор может быть инсертирован в подходящую хозяйскую клетку для амплификации и/или экспрессии полипептида. Трансформация вектора экспрессии по изобретению в выбранной хозяйской клетке может осуществляться хорошо известными способами, включая такие как трансфекция, инфекция, применение хлорида кальция, электропорация, микроинъекция, липофекция, применение DEAE-декстрана или другие методы. Выбранный метод частично является функцией типа хозяйской клетки, которая должна быть использована. Эти и другие методы хорошо известны и описаны, например, в Sambrook et al., supra.
Клетки-хозяева могут быть прокариотными (такими как E.coli) или эукариотными (такими как клетки дрожжей, насекомых или позвоночных). Клетка-хозяин при культивировании в соответствующих условиях синтезирует модифицированный антагонист рецептора мутеина IL-4, который впоследствии может быть собран из культуральной среды (если клетка-хозяин секретирует его в эту среду) или непосредственно из клетки-хозяина, продуцирующей его (если он не секретируется). Выбор подходящей клетки-хозяина зависит от разных факторов, таких как желательная степень экспрессии, модификации полипептидов, которые желательны или необходимы для появления активности (такие как гликозилирование или фосфорилирование) и легкость фолдинга с получением.
Ряд подходящих клеток-хозяев известны из уровня техники и многие доступны в American Type Culture Collection (ATCC), Manassas, VA. Примеры включают, без ограничения, клетки млекопитающих, такие как клетки яичников китайского хомяка (СНО), клетки СНО DHFR(-) (Urnaub et al., 1980, Proc. Natl. Acad. Sci. USA, 97:4216-20), клетки 293 или 293Т почек человеческого эмбриона (НЕК) или клетки 3Т3. Селекция подходящих клеток-хозяев млекопитающих и методы трансформации, культивирования, амплификации, скрининга, получения продуктов и очистки являются известными. Другими подходящими клеточными линиями млекопитающих являются клеточные линии COS-1 и COS-7 обезьян и клеточная линия CV-1. Другие примеры клеток-хозяев млекопитающих включают клеточные линии приматов и клеточные линии грызунов, включая трансформированные клеточные линии. Пригодными являются также нормальные диплоидные клетки, клеточные штаммы из in vitro культуры первичной ткани, а также первичные эксплантаты. Клетки-кандидаты могут иметь генотипный дефект селективного гена или могут содержать доминирующий действующий селективный ген. Другие подходящие клеточные линии млекопитающих включают, без ограничения, клетки нейробластомы N2A мыши, HeLa, клетки L-929 мыши, линии 3Т3, полученные у мышей Swiss, Balb-c или NIH, клеточные линии ВНК или НаК хомячка. Каждая из этих клеточных линий известна и доступна специалистам в области экспрессии белков.
Подходящими по данному изобретению являются также клетки-хозяева, являющиеся бактериальными клетками. Например, в области биотехнологии хорошо известны различные штаммы Е.соli (например, НВ101, DH5S, DH10 и МС1061). В этом способе можно также применять различные штаммы B.subtilis, Pseudomonas spp., другие Bacillus spp., Streptomyces spp. и т.п.
Специалистам также известны и доступны в качестве клеток-хозяев для экспрессии полипептидов по изобретению многие штаммы дрожжевых клеток. Предпочтительные дрожжевые клетки включают, например, Saccharomyces cervisae и Pichia pastoris.
Кроме того, если это желательно, можно в способах по изобретению применять системы клеток насекомых. Такие системы описаны, например, в Kitts et al., 1993, Biotechniques, 14:810-17; Lucklow, 1993, Curr. Opin. Biotechnol. 4:564-72; и Lucklow et al., 1993, J. Virol., 67:4566-79. Предпочтительными клетками насекомых являются Sf-9 и Hi5 (Invitrogen).
Полинуклеотиды по изобретению, содержащиеся в клетке-хозяине, могут быть изолированы без наличия в них других компонентов клетки, таких как компоненты мембраны, белки и липиды. Полинуклеотиды могут быть выделены из клеток стандартными методами очистки нуклеиновых кислот или могут быть синтезированы с применением метода амплификации, такого как полимеразная цепная реакция (PCR), или автоматического синтезатора. Методы выделения полинуклеотидов являются рутинными и известны из уровня техники. Любой такой метод получения полинуклеотида можно использовать для получения изолированных полинуклеотидов, кодирующих антагонисты по изобретению. Например, для изоляции полинуклеотидов, которые кодируют антагонисты, можно применять рестрикционные ферменты и пробы. Предпочтительно, чтобы изолированные полинуклеотиды были в виде препаратов, которые не содержат вообще или не содержат 70, 80 или 90% других веществ.
Специалистам очевидно, что нуклеиновая кислота и полипептиды, описанные в данной заявке, могут быть получены рекомбинантными и другими методами. Например, кДНК модифицированного антагониста рецептора мутеина IL-4 по изобретению может быть получена стандартными методами молекулярной биологии с использованием в качестве темплата мРНК. Затем кДНК может быть реплицирована с применением методов молекулярной биологии, известных из уровня техники и описанных в Примере 1. В Примере 2 описаны специфические методы рекомбинантной экспрессии и очистки, применяемые при получении модифицированных антагонистов мутеина по изобретению.
(в) Оценка терапевтической полезности человеческих антагонистов.
Для оценки потенциальной активности конкретного антагониста в терапии аллергической астмы антагонист может быть испытан in vitro при определении пролиферации клеток, как подробно описано в Примерах 5 и 6. Кроме того, период полураспада в плазме модифицированного антагониста рецептора мутеина IL-4 может быть измерен in vivo при изучении фармакокинетики у крыс, как описано в Примере 6.
(г) Фармацевтические композиции.
Любой из модифицированных антагонистов рецепторов мутеина IL-4, описанных выше, может быть в составе фармацевтической композиции, содержащей фармацевтически приемлемый носитель. Фармацевтически приемлемый носитель предпочтительно является непирогенным. Композиция может вводиться сама по себе или в сочетании с, по меньшей мере, одним другим агентом, таким как стабилизатор, который может быть введен в любом стерильном биосовместимом фармацевтическом носителе, включая, без ограничения, физиологический раствор, забуференный физиологический раствор, декстрозу и воду. Можно применять различные водные носители, например, 0,4% физиологический раствор, 0,3% глицин и т.п. Эти растворы стерильны и обычно не содержат частиц. Эти растворы могут быть стерилизованы обычными, хорошо известными методами стерилизации (например, при фильтрации).
Если требуется, композиции могут содержать фармацевтически приемлемые вспомогательные вещества. Приемлемые вспомогательные вещества, предпочтительно, являются нетоксичными для реципиентов в применяемых дозах и концентрациях. Фармацевтическая композиция может содержать вспомогательные вещества для модификации, сохранения или стабилизации, например, рН, осмолярности, вязкости, прозрачности, цвета, изотоничности, запаха, стерильности, стабильности, скорости растворения или высвобождения, адсорбции или проникновения композиции. Подходящие компоненты составов включают, без ограничения, аминокислоты (такие как глицин, глютамин, аспарагин, аргинин или лизин), антимикробные агенты, антиоксиданты (такие как аскорбиновая кислота, сульфит натрия или кислый сульфит натрия), буферные вещества (такие как борат, бикарбонат, Tris-HCl, цитраты, фосфаты или органические кислоты), агенты, придающие объем (например, маннит или глицин), хелатирующие агенты (такие как этилендиаминтетрауксусная кислота (EDTA)), комплексообразователи (такие как кофеин, поливинилпирролидон, бета-циклодекстрин или гидроксипропил-бета-циклодекстрин), наполнители, моно-сахариды, дисахариды и другие углеводы (такие как глюкоза, манноза или декстрины), белки (такие как альбумин сыворотки, желатин или иммуноглобулины), красители, ароматизаторы и разбавители, эмульгаторы, гидрофильные полимеры (такие как поливинилпирролидон), низкомолекулярные полипептиды, солеобразующие противоионы (такие как натрий), консерванты (такие как бензалконийхлорид, бензойная кислота, салициловая кислота, тимерозал, фенетиловый спирт, метилпарабен, пропилпарабен, хлоргексидин, сорбиновая кислота или перекись водорода), растворители (такие как глицерин, полипропиленгликоль или полиэтиленгликоль), сахарные спирты (такие как маннит или сорбит), суспендирующие агенты, поверхностно-активные вещества или смачивающие агенты (такие как pluronics, ПЭГ, эфиры сорбитана, полисорбаты, такие как полисорбат 20 или полисорбат 80, тритон, трометамин, лецитин, холестерин или тилоксапал), агенты, повышающие стабильность (такие как сахароза или сорбит), агенты, повышающие тоничность (такие как галоиды щелочных металлов, предпочтительно, хлорид натрия или калия или маннит-сорбит), носители для доставки, разбавители, эксципиенты и/или фармацевтические адъюванты. См. Remington's Pharmaceutical Sciences (18th Ed., A.R.Gennaro, ed., Mack Publishing Company, 1990).
Концентрация антагониста по изобретению в таком фармацевтическом составе может меняться в широких пределах, а именно, от менее 0,5%, обычно 1% или, по меньшей мере, около 1%, до 15 или 20% по весу и выбирается, в основном, из расчета на объемы жидкости, вязкости и т.д. в соответствии с конкретным выбранным методом введения. Если это желательно, в фармацевтическую композицию может быть включен более чем один тип антагониста, например, с разной величиной Кd к рецептору IL-4.
Композиции могут вводиться пациенту сами по себе или в комбинации с другими агентами, лекарствами или гормонами. В добавление к активным ингредиентам эти фармацевтические композиции могут содержать подходящие фармацевтически приемлемые носители, включающие эксципиенты и вспомогательные добавки, которые облегчают введение активных соединений в препараты, которые могут быть использованы фармацевтически.
Приемлемые препараты предпочтительно являются нетоксичными для реципиентов в применяемых дозах и концентрациях.
Фармацевтическая композиция может содержать компоненты для модификации, сохранения или стабилизации, например, рН, осмолярности, вязкости, прозрачности, цвета, изотоничности, запаха, стерильности, стабильности, скорости растворения или высвобождения, адсорбции или проникновения композиции. Подходящие компоненты составов включают, без ограничения, аминокислоты (такие как глицин, глютамин, аспарагин, аргинин или лизин), антимикробные агенты, антиоксиданты (такие как аскорбиновая кислота, сульфит натрия или кислый сульфит натрия), буферные вещества (такие как борат, бикарбонат, Tris-HCl, цитраты, фосфаты или органические кислоты), агенты, придающие объем (например, маннит или глицин), хелатирующие агенты (такие как этилендиаминтетрауксусная кислота (EDTA)), комплексообразователи (такие как кофеин, поливинилпирролидон, бета-циклодекстрин или гидроксипропил-бета-циклодекстрин), наполнители, моносахариды, дисахариды и другие углеводы (такие как глюкоза, манноза или декстрины), белки (такие как альбумин сыворотки, желатин или иммуноглобулины), красители, ароматизаторы и разбавители, эмульгаторы, гидрофильные полимеры (такие как поливинилпирролидон), низкомолекулярные полипептиды, солеобразующие противоионы (такие как натрий), консерванты (такие как бензалконийхлорид, бензойная кислота, салициловая кислота, тимерозал, фенетиловый спирт, метилпарабен, пропилпарабен, хлоргексидин, сорбиновая кислота или перекись водорода), растворители (такие как глицерин, полипропиленгликоль или полиэтиленгликоль), сахарные спирты (такие как маннит или сорбит), суспендирующие агенты, поверхностно-активные вещества или смачивающие агенты (такие как pluronics, ПЭГ, эфиры сорбитана, полисорбаты, такие как полисорбат 20 или полисорбат 80, тритон, трометамин, лецитин, холестерин или тилоксапал), агенты, повышающие стабильность (такие как сахароза или сорбит), агенты, повышающие тоничность (такие как галоиды щелочных металлов, предпочтительно, хлорид натрия или калия или маннит-сорбит), носители для доставки, разбавители, эксципиенты и/или фармацевтические адъюванты. См. Remington's Pharmaceutical Sciences (18th Ed., A.R.Gennaro, ed., Mack Publishing Company, 1990).
Оптимальная фармацевтическая композиция может быть получена специалистом в данной области в зависимости, например, от намечаемого пути введения, формы доставки и желательной дозы. См., например. Remington's Pharmaceutical Sciences, supra. Такие композиции могут влиять на физическое состояние, стабильность, скорость in vivo высвобождения и скорость in vivo клиренса нуклеиновой кислоты или модулятор плотности кости по изобретению.
Первичный наполнитель или носитель в составе фармацевтической композиции может быть водным или неводным. Например, подходящим носителем для инъекции может быть вода, физиологический раствор или искусственная спинномозговая жидкость, возможно, дополненная другими веществами, типичными для композиций для парентерального введения. Примерами носителей являются также нейтральный буферный физиологический раствор или физиологический раствор, смешанный с альбумином сыворотки. Другие примеры фармацевтических композиций содержат Tris-буфер с величиной рН около 7,0-8,5 или ацетатный буфер с рН около 4,0-5,5, которые могут также включать сорбит или его подходящий заменитель. Согласно одному из вариантов изобретения фармацевтические композиции по изобретению могут быть приготовлены для хранения путем смешения выбранных компонентов с желательной степенью чистоты с возможными добавками (Remington's Pharmaceutical Sciences, supra) в виде лиофилизированного осадка или водного раствора. Кроме того, композиция может быть в виде лиофилизата, содержащего соответствующие эксципиенты, такие как сахароза.
Фармацевтические композиции могут быть приготовлены для парентеральной доставки. Композиции могут также получаться для ингаляции или для доставки через пищеварительный тракт, например, оральной доставки. Приготовление таких фармацевтически приемлемых композиций известно специалистам.
Компоненты композиции содержатся в концентрациях, которые приемлемы для места введения. Например, буферные вещества применяют для поддержания композиции при физиологическом рН или слегка меньшем значении рН, обычно, в интервале от примерно 5 до примерно 8.
Когда используется парентеральное введение, терапевтические композиции по изобретению могут быть в виде апирогенного, парентерально приемлемого водного раствора, содержащего желательное вещество по изобретению в фармацевтически приемлемом носителе. Особенно подходящим носителем для парентеральной инъекции является стерильная дистиллированная вода, в которой вещество получается в виде стерильного изотонического раствора, надлежащим образом стерилизованного.
Другой препарат может содержать вещество по изобретению вместе с таким агентом, как инъецируемые микросферы, биоразрушаемые частицы, полимерные соединения (такие как полимолочная кислота или полигликолевая кислота), гранулы или липосомы, которые обеспечивают регулируемое или пролонгированное высвобождение продукта, который затем может быть доставлен при помощи инъекции депо. Можно также применять гиалуроновую кислоту, которая промотирует пролонгированное нахождение в циркуляционной системе. Другие подходящие средства для введения вещества по изобретению включают имплантируемые системы для доставки лекарств.
Согласно одному варианту изобретения фармацевтическая композиция может быть получена для введения путем ингаляции. Например, нуклеиновая кислота или модулятор плотности кости по изобретению могут быть в составе сухого порошка для ингаляции. Ингаляционные растворы также могут быть получены с пропеллентом для доставки аэрозоля. Согласно другому варианту растворы могут вводиться при помощи небулайзера. Введение в легкие описано в заявке WO 94/20069, где раскрыто введение в легкие химически модифицированных белков.
В других вариантах составы могут быть введены перорально. Согласно одному из вариантов изобретения нуклеиновые кислоты или модуляторы плотности кости по изобретению, которые вводятся таким путем, могут содержаться вместе с теми носителями, которые обычно используются при получении твердых дозированных форм, таких как таблетки или капсулы, или без этих носителей. Например, может быть получена капсула с целью высвобождения активной части состава в том месте желудочно-кишечного тракта, где максимальна биодоступность и минимизировано досистемное разложение. Для обеспечения абсорбции антагониста или модулятора по изобретению могут включаться дополнительные агенты. Могут также применяться разбавители, ароматизаторы, низкоплавкие воски, растительные масла, смазывающие агенты, суспендирующие агенты, дезинтеграторы для таблеток и связующие.
Другие фармацевтические композиции могут включать эффективное количество нуклеиновых кислот или модуляторов плотности кости по изобретению в смеси с нетоксичными эксципиентами, которые пригодны для изготовления таблеток. Путем растворения таблеток в стерильной воде или другом подходящем носителе могут быть получены растворы в единичной дозированной форме. Подходящие эксципиенты включают, без ограничения, инертные разбавители, такие как карбонат кальция, карбонат или бикарбонат натрия, лактоза или фосфат кальция; или связующие, такие как крахмал, желатин или смола акации; или смазывающие агенты, такие как стеарат магния, стеариновая кислота или тальк.
Другие фармацевтические композиции очевидны для специалистов, они включают нуклеиновые кислоты или модуляторы плотности кости по изобретению в составе композиций для пролонгированной или регулируемой доставки. Способы получения различных других средств для пролонгированной или регулируемой доставки, например, липосомных носителей, биоразлагаемых микрочастиц или пористых гранул и депо для инъекций, хорошо известны специалистам. См., например, PCT/US93/00829, в которой описано регулируемое высвобождение пористых полимерных микрочастиц для доставки фармацевтических композиций.
Дополнительные примеры препаратов с пролонгированным высвобождением включают полупроницаемые полимерные матрицы в виде формованных изделий, например, пленок или микрокапсул. Матрицы с пролонгированным высвобождением могут включать сложные полиэфиры, гидрогели, полилактиды (патент США №3773919 и патент ЕР №058481), сополимеры L-глутаминовой кислоты и гамма-этил-L-глутамата (Sidman et al., 1983, Biopolymers 22:547-56), поли-(2-гидроксиэтилметакрилат) (Langer et al., 1981, J.Biomed. Mater. Res. 15:167-277 и Langer, 1982, Chem. Tech. 12:98-105), сополимер этилена с винилацетатом (Langer et al., supra) или поли-D(-)-3-гидроксимасляную кислоту (патент ЕР №133988). Композиции пролонгированного высвобождения могут также включать липосомы, которые можно получить одним из известных способов. См., например, Eppstein et al., 1985, Proc. Natl. Acad. Sci. USA 82:3688-92; и European Patent Nos. 036676, 088046 и 143949.
Фармацевтическая композиция для введения in vivo обычно должна быть стерильной. Этого можно достигнуть путем фильтрации через стерильные фильтрующие мембраны. Если композиция лиофилизирована, стерилизация с применением указанного метода может быть проведена или до, или после лиофилизации и восстановления. Композиция для парентерального введения может храниться в лиофилизированной форме или в растворе. Кроме того, парентеральные композиции обычно помещены в контейнер, имеющий стерильное входное отверстие, например, пакет для внутривенного раствора или емкость с пробкой, через которую вводится гиподермальная игла для инъекции.
Фармацевтические композиции по изобретению могут быть введены любыми методами, описанными в данной заявке, включая, без ограничения, оральный, внутривенный, внутримышечный, внутриартериальный, интрамедуллярный, интратекальный, интравентрикулярный, трансдермальный, подкожный, интраперитониальный, интраназальный, парентеральный, топический, сублингвальный или ректальный.
После приготовления фармацевтических композиций они могут быть помещены в соответствующий контейнер с этикеткой для лечения указанного состояния. Такая этикетка будет включать указание количества, частоты и метода введения.
(г) Терапевтические способы.
Данное изобретение предусматривает способы ослабления симптомов расстройства за счет связывания альфа-цепи рецептора IL-4 и ингибирования активности, опосредованной IL-4 и IL-13.
Эти расстройства включают, без ограничения, гиперреактивность дыхательных путей и воспаление дыхательных путей, включая рекруитмент и активацию тучных клеток, эозинофилов и лимфоцитов, связанные с астмой и другими иммунологическими или аллергическими нарушениями.
Согласно одному варианту изобретения терапевтически эффективная доза модифицированного антагониста рецептора мутеина IL-4 по изобретению и/или фармацевтической композиции по изобретению вводится пациенту, имеющему расстройство, характеризующееся повышенной активностью IL-4 и IL-13, как расстройства, указанные выше.
(д) Определение терапевтически эффективной дозы.
Определение терапевтически эффективной дозы известно специалистам в данной области. Терапевтически эффективная доза обозначает количество антагониста, которое применяется для эффективного лечения астмы, по сравнению с эффективностью, которая является очевидной в отсутствие терапевтически эффективной дозы.
Терапевтически эффективная доза может быть определена вначале на животных моделях, обычно крыс, мышей, кроликов, собак, свиней или приматов. Животная модель может также применяться для определения соответствующего интервала концентраций и метода введения.
Такая информация может затем быть использована для определения подходящих доз и методов введения людям.
Терапевтическая эффективность и токсичность, например, ED50 (доза, являющаяся терапевтически эффективной у 50% популяции) и LD50 (доза, являющаяся летальной у 50% популяции) человеческого антагониста могут быть определены стандартными фармацевтическими методами в клеточных культурах или экспериментальных животных. Отношение токсичной дозы к дозе, терапевтически эффективной, представляет собой терапевтический индекс и может быть выражено как отношение LD50/ЕD50.
Фармацевтические композиции, которые обладают высокими терапевтическими индексами, являются предпочтительными. Данные, полученные при изучении животных, применяются для определения интервала доз для людей. Дозы, содержащиеся в таких композициях, находятся, предпочтительно, в пределах циркулирующих концентраций, которые включают ED50 с небольшой токсичностью или без токсичности. Дозы варьируются в этом интервале, который зависит от применяемой дозированной формы, чувствительности пациента и метода введения.
Точная доза определяется практикующим врачом на основе факторов, относящихся к пациенту, который подвергается лечению. Дозы и метод введения регулируются таким образом, чтобы обеспечить достаточные уровни антагониста или поддержать желательный эффект. Факторы, которые нужно принять во внимание, включают серьезность болезни, общее состояние здоровья пациента, возраст, вес и пол субъекта, режим питания, время и частоту введения, комбинацию(-и) лекарств, чувствительность реакции и переносимость/реакция терапии.
Фармацевтические композиции длительного действия могут вводиться каждые 3-4 дня, каждую неделю или один раз каждые две недели в зависимости от величины периода полураспада и скорости клиренса конкретного состава.
Полинуклеотиды, кодирующие модифицированные антагонисты рецептора мутеина IL-4 по изобретению, могут быть построены и введены в клетку ex vivo или in vivo с использованием хорошо разработанных методов, включая, без ограничения, перенос ДНК, опосредованной трансферрином-поликатионом, трансфекцию с голыми или инкапсулированными нуклеиновыми кислотами, клеточное слияние, опосредованное липосомами, внутриклеточную транспортацию гранул латекса с покрытием из ДНК, слияние протопластов, вирусную инфекцию, электропорацию, «генное ружье» и трансфекцию, опосредованную DEAE или фосфатом кальция.
Эффективные in vivo дозы антагониста находятся в пределах от примерно 5 мкг до примерно 50 мкг/кг, примерно от 50 мкг до примерно 5 мкг/кг, примерно от 100 мкг до примерно 500 мкг/кг веса пациента и от примерно 200 мкг до примерно 250 мкг/кг веса пациента. При введении полинуклеотидов, кодирующих антагонисты, эффективные in vivo дозы находятся в пределах от примерно 100 нг до примерно 200 нг, от 500 нг до примерно 50 мг, от примерно 1 мкг до примерно 2 мг, от примерно 5 мкг до примерно 500 мкг и от примерно 20 мкг до примерно 100 мкг ДНК.
Метод введения фармацевтических композиций по изобретению, содержащих модифицированные антагонисты рецептора мутеина IL-4, может быть любым методом доставки антагониста хозяину. Фармацевтические композиции по изобретению особенно подходят для парентерального введения, а именно, подкожного, внутримышечного, внутривенного, внутритрахеального или интраназального и другими методами введения в легкие.
Все патенты и заявки на патент, цитируемые в данной заявке, включены в нее в качестве ссылок. Вышеприведенное описание раскрывает данное изобретение в общем. Более подробно оно описано в нижеследующих конкретных примерах, которые приведены только для иллюстрации изобретения и не ограничивают его объем.
Примеры.
Пример 1.
Рекомбинантное получение цистеиновых мутеинов IL-4-RA и IL-4-RE.
Для рекомбинантной экспрессии IL-4 была выбрана система экспрессии рЕТ Directional TOPO® (Invitrogen). Эта система использует высокоэффективную одностадийную стратегию «TOPO® Cloning» для осуществления прямого клонирования продукта PCR с тупым концом и Т71ас промотор для IPTG-индуцируемой экспрессии с высокой степенью нужного гена в E.coli. Дополнительные характеристики включают lacI ген для уменьшения базальной транскрипции, источник pBR322 для репликации и сохранения плазмиды и ген, резистентный к ампициллину для селекции.
IL-4 клонировали в вектор pET101/D-TOPO для продуцирования рекомбинантного белка IL-4. Олигонуклеотидные праймеры приведены в Таблице 4. Был создан передний PCR праймер с 5'САСС липким концом для облегчения прямого клонирования, с уникальным сайтом рестрикционного фермента NdeI для субклонирования и начальным стартовым кодоном ATG. Обратный PCR праймер включал два стоп-кодона для препятствия введению с-терминальных меток и уникальный сайт рестрикционного фермента BamHI для субклонирования. С использованием ранее клонированного человеческого IL-4 в качестве темплата был получен PCR продукт IL-4 с тупым концом. Продукт был очищен на геле и его инкубировали с раствором соли и вектором ТОРО® в течение 5 минут при комнатной температуре для осуществления прямого клонирования в вектор pET101/D-TOPO. Рекомбинантный вектор трансформировали в химически компетентных One Shot ТОР10 E.coli. Рекомбинантную плазмидную ДНК применяли для секвенирования ДНК для подтверждения правильной последовательности.
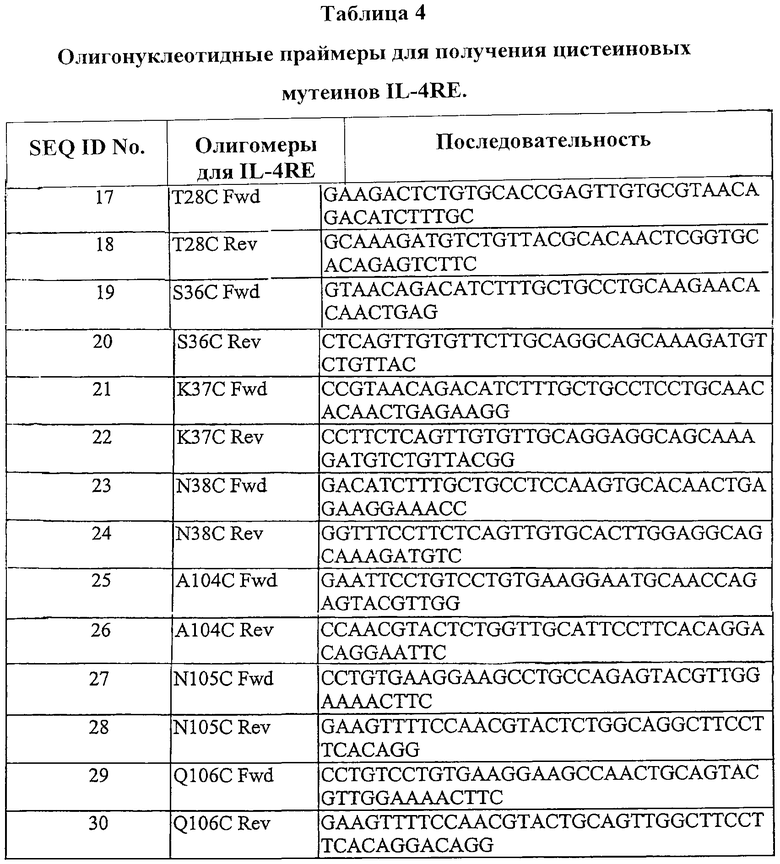
IL-4/pET101/D-TOPO служил в качестве темплата для получения цистеиновых мутеинов IL-4RE при помощи набора QuikChange® Site-Directed Mutagenesis Kit, Strategene. Каждый цистеиновый мутеин получали с применением двух олигонуклеотидных праймеров, каждый из которых комплементарен противоположным нитям вектора, и содержался кодон TGC или GCA для введения желательной мутации цистеина. В Таблице 4 перечислены праймеры, используемые для получения мутеинов IL-4RE. С использованием праймеров циклизации и условий, указанных в протоколе изготовителя, была получена мутационная плазмида, содержащая ступенчатые ники. Этот продукт был обработан DpnI эндонуклеазой в течение 1 часа при 37°С для переваривания метилированного немутированного темплата родительской ДНК. ДНК, обработанная DpnI была трансформирована в суперкомпетентных клетках XL-1 Blue, где были восстановлены ники в мутированной плазмиде. Мутагенную ДНК плазмиды анализировали в соответствии со стандартными методами секвенирования для подтверждения правильной последовательности.
Пример 2.
Рекомбинантная экспрессия и очистка.
Клетки BL21 Star (DE3) One Shot (Invitrogen), которые трансформировали при помощи белка, содержащего плазмиды, были охарактеризованы для оптимальной экспрессии и выращивались при 37°С до достижения величины OD600, равной примерно 0,4, и индуцировали с помощью 1 мМ IPTG (Invitrogen) в течение 3 ч при 37°С. Один литр клеток таблетировали при скорости 13000 об/мин в течение 10 мин, взвешивали и хранили при -80°С. Замороженные таблетки клеток ресуспендировали в 8 мл буфера, деструктирующего клетки (0,1 М фосфатного буфера с рН 7,3, 0,1% Triton X100, 1 мМ EDTA) на грамм клеток и обрабатывали ультразвуком 4х в течение 1 мин с интервалами 1 мин. Клеточный лизат удаляли центрифугированием при 35000 г в течение 10 мин. Таблетки клеток затем промывали 2-3х в суспензии в 30 мл буфера, деструктирующего клетки, обрабатывали ультразвуком в течение 1 мин и центрифугировали. Конечные таблетки клеток, тела включения, хранили при -20°С. Тела включения ресуспендировали в 5 мл солюбилизирующего буфера (0,2М Tris, рН 9, 7М гуанидинхлорида) на грамм клеток. Добавляли реагенты сульфотолиза (0,16 г сульфита натрия, 0,08 г тетратионата калия на грамм клеток) и перемешивали тела включения при комнатной температуре в течение 2 часов. Нерастворенные компоненты затем удаляли центрифугированием при 35000 g в течение 20 мин, оставались солюбилизированные тела включения. Тела включения затем пропускали на колонке вытеснительной хроматографии Superdex200 size (Akta) для изоляции белка. Колонку уравновешивали 2 объемами колонки (CV) 6M смеси гуанидингидрохлорид/PBS, рН 7, со скоростью истечения 1 мл/мин, белок элюировали 1,5 CV. Собирали пиковые фракции (каждая 1,5 мл) и подвергали электрофорезу на геле 12% или 4-20% Bis-Tris-SDS. Собирали фракции, содержащие белок, и добавляли конечную концентрацию 7,5 мМ DTT для уменьшения молекул белка. После инкубации в течение 2 ч при комнатной температуре смесь разбавляли 5х водой и подвергали диализу в 4,5 л 3 мМ NaH2PO4, 7 мМ Na2HPO4, 2 мМ КСl, 120 мМ NaCl. Диализ продолжали 3-4 дня, подавая свежий буфер, по меньшей мере, 3 раза. Диализованный продукт затем фильтровали через фильтр 0,2 мкм и доводили рН до 5 уксусной кислотой. Колонку уравновешивали 10 CV буфера 1 (25 мМ ацетата аммония, рН 5), создавали градиент в течение 20 мин до 100% буфера В (25 мМ ацетата аммония, рН 5/ 1М NaCl). Собирали пиковые фракции (1,5 мл каждая) и подвергали электрофорезу на геле 12% или 4-20% Bis-Tris-SDS. Фракции, содержащие полученный продукт, собирали и разбавляли 2х буфером А (0,1% TFA/вода). Затем белок хроматографировали методом ЖХВР с обращенной фазой С4 (Beckman system Gold), используя петлю 5 мл и скорость истечения 1 мл/мин по следующей программе: 10% буфера А во время инъекции, 10 мин градиент до 40% буфера В (0,1% TFA/ACN), 30 мин градиент до 50% буфера В и 5 мин градиент до 100% буфера В. Собирали пиковые фракции (0,5 мл каждая) и подвергали электрофорезу на геле 12% или 4-20% Bis-Tris-SDS. Фракции, содержащие белок, высушивали и ресуспендировали в 0,1М MES, рН 6,1 для анализа и определений.
Пример 3.
Сайт-специфическое ПЭГилирование цистеина и очистка.
Для ПЭГилирования цистеина, содержащего мутеины IL4 RA, был разработан протокол с использованием стабильной тиоэфирной связи между сульфгидрильной группой белка и мальимидной группой линейного производного метоксиполиэтиленгликоль-малеимида 22 kD (Nektar Therapeutics). К 600M белка, растворенного в реакционном буфере ОЛМ MES, рН 6, добавляли 2-х-молярный избыток mПЭГ-MAL 22 kD. Через 0,5 ч выдержки при комнатной температуре реакцию обрывали 2М избытком цистеина по отношению к mПЭГ-MAL 22 kD (см. чертеж). ПЭГилированный белок очищали от не прореагировавшего mПЭГ-MAL 22 kD (обработанного цистеином) и не прореагировавшего цистеинового мутеина IL4 RA при помощи катионного обмена и вытеснительной хроматографии. Сырые реакционные смеси подавали на катионообменные колонки Vivapure Mini S (Vivascience), уравновешенные 0,4 мл 0,1M MES, pH 6. Колонки дважды промывали 0,4 мл 0,1М MES, pH 6 с последующим центрифугированием 2000х g после каждой промывки. Образцы затем вымывали из колонки центрифугированием при помощи 0,4 мл 0,6М NaCl/0,1M MES, pH 6. Элюированные фракции объемом 0,4 мл загружали в колонку ЖХВР TSK-GEL G2000SWYL (Tosoh Biosep), используя систему Gold Beckman. Образцы вновь растворяли в фосфатно-буферном физиологическом растворе (Dulbecco's PBS), представляющем собой мобильную фазу со скоростью истечения 1 мл/мин в течение 30 мин. Пиковые фракции (0,5 мл) собирали и подвергали электрофорезу на геле 4-12% Bis-Tris-SDS для выделения ПЭГилированного белка. Фракции, содержащие полученный продукт, собирали и концентрировали, используя устройство Ultrafree Biomax-5 (Millipore) по протоколу производителя, до получения примерно 60 мкМ (или ~ 1 мг/мл) для анализа и in vitro испытаний. Конечная концентрация ПЭГилигированных белков была определена методом аминокислотного анализа. Конечные выходы приведены в Таблице 5.
Пример 4.
Реакция связывания с рецептором IL-4 с помощью BiaCore.
Рецептор IL-4 иммобилизировали на сенсорном чипе для исследований BiaCore СМ5 путем присоединения аминогруппы. Поверхность сенсора активировали EDC/NHS импульсом. Рецептор IL-4 растворяли в 10 мМ ацетатном буфере (рН 5,0) и впрыскивали в элемент 2 с проточным электролитом с последующей импульсной подачей 1,0 М этаноламина-НСl для деактивации поверхности. Степень иммобилизации рецептора составляла - 3000 RU. Элемент 1 с проточным электролитом также активировали без лиганда, чтобы он функционировал как контрольный. Для проведения кинетического анализа использовали BiaCore Wizard. Кандидаты-антагонисты IL4RE разбавляли MBS-EP (разделяющий буфер) и впрыскивали со скоростью 30 мкл/мин в течение 30 мин при времени диссоциации 15 мин. Регенерацию чипа проводили путем двух 30-секундных инъекций 10 мМ глицина, рН 2,5, (скорость течения 100 мкл/мин) до базовой линии перед следующей инъекцией в серии концентраций. Величины константы диссоциации (КД) определяли для каждого кандидата, исходя из кинетики прямого связывания (Таблица 5). Результаты показывают, что у всех конструкций IL4-RE-A104C, IL4-RE-N105C и IL4-RE-Q106C константы диссоциации меньше 0,6 мМ.
Пример 5.
Определение пролиферации TF-1-клеток.
Пролиферативный ответ TF-1-клеток на IL-4 (0,5 нг/мл, 0,033 нМ) или IL-13 (0,5 нг/мл, 0,416 нМ) использовали для оценки функциональной антагонистической активности IL-4RE. Для этого TF-1-клетки культивировали в течение 2-4 дней в планшете с 96 лунками (1×104/лунку, объемом 100 мкл) в RPMI+10% сыворотки с IL-4, IL-13 и IL-4RE или без них. Обработку GM-CSF использовали в качестве положительного контроля. За 24 часа до последнего считывания в каждую лунку добавляли 10 мкл AlamarBlue (10 об.%). Измеряли флуоресценцию при 530/590 нм, используя WALLAC Victor 2. Ингибирующую концентрацию (IС50) рассчитывали по титрационной дозе кандидата IL-4RE. Данные биоанализа для TF-1 и ингибирования IL-4 и IL-13 приведены в Таблице 6. Результаты показывают, что конструкции IL4-RE-К37С, IL4-RE-N38C и IL4-RE-A104C имеют величины IС50, сравнимые с IC50 для IL-4-RA в присутствии IL-4 или IL-13.
Пример 6.
Определение пролиферации первичных клеток.
Пролиферативный ответ первичных клеток человека (Т- и В-клеток) на IL-4 оценивали после предварительной обработки IL-4RE. Периферические мононуклеарные кровяные клетки (PBMCs) выделяли из периферической крови и некоторые обрабатывали РНА в течение 4 дней для индуцирования образования бластных Т-клеток. PBMCS также обрабатывали анти-СD40 для активации активности В-клеток и сразу же использовали. Клетки высевали в планшеты с 96 лунками (105 клеток/лунку). Препараты бластных Т-клеток и В-клеток, обработанных РНА, стимулировали в течение 3 дней IL-4 (10 нг/мл, 0,667 нМ) в присутствии меняющихся концентраций IL-4RE. Введение меченного тритием тимидина в последние 20 часов инкубации использовали как индикатор пролиферации. Результаты этих определений показаны в Таблице 7. Эти результаты показывают, что все ПЭГилигированные конструкции обладали величиной IС50, почти в 5 раз превышающей IС50 IL-4RA в двух анализах первичных клеток.
Пример 7.
Изучение фармакокинетики на крысах.
Использовали взрослых самцов крыс Spraque-Dawley. Крыс канюлировали катетером в яремную вену для забора образцов крови. Кроме того, крысам в группе с внутривенным (IV) введением вводили катетеры в бедренную вену для введения лекарства.
Крысам вводили или IL-4RA, или модифицированный антагонист рецептора мутеина IL-4 в дозах 1 и 0,5 мг/кг, соответственно. Использовали и IV (внутривенный) и SC (подкожный) методы введения. IV дозу вводили инъекцией непосредственно в катетер, постоянно находящийся в бедренной вене. SC доза вводилась путем инъекции в дорсальную торакальную область. В каждой группе были 3 крысы.
После инъекции в виде болюса (IV или SC) отбирали образцы крови перед введением дозы и в заданные моменты времени до 168 часов после введения дозы. Центрифугирование образцов крови начинали в течение 1 часа после отбора. Плазму собирали и помещали на сухой лед при примерно -70°С.
Концентрации IL-4RA и модифицированного мутеина в плазме определяли количественно методом иммуноферментного анализа. Анти-1b-4-антитело использовали в качестве реагентов для покрытия и детектирования. Низший предел количественного определения этим методом составлял 0,2 нг/мл. Фармакокинетические параметры определяли методом компартментального анализа с применением WinNonlin (Pharsight, Mountain view, CA). Особенный интерес представляют оценка кинетики абсорбции и элиминации, объемы распределения, а также абсорбированные количества.
| название | год | авторы | номер документа |
|---|---|---|---|
| IL-1бета-СВЯЗЫВАЮЩИЕ АНТИТЕЛА И ИХ ФРАГМЕНТЫ | 2006 |
|
RU2518295C2 |
| СПОСОБЫ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ФИБРОЗА АНТАГОНИСТАМИ IL-21/IL-21R | 2006 |
|
RU2419450C2 |
| МУТЕИНЫ ЛИПОКАЛИНА СЛЕЗЫ, СВЯЗЫВАЮЩИЕ АЛЬФА IL-4 R | 2011 |
|
RU2569745C2 |
| КЛОСТРИДИАЛЬНЫЙ ТОКСИН NetB | 2008 |
|
RU2474587C2 |
| КОМПОЗИЦИИ Т-КЛЕТОК С НЕДОСТАТОЧНОСТЬЮ РЕЦЕПТОРОВ Т-КЛЕТОК | 2013 |
|
RU2653761C2 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИТЕЛ С УЛУЧШЕННЫМИ СВОЙСТВАМИ | 2011 |
|
RU2604811C2 |
| ПОЛИПЕПТИДЫ ТРАНСПОЗАЗЫ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2735700C2 |
| ГЕТЕРОДИМЕРНЫЕ ПОЛИПЕПТИДЫ IL-17 A/F И ВОЗМОЖНОСТИ ИХ ЛЕЧЕБНОГО ПРИМЕНЕНИЯ | 2007 |
|
RU2440134C2 |
| ИММУНОЦИТОКИНЫ НА ОСНОВЕ IL-15 И IL-R[альфа] ДОМЕНА SUSHI | 2012 |
|
RU2644671C2 |
| ПОЛИПЕПТИДЫ С НАПРАВЛЕННЫМ ДЕЙСТВИЕМ | 2006 |
|
RU2393874C2 |
Изобретение относится к области биотехнологии, конкретно к получению модифицированного антагониста рецептора мутеина IL-4 (IL-4RA), и может быть использовано для лечения заболеваний дыхательных путей, таких как астма, эмфизема или хронический бронхит. В модифицированной молекуле IL-4RA, которая ингибирует опосредованную IL-4 и IL-13 активность, аминокислотные остатки 37, 38 или 104 представляют собой цистеин. Полинуклеотидом, кодирующим указанный антагонист, в составе вектора экспрессии трансформируют клетку-хозяина и получают IL-4RA. Полученную молекулу IL-4RA ПЭГилируют и используют для устранения нарушений, связанных с повышенной активностью IL-4 и IL-13. Изобретение позволяет получить антагонист с более длительным периодом полураспада по сравнению с немодифицированным IL-4RA. 8 н. и 9 з.п. ф-лы, 1 ил., 7 табл.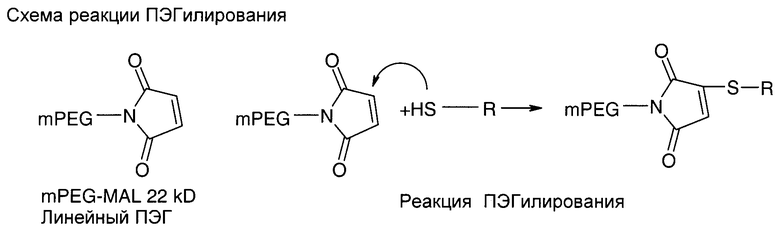
1. Очищенный полинуклеотид, предназначенный для получения модифицированного антагониста рецептора мутеина IL-4, содержащий
(а) нуклеотидную последовательность, указанную как SEQ ID NO:4, или SEQ ID NO:5, или SEQ ID NO:6, или
(б) нуклеотидную последовательность, кодирующую полипептид, содержащий аминокислотную последовательность, указанную как SEQ ID NO:12, или SEQ ID NO:13, или SEQ ID NO:14.
2. Вектор экспрессии, включающий полинуклеотид по п.1.
3. Клетка-хозяин, предназначенная для получения модифицированного антагониста рецептора мутеина IL-4, содержащая вектор экспрессии по п.2.
4. Способ получения модифицированного антагониста рецептора мутеина IL-4, включающий стадии:
(а) культивирования клетки-хозяина по п.3 в условиях, при которых антагонист экспрессируется, и
(б) очистки антагониста от культуры клетки-хозяина.
5. Способ получения модифицированного антагониста рецептора мутеина IL-4 в активной форме, включающий стадии:
а) культивирования клетки-хозяина по п.3 при условиях, когда экспрессируется антагонист;
б) рефолдинга антагониста в присутствии дитиотреитола и
в) очистки антагониста от культуры клетки-хозяина.
6. Способ по п.5, отличающийся тем, что он дополнительно включает стадии:
г) присоединения антагониста к небелковому полимеру и
д) очистки антагониста, присоединенного к небелковому полимеру.
7. Модифицированный антагонист рецептора мутеина IL-4, полученный способом по пп.4 и 5, у которого аминокислотные остатки 37, 38 или 104 представляют собой цистеин и который ингибирует опосредованную IL-4 и IL-13 активность.
8. Модифицированный антагонист рецептора мутеина IL-4, присоединенный к небелковому полимеру, полученный способом по п.6, у которого аминокислотные остатки 37, 38 или 104 представляют собой цистеин и который ингибирует опосредованную IL-4 и IL-13 активность.
9. Модифицированный антагонист рецептора мутеина IL-4 по п.8, отличающийся тем, что небелковый полимер выбран из группы, состоящей из полиэтиленгликоля, полипропиленгликоля и полиоксиалкиленов.
10. Модифицированный антагонист рецептора мутеина IL-4 по п.9, отличающийся тем, что он присоединен к небелковому полимеру через аминокислотный остаток в положении 37, 38 или 104 в IL-4.
11. Модифицированный антагонист рецептора мутеина IL-4 по п.8 или 9, отличающийся тем, что он имеет период полураспада в плазме, который, по меньшей мере, в 2-10 раз больше, чем у немодифицированного антагониста рецептора IL-4.
12. Модифицированный антагонист рецептора мутеина IL-4 по п.9, отличающийся тем, что аминокислотная последовательность представлена SEQ ID №12.
13. Модифицированный антагонист рецептора мутеина IL-4 по п.9, отличающийся тем, что аминокислотная последовательность представлена SEQ ID №13.
14. Модифицированный антагонист рецептора мутеина IL-4 по п.9, отличающийся тем, что аминокислотная последовательность представлена SEQ ID №14.
15. Применение модифицированного антагониста рецептора мутеина IL-4 по пп.7-14 для изготовления средства для лечения у человека нарушения, связанного с повышенной активностью IL-4 и IL-13.
16. Применение по п.15, отличающееся тем, что нарушение представляет собой астму, хроническую обструктивную болезнь легких или связанные с этим легочные состояния.
17. Применение по п.16, отличающееся тем, что хроническая обструктивная болезнь легких является эмфиземой или хроническим бронхитом.
| US 6130318, 10.10.2000 | |||
| ВЫСОКОАФИННЫЕ МУТЕИНЫ ИНТЕРЛЕЙКИНА-4 | 1997 |
|
RU2202364C2 |
| KREITMAN R.J | |||
| et al., Site-specific conjugation to interieukin 4 containing mutated cysteine residues produces interieukin 4-toxin conjugates with improved binding and activity, Biochemistry, 1994, v.33, №38, p.11637-11644. | |||
Авторы
Даты
2010-05-20—Публикация
2004-07-20—Подача