Изобретение - способ удлинения поврежденного нерва - относится к области медицины, в частности к травматологии, и может быть использовано для возмещения травматических дефектов нервов.
Известен способ лечения последствий травм нервного ствола, включающий мобилизацию участка нерва, его фиксацию и дозированную тракцию с помощью специального устройства до получения необходимой длины, резекцию невромы, коррекцию концов, нейрографию и укладку нерва в обход участка рубцово-измененных тканей (Патент РФ №2080826, опубл. 10.06.97, Бюл.№16).
Однако данный способ используется при застарелых повреждениях нерва и не предназначен для возмещения дефектов свежеповрежденного нерва.
Известен способ дистракционного удлинения проксимальной культи нерва путем тракции с помощью лигатур, проведенных через его рубцовую культю (Волкова A.M. Хирургия кисти. - Екатеринбург, Средне-Урал. книжное изд-во, 1991 г., с.304).
Однако используемые в данном способе приемы фиксации культи нерва не обеспечивают возможности крепления к оболочкам свежеповрежденного нерва. Кроме того, удлинение одной проксимальной культи не только увеличивает продолжительность собственно замещения дефекта нерва, но и сроки его функционального восстановления.
Задачей изобретения является разработка способа, обеспечивающего удлинение поврежденного нерва в ранние, оптимальные для регенерации и последующего восстановления функции сроки после травмы.
Указанная задача решается тем, что в способе удлинения поврежденного нерва, включающем обработку концов культей нерва, их фиксацию и дозированную тракцию с помощью устройства на необходимую величину с последующим сшиванием конец в конец, фиксацию культей нерва к тракционным элементам устройства осуществляют швами, сочетающими продольные и поперечные стежки, через оболочки нерва, после чего эти концы изолируют от окружающих тканей, одномоментно устраняют между ними ретракционный диастаз, а затем производят дозированную тракцию одновременно проксимальной и дистальной культей нерва, причем суточное увеличение длины каждой из них осуществляют минимум за 8 микроперемещений в течение 16 часов.
Изобретение поясняется описанием, экспериментальными данными, подтверждающими эффективность его применения, а также иллюстративным материалом, на котором изображено:
Фиг.1 - схема крепления культи нерва к наконечнику тракционной спицы.
Фиг.2 - Эпиневрий (Э) и периневрий (П) удлиненного периферического отрезка нерва. Стрелками обозначены наружная (вверху) и внутренняя (внизу) поверхности периневрия. Импрегнация по Рассказовой. Инструментальное увеличение 500×.
Фиг.3 - Гипертрофия биосинтетического аппарата в периневральной клетке 5 мм проксимальнее наконечника тракционного проводника. Электронограмма. Инструментальное увеличение 40000×.
Фиг.4 - Разные участки дистального отрезка нерва. Срок опыта 33 дня, 28 дней тракции. А - зона удлинения: тяжи леммоцитов прямолинейны, продукты валлеровской дегенерации в их цитоплазме отсутствуют, ядра «светлые и сочные». Б - участок дистальнее зоны удлинения: бюнгнеровы ленты извиты, «плотные» ядра. Импрегнация по Рассказовой. Инструментальное увеличение 600×.
Фиг.5 - Продольный срез проксимального отрезка нерва в зоне удлинения. Срок эксперимента 19 дней, тракции 14 дней. Импрегнация по Рассказовой. Инструментальное увеличение 240×. Л - новообразованные тяжи леммоцитов между зонами реактивно измененных нервных волокон (1) и ретроградной дегенерации (2).
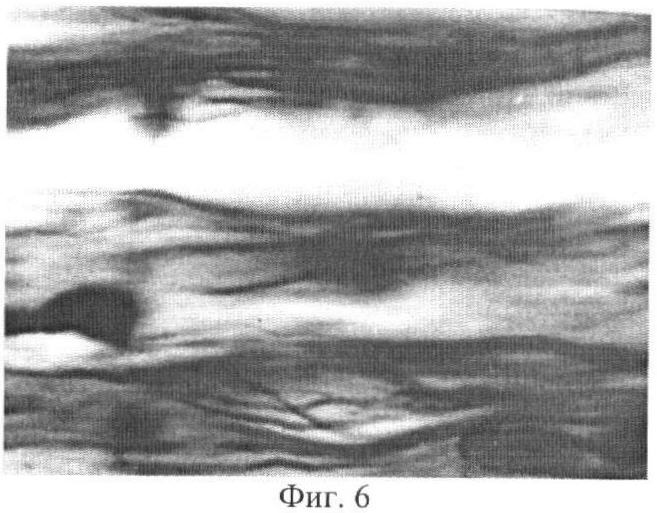
Фиг.6 - Невротизация зоны роста леммоцитарных тяжей пучками аксонов. 19 дней эксперимента, 14 дней тракции. Импрегнация по Рассказовой. Инструментальное увеличение 600х.
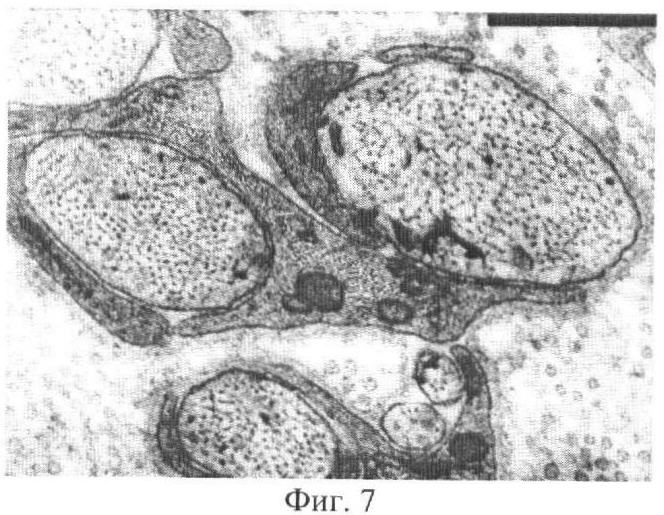
Фиг.7 - Регенерирующие нервные волокна в зоне удлинения. Срок опыта 33 дня, 28 дней тракции. Электронограмма. Инструментальное увеличение 40000×.
Фиг.8 - Миелинизированные волокна на продольном срезе. Собака №5596. Срок эксперимента 19 дней, тракции 14 дней. Окраска гематоксилином Карраци. Инструментальное увеличение 500×. 1 - нормальный перехват Ранвье. 2 - «удлиненный» перехват. 3 - вставочный интернодальный сегмент.
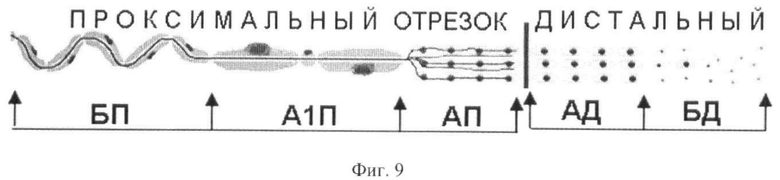
Фиг.9 - Схема зональной структуры отрезков удлиненного нерва перед нейроррафией (ее плоскость - красная линия). АП, А1П и БП - внутрипучковые зоны проксимального отрезка; АД и БД - внутрипучковые зоны дистального отрезка.
Фиг.10 - Чувствительные (а, б) и двигательные (в, г, д) концевые нервные приборы в передней большеберцовой (а, в) и икроножной (б, г, д) мышцах через 2 месяца после сшивания удлиненных отрезков седалищного нерва. Импрегнация по Рассказовой. Инструментальное увеличение 600×.
Способ осуществляется следующим образом.
При наличии показаний к восстановительной операции, после анестезии и обработки операционного поля осуществляют доступ к поврежденному участку нерва, производят его ревизию, выделяя противостоящие концы дистальной и проксимальной культей, которые при необходимости обрабатывают. В ране размещают тракционные элементы устройства, например спицы с наконечниками соответствующего типоразмера. Их свободные концы по планируемому направлению тракции разнонаправленно выводят из раны на поверхность кожи через проколы мягких тканей, а в наконечниках швами, сочетающими продольные и поперечные стежки, крепят концы культей нерва (Фиг.1). Для этого нить на атравматической игле проводят через стенку наконечника в направлении снаружи вовнутрь, затем через эпиневрий и периневрий пучка нервных волокон проводят продольный стежок длиной 4-5 мм, после выкола из оболочек выполняют поперечный стежок, который проводят через эпиневрий на расстоянии 3 мм от конца культи нерва. Симметрично первому продольному стежку, но в противоположном направлении, выполняют второй продольный стежок через эпиневрий и периневрий, после чего нить проводят через стенку наконечника в направлении изнутри-наружу. Наложив не менее трех таких швов, подтягиванием лигатур концы культей нерва помещают в полости наконечников тракционных спиц, а лигатуры завязывают. Тем самым их изолируют от окружающих тканей.
После этого в проекции поврежденного участка нерва осуществляют монтаж внешней тракционной системы, в которой фиксируют свободные концы спиц с закрепленными в их наконечниках культями. С помощью тракционной системы производят плавное сближение противостоящих концов культей нерва до устранения имеющегося между ними ретракционного диастаза. При этом сближение осуществляют на максимально возможную величину, но так, чтобы не было признаков ишемических расстройств и прорезывания крепежных швов. На завершающем этапе операции визуально оценивают состояние васкуляризации нерва; с помощью лазерной доплеровской флоуметрии контролируют показатели интраневрального кровотока. Рану послойно ушивают наглухо.
В послеоперационном периоде осуществляют дозированную тракцию одновременно проксимальной и дистальной культей поврежденного нерва во встречном направлении со средним темпом 1,0 мм в сутки. При этом указанное ежесуточное увеличение длины каждой из культей осуществляют минимум за 8 микроперемещений в течение 16 часов.
По достижении необходимой величины удлинения с частичным перекрытием концов проксимальной и дистальной культей нерва «внахлест» тракцию прекращают. После 2 недель фиксации выполняют повторную операцию: производят демонтаж устройства, концы культей нерва обнажают, отсекают острым лезвием у основания наконечников тракционных спиц и соединяют между собой ультратонкими микрохирургическими швами.
Оценка течения регенераторных процессов была проведена на экспериментальном материале - 27 собак, которым предварительно резецировали участок седалищного нерва, равный 15% длины бедра (3-4 см), а затем с помощью предложенного способа и устройства осуществляли восстановление его целостности.
При гистологическом исследовании установлено, что при встречной дозированной тракции концов нерва в составляющих его тканевых структурах появляются признаки упругой деформации растяжения, затем - интеркалярного роста (ультраструктурные картины активации биосинтетических процессов, увеличения размеров и количества клеток, а также внеклеточных структур) и интеркалярной регенерации.
В оболочках нерва отчетливо выражена ориентация клеточных и волокнистых структур по вектору растяжения (Фиг.2). Активированные фибробласты эпиневрия с крупными светлыми ядрами выстроены плотными продольно ориентированными цепочками. Клетки периневрия расположены непрерывными параллельными слоями, во многих из них выражена гипертрофия биосинтетического аппарата (Фиг.3).
Внутри удлиняющихся периневральных трубок выявляются леммоциты, которые расположены строго продольно ориентированными прямолинейными тяжами. Даже на ранних сроках эксперимента (12 суток - 7 дней тракции) в их цитоплазме нет продуктов распада аксонов и миелина. Крупные овальные ядра имеют хорошо выраженную кариолемму, светлую кариоплазму и, как правило, 2 ядрышка (Фиг.4А; Фиг.9АД). При удалении от уровня крепежных швов поляризация тяжей леммоцитов по вектору растяжения постепенно исчезает. В не подвергавшихся растяжению участках периферического отрезка нерва леммоциты ориентированы распадающимися в результате валлеровской дегенерации аксонами и формируют синусоидально извитые бюнгнеровы ленты. В цитоплазме леммоцитов бюнгнеровых лент видны фрагменты распавшихся аксонов и миелина. На ранних сроках эксперимента они имеют крупно- и мелкогранулярный характер, многие располагаются в «овоидах». К концу периода удлинения (4-5 недель тракции) преобладает наиболее поздний признак валлеровской дегенерации - уже освободившиеся от продуктов распада «тонкие» бюнгнеровы ленты. В леммоцитах бюнгнеровых лент преобладают «плотные» формы ядер. В нейрогистологических препаратах такие ядра темно окрашены, внутренняя структура практически не выявляется. Они нередко изогнуты в соответствии с характерной синусоидальной извитостью бюнгнеровых лент (Фиг.4Б; Фиг.9БД).
Аналогичная зона вставочного роста леммоцитарных тяжей формируется и в центральном отрезке нерва (Фиг.5Л), но, в отличие от периферического отрезка, здесь уже на этапе удлинения происходит невротизация леммоцитарных тяжей аксонами (Фиг.6, 7, 9АП), регенерирующими после арборизации из зоны реактивно измененных нервных волокон.
Проксимальнее зоны реактивных изменений нервные волокна центрального отрезка также упруго деформированы (они утрачивают характерную синусоидальную извитость и прямолинейны) и демонстрируют признаки интеркалярного роста, характерные для постнатального онтогенеза. С 3-4 недель тракции в мякотных волокнах выявляется гипертрофия перикарионов леммоцитов и увеличение средних интернодальных расстояний. Встречаются единичные «удлиненные» перехваты Ранвье (результат ретракции терминальных ламелл миелина - признак так называемой «функциональной» демиелинизации) и одиночные аномально короткие (вставочные) сегменты миелина (Фиг.8).
Вставочные сегменты миелина репарируют участки паранодальной демиелинизации. Сегментарная демиелинизация в условиях дозированного растяжения встречается редко, поэтому с увеличением срока тракции (5-6 недель) вставочные сегменты миелина также располагаются в основном одиночно, а средняя длина их увеличивается. Этот параметр продолжает возрастать и в периоде фиксации, что свидетельствует о продолжении индуцированного дозированным растяжением роста.
Проявления роста шванновских оболочек безмиелиновых волокон также включают гипертрофию органелл цитоплазмы (на свето-оптическом уровне это проявляется усилением базофилии цитоплазмы, а на ультраструктурном - повышением количества свободных рибосом) и снижение доли ядросодержащих профилей безмиелиновых волокон на поперечных срезах, что свидетельствует об увеличении продольных размеров шванновских клеток, входящих в состав этих волокон.
После сшивания удлиненных отрезков нерва происходит эффективная реиннервация пучков и ветвей нерва дистальнее зоны повреждения. Регенерация аксонов во внутримышечных стволиках и регенерирующие нервные окончания обнаруживаются через 2 месяца после шва (Фиг.10). Это дает основание полагать, что скорость роста регенерирующих аксонов в условиях данных опытов составляет не менее 3 мм в день.
По данным электромиографии, во втором полугодии после восстановительного лечения амплитуда моторных ответов передней большеберцовой и икроножной мышц достоверно не отличается от исходного уровня (таблица 1).
23,3±1,8
Использование предложенного способа в РНЦ «ВТО» им. акад. Г.А.Илизарова показало, что его применение обеспечивает удлинение нерва в ранние, оптимальные для функционального восстановления сроки после травмы, причем эффективность способа значительно превосходит результаты аутонейропластики дефектов нервов.







Изобретение относится к области медицины, а именно к травматологии. Осуществляют обработку концов культей нерва, их фиксацию и дозированную тракцию с помощью устройства на необходимую величину с последующим сшиванием конец в конец. При этом фиксацию культей нерва к тракционным элементам устройства осуществляют швами, сочетающими продольные и поперечные стежки через оболочки нерва. После чего концы помещают в полости наконечников тракционных спиц, одномоментно устраняют между ними ретракционный диастаз, а затем производят дозированную тракцию одновременно проксимальной и дистальной культей нерва с темпом 1 мм в сутки. При этом тракцию осуществляют минимум за 8 микроперемещений в течение 16 часов. Способ обеспечивает удлинение поврежденного нерва в ранние сроки, оптимальные для регенерации и последующего восстановления функции нерва. 1 табл., 10 ил.
Способ удлинения поврежденного нерва, включающий обработку концов культей нерва, их фиксацию и дозированную тракцию с помощью устройства на необходимую величину с последующим сшиванием конец в конец, отличающийся тем, что фиксацию культей нерва к тракционным элементам устройства осуществляют швами, сочетающими продольные и поперечные стежки через оболочки нерва, после чего эти концы помещают в полости наконечников тракционных спиц, одномоментно устраняют между ними ретракционный диастаз, а затем производят дозированную тракцию одновременно проксимальной и дистальной культей нерва с темпом 1 мм в сутки, при этом тракцию осуществляют минимум за 8 микроперемещений в течение 16 ч.
| ФОРМОВОЧНЫЙ МАТЕРИАЛ | 2004 |
|
RU2262410C1 |
| СПОСОБ УДЛИНЕНИЯ ПЕРИФЕРИЧЕСКОГО НЕРВА | 1991 |
|
RU2013080C1 |
| ЛАЗЕРНЫЙ МОБИЛЬНЫЙ КОМПЛЕКС | 2008 |
|
RU2370828C1 |
| БОГОВ А.А | |||
| и др | |||
| Показания к применению различных способов тракционного удлинения нервных стволов конечностей | |||
| Актуальные вопросы травматологии, ортопедии и нейрохирургии, 2001, с.77-79 | |||
| RUCH D.S | |||
| et al | |||
| Articulating external fixation to overcome nerve gaps in lower extremity trauma | |||
| J Ortop Trauma | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
Авторы
Даты
2010-09-10—Публикация
2009-04-29—Подача