Уровень техники
Фотодинамическая терапия (ФДТ) - это метод, применяемый для лечения некоторых типов заболеваний, в частности определенных типов рака. Эта методика состоит в том, что в патологические ткани вводят в качестве метки фотосенсибилизатор, затем вызывают избирательное разрушение указанных тканей, подвергая эти ткани воздействию света с определенной длиной волны. Такой монохроматический свет обычно получают с помощью лазера или лазерного диода.
Под фотосенсибилизатором понимается любая молекула, которая способна запасать энергию света, которая может быть активирована указанной энергией, и поэтому предоставлять себя для многочисленных биохимических комбинаций.
Обычно фотосенсибилизатор вводят пациенту в количестве между 0,1 и 0,5 микромоль на 1 кг массы тела, затем его улавливают клетки целого организма. Фотосенсибилизирующая молекула накапливается в основном в раковых клетках, но остается неактивной до тех пор, пока не будет подвергнута воздействию света с подходящей длиной волны. Освещение или облучение опухоли светом активирует молекулу, которая затем взаимодействует с кислородом, и образуются короткоживущие соединения, в частности синглетный кислород. Синглетный кислород - это высокореакционноспособная и токсичная молекула, разрушающая раковые клетки, в которых был сконцентрирован фотосенсибилизатор.
Между введением фотосенсибилизатора и активацией его лазером проходит некоторое время. Свет лазера, используемый в фотодинамической терапии, фокусируют с помощью оптического волокна и воздействуют им только в течение нескольких минут. Специалист, выполняющий эту процедуру, держит оптическое волокно в непосредственной близости от опухоли для того, чтобы доставить точное количество света. В результате, фотодинамическая терапия лишь минимально разрушает здоровые клетки.
На начальной стадии рака цель такой методики может заключаться в полной ликвидации и излечении рака, но на поздней стадии, задача может заключаться в уменьшении объема опухоли с целью смягчения симптомов. Новые нормальные клетки замещают те, что были разрушены фотодинамической терапией, обеспечивающей быстрое выздоровление после лечения и исключающей, в частности, грубые рубцы, которые могут образовываться в результате удаления тканей другими способами.
Даже если пациентов уже лечили с помощью хирургических методов, методов радиотерапии или химиотерапии, к ним, несомненно, может быть применена эта методика.
В качестве примеров заболеваний, которые можно лечить фотодинамической терапией, можно привести, в частности, рак желудка, рак кишечника, рак легкого, рак молочной железы, рак матки, рак пищевода, рак яичника, рак поджелудочной железы, рак печени, рак мочевого пузыря, рак желчного пузыря, рак языка, рак мозга, рак кожи, рак щитовидной железы, рак предстательной железы, рак околоушной железы, а также некоторые вирусные и/или микробные заболевания.
Фотодинамическую терапию можно применять в качестве способа диагностирования некоторых форм рака. С этой точки зрения достаточно, чтобы фотосенсибилизирующие молекулы флуоресцировали и, следовательно, были способны излучать свет, после того, как они были облучены.
В данный момент известно, что в фотодинамической терапии в качестве фотосенсибилизаторов применяют некоторые производные порфиринов, в частности гематопорфирин. Это средство, известное под зарегистрированной AXCAN PHARMA INC. торговой маркой Photofrin, является очищенной смесью гематопорфиринов. Гематопорфирин - это, в свою очередь, производное свиного гемоглобина.
Кроме того, до настоящего времени Photofrin® был единственной фотосенсибилизирующей молекулой, которая была разрешена для продажи в некоторых странах, в частности во Франции, для лечения рака пищевода.
Несмотря на преимущества, продемонстрированные Photofrin®, такие как растворимость в водной среде, хороший выход при образовании синглетного кислорода и легкий синтез, он все еще обладает несколькими недостатками.
Прежде всего, Photofrin® активируют светом с длиной волны 630 нм. Тем не менее, при такой длине волны свет проникает в ткани только в диапазоне от 5 до 10 мм, что является серьезным препятствием, когда опухоль более обширна и лежит глубже. Более того, такой фотосенсибилизатор приводит к возникновению кожной фоточувствительности в течение шести недель после применения. Наконец, тот факт, что Photofrin® является смесью из нескольких молекул, делает более трудным подбор подходящей дозировки как для фотосенсибилизатора, так и для подаваемого света.
Среди других исследуемых соединений, так называемых соединений второго поколения, документ WO-98/50386 описывает некоторые производные бензопорфирина. Такие производные демонстрируют некоторые преимущества по сравнению с Photofrin® в том, что они абсорбируют свет при длине волны 690 нм и, поэтому могут быть применены в лечении более обширных и более глубоко расположенных опухолей. Такие производные, кроме того, обладают лучшей селективностью в отношении раковых клеток.
Тем не менее, сохраняются определенные проблемы, связанные с селективностью, поглощением света и токсичностью.
Целью настоящего изобретения является предложение новых производных порфирина, таких, в частности, как хлоринов и/или бактериохлоринов, в которых устранены вышеупомянутые недостатки, в частности, в отношении предпочтительной аккумуляции в раковых клетках, лучшей стабильности и более низкой фототоксичности.
Другая цель настоящего изобретения - это предложение противораковых, и/или противовирусных, и/или противомикробных препаратов с целью их применения в фотодинамической терапии.
Другие цели и преимущества изобретения прояснятся в последующем описании, которое дано только в виде примеров и не ограничено ими.
Раскрытие изобретения
Настоящее изобретение имеет отношение к производным порфирина, в частности к хлорину, соединению, имеющему следующую формулу:
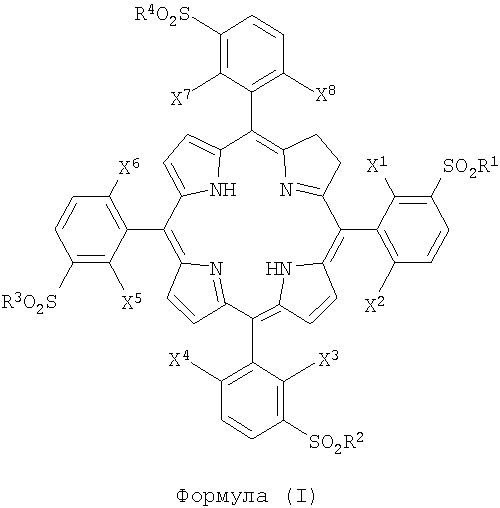
где
- X1, X2, X3, X4, X5, X6, X7, X8, каждый, одинаковые или разные, выбирают из атомов галогена и/или атомов водорода;
- R1, R2, R3, R4, каждый, одинаковые или разные, выбирают из следующих заместителей: OH-групп, аминокислот, OR-групп и NHR-групп и/или атома хлора, где R - это алкильная группа, имеющая от 1 до 12 атомов углерода.
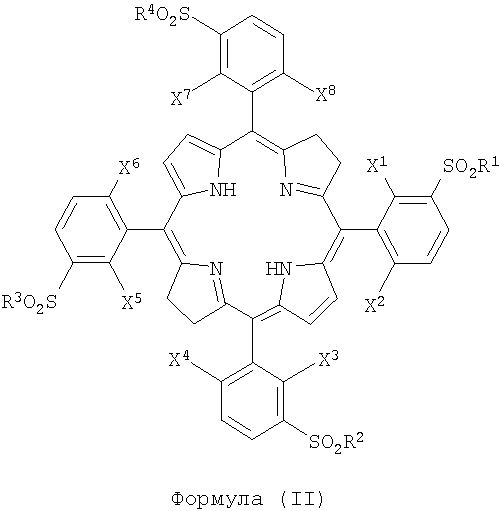
Настоящее изобретение также имеет отношение к производным порфирина, в частности к бактериохлорину, соединению, имеющему следующую формулу:
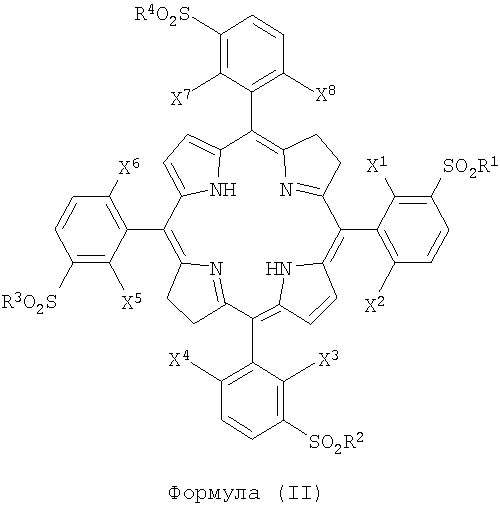
где
- Х1, Х2, Х3, Х4, Х5, Х6, Х7, Х8, каждый, одинаковые или разные, выбирают из атомов галогена и/или атомов водорода;
- R1, R2, R3, R4, каждый, одинаковые или разные, выбирают из OH-групп, аминокислот, OR-групп и NHR-групп и/или атома хлора, где R - это алкильная группа, включающая от 1 до 12 атомов углерода.
Одно из преимуществ этих производных заключается в том, что, как описано в настоящем изобретении, в молекуле присутствует хлорсульфонильная группа, которая дает возможность легко и эффективно вводить широкое разнообразие химических заместителей.
Кроме того, настоящее изобретение имеет отношение к применяемым для лечения людей или животных противораковым, и/или противовирусным и/или противомикробным лекарствам, содержащим в качестве главного действующего вещества одно или несколько соединений, описанных в настоящем изобретении.
Краткое описание чертежей
Изобретение будет лучше понято при чтении нижеследующего описания, сопровождаемого прилагаемыми чертежами, среди которых:
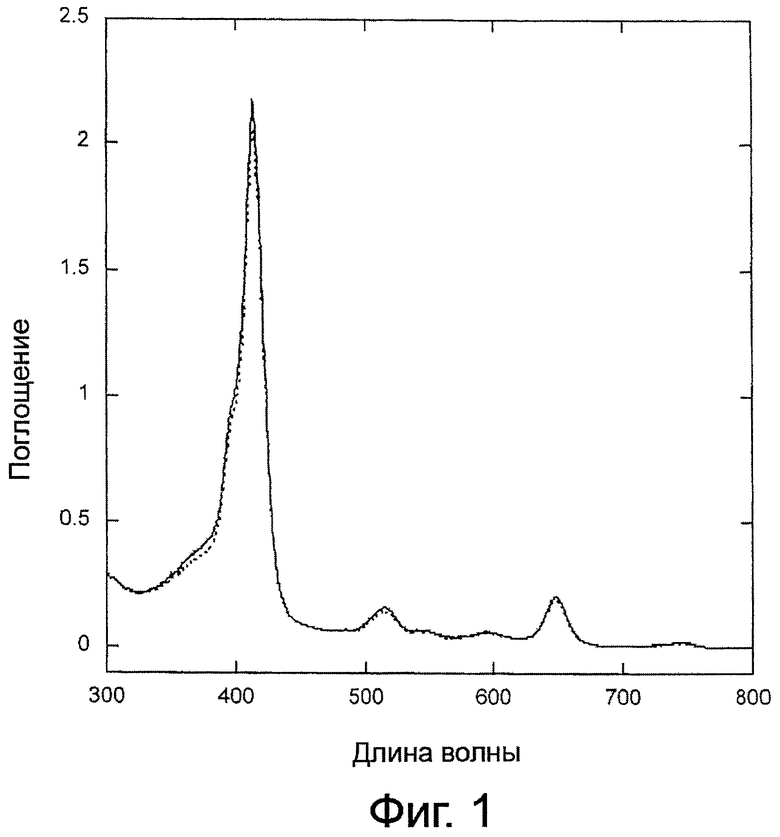
- На фиг.1 представлен спектр поглощения хлорина, соединения, имеющего формулу (I) в водной среде до (сплошная линия) и после (пунктирная линия) облучения образца второй гармоникой лазера Nd:YAG.
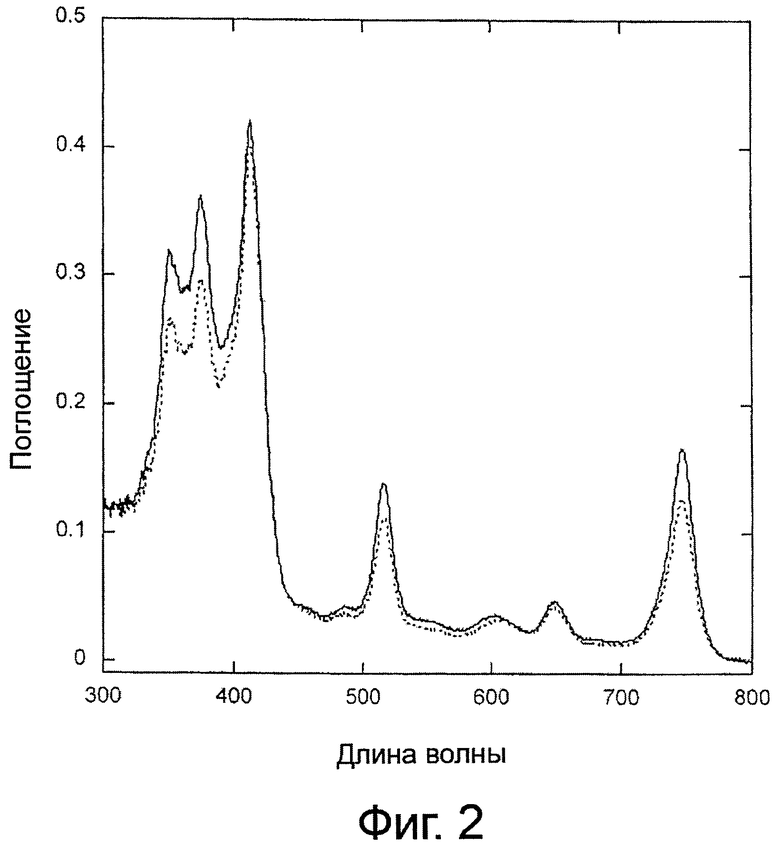
- На фиг.2 представлен спектр поглощения бактериохлорина, соединения, имеющего формулу (II), в водной среде до (сплошная линия) и после (пунктирная линия) облучения образца второй гармоникой лазера Nd:YAG.
Осуществление изобретения
Настоящее изобретение, во-первых, имеет отношение к производным порфирина, в частности к хлорину, соединению, имеющему следующую формулу:
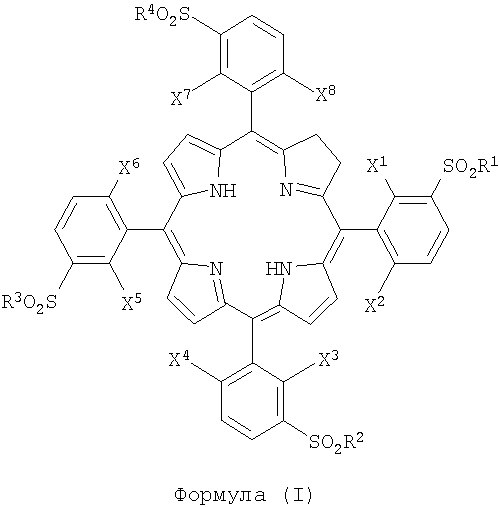
где
- X1, X2, X3, X4, X5, X6, X7, X8, каждый, одинаковые или разные, выбраны из атомов галогена и/или атомов водорода;
- R1, R2, R3, R4, каждый, одинаковые или разные, выбраны из следующих заместителей: ОН-групп, аминокислот, OR-групп и NHR-групп и/или атомов хлора, где R - это алкильная группа, имеющая от 1 до 12 атомов углерода.
Одно из преимуществ таких типов производных заключается в том, что они являются амфифильными веществами. Амфифильность - это существенная черта, так как такие молекулы могут пересекать клеточные мембраны и накапливаться внутри клеток.
Под амфифильным соединением понимается любая молекула, которая проявляет как гидрофильные, так и гидрофобные свойства.
Этот тип производных обладает полосой поглощения при 650 нм, как показано на фиг.1.
Настоящее изобретение также имеет отношение к производным, удовлетворяющим формуле (I), где
- X1, X2, X3, X4, X5, X6, X7, X8, каждый, одинаковые или разные, выбирают из атомов галогена и/или атомов водорода, так что, по меньшей мере, один из радикалов Х в каждой паре X1/X2, X3/X4, X5/X6, X7/X8 является атомом галогена.
Преимущество этого особого типа производных заключается в присутствии атомов галогена в ортоположении фенильного заместителя, который увеличивает квантовый выход образования триплетного состояния без значительного снижения периода его полураспада. С более высоким квантовым выходом триплетное состояние может переносить свою энергию более эффективно по сравнению с кислородом с соответственно более высоким выходом в образовании синглетного кислорода.
Кроме того, атомы галогена в ортоположениях фенильного заместителя делают тетрапиррольный макроцикл более устойчивым и, следовательно, более эффективным при его применении в фотодинамической терапии.
Кроме того, согласно настоящему изобретению и в соответствии с формулой (I):
- X2, X4, X6 и X8 являются либо атомами хлора, либо атомами фтора;
- X1, X3, X5 и X7 являются атомами водорода,
- R1, R2, R3, R4 являются атомами хлора.
Согласно другому варианту настоящего изобретения и в соответствии с формулой (I):
- X2, X4, X6 и X8 являются либо атомами хлора, либо атомами фтора;
- X1, X3, X5 и X7 являются атомами водорода,
- R1, R2, R3, R4 являются OH-группами.
Настоящее изобретение также имеет отношение к производным, соответствующим формуле (I), где:
- X1, X2, X3, X4, X5, X6, X7, X8 являются атомами хлора,
- R1, R2, R3, R4 являются либо атомами хлора, либо ОН-группами.
Настоящее изобретение также имеет отношение к производным порфирина, в частности, к бактериохлорину, соединению, имеющему следующую формулу:
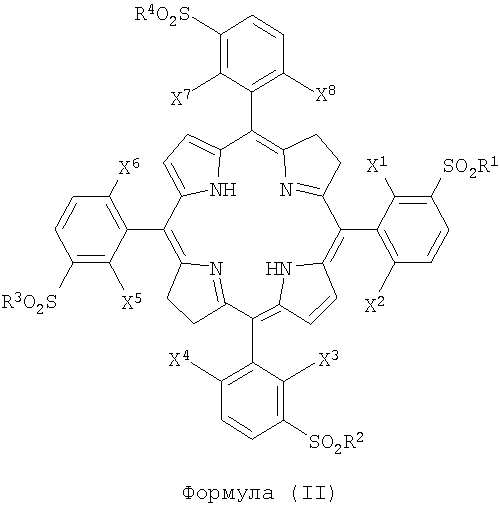
где
- Х1, X2, X3, X4, X5, X6, X7, X8, каждый, одинаковые или разные, выбирают из атомов галогена и/или атомов водорода;
- R1, R2, R3, R4, каждый, одинаковые или разные, выбирают из следующих заместителей: OH-групп, аминокислот, OR-групп и NHR-групп и/или атома хлора, где R - это алкильная группа, имеющая от 1 до 12 атомов углерода.
Преимущество такого типа производных и таких, что были описаны выше для случая хлоринов, заключается в том, что они также амфифильные.
Другое преимущество этих производных, в частности бактериохлорина, соответствующего формуле (II), заключается в поглощении света в красной области при 750 нм, как показано на фиг.2. При такой длине волны эффекты экранирования, вызываемые тканями человека, в частности гемоглобином, выражены не так сильно, что делает возможным увеличивать «количество» света, достигающего фотосенсибилизатора внутри клеток.
Настоящее изобретение также имеет отношение к производным, соответствующим формуле (II), где
- X1, X2, X3, X4, X5, X6, X7, X8, каждый, одинаковые или разные, выбирают из атомов галогена и/или атомов водорода так, что, по меньшей мере, один из радикалов Х в каждой паре X1/X2, Х3/Х4, X5/X6, X7/X8 является атомом галогена.
Как в случае хлорина, описанного выше, присутствие атомов галогена в ортоположениях фенильного заместителя, увеличивает квантовый выход образования триплетного состояния без значительного снижения периода его полураспада и, следовательно, также увеличивает образование синглетного кислорода.
Настоящее изобретение также имеет отношение к определенным производным, соответствующим формуле (II), где
- X2, X4, X6 и X8 являются либо атомами хлора, либо атомами фтора;
- Х1, X3, X5 и X7 являются атомами водорода,
- R1, R2, R3, R4 являются атомами хлора.
Согласно другому варианту настоящего изобретения и в соответствии с формулой (II):
- Х2, Х4, Х6 и Х8 являются либо атомами хлора, либо атомами фтора;
- X1, X3, X5 и X7 являются атомами водорода,
- R1, R2, R3, R4 являются OH-группами.
Кроме того, настоящее изобретение имеет отношение к производным, соответствующим формуле (II), где X1, X2, Х3, X4, X5, X6, X7, X8 являются атомами хлора, R1, R2, R3, R4 являются либо атомами хлора, либо OH-группами.
Присутствие атомов галогена в ортоположениях фенильного заместителя также делает тетрапиррольные макроциклы и их производные более стабильными.
Согласно настоящему изобретению атомы галогена - это фтор, и/или хлор, и/или бром.
Другая цель настоящего изобретения состоит в способе получения описанных выше производных, включающем следующие стадии:
- стадию хлорсульфонирования соответствующего галогенированного порфирина,
- стадию восстановления галогенированного и хлорсульфонированного порфирина до хлорина и/или до бактериохлорина с помощью гидразида в присутствии заторможенных органических оснований,
- стадию взаимодействия между хлорсульфонированной частью молекулы и аминами и/или аминокислотами и/или спиртами или стадию гидролиза хлора хлорсульфонильного остатка водой.
С помощью не ограничивающего примера, химический синтез производного, соответствующего формуле (I), где
- X2, X4, X6 и X8 являются атомами хлора;
- Х1, Х3, Х5 и Х7 являются атомами водорода,
- R1, R2, R3, R4 являются ОН-группами,
проводили, как описано ниже:
5,10,15,20-тетракис(2-хлор-3-хлорсульфонилфенил)порфирин (0,0658 г, 6,55×10-5 моль) предварительно растворяли в N,N-диметилформамиде и/или толуоле и/или пиридине и/или пиколине (50 мл), предварительно обезвоженном и перегнанном, температуру реакционной смеси повышали от 50°С до 150°С. Затем к реакционной смеси добавляли раствор п-толуол-сульфонилгидразида (5,5×10-5 моль) и объемное органическое основание, такое как DABCO и/или DBU в DMF (5 мл). Смесь перемешивали при 150°С под азотом и в отсутствии света.
За протеканием реакции следили с помощью спектрофотометрического метода в видимой области до тех пор, пока полоса Q при 650 нм не достигала максимума.
Затем испаряли растворитель, обрабатывали реакционную смесь, полученный продукт гидролизовали водой и очищали с помощью экстракции из раствора в раствор. После рекристаллизации смесью метанол/дихлорметан получали продукт с выходом 80%. Масс-спектроскопия (FAB), m/z: 1075 (центральный пик).
Видимая ультрафиолетовая область спектра (буферный раствор, NaOH, KH2P04), максимальная длина волны (в нм): 414, 516, 542, 598, 649. Квантовый выход флуоресценции: 0,04.
Период полураспада триплетного состояния в насыщенном азотом водном растворе: 235 мкс.
Период полураспада триплетного состояния в насыщенном воздухом водном растворе: 3,88 мкс.
Квантовый выход образования синглетного кислорода в дейтерированном водном растворе: 0,56.
Период полураспада синглетного кислорода: 65 мкс в дейтерированной воде.
Схематически реакция может быть представлена так, как приведено ниже:
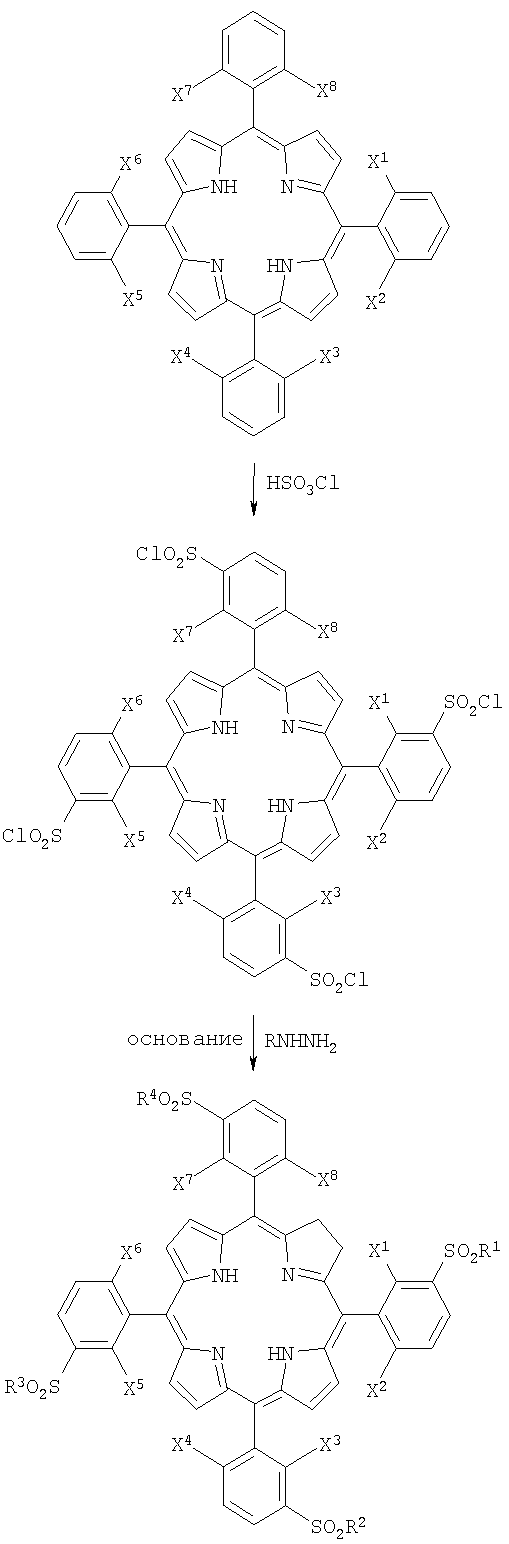
Также, с помощью не ограничивающего примера, химический синтез производного, соответствующего формуле (II), где
- X2, X4, X6 и X8 являются атомами хлора;
- X1, X3, X5 и X7 являются атомами водорода,
- R1, R2, R3, R4 являются ОН-группами,
проводили, как описано ниже:
5,10,15,20-тетракис(2-хлор-3-хлорсульфонилфенил)порфирин (0,0658 г, 6,55×10-5 моль) предварительно растворяли в N,N-диметилформамиде и/или в толуоле и/или в пиридине и/или в пиколине (50 мл), предварительно обезвоженном и перегнанном, температуру реакционной смеси повышали от 50°С до 150°С. Затем раствор п-толуол-сульфонилгидразида (130,0×10-5 моль) и DABCO в DMF (5 мл) добавляли к реакционной смеси. Смесь перемешивали при 150°С под азотом и защищали от света. За протеканием реакции следили с помощью спектрофотометрического метода в видимой области до тех пор, пока полоса Q при 750 нм не достигала максимума.
Затем испаряли растворитель, обрабатывали реакционную смесь, гидролизовали полученный продукт и получали требуемый продукт с выходом 77%. Масс-спектроскопия (FAB), m/z: 1077 (центральный пик).
Видимая ультрафиолетовая область спектра (буферный раствор, NaOH, KH2P04), максимальная длина волны (в нм): 353, 376, 486, 518, 604, 748.
Квантовый выход флуоресценции: 0,013.
Период полураспада триплетного состояния в насыщенном азотом водном растворе: 235 мкс.
Период полураспада триплетного состояния в насыщенном воздухом водном растворе: 3,88 мкс.
Квантовый выход образования синглетного кислорода в дейтерированном водном растворе: более чем 30%.
Период полураспада синглетного кислорода: 65 мкс в дейтерированной воде.
Также, схематически реакция может быть представлена так, как приведено ниже:
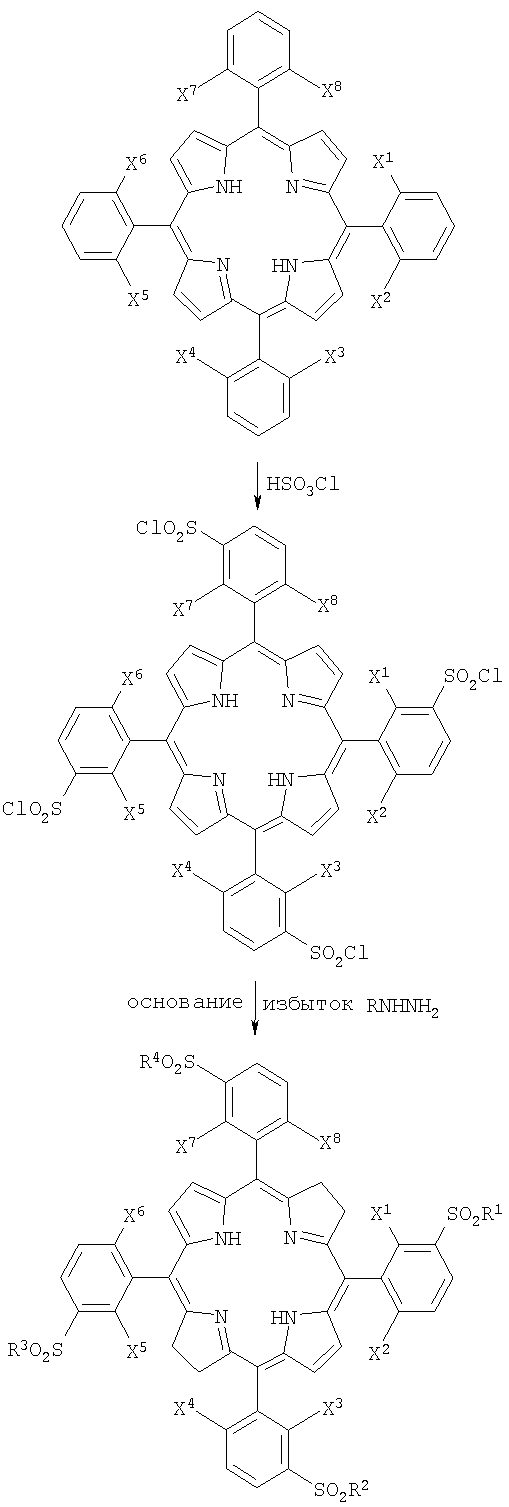
5,10,15,20-тетракис(2-хлор-3-хлорсульфонилфенил)порфирин, применяемый в качестве исходного порфирина в описанном выше синтезе хлорина и бактериохлорина, известен специалистам в этой области техники и описан в литературе, в частности в Journal of Heterocyclic Chemistry, 28: 635 (1991).
Согласно настоящему изобретению квантовые выходы образования синглетного кислорода были получены путем сравнения между интенсивностью фосфоресценции синглетного кислорода при длине волны 1270 нм в растворе, содержавшем исследуемый фотосенсибилизатор, и интенсивностью фосфоресценции, полученной от другого раствора, имевшего такое же поглощение при той же длине волны и содержавшего сравниваемый фотосенсибилизатор.
Согласно настоящему изобретению для сравнения применяли фотосенсибилизатор мезо-тетракис(2-хлор-3-сульфофенил)порфирин (TPPS), величина квантового выхода образования синглетного кислорода в дейтерированной воде которого равна 0,64 при рН-7,4 (Photochem. Photobiol., 70: 391, 1999).
Настоящее изобретение также имеет отношение к противораковым и/или противовирусным и/или противомикробным лекарствам, применяемым для лечения людей или животных, содержащим в качестве основного активного вещества одно или несколько соединений, описанных в настоящем изобретении.
Этот тип лекарств, применяемый, в частности, в фотодинамической терапии, может также содержать один или несколько фармакологически приемлемых наполнителей.
Конечно, другие воплощения настоящего изобретения, доступные специалисту в данной области техники, могут быть рассмотрены без отступления от основы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АТРОПОИЗОМЕРЫ ГАЛОГЕНИРОВАННЫХ ТЕТРАФЕНИЛБАКТЕРИОХЛОРИНОВ И ХЛОРИНОВ И ИХ ПРИМЕНЕНИЕ В ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2016 |
|
RU2712266C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИНОВ И ИХ ФАРМАЦЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2009 |
|
RU2513483C2 |
| НИЗКОМОЛЕКУЛЯРНЫЕ ПРОИЗВОДНЫЕ КАРБОКСАМИДНЫХ ГАЛОГЕНИРОВАННЫХ ПОРФИРИНОВ, А ИМЕННО ХЛОРИНОВ И БАКТЕРИОХЛОРИНОВ, И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2718923C2 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА | 2005 |
|
RU2372989C2 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА | 2003 |
|
RU2326123C2 |
| ЗАМЕЩЕННЫЕ АНИЛИДЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1998 |
|
RU2233269C2 |
| ПРОИЗВОДНЫЕ ЦИКЛОАЛКИЛЕНА ИЛИ ГЕТЕРОЦИКЛОАЛКИЛЕНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, АЭРОЗОЛЬНОЕ УСТРОЙСТВО И СПОСОБ ЛЕЧЕНИЯ | 1995 |
|
RU2159229C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2017 |
|
RU2748693C2 |
| ПРОИЗВОДНЫЕ ГИДРОХИНОНА В СВОБОДНОМ ВИДЕ ИЛИ В ВИДЕ СОЛИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОИЗВОДНЫЕ ПИПЕРИДИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2095339C1 |
| СПОСОБЫ МОДУЛИРОВАНИЯ ФУНКЦИИ СЕРИН/ТРЕОНИН ПРОТЕИНКИНАЗЫ СОЕДИНЕНИЯМИ НА ОСНОВЕ 5-АЗАХИНОКСАЛИНА, СПОСОБ ИДЕНТИФИКАЦИИ СОЕДИНЕНИЙ, МОДУЛИРУЮЩИХ ФУНКЦИЮ СЕРИН/ТРЕОНИН ПРОТЕИНКИНАЗЫ, СПОСОБ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ПАТОЛОГИЧЕСКОГО СОСТОЯНИЯ ОРГАНИЗМА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОЕДИНЕНИЕ НА ОСНОВЕ 5-АЗАХИНОКСАЛИНА И СПОСОБ ЕГО СИНТЕЗА | 1998 |
|
RU2223753C2 |
Изобретение относится к производным порфирина формул I и II, где X1, X2, X3, X4, X5, X6, X7, X8 представляют собой атомы галогенов или атомы водорода, a R1, R2, R3, R4 выбирают из ОН-групп, аминокислот, OR-групп, NHR-групп и/или атомов хлора, где R - это алкил, имеющий от 1 до 12 атомов углерода. Изобретение также включает в себя способы получения таких соединений и лекарственные средства на основе таких соединений. Такие соединения и лекарственные средства могут быть применены в фотодинамической терапии раковых заболеваний. 5 н. и 14 з.п. ф-лы.
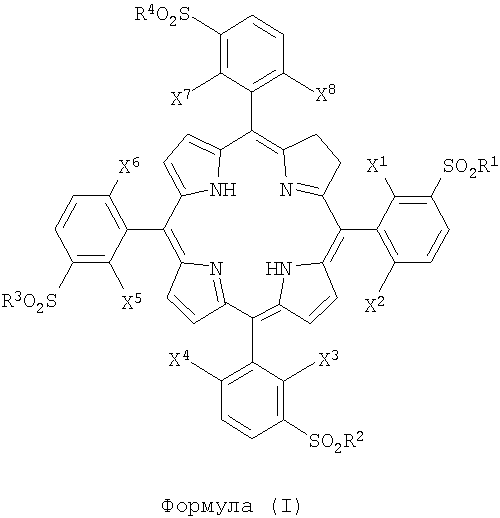
1. Производное порфирина, в частности хлорин, имеющее формулу (I)
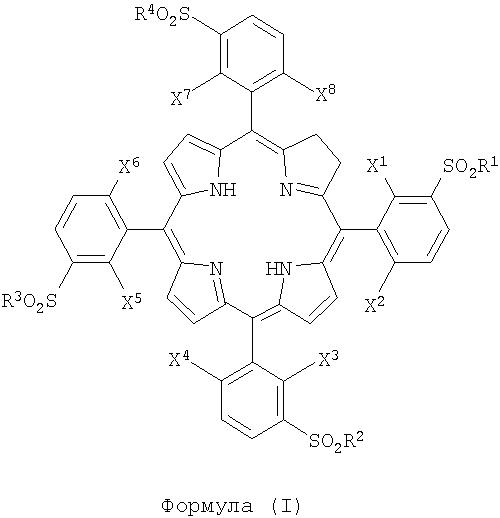
где X1, X2, X3, X4, X5, X6, X7, X8 каждый, одинаковые или разные, выбирают из атомов галогена и/или атомов водорода, так, что, по меньшей мере, один из радикалов Х в каждой паре Х1/Х2, Х3/Х4, Х5/X6, Х7/X8 является атомом галогена,
R1, R2, R3, R4 каждый, одинаковые или разные, выбирают из следующих заместителей: ОН-групп, аминокислот, OR-групп и NHR-групп и/или атома хлора, где R - это алкильная группа, имеющая от 1 до 12 атомов углерода.
2. Производное порфирина по п.1, соответствующее формуле (I), где
X2, X4, X6 и X8 являются атомами хлора;
X1, X3, X5 и X7 являются атомами водорода,
R1, R2, R3, R4 являются атомами хлора.
3. Производное порфирина по п.1, соответствующее формуле (I), где
X2, X4, X6 и X8 являются атомами фтора;
X1, X3, X5 и X7 являются атомами водорода,
R1 R2, R3, R4 являются атомами хлора.
4. Производное порфирина по п.1, соответствующее формуле (I), где
X2, X4, X6 и X8 являются атомами фтора;
X1, X3, X5 и X7 являются атомами водорода,
R1, R2, R3, R4 являются ОН-группами.
5. Производное порфирина по п.1, соответствующее формуле (I), где
X2, X4, X6 и X8 являются атомами фтора;
X1, X3, X5 и X7 являются атомами водорода,
R1, R2, R3, R4 являются ОН-группами.
6. Производное порфирина по п.1, соответствующее формуле (I), где
X1, X2, X3, X4, X5, X6, X7, X8 являются атомами хлора;
R1, R2, R3, R4 являются атомами хлора.
7. Производное порфирина по п.1, соответствующее формуле (I), где
X1, X2, X3, X4, X5, X6, X7, X8 являются атомами хлора;
R1 R2, R3, R4 являются ОН-группами.
8. Производное порфирина, в частности, бактериохлорин, имеющее формулу (II)

где X1, X2, X3, X4, X5, X6, X7, X8 каждый, одинаковые или разные, выбирают из атомов галогена и/или атомов водорода;
R1, R2, R3, R4 каждый, одинаковые или разные, выбирают из следующих заместителей: ОН-групп, аминокислот, OR-групп и NHR-групп и/или атомов хлора, где R - это алкильная группа, имеющая от 1 до 12 атомов углерода.
9. Производное порфирина по п.8, соответствующее формуле (II), где
X1, X2, X3, X4, X5, X6, X7, X8 каждый, одинаковые или разные, выбирают из атомов галогена и/или атомов водорода, так, что, по меньшей мере, один из радикалов Х в каждой паре Х1/X2, Х3/Х4, Х5/X6, Х7/X8 является атомом галогена.
10. Производное порфирина по п.8, соответствующее формуле (II), где
X2, X4, X6 и X8 являются атомами хлора;
X1, X3, X5 и X7 являются атомами водорода,
R1, R2, R3, R4 являются атомами хлора.
11. Производное порфирина по п.8, соответствующее формуле (II), где
X2, X4, X6 и X8 являются атомами фтора;
X1, X3, X5 и X7 являются атомами водорода,
R1, R2, R3, R4 являются атомами хлора.
12. Производное порфирина по п.8, соответствующее формуле (II), где
X2, X4, X6 и X8 являются атомами хлора;
X1, X3, X5 и X7 являются атомами водорода,
R1, R2, R3, R4 являются ОН-группами.
13. Производное порфирина по п.8, соответствующее формуле (II), где
X2, X4, X6 и X8 являются атомами фтора;
X1, X3, X5 и X7 являются атомами водорода,
R1, R2, R3, R4 являются ОН-группами.
14. Производное порфирина по п.8, соответствующее формуле (II), где
X1, X2, X3, X4, X5, X6, X7, X8 являются атомами хлора;
R1, R2, R3, R4 являются атомами хлора.
15. Производное порфирина по п.8, соответствующее формуле (II), где
X1, X2, X3, X4, X5, X6, X7, X8 являются атомами хлора;
R1, R2, R3, R4 являются ОН-группами.
16. Производное порфирина по любому из пп.1 или 8, характеризующееся тем, что атомы галогена представляют собой фтор, и/или хлор, и/или бром.
17. Способ получения производного порфирина по любому из предыдущих пунктов, характеризующийся тем, что он включает:
стадию восстановления соответствующего галогенированного и хлорсульфонированного порфирина до хлорина и/или бактериохлорина с помощью гидразида и объемного органического основания, такого как DABCO (1,4-диазабицикло[2.2.2]октан) и/или DBU (1,8-диазабицикло[5.4.0]ундец-7-ен);
стадию взаимодействия между хлорсульфонильной группировкой и аминами и/или аминокислотами и/или спиртами.
18. Способ получения производного по любому из предыдущих пунктов, характеризующийся тем, что он включает:
стадию восстановления соответствующего галогенированного и хлорсульфонированного порфирина до хлорина и/или бактериохлорина с помощью гидразида и объемного органического основания, такого как DABCO и/или DBU;
стадию гидролиза хлора хлорсульфонильной группировки.
19. Противораковое лекарственное средство для применения на людях или животных, содержащее в качестве основного активного вещества одно или несколько соединений по пп.1-16.
| WO 03020309 A2, 13.03.2003 | |||
| WO 03008430 A2, 30.01.2003 | |||
| WO 9850386 A1, 12.11.1998 | |||
| US 5876989 A, 02.03.1999 | |||
| ВАЛЬЦЫ ДЛЯ МЫТЬЯ ВОЛОКНИСТЫХ РАСТЕНИЙ | 1926 |
|
SU5651A1 |
| Зажим для концов велокамер, насаженных на дорн для вулканизации | 1924 |
|
SU2910A1 |
Авторы
Даты
2010-09-20—Публикация
2005-11-10—Подача