Область техники
Настоящее изобретение относится к фармацевтическим композициям. В частности, оно относится к применению фармацевтически приемлемых носителей, состоящих из (i) модифицированного жидкого носителя и (ii) немодифицированного носителя, в которых объемное отношение модифицированного жидкого носителя к по существу неокисляемому носителю находится в диапазоне от 0,00001:99,99999 до менее чем 0,01:99,99, которое обеспечивает композицию с предсказуемой характеристикой пролонгированного высвобождения.
Предшествующий уровень техники
В фармации доставка лекарственного средства является таким же важным элементом, как и его активность. Многие лекарственные средства или биоактивные средства с явной активностью in vitro не оправдывают ожиданий на клиническом уровне из-за неспособности к получению, хранению или доставке биоактивного средства к месту действия в эффективных концентрациях на протяжении достаточного периода времени.
Носитель имеет большое значение для стабильного хранения и эффективного профиля доставки биоактивного агента. Для специалистов в данной области очевидно, что стабильность хранения и эффективный профиль доставки активного компонента являются, до некоторой степени, специфичными для биоактивных средств, условий, в которых вводят биоактивное средство, и состояния пациента.
Препараты с пролонгированным высвобождением или препараты на масляной основе рассматриваются в WO 97/49402 (Vlaminck); WO 94/00105 (Sabater); патенте США 4297353 (Hawkins); патенте США 5019395 (Mahjour); патенте США 5739159 (Wolf); патенте США 5162057 (Akijama); WO 96/20698 (Levy); содержание которых входит в настоящее описание в виде ссылки. Также в настоящее описание в виде ссылки входит WO 98/41207 (Brown), в которой рассматривается подкожное введение антибиотика в ухо животного.
В патенте США 5721359 раскрывается молекула, кристаллическая свободная кислота цефтиофура (ceftiofur) (CCFA), которая представляет собой цефалоспориновый антибиотик, предназначенный для использования для млекопитающих и, в частности, для животных, используемых для производства продуктов питания (например, крупный рогатый скот, овца, козы и (домашняя) свинья). В патенте утверждается, что можно получить маслянистые суспензии CCFA для введения животным, используемым для производства продуктов питания, в которых масла представляют собой растительные масла. Подразумевается, что масла, раскрытые в патенте, используют в их природной форме. Преимущество вышеуказанной молекулы над другими антибиотиками и, в частности антибиотиками семейства цефтиофура состоит в том, что ее можно использовать для получения фармацевтической композиции с пролонгированным высвобождением. Однако профиль препаратов пролонгированного высвобождения, описанных в патенте США 5721359, не является легко предсказуемым и воспроизводимым в отношении высвобождения активного лекарственного средства для продукта, используемого непосредственно сразу после его получения, в котором используют природные растительные масла. В патентной заявке США 2002/0110561 раскрываются препараты с пролонгированным высвобождением, состоящие из а) модифицированного жидкого носителя и b) по существу неокисляемого носителя, где объемное отношение модифицированного жидкого носителя к по существу неокисляемому носителю находится в диапазоне от 0,01:99,99 до 90:10, что обеспечивает композицию с предсказуемой характеристикой пролонгированного высвобождения.
Несмотря на вышеприведенные ссылочные материалы (отражающие известный уровень техники) в данной области все же существует потребность в фармацевтических композициях, которые могли бы обеспечить доставку биоактивного вещества с пролонгированным его высвобождением и для которых характеристика высвобождения была прогнозируемой и воспроизводимой непосредственно сразу после получения продукта.
Краткое описание изобретения
Неожиданно авторами было обнаружено, что композиция, содержащая:
(a) от одного до трех биоактивных средств и
(b) носитель, содержащий:
(i) модифицированный жидкий носитель и
(ii) немодифицированный жидкий носитель,
обеспечивает желаемую рабочую характеристику высвобождения уже при объемном отношении модифицированного жидкого носителя к неокисляемому носителю 0,00001:99,99999. Таким образом, настоящее изобретение относится к новой фармацевтической композиции, которая обеспечивает пролонгированное высвобождение биоактивного компонента и эта характеристика высвобождения прогнозируема сразу после получения продукта. В частности, предсказуемую характеристику получают, используя модифицированный жидкий носитель в очень низкой пропорции по отношению к неокисляемому носителю.
Один вариант изобретения относится к фармацевтической композиции, содержащей:
(a) от одного до трех биоактивных средств и
(b) носитель, содержащий:
(i) модифицированный жидкий носитель и
(ii) немодифицированный жидкий носитель,
где объемное отношение модифицированного жидкого носителя к немодифицированному жидкому носителю находится в диапазоне от 0,00001:99,99999 до менее чем 0,01:99,99 и где указанная композиция непосредственно сразу после ее получения может быть введена хозяину так, что имеет место пролонгированное высвобождение от одного до трех биоактивных средств.
В другом варианте осуществления биоактивное вещество представляет собой CCFA, и модифицированный жидкий носитель представляет собой модифицированное ненасыщенное масло, такое как модифицированное хлопковое масло, и немодифицированный жидкий носитель представляет собой полностью насыщенное масло, такое как насыщенное кокосовое масло.
Следующий вариант настоящего изобретения представляет собой способ получения фармацевтической композиции, включающий стадию модифицирования жидкого носителя и объединение (смешение) указанного модифицированного жидкого носителя с немодифицированным жидким носителем с получением носителя. Затем носитель объединяют с биоактивным веществом, получая фармацевтическую композицию. Согласно этому способу ненасыщенное масло модифицируют, используя химические, физические или механические способы или их комбинации, получая носитель, который имеет более высокий уровень продуктов окисления по сравнению с его исходной или немодифицированной формой. Один вариант способа включает использование комбинации нагревания и гамма-облучения. Кроме того, стадия модификации этого способа может иметь место либо до, после, либо как до, так и после стадии объединения.
Более конкретный аспект этого способа включает стадии:
(a) нагревание природного хлопкового масла или трилинолеина в присутствии воздуха, чтобы повысить (уровень) его продуктов окисления и получить модифицированное хлопковое масло;
(b) объединение указанного модифицированного масла с насыщенным кокосовым маслом или насыщенными продуктами кокосового масла с получением наполнителя-носителя, где объемное отношение модифицированного масла к насыщенному кокосовому маслу находится в диапазоне от 0,00001:99,99999 до менее чем 0,01:99,99;
(c) добавление кристаллической свободной кислоты цефтиофура к указанному наполнителю-носителю и необязательно после этого;
(d) нагревание указанной фармацевтической композиции;
(e) охлаждение указанной композиции;
(f) заполнение одной или нескольких ампул (флаконов) указанной композицией и
(g) воздействие гамма-радиации на вышеуказанные одну или несколько ампул.
Неограничивающие примеры объемных отношений модифицированного носителя к неокисляемому носителю меньше чем 0,01:99,99 представляют собой отношения 0,0095:99,9905, 0,0090:99,9910 и 0,001:99,999.
Другой вариант настоящего изобретения представляет собой композицию согласно изобретению для использования для лечения животных, нуждающихся в таком лечении.
Дополнительный вариант настоящего изобретения относится к применению предлагаемой (заявляемой) композиции для получения лекарственного препарата для лечения или профилактики болезни у животного, включая людей.
Другой вариант настоящего изобретения представляет собой способ лечения или профилактики заболевания, включающий введение животному, нуждающемуся в таком лечении, эффективного количества предлагаемой (заявляемой) композиции. Один аспект этого способа заключается в лечении бактериальных инфекций у животных, включая животных, используемых для производства продуктов питания, предлагаемой CCFA-содержащей композицией.
Целью настоящего изобретения является разработка новой композиции, которая обеспечивает пролонгированное высвобождение биоактивного вещества.
Следующей целью настоящего изобретения является разработка способа получения новой композиции, которая обеспечивает пролонгированное высвобождение биоактивного вещества.
Другой целью настоящего изобретения является разработка способа лечения заболевания или состояния у животного, нуждающегося в таком лечении.
Эти и другие цели настоящего изобретения будут очевидны для специалистов в данной области техники при прочтении детального описания предпочтительного варианта осуществления со ссылкой на чертежи.
Краткое описание чертежей
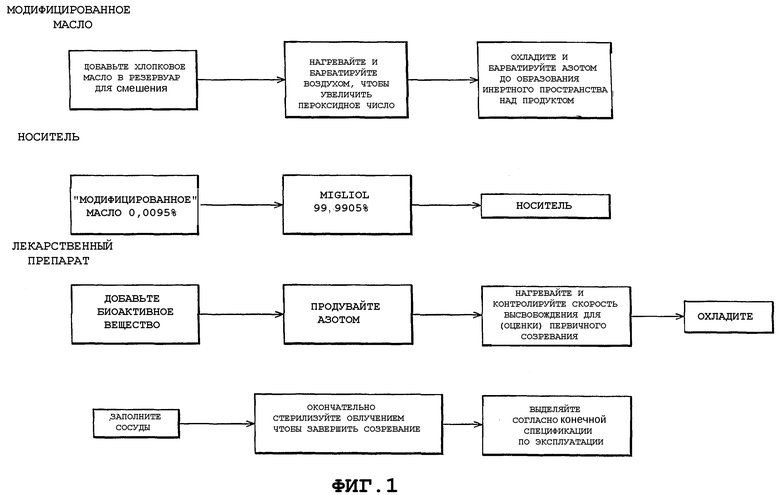
Фиг.1 - схематическое представление способа, который может быть использован для получения заявляемых композиций.
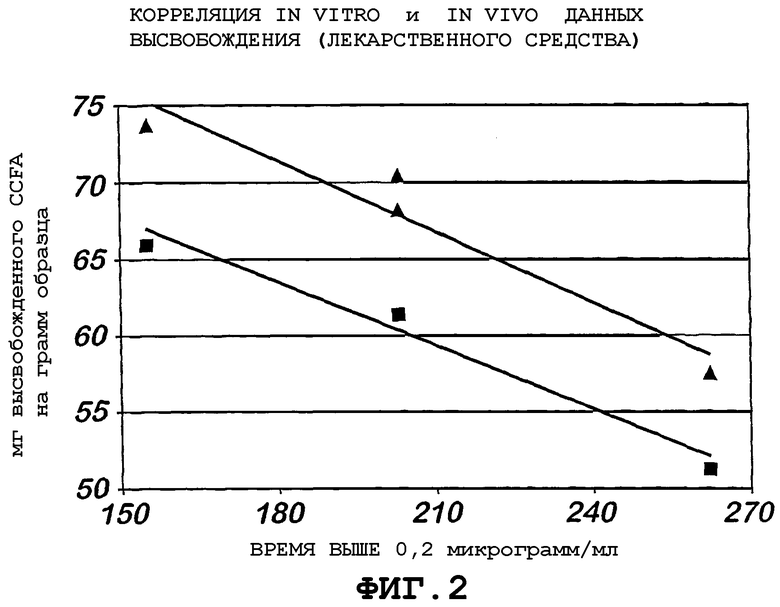
Фиг.2 - график, демонстрирующий корреляцию in vitro и in vivo данных высвобождения лекарственного средства.
Детальное описание изобретения
При описании предпочтительного варианта осуществления для ясности используется определенная терминология. Подразумевается, что указанная терминология охватывает приведенный здесь вариант осуществления, а также все технические эквиваленты, которые действуют аналогичным образом для реализации аналогичной цели, достигая при этом аналогичный результат.
1. Определения терминов
Более полное понимание настоящего изобретения достигается при использовании в настоящем описании нижеследующих определений:
Термин "Биоактивные вещества" в его широком понимании означает фармацевтические препараты, иммуногенные и иммуномодуляторные композиции (включая адъюванты - вещества, повышающие иммуногенностъ антител), векторы, такие как липосомы, и живые векторы, такие как плазмиды, вирусы, споры, пищевые добавки и бактерии и их смеси. Указанные вещества включают без ограничения пищевые добавки, антиинфекционные средства (например, антибиотики, противогрибковые средства, противовирусные средства), противоопухолевые средства (например, противораковые средства, такие как соединения цис-платина), иммуномодуляторы (например, антигистаминные средства, иммуноусилители и иммунодепрессанты), слабительные средства, витамины, противоотечные средства, седативные средства для желудочно-кишечното тракта, антацидные средства, противовоспалительные средства, противоманиакальные средства, вазодилататоры (коронарные, церебральные и периферические), психотропные средства, наркотические средства, стимуляторы, противодиарейные препараты, противоангинальные лекарственные средства, анальгетики, противопиретические средства, снотворные средства, седативные средства, противорвотные средства, стимуляторы роста, средства от тошноты, противосудорожные средства; мышечные релаксанты, действующие в области окончаний двигательных нервов; гипер- и гипогликемические средства; препараты, стимулирующие и тормозящие функцию щитовидной железы, диуретики, цитотоксические соединения, антиспазматические средства, лекарственные средства против артрита, маточные релаксанты, лекарственные средства против ожирения, противоглистные средства, гормоны, вакцины, минеральные и пищевые добавки, нераскрытые в данном перечне средства для ЦНС, и любые их смеси. Особенно предпочтительные биоактивные средства включают без ограничения цефтиофур, включая кристаллическую свободную кислоту цефтиофура (CCFA), соединения платины (например, цис-платин), ибупрофен, пироксикам, 1-[2-(4-фторбензоил)аминоэтил]-4-(7-метоксинафтил)пиперазин гидрохлорид (FAMP), камптотецин, паклитаксел, флуцитозин, ингибиторы циклооксигеназы-II (например, coxibs и хромены) и хинин.
Термин "пролонгированная доставка или пролонгированное высвобождение", используемый здесь в отношении биоактивных веществ, означает непрерывное высвобождение или распределение биоактивного вещества, такое, что количество биоактивного вещества на протяжении длительного периода времени остается в кровотоке пациента при концентрации выше, чем значение, которое дает терапевтически эффективные уровни активного вещества (веществ) в крови. Желаемые эффективные кровяные уровни пролонгированного высвобождения различаются в зависимости от биоактивного вещества, заболевания, подлежащего лечению пациента и т.п., и, как считают, они известны квалифицированному практикующему врачу и могут быть определены рутинным методом. Если, например, биоактивное вещество представляет собой кристаллическую свободную кислоту цефтиофура (CCFA), то для эффективного лечения желательный уровень метаболитов цефтиофура в плазме крови пациента следует поддерживать при или выше 0,2 мкг/мл. В одном варианте осуществления изобретения разовая доза препарата пролонгирующий носитель/CCFA поддерживает уровень метаболитов цефтиофура в плазме крови при или выше 0,2 мкг/мл в течение, по крайней мере, трех и предпочтительно на протяжении четырех-пяти дней после введения. Используемое в настоящем документе выражение "пролонгированная доставка", в частности, следует привести в соответствие с регулятивным определением для такого же термина, который требует, чтобы профиль зависимости концентрации от времени имел три различные фазы (т.е. фазу возрастающей концентрации, фазу плато и фазу убывания концентрации). Несмотря на то, что используемый в настоящем документе термин "пролонгированная доставка" может заключать в себе вышеуказанное регулятивное определение, подразумевается, что используемый термин не ограничивается регулятивным определением, так как композиции, которые представляют собой определенные здесь системы пролонгированной доставки, необязательно имеют три различные фазы (например, композиция может иметь фазу возрастающей концентрации и растянутую (по времени) фазу убывания концентрации).
"Ненасыщенные масла, подходящие для модификации" включают ненасыщенные триглицеридные жиры и масла, включая указанные жиры и масла, полученные из источников растительного, животного происхождения, морских продуктов и синтетическим путем. Примеры жидких носителей, подходящих для модификации, содержащих ненасыщенные углеводородные боковые цепи, включают без ограничения масла природного происхождения, такие как касторовое масло, сафлоровое масло, хлопковое масло, кукурузное масло, оливковое масло, жир печени трески, миндальное масло, масло авокадо, пальмовое масло, кунжутное масло, арахисовое масло и соевое масло. В качестве примера хлопковое масло может быть использовано для получения 70% ненасыщенных жирных кислот (Sigma, St. Louis, МО). Синтетические масла, которые могут быть жидкими носителями, подходящими для модификации, включают глицериды или пропиленгликолевые ди-сложные эфиры ненасыщенных жирных кислот, имеющих от 6 до 24 углеродных атомов. Примеры ненасыщенных карбоновых кислот включают олеиновую, линолевую, линоленовую и т.п. Очевидно, что глицеридный наполнитель может включать моно-, ди- или три-глицериловый сложный эфир жирных кислот или смешанные глицериды и/или пропиленгликолевые ди-сложные эфиры, где, по крайней мере, один гидроксил глицерина был эстерифицирован жирными кислотами, имеющими различную длину цепи углеродных атомов. Примерами три-ненасыщенных триглицериловых сложных эфиров являются триолеин и трилинолеин. Из ди-насыщенных-моно-ненасыщенных: олеодинасыщенными являются 1,2-дипальмитоил-3-олеоил-рац-глицерин или 1,3-дипальмитоил-2-олеоил-рац-глицерин и 1,3-дипальмитоил-2-линолеоил-рац-глицерин. Дополнительными примерами триглицеридов являются моно-насыщенный-ди-ненасыщенные сложные эфиры: моно-насыщенный-олеолинолеин сложные эфиры представляют собой 1-пальмитоил-2-олеоил-3-линолеоил-рац-глицерин и 1-линолеоил-2-олеоил-3-стеароил-рац-глицерин, моно-насыщенный-дилинолеин представляет собой 1,2-дилинолеоил-3-пальмитоил-рац-глицерин. Примеры триглицериловых сложных эфиров: ди-насыщенные сложные эфиры представляют собой 1,2-диолеин или 1,3-диолеин, 1,2-дилинолеин или 1,3-дилинолеин и 1,2-дилиноленин или 1,3-дилиноленин, насыщенные ди-насыщенные сложные эфиры - 1,2-дипальмитин или 1,3-дипальмитин, 1,2-дистеарин или 1,3-дистеарин и 1,2-дидеканоин или 1,3-дидеканоин.
Неограничивающие примеры насыщенных-ненасыщенных диглицериловых сложных эфиров включают три-насыщенные сложные эфиры, а именно, трипальмитин, тристеарин и тридеканоин, 1-пальмитоил-2-олеоил-глицерин или 1-олеоил-2-пальмитоил-глицерин, 1-пальмитоил-2-линолеоил-глицерин или 1-линолеоил-2-пальмитоил-глицерин. Неограничивающие примеры моноглицериловых сложных эфиров: ненасыщенные сложные эфиры представляют собой 1-олеин или 2-олеин, 1-линолеин или 2-линолеин и 1-линолеин или 2-линолеин. Неограничивающие примеры полиэтиленгликоль (ПЭГ, PEG) ненасыщенных ди-эстеров включают 1,2-диолеин или 1,3-диолеин, 1,2-дилинолеин или 1,3-дилинолеин и 1,2-дилиноленин или 1,3-дилиноленин. Среди насыщенных-ненасыщенных диглицериловых сложных эфиров: 1-пальмитоил-2-олеоил-глицерин или 1-олеоил-2-пальмитоил-глицерин, 1-пальмитоил-2-линолеоил-глицерин и 1-линолеоил-2-пальмитоил-глицерин.
Немодифицированный жидкий носитель может представлять собой ненасыщенное масло, подходящее для модификации, которое не было подвергнуто модификации, или, по существу, неокисляемый носитель. Примеры, по существу, неокисляемого носителя включают без ограничения сложные эфиры насыщенных жирных кислот со средне-большой длиной цепи (например, триглицериды насыщенных жирных кислот с длиной цепи от около С6 до около C24). Неограничивающие примеры насыщенных, по существу, неокисляемых масел включают сложные эфиры глицерина или пропиленгликоля и насыщенных жирных кислот, имеющих цепь длиной из от 6 до 24 углеродных атомов, таких как гексановая кислота, октановая (каприловая), нонановая (пеларгоновая), декановая (каприновая), ундекановая, лауриновая, тридекановая, тетрадекановая (миристиновая), пентадекановая, гексадекановая (пальмитиновая), гептадекановая, октадекановая (стеариновая), нонадекановая, гексадекановая (пальмитиновая), гептадекановая, эйкозановая, генэйкозановая, докозановая и лигноцериновая кислота. В некоторых вариантах композиции используют триглицериды средней цепи (МСТ) насыщенных жирных кислот с длиной цепи из от около C8 до C12, полученные из масел природного происхождения (например, кокосовое масло, пальмоядровое масло, масло из бразильского ореха бабассу и т.д.), включая вышеуказанные триглицериды, поставляемые под торговой маркой MIGLYOL от Huls и несущие торговые обозначения 810, 812, 829 и 840. Также отмечаются продукты NeoBeeRTM, поставляемые Drew Chemicals. Изопропилмиристат представляет собой другой пример неокисляемого носителя согласно изобретению. Неограничивающие примеры насыщенных ди-сложных эфиров полиэтиленгликоля (PEG) включают 1,2-дипальмитин или 1,3-дипальмитин, 1,2-дистеарин или 1,3-дистеарин и 1,2-дидеканоин или 1,3-дидеканоин.
Термины "модифицированный" и "модификация" в отношении носителей по изобретению и используемые в формуле изобретения относятся к ненасыщенному носителю, который посредством физического, химического или механического способа был подвергнут изменению по сравнению с его природной (или "немодифицированной" в случае синтетических жидких носителей) формой так, что модифицированный носитель имеет повышенный уровень продуктов окисления. Модификация может быть осуществлена в присутствии источника кислорода тепловой обработкой (модификацией), облучением и/или воздействием источников энергии (например, световое, ультрафиолетовое, инфракрасное, гамма-, рентгеновское излучение или микроволновое излучение), введением катализаторов (т.е. т-бутилпероксида), включением конкретных триглицеридов и их гидропероксидов, включением полимерной разновидности, введением сшивателей или средств, вызывающих полимеризацию, использованием режимов окисления и комбинацией указанных выше способов. Подходящие источники кислорода включают без ограничения воздух, кислород, органические или неорганические пероксиды и т.п. Эти стадии могут быть предприняты до или после добавления лекарственного средства к наполнителю или как до, так и после добавления лекарственного средства к наполнителю.
Термин "существенно перокисленное (peroxidized) ненасыщенное наполнитель-масло" относится к модифицированному жидкому носителю, имеющему пероксидное число от 0,1 до 600, и в некоторых вариантах осуществления изобретения 10, 20, 40 или 80 или любое значение между. Используемые здесь пероксидные числа выражены в виде миллиэквивалентов (мЭкв) пероксида на 1000 грамм образца масла. Пероксидное число обычно измеряют ручным титрованием согласно методу American Oil Chemists' Society (AOCS) (Official Method Cd 8-53)(Official Monographs, Soybean Oil, page 1434), содержание которого включено в настоящее описание в виде ссылки.
2. Изобретение
Настоящее изобретение включает композицию, содержащую:
(а) от одного до трех биоактивных средств;
(b) модифицированный жидкий носитель и
(c) по существу неокисляемый носитель;
где объемное отношение модифицированного жидкого носителя к по существу неокисляемому носителю находится в диапазоне от 0,00001:99,99999 до меньше чем 0,01:99,99 (об./об.), и указанная композиция непосредственно сразу после ее получения может быть введена хозяину, обеспечивая при этом пролонгированное высвобождение от одного до трех биоактивных средств.
Существенное преимущество настоящего изобретения заключается в идентификации лекарственной формы и способа получения лекарственной формы, которая обеспечивает способность пролонгированного высвобождения сразу же после ее получения и которая сохраняет указанный профиль высвобождения при хранении в течение значительного периода времени. В настоящем изобретении определены композиции наполнителя и комбинация стадий их получения, которые обеспечивают получение препаратов с пролонгированным действием после обработки. Во всех вариантах важнейшим признаком является то, что часть наполнителя-носителя подвергают модификации либо до, после, либо как до, так и после объединения указанного наполнителя с биоактивным средством.
Используемые биоактивные средства представляют собой средства, которые определены выше. Предпочтительным биоактивным средством является кристаллическая свободная кислота цефтиофура (CCFA), которую используют в качестве антибиотика в фармацевтических лекарственных формах для лечения имеющих хозяйственное значение млекопитающих и людей, страдающих бактериальными инфекциями. В отдельных вариантах свободную кислоту цефтиофура пролонгированного действия используют в ветеринарии в качестве антибиотического лекарственного средства для лечения таких животных, как крупный рогатый скот, свинья, лошади, овца, коза, домашняя птица и кошки. Такое лечение направлено на борьбу с воздействиями бактериальных инфекций, вызванных чувствительными организмами, такими как Pasteurella haemolytica (Mannheimia Spp.), Pasteurella multocida, Salmonella typhimurium, Salmonella choleraesuis, Actinobacillus pleuropneumoniae, Streptococcus suis, Streptococcus equi (zooepidemicus), и другими Streptococcus бактериями, Haemophilus somnus, Escherichia coli, Staphylococcus aureus и т.п., а также для борьбы с анаэробными инфекциями, вызванными, например, Fusobacterium necrophorum. Указанные типы инфекций обычно ассоциируют с таким заболеваниями у животных, как копытная гниль, респираторная болезнь крупного рогатого скота и респираторная болезнь свиней.
В одном примере модифицированное ненасыщенное масло включает модифицированное хлопковое масло и неокисляемый наполнитель включает насыщенное кокосовое масло или насыщенный продукт кокосового масла (например, MIGLYOL 812). В частности считается, что так называемое "индуцированное" хлопковое масло, которое имеет более высокий уровень продуктов окисления в результате тепловой обработки природного хлопкового масла в присутствии кислорода, является типом модифицированного хлопкового масла. В тех случаях когда биоактивным средством является CCFA, CCFA предпочтительно объединяют с наполнителем этого примера так, чтобы концентрация CCFA в композиции варьировала от 50 мг/мл до 250 мг/мл и обычно от 100 мг/мл до 200 мг/мл. В другом примере модифицированное масло получают из трилинолеина.
На Фиг.1 представлена используемая схема обработки для получения продукта с пролонгированным высвобождением варианта. Природное (немодифицированное) хлопковое масло добавляют в резервуар для смешения, который затем нагревают и барботируют воздухом, чтобы повысить пероксидное число. Затем хлопковое масло охлаждают и барботируют азотом. Хлопковое масло на этой стадии считают модифицированным хлопковым маслом. Затем получают наполнитель смешением соответствующего количества, по объему, модифицированного хлопкового масла с соответствующим количеством, по объему, насыщенного кокосового масла или насыщенный продуктом кокосового масла, например, Miglyol 812, с получением наполнителя, имеющего отношение модифицированного носителя к немодифицированному носителю в диапазоне от 0,00001:99,99999 до меньше чем 0,01:99,99. Биоактивное вещество, например, CCFA, добавляют к наполнителю и смесь продувают азотом. Продуваемую смесь нагревают и контролируют скорость высвобождения лекарственного средства, используя в процессе способ анализа для определения того момента, когда будет достигнута желаемая скорость высвобождения. На этой стадии нагревание прекращают и смесь охлаждают, заполняют смесью сосуды и окончательно стерилизуют посредством гамма-облучения и выделяют согласно конечной спецификации по эксплуатации.
Кроме того, считается, что препараты с пролонгированным действием согласно другим вариантам можно получить альтернативными путями, не выходящими за рамки раскрываемого способа. Например, в одном таком способе лекарственное средство добавляют к смеси немодифицированного ненасыщенного масла и по существу неокисляемого масла и полученную смесь непосредственно подвергают терминальному облучению, чтобы модифицировать ненасыщенное масло и получить наполнитель с характеристикой пролонгированного высвобождения. В другом случае способ завершают после заполнения сосудов и без окончательной стерилизации. В варианте композиции, состоящей из смеси модифицированного носителя, не являющегося маслом, такого как PEG 400, и, по существу, неокисляемого масла, такого как Miglyol 812, смесь лекарственное средство/РЕС-400/Miglyol 812 продувают азотом, нагревают, охлаждают и заполняют в сосуды. Важным аспектом настоящего изобретения является то, что для получения композиции с пролонгированным высвобождением в каждом протоколе не требуется проведения всех стадий обработки. Однако в соответствии с настоящим изобретением необходимым является проведение некоторого типа химической, физической или механической модификации или любая комбинация из вышеперечисленных модификаций.
Помимо этого предлагаемого в настоящем изобретении наполнителя композиции по изобретению могут быть использованы в смеси с обычными наполнителями, т.е. фармацевтически приемлемыми органическими или неорганическими веществами-носителями, подходящими для парентерального, энтерального (например, перорального или путем ингаляции) или местного применения, которые не взаимодействуют с заявляемыми активными композициями, с оказанием вредного воздействия на их активность. Подходящие фармацевтически приемлемые носители включают без ограничения воду, растворы солей, спирты, аравийскую камедь, растительные масла, бензиловые спирты, полиэтиленгликоли, желатин, углеводы, такие как лактоза, амилоза или крахмал, стерат магния, тальк, кремниевую кислоту, вязкий парафин, ароматизированное масло, сложные эфиры жирных кислот, гидроксиметилцеллюлозу, поливинилпирролидон и т.д. Фармацевтические препараты могут быть стерилизованы и, если это требуется, смешаны с вспомогательными средствами, например, смазками, консервантами, стабилизаторами, увлажняющими средствами, эмульгаторами, солями, воздействующими на осмотическое давление, буферами, красителем, ароматизирующими и/или ароматическими веществами и т.п., которые не взаимодействуют с активными композициями, оказывая вредное воздействие на их активность. Кроме того, они могут быть объединены, если требуется, с другими активными средствами, например, витаминами. В конкретных вариантах жидкий носитель может дополнительно содержать загуститель, например, пчелиный воск, твердый парафин или цетиловый спирт. Также в качестве необязательных добавок упоминаются бензиловые спирты, полиэтиленгликоли, вязкий парафин, ароматизированное масло и сложные эфиры жирных кислот.
Заявляемые композиции используют в ветеринарии и медицине. В частности, композиции согласно настоящему изобретению могут быть использованы для лечения людей, животных, используемых для производства продуктов, питания, или домашних животных. К ним относятся без ограничения следующие: животные, используемые для производства продуктов питания, такие как крупный рогатый скот, свинья, овца, козы и олень; домашние животные, такие как кони, кошки и собаки; домашняя птица; или люди. Количество заявляемой композиции, подлежащей введению, должно быть таким, которое может доставить биоактивное средство в количестве и для продолжительности действия, которые необходимы для обеспечения терапевтической пользы при лечении или профилактики заболевания, не вызывая при этом у пациента проблем, связанных с токсичностью. Считается, что определение конкретных количеств, которые следует выбрать для введения, находится в пределах квалификации специалиста в данной области. Например, когда в качестве биоактивного средства выбрана CCFA, в случае внутримышечного или подкожного введения композицию вводят в дозированной лекарственной форме, содержащей от около 0,5 до около 10,0 мг CCFA/кг массы тела пациента, при этом для крупного рогатого скота предпочтительны диапазоны около 4,4-6,6 мг/кг и для свиней 5,0-7,5 мг/кг. Для диапазона, необходимого для завершения, дозы, описанные в патентах США 5721359 и 6074657, явно включены в настоящее описание в виде ссылки.
Введение композиции, как считается, включает хроническую, острую или интермиттирующую схемы лечения, и может быть выбран любой способ, где возможно введение жидкости. Композиции согласно настоящему изобретению могут быть введены парентерально (например, подкожная, интрамаммарная, внутривенная, внутрибрюшинная или внутримышечная инъекция), местно (включая без ограничения лечение поверхности, трансдермальное применение и назальное применение), интравагинально, перорально или ректально.
В случае перорального терапевтического введения композиция может быть введена в форме капсул, эликсиров, суспензий, сиропов и т.п. Такие композиции и препараты должны, как правило, содержать по крайней мере 0,1% активного соединения. Содержание композиций и препаратов может, конечно, варьироваться и обычно составляет от 2 до около 60% массы вводимой дозированной лекарственной формы. Количество активного соединения в таких терапевтически используемых композициях является таким, чтобы можно было получить эффективный уровень дозы. Сироп или эликсир могут содержать активное соединение, сахарозу или фруктозу в качестве подслащивающего средства, метил- и пропилпарабен в качестве консервантов, краситель и ароматизирующее средство, такое как вишневую или апельсиновую отдушку.
Конечно, любое вещество, используемое для получения любой дозированной лекарственной формы, должно быть фармацевтически приемлемым и практически нетоксичным для тех количеств, в которых его используют.
В случае парентерального применения композиции могут быть введены внутривенно или внутрибрюшинно путем инфузии или инъекции. В одном варианте, где CCFA представляет собой биоактивное средство, соответствующим способом введения в соответствии с патентом США 6074657 является подкожная инъекция в ухо. В частности, предусматривается также внутримышечное, интрамаммарное и обычное подкожное введение.
В случае местного введения композиция может быть применена в форме капель (например, для лечения заболеваний или инфекций глаза) или в случае нанесения на кожу в форме способных к растеканию паст, гелей, мазей, мыла и т.п. Полученные жидкие композиции могут также быть применены, используя адсорбирующие повязки или суппозитории, или их можно нанести на поврежденную область распылением, используя распылители насосного типа или аэрозоль.
Следует иметь в виду, что фактические предпочтительные количества активных композиций в каждом отдельном случае обычно варьирует в зависимости от конкретных используемых композиций; конкретных конечных составов композиций; способа применения; конкретного местоположения и организма, подлежащего лечению. Дозы для данного хозяина можно определить, используя обычные методы, например, при обычном сравнении различных активностей заявляемых композиций и известного средства, например, при помощи соответствующего, обычного фармакологического протокола.
Важная особенность настоящего изобретения заключается в том, что посредством осуществления модификации наполнителя-носителя можно полностью регулировать и предсказать эксплуатационную характеристику биоактивного вещества in vivo. По существу, вышеуказанная характеристика биоактивного вещества in vivo остается практически неизменной, начиная от времени получения и на протяжении многих месяцев хранения. В качестве примера указанная характеристика биоактивного средства, вводимого in vivo через 30 дней, 60 дней, 90 дней, 180 дней, 360 дней или 720 дней после получения препарата, оказывается сопоставимой с его характеристикой сразу после получения.
В дальнейшем изобретение поясняется нижеследующими неограничивающими примерами.
Пример 1: Получение модифицированного хлопкового масла
Существенно перокисленное ненасыщенное масло получают из природного хлопкового масла. Природное хлопковое масло добавляют в сосуд, имеющий паровую рубашку для нагревания. Пар подают в рубашку, чтобы нагреть масло до температуры от 85 до 110°С. Воздух барботируют через масло, в то время как масло перемешивают. Скорость потока воздуха варьируется от около 1 стандартного кубического фута в час (SCFH)/литр до 20 (SCFH)/литр. Перемешивание устанавливают таким, чтобы температура масла оставалась постоянной на протяжении периода времени нагревания. Масло нагревают в течение времени и при температуре, необходимых для того, чтобы достичь пероксидного числа, измеряемого согласно способу US Pharmacopea (USP 24 NF 19 at page 1870) или согласно способу 8-53 AOCS, и затем охлаждают, переносят в другой контейнер и хранят в атмосфере азота. Чтобы достичь пероксидного числа около 10, при температуре около 89°С масло нагревают в течение около 9 часов; при температуре около 100°С масло нагревают в течение около 3 часов; при температуре около 105°С масло нагревают в течение около 2,3 часов. Для достижения пероксидного числа около 40 при температуре около 100°С масло нагревают в течение около 6,75 часов, а при температуре около 105°С масло нагревают в течение около 5,5 часов. Для достижения пероксидного числа около 80 при температуре около 100°С масло нагревают в течение около 8 часов. Считается, что связь между временем и температурой масла в сравнении с его пероксидным числом носит линейный характер и что специалист в данной области может достичь желательного пероксидного числа в зависимости от выбранных для обработки времен и температур.
Пример 2: Анализ характеристики высвобождения
В нижеследующем примере описывается способ определения характеристики пролонгированного высвобождения активного компонента из цефтиофурсодержащей композиции с пролонгированным действием. Этот способ, как было показано, коррелирует in vitro результаты с in vivo уровнями в крови, как это иллюстрировано на Фиг.2, где высвобождение активного компонента (цефтиофура) из фармацевтической композиции лекарственного препарата сравнивают с его уровнями в крови in vivo.
In vitro испытание заявляемых композиций
(а) Общая методика растворения
Оборудование:
В экспериментах по высвобождению лекарственного средства в качестве среды растворения использовали 0,05 молярный фосфатный буфер с рН 6,5, полученной путем добавления 31,98 грамм первичного кислого ортофосфата калия (KH2PO4) и 15,39 грамм вторичного кислого ортофосфата калия (K2HPO4) к деионизированной воде и разбавления до 1000 мл, затем разбавляя снова согласно коээфициенту разбавления 10 деионизированной водой (т.е. 100 мл исходного буфера до 1000 мл деионизированной водой).
b) Методика:
Диспергируйте соответствующее количество (например, 30-70 мг) композиции для испытания на растворение в пустом сосуде объемом 40 мл. Уравновесьте среду растворения при соответствующей температуре (например, 22°С). Добавьте соответствующий объем (например, 30 мл) среды растворения в сосуд, содержащий образец для испытания на растворение. Повторите для всех образцов. Выполните вышеописанную процедуру в течение 2-3 минут. Начните перемешивание.
В предварительно определенные моменты времени (например 30 минут или 60 минут) отберите пробы для количественного анализа. Отфильтруйте их, если необходимо. Приступите к количественному анализу.
с) Общая методика (проведения) количественного анализа
Если не оговорено особо, далее придерживаются нижеследующей общей методики.
d) Расчет выделившегося количества анализируемого вещества
Количество выделившегося анализируемого вещества (например, цефтиофура) в каждый момент времени можно рассчитать согдасно нижеследующей формуле.
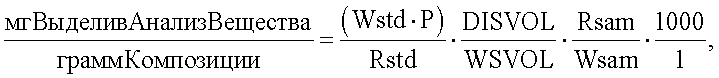
где
Wstd = Масса стандартного препарата, в мг.
Р = Чистота эталонного (сравнительного) стандарта в виде свободной кислоты цефтиофура.
Rstd = Площадь пика стандартного препарата.
DISVOL = Объем жидкости для растворения, в мл (30).
WSVOL = Объем общепринятого стандарта, в мл (10).
Rsam = Площадь пика (образца) испытываемого) препарата.
Wsam = Масса суспензии образца, в мг.
1000 = Пересчет массы образца из мг в грамм.
In vivo испытание заявляемых композиций
Коровам, страдающим либо заболеваниями органов дыхания крупного рогатого скота, либо анаэробной инфекцией межпальцевого пространства, вводят инъекцией любую из композиций Примеров 3-6 так, чтобы уровень введения CCFA находился в диапазоне от около 4,4 до около 6,6 мг CCFA/кг массы тела животного. Введение осуществляют подкожной инъекцией в шею или подкожной инъекцией в ухо, как описано в патенте США 6074657. Концентрация эффективных метаболитов CCFA в плазме крови коров возрастает до, по крайней мере, 0,2 мкг/мл в пределах одного часа после введения и остается постоянной при или выше указанного уровня в течение, по крайней мере, от 80 до около 140 часов. Для схемы (программы) лечения требуется только одно введение CCFA.
Корреляция in vitro и in vivo высвобождения лекарственного средства
Три партии суспензии свободной кислоты цефтиофура, которые показали различную in vivo фармококинетическую характеристику, были использованы для оценки взаимосвязи между in vivo высвобождением лекарственного средства и результатами in vitro испытания. Партии демонстрировали различную in vivo фармакокинетическую характеристику. Различия в фармакокинетической характеристике подтверждались различиями в продолжительности эффекта пролонгированного высвобождения активного компонента, которая представлена количеством часов, на протяжении которых цефтиофур обнаруживали в кровотоке животных, обычно называемой "время выше 0,2 мкг/мл". Корреляция результатов in vitro высвобождения лекарственного средства с "временем выше 0,2 мкг/мл" представлена на Фиг.2. In vitro результаты представлены для образцов (проб), взятых в моменты времени: на 60 минуте (точки данных, представленные квадратами) и 150 минуте (точки данных, представленные треугольниками). Сплошные линии на графике представляют собой наилучший подбор (кривых) методом наименьших квадратов для данных и включены для иллюстрации обратной связи между высвобожденным количеством лекарственного средства, in vitro, и продолжительностью эффекта пролонгированного высвобождения, наблюдаемого in vivo. Партии, которые выделили большее количество CCFA на данный момент времени in vitro, имели более короткую продолжительность пролонгированного высвобождения in vivo. Как можно видеть из Фиг.2, композиции, демонстрирующие скорость высвобождения лекарственного средства в in vitro анализе от 50 до 70 мг на грамм композиции за 60 минут, обеспечивают пролонгированное высвобождение лекарственного средства в условиях in vivo на протяжении больше чем 150 часов.
Пример 3: Получение препарата CCFA конц. 100 мг/мл в наполнителе, содержащем 0,01% (0,0001 частей) хлопкового масла (CSO) и 99,99% (0,9999 частей) Migliol 812
(i) 0,0001 частей (0,3 мл), по объему, CSO смешивают с 0,9999 частей (2999,7 мл), по объему, Migliol 812, получая наполнитель-носитель.
(ii) Добавляют 0,111 мас. частей CCFA и смешивают, получая однородную суспензию такую, что конечная концентрация CCFA составляет 100 мг/мл.
(iii) Суспензию нагревают при 95°С в течение 22,9 часов.
(iv) Суспензию упаковывают и стерилизуют гамма-облучением.
Полученный продукт представляет собой стабильный препарат CCFA с пролонгированным действием, имеющий концентрацию 100 мг/мл и in vitro пролонгированное высвобождение 52,6 мг/мл.
Пример 4: Получение препарата CCFA конц. 100 мг/мл в наполнителе, содержащем 0,001% (0,0001 частей) хлопкового масла (CSO) и 99,999% (0,99999 частей) Migliol 812
(i) 0,00001 частей (0,03 мл), по объему, CSO смешивают с 0,99999 частей (2999,97 мл), по объему, Migliol 812, получая наполнитель-носитель.
(ii) Добавляют 0,111 мас. частей. CCFA и смешивают, получая однородную суспензию такую, что конечная концентрация CCFA составляет 100 мг/мл.
(iii) Суспензию нагревают при 95°С в течение 22,6 часов.
(iv) Суспензию упаковывают и стерилизуют гамма-облучением.
Полученный продукт представляет собой стабильный препарат CCFA с пролонгированным действием, имеющий концентрацию 100 мг/мл и пролонгированное высвобождение, определенное in vitro испытанием 52,0 мг/мл.
Пример 5: Получение препарата CCFA конц. 100 мг/мл в наполнителе, содержащем 0,0001% (0,000001 частей) хлопкового масла (CSO) и 99,9999% (0,999999 частей) Migliol 812
(i) 0,000001 частей (0,003 мл), по объему, CSO смешивают с 0,999999 частей (2999,997 мл), по объему, Migliol 812, получая наполнитель-носитель.
(ii) Добавляют 0,111 мас. частей CCFA и смешивают, получая однородную суспензию такую, что конечная концентрация CCFA составляет 100 мг/мл.
(iii) Суспензию нагревают при 95°С в течение 23,0 часов.
(iv) Суспензию упаковывают и стерилизуют гамма-облучением.
Полученный продукт представляет собой стабильный препарат CCFA с пролонгированным действием, имеющий концентрацию 100 мг/мл и пролонгированное высвобождение, определенное in vitro испытанием 52,0 мг/мл.
Пример 6: Получение препарата CCFA конц. 200 мг/мл в наполнителе, содержащем 0,00000048 частей трилинолеина и 0,99999952 частей Migliol 812
(i) 0,00000048 частей (0,0009 мл), по объему, трилинолеина смешивают с 0,99999952 частей (1874,9991 мл), по объему, Migliol 812, получая наполнитель-носитель.
(ii) Добавляют 0,22 мас. частей CCFA и смешивают в течение 1 часа, получая однородную суспензию такую, что конечная концентрация CCFA составляет 200 мг/мл.
(iii) Суспензию нагревают при около 85-110°С и предоставляют возможность охладиться.
(iv) Суспензию упаковывают и стерилизуют гамма-облучением.
Полученный продукт представляет собой стабильный препарат CCFA с пролонгированным действием, имеющий концентрацию 200 мг/мл.
После детального описания изобретения и рассмотрения предпочтительных вариантов его выполнения становится очевидным, что возможны различные модификации и вариации изобретения, не выходящие за рамки объема нижеследующей формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ИЗМЕРЕНИЯ СКОРОСТИ РАСТВОРЕНИЯ АНАЛИЗИРУЕМОГО ВЕЩЕСТВА В НЕВОДНОЙ ЖИДКОЙ КОМПОЗИЦИИ | 2003 |
|
RU2300766C2 |
| ДИСПЕРГИРУЕМЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2003 |
|
RU2311201C2 |
| ДИСПЕРГИРУЕМЫЙ ПРЕПАРАТ ПРОТИВОВОСПАЛИТЕЛЬНОГО АГЕНТА | 2004 |
|
RU2319508C2 |
| 2-S-БЕНЗИЛЗАМЕЩЕННЫЕ ПИРИМИДИНЫ В КАЧЕСТВЕ АНТАГОНИСТОВ CRTH2 | 2008 |
|
RU2491279C2 |
| СПОСОБ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ДОСТАВКИ ПРОТИВОВОСПАЛИТЕЛЬНОГО СРЕДСТВА | 2004 |
|
RU2325189C2 |
| АЛКИЛТИОПИРИМИДИНЫ В КАЧЕСТВЕ АНТАГОНИСТОВ CRTH2 | 2008 |
|
RU2491280C2 |
| КОНЪЮГАТ АНТИБИОТИКА И АНТИБАКТЕРИАЛЬНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2007 |
|
RU2371447C2 |
| КРИСТАЛЛИЧЕСКАЯ СВОБОДНАЯ ЦЕФТИОФУРОВАЯ КИСЛОТА, КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1994 |
|
RU2136685C1 |
| ОЧИЩЕННОЕ ПРОИЗВОДНОЕ ЦИКЛОДЕКСТРИНА, КЛАТРАТНЫЙ КОМПЛЕКС ОЧИЩЕННОГО ПРОИЗВОДНОГО ЦИКЛОДЕКСТРИНА С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2099354C1 |
| БЕНЗОЙНАЯ КИСЛОТА, ПРОИЗВОДНЫЕ БЕНЗОЙНОЙ КИСЛОТЫ И КОНЪЮГАТЫ ГЕТЕРОАРИЛКАРБОНОВОЙ КИСЛОТЫ С ГИДРОМОРФОНОМ, ПРОЛЕКАРСТВА, СПОСОБЫ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2573388C2 |
Настоящее изобретение относится к фармацевтическим композициям и способам их получения. Разработаны новые фармацевтические композиции с пролонгированным высвобождением, содержащие кристаллическую свободную кислоту цефтиофура и носитель, содержащий (i) модифицированный жидкий носитель и (ii) немодифицированный жидкий носитель. Предложенные композиции обеспечивают пролонгированное высвобождение биоактивного вещества. 2 н. и 10 з.п. ф-лы, 2 ил.
1. Фармацевтическая композиция с пролонгированным высвобождением, содержащая:
(a) кристаллическую свободную кислоту цефтиофура; и
(b) носитель, содержащий:
(i) модифицированный жидкий носитель, и
(ii) немодифицированный жидкий носитель,
где отношение, по объему, модифицированного жидкого носителя к немодифицированному жидкому носителю находится в диапазоне от 0,00001:99,99999 до менее чем 0,0095:99,9905, что обеспечивает пролонгированное высвобождение и где эта указанная композиция непосредственно сразу после ее получения может вводиться реципиенту так, что кристаллическая свободная кислота цефтиофура поставляется реципиенту пролонгированным образом.
2. Композиция по п.1, где указанный носитель включает модифицированный жидкий носитель и немодифицированное ненасыщенное масло, подходящее для модификации.
3. Композиция по п.1, где указанный носитель включает модифицированное и неокисляемое масло.
4. Композиция по п.1, где указанный модифицированный жидкий носитель включает модифицированное растительное масло, и это указанное растительное масло выбрано из группы, состоящей из кукурузного масла, арахисового масла, кунжутного масла, оливкового масла, пальмового масла, сафлорового масла, соевого масла, хлопкового масла, рапсового масла, подсолнечного масла и их смесей.
5. Композиция по п.2, где указанный модифицированный жидкий носитель включает модифицированное хлопковое масло.
6. Композиция по п.2, где указанный немодифицированный жидкий носитель включает кокосовое масло.
7. Композиция по п.1, содержащая кристаллическую свободную кислоту цефтиофура, модифицированное хлопковое масло и насыщенное кокосовое масло.
8. Композиция по п.1, содержащая кристаллическую свободную кислоту цефтиофура, модифицированный трилинолеин и насыщенное кокосовое масло.
9. Композиция по пп.7 и 8, где отношение, по объему, модифицированного хлопкового масла к насыщенному кокосовому маслу находится в диапазоне от 0,00001:99,99999 до менее чем 0,0095:99,9905.
10. Композиция по п.7, где концентрация кристаллической свободной кислоты цефтиофура в указанной композиции варьирует от около 50 мг/мл до около 250 мг/мл.
11. Композиция по п.7, где концентрация кристаллической свободной кислоты цефтиофура в указанной композиции варьирует от около 100 мг/мл до около 200 мг/мл.
12. Способ получения фармацевтической композиции, включающий стадии:
(а) получения носителя, содержащего модифицированный жидкий носитель и немодифицированный жидкий носитель, где отношение, по объему, модифицированного жидкого носителя к немодифицированному жидкому носителю находится в диапазоне от 0,00001:99,99999 до менее чем 0,01:99,99, что обеспечивает пролонгированное высвобождение, и
(b) объединения указанного модифицированного носителя с кристаллической свободной кислотой цефтиофура.
| АВТООПЕРАТОР ДЛЯ ГАЛЬВАНОАВТОМАТОВ | 0 |
|
SU222107A1 |
| US 6074657 A, 13.06.2000 | |||
| US 5721359 A, 24.02.1998. | |||
Авторы
Даты
2010-10-10—Публикация
2003-11-17—Подача