Область, к которой относится изобретение
Настоящее изобретение относится к фармацевтическому средству для стимуляции неогенеза или регенерации панкреатических β-клеток, продуцирующих инсулин. Настоящее изобретение также относится к способу снижения или лечения гипергликемии посредством стимуляции неогенеза или регенерации панкреатических β-клеток.
Предшествующий уровень техники
Диабет, также называемый гипергликемией, представляет собой метаболическое расстройство, главным образом нарушение метаболизма глюкозы, вызываемое, например, недостаточной секрецией инсулина или пониженной чувствительности клеток-мишеней к инсулину и характеризующееся высоким уровнем сахара в крови. Если высокий уровень сахара поддерживается в течение длительного периода времени, то в различных органах и в нервных тканях могут возникать серьезные осложнения, такие как ретинопатия, нефропатия и невропатия, обусловленные главным образом ангиопатией. Поэтому регуляция и поддержание нормальных уровней сахара в крови имеют очень важное значение для лечения диабета, и в настоящее время проводятся исследования в целях получения подходящих средств для регуляции уровней сахара в крови.
Для диагностики диабета (гипергликемии) проводят тест на толерантность к глюкозе (пероральное введение 75 г глюкозы). Для проведения такой диагностики у индивидуума берут кровь натощак для измерения уровней инсулина и сахара в крови, а затем через некоторый период времени после употребления этим индивидуумом воды, содержащей растворенные в ней 75 г глюкозы, снова берут кровь для измерения уровней инсулина и сахара в крови. Если величина (ΔIRI/ΔBG) “разности уровней инсулина в крови за 30 минут до употребления глюкозы и через 30 минут после употребления глюкозы” (ΔIRI), деленная на “разность уровней сахара в крови за 30 минут до употребления глюкозы и через 30 минут после употребления глюкозы” (ΔBG) не превышает 0,4, то это указывает на высокий риск серьезного обострения гипергликемии.
Диабет подразделяется главным образом на два класса, диабет типа 1 и диабет типа 2. Диабет типа 1 развивается при полном отсуствии секреции инсулина, вызываемом нарушением функции или гибелью панкреатических β-клеток, которая приводит к прекращению или к сильному снижению секреции инсулина. Это может быть вызвано вирусной инфекцией или аутоиммунной патологией, возникающей вследствие вирусной инфекции. Диабет типа 2 развивается вследствие снижения секреции инсулина из панкреатических β-клеток (количественной недостаточности инсулина) или вследствие снижения функции инсулина в клетках, поглощающих глюкозу (инсулинорезистентности), и по мере повышения инсулинорезистентности относительное количество инсулина становится недостаточным и уровни сахара в крови начинают повышаться. В последнем случае, из панкреатических β-клеток начинает секретироваться избыточное количество инсулина, что приводит к его относительной недостаточности, и когда избыточная секреция инсулина достигает максимального уровня и поддерживается в течение длительного периода времени, панкреатические β-клетки полностью истощаются и секреция инсулина из этих клеток снижается.
Поэтому считается, что основной причиной диабета (гипергликемии) является дефицит панкреатических β-клеток и снижение уровня продуцирования или недостаточная секреция инсулина в этих клетках.
Хотя в настоящее время для снижения уровней сахара в крови используются инсулиновые препараты, бигуанид-содержащие средства; средства, содержащие сульфонилмочевину, тиазолидиндион-содержащие средства и т.п., однако применяемые в настоящее время гипогликемические средства пока еще не удовлетворяют современным требованиям из-за их побочных эффектов и т.п. Кроме того, поскольку эти средства были разработаны в целях снижения уровней сахара в крови, то такие средства могут быть использованы для симптоматического лечения, направленного на регуляцию уровней сахара в крови, и пока еще являются недостаточными для проведения лечебной терапии, позволяющей устранить основные причины диабета, описанные выше, то есть дефицит самих β-клеток и снижение уровня продуцирования или недостаточную секрецию инсулина в этих клетках.
Исходя из вышеописанного, очевидно, что для снижения или лечения гипергликемии крайне необходимо разработать средства, способные стимулировать неогенез или регенерацию панкреатических β-клеток, предотвращать истощение или гибель панкреатических β-клеток и, кроме того, стимулировать продуцирование инсулина в панкреатических β-клетках.
С другой стороны, в 1999 году в желудке крыс был обнаружен гормон грелин, который представляет собой пептид, имеющий совершенно уникальную химическую структуру, где 3-я N-концевая аминокислота ацилирована жирной кислотой (Nature, 402, pp.656-660, 1999). Было показано, что грелин обладает активностью, стимулирующей секрецию гормона роста из гипофиза, и недавно проведенные исследования также показали, что этот гормон обладает такими функциями, как стимуляция потребления пищи или накопление жира, что приводит к увеличению массы тела и нарушению сердечной функции (Nature, 409, pp.194-198, 2001; Endocr. Rev., 25, pp.426-457, 2004; Front Neuroendocrinol., 25, pp.27-68, 2004).
Грелин был выделен у крыс и очищен как эндогенный фактор, стимулирующий секрецию гормона роста (GHS), для секреторного рецептора гормона роста (GHS-R). Помимо крысиного грелина, известны также аминокислотные последовательности грелина других позвоночных, таких как, например, человек, мышь, свинья, курица, угорь, корова, лошадь, овца, лягушка, форель и собака, у которых этот гормон имеет аналогичные первичные структуры.
Человек:
GSS(н-октаноил)FLSPEHQRVQQRKESKKPPAKLQPR (последовательность No.1)
GSS (н-октаноил)FLSPEHQRVQRKESKKPPAKLQPR (последовательность No. 2)
Крыса:
GSS(н-октаноил)FLSPEHQKAQQRKESKKPPAKLQPR (последовательность No. 3)
GSS(н-октаноил)FLSPEHQKAQRKESKKPPAKLQPR (последовательность No. 4)
Мышь:
GSS(н-октаноил)FLSPEHQKAQQRKESKKPPAKLQPR (последовательность No. 5)
Свинья:
GSS(н-октаноил)FLSPEHQKVQQRKESKKPAAKLKPR (последовательность No. 6)
Корова:
GSS(н-октаноил)FLSPEHQKLQRKEAKKPSGRLKPR (последовательность No. 7)
Овца:
GSS(н-октаноил)FLSPEHQKLQRKEPKKPSGRLKPR (последовательность No. 8)
Собака:
GSS(н-октаноил)FLSPEHQKLQQRKESKKPPAKLQPR (последовательность No. 9)
Угорь:
GSS(н-октаноил)FLSPSQRPQGKDKKPPRV-NH2 (последовательность No. 10)
Форель:
GSS(н-октаноил)FLSPSQKPQVRQGKGKPPRV-NH2 (последовательность No. 11)
GSS(н-октаноил)FLSPSQKPQGKGKPPRV-NH2 (последовательность No. 12)
Курица:
GSS(н-октаноил)FLSPTYKNIQQQKGTRKPTAR (последовательность No. 13)
GSS(н-октаноил)FLSPTYKNIQQQKDTRKPTAR (последовательность No. 14)
GSS(н-октаноил)FLSPTYKNIQQQKDTRKPTARLH (последовательность No. 15)
Лягушка-бык:
GLT(н-октаноил)FLSPADMQKIAERQSQNKLRHGNM (последовательность No. 16)
GLT(н-деканоил)FLSPADMQKIAERQSQNKLRHGNM (последовательность No. 16)
GLT(н-октаноил)FLSPADMQKIAERQSQNKLRHGNMN (последовательность No. 17)
Тилапия:
GSS(н-октаноил)FLSPSQKPQNKVKSSRI-NH2 (последовательность No. 18)
Зубатка:
GSS(н-октаноил)FLSPTQKPQNRGDRKPPRV-NH2 (последовательность No. 19)
GSS(н-октаноил)FLSPTQKPQNRGDRKPPRVG (последовательность No. 20)
Лошадь:
GSS(н-бутаноил)FLSPEHHKVQHRKESKKPPAKLKPR (последовательность No. 21)
(В вышеуказанных последовательностях аминокислотные остатки представлены однобуквенными кодами).
Описанный выше пептид имеет специфическую структуру, где сериновый остаток (S) или треониновый остаток (Т) в 3-м положении имеет боковую гидроксильную группу, ацилированную жирной кислотой, такой как октановая кислота или декановая кислота. За исключением грелина, не имеется каких-либо других примеров выделенного из организма биологически активного пептида, который имел бы такую же гидрофобную модифицированную структуру. Известно, что этот пептид обладает сильной активностью, направленной на высвобождение гормона роста, и участвует в регуляции секреции гормона роста (публикация Международной заявки WO 01/07475).
Поскольку грелин и его рецептор (GHS-R) также экспрессируются в поджелудочной железе (Endocrinology, 145, pp.3813-3820, 2004; Brain Res. Mol. Brain Res., 48, pp.23-29, 1997; J.Clin. Endocrinol. Metab., 87, pp.1300-1308, 2002), то были проведены исследования метаболизма глюкозы или секреции инсулина, которые показали, что грелин регулирует уровень инсулина и глюкозы в крови, а также сообщалось, что грелин повышает уровень сахара в крови и подавляет или стимулирует секрецию инсулина (Pancreas, 27, pp.161-166, 2003; Endocrinology, 144, pp.916-921, 2003; Eur. J. Endocrinol., 146, pp.241-244, 2002; Endocrinology, 143, pp.185-190, 2002; J.Neuroendcrinol., 14, pp.555-560, 2002). Однако не было высказано каких-либо предположений о том, что грелин стимулирует неогенез или регенерацию панкреатических β-клеток.
Кроме того, хотя в публикации Международной заявки WO2001/56592 (и в публикациях патентных заявок США 2001/0020012A1 и 2004/0063636A1) высказываются предположения о возможности применения лиганда для рецептора GHS-R 1A, включая грелин, в качестве фармацевтического средства для лечения диабета типа 2, однако в этих публикациях нигде не указыватся на возможность применения грелина в качестве лекарственного средства для лечения диабета типа 2, и специалистам не известно, является ли такое средство действительно эффективным, как это предполагается в указанной публикации. Кроме того, хотя в публикации Международной заявки WO2002/60472 описано действие грелина, способствующее ожирению, однако его эффективность в лечении диабета не была продемонстрирована.
Что касается взаимосвязи между панкреатическими β-клетками и действием грелина, то известен феномен, заключающийся в том, что при подавлении дифференцировки β-клеток панкреатические β-клетки заменяются грелин-продуцирующими клетками (ε-клетками) (Proc. Natl. Acad. Sci., 101, pp. 2924-2929, 2004). Хотя было высказано предположение о вероятности того, что клетки этих двух типов могут происходить от одной и той же клетки-предшественника и что в будущем продуцирование группы чистых β-клеток из стволовых клеток или т.п. с использованием грелин-продуцирующих клеток позволит лечить диабет на клеточном уровне, однако такая вероятность остается лишь предположением и пока не нашла своего подтверждения. Кроме того, в этой публикации не высказывается какого-либо предположения или утверждения, что действие грелина стимулирует неогенез или регенерацию β-клеток или стимулирует продуцирование инсулина в панкреатических β-клетках.
Описание изобретения
Проблемы, решаемые с помощью настоящего изобретения
Целью настоящего изобретения является разработка способа стимуляции неогенеза или регенерации панкреатических β-клеток, продуцирующих и секретирующих инсулин, и получение фармацевтического препарата для снижения или лечения гипергликемии путем стимуляции неогенеза или регенерации панкреатических β-клеток, продуцирующих и секретирующих инсулин при гипергликемии, вызываемой отсутствием секреции инсулина или очень низким уровнем секреции инсулина, обусловленными нарушением функций или гибелью панкреатических β-клеток, или при гипергликемии, вызываемой снижением уровня секреции инсулина в β-клетках.
Способы решения указанных проблем
В результате самого тщательного исследования, проводимого в целях решения вышеуказанных проблем, авторами настоящего изобретения было обнаружено, что грелин в значительной степени стимулирует неогенез или регенерацию панкреатических β-клеток и что грелин обладает активностью, стимулирующей продуцирование инсулина в панкреатических β-клетках. И эти данные были положены в основу разработки настоящего изобретения.
Более конкретно, настоящее изобретение относится:
(1) к фармацевтической композиции для снижения или лечения гипергликемии, где указанная композиция содержит в качестве эффективного компонента пептид, выбранный из группы, состоящей из пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста (GHS-R); пептида, имеющего аминокислотную последовательность, описанную как последовательность No.1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No.1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R, или их фармацевтически приемлемой соли;
(2) к фармацевтической композиции по вышеуказанному пункту (1), где гипергликемия вызывается отсутствием секреции инсулина или очень низким уровнем секреции инсулина, обусловленными нарушением функции или гибелью панкреатических β-клеток, либо она вызывается снижением уровня секреции инсулина в панкреатических β-клетках;
(3) к фармацевтической композиции по вышеуказанному пункту (2), где гипергликемия вызывается отсутствием секреции инсулина или очень низким уровнем секреции инсулина, обусловленными нарушением функции или гибелью панкреатических β-клеток;
(4) к фармацевтической композиции по вышеуказанному пункту (2), где гипергликемия вызывается снижением секреции инсулина в панкреатических β-клетках;
(5) к фармацевтической композиции по любому из вышеуказанных пунктов (1)-(4), где величина ΔIRI/ΔBG при гипергликемии не превышает 0,4;
(6) к фармацевтической композиции по любому из вышеуказанных пунктов (1)-(5), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(7) к фармацевтической композиции по вышеуказанному пункту (6), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(8) к фармацевтической композиции для стимуляции неогенеза или регенерации панкреатических β-клеток, где указанная композиция содержит в качестве эффективного компонента: пептид, выбранный из группы, состоящей из пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R, или их фармацевтически приемлемой соли;
(9) к фармацевтической композиции по вышеуказанному пункту (8), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(10) к фармацевтической композиции по вышеуказанному пункту (9), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(11) к фармацевтической композиции для стимуляции продуцирования инсулина в панкреатических β-клетках, где указанная композиция содержит в качестве эффективного компонента: пептид, выбранный из группы, состоящей из пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R, или их фармацевтически приемлемой соли;
(12) к фармацевтической композиции по вышеуказанному пункту (11), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(13) к фармацевтической композиции по вышеуказанному пункту (12), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(14) к способу снижения или лечения гипергликемии, включающему стадию введения индивидууму, страдающему гипергликемией, пептида, выбранного из группы, состоящей из пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R, или их фармацевтически приемлемой соли;
(15) к способу по вышеуказанному пункту (14), где гипергликемия вызывается отсутствием секреции инсулина или очень низким уровнем секреции инсулина, обусловленными нарушением функции или гибелью панкреатических β-клеток, либо она вызывается снижением уровня секреции инсулина в панкреатических β-клетках;
(16) к способу по вышеуказанному пункту (15), где гипергликемия вызывается отсутствием секреции инсулина или очень низким уровнем секреции инсулина, обусловленными нарушением функции или гибелью панкреатических β-клеток;
(17) к способу по вышеуказанному пункту (15), где гипергликемия вызывается снижением секреции инсулина в панкреатических β-клетках;
(18) к способу по любому из вышеуказанных пунктов (14)-(17), где величина ΔIRI/ΔBG при гипергликемии не превышает 0,4;
(19) к способу по любому из вышеуказанных пунктов (14)-(18), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(20) к способу по вышеуказанному пункту (19), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(21) к способу стимуляции неогенеза или регенерации панкреатических β-клеток, включающему стадию введения индивидууму пептида, выбранного из группы, состоящей из пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R, или их фармацевтически приемлемой соли;
(22) к способу по вышеуказанному пункту (21), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(23) к способу по вышеуказанному пункту (22), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(24) к способу стимуляции продуцирования инсулина в панкреатических β-клетках, включающему стадию введения индивидууму пептида, выбранного из группы, состоящей из пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R, или их фармацевтически приемлемой соли;
(25) к способу по вышеуказанному пункту (24), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(26) к способу по вышеуказанному пункту (25), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(27) к применению пептидного или не-пептидного соединения в целях получения фармацевтических композиций для снижения или лечения гипергликемии, где:
указанный пептид выбран из группы, состоящей из: пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R;
(28) к применению по вышеуказанному пункту (27), где гипергликемия вызывается отсутствием секреции инсулина или очень низким уровнем секреции инсулина, обусловленными нарушением функции или гибелью панкреатических β-клеток, либо она вызывается снижением уровня секреции инсулина в панкреатических β-клетках;
(29) к применению по вышеуказанному пункту (28), где гипергликемия вызывается отсутствием секреции инсулина или очень низким уровнем секреции инсулина, обусловленными нарушением функции или гибелью панкреатических β-клеток;
(30) к применению по вышеуказанному пункту (28), где гипергликемия вызывается снижением секреции инсулина в панкреатических β-клетках;
(31) к применению по любому из вышеуказанных пунктов (27)-(30), где величина ΔIRI/ΔBG при гипергликемии не превышает 0,4;
(32) к применению по любому из вышеуказанных пунктов (27)-(31), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(33) к применению по вышеуказанному пункту (32), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(34) к применению пептидного или не-пептидного соединения в целях получения фармацевтических композиций для стимуляции неогенеза или регенерации панкреатических β-клеток, где:
указанный пептид выбран из группы, состоящей из: пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R;
(35) к применению по вышеуказанному пункту (34), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(36) к применению по вышеуказанному пункту (35), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(37) к применению пептидного или не-пептидного соединения в целях получения фармацевтической композиции для стимуляции продуцирования инсулина в панкреатических β-клетках, где:
указанный пептид выбран из группы, состоящей из: пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R;
(38) к применению по вышеуказанному пункту (37), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(39) к применению по вышеуказанному пункту (38), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(40) к способу предотвращения нарушения функции, гибели или истощения панкреатических β-клеток, включающему стадию введения индивидууму пептида, выбранного из группы, состоящей из пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; или их фармацевтически приемлемой соли;
(41) к способу по вышеуказанному пункту (40), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(42) к способу по вышеуказанному пункту (41), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой;
(43) к способу индуцирования неогенеза или регенерации панкреатических β-клеток посредством воздействия пептида на панкреатические β-клетки или на клетки-предшественники панкреатических β-клеток, выделенных у индивидуума, где указанный пептид выбран из группы, состоящей из пептидного или не-пептидного соединения, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь; пептида, имеющего аминокислотную последовательность, описанную как последовательность No. 1 и включающую делецию, замену и/или добавление одной или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от амино-конца, где 3-й аминокислотный остаток от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в его боковую цепь; и пептида, обладающего активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с GHS-R;
(44) к способу по вышеуказанному пункту (43), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, и где сериновый остаток в 3-положении от амино-конца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи указанного остатка;
(45) к способу по вышеуказанному пункту (44), где указанный пептид имеет аминокислотную последовательность, описанную как последовательность No. 1, а гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована н-октаноильной группой.
Краткое описание графического материала
На фиг. 1 представлены результаты анализа на уровни инсулина в поджелудочной железе на 21-й день после рождения. На этой фигуре А представляет собой график, иллюстрирующий экспрессию гена инсулина, на В-D представлены результаты иммуногистологического окрашивания на инсулин (В - контрольная группа; С - n0-STZ-группа; D - группа n0-STZ/грелин, соответственно с увеличением ×100), а на E представлены результаты количественной оценки площади клеток с позитивным окрашиванием на инсулин. В каждом из A и E “Cont” означает
контрольную группу, “STZ” означает n0-STZ-группу, “STZ+G” означает группу n0-STZ/грелин, а величины для каждой группы представляют собой среднюю величину для трех наблюдений ± ср. кв.от. Кроме того, * означает P<0,001, ** означает P<0,01, и *** означает P<0,005.
На фиг. 2 представлены результаты анализа на уровни pdx-1 в поджелудочной железе на 21-й день после рождения. На фигуре А показан уровень экспрессии мРНК, а на B-D представлены результаты иммуногистологического окрашивания (В - контрольная группа; С - n0-STZ-группа; D - группа n0-STZ/грелин, соответственно с увеличением ×500). На фигуре A “Cont” означает контрольную группу, “STZ” означает n0-STZ-группу, “STZ+G” означает группу n0-STZ/грелин, а величины для каждой группы представляют собой среднюю величину для трех наблюдений ± ср. кв.от. Кроме того, * означает P<0,0005, и ** означает P<0,0001.
На фиг. 3 представлены результаты анализа на уровни инсулина на 70-й день после рождения. На этой фигуре А представляет собой график, иллюстрирующий взаимосвязь между концентрациями глюкозы и инсулина в крови, В представляет собой график, иллюстрирующий уровень экспрессии гена инсулина в поджелудочной железе, на С-F представлены результаты иммуногистологического окрашивания на инсулин в поджелудочной железе (С - контрольная группа; D - n0-STZ-группа; и Е - группа n0-STZ/грелин, соответственно с увеличением ×100), а на F представлены результаты количественной оценки площади клеток с позитивным окрашиванием на инсулин. В каждом из В и F “Cont” означает контрольную группу, "STZ" означает n0-STZ-группу, "STZ+G" означает группу n0-STZ/грелин, а величины для каждой группы представляют собой среднюю величину для трех наблюдений ± ср. кв.от. Кроме того, * означает Р<0,001, ** означает Р<0,05, и *** означает Р<0,01.
На фиг.4 представлены результаты анализа на уровни pdx-1 в поджелудочной железе на 70-й день после рождения. На фигуре А показан уровень экспрессии мРНК, а на B-D представлены результаты иммуногистологического окрашивания (В - контрольная группа; С - n0-STZ-группа; D - группа n0-STZ/грелин, соответственно с увеличением ×500). На фигуре A "Cont" означает контрольную группу, "STZ" означает n0-STZ-группу, "STZ+G" означает группу n0-STZ/грелин, а значения для каждой группы представляют собой среднюю величину для трех наблюдений ± ср. кв.от. Кроме того, * означает Р<0,01, и ** означает Р<0,05.
На фиг.5 представлен результат окрашивания на фосфогистон НЗ для оценки репликации β-клеток у 21-дневных крыс. На фигуре А представлен результат иммуногистологического окрашивания на фосфогистон Н3 (зеленый) и инсулин (красный) для крыс в группе n0-STZ/грелин, а на фигуре В указан индекс мечения фосфогистоном Н3 (%) β-клеток (из 1000 клеток). "Cont" означает контрольную группу, "G" обозначает группу грелина, "STZ" означает n0-STZ-группу, "STZ+G" означает группу n0-STZ/грелин, а * означает Р<0,01.
На фиг.6 показан индекс мечения фосфогистоном Н3 (%) β-клеток для 70-дневных крыс. "Cont" означает контрольную группу, "STZ" означает n0-STZ-rpynny, a "STZ+G" означает группу n0-STZ/грелин.
На фиг. 7 указана масса тела (A) и масса поджелудочной железы (B) на 9-ю неделю после рождения. Контроль: нормальная контрольная группа, 8 крыс; STZ-носитель: группа, которой вводили STZ-обработанный носитель (5% раствор маннита), 9 крыс; STZ-человеческий грелин: группа, которой вводили STZ-обработанный человеческий грелин, 8 крыс. Каждая величина представляет собой среднюю величину ± ср. кв.от. * означает P<0,05 по сравнению с контрольной группой, а # означает P<0,05 по сравнению с группой, которой вводили STZ-носитель (критерий множественного сравнения Даннета).
На фиг. 8 приводится масса тела (A) и масса поджелудочной железы (B) на 9-ю неделю после рождения. Контроль: нормальная контрольная группа, 8 крыс; STZ-носитель: группа, которой вводили STZ-обработанный носитель (5% раствор маннита), 12 крыс; STZ-GHRP-2: группа, которой вводили STZ-обработанный GHRP-2, 12 крыс. Каждая величина представляет собой среднюю величину ± ср. кв.от. * означает P<0,05 по сравнению с контрольной группой (критерий множественного сравнения Даннета), а # означает P<0,05 по сравнению с группой, которой вводили STZ-носитель (т-критерий Стьюдента).
На фиг. 9 приводится масса тела (A) и величины уровней глюкозы в крови (B) у мышей, которым давали обычный корм или корм с высоким содержанием жирных кислот. На фиг. А приводятся массы тела, измеренные приблизительно в 9 а.m. на 42-й день после кормления пищей с высоким содержанием жирных кислот и введения тестируемого вещества, а на фиг. В указаны величины уровней глюкозы в крови, измеренные приблизительно в 9 а.m. на 43-й день после кормления пищей с высоким содержанием жирных кислот и введения тестируемого вещества. ND: группа, которой давали обычный корм; HFD-носитель: группа, которой давали корм с высоким содержанием жирных кислот - носитель (5% раствор маннита); HFD-грелин: группа, которой давали корм с высоким содержанием жирных кислот - 300 мкг/кг человеческого грелина. Тестируемое вещество подкожно вводили два раза в каждый будний день и один раз в каждый выходной день. Каждая величина представляет собой среднюю величину для 8 мышей ± стандартная ошибка. * означает P<0,05 по сравнению с ND-группой (критерий множественного сравнения Даннета).
На фиг. 10 показаны концентрации инсулина в плазме (A) и концентрации глюкозы в плазме (B) у мышей, которым давали обычный корм и корм с высоким содержанием жирных кислот и которым внутрибрюшинно вводили линолевую кислоту. Через 50 дней после кормления пищей с высоким содержанием жирных кислот и введения тестируемого вещества мышей выдерживали в течение ночи в условиях голодания, а затем внутрибрюшинно вводили 1 мл/кг линолевой кислоты. Через 1 час брали кровь для определения концентраций инсулина и глюкозы в плазме. ND: группа, которой давали обычный корм; HFD-носитель: группа, которой давали корм с высоким содержанием жирных кислот - носитель (5% раствор маннита); HFD-грелин: группа, которой давали корм с высоким содержанием жирных кислот - 300 мкг/кг человеческого грелина.
Каждая величина представляет собой среднюю величину для 8 мышей ± ср. кв.от. * означает Р<0,05 по сравнению с ND-группой (критерий множественного сравнения Даннета).
НАИЛУЧШИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Фармацевтический препарат согласно изобретению может быть использован для введения животному (индивидууму), включая человека. Веществом, которое может быть использовано в настоящем изобретении, является вещество, усиливающее секрецию гормона роста (GHS), то есть лиганд рецептора (GHS-R). Хотя в качестве GHS могут быть использованы известные пептидные соединения или низкомолекулярные соединения, однако особенно предпочтительным является пептидное соединение грелин.
Как описано выше, таким грелином может быть человеческий грелин, а также грелин, выделенный у других животных, таких как крысы, мыши, свиньи и коровы, и его производные.
Для каждого индивидуума желательно использовать грелин, полученный от этого индивидуума. Так, например, для человека желательно использовать человеческий грелин. Человеческим грелином является пептид, состоящий из 28 аминокислот, где гидроксильная группа боковой цепи серинового остатка в 3-положении от амино-конца ацилирована жирной кислотой (н-октаноильной группой) (последовательность №1). Примером производного грелина, которое может быть использовано, является пептид, имеющий аминокислотную последовательность, описанную как последовательность No.1 с заменой, инсерцией или делецией одной или нескольких аминокислотных остатков в 5-28-положениях от амино-конца, и обладающий активностью, направленной на увеличение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующим секрецию гормона роста (GHS-R). При этом, желательно, чтобы аминокислотная последовательность указанного производного была на 70%, предпочтительно на 80%, более предпочтительно на 90%, а особенно предпочтительно на 95% и наиболее предпочтительно на 97%, гомологична природной аминокислотной последовательности. Это также относится к грелину, выделенному у других животных (последовательности Nos. 2-22).
Грелин и его производное, используемые в фармацевтическом препарате согласно изобретению, могут быть получены стандартными методами. Так, например, они могут быть выделены из природного источника или получены методами рекомбинантных ДНК и/или методами химического синтеза. Если необходима дополнительная модификация (ацилирование) аминокислотного остатка, то такая реакция модификации может быть проведена известными методами. В методе продуцирования с применением техники рекомбинантных ДНК, например, может быть осуществлено культивирование клетки-хозяина, трансформированной экспрессионным вектором, содержащим ДНК, кодирующую пептид согласно изобретению, а затем нужный пептид может быть выделен из указанной культуры с получением грелина или его производного согласно изобретению. Путем выбора соответствующей клетки-хозяина можно получить клетку, содержащую соединение, имеющее нужный модифицированный (ацилированный) пептид. Если пептид не является модифицированным (ацилированным), то реакция модификации, такая как ацилирование, может быть осуществлена, если это необходимо, известными методами.
Примерами векторов для введения в них гена являются векторы Escherichia coli (pBR322, pUC18, pUC19 и т.п.), векторы Bacillus subtilis (pUB110, pTP5, pC194 и т.п.), дрожжевые векторы (типа YEp, типа YRp, типа YIp) и векторы клеток животных (ретровирусы, вирус коровьей оспы и т.п.), но могут быть также использованы и любые другие векторы, при условии, что такие векторы могут стабильно сохранять нужный ген в клетке-хозяине. Указанный вектор вводят в соответствующую клетку-хозяина.
Методами введения нужного гена в плазмиду или в клетку-хозяина могут быть, например, методы, описанные в руководстве Molecular Cloninng (Sambrook et al., 1989).
Для экспрессии нужного гена пептида в описанной выше плазмиде к этому гену, для его функционирования, может быть присоединен промотор в сайте, локализованном выше этого гена. Для этих целей может быть использован любой промотор, при условии, что такой промотор является подходящим для экспрессии нужного гена в клетке-хозяине. Так, например, в случае, если трансформированной клеткой-хозяином является клетка рода Esсherichia, то могут быть использованы, например, промотор lac, промотор trp, промотор lpp, промотор λPL, промотор recA или т.п.; в случае, если такой клеткой является клетка рода Bacillus, то могут быть использованы промотор SPO1, промотор SPO2 или т.п.; в случае, если такой клеткой является дрожжевая клетка, то могут быть использованы промотор GAP, промотор PHO5, промотор ADH или т.п.; а в случае, если такой клеткой является клетка животного, то могут быть использованы промотор SV40, ретровирусный промотор или т.п.
Клетка-хозяин может быть трансформирована с использованием вектора, содержащего нужный ген, полученный, как описано выше. В качестве клетки-хозяина могут быть использованы клетки бактерий (например, бактерии рода Escherichia или Bacillus), дрожжевые клетки (рода Saccharomyces, Pichia, Candida или т.п.), клетки животных (клетки CHO, COS или т.п.) или т.п. Жидкая среда является подходящей в качестве культуральной среды, а особенно предпочтительно, чтобы такая среда включала источник углерода, источник азота и т.п., необходимые для роста культивируемой трансформированной клетки. При необходимости, могут быть добавлены витамины, фактор, стимулирующий рост клеток, сыворотка и т.п.
Для прямого продуцирования пептида, модифицированного жирной кислотой (ацилированного), предпочтительные клетки должны иметь протеазу, обладающую процессирующей активностью и способную разрезать полипептид-предшественник данного пептида в соответствующем положении, а также они должны обладать активностью, направленной на ацилирование серинового остатка в данном пептиде. Клетки-хозяева, обладающие процессирующей протеазной активностью и серин-ацилирующей активностью, могут быть отобраны после трансформации клеток-хозяев экспрессионным вектором, включающим кДНК, кодирующую полипептид-предшественник, и после подтверждения того, что эти трансформированные клетки продуцируют пептид, модифицированный жирной кислотой и обладающий активностью, направленной на увеличение уровня кальция или высвобождения гормона роста.
После культивирования грелин может быть выделен и очищен из культуры стандартным методом. Так, например, для экстракции нужного вещества из культивированных клеточных телец или клеток такие клеточные тельца или клетки могут быть собраны после культивирования и суспендированы в буферном растворе, включающем белок-денатурирующий агент (такой как гидрохлорид гуанидина), а затем эти клеточные тельца или клетки могут быть гомогенизированы путем обработки ультразвуком или т.п. и подвергнуты центрифугированию. Для очистки нужного вещества от супернатанта могут быть применены методы выделения и очистки, такие как гель-фильтрация, ультрафильтрация, диализ, электрофорез в ДСН-ПААГ и хроматография различных типов, которые могут быть соответствующим образом объединены в зависимости от молекулярной массы, растворимости, заряда (изоэлектрической точки), аффинности и т.п. нужного вещества.
Грелин и его производное могут быть химически синтезированы стандартным методом. Так, например, грелин и его производное могут быть получены посредством реакции конденсации аминокислот, имеющих защитные группы, жидкофазным методом и/или твердофазным методом для удлинения пептидной цепи, удаления всех защитных групп с помощью кислоты и очистки полученного неочищенного продукта методом очистки, описанным выше. Боковая цепь аминокислоты в нужном положении может быть селективно ацилирована ацилирующим ферментом или ацилтрансферазой.
Существуют различные методы получения пептидов, хорошо известные специалистам, и грелин может быть также легко получен известным методом. Так, например, грелин может быть легко получен классическим методом пептидного синтеза или твердофазным методом.
Кроме того, такое продуцирование может быть также осуществлено с применением комбинации техники рекомбинантных ДНК и химического синтеза. Грелин может быть получен методом, в котором один фрагмент, включающий модифицированный аминокислотный остаток, продуцируют путем химического синтеза, а другой фрагмент, не включающий модифицированного аминокислотного остатка, продуцируют с помощью техники рекомбинантных ДНК, после чего полученные фрагменты присоединяют друг к другу (см. публикацию Международной заявки WO01/07475).
Солью грелина и его производного, которая может быть использована в настоящем изобретении, является предпочтительно фармацевтически приемлемая соль, например соль неорганического основания, соль органического основания, соль неорганической кислоты, соль органической кислоты или соль основной или кислотной аминокислоты.
Подходящими примерами солей неорганического основания являются соль щелочного металла, такая как соль натрия и соль калия; соль щелочноземельного металла, такая как соль кальция и соль магния; а также соль алюминия и соль аммония.
Подходящими примерами солей органического основания являются соли триметиламина, триэтиламина, пиридина, пиколина, этаноламина, диэтаноламина, триэтаноламина, дициклогексиламина, N,N'-дибензилэтилендиамина и т.п.
Подходящими примерами солей неорганических кислот являются соли хлористоводородной кислоты, бромистоводородной кислоты, азотной кислоты, серной кислоты, фосфорной кислоты и т.п.
Подходящими примерами солей органических кислот являются соли муравьиной кислоты, уксусной кислоты, трифторуксусной кислоты, фумаровой кислоты, щавелевой кислоты, винной кислоты, малеиновой кислоты, лимонной кислоты, янтарной кислоты, яблочной кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты и т.п.
Подходящими примерами солей основных аминокислот являются соли аргинина, лизина, орнитина и т.п., а подходящими примерами солей кислотных аминокислот являются соли аспарагиновой кислоты, глутаминовой кислоты и т.п.
Из описанных выше солей наиболее предпочтительными являются соль натрия и соль калия.
Принимая во внимание биологическое или физиологическое действие грелина, описанное в вышеупомянутой публикации, его производное может быть выбрано с использованием в качестве индикатора его активности связывания с рецептором GHS-R 1A. Для измерения концентрации ионов внутриклеточного кальция может быть применен известный метод; так, например, может быть применен метод измерения на FLIPR (флуорометрическом визуализирующем планшет-ридере, Molecular Devices), основанный на изменении интенсивности флуоресценции Fluo-4 AM (Molecular Probe), обусловленной изменением концентрации ионов кальция. Кроме того, для того чтобы определить, способен ли данный пептид, обладающий активностью, направленной на увеличение уровня кальция, высвобождать гормон роста in vitro и in vivo, может быть применен известный метод. Так, например, в случае in vitro указанный пептид может быть введен в клетки гипофиза, которые секретируют гормон роста и, как было показано, экспрессируют GHS-R, и уровень гормона роста, секретированного в клеточную культуральную среду, может быть измерен с помощью радиоиммуноанализа с использованием антитела против гормона роста. Для оценки активности высвобождения гормона роста in vivo указанный пептид, обладающий способностью повышать уровень кальция, может быть инъецирован в периферическую вену животного для измерения концентрации гормона роста в сыворотке. Производное грелина и способ его получения также описаны, например, в публикации J. Med. Chem., 43, pp.4370-4376, 2000.
Как конкретно показано в примерах, представленных в настоящем описанни, грелин и его производное, при их введении индивидууму, стимулируют неогенез или регенерацию панкреатических β-клеток и могут значительно увеличивать число инсулин-позитивных клеток в панкреатических β-клетках. Грелин и его производное также обладают способностью стимулировать продуцирование инсулина в панкреатических β-клетках и аккумуляцию инсулина в панкреатических β-клетках.
Хотя сообщалось, что грелин способствует снижению секреции инсулина из панкреатических β-клеток, однако механизм продуцирования и аккумуляции инсулина может отличаться от механизма секреции инсулина, и действие фармацевтического препарата согласно изобретению может быть основано на стимуляции неогенеза или регенерации панкреатических β-клеток и на стимуляции продуцирования инсулина в панкреатических β-клетках, которое приводит к увеличению количества запасного инсулина и тем самым может способствовать усилению секреции инсулина.
Поэтому при введении индивидууму фармацевтического препарата согласно изобретению число β-клеток, способных секретировать инсулин в поджелудочной железе, может увеличиваться и тем самым может осуществляться неогенез или регенерация панкреатических β-клеток, обладающих инсулин-секретирующей функцией.
В соответствии с этим фармацевтический препарат согласно изобретению, способный стимулировать неогенез или регенерацию панкреатических β-клеток, может быть использован для предотвращения разрушения, гибели или истощения панкреатических β-клеток у индивидуума и для сохранения панкреатических β-клеток. Кроме того, прогресирование диабета может быть предотвращено путем введения фармацевтического препарата согласно изобретению индивидууму, у которого наблюдается гипергликемическое состояние, но у которого пока еще отсутствует диабет. Кроме того, если диабет не имеет осложнений, то прогрессирование диабета может быть предотвращено путем введения этому индивидууму фармацевтического препарата согласно изобретению. В случае тяжелого диабета (если величина ΔIRI/ΔBG не превышает 0,4), лечение диабета посредством стимуляции неогенеза или регенерации панкреатических β-клеток может быть осуществлено путем введения индивидууму фармацевтического препарата согласно изобретению. Осуществление неогенеза или регенерации панкреатических β-клеток может быть продемонстрировано, например, путем подтверждения экспрессии pdx-1, одного из основных транскрипционных факторов дифференцировки клеток в поджелудочной железе.
Кроме того, терапия, проводимая на основе регенерации панкреатических β-клеток, может быть осуществлена путем обработки панкреатических β-клеток, выделенных у индивидуума и помещенных в тест-пробирку, фармацевтическим препаратом согласно изобретению для стимуляции регенерации панкреатических β-клеток, и пролиферации этих клеток, и последующей трансплантации этих клеток в тот участок организма индивидуума, в котором наблюдается нарушение функции или гибель панкреатических β-клеток, либо в тот участок организма индивидуума, в котором предположительно имеет место нарушение функции или гибель панкреатических β-клеток. В настоящее время многими группами ученых во всем мире проводятся интенсивные исследования по разработке методов идентификации и выделения клеток-предшественников панкреатических β-клеток, и в результате этих исследований был разработан ряд методов (см., например, Lancet, 364, pp.203-205, 2004). Неогенез или регенерация панкреатических β-клеток могут быть осуществлены путем воздействия грелина или его производного на выделенные клетки-предшественники панкреатических β-клеток, и полученная группа клеток может быть трансплантирована в живой организм индивидуума в целях проведения терапии, способствующей регенерации панкреатических β-клеток.
Фармацевтический препарат согласно изобретению, включающий грелин, его производное или фармацевтически приемлемую соль в качестве эффективного компонента, может быть смешан с фармацевтически приемлемым носителем, наполнителем, разбавителем или т.п. и введен индивидууму (например, человеку, мыши, крысе, кролику, собаке, кошке, корове, лошади, свинье, обезьяне и т.п.). Доза не имеет конкретных ограничений и может быть выбрана, например, в зависимости от цели применения фармацевтического препарата согласно изобретению или от возраста, массы тела или вида индивидуума. Так, например, для взрослого человека доза грелина или его производного, составляющего 50-200 мкг/массу тела, может быть введена примерно один раз или два раза в день, либо такая доза может быть введена непрерывно в течение примерно нескольких дней или нескольких недель.
Грелин, его производное или фармацевтически приемлемая соль могут быть смешаны с фармацевтически приемлемым носителем и введены перорально или парентерально в виде твердого препарата, такого как таблетка, капсула, гранула или порошок либо в виде жидкого препарата, такого как сироп или раствор для инъекций.
Различные органические или неорганические вещества-носители, обычно применяемые в качестве технологической добавки, используются как фармацевтически приемлемый носитель, который смешивают, например, с наполнителем, замасливателем, связывающим агентом или с дезинтегратором в твердом препарате, или с растворителем, адъювантом растворения, суспендирующим агентом, средством, придающим изотоничность, буфером или мягчителем в жидком препарате.
Кроме того, при необходимости, может быть также использована технологическая добавка, такая как консервант, антиоксидант, краситель или подсластитель.
Подходящими примерами наполнителей являются лактоза, сахароза, D-маннит, крахмал, кристаллическая целлюлоза, ангидрид легкой кремниевой кислоты и т.п. Подходящими примерами замасливателей являются стеарат магния, стеарат кальция, тальк, коллоидная двуокись кремния и т.п.
Подходящими примерами связующих агентов являются кристаллическая целлюлоза, сахароза, D-маннит, декстрин, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, поливинилпирролидон и т.п.
Подходящими примерами дезинтегрирующих средств являются крахмал, карбоксиметилцеллюлоза, кальций-содержащая карбоксиметилцеллюлоза, натрий-содержащая кроскармеллоза, натрий-содержащий карбоксиметилированный крахмал и т.п.
Подходящими примерами растворителей являются вода для инъекций, спирт, пропиленгликоль, макрогол, кунжутное масло, кукурузное масло и т.п.
Подходящими примерами адъювантов растворения являются полиэтиленгликоль, пропиленгликоль, D-маннит, бензилбензоат, этанол, трисаминометан, холестерин, триэтаноламин, карбонат натрия, цитрат натрия и т.п.
Подходящими примерами суспендирующих агентов являются поверхностно-активные вещества, такие как стеарилтриэтаноламин, лаурилсульфат натрия, лауриламинопропионат, лецитин, хлорид бензалкония, хлорид бензэтония и моностерат глицерина; и гидрофильные полимеры, такие как поливиниловый спирт, поливинилпирролидон, натрий-содержащая карбоксиметилцеллюлоза, метилцеллюлоза, гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза и гидроксипропилцеллюлоза.
Подходящими примерами средств, придающих изотоничность, являются хлорид натрия, глицерин, D-маннит и т.п.
Подходящими примерами буферов являются буферные растворы фосфата, ацетата, карбоната, цитрата и т.п.
Подходящим примером мягчителя является бензиловый спирт.
Подходящими примерами консервантов являются параоксибензоаты, хлорбутанол, бензиловый спирт, фенетиловый спирт, дегидроуксусная кислота, сорбиновая кислота и т.п.
Подходящими примерами антиоксидантов являются сульфит, аскорбиновая кислота и т.п.
Примерами готовых лекарственных форм, подходящих для парентерального введения, являются инъекции для внутривенного введения, внутрикожного введения, подкожного введения, внутримышечного введения и т.п., капли, суппозитории, средство для чрескожной абсорбции, средство для абсорбции через слизистую и средство для введения путем ингаляции, а примерами готовых лекарственных форм, подходящих для перорального введения, являются капсулы, таблетки, сиропы и т.п. Однако предпочтительными готовыми фармацевтическими препаратами согласно изобретению являются препараты, подходящие для парентерального введения, такие как инъекции, капли или аэрозоли. Различные готовые лекарственные формы известны специалистам, и специалист в данной области может самостоятельно выбрать лекарственную форму, подходящую для соответствующего способа введения, в целях приготовления препарата в форме фармацевтической композиции с использованием, если это необходимо, одной или нескольких технологических добавок, доступных специалисту.
Так, например, фармацевтический препарат в форме инъекции или капель может быть получен путем растворения грелина или его производного, используемого в качестве эффективного компонента, вместе с одной или несколькими технологическими добавками, такими как средство, придающее изотоничность, рН-корректирующее средство, мягчитель или консервант, в дистиллированной воде для инъекций, с последующей стерилизацией этого препарата. Кроме того, фармацевтический препарат в форме инъекции или капель может быть также получен в лиофилизованной форме. Такой фармацевтический препарат может быть растворен непосредственно перед его применением путем добавления дистиллированной воды для инъекций, физиологического раствора или т.п., а затем он может быть использован в качестве прапарата для инъекций или капель. Кроме того, для введения через слизистую, например, может быть также использовано средство для интраназального введения, такое как раствор для орошения полости носа или носовой спрей, либо средство для введения в полость рта, такое как подъязычное средство.
Примеры
Для более подробного описания настоящего изобретения приводятся нижеследующие примеры, однако эти примеры не должны рассматриваться как ограничение объема изобретения.
Пример 1
1. Материалы и методы
Самок или самцов крыс Sprague Dawley, закупленных у фирмы Charles River, содержали в условиях свободного доступа к водопроводной воде и к стандартному гранулированному крысиному корму (352 ккал/100 г, CE-2, CLEA). Самок помещали вместе с самцами в клетку на одну ночь и через 14 дней определяли их беременность путем пальпации брюшной полости. В природе роды у крыс происходят через 22 дня после спаривания. Авторами настоящего изобретения были исследованы следующие три экспериментальные группы: контрольная группа (крысы Sprague Dawley), в которой новорожденным крысам вводили одну внутрибрюшинную инъекцию цитратного буфера; n0-STZ-группа, в которой крысам вводили одну внутрибрюшинную инъекцию стрептозотоцина (STZ); и группа n0-STZ/грелин, в которой крысам вводили одну внутрибрюшинную инъекцию стрептозотоцина, а затем вводили грелин, выделенный у крыс (далее называемый крысиным грелином, последовательность No. 3, 100 мг/кг массы тела), путем подкожной инъекции два раза в день на 2-8 дни после рождения в течение 7 дней.
Стрептозотоцин (Sigma, 100 мг/кг массы тела) растворяли в цитратном буфере (0,05 ммоль/л, pH 4,5) и за один раз внутрибрюшинно инъецировали крысам сразу после их рождения. Крысят оставляли с их матерями. На 2-й день каждую новорожденную крысу анализировали на содержание сахара в моче с помощью устройства Multistix SG (Bayer Medical). В группу n0-STZ-модели были включены только те крысы, у которых через 2 дня после их рождения наблюдалась гликозурия (значение 3+ в тесте Multistix SG). Животных умерщвляли на 21-й или 70-й дни путем кровопускания под анестезией посредством внутрибрюшинной инъекции пентобарбитал-натрия (50 мг/кг). Из нижней полой вены брали пробы крови, которые затем сразу центрифугировали при 4oC и помещали на хранение при -80oC вплоть до проведения анализа.
После вскрытия извлекали поджелудочную железу и взвешивали. Для измерения уровня инсулина поджелудочные железы (35-50 мг) гомогенизировали и центрифугировали в 5 мл кислоты-этанола (75% (об./об.) этанолового раствора 0,15M HCl), и супернатанты хранили при -80°C. Для проведения иммуногистохимического анализа дополнительные поджелудочные железы фиксировали в 4% фиксирующем параформальдегиде в течение 24 часов и заливали в парафин.
Затем на тканевых срезах толщиной 3 мкм проводили иммуногистохимический анализ для детекции инсулина и pdx-1 с применением непрямого метода мечения пероксидазой. Каждый срез инкубировали с “первым” антителом (антитело морских свинок против свиного инсулина, DACO, или кроличьим антителом против мышиного/крысиного IDX-1; CHEMICON) в течение 1 часа. Окрашивание осуществляли путем инкубирования с использованием набора, содержащего тетрагидрохлорид 3,3'-диаминобензидина (DAB) (DakoCytomation). Количественную оценку общей площади β-клеток осуществляли в соответствии с аналитической процедурой компьютерной визуализации с использованием микроскопа Olympus BX 51, к которому была подсоединена цифровая камера DP 12, и с использованием компьютерной программы Mac SCOPE Ver2.6 (Mitani, Fukui, Japan). Площадь β-клеток и общую площадь срезов поджелудочной железы оценивали для каждого окрашенного среза. Относительный объем β-клеток определяли стерологическим морфологическим методом, в котором вычисляли отношение между площадью, занимаемой иммунореактивными клетками, и площадью, занимаемой всеми панкреатическими клетками.
Полноразмерную РНК экстрагировали из поджелудочной железы крыс, как описано в литературе (Biochem. Biophys. Res. Commun., 214, pp.239-246, 1995). Для синтеза кДНК первой цепи экстрагированные продукты использовали в качестве матриц в реакционных смесях, содержащих обратную транскриптазу (ОТ) (Invitrogen) и нужный 3'-праймер. ОТ-ПЦР-анализ проводили методом, описанным ранее (Biochem. Biophys. Res. Commun., 214, pp.239-246, 1995). В последующих ПЦР-анализах использовали кДНК первой цепи. В ПЦР-анализах для каждой целевой кДНК использовали нижеследующие олигонуклеотидные праймеры. Идентичность ПЦР-продукта подтверждали с помощью электрофореза в агарозном геле.
Инсулин-1:
5'-tagaccatcagcaagcaggtc (последовательность No. 22)
3'-cacaccaggtacagagcct (последовательность No. 23)
Инсулин-2:
5'-cacttggtggaagctctctacc (последовательность No. 24)
3'-gacagggtagtggtgggcctagt (последовательность No. 25)
Rdx-1:
5'-aggaggtgcatacgcagcag (последовательность No. 26)
3'-gaggccgggagatgtatttgtt (последовательность No. 27)
ПЦР в реальном времени осуществляли следующим образом. кДНК (1 мкл) смешивали с реагентом 2×PCR Master Mix (Applied Biosystems) (25 мкл), со стерилизованной дистиллированной водой (23 мкл) и со смысловыми и антисмысловыми праймерами (10 пмоль/мкл, 0,5 мкл) для инсулина и для Pdx-1. Сорок циклов ПЦР-амплификации осуществляли с использованием системы термоячеек (ABI PRISM 7700, Applied Biosystems, Japan) в течение 15 секунд при 95°C, а затем в течение 60 секунд при 60°C. Концентрацию каждого мРНК-продукта количественно оценивали с использованием калибровочных кривых зависимости уровней интенсивности флуоресценции от количества стандартизированного ПЦР-продукта.
Все данные, полученные из кривой, были нормализованы на количество РНК рибосомы 18S в образце, взятом от одного и того же индивидуума.
Уровни глюкозы в плазме и крови измеряли с помощью анализатора глюкозы (Antsense 2, Sankyo). Инсулин экстрагировали из поджелудочной железы, как описано в литературе (Endocrinology, 140, pp.4861-4873, 1999). Концентрации инсулина измеряли с использованием набора для ELISA-анализа инсулина Lebis ELISA (Shibayagi).
Измеренные величины выражали как средние величины ± ср. кв.от. Разницу между полученными величинами и величинами, полученными для крыс контрольной группы, которым вводили STZ, оценивали с помощью дисперсионного анализа ANOVA.
2. Результаты
Данные, полученные для 21-дневных крыс, систематизированы в таблице 1. У контрольной группы и n0-STZ-группы не наблюдалось заметного отличия в массах тел, уровнях глюкозы в крови натощак (FBG) и в концентрациях инсулина. У n0-STZ-группы и у группы n0-STZ/грелин также не отмечалось значимого отличия для каждого из других рассматриваемых параметров. Однако концентрации FBG у группы «n0-STZ/грелин» были значительно ниже, чем у контрольной группы (P<0,01).
*1: P<0,01 (по сравнению с контролем).
У n0-STZ-группы уровни экспрессии мРНК инсулина в поджелудочной железе были значительно ниже, чем у контрольной группы. Однако после введения крысиного грелина эти уровни возвращались до уровней, аналогичных уровням контрольной группы (группа «n0-STZ/грелин») (фиг. 1A). Уровень экспрессии мРНК инсулина в поджелудочной железе у n0-STZ-группы составлял примерно 1/3 от уровня группы n0-STZ/грелин, но у n0-STZ-группы наблюдались уровни инсулина в плазме, сравнимые с уровнями инсулина у контрольной группы и у группы «n0-STZ/грелин». Результаты иммунологического окрашивания инсулина поджелудочной железы соответствовали полученным уровням экспрессии гена (фиг. 1A-E). У n0-STZ-группы островки Лангерганса были меньше, чем у контрольной группы (фиг. 1B, C, E). У группы n0-STZ/грелин островки Лангерганса были больше, чем у n0-STZ-группы, но меньше, чем у контрольной группы (фиг. 1B-E).
Для оценки механизма регуляции изменения экспрессии инсулина в поджелудочной железе авторами настоящего изобретения была оценена экспрессия pdx-1, то есть одного из главных транскрипционных факторов дифференцировки клеток поджелудочной железы. Изменения уровней мРНК и белка Pdx-1 были аналогичны изменениям уровней инсулина (фиг. 2A-D). Хотя уровни экспрессии генов pdx-1 у n0-STZ-группы составляли менее 1/10 от уровней, наблюдаемых у контрольной группы, однако эти уровни у животных группы n0-STZ/грелин после введения крысиного грелина восстанавливались до уровней, аналогичных уровням контрольной группы (фиг. 2A). Результаты иммунолофлуоресцентного окрашивания на pdx-1 в поджелудочной железе соответствовали результатам окрашивания на инсулин (фиг. 2B-D).
Таким образом, у этой n0-STZ-модели наблюдалось снижение продуцирования инсулина на 21-й день, а уровни глюкозы в крови не изменялись. Предотвращение снижения продуцирования инсулина у животных этой модели после введения им крысиного грелина было подтверждено на уровне мРНК и белка.
Поскольку известно, что у крыс с n0-STZ-моделью после достижения ими 8-10-недельного возраста постепенно развивалась гипергликемия, то была проведена оценка длительности эффекта раннего введения грелина крысам этой модели. Данные, полученные для 10-недельных животных контрольной группы, n0-STZ-группы и группы n0-STZ/грелин представлены в таблице 2.
*1: P<0,05, *2: P<0,01, *3: P<0,0001; по сравнению с контролем,
#1: P<0,0001, #2: P<0,01; по сравнению с n0-STZ-группой.
У n0-STZ-группы наблюдалось снижение массы тела и гипергликемии по сравнению с контрольной группой. Хотя концентрация инсулина в плазме у этой группы не снижалась, однако концентрация инсулина у каждого животного была относительно низкой для такой повышенной концентрации глюкозы (таблица 2, фиг. 3A). Действительно, уровни инсулина в поджелудочной железе были меньше, чем у контрольной группы (таблица 2).
С другой стороны, уровни FBG у животных группы n0-STZ/грелин были значительно ниже, чем у животных n0-STZ-группы, однако они не были значительно выше, чем у контрольной группы. Кроме того, содержание инсулина в поджелудочной железе сохранялось почти на таком же уровне, как и в контрольной группе. Масса тела у животных группы n0-STZ/грелин была значительно ниже, чем масса тела животных контрольной группы, но она не отличалась от массы тела животных n0-STZ-группы.
Экспрессия мРНК инсулина у взрослых животных n0-STZ-группы все еще оставалась на низком уровне, хотя и наблюдалось некоторое ее увеличение.
С другой стороны, у животных группы “n0-STZ/грелин” уровень инсулина был аналогичен уровню, наблюдаемому у контрольной группы, на 21-й день после их рождения (фиг. 3B). Кроме того, при иммуногистохимическом окрашивании на инсулин островки Лангерганса у животных группы n0-STZ/грелин были больше, чем у n0-STZ-группы, но меньше, чем у контрольной группы (фиг. 3C-F).
Профили уровней экспрессии мРНК и белка pdx-1 у взрослых крыс трех групп были аналогичны профилям этих уровней, наблюдаемых в животных на 21-й день после их рождения (фиг. 4). Экспрессиия гена Pdx-1 у n0-STZ-группы снижалась приблизительно на 1/3 по сравнению с контрольной группой, а уровень у группы n0-STZ/грелин восстанавливался до уровней, близких к уровням контрольной группы (фиг. 4A). При иммунофлуоресцентном окрашивании на pdx-1 в поджелудочной железе наблюдаемые профили были аналогичны профилям, полученным для инсулина (фиг. 4B-D).
Как описано выше, у животных n0-STZ-модели через 10 недель после их рождения наблюдались низкие уровни продуцирования инсулина в поджелудочной железе и развивалась гипергликемия. Введение крысиного грелина должно ингибировать такое прогрессирование гипергликемии путем поддержания или стимуляции продуцирования инсулина. Увеличение уровня экспрессии pdx-1 может также частично способствовать такому поддержанию уровней продуцирования инсулина. Поскольку у группы “n0-STZ/грелин” наблюдалось увеличение уровней экспрессии pdx-1, то есть транскрипционного фактора, который играет важную роль в развитии и дифференцировки клеток поджелудочной железы, то было высказано предположение, что панкреатические β-клетки, разрушенные при введении STZ сразу после рождения животных, могут быть регенерированы путем введения грелина, а регенерация панкреатических β-клеток может способствовать поддержанию уровней продуцирования инсулина.
Пример 2
1. Материалы и методы
Срезы поджелудочной железы, которые не были использованы для морфологических исследований, использовали для оценки репликации β-клеток. Эти срезы подвергали двойному окрашиванию на фосфогистон Н3 (Ser10) и инсулин. Эти срезы инкубировали в течение ночи с 50-кратным разведением антитела против фосфогистона H3 (Ser10) (Cell Signaling Technology) при 4oC. Затем срезы инкубировали с антителом морских свинок против инсулина при комнатной температуре в течение 1 часа. После 6-кратной промывки PBS эти срезы инкубировали при комнатной температуре в течение 30 минут в блокирующем растворе со “вторым” антителом, конъюгированным с флуоресцетной меткой (Alexa Fluor 488 and 546, Molecular Probe). После промывки PBS срезы заливали заливочной средой, содержащей DAPI (Vector Laboratories), и оценивали с помощью конфокального лазерного сканирующего микроскопа (Leica Microsystems). Для каждого среза насчитывали, по меньшей мере, 1000 β-клеток.
2. Результаты
Для того чтобы определить, оказывает ли индуцированная грелином пролиферация β-клеток какое-либо воздействие на продуцирование инсулина и на число β-клеток у STZ-обработанных крыс, авторами настоящего изобретения был проведен иммуногистохимический анализ на фосфогистон H3. Фосфогистон H3 представляет собой маркер митоза в процессе пролиферации клеток (J. Clin. Invest., 113, pp.1364-1374, 2004; Br. J. Cancer, 88, pp.257-262, 2003). Результат этого анализа представлен на фиг. 5A. У 21-дневных крыс после обработки крысиным грелином число клеток, позитивных как на фосфогистон Н3, так и на инсулин, увеличивалось примерно в 1,7 раз, а у крыс в группе, обработанной грелином, и у крыс в группе, обработанной n0-STZ/грелином, это число увеличивалось в 15 раз по сравнению с крысами контрольной группы и n0-STZ-группы соответственно (фиг. 5B). У 10-недельных крыс, хотя и не наблюдалось значимого различия между всеми четырьмя группами, однако у животных STZ-модели, обработанных крысиным грелином, наблюдалась тенденция к увеличению числа дважды позитивных клеток, то есть клеток, позитивных на фосфогистон Н3 и инсулин, тогда как у животных контрольной группы наблюдалась тенденция к снижению числа дважды позитивных клеток (фиг. 6). Поскольку уровень экспрессии pdx-1, инсулина и фосфогистона H3 у крыс группы “n0-STZ/грелин” значительно повышался по сравнению с уровнями, наблюдаемыми у 21-дневных животных контрольной n0-STZ-группы, было высказано предположение, что грелин стимулирует регенерацию и репликацию β-клеток у STZ-обработанных новорожденных крыс.
Пример 3
Так как действие крысиного грелина было подтверждено в примере 1 и в примере 2, то затем было оценено действие грелина, выделенного у человека (далее называемого человеческим грелином, последовательность No. 1) у новорожденных крыс STZ-модели, как описано в примере 1. Человеческий грелин отличается от крысиного грелина двумя аминокислотами.
1. Материалы и методы
Беременных самок крыс Sprague Dawley female, закупленных у фирмы Charles River, содержали в условиях свободного доступа к водопроводной воде и к стандартному гранулированному крысиному корму (CRF-1, Oriental Yeast Co., Ltd.) и обеспечивали роды в естественных условиях. Животные были распределены на три следующие экспериментальные группы: контрольная группа, которой вводили одну внутрибрюшинную инъекцию цитратного буфера сразу после рождения; группа “STZ-носитель”, которой вводили одну внутрибрюшинную инъекцию STZ, а затем подкожно вводили носитель (5% раствор маннита) два раза в день, начиная со 2-го дня после рождения в течение 7 дней; и группа “STZ/человеческий грелин”, которой вводили одну внутрибрюшинную инъекцию STZ, а затем подкожно вводили человеческий грелин (последовательность No 1, 100 мг/кг массы тела) два раза в день, начиная со 2-го дня после рождения в течение 7 дней.
STZ приготавливали и вводили, как описано в примере 1. Каждого самца новорожденных крыс на 2-й день после его рождения анализировали на уровень сахара в моче в предварительном тесте Pretest 3aII (Wako Pure Chemical Industries, Ltd.). В описанные ниже исследования были включены только те крысы, у которых на 2-й день после рождения наблюдалась гликозурия (величина 3+ в предварительном тесте 3aII). Отъем крыс от матери осуществляли вечером на 20-й день после рождения. Пробы крови брали из хвостовой вены неанестезированных крыс на 8-ю неделю (57-й день) после рождения для измерения концентраций глюкозы и инсулина в плазме. Кроме того, после измерения массы тела на 9-ю неделю (62-й или 63-й дни) после рождения из брюшной аорты брали пробы крови под анестезией, проводимой путем внутрибрюшинной инъекции пентобарбитал-натрия (50 мг/кг). Все поджелудочные железы извлекали и взвешивали. Затем поджелудочные железы разделяли на две части и сохраняли для определени содержания инсулина. Пробы крови сразу центрифугировали при 4°С для получения проб плазмы и хранили при -80oC вплоть до их использования для определения концентраций глюкозы и инсулина. Концентрацию глюкозы измеряли с помощью теста на глюкозу CII-test Wako (Wako Pure Chemical Industries, Ltd.), а концентрацию инсулина измеряли с помощью набора для высокочувствительного теста на инсулин (Morinaga Institute of Biological Science, Inc.).
2. Результаты
Была проведена оценка влияния человеческого грелина, который вводили сразу после введения STZ в течение 7 дней, на концентрации глюкозы и инсулина в плазме на 8-ю неделю (после 4-часового голодания). Результаты приводятся в таблице 3. Концентрации глюкозы в плазме у группы, которой вводили носитель, были значительно выше, чем у контрольной группы, а концентрации глюкозы у группы “STZ-человеческий грелин” были несколько выше, но значительно не отличались от концентраций глюкозы у контрольной группы. С другой стороны, у этих групп концентрации инсулина в плазме не имели значимого различия.
*1: P<0,05; по сравнению с контрольной группой (критерий множественного сравнения Даннета).
Затем определяли массу тела, массу поджелудочной железы и содержание инсулина в поджелудочной железе на 9-ю неделю. Результаты определения массы тела и массы поджелудочной железы приводятся на фиг. 7. Масса тела животных группы STZ-носитель была значительно ниже, чем у животных контрольной группы, а у животных группы “STZ-человеческий грелин” снижение массы тела прекращалось и масса тела этих животных была сравнима с массой тела животных контрольной группы. У животных группы “STZ-носитель” наблюдалось небольшое снижение массы поджелудочной железы по сравнению с животными контрольной группы. С другой стороны, у животных группы “STZ-человеческий грелин” масса поджелудочной железы была значительно выше, чем у животных группы STZ-носитель.
Поскольку у животных группы “STZ-человеческий грелин” наблюдалось увеличение массы поджелудочной железы, то было проведено сравнение содержания инсулина в их поджелудочных железах. Поджелудочные железы разделяли для получения двух образцов: образца ткани со стороны селезенки и образца ткани со стороны кишечника, после чего содержание инсулина в поджелудочной железе вычисляли исходя из содержания инсулина в каждом образце, а затем анализировали. Результаты приводятся в таблице 4. У животных группы STZ-носитель содержание инсулина в поджелудочной железе, вычисленное для двух образцов, было значительно ниже, чем у контрольной группы. Хотя содержание инсулина у животных группы “STZ-человеческий грелин” было также значительно ниже, чем у контрольной группы, однако содержание инсулина у животных этой группы было примерно в два раза выше, чем у группы STZ-носитель.
*1: P<0,05; по сравнению с контрольной группой (критерий множественного сравнения Даннета).
Исходя из вышеуказанных результатов было установлено, что обработка новорожденных крыс STZ-модели человеческим грелином, проводимая сразу после введения им STZ, приводила к снижению гипергликемии и к уменьшению массы тела у взрослых животных. Поскольку было также обнаружено увеличение массы поджелудочной железы и наблюдалась тенденция к замедлению снижения содержания инсулина в поджелудочной железе, то было высказано предположение, что, как было показано в примере 1 для крысиного грелина, панкреатические β-клетки, разрушенные в результате введения животным STZ сразу после их рождения, могут регенерироваться путем введения человеческого грелина, при этом уровень продуцирования инсулина будет частично сохраняться, что может играть определенную роль в снижении гипергликемии.
Пример 4
Поскольку считается, что физиологические функции грелина опосредуются GHS-R, то можно предположить, что соединения-агонисты GHS-R, не являющиеся грелином (соединения, усиливающие секрецию гормона роста, далее называемые GHS-соединениями), могут так же, как и грелин, стимулировать регенерацию β-клеток и подавление развития гипергликемии или диабета. Поэтому впоследствии была исследована функция GHS-соединения у новороженных животных STZ-модели. Хотя существуют различные пептидные и не-пептидные соединения, известные как GHS-соединения, однако в этом примере для исследований было выбрано пептидное GHS-соединение GHRP-2 (Ala-D-Trp-Ala-Trp-D-Phe-Lys-NH2, Drugs of the Future 30, pp124-127, 2005, CAS No, 158861-67-7).
1. Материалы и методы
Были использованы экспериментальные материалы, экспериментальные методы и методы оценки, аналогичные материалам и методам, описанным в примере 2. 100 мг/кг тестируемого вещества GHRP-2 подкожно вводили два раза в день, начиная со 2-го дня после рождения, в течение 7 дней (STZ-GHRP-2-группа).
2. Результаты
Была проведена оценка влияния раннего введения GHRP-2 после рождения на концентрации глюкозы и инсулина в плазме на 8-ю неделю (после 4-часового голодания). Результаты приводятся в таблице 6. Концентрации глюкозы в плазме у группы “STZ-носитель” были значительно выше, чем у контрольной группы, а у STZ-GHRP-2-группы такое увеличение было незначительным, и эти концентрации были значительно ниже, чем у группы STZ-носитель. С другой стороны, у этих групп концентрации инсулина в плазме не имели значимого различия.
*1: P<0,05; по сравнению с контрольной группой. #1: P<0,05; по сравнению с группой STZ-носитель (критерий множественного сравнения Даннета).
Затем определяли массу тела, массу поджелудочной железы и содержание инсулина в поджелудочной железе на 9-ю неделю. Результаты определения массы тела и массы поджелудочной железы приводятся на фиг. 8. Хотя масса тела животных группы STZ-носитель была значительно ниже, чем у контрольной группы, однако у животных STZ-GHRP-2-группы снижение массы тела прекращалось, и масса тела этих животных значительно не отличалась от массы тела животных контрольной группы. У животных группы “STZ-носитель” наблюдалась тенденция к снижению массы поджелудочной железы по сравнению с животными контрольной группы. С другой стороны, у животных STZ-GHRP-2-группы масса поджелудочной железы была выше, чем у животных группы “STZ-носитель”.
Авторами настоящего изобретения было проведено сравнение уровней инсулина в поджелудочных железах. Поджелудочные железы разделяли для получения двух образцов: образца ткани со стороны селезенки и образца ткани со стороны кишечника, а затем содержание инсулина в поджелудочных железах вычисляли исходя из содержания инсулина в каждом образце, и результаты этих вычислений приводятся в таблице 6. У животных группы “STZ-носитель” содержание инсулина в поджелудочной железе, вычисленное для каждого из двух образцов, было значительно ниже, чем у контрольной группы. Содержание инсулина у животных STZ-GHRP-2-группы было также значительно ниже, чем у контрольной группы, однако у этой группы содержание инсулина было выше, чем у группы “STZ-носитель”, что указывало на тенденцию у животных этой группы к сохранению способности продуцировать инсулин.
*1: P<0,05; по сравнению с контрольной группой (критерий множественного сравнения Даннета).
Как описано выше, было также показано, что, помимо крысиного грелина и человеческого грелина, соединение GHRP-2, обладающее способностью связываться с GHS-R и активировать его, обнаруживало также способность к увеличению продуцирования инсулина после раннего введения этого соединения новорожденным животным STZ-модели и к подавлению развития гипергликемии у взрослых животных. Поэтому было высказано предположение, что действие грелина на регенерацию β-клеток и его способность снижать гипергликемию опосредуется GHS-R и что соединение (GHS), обладающее способностью связываться с GHS-R и активировать его, дает аналогичные эффекты.
Как описано выше, авторами настоящего изобретения было продемонстрировано, что крысиный грелин, человеческий грелин и GHS-соединение подавляют гипергликемию на ее поздней стадии у новорожденных животных STZ-модели. Затем оценивали эффект человеческого грелина на другой модели гипергликемии.
Пример 5
Известно, что пища с высоким содержанием жира, традиционная для западных стран, является причиной развития ожирения или диабета. Кроме того, жирная кислота, такая как линолевая кислота, представляет собой лиганд GRP40, то есть один из рецепторов, сопряженных с G-белком, при этом сообщалось, что активация GPR40 жирной кислотой стимулирует глюкозочувствительную секрецию инсулина из панкреатических β-клеток (Itoh Y et al. Nature 422, pp173-176, 2003). С другой стороны, было высказано предположение, что хотя кратковременнoе воздействие жирной кислоты стимулирует секрецию инсулина, однако длительное ее воздействие приводит к снижению секреции инсулина и к снижению уровней инсулина в поджелудочной железе (Steneberg P et al. Cell Metab 1, pp245-258, 2005). Поэтому для оценки влияния человеческого грелина на секрецию инсулина и на концентрацию глюкозы в крови мышам давали корм с высоким содержанием жирных кислот, а именно линолевой кислоты.
1. Материалы и методы
Самцов мышей Crj:CD1(ICR) (Charles River Japan) содержали в условиях свободного доступа к водопроводной воде и к стандартному гранулированному мышиному корму (CRF-1, Oriental Yeast Co., Ltd.) (с включением света с 21 часа до 9 часов). Контрольных, то есть нормальных, мышей содержали в тех же условиях (нормальный корм, ND-группа). Группе животных, которым через 4 недели после рождения давали корм с высоким содержанием жира (High Fat Diet, HFD-группа), обеспечивали свободный доступ к смеси, содержащей 5 г CRF-1 (порошок) и 1 г линолевой кислоты и представляющей собой корм с высоким содержанием жирной кислоты. Этим животным в течение примерно 7 недель со дня начала кормления пищей с высоким содержанием жирных кислот вводили два раза в день (в выходные, один раз в день) тестируемые вещества, а именно носитель (5% раствор маннита) (группа “HFD-носитель”) или 300 мкг/кг человеческого грелина (группа “HFD-грелин”). Затем проводили мониторинг изменения массы тела и уровней сахара в крови ad lib после начала введения тестируемого вещества. Кроме того, на 50-й день, начиная со дня введения тестируемого вещества, мышей выдерживали в режиме голодания в течение ночи, а затем на следующий день вводили ударную дозу линолевой кислоты (1 мл/кг, внутрибрюшинно) и через 1 час измеряли концентрации глюкозы и инсулина в плазме. Уровень сахара в крови измеряли с использованием устройства Antsense II (Horiba, Ltd.), а концентрацию глюкозы и инсулина в плазме измеряли с использованием теста на глюкозу CII-test Wako (Wako Pure Chemical Industries, Ltd.) и набора для определения уровня инсулина Lebis (TMB для мышей) (Shibayagi Co. Ltd.) соответственно.
2. Результаты
Была проведена оценка влияния введения человеческого грелина на массу тела и уровни сахара в крови у мышей, которым давали корм с высоким содержанием жирных кислот. На фиг. 9 указана масса тела на 42-й день после введения грелина и уровни сахара в крови ad lib на 43-й день после его введения. Масса тела у мышей группы HFD-носитель была выше, чем у ND-группы, а у группы HFD-грелин она была еще выше. Кроме того, уровни сахара в крови у животных группы HFD-носитель были значительно выше, чем у ND-группы. С другой стороны, уровни сахара в крови у животных группы HFD-грелин имели тенденцию к снижению по сравнению с уровнями сахара у животных HFD-носитель и не имели значительных отличий от уровней ND-группы. Таким образом, было показано, что введение грелина приводит к снижению индуцирования гипергликемии, вызываемой потреблением корма с высоким содержанием жирных кислот.
Затем были проанализированы изменения концентраций инсулина в плазме и концентраций глюкозы в плазме после введения ударной дозы линолевой кислоты мышам, которые получали корм с высоким содержанием жирных кислот.
На фиг. 10 показаны концентрации инсулина в плазме (A) и концентрации глюкозы в плазме (B) у мышей, которым давали обычный корм или корм с высоким содержанием жирных кислот и внутрибрюшинно вводили 1 мл/кг линолевой кислоты. У животных группы “HFD-носитель” по сравнению с ND-группой концентрации инсулина в плазме после введения линолевой кислоты в среднем снижались самое большее на 1/3, что позволяет предположить, что при длительном потреблении корма с высоким содержанием жирных кислот способность к секреции инсулина нарушается. Концентрации инсулина у животных группы HFD-грелин были выше, чем у животных группы HFD-носитель, и значительно не отличались от концентраций инсулина у животных ND-группы (фиг. 10A). С другой стороны, хотя до введения линолевой кислоты у животных этих 3 групп почти не наблюдалось различий в концентрациях глюкозы в плазме (ND-группа: 138±5; группа HFD-носитель: 146±12; группа HFD-грелин: 141±5 мг/дл; среднее для 8 мышей ± стандартная ошибка для каждой группы), однако через 1 час после введения линолевой кислоты концентрации глюкозы в плазме у всех групп значительно повышались по сравнению с концентрациями глюкозы до введения этой кислоты (P<0,05, парный т-критерий). Увеличение концентраций глюкозы в плазме после введения линолевой кислоты было более значимым у животных группы “HFD-носитель” по сравнению с ND-группой.
Концентрации глюкозы в плазме после введения линолевой кислоты животным группы “HFD-грелин” имели тенденцию к снижению по сравнению с концентрациями у животных группы “HFD-носитель” и значительно не отличались от концентраций у ND-группы (фиг. 10B).
Как описано выше, было показано, что повторное введение человеческого грелина предотвращает повышение уровней сахара в крови у мышей, которые получали корм с высоким содержанием жирных кислот. При потреблении такого корма с высоким содержанием жирных кислот наблюдалось снижение секреции инсулина, индуцируемое линолевой кислотой, но у группы животных, которым вводили человеческий грелин, такое снижение имело тенденцию к замедлению. Поэтому было высказано предположение, что человеческий грелин улучшает функцию β-клеток, то есть устраняет недостаточность секреции инсулина, вызываемую потреблением корма с высоким содержанием жирных кислот и тем самым предотвращает развитие гипергликемии.
ПРОМЫШЛЕННОЕ ПРИМЕНЕНИЕ
Фармацевтический препарат согласно изобретению обладает действием, стимулирующим неогенез или регенерацию панкреатических β-клеток, продуцирующих и секретирующих инсулин, и действием, стимулирующим продуцирование инсулина в панкреатических β-клетках, а поэтому он может быть использован для снижения или лечения гипергликемии путем стимуляции неогенеза или регенерации панкреатических β-клеток, продуцирующих и секретирующих инсулин при гипергликемии, вызываемой отсутствием или очень низким уровнем секреции инсулина, обусловленным нарушением функций или гибелью панкреатических β-клеток, или при гипергликемии, вызываемой снижением уровня секреции инсулина в панкреатических β-клетках. Кроме того, указанный фармацевтический препарат может быть также использован в качестве фармацевтического средства для проведения терапии, способствующей регенерации панкреатических β-клеток, обладающих инсулин-продуцирующей функцией. Поскольку настоящее изобретение дает возможность стимулировать неогенез или регенерацию панкреатических β-клеток, продуцирующих и секретирующих инсулин, то преимущество настоящего изобретения заклеючается в том, что оно позволяет устранить главную причину гипергликемии, то есть дефицит панкреатических β-клеток и недостаточное продуцирование или секрецию инсулина в этих клетках.











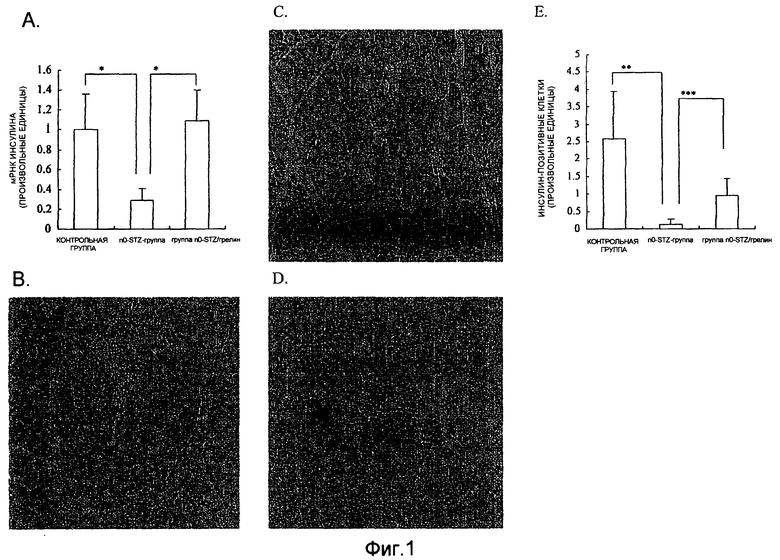
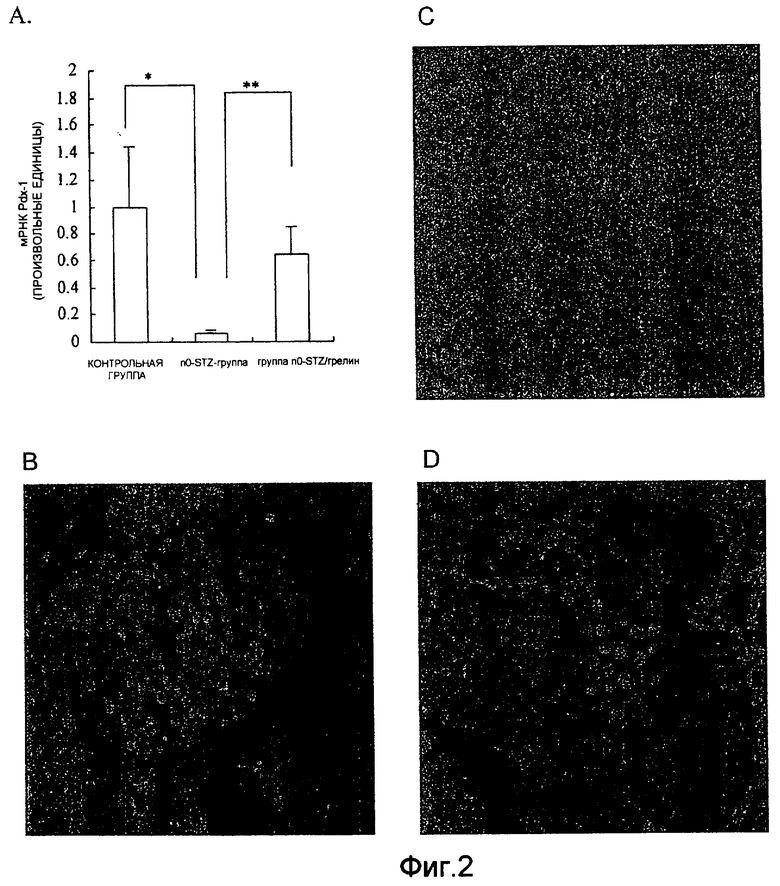
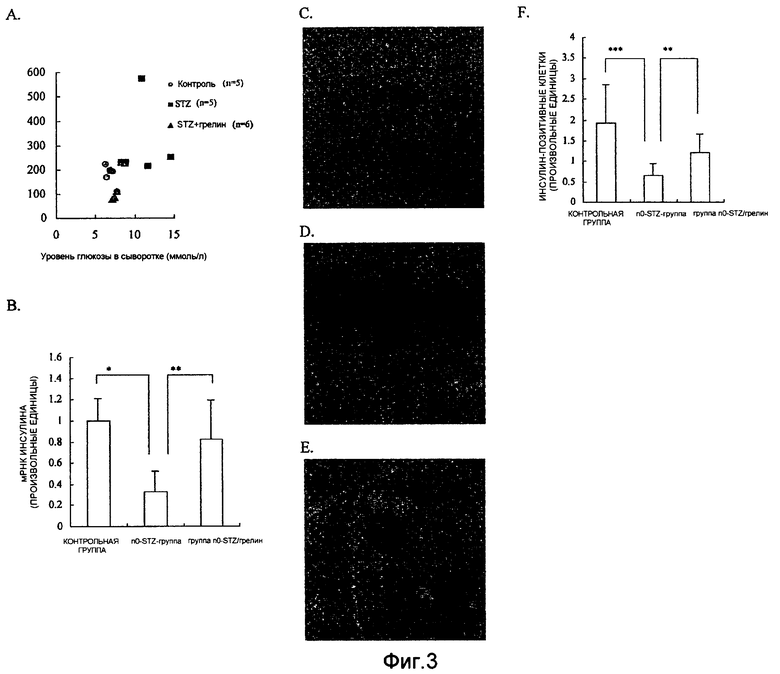
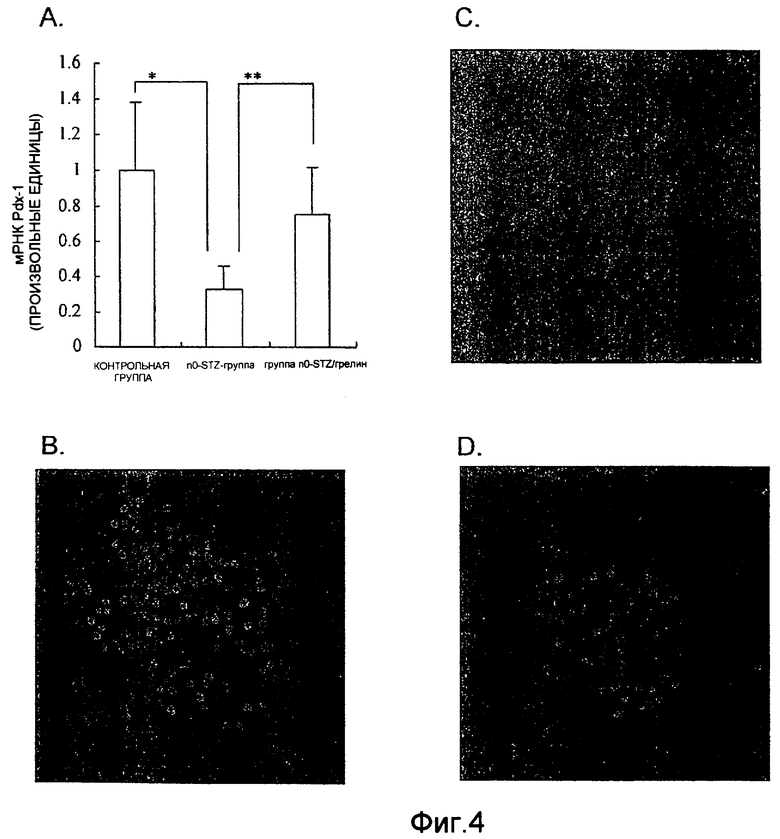
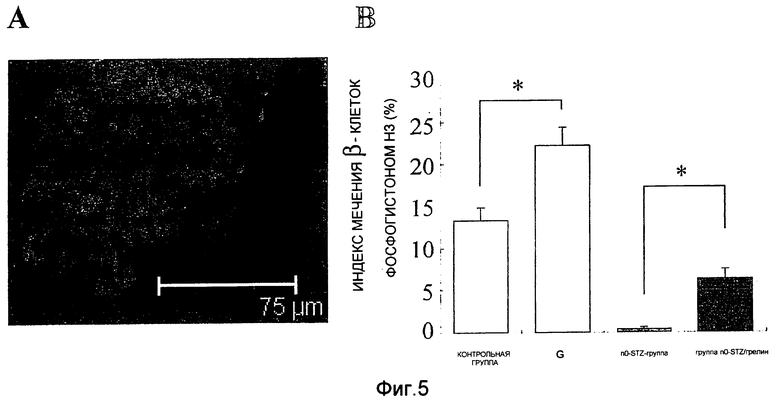
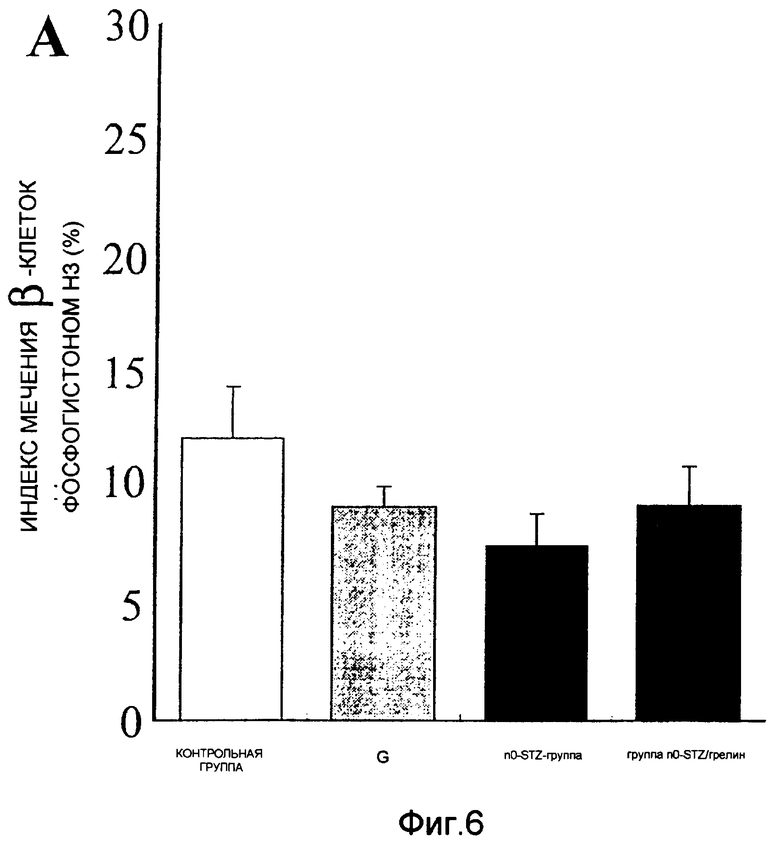

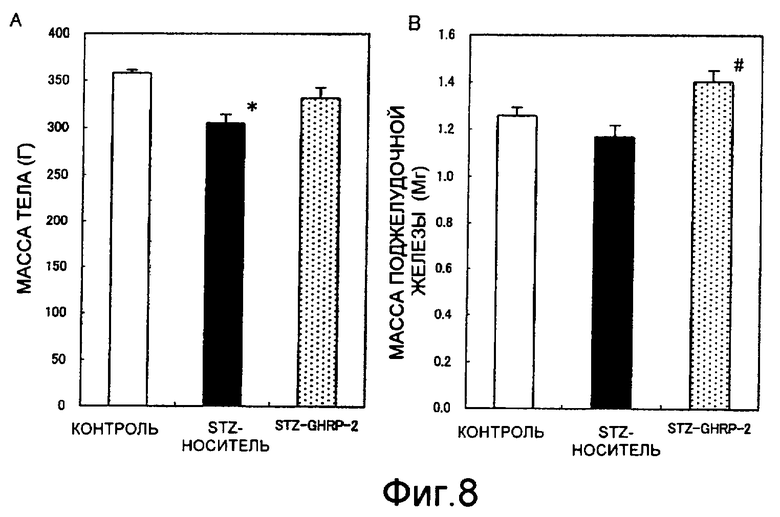
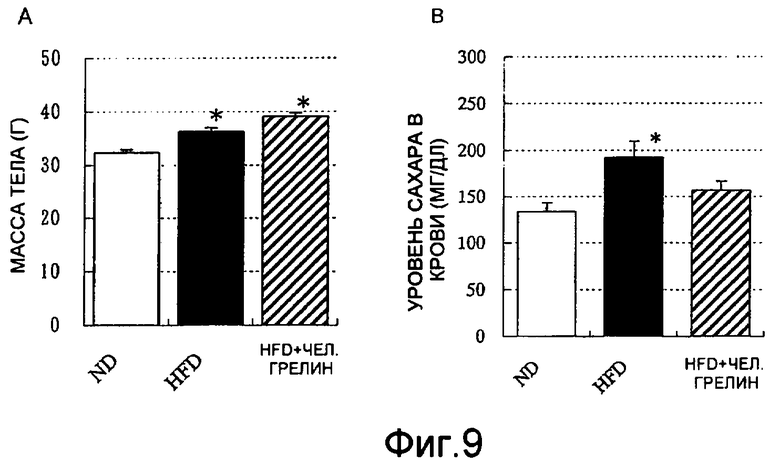
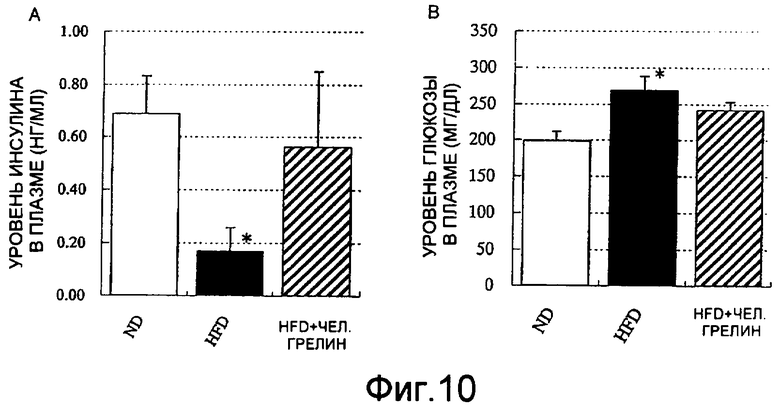
Изобретение относится к области медицины и касается стимулятора регенерации панкреатических бета-клеток и продуцирования инсулина в панкреатических бета-клетках. Сущность изобретения включает фармацевтическую композицию для стимуляции неогенеза или регенерации панкреатических бета-клеток, продуцирующих и секретирующих инсулин, и для стимуляции продуцирования инсулина в бета-клетках, где указанная композиция содержит грелин или его производное в качестве эффективного компонента. Преимущество изобретения заключается в разработке способа стимуляции неогенеза или регенерации панкреатических бета-клеток. 12 н. и 6 з.п. ф-лы, 6 табл., 10 ил.
1. Фармацевтическая композиция для снижения или лечения гипергликемии, содержащая в качестве эффективного компонента пептидное соединение, способное повышать секрецию гормона роста и обладающее активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, или его фармацевтически приемлемую соль.
2. Фармацевтическая композиция, стимулирующая неогенез или регенерацию панкреатических β-клеток, содержащая в качестве эффективного компонента пептидное соединение, способное повышать секрецию гормона роста и обладающее активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, или его фармацевтически приемлемую соль.
3. Фармацевтическая композиция, стимулирующая продукцию инсулина в панкреатических β-клетках, содержащая в качестве эффективного компонента пептидное соединение, способное повышать секрецию гормона роста и обладающее активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, или его фармацевтически приемлемую соль.
4. Фармацевтическая композиция для подавления нарушения функции, гибели или истощения панкреатических β-клеток, содержащая в качестве эффективного компонента пептидное соединение, способное повышать секрецию гормона роста и обладающее активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, или его фармацевтически приемлемую соль.
5. Применение пептидного соединения или его фармацевтически приемлемой соли, способных повышать секрецию гормона роста и обладающих активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, для получения фармацевтической композиции для подавления или лечения гипергликемии.
6. Применение пептидного соединения или его фармацевтически приемлемой соли, способных повышать секрецию гормона роста и обладающих активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, для получения фармацевтической композиции, стимулирующей неогенез или регенерацию панкреатических β-клеток.
7. Применение пептидного соединения или его фармацевтически приемлемой соли, способных повышать секрецию гормона роста и обладающих активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, для получения фармацевтической композиции, стимулирующей продукцию инсулина в панкреатических β-клетках.
8. Применение пептидного соединения или его фармацевтически приемлемой соли, способных повышать секрецию гормона роста и обладающих активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, для получения фармацевтической композиции, подавляющей недостаточность, гибель или истощение панкреатических β-клеток.
9. Способ подавления или лечения гипергликемии, включающий введение эффективного количества пептидного соединения или его фармацевтически приемлемой соли, способных повышать секрецию гормона роста и обладающих активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, пациенту.
10. Способ стимуляции неогенеза или регенерации панкреатических β-клеток, включающий введение эффективного количества пептидного соединения или его фармацевтически приемлемой соли, способных повышать секрецию гормона роста и обладающих активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, пациенту.
11. Способ стимуляции продукции инсулина в панкреатических β-клетках, включающий введение эффективного количества пептидного соединения или его фармацевтически приемлемой соли, способных повышать секрецию гормона роста и обладающих активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, пациенту.
12. Способ, подавляющий недостаточность, гибель или истощение панкреатических β-клеток, включающий введение эффективного количества пептидного соединения или его фармацевтически приемлемой соли, способных повышать секрецию гормона роста и обладающих активностью, направленной на повышение концентрации ионов внутриклеточного кальция посредством связывания с рецептором вещества, стимулирующего секрецию гормона роста, пациенту.
13. Фармацевтическая композиция по п.1, применение по п.5 или способ по п.9, где гиперинсулинемия вызвана прекращением секреции инсулина или очень незначительной секрецией инсулина, связанных со снижением секреции инсулина панкреатическими β-клетками.
14. Фармацевтическая композиция по п.1, применение по п.5 или способ по п.9, где величина ΔIRI/ΔBG при гиперинсулинемии не превышает 0,4.
15. Фармацевтическая композиция, ее применение или способ по любому из пп.1-14, где пептид выбран из группы, состоящей из (1) пептида с аминокислотной последовательностью SEQ ID NO: 1, где 3-ий аминокислотный остаток от аминоконца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в боковую цепь аминокислотного остатка, (2) пептида с аминокислотной последовательностью SEQ ID NO: 1 с делецией, заменой и/или инсерцией одного или нескольких аминокислот в аминокислотной последовательности в 5-28-положениях аминокислот от аминоконца, где 3-й аминокислотный остаток от аминоконца является модифицированным аминокислотным остатком, содержащим жирную кислоту, введенную в его боковую цепь, и (3) GHRP-2.
16. Фармацевтическая композиция, ее применение или способ по п.15, где пептид имеет аминокислотную последовательность SEQ ID NO: 1 и сериновый остаток в 3-ем положении от аминоконца является модифицированным аминокислотным остатком, имеющим жирную кислоту, введенную в гидроксильную группу боковой цепи остатка.
17. Фармацевтическая композиция, ее применение или способ по п.16, где пептид имеет аминокислотную последовательность SEQ ID NO: 1 и гидроксильная группа боковой цепи серинового остатка в 3-ем положении от аминоконца ацилирована н-октаноильной группой.
18. Фармацевтическая композиция, ее применение или способ по п.15, где пептид представляет собой GHRP-2.
| ASANUMA N | |||
| et al | |||
| New analytical method for pancreas and liver regeneration: normalization of streptpozocin-induced hyperglycemia by retrograde injection of insulin producing cells | |||
| Endocrine Journal | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| et al | |||
| Activin A and betacellulin: effect on regeneration of pancreatic beta-cells in neonatal streptozocin-treated | |||
Авторы
Даты
2010-11-10—Публикация
2006-02-23—Подача