Настоящее изобретение относится к производным пиримидина, обладающим способностью ингибировать репликацию ВИЧ (вируса иммунодефицита человека). Далее, изобретение относится к способам получения указанных соединений и к содержащим их фармацевтическим композициям. Кроме этого, изобретение относится к применению указанных соединений для предотвращения или лечения ВИЧ-инфекции.
Устойчивость вируса ВИЧ по отношению к имеющимся в настоящее время лекарственным средствам против ВИЧ продолжает оставаться основной причиной неудачного лечения. Это привело к появлению комбинированной терапии, использующей два или несколько средств против ВИЧ, обладающих, как правило, различным профилем активности. Значительный прогресс был достигнут с введением терапии HAART (интенсивной антиретровирусной терапии), которая привела к значительному сокращению заболеваемости и смертности среди ВИЧ-пациентов, подвергавшихся указанной терапии. HAART включает различные комбинации нуклеозидных ингибиторов обратной транскриптазы (NRTI), ненуклеозидных ингибиторов обратной транскриптазы (NNRTI) и ингибиторов протеазы (PI). Современные руководства по антиретровирусной терапии рекомендовали такой режим тройной комбинированной терапии для первоначального лечения. Однако эта мультилекарственная терапия не устраняет ВИЧ полностью, причем длительное лечение, как правило, приводит к мультилекарственной устойчивости. В частности, у половины пациентов, получающих комбинированную терапию против ВИЧ, не проявляется полный эффект лечения, в основном из-за устойчивости вируса к одному или нескольким из применяемых лекарств. Также было показано, что устойчивый вирус передается вновь инфицированным людям, что приводит к существенному ограничению возможностей лечения этих пациентов, еще не принимавших лекарства.
Следовательно, существует постоянная потребность в новых комбинациях активных ингредиентов, которые эффективны против ВИЧ. Новые типы эффективных против ВИЧ активных ингредиентов, отличающихся по химической структуре и профилю активности, применимы в новых типах комбинированной терапии. Следовательно, обнаружение таких активных ингредиентов является в высшей степени желательной целью для исследователей.
Настоящее изобретение нацелено именно на разработку нового ряда бициклических производных, обладающих способностью ингибировать репликацию ВИЧ. WO-99/50250, WO-00/27825 и WO-01/85700 раскрывают некоторые замещенные аминопиримидины, и WO-99/50256 и EP-A-834507 раскрывают аминотриазины, обладающие способностью ингибировать репликацию ВИЧ. В DD-21593 описан ряд бисариламинозамещенных пуринов, в качестве соединений, имеющих противогрибковую активность.
В настоящем изобретении было обнаружено, что некоторые бисарилзамещенные бициклические соединения действуют предпочтительно не только с точки зрения их способности ингибировать репликацию ВИЧ, но также за счет их лучшей способности ингибировать репликацию мутировавших штаммов, в частности штаммов, которые приобрели устойчивость к одному или нескольким известным лекарственным препаратам NNRTI (ненуклеозидным ингибиторам обратной транскриптазы), причем эти штаммы называют штаммами ВИЧ с лекарственной или мультилекарственной устойчивостью.
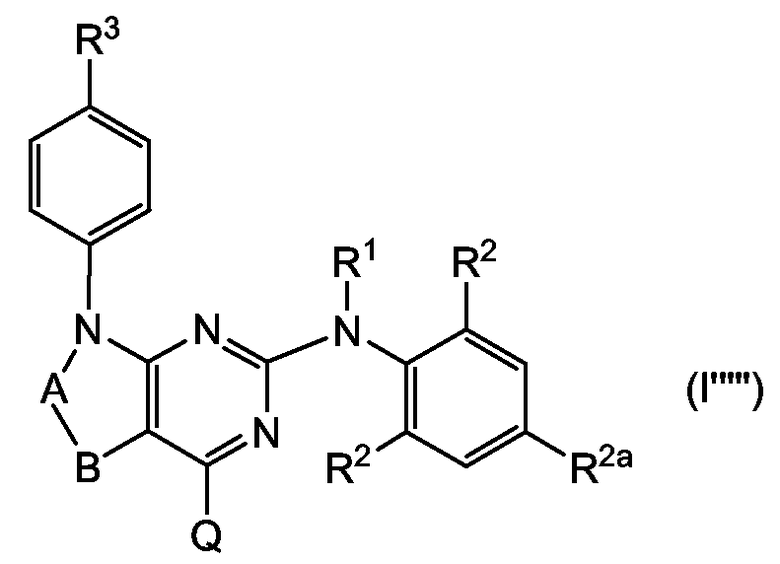
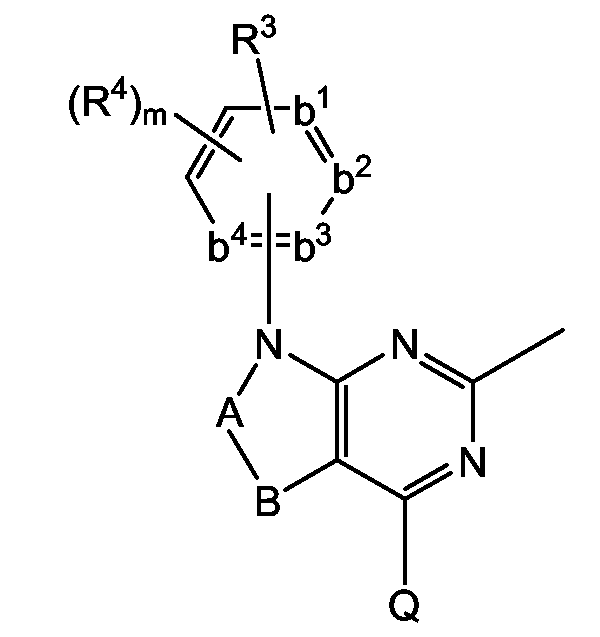
Настоящее изобретение относится к соединениям следующей формулы:
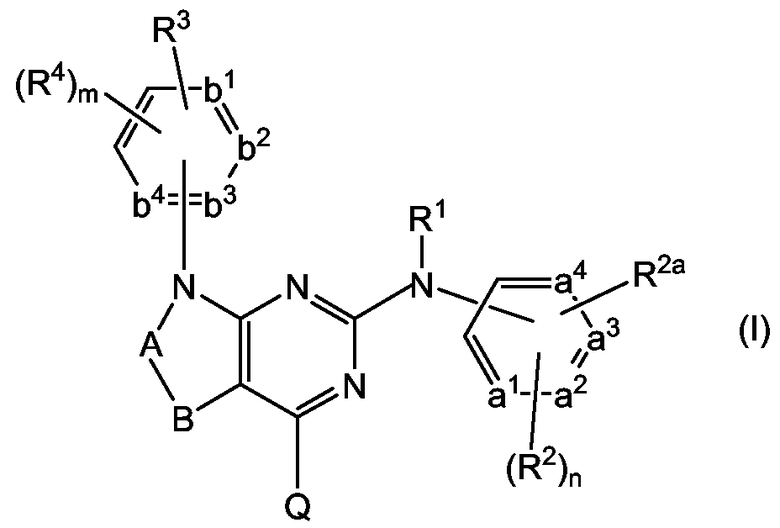
их N-оксидам, фармацевтически приемлемым аддитивным солям, четвертичным аммониевым производным или стереохимически изомерным формам, где
-a1=a2-a3=a4- представляет собой двухвалентный радикал формулы
-b1=b2-b3=b4- представляет собой двухвалентный радикал формулы
n представляет собой 0, 1, 2, 3 и в случае, если -a1=a2-a3=a4- представляет собой (a-1), n также может равняться 4;
m представляет собой 0, 1, 2, 3 и в случае, если -b1=b2-b3=b4- представляет собой (b-1), m также может равняться 4;
-A-B- представляет собой двухвалентный радикал формулы
R1 представляет собой водород; арил; формил; C1-6алкилкарбонил; C1-6алкил; C1-6алкилоксикарбонил; C1-6алкил, замещенный формилом, C1-6алкилкарбонилом или C1-6алкилоксикарбонилом;
каждый из R2 независимо представляет собой гидрокси; галоген; C1-6алкил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано и -C(=O)R6; C3-7циклоалкил; C2-6алкенил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано и -C(=O)R6; C2-6алкинил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано и -C(=O)R6; C1-6алкилоксикарбонил; карбоксил; циано; нитро; амино; моно- или ди(C1-6алкил)амино; полигалогенметил; полигалогенметилтио; -S(=O)pR6; -NH-S(=O)pR6; -C(=O)R6; -NHC(=O)H; -C(=O)NHNH2; NHC(=O)R6; C(=NH)R6;
R2a представляет собой циано; аминокарбонил; амино; C1-6алкил; галоген; C1-6алкилокси, где C1-6алкил может быть необязательно замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; C1-6алкилоксиC1-6алкил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; C2-6алкинил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; -C(=N-O-R8)-C1-4алкил; R7 или -X-R7;
R3 представляет собой циано; аминокарбонил; амино; C1-6алкил; галоген; C1-6алкилокси, где C1-6алкил может быть необязательно замещен цианогруппой; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкилоксиC1-6алкил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкинил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; -C(=N-O-R8)-C1-4алкил; R7 и -X-R7;
X представляет собой -NR1-, -O-, -C(=O), -S-, -S(=O)p-;
каждый из R4 независимо представляет собой галоген; гидрокси; C1-6алкил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано и -C(=O)R6; C2-6алкенил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано и -C(=O)R6; C2-6алкинил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано и -C(=O)R6; C3-7циклоалкил; C1-6алкилокси; циано; нитро; полигалогенC1-6алкил; полигалогенC1-6алкилокси; аминокарбонил; моно- или ди(C1-4алкил)аминокарбонил; C1-6алкилоксикарбонил; C1-6алкилкарбонил; формил; амино; моно- или ди(C1-4алкил)амино или R7;
Q представляет собой водород, C1-6алкил, галоген, полигалогенC1-6алкил или -NR9R10;
R5 представляет собой водород, C1-6алкил, арил, пиридил, тиенил, фуранил, амино, моно- или ди(C1-4алкил)амино;
R6 представляет собой C1-4алкил, амино, моно- или ди(C1-4алкил)амино или полигалогенC1-4алкил;
R7 представляет собой моноциклический, бициклический или трициклический, насыщенный, частично насыщенный или ароматический карбоцикл или же моноциклический, бициклический или трициклический, насыщенный, частично насыщенный или ароматический гетероцикл, где каждый из упомянутых карбоциклических или гетероциклических фрагментов может быть необязательно замещен одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, моно- и ди(C1-6алкил)аминоC1-6алкила, формила, C1-6алкилкарбонила, C3-7циклоалкила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, полигалогенC1-6алкила, полигалогенC1-6алкилокси, аминокарбонила, -C(=N-O-R8), R7a, -X-R7a, и R7a-C1-4алкила;
R7a представляет собой моноциклический, бициклический или трициклический, насыщенный, частично насыщенный или ароматический карбоцикл или же моноциклический, бициклический или трициклический, насыщенный, частично насыщенный или ароматический гетероцикл, где каждый из упомянутых карбоциклических или гетероциклических фрагментов может быть необязательно замещен одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, моно- или ди(C1-6алкил)аминоC1-6алкила, формила, C1-6алкилкарбонила, C3-7циклоалкила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, полигалогенC1-6алкила, полигалогенC1-6алкилокси, аминокарбонила и -CH(=N-O-R8);
R8 представляет собой водород, C1-4алкил, арил или арилC1-4алкил.
Каждый из R9 и R10 независимо представляет собой водород; гидроксигруппу; C1-6алкил; C1-6алкилокси; C1-6алкилкарбонил; C1-6алкилоксикарбонил; амино; моно- или ди(C1-6алкил)амино; моно- или ди(C1-6алкил)аминокарбонил; -CH(=NR11) или R7, где каждая из упомянутых выше C1-6алкильных групп может быть необязательно, причем каждая в отдельности, замещена одним или двумя заместителями, каждый из которых независимо выбран из гидрокси, C1-6алкилокси, гидроксиC1-6алкилокси, карбоксила, C1-6алкилоксикарбонила, циано, амино, имино, моно- и ди(C1-4алкил)амино, полигалогенметила, полигалогенметилокси; полигалогенметилтио, -S(=O)pR6, -NH-S(=O)pR6, -C(=O)R6, -NHC(=O)H, -C(=O)NHNH2, NHC(=O)R6, C(=NH)R6, R7; или
R9 и R10 совместно могут образовывать двухвалентный или трехвалентный радикал формулы:
R11 представляет собой циано; C1-4алкил, необязательно замещенный C1-4алкилокси, циано, амино, моно- или ди(C1-4алкил)амино или аминокарбонилом; C1-4алкилкарбонил; C1-4алкилоксикарбонил; аминокарбонил; моно- или ди(C1-4алкил)аминокарбонил;
R12 представляет собой водород или C1-4алкил;
каждый из R13 и R14 независимо представляет собой C1-6алкил, необязательно замещенный цианогруппой или аминокарбонилом, C2-6алкенил, необязательно замещенный цианогруппой или аминокарбонилом, C2-6алкинил, необязательно замещенный цианогруппой или аминокарбонилом;
R15 представляет собой C1-6алкил, замещенный цианогруппой или аминокарбонилом;
R16 представляет собой C1-6алкил, необязательно замещенный цианогруппой или аминокарбонилом, или R7;
каждый из индексов p равняется 1 или 2;
каждый из арилов представляет собой фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, моно- или ди(C1-6алкил)аминоC1-6алкила, C1-6алкилкарбонила, C3-7циклоалкила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, полигалогенC1-6алкила, полигалогенC1-6алкилокси, аминокарбонила, радикалов Het и -X-Het;
Het представляет собой пиридил, тиенил, фуранил, оксазолил, изоксазолил, имидазолил, пиразолил, тиазолил, тиадиазолил, оксадиазолил, хинолинил, бензотиенил, бензофуранил, каждый из которых может быть необязательно замещен одним или двумя C1-4алкильными радикалами.
Настоящее изобретение также относится к применению соединения для производства лекарственного средства, предназначенного для лечения или предотвращения ВИЧ-инфекции, причем соединение принадлежит к группе соединений, имеющих формулу (I), или к любой из подгрупп соединений, описанных в настоящей заявке.
Выше и ниже по тексту настоящей заявки термин «C1-4алкил» в качестве самостоятельной группы или составной части другой группы определяет насыщенные углеводородные радикалы с линейной или разветвленной цепью, включающие от 1 до 4 атомов углерода, такие как метил, этил, пропил, 1-метилэтил, бутил; термин «C1-6алкил» в качестве самостоятельной группы или составной части другой группы определяет насыщенные углеводородные радикалы с линейной или разветвленной цепью, включающие от 1 до 6 атомов углерода, такие как группы, определенные термином «C1-4алкил», а также пентил, гексил, 2-метилбутил и т.п.; термин «C1-2алкил» определяет метил и этил; термин «C2-6алкил» в качестве самостоятельной группы или составной части другой группы определяет насыщенные углеводородные радикалы с линейной или разветвленной цепью, включающие от 2 до 6 атомов углерода, такие как этил, пропил, 1-метилэтил, бутил, пентил, гексил, 2-метилбутил и т.п.; термин «C3-7циклоалкил» объединяет циклопропил, циклобутил, циклопентил, циклогексил и циклогептил; термин «C2-6алкенил» определяет углеводородные радикалы с линейной или разветвленной цепью, включающие от 2 до 6 атомов углерода и содержащие двойную связь, такие как этенил, пропенил, бутенил, пентенил, гексенил и т.п.; термин «C2-6алкинил» определяет углеводородные радикалы с линейной или разветвленной цепью, включающие от 2 до 6 атомов углерода и содержащие тройную связь, такие как этинил, пропинил, бутинил, пентинил, гексинил и т.п. Среди C2-6алкенилов и C2-6алкинилов предпочтительными являются ненасыщенные аналоги, включающие от 2 до 4 атомов углерода, т.е. соответственно C2-4алкенил и C2-4алкинил. Любой из C2-6алкенилов и C2-6алкинилов, связанных с гетероатомом, предпочтительно связан с указанным гетероатомом через насыщенный атом углерода.
В некоторых случаях радикалы C1-6алкинил, C2-6алкенил или C2-6алкинил могут быть замещены одним двумя или тремя заместителями. Предпочтительно указанные радикалы замещены одним или двумя заместителями, более предпочтительно одним заместителем.
Моноциклический, бициклический или трициклический насыщенный карбоцикл представляет собой циклическую систему, состоящую из 1, 2 или 3 циклов, причем указанная циклическая система состоит только из атомов углерода и указанная циклическая система содержит только простые связи; моноциклический, бициклический или трициклический частично насыщенный карбоцикл представляет собой циклическую систему, состоящую из 1, 2 или 3 циклов, причем указанная циклическая система состоит только из атомов углерода и включает по меньшей мере двойную связь, при условии, что циклическая система не является ароматической циклической системой; моноциклический, бициклический или трициклический ароматический карбоцикл представляет собой ароматическую циклическую систему, состоящую из 1, 2 или 3 циклов, причем указанная циклическая система состоит только из атомов углерода; термин «ароматический» очень хорошо известен специалистам в данной области техники, и он означает циклические сопряженные системы, включающие 4n+2 электронов, т.е. 6, 10, 14 и т.д. π-электронов (правило Хюккеля); моноциклический, бициклический или трициклический насыщенный гетероцикл представляет собой циклическую систему, состоящую из 1, 2 или 3 циклов и включающую хотя бы один гетероатом, выбранный из O, N или S, причем указанная циклическая система содержит только простые связи; моноциклический, бициклический или трициклический частично насыщенный гетероцикл представляет собой циклическую систему, состоящую из 1, 2 или 3 циклов и включающую по меньшей мере один гетероатом, выбранный из O, N или S, и по меньшей мере одну двойную связь, при условии, что циклическая система не является ароматической циклической системой; моноциклический, бициклический или трициклический ароматический гетероцикл представляет собой ароматическую циклическую систему, состоящую из 1, 2 или 3 циклов и включающую хотя бы один гетероатом, выбранный из O, N или S.
Конкретными примерами моноциклических, бициклических или трициклических насыщенных карбоциклов являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, бицикло[4,2,0]-октанил, циклононанил, циклодеканил, декагидронафталинил, тетрадекагидроантраценил и т.п. Предпочтительными являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, более предпочтительными являются циклопентил, циклогексил, циклогептил.
Конкретными примерами моноциклических, бициклических или трициклических частично насыщенных карбоциклов являются циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил, бицикло[4,2,0]октенил, циклононенил, циклодеценил, октагидронафталинил, 1,2,3,4-тетрагидронафталинил, 1,2,3,4,4a,9,9a,10-октагидроантраценил и т.п.
Конкретными примерами моноциклических, бициклических или трициклических ароматических карбоциклов являются фенил, нафталинил, антраценил. Предпочтительным является фенил.
Конкретными примерами моноциклических, бициклических или трициклических насыщенных гетероциклов являются тетрагидрофуранил, пирролидинил, диоксоланил, имидазолидинил, тиазолидинил, тетрагидротиенил, дигидрооксазолил, изотиазолидинил, изоксазолидинил, оксадиазолидинил, триазолидинил, тиадиазолидинил, пиразолидинил, пиперидинил, гескагидропиримидинил, гексагидропиразинил, диоксанил, морфолинил, дитианил, тиофорфолинил, пиперазинил, тритианил, декагидрохинолинил, октагидроиндолил и т.п. Предпочтительными являются тетрагидрофуранил, пирролидинил, диоксоланил, имидазолидинил, тиазолидинил, дигидрооксазолил, триазолидинил, пиперидинил, диоксанил, морфолинил, тиоморфолинил, пиперазинил. Особенно предпочтительными являются тетрагидрофуранил, пирролидинил, диоксоланил, пиперидинил, диоксанил, морфолинил, тиоморфолинил, пиперазинил.
Конкретными примерами моноциклических, бициклических и трициклических частично насыщенных гетероциклов являются пирролинил, имидазолинил, пиразолинил, 2,3-дигидробензофуранил, 1,3-бензодиоксолил, 2,3-дигидро-1,4-бензодиоксинил, индолинил и т.п. Предпочтительными являются пирролинил, имидазолинил, 2,3-дигидробензофуранил, 1,3-бензодиоксолил, индолинил.
Конкретными примерами моноциклических, бициклических или трициклических ароматических гетероциклов являются азетил, оксетилиденил, пирролил, фурил, тиенил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тиадиазолил, оксадиазолил, тетразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, пиранил, бензофурил, изобензофурил, бензотиенил, изобензотиенил, индолизинил, индолил, изоиндолил, бензоксазолил, бензимидазолил, индазолил, бензизоксазолил, бензизотиазолил, бензопиразолил, бензоксадиазолил, бензотиадиазолил, бензотриазолил, пуринил, хинолинил, изохинолинил, циннолинил, хинолизинил, фталазинил, хиноксалинил, хиназолинил, нафтиридинил, птеридинил, бензопиранил, пирролопиридил, тиенопиридил, фуропиридил, изотиазолопиридил, тиазолопиридил, изоксазолопиридил, оксазолопиридил, пиразолопиридил, имидазопиридил, пирролопиразинил, тиенопиразинил, фуропиразинил, изотиазолопиразинил, тиазолопиразинил, изоксазолопиразинил, оксазолопиразинил, пиразолопиразинил, имидазопиразинил, пирролопиримидинил, тиенопиримидинил, фуропиримидинил, изотиазолопиримидинил, тиазолопиримидинил, изоксазолопиримидинил, оксазолопиримидинил, пиразолопиримидинил, имидазопиримидинил, пирролопиридазинил, тиенопиридазинил, фуропиридазинил, изотиазолопиридазинил, тиазолопиридазинил, изоксазолопиридазинил, оксазолопиридазинил, пиразолопиридазинил, имидазопиридазинил, оксадиазолопиридил, тиадиазолопиридил, триазолопиридил, оксадиазолопиразинил, тиадиазолопиразинил, триазолопиразинил, оксадиазолопиримидинил, тиадиазолопиримидинил, триазолопиримидинил, оксадиазолопиридазинил, тиадиазолопиридазинил, триазолопиридазинил, имидазооксазолил, имидазотиазолил, имидазоимидазолил, изоксазолотриазинил, изотиазолотриазинил, пиразолотриазинил, оксазолотриазинил, тиазолотриазинил, имидазотриазинил, оксадиазолотриазинил, тиадиазолотриазинил, триазолотриазинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил и т.п.
Предпочтительными ароматическими гетероциклами являются моноциклические или бициклические ароматические гетероциклы. Представляющими интерес моноциклическими, бициклическими или трициклическими ароматическими гетероциклами являются пирролил, фурил, тиенил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тиадиазолил, оксадиазолил, тетразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, пиранил, бензофурил, изобензофурил, бензотиенил, изобензотиенил, индолил, изоиндолил, бензоксазолил, бензимидазолил, индазолил, бензизоксазолил, бензизотиазолил, бензопиразолил, бензоксадиазолил, бензотиадиазолил, бензотриазолил, пуринил, хинолинил, изохинолинил, фталазинил, хиноксалинил, хиназолинил, бензопиранил, пирролопиридил, тиенопиридил, фуропиридил, изотиазолопиридил, тиазолопиридил, изоксазолопиридил, оксазолопиридил, пиразолопиридил, имидазопиридил, пирролопиразинил, тиенопиразинил, фуропиразинил, изотиазолопиразинил, тиазолопиразинил, изоксазолопиразинил, оксазолопиразинил, пиразолопиразинил, имидазопиразинил, пирролопиримидинил, тиенопиримидинил, фуропиримидинил, изотиазолопиримидинил, тиазолопиримидинил, изоксазолопиримидинил, оксазолопиримидинил, пиразолопиримидинил, имидазопиримидинил, оксадиазолопиридил, тиадиазолопиридил, триазолопиридил, оксадиазолопиразинил, тиадиазолопиразинил, триазолопиразинил, оксадиазолопиримидинил, тиадиазолопиримидинил, триазолопиримидинил, карбазолил, акридинил, фенотиазинил, феноксазинил и т.п.
Ароматическими гетероциклами, представляющими особый интерес, являются пирролил, фурил, тиенил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тиадиазолил, оксадиазолил, тетразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, пиранил, бензофурил, изобензофурил, бензотиенил, изобензотиенил, индолил, изоиндолил, бензоксазолил, бензимидазолил, индазолил, бензизоксазолил, бензизотиазолил, бензопиразолил, бензоксадиазолил, бензотиадиазолил, бензотриазолил, пуринил, хинолинил, изохинолинил, фталазинил, хиноксалинил, хиназолинил и т.п.
Использованный выше в настоящем описании фрагмент (=O) образует карбонильную группу, если он присоединен к атому углерода, сульфоксидную группу, если он присоединен к атому серы, и сульфонильную группу, если к атому серы присоединены два таких фрагмента.
Термины «карбоксил», «карбокси» или «гидроксикарбонил» относятся к группе -COOH.
Термин «галоген» является общим для фтора, хлора, брома и йода. Использованный выше и ниже по тексту термин «полигалогенметил» в качестве группы или части группы определен как моно- или полигалогензамещенный метил, в частности метил с одним или несколькими атомами фтора, например дифторметил или трифторметил; термины "полигалогенC1-4алкил" или "полигалогенC1-6алкил" в виде группы или части группы определены как моно- или полигалогензамещенные C1-4алкил или C1-6алкил, например группы, определенные терминами галогенметил, 1,1-дифторэтил и т.п. В случае если к алкильной группе присоединено более одного атома галогена, в рамках терминов «полигалогенметил», «полигалогенC1-4алкил» или «полигалогенC1-6алкил» эти атомы могут быть одинаковыми или различными.
При любом упоминании в определении соединений формулы (I) или любой из подгрупп этих соединений, выделенных в настоящем описании, каждый из арилов независимо соответствует определениям, приведенным выше при описании соединений формулы (I), или каждый из арилов может соответствовать любому из значений, приведенных ниже в настоящем описании.
Предполагается, что термин «гетероцикл» в определении заместителей R7 или R7a включает все возможные изомерные формы гетероциклов, например пирролил включает 1H-пирролил и 2H-пирролил.
Карбоциклы или гетероциклы, упоминаемые в определении R7 или R7a, могут быть присоединены к остальной части молекулы формулы (I) через любой подходящий циклический атом углерода или гетероатом, если конкретно не указано иное. Так, например, если гетероцикл представляет собой имидазолил, он может являться 1-имидазолилом, 2-имидазолилом, 4-имидазолилом и т.д., или, если карбоцикл представляет собой нафталинил, он может быть 1-нафталинилом, 2-нафталинилом и т.д.
Если любой из заместителей (например, R7) одновременно встречается в одном и том же соединении более одного раза, каждое из определений такого заместителя является независимым.
Подразумевается, что любые ограничения в определении радикалов в настоящем описании применимы к группе соединений формулы (I), а также к любой подгруппе, определенной или упомянутой в настоящем описании.
Линии, проведенные от заместителей внутрь циклических систем, показывают, что данная связь может быть присоединена к любому из подходящих атомов в цикле.
Солями соединений формулы (I), пригодными для терапевтического применения, являются такие соли, противоион которых является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, также могут найти применение, например, в получении или очистке фармацевтически приемлемых соединений. Все соли, независимо от того, являются они фармацевтически приемлемыми или нет, включены в объем настоящего изобретения.
Как упоминалось выше, подразумевается, что фармацевтически приемлемые аддитивные соли включают терапевтически активные нетоксичные формы кислотно-аддитивных солей, которые способны образовывать соединения формулы (I). Последние могут быть легко получены обработкой основной формы такими подходящими кислотами, как неорганические кислоты, например, галогеноводородные кислоты, такие как хлористоводородная кислота, бромистоводородная кислота и т.п.; серная кислота, азотная кислота, фосфорная кислота и т.п.; или как органические кислоты, например уксусная, пропионовая, гидроксиуксусная, 2-гидроксипропионовая, 2-оксопропионовая, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, 2-гидрокси-1,2,3-пропантрикарбоновая, метансульфоновая, этансульфоновая, бензолсульфоновая, 4-метилбензолсульфоновая, циклогексансульфаминовая, 2-гидроксибензойная, 4-амино-2-гидроксибензойная и тому подобные кислоты. Напротив, соединение в форме соли может быть превращено в форму свободного основания обработкой щелочью.
Соединения формулы (I), содержащие кислотные протоны, могут быть превращены в терапевтически активные нетоксичные формы аддитивных солей металлов или аминов обработкой подходящими органическими или неорганическими основаниями. Подходящие формы солей с основаниями включают, например, соли аммония, соли щелочных и щелочноземельных металлов, например соли лития, натрия, калия, магния, кальция и т.п., соли с органическими основаниями, например первичными, вторичными и третичными алифатическими и ароматическими аминами, такими как метиламин, этиламин, пропиламин, изопропиламин, четыре изомера бутиламина, диметиламин, диэтиламин, диэтаноламин, дипропиламин, диизопропиламин, ди-н-бутиламин, пирролидин, пиперидин, морфолин, триметиламин, триэтиламин, трипропиламин, хиноклидин, пиридин, хинолин и изохинолин, бензатин, N-метил-D-глюкамин, 2-амино-2-(гидроксиметил)-1,3-пропандиол, гидрабаминовые соли, а также соли с такими аминокислотами, как, например, аргинин, лизин и т.п. Напротив, соединение в форме соли может быть превращено в форму свободной кислоты обработкой кислотой. Термин «аддитивная соль» включает также гидраты и формы аддитивных соединений с растворителем, которые способны образовывать соединения формулы (I). Примерами таких форм являются гидраты, алкоголяты и т.п.
Термин «четвертичные аммониевые производные», использованный выше в настоящей заявке, означает четвертичные аммониевые соли, которые могут образовывать соединения формулы (I) за счет реакции между основным атомом азота соединения формулы (I) и подходящим кватернизирующим реагентом, таким как, например, необязательно замещенный алкилгалогенид, арилгалогенид или арилалкилгалогенид, например, йодистый метил или йодистый бензил. Также могут применяться другие реагенты, содержащие хорошие уходящие группы, такие как алкилтрифторметансульфонаты, алкилметансульфонаты и алкил п-толуолсульфонаты. Четвертичные аммониевые производные включают положительно заряженный атом азота. Фармацевтически приемлемые противоионы включают хлор, бром, йод, трифторацетат и ацетат. Выбранный противоион может быть введен с применением ионообменных смол.
Имеется в виду, что формы N-оксидов соединений по настоящему изобретению включают соединения формулы (I), в которых один или несколько третичных атомов азота окислены до т.н. N-оксидов.
Следует принять во внимание, что некоторые из соединений формулы (I), а также их N-оксидов, аддитивных солей, четвертичных аммониевых производных и стереохимически изомерных форм могут содержать один или несколько центров хиральности и существовать в виде стереохимически изомерных форм.
Термин «стереохимически изомерные формы», использованный выше по тексту настоящего описания, определяет все возможные стереоизомерные формы, которыми могут обладать соединения формулы (I), а также их N-оксиды, аддитивные соли, четвертичные аммониевые производные или физиологически функциональные производные. Если не показано или не упомянуто иное, химическое наименование соединения указывает на смесь всех возможных стереохимически изомерных форм, причем имеется в виду, что упомянутые смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры, а также на каждую из отдельных изомерных форм соединений формулы (I), и их N-оксидов, солей, сольватов или четвертичных аммониевых производных, в основном свободную от других изомеров, т.е. смешанную с менее чем 10%, предпочтительно, менее чем 5%, в особенности, менее чем 2% и наиболее предпочтительно менее чем 1% других изомеров. Таким образом, если соединение формулы (I) обозначено, например, как (E), это значит, что соединение в основном свободно от (Z) изомера. В частности, центры пространственной изомерии могут иметь R- или S-конфигурацию; заместители у двухвалентных циклических (частично) насыщенных радикалов могут иметь либо цис- либо транс-конфигурацию. Соединения, включающие двойные связи, могут иметь при указанной двойной связи пространственное строение E(entgegen) или Z(zusammen). Обозначения цис, транс, R, S, E и Z хорошо известны специалисту в данной области техники. Подразумевается, что стереохимически изомерные формы соединений формулы (I) входят в объем данного изобретения.
Некоторые из соединений формулы (I) также могут существовать в таутомерных формах. Хотя такие формы не показаны в явном виде в приведенной выше формуле, имеется в виду, что они включены в объем настоящего изобретения.
Подразумевается, что термин «соединения формулы (I)» при использовании в любом месте последующего текста заявки также включает формы их N-оксидов, их солей, их четвертичных аммониевых производных, а также их стереохимически изомерные формы. Особый интерес представляют те соединения формулы (I), которые являются стереохимически чистыми.
Отдельными подгруппами соединений формулы (I) или любой из подгрупп соединений формулы (I), выделенных в настоящей заявке, являются несолевые формы, соли, формы N-оксидов и стереохимически изомерные формы. Среди этих подгрупп интерес представляют несолевые формы, соли и стереохимически изомерные формы. В настоящем описании термин «несолевая форма» относится к форме соединения, которая не является солью, и которая в большинстве случаев будет представлять собой форму свободного основания.
Следует понимать, что любая из подгрупп соединений формулы (I), определенных в настоящей заявке, как подразумевается, включает также любые пролекарства, N-оксиды, аддитивные соли, четвертичные аммониевые производные, комплексы металлов и стереохимически изомерные формы таких соединений.
Где бы в настоящей заявке выше или ниже по тексту не осуществлялось упоминание того, что каждый из заместителей может быть независимо выбран из многочисленного списка определений, как, например, в случае R9 и R10, подразумеваются все возможные комбинации, которые возможны с химической точки зрения или которые ведут к образованию химически стабильных молекул.
Далее по тексту определен ряд подгрупп соединений формулы (I). Приведенные ниже подгруппы соединений формулы (I), перечисление которых является частью изложения настоящего изобретения, могут включать подстановки любого из определений, использованных для описания подгрупп, определенных ниже по тексту.
Представляют интерес такие соединения формулы (I) или любая подгруппа определенных в настоящей заявке соединений формулы (I), которые отличаются от 2-п-толуидино-6-метил-9-п-толуилпурина и 2-п-фенетидино-6-метил-9-п-этоксифенилпурина.
Представляют интерес такие соединения формулы (I) или любая подгруппа определенных в настоящей заявке соединений формулы (I), в которых R2a отличается от метила или этокси; или в которых R2a отличается от C1-2алкила или C1-2алкилокси; R2a отличается от C1-4алкила или C1-4алкилокси; или в которых R2a отличается от C1-6алкила или C1-6алкилокси. Также интерес представляют те соединения формулы (I) или любая подгруппа определенных в настоящей заявке соединений формулы (I), в которых R3 отличается от метила или этокси; или в которых R3 отличается от C1-2алкила или C1-2алкилокси; R2a отличается от C1-4алкила или C1-4алкилокси; или в которых R3 отличается от C1-6алкила или C1-6алкилокси.
Кроме этого, представляют интерес те соединения формулы (I) или любая подгруппа определенных в настоящей заявке соединений формулы (I), в которых R2a и R3 отличаются от метила или этокси; или в которых R2a и R3 отличаются от C1-2алкила или C1-2алкилокси; или в которых R2a и R3 отличаются от C1-4алкила или C1-4алкилокси; или в которых R2a и R3 отличаются от C1-6алкила или C1-6алкилокси.
Отдельными подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых фрагмент -a1=a2-a3=a4- представляет собой -CH=CH-CH=CH-(a-1).
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых фрагмент -b1=b2-b3=b4- представляет собой CH=CH-CH=CH- (b-1).
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых (a) n равняется 0, 1, 2, 3; или в которых (b) n равняется 0, 1 или 2; или (c) n равняется 0.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых (a) m равняется 0, 1, 2, 3; или в которых (b) m равняется 0, 1 или 2; или (c) m равняется 2.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R1 представляет собой водород; формил; C1-6алкилкарбонил; C1-6алкил; C1-6алкилоксикарбонил; или
(b) R1 представляет собой водород; C1-6алкил; или
(c) R1 представляет собой водород.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R2 представляет собой гидрокси; галоген; C1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано и -C(=O)R6; C3-7циклоалкил; C2-6алкенил, необязательно замещенный одним заместителем, выбранным из галогена, циано и -C(=O)R6; C2-6алкинил, необязательно замещенный одним заместителем, выбранным из галогена, циано и -C(=O)R6; C1-6алкилоксикарбонил; карбоксил; циано; нитро; амино; моно- или ди(C1-6алкил)амино; полигалогенметил; полигалогенметилтио; -S(=O)pR6; -NH-S(=O)pR6; -C(=O)R6; -NHC(=O)H; -C(=O)NHNH2; NHC(=O)R6; C(=NH)R6;
(b) R2 представляет собой гидрокси; галоген; C1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано и -C(=O)R6; C2-6алкенил, необязательно замещенный одним заместителем, выбранным из галогена, циано и -C(=O)R6; C2-6алкинил, необязательно замещенный одним заместителем, выбранным из галогена, циано и -C(=O)R6; C1-6алкилоксикарбонил; карбоксил; циано; нитро; амино; моно- или ди(C1-6алкил)амино; трифторметил;
(c) R2 представляет собой галоген; C1-6алкил, необязательно замещенный цианогруппой; C2-6алкенил, необязательно замещенный цианогруппой; C2-6алкинил, необязательно замещенный цианогруппой; C1-6алкилоксикарбонил; карбоксил; циано; амино; моно(C1-6алкил)амино, ди(C1-6алкил)амино;
(d) R2 представляет собой галоген, циано, аминокарбонил, C1-6алкилокси, C1-6алкил, C1-6алкил, замещенный цианогруппой, или C2-6алкенил, замещенный цианогруппой;
(e) R2 представляет собой галоген, циано, аминокарбонил, C1-4алкил, замещенный цианогруппой, или C2-4алкенил, замещенный цианогруппой;
(f) R2 представляет собой циано, аминокарбонил; или
(g) R2 представляет собой циано.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R2a представляет собой циано; аминокарбонил; амино; C1-6алкил; галоген; C1-6алкилокси, где C1-6алкил может быть необязательно замещен цианогруппой; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; C1-6алкилоксиC1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкенил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкинил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; -C(=N-O-R8)-C1-4алкил; R7 или -X-R7;
(b) R2a представляет собой циано; аминокарбонил; амино; C1-6алкил; галоген; C1-6алкилокси, где C1-6алкил может быть необязательно замещен цианогруппой; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C1-6алкилоксиC1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C2-6алкенил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C2-6алкинил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10;
(c) R2a представляет собой галоген, циано, аминокарбонил, C1-6алкил, необязательно замещенный циано или аминокарбонилом, C2-6алкенил, необязательно замещенный циано или аминокарбонилом;
(d) R2a представляет собой галоген, циано, аминокарбонил, C1-6алкил, замещенный циано или аминокарбонилом, или C2-6алкенил, замещенный циано или аминокарбонилом;
(e) R2a представляет собой циано, аминокарбонил, C1-6алкил, замещенный циано, или C2-6алкенил, замещенный циано;
(f) R2a представляет собой циано, аминокарбонил, C1-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(g) R2a представляет собой циано, C1-4алкил, замещенный циано, или C2-4алкенил, замещенный циано; или
(h) R2a представляет собой циано.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) -A-B- представляет собой двухвалентный радикал формулы
(b) -A-B- представляет собой двухвалентный радикал формулы
(c) -A-B- представляет собой двухвалентный радикал формулы
(d) -A-B- представляет собой двухвалентный радикал формулы
(e) -A-B- представляет собой двухвалентный радикал формулы
(f) -A-B- представляет собой двухвалентный радикал формулы
(g) -A-B- представляет собой двухвалентный радикал формулы
(h) -A-B- представляет собой двухвалентный радикал формулы
-CH=N-.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R3 представляет собой циано; аминокарбонил; амино; C1-6алкил; галоген; C1-6алкилокси, где C1-6алкил может быть необязательно замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкилоксиC1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкенил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкинил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; -C(=N-O-R8)-C1-4алкил; R7 или -X-R7;
(b) R3 представляет собой циано; аминокарбонил; амино; C1-6алкил; галоген; C1-6алкилокси, где C1-6алкил может быть необязательно замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C1-6алкилоксиC1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C2-6алкенил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C2-6алкинил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10;
(c) R3 представляет собой галоген, циано, аминокарбонил, C1-6алкил, необязательно замещенный циано или аминокарбонилом, C2-6алкенил, необязательно замещенный циано или аминокарбонилом;
(d) R3 представляет собой галоген, циано, аминокарбонил, C1-6алкил, замещенный циано или аминокарбонилом, или C2-6алкенил, замещенный циано или аминокарбонилом;
(e) R3 представляет собой циано, C1-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(f) R3 представляет собой C1-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(g) R3 представляет собой C2-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(h) R3 представляет собой C2-4алкенил, замещенный циано;
(i) R3 представляет собой этенил, замещенный циано;
(j) R3 представляет собой (E)-2-цианоэтенил.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R4 представляет собой галоген; гидрокси; C1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано или -C(=O)R6; C2-6алкенил, необязательно замещенный одним заместителем, выбранным из галогена, циано или -C(=O)R6; C2-6алкинил, необязательно замещенный одним заместителем, выбранным из галогена, циано или -C(=O)R6; C3-7циклоалкил; C1-6алкилокси; циано; нитро; полигалогенC1-6алкил; полигалогенC1-6алкилокси; аминокарбонил; моно- или ди(C1-4алкил)аминокарбонил; C1-6алкилоксикарбонил; C1-6алкилкарбонил; формил; амино; моно- или ди(C1-4алкил)амино или R7;
(b) R4 представляет собой галоген; гидрокси; C1-6алкил, необязательно замещенный одним заместителем, выбранным из циано; C2-6алкенил, необязательно замещенный циано; C2-6алкинил, необязательно замещенный циано; C3-7циклоалкил; C1-6алкилокси; циано; нитро; трифторметил; аминокарбонил; моно- или ди(C1-4алкил)аминокарбонил; C1-6алкилоксикарбонил; C1-6алкилкарбонил; формил; амино; моно- или ди(C1-4алкил)амино и R7;
(c) R4 представляет собой галоген; гидрокси; C1-6алкил, необязательно замещенный циано; C2-6алкенил, необязательно замещенный циано; C2-6алкинил, необязательно замещенный циано; C1-6алкилокси; циано; нитро; трифторметил; аминокарбонил; моно- или ди(C1-4алкил)аминокарбонил; C1-6алкилоксикарбонил; C1-6алкилкарбонил; формил; амино; моно- или ди(C1-4алкил)амино;
(d) R4 представляет собой галоген, гидрокси, C1-6алкил, C2-6алкенил, C2-6алкинил, C1-6алкилокси, циано, нитро, амино;
(e) R4 представляет собой галоген, гидрокси, C1-4алкил, C1-4алкилокси, циано; или
(f) R4 представляет собой галоген, C1-4алкил, C1-4алкилокси.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R5 представляет собой водород, C1-6алкил, арил, пиридил, тиенил, фуранил;
(b) R5 представляет собой водород, C1-6алкил, арил, пиридил, фуранил; где арил в п.п. (a) и (b) может иметь значения, определенные выше или ниже по тексту заявки.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) Q представляет собой водород, C1-6алкил или -NR9R10;
(b) Q представляет собой водород или -NR9R10;
(c) Q представляет собой водород, амино, моно- или ди-C1-4алкиламино;
(d) Q представляет собой водород или C1-6алкил; или
(e) Q представляет собой водород;
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R6 представляет собой C1-4алкил, амино, моно- или ди(C1-4алкил)амино; в частности
(b) R6 представляет собой C1-4алкил или амино; или
(c) R6 представляет собой C1-4алкил.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R7 представляет собой моноциклический или бициклический, частично насыщенный или ароматический карбоцикл или же моноциклический или бициклический, частично насыщенный или ароматический гетероцикл, где каждая из упомянутых карбоциклических или гетероциклических систем может быть необязательно замещена одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, C1-6алкилкарбонила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, полигалогенC1-6алкила, полигалогенC1-6алкилокси и аминокарбонила; в частности
(b) R7 представляет собой любой из конкретных моноциклических или бициклических, частично насыщенных или ароматических карбоциклов, или же моноциклических или бициклических, частично насыщенных или ароматических гетероциклов, конкретно упомянутых в данном описании, где каждая из указанных карбоциклических или гетероциклических систем может быть необязательно замещена одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, C1-6алкилкарбонила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, полигалогенC1-6алкила, полигалогенC1-6алкилокси и аминокарбонила;
(c) R7a представляет собой моноциклический или бициклический, частично насыщенный или ароматический карбоцикл, или же моноциклический или бициклический, частично насыщенный или ароматический гетероцикл, где каждая из упомянутых карбоциклических или гетероциклических систем может быть необязательно замещена одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, C1-6алкилкарбонила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, полигалогенC1-6алкила, полигалогенC1 6алкилокси и аминокарбонила; в частности
(d) R7a представляет собой любой из конкретных моноциклических или бициклических, частично насыщенных или ароматических карбоциклов, или же моноциклических или бициклических, частично насыщенных или ароматических гетероциклов, конкретно упомянутых в данном описании, где каждая из указанных карбоциклических или гетероциклических систем может быть необязательно замещена одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, C1-6алкилкарбонила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, полигалогенC1-6алкила, полигалогенC1-6алкилокси и аминокарбонила.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) X представляет собой -NR1-, -O-, или -S-;
(b) X представляет собой -NR1- или -O-;
(c) X представляет собой -NH-, -N(C1-4алкил)-, -O-;
(d) X представляет собой -NH-, -N(CH3)-, -O-; или
(e) X представляет собой -NH-, -O-.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R8 представляет собой водород, C1-4алкил или арилC1-4алкил; или
(b) R8 представляет собой водород или C1-4алкил; или
(c) R8 представляет собой водород или метил.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) каждый из R9 и R10 независимо представляет собой водород; C1-6алкил; C1-6алкилкарбонил; C1-6алкилоксикарбонил; моно- или ди(C1-6алкил)аминокарбонил; -CH(=NR11), где каждая из упомянутых выше C1-6алкильных групп может быть необязательно замещена одним или двумя заместителями, каждый из которых независимо выбран из гидрокси, C1-6алкилокси, гидроксиC1-6алкилокси, карбоксила, C1-6алкилоксикарбонила, циано, амино, моно- и ди(C1-4алкил)амино, полигалогенметила, полигалогенметилокси;
(b) каждый из R9 и R10 независимо представляет собой водород; C1-6алкил; C1-6алкилкарбонил или C1-6алкилоксикарбонил;
(c) каждый из R9 и R10 независимо представляет собой водород или C1-6алкил;
(d) R9 и R10 представляют собой водород.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) каждый из R13 и R14 независимо представляет собой C1-6алкил, необязательно замещенный циано, C2-6алкенил, необязательно замещенный циано, C2-6алкинил, необязательно замещенный циано;
(b) каждый из R13 и R14 независимо представляет собой водород или C1-6алкил;
(c) R13 и R14 представляют собой водород.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых R15 представляет собой C1-6алкил, необязательно замещенный циано.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) R16 представляет собой C1-6алкил, необязательно замещенный циано или аминокарбонилом; или в котором
(b) R16 представляет собой C1-6алкил, необязательно замещенный циано.
Другими подгруппами соединений формулы (I) являются такие соединения формулы (I) или любая подгруппа соединений формулы (I), определенных в настоящей заявке, в которых
(a) арил представляет собой фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, моно- или ди(C1-6алкил)аминоC1-6алкила, C1-6алкилкарбонила, C3-7циклоалкила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, полигалогенC1-6алкила, полигалогенC1-6алкилокси, аминокарбонила, фенила, тиенила и пиридила;
(b) арил представляет собой фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, моно- или ди(C1-6алкил)аминоC1-6алкила, C1-6алкилкарбонила, C1-6алкилокси, C1-6алкилоксикарбонила, C1-6алкилтио, циано, нитро, трифторметила, трифторметокси, аминокарбонила, фенила;
(c) арил представляет собой фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, гидрокси, C1-6алкила, гидроксиC1-6алкила, аминоC1-6алкила, моно- или ди(C1-6алкил)аминоC1-6алкила, C1-6алкилкарбонила, C1-6алкилокси, C1-6алкилоксикарбонила, циано, нитро, трифторметила;
(d) арил представляет собой фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, гидрокси, C1-6алкила, C1-6алкилокси, циано, нитро, трифторметила;
Один из вариантов осуществления относится к подгруппе соединений формулы (I), имеющих формулу

их N-оксидам, фармацевтически приемлемым аддитивным солям, четвертичным аммониевым производным или стереохимически изомерным формам, в которых -b1=b2-b3=b4-, R', каждый из R2, R2a, R3, каждый из R4, -A-B-, m, n и Q соответствуют определениям, данным выше, в общем определении соединений формулы (I) или в определениях их различных подгрупп.
Еще один вариант осуществления относится к подгруппе соединений формулы (I), имеющих формулу
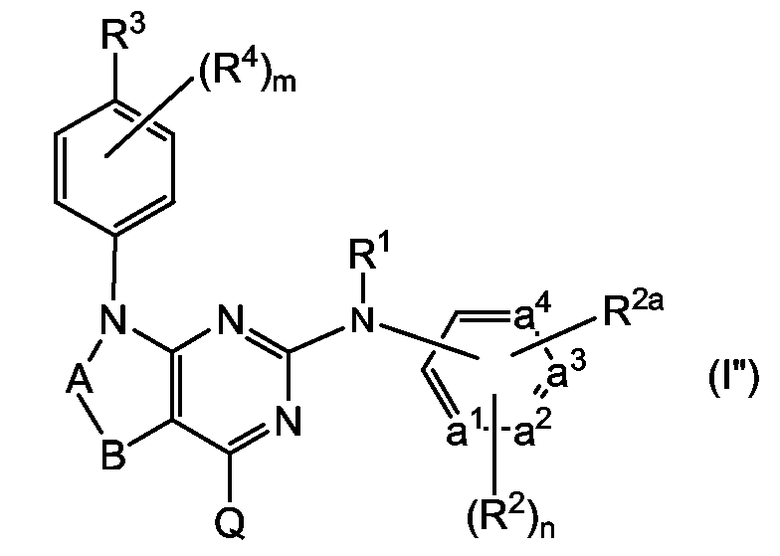
их N-оксидам, фармацевтически приемлемым аддитивным солям, четвертичным аммониевым производным или стереохимически изомерным формам, в которых -a1=a2-a3=a4-, R1, каждый из R2, R2a, R3, каждый из R4, -A-B-, m, n и Q соответствуют определениям, данным выше, в общем определении соединений формулы (I) или в определениях их различных подгрупп.
Другой вариант осуществления относится к подгруппе соединений формулы (I), имеющих формулу
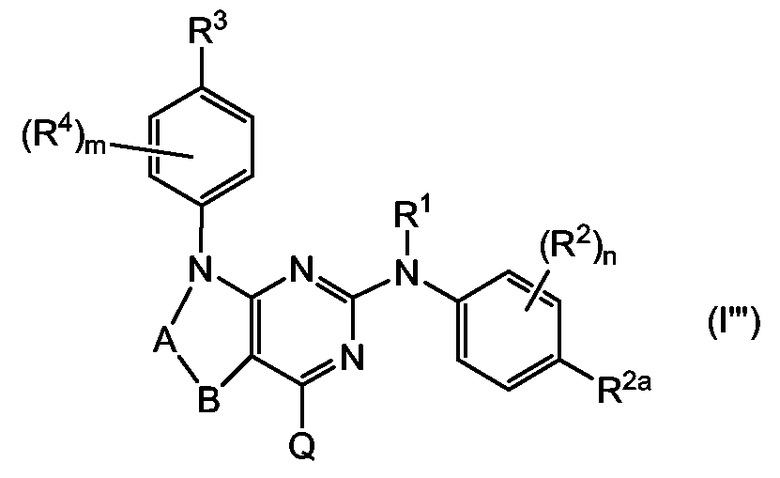
их N-оксидам, фармацевтически приемлемым аддитивным солям, четвертичным аммониевым производным или стереохимически изомерным формам, в которых R1, каждый из R2, R2a, R3, каждый из R4, -A-B-, m, n и Q соответствуют определениям, данным выше, в общем определении соединений формулы (I) или в определениях их различных подгрупп.
Другой вариант осуществления относится к подгруппе соединений формулы (I), имеющих формулу
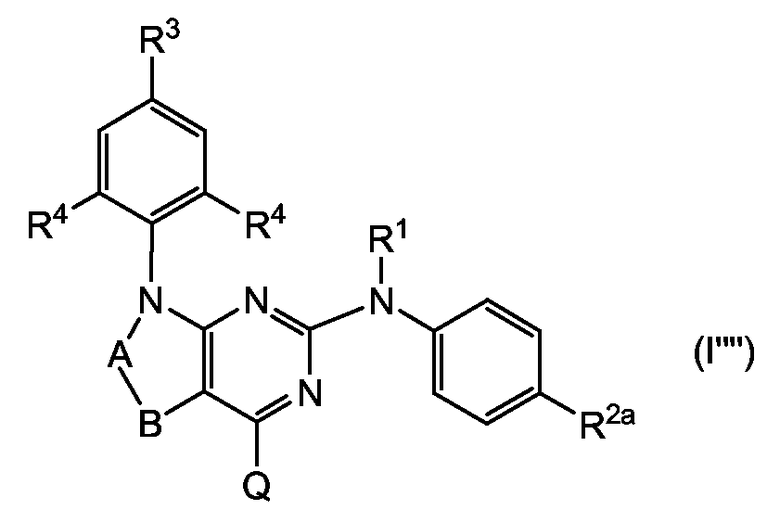
их N-оксидам, фармацевтически приемлемым аддитивным солям, четвертичным аммониевым производным или стереохимически изомерным формам, в которых R1, R2a, R3, каждый из R4, -A-B- и Q соответствуют определениям, данным выше, в общем определении соединений формулы (I) или в определениях их различных подгрупп.
Кроме того, представляющий интерес вариант осуществления изобретения относится к подгруппе соединений формулы (I), имеющих формулу
их N-оксидам, фармацевтически приемлемым аддитивным солям, четвертичным аммониевым производным или стереохимически изомерным формам, в которых R1, R2, R2a, R3, -A-B- и Q соответствуют определениям, данным выше, в общем определении соединений формулы (I) или в определениях их различных подгрупп.
Отдельными подгруппами соединений формул (I), (I'), (I”), (I'''), (I'''') или (I''''') являются такие подгруппы, в которых фрагмент -A-B- представляет собой радикал -CR5=N- (c-1), причем R2a имеет значения, определенные в п.п. (a)-(i), и R3 имеет значения, определенные в п.п.(j)-(t), следующим образом:
(a) R2a представляет собой циано; аминокарбонил; амино; галоген; C1-6алкилокси, где C1-6алкил замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкилоксиC1-6алкил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкинил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; -C(=N-O-R8)-C1-4алкил; R7 или -X-R7;
(b) R2a представляет собой циано; аминокарбонил; амино; галоген; C1-6алкилокси, где C1-6алкил замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; C1-6алкилоксиC1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкенил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкинил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; -C(=N-O-R8)-C1-4алкил; R7 или -X-R7;
(c) R2a представляет собой циано; аминокарбонил; амино; галоген; C1-6алкилокси, где C1-6алкил замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C1-6алкилоксиC1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C2-6алкенил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C2-6алкинил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10;
(d) R2a представляет собой галоген, циано, аминокарбонил, C1-6алкил, замещенный циано или аминокарбонилом, C2-6алкенил, необязательно замещенный циано или аминокарбонилом;
(e) R2a представляет собой галоген, циано, аминокарбонил, C1-6алкил, замещенный циано или аминокарбонилом, или C2-6алкенил, замещенный циано или аминокарбонилом;
(f) R2a представляет собой циано, аминокарбонил, C1-6алкил, замещенный циано, или C2-6алкенил, замещенный циано;
(g) R2a представляет собой циано, аминокарбонил, C1-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(h) R2a представляет собой циано, C1-4алкил, замещенный циано, или C2-4алкенил, замещенный циано; или
(i) R2a представляет собой циано;
(j) R3 представляет собой циано; аминокарбонил; амино; галоген; C1-6алкилокси, где C1-6алкил замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкилоксиC1-6алкил, необязательно замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкинил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7; -C(=N-O-R8)-C1-4алкил; R7 и -X-R7;
(k) R3 представляет собой циано; аминокарбонил; амино; галоген; C1-6алкилокси, где C1-6алкил замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C1-6алкилоксиC1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкенил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; C2-6алкинил, замещенный одним заместителем, выбранным из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила и R7; -C(=N-O-R8)-C1-4алкил; R7 или -X-R7;
(l) R3 представляет собой циано; аминокарбонил; амино; C1-6алкил; галоген; C1-6алкилокси, где C1-6алкил может быть необязательно замещен циано; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; C1-6алкил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C1-6алкил, замещенный гидроксигруппой и вторым заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C1-6алкилоксиC1-6алкил, необязательно замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C2-6алкенил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10; C2-6алкинил, замещенный одним заместителем, выбранным из галогена, циано, -C(=O)-NR9R10;
(m) R3 представляет собой галоген, циано, аминокарбонил, C1-6алкил, необязательно замещенный циано или аминокарбонилом, C2-6алкенил, необязательно замещенный циано или аминокарбонилом;
(n) R3 представляет собой галоген, циано, аминокарбонил, C1-6алкил, замещенный циано или аминокарбонилом, или C2-6алкенил, замещенный циано или аминокарбонилом;
(o) R3 представляет собой циано, C1-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(p) R3 представляет собой C1-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(q) R3 представляет собой C2-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(r) R3 представляет собой C2-4алкенил, замещенный циано;
(s) R3 представляет собой этенил, замещенный циано;
(t) R3 представляет собой (E)-2-цианоэтенил.
Отдельными подгруппами соединений формул (I), (I'), (I”), (I'''), (I'''') или (I''''') являются такие подгруппы, в которых фрагмент -A-B- представляет собой радикал -N=N- (c-2), или в которых фрагмент -A-B- представляет собой радикал формулы -CH2-CH2- (c-3); и в которых
(a) R3 представляет собой C1-6алкил, замещенный циано или аминокарбонилом, или C2-6алкенил, замещенный циано или аминокарбонилом;
(b) R3 представляет собой C2-6алкил, замещенный циано или аминокарбонилом, или C2-6алкенил, замещенный циано или аминокарбонилом;
(c) R3 представляет собой C2-4алкил, замещенный циано или аминокарбонилом, или C2-4алкенил, замещенный циано или аминокарбонилом;
(d) R3 представляет собой C2-6алкил, замещенный циано, или C2-6алкенил, замещенный циано;
(e) R3 представляет собой C2-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(f) R3 представляет собой C2-6алкенил, замещенный циано или аминокарбонилом;
(g) R3 представляет собой C2-4алкенил, замещенный циано или аминокарбонилом;
(h) R3 представляет собой C2-6алкенил, замещенный циано;
(i) R3 представляет собой C2-6алкенил, замещенный циано;
(j) R3 представляет собой этенил, замещенный циано; или в которых
(k) R3 представляет собой (E)-2-цианоэтенил.
Отдельными подгруппами соединений формул (I), (I'), (I”), (I'''), (I'''') или (I''''') являются такие подгруппы, в которых фрагмент -A-B- представляет собой радикал -N=N- (c-2), или в которых фрагмент -A-B- представляет собой радикал формулы -CH2-CH2- (c-3); и в которых
(a) R2a представляет собой циано или аминокарбонил; или в которых
(b) R2a представляет собой циано;
Отдельными подгруппами соединений формул (I), (I'), (I”), (I'''), (I'''') или (I''''') являются такие подгруппы, в которых фрагмент -A-B- представляет собой радикал -N=N- (c-2), или в которых фрагмент -A-B- представляет собой радикал формулы -CH2-CH2- (c-3); и в которых
(a) R3 представляет собой C1-6алкил, замещенный циано или аминокарбонилом, или C2-6алкенил, замещенный циано или аминокарбонилом;
(b) R3 представляет собой C2-6алкил, замещенный циано или аминокарбонилом, или C2-6алкенил, замещенный циано или аминокарбонилом;
(c) R3 представляет собой C2-4алкил, замещенный циано или аминокарбонилом, или C2-4алкенил, замещенный циано или аминокарбонилом;
(d) R3 представляет собой C2-6алкил, замещенный циано, или C2-6алкенил, замещенный циано;
(e) R3 представляет собой C2-4алкил, замещенный циано, или C2-4алкенил, замещенный циано;
(f) R3 представляет собой C2-6алкенил, замещенный циано или аминокарбонилом;
(g) R3 представляет собой C2-4алкенил, замещенный циано или аминокарбонилом;
(h) R3 представляет собой C2-6алкенил, замещенный циано;
(i) R3 представляет собой C2-6алкенил, замещенный циано;
(j) R3 представляет собой этенил, замещенный циано; или в которых
(k) R3 представляет собой (E)-2-цианоэтенил;
причем для каждого из возможных п.п. (a)-(k) R2a представляет собой циано или аминокарбонил; или R2a представляет собой циано.
Соединения формулы (I) могут быть получены взаимодействием промежуточных соединений формулы (II-a) или (II-b) с промежуточными соединениями формулы (III-a) или (III-b). В данной и следующих схемах реакций каждый из заместителей W независимо представляет собой подходящую уходящую группу, например, такую как галоген, например, хлор, бром, йод, ацетатную группу, нитробензоатную группу, азидную группу, арилсульфонильную группу, например, тозилат, брозилат, мезилат, нозилат, трифлат и т.п. Особенный интерес представляют галогены, в частности хлор или бром.
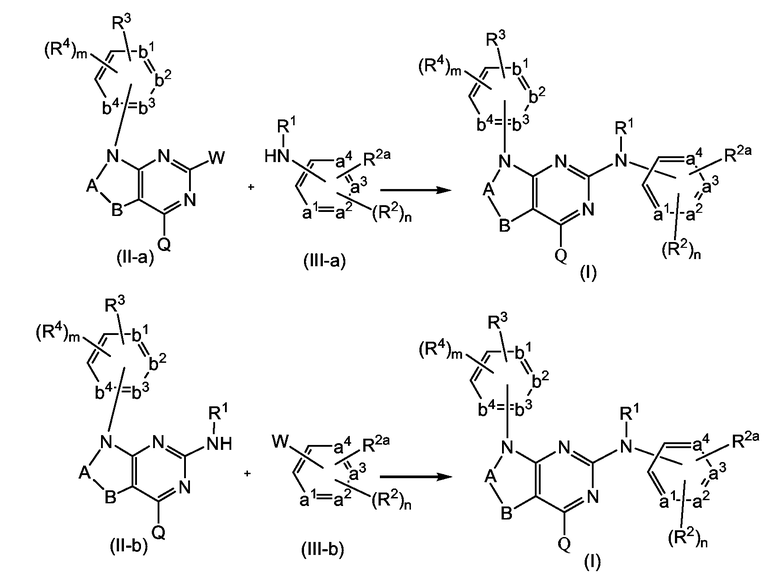
Реакцию пиримидинового производного (II-a) или соответственно (II-b) с амином (III-a) или соответственно с промежуточным соединением (III-b), как правило, проводят в подходящем растворителе. Подходящими растворителями являются, например, спирты, такие как, например, этанол, 2-пропанол; биполярные апротонные растворители, такие как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, 1-метил-2-пирролидинон; простые эфиры, такие как тетрагидрофуран, 1,4-диоксан, монометиловый эфир пропиленгликоля. Эти реакции могут проводиться в нейтральной среде или, что предпочтительно, в кислой среде, как правило, при повышенных температурах и при перемешивании. Кислая среда может быть получена добавлением определенного количества подходящей кислоты, например камфорсульфоновой кислоты, или применением кислотных растворителей, например хлористоводородной кислоты, или в спирте, таком как 1- или 2-пропанол или простом эфире, таком как тетрагидрофуран.
Соединения формулы (I) также могут быть получены взаимодействием бициклического производного (IV) с соединением (V), как изображено на следующей схеме.
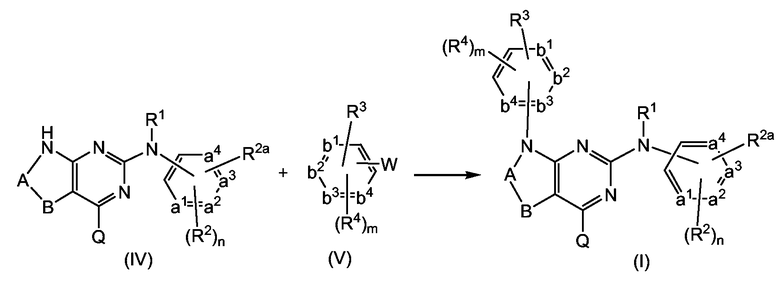
В данной схеме реакции заместитель W представляет собой подходящую уходящую группу, как описано выше. Взаимодействие проводят в условиях, подобных описанным выше, для взаимодействия (II-a) с (III-a) и (II-b) с (III-b).
Соединения формулы (I-a), являющиеся соединениями формулы (I), в которых -A-B- представляет собой -CH2-CH2-, могут быть получены взаимодействием пиримидинового производного (VI), в котором каждая из групп W представляет собой определенную выше уходящую группу, и предпочтительно представляет собой хлор или бром, с ароматическим амином формулы (VII).
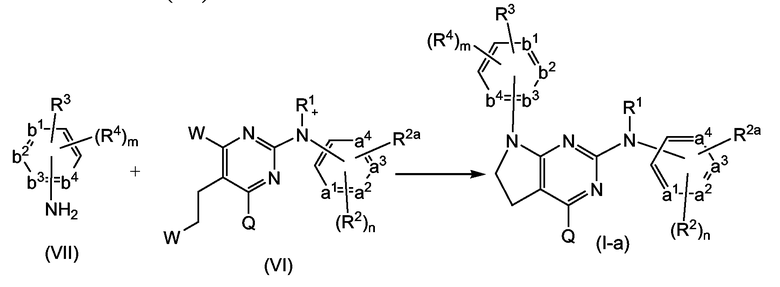
Соединения формулы (I-a) могут быть превращены в соответствующие соединения (I-b), являющиеся соединениями формулы (I), в которых -A-B- представляет собой -CH=CH-, с помощью реакции элиминирования, в частности элиминированием водорода из соответствующего насыщенного аналога (I-a), с применением подходящего дегидрирующего реагента, такого как 2,3-дихлор-5,6-дициано-1,4-бензохинона (DDQ).
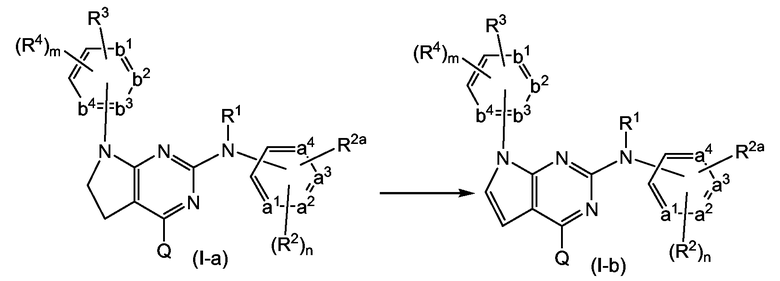
Соединения формулы (I-c), являющиеся соединениями формулы (I), в которых -A-B- представляет собой -CR5=N-, могут быть получены взаимодействием аминопиримидина (VIII) с ортоформиатом R5C(OEt)3 или альдегидом R5CH=O в присутствии мягкого окислителя, такого как нитробензол.
Соединения формулы (I-c-1), являющиеся соединениями формулы (I), в которых -A-B- представляет собой -CR5=N-, где R5 означает аминогруппу, могут быть получены взаимодействием аминопиримидина (VIII) с цианогалогенидом, в частности с бромистым цианом. Взаимодействие можно проводить в подходящем растворителе, таком как спирт, например, метанол или этанол, или простой эфир, например, ТГФ или диоксан, или их смесях.

Соединения формулы (I-c-1) могут подвергаться моно- или бис-алкилированию с получением соответствующих соединений, в которых R5 представляет собой моно- или ди(C1-4алкил)амино, с применением реагента формулы C1-4алкил-W в качестве алкилирующего средства.
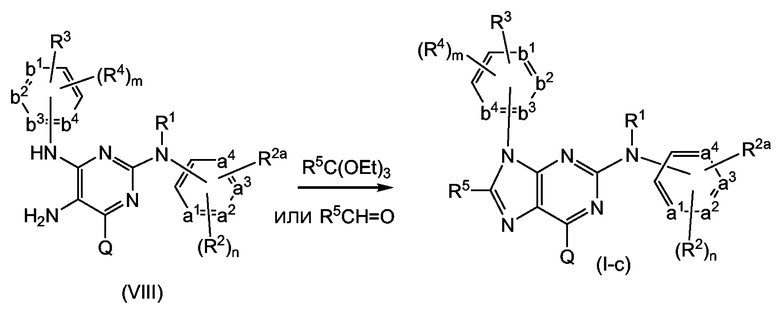
Соединения формулы (I-d), являющиеся соединениями формулы (I), в которых фрагмент -A-B- представляет собой -N=N-, могут быть получены взаимодействием аминопиримидина (VIII) с диазотирующим реагентом, таким как нитрит, в частности нитрит щелочного металла, например нитрит натрия или калия, в присутствии уксусной кислоты.
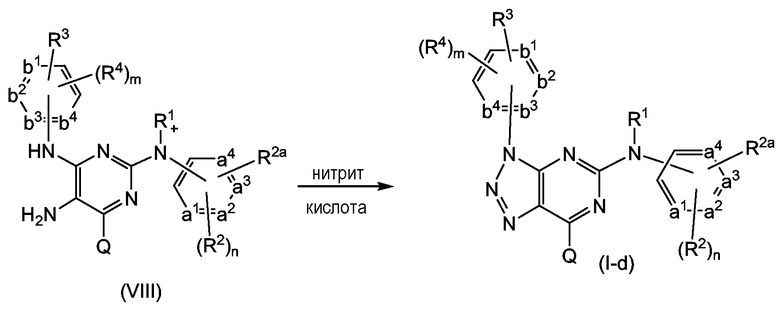
Соединения формулы (I-e) или (I-f), являющиеся соединениями формулы (I), в которых -A-B- представляет собой -CS-NH- или, соответственно, -CO-NH-, могут быть получены взаимодействием аминопиримидина (VIII) c производным тиофосгена (W1)2C=S, которое приводит к получению соединений (I-e), или производным фосгена (W1)2C=O, которое приводит к получению соединений (I-f). В этих схемах реакций каждый из заместителей W1 независимо означает уходящую группу, например, относящуюся к числу групп W, описанных ранее, предпочтительно W1 представляет собой галоген, в частности, хлор.
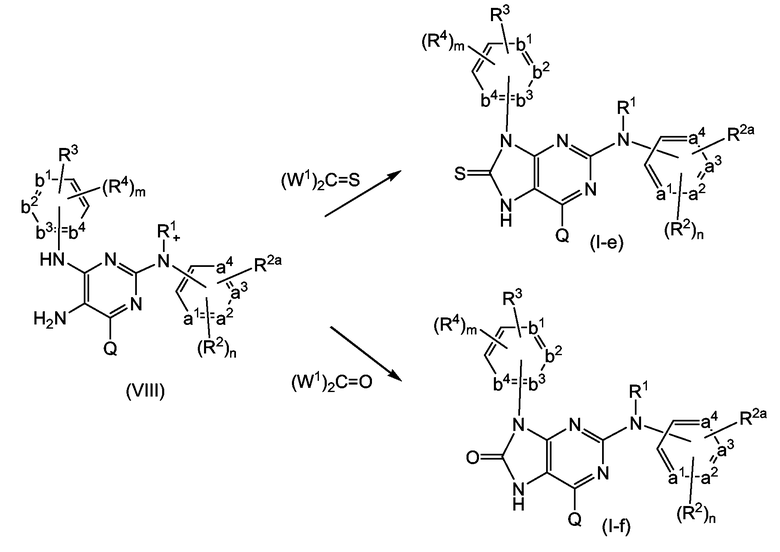
В любой из схем реакций, приведенных выше или ниже, каждый из радикалов R2, R2a, R3 или R4 может соответствовать данным выше определениям, или может являться группой-предшественником, которую превращают в желаемую группу R2, R2a, R3 или R4. Например, соединения формулы (I), в которых R3 означает C2-6алкенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7, могут быть получены, исходя из аналогов этих соединений, в которых R3 является сложноэфирной группой, как, например, C1-6алкилоксикарбонильной группой, которую восстанавливают до гидроксиметиленовой группы, например, комплексом гидрида металла, таким как литийалюминийгидрид, которую затем окисляют до альдегидной группы, с использованием мягкого окислителя (например, MnO2). Затем альдегидную группу превращают в алкенильную или замещенную алкенильную группу, используя реакцию Виттига или реакцию Виттига-Хорнера. В первом случае используют реактив Виттига, как, например, трифенилфосфонийлид. Реакцию Виттига проводят в подходящем инертном растворителе, таком как простой эфир, используя в качестве исходных соединений трифенилфосфин и, например, галогенацетонитрил (например, хлорацетонитрил) или галогензамещенный эфир уксусной кислоты формулы Rx-CH(Halo)-COORy, где Rx и Ry независимо являются C1-6алкильными, C1-4алкильными или C1-2алкильными группами. Реакцию Виттига-Хорнера проводят с использованием фосфоната, например, такого, как реагент формулы ди(C1-6алкилокси)-P(=O)-CH(Rx)-COORy или ди(C1-6алкилокси)-P(=O)-CH(Rx)-CN в присутствии основания, предпочтительно, сильного основания, например алкоксида щелочного металла, такого как метилат, этилат или трет-бутилат натрия или калия, в простом эфире, например ТГФ или диоксане, апротонном органическом растворителе, например ДМФА, ДМА, ГМФТ, ДМСО и т.п. Подобная последовательность реакций может быть осуществлена для таких соединений формулы (I), в которых R2, R2a или R4 представляют собой замещенную C2-6алкенильную группу, определенную выше.
Как описано далее, любые превращения промежуточных соединений также могут осуществляться для аналогов соединений формулы (I), в которых R2, R2a, R3 или R4 является группой-предшественником. Например, что касается реакций (III-b) или (V-b) с (XIII) с получением (III-c) или (V-c), превращений (III-f) в (III-c), (V-f) в (V-c), (III-b) в (III-f) и т.д., то все эти взаимодействия, описанные далее более подробно, также могут осуществляться в отношении аналогов исходных соединений, в которых группа -NHR1 является группой формулы

или группой формулы
Далее соединения формулы (I) могут быть получены превращением соединений формулы (I) друг в друга, в соответствии с известными в технике реакциями.
Соединения формулы (I) могут быть превращены в соответствующие формы N-оксидов с использованием известных в технике методик превращения третичного азота в его N-оксидную форму. Указанная реакция получения N-оксидов может проводиться, как правило, путем взаимодействия исходного соединения формулы (I) с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных и щелочноземельных металлов, например пероксид натрия, пероксид калия; подходящие органические пероксиды могут включать пероксикислоты, например, такие как пероксибензойная кислота или галогензамещенная пероксибензойная кислота, например, 3-хлорпероксибензойная кислота, пероксиалкановые кислоты, например пероксиуксусную кислоту, алкилгидропероксиды, например, трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие спирты, например, этанол и т.п., углеводороды, например, толуол, кетоны, например 2-бутанон, галогенированные углеводороды, например, дихлорметан, и смеси подобных растворителей.
Соединения формулы (I), где R2, R2a, R3 или R4 представляют собой C2-6алкенил, замещенный аминокарбонилом, могут быть превращены в соединения формулы (I), в которых R2, R2a, R3 или R4 представляют собой C2-6алкенил, замещенный циано, взаимодействием с POCl3.
Соединения формулы (I), в которых m равняется нулю, могут быть превращены в соединения формулы (I), в которых m отлично от нуля, и R4 представляет собой галоген, взаимодействием с походящим галогенирующим реагентом, таким как, например, N-хлорсукцинимид или N-бромсукцинимид, или их комбинацией в присутствии подходящего растворителя, например, такого как уксусная кислота.
Соединения формулы (I), в которых R3 представляет собой галоген, могут быть превращены в соединения формулы (I), в которых R3 представляет собой C2-6алкенил, замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7, взаимодействием с соответствующим C2-6алкеном, замещенным одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7, в присутствии подходящего основания, такого как, например, N,N-диэтилэтанамин, подходящего катализатора, как, например, ацетат палладия, в присутствии трифенилфосфина и подходящего растворителя, например N,N-диметилформамида.
Соединения формулы (I), в которых R2a представляет собой галоген, могут быть превращены в соединения формулы (I), в которых R2a представляет собой C2-6алкенил, замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7, взаимодействием с соответствующим C2-6алкеном, замещенным одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, NR9R10, -C(=O)-NR9R10, -C(=O)-C1-6алкила или R7, в присутствии подходящего основания, такого как, например, N,N-диэтилэтанамин, подходящего катализатора, как, например, ацетат палладия, в присутствии трифенилфосфина и подходящего растворителя, например N,N-диметилформамида.
Соединения формулы (I), в которых R1 представляет собой C1-6алкилоксикарбонил, могут быть превращены в соединения формулы (I), где R1 представляет собой водород, взаимодействием с подходящим основанием, как, например, гидроксидом или метилатом натрия. Если R1 представляет собой трет-бутоксикарбонил, соответствующие соединения, где R1 представляет собой водород, могут быть получены обработкой трифторуксусной кислотой.
Некоторые из соединений формулы (I) и некоторые из промежуточных соединений по настоящему изобретению могут содержать асимметрический атом углерода. Чистые стереохимически изомерные формы указанных соединений и промежуточных соединений могут быть получены с применением известных в технике методик. Например, диастереомеры могут быть разделены физическими методами, такими как селективная кристаллизация или хроматографические методики, например, противоточное распределение, жидкостная хроматография и тому подобные методики. Энантиомеры могут быть получены из рацемических смесей, во-первых, превращением указанных рацемических смесей с помощью подходящих реагентов, например хиральных кислот, в смеси диастереомерных солей соединений; затем физического разделения указанных смесей диастереомерных солей или соединений с помощью, например, селективной кристаллизации или хроматографических методик, например жидкостной хроматографии и подобных способов; и, наконец, превращением указанных разделенных диастереомерных солей или соединений в соответствующие энантиомеры. Чистые стереохимически изомерные формы также могут быть получены из чистых стереохимически изомерных форм подходящих промежуточных соединений и исходных соединений, при условии, что промежуточные реакции протекают стереоспецифично.
Альтернативный способ разделения энантиомерных форм соединений формулы (I) и промежуточных соединений включает жидкостную хроматографию, в частности жидкостную хроматографию с использованием хиральной неподвижной фазы.
Некоторые из промежуточных соединений и исходных веществ являются известными соединениями и могут быть коммерчески доступны или могут быть получены в соответствии с известными в технике методиками.
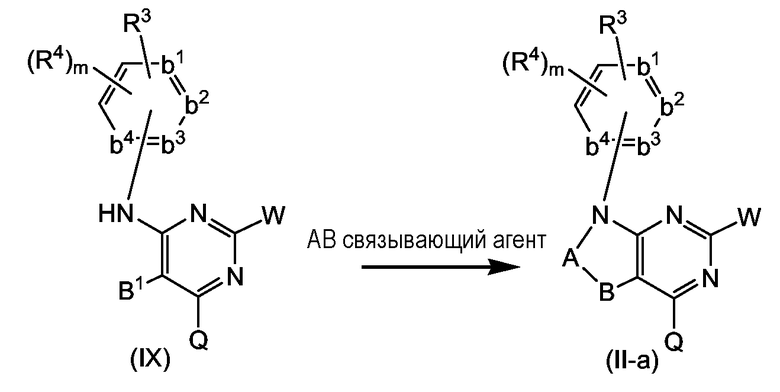
Промежуточные соединения формулы (II-a) могут быть получены, как показано на следующей схеме реакции. На этой схеме W представляет собой подходящую уходящую группу, например, одну из групп W, описанных выше, или группу-предшественника уходящей группы, которая может быть без труда превращена в уходящую группу, например гидроксигруппа или защищенная гидроксигруппа, реакцией с галогенирующим реагентом. B1 представляет собой предшественника группы B, как, например, аминогруппу или группу CH2-CH2-W. Связывающий агент -A-B- может быть любым из агентов, упомянутых выше, в связи с получением соединений (I-a), (I-c), (I-d), (I-e) и (I-f). При получении (II-a) могут применяться те же самые или аналогичные условия реакции, которые описаны для получения соединений, упомянутых в предыдущем предложении.
Аналогичным образом промежуточные соединения (II-b) могут быть получены, исходя из пиримидина (X), как показано на следующей схеме:
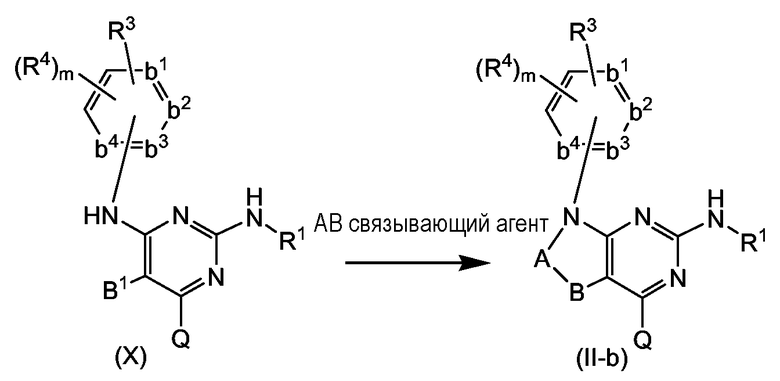
В показанной выше реакции аминогруппа может быть или не быть защищена подходящей защитной группой, например ацетилом, трифторацетилом, бензилом, бутилоксикарбонилом, бензилоксикарбонилом и подобными N-защитными группами.
Промежуточные соединения формулы (III-a), где R1 представляет собой водород, причем указанные промежуточные соединения отображаются формулой (III-a'), или промежуточные соединения формулы (VII) могут быть получены взаимодействием промежуточных соединений формулы (XI) или (XII) с подходящим восстановителем, например Fe в присутствии NH4Cl и подходящего растворителя, как, например, тетрагидрофуран, H2O и спирт, например метанол и т.п. Промежуточные соединения формулы (III-a') могут быть превращены в промежуточные соединения формулы (III-a), в которых R1 отличается от водорода, реакцией N-алкилирования с реагентом формулы R1-W, где W соответствует определению, данному выше.
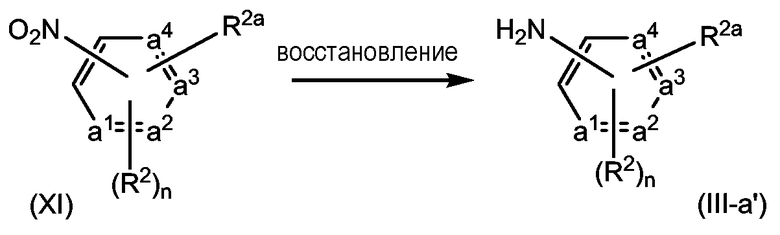
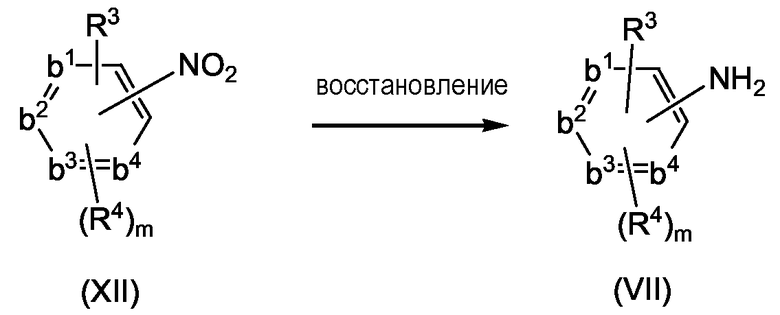
Промежуточные соединения формул (III-b) или (V) являются либо коммерчески доступными, либо могут быть получены простым способом, например превращением гидроксигруппы, входящей в соответствующие промежуточные соединения, в группу W, например реакцией с галогенирующим реагентом (например, POCl3, SOCl2, PCl3 и т.п.).
Промежуточные соединения формулы (III-a), в которой R2a представляет собой C2-6алкил, замещенный циано, и R1 представляет собой водород, причем указанные промежуточные соединения отображаются формулой (III-a-1), могут быть получены взаимодействием промежуточного соединения формулы (XI-a) с Pd/C в присутствии подходящего растворителя, такого как спирт, например, этанол и т.п. Аналогично промежуточные соединения формулы (XII-a) могут быть превращены в промежуточные соединения формулы (VII-a), являющиеся промежуточными соединениями формулы (VII), в которых R2a представляет собой C2-6алкил, замещенный циано.
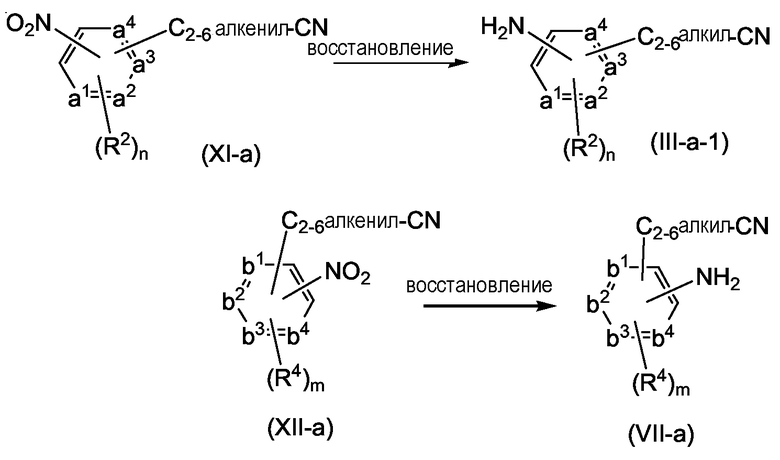
Промежуточные соединения формул (III-a) или (VII), где R2a или R3 представляют собой галоген, причем указанные промежуточные соединения отображаются формулами (III-a-2) и (VII-b), могут быть превращены в промежуточные соединения формул (III-a-3) и (VII-c) соответственно, где R2a или соответственно R3 представляют собой C2-6алкенил, замещенный -C(=O)-NR9R10, взаимодействием исходных промежуточных соединений с промежуточным соединением формулы (XIII) в присутствии Pd(OAc)2, P(o-Tol)3, подходящего основания, например N,N-диэтилэтанамина, и подходящего растворителя например CH3CN.
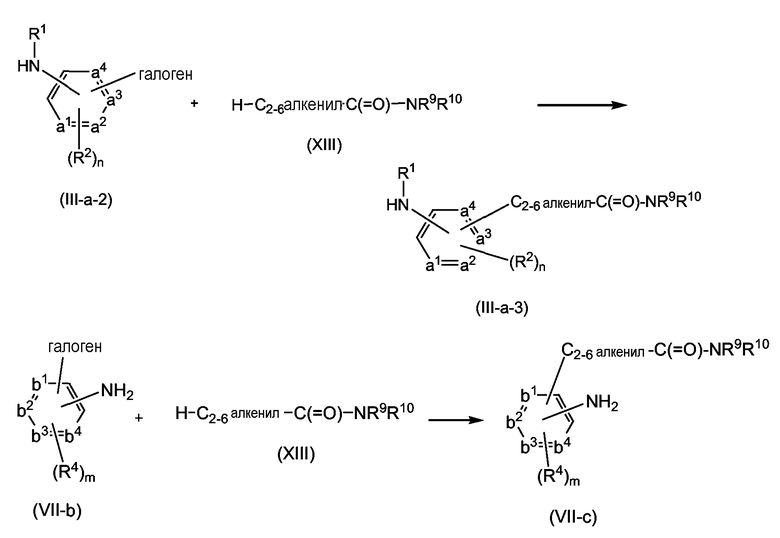
Промежуточные соединения формул (III-a-3) и (VII-c) также могут быть получены взаимодействием промежуточных соединений формул (III-a-4) или (VII-d) с H-NR9R10 в присутствии оксалилхлорида и подходящего растворителя, как, например, N,N-диметилформамид, CH2Cl2 и тетрагидрофурана.
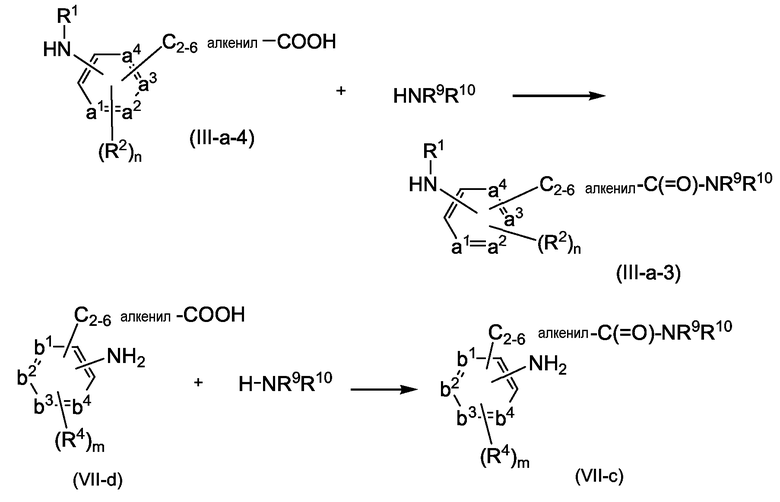
Промежуточные соединения формул (III-a-4) и (VII-d) могут быть получены взаимодействием промежуточных соединений формул (III-a-2) и (VII-b) с H-C2-6алкенил-C(=O)-OH в присутствии Pd(OAc)2, P(o-Tol)3, подходящего основания, как, например, N,N-диэтилэтанамин, и подходящего растворителя, например CH3-CN.
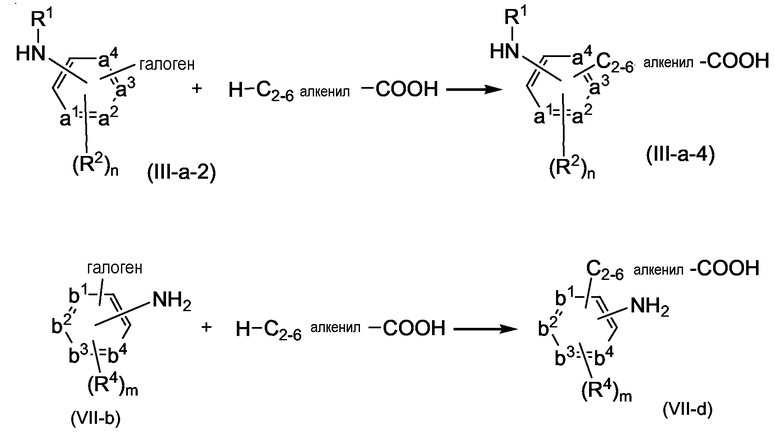
Промежуточные соединения формул (III-a-2) и (VII-b) также могут быть превращены в промежуточные соединения формул (III-a) или (VII), в которых R2a и соответственно R3 представляют собой C2-6алкенил, замещенный CN, причем указанные промежуточные соединения отображаются формулами (III-a-5) и (VII-e), реакцией с H-C2-6алкенил-CN в присутствии Pd(OAc)2, P(o-Tol)3, подходящего основания, как, например, N,N-диэтилэтанамин, и подходящего растворителя, например CH3-CN.
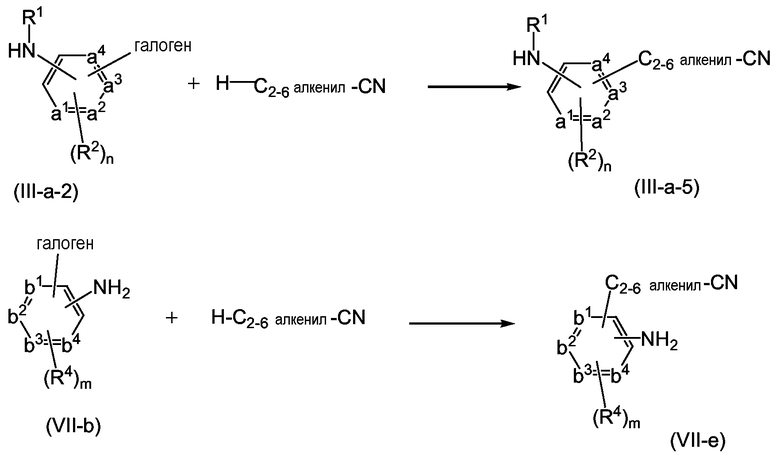
Промежуточные соединения формулы (XIII) могут быть получены взаимодействием промежуточного соединения формулы (XIII'), в котором W представляет собой подходящую уходящую группу из числа определенных выше, и в частности галоген, например хлор, с H-NR9R10 в присутствии подходящего растворителя, например диэтилового эфира, и тетрагидрофурана.
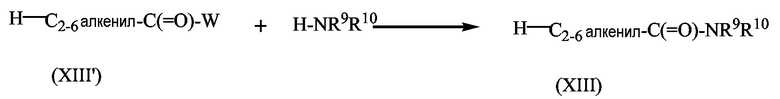
Промежуточные соединения формул (XI) или (XII), в которых R2a и соответственно R3 представляют собой циановинил, причем указанные промежуточные соединения отображаются формулами (XI-a) и (XII-a), могут быть получены взаимодействием промежуточных соединений формулы (XV) или соответственно (XVI) с диэтилцианометилфосфонатом в присутствии подходящего основания, как, например, NaOCH3, и подходящего растворителя, например тетрагидрофурана.
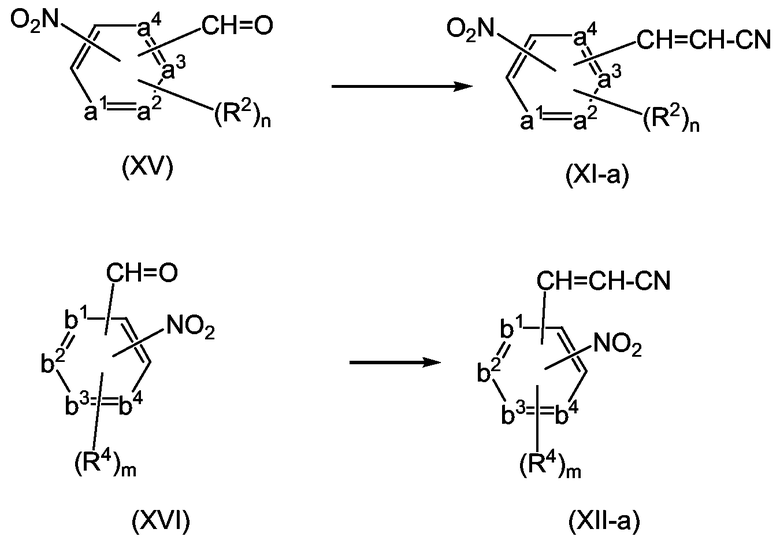
Промежуточные соединения формул (XI) или (XII), в которых R2a или соответственно R3 представляют собой -C(CH3)=CH-CN, причем указанные промежуточные соединения отображаются формулами (XI-b) и (XII-b), могут быть получены взаимодействием промежуточных соединений формулы (XV') или соответственно (XVI') с диэтилцианометилфосфонатом в присутствии подходящего основания, как, например, NaOCH3, и подходящего растворителя, например тетрагидрофурана.
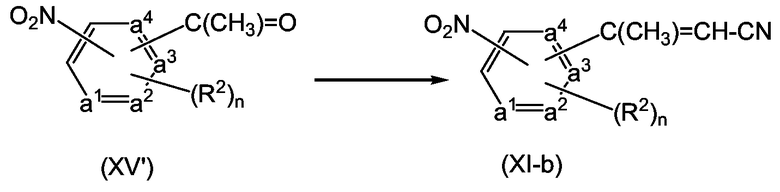
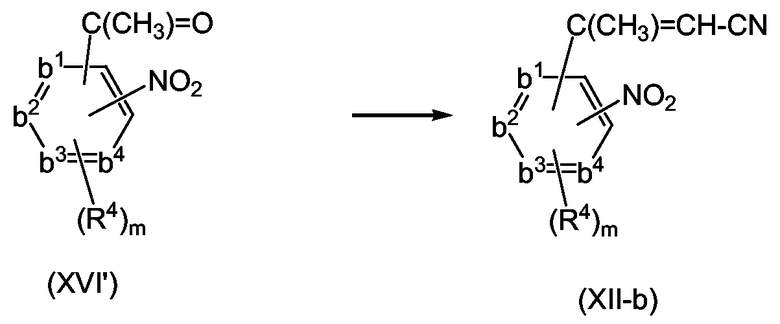
Промежуточные соединения формул (XV) и (XVI) могут быть получены взаимодействием промежуточных соединений формул (XVII) или соответственно (XVIII) с подходящим окислителем, таким как, например, MnO2, в присутствии подходящего растворителя, такого как кетон, например ацетон, простой эфир, например ТГФ или диоксан, галогенированный углеводород, например дихлорметан или хлороформ.
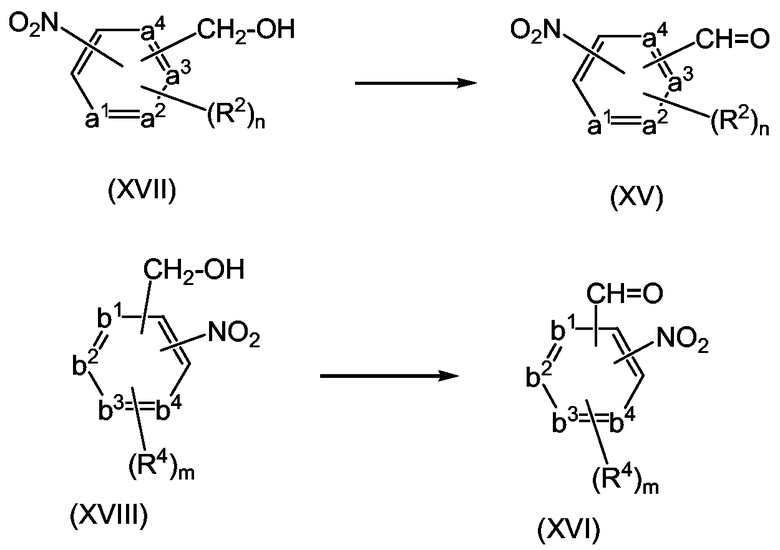
Промежуточные соединения формул (XVII) и (XVIII) могут быть получены взаимодействием промежуточных соединений формул (XIX) или соответственно (XX) с NaBH4 в присутствии этилхлорформиата, подходящего основания, как, например, N,N-диэтилэтанамин, и подходящего растворителя, как, например, тетрагидрофуран.
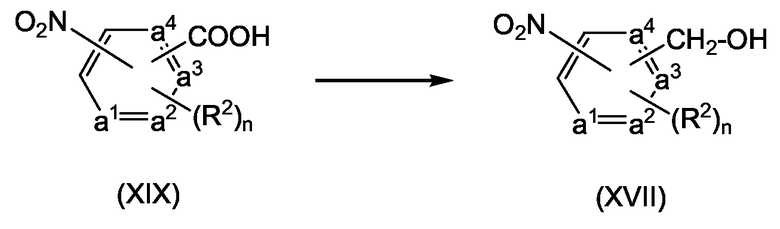
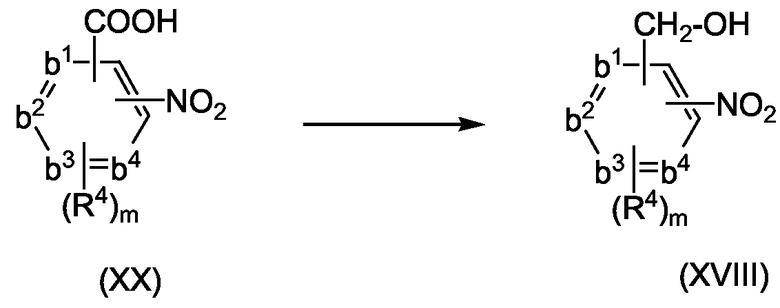
Промежуточные соединения формул (XI) и (XII), в которых R2a или соответственно R3 представляет собой гидрокси, причем указанные промежуточные соединения отображаются формулами (XI-c) или соответственно (XII-c) могут быть превращены в промежуточные соединения формул (XI) или соответственно (XII), в которых R2a или соответственно R3 представляет собой C1-6алкилокси, где C1-6алкил может быть необязательно замещен циано, причем указанные R2a или соответственно R3 представлены символом P, и указанные промежуточные соединения отображены формулами (XI-d) или соответственно (XII-d), взаимодействием с промежуточным соединением формулы (XXI), в котором W представляет собой подходящую уходящую группу из числа упомянутых выше уходящих групп, и в частности является галогеном, например хлором и т.д., необязательно в присутствии катализатора, например йодида щелочного металла, например NaI или KI, и, кроме этого, необязательно в присутствии подходящего основания, такого как карбонат щелочного металла, например K2CO3, и подходящего растворителя, такого как кетон, например ацетон, простой эфир, например ТГФ, диоксан, галогенированный углеводород, например хлороформ, дихлорметан.
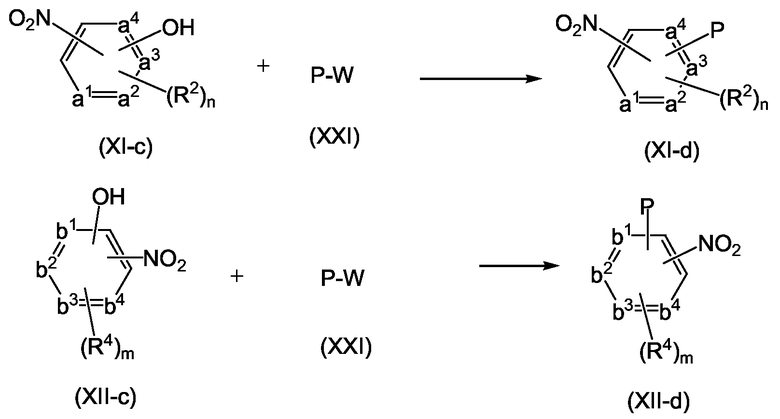
Промежуточные соединения формул (XI) и (XII) могут быть получены взаимодействием промежуточного соединения формулы (XXII) или соответственно (XXIII) с NaNO3 в присутствии CH3SO3H.
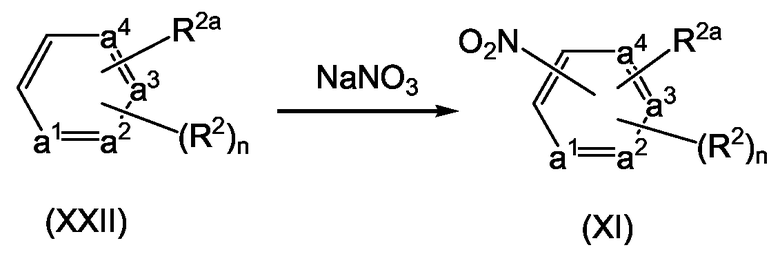
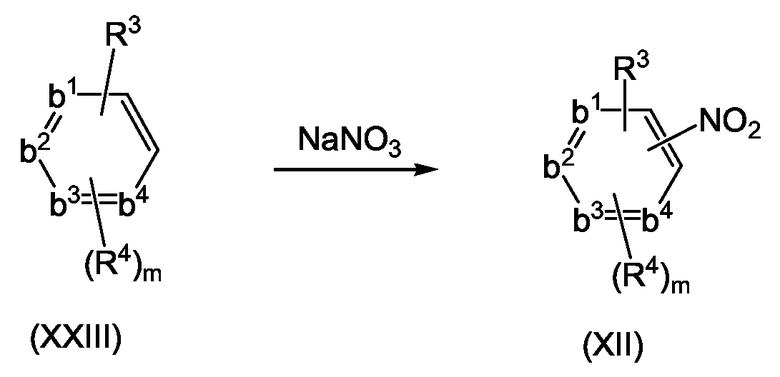
Промежуточные соединения формулы (IV) могут быть получены взаимодействием промежуточного соединения формулы (XXIV), где W соответствует описанному выше, с (III-a).
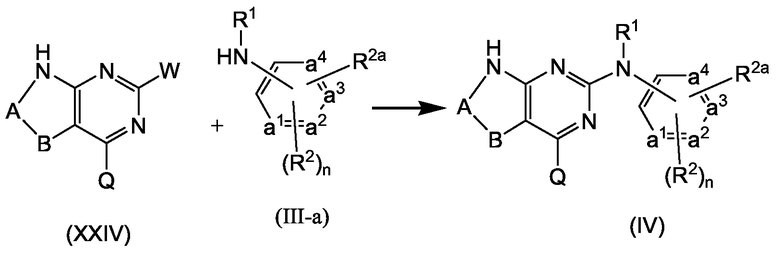
Промежуточные соединения (XXIV) являются либо коммерчески доступными, либо могут быть получены с использованием связывающего реагента -A-B-, как описано выше в реакциях превращения (IX) в (II-a) и (X) в (II-b).
Соединения формулы (I) демонстрируют антиретровирусные свойства (способность ингибировать обратную транскриптазу), в частности против вируса иммунодефицита человека (ВИЧ), который является этиологическим агентом синдрома приобретенного иммунодефицита (СПИД) у людей. Вирус ВИЧ заражает преимущественно клетки T-4 человека и разрушает их или изменяет их нормальную деятельность, в частности координирование иммунной системы. В результате у инфицированного пациента наблюдается постоянное уменьшение количества клеток T-4, которые, кроме того, ведут себя аномально. Следовательно, защитная иммунологическая система не способна бороться с инфекциями и новообразованиями, и ВИЧ-инфицированный субъект обычно умирает вследствие условно-патогенных инфекций, таких как пневмония, или от рака. Другие состояния, связанные с ВИЧ-инфекцией, включают тромбоцитопению, саркому Капоши и инфекцию центральной нервной системы, характеризующуюся прогрессирующей демиелинизацией, и приводящую к деменции и таким симптомам, как прогрессирующая дизартрия, атаксия и дезориентация. Кроме того, ВИЧ-инфекцию связывали с периферической нейропатией, прогрессирующей генерализованной лимфоаденопатией (PGL) и СПИД-ассоциированным комплексом (ARC).
Соединения по настоящему изобретению также демонстрируют активность против (мульти) устойчивых к лекарственным препаратам штаммов ВИЧ, в частности (мульти) устойчивым штаммов ВИЧ-1, более конкретно, соединения по настоящему изобретению проявляют активность против штаммов ВИЧ, особенно штаммов ВИЧ-1, которые обладают приобретенной устойчивостью к одному или нескольким известным в технике ненуклеозидным ингибиторам обратной транскриптазы. Известными в технике ненуклеозидными ингибиторами обратной транскриптазы являются такие ненуклеозидные ингибиторы обратной транскриптазы, которые отличаются от соединений по настоящему изобретению и известны специалистам в данной области техники, в частности коммерческие ненуклеозидные ингибиторы обратной транскриптазы. Кроме этого, соединения по настоящему изобретению не обладают или обладают небольшим сродством к связыванию с человеческим α-1 кислым гликопротеином; человеческий α-1 кислый гликопротеин не влияет на активность соединений по настоящему изобретению против ВИЧ или влияет лишь в слабой степени.
Благодаря своим антиретровирусным свойствам, в частности анти-ВИЧ свойствам, особенно анти-ВИЧ-1 активности, соединения формулы (I), их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные аммониевые производные и стереохимически изомерные формы применимы в лечении пациентов, инфицированных ВИЧ, а также для профилактики этих инфекций. В основном соединения по настоящему изобретению могут применяться в лечении теплокровных животных, инфицированных вирусами, существование которых опосредовано или зависит от фермента обратной транскриптазы. Состояния, которые могут быть предотвращены или подвергнуты лечению соединениями по настоящему изобретению, в особенности состояния, связанные с ВИЧ и другими патогенными ретровирусами, включают СПИД, СПИД-ассоциированный комплекс (ARC), прогрессирующую генерализованную лимфаденопатию (PGL), а также хронические заболевания центральной нервной системы, вызванные ретровирусами, как, например, деменция и рассеянный склероз, опосредованные ВИЧ.
Следовательно, соединения по настоящему изобретению или любая их подгруппа могут применяться в качестве лекарственных средств против указанных выше состояний. Указанное применение в качестве лекарственных средств или способа лечения включает введение ВИЧ-инфицированным субъектам соединений в количестве, эффективном для борьбы с состояниями, связанными с ВИЧ и другими патогенными ретровирусами, в особенности ВИЧ-1. В частности, соединения формулы (I) могут применяться в производстве лекарственного средства для лечения или предотвращения ВИЧ-инфекций.
Ввиду указанной применимости соединений формулы (I) разработан способ лечения теплокровных животных, включая человека, страдающих от вирусных инфекций, в особенности ВИЧ-инфекций, или способ предотвращения таких инфекций у теплокровных животных, включая людей. Указанный способ включает введение, предпочтительно пероральное введение, эффективного количества соединения формулы (I), его N-оксидной формы, фармацевтически приемлемой аддитивной соли, четвертичного аммониевого производного или возможной стереоизомерной формы теплокровным животным, включая людей.
Настоящее изобретение также относится к композициям, предназначенным для лечения вирусных инфекций, включающим терапевтически эффективное количество соединения формулы (I), а также фармацевтически приемлемый носитель или разбавитель.
Соединения по настоящему изобретению или относящиеся к любой их подгруппе могут быть включены в состав различных лекарственных форм для целей введения. В качестве подходящих композиций могут быть упомянуты все композиции, которые обычно применяются для системного введения лекарственных средств. Для получения фармацевтических композиций по настоящему изобретению эффективное количество конкретного соединения, необязательно в форме аддитивной соли, взятого в качестве действующего ингредиента, объединяют в однородную смесь с фармацевтически приемлемым носителем, который может иметь большое разнообразие форм в зависимости от желательной для введения формы препарата. Эти фармацевтические композиции предпочтительны в виде лекарственных форм разовой дозировки, удобных, в частности, для введения перорально, ректально, через кожу или с помощью парентеральной инъекции. Например, при получении композиции в виде лекарственной формы для перорального введения может применяться любая из обычных фармацевтических сред, как, например, вода, гликоли, масла, спирты и т.п., в случае жидких препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, смазывающие средства, связующие вещества, дезинтегрирующие средства и т.п., в случае порошков, пилюль, капсул и таблеток. Благодаря легкости введения, таблетки и капсулы представляют собой наиболее предпочтительные лекарственные формы для разовой пероральной дозировки, в случае которой, очевидно, применяются твердые фармацевтические носители. Для парентеральных композиций носитель обычно будет включать стерильную воду, по меньшей мере, в качестве основного компонента, хотя могут включаться и иные ингредиенты, например, для улучшения растворимости. Например, могут быть приготовлены растворы для инъекций, в которых носитель включает солевой раствор, раствор глюкозы или смесь солевого раствора и раствора глюкозы. Также могут быть получены пригодные для инъекции суспензии, и в этом случае могут применяться подходящие жидкие носители, суспендирующие агенты и т.п. Также в объем изобретения включены препараты в твердой форме, которые предназначены для превращения в жидкие формы препаратов незадолго до их использования. В композициях, пригодных для введения через кожу, носитель необязательно включает средство для улучшения проникания и/или подходящее смачивающее средство, необязательно объединенное с подходящими добавками любой природы в небольших количествах, причем эти добавки не оказывают заметного вредного воздействия на кожу. Указанные добавки могут облегчить нанесение на кожу и/или могут быть полезными для получения желаемых композиций. Эти композиции могут вводиться разными путями, например, в виде трансдермальных пластырей, точечно или в виде мазей.
Кроме того, соединения по настоящему изобретению также могут вводиться ингаляцией или инсуффляцией с применением способов и составов, используемых в технике для введения подобными путями. Такими способами соединения по настоящему изобретению, как правило, вводят в легкие, в форме раствора, суспензии или сухого порошка. Для введения соединений по настоящему изобретению подходит любая система, разработанная для доставки растворов, суспензий или сухих порошков с помощью пероральной или назальной ингаляции или инсуффляции.
Для улучшения растворимости соединений формулы (I) в композиции могут быть включены подходящие ингредиенты, например циклодекстрины. Подходящими циклодекстринами являются α-, β-, γ-циклодекстрины или их простые эфиры, или смешанные простые эфиры, в которых одна или несколько гидроксигрупп ангидроглюкозных единиц циклодекстрина замещены C1-6алкилом, в частности метилом, этилом или изопропилом, например β-CD, случайным образом метилированным гидроксиC1-6алкилом, в частности гидроксиэтилом, гидроксипропилом или гидроксибутилом; карбоксиC1-6алкилом, в частности карбоксиметилом или карбоксиэтилом; C1-6алкилкарбонилом, в частности ацетилом. Особенно заслуживают упоминания в качестве комплексообразователей и/или средств для увеличения растворимости β-CD, случайным образом метилированный β-CD, 2,6-диметил-β-CD, 2-гидроксиэтил-β-CD, 2-гидроксипропил-β-CD и (2-карбоксиметокси)пропил-β-CD и в особенности 2-гидроксипропил-β-CD (2-HP-β-CD).
Термин «смешанный эфир» означает производные циклодекстрина, в которых, по меньшей мере, две гидроксигруппы циклодекстрина этерифицированы различными группами, например гидроксипропилом и гидроксиэтилом.
Среднее мольное замещение (M.S.) используется в качестве меры среднего количества молей алкокси-фрагментов на моль ангидроглюкозы. Средняя степень замещения (D.S.) относится к среднему числу замещенных гидроксильных групп на ангидроглюкозную единицу. Величины M.S. и D.S. могут быть определены различными аналитическими методиками, такими как ядерный магнитный резонанс (ЯМР), масс-спектрометрия (МС) и инфракрасная спектроскопия (ИК). В зависимости от используемой методики для одного производного циклодекстрина могут быть получены несколько различающиеся величины. По данным масс-спектрометрии, M.S. предпочтительно изменяется в пределах от 0,125 до 10, и D.S. изменяется от 0,125 до 3.
Другие подходящие композиции для перорального или ректального введения включают частицы, состоящие из твердой дисперсии, включающей соединение формулы (I) и один или несколько подходящих фармацевтически приемлемых водорастворимых полимеров.
Термин «твердая дисперсия», использованный ниже в настоящем описании, определяет систему в твердом состоянии (в противоположность жидкому или газообразному состоянию), включающую по меньшей мере два компонента, в данном случае соединение формулы (I) и водорастворимый полимер, причем один компонент более-менее равномерно распределен по объему другого компонента или компонентов (в случае, если в рецептуру включены дополнительные фармацевтически приемлемые компоненты, в основном известные в технике, такие как пластификаторы, консерванты и т.п.). Если указанная дисперсия компонентов такова, что система химически и физически однородна, или гомогенна, по всему объему или состоит из одной фазы согласно определению термодинамики, такая твердая дисперсия будет именоваться «твердым раствором». Твердые растворы являются предпочтительными физическими системами, так как их компоненты обычно легко биодоступны для организма, в который их вводят. Это преимущество, вероятно, может быть объяснено легкостью, с которой указанные твердые растворы могут образовывать жидкие растворы при контакте с жидкой средой, такой как желудочно-кишечные соки. Легкость растворения может быть объяснена, хотя бы частично, тем фактом, что энергия, требуемая для растворения компонентов твердого раствора, меньше, чем энергия, требуемая для растворения компонентов кристаллической или микрокристаллической твердой фазы.
Термин «твердая дисперсия» также включает дисперсии, обладающие меньшей степенью гомогенности по сравнению с твердыми растворами. Такие дисперсии не являются химически и физически однородными по всему объему или включают более одной фазы. Например, термин «твердая дисперсия» также относится к системам, имеющим домены или небольшие области, в которых аморфное, микрокристаллическое или кристаллическое соединение формулы (I) или аморфный, микрокристаллический или кристаллический водорастворимый полимер, или оба упомянутых вещества, более или менее равномерно диспергированы в другой фазе, включающей водорастворимый полимер, или соединение формулы (I), или твердый раствор, включающий соединение формулы (I) и водорастворимый полимер. Указанные домены являются областями, в которых твердая дисперсия явно отмечена каким-либо физическим свойством, является небольшой по объему, и они равномерно и случайно распределены по объему твердой дисперсии.
Существуют различные методики получения твердых дисперсий, включающие экструзию расплава, распылительную сушку и упаривание растворов.
Способ упаривания растворов включает следующие стадии:
a) растворение соединения формулы (I) и водорастворимого полимера в подходящем растворителе, необязательно при повышенных температурах;
b) нагревание раствора, полученного в п. a), необязательно в вакууме, до выпаривания растворителя. Кроме того, раствор может быть вылит на поверхность большой площади для образования тонкой пленки, из которой удаляют растворитель.
В методике распылительной сушки два указанных компонента также растворяют в подходящем растворителе, и полученный раствор распыляют через форсунку агрегата для распылительной сушки с последующим выпариванием растворителя из образующихся капелек при повышенных температурах.
Предпочтительной методикой получения твердых дисперсий является способ экструзии расплава, включающий следующие стадии:
a) смешивание соединения формулы (I) и подходящего водорастворимого полимера,
b) необязательное внесение добавок в полученную смесь,
c) нагревание и перемешивание полученной таким образом смеси до получения гомогенного расплава,
d) экструзия полученного таким образом расплава через одно или несколько выпускных отверстий; и
e) охлаждение расплава до затвердевания.
Термины «плавиться» и «плавление» следует интерпретировать в широком смысле. Эти термины означают не только переход из твердого состояния в жидкое, но также относятся к переходу в стеклообразное состояние или резиноподобное состояние, в котором появляется возможность того, чтобы один компонент смеси более-менее однородно внедрился в другой. В отдельных случаях один компонент будет плавиться, и другой компонент (компоненты) будет (будут) растворяться в расплаве, таким образом образуя раствор, который при охлаждении может превратиться в твердый раствор, имеющий лучшие свойства с точки зрения растворимости.
После получения твердых дисперсий, как описано выше, полученные продукты могут быть необязательно измельчены и просеяны.
Продукты, являющиеся твердыми дисперсиями, могут быть измельчены или размолоты до частиц, имеющих размер менее 600 мкм, предпочтительно менее 400 мкм и наиболее предпочтительно менее 125 мкм.
Частицы, полученные по способу, описанному выше, затем могут быть включены в состав таких лекарственных форм, как таблетки и капсулы, с помощью обычных методик.
Следует иметь в виду, что специалист в данной области техники сможет оптимизировать параметры описанной выше методики получения твердой дисперсии, такие как наиболее подходящий растворитель, рабочая температура, тип используемой аппаратуры, скорость распылительной сушки, пропускная способность экструдера расплава.
Водорастворимые полимеры в частицах представляют собой полимеры, которые при 20°C в водном растворе при концентрации 2% (масса/объем) имеют кажущуюся вязкость от 1 до 5000 мПа·с, более предпочтительно от 1 до 700 мПа·с и наиболее предпочтительно от 1 до 100 мПа·с. Например, подходящие водорастворимые полимеры включают алкилцеллюлозы, гидроксиалкилцеллюлозы, гидроксиалкилалкилцеллюлозы, карбоксиалкилцеллюлозы, соли щелочных металлов и карбоксиалкилцеллюлоз, карбоксиалкилалкилцеллюлозы, сложные эфиры карбоксиалкилцеллюлозы, крахмалы, пектины, производные хитина, ди-, олиго- и полисахариды, такие как трегалоза, альгиновая кислота или ее соли со щелочными металлами и аммонием, каррагенаны, галактоманнаны, трагакант, агар-агар, гумиарабик, гуаровую камедь и ксантановую камедь, полиакриловые кислоты и их соли, полиметакриловые кислоты и их соли, метакриловые сополимеры, поливиниловый спирт, поливинилпирролидон, сополимеры поливинилпирролидона с винилацетатом, комбинации поливинилового спирта и поливинилпирролидона, полиалкиленоксиды и сополимеры этиленоксида и пропиленоксида. Предпочтительными водорастворимыми полимерами являются гидроксипропилметилцеллюлозы.
Кроме этого, в качестве водорастворимого полимера при получении указанных выше частиц можно применить один или несколько циклодекстринов, что раскрыто в WO 97/18839. Указанные циклодекстрины включают фармацевтически приемлемые незамещенные и замещенные циклодекстрины, известные в технике, более конкретно α-, β- или γ-циклодекстрины, или их фармацевтически приемлемые производные.
Замещенные циклодекстрины, которые могут применяться для получения описанных выше частиц, включают полиэфиры, описанные в патенте США 3459731. Дополнительно замещенные циклодекстрины представляют собой простые эфиры, в которых водород одной или нескольких гидроксигрупп циклодекстрина замещен C1-6алкилом, гидроксиC1-6алкилом, карбоксиC1-6алкилом или C1-6алкилоксикарбонилC1-6алкилом, или их смешанные простые эфиры. В частности, такие замещенные циклодекстрины представляют собой простые эфиры, в которых водород одной или нескольких гидроксигрупп циклодекстрина замещен C1-3алкилом, гидроксиC2-4алкилом, карбоксиC1-2алкилом или, более конкретно, метилом, этилом, гидроксиэтилом, гидроксипропилом, гидроксибутилом, карбоксиметилом или карбоксиэтилом.
Особенной эффективностью обладают β-циклодекстриновые простые эфиры, например диметил-β-циклодекстрин, как указано M.Nogradi в Drugs of the Future, vol. 9, No 8, p. 577-578 (1984), а также полиэфиры, например гидроксипропил β-циклодекстрина и гидроксиэтил β-циклодекстрина. Такие алкиловые эфиры могут представлять собой метиловый эфир со степенью замещения от примерно 0,125 до 3, например от примерно 0,3 до 2. Такой гидроксипропилциклодекстрин может быть, например, получен по реакции между β-циклодекстрином и пропиленоксидом и может иметь величину MS от примерно 0,125 до 10, например от примерно 0,3 до 3.
Другим типом замещенных циклодекстринов являются сульфобутилциклодекстрины.
Соотношение между соединением формулы (I) и водорастворимым полимером может меняться в широких пределах. Например, могут применяться соотношения от 1/100 до 100/1. Представляющие интерес соотношения соединения формулы (I) и циклодекстрина находятся в пределах от примерно 1/10 до 10/1. Больший интерес представляют соотношения от примерно 1/5 до 5/1.
Далее может оказаться подходящим создание препаратов на основе соединений формулы (I) в форме наночастиц, на поверхности которых адсорбирован модификатор поверхности в количестве, достаточном для сохранения эффективного среднего размера частиц менее 1000 нм. Считается, что применимые модификаторы поверхности включают такие вещества, которые физически прикрепляются к поверхности соединения формулы (I), но не связываются с указанным соединением химически.
Подходящие модификаторы поверхности предпочтительно могут быть выбраны из известных органических и неорганических фармацевтических наполнителей. Такие наполнители включают различные полимеры, олигомеры низкой молекулярной массы, природные вещества и ПАВ. Предпочтительные модификаторы поверхности включают неионные и анионные ПАВ.
Еще один интересный способ создания препаратов на основе соединения формулы (I) включает образование фармацевтических композиций, в которых соединения формулы (I) включены в гидрофильные полимеры, и применение этой смеси в качестве покрывающей пленки для большого количества маленьких шариков, что приводит к композиции, которая удобна в производстве и которая подходит для получения лекарственных форм для перорального введения.
Указанные шарики содержат центральное округлое или сферическое ядро, покрывающую пленку из гидрофильного полимера и соединения формулы (I), и необязательно слой герметичного покрытия.
Имеется большое количество материалов, подходящих для применения в качестве ядер, при условии, что указанные материалы являются фармацевтически приемлемыми и имеют подходящие размеры и твердость. Примерами таких материалов являются полимеры, неорганические вещества, органические вещества, а также сахариды и их производные.
Особенно предпочтительно создание из описанных выше фармацевтических композиций лекарственных форм разовой дозировки для облегчения введения и однородности дозирования. Термин «лекарственные формы разовой дозировки» в настоящем описании относится к физически дискретным единицам, подходящим в качестве разовых доз, причем каждая доза содержит заранее определенное количество действующего ингредиента, рассчитанное на достижение желаемого терапевтического эффекта, в сочетании с требуемым фармацевтическим носителем. Примерами таких лекарственных форм разовой дозировки являются таблетки (включая таблетки с риской или таблетки с покрытием), капсулы, пилюли, пакеты с порошком, облатки, суппозитории, растворы или суспензии для инъекций и т.п., а также определенные количества указанных лекарственных форм в отдельных упаковках.
Специалисты в лечении ВИЧ-инфекции могли бы определить эффективную дневную дозу на основе представленных в настоящей заявке результатов тестирования. Как правило, считается, что эффективная дневная доза будет составлять от 0,01 мг/кг до 50 мг/кг массы тела, более предпочтительно от 0,1 мг/кг до 10 мг/кг массы тела. Может быть приемлемо введение дневной дозы и виде двух, трех, четырех или большего количества субдоз через соответствующие промежутки времени в течение дня. Указанные субдозы могут быть включены в состав лекарственных форм разовой дозировки, например, содержащих от 1 до 1000 мг, и в частности от 5 до 200 мг действующего ингредиента на единицу лекарственной формы.
Точная дозировка и частота введения зависят от конкретного применяемого соединения формулы (I), конкретного подвергаемого лечению состояния, тяжести этого состояния, возраста, веса и общего физического состояния конкретного пациента, а также других лекарственных средств, которые могут приниматься пациентом, что очень хорошо известно специалистам в данной области техники. Кроме того, очевидно, что указанное эффективное дневное количество может уменьшаться или увеличиваться в зависимости от реакции подвергаемого лечению пациента и/или в зависимости от оценки врача, прописавшего прием соединений по настоящему изобретению. Следовательно, диапазоны изменения эффективной дневной дозы, приведенные выше и ниже по тексту, являются только общими указаниями, и не предполагается, что они в какой бы то ни было степени ограничивают область применения настоящего изобретения.
Соединения формулы (I) по настоящему изобретению могут применяться отдельно либо в комбинации с другими терапевтическими средствами, такими как антивирусные препараты, антибиотики, иммуномодуляторы или вакцины для лечения вирусных инфекций. Помимо этого, они могут применяться отдельно либо в комбинации с другими профилактическими средствами для предотвращения вирусных инфекций. Соединения по настоящему изобретению могут применяться в вакцинах, а также в способах защиты индивидуумов от вирусных инфекций на продолжительный период времени. Эти соединения могут применяться в указанных вакцинах либо сами по себе, либо совместно с другими соединениями по настоящему изобретению, либо совместно с другими антивирусными средствами, способом, согласующимся с общепринятым применением ингибиторов обратной транскриптазы в вакцинах. Таким образом, соединения по настоящему изобретению могут быть объединены с фармацевтически приемлемыми вспомогательными веществами, обычно применяемыми в вакцинах, и введены в профилактически эффективных количествах для защиты индивидуумов от ВИЧ-инфекции на продолжительный период времени.
Кроме этого, комбинация одного или нескольких дополнительных антиретровирусных соединений и соединения формулы (I) может применяться в качестве лекарственного средства. Таким образом, настоящее изобретение относится также к продукту, содержащему (a) соединение формулы (I) и (b) одно или несколько дополнительных антиретровирусных соединений, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения в анти-ВИЧ лечении. Различные лекарственные средства могут быть объединены в одном препарате вместе с фармацевтически приемлемыми носителями. Указанные дополнительные антиретровирусные соединения могут представлять собой любые известные антиретровирусные соединения, такие как сурамин, пентамидин, тимопентин, кастаноспермин, декстран (декстран сульфат) фоскарнет-натрий (тринатрийфосфоноформиат); нуклеозидные ингибиторы обратной транскриптазы (NRTI), например зидовудин (AZT), диданозин (ddI), залцитабин (ddC), ламивудин (3TC), ставудин (d4T), эмтрицитабин (FTC), абакавир (ABC), D-D4FC (ReversetTM), аловудин (MIV-310), амдоксовир (DAPD), элвуцитабин (ACH-126,443) и т.п.; ненуклеозидные ингибиторы обратной транскриптазы (NNRTIs), такие как деларвидин (DLV), эфавиренц (EFV), невирапин (NVP), каправирин (CPV), каланолид A, TMC120, этравирин (TMC125), TMC278, BMS-561390, DPC-083 и т.п.; нуклеотидные ингибиторы обратной транскриптазы (NtRTI), например тенофовир (TDF) и тенофовир дизопроксил фумарат и т.п.; соединения типа TIBO (тетрагидроимидазо[4,5,1-jk][1,4]-бензодиазепин-2(1H)-она и тиона), например, (S)-8-хлор-4,5,6,7-тетрагидро-5-метил-6-(3-метил-2-бутенил)имидазо-[4,5,1-jk][1,4]-бензодиазепин-2(1H)-тион; соединения типа α-APA (α-анилинофенилацетамида), например α-[(2-нитрофенил)амино]-2,6-дихлорбензолацетамид и т.п.; ингибиторы трансактивирующих белков, такие как TAT-ингибиторы, например, RO-5-3335; ингибиторы REV; ингибиторы протеазы, например ритонавир (RTV), саквинавир (SQV), лопинавир (ABT-378 или LPV), индинавир (IDV), ампренавир (VX-478), TMC-126, BMS-232632, VX-175, DMP-323, DMP-450 (мозенавир), нелфинавир (AG-1343), атазанавир (BMS 232 632), палинавир, TMC-114, RO033-4649, фосампренавир (GW433908 или VX-175), P-1946, BMS 186 318, SC-55389a, L-756 423, трипранавир (PNU-140690), BILA 1096 BS, U-140690, и т.п.; ингибиторы входа, которые включают ингибиторы слияния (например, T-20, T-1249), ингибиторы прикрепления и ингибиторы корецептора; последние включают антагонистов CCR5 и CXR4 (например, AMD-3100); примерами ингибиторов входа являются энфувиртид (ENF), GSK-873 140, PRO-542, SCH-417 690, TNX-355, маравирок (UK-427 857); ингибитором созревания является, например, PA-457 (Panacos Pharmaceuticals); ингибиторы вирусной интегразы; ингибиторы рибонуклеотидредуктазы (клеточные ингибиторы), например гидроксимочевина и т.п.
При введении соединений по настоящему изобретению совместно с другими антивирусными средствами, которые нацелены на различные события жизненного цикла вируса, терапевтическое действие этих соединений может быть усилено. Комбинированная терапия, описанная выше, приводит в действие синергический эффект в ингибировании репликации ВИЧ, поскольку каждый компонент комбинации действует на другой участок репликации ВИЧ. Применение таких комбинаций может привести к уменьшению дозировки данного традиционного антиретровирусного средства, по сравнению с той дозировкой, которая потребовалась бы для желаемого терапевтического или профилактического эффекта при введении данного средства в режиме монотерапии. Эти комбинации могут уменьшить или устранить побочные эффекты обычной монолекарственной ретровирусной терапии, не препятствуя при этом антивирусной активности средств. Эти комбинации уменьшают потенциал сопротивления монолекарственной терапии, минимизируя при этом любую сопутствующую токсичность. Помимо этого, указанные комбинации могут увеличить эффективность традиционных средств без увеличения сопутствующей токсичности.
Кроме того, соединения по настоящему изобретению могут вводиться в комбинации с иммуномодулирующими средствами, например, левамизолом, бропиримином, антителом против человеческого интерферона альфа, интерфероном альфа, интерлейкином 2, метионин-энкефалином, диэтилдитиокарбаматом, фактором некроза опухолей, налтрексоном и т.п.; антибиотиками, например пентамидинизетиоратом и т.п.; холинергическими средствами, например такрином, ривастигмином, донепезилом, галантамином и т.п.; блокаторами каналов NDMA, например мемантином, для предотвращения или борьбы с инфекциями и заболеваниями или симптомами заболеваний, связанных с ВИЧ-инфекциями, такими как СПИД и ARC, например деменцией. Помимо этого, соединение формулы (I) может быть скомбинировано с другим соединением формулы (I).
Хотя в настоящем изобретении внимание сосредоточено на применении соединений по настоящему изобретению для предотвращения или лечения ВИЧ-инфекций, эти соединения также могут применяться в качестве ингибирующих средств для других вирусов, у которых обязательные события в жизненном цикле зависят от сходных обратных транскриптаз.
Настоящее изобретение более подробно разъяснено в следующих неограничивающих примерах.
Примеры
Пример 1 - Синтез промежуточных соединений B,C и D
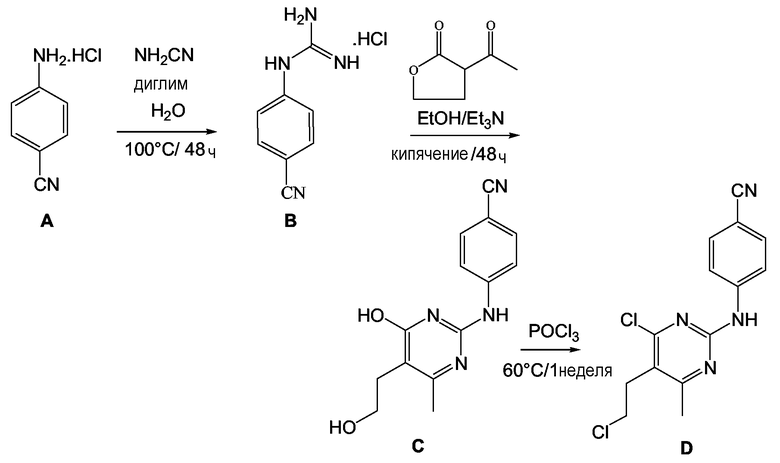
Получение промежуточного соединения B
Смесь A (0,420 моль) и 2-метоксиэтилового эфира (диглима, 250 мл) перемешивали при 100°C в течение 30 минут. Затем порциями добавляли смесь цианамида (0,630 моль) и воды (30 мл) в течение 45 минут. После перемешивания в течение 24 ч при 100°C добавляли цианамид (0,210 моль). Смесь вновь перемешивали при 100°C в течение 48 ч. Смесь упаривали досуха и остаток перекристаллизовывали из ацетона. Выход промежуточного соединения B 70,5 г (85%, температура плавления: 225°C).
Получение промежуточного соединения C
Смесь B (0,356 моль) и 2-ацетилбутиролактона (1,068 моль) в этаноле (200 мл) и триэтиламине (75 мл) перемешивали при кипячении с обратным холодильником в течение 48 ч. Смесь охлаждали, осадок отфильтровывали, затем промывали этанолом и высушивали. Выход C 71 г (74%, температура плавления >250°C).
Получение промежуточного соединения D
Смесь C (0,189 моль) и оксихлорида фосфора (200 мл) перемешивали при 60°C в течение 1 недели. После охлаждения оксихлорид фосфора выпаривали. Добавляли воду и 10% K2CO3 и смесь экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и выпаривали растворитель. Выход D 45 г (78%, температура плавления: 168°C).
Пример 2. Получение промежуточного соединения E9 (4-бром-2-хлор-6-фторанилин)
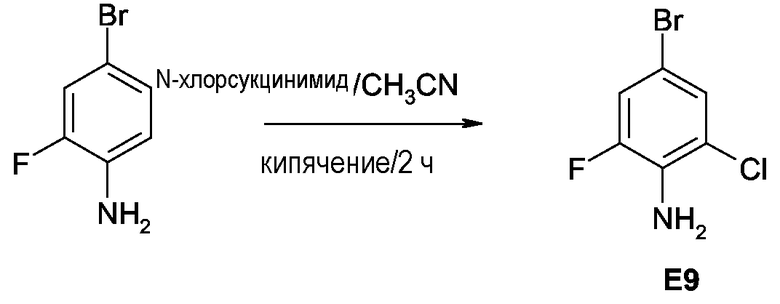
N-хлорсукцинимид (0,199 моль) порциями добавляли к смеси 4-бром-2-фторанилина (0,158 моль) и ацетонитрила (50 мл). Смесь перемешивали при кипячении с обратным холодильником в течение 2 часов, охлаждали и выливали в смесь воды и 10% K2CO3. Смесь экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и растворитель выпаривали. Остаток очищали колоночной хроматографией на силикагеле (элюент: циклогексан/этилацетат 80/20; 35-70 мкм). Собирали фракции с чистым веществом и выпаривали растворитель. Выход 4-бром-2-хлор-6-фторанилина (промежуточного соединения E9) 31,6 г (89%, температура плавления:<50°C). Промежуточное соединение E9 использовали для получения промежуточного соединения F9 (см. табл.1).
Пример 3. Получение промежуточных соединений F3, F4, F6
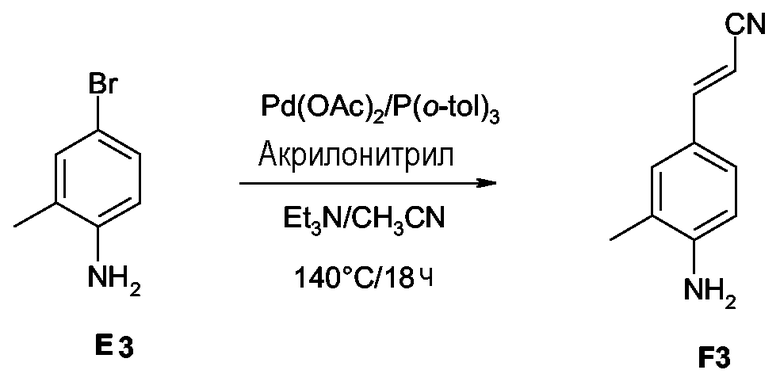
Смесь 4-бром-2-метиланилина (0,0268 моль), промежуточного соединения E3, ацетата палладия(0) (0,00537 моль), три-о-толилфосфина (0,0268 моль) и акрилонитрила (0,0896 моль) в триэтиламине (0,107 моль) и ацетонитриле (70 мл) перемешивали при 140°C в автоклаве из нержавеющей стали в течение 18 часов. После охлаждения смесь фильтровали через целит, фильтрат выливали в воду и экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и выпаривали растворитель. Остаток очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2/циклогексан 50/50; 35-70 мкм). Фракции с чистым веществом собирали и растворитель выпаривали. Выход промежуточного соединения F3: 3,2 г (75%, температура плавления: 105°C).
Получение промежуточных соединений F4 и F6
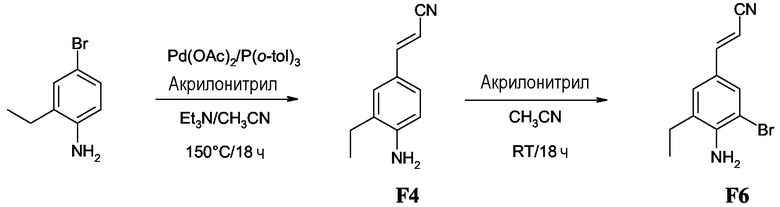
Промежуточное соединение F4 получали, как описано выше для получения F3, используя 4-бром-2-этиланилин в качестве исходного вещества. На второй стадии порциями добавляли N-бромсукцинимид (0,015 моль) к смеси 4-акрилонитрил-2-этиланилина F4 (0,012 моль) и ацетонитрила (25 мл). Смесь перемешивали при комнатной температуре в течение ночи, затем выливали в смесь воды и 10% K2CO3. Смесь экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и растворитель выпаривали. Остаток очищали колоночной хроматографией на силикагеле (элюент: циклогексан/этилацетат 90/10; 15-40 мкм). Фракции с чистым веществом собирали и выпаривали растворитель. Выход промежуточного соединения F6: 0,75 г (26%).
Пример 4. Получение промежуточных соединений H, I и J
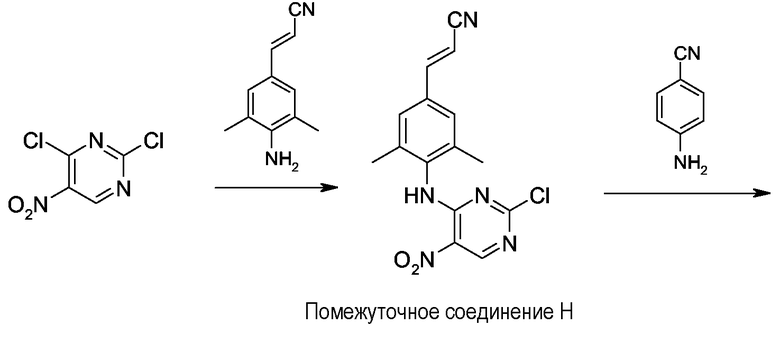
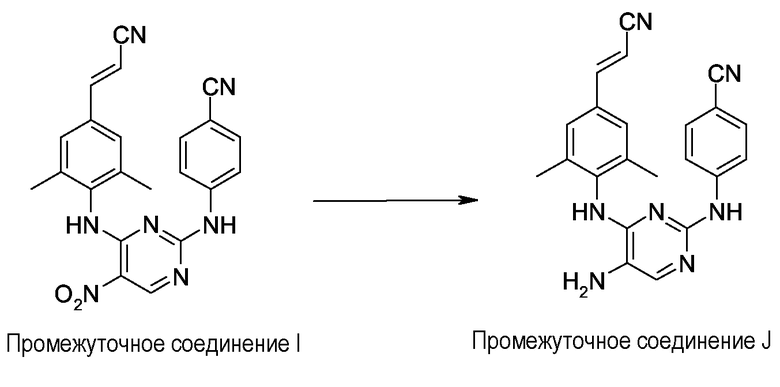
Получение промежуточного соединения H
Смесь 2,4-дихлор-5-нитропиримидина (0,0516 моль) и 4-(2-цианоэтенил)-2,6-диметилфениламина (0,0516 моль) перемешивали при 140°C на масляной бане в течение 45 минут, затем выливали в смесь воды и 10% K2CO3. Осадок отфильтровывали и фильтрат экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и растворитель выпаривали. Остаток очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2 100; 35-70 мкм). Собирали фракции с чистым веществом и выпаривали растворитель, получая 6,0 г промежуточного соединения H (35%, температура плавления: >250°C).
Получение промежуточного соединения I
Смесь промежуточного соединения H (0,0182 моль) и 4-цианоанилина (0,0182 моль) нагревали в расплавленном состоянии в течение 5 минут, затем выливали в смесь воды и 10% K2CO3. Добавляли CH2Cl2 с небольшим количеством MeOH, отфильтровывали и высушивали осадок, получая 7,4 г промежуточного соединения I (95%, температура плавления: >250°C).
Получение промежуточного соединения J
Смесь промежуточного соединения I (0,0180 моль) и дигидрата хлорида олова(II) (0,125 моль) в этаноле (100 мл) перемешивали при 70°C в течение ночи, затем выливали в смесь воды и 10% K2CO3. Осадок отфильтровывали через целит. Фильтрат удаляли и осадок промывали CH2Cl2 и ТГФ. Растворитель выпаривали. Выход промежуточного соединения J: 6,0 г (87%, температура плавления: >250°C).
Пример 5. Получение промежуточных соединений K, L и M (6-хлор-2-фторфенилсодержащих аналогов промежуточных соединений H, I и J)
Смесь 2,4-дихлор-5-нитропиримидина (0,0153 моль) и 4-(2-цианоэтенил)-6-хлор-2-фторфениламина (0,0153 моль) нагревали в расплавленном состоянии в течение 5 минут, затем выливали в смесь воды и 10% K2CO3 и экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и выпаривали растворитель. Остаток очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2 100; 35-70 мкм). Собирали фракции с чистым веществом и выпаривали растворитель. Выход 2-хлор-4-[4-(2-цианоэтенил)-2-фтор-6-хлорфениламино]-5-нитропиримидина, т.е. промежуточного соединения K, 1,9 г (35%, температура плавления: 217°C).
Смесь промежуточного соединения K (0,000424 моль) и 4-цианоанилина (0,000424 моль) нагревали в расплавленном состоянии в течение 5 минут, затем выливали в смесь воды и 10% K2CO3. Добавляли CH2Cl2 с небольшим количеством MeOH, осадок отфильтровывали и высушивали, выход 4-[4-[4-(2-цианоэтенил)-2-фтор-6-хлорфениламино]-5-нитропиримидин]амино]бензонитрила, т.е. промежуточного соединения L: 1,34 г (73%, температура плавления: >250°C).
Смесь промежуточного соединения L (0,00306 моль) и дигидрата хлорида олова(II) (0,0214 моль) в этаноле (20 мл) перемешивали при 70°С в течение ночи, затем выливали в смесь воды и 10% K2CO3. Осадок отфильтровывали через целит. Фильтрат удаляли и осадок промывали CH2Cl2 и ТГФ. Растворитель выпаривали. Выход 4-[4-[4-(2-цианоэтенил)-2-фтор-6-хлорфениламино]-5-аминопиримидин]амино]бензонитрил, т.е. промежуточного соединения M, 1,1 г (89%, температура плавления: >250°C).
Пример 6. Получение дигидропирролопиримидинового соединения 1
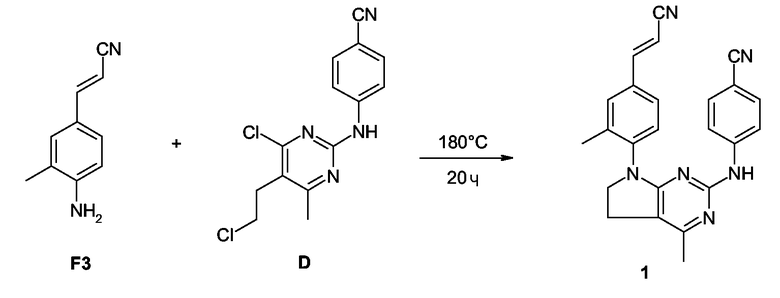
Смесь F3 (0,00126 моль) и D (0,00126 моль) перемешивали при 180°C на масляной бане в течение 20 часов, затем выливали в смесь воды и 10% K2CO3 и экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и растворитель выпаривали. Остаток очищали колоночной хроматографией на силикагеле (элюент: MeOH/AcNH4/ТГФ 40/40/20; Kromasil C18, 10 мкм). Собирали фракции с чистым веществом и выпаривали растворитель. Выход: 0,18 г соединения 1 (E/Z:95/5) и 0,124 г соединения 1 (E/Z:65/35) (общий выход 61%, температура плавления (E/Z:95/5): 244°C).
Пример 7. Получение дигидропирролопиримидинового производного 14
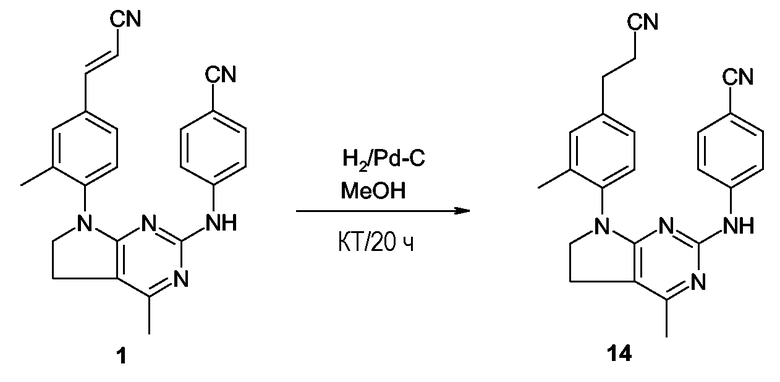
К раствору соединения 1 (0,00051 моль) в MeOH (20 мл) в токе азота добавляли 10% палладий на активированном угле (0,2 г, 10 мас.%). Смесь перемешивали при комнатной температуре при давлении газообразного водорода 3 бар в течение 20 часов, затем фильтровали на целите и выпаривали растворитель. Остаток перекристаллизовывали из смеси CH2Cl2/диизопропиловый-этиловый эфир. Выход соединения 14: 0,05 г (25%, температура плавления: 195°C).
Пример 8. Получение пирролопиримидинового производного 28

2,3-дихлор-5,6-дициано-1,4-бензохинон (0,00222 моль) добавляли к смеси соединения 11 (0,000738 моль), полученного по методике, аналогичной методике примера 1, и 1,4-диоксана (10 мл). Смесь перемешивали при кипячении с обратным холодильником в течение 2 ч, затем охлаждали и выливали на лед. Осадок отфильтровывали и очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2/MeOH/NH4OH 98/2/0,1; 10 мкм). Собирали фракции с чистым веществом и выпаривали растворитель. Остаток перекристаллизовывали из смеси диизопропиловый-этиловый эфир. Выход соединения 28: 0,022 г (7%, температура плавления: 217°C).
Пример 9. Получение пирролопиримидинового производного 34
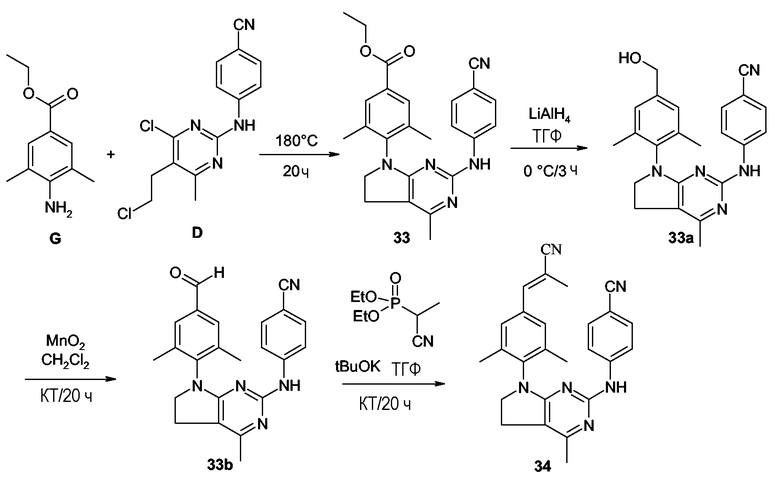
Получение дигидропирролопиримидинового соединения 33
Смесь этил 4-амино-3,5-диметилбензоата G (0,0155 моль) и D (0,0155 моль) перемешивали при 180°C на масляной бане в течение 20 часов, затем выливали в смесь воды и 10% K2CO3 и экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и выпаривали растворитель. Остаток очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2; 70-200 мкм). Собирали фракции, содержащие чистое вещество, и выпаривали растворитель. Выход соединения 33: 2,2 г (33%, температура плавления: 92°C).
Получение дигидропирролопиримидинового производного 33a
Соединение 33 (0,00234 моль) порциями добавляли к смеси литийалюминийгидрида (0,00702 моль) и ТГФ (15 мл) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 часов. Добавляли этилацетат, затем воду и смесь экстрагировали этилацетатом. Органический слой высушивали над сульфатом магния, фильтровали и выпаривали растворитель. Остаток использовали на следующей стадии без дальнейшей очистки.
Получение дигидропирролопиримидинового производного 33b
К остатку соединения 33a (0,860 г) в CH2Cl2 добавляли оксид марганца (IV) (0,0104 моль) и смесь перемешивали при комнатной температуре в течение 20 часов. После фильтрования на целите выпаривали растворитель. Остаток очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2; 70-200 мкм). Собирали фракции, содержащие чистое вещество, и выпаривали растворитель. Выход соединения 33b: 0,160 г (18% для двух стадий, температура плавления: масло).
Получение дигидропирролопиримидинового соединения 34
К смеси диэтил-(1-цианоэтил)фосфоната (0,000782 моль) и ТГФ (5 мл) при 0°C в атмосфере азота добавляли трет-бутилат калия (0,000782 моль) и смесь перемешивали при комнатной температуры в течение 1 часа. Добавляли соединение 33b (0,000261 моль) и перемешивали смесь при комнатной температуре в течение 20 часов, затем выливали в воду и экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и выпаривали растворитель. Остаток очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2; 35-70 мкм). Собирали фракции, содержащие чистое вещество, и выпаривали растворитель. Остаток перекристаллизовывали из смеси диизопропиловый-этиловый эфир. Выход соединения 34 (E/Z:50/50): 0,075 г (68%, температура плавления: 105°C).
Пример 10. Получение соединения 20
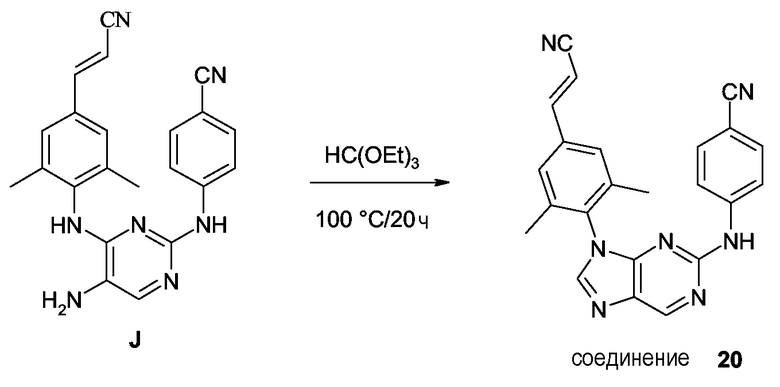
Смесь J (0,000524 моль) и триэтилортоформиата (5 мл) перемешивали при 100°C в течение 20 часов. После охлаждения добавляли воду и 10% K2CO3. Осадок отфильтровывали и высушивали. Выход соединения 20: 0,155 г (76%, температура плавления >250°C).
Пример 11. Получение соединения 21
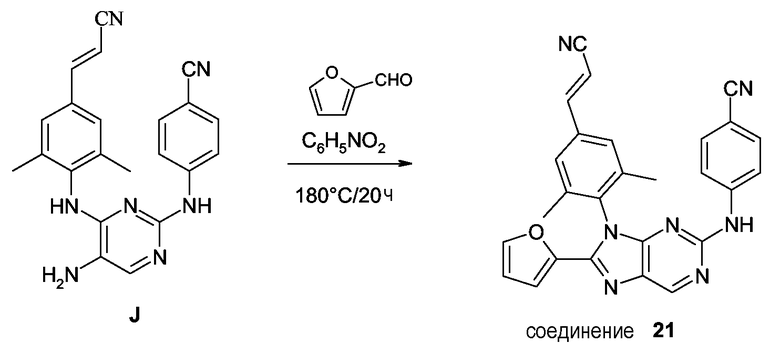
Смесь J (0,000524 моль) и 2-фуральдегида (0,00524 моль) в нитробензоле (5 мл) перемешивали при 180°C в течение 20 часов. После охлаждения остаток отфильтровывали на силикагеле для удаления нитробензола. Растворитель выпаривали и остаток очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2/MeOH/NH4OH 99/1/0,1; 10 мкм). Собирали фракции, содержащие чистое вещество, и выпаривали растворитель. Остаток перекристаллизовывали из смеси диизопропиловый-этиловый эфир. Выход соединения 21: 0,055 г (23%, температура плавления: 236°C).
Пример 12. Получение соединения 29 (производные триазола)
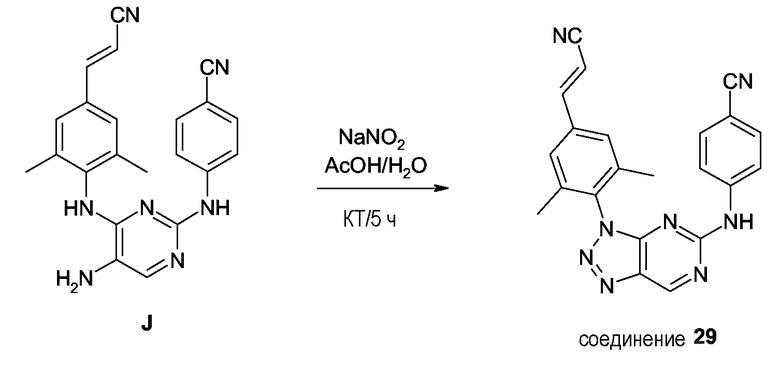
Нитрит натрия (0,000629 моль) в воде (2 мл) при 0°C медленно добавляли к смеси J (0,000524 моль), воды (2,5 мл) и уксусной кислоты (1,5 мл). Смесь перемешивали при комнатной температуре в течение 5 часов. Осадок отфильтровывали, промывали водой и смесью диизопропиловый-этиловый эфир и высушивали. Выход соединения 29: 0,110 г (53%, температура плавления >250°C).
Пример 13. Получение соединения 30
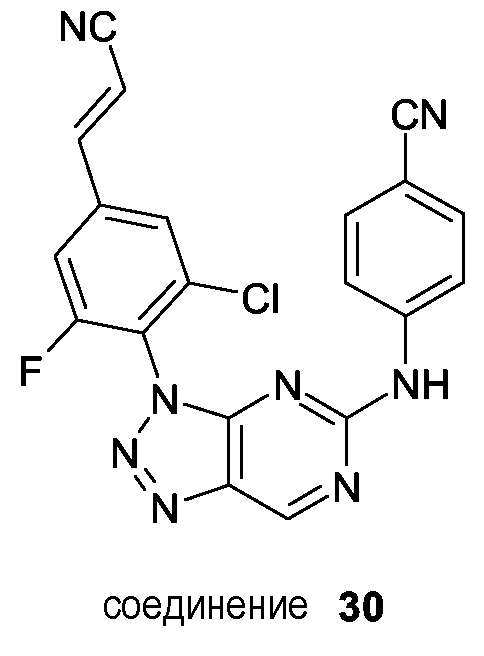
Для получения этого соединения применяли ту же методику, что и в примере 12, исходя из 0,000370 моль аналога J и 0,000444 моль нитрита натрия. Выход соединения 30: 0,065 г (42%, температура плавления >250°C).
Пример 14. Получение соединения 31
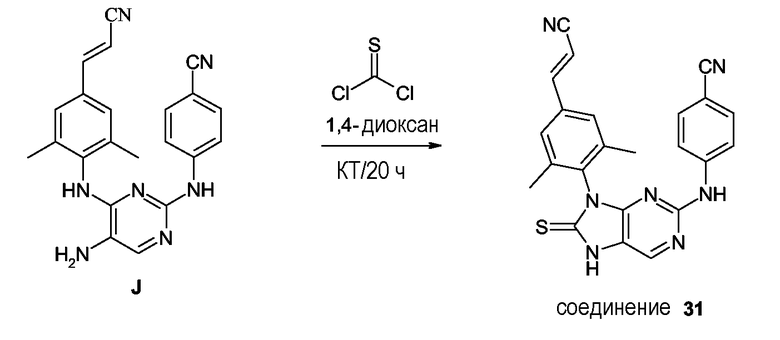
Тиофосген (0,000786 моль) медленно по каплям при 0°C добавляли к смеси J (0,000524 моль) и 1,4-диоксана (5 мл). Смесь перемешивали при комнатной температуре в течение 4 часов, добавляли дополнительную порцию тиофосгена (0,000393 моль) и перемешивали смесь в течение ночи. При 0°C медленно добавляли NH4OH и смесь экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и выпаривали растворитель. Выход соединения 31: 0,105 г (47%, температура плавления >250°C).
Пример 15. Получение соединения 32
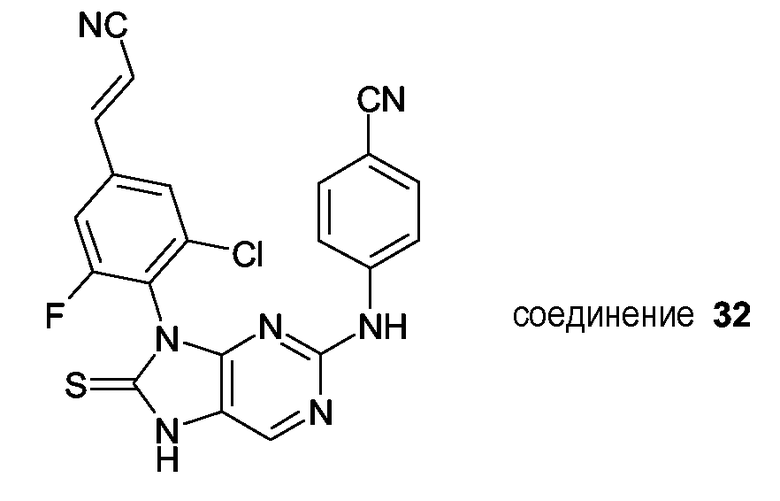
Для получения соединения 32 применяли ту же методику, что и в примере 14, исходя из 0,000370 моль промежуточного соединения M и 0,000554 моль тиофосгена. Выход соединения 32: 0,140 г (85%, температура плавления >250°C).
Пример 16. Получение соединения 26
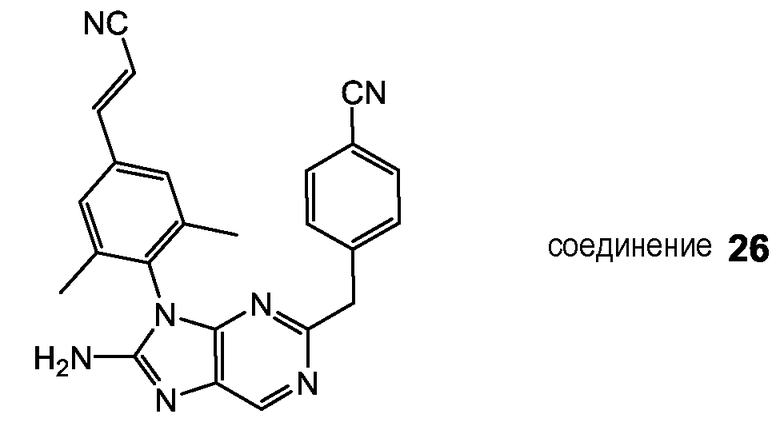
Бромциан (0,000793 моль) порциями добавляли при комнатной температуре к промежуточному соединению J (0,000524 моль) в EtOH (6 мл) и ТГФ (5 мл). Смесь перемешивали при комнатной температуре в течение ночи. Добавляли дополнительное количество бромциана (0,000264 моль) и смесь перемешивали при комнатной температуре один день. Эту смесь выливали в смесь воды и 10% K2CO3 и экстрагировали CH2Cl2. Органический слой высушивали над сульфатом магния, фильтровали и выпаривали растворитель. Остаток перекристаллизовывали из CH2Cl2. Выход соединения 26: 0,092 г (43%, температура плавления: >250°C).
В таблицах 1-6 приведен перечень промежуточных соединений и соединений, которые были получены в соответствии с каким-либо из приведенных выше примеров (№ примера).

№
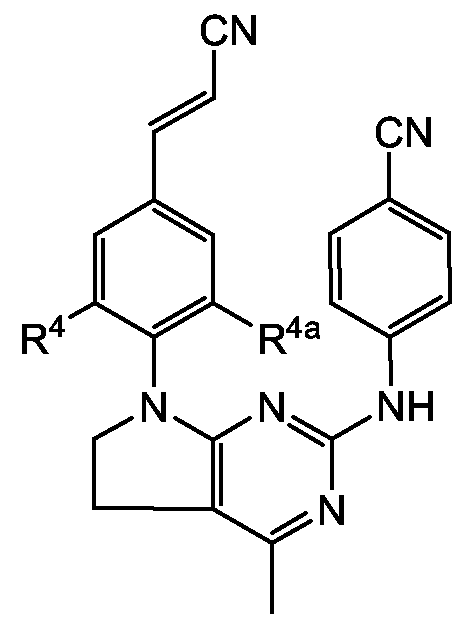
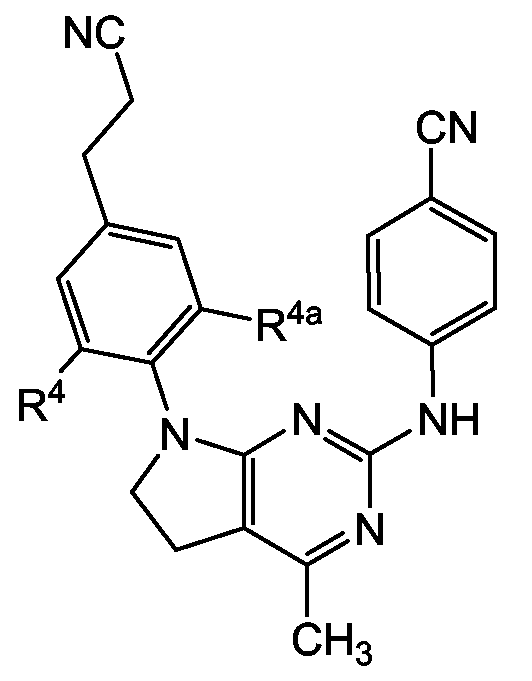
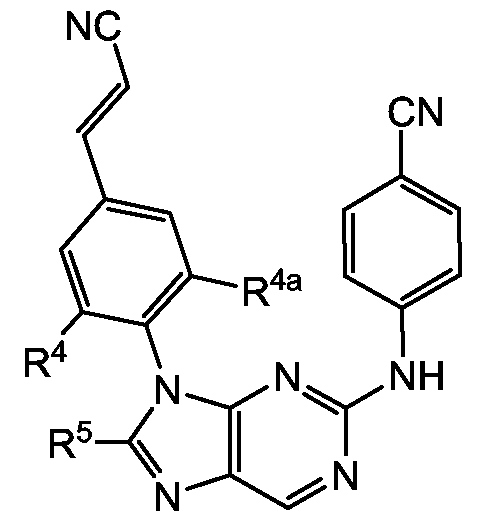
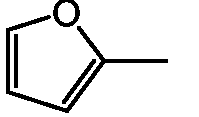
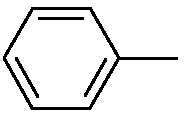
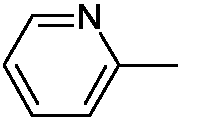
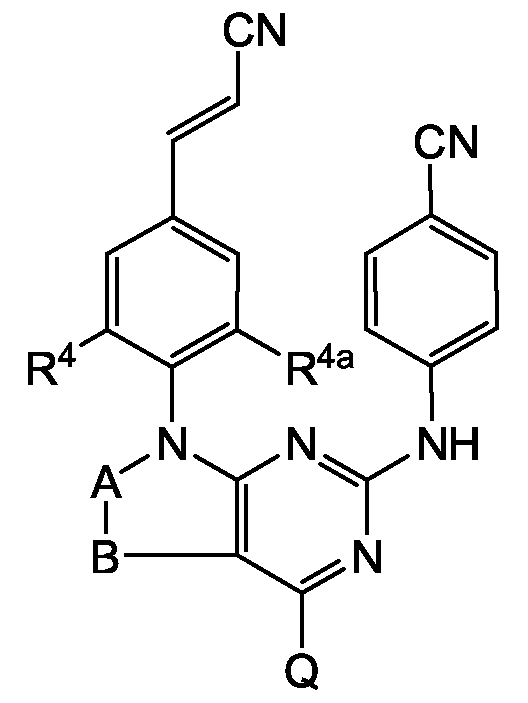
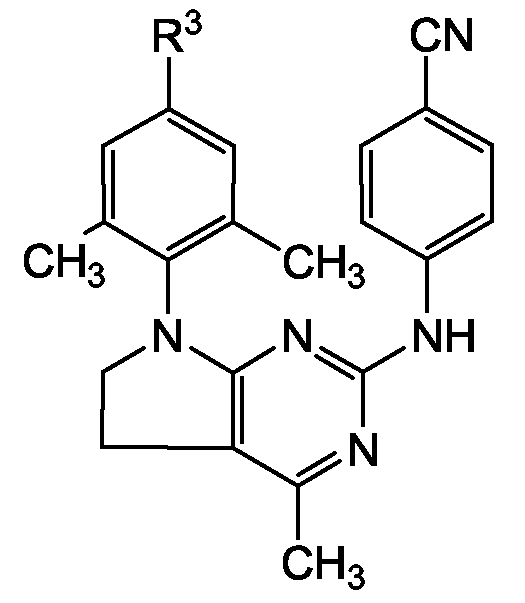
Примеры фармацевтических форм
Капсулы
Соединение формулы (I) растворяли в органическом растворителе, таком как этанол, метанол или хлористый метилен, предпочтительно в смеси этанола и хлористого метилена. Полимеры, как, например, сополимер поливинилпирролидона и винилацетата (PVP-VA), или гидроксипропилметилцеллюлозу (HPMC), как правило, 5 мПа·с, растворяли в органических растворителях, таких как этанол, метанол, хлористый метилен. Удобнее растворять полимер в этаноле. Растворы соединения и полимера смешивали и затем подвергали распылительной сушке. Соотношение соединение/полимер выбирали в пределах от 1/1 до 1/6. Промежуточными соотношениями могут быть 1/1,5 и 1/3. Подходящим соотношением может быть 1/6. Затем порошком, полученным в результате распылительной сушки, т.е. твердой дисперсией, наполняли капсулы для введения пациентам. Количество лекарственного средства, помещенного в одну капсулу, находилось в пределах от 50 до 100 мг, в зависимости от размера используемой капсулы.
Таблетки, покрытые пленкой
Получение ядра таблеток
Смесь 100 г соединения формулы (I), 570 г лактозы и 200 г крахмала хорошо перемешивали и затем увлажняли раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона в приблизительно 200 мл воды. Увлажненную порошкообразную смесь просеивали, высушивали и вновь просеивали. Затем туда добавляли 100 г микрокристаллической целлюлозы и 15 г гидрогенизированного растительного масла. Все компоненты хорошо перемешивали и прессовали в таблетки, получая 10000 таблеток, каждая из которых содержала 10 мг действующего ингредиента.
Покрытие
К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляли раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляли 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. Расплавляли 10 г полиэтиленгликоля и растворяли в 75 мл дихлорметана. Второй раствор добавляли к первому, затем добавляли 2,5 г октадеканоата магния, 5 мл поливинилпирролидона и 30 мл концентрированной суспензии красителя, и смесь гомогенизировали. Ядра таблеток покрывали полученной указанным образом смесью в устройстве для покрытия.
Спектр антивирусного действия
По причине возрастающего появления штаммов ВИЧ, устойчивых к лекарствам, соединения по настоящему изобретению испытывали на эффективность против выделенных клинически штаммов ВИЧ, накопивших несколько мутаций. Эти мутации связаны с устойчивостью к ингибиторам обратной транскриптазы и приводят к появлению вирусов, которые демонстрируют различные степени фенотипической перекрестной устойчивости к коммерчески доступным в настоящее время препаратам, как, например, AZT и делавирдину.
Антивирусную активность соединений по настоящему изобретению оценивали в присутствии вируса ВИЧ дикого типа и мутантов ВИЧ, имеющих мутации в гене обратной транскриптазы. Активность указанных соединений оценивали с использованием клеточного анализа и остаточную активность выражали в величинах pEC50. В колонках IIIB и A-G таблицы приведены величины pEC50 против различных штаммов IIIB, A-G.
Штамм IIIB является штаммом дикого типа ВИЧ-LAI,
штамм A содержит мутацию Y181C в обратной транскриптазе ВИЧ,
штамм B содержит мутацию K103N в обратной транскриптазе ВИЧ,
штамм C содержит мутацию L100I в обратной транскриптазе ВИЧ,
штамм D содержит мутацию Y181L в обратной транскриптазе ВИЧ,
штамм E содержит мутации L100I и K103N в обратной транскриптазе ВИЧ,
штамм F содержит мутации K103N и Y181C в обратной транскриптазе ВИЧ и
штамм G содержит мутации L100I, K103N, Y181C, V179I, E138G, L214F, V278V/I и A327A/V в обратной транскриптазе ВИЧ.
| название | год | авторы | номер документа |
|---|---|---|---|
| 5-ГЕТЕРОЦИКЛИЛПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2405778C2 |
| ПРОИЗВОДНЫЕ 1, 2, 4-ТРИАЗИН-6-ОНА, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2401833C2 |
| ВИЧ-ИНГИБИРУЮЩИЕ 5-КАРБО- ИЛИ ГЕТЕРОЦИКЛИЧЕСКИЕ ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ | 2005 |
|
RU2403244C2 |
| ПРОИЗВОДНЫЕ 5- ИЛИ 6-ЗАМЕЩЕННЫХ БЕНЗИМИДАЗОЛОВ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ РЕСПИРАТОРНОГО СИНЦИТИАЛЬНОГО ВИРУСА | 2004 |
|
RU2369606C2 |
| 5-АМИДО-ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2007 |
|
RU2480464C2 |
| 1,5,6-ЗАМЕЩЕННЫЕ 2-ОКСО-3-ЦИАНО-1,6А-ДИАЗАТЕТРАГИДРОФЛУОРАНТЕНЫ | 2006 |
|
RU2389730C2 |
| АНТИБАКТЕРИАЛЬНЫЕ ХИНОЛИНОВЫЕ ПРОИЗВОДНЫЕ | 2007 |
|
RU2439058C2 |
| 2-ЗАМЕЩЕННЫЕ БЕНЗИМИДАЗОЛЫ | 2006 |
|
RU2441866C2 |
| ПРОИЗВОДНЫЕ АМИНОБЕНЗИМИДАЗОЛОВ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ РЕСПИРАТОРНОГО СИНЦИТИАЛЬНОГО ВИРУСА | 2004 |
|
RU2332414C2 |
| АНТИБАКТЕРИАЛЬНЫЕ ПРОИЗВОДНЫЕ ХИНОЛИНА | 2007 |
|
RU2446159C2 |
Изобретение относится к новым соединениям, ингибирующим репликацию ВИЧ, формулы (I)
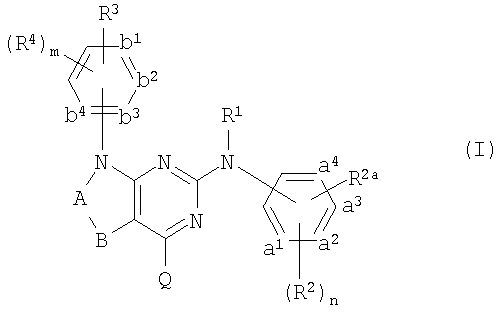
его фармацевтически приемлемой аддитивной соли; или стереохимически изомерной форме, где -а1=а2-а3=а4- представляет собой двухвалентный радикал формулы 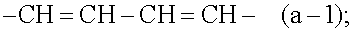 -b1=b2-b3=b4- представляет собой двухвалентный радикал формулы
-b1=b2-b3=b4- представляет собой двухвалентный радикал формулы 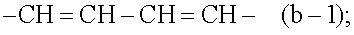 n представляет собой 0; m представляет собой 1, 2; -А-В- представляет собой двухвалентный радикал формулы
n представляет собой 0; m представляет собой 1, 2; -А-В- представляет собой двухвалентный радикал формулы 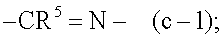
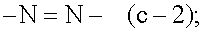
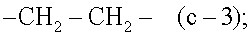
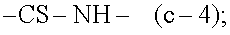
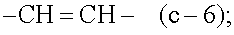 R1 представляет собой водород; R2a представляет собой циано; R3 представляет собой С1-6алкил, замещенный циано; С2-6алкенил, замещенный циано; каждый из R4 независимо представляет собой галоген или С1-6алкил; Q представляет собой водород или С1-6алкил; R5 представляет собой водород, С1-6алкил, арил, пиридил, тиенил, фуранил, амино, моно- или ди (С1-4алкил) амино, где арил представляет собой фенил. Изобретение также относится к фармацевтической композиции, применению и способу получения соединений. 3 н. и 2 з.п. ф-лы, 7 табл.
R1 представляет собой водород; R2a представляет собой циано; R3 представляет собой С1-6алкил, замещенный циано; С2-6алкенил, замещенный циано; каждый из R4 независимо представляет собой галоген или С1-6алкил; Q представляет собой водород или С1-6алкил; R5 представляет собой водород, С1-6алкил, арил, пиридил, тиенил, фуранил, амино, моно- или ди (С1-4алкил) амино, где арил представляет собой фенил. Изобретение также относится к фармацевтической композиции, применению и способу получения соединений. 3 н. и 2 з.п. ф-лы, 7 табл.
1. Соединение формулы
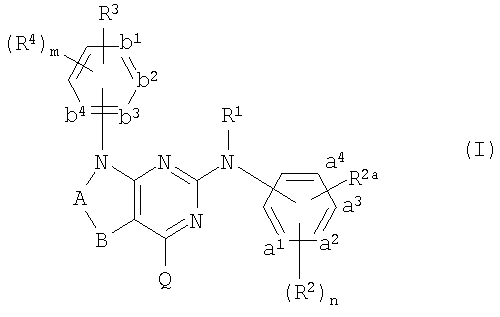
его фармацевтически приемлемая аддитивная соль или стереохимически изомерная форма,
где -а1=а2-а3=а4 представляет собой двухвалентный радикал формулы
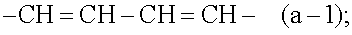
-b1=b2-b3=b4 представляет собой двухвалентный радикал формулы
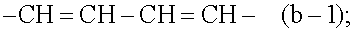
n представляет собой 0;
m представляет собой 1,2;
-А-В- представляет собой двухвалентный радикал формулы
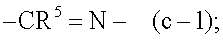

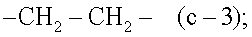
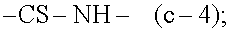
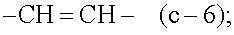
R1 представляет собой водород;
R2a представляет собой циано;
R3 представляет собой С1-6алкил, замещенный циано; С2-6лкенил, замещенный циано; каждый из R4 независимо представляет собой галоген или С1-6алкил;
Q представляет собой водород или С1-6алкил;
R5 представляет собой водород, C1-6алкил, арил, пиридил, тиенил, фуранил, амино, моно- или ди(C1-4алкил)амино, где арил представляет собой фенил.
2. Соединение по п.1, где соединение имеет формулу
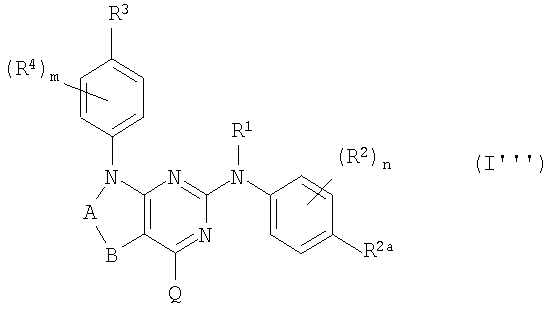
где R1, R2, R2a, R3, R4, -А-В-, m, n и Q соответствуют определениям, данным в п.1.
3. Соединение по п.1, где соединение имеет формулу
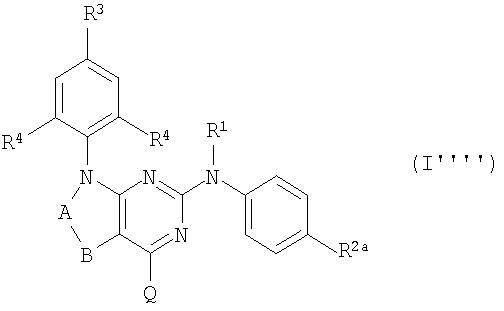
где R1, R2a, R3, R4, -А-В- и Q соответствуют определениям, данным в п.1.
4. Фармацевтическая композиция, ингибирующая репликацию ВИЧ, включающая фармацевтически приемлемый носитель и терапевтически эффективное количество соединения по любому из пп.1-3 в качестве действующего ингредиента.
5. Способ получения соединения по любому из пп.1-3 превращением соединений формулы (I-а) в соответствующие соединения (I-b), в которых фрагмент -А-В- представляет собой -СН=СН-, реакцией элиминирования, в частности элиминированием водорода из соответствующего насыщенного аналога (1-а) с применением подходящего дегидрирующего реагента:
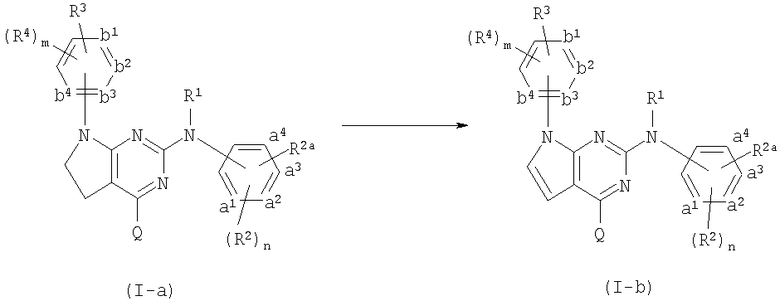
и, если это является желательным, получение солевых форм обработкой соединения формулы (I) в форме свободного основания или кислоты подходящей кислотой или основанием; или, наоборот, превращение солевых форм в соединение формулы (I) в форме свободного основания или кислоты обработкой подходящим основанием или кислотой.
| Турбина внутреннего горения | 1930 |
|
SU21593A1 |
| WO 03074530 А1, 12.09.2003 | |||
| Приспособление для спуска затвора Фотографической камеры | 1931 |
|
SU27825A1 |
Авторы
Даты
2010-11-10—Публикация
2005-10-27—Подача