Изобретение относится к производным 1,2,4-триазин-6-она, обладающим свойствами ингибирования репликации ВИЧ (вируса иммунодефицита человека). Изобретение также относится к способам их получения и фармацевтическим композициям, содержащим такие соединения. Изобретение также относится к применению указанных соединений для получения лекарственного средства для лечения или предупреждения ВИЧ-инфекции.
В ЕР 834507, WO 99/50256, WO 00/27828 и WO 01/85700 раскрываются производные триазина, ингибирующие ВИЧ.
В WO 99/50250, WO 00/27825, WO 01/85700 и WO 03/16306 раскрываются производные пиримидина, ингибирующие ВИЧ.
В WO 02/078708 раскрываются производные пиразинона, ингибирующие ВИЧ.
Соединения настоящего изобретения отличаются от соединений известного уровня техники по структуре, фармакологической активности или эффективности.
Соединения изобретения являются высокоактивными в отношении ингибирования репликации вируса иммунодефицита человека (ВИЧ), и, в частности, они являются высокоактивными в отношении ингибирования репликации мутантных штаммов, в частности, штаммов ВИЧ, резистентных к одному или нескольким лекарственным средствам, т.е. штаммам, которые становятся резистентными к одному или нескольким известным в технике лекарственным средствам NNRTI (лекарственные средства - ненуклеозидные ингибиторы обратной транскриптазы).
Настоящее изобретение относится к соединению формулы
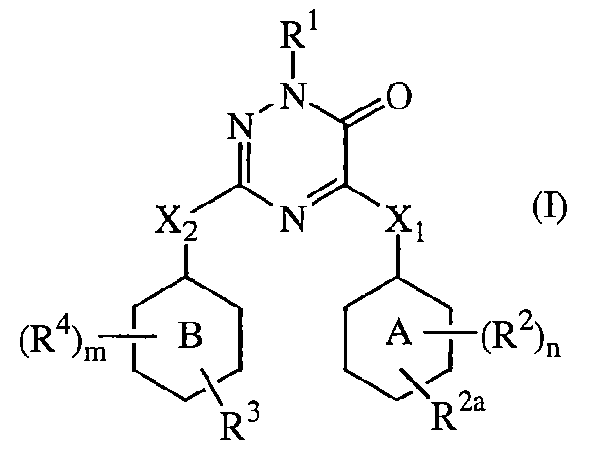
его N-оксиду, фармацевтически приемлемой аддитивной соли, четвертичному амину или стереохимически изомерной форме, где в указанной формуле
кольцо А представляет фенил, пиридил, пиридазинил, пиримидинил или пиразинил;
кольцо В представляет фенил, пиридил, пиридазинил, пиримидинил или пиразинил;
n равно 1, 2, 3, и в случае, когда кольцо А представляет фенил, n также может быть равно 4;
m равно 1, 2, 3, и в случае, когда кольцо В представляет фенил, m также может быть равно 4;
R1 представляет водород; арил; формил; С1-6алкилкарбонил; С1-6алкилоксикарбонил; С1-6алкил, необязательно замещенный R5; или С1-6алкилоксиС1-6алкилкарбонил, замещенный С1-6алкилоксикарбонилом;
каждый R2 независимо представляет водород; гидрокси; галоген; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С3-7циклоалкил; С1-6алкилокси; С1-6алкилоксикарбонил; С1-6алкилкарбонилокси; карбоксил; циано; нитро; амино; моно- или ди(С1-6алкил)амино; полигалогенС1-4алкил; полигалогенС1-4алкилокси; полигалогенС1-4алкилтио; -S(=O)pR6; -NH-S(=O)pR6; -С(=О)R6; -NHC(=O)H; -C(=O)NHNH2; NHC(=O)R6; C(=NH)R6; или R7;
R2а представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)- полигалогенС1-6-алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6-алкила, -C(=O)-О-полигалогенС1-6алкила или R7; -C(=N-O-R8)-С1-4алкил R7 или -X3-R7;
Х1 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -С1-4алкандиил-; -СНОН-; -S-; -S(=O)p-; -X4-С1-4алкандиил-; -С1-4алкандиил-X4- или -С1-4алкандиил-X4-С1-4алкандиил-;
Х2 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -С1-4алкандиил-; -СНОН-; -S-; -S(=O)p-; -X4-С1-4алкандиил-; -С1-4алкандиил-X4- или -С1-4алкандиил-X4-С1-4алкандиил-;
Х3 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -S-; -S(=O)p-; -X4а-С1-4алкандиил-; -С1-4алкандиил-X4b-, -С1-4алкандиил-X4а-С1-4алкандиил- или -С(=N-OR8)-С1-4алкандиил-;
Х4 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -СНОН-; -S- или -S(=O)p-;
Х4а представляет -NR1-; -NH-NH-; -N=N-; -C(=O)-; -S- или -S(=O)p-;
Х4b представляет -NH-NH-; -N=N-; -O-; -C(=O)-; -S- или -S(=O)p-;
R3 представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; -C(=N-O-R8)-С1-4алкил; R7 или -X3-R7;
каждый R4 независимо представляет водород; гидрокси; галоген; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С3-7циклоалкил; С-6алкилокси; С1-6алкилоксикарбонил; С1-6алкилкарбонилокси; карбоксил; циано; нитро; амино; моно- или ди(С1-6алкил)амино; полигалогенС1-4алкил; полигалогенС1-4алкилокси; полигалогенС1-4алкилтио; -S(=O)pR6; -NH-S(=O)pR6; -С(=О)R6; -NHC(=O)H; -C(=O)NHNH2; NHC(=O)R6; C(=NH)R6; или R7;
R5 представляет формил, циано, аминокарбонил, моно- или ди(С1-4алкил)аминокарбонил, гидрокси, С1-6алкилкарбонил, С1-6алкилоксикарбонил или С1-6алкилкарбонилокси;
R6 представляет С1-4алкил, амино, моно- или ди(С1-4алкил)амино или полигалогенС1-4алкил;
R7 представляет моноциклический, бициклический или трициклический насыщенный карбоцикл; моноциклический, бициклический или трициклический частично насыщенный карбоцикл; моноциклический, бициклический или трициклический ароматический карбоцикл; моноциклический, бициклический или трициклический насыщенный гетероцикл; моноциклический, бициклический или трициклический частично насыщенный гетероцикл; или моноциклический, бициклический или трициклический ароматический гетероцикл; где каждая указанная карбоциклическая или гетероциклическая кольцевая система может быть, когда это возможно, необязательно замещена одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбирают из галогена, гидрокси, меркапто, С1-6алкила, гидроксиС1-6алкила, аминоС1-6алкила, моно- или ди(С1-6алкил)аминоС1-6алкила, формила, С1-6алкилкарбонила, С3-7циклоалкила, С1-6алкилокси, С1-6алкилоксикарбонила, С1-6алкилтио, циано, нитро, полигалогенС1-6алкила, полигалогенС1-6алкилокси, аминокарбонила, -СН(=N-O-R8), R7а, -Х3-R7а или R7а-С1-4алкандиила;
R7а представляет моноциклический, бициклический или трициклический насыщенный карбоцикл; моноциклический, бициклический или трициклический частично насыщенный карбоцикл; моноциклический, бициклический или трициклический ароматический карбоцикл; моноциклический, бициклический или трициклический насыщенный гетероцикл; моноциклический, бициклический или трициклический частично насыщенный гетероцикл; или моноциклический, бициклический или трициклический ароматический гетероцикл; где каждая указанная карбоциклическая или гетероциклическая кольцевая система может быть необязательно замещена одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбирают из галогена, гидрокси, меркапто, С1-6алкила, гидроксиС1-6алкила, аминоС1-6алкила, моно- или ди(С1-6алкил)аминоС1-6алкила, формила, С1-6алкилкарбонила, С3-7циклоалкила, С1-6алкилокси, С1-6алкилоксикарбонила, С1-6алкилтио, циано, нитро, полигалогенС1-6алкила, полигалогенС1-6алкилокси, аминокарбонила, -СН(=N-O-R8);
R8 представляет водород, С1-4алкил, необязательно замещенный арилом, или арил;
R9 и R10 каждый независимо представляет водород; гидрокси; С1-6алкил; С1-6алкилокси; С1-6алкилкарбонил; С1-6алкилоксикарбонил; амино; моно- или ди(С1-6алкил)амино; моно- или ди(С1-6алкил)аминокарбонил; -СН(=NR11) или R7, где каждая из вышеуказанных С1-6алкильных групп может быть, необязательно и каждая в отдельности, замещена одним или двумя заместителями, каждый из которых независимо выбирают из гидрокси, С1-6алкилокси, гидроксиС1-6алкилокси, карбоксила, С1-6алкилоксикарбонила, циано, амино, имино, моно- или ди(С1-4алкил)амино, полигалогенметила, полигалогенметилокси, полигалогенметилтио, -S(=O)pR6, -NH-S(=O)pR6, -C(=O)R6, -NHC(=O)H, -C(=O)NHNH2, -NHC(=O)R6, -C(=NH)R6 или R7; или
R9 и R10 могут быть взяты вместе с образованием двухвалентного или трехвалентного радикала формулы
R11 представляет циано; С1-4алкил, необязательно замещенный С1-4алкилокси, циано, амино, моно- или ди(С1-4алкил)амино или аминокарбонилом; С1-4алкилкарбонил; С1-4алкилоксикарбонил; аминокарбонил; моно- или ди(С1-4алкил)аминокарбонил;
R12 представляет водород или С1-4алкил;
R13 и R14 каждый независимо представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом; С2-6алкенил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом; С2-6-алкинил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом;
R15 представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом;
R16 представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом, или R7;
р равно 1 или 2;
арил представляет фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, С1-6алкила, гидроксиС1-6алкила, аминоС1-6алкила, моно- или ди(С1-6алкил)аминоС1-6-алкила, С1-6алкилкарбонила, С3-7циклоалкила, С1-6алкилокси, С1-6алкилоксикарбонила, С1-6алкилтио, циано, нитро, полигалогенС1-6алкила, полигалогенС1-6алкилокси, аминокарбонила, R7 или -Х3-R7.
Настоящее изобретение также относится к применению соединения формулы (I), его N-оксида, фармацевтически приемлемой аддитивной соли, четвертичного амина или стереохимически изомерной формы для получения лекарственного средства для лечения или предупреждения ВИЧ-инфекции, в частности, для лечения ВИЧ-инфекции.
Используемый в данном описании выше и далее термин «С1-4алкил», обозначающий группу или часть группы, определяет насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 1 до 4 атомов углерода, такие как метил, этил, пропил, 1-метилэтил, бутил; термин «С1-6алкил», обозначающий группу или часть группы, определяет насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 1 до 6 атомов углерода, такие как группы, указанные для С1-4алкила, и пентил, гексил, 2-метилбутил и т.д.; термин «С2-6алкил», обозначающий группу или часть группы, определяет насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 2 до 6 атомов углерода, такие как этил, пропил, 1-метилэтил, бутил, пентил, гексил, 2-метилбутил и т.д.; термин «С1-4-алкандиил» определяет насыщенные двухвалентные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 1 до 4 атомов углерода, такие как метилен, 1,2-этандиил или 1,2-этилиден, 1,3-пропандиил или 1,3-пропилиден, 1,4-бутандиил или 1,4-бутилиден, и т.п.; «С2-6алкандиил» определяет насыщенные двухвалентные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 2 до 6 атомов углерода, такие как 1,2-этандиил или 1,2-этилиден, 1,3-пропандиил или 1,3-пропилиден, 1,4-бутандиил или 1,4-бутилиден, 1,5-пентандиил или 1,5-пентилиден, 1,6-гександиил или 1,6-гексилиден, и т.п.; термин «С3-7циклоалкил» является общим термином для циклопропила, циклобутила, циклопентила, циклогексила и циклогептила; «С2-6алкенил» определяет углеводородные радикалы с прямой или разветвленной цепью, содержащие от 2 до 6 атомов углерода и имеющие двойную связь, такие как этенил, пропенил, бутенил, пентенил, гексенил и т.п.; «С2-6алкинил» определяет углеводородные радикалы с прямой или разветвленной цепью, содержащие от 2 до 6 атомов углерода и имеющие тройную связь, такие как этинил, пропинил, бутинил, пентинил, гексинил и т.п.; моноциклический, бициклический или трициклический насыщенный карбоцикл представляет кольцевую систему, состоящую из 1, 2 или 3 колец, причем указанная кольцевая система составлена только из атомов углерода, и указанная кольцевая система содержит только простые связи; моноциклический, бициклический или трициклический частично насыщенный карбоцикл представляет кольцевую систему, состоящую из 1, 2 или 3 колец, причем указанная кольцевая система составлена только из атомов углерода и содержит, по меньшей мере, одну двойную связь, при условии, что кольцевая система не является ароматической кольцевой системой; моноциклический, бициклический или трициклический ароматический карбоцикл представляет ароматическую кольцевую систему, состоящую из 1, 2 или 3 колец, причем указанная кольцевая система составлена только из атомов углерода; термин «ароматическая» хорошо известен специалистам в данной области техники и обозначает циклически конъюгированные системы с 4n+2 электронами, т.е. с 6, 10, 14 и т.д. π-электронами (правило Хюккеля); моноциклический, бициклический или трициклический насыщенный гетероцикл представляет кольцевую систему, состоящую из 1, 2 или 3 колец и содержащую, по меньшей мере, один гетероатом, выбранный из O, N или S, причем указанная кольцевая система содержит только простые связи; моноциклический, бициклический или трициклический частично насыщенный гетероцикл представляет кольцевую систему, состоящую из 1, 2 или 3 колец и содержащую, по меньшей мере, один гетероатом, выбранный из O, N или S, и, по меньшей мере, одну двойную связь, при условии, что кольцевая система не является ароматической кольцевой системой; моноциклический, бициклический или трициклический ароматический гетероцикл представляет ароматическую кольцевую систему, состоящую из 1, 2 или 3 колец и содержащую, по меньшей мере, один гетероатом, выбранный из O, N или S.
Конкретными примерами моноциклических, бициклических или трициклических насыщенных карбоциклов являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, бицикло[4,2,0]октанил, циклононанил, циклодеканил, декагидронафталенил, тетрадекагидроантраценил и т.п.
Конкретными примерами моноциклических, бициклических или трициклических частично насыщенных карбоциклов являются циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил, бицикло[4,2,0]октенил, циклононенил, циклодеценил, октагидронафталенил, 1,2,3,4-тетрагидронафталенил, 1,2,3,4,4а,9,9а,10-октагидроантраценил и т.п.
Конкретными примерами моноциклических, бициклических или трициклических ароматических карбоциклов являются фенил, нафталенил, антраценил.
Конкретными примерами моноциклических, бициклических или трициклических насыщенных гетероциклов являются тетрагидрофуранил, пирролидинил, диоксоланил, имидазолидинил, тиазолидинил, тетрагидротиенил, дигидрооксазолил, изотиазолидинил, изоксазолидинил, оксадиазолидинил, триазолидинил, тиадиазолидинил, пиразолидинил, пиперидинил, гексагидропиримидинил, гексагидропиразинил, диоксанил, морфолинил, дитианил, тиоморфолинил, пиперазинил, тритианил, декагидрохинолинил, октагидроиндолил и т.п.
Конкретными примерами моноциклических, бициклических или трициклических частично насыщенных гетероциклов являются пирролинил, имидазолинил, пиразолинил, 2,3-дигидробензофуранил, 1,3-бензодиоксолил, 2,3-дигидро-1,4-бензодиоксинил, индолинил и т.п.
Конкретными примерами моноциклических, бициклических или трициклических ароматических гетероциклов являются азетил, оксетилиденил, пирролил, фурил, тиенил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тиадиазолил, оксадиазолил, тетразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, пиранил, бензофурил, изобензофурил, бензотиенил, изобензотиенил, индолизинил, индолил, изоиндолил, бензоксазолил, бензимидазолил, индазолил, бензизоксазолил, бензизотиазолил, бензопиразолил, бензоксадиазолил, бензотиадиазолил, бензотриазолил, пуринил, хинолинил, изохинолинил, циннолинил, хинолизинил, фталазинил, хиноксалинил, хиназолинил, нафтиридинил, птеридинил, бензопиранил, пирролопиридил, тиенопиридил, фуропиридил, изотиазолопиридил, тиазолопиридил, изоксазолопиридил, оксазолопиридил, пиразолопиридил, имидазопиридил, пирролопиразинил, тиенопиразинил, фуропиразинил, изотиазолопиразинил, тиазолопиразинил, изоксазолопиразинил, оксазолопиразинил, пиразолопиразинил, имидазопиразинил, пирролопиримидинил, тиенопиримидинил, фуропиримидинил, изотиазолопиримидинил, тиазолопиримидинил, изоксазолопиримидинил, оксазолопиримидинил, пиразолопиримидинил, имидазопиримидинил, пирролопиридазинил, тиенопиридазинил, фуропиридазинил, изотиазолопиридазинил, тиазолопиридазинил, изоксазолопиридазинил, оксазолопиридазинил, пиразолопиридазинил, имидазопиридазинил, оксадиазолопиридил, тиадиазолопиридил, триазолопиридил, оксадиазолопиразинил, тиадиазолопиразинил, триазолопиразинил, оксадиазолопиримидинил, тиадиазолопиримидинил, триазолопиримидинил, оксадиазолопиридазинил, тиадиазолопиридазинил, триазолопиридазинил, имидазооксазолил, имидазотиазолил, имидазоимидазолил, изоксазолотриазинил, изотиазолотриазинил, пиразолотриазинил, оксазолотриазинил, тиазолотриазинил, имидазотриазинил, оксадиазолотриазинил, тиадиазолотриазинил, триазолотриазинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил и т.п.
Используемый в данном описании ранее символ (=О) служит для образования карбонильной группы, если присоединен к атому углерода, сульфоксидной группы, если присоединен к атому серы, и сульфонильной группы, если два таких символа присоединены к атому серы.
Термин «галоген» является общим для фтора, хлора, брома и йода. Используемый в данном описании выше и далее термин «полигалогенметил» как обозначение группы или части группы определяет моно- или полигалогензамещенный метил, в частности, метил, замещенный одним или несколькими атомами фтора, например, дифторметил или трифторметил; термины «полигалогенС1-4алкил» или «полигалогенС1-6алкил» как обозначения группы или части группы определяют моно- или полигалогензамещенный С1-4алкил или С1-6алкил, например, группы, определенные в галогенметиле, 1,1-дифторэтиле и т.п. В рамках определений «полигалогенметил», «полигалогенС1-4алкил» или «полигалогенС1-6алкил» в случае, когда к алкильной группе присоединено несколько атомов галогена, такие атомы могут быть одинаковыми или различными.
Термин «гетероцикл» в определениях R7 или R7a предназначен для охвата всех возможных изомерных форм гетероциклов, например, пирролил включает 1Н-пирролил и 2Н-пирролил.
Карбоцикл или гетероцикл в определении R7 или R7a могут быть присоединены к остальной части молекулы формулы (I) через любой кольцевой атом углерода или гетероатом соответствующим образом, если не указано иное. Так, например, когда гетероциклом является имидазолил, он может представлять собой 1-имидазолил, 2-имидазолил, 4-имидазолил и т.п., или когда карбоциклом является нафталенил, он может представлять собой 1-нафталенил, 2-нафталенил и т.п.
Когда любая переменная (например, R7, R6) встречается несколько раз в любом элементе, каждая такая переменная имеет независимое значение.
Черточки, отходящие от заместителей к кольцевым системам, указывают, что связь может быть образована с любым из подходящих кольцевых атомов.
Для лечебного применения соли соединений формулы (I) представляют собой соли, в которых противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, также могут найти применение, например, при получении или очистке фармацевтически приемлемого соединения. Все соли, являются ли они фармацевтически приемлемыми или нет, входят в объем настоящего изобретения.
Фармацевтически приемлемые аддитивные соли, указанные выше, включают терапевтически активные нетоксичные формы аддитивных солей, которые способны образовывать соединения формулы (I). Такие соли могут быть обычно получены обработкой формы основания такими соответствующими кислотами, как неорганические кислоты, например, галоидоводородные кислоты, например, хлористоводородная, бромистоводородная и т.п.; серная кислота; азотная кислота; фосфорная кислота и т.п.; или органические кислоты, например, уксусная, пропановая, гидроксиуксусная, 2-гидроксипропановая, 2-оксопропановая, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, 2-гидрокси-1,2,3-пропантрикарбоновая, метансульфоновая, этансульфоновая, бензолсульфоновая, 4-метилбензолсульфоновая, циклогексансульфаминовая, 2-гидроксибензойная, 4-амино-2-гидроксибензойная и подобные кислоты. Наоборот, солевая форма может быть преобразована в форму свободного основания обработкой щелочью.
Соединения формулы (I), содержащие кислотные протоны, могут быть преобразованы в формы их терапевтически активных нетоксичных солей присоединения металла или амина обработкой соответствующими органическими и неорганическими основаниями. Подходящие солевые формы оснований включают, например, аммониевые соли, соли щелочных и щелочноземельных металлов, например, литиевые, натриевые, калиевые, магниевые, кальциевые соли и т.п., соли органических оснований, например, первичных, вторичных и третичных алифатических и ароматических аминов, таких как метиламин, этиламин, пропиламин, изопропиламин, четыре изомера бутиламина, диметиламин, диэтиламин, диэтаноламин, дипропиламин, диизопропиламин, ди-н-бутиламин, пирролидин, пиперидин, морфолин, триметиламин, триэтиламин, трипропиламин, хинуклидин, пиридин, хинолин и изохинолин, бензатин, N-метил-D-глюкамин, 2-амино-2-(гидроксиметил)-1,3-пропандиол, соли гидрабамина и соли с аминокислотами, такими как, например, аргинин, лизин и т.п. Наоборот, солевая форма может быть преобразована обработкой кислотой в форму свободной кислоты.
Термин «аддитивная соль» также включает гидраты и формы присоединения растворителей, которые способны образовывать соединения формулы (I). Примерами таких форм являются, например, гидраты, алкоголяты и т.п.
Термин «четвертичный амин», используемый в данном описании ранее, определяет соли четвертичного аммония, которые способны образовывать соединения формулы (I) за счет взаимодействия между основным азотом соединения формулы (I) и соответствующим агентом кватернизации, таким как, например, необязательно замещенный алкилгалогенид, арилгалогенид или арилалкилгалогенид, например, метилйодид или бензилйодид. Также можно использовать другие реагенты с легко уходящими группами, такие как алкилтрифторметансульфонаты, алкилметансульфонаты и алкил-п-тоуолсульфонаты. Четвертичный амин имеет положительно заряженный азот. Фармацевтически приемлемые противоионы включают ионы хлора, брома, йода, трифторацетат и ацетат. Ввести выбранный противоион можно с использованием ионообменных смол.
N-Оксидные формы соединений настоящего изобретения включают соединения формулы (I), в которых один или несколько третичных атомов азота окислены до так называемого N-оксида.
Следует иметь в виду, что некоторые соединения формулы (I) и их N-оксиды, аддитивные соли, четвертичные амины и стереохимически изомерные формы могут содержать один или несколько центров хиральности и существовать в виде стереохимически изомерных форм.
Термин «стереохимически изомерные формы», используемый в данном описании, определяет все возможные стереоизомерные формы, которые могут иметь соединения формулы (I) и их N-оксиды, аддитивные соли, четвертичные амины или физиологически функциональные производные. Если не упомянуто или не указано иное, химическая формула соединений обозначает смесь всех возможных стереохимически изомерных форм, причем указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры, а также каждую из отдельных изомерных форм формулы (I) и их N-оксидов, солей, сольватов или четвертичных аминов, по существу свободных, т.е. ассоциированных менее чем с 10%, предпочтительно, менее чем с 5%, в частности, менее чем с 2% и наиболее предпочтительно, менее чем с 1%, других изомеров. Таким образом, когда соединение формулы (I), например, характеризуется как (Е), это означает, что соединение по существу свободно от (Z)-изомера.
В частности, стереогенные центры могут иметь R- или S-конфигурацию; заместители двухвалентных циклических (частично) насыщенных радикалов могут иметь или цис- или транс-конфигурацию. Соединения, включающие двойные связи, могут иметь Е (entegegen) или Z (zusammen) стереохимию по указанной двойной связи. Термины цис, транс, R, S, E и Z хорошо известны специалистам в данной области техники.
Очевидно подразумевается, что стереохимически изомерные формы соединений формулы (I) охватываются объемом данного изобретения.
Некоторые соединения формулы (I) могут также существовать в их таутомерных формах. Подразумевается, что такие формы хотя специально не указываются в приведенной выше формуле, входят в объем настоящего изобретения. Таким образом, настоящее изобретение включает следующие соединения:
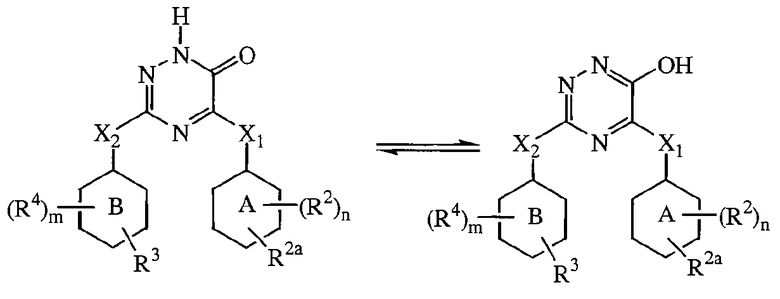
Когда бы ни использовался термин «соединения формулы (I)» или его любой уточняющий термин, такой как «соединения формулы (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2) или (I-2-3)», это означает, что также имеются в виду их N-оксидные формы, их соли, их четвертичные амины и их стереохимически изомерные формы. Особый интерес представляют такие соединения формулы (I), которые являются стереохимически чистыми.
Когда бы ни указывалось в данном описании ранее или впоследствии, что заместители могут быть выбраны, каждый независимо, из перечня ряда определений, как например, для R9 и R10, предполагаются все возможные сочетания, которые возможны химически или которые приводят к химически устойчивым молекулам.
Настоящее изобретение также относится к соединению формулы
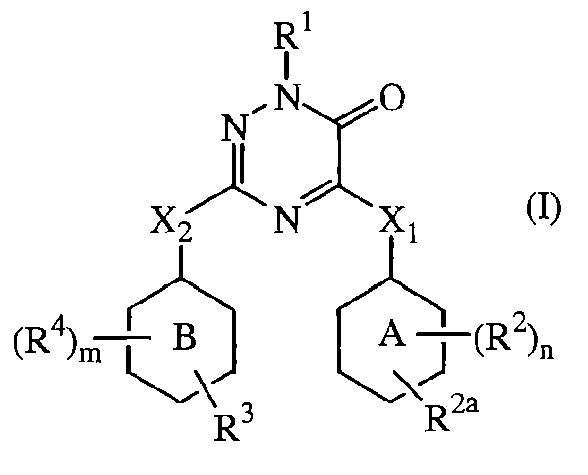
его N-оксиду, фармацевтически приемлемой аддитивной соли, четвертичному амину или стереохимически изомерной форме, где в указанной формуле
кольцо А представляет фенил, пиридил, пиридазинил, пиримидинил или пиразинил;
кольцо В представляет фенил, пиридил, пиридазинил, пиримидинил или пиразинил;
n равно 1, 2, 3, и в случае, когда кольцо А представляет фенил, n также может быть равно 4;
m равно 1, 2, 3, и в случае, когда кольцо В представляет фенил, m также может быть равно 4;
R1 представляет водород; арил; формил; С1-6алкилкарбонил; С1-6-алкилоксикарбонил; С1-6алкил, необязательно замещенный R5; или С1-6алкилоксиС1-6алкилкарбонил, замещенный С1-6алкилоксикарбонилом;
каждый R2 независимо представляет водород; гидрокси; галоген; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С3-7циклоалкил; С1-6алкилокси; С1-6алкилоксикарбонил; С1-6алкилкарбонилокси; карбоксил; циано; нитро; амино; моно- или ди(С1-6алкил)амино; полигалогенС1-4алкил; полигалогенС1-4алкилокси; полигалогенС1-4алкилтио; -S(=O)pR6; -NH-S(=O)pR6; -С(=О)R6; -NHC(=O)H; -C(=O)NHNH2; NHC(=O)R6; C(=NH)R6; или R7;
R2а представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1- 6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; -C(=N-O-R8)-С1-4алкил; R7 или -X3-R7;
Х1 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -С1-4алкандиил-; -СНОН-; -S-; -S(=O)p-; -X4-С1-4алкандиил-; -С1-4алкандиил-X4-; или -С1-4алкандиил-X4-С1-4алкандиил-;
Х2 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -С1-4алкандиил-; -СНОН-; -S-; -S(=O)p-; -X4-С1-4алкандиил-; -С1-4алкандиил-X4-; или -С1-4алкандиил-X4-С1-4алкандиил-;
Х3 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -S-; -S(=O)p-; -X4а-С1-4алкандиил-; -С1-4алкандиил-X4b-, -С1-4алкандиил-X4а-С1-4алкандиил-; или -С(=N-OR8)-С1-4алкандиил-;
Х4 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -СНОН-; -S- или -S(=O)p-;
Х4а представляет -NR1-; -NH-NH-; -N=N-; -C(=O)-; -S- или -S(=O)p-;
Х4b представляет -NH-NH-; -N=N-; -O-; -C(=O)-; -S- или -S(=O)p-;
R3 представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; -C(=N-O-R8)-С1-4алкил; R7 или -X3-R7;
каждый R4 независимо представляет водород; гидрокси; галоген; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С3-7циклоалкил; С1-6алкилокси; С1-6алкилоксикарбонил; С1-6алкилкарбонилокси; карбоксил; циано; нитро; амино; моно- или ди(С1-6алкил)амино; полигалогенС1-4алкил; полигалогенС1-4алкилокси; полигалогенС1-4алкилтио; -S(=O)pR6; -NH-S(=O)pR6; -С(=О)R6; -NHC(=O)H; -C(=O)NHNH2; NHC(=O)R6; C(=NH)R6; или R7;
R5 представляет формил, циано, аминокарбонил, моно- или ди(С1-4алкил)аминокарбонил, гидрокси, С1-6алкилкарбонил, С1-6алкилоксикарбонил или С1-6алкилкарбонилокси;
R6 представляет С1-4алкил, амино, моно- или ди(С1-4алкил)амино или полигалогенС1-4алкил;
R7 представляет моноциклический, бициклический или трициклический насыщенный карбоцикл; моноциклический, бициклический или трициклический частично насыщенный карбоцикл; моноциклический, бициклический или трициклический ароматический карбоцикл; моноциклический, бициклический или трициклический насыщенный гетероцикл; моноциклический, бициклический или трициклический частично насыщенный гетероцикл; или моноциклический, бициклический или трициклический ароматический гетероцикл; где каждая указанная карбоциклическая или гетероциклическая кольцевая система может быть, когда это возможно, необязательно замещена одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбирают из галогена, гидрокси, меркапто, С1-6алкила, гидроксиС1-6алкила, аминоС1-6алкила, моно- или ди(С1-6алкил)аминоС1-6алкила, формила, С1-6алкилкарбонила, С3-7циклоалкила, С1-6алкилокси, С1-6алкилоксикарбонила, С1-6алкилтио, циано, нитро, полигалогенС1-6алкила, полигалогенС1-6алкилокси, аминокарбонила, -СН(=N-O-R8), R7а, -Х3-R7а или R7а-С1-4алкандиила;
R7а представляет моноциклический, бициклический или трициклический насыщенный карбоцикл; моноциклический, бициклический или трициклический частично насыщенный карбоцикл; моноциклический, бициклический или трициклический ароматический карбоцикл; моноциклический, бициклический или трициклический насыщенный гетероцикл; моноциклический, бициклический или трициклический частично насыщенный гетероцикл; или моноциклический, бициклический или трициклический ароматический гетероцикл; где каждая указанная карбоциклическая или гетероциклическая кольцевая система может быть необязательно замещена одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбирают из галогена, гидрокси, меркапто, С1-6алкила, гидроксиС1-6алкила, аминоС1-6алкила, моно- или ди(С1-6алкил)аминоС1-6алкила, формила, С1-6алкилкарбонила, С3-7циклоалкила, С1-6алкилокси, С1-6алкилоксикарбонила, С1-6алкилтио, циано, нитро, полигалогенС1-6алкила, полигалогенС1-6алкилокси, аминокарбонила, -СН(=N-O-R8);
R8 представляет водород, С1-4алкил, необязательно замещенный арилом, или арил;
R9 и R10 каждый независимо представляет водород; гидрокси; С1-6алкил; С1-6алкилокси; С1-6алкилкарбонил; С1-6алкилоксикарбонил; амино; моно- или ди(С1-6алкил)амино; моно- или ди(С1-6алкил)аминокарбонил; -СН(=NR11) или R7, где каждая из вышеуказанных С1-6алкильных групп может быть, необязательно и каждая в отдельности, замещена одним или двумя заместителями, каждый из которых независимо выбирают из гидрокси, С1-6алкилокси, гидроксиС1-6алкилокси, карбоксила, С1-6алкилоксикарбонила, циано, амино, имино, моно- или ди(С1-4алкил)амино, полигалогенметила, полигалогенметилокси, полигалогенметилтио, -S(=O)pR6, -NH-S(=O)pR6, -C(=O)R6, -NHC(=O)H, -C(=O)NHNH2, -NHC(=O)R6, -C(=NH)R6 или R7; или
R9 и R10 могут быть взяты вместе с образованием двухвалентного или трехвалентного радикала формулы
R11 представляет циано; С1-4алкил, необязательно замещенный С1-4алкилокси, циано, амино, моно- или ди(С1-4алкил)амино или аминокарбонилом; С1-4алкилкарбонил; С1-4алкилоксикарбонил; аминокарбонил; моно- или ди(С1-4алкил)аминокарбонил;
R12 представляет водород или С1-4алкил;
R13 и R14 каждый независимо представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом, С2-6алкенил, необязательно замещенный циано или аминокарбонилом, С2-6алкинил, необязательно замещенный циано или аминокарбонилом;
R15 представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом;
R16 представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом, или R7;
р равно 1 или 2;
арил представляет фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, С1-6алкила, гидроксиС1-6алкила, аминоС1-6алкила, моно- или ди(С1-6алкил)аминоС1-6алкила, С1-6алкилкарбонила, С3-7циклоалкила, С1-6алкилокси, С1-6алкилоксикарбонила, С1-6алкилтио, циано, нитро, полигалогенС1-6алкила, полигалогенС1-6алкилокси, аминокарбонила, R7 или -Х3-R7.
Первым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), имеющие следующую формулу
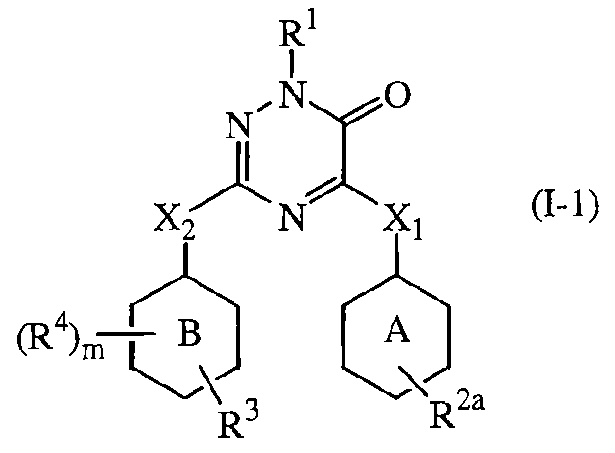
их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы, где в указанной формуле R1, R2a, R3, R4, m, X1, X2, кольцо А и кольцо В имеют значения, указанные выше.
Вторым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), имеющие следующую формулу
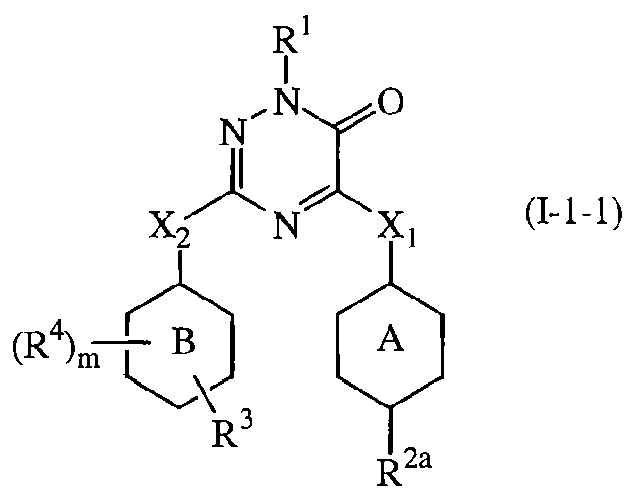
их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы, где в указанной формуле R1, R2a, R3, R4, m, X1, X2, кольцо А и кольцо В имеют значения, указанные выше.
Третьим представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), имеющие следующую формулу
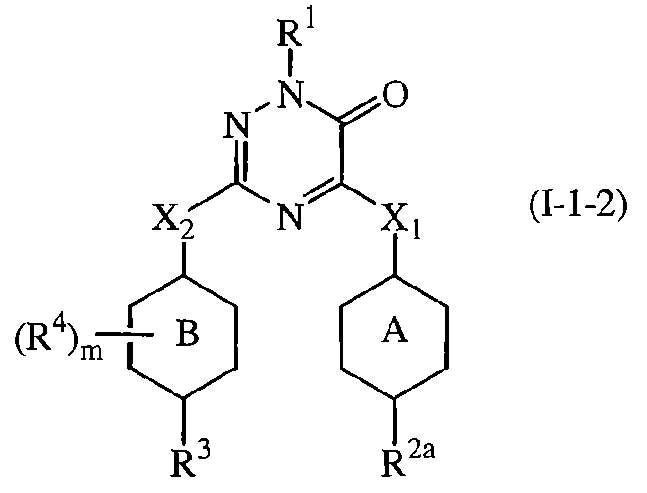
их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы, где в указанной формуле R1, R2a, R3, R4, m, X1, X2, кольцо А и кольцо В имеют значения, указанные выше.
Четвертым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), имеющие следующую формулу
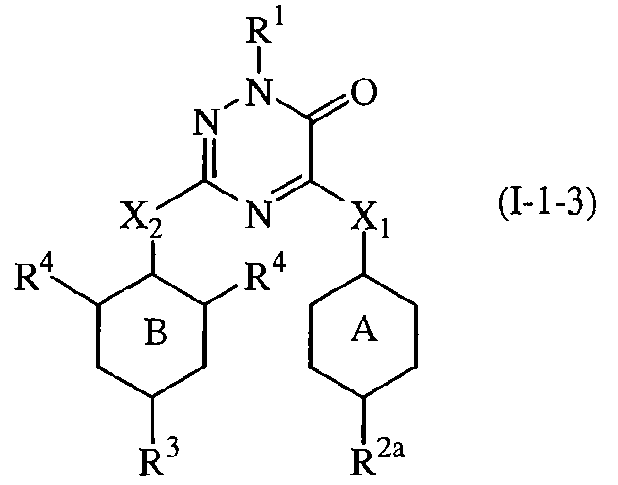
их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы, где в указанной формуле R1, R2a, R3, R4, X1, X2, кольцо А и кольцо В имеют значения, указанные выше, при условии, что R4 является иным, чем водород.
Пятым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), имеющие следующую формулу
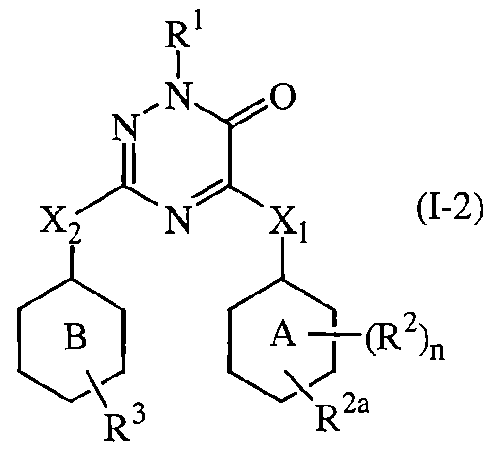
их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы, где в указанной формуле R1, R2a, R2, R3, X1, X2, n, кольцо А и кольцо В имеют значения, указанные выше.
Шестым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), имеющие следующую формулу
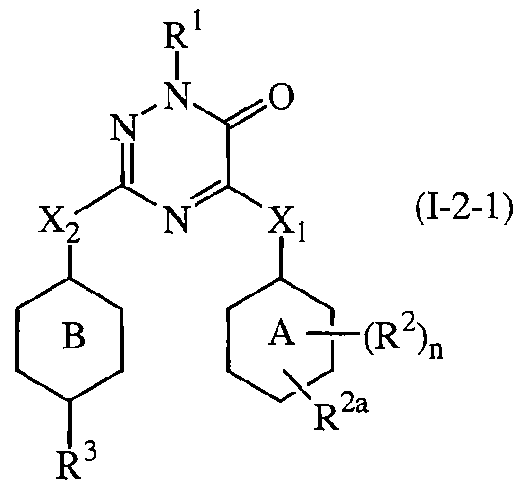
их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы, где в указанной формуле R1, R2a, R2, R3, X1, X2, n, кольцо А и кольцо В имеют значения, указанные выше.
Седьмым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), имеющие следующую формулу
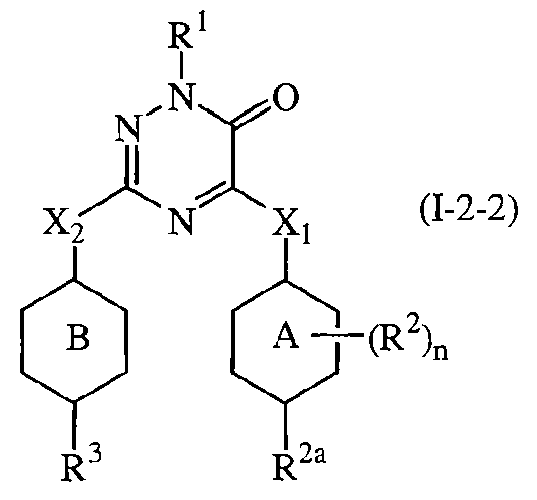
их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы, где в указанной формуле R1, R2a, R2, R3, X1, X2, n, кольцо А и кольцо В имеют значения, указанные выше.
Восьмым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), имеющие следующую формулу
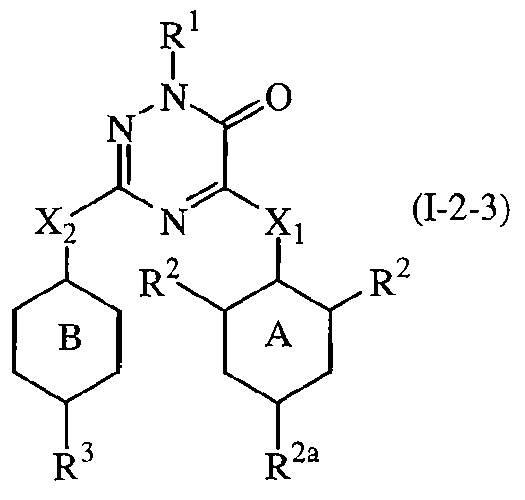
их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы, где в указанной формуле R1, R2a, R2, R3, X1, X2, кольцо А и кольцо В имеют значения, указанные выше, при условии, что R2 является иным, чем водород.
Девятым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3), где кольцо А представляет фенил.
Десятым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3), где кольцо В представляет фенил.
Одиннадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3), где кольцо А и кольцо В представляют фенил.
Двенадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3), в которых в любом случае, когда присутствуют заместители,
кольцо А представляет фенил, пиридил, пиридазинил, пиримидинил или пиразинил;
кольцо В представляет фенил, пиридил, пиридазинил, пиримидинил или пиразинил;
n равно 1, 2, 3, и в случае, когда кольцо А представляет фенил, n также может быть равно 4;
m равно 1, 2, 3, и в случае, когда кольцо В представляет фенил, m также может быть равно 4;
R1 представляет водород; арил; формил; С1-6алкилкарбонил; С1-6алкилоксикарбонил; С1-6алкил, необязательно замещенный R5; или С1-6алкилоксиС1-6алкилкарбонил, замещенный С1-6алкилоксикарбонилом;
каждый R2 независимо представляет водород; гидрокси; галоген; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С3-7циклоалкил; С1-6алкилокси; С1-6алкилоксикарбонил; С1-6алкилкарбонилокси; карбоксил; циано; нитро; амино; моно- или ди(С1-6алкил)амино; полигалогенС1-4алкил; полигалогенС1-4алкилокси; полигалогенС1-4алкилтио; -S(=O)pR6; -NH-S(=O)pR6; -С(=О)R6; -NHC(=O)H; -C(=O)NHNH2; NHC(=O)R6; C(=NH)R6;
R2а представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; или -C(=N-O-R8)-С1-4алкил;
Х1 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -С1-4алкандиил-; -СНОН-; -S-; -S(=O)p-; -X4-С1-4алкандиил-; -С1-4алкандиил-X4-; или -С1-4алкандиил-X4-С1-4алкандиил-;
Х2 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -С1-4алкандиил-; -СНОН-; -S-; -S(=O)p-; -X4-С1-4алкандиил-; -С1-4алкандиил-X4-; или -С1-4алкандиил-X4-С1-4алкандиил-;
Х4 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -СНОН-; -S- или -S(=O)p-;
R3 представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; или -C(=N-O-R8)-С1-4алкил;
каждый R4 независимо представляет водород; гидрокси; галоген; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С3-7циклоалкил; С1-6алкилокси; С1-6алкилоксикарбонил; С1-6алкилкарбонилокси; карбоксил; циано; нитро; амино; моно- или ди(С1-6алкил)амино; полигалогенС1-4алкил; полигалогенС1-4алкилокси; полигалогенС1-4алкилтио; -S(=O)pR6; -NH-S(=O)pR6; -С(=О)R6; -NHC(=O)H; -C(=O)NHNH2; NHC(=O)R6; C(=NH)R6;
R5 представляет формил, циано, аминокарбонил, моно- или ди(С1-4алкил)аминокарбонил, гидрокси, С1-6алкилкарбонил, С1-6алкилоксикарбонил или С1-6алкилкарбонилокси;
R6 представляет С1-4алкил, амино, моно- или ди(С1-4алкил)амино или полигалогенС1-4алкил;
R8 представляет водород, С1-4алкил, арил или арилС1-4алкил;
R9 и R10 каждый независимо представляет водород; гидрокси; С1-6алкил; С1-6алкилокси; С1-6алкилкарбонил; С1-6алкилоксикарбонил; амино; моно- или ди(С1-6алкил)амино; моно- или ди(С1-6алкил)аминокарбонил; -СН(=NR11), где каждая из вышеуказанных С1-6алкильных групп может быть, необязательно и каждая в отдельности, замещена одним или двумя заместителями, каждый из которых независимо выбирают из гидрокси, С1-6алкилокси, гидроксиС1-6алкилокси, карбоксила, С1-6алкилоксикарбонила, циано, амино, имино, моно- или ди(С1-4алкил)амино, полигалогенметила, полигалогенметилокси, полигалогенметилтио, -S(=O)pR6, -NH-S(=O)pR6, -C(=O)R6, -NHC(=O)H, -C(=O)NHNH2, -NHC(=O)R6 или -C(=NH)R6;
R11 представляет циано; С1-4алкил, необязательно замещенный С1-4алкилокси, циано, амино, моно- или ди(С1-4алкил)амино или аминокарбонилом; С1-4алкилкарбонил; С1-4алкилоксикарбонил; аминокарбонил; моно- или ди(С1-4алкил)аминокарбонил;
R12 представляет водород или С1-4алкил;
R13 и R14 каждый независимо представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом; С2-6алкенил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом; С2-6алкинил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом; в частности, С1-6алкил, необязательно замещенный циано или аминокарбонилом, С2-6алкенил, необязательно замещенный циано или аминокарбонилом, С2-6алкинил, необязательно замещенный циано или аминокарбонилом;
R15 представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом; в частности, С1-6алкил, необязательно замещенный циано или аминокарбонилом;
R16 представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом или моно- или ди(С1-4алкил)аминокарбонилом, или R7; в частности, С1-6алкил, необязательно замещенный циано или аминокарбонилом, или R7;
р равно 1 или 2;
арил представляет фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, С1-6алкила, гидроксиС1-6алкила, аминоС1-6алкила, моно- или ди(С1-6алкил)аминоС1-6алкила, С1-6алкилкарбонила, С3-7циклоалкила, С1-6алкилокси, С1-6алкилоксикарбонила, С1-6алкилтио, циано, нитро, полигалогенС1-6алкила, полигалогенС1-6алкилокси, аминокарбонила.
Тринадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3), в которых в каждом случае, когда присутствуют заместители,
кольцо А представляет фенил, пиридил, пиридазинил, пиримидинил или пиразинил; в частности, фенил;
кольцо В представляет фенил, пиридил, пиридазинил, пиримидинил или пиразинил; в частности, фенил;
n равно 1, 2, 3, и в случае, когда кольцо А представляет фенил, n также может быть равно 4;
m равно 1, 2, 3, и в случае, когда кольцо В представляет фенил, m также может быть равно 4;
R1 представляет водород; формил; С1-6алкилкарбонил; С1-6алкилоксикарбонил; или С1-6алкил, необязательно замещенный R5;
каждый R2 независимо представляет водород; гидрокси; галоген; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С3-7циклоалкил; С1-6алкилокси; С1-6алкилоксикарбонил; С1-6алкилкарбонилокси; карбоксил; циано; нитро; амино; моно- или ди(С1-6алкил)амино; полигалогенС1-4алкил; полигалогенС1-4алкилокси; полигалогенС1-4алкилтио; или -С(=О)R6;
R2а представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила;
Х1 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -С1-4алкандиил-; -СНОН-; -S-; -S(=O)p-; -X4-С1-4алкандиил-; -С1-4алкандиил-X4- или -С1-4алкандиил-X4-С1-4алкандиил-;
Х2 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -С1-4алкандиил-; -СНОН-; -S-; -S(=O)p-; -X4-С1-4алкандиил-; -С1-4алкандиил-X4- или -С1-4алкандиил-X4-С1-4алкандиил-;
Х4 представляет -NR1-; -NH-NH-; -N=N-; -O-; -C(=O)-; -СНОН-; -S-; -S(=O)p-;
R3 представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила;
каждый R4 независимо представляет водород; гидрокси; галоген; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси или -С(=О)R6; С3-7циклоалкил; С1-6алкилокси; С1-6алкилоксикарбонил; С1-6алкилкарбонилокси; карбоксил; циано; нитро; амино; моно- или ди(С1-6алкил)амино; полигалогенС1-4алкил; полигалогенС1-4алкилокси; полигалогенС1-4алкилтио; или -С(=О)R6;
R5 представляет формил, циано, аминокарбонил, моно- или ди(С1-4алкил)аминокарбонил, гидрокси, С1-6алкилкарбонил, С1-6алкилоксикарбонил или С1-6алкилкарбонилокси;
R6 представляет С1-4алкил, амино, моно- или ди(С1-4алкил)амино или полигалогенС1-4алкил;
R8 представляет водород или С1-4алкил;
R9 и R10 каждый независимо представляет водород; гидрокси; С1-6алкил; С1-6алкилокси; С1-6алкилкарбонил; С1-6алкилоксикарбонил; амино; моно- или ди(С1-6алкил)амино; моно- или ди(С1-6алкил)аминокарбонил; или -СН(=NR11), где каждая из вышеуказанных С1-6алкильных групп может быть, необязательно и каждая в отдельности, замещена одним или двумя заместителями, каждый из которых независимо выбирают из гидрокси, С1-6алкилокси, гидроксиС1-6алкилокси, карбоксила, С1-6алкилоксикарбонила, циано, амино, имино, моно- или ди(С1-4алкил)амино, полигалогенметила, полигалогенметилокси, полигалогенметилтио или -C(=O)R6;
R11 представляет циано; С1-4алкил, необязательно замещенный С1-4алкилокси, циано, амино, моно- или ди(С1-4алкил)амино или аминокарбонилом; С1-4алкилкарбонил; С1-4алкилоксикарбонил; аминокарбонил или моно- или ди(С1-4алкил)аминокарбонил;
R12 представляет водород или С1-4алкил;
R13 и R14 каждый независимо представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом, или С2-6алкенил, необязательно замещенный циано или аминокарбонилом;
R15 представляет С1-6алкил, необязательно замещенный циано или аминокарбонилом;
R16 представляет С1-6алкил, необязательно циано или аминокарбонилом;
р равно 1 или 2;
арил представляет фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбран из галогена, гидрокси, меркапто, С1-6алкила, гидроксиС1-6алкила, аминоС1-6алкила, моно- или ди(С1-6алкил)аминоС1-6алкила, С1-6алкилкарбонила, С3-7циклоалкила, С1-6алкилокси, С1-6алкилоксикарбонила, С1-6алкилтио, циано, нитро, полигалогенС1-6алкила, полигалогенС1-6алкилокси или аминокарбонила.
Четырнадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых в каждом случае, когда присутствуют заместители,
R2 представляет водород; и
R2а представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом.
Пятнадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых в каждом случае, когда присутствуют заместители,
R4 представляет водород; и
R3 представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом.
Шестнадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых в каждом случае, когда присутствуют заместители,
n равно 1 или 2;
R2 представляет галоген, С1-6алкил; или С1-6алкилокси; и
R2а представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; в частности, R2а представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; более в частном случае R2а представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; даже еще более в частном случае R2а представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом.
Семнадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых в каждом случае, когда присутствуют заместители,
m равно 1 или 2;
R4 представляет галоген, С1-6алкил, С1-6алкилокси; и
R3 представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; в частности, R3 представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; более в частном случае R3 представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; даже еще более в частном случае R3 представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом.
Восемнадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых в каждом случае, когда присутствуют заместители,
R2 представляет водород;
R2а представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом;
m равно 1 или 2;
R4 представляет галоген, С1-6алкил, С1-6алкилокси; и
R3 представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; в частности, R3 представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; более в частном случае R3 представляет циано; аминокарбонил; галоген; С1-6алкил, замещенный циано или аминокарбонилом; С1-6алкилокси; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; даже еще более в частном случае R3 представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; в особенности, циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом.
Девятнадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых в каждом случае, когда присутствуют заместители,
n равно 1 или 2;
R2 представляет галоген, С1-6алкил или С1-6алкилокси; и
R2а представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила, -C(=O)-О-полигалогенС1-6алкила или R7; в частности, R2а представляет циано; аминокарбонил; амино; галоген; NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)-R15; -CH=N-NH-C(=O)-R16; С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилокси, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С1-6алкилоксиС1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; С2-6алкинил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена, циано, гидрокси, NR9R10, -C(=O)-NR9R10, -C(=O)-С1-6алкила, -C(=O)-О-С1-6алкила, -C(=O)-полигалогенС1-6алкила или -C(=O)-О-полигалогенС1-6алкила; более в частном случае R2а представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С1-6алкилокси; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; даже более в частном случае R2а представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; в особенности, циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом;
R4 представляет водород; и
R3 представляет циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом; или С2-6алкинил, замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; С1-6алкил, замещенный циано или аминокарбонилом; С2-6алкенил, замещенный циано или аминокарбонилом.
Двадцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых в каждом случае, когда присутствуют заместители, по меньшей мере, один из R2 или R4 является иным, чем водород. В частности, когда R2 является иным, чем водород, тогда R4 представляет собой водород, или когда R4 является иным, чем водород, тогда R2 представляет собой водород.
Двадцать первым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, к которым применимо одно или, где возможно, несколько из следующих условий:
а) m равно 1, 2 или 3, в частности, 2 или 3, более в частном случае, 2, даже более в частном случае m равно 2, и указанные два заместителя R4 находятся в положениях 2 и 6 (орто-положение) относительно линкера Х2;
b) m равно 1, и R4 представляет собой водород; в частности, m равно 1, R4 представляет собой водород, и R3 представляет собой циано или аминокарбонил;
с) Х1 представляет собой -NR1-, -O-, -C(=O)-, C1-4алкандиил, -СНОН-, -S(=O)p- или S; в частности, -NR1-, O или S;
d) n равно 1, и R2 представляет собой водород; в частности, n равно 1, R2 представляет собой водород, и R2а представляет собой циано или аминокарбонил;
f) n равно 1, 2 или 3, в частности, 2 или 3, более в частном случае, 2, даже более в частном случае n равно 2, и указанные два заместителя R2 находятся в положениях 2 и 6 (орто-положение) относительно линкера Х1;
g) n равно 2, и R2а представляет собой циано; галоген; аминокарбонил; C1-6алкилокси; C1-6алкил, необязательно замещенный циано или аминокарбонилом; или C2-6алкенил, необязательно замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; C1-6алкил, необязательно замещенный циано или аминокарбонилом; или C2-6алкенил, необязательно замещенный циано или аминокарбонилом;
h) R2а представляет собой циано; аминокарбонил; C1-6алкил, замещенный циано или аминокарбонилом; или C2-6алкенил, замещенный циано или аминокарбонилом; в частности, циано;
i) m равно 2, и R3 представляет собой циано; галоген; аминокарбонил; C1-6алкилокси; C1-6алкил, необязательно замещенный циано или аминокарбонилом; или C2-6алкенил, необязательно замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; C1-6алкил, необязательно замещенный циано или аминокарбонилом; или C2-6алкенил, необязательно замещенный циано или аминокарбонилом.
Двадцать вторым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых R1 представляет водород или C1-6алкил, необязательно замещенный R5; в частности, R1 представляет водород или C1-6алкил, необязательно замещенный циано, аминокарбонилом или гидрокси; более в частном случае R1 представляет собой водород.
Двадцать третьим представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых R2 представляет водород, галоген, C1-6алкил или C1-6алкилокси; в частности, водород, галоген или C1-6алкил.
Двадцать четвертым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых R2а представляет циано; аминокарбонил; галоген; C1-6алкил, необязательно замещенный циано или аминокарбонилом; C1-6алкилокси; или C2-6алкенил, замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; галоген; C1-6алкил; или C2-6алкенил, замещенный циано или аминокарбонилом; более в частном случае, циано; аминокарбонил; C1-6алкил; или C2-6алкенил, замещенный циано или аминокарбонилом.
Двадцать пятым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I- 1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых R3 представляет циано; аминокарбонил; галоген; C1-6алкил, необязательно замещенный циано или аминокарбонилом; C1-6алкилокси или C2-6алкенил, замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; галоген; C1-6алкил; или C2-6алкенил, замещенный циано или аминокарбонилом; более в частном случае, циано; аминокарбонил; C1-6алкил; или C2-6алкенил, замещенный циано или аминокарбонилом.
Двадцать шестым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых R4 представляет водород; галоген; C1-6алкил или C1-6алкилокси; в частности, водород; галоген или C1-6алкил.
Двадцать седьмым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых Х1 представляет -NR1-; -O-; -S; или -S(=O)p-; в частности, -NR1-; -O- или -S-.
Двадцать восьмым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых Х2 представляет -NR1-; -O-; -S- или -S(=O)p-.
Двадцать девятым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых R5 представляет циано, аминокарбонил или гидрокси.
Тридцатым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых р равно 2.
Тридцать первым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых R3 представляет собой R7, NR13R14, -C(=O)R15, -CH=N-NH-C(=O)R16, -C(=O)NHR13, -C(=O)NR13R14, -C(=N-OR8)-С1-4алкил, С1-6алкил, замещенный циано, С1-6алкил, дважды замещенный циано, С1-6алкил, замещенный NR9R10, С1-6алкил, замещенный гидрокси и циано, С1-6алкил, замещенный гидрокси и R7, С1-6алкилоксиС1-6алкил, С1-6алкилоксиС1-6алкил, замещенный циано, С2-6алкенил, замещенный R7, С2-6алкенил, замещенный циано, С2-6алкенил, дважды замещенный циано, С2-6алкенил, замещенный циано и R7, С2-6алкенил, замещенный циано и -С(=О)-С1-6алкилом, С2-6алкенил, замещенный циано и галогеном, С2-6алкенил, замещенный -С(=О)-NR9R10, С2-6алкенил, замещенный галогеном, С2-6алкенил, дважды замещенный галогеном, или С2-6алкенил, замещенный NR9R10.
Тридцать вторым представляющим интерес воплощением настоящего изобретения являются такие соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых
кольцо А представляет фенил;
кольцо В представляет фенил;
n равно 1, 2 или 3;
m равно 1, 2 или 3;
R1 представляет водород, С1-6алкил, необязательно замещенный R5; в частности, водород или С1-6алкил, необязательно замещенный циано, аминокарбонилом или гидрокси;
каждый R2 независимо представляет водород; галоген; С1-6алкил или С1-6алкилокси;
R2а представляет циано; аминокарбонил; галоген; С1-6алкил, необязательно замещенный циано или аминокарбонилом; С1-6алкилокси, необязательно замещенный циано или аминокарбонилом; или С2-6алкенил, необязательно замещенный циано или аминокарбонилом; в частности, циано; аминокарбонил; С1-6алкил или С2-6алкенил, необязательно замещенный циано или аминокарбонилом;
Х1 представляет -NR1-; -O-; -S- или -S(=O)p-; в частности, -NR1-; -O- или -S-;
Х2 представляет -NR1-; -O-; -S- или -S(=O)p-;
R3 представляет циано; аминокарбонил; галоген; С1-6алкил, необязательно замещенный циано или аминокарбонилом; С1-6алкилокси, необязательно замещенный циано или аминокарбонилом; или С2-6алкенил, необязательно замещенный циано или аминокарбонилом;
каждый R4 независимо представляет водород; галоген; С1-6алкил или С1-6алкилокси;
р равно 2.
Тридцать третьим представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I) или любая их подгруппа, указанная в данном описании выше как воплощение, представляющее интерес, в которых n равно 1, и R2 представляет собой водород, R2а представляет собой циано, m равно 2, и R3 представляет собой С1-6алкил, замещенный циано, или С2-6алкенил, замещенный циано, предпочтительно, цианоэтил или циановинил.
Тридцать четвертым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), в которых n равно 2, R3 представляет собой циано, m равно 1, и R4 представляет собой водород, и R2а представляет собой С1-6алкил, замещенный циано, или С2-6алкенил, замещенный циано, предпочтительно, цианоэтил или циановинил.
Тридцать пятым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), в которых R2а представляет собой С1-6алкил, замещенный циано, или С2-6алкенил, замещенный циано, предпочтительно, цианоэтил или циановинил, более предпочтительно, цианоэтил.
Тридцать шестым представляющим интерес воплощением настоящего изобретения являются такие соединения формулы (I), в которых R3 представляет собой С1-6алкил, замещенный циано, или С2-6алкенил, замещенный циано, предпочтительно, цианоэтил или циановинил, более предпочтительно, цианоэтил.
Предпочтительными соединениями настоящего изобретения являются соединения 16, 17, 20, 21, 4, 23, 24, 10, 5, 11, 25, 1, 26, 27, 30, 31, 33, 8, 36, 37, 38, 39, 2, 40, 41, 42, 43, 14, 9, 15, 46, 47, 48, 49, 50, 51, 53, 3, 56, 55, 62, 69, 70, 71, 72, 73, 74, 75, 77, 78, 67 (см. таблицу 1, приведенную в данном описании ниже), их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины или стереохимически изомерные формы.
В общем случае, соединения формулы (I), в которых R1 представляет водород, причем указанные соединения представлены формулой (I-a), могут быть получены взаимодействием промежуточного соединения формулы (II), где W1 представляет подходящую уходящую группу, такую как, например, галоген, например, хлор и т.п., с подходящей кислотой, такой как, например, уксусная кислота, необязательно в присутствии йодида натрия или воды.
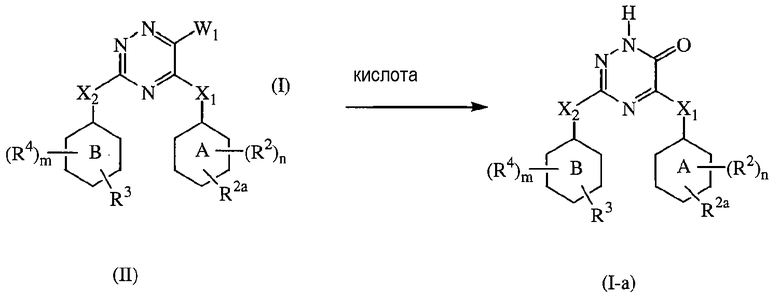
Соединения формулы (I), где R1 представляет необязательно замещенный С1-6алкил, причем указанный R1 представлен формулой R1а и указанные соединения представлены формулой (I-b), могут быть получены взаимодействием соединения формулы (I-a) с промежуточным соединением формулы (III), где W2 представляет подходящую уходящую группу, такую как, например, галоген, например, хлор, бром и т.п., в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, тетрагидрофуран.
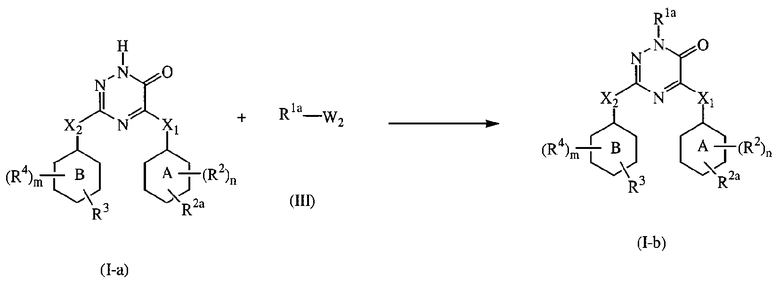
Соединения формулы (I-b), где R1а представляет С1-6алкил, замещенный циано, причем указанные соединения представлены формулой (I-b-1), могут быть получены взаимодействием соединения формулы (I-a) с СН2=СН-CN в присутствии подходящего катализатора, такого как, например, Pd(OAc)2, подходящего лиганда, такого как, например, три-о-толилфосфин, подходящего основания, такого как, например, N,N-диэтилэтанамин, и подходящего растворителя, такого как, например, N,N-диметилформамид или ацетонитрил.
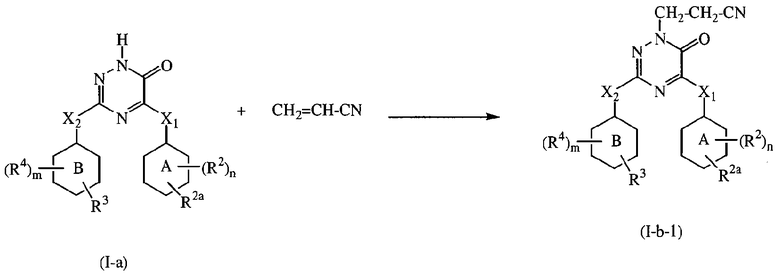
Соединения формулы (I), где Х1, соответственно Х2, представляет S(=O)2, причем указанные соединения представлены формулой (I-с), соответственно (I-d), могут быть получены окислением соединения формулы (I), где Х1, соответственно Х2, представляет S, причем указанные соединения представлены формулой (I-е), соответственно (I-f), в присутствии подходящего окислителя, такого как, например, Н2О2, в присутствии подходящей кислоты, такой как, например, уксусная кислота.
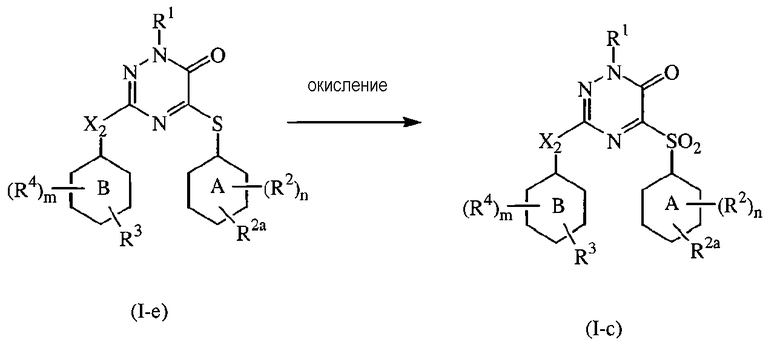
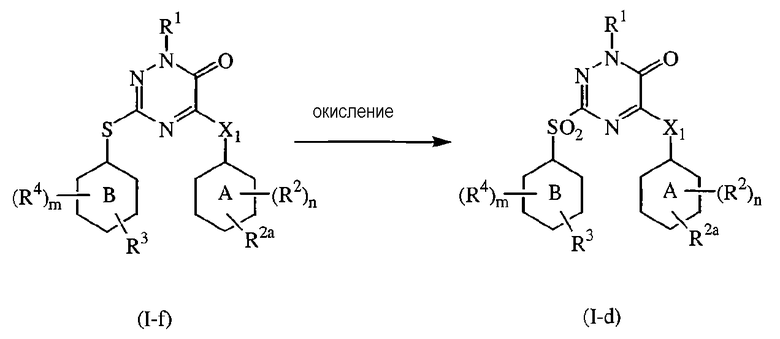
Соединения формулы (I) также могут быть получены преобразованием соединений формулы (I) друг в друга согласно известным в технике реакциям перегруппировки.
Соединения формулы (I) могут быть преобразованы в соответствующие N-оксидные формы, следуя известным в технике методикам преобразования трехвалентного азота в N-оксидную форму. Указанную реакцию N-окисления, как правило, можно осуществить взаимодействием исходного вещества формулы (I) с соответствующим органическим или неорганическим пероксидом. Соответствующие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных металлов или щелочноземельных металлов, например, пероксид натрия, пероксид калия; соответствующие органические пероксиды могут включать, например, пероксикислоты, такие как, например, надбензойная кислота или галогензамещенная надбензойная кислота, например, 3-хлорнадбензойная кислота, пероксоалкановые кислоты, например, надуксусная кислота, алкилгидропероксиды, например, трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие спирты, например, этанол и т.п., углеводороды, например, толуол, кетоны, например, 2-бутанон, галогенированные углеводороды, например, дихлорметан, и смеси таких растворителей.
Соединения формулы (I), где R2, R2a, R3 или R4 представляет собой С2-6алкенил, замещенный аминокарбонилом, могут быть преобразованы в соединения формулы (I), где R2, R2a, R3 или R4 представляет собой С2-6алкенил, замещенный циано, взаимодействием с POCl3.
Соединения формулы (I), где R1 представляет С1-6алкилоксикарбонил, могут быть преобразованы в соединения формулы (I), где R1 представляет водород, взаимодействием с подходящей кислотой, такой как, например, трифторуксусная кислота.
Соединения формулы (I), где R2, R2a, R3 или R4 представляет собой С2-6алкенил, замещенный циано, могут быть преобразованы в соединения формулы (I), где R2, R2a, R3 или R4 представляет собой С2-6алкил, замещенный циано, взаимодействием с подходящим восстановителем, таким как, например, водород, в присутствии подходящего катализатора, такого как, например, палладий-на-угле, и в присутствии подходящего растворителя, такого как, например, этанол.
Некоторые соединения формулы (I) и некоторые промежуточные соединения в настоящем изобретении могут содержать асимметричный атом углерода. Чистые стереохимически изомерные формы указанных соединений и указанных промежуточных соединений можно получить, применяя методики, известные в технике. Например, диастереоизомеры можно разделить физическими способами, такими как селективная кристаллизация, или хроматографическими методами, например, противоточной хроматографией, жидкостной хроматографией и подобными способами. Энантиомеры можно получить из рацемических смесей, преобразуя сначала указанные рацемические смеси с помощью подходящих расщепляющих агентов, таких как, например, хиральные кислоты, в смеси диастереомерных солей или соединений, а затем физически разделяя указанные смеси диастереомерных солей или соединений, например, селективной кристаллизацией или хроматографическими методами, например, жидкостной хроматографией и подобными способами, и, наконец, преобразуя указанные разделенные диастереомерные соли или соединения в соответствующие энантиомеры. Стереохимически чистые изомерные формы также можно получить из стереохимически чистых изомерных форм соответствующих промежуточных соединений и исходных веществ, при условии, что имеющие место реакции происходят стереоспецифически.
Альтернативные способы разделения энантиомерных форм соединений формулы (I) и промежуточных соединений включают жидкостную хроматографию, в частности, жидкостную хроматографию с использованием хиральной неподвижной фазы.
Некоторые промежуточные соединения и исходные вещества являются известными соединениями и могут быть коммерчески доступными, или их можно получить согласно известным в технике методикам, например, по методикам, описанным в ЕР 834507, WO 99/50256, WO 00/27828, WO 01/85700, WO 99/50250, WO 00/27825, WO 03/016306, WO 02/078708.
Промежуточные соединения формулы (II), где Х2 представляет NR1, причем указанные промежуточные соединения представлены формулой (II-а), могут быть получены взаимодействием промежуточного соединения формулы (IV), где W3 представляет подходящую уходящую группу, такую как, например, галоген, например, хлор и т.п., с промежуточным соединением формулы (V) в присутствии камфорсульфоновой кислоты (CSA), подходящего растворителя, такого как, например, тетрагидрофуран или спирт, например, 2-пропанол.
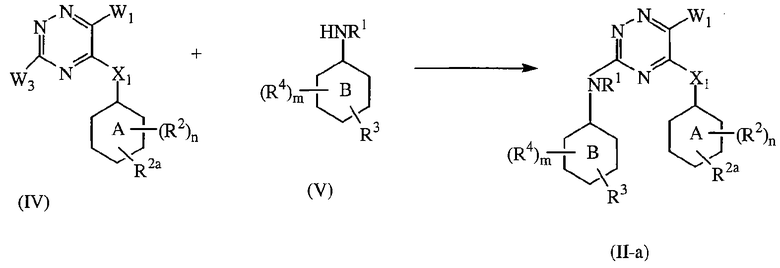
Промежуточные соединения формулы (II), где Х2 представляет О, причем указанные промежуточные соединения представлены формулой (II-b), могут быть получены взаимодействием промежуточного соединения формулы (IV) с промежуточным соединением формулы (VI) в присутствии подходящего основания, такого как, например, К2СО3, и подходящего растворителя, такого как, например, тетрагидрофуран.
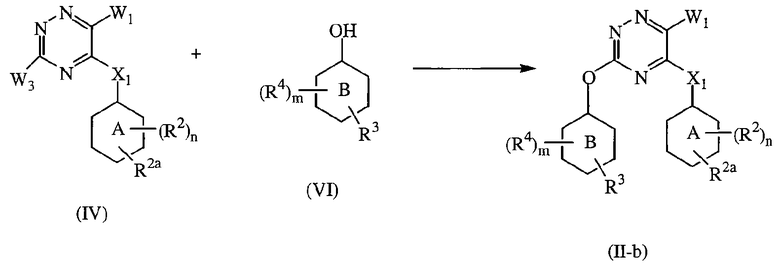
Такую же методику взаимодействия можно использовать для получения промежуточных соединений формулы (II), где Х2 представляет S.
В описанной выше реакции, когда Х1 представляет NН, указанный линкер NН можно защитить в процессе реакции подходящей защитной группой, такой как, например, трет-бутоксикарбонил. Защитную группу можно удалить по окончании взаимодействия подходящей реакцией удаления защитной группы, например, взаимодействием с трифторуксусной кислотой.
Промежуточные соединения формулы (II) могут быть преобразованы одно в другое. Например, промежуточные соединения формулы (II), где R4 представляет собой водород, можно преобразовать в промежуточные соединения формулы (II), где R4 представляет галоген, взаимодействием с подходящим агентом галогенирования, таким как, например, N-хлорсукцинимид или N-бромсукцинимид, или их сочетание, в присутствии подходящего растворителя, такого как, например, уксусная кислота.
Промежуточные соединения формулы (II), где R2 представляет собой водород, могут быть преобразованы в промежуточные соединения формулы (II), где R2 представляет галоген, взаимодействием с подходящим агентом галогенирования, таким как, например, N-хлорсукцинимид или N-бромсукцинимид, или их сочетание, в присутствии подходящего растворителя, такого как, например, уксусная кислота.
Промежуточные соединения формулы (II), где R3 представляет йод, могут быть преобразованы в промежуточные соединения формулы (II), где R3 представляет необязательно замещенный С2-6алкенил, взаимодействием с необязательно замещенным С2-6алкеном в присутствии подходящего катализатора, такого как, например, Pd(OAс)2, подходящего лиганда, такого как, например, трифенилфосфин, подходящего основания, такого как, например, N,N-диэтилэтанамин, и подходящего растворителя, такого как, например, N,N-диметилформамид.
Промежуточные соединения формулы (II), где R2а представляет йод, могут быть преобразованы в промежуточные соединения формулы (II), где R2а представляет необязательно замещенный С2-6алкенил, взаимодействием с необязательно замещенным С2-6алкеном в присутствии подходящего катализатора, такого как, например, Pd(OAс)2, подходящего лиганда, такого как, например, трифенилфосфин, подходящего основания, такого как, например, N,N-диэтилэтанамин, и подходящего растворителя, такого как, например, N,N-диметилформамид.
Промежуточные соединения формулы (IV) могут быть получены взаимодействием промежуточного соединения формулы (VII), где W4 представляет подходящую уходящую группу, такую как, например, галоген, например, хлор и т.п., с промежуточным соединением формулы (VIII) в присутствии подходящего растворителя, такого как, например, тетрагидрофуран или дихлорметан, и необязательно в присутствии подходящего основания, такого как, например, гидрид натрия или Na2CO3.
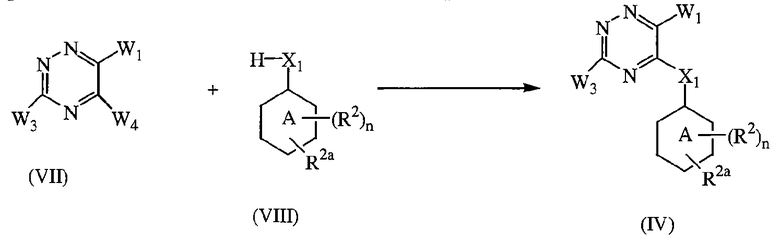
В приведенной выше реакции, когда Х1 представляет NH, указанный линкер NH можно защитить в процессе реакции подходящей защитной группой, такой как, например, трет-бутоксикарбонил.
Промежуточные соединения формулы (VIII), где Х1-Н представляет NH2, могут быть преобразованы в промежуточное соединение, где Х1-Н представляет NH-C(=O)-O-C(CH3)3, взаимодействием с ди-трет-бутилдикарбонатом в присутствии 4-диметиламинопиридина.
Промежуточные соединения формулы (VII), где W1, W3 и W4 представляют хлор, причем указанные промежуточные соединения представлены формулой (VII-а), могут быть получены взаимодействием промежуточного соединения формулы (IХ) с POCl3 и PCl5 в присутствии подходящего основания, такого как, например, N,N-диэтиланилин.
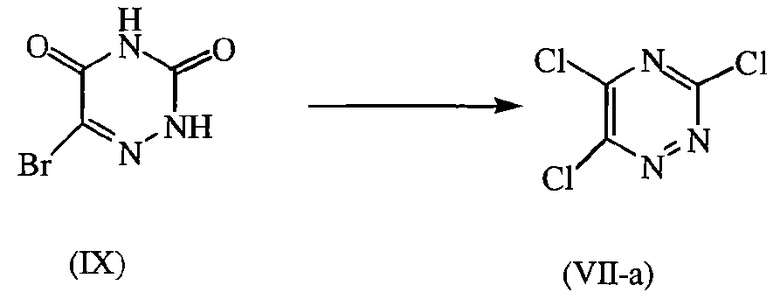
Промежуточные соединения формулы (IХ) могут быть получены взаимодействием 1,2,4-триазин-3,5-(2Н,4Н)диона с Br2 в присутствии подходящего растворителя, такого как, например, Н2О.
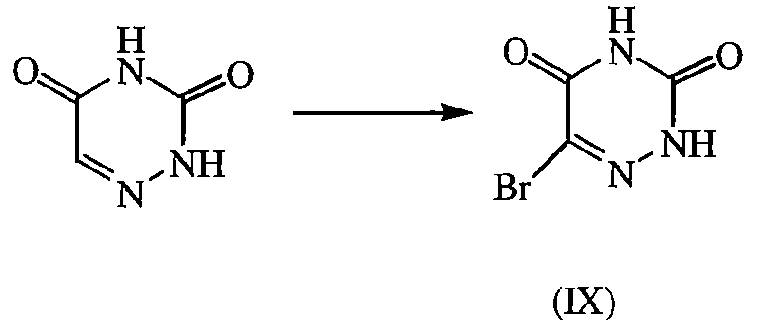
Промежуточные соединения формулы (VIII), где Х1-Н представляет NH2, причем указанные промежуточные соединения представлены формулой (VIII-а), могут быть преобразованы в промежуточное соединение формулы (VIII), где Х1-Н представляет ОН, причем указанное промежуточное соединение представлено формулой (VIII-b), взаимодействием с NaNO2 в присутствии подходящей кислоты, такой как, например, HCl, и подходящего растворителя, такого как, например, Н2О.
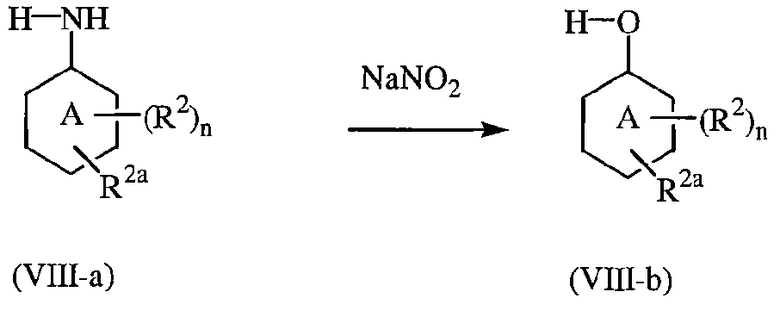
Такое же взаимодействие можно использовать для преобразования промежуточного соединения формулы (V), где R1 представляет собой водород, в промежуточное соединение формулы (VI).
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет йод или бром, могут быть преобразованы в промежуточное соединение формулы (V), (VI) или (VIII), где R3 или R2а представляет необязательно замещенный С2-6алкенил, взаимодействием с необязательно замещенным С2-6алкеном в присутствии подходящего катализатора, такого как, например, Pd(OAс)2, подходящего лиганда, такого как, например, трифенилфосфин или трис(2-метилфенил)фосфин, подходящего основания, такого как, например, N,N-диэтилэтанамин или N,N-диметилэтанамин, и подходящего растворителя, такого как, например, ацетонитрил или N,N-диметилформамид.
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет бром, могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет циано, взаимодействием с CuCN в присутствии подходящего растворителя, такого как, например, N,N-диметилформамид.
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет необязательно замещенный С2-6алкенил, могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет необязательно замещенный С2-6алкил, взаимодействием с подходящим восстановителем, таким как, например, Н2, в присутствии подходящего катализатора, такого как, например, палладий-на-угле, в присутствии подходящего растворителя, такого как, например, спирт, например, этанол.
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет С2-6алкенил, замещенный аминокарбонилом, могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет С2-6алкенил, замещенный циано, взаимодействием с POCl3.
Промежуточные соединения формул (V) или (VIII), где Х1 представляет NH и где R3 или R2а представляет йод, могут быть получены взаимодействием промежуточного соединения, где указанный R3 или R2а представляет водород, с подходящим агентом галогенирования, таким как, например, IСl для введения йода или Br2 для введения брома, в присутствии подходящей кислоты, такой как, например, уксусная кислота.
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет йод и R4 или R2 представляет гидрокси или метокси, причем указанный заместитель R4 или R2 находится в мета-положении относительно йода, могут быть получены взаимодействием 2-бензоксазолона с монохлоридом йода в присутствии подходящей кислоты, такой как, например, уксусная кислота, с последующим взаимодействием полученного продукта реакции с ди-трет-бутилкарбонатом, N,N-диэтилэтанамином, 4-N,N-диметиламинопиридином в присутствии подходящего растворителя, такого как, например, тетрагидрофуран, с последующим преобразованием группы NH-C(=O)-C(CH3)3 в NH2 взаимодействием c подходящей кислотой, такой как, например, трифторуксусная кислота. Когда R4 или R2 представляет ОН, такой заместитель можно превратить в метокси взаимодействием с метилйодидом в присутствии подходящего основания, такого как, например, К2СО3, и подходящего растворителя, такого как, например, тетрагидрофуран.
Промежуточные соединения формул (V), (VI) или (VIII), где R4 или R2 представляет водород, могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R4 или R2 представляет галоген, взаимодействием с подходящим агентом галогенирования, таким как, например, N-хлорсукцинимид или N-бромсукцинимид, или их сочетание, в присутствии подходящего растворителя, такого как, например, ацетонитрил.
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет галоген, могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет СН3-С(=О)-, взаимодействием с трибутил(1-этоксиэтенил)оловом в присутствии Pd(OAс)2, Р(о-Tol)3, подходящего основания, такого как, например, N,N-диэтилэтанамин, и подходящего растворителя, такого как, например, ацетонитрил.
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет СН3-С(=О)-, могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет -C(CH3)=CH-CN, взаимодействием с диэтилцианометилфосфонатом в присутствии подходящего основания, такого как, например, NaOCH3 или трет-бутил-ОК, и подходящего растворителя, такого как, например, тетрагидрофуран.
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет бром, могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет СН3-С(=О)-, взаимодействием с бутилвиниловым эфиром в присутствии подходящего катализатора, такого как, например, Pd(OAс)2, подходящего лиганда, такого как, например, 1,3-бис(дифенилфосфино)пропан, подходящего основания, такого как, например, К2СО3, и подходящего растворителя, такого как, например, вода или N,N-диметилформамид.
Промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет галоген, могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет -C(CN)-C(=O)-O-С1-6алкил, взаимодействием с CN-CH2-C(=O)-O-С1-6алкилом в присутствии Pd2(dba)3, P(трет-Bu)3, Na3PO4 и подходящего растворителя, такого как, например, толуол. Указанные промежуточные соединения затем могут быть преобразованы в промежуточные соединения формул (V), (VI) или (VIII), где R3 или R2а представляет -CH2-CN, взаимодействием с NаCl в присутствии подходящего растворителя, такого как, например, Н2О или диметилсульфоксид.
Промежуточные соединения формул (V) или (VIII), где NHR1, соответственно Х1-Н, представляет NH2, причем указанные промежуточные соединения представлены формулами (V-а) или (VIII-а), могут быть получены восстановлением промежуточного соединения формулы (Х) или (XI) подходящим восстановителем, таким как, например, Н2, в присутствии подходящего катализатора, такого как, например, палладий-на-угле, в присутствии подходящего растворителя, такого как, например, спирт, например, этанол, или взаимодействием с SnCl2 в присутствии подходящего растворителя, такого как, например, спирт, например, этанол.
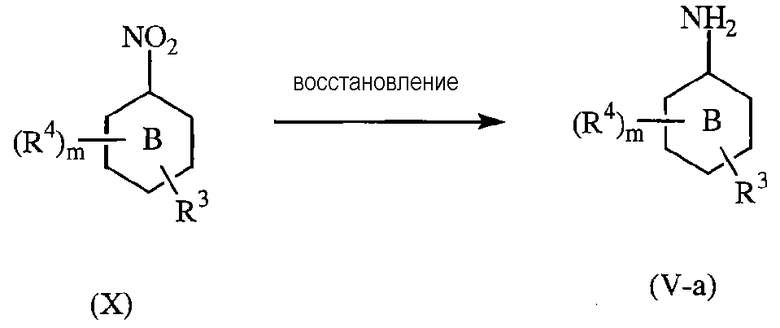
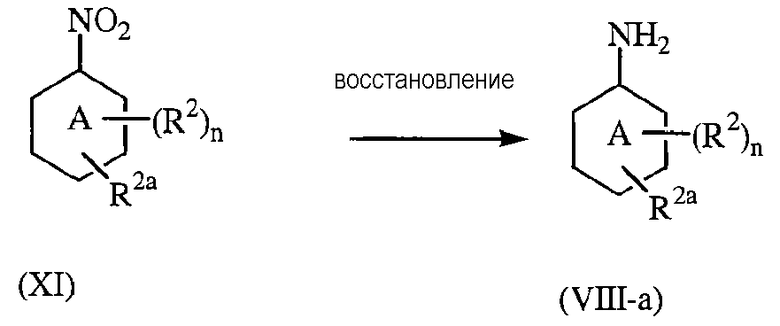
Промежуточные соединения формул (Х) или (XI) могут быть получены взаимодействием промежуточного соединения формулы (XII) или (XIII) с HNO3 в присутствии подходящей кислоты, такой как, например, H2SO4.
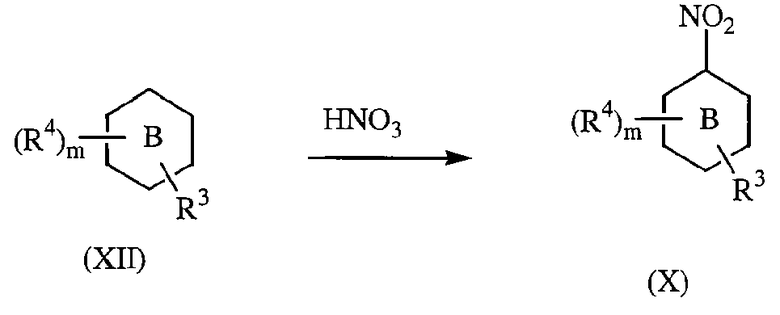
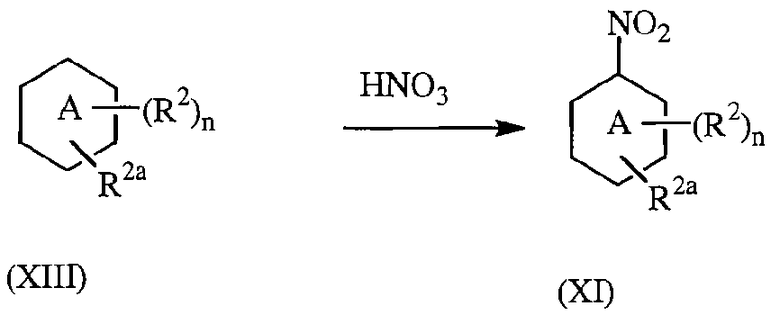
Соединения формул (I), (I-1), (I-1-1), (I-1-2), (I-1-3), (I-2), (I-2-1), (I-2-2), (I-2-3) демонстрируют противовирусные свойства (свойства ингибирования обратной транскриптазы), в частности, против вируса иммунодефицита человека (ВИЧ), который является этиологическим фактором синдрома приобретенного иммунодефицита (СПИДа) у людей. Вирус ВИЧ преимущественно заражает клетки Т-4 человека и разрушает их или изменяет их нормальную функцию, особенно координацию иммунной системы. В результате, инфицированный пациент имеет значительно уменьшающееся число клеток Т-4, которые, кроме того, ведут себя аномально. Следовательно, система иммунной защиты неспособна бороться с инфекциями и неоплазмами, и ВИЧ-инфицированный субъект, как правило, погибает от инфекций, вызванных условно-патогенными микроорганизмами, таких как пневмония, или от онкологических заболеваний. Другие состояния, связанные с ВИЧ-инфекцией, включают тромбоцитопению, саркому Капоши и инфекционное заболевание центральной нервной системы, характеризующееся прогрессирующей демиелинизацией, приводящей к деменции и таким симптомам, как прогрессирующая дизартрия, атаксия и дезориентация. ВИЧ-инфекция также ассоциируется с периферической невропатией, прогрессирующей генерализованной лимфаденопатией (PGL) и СПИД-ассоциированным комплексом (ARC).
Соединения настоящего изобретения также показывают активность против штаммов ВИЧ, устойчивых к одному или нескольким лекарственным средствам, в частности, штаммов ВИЧ-1, устойчивых к одному или нескольким лекарственным средствам, более конкретно, соединения настоящего изобретения показывают активность против штаммов ВИЧ, особенно штаммов ВИЧ-1, которые обладают приобретенной устойчивостью к одному или нескольким известным в технике ненуклеозидным ингибиторам обратной транскриптазы. Известные в технике ненуклеозидные ингибиторы обратной транскриптазы представляют собой ненуклеозидные ингибиторы обратной транскриптазы иные, чем соединения настоящего изобретения, и известны специалистам в данной области техники, в частности, коммерческие ненуклеозидные ингибиторы обратной транскриптазы. Соединения настоящего изобретения также имеют небольшую аффинность к человеческому гликопротеину с кислотой α-1 или не имеют ее; человеческий гликопротеин с кислотой α-1 не влияет или только слабо влияет на активность соединений настоящего изобретения против ВИЧ.
Благодаря своим противовирусным свойствам, в частности, анти-ВИЧ свойствам, особенно своей активности против ВИЧ-1, соединения формулы (I) или их любая подгруппа, их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины и стереохимически изомерные формы применимы для лечения индивидуумов, инфицированных ВИЧ, и для профилактики таких инфекций. Как правило, соединения настоящего изобретения можно применять при лечении теплокровных животных, инфицированных вирусами, существование которых опосредуется или зависит от фермента обратной транскриптазы (ревертазы). Состояния, которые можно предупреждать или лечить соединениями настоящего изобретения, особенно состояния, ассоциированные с ВИЧ и другими патогенными ретровирусами, включают СПИД, СПИД-ассоциированный комплекс (ARC), прогрессирующую генерализованную лимфаденопатию (PGL), а также хронические заболевания центральной нервной системы, вызванные ретровирусами, такие как, например, ВИЧ-ассоциированная деменция и рассеянный склероз.
Следовательно, соединения настоящего изобретения или их любую подгруппу можно использовать в качестве лекарственных средств против вышеуказанных состояний. Указанное применение в качестве лекарственного средства или способ лечения включает введение ВИЧ-инфицированным субъектам количества, эффективного для борьбы с состояниями, ассоциированными с ВИЧ и другими патогенными ретровирусами, особенно ВИЧ-1. В частности, соединения формулы (I) можно использовать при получении лекарственного средства для лечения или предупреждения ВИЧ-инфекций.
С учетом применимости соединений формулы (I) предлагается способ лечения млекопитающих, включая людей, страдающих от вирусных инфекций, или способ предупреждения страдания млекопитающих, включая людей, от вирусных инфекций, в особенности, ВИЧ-инфекций. Указанный способ включает введение, предпочтительно, пероральное введение, млекопитающим, включая людей, эффективного количества соединения формулы (I) или любой его подгруппы, его N-оксидной формы, фармацевтически приемлемой аддитивной соли, четвертичного амина или возможной стереоизомерной формы.
Настоящее изобретение также относится к композициям для лечения вирусных инфекций, включающим терапевтически эффективное количество соединения формулы (I) и фармацевтически приемлемый носитель или разбавитель.
Соединения настоящего изобретения или их любая подгруппа могут быть включены в состав различных фармацевтических форм для целей введения. В качестве подходящих композиций можно назвать все композиции, обычно используемые для системного введения лекарственных средств. Чтобы получить фармацевтические композиции данного изобретения, эффективное количество определенного соединения, необязательно в форме аддитивной соли, в качестве активного ингредиента объединяют при тщательном перемешивании с фармацевтически приемлемым носителем, который может принимать самые различные формы, в зависимости от формы препарата, необходимого для введения. Такие фармацевтические композиции являются подходящими в стандартной лекарственной форме, подходящей, в частности, для перорального, ректального, чрескожного введения или введения путем парентеральной инъекции. Например, при получении композиции в пероральной лекарственной форме можно использовать любые обычные фармацевтические среды, такие как, например, вода, гликоли, масла, спирты и т.п., в случае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, смазывающие вещества, связующие вещества, дезинтегрирующие вещества и т.п., в случае порошков, пилюль, капсул и таблеток. Благодаря простоте введения таблетки и капсулы представляют наиболее благоприятные пероральные стандартные лекарственные формы, в таком случае, очевидно, используют твердые фармацевтические носители. В случае парентеральных композиций носитель, как правило, будет содержать стерильную воду, по меньшей мере, большей частью, хотя могут быть включены другие ингредиенты, например, способствующие растворению. Например, могут быть получены растворы для инъекций, в которых носитель включает физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Также могут быть получены суспензии для инъекций, в которых можно использовать соответствующие жидкие носители, суспендирующие агенты и т.п. Также включаются препараты в твердой форме, которые предполагается преобразовать, незадолго до применения, в препараты жидкой формы. В композициях, подходящих для чрескожного введения, носитель необязательно включает вещество, усиливающее проникание, и/или подходящее смачивающее вещество, необязательно в сочетании с подходящими добавками любой природы в небольших соотношениях, и такие добавки не оказывают существенного вредного действия на кожу. Указанные добавки могут облегчить введение в кожу и/или могут способствовать получению требуемых композиций. Такие композиции можно вводить различными способами, например, в виде трансдермального пластыря, непосредственно по месту, мази. Соединения настоящего изобретения также можно вводить ингаляцией или инсуффляцией с помощью способов и препаратов, используемых в технике для введения таким путем. Так, как правило, соединения настоящего изобретения можно вводить в легкие в форме раствора, суспензии или сухого порошка. Любая система, разработанная для доставки растворов, суспензий или сухих порошков посредством пероральной или назальной ингаляции или инсуффляции, подходят для введения соединений настоящего изобретения.
Для того чтобы способствовать растворимости соединений формулы (I) или любой их подгруппы, в композиции можно включать подходящие ингредиенты, например, циклодекстрины. Подходящими циклодекстринами являются α-, β-, γ-циклодекстрины или их простые или смешанные простые эфиры, где одна или несколько гидроксигрупп ангидроглюкозных звеньев циклодекстрина замещены С1-6алкилом, в частности, метилом, этилом или изопропилом, например, произвольно метилированные β-CD; гидроксиС1-6алкилом, в частности, гидроксиэтилом, гидроксипропилом или гидроксибутилом; карбоксиС1-6алкилом, в частности, карбоксиметилом или карбоксиэтилом; С1-6алкилкарбонилом, в частности, ацетилом. Особенно заслуживающими внимания в качестве комплексообразователей и/или солюбилизаторов являются β-CD, произвольно метилированные β-CD, 2,6-диметил-β-CD, 2-гидроксиэтил-β-CD, 2-гидроксипропил-β-CD и (2-карбоксиметокси)пропил-β-CD, и особенно 2-гидроксипропил-β-CD (2- НР-β-CD).
Термин «смешанные простые эфиры» обозначает производные циклодекстринов, в которых, по меньшей мере, две гидроксигруппы циклодекстрина этерифицированы различными группами, такие как, например, гидроксипропил и гидроксиэтил.
Среднее молярное замещение (M.S.) используют в качестве меры среднего числа молей алкоксизвеньев на моль ангидроглюкозы. Средней степенью замещения (D.S.) называют среднее число замещенных гидроксилов на звено ангидроглюкозы. Величины M.S. и D.S. можно определить различными аналитическими методами, такими как ядерный магнитный резонанс (ЯМР), масс-спектрометрия (МС) и инфракрасная спектрометрия (ИК). В зависимости от используемого метода можно получить несколько различные величины для одного данного производного циклодекстрина. Предпочтительно, при измерении методом масс-спектрометрии M.S. колеблется от 0,125 до 10 и D.S. колеблется от 0,125 до 3.
Другие подходящие композиции для перорального или ректального введения содержат частицы, состоящие из твердой дисперсии, содержащей соединение формулы (I) и один или несколько соответствующих фармацевтически приемлемых водорастворимых полимеров.
Термин «твердая дисперсия», используемый в данном описании далее, определяет систему в твердом состоянии (в противоположность жидкому или газообразному состоянию), содержащую, по меньшей мере, два компонента, в данном случае соединение формулы (I) и водорастворимый полимер, где один компонент диспергирован более или менее равномерно в другом компоненте или компонентах (в случае, когда в препарат включают другие фармацевтически приемлемые вещества, как правило, известные в технике, такие как пластификаторы, консерванты и т.п.). Когда указанная дисперсия компонентов такова, что система является химически и физически однородной или гомогенной, или состоит из одной фазы, как ее определяет термодинамика, такая твердая дисперсия будет называться «твердым раствором». Твердые растворы являются предпочтительными физическими системами, поскольку компоненты в них, как правило, являются легко биодоступными для организмов, в которые их вводят. Такое преимущество можно, вероятно, объяснить легкостью, с которой указанные твердые растворы могут образовывать жидкие растворы при контакте с жидкой средой, такой как пищеварительные соки желудочно-кишечного тракта. Легкость растворения может быть приписана, по меньшей мере, частично, тому факту, что энергия, требуемая для растворения компонентов твердого раствора, меньше энергии, требуемой для растворения компонентов кристаллической или микрокристаллической твердой фазы.
Термин «твердая дисперсия» также включает дисперсии, которые являются менее гомогенными, чем твердые растворы. Такие дисперсии не являются химически и физически однородными или содержат более одной фазы. Например, термин «твердая дисперсия» также относится к системе, содержащей домены или небольшие участки, в которых аморфное, микрокристаллическое или кристаллическое соединение формулы (I), или аморфный, микрокристаллический или кристаллический водорастворимый полимер, или оба компонента, диспергированы более или менее равномерно в другой фазе, содержащей водорастворимый полимер или соединение формулы (I), или твердый раствор, включающий соединение формулы (I) и водорастворимый полимер. Указанные домены и участки в твердой дисперсии явно характеризуются некоторым физическим свойством, невелики по размеру и равномерно и случайно распределены в твердой дисперсии.
Существуют различные методы получения твердых дисперсий, в том числе, экструзия из расплава, сушка распылением и выпаривание раствора.
Способ выпаривания раствора включает следующие стадии:
а) растворение соединения формулы (I) и водорастворимого полимера в соответствующем растворителе, необязательно при повышенных температурах;
b) нагревание раствора, полученного по пункту а), необязательно в вакууме, до тех пор, пока растворитель не выпарится. Раствор также можно вылить на большую поверхность так, что образуется тонкая пленка, и выпарить из нее растворитель.
В методе сушки распылением два компонента также растворяют в соответствующем растворителе, а затем полученный раствор распыляют через сопло распылительной сушилки с последующим выпариванием растворителя из полученных капелек при повышенных температурах.
Предпочтительным методом получения твердых дисперсий является способ экструзии из расплава, включающий следующие стадии:
а) смешивание соединения формулы (I) и соответствующего водорастворимого полимера,
b) необязательно, смешивание добавок с полученной таким образом смесью,
с) нагревание и перемешивание полученной таким образом смеси до получения гомогенного расплава,
d) выдавливание полученного таким образом расплава через одно или несколько выпускных отверстий и
е) охлаждение расплава до его отверждения.
Термины «расплав» и «плавление» следует интерпретировать в широком смысле. Указанные термины означают не только изменение от твердого состояния до жидкого состояния, но также могут относиться к переходу в стеклообразное или высокоэластическое состояние, в котором существует возможность для одного компонента смеси внедриться более или менее равномерно в другой компонент. В отдельных случаях один компонент будет плавиться, а другой(ие) компонент(ы) будут растворяться в расплаве, образуя таким образом раствор, который после охлаждения может образовать твердый раствор с выгодными свойствами растворения.
После получения твердых дисперсий, как описано выше, полученные продукты можно, необязательно, измельчить и просеять.
Продукт - твердую дисперсию можно измельчить или раздробить до частиц размером менее 600 мкм, предпочтительно, менее 400 мкм и наиболее предпочтительно, менее 125 мкм.
Затем частицы, полученные так, как описано в данном описании выше, можно ввести обычными методами в состав фармацевтических лекарственных форм, таких как таблетки и капсулы.
Следует иметь в виду, что специалист в данной области техники сможет оптимизировать параметры методов получения твердых дисперсий, описанных выше, такие как наиболее соответствующий растворитель, рабочая температура, вид используемой аппаратуры, скорость сушки распылением, скорость пропускания расплава в экструдере.
Водорастворимые полимеры в частицах представляют собой полимеры, которые имеют кажущуюся вязкость, когда растворены при 20°С, в водном 2% (мас./об.) растворе 1-5000 мПа.с, более предпочтительно, 1-700 мПа.с и наиболее предпочтительно, 1-100 мПа.с. Например, подходящие водорастворимые полимеры включают алкилцеллюлозы, гидроксиалкилцеллюлозы, гидроксиалкилалкилцеллюлозы, карбоксиалкилцеллюлозы, соли щелочных металлов карбоксиалкилцеллюлоз, карбоксиалкилалкилцеллюлозы, сложные эфиры карбоксиалкилцеллюлозы, крахмалы, пектины, производные хитина, ди-, олиго- и полисахариды, такие как трегалоза, альгиновую кислоту или ее соли щелочных металлов и аммония, каррагенаны, галактоманнаны, трагакант, агар-агар, аравийскую камедь, гуаровую камедь и ксантановую камедь, полиакриловые кислоты и их соли, полиметакриловые кислоты и их соли, сополимеры метакрилата, поливиниловый спирт, поливинилпирролидон, сополимеры поливинилпирролидона и винилацетата, сочетания поливинилового спирта и поливинилпирролидона, полиалкиленоксиды и сополимеры этиленоксида и пропиленоксида. Предпочтительными водорастворимыми полимерами являются гидроксипропилметилцеллюлозы.
Также один или несколько циклодекстринов можно использовать в качестве водорастворимого полимера при получении вышеуказанных частиц, как раскрывается в WO 97/18839. Указанные циклодекстрины включают фармацевтически приемлемые незамещенные или замещенные циклодекстрины, известные в технике, более конкретно, α-, β- или γ-циклодекстрины или их фармацевтически приемлемые производные.
Замещенные циклодекстрины, которые можно использовать для получения вышеописанных частиц, включают простые полиэфиры, описанные в патенте США 3459731. Также замещенными циклодекстринами являются простые эфиры, в которых водород одной или нескольких гидроксигрупп циклодекстрина заменен С1-6алкилом, гидроксиС1-6алкилом, карбоксиС1-6алкилом или С1-6алкоксикарбонилС1-6алкилом, или их смешанные простые эфиры. В частности, такие замещенные циклодекстрины представляют собой простые эфиры, в которых водород одной или нескольких гидроксигрупп циклодекстрина заменен С1-3алкилом, гидроксиС2-4алкилом или карбоксиС1-2алкилом, или, в частности, метилом, этилом, гидроксиэтилом, гидроксипропилом, гидроксибутилом, карбоксиметилом или карбоксиэтилом.
Конкретную применимость имеют эфиры β-циклодекстрина, например, диметил-β-циклодекстрин, как описано в Drugs of the Future, Vol.9, No.8, p. 577-578, M. Nogradi (1984), и полиэфиры, например, гидроксипропил-β-циклодекстрин и гидроксиэтил-β-циклодекстрин, как примеры. Такой алкиловый эфир может представлять собой метиловый эфир со степенью замещения примерно 0,125-3, например, примерно 0,3-2. Такой гидроксипропилциклодекстрин может быть получен, например, взаимодействием между β-циклодекстрином и пропиленоксидом, и он может иметь величину MS примерно 0,125-10, например, примерно 0,3-3.
Другим типом замещенных циклодекстринов являются сульфобутилциклодекстрины.
Отношение соединения формулы (I) к водорастворимому полимеру может изменяться в широких пределах. Например, можно применять соотношения от 1/100 до 100/1. Представляющие интерес отношения соединения формулы (I) к водорастворимому полимеру находятся в диапазоне от примерно 1/10 до 10/1. Более интересные отношения находятся в диапазоне от примерно 1/5 до 5/1.
Также может быть удобно вводить соединения формулы (I) в состав препаратов в форме наночастиц, имеющих модификатор поверхности, адсорбированный на их поверхности в количестве, достаточном для сохранения эффективного среднего размера частиц менее 1000 нм. Полагают, что применимые модификаторы поверхности включают такие модификаторы, которые физически сцепляются с поверхностью частицы соединения формулы (I), а не с помощью химической связи с указанным соединением.
Подходящие модификаторы поверхности могут быть предпочтительно выбраны из известных органических и неорганических фармацевтических эксципиентов. Такие эксципиенты включают различные полимеры, низкомолекулярные олигомеры, природные продукты и поверхностно-активные вещества. Предпочтительные модификаторы поверхности включают неионные и анионные поверхностно-активные вещества.
Еще один представляющий интерес способ получения препаратов соединений формулы (I) включает фармацевтическую композицию, в которой соединения формулы (I) включены в гидрофильные полимеры, и такая смесь нанесена в виде пленочного покрытия на множество мелких гранул, причем таким образом получается композиция, которая может быть удобно изготовлена и которая подходит для получения фармацевтических лекарственных форм для перорального введения.
Указанные гранулы имеют центральную круглую или сферическую сердцевину, пленочное покрытие из гидрофильного полимера и соединения формулы (I) и, необязательно, слой наружного покрытия.
Материалами, подходящими для применения в качестве сердцевины, являются самые разные материалы, при условии, что указанные материалы фармацевтически приемлемы и их частицы имеют соответствующие размеры и устойчивость. Примерами таких материалов являются полимеры, неорганические вещества, органические вещества и сахариды и их производные.
Особенно выгодно составлять вышеуказанные фармацевтические композиции в стандартной лекарственной форме для облегчения введения и равномерности дозирования. Термин «стандартная лекарственная форма», используемый в данном описании, относится к физически дискретным единицам, подходящим в качестве однократных доз, причем каждая единица содержит предварительно установленное количество активного ингредиента, рассчитанное на получение желательного лечебного действия, в сочетании с требуемым фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включая таблетки с насечкой или с покрытием), капсулы, пилюли, пакетики с порошком, облатки, суппозитории, растворы или суспензии для инъекций и т.п., и множества таких отдельных форм.
Специалисты в области лечения ВИЧ-инфекции могут определить эффективное суточное количество из результатов испытаний, представленных в данном описании. Обычно предполагается, что эффективное суточное количество может составлять от 0,01 мг/кг до 50 мг/кг массы тела, более предпочтительно, от 0,1 мг/кг до 10 мг/кг массы тела. Подходящим может быть введение требуемой дозы в виде двух, трех, четырех или большего числа субдоз с соответствующими интервалами в течение суток. Указанные субдозы могут быть в виде стандартных лекарственных форм, например, содержащих 1-1000 мг, и в частности, 5-200 мг активного ингредиента на стандартную лекарственную форму.
Точная дозировка и частота введения зависят от конкретного используемого соединения формулы (I), конкретного состояния, подвергаемого лечению, тяжести состояния, подвергаемого лечению, возраста, массы тела и общего физического состояния конкретного пациента, а также учитываются другие медицинские показания индивидуума, что хорошо известно специалистам в данной области техники. Кроме того, очевидно, что указанное эффективное суточное количество можно снижать или повышать, в зависимости от реакции субъекта, которого лечат, и/или в зависимости от оценки врача, предписывающего соединения данного изобретения. Поэтому интервалы эффективного суточного количества, указанные выше, являются только направляющими указаниями и не предназначены для ограничения объема или применения изобретения в какой-либо мере.
Соединения настоящего изобретения формулы (I) или любой их подгруппы можно использовать индивидуально или в сочетании с другими лечебными средствами, такими как противовирусные средства, антибиотики, иммуномодуляторы или вакцины для лечения вирусных инфекций. Их также можно использовать индивидуально или в сочетании с другими профилактическими средствами для предупреждения вирусных инфекций. Соединения настоящего изобретения можно использовать в вакцинах и способах защиты индивидуумов от вирусных инфекций в течение длительного периода времени. Соединения можно использовать в таких вакцинах или индивидуально, или вместе с другими соединениями данного изобретения, или вместе с другими противовирусными средствами способом, согласующимся с обычным применением в вакцинах ингибиторов обратной транскриптазы. Таким образом, соединения настоящего изобретения можно объединять с фармацевтически приемлемыми адъювантами, обычно используемыми в вакцинах, и вводить в профилактически эффективных количествах для защиты индивидуумов в течение длительного периода времени от ВИЧ-инфекции.
Также в качестве лекарственного средства можно использовать сочетание одного или нескольких дополнительных противовирусных соединений и соединения формулы (I). Таким образом, настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) одно или несколько других противовирусных соединений, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения при лечении анти-ВИЧ. Различные лекарственные средства могут быть объединены в единый препарат вместе с фармацевтически приемлемыми носителями. Указанные другие антиретровирусные средства могут представлять собой известные антиретровирусные соединения, такие как сурамин, пентамидин, тимопентит, кастаноспермин, декстран (сульфат декстрана), фоскарнет-натрий (фосфоноформиат тринатрия); нуклеозидные ингибиторы обратной транскриптазы, например, зидовудин (3'-азидо-3'-дезокситимидин, AZT), диданозин (2',3'-дидезоксиинозин; ddI), залцитабин (дидезоксицитидин, ddC) или ламивудин (2',3'-дидезокси-3'-тиацитидин, 3ТС), ставудин (2',3'-дидегидро-3'-дезокситимидин, d4T), абакавир и т.п.; ненуклеозидные ингибиторы обратной транскриптазы, такие как невирапин (11-циклопропил-5,11-дигидро-4-метил-6Н-дипиридо[3,2-b:2',3'-e][1,4]диазепин-6-он), эфавиренц, делавирдин, ТМС-120, ТМС-125, 4-[[4-[[4-(2-цианоэтил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрил (Е) и т.п.; фосфонатные ингибиторы обратной транскриптазы, например, тенофовир и т.п.; соединения TIBO типа (тетрагидроимидазо[4,5,1-jk][1,4]бензодиазепин-2(1Н)-он или -тион), например, (S)-8-хлор-4,5,6,7-тетрагидро-5-метил-6-(3-метил-2-бутенил)имидазо-[4,5,1-jk][1,4]бензодиазепин-2(1Н)-тион; соединения типа α-АРА (α-анилинофенилацетамид), например, α-[(2-нитрофенил)амино-2,6-дихлорбензолацетамид и т.п.; ингибиторы транс-активирующих белков, такие как ТАТ-ингибиторы, например, RO-5-3335, или ингибиторы REV, и т.п.; ингибиторы протеаз, например, индинавир, ритонавир, саквинавир, лопинавир (АВТ-378), нелфинавир, ампренавир, ТМС-126, BMS-232632, VX-175 и т.п.; ингибиторы слияния, например, Т-20, Т-1249 и т.п.; антагонисты рецепторов CXCR4, например, AMD-3100 и т.п.; ингибиторы вирусной интегразы; нуклеотидные аналоги ингибиторов обратной транскриптазы, например, тенофовир и т.п.; ингибиторы рибонуклеотидредуктазы, например, гидроксимочевина и т.п.
Путем введения соединений настоящего изобретения с другими противовирусными средствами, которые нацелены на различные события в жизненном цикле вирусов, можно усилить лечебное действие таких соединений. Комбинированные терапии, описанные выше, проявляют синергическое действие при ингибировании репликации ВИЧ, поскольку каждый компонент сочетания действует на различные участки репликации ВИЧ. Применение таких сочетаний может уменьшить дозировку данного обычного антиретровирусного средства, которая может потребоваться для желательного лечебного или профилактического действия, по сравнению с дозировкой, требуемой когда такое средство вводят как монотерапию. Такие сочетания могут ослабить или устранить побочное действие обычной монотерапии с антиретровирусным средством, не препятствуя в то же время противовирусной активности средств. Такие сочетания уменьшают возможность резистентности к монотерапии, минимизируя в то же время любую связанную с ней токсичность. Такие сочетания также могут повысить эффективность обычного средства, не повышая связанную с ним токсичность.
Соединения настоящего изобретения также можно вводить в сочетании с иммуномодуляторами, например, левамизолом, бропиримином, антителами против человеческого альфа-интерферона, интерфероном-альфа, интерлейкином 2, метионинэнкефалином, диэтилдитиокарбаматом, фактором некроза опухоли, налтрексоном и т.п.; антибиотиками, например, пентамидина изетионатом и т.п.; холинергическими средствами, например, такрином, ривастигмином, донепезилом, галантамином и т.п.; блокаторами каналов NMDA, например, мемантином, для предупреждения или борьбы с инфекцией и болезнями или симптомами болезней, ассоциированных с ВИЧ-инфекциями, такими как СПИД и ARC, например, деменцией. Соединение формулы (I) также можно сочетать с другим соединением формулы (I).
Хотя настоящее изобретение сосредоточено на применении соединений настоящего изобретения для предупреждения или лечения ВИЧ-инфекций, соединения настоящего изобретения также можно применять в качестве ингибиторов для других вирусов, зависящих от подобных обратных транскриптаз для облигатных событий в их жизненном цикле.
Приведенные далее примеры предназначены для пояснения настоящего изобретения.
Экспериментальная часть
Далее в описании «ТФУК» обозначает трифторуксусную кислоту, «ДМФА» обозначает N,N-диметилформамид, «ТГФ» обозначает тетрагидрофуран, [M+H+] представляет собой массу протонированного соединения, обозначение «CI-МС» ставится для масс-спектра в случае химической ионизации.
А. Получение промежуточных соединений
Пример А1
а) Получение промежуточного соединения 1
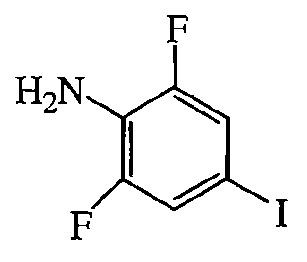
2,6-Дифторбензоламин (3,0 г, 22,56 ммоль) растворяют в уксусной кислоте (10 мл). К раствору добавляют монохлорид йода (3,581 г, 22,56 ммоль). Смесь перемешивают в течение 15 минут при комнатной температуре. После выпаривания растворителя остаток обрабатывают водным раствором карбоната натрия. Водный раствор экстрагируют дихлорметаном. Органический экстракт сушат над MgSO4 и упаривают. Выход: 95% промежуточного соединения 1.
b) Получение промежуточного соединения 2
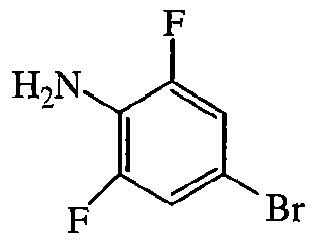
2,6-Дифторбензоламин (3,0 г, 22,56 ммоль) растворяют в уксусной кислоте (10 мл). К раствору добавляют бром (1,2 мл). Смесь перемешивают в течение 15 минут при комнатной температуре. После выпаривания растворителя остаток обрабатывают водным раствором карбоната натрия. Водный раствор экстрагируют дихлорметаном. Органический экстракт сушат над MgSO4 и упаривают. Выход: 92% промежуточного соединения 2.
Пример А2
а) Получение промежуточного соединения 3
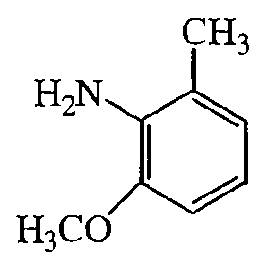
1-Метокси-3-метил-2-нитробензол (25 г, 149,7 ммоль) растворяют в EtOH (100 мл). Добавляют 10% Pd/C (2,5 г) и смесь гидрируют в течение 24 часов при комнатной температуре, после чего смесь фильтруют через целит. Смесь упаривают. Выход: 20,02 г (97%) промежуточного соединения 3 (CI-MC: 138 [M+H]+).
b) Получение промежуточного соединения 4
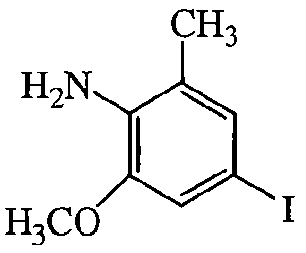
Промежуточное соединение 3 (3,3 г, 24,1 ммоль) растворяют в уксусной кислоте (15 мл). Добавляют монохлорид йода (5,87 г, 36 ммоль). Смесь перемешивают при комнатной температуре в течение 30 минут и упаривают. Остаток суспендируют в водном растворе Na2CO3 и экстрагируют дихлорметаном. После сушки дихлорметанового экстракта над MgSO4 его упаривают, и остаток очищают на колонке с силикагелем, используя дихлорметан в качестве элюента. Выход: 0,758 г (13%) промежуточного соединения 4 (CI-MC: 264 [M+H]+).
Пример А3
а) Получение промежуточного соединения 5
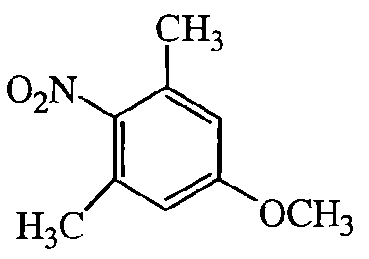
1-Метокси-3,5-диметибензол (4,12 г, 30 ммоль) растворяют в уксусной кислоте (20 мл). К полученному раствору добавляют по каплям смесь дымящей азотной кислоты (1,26 мл, 30 ммоль) и концентрированной серной кислоты (1,9 мл, 35 ммоль). Смесь нагревают при 70°С в течение 15 минут. После охлаждения добавляют воду и смесь экстрагируют дихлорметаном. Органический экстракт сушат и упаривают. Полученный остаток очищают колоночной хроматографией (30% гептана в CH2Cl2). Выход: 1,91 г (35%) промежуточного соединения 5 (CI-MC: 182 [M+H]+).
b) Получение промежуточного соединения 6
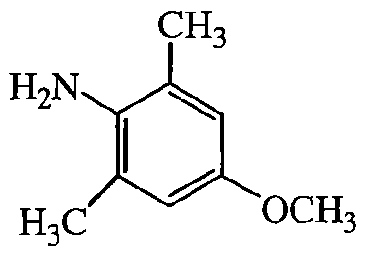
К раствору промежуточного соединения 5 (1,81 г, 10 ммоль) в этаноле (20 мл) добавляют дигидрат хлорида олова(II) (11,51 г, 50 ммоль) и смесь кипятят с обратным холодильником в течение ночи. После охлаждения к реакционной смеси добавляют лед, а затем смесь подщелачивают 2N раствором NaOН. Смесь фильтруют и фильтрат концентрируют при пониженном давлении. Водный раствор экстрагируют дихлорметаном (4 × 30 мл). Органические слои объединяют и сушат над безводным MgSO4, и удаляют растворитель при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (элюент CH2Cl2). Выход: 1,18 г (78%) промежуточного соединения 6 (CI-MC: 152 [M+H]+).
Пример А4
а) Получение промежуточных соединений 7 и 8
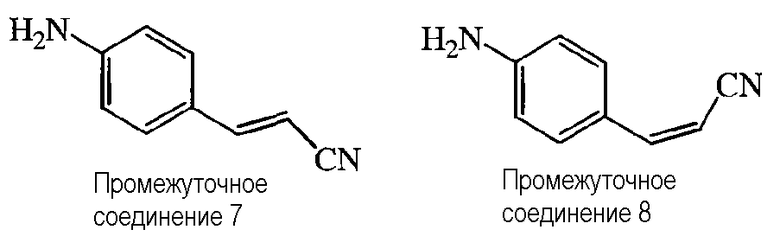
К раствору 4-йодбензоламина (10 г, 45,20 ммоль) в ДМФА (20 мл) добавляют акрилонитрил (10 мл), триэтиламин (8 мл), ацетат палладия (0,540 г, 1,13 ммоль) и трифенилфосфин (0,598 г, 2,26 ммоль). После дегазирования реакционной смеси ее продувают азотом и колбу закрывают перегородкой (was stopped with septum). Затем смесь перемешивают в течение ночи при 100°С. После охлаждения реакционную смесь разбавляют дихлорметаном. Раствор в CH2Cl2 промывают водой (3 раза), сушат над MgSO4 и упаривают. После упаривания остаток очищают колоночной хроматографией на силикагеле с элюированием CH2Cl2. Выход: 2,50 г (38%) промежуточного соединения 7 (CI-MC: 145 [M+H]+) с образованием промежуточного соединения 8.
b) Получение промежуточного соединения 9
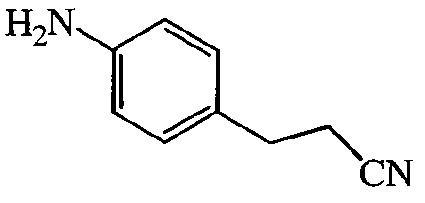
Промежуточное соединение 7 (1,58 г) растворяют в EtOH (15 мл). Добавляют 10% Pd/C (100 мг) и смесь гидрируют в течение 24 часов при комнатной температуре, после чего смесь фильтруют через целит. Растворитель выпаривают. Выход: 1,56 г (97%) промежуточного соединения 9 (CI-MC: 147 [M+H]+).
с) Получение промежуточного соединения 10
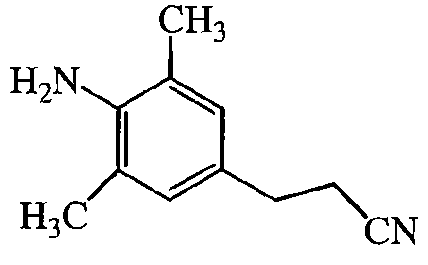
3-(4-Амино-3,5-диметилфенил)-2-пропеннитрил (3,44 г, 20 ммоль) растворяют в EtOH (20 мл). Добавляют 10% Pd/C (0,300 г) и смесь гидрируют в течение 24 часов при комнатной температуре, после чего смесь фильтруют через целит. Растворитель выпаривают. Выход: 3,21 г (92%) промежуточного соединения 10 (CI-MC: 175 [M+H]+).
d) Получение промежуточных соединений 39 и 40
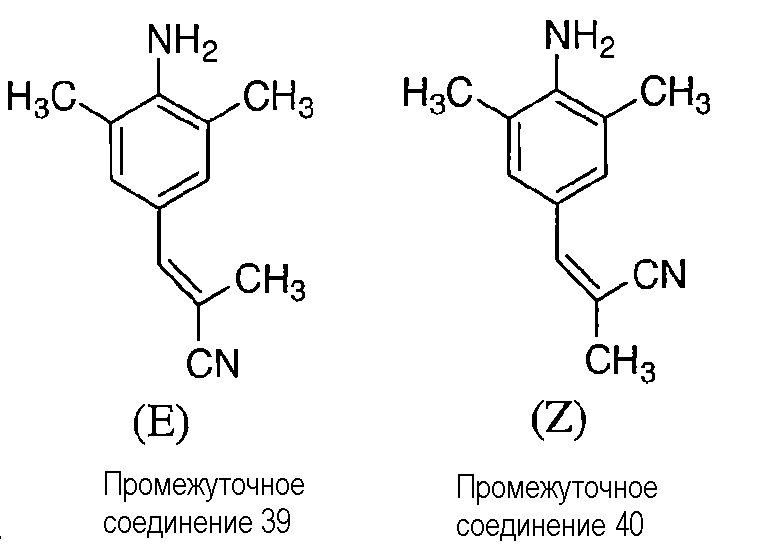
К раствору 4-бром-2,6-диметиланилина (2,00 г, 10 ммоль) в ацетонитриле (20 мл) добавляют метакрилонитрил (2,6 мл, 30 ммоль), триэтиламин (2,20 мл, 15 ммоль), Pd(OAc)2 (0,478 г (47%), 1 ммоль) и (о-тол)3Р (0,614 г, 2 ммоль). После дегазирования реакционной смеси ее перемешивают в течение ночи при 80°С. После охлаждения реакционную смесь разбавляют CH2Cl2 и промывают водным раствором карбоната калия. Органический раствор упаривают и остаток очищают колоночной хроматографией (20% EtOAc в гептане). Выход: 0,384 г смеси 1:1 промежуточных соединений 39 и 40 (CI-MC: 187 [M+H]+) и извлекают 1,420 г 4-бром-2,6-диметиланилина.
Пример А4А
а) Получение промежуточного соединения 41
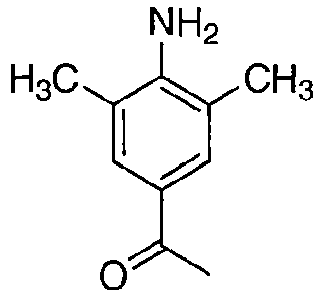
К раствору 4-бром-2,6-диметиланилина (4,00 г, 20 ммоль) в ДМФА (25 мл) и Н2О (3 мл) добавляют бутилвиниловый эфир (6,7 мл, 50 ммоль), Pd(OAc)2 (0,286 г, 0,60 ммоль), 1,3-бис(дифенилфосфино)пропан (DPPP, 0,561 г, 1,32 ммоль) и К2СО3. Смесь дегазируют в течение нескольких минут, а затем нагревают в течение ночи. После охлаждения к реакционной смеси добавляют Н2О (50 мл) и затем экстрагируют CH2Cl2 (3 × 100 мл). Органический слой упаривают и остаток растворяют в ТГФ (20 мл). Добавляют концентрированную HCl (1 мл) и смесь перемешивают в течение 1 часа. Смесь подщелачивают, добавляя водный раствор К2СО3 и затем экстрагируют CH2Cl2. После упаривания органического слоя полученный остаток очищают колоночной хроматографией (3% EtOAc в CH2Cl2). Выход: 0,650 г (20%) промежуточного соединения 41 (CI-MC: 164 [M+H]+).
b) Получение промежуточных соединений 42 и 43
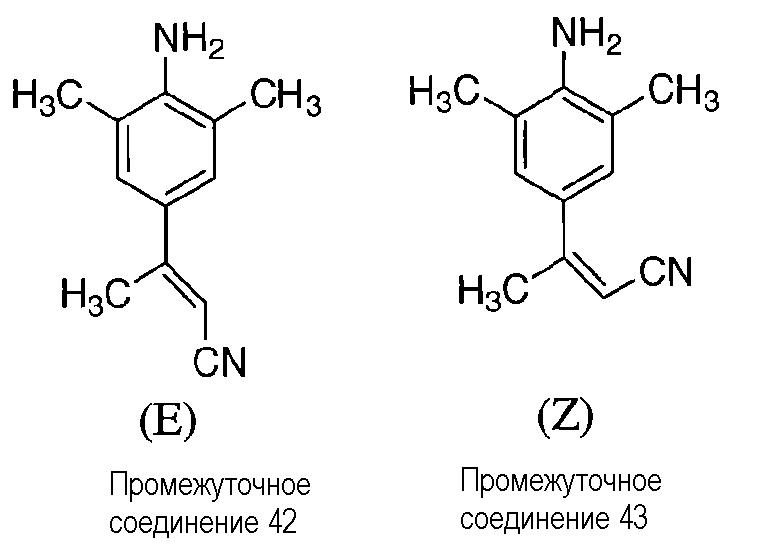
К раствору диэтилцианометилфосфоната (1,470 г, 8,28 ммоль) в ТГФ (10 мл) при 5°С добавляют трет-BuOK (0,947 г, 8,28 ммоль). Смесь доводят до комнатной температуры и перемешивают в течение 30 минут. К полученной смеси добавляют по каплям раствор промежуточного соединения 41 (0,900 г, 5,52 ммоль) в ТГФ (10 мл). Смесь перемешивают в течение 7 суток и упаривают. Остаток распределяют между Н2О и CH2Cl2. Органический слой упаривают и остаток очищают колоночной хроматографией (20% EtOAc в гептане). Выход: 0,565 г (55%) промежуточного соединения 42 (CI-MC: 187 [M+H]+) и 0,154 г (15%) смеси промежуточных соединений 42 и 43.
Пример А4В
а) Получение промежуточного соединения 44
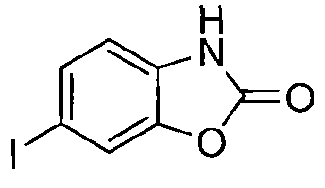
К раствору 2-бензоксазолона (4,05 г, 30 ммоль) в уксусной кислоте (30 мл) добавляют монохлорид йода (8,71 г, 33,99 ммоль). Смесь перемешивают в течение 48 часов. После упаривания остаток растворяют в этилацетате и полученный раствор промывают водным раствором карбоната калия. Органический раствор сушат над MgSO4 и упаривают. Выход: 7,42 г (95%) промежуточного соединения 44 (CI-MC: 262 [M+H]+).
b) Получение промежуточного соединения 45
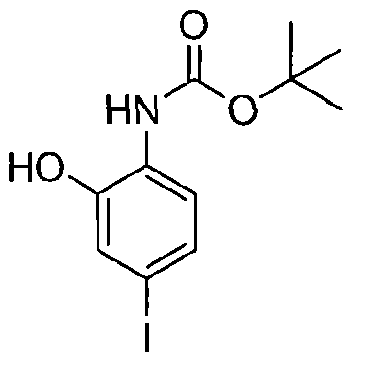
К раствору промежуточного соединения 44 (7,42 г, 28,50 ммоль) в ТГФ (100 мл) добавляют триэтиламин (4,8 мл, 34,2 ммоль), 4-N,N-диметиламинопиридин (0,704 г, 5,7 ммоль) и ди-трет-бутилдикарбонат (8,11 г, 37,2 ммоль). Смесь перемешивают в течение 3 часов, а затем упаривают. Полученный остаток растворяют в метаноле (100 мл) и к полученному раствору добавляют карбонат калия (4 г, 28,98 ммоль). Смесь перемешивают в течение ночи. Добавляют уксусную кислоту (4 мл) и затем смесь упаривают. Остаток распределяют между метиленхлоридом и водой. Органический раствор сушат над MgSO4 и упаривают. Выход: 8,46 г промежуточного соединения 45 (CI-MC: 336 [M+H]+), которое используют без дополнительной очистки.
с) Получение промежуточного соединения 46
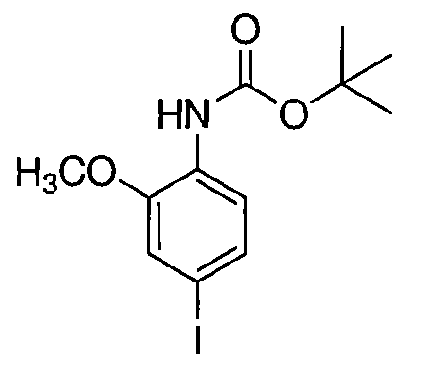
Карбонат калия (6,67 г, 50,50 ммоль) и метилйодид (10,90 г, 75,75 ммоль) добавляют к раствору промежуточного соединения 45 (8,46 г, 25,5 ммоль) в ТГФ (30 мл). Смесь перемешивают в течение ночи. После упаривания остаток растворяют в CH2Cl2 и раствор промывают водой. Органический раствор упаривают. Полученное промежуточное соединение 46 (CI-MC: 350 [M+H]+) используют без дополнительной очистки.
d) Получение промежуточного соединения 47
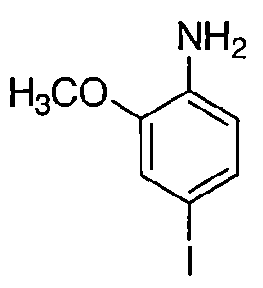
Промежуточное соединение 46, полученное на стадии с), растворяют в трифторуксусной кислоте (10 мл). Через 10 минут смесь упаривают. Остаток растворяют в CH2Cl2 и раствор промывают водным раствором карбоната калия. Органический слой упаривают и остаток очищают колоночной хроматографией (30% гептана в CH2Cl2). Выход: 3,87 г промежуточного соединения 47 (CI-MC: 250 [M+H]+).
е) Получение промежуточного соединения 48
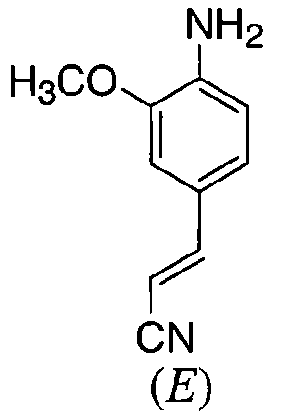
К раствору промежуточного соединения 47 (8,40 г, 33,73 ммоль) в ацетонитриле (20 мл) добавляют акрилонитрил (5,37 г, 101,20 ммоль), триэтиламин (7,70 мл, 101,50 ммоль), диметилацетамид (4,5 мл), Pd(OAc)2 (0,806 г, 1,69 ммоль) и (о-тол)3Р (1,027 г, 3,38 ммоль). После дегазирования смеси ее перемешивают в течение ночи при 80°С. После охлаждения реакционную смесь разбавляют CH2Cl2 и промывают водным раствором карбоната калия. Органический раствор упаривают и остаток очищают колоночной хроматографией (CH2Cl2). Выход: 4,77 г (85%) промежуточного соединения 48 (CI-MC: 175 [M+H]+).
f) Получение промежуточного соединения 49
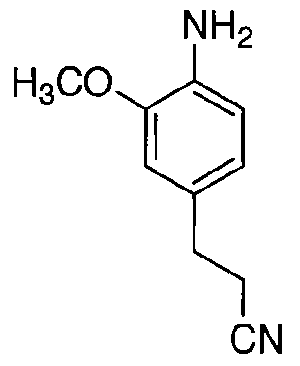
Промежуточное соединение 48 (4,63 г, 26,61 ммоль) растворяют в EtOH (50 мл). Добавляют 10% Pd/C (1,00 г) и смесь гидрируют в течение 24 часов при комнатной температуре, после чего ее фильтруют через целит. Растворитель выпаривают. Выход: 4,55 г (97%) промежуточного соединения 49 (CI-MC: 177 [M+H]+).
g) Получение промежуточных соединений 50 и 51
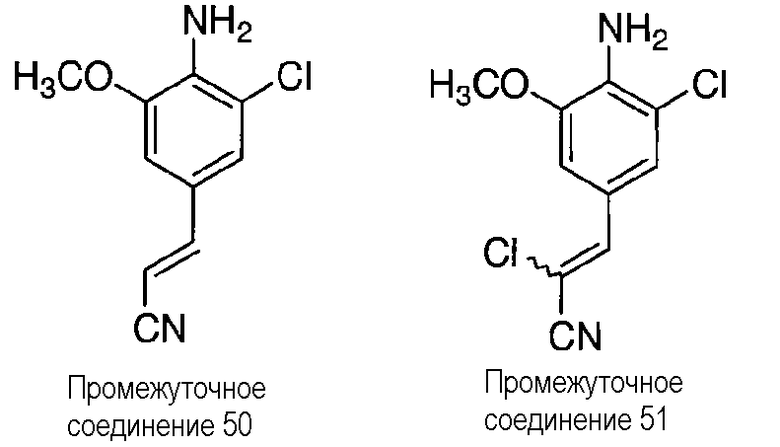
К раствору промежуточного соединения 48 (2,4 г, 13,79 ммоль) в ацетонитриле (30 мл) добавляют N-хлорсукцинимид (3,683 г, 27,59 ммоль). Смесь нагревают при 50°С в течение 2 часов и упаривают. Остаток распределяют между водой и CH2Cl2. Органический слой упаривают и остаток очищают колоночной хроматографией (CH2Cl2). Выход: 0,420 г (15%) промежуточного соединения 50 (CI-MC: 209 [M+H]+) и 0,840 г (25%) промежуточного соединения 51 (CI-MC: 243 [M+H]+).
h) Получение промежуточного соединения 52
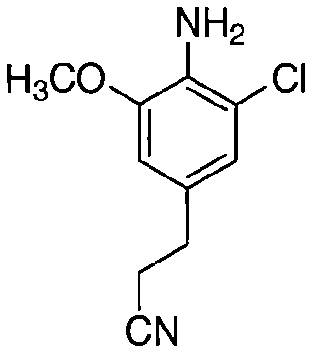
Промежуточное соединение 51 (0,840 г, 3,45 ммоль) растворяют в EtOH (10 мл). Добавляют 10% Pd/C (0,100 г) и смесь гидрируют в течение 3 часов при комнатной температуре, после чего ее фильтруют через целит. Растворитель выпаривают. Выход: 0,280 г (38%) промежуточного соединения 52 (CI-MC: 213 [M+H]+).
Пример А5
а) Получение промежуточного соединения 11
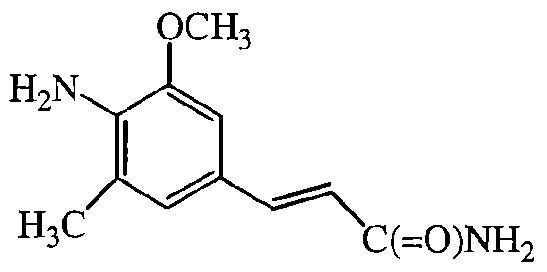
4-Бром-6-метокси-2-метиланилин, полученный согласно A1b (7,06 г, 32,4 ммоль), растворяют в 30 мл ацетонитрила. К полученному раствору добавляют акриламид (3,45 г, 48,6 ммоль), 47% Pd(OAc)2 (0,726 г, 3,24 ммоль), трис(2-метилфенил)фосфин (1,9 г, 6,48 ммоль), N,N-диметилэтанамин (4,3 мл) и триэтиламин (7,5 мл). Смесь продувают азотом в течение 10 минут и перемешивают в течение ночи. Смесь разбавляют 200 мл дихлорметана и промывают три раза 75 мл воды. Водные слои объединяют и 5 раз экстрагируют 150 мл этилацетата. Дихлорметановые и этилацетатные слои объединяют, сушат (MgSO4) и фильтруют. Растворитель выпаривают и остаток перемешивают с диизопропиловым эфиром с последующим фильтрованием. Выход: 5,51 г (83%) промежуточного соединения 11 (CI-MC: 207 [M+H]+).
b) Получение промежуточного соединения 12
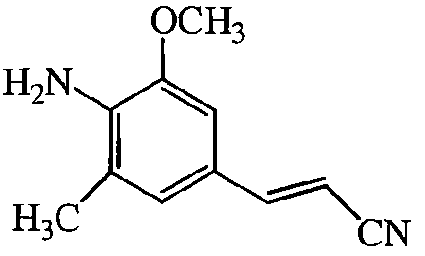
POCl3 (15 мл) охлаждают до 0°С и добавляют к 5,50 г (26,7 ммоль) промежуточного соединения 11 на ледяной бане. Реакционную смесь доводят до комнатной температуры и перемешивают в течение ночи при этой температуре. Смесь добавляют по каплям к 250 мл диизопропилового эфира при энергичном перемешивании. Выпавшее в осадок вещество отфильтровывают и промывают диизопропиловым эфиром. Остаток (7,1 г) добавляют к 150 мл дихлорметана. Добавляют водный раствор К2СО3 и дихлорметановый слой отделяют и упаривают. Остаток очищают на колонке с силикагелем (элюент CH2Cl2). Выход: 3,21 г (64%) промежуточного соединения 12 (CI-MC: 189 [M+H]+).
с) Получение промежуточного соединения 13
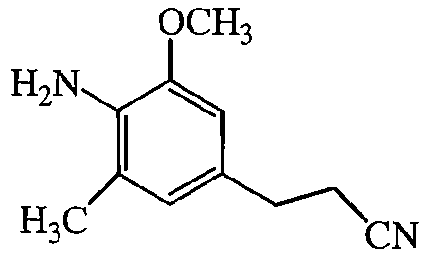
Промежуточное соединение 12 (1,70 г, 9,04 ммоль) растворяют в EtOH (20 мл). Добавляют 10% Pd/C (0,300 г) и смесь гидрируют в течение 24 часов при комнатной температуре, после чего ее фильтруют через целит. Растворитель выпаривают. Выход: 1,57 г (91%) промежуточного соединения 13 (CI-MC: 191 [M+H]+).
Пример А6
а) Получение промежуточного соединения 14
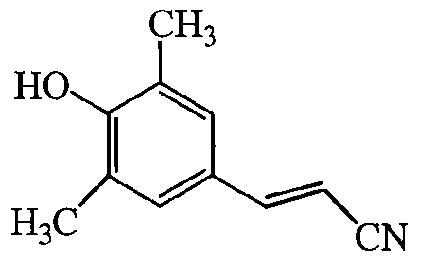
3-(4-Амино-3,5-диметилфенил)-2-пропеннитрил в виде гидрохлоридной соли (4,16 г, 20 ммоль) суспендируют в 10 мл воды. Добавляют концентрированную HCl (5 г), а затем 10 г толченого льда. Полученную смесь охлаждают до 0°С и диазотируют, добавляя по каплям раствор NaNO2 (1,40 г, 20 ммоль). После перемешивания в течение 25 минут реакционную смесь добавляют по каплям к раствору 1 мл концентрированной HCl в 20 мл Н2О при 50°С и перемешивают в течение 30 минут. Добавляют дихлорметан (50 мл) и органический слой отделяют. Растворитель выпаривают и остаток очищают на колонке с силикагелем, элюируя дихлорметаном. Выход: 1,59 г (48%) промежуточного соединения 14 (CI-MC: 174 [M+H]+).
b) Получение промежуточного соединения 15
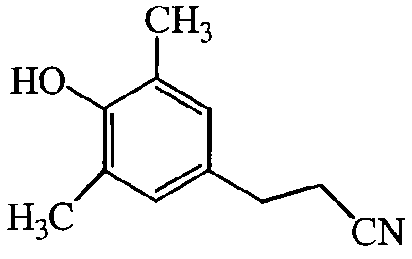
Промежуточное соединение 14 (1,2 г, 6,9 ммоль) растворяют в EtOH (20 мл). Добавляют 10% Pd/C (0,250 г) и смесь гидрируют в течение ночи. После фильтрования через целит растворитель выпаривают. Выход: 1,15 г (95%) промежуточного соединения 15 (CI-MC: 176 [M+H]+).
Пример А7
а) Получение промежуточного соединения 16
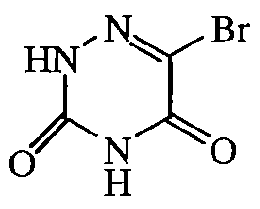
Смесь 25 г (217 ммоль) 6-азаурацила, брома (25 мл) и воды (250 мл) перемешивают при комнатной температуре в течение 30 часов. Кристаллический продукт реакции отфильтровывают. Фильтрат концентрируют и второе выпавшее в осадок вещество собирают фильтрованием. Две фракции выпавшего в осадок вещества объединяют и сушат. Выход: 38,3 г (92%) промежуточного соединения 16 (5-бром-6-азаурацил) (т.пл. 231-234°С).
b) Получение промежуточного соединения 17
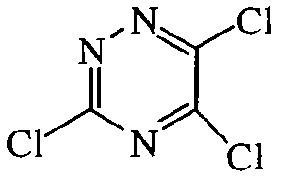
К 18 г (93,75 ммоль) 5-бром-6-азаурацила (промежуточное соединение 16) в 150 мл оксихлорида фосфора добавляют 39,2 г (188 ммоль) пентахлорида фосфора и 38 мл (240 ммоль) N,N-диэтиланилина. Смесь перемешивают при 120°С в течение 5 часов, после чего избыток растворителя выпаривают. Остаток несколько раз экстрагируют тетрахлоридом углерода. После выпаривания растворителя оставшийся маслянистый остаток помещают в холодильник, где он отверждается. Выход: 13 г (78%) промежуточного соединения 17 (3,5,6-трихлор[1,2,4]триазин) (т.пл. 57-60°С).
Пример А8
а) Получение промежуточного соединения 18
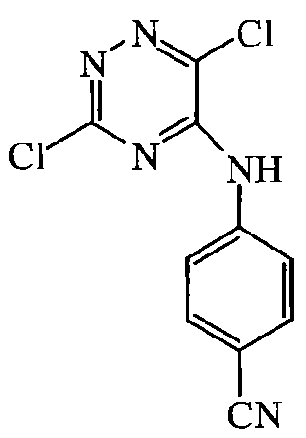
Промежуточное соединение 16 (7,68 г, 40 ммоль) растворяют в оксихлориде фосфора (40 мл). Раствор охлаждают на ледяной бане. Добавляют по каплям триэтиламин (8 мл). По окончании добавления баню удаляют и смесь нагревают при 70°С в течение 30 минут. Добавляют вторую порцию триэтиламина (2 мл). Нагревание продолжают в течение 30 минут, затем избыток растворителя выпаривают. Остаток растворяют в сухом CH2Cl2 (60 мл). Полученный раствор охлаждают на ледяной бане. Добавляют раствор 4-аминобензонитрила (4,34 г, 36 ммоль) в сухом CH2Cl2 (40 мл). После перемешивания в течение 5 минут ледяную баню удаляют. После перемешивания в течение 15 минут появляется осадок. Добавляют по каплям триэтиламин (примерно 3 мл) до полного растворения выпавшего в осадок вещества. К раствору добавляют лед и образовавшийся осадок удаляют фильтрованием. Фильтрат промывают водным раствором Na2CO3. Органический раствор сушат над MgSO4 и упаривают. Выход: 4,885 г (51%) промежуточного соединения 18 (CI-MC: 266 [M+H]+).
b-1) К раствору 4-аминобензонитрила (10 г, 84,6 ммоль) в сухом ТГФ (80 мл) добавляют ди-трет-бутилдикарбонат (27,1 г, 127 ммоль) и 4-диметиламинопиридин (500 мг). Смесь кипятят с обратным холодильником в течение 3 часов. После упаривания остаток хроматографируют на колонке с силикагелем, используя в качестве элюента CH2Cl2. После перекристаллизации из смеси метанола и воды выделяют промежуточное соединение. Выход: 42% 1,1-диметилэтилового эфира 4-цианофенилкарбаминовой кислоты (CI-MC: 219 [M+H]+).
b-2) Получение промежуточного соединения 19
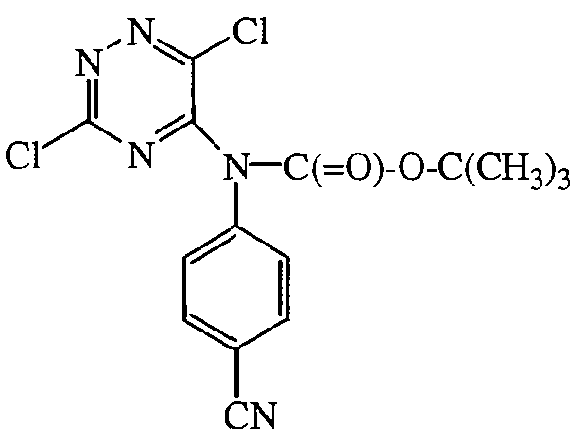
К раствору 1,1-диметилэтилового эфира 4-цианофенилкарбаминовой кислоты (1,18 г, 5,42 ммоль) в сухом ТГФ (20 мл) при 0°С добавляют NaH (0,22 г, 5,42 ммоль). После перемешивания в течение 5 минут при указанной температуре добавляют раствор промежуточного соединения 17 (1 г, 5,42 ммоль) в ТГФ (10 мл). Смесь перемешивают в течение ночи при 50°С. После выпаривания растворителя добавляют воду и осуществляют экстракцию раствором 7% метанола в дихлорметане. Экстракт сушат над MgSO4 и упаривают. Сырое промежуточное соединение 19 используют в дальнейшем без дополнительной очистки.
с) Получение промежуточного соединения 20
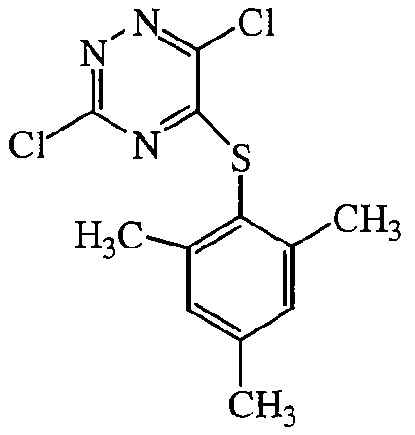
К раствору промежуточного соединения 17 (0,560 г, 3 ммоль) в сухом ТГФ (30 мл) при -78°С в атмосфере азота добавляют 2,4,6-триметилтиофенол (3 ммоль) и карбонат натрия (0,318 г, 3 ммоль). Реакционную смесь доводят до комнатной температуры и затем перемешивают в течение ночи при этой температуре. Растворитель выпаривают. Полученный остаток суспендируют в воде и экстрагируют дихлорметаном. Дихлорметановый раствор сушат над MgSO4 и упаривают. Остаток хроматографируют на колонке с силикагелем, используя в качестве элюента смесь 30% гептана в дихлорметане. Выход: 68% промежуточного соединения 20 (CI-MC: 300 [M+H]+).
Аналогично получают промежуточные соединения с линкером кислородом вместо линкера серы.
d) Получение промежуточного соединения 21
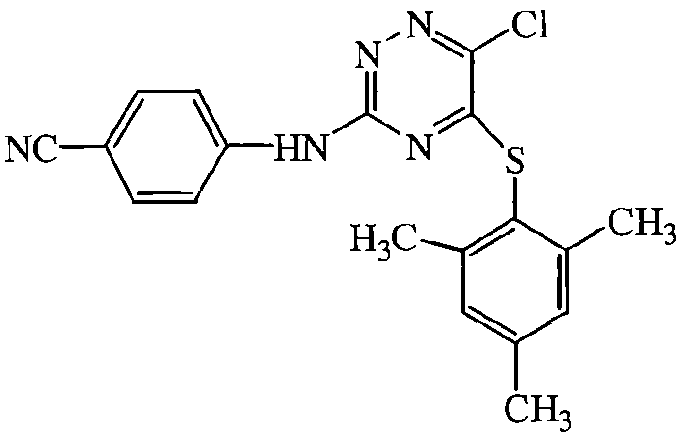
Смесь промежуточного соединения 20 (1 эквив.), 4-аминобензонитрила (1,5 эквив.) и камфорсульфоновой кислоты (CSA) (0,7 эквив.) в ТГФ кипятят с обратным холодильником в течение 48 часов. После выпаривания растворителя остаток суспендируют в водном растворе Na2CO3 и экстрагируют CH2Cl2. Дихлорметановый раствор сушат над MgSO4 и упаривают. Полученный остаток очищают колоночной хроматографией с использованием в качестве элюента смеси 5% этилацетата в дихлорметане. Выход: 46% промежуточного соединения 21 (т.пл. 295-296°С).
Пример А9
а) Получение промежуточного соединения 22
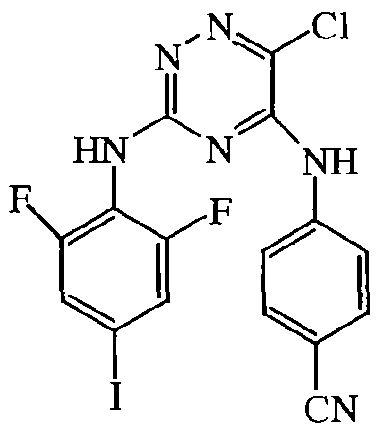
Смесь промежуточного соединения 18 (1 эквив.), 2,6-дифтор-4-йодбензоламина (1,5 эквив.) и камфорсульфоновой кислоты (0,7 эквив.) в 2-пропаноле кипятят с обратным холодильником в течение 20-48 часов (масляная баня, 120°С). Выпавшее в осадок вещество собирают фильтрованием и последовательно промывают на фильтре водным раствором Na2CO3, водой и дихлорметаном, получая промежуточное соединение 22. Для того чтобы увеличить выход или получить аналитические образцы, фильтраты с 2-пропанолом и CH2Cl2 объединяют и упаривают. Остаток суспендируют в водном растворе Na2CO3 и экстрагируют CH2Cl2. После сушки над MgSO4 и упаривания дихлорметанового экстракта остаток очищают колоночной хроматографией, используя в качестве элюента 10% этилацетата в дихлорметане, с получением промежуточного соединения 22. Общий выход 49% (CI-MC: 485 [M+H]+).
b) Получение промежуточного соединения 24
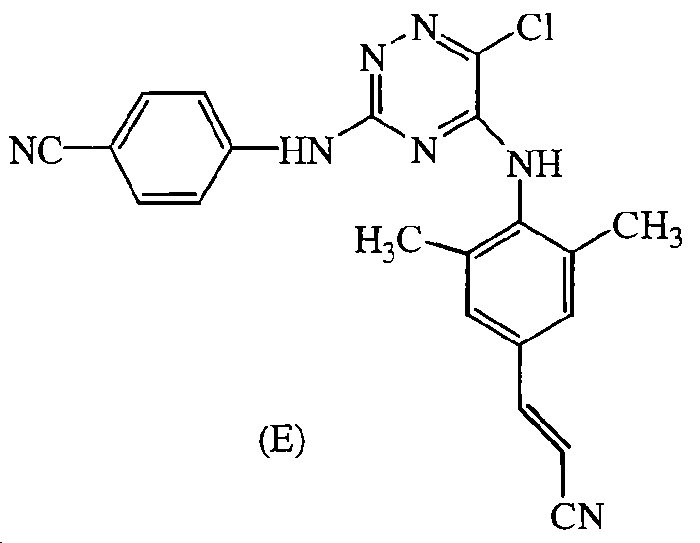
К раствору 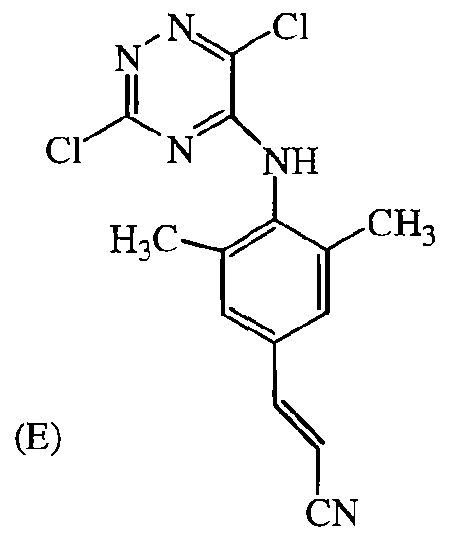 (промежуточное соединение 23; получено согласно примеру А8а) (1 эквив.) в 2-пропаноле добавляют 4-аминобензонитрил (1,5 эквив.) и камфорсульфоновую кислоту (CSA, 0,7 эквив.). Смесь кипятят с обратным холодильником в течение 48 часов при 120°С. После выпаривания растворителя остаток суспендируют в водном растворе Na2CO3 и экстрагируют CH2Cl2. Дихлорметановый раствор сушат над MgSO4 и упаривают. Полученный остаток очищают колоночной хроматографией, используя в качестве элюента 10% этилацетата в дихлорметане. Выход: 65% промежуточного соединения 24 (т.пл. 281-282°С).
(промежуточное соединение 23; получено согласно примеру А8а) (1 эквив.) в 2-пропаноле добавляют 4-аминобензонитрил (1,5 эквив.) и камфорсульфоновую кислоту (CSA, 0,7 эквив.). Смесь кипятят с обратным холодильником в течение 48 часов при 120°С. После выпаривания растворителя остаток суспендируют в водном растворе Na2CO3 и экстрагируют CH2Cl2. Дихлорметановый раствор сушат над MgSO4 и упаривают. Полученный остаток очищают колоночной хроматографией, используя в качестве элюента 10% этилацетата в дихлорметане. Выход: 65% промежуточного соединения 24 (т.пл. 281-282°С).
Описанное выше взаимодействие можно осуществить в ТГФ в качестве растворителя, в таком случае реакционную смесь кипятят с обратным холодильником в течение 48 часов.
с) Получение промежуточного соединения 53
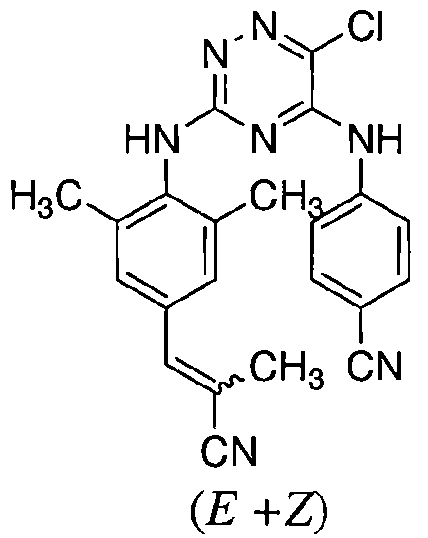
К раствору смеси промежуточных соединений 39 и 40 (E+Z изомеры, 0,380 г, 2,04 ммоль) в ТГФ (20 мл) добавляют промежуточное соединение 18 (0,707 г, 2,66 ммоль) и камфорсульфоновую кислоту (0,331 г, 1,43 ммоль). Смесь в 20 мл ТГФ кипятят с обратным холодильником в течение ночи (масляная баня, 130°С) и затем упаривают. После охлаждения выпавшее в осадок вещество собирают фильтрованием и затем последовательно промывают водным раствором К2CO3 (3×), водой, CH2Cl2 и Et2O. Получают промежуточное соединение 53. Супернатант упаривают и остаток суспендируют в водном растворе К2CO3 и экстрагируют дихлорметаном (3 раза). После упаривания дихлорметанового экстракта остаток очищают колоночной хроматографией (10% этилацетата в дихлорметане), получая еще некоторое количество промежуточного соединения 53. Выход: 0,315 г (27%) промежуточного соединения 53 (CI-MC: 416 [M+H]+).
d) Получение промежуточного соединения 54
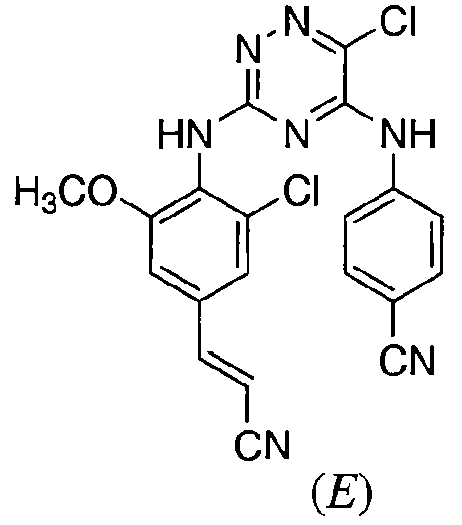
Смесь промежуточного соединения 18 (0,638 г, 2,398 ммоль), промежуточного соединения 50 (0,250 г, 1,20 ммоль) и камфорсульфоновой кислоты (0,194 г, 0,83 ммоль) в 10 мл ТГФ кипятят с обратным холодильником в течение ночи (масляная баня, 130°С) и затем упаривают. Остаток суспендируют в водном растворе К2CO3 и экстрагируют дихлорметаном (3 раза). После упаривания дихлорметанового экстракта остаток очищают колоночной хроматографией (10% этилацетата в дихлорметане). Выход: 0,110 г (19%) промежуточного соединения 54 (CI-MC: 438 [M+H]+).
е) Получение промежуточного соединения 55
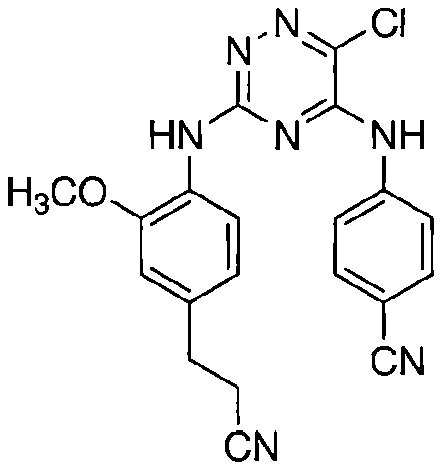
Смесь промежуточного соединения 18 (2,75 г, 10,33 ммоль), промежуточного соединения 49 (2,182 г, 12,4 ммоль) и камфорсульфоновой кислоты (1,624 г, 7,0 ммоль) в 60 мл ТГФ кипятят с обратным холодильником в течение ночи (масляная баня, 130°С) и затем упаривают. После охлаждения выпавшее в осадок вещество (=промежуточное соединение 55·HCl) собирают фильтрованием и затем последовательно промывают водным раствором К2CO3 (3×), водой, CH2Cl2 и Et2O. Выход: 3,40 г (81%) промежуточного соединения 55 (CI-MC: 406 [M+H]+).
Пример А10
а) Получение промежуточного соединения 25
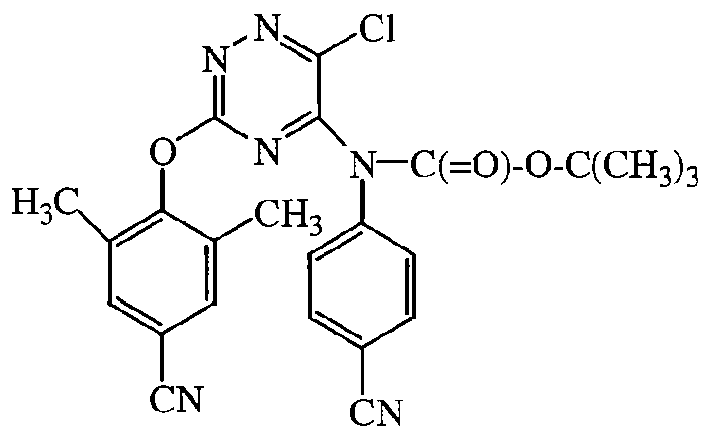
К раствору промежуточного соединения 19 (1 эквив.) в ТГФ добавляют 4-гидрокси-3,5-диметилбензонитрил (1 эквив.) и К2CO3 (1 эквив.). Смесь нагревают в течение 15-30 минут при 100°С. После упаривания остаток растворяют в дихлорметане. Дихлорметановый раствор промывают водой и затем сушат над MgSO4 и упаривают. Выход: промежуточное соединение 25, которое используют на следующей стадии.
b) Получение промежуточного соединения 26
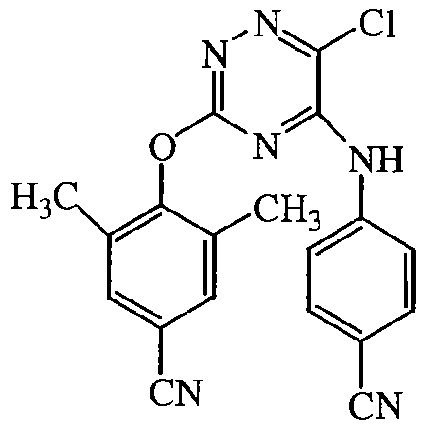
Остаток, полученный на стадии а), обрабатывают трифторуксусной кислотой (ТФУК) в течение 5 минут. После выпаривания ТФУК остаток растворяют в дихлорметане и добавляют триэтиламин (5 эквив.). После выпаривания растворителя остается остаток, который очищают колоночной хроматографией на силикагеле с использованием в качестве элюента смеси 10% EtOAc/90% CH2Cl2. Выход: 43% промежуточного соединения 26 (т.пл. 262-264°С).
Пример А11
Получение промежуточного соединения 27
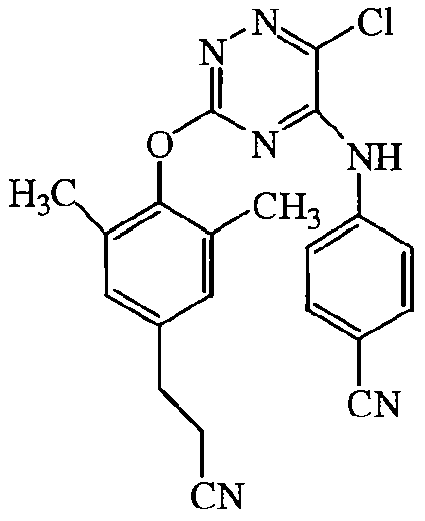
К раствору промежуточного соединения 18 (0,585 г, 2,2 ммоль) в ТГФ (10 мл) добавляют 3-(4-гидрокси-3,5-диметилфенил)пропаннитрил (0,580 г, 3,3 ммоль) и К2CO3 (0,910 г, 6,6 ммоль). Смесь нагревают при 135°С в течение 48 часов и упаривают. К остатку добавляют дихлорметан (50 мл) и воду (20 мл). Слои разделяют. Органический раствор упаривают и остаток очищают колоночной хроматографией (диоксид кремния, 10% EtOAc в CH2Cl2). Выход: 0,232 г (26%) промежуточного соединения 27 (CI-MC: 405 [M+H]+).
Пример А12
а) Получение промежуточного соединения 29
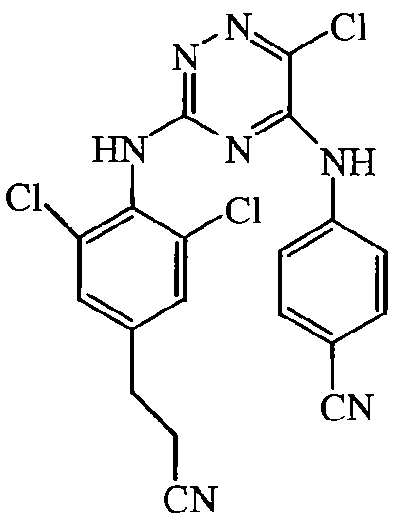
В двугорлой колбе, защищенной алюминиевой фольгой и снабженной холодильником, растворяют 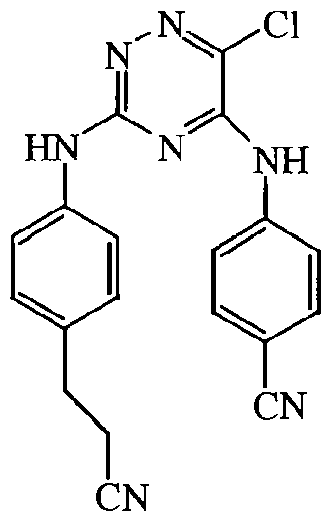 (промежуточное соединение 28; получено согласно примеру А9а) (0,200 г, 0,53 ммоль) в уксусной кислоте (5 мл). Добавляют N-хлорсукцинимид (NCS, 0,212 г, 1,60 ммоль). Смесь дегазируют и нагревают при 110°С в течение 15-30 минут. После упаривания остаток растворяют в этилацетате. Раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Остаток хроматографируют на колонке с силикагелем (10% EtOAc в CH2Cl2). Выход: 17% промежуточного соединения 29 (т.пл. 254-257 °С).
(промежуточное соединение 28; получено согласно примеру А9а) (0,200 г, 0,53 ммоль) в уксусной кислоте (5 мл). Добавляют N-хлорсукцинимид (NCS, 0,212 г, 1,60 ммоль). Смесь дегазируют и нагревают при 110°С в течение 15-30 минут. После упаривания остаток растворяют в этилацетате. Раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Остаток хроматографируют на колонке с силикагелем (10% EtOAc в CH2Cl2). Выход: 17% промежуточного соединения 29 (т.пл. 254-257 °С).
b) Получение промежуточных соединений 30 и 31
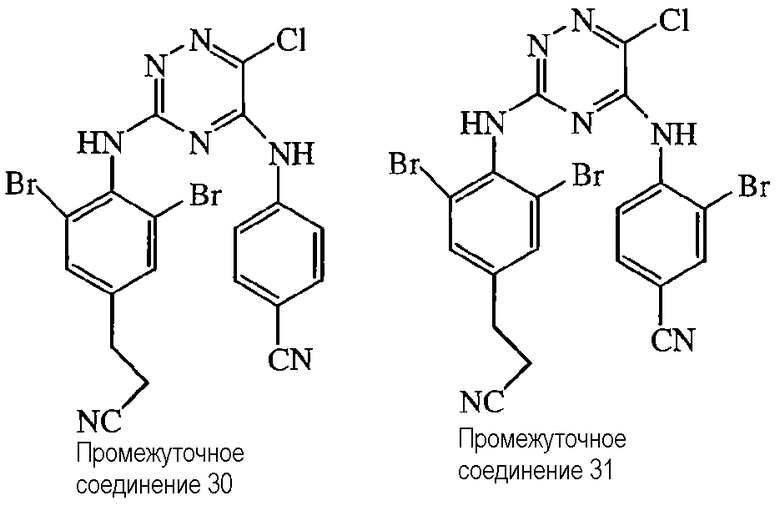
В двугорлой колбе, защищенной алюминиевой фольгой и снабженной холодильником, растворяют промежуточное соединение 28 (1,502 г, 4 ммоль) в уксусной кислоте (15 мл). Добавляют N-бромсукцинимид (2,140 г, 12 ммоль). Смесь дегазируют и нагревают при 120°С в течение 30 минут. Затем смесь выливают в 250 мл воды. Выпавшее в осадок вещество, собранное фильтрованием, растворяют в 150 мл этилацетата. Полученный раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Остаток хроматографируют на колонке с силикагелем (5% и 10% EtOAc в CH2Cl2). Выход: 0,491 г (23%) промежуточного соединения 30 (т.пл. 256-257°С) и 0,123 г (5%) промежуточного соединения 31 (т.пл. 273-275°С).
с) Получение промежуточного соединения 32
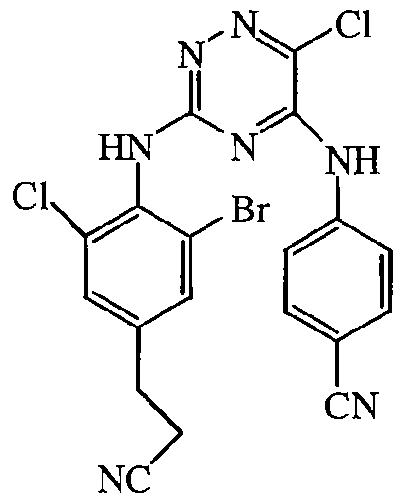
В двугорлой колбе, защищенной алюминиевой фольгой и снабженной холодильником, растворяют промежуточное соединение 28 (0,207 г, 0,55 ммоль) в уксусной кислоте. Добавляют N-бромсукцинимид (0,198 г, 1,1 ммоль). Смесь дегазируют и нагревают при 110°С в течение 15 минут. Остаток после упаривания растворяют в этилацетате. Раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Остаток растворяют в уксусной кислоте в двугорлой колбе, защищенной алюминиевой фольгой и снабженной холодильником, как описано выше, и добавляют N-хлорсукцинимид (0,111 г, 0,83 ммоль). Смесь дегазируют и нагревают при 110°С в течение 15 минут. Остаток после упаривания растворяют в этилацетате. Раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Остаток очищают колоночной хроматографией на силикагеле (10% EtOAc в CH2Cl2). Выход: 0,110 г (41%) промежуточного соединения 32 (т.пл. 252-254°С).
d) Получение промежуточного соединения 56
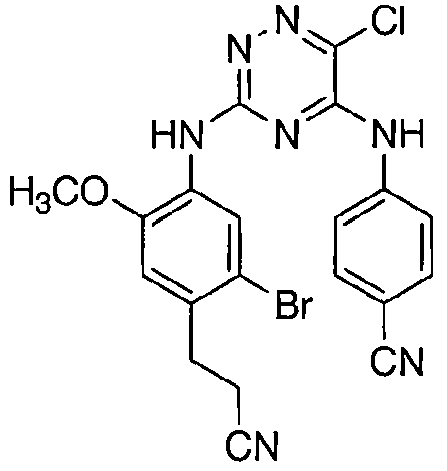
К раствору промежуточного соединения 55·HCl (0,550 г, 1,25 ммоль) в уксусной кислоте (10 мл) добавляют N-бромсукцинимид (0,338 г, 1,88 ммоль). Смесь нагревают в течение 2 часов при 120°С и затем упаривают. К остатку добавляют воду (20 мл) и смесь экстрагируют этилацетатом (3 × 50 мл). Органический слой сушат над MgSO4 и упаривают. Остаток очищают колоночной хроматографией (10% этилацетата в CH2Cl2). Выход: 0,109 г (18%) промежуточного соединения 56 (CI-MC: 484 [M+H]+).
е) Получение промежуточных соединений 57 и 58
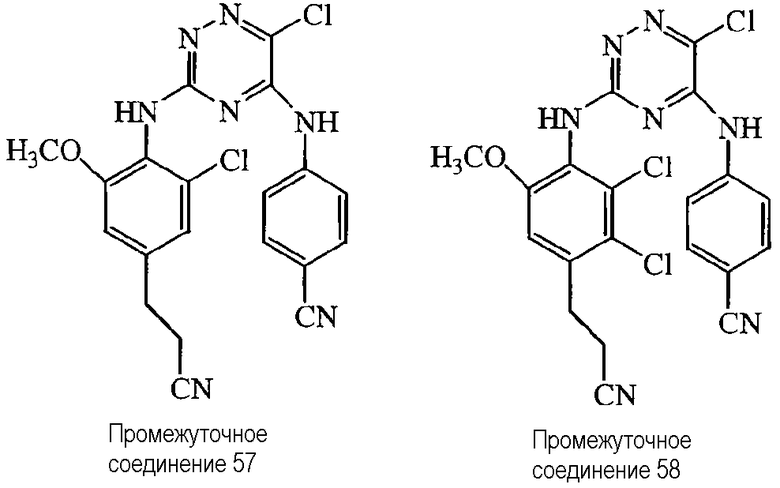
К раствору промежуточного соединения 55 (0,500 г, 1,23 ммоль) в уксусной кислоте (10 мл) добавляют N-хлорсукцинимид (0,248 г, 1,85 ммоль). Смесь нагревают в течение 1 часа при 120°С и затем упаривают. К остатку добавляют воду (20 мл) и смесь экстрагируют этилацетатом (3 × 50 мл). Органический слой сушат над MgSO4 и упаривают. Остаток очищают колоночной хроматографией (10% этилацетата в CH2Cl2). Выход: 0,200 г смеси промежуточных соединений 57 и 58 (CI-MC: 474 [M+H]+).
Пример А13
а) Получение промежуточного соединения 34
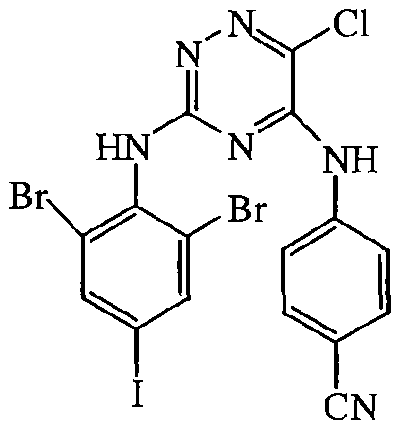
В двугорлой колбе, защищенной алюминиевой фольгой и снабженной холодильником, растворяют 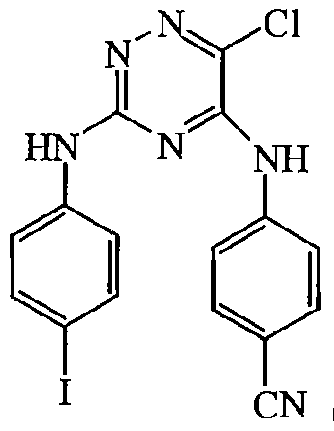 (промежуточное соединение 33; получено согласно примеру А9а) (1 г, 2,23 ммоль) в уксусной кислоте (10 мл). Добавляют N-бромсукцинимид (NВS, 1,603 г, 8,92 ммоль). Смесь дегазируют и нагревают при 120°С в течение 15 минут. После упаривания остаток растворяют в этилацетате. Раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Выход: промежуточное соединение 34, которое используют на следующей стадии.
(промежуточное соединение 33; получено согласно примеру А9а) (1 г, 2,23 ммоль) в уксусной кислоте (10 мл). Добавляют N-бромсукцинимид (NВS, 1,603 г, 8,92 ммоль). Смесь дегазируют и нагревают при 120°С в течение 15 минут. После упаривания остаток растворяют в этилацетате. Раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Выход: промежуточное соединение 34, которое используют на следующей стадии.
b) Получение промежуточного соединения 35
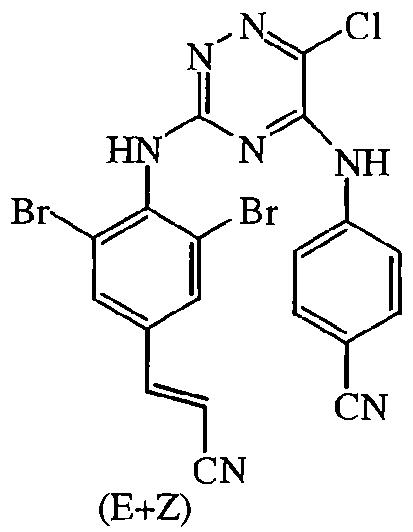
К раствору в ДМФА промежуточного соединения 34, полученного на стадии а), добавляют акрилонитрил (0,12 мл, 1,856 ммоль), триэтиламин (0,26 мл, 1,856 ммоль), ацетат палладия (0,0111 г, 0,023 ммоль) и трифенилфосфин (0,0123 г, 0,046 ммоль). После дегазирования реакционную смесь продувают азотом и колбу закрывают перегородкой. Затем реакционную смесь перемешивают в течение ночи при 100°С. После охлаждения реакционную смесь разбавляют дихлорметаном. Раствор в CH2Cl2 промывают водой (3 раза), сушат над MgSO4 и затем упаривают. Остаток после упаривания очищают колоночной хроматографией на силикагеле (10% EtOAc в CH2Cl2). Выход: 6% промежуточного соединения 35 (E+Z) (из промежуточного соединения 33) (CI-MC: 530 [M+H]+).
Пример 14
а) Получение промежуточного соединения 36
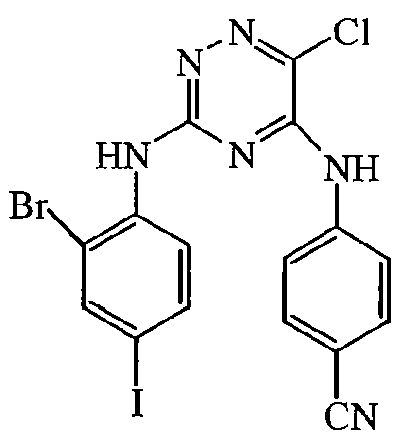
В двугорлой колбе, защищенной алюминиевой фольгой и снабженной холодильником, растворяют промежуточное соединение 33 (1 г, 2,23 ммоль) в уксусной кислоте. Добавляют N-бромсукцинимид (0,601 г, 3,345 ммоль). Смесь дегазируют и нагревают при 110°С в течение 15 минут. После упаривания остаток растворяют в этилацетате. Раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Выход: промежуточное соединение 36, которое используют на следующей стадии.
b) Получение промежуточного соединения 37
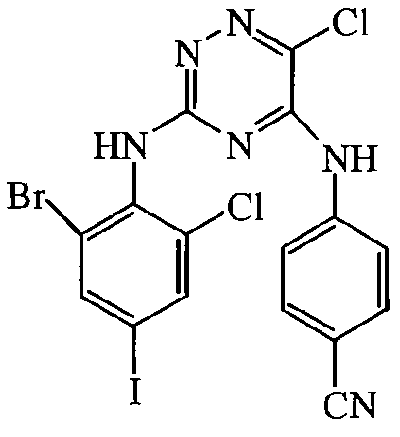
Промежуточное соединение 36, полученное на стадии а), растворяют в уксусной кислоте в двугорлой колбе, защищенной алюминиевой фольгой и снабженной холодильником, как описано выше. Добавляют N-хлорсукцинимид (0,447 г, 3,345 ммоль). Смесь дегазируют и нагревают при 110°С в течение 15 минут. После упаривания остаток растворяют в этилацетате. Раствор последовательно промывают водным раствором Na2CO3 и водой, затем сушат над MgSO4 и упаривают. Выход: промежуточное соединение 37, которое используют на следующей стадии.
с) Получение промежуточного соединения 38
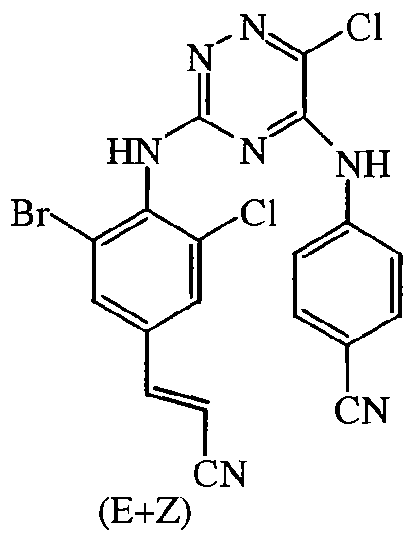
Промежуточное соединение 37, полученное на стадии b), растворяют в ДМФА и добавляют акрилонитрил (0,12 мл, 1,856 ммоль), триэтиламин (0,26 мл, 1,856 ммоль), ацетат палладия (0,0111 г, 0,023 ммоль) и трифенилфосфин (0,0123 г, 0,046 ммоль). После дегазирования реакционную смесь продувают азотом и колбу закрывают перегородкой. Затем реакционную смесь перемешивают в течение ночи при 100°С. После охлаждения реакционную смесь разбавляют дихлорметаном. Раствор в CH2Cl2 промывают водой (3 раза) и сушат над MgSO4, затем упаривают. Остаток после упаривания очищают колоночной хроматографией на силикагеле (10% EtOAc в CH2Cl2). Выход: 9% промежуточного соединения 38 (E/Z) (из промежуточного соединения 33) (CI-MC: 486 [M+H]+).
В. Получение конечных соединений
Пример В1
а) Получение соединения 1
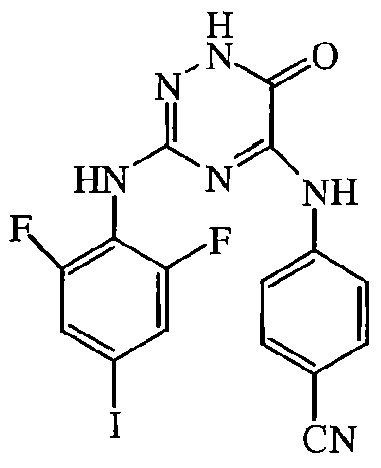
Промежуточное соединение 22 (1 эквив.) растворяют в уксусной кислоте. Добавляют йодид натрия (3 эквив.). Смесь нагревают при 100-120°С в течение 6-48 часов. После упаривания остаток очищают колоночной хроматографией с использованием в качестве элюента 20% EtOAc в CH2Cl2. Выход: 18% соединения 1 (т.пл. 287-290°С).
b-1) Получение соединения 2
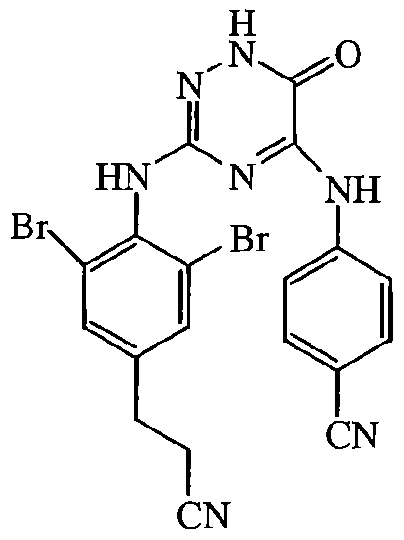
Промежуточное соединение 30 (1 эквив.) растворяют в 95% водной уксусной кислоте. Смесь нагревают при 120-150°С в течение 6-48 часов. После упаривания остаток обрабатывают Et3N в CH2Cl2 и затем полученную смесь упаривают. Остаток очищают колоночной хроматографией на силикагеле (7% МеОН в CH2Cl2. Выход: 31% соединения 2 (CI-MC: 514 [M+H]+; т.пл. 339-340°С).
b-2) Получение соединения 3
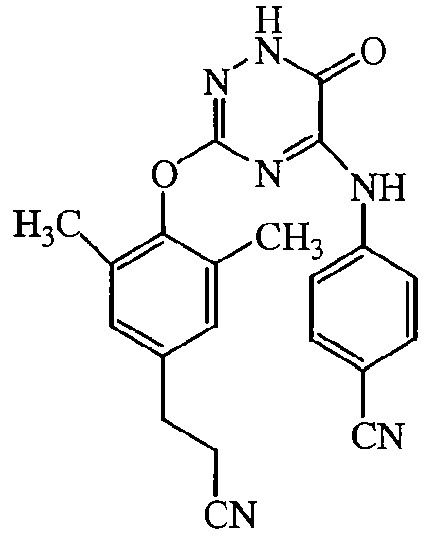
Промежуточное соединение 27 нагревают в течение 3 часов при 150°С в 80% водной уксусной кислоте. После упаривания остаток обрабатывают Et3N в CH2Cl2 и смесь упаривают. Остаток обрабатывают CH2Cl2 и выпавшее в осадок вещество собирают фильтрованием. Фильтрат промывают CH2Cl2 и небольшим объемом 7% МеОН в CH2Cl2. Дополнительное количество соединения получают упариванием супернатанта с последующей колоночной хроматографией полученного остатка на колонке с силикагелем (20% EtOAc в CH2Cl2). Выход: 55% соединения 3 (т.пл. 351-352°С).
b-3) Получение соединения 71
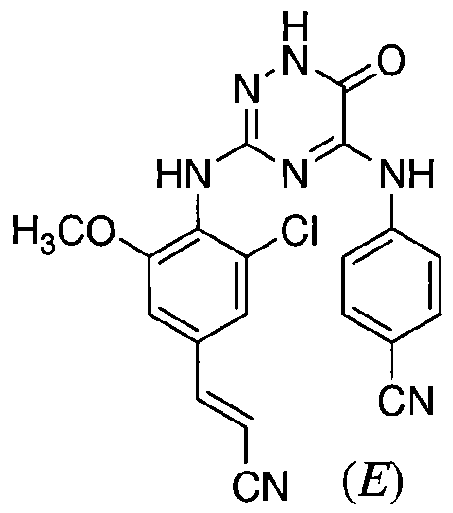
Промежуточное соединение 54 (0,140 г) растворяют в 80% водной уксусной кислоте. Смесь нагревают в течение ночи при 150°С. После упаривания остаток обрабатывают Et3N в CH2Cl2 и смесь упаривают. Остаток очищают колоночной хроматографией (20% EtOAc в CH2Cl2). Выход: 0,037 г соединения 71 (CI-MC: 420 [M+H]+).
Пример В2
Получение соединения 5
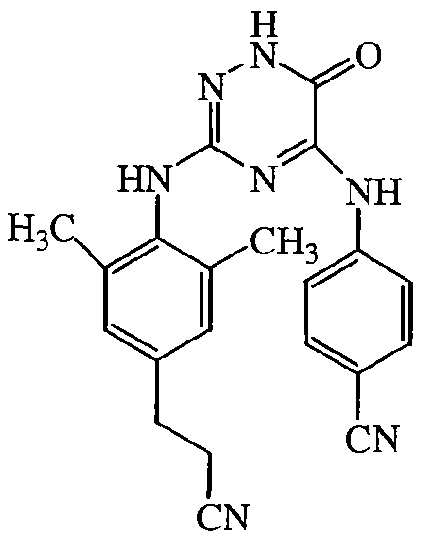
Соединение 4 (полученное согласно пр. В1b-1)) 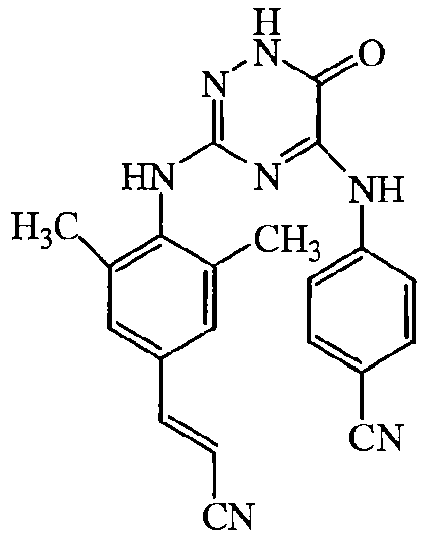 (0,042 г, 0,11 ммоль) растворяют в EtOH. Добавляют 10% Pd/C, и смесь гидрируют в течение 24 часов при комнатной температуре, после чего ее фильтруют через целит. После упаривания растворителя остаток очищают на колонке с силикагелем (7% МеОН в CH2Cl2). Выход: 43% соединения 5 (т.пл. 336-337°С).
(0,042 г, 0,11 ммоль) растворяют в EtOH. Добавляют 10% Pd/C, и смесь гидрируют в течение 24 часов при комнатной температуре, после чего ее фильтруют через целит. После упаривания растворителя остаток очищают на колонке с силикагелем (7% МеОН в CH2Cl2). Выход: 43% соединения 5 (т.пл. 336-337°С).
Пример В3
Получение соединения 7
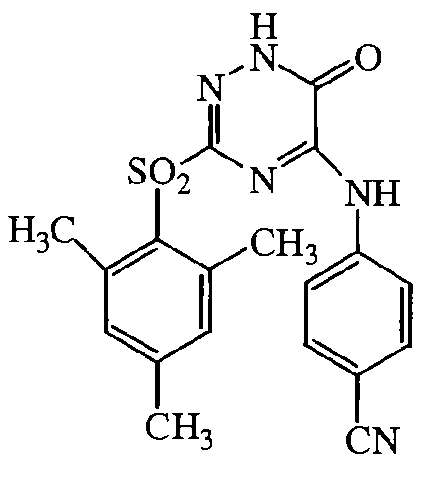
Соединение 6 (полученное согласно пр. В1b-1)) 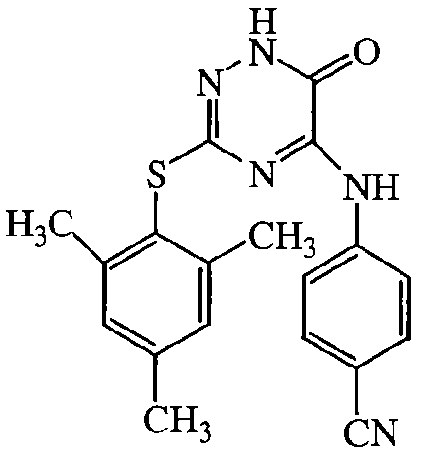 (0,080 г, 0,22 ммоль) растворяют в растворе 30% пероксида водорода в уксусной кислоте (5 мл). Смесь нагревают при 100°С в течение 3 часов и упаривают. Остаток очищают колоночной хроматографией (20% EtOAc в CH2Cl2). Выход: 0,042 г (48%) соединения 7 (т.пл. 303-304°С).
(0,080 г, 0,22 ммоль) растворяют в растворе 30% пероксида водорода в уксусной кислоте (5 мл). Смесь нагревают при 100°С в течение 3 часов и упаривают. Остаток очищают колоночной хроматографией (20% EtOAc в CH2Cl2). Выход: 0,042 г (48%) соединения 7 (т.пл. 303-304°С).
Пример В4
а) Получение соединения 8
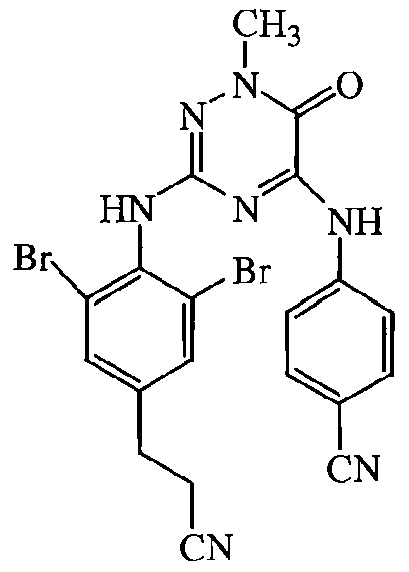
Соединение 2 (1 эквив.) растворяют в сухом ТГФ. Смесь охлаждают на ледяной бане. Добавляют гидрид натрия (1 эквив.) и смесь перемешивают в течение 5 минут, затем добавляют избыток метилйодида (приблизительно 3 эквив.). Охлаждающую баню удаляют и реакционной смеси дают реагировать в течение 6-24 часов. По завершении реакции ТГФ выпаривают. Остаток растворяют в CH2Cl2, и полученный раствор промывают водой, сушат над MgSO4 и упаривают. Полученный остаток очищают колоночной хроматографией с использованием в качестве элюента 10% EtOAc в дихлорметане. Выход: 19% соединения 8 (CI-MC: 528 [M+H]+).
b) Получение соединения 9
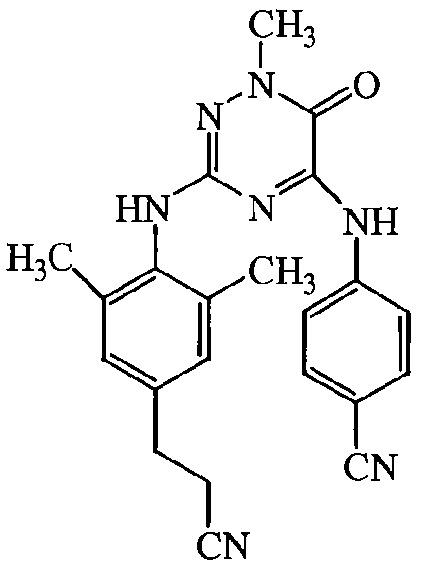
Соединение 5 растворяют в сухом ТГФ. Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (1,1 эквив.). Смесь перемешивают в течение 5 минут, затем добавляют метилйодид (3 эквив.). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают на колонке с силикагелем, используя раствор 10% EtOAc в CH2Cl2. Выход: соединение 9 (т.пл. 317-320°С).
с) Получение соединения 78
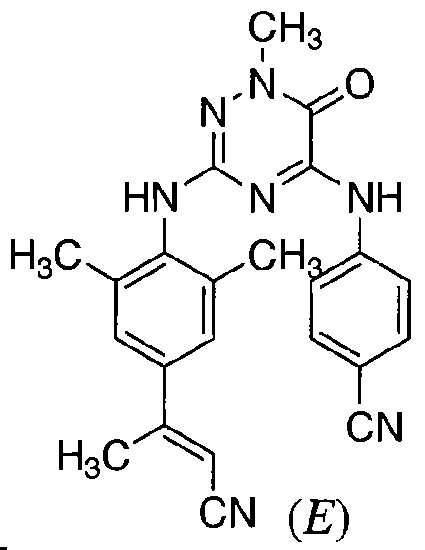
Соединение 77 (0,040 г, 0,100 ммоль) растворяют в сухом ТГФ (3 мл). Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (60% дисперсия в минеральном масле, 0,004 г, 0,111 ммоль). Смесь перемешивают в течение 5 минут, затем добавляют избыток метилйодида (0,5 мл). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают препаративной тонкослойной хроматографией на диоксиде кремния (10% EtOAc в CH2Cl2). Выход: 0,015 г соединения 78 (CI-MC: 412 [M+H]+).
Пример В5
Получение соединения 11
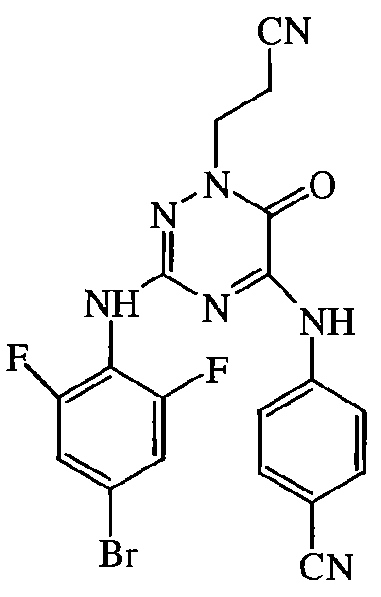
К раствору в ДМФА (3 мл) 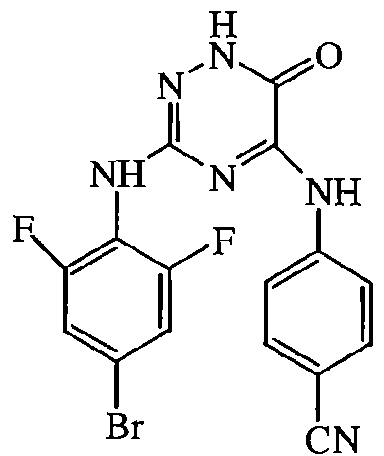 (соединение 10; получено согласно примеру В1а)) (0,111 г, 0,265 ммоль) добавляют акрилонитрил (0,05 мл), триэтиламин (0,04 мл, 0,291 ммоль), ацетат палладия (0,0128 г, 0,0026 ммоль) и три-о-толилфосфин (0,0164 г, 0,0052 ммоль). После дегазирования реакционную смесь продувают азотом и колбу закрывают перегородкой. Затем реакционную смесь перемешивают в течение 4 суток при 120°С. После охлаждения реакционную смесь разбавляют дихлорметаном. Раствор в CH2Cl2 промывают водой (3 раза) и сушат над MgSO4, затем упаривают. Остаток после упаривания очищают колоночной хроматографией на силикагеле (10% EtOAc в CH2Cl2). Выход: 0,067 г (53%) соединения 11 (т.пл. 246-247°С).
(соединение 10; получено согласно примеру В1а)) (0,111 г, 0,265 ммоль) добавляют акрилонитрил (0,05 мл), триэтиламин (0,04 мл, 0,291 ммоль), ацетат палладия (0,0128 г, 0,0026 ммоль) и три-о-толилфосфин (0,0164 г, 0,0052 ммоль). После дегазирования реакционную смесь продувают азотом и колбу закрывают перегородкой. Затем реакционную смесь перемешивают в течение 4 суток при 120°С. После охлаждения реакционную смесь разбавляют дихлорметаном. Раствор в CH2Cl2 промывают водой (3 раза) и сушат над MgSO4, затем упаривают. Остаток после упаривания очищают колоночной хроматографией на силикагеле (10% EtOAc в CH2Cl2). Выход: 0,067 г (53%) соединения 11 (т.пл. 246-247°С).
Пример В6
а-1) Получение соединения 12
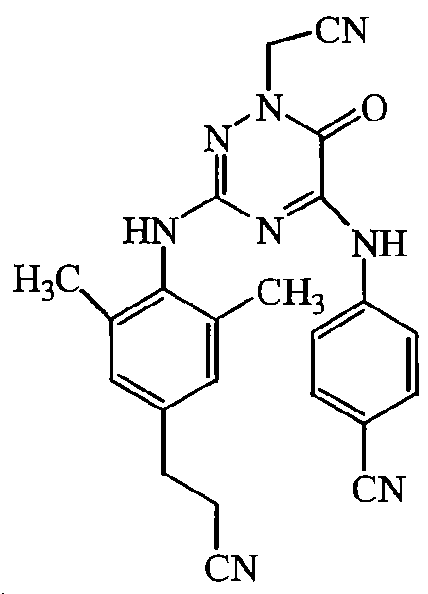
Соединение 5 растворяют в сухом ТГФ. Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (1,1 эквив.). Смесь перемешивают в течение 5 минут, затем добавляют Br-CH2-CN (3 эквив.). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают на колонке с силикагелем, используя в качестве элюента раствор 10% EtOAc в CH2Cl2. Выход: соединение 12 (т.пл. 243-246°С).
а-2) Получение соединения 75
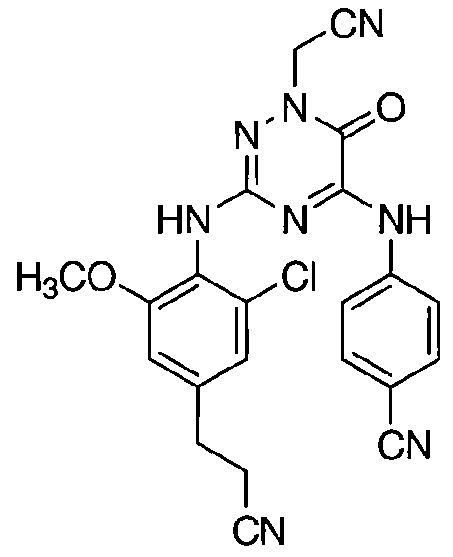
Соединение 63 (0,050 г, 0,118 ммоль) растворяют в сухом ТГФ (3 мл). Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (60% дисперсия в минеральном масле, 0,006 г, 0,131 ммоль). Смесь перемешивают в течение 5 минут, затем добавляют избыток Br-CH2-CN (0,5 мл). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают препаративной тонкослойной хроматографией на диоксиде кремния (10% EtOAc в CH2Cl2). Выход: 0,030 г соединения 75 (CI-MC: 461 [M+H]+). Соответственно получают соединение 60.
Соединение 57 получают соответственно, исходя из соединения 45. Полученный остаток очищают препаративной тонкослойной хроматографией на диоксиде кремния (50% EtOAc в гептане). Выход: 0,026 г соединения 57 (т.пл. 276-277°С). Такую методику также используют для получения соединения 55 (выход: 0,027 г; (CI-MC: 426 [M+H]+).
b-1) Получение соединения 13

Соединение 5 растворяют в сухом ТГФ. Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (1,1 эквив.). Смесь перемешивают в течение 5 минут, затем добавляют I-CH2-C(=О)NН2 (3 эквив.). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают на колонке с силикагелем, используя в качестве элюента раствор 80% EtOAc в CH2Cl2. Выход: соединение 13 (т.пл. 289-291°С).
b-2) Получение соединения 76
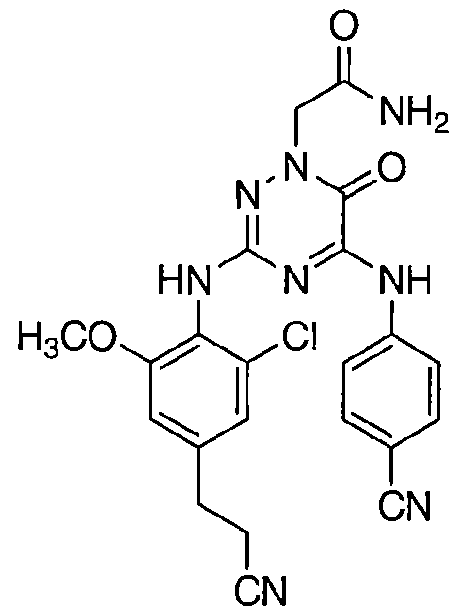
Соединение 63 (0,050 г, 0,118 ммоль) растворяют в сухом ТГФ (3 мл). Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (60% дисперсия в минеральном масле, 0,006 г, 0,131 ммоль). Смесь перемешивают в течение 5 минут, затем добавляют I-CH2-C(=О)NН2 (0,044 г, 0,237 ммоль). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток обрабатывают 7% МеОН в CH2Cl2. Выпавшее в осадок вещество собирают фильтрованием и последовательно промывают Н2О и 7% МеОН в CH2Cl2. Выход: 0,013 г соединения 76 (CI-MC: 479 [M+H]+).
с-1) Получение соединения 14
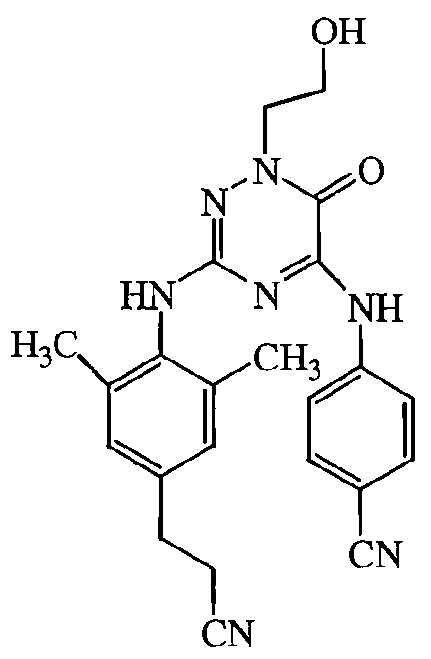
Соединение 5 растворяют в сухом ТГФ. Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (6 эквив.). Смесь перемешивают в течение 5 минут, затем добавляют избыток йодэтанола. Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают на колонке с силикагелем, используя в качестве элюента раствор 60% EtOAc в CH2Cl2. Выход: соединение 14 (CI-MC: 430 [M+H]+).
с-2) Получение соединения 74
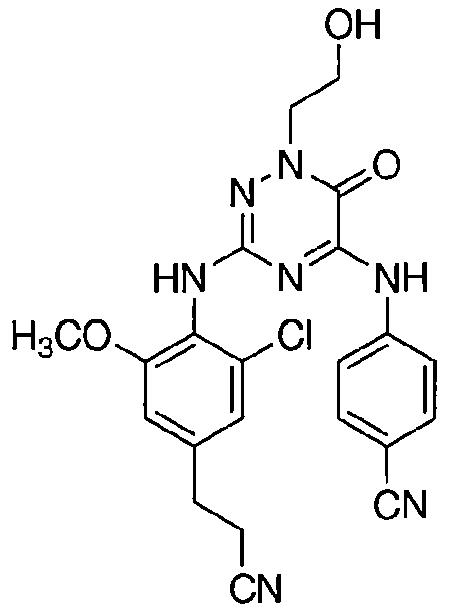
Соединение 63 (0,050 г, 0,118 ммоль) растворяют в сухом ТГФ (3 мл). Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (60% дисперсия в минеральном масле, 0,006 г, 0,131 ммоль). Смесь перемешивают в течение 5 минут, затем добавляют избыток 2-йодэтанола (0,5 мл) и еще некоторое количество гидрида натрия (0,030 г, 0,655 ммоль). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают препаративной тонкослойной хроматографией на диоксиде кремния (60% EtOAc в CH2Cl2). Выход: 0,029 г соединения 74 (CI-MC: 466 [M+H]+).
Соответственно получают соединение 70, исходя из соединения 3. Полученный остаток очищают препаративной тонкослойной хроматографией на диоксиде кремния (45% EtOAc в CH2Cl2). Выход: 0,012 г соединения 70 (CI-MC: 431 [M+H]+). Данную методику также используют для получения соединения 61 (выход: 0,012 г; CI-MC: 429 [M+H]+).
d-1) Получение соединения 15
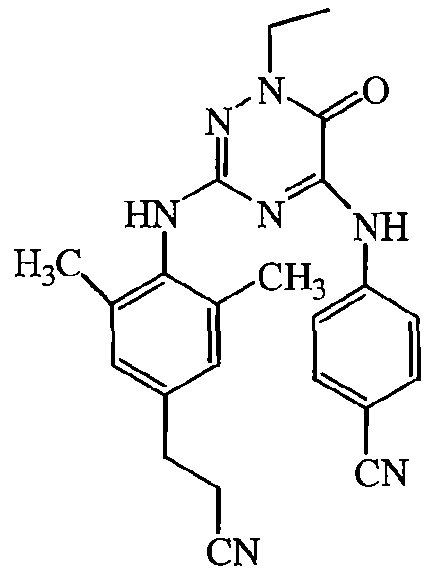
Соединение 5 растворяют в сухом ТГФ. Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (1,1 эквив.). Смесь перемешивают в течение 5 минут, затем добавляют I-CH2-CH3 (3 эквив.). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают на колонке с силикагелем, используя в качестве элюента раствор 10% EtOAc в CH2Cl2. Выход: соединение 15 (т.пл. 243-245°С).
d-2) Получение соединения 73
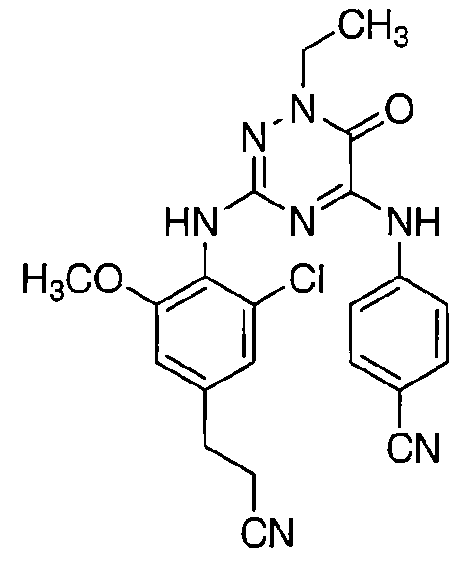
Соединение 63 (0,050 г, 0,118 ммоль) растворяют в сухом ТГФ (3 мл). Раствор охлаждают на ледяной бане. Добавляют гидрид натрия (60% дисперсия в минеральном масле, 0,006 г, 0,131 ммоль). Смесь перемешивают в течение 5 минут, затем добавляют избыток этилйодида (0,5 мл). Ледяную баню удаляют и после перемешивания в течение 5 часов смесь упаривают. Остаток очищают препаративной тонкослойной хроматографией на диоксиде кремния (10% EtOAc в CH2Cl2). Выход: 0,013 г соединения 73 (CI-MC: 450 [M+H]+).
В таблице 1 приводится перечень соединений (Соед. №), которые получают согласно одному из вышеприведенных примеров (Пр.). Соединения характеризуются температурами плавления (т.пл.) или протонированной массой ([M+H]+).
Таблица 1
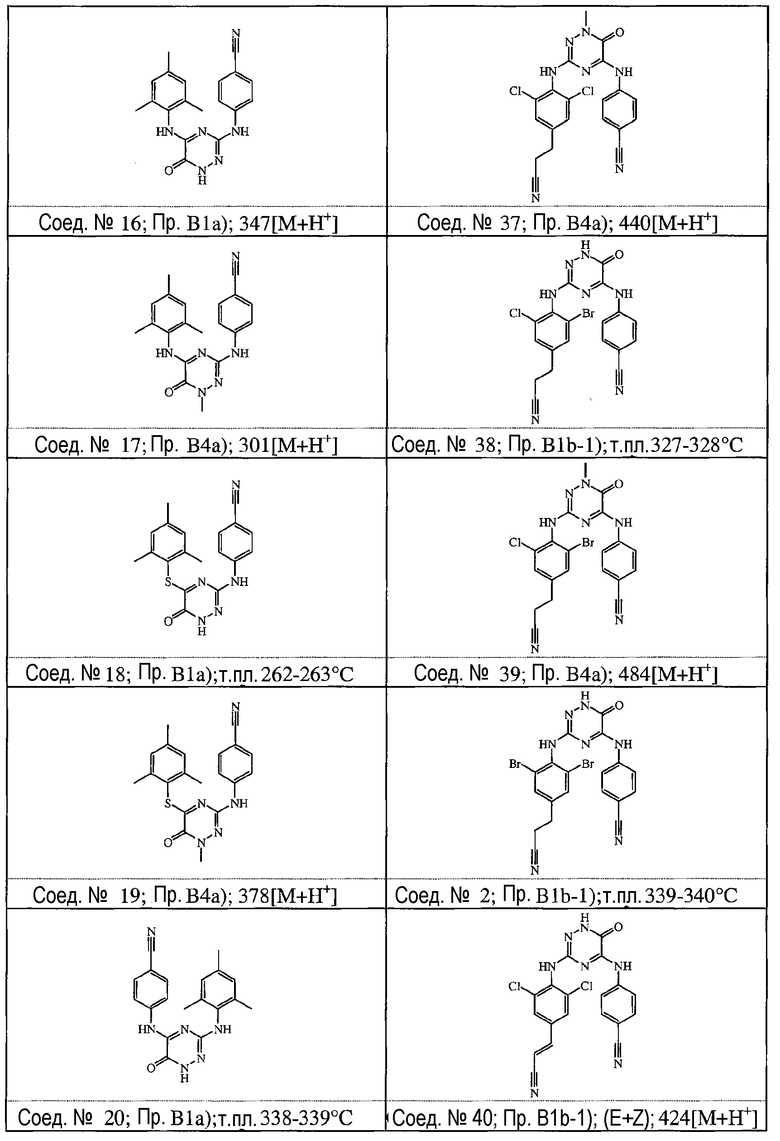
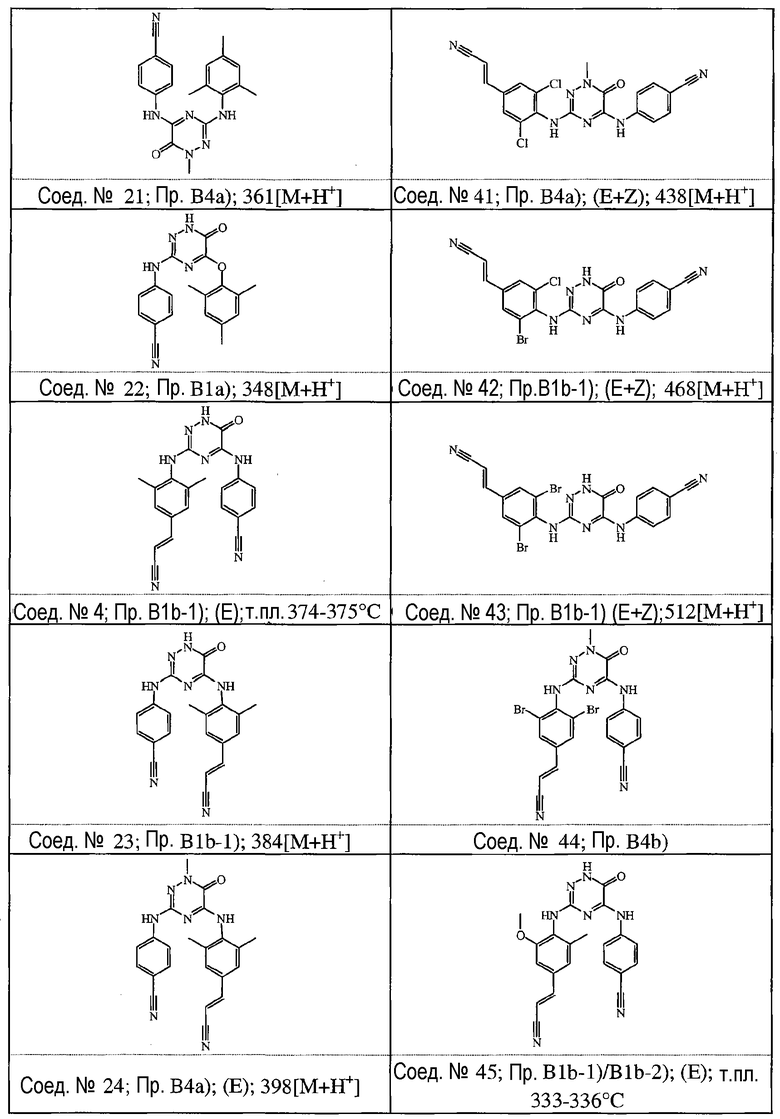
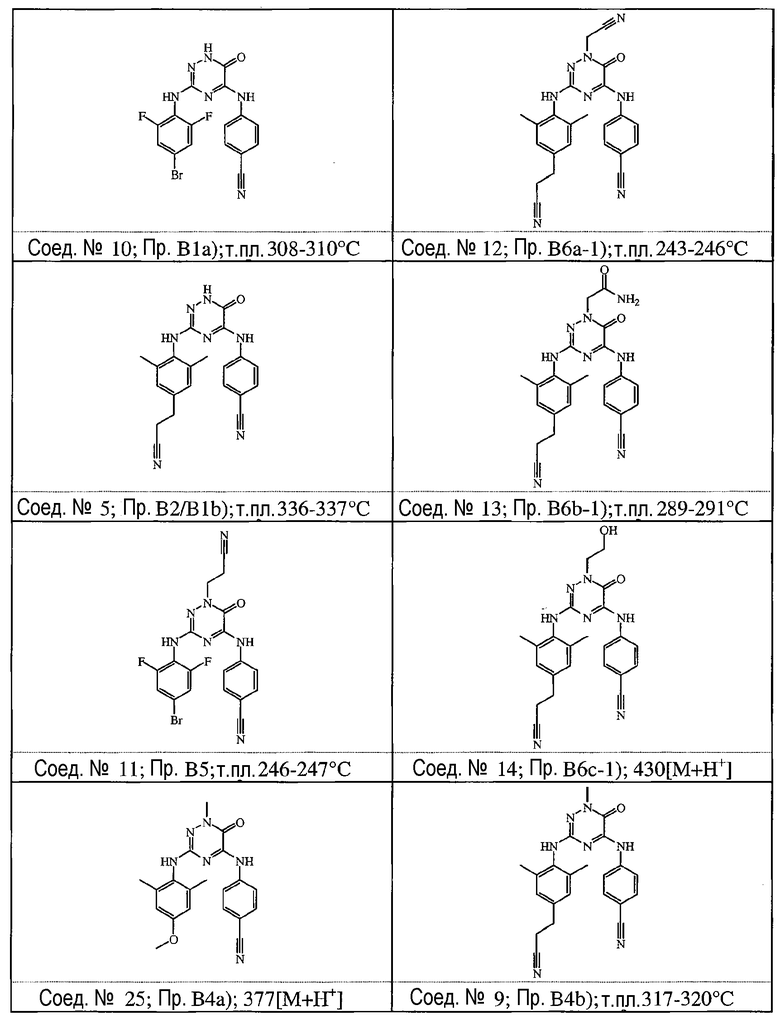
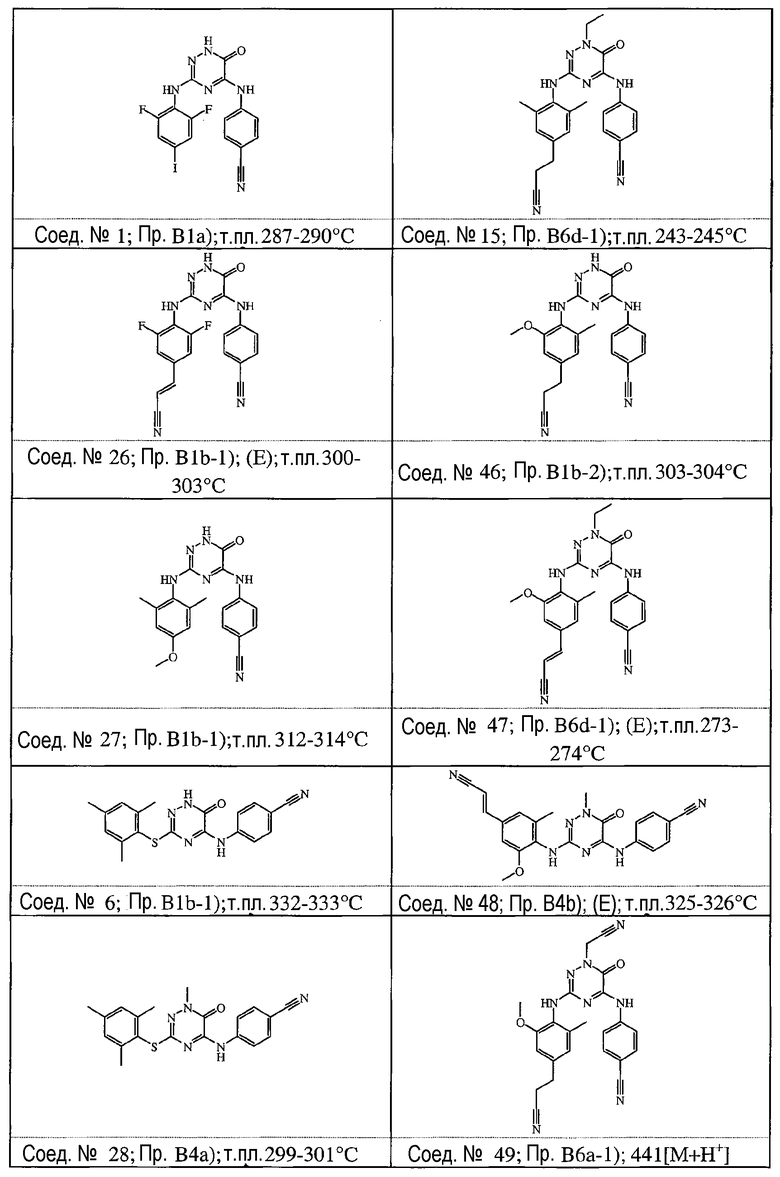
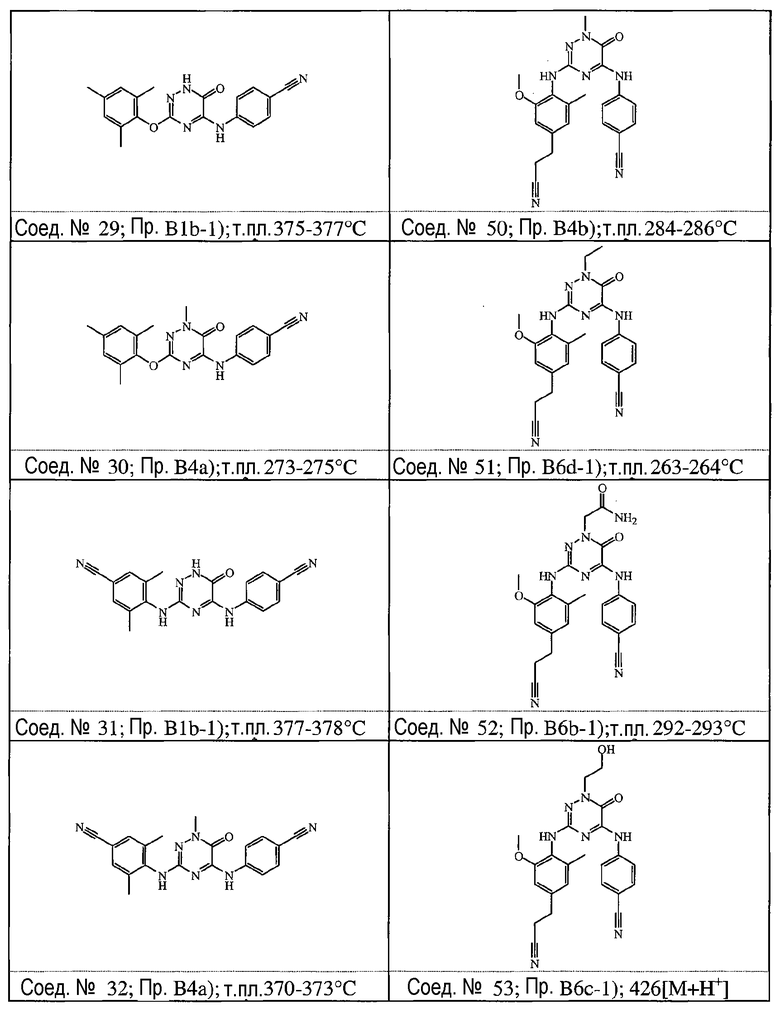
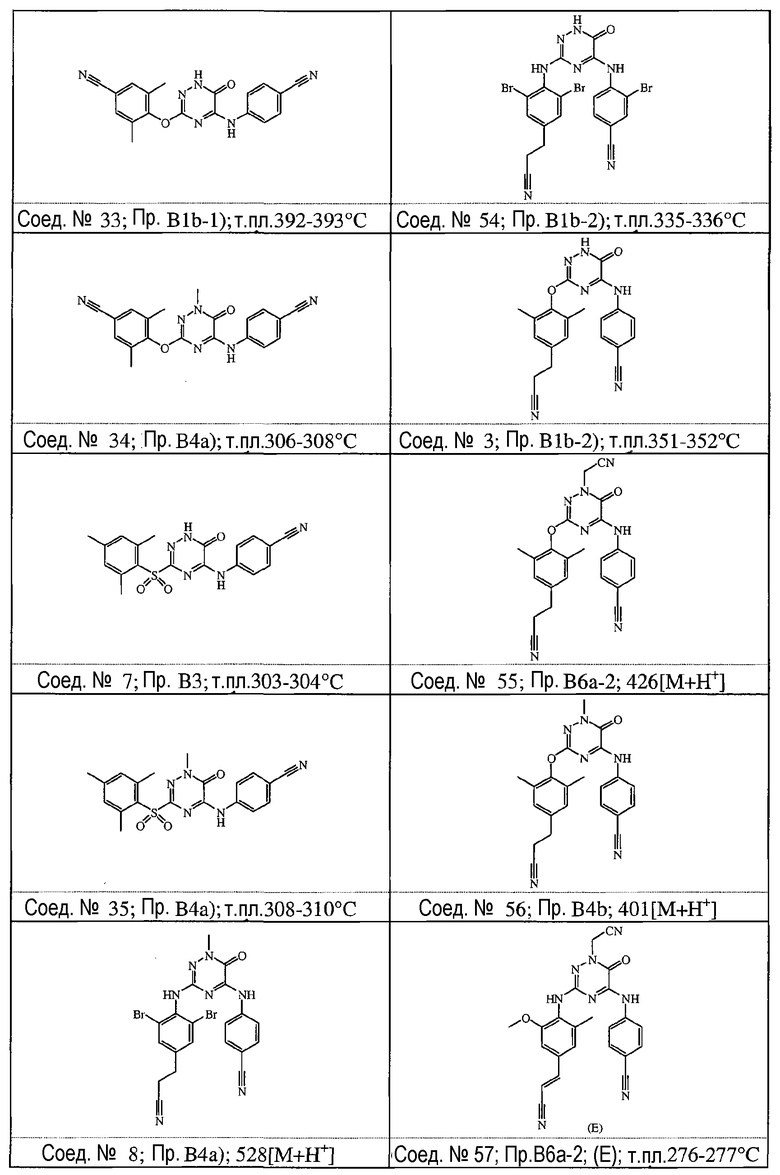
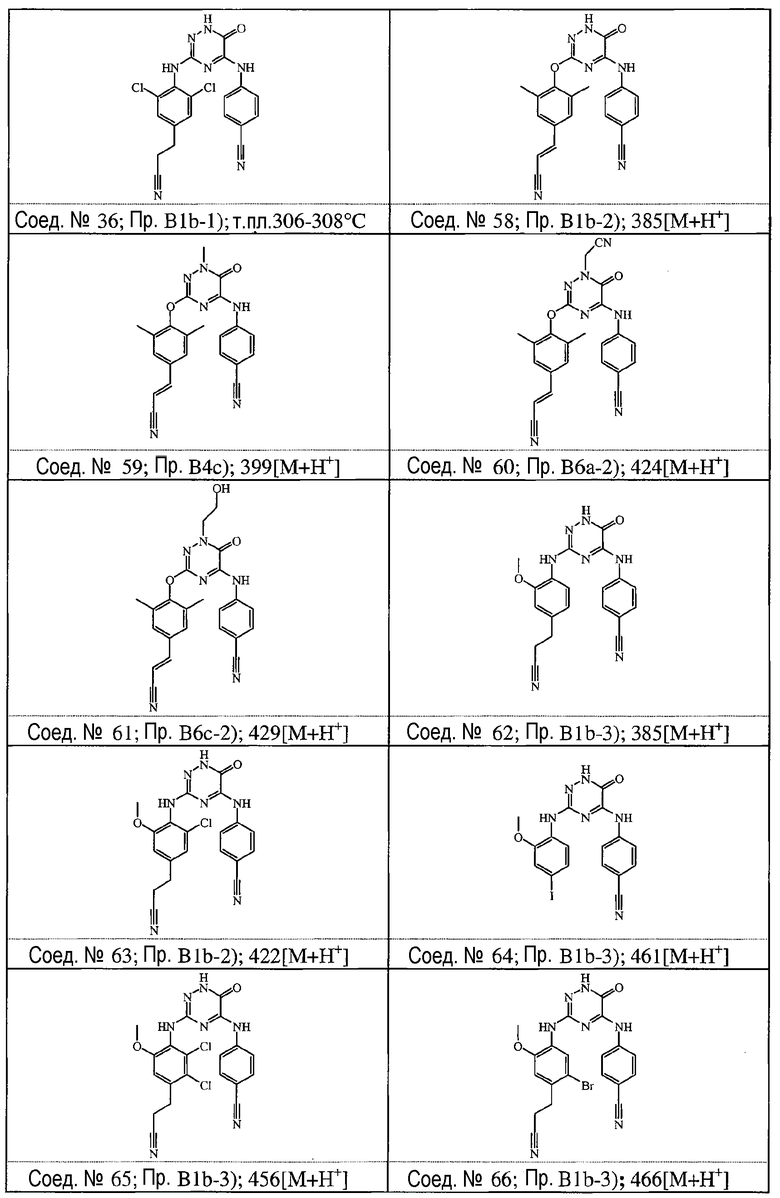
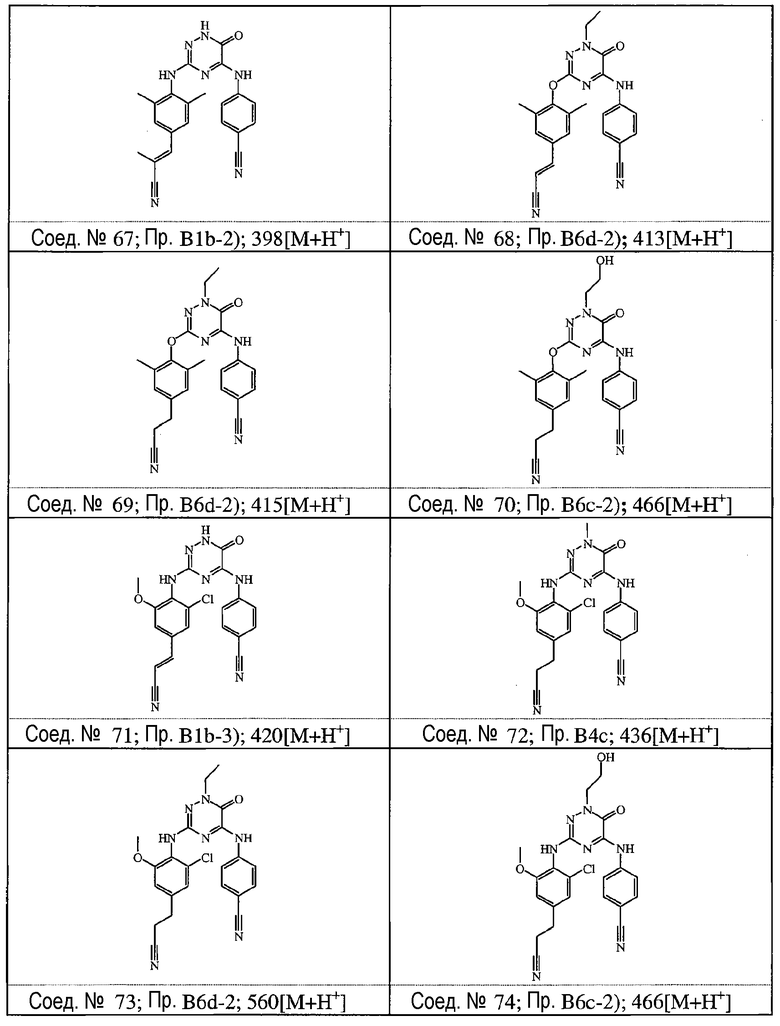
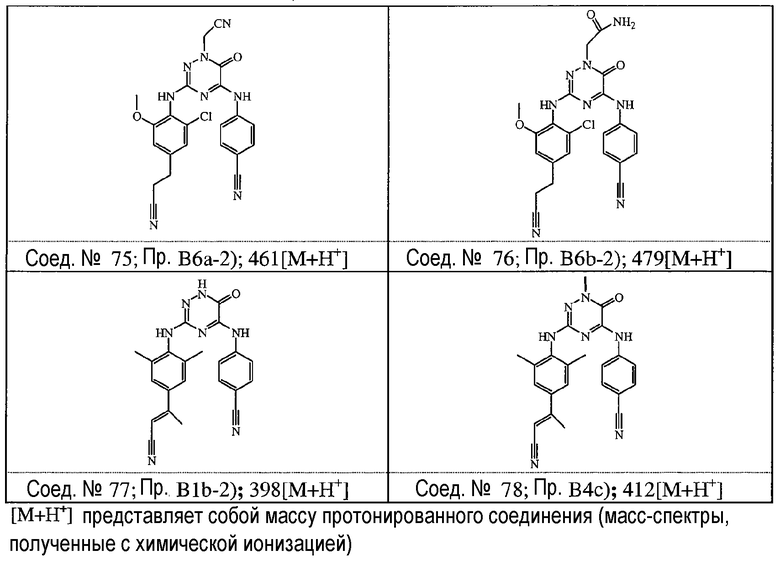
С. Фармакологический пример
Фармакологическую активность соединений настоящего изобретения проверяют с использованием теста, описанного далее.
Используют быструю, чувствительную и автоматизированную методику анализа для оценки in vitro агентов против ВИЧ. Трансформированная ВИЧ-1 линия клеток Т4, МТ4, которая, как показано ранее (Koyanagi et al., Int. J. Cancer, 36, 445-451, 1985), обладает высокой чувствительностью и восприимчивостью в отношении ВИЧ-инфекции, служит в качестве клеточной линии-мишени. В таких клетках, созданных с GFP (и ВИЧ-специфическим промотором), имеющуюся ВИЧ-инфекцию определяют флуорометрически. Цитотоксичность измеряют в таких же клетках, но созданных с GFP при соответствующем промоторе. Инфекцию (или ее ингибирование) ВИЧ-инифицированных клеток и флуоресценцию псевдоинфицированных клеток оценивают по сигналу флуоресценции GFP, генерированному обеими вышеуказанными клеточными линиями.
Эффективную 50% концентрацию (ЕС50 в мкМ) определяют как концентрацию соединения, которая снижает интенсивность флуоресценции ВИЧ-инфицированных клеток на 50%. Цитотоксическую 50% концентрацию (СС50 в мкМ) определяют как концентрацию соединения, которая снижает интенсивность флуоресценции псевдоинфицированных клеток на 50%.
Показано, что соединения формулы (I) эффективно ингибируют ВИЧ-1. Конкретные величины рЕС50 (-logЕС50) приводятся в таблице 2. Например, соединение с величиной ЕС50 10-9М имеет рЕС50=9.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВИЧ-ИНГИБИРУЮЩИЕ 5-КАРБО- ИЛИ ГЕТЕРОЦИКЛИЧЕСКИЕ ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ | 2005 |
|
RU2403244C2 |
| БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ПИРИМИДИНА, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2403254C2 |
| 5-ГЕТЕРОЦИКЛИЛПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2405778C2 |
| ПРОИЗВОДНЫЕ 5- ИЛИ 6-ЗАМЕЩЕННЫХ БЕНЗИМИДАЗОЛОВ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ РЕСПИРАТОРНОГО СИНЦИТИАЛЬНОГО ВИРУСА | 2004 |
|
RU2369606C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА/ПИПЕРАЗИНА | 2008 |
|
RU2470017C2 |
| 6,7,8,9-ЗАМЕЩЕННЫЕ 1-ФЕНИЛ-1,5-ДИГИДРОПИРИДО (3,2-b) ИНДОЛ-2-ОНЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ АНТИИНФЕКЦИОННЫХ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2005 |
|
RU2377243C2 |
| ПРОИЗВОДНЫЕ (1,10b-ДИГИДРО-2-(АМИНОАЛКИЛФЕНИЛ)-5Н-ПИРАЗОЛО[1,5-c][1,3]БЕНЗОКСАЗИН-5-ИЛ)ФЕНИЛМЕТАНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ ВИРУСНОЙ РЕПЛИКАЦИИ ВИЧ | 2006 |
|
RU2416615C2 |
| 2-ЗАМЕЩЕННЫЕ БЕНЗИМИДАЗОЛЫ | 2006 |
|
RU2441866C2 |
| 5-АМИДО-ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2007 |
|
RU2480464C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА/ПИПЕРАЗИНА | 2008 |
|
RU2478628C2 |
Описываются новые производные 1,2,4-триазин-6-она общей формулы (I)
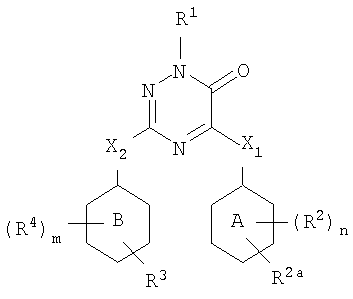
или их фармацевтически приемлемые кислотно-аддитивные соли, или стереохимически изомерные формы, где кольца А и В означают фенил; значения остальных радикалов приведены в формуле изобретения; способ их получения, фармацевтическая композиция на их основе, способ получения композиции и применение новых соединений для лечения или предупреждения ВИЧ-инфекции. 5 н. и 17 з.п. ф-лы, 2 табл.
1. Производное 1,2,4-триазин-6-она формулы
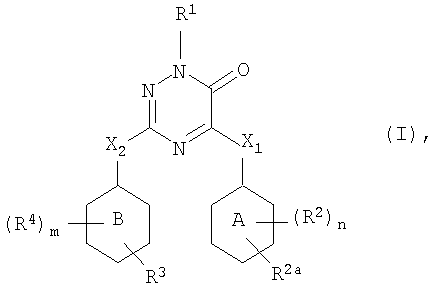
его фармацевтически приемлемая кислотно-аддитивная соль или стереохимически изомерная форма, где кольцо А и В представляют фенил;
n равно 1 или 2;
m равно 1, 2 или 3;
R1 представляет водород или С1-6алкил, необязательно замещенный
R5;
каждый R2 независимо представляет водород, галоген или С1-6алкил;
R2a представляет циано, С1-6алкил или С2-6алкенил, замещенный циано;
X1 представляет -NH-, -О- или -S-;
Х2 представляет -NH-, -O-, -S- или -S(=O)p-;
p равно 1 или 2;
R представляет циано; галоген; C1-6алкил, необязательно замещенный циано; C1-6алкилокси; или С2-6алкенил, замещенный циано;
каждый R4 независимо представляет водород, галоген, С1-6алкил или C1-6алкилокси;
R5 представляет циано, аминокарбонил или гидрокси.
2. Соединение по п.1, имеющее формулу
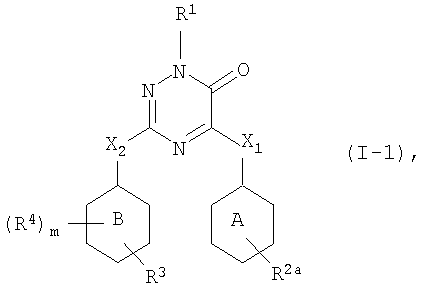
где R1, R2a, R3, R4, m, X1, Х2, кольцо А и кольцо В имеют значения, указанные в п.1.
3. Соединение по п.2, имеющее формулу

где R1, R2a, R3, R4, m, X1, Х2, кольцо А и кольцо В имеют значения, указанные в п.1.
4. Соединение по п.3, имеющее формулу
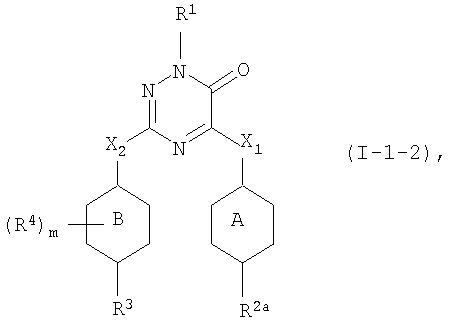
где R1, R2а, R3, R4, m, X1, X2, кольцо А и кольцо В имеют значения, указанные в п.1.
5. Соединение по п.4, имеющее формулу
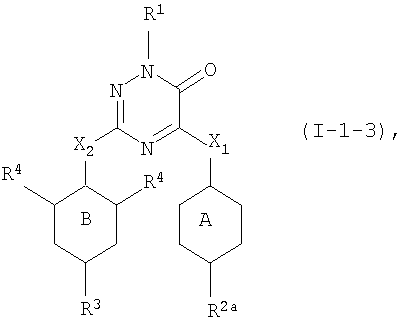
где R1, R2a R3, R4, X1, Х2, кольцо А и кольцо В имеют значения, указанные в п.1, при условии, что R4 является иным, чем водород.
6. Соединение по п.1, имеющее формулу
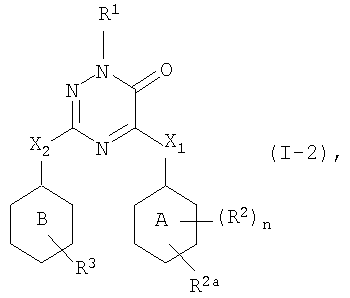
где R1, R2a, R2, R3, X1, Х2, n, кольцо А и кольцо В имеют значения, указанные в п.1.
7. Соединение по п.6, имеющее формулу
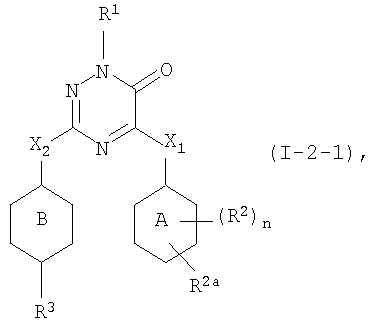
где R1, R2а, R2, R3, X1, Х2, n, кольцо А и кольцо В имеют значения, указанные в п.1.
8. Соединение по п.7, имеющее формулу
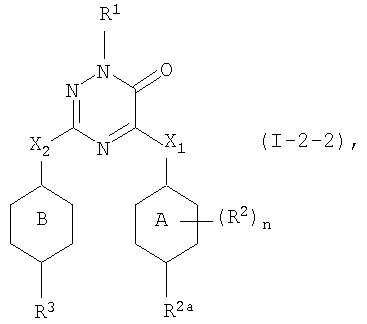
где R1, R2a R2, R3, X1, X2, n, кольцо А и кольцо В имеют значения, указанные в п.1.
9. Соединение по п.8, имеющее формулу
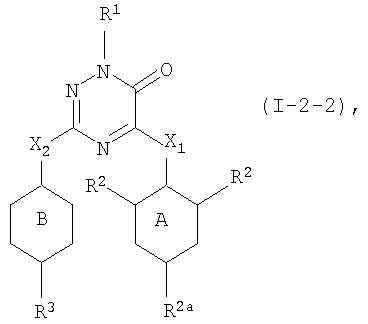
где R1, R2a, R2, R3, X1, X2, кольцо А и кольцо В имеют значения, указанные в п.1, при условии, что R2 является иным, чем водород.
10. Соединение по п.1, где m равно 1 или 2;
R4 представляет галоген; С1-6алкил; С1-6алкилокси.
11. Соединение по п.10, где R3 представляет циано; C1-6алкил, замещенный циано; или С2-6алкенил, замещенный циано.
12. Соединение по п.1, где
R2 представляет галоген; С1-6алкил.
13. Соединение по п.12, где R2a представляет циано или С2-6алкенил, замещенный циано.
14. Соединение по п.1, где R2a представляет собой циано или С2-6алкенил, замещенный циано.
15. Соединение по п.1, где R3 представляет собой циано, С1-6алкил, замещенный циано, или С2-6алкенил, замещенный циано.
16. Соединение по п.1, где
Х2 представляет -NH-; -O-; -S- или -S(=O)p-;
p равно 2.
17. Соединение по п.1 для применения в качестве лекарственного средства.
18. Применение соединения по любому из пп.1-16 для получения лекарственного средства для лечения или предупреждения ВИЧ-инфекции.
19. Применение соединения по п.18 для получения лекарственного средства для лечения или предупреждения ВИЧ-инфекции, резистентной к лекарственному средству или нескольким лекарственным средствам.
20. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении репликации ВИЧ, содержащая фармацевтически приемлемый носитель и в качестве активного ингредиента терапевтически эффективное количество соединения по любому из пп.1-16.
21. Способ получения фармацевтической композиции по п.20, отличающийся тем, что терапевтически эффективное количество соединения по любому из пп.1-16 тщательно смешивают с фармацевтически приемлемым носителем.
22. Способ получения соединения общей формулы (I) по п.1,
где R1 означает водород,
a R2, R2а, R3, R4, m, n, X1, Х2, кольцо А и кольцо В имеют значения, указанные в п.1, заключающийся в том, что соединение общей формулы (II)
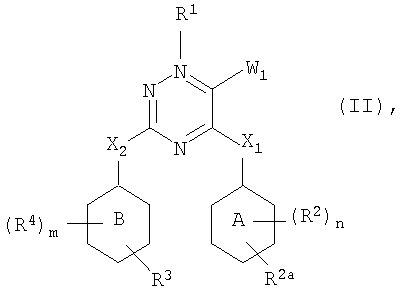
где R2, R2a, R3, R4, m, n, X1, Х2, кольцо А и кольцо В имеют значения, указанные в п.1, и W1 представляет подходящую уходящую группу;
подвергают взаимодействию с подходящей кислотой,
и, при необходимости, преобразуют соединение формулы (I) в терапевтически активную нетоксичную кислотно-аддитивную соль обработкой кислотой, или, наоборот, преобразуют кислотно-аддитивную соль в свободное основание обработкой щелочью; и, при необходимости, получают их стереохимически изомерные формы.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| 3,5-ДИЗАМЕЩЕННЫЕ 1,2,4-ТРИАЗИНОНЫ-6, ОБЛАДАЮЩИЕ РОСТРЕГУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1999 |
|
RU2156242C1 |
| ПРОИЗВОДНЫЕ 1,2,4-ТРИАЗИНДИОНОВ, ОБЛАДАЮЩИЕ ГЕРБИЦИДНОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2241704C1 |
Авторы
Даты
2010-10-20—Публикация
2005-08-10—Подача