Область техники, к которой относится изобретение
Изобретение относится к 6,7-ненасыщенным 7-карбамоилзамещенным производным морфинана, которые являются полезными в качестве агентов для лечения и/или профилактики тошноты, рвоты и/или констипации, особенно в качестве агента для ослабления и/или профилактики побочного действия (тошноты, рвоты и/или констипации и т.д.), вызванного соединением, имеющим агонистическую активность для опиоидного рецептора (например, опиоидного µ-рецептора).
Уровень техники
Агонист опиоидного рецептора, такой как морфин и тому подобное, который применяют в качестве аналгетика, является очень эффективным для пациента, имеющего раковую боль, но в качестве побочного действия вызывает тошноту, рвоту, констипацию, энурез и зуд. Клинически применяют различные противорвотные агенты и агенты против констипации, но нельзя сказать, что любой из них проявляет достаточное действие, и существует потребность в превосходном агенте, ослабляющем побочное действие для улучшения QOL пациента.
В патентных литературных ссылках 1 и 2 и непатентной литературной ссылке 1 описано, что производное морфинана является эффективным при лечении или профилактике тошноты и рвоты, индуцированных агонистом опиоидного µ-рецептора, и в непатентной литературной ссылке 2 описано, что 6,7-насыщенные 7-карбамоилзамещенные производные морфинана обладают антагонизмом для опиоидного δ-рецептора. Однако ни в одном из них не описано или не предложено настоящее соединение.
Патентная литературная ссылка 1 - публикация Международной патентной заявки WO 2004-007503.
Патентная литературная ссылка 2 - публикация Международной патентной заявки WO 95/13071.
Непатентная литературная ссылка 1 - Journal of Medicinal Chemistry 41, 4177-4180.
Непатентная литературная ссылка 2 - Chemical and Pharmaceutical Bulletin, 52 (66) 747-750 (2004).
Описание изобретения
Проблемы, которые должны быть разрешены изобретением
Авторами изобретения обнаружено, что 6,7-ненасыщенные 7-карбамоилзамещенные производные морфинана являются полезными в качестве композиции для лечения и/или профилактики тошноты, рвоты и/или констипации.
Способ разрешения проблем
Настоящее изобретение предлагает:
(1) соединение, представленное формулой (I):
 ,
,
где R1 и R2, каждый независимо, представляет собой водород, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный низший алкилсульфонил, необязательно замещенный ацил, необязательно замещенный циклоалкил, необязательно замещенный циклоалкенил, необязательно замещенный арил, необязательно замещенную гетероциклическую группу или необязательно замещенный арилсульфонил, или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют необязательно замещенный гетероцикл;
R3 представляет собой водород, гидрокси, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный низший алкокси, меркапто, необязательно замещенный низший алкилтио, необязательно замещенный амино, необязательно замещенный карбамоил, необязательно замещенный ацил, необязательно замещенный ацилокси, необязательно замещенный арил или необязательно замещенную гетероциклическую группу;
группа, представленная формулой:
 может быть
может быть
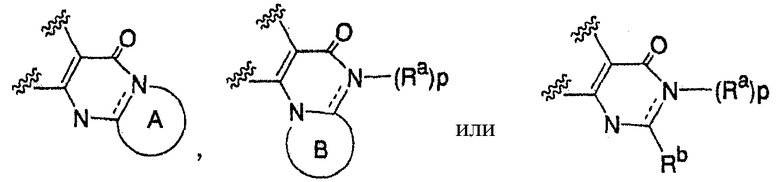 ,
,
где кольцо А или кольцо В, каждое независимо, представляет собой необязательно замещенный азотсодержащий гетероцикл, необязательно содержащий дополнительный атом азота, атом кислорода и/или атом серы в кольце;
пунктирная линия означает присутствие или отсутствие связи;
когда пунктирная линия означает присутствие связи, р равно 0;
когда пунктирная линия означает отсутствие связи, р равно 1;
Ra представляет собой водород, необязательно замещенный низший алкил, необязательно замещенный низший алкенил или необязательно замещенный низший алкинил;
и Rb представляет собой водород или оксо;
R4 представляет собой водород или низший алкил;
R5 представляет собой водород, низший алкил, циклоалкил-низший алкил или низший алкенил,
или его фармацевтически приемлемую соль или сольват;
(1') соединение, представленное формулой (I):
 ,
,
где R1 и R2, каждый независимо, представляет собой водород, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный циклоалкил, необязательно замещенный арил или необязательно замещенную гетероциклическую группу, или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют необязательно замещенный гетероцикл;
R3 представляет собой водород, гидрокси, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный низший алкокси, меркапто, необязательно замещенный низший алкилтио, необязательно замещенный арил или необязательно замещенную гетероциклическую группу;
R4 представляет собой водород или низший алкил;
R5 представляет собой водород, низший алкил, циклоалкил-низший алкил или низший алкенил;
или его фармацевтически приемлемую соль или сольват;
(2) соединение согласно (1) или (1'), где R3 представляет собой гидрокси,
или его фармацевтически приемлемую соль или сольват,
(3) соединение согласно (1) или (1'), где R3 представляет собой необязательно замещенный амино,
или его фармацевтически приемлемую соль или сольват;
(4) соединение согласно (1) или (1'), где R3 представляет собой амино, замещенный необязательно замещенным арилсульфонилом,
или его фармацевтически приемлемую соль или сольват;
(5) соединение согласно любому из (1)-(4) и (1'), где R1 представляет собой водород или низший алкил, R2 представляет собой необязательно замещенный низший алкил, необязательно замещенный фенил, необязательно замещенный циклоалкил или необязательно замещенную гетероциклическую группу, и R5 представляет собой циклопропилметил,
или его фармацевтически приемлемую соль, или сольват;
(6) соединение согласно любому из (1)-(5) и (1'), где R1 представляет собой водород, R2 представляет собой низший алкил, необязательно замещенный гетероциклической группой, или низший алкокси, необязательно замещенный арилом, фенил, необязательно замещенный низшим алкилом или низшим алкокси, циклоалкил, замещенный низшим алкилкарбонилом, или гетероциклическую группу, замещенную низшим алкокси или арилом, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
или его фармацевтически приемлемую соль или сольват;
(7) фармацевтическую композицию, содержащую соединение согласно любому из (1)-(6) и (1') или его фармацевтически приемлемую соль или сольват,
(8) композицию, обладающую антагонистической активностью для опиоидного рецептора и содержащую соединение согласно (1)-(6) и (1') или его фармацевтически приемлемую соль или сольват;
(9) композицию для лечения и/или профилактики тошноты, рвоты и/или констипации, содержащую соединение согласно любому из (1)-(6) и (1') или его фармацевтически приемлемую соль или сольват;
(10) композицию для ослабления и/или профилактики побочного действия, вызванного соединением, обладающим агонистической активностью для опиоидного рецептора, содержащую соединение согласно любому из (1)-(6) и (1') или его фармацевтически приемлемую соль или сольват;
(11) композицию для лечения и/или профилактики согласно (10), где побочным действием является тошнота, рвота и/или констипация;
(12) агент для лечения и/или профилактики согласно (10) или (11), где соединением, обладающим агонистической активностью для опиоидного рецептора, является морфин, оксикодон или его фармацевтически приемлемая соль или сольват;
(13) применение соединения согласно любому из (1)-(6) и (1') или его фармацевтически приемлемой соли или сольвата для получения лекарственного средства для лечения и/или профилактики тошноты, рвоты и/или констипации;
(14) применение соединения согласно любому из (1)-(6) и (1') или его фармацевтически приемлемой соли или сольвата для получения лекарственного средства для ослабления и/или профилактики побочного действия, вызванного соединением, обладающим агонистической активностью для опиоидного рецептора;
(15) способ лечения и/или профилактики тошноты, рвоты и/или констипации, включающий введение соединения согласно любому из (1)-(6) и (1') или его фармацевтически приемлемой соли или сольвата;
(16) способ ослабления и/или профилактики побочного действия, вызванного соединением, обладающим агонистической активностью для опиоидного рецептора, включающий введение соединения согласно любому из (1)-(6) и (1'), его фармацевтически приемлемой соли или ее сольвата;
(17) композицию для аналгезии, содержащую соединение, обладающее агонистической активностью для опиоидного рецептора, и эффективное количество соединения согласно любому из (1)-(6) и (1') или его фармацевтически приемлемой соли или сольвата для ослабления и/или профилактики побочного действия, вызванного введением соединения, обладающего агонистической активностью для опиоидного рецептора;
(18) композицию для аналгезии, содержащую соединение, обладающее агонистической активностью для опиоидного рецептора, и эффективное количество соединения согласно любому из (1)-(6) и (1') или его фармацевтически приемлемой соли или сольвата для лечения и/или профилактики тошноты, рвоты и/или констипации, вызванной введением соединения, обладающего агонистической активностью для опиоидного рецептора;
(19) аналгетик согласно (17) или (18), где соединением, обладающим агонистической активностью для опиоидного рецептора, является морфин, оксикодон, его фармацевтически приемлемая соль или сольват.
Эффект изобретения
Соединение (I) настоящего изобретения обладает активностью при лечении и/или профилактике тошноты, рвоты и/или констипации, особенно тошноты, рвоты и/или констипации, вызванной соединением, обладающим агонистической активностью для опиоидного рецептора (например, опиоидного µ-рецептора), и является полезным в качестве средства для ослабления побочного действия у пациента, которому вводят соединение, обладающее агонистической активностью опиоидного рецептора, или который находится в средней стадии его введения.
Лучший способ выполнения изобретения
Применяемый здесь термин «галоген» включает фтор, хлор, бром и йод. Галогенная часть «низшего галогеналкила», «низшего галогеналкокси» и «низшего галогеналкилтио» имеет такое же значение.
«Низший алкил» включает неразветвленный или разветвленный алкил с числом атомов углерода 1-10, предпочтительно с числом атомов углерода 1-6, еще предпочтительнее 1-3, и примеры его включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, гексил, изогексил, н-гептил, изогептил, н-октил, изооктил, н-нонил и н-децил. Предпочтительными являются метил, этил, изопропил, н-бутил, втор-бутил, трет-бутил и 1-этилпропил.
Примеры заместителя «необязательно замещенного низшего алкила» включают галоген, гидрокси, низший алкокси, низший галогеналкокси, низший гидроксиалкокси, низший алкилтио, низший алкиламино, ациламино, ацил, ацилокси, циано, карбокси, низший алкоксикарбонил, карбамоил, низший алкилкарбамоил, цианокарбамоил, низший алкилсульфонилкарбамоил, арилсульфонилкарбамоил, сульфамоил, низший алкилсульфамоил, низший алкилсульфонил, циклоалкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α (где группой заместителей α являются галоген, гидрокси, низший алкил, низший галогеналкил, низший гидроксиалкил, низший алкокси-низший алкил, низший карбоксиалкил, низший алкоксикарбонил-низший алкил, низший аминоалкил, низший алкиламино-низший алкил, ациламино-низший алкил, низший цианоалкил, низший алкокси, низший галогеналкокси, низший гидроксиалкокси, низший алкилтио, низший галогеналкилтио, ацил, ацилокси, амино, низший алкиламино, ациламино, циано, карбокси, низший алкоксикарбонил, карбамоил, низший алкилкарбамоил, арилкарбамоил, цианокарбамоил, низший алкилсульфонилкарбамоил, сульфамоил, низший алкилсульфамоил, низший алкилсульфонил, арил, необязательно замещенный низшим алкилендиокси, и гетероциклическая группа), циклоалкенил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, арил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, арилокси, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, арилтио, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, гетероциклическую группу, необязательно замещенную одним или несколькими заместителями, выбранными из группы заместителей α, и гетероциклилокси, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α.
Низшая алкильная часть «низшего галогеналкила», «низшего гидроксиалкила», «низшего аминоалкила», «ациламино-низшего алкила», «ацилокси-низшего алкила», «циклоалкил-низшего алкила», «низшего алкокси», «низшего галогеналкокси», «низшего гидроксиалкокси», «низшего алкокси-низшего алкила», «низшего алкоксикарбонила», «низшего карбоксиалкила», «низшего алкоксикарбонил-низшего алкила», «низшего алкилтио», «низшего галогеналкилтио», «низшего алкиламино», «низшего алкиламино-низшего алкила», «низшего алкилкарбамоила», «низшего алкилсульфамоила», «низшего алкилсульфонила», «арил-низшего алкила», «три-низшего алкилсилила», «низшего алкилдиарилсилила», «триарил-низшего алкилсилила», «низшего алкокси-низшего алкокси-низшего алкила», «низшего алкилтио-низшего алкила», «арил-низшего алкокси-низшего алкила», «низшего алкилсульфонила», «низшего алкилсульфонилкарбамоила», «низшего алкилкарбонила», «низшего цианоалкила», «низшего алкоксикарбониламино», «низшего алкилендиокси» и гетероциклил-низшего алкила» является такой же, как вышеуказанный «низший алкил».
Заместитель «необязательно замещенного низшего алкокси», «необязательно замещенного низшего алкилтио» и «необязательно замещенного низшего алкилсульфонила» является таким же, как указанный выше заместитель «необязательно замещенного низшего алкила».
«Низший алкенил» включает неразветвленный или разветвленный алкенил с числом атомов углерода 2-10, предпочтительно с числом атомов углерода 2-8, еще предпочтительнее с числом атомов углерода 3-6, имеющий одну или несколько двойных связей в произвольном положении. В частности, примеры его включают винил, аллил, пропенил, изопропенил, бутенил, изобутенил, пренил, бутадиенил, пентенил, изопентенил, пентадиенил, гексенил, изогексенил, гексадиенил, гептенил, октенил, ноненил и деценил. Низший алкенил в R5 предпочтительно представляет собой аллил.
Заместителем «необязательно замещенного низшего алкенила» является такой же заместитель, как заместитель «необязательно замещенного низшего алкила».
«Низший алкинил» включает неразветвленный или разветвленный алкинил с числом атомов углерода 2-10, предпочтительно с числом атомов углерода 2-8, еще предпочтительнее с числом атомов углерода 3-6, имеющий одну или несколько тройных связей в произвольном положении. В частности, примеры его включают этинил, пропинил, бутинил, пентинил, гексинил, гептинил, октинил, нонинил и децинил. Они могут дополнительно иметь двойную связь в произвольном положении.
Заместителем «необязательно замещенного низшего алкинила» является такой же заместитель, как заместитель «необязательно замещенного низшего алкила».
Примеры заместителя «необязательно замещенного амино» включают низший алкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, циклоалкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, ацил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, амино, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, арил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, сульфамоил, низший алкилсульфамоил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, арилсульфамоил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, низший алкилсульфонил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, арилсульфонил, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, ариламино, необязательно замещенный одним или несколькими заместителями, выбранными из группы заместителей α, и гетероциклическую группу, необязательно замещенную одним или несколькими заместителями, выбранными из группы заместителей α.
Заместителем «необязательно замещенного карбамоила» является такой же заместитель, как заместитель «необязательно замещенного амина».
«Циклоалкил» представляет собой карбоциклическую группу с числом атомов углерода 3-10, предпочтительно с числом атомов углерода 3-8, более предпочтительно с числом атомов углерода 4-8 и, например, включает циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил и циклодецил. Он может быть дополнительно конденсирован с «арилом», описанным ниже, или «гетероциклической группой», описанной ниже, в производном положении.
В качестве «циклоалкила» в R1 и R2 предпочтительными являются циклопропил, циклобутил, циклопентил и циклогексил.
Циклоалкильная часть «циклоалкил-низшего алкила» и «циклоалкилкарбонила» является такой же, как указанный выше «циклоалкил».
В качестве «циклоалкил-низшего алкила» в R5 предпочтительным является циклопропилметил.
Примеры заместителя «необязательно замещенного «циклоалкила» включают один или несколько заместителей, выбранных из группы заместителей α. Заместитель может быть расположен в произвольном положении и может быть у атома углерода, имеющего связь циклоалкила.
Термин «циклоалкенил» включает циклоалкенил, имеющий одну или несколько двойных связей в произвольном положении в кольце указанного выше циклоалкила, и примеры его включают циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил и циклогексадиенил.
В качестве «циклоалкенила» в R1 и R2 предпочтительными являются циклопропенил, циклобутенил, циклопентенил и циклогексенил.
Циклоалкенильная часть «циклоалкенилкарбонила» является такой же, как указанный выше «циклоалкенил».
Заместителем «необязательно замещенного циклоалкенила» является такой же заместитель, как заместитель указанного выше «необязательно замещенного циклоалкила».
«Арил» включает фенил, нафтил, антрил и фенантрил, особенно предпочтительным является фенил.
Арильная часть «арилокси», «арилтио», арил-низшего алкила», «низшего алкилдиарилсилила», триарил-низшего алкилсилила, «арил-низший алкилокси-низшего алкила», «арилсульфонила», «арилсульфамоила», «ариламино», «арилкарбамоила» и «арилсульфонилкарбамоила» является такой же, как указанный выше «арил».
Примеры заместителя «необязательно замещенного арила», «необязательно замещенного фенила» и «необязательно замещенного арилсульфонила» включают заместитель группы α, фенил, замещенный одной или несколькими группами, выбранными из группы заместителей α, фенокси, замещенный одной или несколькими группами, выбранными из группы заместителей α, и низший алкилендиокси.
«Гетероциклическая группа» включает гетероциклическую группу, имеющую в кольце один или несколько гетероатомов, произвольно выбранных из О, S и N, и в частности включает 5-6-членный гетероарил, такой как пирролил, имидазолил, пиразолил, пиридил, пиридазинил, пиримидинил, пиразинил, триазолил, триазинил, тетразолил, изоксазолил, оксазолил, оксадиазолил, изотиазолил, тиазолил, тиадиазолил, фурил и тиенил; бициклическую конденсированную гетероциклическую группу, такую как индолил, изоиндолил, индазолил, индолидинил, индолинил, изоиндолинил, хинолил, изохинолил, циннолинил, фталазинил, хиназолинил, нафтиридинил, хиноксалинил, пуринил, птеридинил, бензопиранил, бензимидазолил, бензизоксазолил, бензоксазолил, бензоксадиазолил, бензоизотиазолил, бензотиазолил, бензотиадиазолил, бензофурил, изобензофурил, бензотиенил, бензотриазолил, имидазопиридил, триазолопиридил, имидазотиазолил, пиразинопиридазинил, хиназолинил, хинолил, изохинолил, нафтиридинил, дигидропиридил, тетрагидрохинолил и тетрагидробензотиенил; трициклическую конденсированную гетероциклическую группу, такую как карбазолил, акридинил, ксантенил, фенотиазинил, феноксатиинил, феноксазинил и дибензофурил; неароматическую гетероциклическую группу, такую как диоксанил, тииранил, тиоранил, тиетанил, оксиланил, оксетанил, оксатиоранил, азетидинил, тианил, пирролидинил, пирролинил, имидазолидинил, имидазолинил, пиразолидинил, пиразолинил, пиперидил, пиперазинил, морфолинил, морфолино, тиоморфолинил, тиоморфолино, дигидропиридил, дигидрофурил, тетрагидрофурил, тетрагидропиранил, тетрагидротиазолил и тетрагидроизотиазолил. Предпочтительной является 5-6-членная гетероарильная или неароматическая гетероциклическая группа.
В качестве «гетероциклической группы» в R1 и R2 предпочтительными являются пиразолил, пиридил, пиридазинил, пиримидинил, пиразинил, изоксазолил, тиазолил, тиадиазолил, фурил, тиенил, индолил, индазолил, хинолил, изохинолил, бензоксазолил, бензотиазолил, оксетанил, тетрагидрофурил и тетрагидропиранил. Более предпочтительными являются пиридил, пиридазинил, пиримидинил и пиразинил. Особенно предпочтительными являются пиридил и пиримидинил.
В качестве гетероциклической группы «необязательно замещенного низшего алкила» в R1 и R2 предпочтительными являются изоксазолил, оксазолил и оксадиазолил. Особенно предпочтительным является оксадиазолил.
Гетероциклическая часть «гетероциклилокси» и «гетероциклил-низшего алкила» является такой же, как указанная выше «гетероциклическая группа».
Примеры заместителя «необязательно замещенной гетероциклической группы» включают одну или несколько групп, выбранных из группы, состоящей из заместителей группы α, и оксо. Заместитель может быть расположен в произвольном положении или может быть у атома углерода или атома азота, имеющего связь гетероциклической группы.
«Ацил» включает подобный неразветвленной или разветвленной цепи алифатический ацил с числом атомов углерода 1-10, предпочтительно с числом атомов углерода 1-6, более предпочтительно с числом атомов углерода 1-4, циклоалифатический ацил с числом атомов углерода 4-9, предпочтительно с числом атомов углерода 4-7, ароил и гетероциклилкарбонил. Здесь термин «подобный цепи алифатический радикал» включает указанный выше «низший алкил», указанный выше «низший алкенил» и указанный выше «низший алкинил». Термин «циклоалифатический радикал» включает указанный выше «циклоалкил» и указанный выше «циклоалкенил». Гетероциклическая часть гетероциклилкарбонила является такой же, как указанная выше «гетероциклическая группа». Примеры ацила включают формил, ацетил, пропионил, бутирил, изобутирил, валерил, пивалоил, гексаноил, акрилоил, пропиолоил, метакрилоил, кротоноил, циклопропилкарбонил, циклогексилкарбонил, циклооктилкарбонил, бензоил, пиридинкарбонил, пиперидинкарбонил, пиперазинкарбонил, морфолинокарбонил и тому подобное.
Ацильная часть «ацилокси», «ациламино», «ациламино-низший алкил» и «ацилокси-низший алкил» является такой же, как указанный выше «ацил».
Заместитель «необязательно замещенного ацила» или «необязательно замещенного» является таким же, как заместитель указанного выше «необязательно замещенного низшего алкила», когда «ацил» является подобным цепи алифатическим ацилом, и включает одну или несколько групп, выбранных из группы заместителей α, когда «ацил» представляет собой циклоалифтический ацил, ароил или гетероциклилкарбонил.
«Необязательно замещенный гетероцикл», образованный, когда R1 и R2 взяты вместе с атомом азота, к которому они присоединены, включает 5-членный или 6-членный гетероцикл, содержащий атом азота, к которому присоединены R1 и R2, и дополнительно необязательно содержащий один или несколько гетероатомов, выбранных из N, S и О. Например, включен случай, когда  представляет собой насыщенную гетероциклическую группу, такую как
представляет собой насыщенную гетероциклическую группу, такую как
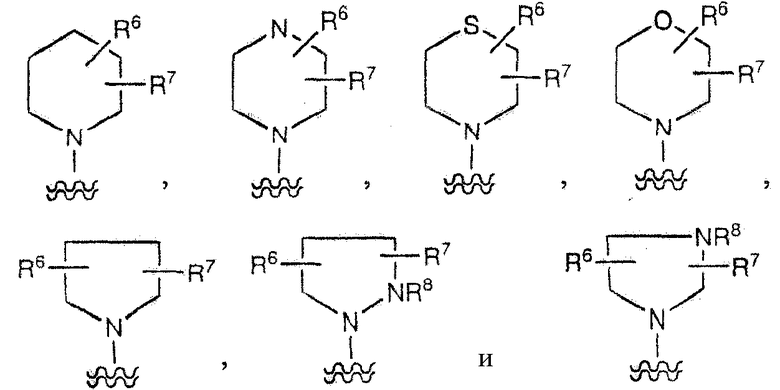 ,
,
или ненасыщенную гетероциклическую группу, такую как
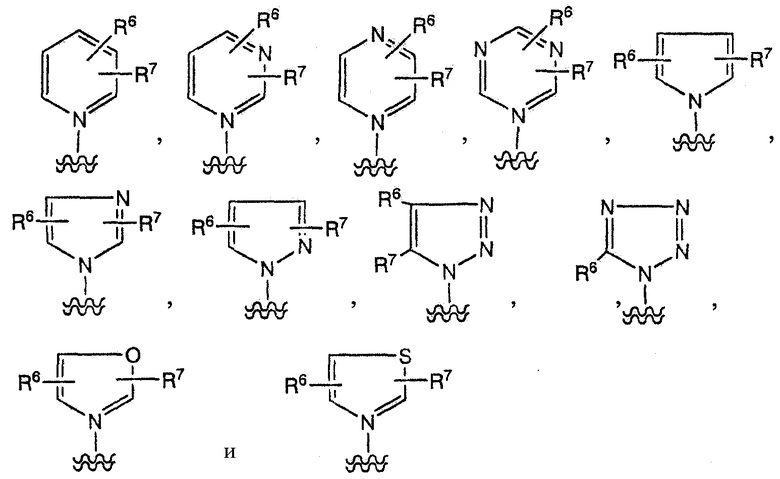 ,
,
где R6, R7 и R8, каждый независимо, представляет собой водород, галоген, гидрокси, низший алкил, низший алкокси, низший алкилтио, ацил, ацилокси, амино, низший алкиламино, ациламино, низший алкоксикарбониламино, карбокси или низший алкоксикарбонил, и предпочтительно насыщенную гетероциклическую группу, такую как кольцо морфолина, кольцо пирролидина, кольцо пиперидина, кольцо пиперазина и тому подобное, необязательно замещенное водородом, галогеном, гидрокси или низшим алкилом.
Заместителем «необязательно замещенного гетероцикла, который образован, когда R1 и R2 взяты вместе с атомом азота, к которому они присоединены», является такой же заместитель, как заместитель «необязательно замещенной гетероциклической группы».
Радикал формулы  представляет собой радикал формулы
представляет собой радикал формулы 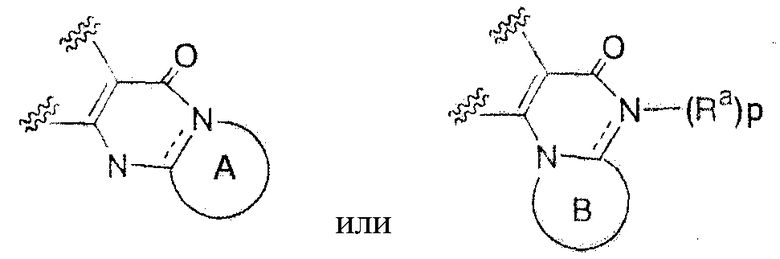 , который включает, например, следующие радикалы:
, который включает, например, следующие радикалы:

 ,
,
где Ra имеет указанные выше значения, и R представляет собой водород или группу, выбранную из группы заместителей α.
Здесь «сольват» включает, например, сольват органического растворителя, гидрат и тому подобное. Когда образуется гидрат, может быть координировано любое число молекул воды.
Соединение (I) включает фармацевтически приемлемую соль. Примеры ее включают соли со щелочными металлами (литием, натрием или калием), с щелочноземельными металлами (магнием или кальцием), аммонием, органическими основаниями или аминокислотами и соли с неорганическими кислотами (хлористоводородной кислотой, серной кислотой, азотной кислотой, бромистоводородной кислотой, фосфорной кислотой и йодистоводородной кислотой) или органическими кислотами (уксусной кислотой, трифторуксусной кислотой, лимонной кислотой, молочной кислотой, винной кислотой, щавелевой кислотой, малеиновой кислотой, фумаровой кислотой, миндальной кислотой, глутаровой кислотой, яблочной кислотой, бензойной кислотой, фталевой кислотой, бензолсульфоновой кислотой, п-толуолсульфоновой кислотой, метансульфоновой кислотой или этансульфоновой кислотой). Особенно предпочтительной является хлористоводородная кислота, фосфорная кислота, винная кислота или метансульфоновая кислота. Эти соли можно получить общепринятым способом.
Кроме того, соединение (I) не ограничивается определенным изомером, но включает все возможные изомеры и рацематы. Например, когда R3 соединения (I) является гидрокси, соединение (I) включает другой таутомер, то есть нижеследующее соединение (I').

Настоящее соединение (I) можно получить нижеследующим способом.
Способ А
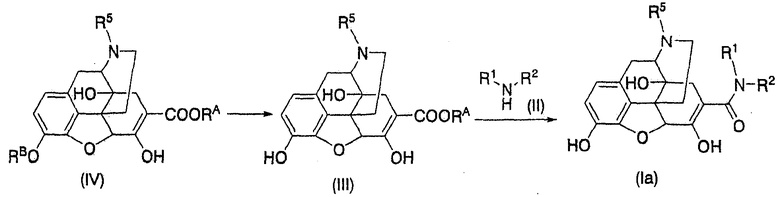 ,
,
где RA представляет собой остаток сложного эфира, RB представляет собой водород или гидроксизащитную группу, и другие символы имеют значения, указанные выше.
Здесь остаток сложного эфира включает низший алкил, такой как метил, этил и тому подобное, арил-низший алкил, такой как бензил, фенетил и тому подобное, ацилокси-низший алкил, такой как ацетилоксиметил и тому подобное и т.д.
Гидроксизащитная группа не ограничивается перечисленным, но включает низший алкил (метил, трет-бутил и т.д.), арил-низший алкил (трифенилметил, бензил и т.д.), три-низший алкилсилил (триметилсилил, трет-бутилдиметилсилил, триэтилсилил, триизопропилсилил и т.д.), низший алкилдиарилсилил (трет-бутилдифенилсилил и т.д.), триарил-низший алкилсилил (трибензилсилил и т.д.), низший алкокси-низший алкил (метоксиметил, 1-этоксиэтил, 1-метил-1-метоксиэтил и т.д.), низший алкокси-низший алкокси-низший алкил (метоксиэтоксиметил и т.д.) низший алкилтио-низший алкил (метилтиометил и т.д.), необязательно замещенный тетрагидропиранил (тетрагидропиранил-2-ил, 4-метокситетрагидропиран-4-ил и т.д.), тетрагидротиопиранил (тетрагидротиопиран-2-ил и т.д.), тетрагидрофуранил (тетрагидрофуран-2-ил и т.д.), тетрагидротиофуранил (тетрагидротиофуран-2-ил и т.д.), арил-низший алкилокси-низший алкил (бензилоксиметил и т.д.), низший алкилсульфонил (метансульфонил, этансульфонил и т.д.), ацил (ацетил и т.д.) и арилсульфонил (п-толуолсульфонил и т.д.).
Первая стадия
Сначала известное соединение или соединение (IV), полученное из него, освобождают от защитной группы общепринятым способом.
Например, когда защитной группой является бензил, соединение растворяют или суспендируют в подходящем растворителе (этилацетате, метаноле, этаноле, тетрагидрофуране, диоксане, диметилформамиде, уксусной кислоте, разбавленной хлористоводородной кислоте или их смеси), и реакцией гидрирования с применением палладиевого катализатора (гидроксида палладия, палладия на угле, палладия на сульфате бария, палладия на оксиде алюминия, палладиевой черни и т.д.) получают соединение (III). Реакцию можно проводить при температуре от приблизительно 0°С до приблизительно 100°С, предпочтительно от приблизительно 20°С до приблизительно 50°С в течение от приблизительно 15 минут до приблизительно 24 часов, предпочтительно от приблизительно 1 часа до приблизительно 5 часов.
Вторая стадия
Затем образовавшееся соединение (III) непосредственно амидируют, получая при этом соединение (Ia).
Например, соединение (III) и соединение (II) могут быть подвергнуты реакции нагреванием в подходящем растворителе (метаноле, этаноле, тетрагидрофуране, диметилформамиде, диэтиловом простом эфире, дихлорметане, дихлорэтане, толуоле, ксилоле, хлорбензоле, ортодихлорбензоле, 2-метоксиэтаноле и диметиловом эфире диэтиленгликоля или их смеси) или без растворителя при температуре от приблизительно 0°С до приблизительно 250°С, предпочтительно от приблизительно 80°С до приблизительно 200°С в течение от приблизительно 30 минут до приблизительно 24 часов, предпочтительно приблизительно 1-12 часов, в присутствии или в отсутствие аминового соединения (аммиака, диметиламина, триэтиламина, пиридина, диметиланилина, диметиламинопиридина, лутидина и т.д.).
Для эффективного проведения реакции ее можно проводить облучением микроволнами. Температуру реакции и время облучения конкретно не ограничивают, но ее проводят при температуре приблизительно от 100°С до приблизительно 200°С и в течение от приблизительно 5 минут до приблизительно 5 часов, предпочтительно от приблизительно 10 минут до приблизительно 1 часа. В качестве растворителя предпочтительно применяют полярный растворитель, такой как метанол, этанол, 1-пропанол, этиленгликоль, глицерин, 2-метоксиэтанол, 2-этоксиэтанол, N,N-диметилформамид, диметиловый эфир диэтиленгликоля и тому подобное.
Когда R4 рассматриваемого соединения (I) представляет собой низший алкил, рассматриваемое соединение можно получить общепринятой реакцией получения простого эфира в произвольной стадии.
Способ В
 ,
,
где R3a представляет собой гидрокси или необязательно замещенный низший алкокси, и другие символы имеют значения, указанные выше.
Первая стадия
Когда R3 рассматриваемого соединения (I) представляет собой необязательно замещенный низший алкокси, сначала известное соединение (IV) превращают в простой эфир общепринятым методом.
Например, соединение подвергают взаимодействию с алкилирующим агентом или спиртом, имеющим группу R3a, соответствующую такой группе рассматриваемого соединения, в присутствии основания (гидрида натрия, гидрида калия, гидроксида натрия, гидроксида калия, гидроксида кальция, гидроксид бария, карбоната натрия, карбоната калия, карбоната кальция, карбоната цезия, метоксида натрия, этоксида натрия, трет-бутоксида калия, бикарбоната натрия или металлического натрия) или в условиях Мицунобу в подходящем растворителе (N,N-диметилформамиде, диметилсульфоксиде, толуоле, бензоле, ксилоле, их смеси или тому подобном, циклогексане, гексане, дихлорметане, 1,2-дихлорэтане, тетрагидрофуране, диоксане, ацетоне, метилэтилкетоне, ацетонитриле, воде или их смеси), получая при этом соединение (VII). Реакцию можно проводить при температуре от -70 до 180°С, предпочтительно приблизительно 0-150°С в течение приблизительно от 15 минут до приблизительно 24 часов, предпочтительно от приблизительно 1 часа до приблизительно 5 часов.
Вторая стадия
Затем соединение (VII) гидролизуют для получения соединения (VI). Реакцию можно проводить при от температуры охлаждения льдом до температуры флегмы растворителя в течение от приблизительно 15 минут до приблизительно 24 часов, предпочтительно от 1 часа до приблизительно 5 часов с применением неорганического основания (гидроксида натрия, гидроксид лития или гидроксида калия) в подходящем растворителе (метаноле, этаноле, тетрагидрофуране, диоксане, диметилформамиде или их смеси).
Третья стадия и четвертая стадия
Затем соединение (VI) амидируют и образовавшееся соединение (V) освобождают от защитной группы, получая при этом рассматриваемое соединение (Ib). Эти реакции можно проводить такими же методами, как методы второй стадии и первой стадии в способе А, соответственно. В стадии амидирования реакцию можно проводить, если необходимо, в присутствии конденсирующего агента (N,N'-дициклогексилкарбодиимида, N-диметиламинопропил-N'-этилкарбодиимида, диэтилфосфорилцианида, дифенилфосфорилазида и т.д.).
Помимо этого, когда R4 рассматриваемого соединения (I) представляет собой низший алкил, реакцию образования простого эфира можно проводить на произвольной стадии, как описано выше.
Способ С
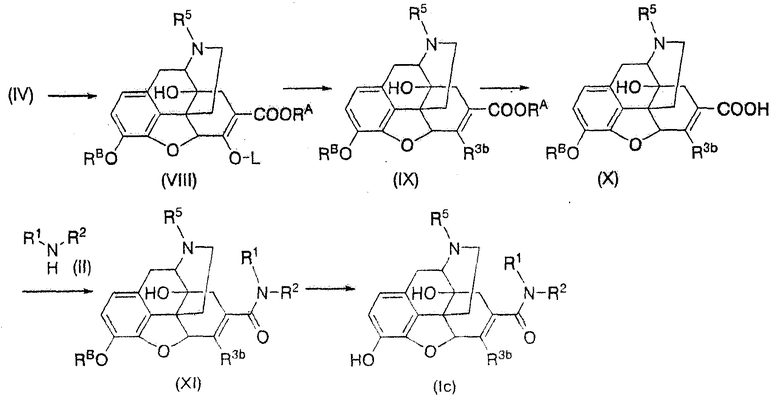 ,
,
где L представляет собой уходящую группу, R3b представляет собой водород, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный низший алкокси, меркапто, необязательно замещенный низший алкилтио, необязательно замещенный амино, необязательно замещенный карбамоил, необязательно замещенный арил или необязательно замещенную гетероциклическую группу, и другие символы имеют значения, указанные выше.
Первая стадия
Когда R3 рассматриваемого соединения (I) представляет собой R3b, уходящую группу L (например, трифторметансульфонил, метансульфонил, эфир фосфорной кислоты и т.д.) вводят в известное соединение (IV). Например, соединение подвергают взаимодействию с трифторметансульфоновым ангидридом, трифторметансульфонилхлоридом, метансульфонилхлоридом, метансульфоновым ангидридом, п-толуолсульфонилхлоридом, N-фенилтрифторметансульфонимидом или различными этерифицирующими реагентами фосфорной кислоты в присутствии основания (пиридина, триэтиламина, аммиака, диметиламина, диметиланилина, диметиламинопиридина, 2,6-лутидина или 2,6-ди-трет-бутилпиридина) с применением дихлорметана, хлороформа, тетрагидрофурана, бензола, толуола, диметилформамида, этилацетата или их смеси в качестве растворителя.
Вторая стадия
Полученное таким образом соединение (VIII) подвергают известной реакции введения заместителя для получения соединения (IX).
Третья стадия, четвертая стадия и пятая стадия
Соединение (IX) гидролизуют, амидируют и освобождают от защитной группы такими же методами, как методы второй стадии в способе В, второй стадии в способе А и первой стадии в способе А, соответственно, получая при этом рассматриваемое соединение (Ic).
Помимо этого, когда R4 рассматриваемого соединения (I) представляет собой низший алкил, реакцию образования простого эфира можно проводить в произвольной стадии, как описано выше.
Способ D
Соединение (VIII) получают первой стадией в способе С, амидируют согласно методу четвертой стадии способа С и подвергают реакции введения заместителя R3b, реакции снятия защиты и реакции гидролиза согласно методам второй стадии, третьей стадии и пятой стадии в способе С, соответственно, тем самым получая соединение (I).
Все из таким образом полученных настоящих соединений обладают антагонистической активностью для опиоидного рецептора и являются полезными в качестве лекарственных средств, среди соединений, представленных формулой (I), нижеследующие соединения являются особенно предпочтительными:
а) соединение, у которого R1 представляет собой водород или низший алкил,
b) соединение, у которого R1 представляет собой водород или С1-С3-алкил,
с) соединение, у которого R2 представляет собой:
(с-i) низший алкил, необязательно замещенный одной или несколькими группами, выбранными из группы заместителей β (здесь группой заместителей β являются циклоалкил, необязательно замещенный гидрокси, галогеном, гидрокси, низшим алкокси, низшим галогеналкокси, низшим алкилтио, амино, низшим алкиламино, карбокси, низшим алкоксикарбонилом, циано, низшим алкилсульфонилом, арилом, арилокси и низшим алкилендиокси),
(с-ii) фенил, необязательно замещенный одной или несколькими группами, выбранными из группы, состоящей из группы заместителей β, низшего алкила и низшего галогеналкила,
(с-iii) арил-низший алкил, необязательно замещенный одной или несколькими группами, выбранными из группы заместителей β,
(с-iv) циклоалкил, необязательно замещенный одной или несколькими группами, выбранными из группы заместителей β,
(с-v) гетероциклическую группу, необязательно замещенную одной или несколькими группами, выбранными из группы заместителей β, или
(с-vi) гетероциклил-низший алкил, необязательно замещенный одной или несколькими группами, выбранными из группы заместителей β,
d) соединение, у которого R2 представляет собой:
(d-1) низший алкил, необязательно замещенный гидрокси, циклоалкил, необязательно замещенный гидрокси, низшим алкокси, низшим алкилтио, низшим алкиламино или арилокси,
(d-ii) фенил, необязательно замещенный галогеном, низшим алкилом, низшим галогеналкилом, низшим алкокси, низшим галогеналкокси, низшим алкилтио, амино, низшим алкиламино, циано, низшим алкилсульфонилом или низшим алкилендиокси,
(d-iii) арил-низший алкил, необязательно замещенный низшим алкокси или низшим алкилтио,
(d-iv) циклоалкил, необязательно замещенный низшим алкилом, карбокси или низшим алкоксикарбонилом,
(d-v) гетероциклическую группу, необязательно замещенную низшим алкилом, низшим алкокси или фенилом, или
(d-vi) гетероциклил-низший алкил, необязательно замещенный низшим алкилом или арилом,
е) соединение, у которого R1 и R2, взятые вместе с атомом N, к которому они присоединены, образуют 5-членный или 6-членный насыщенный гетероцикл,
f) соединение, у которого R3 представляет собой гидрокси или низший алкокси,
g) соединение, у которого R3 представляет собой гидрокси,
h) соединение, у которого R3 представляет собой амино, необязательно замещенный одной или несколькими группами, выбранными из группы заместителей α,
i) соединение, у которого R3 представляет собой галоген, низший алкил или амино, замещенный арилсульфонилом, необязательно замещенным низшим алкокси,
j) соединение, у которого R4 представляет собой водород или метокси,
k) соединение, у которого R5 представляет собой циклоалкил-низший алкил или низший алкенил,
l) соединение, у которого R5 представляет собой циклопропилметил или аллил,
m) соединение, у которого R5 представляет собой циклопропилметил,
n) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-i), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклоалкил-низший алкил или -низший алкенил,
о) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-i), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
р) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-i), R3 представляет собой галоген, низший алкил или амино, замещенный арилсульфонилом, необязательно замещенным низшим алкокси, R4 представляет собой водород, и R5 представляет собой циклоалкил-низший алкил или -низший алкенил,
q) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-i), R3 представляет собой галоген, низший алкил или амино, замещенный арилсульфонилом, необязательно замещенным низшим алкокси, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
r) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-ii), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклоалкил-низший алкил или -низший алкенил,
s) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-ii), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
t) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-iii), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклоалкил-низший алкил или -низший алкенил,
u) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-iii), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
v) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-iv), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклоалкил-низший алкил или -низший алкенил,
w) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-iv), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
х) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-v), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклоалкил-низший алкил или -низший алкенил,
y) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-v), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
z) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-vi), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклоалкил-низший алкил или -низший алкенил,
аа) соединение, у которого R1 представляет собой водород или низший алкил, R2 представляет собой (d-vi), R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
ab) соединение, у которого R1 и R2, взятые вместе с атомом N, с которым они связаны, образуют 5-членный или 6-членный насыщенный гетероцикл, R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклоалкил-низшая алкильная группа или низший алкенил,
ас) соединение, у которого R1 и R2, взятые вместе с атомом N, с которым они связаны, образуют 5-членный или 6-членный насыщенный гетероцикл, R3 представляет собой гидрокси или низший алкокси, R4 представляет собой водород, и R5 представляет собой циклопропилметил,
или их фармацевтически приемлемые соли или сольваты.
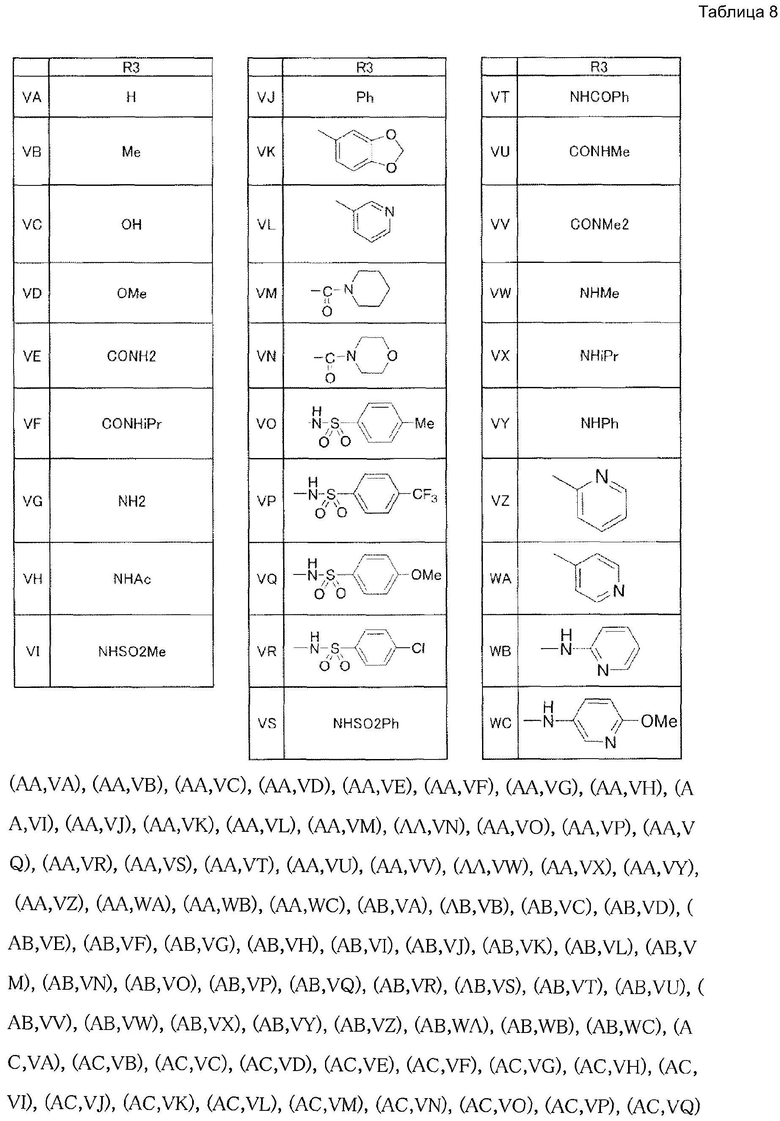
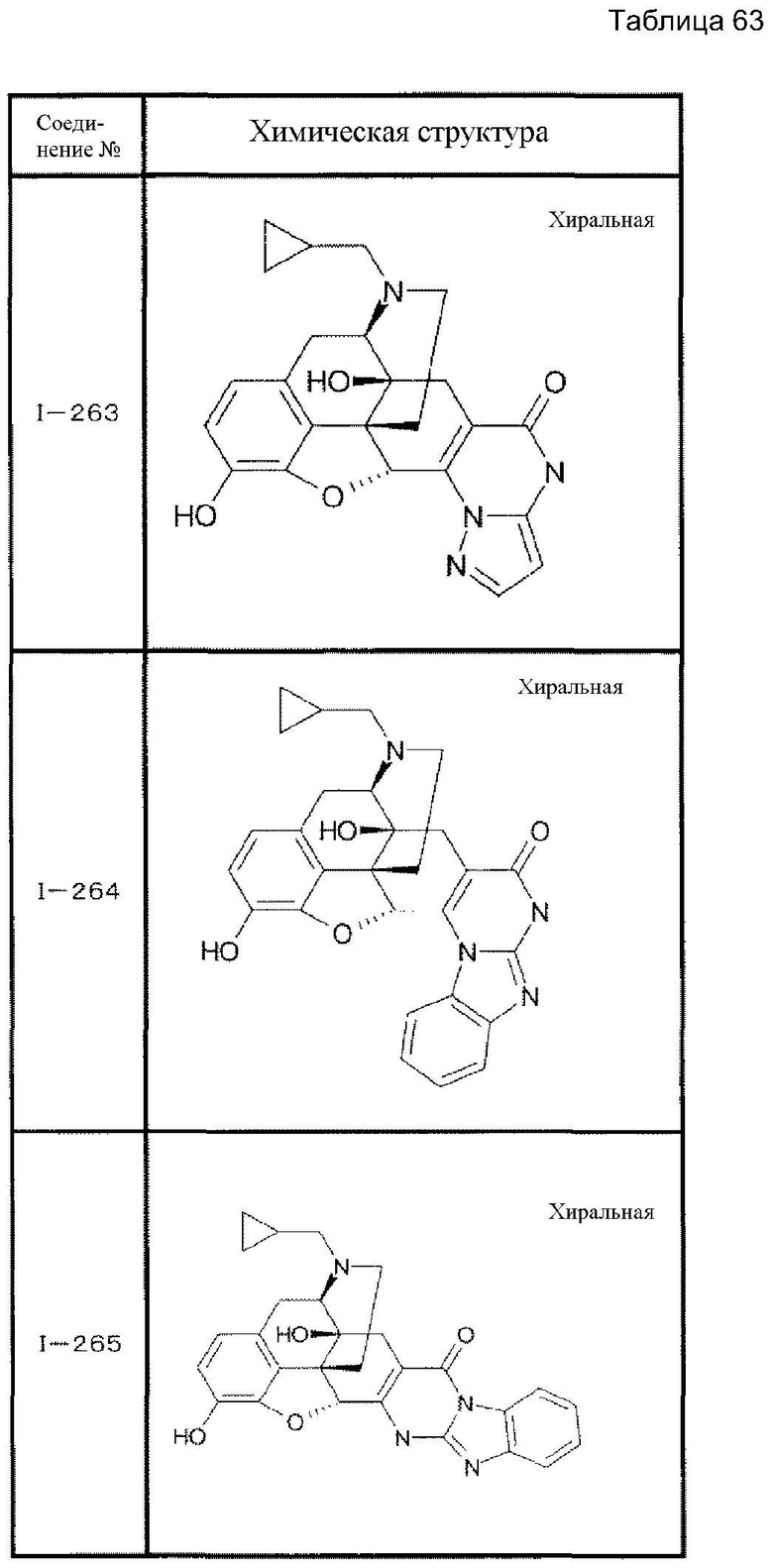
В соединении, представленном формулой (I), соединение, у которого R4 представляет собой водород, R5 представляет собой циклопропилметил, комбинация NR1R2 и R3 (NR1R2, R3) является следующей (см. табл 1-8 в конце описания).
Применяемая здесь фраза «тошнота, рвота и/или запор» включает тошноту, рвоту и/или запор, которые вызваны приемом внутрь соединения, обладающего агонистической активностью для опиоидного рецептора (особенно, опиоидного рецептора). В частности, примеры «соединения, обладающего агонистической активностью для опиоидного рецептора», включают морфин, оксикодон, фентанил, метадон, кодеин, дигидрокодеин, гидроморфон, леворфанол, меперидин, пропоксифен, декстропропоксифен, трамадол и их фармацевтически приемлемые соли или сольваты. В частности, когда соединением является морфин, оксикодон или его фармацевтически приемлемая соль или сольват, настоящее соединение является особенно эффективным.
Влияние настоящего изобретения на тошноту или рвоту можно подтвердить, например, следующим испытанием.
Спустя тридцать минут после проглатывания пищи африканскому хорьку вводят каждое испытуемое соединение. Испытуемое соединение растворяют в 5% ксилите и вводят в количестве 5 мг/кг. Спустя тридцать минут после введения испытуемого соединения подкожно вводят 0,6 мг/кг морфина и симптомы рвоты наблюдают обычно до 30-ти минут после введения морфина.
Для каждого из типа тошноты (периодическое сократительное движение абдоминальной части и экскреция пищевого вещества, проявляющаяся в виде рвоты, или подобное поведение) отмечают время появления рвоты, латентное время (время от введения морфина до начального появления симптома рвоты) и время длительности (время от начала рвоты до конца рвоты).
Кроме того, влияние настоящего соединения на констипацию можно подтвердить, например, следующим испытанием.
1) Получение корма для испытания (с красителем)
С применением 0,% масс./об. водного раствора синего Evans получают 2,5% масс./об. раствор соли карбоксиметилцеллюлозы и его применяют в качестве корма для испытания.
2) Животное
Можно применять, например, самцов крыс Wistar (возраст 6-7 недель). Животных выдерживают в голодном состоянии в течение приблизительно 20 или более часов до начала испытания, воду дают в количестве, сколько требуется ее животным.
3) Испытуемое соединение и среда
Испытуемое соединение растворяют в растворителе (DMAA/солютол/5% меглумин = 15/15/70).
DMAA: N,N-диметилацетамид,
солютол (зарегистрированный товарный знак) HS15,
меглумин: D-(-)-N-метилглюкамин.
Гидрохлорид морфина растворяют в физиологическом солевом растворе.
Испытуемое соединение, растворитель и морфин, все, вводят в виде жидкости в количестве 2 мл/кг.
4) Метод
Испытуемое соединение в количестве 0,03, 0,1, 0,3, 1 или 3 мг/кг (для группы введения испытуемого соединения) или растворитель (для группы введения растворителя) вводят подкожно, и морфин в количестве 3 мг/кг вводят подкожно для всех групп спустя 75 минут. Контрольной группе подкожно вводят растворитель, и физиологический солевой раствор вводят спустя 75 минут.
Корм для испытания 2 мл/крысу перорально вводят через 30 минут после введения морфина. Через пятнадцать минут после введения корма для испытания (через 120 минут после введения испытуемого соединения) у крыс отделяют область от пищевода до илеоцекальной части около кардиального отверстия желудка. Измеряют расстояние от пилорической части желудка до илеоцекальной части (полная длина тонкой кишки) и расстояние до достижения красителем фронтальной части (расстояние, которое проходит краситель).
5) Обработка данных
Степень переноса (%) = (расстояние, которое проходит краситель (см))/полная длина тонкой кишки (см) × 100.
М.Р.Е. (%) = {(степень переноса тонкой кишкой (%) группы введения каждого индивидуального испытуемого соединения - средняя степень переноса тонкой кишкой (%) группы введения растворителя)/(средняя степень переноса тонкой кишкой (%) контрольной группы - средняя степень переноса тонкой кишкой (%) группы введения растворителя)} × 100.
Величину ED50 вычисляют реверсной оценкой программы SAS регрессии с применением %МРЕ и допущением того, что величиной контрольной группы является 100%.
Настоящее соединение обладает антагонистической активностью для опиоидного рецептора (особенно опиоидных рецепторов δ и µ). Поэтому настоящее соединение является эффективным при лечении и/или профилактике нарушения прохода через пищеварительный тракт, которое имеет место из-за такой причины, как острая диспепсия, алкогольное опьянение, пищевое отравление, простуда, язва желудка, язва двенадцатиперстной кишки, рак желудка, непроходимость кишечника, аппендицит, перитонит, желчнокаменная болезнь, гепатит, воспаление печени, энцефалит, менингит, повышенное давление головного мозга, травма головы, укачивание, рвота при беременности, побочное действие вследствие химиотерапии, побочное действие вследствие лучевой терапии, побочное действие вследствие лечения противораковым агентом, давление-стеноз пищеварительного тракта и срастание пищеварительного тракта после операции, при лечении и/или профилактике тошноты и рвоты, которые имеют место из-за такой причины, как повышение давления в головном мозге вследствие опухоли головного мозга, кровотечения в головном мозге, менингита, радиационного облучения мозга, и при лечении и/или профилактике острой констипации, вызванной такой причиной, как непроходимость кишечника, язва двенадцатиперстной кишки или аппендицит, релаксирующей констипации, вызванной такой причиной, как нервное нарушение, недостаточное питание, общая слабость, дефицит витаминов, анемия, снижение чувствительности или недостаточность механической стимуляции, или конвульсивной констипации, вызванной такой причиной, как стресс, помимо тошноты, рвоты и констипации, вызванных соединением, обладающим агонистической активностью для опиоидного рецептора.
Поскольку настоящее соединение имеет слабую доставку в головной мозг, оно сильно облегчает побочное действие, такое как тошнота, рвота, констипация и тому подобное, вызванное агонистической активностью для опиоидного рецептора, почти без ингибирования аналгезирующей активности соединения, обладающего агонистической активностью для опиоидного рецептора, которое вводят пациенту с заболеванием, сопровождаемым болью (например, раковой болью, болью вследствие костного прохождения, нервного напряжения, повышенного внутричерепного давления, инфильтрации через мягкие ткани, болью вследствие запора или спазм мышцы, болью внутреннего органа, мышцы, фасции, талии или периферической части плечевого сустава, хронической болью после операции, СПИДа и т.д.). Помимо этого, настоящее соединение обладает явной антагонистической активностью в отношении опиоидного рецептора и имеет также преимущество в вопросе безопасности, заключающееся в том, что, поскольку ингибирующая активность для каналов hERG является низкой, не имеется сердечной токсичности и так далее. Кроме того, настоящее соединение имеет также подходящую характеристику динамик в организме, такую как высокая пероральная абсорбирующая способность, высокая стабильность в плазме человека, высокая биологическая доступность и тому подобное, и является очень эффективным в качестве лекарственного средства.
Когда настоящее соединение вводят против тошноты, рвоты и констипации, вызванной соединением, обладающим агонистической активностью для опиоидного рецептора, его введение можно проводить до, после или одновременно с введением соединения, имеющего агонистическую активность для опиоидного рецептора. Интервал времени между введениями этих двух типов лекарственных средств конкретно не ограничивают. Например, когда настоящее соединение вводят после введения соединения, имеющего агонистическую активность для опиоидного рецептора, если введение проводят сразу или через приблизительно 3 дней, предпочтительно сразу или через приблизительно 1 день после введения соединения, имеющего агонистическую активность для опиоидного рецептора, настоящее соединение действует более эффективно. Кроме того, когда настоящее соединение вводят перед введением соединения, имеющего агонистическую активность для опиоидного рецептора, если введение проводят непосредственно перед введением или приблизительно за 1 день, предпочтительно непосредственно перед введением или приблизительно за 12 часов до введения соединения, имеющего агонистическую активность для опиоидного рецептора, настоящее соединение действует более эффективно.
Когда настоящее соединение вводят в качестве агента для лечения и/или профилактики тошноты, рвоты и/или констипации, его можно применять одновременно с другим агентом для лечения и/или профилактики тошноты, рвоты и/или констипации. Например, данный агент можно вводить одновременно с гидрохлоридом ондансетрона, кортикальным стероидом надпочечников (метилпреднизолоном, преднизолоном, дексаметазоном и т.д.), прохлорперазином, галогенперидолом, тимипероном, перфеназином, метоклопрамидом, домперидоном, скополамином, гидрохлоридом хлорпромазина, дроперидолом, стимулирующим слабительным средством (сеннозидом, пикосульфатом натрия и т.д.), осмотическим слабительным средством (лактулозой и т.д.) или слабительным средством в виде соли (оксидом магния и т.д.).
В альтернативном случае можно вводить сочетание настоящего соединения и соединения, обладающего агонистической активностью для опиоидного рецептора, или сочетание настоящего соединения и другого агента для лечения и/или профилактики тошноты, рвоты и/или констипации.
Когда настоящее соединение вводят человеку, его можно вводить перорально в виде порошков, гранул, таблеток, капсул, пилюль, растворов или тому подобного или парентерально в виде инъекций, суппозиториев, чрескожных абсорбируемых агентов, абсорбируемых агентов или тому подобного. Предпочтительными являются пероральные агенты.
Кроме того, настоящее соединение можно изготовить в виде фармацевтических препаратов добавлением фармацевтических добавок, таких как эксципиенты, связывающие вещества, смачивающие агенты, дезинтегрирующие агенты, смазывающие агенты и тому подобное, которые являются подходящими для таких препаратов, и эффективного количества настоящего соединения.
Настоящее соединение можно изготовить в виде лекарственных смесей, в которых присутствует соединение, обладающее агонистической активностью для опиоидного рецептора, и/или другой агент для лечения и/или профилактики тошноты, рвоты и/или констипации и, если необходимо, различные фармацевтические добавки.
Дозу изменяют в зависимости от состояния заболевания, пути введения и возраста и массы пациента, она обычно бывает 0,1 мкг-1 г/день, предпочтительно 0,01-200 мг/день при пероральном введении взрослому человеку и обычно 0,1 мкг-10 г/день, предпочтительно 0,1-2 г/день при парентеральном введении.
Нижеследующие примеры и примеры испытаний иллюстрируют настоящее изобретение более подробно, но настоящее изобретение не ограничивается этими примерами.
ПРИМЕР 1
Получение соединения (I-4)
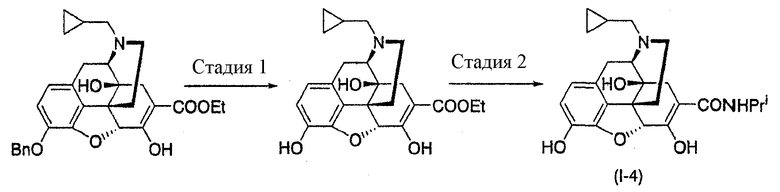 ,
,
где Bn представляет собой бензил, Et представляет собой этил, и Pri представляет собой изопропил.
Первая стадия - 7-Этоксикарбонилналтрексон
К суспензии 3-О-бензил-7-этоксикарбонилналтрексона, описанного в непатентной ссылке 2, (11,16 г, 22,15 ммоль) в этилацетате (50 мл) и метаноле (50 мл) добавляют гидроксид палладия (катализатор Перлмана) (1,2 г) и смесь энергично перемешивают в течение 2 часов в атмосфере водорода. После отделения катализатора фильтрованием фильтрат концентрируют и остаток кристаллизуют из этилацетата и гексана, получая при этом 8,96 г (92%) указанного в заголовке соединения в виде бесцветных кристаллов.
ЯМР (300 МГц, CDCl3)
δ 0,14-0,17 (м, 2Н), 0,55-0,58 (м, 2Н), 0,86 (м, 1Н), 1,23-1,29 (м, 3Н), 1,67 (д, 1Н, J=9,6 Гц), 2,02 (дд, 1Н, J=1,2, 16,2 Гц), 2,20-2,79 (м, 8Н), 3,08 (д, 1Н, J=18,6 Гц), 3,24 (ушир., 1Н), 4,12-4,20 (м, 2Н), 4,96 (с, 1Н), 5,17 (ушир., 1Н), 6,59 (д, 1Н, J=8,1 Гц), 6,72 (д, 1Н, J=8,1 Гц), 12,12 (с, 1Н).
Элементный анализ (С23Н27NO6 • 0,2 Н2О).
Вычисленная величина С, 66,24; Н, 6,62; N, 3,36.
Найденная величина С, 66,29; Н, 6,50; N, 3,45.
Вторая стадия - 7-Изопропиламинокарбонилналтрексон
Раствор 7-этоксикарбонилналтрексона, полученного в первой стадии (200 мг, 0,484 ммоль), изопропиламина (0,412 мл, 4,84 ммоль) и триэтиламина (0,202 мл, 1,45 ммоль) в 2-метоксиэтаноле (1,5 мл) перемешивают при 180°С в течение 45 минут при облучении микроволнами. После охлаждения до комнатной температуры к реакционной смеси добавляют 7 мл 5 моль/л хлористоводородной кислоты и перемешивание продолжают при 70°С в течение 20 минут. После охлаждения реакционной смеси величину рН регулируют до 8,5 водным аммиаком с последующей экстракцией этилацетатом. Органический слой промывают водой и сушат, и растворитель выпаривают. Остаток очищают колоночной хроматографией на силикагеле (хлороформ:метанол = 99:1-94:6), получая при этом 140 мг указанного в заголовке соединения с выходом 68%.
ЯМР (300 МГц, d6-ДМСО)
δ 0,12-0,15 (м, 2Н), 0,44-0,53 (м, 2Н), 0,83 (м, 1Н), 1,02 (д, 3Н, J=6,6 Гц), 1,08 (д, 3Н, J=6,6 Гц), 1,41 (д, 1Н, J=11,4 Гц), 1,85 (д, 1Н, J=15,6 Гц), 2,04-2,62 (м, 8Н), 3,04 (д, 1Н, J=18,6 Гц), 3,24 (м, 1Н), 3,96 (м, 1Н), 4,71 (с, 1Н), 4,74 (с, 1Н), 6,51 (д, 1Н, J=8,4 Гц), 6,56 (д, 1Н, J=8,4 Гц), 7,40 (ушир. д, 1Н, J=7,2 Гц), 9,16 (с, 1Н), 14,50 (с, 1Н).
Элементный анализ (С24Н30N2O5 • 0,2 Н2О).
Вычисленная величина С, 67,02; Н, 7,12; N, 6,51.
Найденная величина С, 67,02; Н, 7,20; N, 6,49.
ПРИМЕР 2
Получение соединения (I-44)
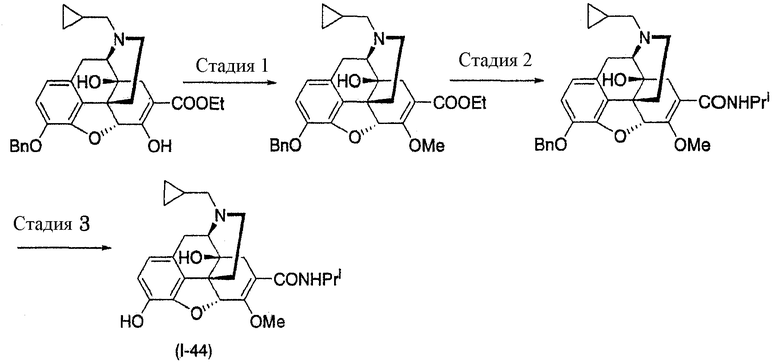 ,
,
где Bn представляет собой бензил, Ме представляет собой метил, Et представляет собой этил, и Pri представляет собой изопропил.
Первая стадия - 3-О-Бензил-7-этоксикарбонил-6-О-метилналтрексон
К раствору 3-О-бензил-7-этоксикарбонилналтрексона, описанного в непатентной ссылке 2, (504 мг, 1 ммоль) в тетрагидрофуране (10 мл) последовательно добавляют 1,1'-азодикарбонилпиперидин (379 мг, 1,5 ммоль), три-н-бутилфосфин (370 мкл, 1,5 ммоль) и метанол (41 мкл, 1 ммоль), и смесь перемешивают при комнатной температуре в течение 7 часов. Реакционный раствор концентрируют при пониженном давлении, и остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат), получая при этом указанное в заголовке соединение (421 мг, 81%) в виде бесцветного масла.
1Н ЯМР (CDCl3, δ м.д.): 0,10-0,20 (м, 2Н), 0,50-0,65 (м, 2Н), 0,88 (м, 1Н), 1,26 (т, J=6,6 Гц, 3Н), 1,67 (д, J=11,4 Гц, 1Н), 2,15-2,80 (м, 8Н), 3,00-3,30 (м, 2Н), 3,93 (с, 3Н), 4,05-4,20 (м, 2Н), 4,86 (ушир. с, 1Н), 5,15 (с, 2Н), 5,18 (ушир. с, 1Н), 6,57 (д, J=8,1 Гц, 1Н), 6,72 (д, J=8,1 Гц, 1Н), 7,28-7,45 (м, 5Н).
Вторая стадия - 3-О-Бензил-7-изопропиламинокарбонил-6-О-метилналтрексон
К смешанному раствору 3-О-бензил-7-этоксикарбонил-6-О-метилналтрексона, полученного в первой стадии (145 мг, 0,28 ммоль), в метаноле (6 мл) и диоксане (2 мл) добавляют 50% водный раствор гидроксида калия (2 мл), и смесь перемешивают при 50°С в течение 30 минут. Реакционную смесь охлаждают до комнатной температуры и рН регулируют до 4 0,5М водным раствором лимонной кислоты с последующей экстракцией этилацетатом. Органический слой последовательно промывают водой, насыщенным раствором соли, сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Образовавшийся кристаллический остаток, 3-О-бензил-7-карбокси-6-О-метилналтрексон, применяют в следующей реакции без очистки. К раствору указанного выше остатка в диметилформамиде (3 мл) последовательно добавляют гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (40 мг, 0,2 ммоль), 1-гидроксибензотриазол (27 мг, 0,2 ммоль) и изопропиламин (16 мкл, 0,182 ммоль), и смесь перемешивают при комнатной температуре в течение 15 часов. Реакционный раствор выливают в воду, и смесь экстрагируют этилацетатом, и органический слой промывают водой, сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (хлороформ/метанол = 9/1), получая при этом указанное в заголовке соединение (39 мг, 44%) в виде бесцветной пены.
1Н ЯМР (CDCl3, δ м.д.): 0,10-0,20 (м, 2Н), 0,50-0,65 (м, 2Н), 0,88 (м, 1Н), 1,13 (д, J=2,1 Гц, 3Н), 1,15 (д, J=1,8 Гц, 3Н), 1,58 (д, J=11,4 Гц, 1Н), 2,08-2,80 (м, 8Н), 2,99-3,30 (м, 2Н), 3,94 (с, 3Н), 4,06 (м, 1Н), 4,83 (ушир. с, 1Н), 5,14 (д, J=2,4 Гц, 2Н), 5,23 (ушир. с, 1Н), 6,56 (д, J=8,4 Гц, 1Н), 6,72 (д, J=8,4 Гц, 1Н), 7,28-7,45 (м, 6Н).
Третья стадия - 7-Изопропиламинокарбонил-6-О-метилналтрексон
К раствору 3-О-бензил-7-изопропиламинокарбонил-6-О-метилналтрексона, полученного во второй стадии (33 мг, 0,073 ммоль), в тетрагидрофуране (5 мл) добавляют гидроксид палладия (33 мг) и смесь перемешивают в течение 1 часа в атмосфере водорода. Реакционный раствор фильтруют через целит, и фильтрат концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (хлороформ/метанол = 9/1), получая при этом указанное в заголовке соединение (13 мг, 41%) в виде бесцветной пены.
1Н ЯМР (CDCl3, δ м.д.): 0,10-0,15 (м, 2Н), 0,50-0,70 (м, 2Н), 0,85 (м, 1Н), 1,12 (д, J=0,9 Гц, 3Н), 1,14 (д, J=0,9 Гц, 3Н), 1,66 (д, J=11,4 Гц, 1Н), 2,06-2,80 (м, 8Н), 3,00-3,30 (м, 2Н), 3,92 (с, 3Н), 4,05 (м, 1Н), 4,80 (ушир. с, 1Н), 5,26 (ушир. с, 1Н), 6,56 (д, J=8,1 Гц, 1Н), 6,69 (д, J=8,1 Гц, 1Н), 7,36 (д, J=7,8 Гц, 1Н).
ПРИМЕР 3
 ,
,
где Bn представляет собой бензил, Ме представляет собой метил, и Et представляет собой этил.
Первая стадия
Раствор соединения (1) (28,7 г, 57,0 ммоль) в тетрагидрофуране (250 мл) охлаждают до -10°С и к раствору добавляют 1,1'-азодикарбонилпиперидин (21,6 г, 85,5 моль), три-н-бутилфосфин (21,4 мл, 85,5 ммоль) и бензиловый спирт (6,50 мл, 62,7 ммоль), и смесь перемешивают при комнатной температуре в течение 6 часов и 45 минут. Реакционный раствор фильтруют, и фильтрат концентрируют при пониженном давлении, и остаток очищают колоночной хроматографией на силикагеле (хлороформ→хлороформ/метанол = 50/1), получая при этом с количественным выходом рассматриваемое соединение (2) (33,8 г) в виде светло-желтого масла.
1Н ЯМР (CDCl3, δ м.д.): 0,10-0,20 (м, 2Н), 0,50-0,65 (м, 2Н), 0,88 (м, 1Н), 0,94 (т, J=7,2 Гц, 3Н), 1,20-3,60 (м, 11Н), 4,14 (кв., J=7,2 Гц, 2Н), 5,10-5,35 (м, 5Н), 6,58 (д, J=8,1 Гц, 1Н), 6,74 (д, J=8,1 Гц, 1Н), 7,15-7,50 (м, 10Н).
Вторая стадия
К смешанному раствору соединения (2), полученного в первой стадии (33,8 г, 57,0 ммоль), в метаноле (130 мл) и диоксане (43 мл) добавляют 4Н водный раствор гидроксида калия (43 мл) и смесь перемешивают при 50°С в течение 14 часов и 35 минут. Реакционный раствор охлаждают до комнатной температуры и концентрируют при пониженном давлении, и рН остатка регулируют до 3-4 ледяной водой и 2Н хлористоводородной кислотой с последующей экстракцией смешанным раствором этилацетата и тетрагидрофурана. Органический слой промывают последовательно водой и насыщенным раствором соли, сушат безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток превращают в порошок простым эфиром, получая при этом рассматриваемое соединение (3) (24,8 г, 77%) в виде бесцветного порошка.
1Н ЯМР (ДМСО-d6, δ м.д.): 0,20-0,40 (м, 2Н), 0,50-0,65 (м, 2Н), 0,95 (м, 1Н), 1,30-3,60 (м, 11Н), 5,00-5,25 (м, 5Н), 5,39 (с, 1Н), 6,68 (д, J=8,1 Гц, 1Н), 6,88 (д, J=8,1 Гц, 1Н), 7,27-7,52 (м, 10Н).
Третья стадия
К раствору соединения (3), полученного во второй стадии (350 мг, 0,619 ммоль), в тетрагидрофуране (4 мл) последовательно добавляют гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (142 мг, 0,743 ммоль), 1-гидроксибензотриазол (100 мг, 0,743 ммоль), гидрохлорид метилового эфира диметилглицина (114 мг, 0,743 ммоль) и N-метилморфолин (82 мкл, 0,743 ммоль), и смесь перемешивают при комнатной температуре на протяжении ночи. Реакционный раствор выливают в ледяную воду и насыщенный водный раствор бикарбоната натрия с последующей экстракцией этилацетатом, и органический слой промывают насыщенным раствором соли, сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (хлороформ/метанол = 50/1), получая при этом рассматриваемое соединение (4) (300 мг, 73%) в виде светло-желтой пены.
1Н ЯМР (CDCl3, δ м.д.): 0,08-0,20 (м, 2Н), 0,50-0,60 (м, 2Н), 0,87 (м, 1Н), 1,13 (c, 3Н), 1,22 (с, 3Н), 1,55-2,80 (м, 11Н), 3,62 (с, 3Н), 4,85 (ушир. с, 1Н), 5,13-5,40 (м, 5Н), 6,58 (д, J=8,4 Гц, 1Н), 6,76 (д, J=8,4 Гц, 1Н), 7,26-7,48 (м, 10Н), 7,94 (с, 1Н).
Четвертая стадия
К раствору соединения (4), полученного в третьей стадии (290 мг, 0,436 ммоль), в метаноле (4 мл) добавляют гидроксид палладия (60 мг) с последующим перемешиванием в течение 3 часов в атмосфере водорода. Реакционный раствор фильтруют через целит, и фильтрат концентрируют при пониженном давлении. Остаток кристаллизуют с применением смеси гексан/этилацетат, получая при этом рассматриваемое соединение (I-49) (181 мг, 86%) в виде бесцветных кристаллов.
1Н ЯМР (ДМСО-d6, δ м.д.): 0,10-0,20 (м, 2Н), 0,40-0,57 (м, 2Н), 0,84 (м, 1Н), 1,33 (c, 3Н), 1,37 (с, 3Н), 1,40-3,40 (м, 11Н), 3,55 (с, 3Н), 4,72 (с, 1Н), 4,77 (ушир. с, 1Н), 6,52 (д, J=8,1 Гц, 1Н), 6,57 (д, J=8,1 Гц, 1Н), 7,68 (ушир. с, 1Н), 9,18 (ушир. с, 1Н), 13,78 (ушир. с, 1Н).
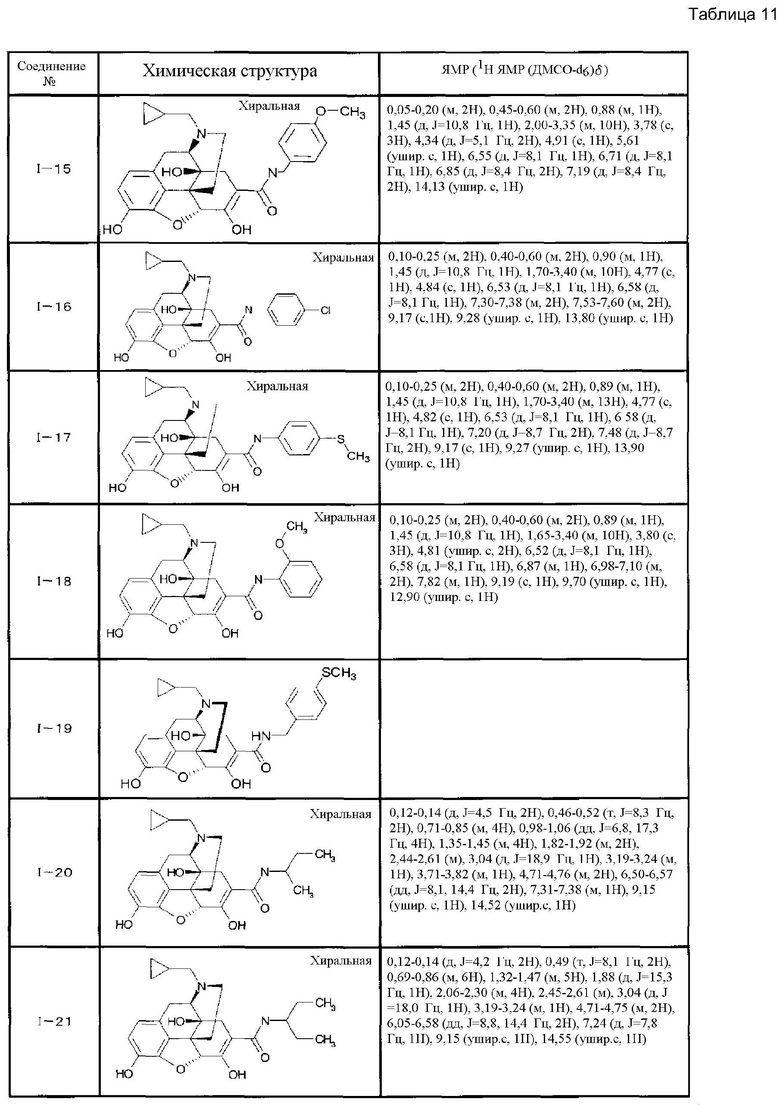
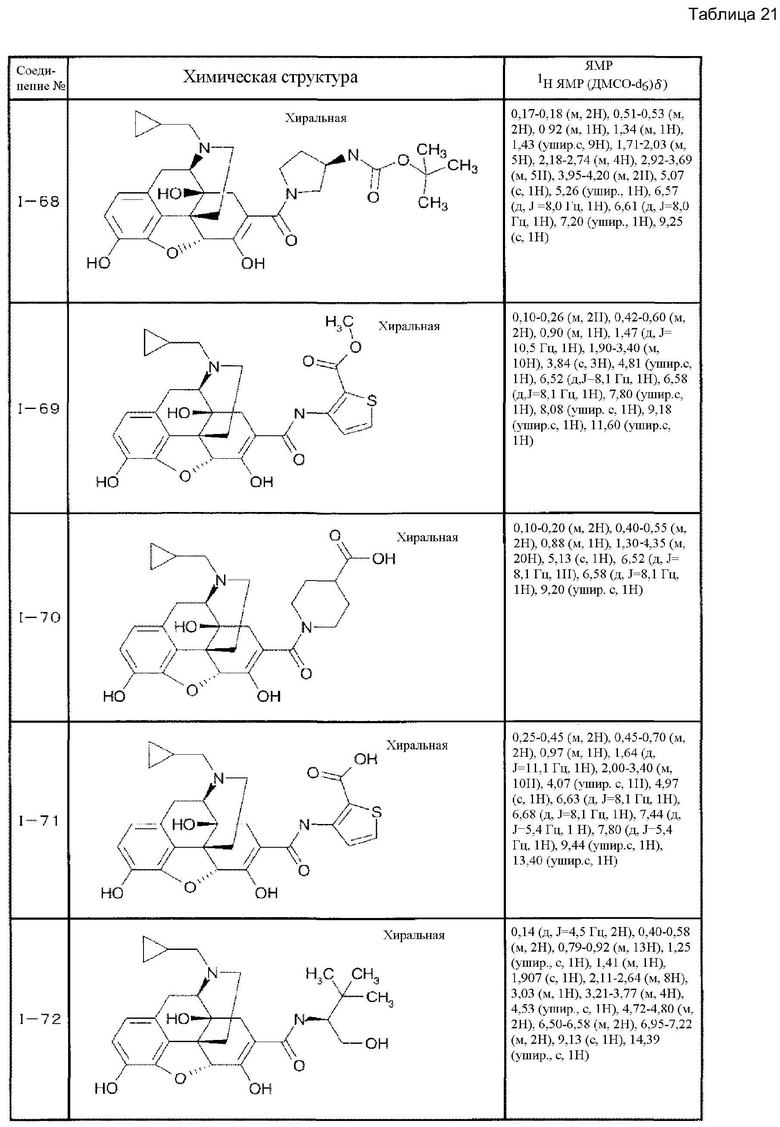
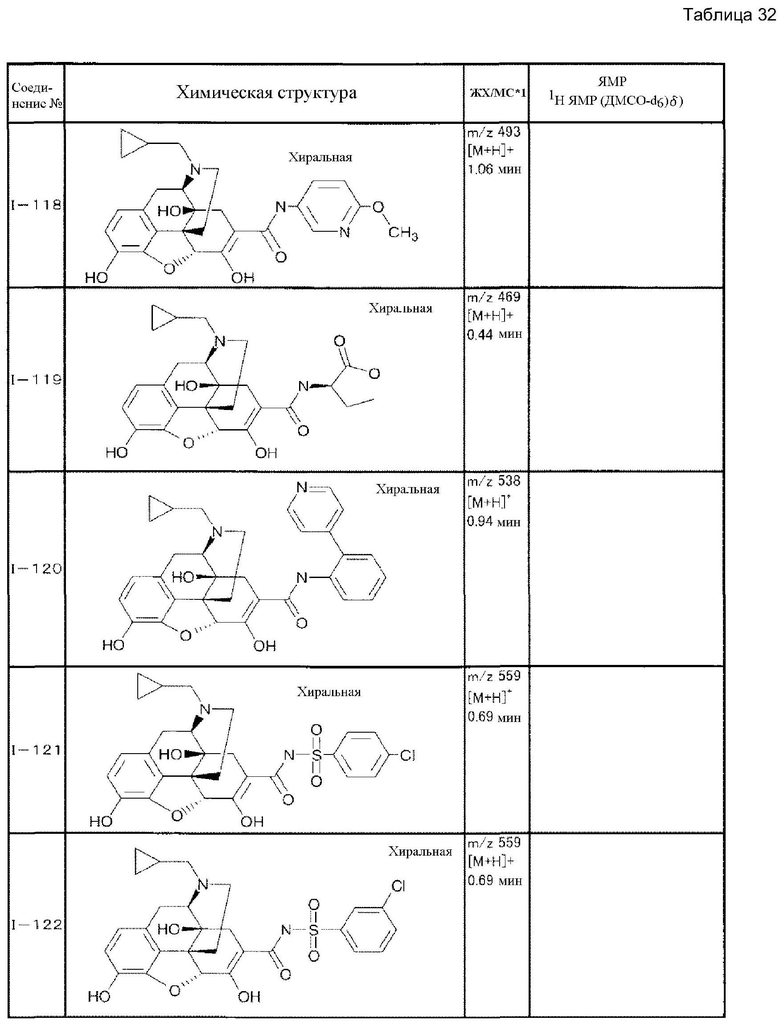
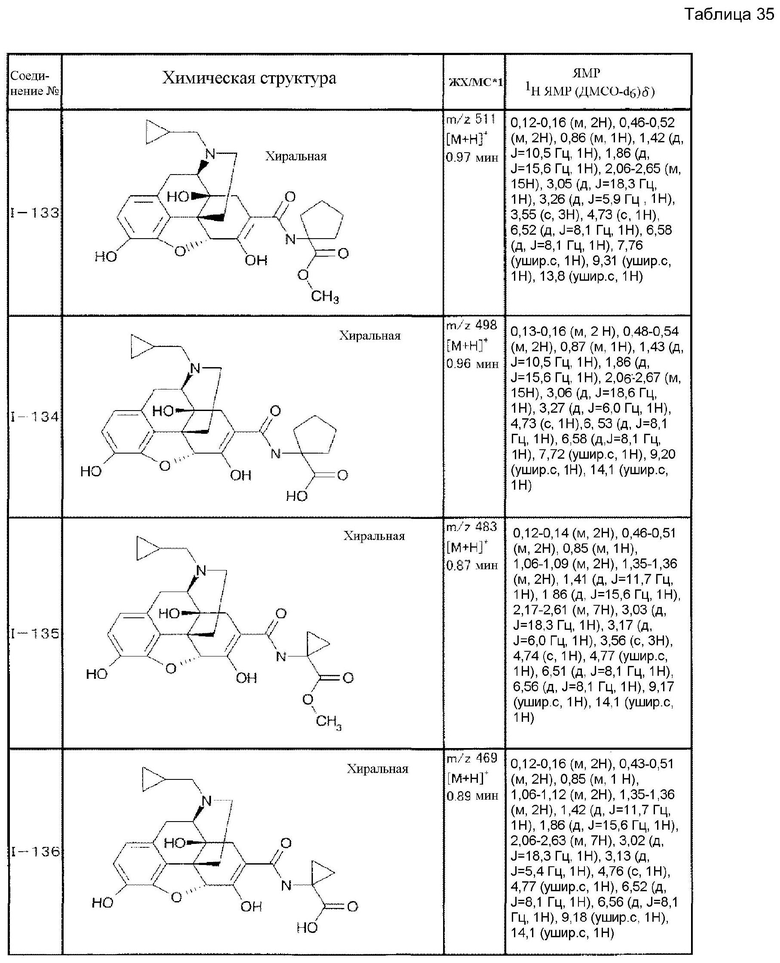
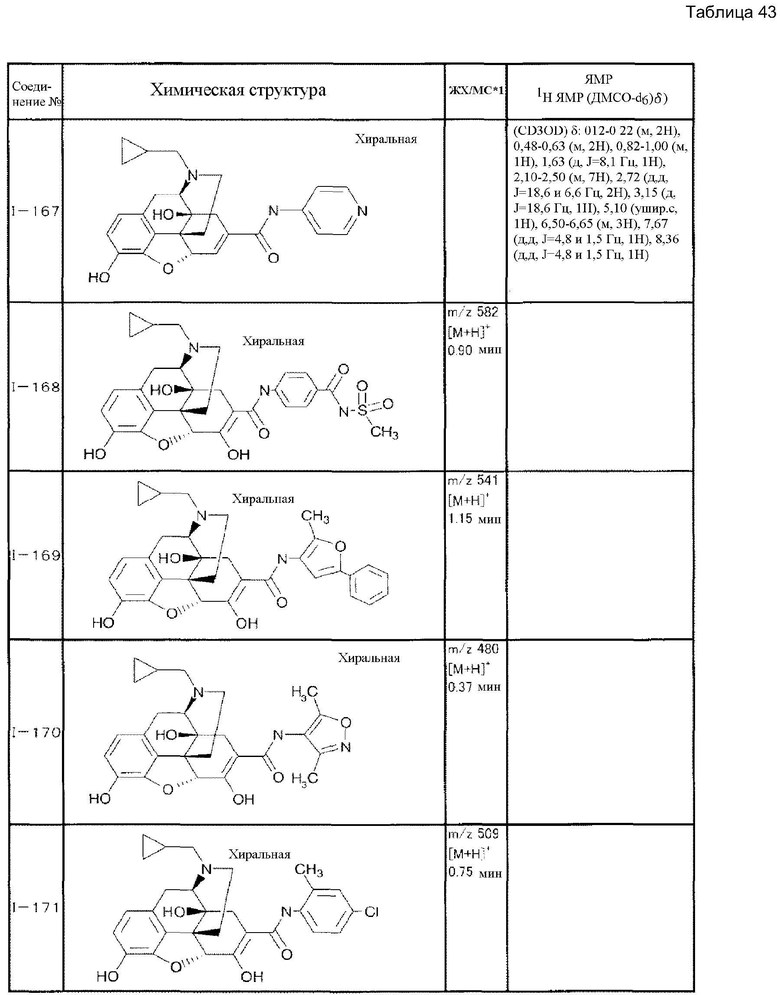
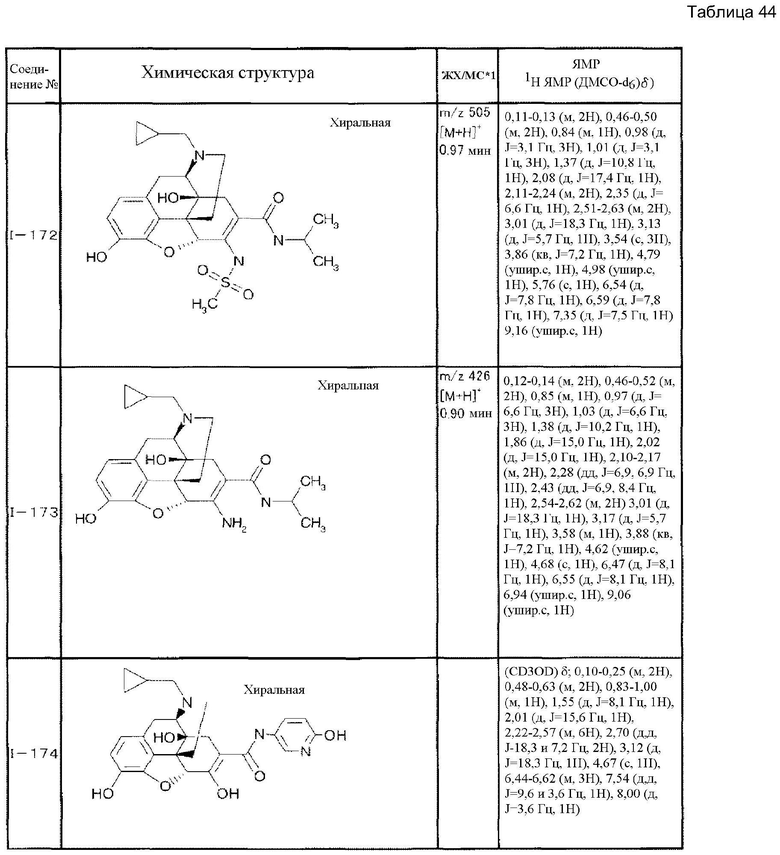
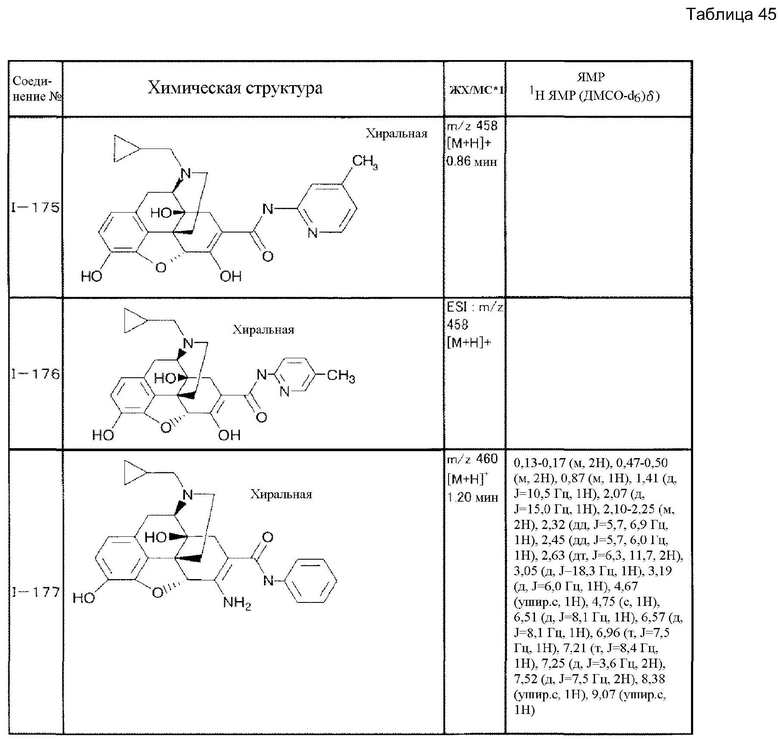
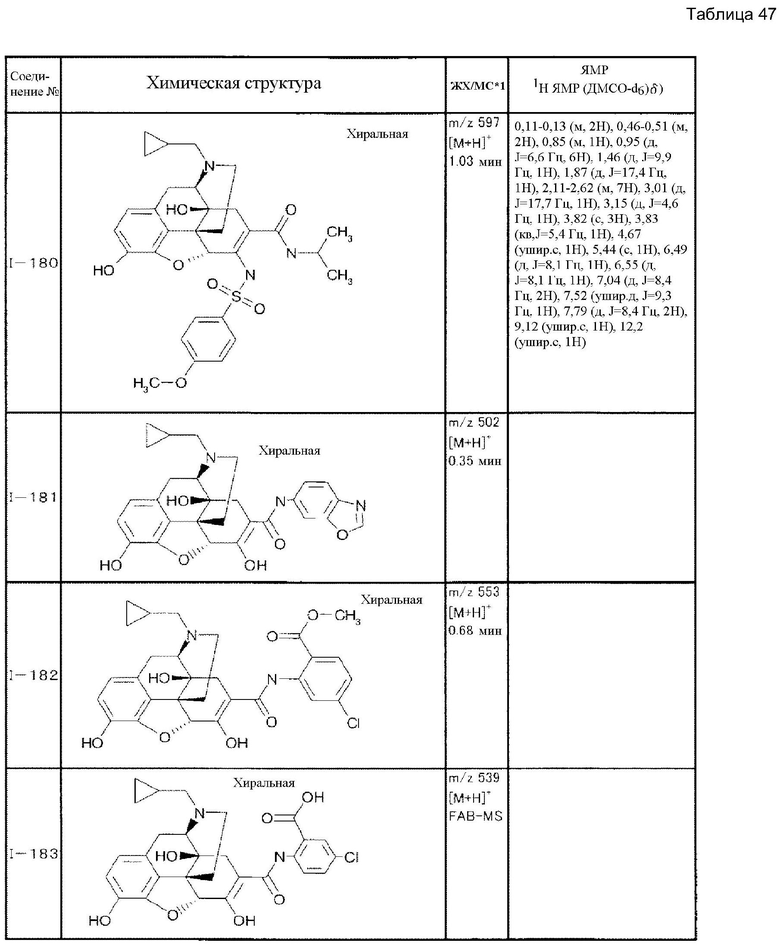
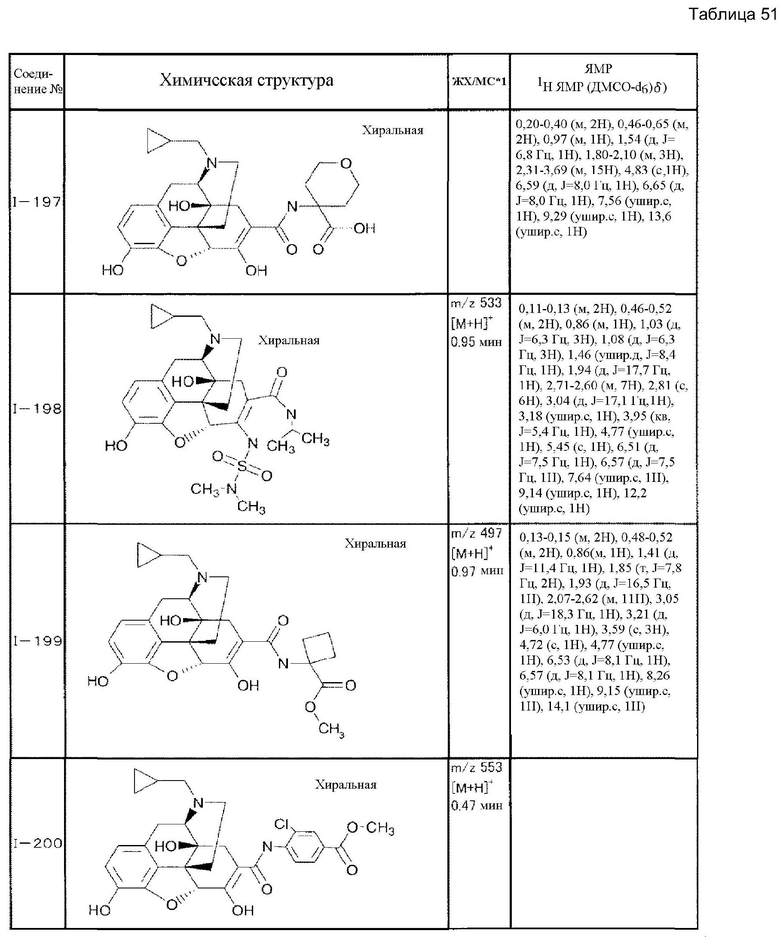
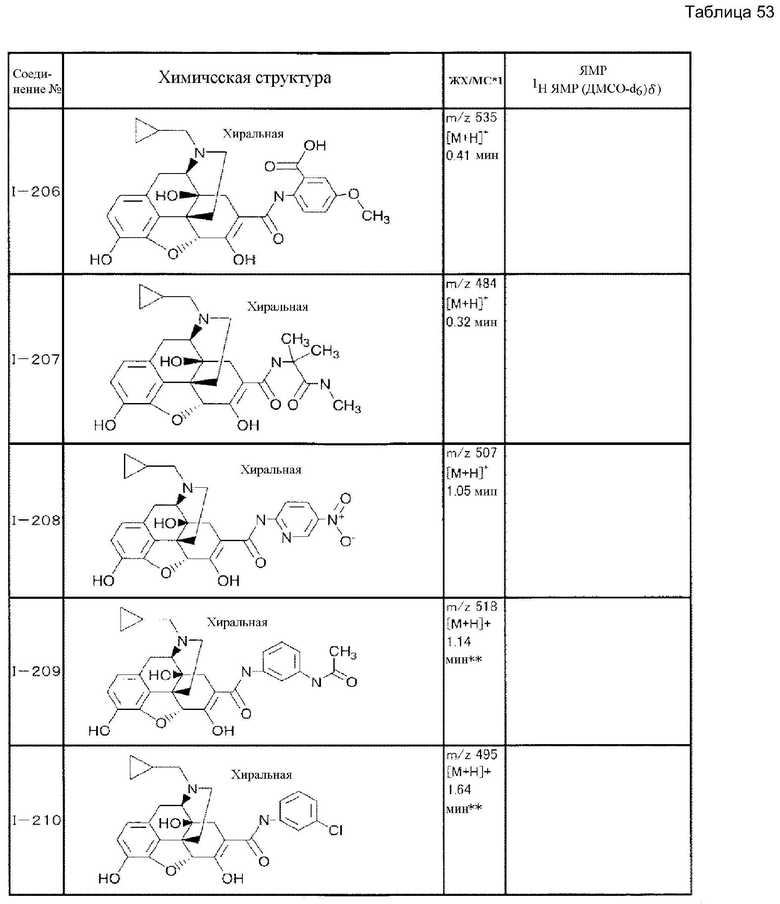
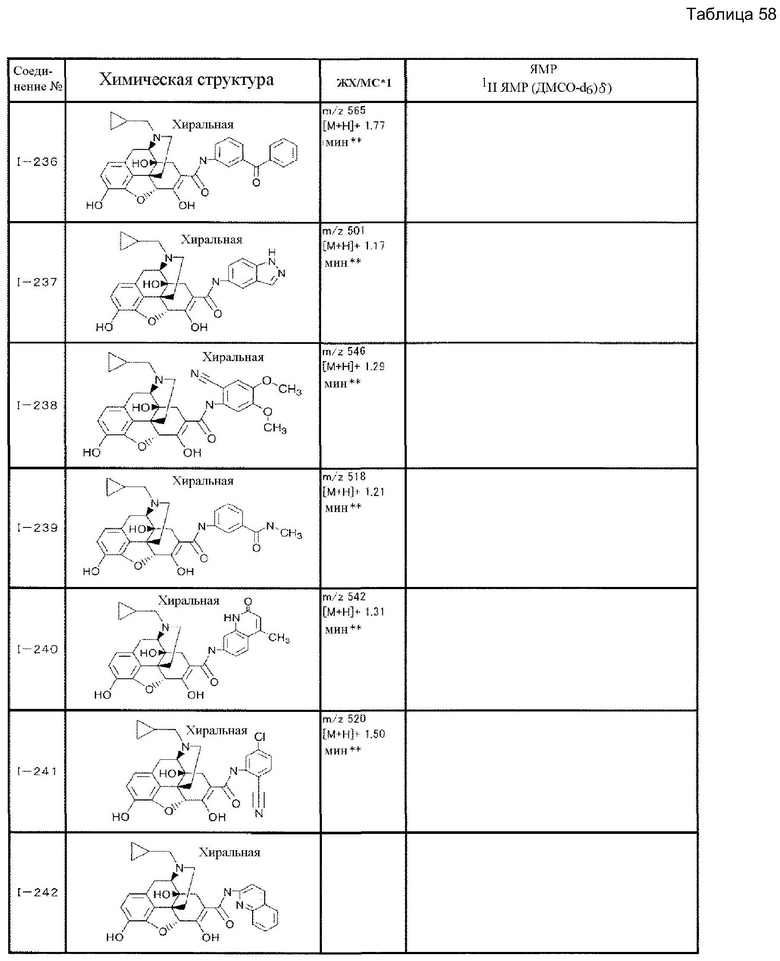
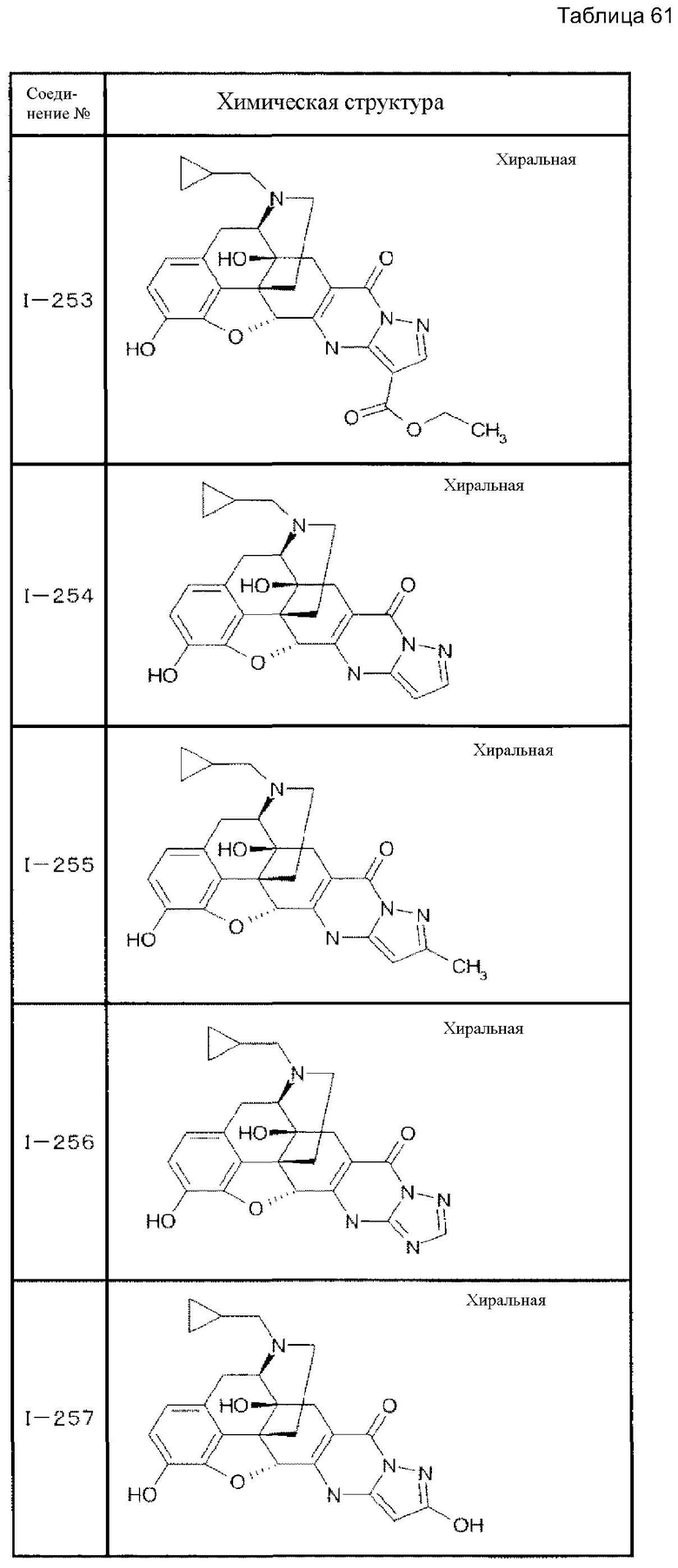
Согласно такой же методике можно синтезировать другие соединения (I). Структурные формулы и физические константы показаны ниже.
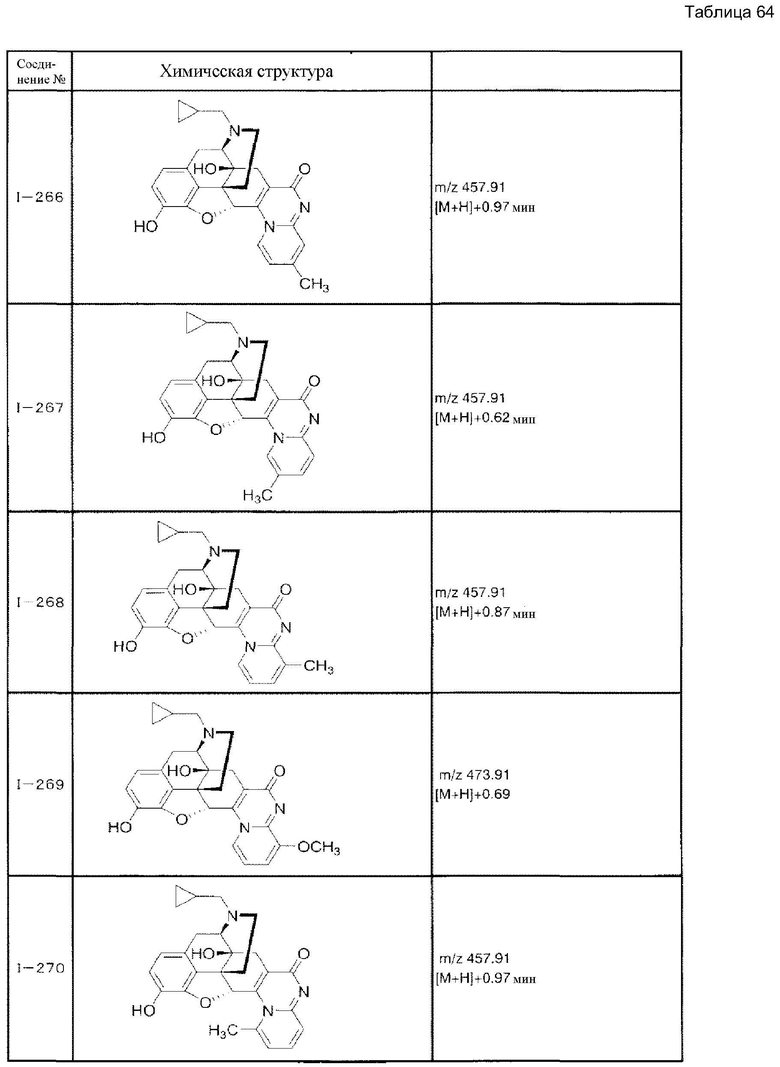
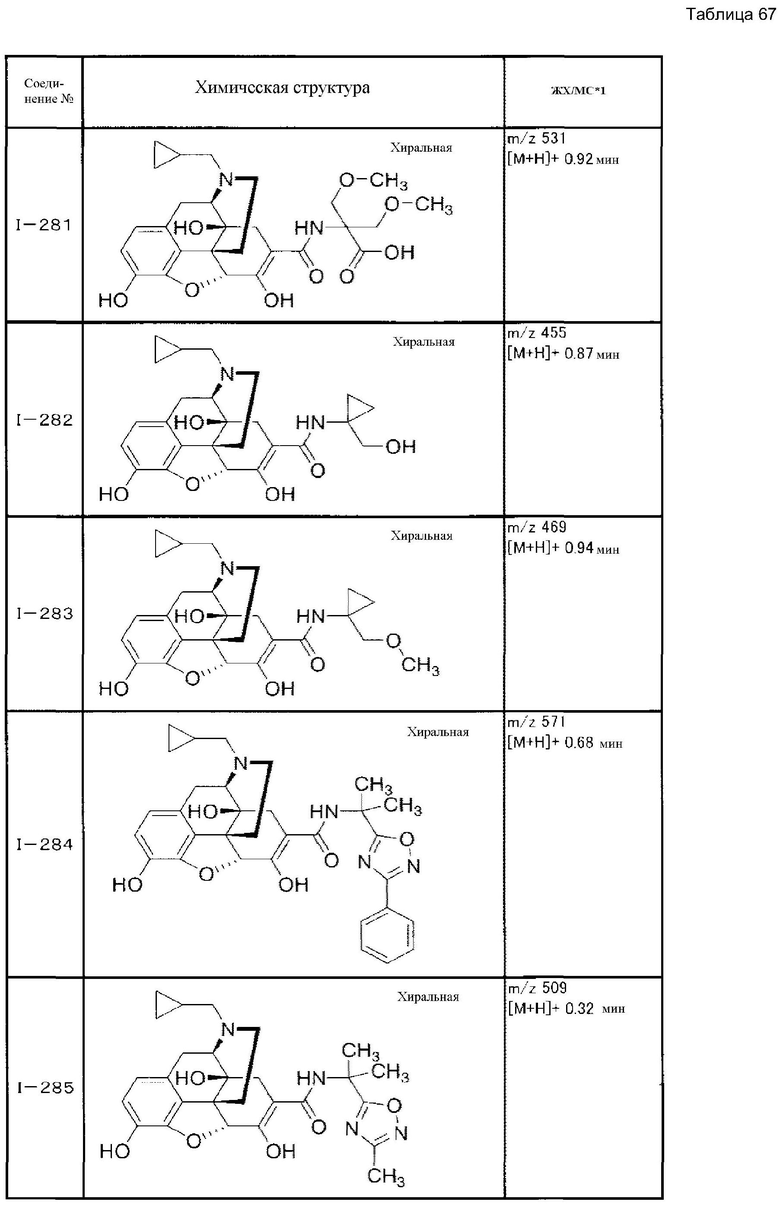
В таблицах Ме представляет собой метил, Et представляет собой этил, Pri представляет собой изопропил, и Ph представляет собой фенил (см. табл. 9-68).
Помимо этого, в таблицах
 означает
означает
(Условия измерения ЖХ/МС)*1:
Колонка: Chromolith Flash ROD PP-18e, 25Ч4,6 мм ID.
Скорость потока: 2 мл/мин.
УФ-детектор: 280 нм.
Система растворителей: [A]=Н2О, 0,05% НСООН, [B]=МеОН, 0,05% НСООН.
Градиент: 0 мин, 90% [A], 10% [B]; 0,2 мин, 90% [A], 10% [B]; 1,0 мин, 10% [A], 90% [B]; 1,80 мин, 10% [A], 90% [B].
Примечание: величины с символом ** относятся к указанным ниже условиям измерения:
колонка: Phenomenex Luna 5 мк, С18(2) 100А, размер 50Ч4,60 мм,
градиент: линейный градиент 10%-100% ацетонитрила в течение 3,0 мин при 3,0 мл/мин.
Пример 1 испытания. Анализ связывания опиоидного δ-рецептора
1) Метод приготовления мембранного образца для анализа связывания
Применяли головной мозг крыс (Slc:SD), который сохраняли при -80°С. К головному мозгу, который был взвешен, добавляли 20-кратное количество охлажденного льдом буфера 10 мМ Трис-HCl (рН 7,0), и смесь гомогенизировали (25000 об./мин, 30 секунд) гомогенизатором Histocolon (NITI-ON) и центрифугировали при 36600×g в течение 20 минут. К образовавшемуся осадку добавляли 15 мл того же буфера, и смесь обрабатывали аналогично гомогенизатором Histocolon и центрифугировали. Этот процесс промывания проводили два раза. После центрифугирования к образовавшемуся осадку добавляли 15 мл буфера 50 мМ Трис-HCl (рН 7,4), и смесь обрабатывали гомогенизатором Histocolon и, наконец, снова суспендировали в 10-кратном количестве того же буфера, и продукт применяли в качестве сырой мембранной фракции (Life Sci. 48, 111-116, 1991). Полученный мембранный образец замораживали и сохраняли при -80°С, и при проведении анализа образец быстро размораживали и разводили до концентрации приблизительно 900 мкг/мл буфером 50 мМ Трис-HCl (рН 7,4) после центрифугирования и обработки Histocolon, и применяли в эксперименте. Для измерения концентрации белка мембранного образца применяли набор для анализа белка Micro BCA (PIERCE).
2) Метод анализа связывания δ-рецептора и анализ данных
К раствору 10 мкл испытуемого соединения, разведенного на стадии 10-кратного разведения, добавляли 10 мкл конечного 3 нМ [3H]-DADLE (51,5 Ки/ммоль: Перкин-Элмер)) в качестве лиганда. В пробирку помещали 480 мкл мембранной фракции головного мозга крыс, к которой был добавлен 100 мМ хлорид холина, 3 мМ MnCl2 и 100 нМ DAMGO, и смесь инкубировали при 25°С в течение 2 часов. После инкубации смесь фильтровали с отсосом через фильтр Ватмана GF/C, который предварительно обрабатывали 0,5% полиэтиленимином, и промывали 2,5 мл охлажденного льдом буфера 10 мМ Трис-HCl (рН 7,4) четыре раза. После промывания фильтр переносили в минипробирку для сцинтилляционного счетчика, добавляли 5 мл сцинтиллятора (Cleasol I), пробирку выдерживали на протяжении ночи и радиоактивность измеряли в течение 3 минут сцинтилляционным счетчиком Tri-Carb 2200CA (PACKARD). Для общего связывания (общее связывание: TB) для анализа данных применяли ДМСО, и 20 мкМ леваллорфана применяли для неспецифического связывания (неспецифическое связывание: NB), и вычисляли величину Ki испытуемого соединения с применением величины KD (2,93 нМ), полученной заранее анализом по графикам Скетчерда.
Результаты показаны в таблице 69.
Таблица 69

Из приведенных выше результатов видно, что соединение (I) обладает аффинностью для опиоидного δ-рецептора.
Пример 2 испытания. Анализ связывания опиоидного µ-рецептора
1) Метод приготовления мембранного образца для анализа связывания
Применяли головной мозг крыс (Slc:SD), который сохраняли при -80°С. К головному мозгу, который был взвешен, добавляли 20-кратное количество охлажденного льдом буфера 10 мМ Трис-HCl (рН 7,0), и смесь гомогенизировали (25000 об/мин, 30 секунд) гомогенизатором Histocolon (NITI-ON) и центрифугировали при 36600×g в течение 20 минут. К образовавшемуся осадку добавляли 15 мл того же буфера, и смесь обрабатывали аналогично на гомогенизаторе Histocolon и центрифугировали. Этот процесс промывания проводили два раза. После центрифугирования к образовавшемуся осадку добавляли 15 мл буфера 50 мМ Трис-HCl (рН 7,4), смесь обрабатывали гомогенизатором Histocolon и, наконец, снова суспендировали в 10-кратном количестве того же буфера, и продукт применяли в качестве сырой мембранной фракции (Life Sci. 48, 111-116, 1991). Полученный мембранный образец замораживали и сохраняли при -80°С, и при проведении анализа образец быстро размораживали и разводили до концентрации приблизительно 900 мкг/мл буфером 50 мМ Трис-HCl (рН 7,4) после центрифугирования и обработки Histocolon, и применяли в эксперименте. Для измерения концентрации белка мембранного образца применяли набор для анализа белка Micro BCA (PIERCE).
2) Метод анализа связывания µ-рецептора и анализ данных
К раствору 10 мкл испытуемого соединения, разведенного на стадии 10-кратного разведения испытуемого соединения, добавляли 10 мкл конечного 2 нМ [3H]-DAMGO (51,5 Ки/ммоль: Перкин-Элмер) в качестве лиганда, далее в пробирку помещали 480 мкл мембранной фракции головного мозга крыс и смесь инкубировали при 25°С в течение 2 часов. После инкубации смесь фильтровали с отсосом через фильтр Ватмана GF/C, который предварительно обрабатывали 0,5% полиэтиленимином, и промывали 2,5 мл охлажденного льдом буфера 10 мМ Трис-HCl (рН 7,4) четыре раза. После промывания фильтр переносили в минипробирку для сцинтилляционного счетчика, добавляли 5 мл сцинтиллятора (Cleasol I), пробирку выдерживали на протяжении ночи и радиоактивность измеряли в течение 3 минут сцинтилляционным счетчиком Tri-Carb 2200CA (PACKARD). Для общего связывания (общее связывание: TB) для анализа данных применяли ДМСО, и 20 мкМ леваллорфана применяли для неспецифического связывания (неспецифическое связывание: NB), и вычисляли величину Ki испытуемого соединения с применением величины KD (1,72 нМ), полученную заранее анализом по графикам Скетчерда (Anal. Biochem. 107(1), 220-239, 1980).
Результаты показаны в таблице 70.
Таблица 70

Пример 3 испытания. Анализ переноса угольного порошка
1) Приготовление корма для испытания (с угольным порошком)
С применением 10% масс./об. водного раствора аравийской камеди получали содержащий 5% масс./об. активного угля раствор, который применяли в качестве корма для испытания.
2) Животное
Применяли самцов мышей (возраст 5-6 недель) линии ddY.
Животные голодали в течение приблизительно 20 или более часов до начала анализа, воду давали без ограничения.
3) Испытуемое соединение и среда
Испытуемое соединение растворяли в растворителе (DMAA/cолютол/5% меглумин = 15/15/70).
DMAA: N,N-диметилацетамид,
солютол: солютол (зарегистрированный товарный знак) HS15,
меглумин: D-(-)-N-метилглюкамин.
Гидрохлорид морфина растворяли в физиологическом солевом растворе. Испытуемое соединение, указанный выше растворитель и морфин, все, вводили в виде жидкости в количестве 10 мл/кг.
4) Метод анализа
Испытуемое соединение в количестве 3 мг/кг (для группы введения испытуемого соединения) или растворитель (для группы введения растворителя) вводили подкожно, и 3 мг/кг морфина вводили подкожно для всех групп спустя 15 минут. Контрольной группе подкожно вводили растворитель и спустя 15 минут вводили физиологический солевой раствор.
10 мл/кг корма для испытания перорально вводили через 15 минут после введения морфина. Через тридцать минут после введения корма для испытания (через 60 минут после введения испытуемого соединения) у всех крыс отделяли область от пищевода до илеоцекальной части около кардиального отверстия желудка. Измеряли расстояние от пилорической части желудка до илеоцекальной части (полная длина тонкой кишки) и расстояние до достижения угольным порошком фронтальной части (расстояние движения угольного порошка). Антагонистическую активность, направленную против активности морфина, ингибирующей перенос угольного порошка, вычисляли как МРЕ (%) с применением нижеследующего уравнения. Результаты показаны в таблице 71.
Степень переноса (%) = (расстояние, которое проходит угольный порошок)/полная длина тонкой кишки (см)) × 100
М.Р.Е. (%) = {(степень переноса тонкой кишкой (%) для группы введения каждого индивидуального испытуемого соединения - средняя степень переноса тонкой кишкой (%) для группы введения растворителя)/(средняя степень переноса тонкой кишкой (%) для контрольной группы - средняя степень переноса тонкой кишкой (%) для группы введения растворителя)} × 100.
Таблица 71

Пример 1 готовой препаративной формы
Получают гранулы, содержащие следующие ингредиенты.
Соединение, представленное формулой (I), и лактозу пропускают через сито 60 меш. Кукурузный крахмал пропускают через сито 120 меш. Эти компоненты смешивают мешалкой V-типа. К смешанному порошку добавляют водный раствор HPC-L (гидроксипропилцеллюлозы низкой вязкости), смесь замешивают, гранулируют (грануляция экструзией, диаметр пор 0,5-1 мм) и сушат. Образовавшиеся сухие гранулы пропускают через сито с применением вибрационного сита (12/60 меш), получая при этом требуемые гранулы.
Пример 2 готовой препаративной формы
Получают гранулы для заполнения капсулы, содержащие следующие ингредиенты.
Соединение, представленное формулой (I), и лактозу пропускают через сито 60 меш. Кукурузный крахмал пропускают через сито 120 меш. Эти компоненты смешивают, к смешанному порошку добавляют раствор HPC-L, вещества замешивают, гранулируют и сушат. Размер образовавшихся сухих гранул регулируют, и твердую желатиновую капсулу № 4 заполняют 150 мг полученных гранул.
Пример 3 готовой препаративной формы
Получают таблетку, содержащую следующие ингредиенты.
СМС-Na
15 мг
Соединение, представленное формулой (I), лактозу, микрокристаллическую целлюлозу, СМС-NA (натриевая соль карбоксиметилцеллюлозы) пропускают через сито 60 меш и смешивают. Смешанный порошок смешивают со стеаратом магния, получая при этом смешанный порошок для таблетирования. Указанный смешанный порошок прессуют с получением 150 мг таблетки.
Пример 4 готовой препаративной формы
Нижеследующие ингредиенты нагревают, смешивают и стерилизуют с получением инъецируемого препарата.
Промышленная применимость
Настоящим изобретением является агент, полезный для ослабления побочного действия, такого как тошнота, рвота и/или констипация.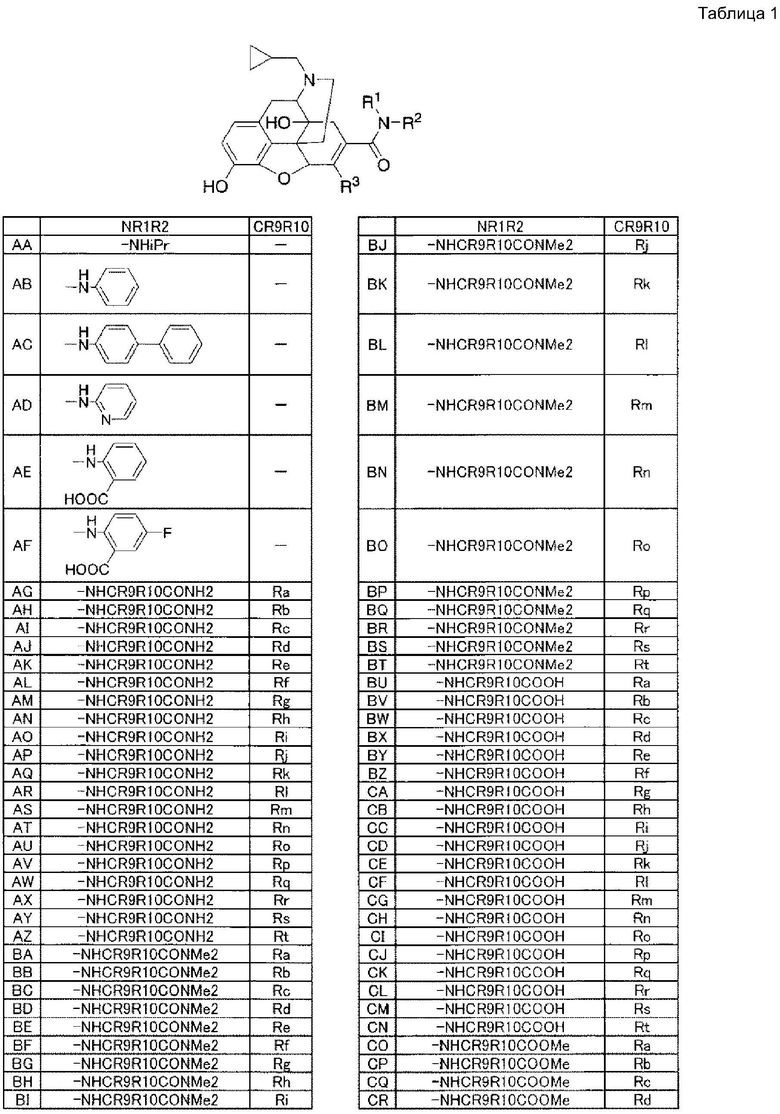



























































































| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛЫ ПРОИЗВОДНЫХ 6,7-НЕНАСЫЩЕННОГО-7-КАРБАМОИЛМОРФИНАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2643807C1 |
| КРИСТАЛЛЫ ПРОИЗВОДНЫХ 6,7-НЕНАСЫЩЕННОГО-7-КАРБАМОИЛМОРФИНАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2607084C2 |
| АНАЛОГИ БУПРЕНОРФИНА | 2009 |
|
RU2520222C2 |
| МОНОМЕРНЫЕ ПРОИЗВОДНЫЕ ГЛИКОПЕПТИДНОГО АНТИБИОТИКА | 2005 |
|
RU2424248C2 |
| СПОСОБЫ ЛЕЧЕНИЯ СОСТОЯНИЙ, ОБУСЛОВЛЕННЫХ p38 КИНАЗАМИ, И ПИРРОЛОТРИАЗИНОВЫЕ СОЕДИНЕНИЯ, ПРИМЕНИМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2001 |
|
RU2316556C2 |
| СОЕДИНЕНИЯ СПИРОПИРАЗОЛА, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ МОДУЛЯЦИИ ОПИОИДНОГО РЕЦЕПТОРА И СПОСОБ ЛЕЧЕНИЯ С ПРИМЕНЕНИЕМ ТАКИХ СОЕДИНЕНИЙ | 2002 |
|
RU2299883C2 |
| ПРИМЕНЕНИЕ МОДУЛЯТОРОВ РЕЦЕПТОРА S1P В ОФТАЛЬМОЛОГИИ | 2006 |
|
RU2497513C2 |
| ИСПОЛЬЗОВАНИЕ ИНГИБИТОРОВ PDE7 ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ ДВИЖЕНИЙ | 2010 |
|
RU2600869C2 |
| ЛЕЧЕНИЕ ЗАВИСИМОСТИ И РАССТРОЙСТВ ПОБУЖДЕНИЙ С ПРИМЕНЕНИЕМ ИНГИБИТОРОВ ФДЭ7 | 2013 |
|
RU2665134C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ, ВКЛЮЧАЮЩАЯ ИНГИБИТОРЫ SGLT И ИНГИБИТОРЫ DPP4 | 2009 |
|
RU2481106C2 |
Изобретение относится к новому соединению общей формулы (I):

где R1 и R2, каждый независимо, представляет собой водород, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный циклоалкил, необязательно замещенный арил и т.д., R3 представляет собой водород, гидрокси, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный низший алкокси и т.д., R4 представляет собой водород или низший алкил, R5 представляет собой водород, низший алкил, циклоалкил-низший алкил, или низший алкенил, или его фармацевтически приемлемая соль или сольват. Изобретение также относится к фармацевтической композиции на основе этих соединений и способу лечения и/или профилактики тошноты, рвоты и/или констипации. 7 н. и 6 з.п. ф-лы, 71 табл.
1. Соединение, представленное формулой (I)

где R1 и R2 каждый независимо представляет собой водород, необязательно замещенный низший алкил, необязательно замещенный низший алкилсульфонил, необязательно замещенный ацил, необязательно замещенный циклоалкил, необязательно замещенный арил, необязательно замещенная гетероциклическая группа, необязательно замещенный арилсульфонил или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют необязательно замещенный гетероцикл;
R3 представляет собой водород, гидрокси, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный низший алкокси, необязательно замещенный амино, необязательно замещенный карбамоил или необязательно замещенную гетероциклическую группу;
группа, представленная формулой:

может быть
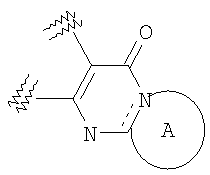
 или
или 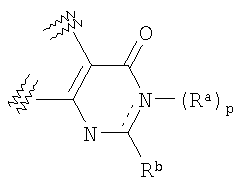
где кольцо А и кольцо В каждое независимо представляет собой необязательно замещенный азотсодержащий гетероцикл, необязательно содержащий дополнительный атом азота в кольце;
пунктирная линия означает присутствие или отсутствие связи;
когда пунктирная линия означает присутствие связи, р равно 0;
когда пунктирная линия означает отсутствие связи, р равно 1;
Ra представляет собой водород, необязательно замещенный низший алкил, необязательно замещенный низший алкенил
и Rb представляет собой водород или оксо;
R4 представляет собой водород или низший алкил;
R5 представляет собой водород, циклоалкил-низший алкил,
или его фармацевтически приемлемая соль или сольват.
2. Соединение по п.1, где R3 представляет собой гидрокси, или его фармацевтически приемлемая соль или сольват.
3. Соединение по п.1, где R3 представляет собой необязательно замещенный амино, или его фармацевтически приемлемая соль или сольват.
4. Соединение по любому из пп.1-3, где R1 представляет собой водород или низший алкил, R2 представляет собой необязательно замещенный низший алкил, необязательно замещенный фенил, необязательно замещенный циклоалкил или необязательно замещенную гетероциклическую группу и R5 представляет собой циклопропилметил,
или его фармацевтически приемлемая соль или сольват.
5. Соединение по п.1 или 2, где
R1 представляет собой водород;
R2 представляет собой низший алкил, необязательно замещенный гетероциклической группой, необязательно замещенной арилом или низшим алкокси; фенил, необязательно замещенный низшим алкилом или низшим алкокси; циклоалкил, замещенный низшим алкилкарбонилом, или гетероциклическую группу, замещенную низшим алкокси или арилом;
R3 представляет собой гидрокси;
R4 представляет собой водород и
R5 представляет собой циклопропилметил,
или его фармацевтически приемлемая соль или сольват.
6. Фармацевтическая композиция, обладающая антагонистической активностью для опиоидного рецептора, содержащая соединение по любому из пп.1-5, или его фармацевтически приемлемую соль, или сольват.
7. Композиция для лечения и/или профилактики тошноты, рвоты и/или констипации, содержащая соединение по любому из пп.1-5, или его фармацевтически приемлемую соль, или сольват.
8. Композиция для ослабления и/или профилактики побочного действия, вызванного соединением, обладающим агонистической активностью для опиоидного рецептора, содержащая соединение по любому из пп.1-5, или его фармацевтически приемлемую соль, или сольват.
9. Композиция по п.8, где побочным действием является тошнота, рвота и/или констипация.
10. Композиция по п.8 или 9, где соединением, обладающим агонистической активностью для опиоидного рецептора, является морфин, оксикодон, или его фармацевтически приемлемая, соль или сольват.
11. Применение соединения по любому из пп.1-6, или его фармацевтически приемлемой соли, или сольвата для получения фармацевтической композиции для лечения и/или профилактики тошноты, рвоты и/или констипации.
12. Способ лечения и/или профилактики тошноты, рвоты и/или констипации, включающий введение соединения по любому из пп.1-5, или его фармацевтически приемлемой соли, или сольвата.
13. Композиция для аналгезии, содержащая соединение, обладающее агонистической активностью для опиоидного рецептора, и эффективное количество соединения по любому из пп.1-5, или его фармацевтически приемлемой соли, или сольвата для ослабления и/или профилактики побочного действия, вызванного введением соединения, обладающего агонистической активностью для опиоидного рецептора.
| US 20010047005 A1, 29.11.2001 | |||
| WO 95130071 A2, 18.05.1995 | |||
| WO 2004007503 A1, 22.01.2004 | |||
| Способ получения производных бензоатных эфиров 3-оксиморфинанов | 1987 |
|
SU1508960A3 |
| RU 2004108210 A, 10.04.2005. | |||
Авторы
Даты
2010-11-10—Публикация
2006-05-25—Подача