Изобретение относится к области химии полимеров и медицины, а именно к способу получения тромборезистентных полимерных материалов, которые находят широкое применение в медицинской промышленности для изготовления контактирующих с кровью изделий, например, протезов кровеносных сосудов, деталей имплантируемых в живой организм искусственных органов, магистралей аппаратов искусственного кровообращения, емкостей для хранения и переливания крови и т.д.
Все применяемые в настоящее время в контакте с кровью материалы не являются истинно тромборезистентными. Контакт крови с любым чужеродным материалом, включая полимеры, приводит к немедленному ее свертыванию, что является естественной защитной реакцией организма. Положительные результаты имплантации некоторых полимерных материалов определяются либо относительно небольшими размерами имплантата (сердечные клапаны), либо тем, что в условиях интенсивного кровотока продукты тромбообразования постоянно смываются с поверхности полимера и гидролизуются фибринолитическими ферментами крови. В обоих случаях защитные системы организма в состоянии справиться с тромбоэмболией.
Наиболее распространенным подходом к повышению тромборезистентности полимеров является модификация их поверхности биологически активными соединениями, воздействующими на ту или иную стадию процесса тромбообразования. В качестве биологически активного соединения наибольшее распространение получил гепарин - гетерополисахарид с молекулярной массой 10-30 тысяч, основная функция которого заключается в предотвращении свертывания крови. Гепарин нейтрализует активность тромбина - фермента крови, ответственного за образование тромба, путем катализа реакции тромбина с присутствующим в крови антитромбином III.
Впервые для повышения тромборезистентности полимерных материалов гепарин был использован в работе [V.L.Gott, J.D.Whiffen, R.S.Dutton, Heparin bonding on colloidal graphite surfaces // Science. 1963. V.142. №7. P.1297-1298]. На поверхность полимера сначала наносят слой графита, поверхность обрабатывают раствором бензалконийхлорида и затем раствором гепарина. Содержание гепарина на поверхности полимера составляет 0,002 мг/см2 поверхности.
Недостатком этого способа является невысокая гемосовместимость полимера, обусловленная низким содержанием гепарина, а также низкая устойчивость гепаринсодержащих полимеров к действию компонентов крови. После 24 часов пребывания в крови содержание гепарина на поверхности полимера уменьшается на 77%. При этом полностью отсутствует возможность повторной гепаринизации полимера.
Известен способ получения тромборезистентных полимерных материалов путем радиационной привитой сополимеризации на поверхность полимерного материала ненасыщенного производного гепарина или его смеси с гидрофильным мономером [авторское свидетельство СССР №1120679, C08F 291/00, 1979]. В качестве ненасыщенного производного гепарина используют гепарин, ацилированный хлорангидридом акриловой или метакриловой кислоты, а в качестве ненасыщенного мономера - растворимые в воде акриламид, винилпирролидон, гидроксиэтилметакрилат и т.п. Относительное время свертывания крови, равное отношению времени свертывания крови на поверхности полимера к времени свертывания крови на поверхности стекла, составляет 12,0 для гепаринсодержащего полимера и 1,7 для исходного полимера. Этот показатель не изменяется при хранении полимеров в физиологическом растворе (0,9%-ный раствор NaCl) в течение 8 месяцев.
Недостатком этого способа является низкая тромборезистентность полимера (относительный показатель адгезии тромбоцитов, равный отношению числа тромбоцитов на единице площади образца к числу тромбоцитов на единице площади стандарта - стекла, для исходного и модифицированного полимера составляет 1,0±0,2), а также существенное уменьшение антикоагулянтной активности гепарина на поверхности полимера при взаимодействии с плазмой крови. Известно, что в плазме крови присутствует более 20 белков, способных нейтрализовать антикоагулянтную активность гепарина [Биосовместимость. Под ред. В.И.Севастьянова. - М.: ГУП «Информационный центр ВНИИгеосистем», 1999, с.319]. Относительное время свертывания крови после хранения полимера в плазме крови человека в течение двух недель и одного месяца уменьшается с 12,0 до 5,3 и 3,6 соответственно. При этом отсутствует возможность повторной гепаринизации полимера без извлечения его из раствора плазмы крови и повторения процесса радиационной привитой сополимеризации.
Наиболее близким по технической сущности и достигаемым результатам является способ получения тромборезистентных полимерных материалов путем радиационной привитой сополимеризации на поверхность полимерного материала смеси гидрофильного мономера и ненасыщенного лиганда при массовом соотношении гидрофильный мономер 6 ненасыщенный лиганд 10:1-3 с последующей обработкой полимера раствором физиологически активного соединения [Авторское свидетельство СССР №833999, C08F 291/00, 1981]. В качестве раствора физиологически активного соединения используют водный раствор гепарина. В качестве гидрофильного мономера используют акриламид или N-винилпирролидон, а в качестве ненасыщенного лиганда, способного избирательно адсорбировать гепарин, используют холестериновый эфир N-метакрилоил-β-аланина, холестериновый эфир N-акрилоил-ω-аминоэнантовой кислоты или холестериновый эфир N-метакрилоил-ω-аминолауриновой кислоты. Функция гидрофильного мономера заключается в создании на поверхности полимера гидрофильного слоя, в котором иммобилизованы производные холестерина. При этом создаются наиболее благоприятные условия для функционирования производных холестерина: они связаны не с гидрофобной поверхностью полимера, а с гидрофильными цепями привитого полимера, что облегчает их селективное взаимодействие с водорастворимым гепарином. При этом концентрация гепарина на поверхности полимера составляет 0,17-0,40 мг/см2 поверхности. Время свертывания крови на поверхности полимера в результате гепаринизации увеличивается с 6 до 30 минут. Селективное взаимодействие производных холестерина с гепарином обеспечивает возможность повторной гепаринизации поверхности после удаления с поверхности изначально иммобилизованного гепарина. Время свертывания крови на поверхности полимера практически не изменяется и составляет 30±1 минут после проведения процедуры: удаление адсорбированного гепарина промыванием насыщенным раствором NaCl, повторная адсорбция гепарина.
Недостатком этого способа является невысокая тромборезистентность материала (время свертывания крови на поверхности полимера в результате его обработки повышается с 6 до 30 минут), а также необходимость повторного введения гепарина в кровоток для восстановления тромборезистентности после разрушения и удаления гепарина с поверхности полимера, что существенно усложняет процесс и приводит к снижению свертываемости всей крови.
Задачей изобретения является разработка способа получения полимерных материалов, обладающих повышенной самопроизвольной тромборезистентностью, проявляющейся при контакте с кровью или плазмой крови.
Техническим результатом, достигаемым при использовании изобретения, является повышение тромборезистентности полимерных материалов и придание им способности к самопроизвольному повышению тромборезистентности при контакте с кровью или плазмой крови.
Технический результат достигается тем, что в способе получения тромборезистентных полимерных материалов путем радиационной привитой сополимеризации на поверхность полимерного материала смеси гидрофильного мономера и ненасыщенного лиганда при массовом соотношении гидрофильный мономер: ненасыщенный лиганд 10:1-3 с последующей обработкой полимера раствором физиологически активного соединения в качестве ненасыщенного лиганда используют Nε-(мет)акрилоил-L-лизин, а в качестве раствора физиологически активного соединения используют кровь или плазму крови.
Привитую сополимеризацию проводят в вакууме под действием γ-излучения с суммарной дозой 1,0-10,0 Мрад при температуре 0-50°С. В зависимости от мощности дозы время облучения составляет 0,5-20 часов. Предпочтительно облучение проводят при комнатной температуре, мощности дозы 0,3-1,0 Мрад/час и суммарной дозе 1,0-3,0 Мрад. Привитую сополимеризацию проводят путем облучения полимерного материала, погруженного в водный раствор смеси гидрофильного мономера и Nε-(мет)акрилоил-L-лизина. При обработке материала кровью или плазмой крови на его поверхности концентрируется плазминоген за счет биоспецифического взаимодействия с привитым Nε-(мет)акрилоил-L-лизином. Концентрирование плазминогена на поверхности полимера приводит к возникновению контактов молекул плазминогена между собой и автокаталитическому превращению плазминогена в плазмин - наиболее активный фибринолитический фермент крови, ответственный за растворение тромбов в случае их возникновения [В.В.Мосолов. Протеолитические ферменты. - М.: Наука. 1971. C.185]. Конечным результатом взаимодействия полимера с кровью является появление на поверхности полимера, принадлежащего данному организму и поэтому не вызывающего реакций отторжения, плазмина. При разрушении адсорбированного плазмина его взаимодействие с Nε-(мет)акрилоил-L-лизином нарушается и он замещается новой молекулой плазминогена из крови. Таким образом, на поверхности полимера непрерывно генерируется плазмин, который и обеспечивает повышенную тромборезистентность полимера за счет разрушения тромбов в случае их образования.
Тромборезистентность полимерных материалов оценивают по времени свертывания крови.
Нижеследующие примеры иллюстрируют предлагаемое изобретение, но никоим образом не ограничивают область его применения.
Пример 1
В ампулу загружают 50 мл водного раствора, содержащего 1,0 г акриламида и 0,1 г Nε-акрилоил-L-лизина, и полиэтиленовую пленку с площадью 42 см2. Ампулу вакуумируют до 10-3 мм рт.ст., запаивают и облучают Со60 при 0°С, мощности дозы 0,3 Мрад/час в течение 10 часов. Ампулу вскрывают, полимер промывают водой, физиологическим раствором (0,9%-ный раствор NaCl) и выдерживают в плазме крови человека при комнатной температуре в течение 2 минут. Время свертывания крови на обработанной пленке составляет 48±2 минут. Время свертывания крови на исходной пленке равно 6±1 минутам. Для удаления адсорбированного плазминогена и плазмина пленку обрабатывают аминокапроновой кислотой. После этого время свертывания крови на поверхности пленки уменьшается до 9±1 минут. Пленку повторно обрабатывают плазмой крови человека. Время свертывания крови на поверхности пленки вновь повышается до 46±2 минут. Время свертывания крови на поверхности пленки, 6 раз подвергнутой процедуре «удаление плазминогена - обработка плазмой крови человека», составляет 45±2 минут.
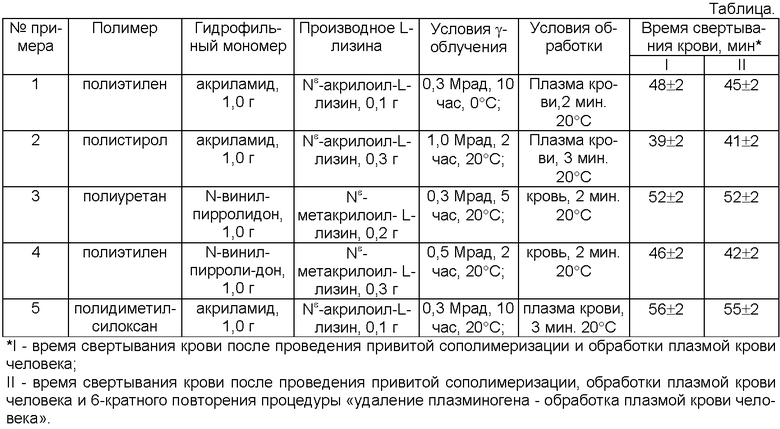
Примеры 2-5
Процесс проводят по примеру 1, используя различные исходные вещества и их количества, а также различные условия проведения привитой сополимеризации и обработки полимера. Для всех исходных полимеров время свертывания крови на их поверхности составляет 5±2 минуты. Результаты приведены в таблице.
Пример 6
В ампулу загружают 100 мл водного раствора, содержащего 1,5 г акриламида и 0,3 г Nε-акрилоил-L-лизина, и 3 плетеных лавсановых протеза кровеносных сосудов диаметром 4 мм и длиной 45 мм. Ампулу вакуумируют до 10-3 мм рт.ст., запаивают и облучают Со60 при 20°С, мощности дозы 0,3 Мрад/час в течение 10-3 часов. Ампулу вскрывают, протезы промывают водой, физиологическим раствором и выдерживают в плазме крови собаки при комнатной температуре в течение 5 минут. Под внутривенным наркозом выделяют сонную артерию собаки (3 животных). После резекции участка сосуда производят протезирование дефекта модифицированным сосудистым протезом конец в конец. После наложения дистального анастомоза протез промывают кровью, после чего кровь удаляют и накладывают проксимальный анастомоз. Во время операции и в послеоперационном периоде никакой антикоагулянтной терапии не проводят. Время наблюдения за оперированными животными составляет 6 месяцев. В течение всего времени наблюдения у животных сохраняется активная пульсация выше и ниже места протезирования. Не изменяется также давление и объем протекающей через протез крови, что свидетельствует о полной проходимости протезов.
Для сравнения с предлагаемым изобретением испытывают исходные немодифицированные протезы (2 протеза), которые полностью забиваются тромбом через 3-5 суток после протезирования.
Проведение испытаний на 3 протезах, модифицированных по способу-прототипу радиационной привитой сополимеризацией смеси 2 г акриламида и 0,3 г холестеринового эфира N-метакрилоил-β-аланина и обработанных раствором гепарина, показали, что после имплантации собакам первый протез тромбируется на 24-ые сутки, второй - на 32-ые сутки, а третий - на 40-ые сутки.
Таким образом, предлагаемое изобретение позволяет получать тромборезистентные полимерные материалы с повышенной тромборезистентностью и способностью к самопроизвольному повышению тромборезистентности при контакте с кровью или плазмой крови.
Предельные количества модифицирующих соединений, используемых при получении полимерных материалов, определяются следующим. При соотношении гидрофильный мономер: Nε-(мет)акрилоил-L-лизин больше, чем 10:1, снижается емкость привитого сополимера по плазминогену и снижается время свертывания крови на поверхности модифицированного полимера. При соотношении гидрофильный мономер: Nε-(мет)акрилоил-L-лизин 10:3 достигается предельное значение емкости привитого сополимера по плазминогену и уменьшение этого соотношения уже не приводит к увеличение времени свертывания крови на поверхности модифицированного полимера.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТРОМБОРЕЗИСТЕНТНОГО ПОЛИМЕРНОГО МАТЕРИАЛА | 2014 |
|
RU2556996C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРОМБОРЕЗИСТЕНТНЫХ ПОЛИМЕРНЫХ МАТЕРИАЛОВ | 2008 |
|
RU2388495C1 |
| Способ получения гемосовместимыхпОлиМЕРНыХ МАТЕРиАлОВ | 1979 |
|
SU833999A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ | 1985 |
|
SU1287541A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ | 1982 |
|
SU1078894A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРОВ | 1983 |
|
SU1114039A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРНЫХ МАТЕРИАЛОВ | 1986 |
|
SU1434729A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРНЫХ МАТЕРИАЛОВ | 1986 |
|
SU1407013A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННЫХ ФИЗИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ | 2007 |
|
RU2329053C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО АДСОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОФИБРИНОЛИЗИНА ИЗ ПЛАЗМЫ КРОВИ | 1988 |
|
SU1508548A1 |
Изобретение относится к области химии полимеров и медицины, а именно к способу получения тромборезистентных полимерных материалов. Описан способ получения тромборезистентных полимерных материалов путем радиационной привитой сополимеризации на поверхность полимерного материала смеси гидрофильного мономера и ненасыщенного лиганда при массовом соотношении гидрофильный мономер: ненасыщенный лиганд 10:1-10:3 с последующей обработкой полимера раствором физиологически активного соединения, отличающийся тем, что в качестве ненасыщенного лиганда используют Nε-(мет)акрилоил-L-лизин, а в качестве раствора физиологически активного соединения используют кровь или плазму крови. Технический результат - описанный способ позволяет получать тромборезистентные материалы с повышенной тромборезистентностью и способностью к самопроизвольному повышению тромборезистентности при контакте с кровью или плазмой крови. 1 табл.
Способ получения тромборезистентных полимерных материалов путем радиационной привитой сополимеризации на поверхность полимерного материала смеси гидрофильного мономера и ненасыщенного лиганда при массовом соотношении гидрофильный мономер: ненасыщенный лиганд 10:1-10:3 с последующей обработкой полимера раствором физиологически активного соединения, отличающийся тем, что в качестве ненасыщенного лиганда используют Nε-(мет)акрилоил-L-лизин, а в качестве раствора физиологически активного соединения используют кровь или плазму крови.
| Способ получения гемосовместимыхпОлиМЕРНыХ МАТЕРиАлОВ | 1979 |
|
SU833999A1 |
| SU 1120680 А1, 10.01.1998 | |||
| Диметил-(2-оксиэтил)-аммонийная соль поли- @ -акрилоилоксибензойной кислоты в качестве гемосовместимого полимерного материала | 1982 |
|
SU1055130A1 |
| US 3617344 А, 02.11.1971 | |||
| US 4897433 А, 30.01.1990. | |||
Авторы
Даты
2010-11-27—Публикация
2009-03-20—Подача