Изобретение относится к химии полимеров, биоорганической химии и медицине, а именно к способам получения полимерного адсорбента для выделения профибринолизина из плазмы крови, и может быть использовано в препаративной и аналитической биохимии и медицине для лечения различных заболеваний, связанных с дефицитом профибринолизина или тромбозами.
Цель изобретения повышение емкости адсорбента по профибринолизину и повышение его проницаемости для плазмы крови.
Пример 1. Получение Nα метакрилоил-L-лизина.
К охлажденному до 4oC раствору 10 г L-лизина (0,067 моль) в 100 мл 0,5 М раствора KOH при интенсивном перемешивании медленно по каплям прибавляют 7,0 г (0,067 моль) хлорангидрида метакриловой кислоты. После прибавления всего количества реагента смесь при постоянном перемешивании доводят до комнатной температуры и выливают в 200 мл подкисленного HCl (20 мл концентрированной HCl на 1000 мл 96% -ного этанола) этилового спирта. Выделяющееся масло растворяют в эфире и высаживают в диоксан. Получают 14 г белого порошка (выход 98,9%).
Найдено, C 56,12; H 8,40; N 13,66.
C40H18N2O3
Вычислено, C 56; H 8,45; N 13,84.
Удельное оптическое вращение в воде +12,5 град. Удельное оптическое вращение исходного L-лизина в воде +14,0 град.
В ИК-спектре соединения присутствуют полосы поглощения, локализующиеся на частотах, см-1: 3360 (амид-А), 3300 (амид Б), 1650 (амид-I), 1540 (амид-I) и 820 (колебания С=С связи). Соединение разлагается, не плавясь, при 370oC.
Пример 2. Получение Nα -акрилоил-L-лизина.
Все операции проводят, как в примере 1, используя в качестве ацилирующего агента 6,0 г (0,067 моль) хлорангидрида акриловой кислоты. Получают 13 г белого порошка (выход 99%).
Найдено, C 53,95; H 8,05; N 13,85.
C9H16N2O3
Вычислено, C 54,00; H 8,00; N 14,00.
Удельное оптическое вращение в воде +12 град.
В ИК-спектрах соединения присутствуют те же полосы, что и в соединении, полученном по примеру 1. Температура разложения (без плавления) 356oC.
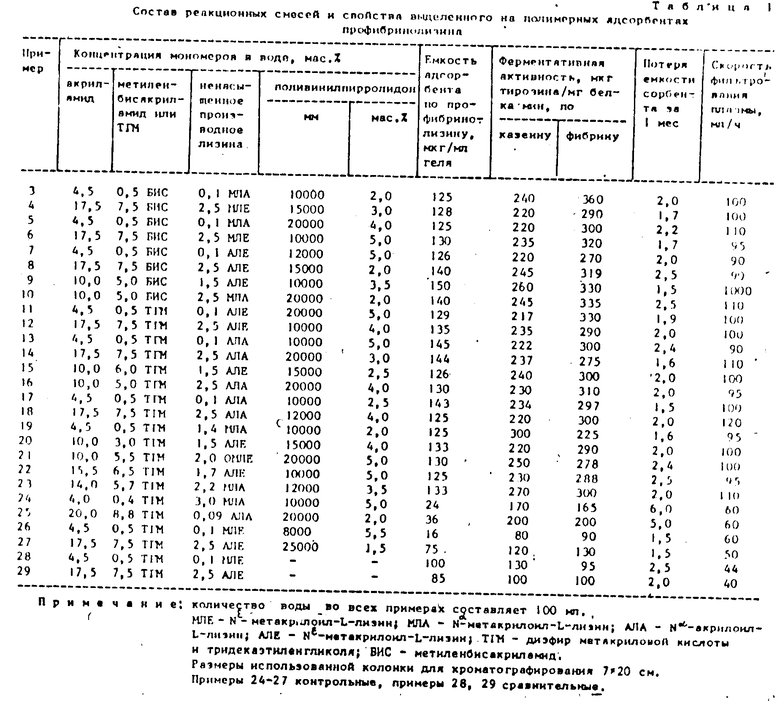
Пример 3. 4,5 г акриламида, 0,5 г метиленбисакриламида, 0,1 г Nα -метакрилоил-L-лизина и 0,051 г поли-N-винилпирролидона (ПВП) с мол. м. 10000 растворяют в 100 мл дистиллированной воды (содержание ПВП 2 мас. от сомономеров), продувают аргоном в течение 30 мин, добавляют 0,3 г персульфата аммония и 0,2 г метабисульфита калия и полимеризуют смесь в течение 0,5-1 ч. Полученный гель измельчают, отмучивают, промывают водой и физиологическим раствором до исчезновения в промывных водах поглощения при 220 нм, фиксируемого спектрофотометрически. Промытый полимерный адсорбент лиофильно высушивают и хранят в сухом виде при комнатной температуре.
Данные по примерам 3-29 приведены в табл. 1.
Пример 30. Выделение профибринолизина.
Полимерный адсорбент, полученный по примеру 1, помещают в физиологический раствор до прекращения изменения массы адсорбента. Набухший гель помещают в колонку (7x20 см), уравновешенную цитратным буфером с pH 7,4 и наносят плазму крови (свежая цитратная плазма). Элюирование начинают осуществлять через 20 мин сначала цитратным буфером (до исчезновения поглощения в элюенте при 280 нм), после чего 0,2 M раствором ε -аминокапроновой кислоты. Скорость элюрования составляет 100 мл/ч. Раствор плазминогена стерилизуют, помещают в стеклянные ампулы и лофилизуют. Препараты хранят при 4oC. Полученный белок электрофоретически гомогенен (гель-электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия показывает одну зону), имеет аргинин в качестве С-концевой аминокислоты и лизин в качестве N-концевой. После активации белка стрептокиназой образуется активный фермент фибринолизин, обладающий казеинолитической (240 мгк тирозина/мг белка) и фибринолитической активностью (360 мкг тирозина/мг белка).
Пример 31. Применение профибринолизина.
Полученный по примеру 30 белок в дозе 100-500 мкг на 1 кг живой массы вводят девяти беспородным кроликам. При этом изменений общего состояния и поведения животных, гематометрических и биохимических показателей не обнаруживается, масса всех органов животных соответствует усредненным данным для здоровых животных. Морфологические исследования тканей глаза при введении препарата профибринолизина в подконъюнктиву показывают слабо выраженную неспецифическую реакцию, сравниваемую с реакцией на введение физиологического раствора, что свидетельствует о нетоксичности полученного белка.
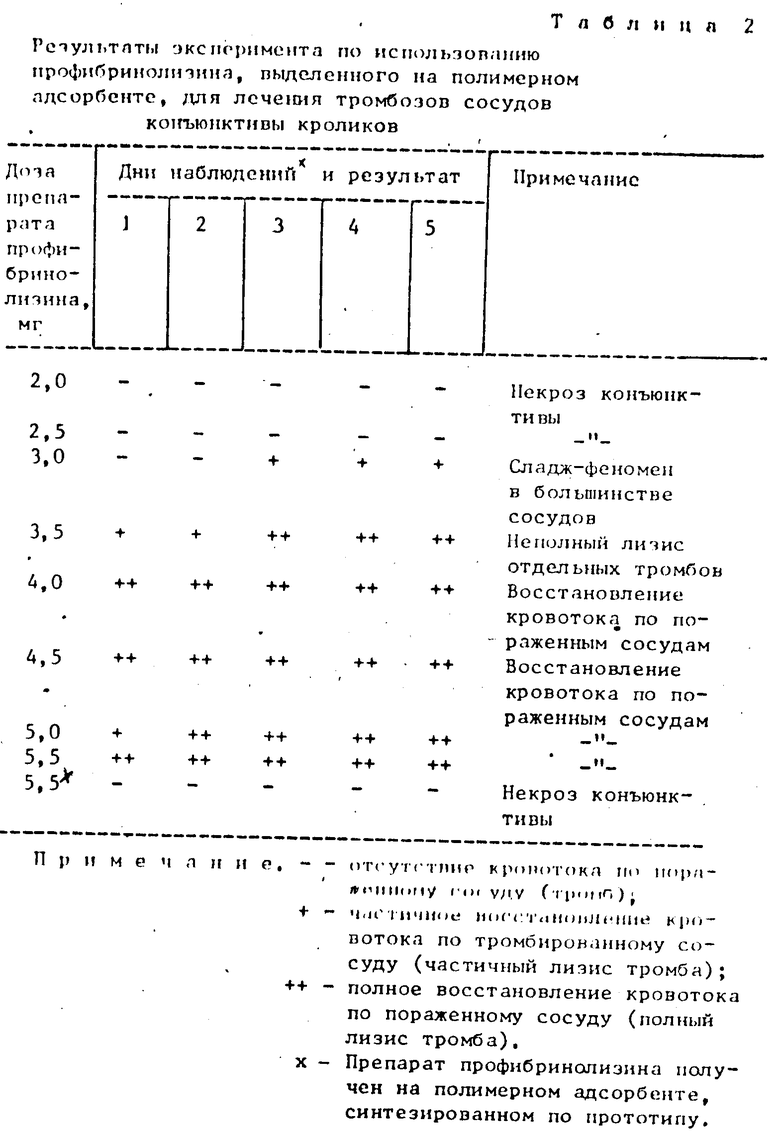
Полученный, как описано, препарат профибринолизина в дозе 2,0-5,5 мг вводят субконъюнктивально десяти кроликам-самцам (20 глаз) породы "Шиншилла" массой 2,5-3,0 кг, у которых смоделирован тромбоз сосудов конъюнктивы. Результаты эксперимента приведены в табл. 2. Введение профибринолизина, выделенного в помощью полимерного адсорбента, полученного предлагаемым способом, вызывает эффект растворения тромбов. Профибринолизин, полученный по способу-прототипу, не обладает литическим действием в описанном эксперименте.
Адсорбент является устойчивым при хранении и может быть использован многократно.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО АДСОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ И ОЧИСТКИ СЫВОРОТОЧНОГО АЛЬБУМИНА | 1981 |
|
SU1047159A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ | 1985 |
|
SU1287541A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО АДСОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ И ОЧИСТКИ ПРОФИБРИНОЛИЗИНА | 1987 |
|
SU1462756A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРОМБОРЕЗИСТЕНТНЫХ ПОЛИМЕРНЫХ МАТЕРИАЛОВ | 2009 |
|
RU2405002C1 |
| АФФИННЫЙ АДСОРБЕНТ ДЛЯ УДАЛЕНИЯ ИЗ КРОВИ БИЛИРУБИНА И ДРУГИХ ТОКСИЧНЫХ ПРОДУКТОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1978 |
|
SU731750A1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО АДСОРБЕНТА | 1979 |
|
SU803193A1 |
| БИОСПЕЦИФИЧЕСКИЕ АДСОРБЕНТЫ ЛИПОПРОТЕИДОВ И ХОЛЕСТЕРИНА | 1986 |
|
SU1369055A1 |
| СПОСОБ ПОЛУЧЕНИЯ АФФИННОГО АДСОРБЕНТА ДЛЯ УДАЛЕНИЯ ИЗ КРОВИ БИЛИРУБИНА И ДРУГИХ ТОКСИЧНЫХ ПРОДУКТОВ | 1978 |
|
SU731751A1 |
| Способ получения гемосовместимыхпОлиМЕРНыХ МАТЕРиАлОВ | 1979 |
|
SU833999A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРНЫХ МАТЕРИАЛОВ | 1986 |
|
SU1407013A1 |
Изобретение относится к химии полимеров и медицине и может быть использовано для создания препаратов плазмы крови. Изобретение позволяет получить полимерный адсорбент для выделения плазминогена из плазмы крови с высокой (125-150 мкг/мл набухшего адсорбента) емкостью и проницаемостью для плазмы крови, что достигается осуществлением радикальной сополимеризации в водном растворе 4,5-17,5 мас.% акриламида, 0,5-7,5 мас.% бифункционального мономера-сшивателя и 0,1-2,5 мас.% (мет)акрилоильного производного L-дизина в присутствии 2-5 мас.% от смеси сомономеров поли-N-винилпирролидона мол. м. 10000-20000. 2 табл.
Способ получения полимерного адсорбента для выделения профибринолизина из плазмы крови путем радикальной сополимеризации в водном растворе 4,5 17,5 мас. акриламида, 0,5 7,5 мас. бифункционального мономера-сшивателя и 0,1 - 2,5 мас. (мет)акрилоильного производного L-лизина, отличающийся тем, что, с целью повышения емкости по профибринализину и проницаемости адсорбента для плазмы крови, сополимеризацию проводят в присутствии 2 5 мас. от смеси сомономеров поли-N-винилпирролидона с мол.м. 10000 20000.
| Lui T.H., Mertz E.T | |||
| Purlfication of Human: Plasminogen BV Affinniti chromatographi, Canad | |||
| - J | |||
| Biochim, 1971, v | |||
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
| ВСПОМОГАТЕЛЬНАЯ МАШИНА ДЛЯ РЕГУЛИРОВАНИЯ СКОРОСТИ ТРЕХФАЗНОГО АСИНХРОННОГО ДВИГАТЕЛЯ | 1924 |
|
SU1055A1 |
| Rickli E., Glended R.A | |||
| Purification of Bovine Plasminogen BV chromatography Biochim.Biophys | |||
| acta, 1971, v | |||
| Катодное реле | 1921 |
|
SU250A1 |
| КОПИРОВАЛЬНЫЙ СТАНОК ДЛЯ ДЕРЕВА | 1921 |
|
SU447A1 |
| Авторское свидетельство СССР N 818149, кл | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
Авторы
Даты
1998-01-10—Публикация
1988-02-26—Подача