Настоящее изобретение относится к новому противовирусному активному компоненту, фармацевтической композиции, противовирусному лекарственному средству, способу профилактики и лечения вирусных заболеваний, особенно вызываемых вирусами гепатита С (HCV).
Вирусные инфекции могут вызывать множество заболеваний, что создает серьезную угрозу для здоровья и жизни человечества. За последние 20 лет обнаружено не менее 30 совершенно новых возбудителей инфекционных болезней: СПИДа, вирусных гепатитов, острых и хронических диарей, геморрагических лихорадок (Эбола, венесуэльской, бразильской, долины Рифт) [a) Lednicky J.A., Rayner J.O. Uncommon respiratory pathogens. Curr. Opin. Pulm. Med. 2006, 12(3), 235-239. b) Hayden F.G. Respiratory viral threats. Curr. Opin. Infect. Dis. 2006, 19(2), 169-178]. В частности, особую тревогу вызывает возможность заболевания человека так называемым «птичьим гриппом» [a) Liu J.P. Avian influenza--a pandemic waiting to happen? J. Microbiol. Immunol. Infect. 2006, 39(1), 4-10. b) Henter J.I.; Chow C.B.; Leung C.W, Lau Y.L. Cytotoxic therapy for severe avian influenza A (H5N1) infection. Lancet. 2006 367(9513), 870-873. Review]. Согласно статистическим данным, 60-65% эпидемических инфекций имеют вирусную этиологию. Из-за сложности взаимодействия в триаде «вирус - организм хозяина - лекарство», большинство современных противовирусных препаратов в процессе терапии проявляют побочные эффекты и формируют резистентные вирусные штаммы [Jain R., Clark N.M., Diaz-Linares M., Grim S.A. Limitations of current antiretroviral agents and opportunities for development. Curr. Pharm. Des. 2006, 12(9), 1065-1074]. В настоящее время количество противовирусных лекарственных препаратов, которые могут быть использованы в клинической практике, чрезвычайно ограничено - всего 43 низкомолекулярных вещества [http://integrity.prous.com/integrity], что далеко не удовлетворяет потребностям профилактики и лечения вирусных заболеваний. Кроме того, существует значительное число вирусных инфекций, вызывающих заболевания, для лечения которых в настоящее время не существует химиотерапевтических средств. Это относится, например, к заболеваниям, вызываемым вирусами папилломы, аденовирусам, герпеса-6, оспы, синдрома SARS, геморрагических лихорадок, лихорадки Западного Нила, птичьего гриппа и т.д. [De Clercq E. Recent highlights in the development of new antiviral drugs. Curr Opin Microbiol. 2005, 8(5), 552-560].
Таким образом, большое значение имеет изыскание новых противовирусных препаратов, в особенности, обладающих новым механизмом противовирусного действия, высокой активностью и низкой токсичностью.
В литературе имеются публикации, посвященные различным биологически активным производным бензимидазола. Так, например, известны 1,2-дизамещенные бензимидазола общей формулы А1, обладающие противовоспалительной активностью [FR 2280380, 1976; DE 2436883, 1976],
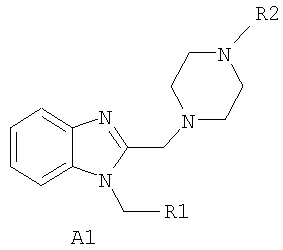
где R1 представляет собой о-гидроксифенил, п-хлорфенил или п-фторфенил; R2 представляет собой С2-С4 алкил.
Известны 1,2-дизамещенные бензимидазола, обладающие антигистаминной активностью [S.M. Rida, S.A. Shams El - Dine, I.M. Labouta. Synthesis of benzimidazole derivatives with potential antihistaminic activity. Pharmazie, 1977, 32, 577-579; BE 667333, 1966], способностью оказывать спазмолитическое влияние на гладкую мускулатуру [US 2689853, 1954; DE 890644], например, производные бензимидазола общей формулы А2 [US 2689853, 1954],
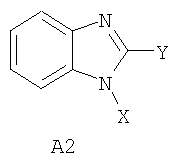
где Х представляет собой замещенный фенил или замещенный бензил; Y представляет собой низший алкил, замещенный низшей алкил- или низшей диалкил-аминогруппой, N-пирролидином.
Однако замещенные 2-аминометил-1-бензил-1Н-бензо[d]имидазола, обладающие противовирусной активностью, до настоящего времени не были известны.
Поиск высокоэффективных противовирусных лекарственных препаратов в настоящее время по-прежнему является одним из основных направлений создания новых фармакологических средств для лечения широкого и разнообразного круга вирусных инфекций. В этой связи актуальным является разработка новых противовирусных лекарственных начал, фармацевтических композиций и лекарственных средств, а также способов их получения и применения.
Ниже приведены определения терминов, которые использованы в описании этого изобретения.
«Азагетероцикл» означает ароматическую или неароматическую моноциклическую или полициклическую систему, содержащую в цикле, по крайней мере, один атом азота. Азагетероцикл может иметь один или более «заместителей циклической» системы.
«Алкил» означает алифатическую углеводородную линейную или разветвленную группу с 1-12 атомами углерода в цепи. Разветвленная означает, что алкильная цепь имеет один или несколько «низших алкильных» заместителей. Алкил может иметь один или несколько одинаковых или различных заместителей («алкильных заместителей»), включая галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонилгетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, Rk aRk+1 aNC(=S)-, Rk aRk+1 aNSO2, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители аминогруппы», например, атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом N, с которым они связаны, образуют через Rk a и Rk+1 a 4-7 членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил, метоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Алкилокси» означает алкил-O- группу, в которой алкил определен в данном разделе.
Предпочтительными алкилокси группами являются метокси, этокси, н-пропокси, изо-пропокси и н-бутокси.
«Аминогруппа» означает Rk aRk+1 aN- группу, замещенную или незамещенную «заместителем аминогруппы» Rk a и Rk+1 a, значение которых определено в данном разделе, например, амино (H2N-), метиламине, диэтиламино, пирролидин, морфолин, бензиламино или фенетиламино.
«Арил» означает ароматическую моноциклическую или полициклическую систему, включающую от 6 до 14 атомов углерода, преимущественно от 6 до 10 атомов углерода.
Арил может содержать один или более «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями арильных групп являются фенил или нафтил, замещенный фенил или замещенный нафтил. Арил может быть аннелирован с неароматической циклической системой или гетероциклом.
«Ацил» означает Н-С(=O)-, алкил-С(=O)-, циклоалкил-С(=O)-, гетероциклил-С(=O)-, гетероциклилалкил-С(=O)-, арил-С(=O)-, арилалкил-С(=O)-, гетероарил-С(=O)-, гетероарилалкил-С(=O)- группу, в которых алкил-, циклоалкил-, гетероциклил-, гетероциклилалкил, арил-, арилалкил, гетероарил-, гетероарилалкил определены в данном разделе.
«Ациламино» означает ацил-NH- группу, в которой значение ацил определено в данном разделе.
«Галоген» означает фтор, хлор, бром и йод. Предпочтительными являются фтор, хлор и бром.
«Гетероарил» означает ароматическую моноциклическую или полициклическую систему, включающую от 5 до 14 атомов углерода, предпочтительно от 5 до 10, в которой один или больше атомов углерода замещены гетероатомом или гетероатомами, такими как, азот, сера или кислород. Приставка «аза», «окса» или «тиа» перед «гетероарил» означает наличие в циклической системе атома азота, атома кислорода или атома серы, соответственно. Атом азота находящийся в гетероариле может быть окисленным до N-оксида. Гетарил может иметь один или несколько «заместителей циклической системы», которые могут быть одинаковыми или разными.
Представителями гетероарилов являются пирролил, фуранил, тиенил, пиридил, пиразинил, пиримидинил, изооксазолил, изотиазолил, тетразолил, охазолил, тиазолил, пиразолил, фуразанил, триазолил, 1,2,4-тиадиазолил, пиридазинил, хиноксалинил, фталазинил, имидазо[1,2-а]пиридинил, имидазо[2,1-b]тиазолил, бензофуразанил, индолил, азаиндолил, бензимидазолил, бензотиазенил, хинолинил, имидазолил, тиенопиридил, хиназолинил, тиенопиримидинил, пирролопиридин, имидазопиридил, изохинолинил, бензоазаиндолил, 1,2,4-триазинил, тиенопирролил, фуропирролил и др.
«Гетероциклил» означает ароматическую или неароматическую насыщенную моноциклическую или полициклическую систему, включающую от 3 до 10 атомов углерода, преимущественно от 5 до 6 атомов углерода, в которой один или несколько атомов углерода заменены на гетероатом, такой как азот, кислород, сера. Приставка «аза», «окса» или «тиа» перед гетероциклилом означает наличие в циклической системе атома азота, атома кислорода или атома серы, соответственно. Гетероциклил может иметь один или несколько «заместителей циклической системы», которые могут быть одинаковыми или разными. Атомы азота и серы, находящиеся в гетероциклиле могут быть окислены до N-оксида, S-оксида или S-диоксида. Представителями гетероциклилов являются пиперидин, пирролидин, пиперазин, морфолин, тиоморфолин, тиазолидин, 1,4-диоксан, тетрагидрофуран, тетрагидротиофен и др.
«Гидрат» означает сольват, в котором вода является молекулой или молекулами растворителя.
«Заместитель» означает химический радикал, который присоединяется к скэффолду (фрагменту), например, «заместитель алкильный», «заместитель аминогруппы», «заместитель карбамоильный», «заместитель циклической системы».
«Заместитель алкильный» означает заместитель, присоединенный к алкилу, алкенилу, значение которых определено в данном разделе. Заместитель алкильный представляет собой водород, алкил, галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонил, гетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, Rk aRk+1 aNSO2-, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например, атом водорода, алкил, арил, аралкил, гетероаралкил, Гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом азота, с которым они связаны, образуют через Rk a и Rk+1 a 4-7 членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил, метоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Заместитель аминогруппы» означает заместитель, присоединенный к аминогруппе. Заместитель аминогруппы представляет собой водород, алкил, циклоалкил, арил, гетероарил, гетероциклил, ацил, ароил, алкилсульфонил, арилсульфонил, гетероарилсульфонил, алкиламинокарбонил, ариламинокарбонил, гетероариламинокар-бонил, гетероциклиламинокарбонил, алкиламинотиокарбонил, ариламинотиокарбонил, гетероариламинотиокарбонил, гетероциклиламинотиокарбонил, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил.
«Заместитель циклической системы» означает заместитель, присоединенный к ароматической или неароматической циклической системе, включая водород, алкил, алкенил, алкинил, арил, гетероарил, аралкил, гетероаралкил, гидрокси, гидроксиалкил, амино, аминоалкил, алкокси, арилокси, ацил, ароил, галоген, нитро, циано, карбокси, алкоксикарбонил, арилоксикарбонил, аралкоксикарбонил, алкилоксиалкил, арилоксиалкил, гетероциклилоксиалкил, арилалкилоксиалкил, гетероциклилалкилоксиалкил, алкилсульфонил, арилсульфонил, гетероциклилсульфонил, алкилсульфинил, арилсульфинил, гетероциклилсульфинил, алкилтио, арилтио, гетероциклилтио, алкилсульфонилалкил, арилсульфонилалкил, гетероциклилсульфонилалкил, алкилсульфинилалкил, арилсульфинилалкил, гетероциклилсульфинилалкил, алкилтиоалкил, арилтиоалкил, гетероциклилтиоалкил, арилалкилсульфонилалкил, гетероциклилалкилсульфонилалкил, арилалкилтиоалкил, гетероциклилалкилтиоалкил, циклоалкил, циклоалкенил, гетероциклил, гетероцикленил, амидино, Rk aRk+1 aN-, Rk aN=, Rk aRk+1 aN-алкил-, Rk aRk+1 aNC(=O)-, или Rk aRk+1 aNSO2-, где Rk a и Rk+1 a представляют собой независимо друг от друга «заместители аминогруппы», значение которых определено в данном разделе, например, водород, необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероаралкил или заместитель Rk aRk+1 aN-, в котором Rk a может быть ацил или ароил, а значение Rk+1 a определено выше, или «заместителем циклической системы» являются Rk aRk+1 aNC(=O)-, или Rk aRk+1 aNSO2-, в которых Rk a и Rk+1 a вместе с атомом азота, с которым они связаны, образуют через Rk a и Rk+1 a 4-7 членный гетероциклил или гетероцикленил.
«Замещенная аминогруппа» означает Rk aRk+1 aN-группу, в которой Rk a и Rk+1 a представляют собой заместители аминогруппы, значение которых определено в данном разделе.
«Активный компонент» (лекарственное вещество, лекарственная субстанция, drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и других готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Необязательно замещенный радикал» означает радикал без заместителей или содержащий один или несколько заместителей.
«Низший алкил» означает линейный или разветвленный алкил с 1-4 атомами углерода.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение формулы I и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлимых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как, парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" J. Pharm. Sci. 1977, 66:1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как, холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
Предметом данного изобретения является новый противовирусный активный компонент, представляющий собой замещенный 2-аминометил-1-бензил-1Н-бензо[d]имидазол общей формулы 1 или его фармацевтически приемлемую соль,
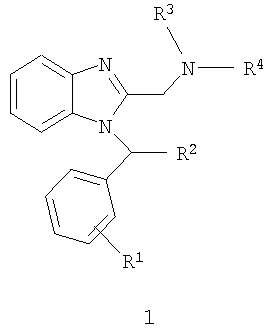
где R1 представляет собой один или два заместителя циклической системы, в том числе атом водорода, C1-С3 алкил, C1-С3 алкилокси или атом галогена;
R2 представляет собой атом водорода или C1-С3 алкил;
R3 и R4 представляют собой неодинаковые заместители аминогруппы, в том числе водород, C1-C2 алкил, C1-С3-алканоил, необязательно замещенный фураноил; необязательно замещенный или необязательно аннелированный с 5-6 членным азагетероциклом фенил;
или R3 и R4 вместе с атомом азота, с которым они связаны, образуют морфолин-4-ил, 4-(C1-С3алкилзамещенный)-пиперазин-1-ил, a R1 и R2 имеют вышеуказанное значение, или пиперидин-1-ил, при условии, что R1 имеет вышеуказанное значение, а R2 представляет собой C1-С3 алкил, или при условии, что R1 представляет собой водород или о-фтор, а R2 имеет вышеуказанное значение.
Более предпочтительным является противовирусный активный компонент, обладающий противовирусной активностью в отношении вируса гепатита С (HCV), представляющий собой замещенный 2-аминометил-1-бензил-1Н-бензо[d]имидазол общей формулы 1 или его фармацевтически приемлемую соль.
Предметом данного изобретения является также фармацевтическая композиция, обладающая противовирусной активностью, содержащая фармацевтически эффективное количество активного компонента, представляющего собой, по крайней мере, один замещенный 2-аминометил-1-бензил-1Н-бензо[d]имидазол общей формулы 1 или его фармацевтически приемлемую соль.
Более предпочтительной является фармацевтическая композиция, обладающая противовирусной активностью в отношении вируса гепатита С (HCV), содержащая в качестве активного компонента, по крайней мере, один замещенный 2-аминометил-1-бензил-1Н-бензо[d]имидазол общей формулы 1 или его фармацевтически приемлемую соль.
Фармацевтические композиции могут включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция наряду с соединением общей формулы 1 по настоящему изобретению может включать и другие активные ингредиенты, при условии, что они не вызывают нежелательных эффектов, например, аллергических реакций.
При необходимости использования фармацевтических композиций по настоящему изобретению в клинической практике они могут смешиваться для изготовления различных форм, при этом они могут включать в свой состав традиционные фармацевтические носители; например, пероральные формы (такие как, таблетки, желатиновые капсулы, пилюли, растворы или суспензии); формы для инъекций (такие как, растворы или суспензии для инъекций, или сухой порошок для инъекций, который требует лишь добавления воды для инъекций перед использованием); местные формы (такие как, мази или растворы).
Носители, используемые в фармацевтических композициях по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в том числе: в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, бесцветные агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Предметом настоящего изобретения также является способ получения фармацевтической композиции.
Поставленная цель достигается смешением с инертным наполнителем и/или растворителем противовирусного активного компонента, представляющего собой, по крайней мере, один замещенный 2-аминометил-1-бензил-1Н-бензо[d]имидазол общей формулы 1 или его фармацевтически приемлемую соль.
Предметом данного изобретения является также лекарственное средство, обладающее противовирусной активностью, в форме таблеток, капсул иди инъекций, помещенных в фармацевтически приемлемую упаковку, включающее в свой состав новый противовирусный активный компонент, представляющее собой, по крайней мере, один замещенный 2-аминометил-1-бензил-1Н-бензо[d]имидазол общей формулы 1 или его фармацевтически приемлемую соль, или новую фармацевтическую композицию, предназначенную для лечения вирусных заболеваний.
Согласно данному изобретению более предпочтительным лекарственным средством является лекарственное средство, предназначенное для лечения вируса гепатита С (HCV).
Лекарственные средства могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно). Клиническая дозировка фармацевтической композиции или лекарственного средства, содержащих активный компонент общей формулы 1, у пациентов может корректироваться в зависимости от: терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 10~500 мг, предпочтительно 50~300 мг. Поэтому во время приготовления из фармацевтической композиции лекарственного средства по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10~500 мг активного компонента общей формулы 1, предпочтительно 50~300 мг. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно - от одного до шести раз).
Предметом данного изобретения является также способ профилактики и лечения вирусных заболеваний у животных и людей.
В соответствии с данным изобретением способ профилактики и лечения вирусных заболеваний животных и людей, в том числе вызванных вирусами гепатита С, заключается во введении теплокровному животному или человеку нового активного компонента, новой фармацевтической композиции или нового терапевтического коктейля, содержащих активный компонент общей формулы 1 в эффективном количестве.
Ниже приводятся конкретные примеры, которые иллюстрируют, но не ограничивают объема настоящего иизобретения.
Замещенные 2-аминометил-1-бензил-1Н-бензо[d]имидазолы общей формулы 1 и их фармацевтически приемлемые соли являются коммерчески доступными продуктами или могут быть синтезированы с использованием общеизвестных способов, например описанных в [US 2689853, 1954; US 3423413, 1969; V.D. Jerchel, H. Fischer, M. Kraclit. Zur Darstellung der Benzimidazole. Annalen der Chemie, 575, 1952, 162-173; S.M. Rida, S.A. Shams El-Dine, I.M. Labouta. Synthesis of benzimidazole derivatives with potential antihistaminic activity. Pharmazie, 32, 1977, 577-579].
Пример 1. Определение противовирусной активности соединений общей формулы 1 в отношении вирусов гепатита С.
Определение противовирусной активности и цитотоксичности фармацевтической композиции, содержащей в качестве активного компонента одно из соединений общей формулы 1, в отношении вирусов гепатита С (HCV) штамм JFH-1 в культуре клеток человеческой гепатомы (Huh7), зараженной HCV.
Для определения активности соединений использовался иммунный in vitro тест ИФА на кор-антиген вируса HCV. С помощью этого теста измерялась эффективность ингибирования тестируемыми соединениями продукции антигена (и, следовательно, репликации вируса) в клетках, инфицированных вирусом JFH-1. Использованная в данном эксперименте культура клеток Huh7 способна, будучи инфицированной вирусом HCV, поддерживать полный цикл вирусной репликации.
Рекомбинантный вирус JFH-1 HCV, использованный в эксперименте, был получен путем трансфекции клеток Huh7 РНК JFH-1, полученных путем транскрипции in vitro. ДНК JFH-1 (NCBI, каталожный номер АВ047639 [Wakita, Т. и др. Production of Infectious Hepatitis С Virus in Tissue Culture from a Cloned Viral Genome. Nature Medicine 2005, 11:791-796]), использованная в качестве матричной ДНК для транскрипции, была синтезирована химически.
Клетки Huh7 были высеяны в 96-луночные платы (3,0×103 клеток на лунку) в среде Huh-7 (50 мкл на каждую лунку). Для каждого тестируемого соединения приготовили раствор в среде Huh-7 при концентрации 20 мкМ. Спустя 4 часа после высеивания клеток, исходный раствор был удален при помощи аспирации, после чего к каждой лунке добавили 50 мкл раствора тестируемого соединения, а также 50 мкл препарата JFH-1 HCV. Таким образом, финальные концентрации тестируемых соединений были в диапазоне 10 мкмоль/л. После инкубации в течение 16 часов вирусная среда была удалена при помощи аспирации, и к культурам были добавлены тестируемые соединения в исходных концентрациях до конечного объема 200 мкл. Клетки и тестируемые соединения инкубировали дополнительно в течение 3 дней при 37°С в атмосфере воздуха, содержащей 5% углекислого газа (СО2). После удаления питательной среды клетки были зафиксированы выдерживанием в 250 мкл смеси ацетон-метанол (1:1) в течение 1 минуты. Затем клетки трижды промывали фосфатным буфером (буфер PBS). Далее клетки блокировали 10% раствором FBS-PBS (150 мкл/лун) в течение 1 часа при комнатной температуре. Промывали каждую лунку троекратно промывочным раствором PBS, затем инкубировали с моноклональными мышиными антителами к кор-антигену HCV (Affinity BioReagents, каталожный номер МА1-080), растворенными в буфере FBS-PBS (100 мкл/лун. раствора, приготовленного из исходного концентрата, разведенного в соотношении 1:500 в 10% FBS-PBS), в течение 2 часов при 37°С. Промывали каждую лунку троекратно раствором PBS, затем инкубировали с антителами, специфичными к мышиным иммуноглобулинам, конъюгированными с пероксидазой хрена (HRP, 100 мкл/лун. раствора, приготовленного из исходного концентрата, разведенного в соотношении 1:2500 в 10% FBS-PBS) в течение 1 часа при 37°С. Промывали каждую лунку троекратно раствором PBS, затем обрабатывали 100 мкл/лун. раствора OPD (приготовлен растворением 1 таблетки OPD в 12 мл цитрат-фосфатного буфера с добавлением 5 мкл 30% Н2O2) в течение 30 минут в темноте при комнатной температуре. Реакцию останавливали добавлением к каждой лунке 100 мкл 2N H2SO4, после чего измеряли поглощение при длине волны 490 нм.
В таблице представлен % ингибирования вируса гепатита С соединениями общей формулы 1 при их концентрации 10 мкмоль/л.
Таблица. Ингибирование вируса гепатита С (%) соединениями общей формулы 1 при их концентрации 10 мкмоль/л
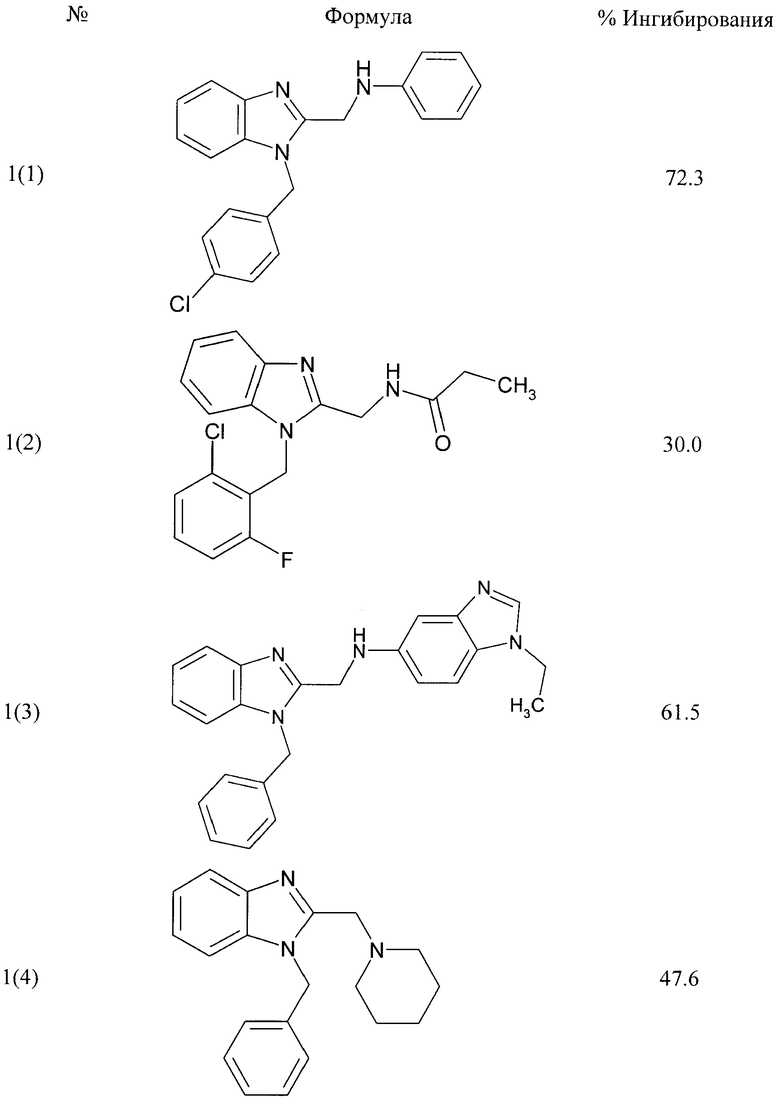
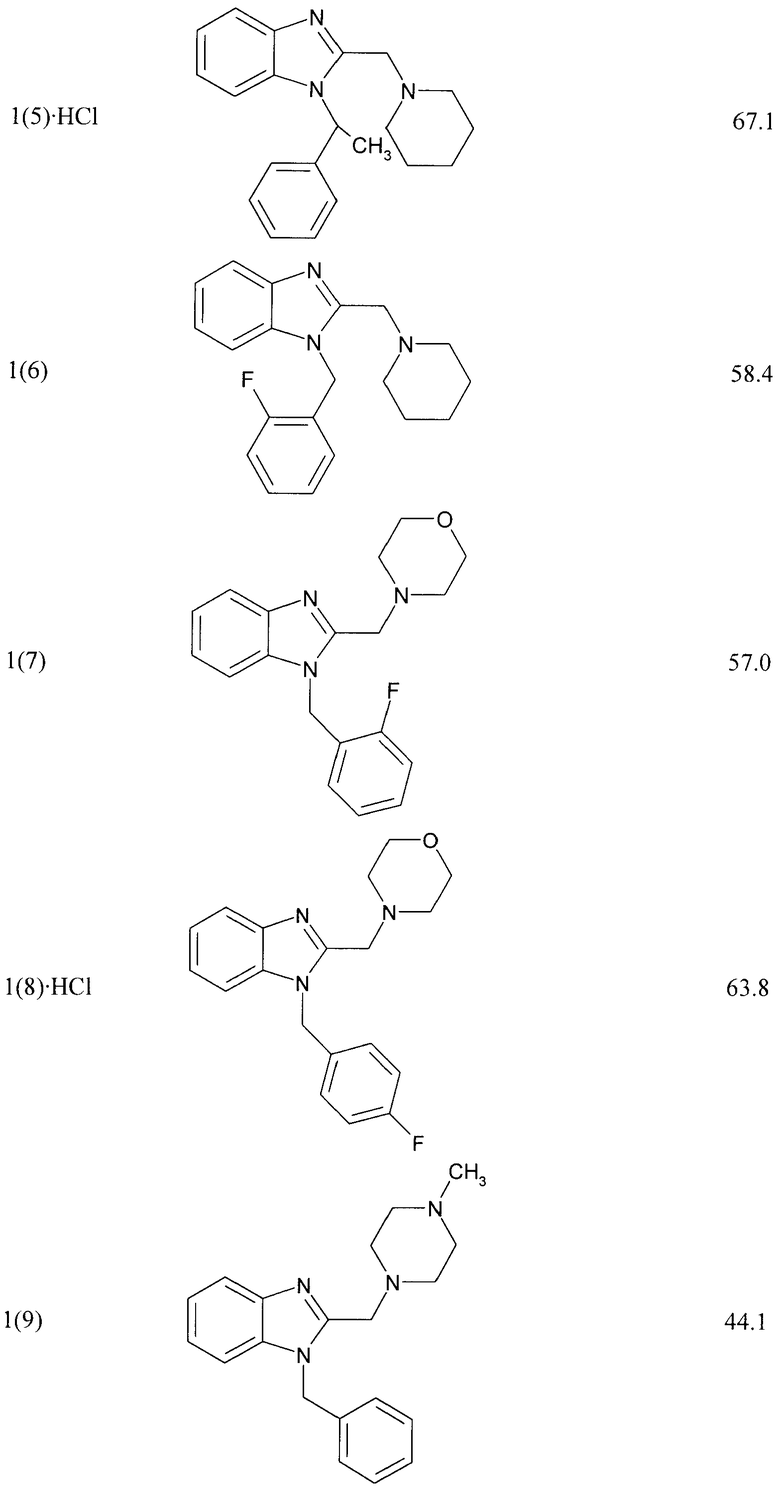
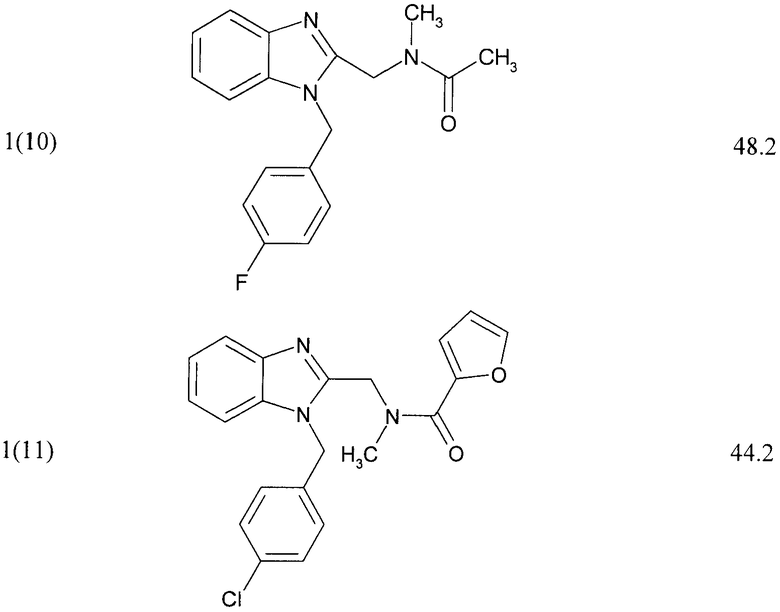
Пример 2. Получение лекарственного средства в форме таблеток. Смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг 1-(4-хлорбензил)-2-фениламинометил-1Н-бензимидазола 1(1). Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетируют в подходящую форму таблетки весом 560 мг каждая.
Пример 3. Получение лекарственного средства в форме капсул. Тщательно смешивают 1-(4-хлорбензил)-2-фениламинометил-1Н-бензимидазол 1(1) с порошком лактозы в соотношении 2:1. Полученную порошкообразную смесь упаковывают по 300 мг в желатиновые капсулы подходящего размера.
Пример 4. Получение лекарственного средства в форме инъекционных композиций для внутримышечных, внутрибрюшинных или подкожных инъекций. Смешивают 500 мг 1-(1-фенилэтил)-2-(пиперидин-1-ил)метил-1Н-бензимидазола гидрохлорида 1(5)·НС1 с 300 мг хлорбутанола, 2 мл пропиленгликоля и 100 мл инъекционной воды. Полученный раствор фильтруют и помещают по 1 мл в ампулы, которые запаивают.
Настоящее изобретение относится к новым противовирусным активным компонентам, представляющим собой замещенные 2-аминометил-1-бензил-1Н-бензо[d]имидазола общей формулы 1 или их фармацевтически приемлемым солям, фармацевтической композиции, противовирусным лекарственным средствам, способу профилактики и лечения вирусных заболеваний, особенно вызываемых вирусами гепатита С (HCV). В общей формуле 1

R1 представляет собой один или два заместителя циклической системы, в том числе атом водорода, C1-С3алкил, C1-С3алкилокси или атом галогена; R2 представляет собой атом водорода или C1-С3алкил; R3 и R4 представляют собой неодинаковые заместители аминогруппы, в том числе водород, C1-C2алкил, C1-С3-алканоил, необязательно замещенный фураноил; необязательно замещенный или необязательно аннелированный с 5-6 членным азагетероциклом фенил; или R3 и R4 вместе с атомом азота, с которым они связаны, образуют морфолин-4-ил, 4-(C1-С3алкилзамещенный)-пиперазин-1-ил, a R1 и R2 имеют вышеуказанное значение, или пиперидин-1-ил, при условии, что R1 имеет вышеуказанное значение, а R2 представляет собой C1-С3алкил, или при условии, что R1 представляет собой водород или о-фтор, а R2 имеет вышеуказанное значение. 5 н. и 2 з.п. ф-лы, 1 табл.
1. Противовирусный активный компонент, представляющий собой замещенный 2-аминометил-1-бензил-1Н-бензо[d]имидазол общей формулы 1 или его фармацевтически приемлемую соль,

где R1 представляет собой один или два заместителя циклической системы, в том числе атом водорода,
C1-С3алкил, C1-С3алкилокси или атом галогена;
R2 представляет собой атом водорода или C1-С3алкил;
R3 и R4 представляют собой неодинаковые заместители аминогруппы, в том числе водород, С1-С2алкил, C1-С3алканоил, необязательно замещенный фураноил; необязательно замещенный или необязательно аннелированный с 5-6-членным азагетероциклом фенил;
или R3 и R4 вместе с атомом азота, с которым они связаны, образуют морфолин-4-ил, 4-(С1-С3алкилзамещенный)-пиперазин-1-ил, a R1 и R2 имеют вышеуказанное значение,
или пиперидин-1-ил, при условии, что R1 имеет вышеуказанное значение, а R2 представляет собой C1-С3алкил, или при условии, что R1 представляет собой водород или о-фтор, а R2 имеет вышеуказанное значение.
2. Противовирусный активный компонент по п.1, обладающий противовирусной активностью в отношении вируса гепатита С (HCV).
3. Фармацевтическая композиция, обладающая противовирусной активностью, содержащая фармацевтически эффективное количество противовирусного активного компонента по любому из пп.1, 2.
4. Способ получения фармацевтической композиции по п.3 смешением с инертным наполнителем и/или растворителем, по крайней мере, одного противовирусного активного компонента по пп.1, 2.
5. Лекарственное средство, обладающее противовирусной активностью, в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, предназначенное для лечения вирусных заболеваний, включающее в свой состав противовирусный активный компонент по пп.1, 2 или фармацевтическую композицию по п.3 в эффективном количестве.
6. Лекарственное средство по п.5, предназначенное для лечения гепатита С.
7. Способ профилактики и лечения вирусных заболеваний, в том числе вызванных вирусами гепатита С, введением противовирусного активного компонента по пп.1 или 2 или фармацевтической композиции по п.3, или лекарственного средства по пп.5 или 6 в эффективном количестве.
| Колосоуборка | 1923 |
|
SU2009A1 |
| YU KUO-LONG et al | |||
| "Fundamental structur-activity relationships associated with a new structural class of respiratory syncytial virus inhibitor" Bioorganic & Medicinal Chemistry Letters, 2003, 13(13), 2141-2144 | |||
| WO 2002092575 A1, 12.11.2009 | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| WO 2000004900 A1, 03.02.2000 | |||
| МАШИНА ДЛЯ КОНТАКТНОЙ СТЫКОВОЙ СВАРКИ | 0 |
|
SU252507A1 |
Авторы
Даты
2010-12-27—Публикация
2009-07-03—Подача