Данное изобретение относится к новым замещенным 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диаминам, антагонистам серотониновых 5-НТ6 рецепторов, лекарственным началам и фармацевтическим композициям, содержащим лекарственные начала в виде указанных соединений, а также к способу лечения и предупреждения развития различных заболеваний центральной нервной системы (ЦНС), патогенез которых связан с 5-НТ6 рецепторами. В основе фармакологического эффекта новых лекарственных начал лежит их способность взаимодействовать с серотониновыми 5-НТ6 рецепторами, играющими важную роль для лечения заболеваний ЦНС, в частности болезни Альцгеймера (БА), болезни Паркинсона, болезни Гантингтона, шизофрении, нейродегенеративных заболеваний, когнитивных и тревожных расстройств и ожирения.
Использование эффективных и селективных антагонистов серотониновых 5-НТ6 рецепторов для лечения заболеваний ЦНС, в частности шизофрении, БА и других нейродегенеративных заболеваний и когнитивных расстройств, является перспективным направлением для получения новых лекарств [Holenz J., Pauwels P.J., Diaz J.L., Merce R., Codony X., Buschmann H. Medicinal chemistry strategies to 5-НТ6 receptor ligands as potential cognitive enhancers and antiobesity agents. Drug Disc. Today. 2006; 11:283-299]. Эти рецепторы у млекопитающих находятся исключительно в центральной нервной системе, причем главным образом в участках головного мозга, ответственных за обучение и память [Ge'rard С., Martres M.-P., Lefe'vre K., Miquel M.-C., Verge' D., Lanfumey L., Doucet E., Hamon M., El Mestikawy S. Immune-localisation of serotonin 5-НТ6 receptor-like material in the rat central nervous system. Brain Research. 1997; 746:207-219]. Кроме того, показано [Dawson L.A., Nguyen H.Q., Li P. The 5-HT(6) receptor antagonist SB-271046 selectively enhances excitatory neurotransmission in the rat frontal cortex and hippocampus. Neuropsychopharmacology. 2001; 25: 662-668], что 5-НТ6 рецепторы являются модуляторами нескольких нейромедиаторных систем, включая холинэргическую, норадренэргическую, глутаматэргическую и допаминэргическую. Учитывая фундаментальную роль этих систем в нормальных когнитивных процессах, а также их дисфункцию при нейродегенерации, становится очевидной исключительная роль 5-НТ6 рецепторов в формировании нормальной или «патологической» памяти. В большом числе современных работ показано, что блокирование 5-НТ6 рецепторов большом числе современных работ показано, что блокирование 5-НТ6 рецепторов приводит к значительному усилению консолидации памяти в различных животных моделях обучения-запоминания-воспроизведения [Foley A.G., Murphy K.J., Hirst W.D., Gallagher H.C., Hagan J.J., Upton N., Walsh F.S., Regan C.M. The 5-HT(6) receptor antagonist SB-271046 reverses scopolamine-disrupted consolidation of a passive avoidance task and ameliorates spatial task deficits in aged rats. Neuropsychopharmacology, 2004; 29: 93-100. Riemer С., Borroni E., Levet-Trafit В., Martin J.R., Poli S., Porter R.H., Bos M. Influence of the 5-HT6 receptor on acetylcholine release in the cortex: pharmacological characterization of 4-(2-bromo-6-pyrrolidin-l-ylpyridine-4-sulfonyl)phenylamine, a potent and selective 5-НТ6 receptor antagonist. J. Med. Chem. 2003; 46:1273-1276. King M.V., Woolley M.L., Topham LA., Sleight A.J., Marsden C.A., Fone K.C. 5-HT6 receptor antagonists reverse delay-dependent deficits in novel object discrimination by enhancing consolidation e an effect sensitive to NMDA receptor antagonism. Neuropharmacology 2004; 47:195-204]. Также показано значительное улучшение когнитивных функций у старых крыс в модели водного лабиринта Моррисона при воздействии антагонистом 5-НТ6 рецепторов [Foley A.G., Murphy K.J., Hirst W.D., Gallagher H.C., Hagan J.J., Upton N., Walsh F.S., Regan C.M. The 5-HT(6) receptor antagonist SB-271046 reverses scopolamine-disrupted consolidation of a passive avoidance task and ameliorates spatial task deficits in aged rats. Neuropsychopharmacology. 2004; 29:93-100]. В последнее время достигнуто не только более глубокое понимание роли 5-НТ6 рецепторов в когнитивных процессах, но более четкое формирование представлений о возможных фармакофорных свойствах их антагонистов [Holenz J., Pauwels P.J., Diaz J.L., Merce R., Codony X., Buschmann H. Medicinal chemistry strategies to 5-НТ6 receptor ligands as potential cognitive enhancers and antiobesity agents. Drug Disc. Today. 2006; 11: 283-299]. Это привело к созданию высокоаффинных селективных лигандов («молекулярных инструментов»), а затем и клинических кандидатов. В настоящее время ряд антагонистов 5-НТ6 рецепторов находятся на разных стадиях клинических испытаний как лекарственные кандидаты для лечения БА, болезни Гантингтона, шизофрении (антипсихотики) и других нейродегенеративных и когнитивных заболеваний (таблица 1) [http://integrity.prous.com].
Еще одним привлекательным свойством антагонистов 5-НТ6 рецепторов является их способность подавлять аппетит, что может привести к созданию на их основе принципиально новых средств для понижения избыточного веса и ожирения [Vicker S.P., Dourish С.Т. Serotonin receptor ligands and the treatment of obesity. Curr. Opin. Investig. Drugs. 2004; 5:377-388]. Этот эффект подтвержден во многих исследованиях [Holenz J., Pauwels P.J., Diaz J.L., Merce R., Codony X., Buschmann H. Medicinal chemistry strategies to 5-НТ6 receptor ligands as potential cognitive enhancers and antiobesity agents. Drug Disc. Today. 2006; 11: 283-299. Davies S.L. Drug discovery targets: 5-НТ6 receptor. Drug Future. 2005; 30:479-495], его механизм основан на подавлении антагонистами 5-НТ6 рецепторов сигналинга гамма-аминомасляной кислоты и увеличении выброса альфа-меланоцитстимулирующего гормона, что в конечном итоге приводит к уменьшению потребности в пище [Woolley M.L. 5-ht6 receptors. Curr. Drug Targets CNS Neurol. Disord. 2004; 3: 59-79]. В настоящее время два антагониста 5-НТ6 рецепторов находятся на первой стадии клинических испытаний как лекарственные кандидаты для лечения избыточного веса (таблица 1) [http://integrity.prous.com].
В этой связи поиск селективных и эффективных антагонистов серотониновых 5-НТ6 рецепторов представляется оригинальным и перспективным подходом к созданию новых лекарственных средств для лечения широкого круга заболеваний ЦНС, в том числе неврологических и нейродегенеративных заболеваний и когнитивных расстройств.
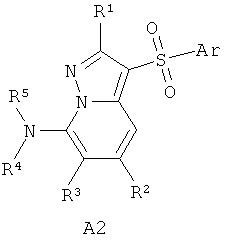
В литературе имеется значительное число публикаций, посвященных различным биологически активным сульфонилпроизводным азагетероциклам, в том числе лигандам серотониновых рецепторов. Так, например, известны замещенные 1-(2-аминоэтил)-4-арилсульфонил-пиразолы общей формулы А1 в качестве лигандов серотониновых 5-НТ2с рецепторов [WO 2003057674 А1] и 7-амино-3-сульфонил-пиразоло[1,5-а]пиримидины общей формулы А2 в качестве антагонистов серотониновых 5-НТ6 рецепторов [ЕР 941994 А1, 1999]
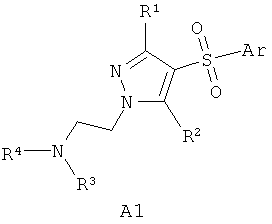
А1: Ar = алкил, арил; R1 и R2 = Н, ОН, алкил, алкокси; R3 и R4 = Н, алкил, арил.
А2: Ar = арил, гетероциклил; R1 = Н, алкил, алкилтио; R2 = Н, алкил, галоген; R3 = Н, алкил, гидроксиалкил; R4 и R5 = Н; NR4R5 = пиперазинил.
С целью разработки новых высокоэффективных лекарственных препаратов авторами данного изобретения выполнены широкие исследования в ряду замещенных 2-алкиламино-3-сульфонил-пиразоло[1,5-а]пиримидинов, в результате чего найдены новые лекарственные начала, представляющие собой антагонисты 5-НТ6 рецепторов.
Ниже приведены определения терминов, которые использованы в описании этого изобретения:
«Агонисты» означают лиганды, которые, связываясь с рецепторами данного типа, активно способствуют передаче этими рецепторами свойственного им специфического сигнала и тем самым вызывают биологический ответ клетки.
«Азагетероцикл» означает ароматическую или неароматическую моноциклическую или полициклическую систему, содержащую в цикле, по крайней мере, один атом азота. Азагетероцикл может иметь один или более «заместителей циклической системы».
«Алкил» означает алифатическую углеводородную линейную или разветвленную группу с 1-12 атомами углерода в цепи. Разветвленная означает, что алкильная цепь имеет один или несколько «низших алкильных» заместителей. Алкил может иметь один или несколько одинаковых или различных заместителей («алкильных заместителей»), включая галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонил, гетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, Rk aRk+1 aNC(=S)-, Rk aRk+1 аNSO2-, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например, атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом N, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, этил, пропил, циклопропилметил, циклопентилметил, этил, н-пропил, изопропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 аN-, Rk aRk+1 aNC(=O)-, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Алкиламино» означает CnH2n+1NH- или (CnH2n+1)(CnH2n+1)N- группу, в которой алкил определен в данном разделе. Предпочтительными алкиламиногруппами являются метиламино, этиламино, н-пропиламино, изопропиламино и н-бутиламино.
«Алкилокси» означает CnH2n+1O- группу, в которой алкил определен в данном разделе.
Предпочтительными алкилокси группами являются метилокси, этилокси, н-пропилокси, изопропилокси и н-бутилокси.
«Алкилоксикарбонил» означает -C(O)OCnH2n+1 группу, в которой алкил определен в данном разделе.
«Аминогруппа» означает Rk aRk+1 aN - группу, замещенную или незамещенную необязательно одинаковыми «заместителями аминогруппы» Rk a и Rk+1 a, значение которых определено в данном разделе, например, амино (H2N-), метиламино, диэтиламино, пирролидино, морфолино, бензиламино или фенетиламино.
«Аминокарбонил» означает C(=O)N Rk aRk+1 a - группу, замещенную или незамещенную необязательно одинаковыми «заместителями карбамоильными» Rk a и Rk+1 a, включая водород, алкенил, алкил, арил, гетероарил, гетероциклил, значение которых определено в данном разделе.
«Анксиолитик» или «Транквилизатор» означает лекарственное средство, предназначенное для лечения тревожных расстройств.
«Антагонисты» означают лиганды, которые связываются с рецепторами определенного типа и не вызывают активного клеточного ответа. Антагонисты препятствуют связыванию агонистов с рецепторами и тем самым блокируют передачу специфического рецепторного сигнала.
«Антидепрессант» означает лекарственное средство, предназначенное для лечения депрессии.
«Антипсихотик» означает лекарственное средство, предназначенное для лечения психотических заболеваний.
«Арил» означает ароматическую моноциклическую или полициклическую систему, включающую от 6 до 14 атомов углерода, преимуществено от 6 до 10 атомов углерода.
Арил может содержать один или более «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями арильных групп являются фенил или нафтил, замещенный фенил или замещенный нафтил. Арил может быть аннелирован с неароматической циклической системой или гетероциклом.
«Арилсульфонил» означает арил-SO2- группу, в которой значение арил определено в данном разделе.
«Галоген» означает фтор, хлор, бром и йод. Предпочтительными яляются фтор, хлор и бром.
«Гидрат» означает сольват, в котором вода является молекулой или молекулами растворителя.
«Депрессия» означает большую депрессию; эпизодическую, хроническую и рецидивирующую формы большой депрессии; дистимическое расстройство (дистимию); циклотимию; аффективные расстройства; синдром сезонного аффективного расстройства; биполярные расстройства, включая биполярные расстройства I и II типа; а также другие депрессивные расстройства и состояния. Термин депрессия означает также депрессивные состояния, сопровождающие болезнь Альцгеймера, васкулярную деменцию; расстройства настроения, индуцированные алкоголем и веществами; шизоаффективные расстройства депрессивного типа; расстройства адаптации. Кроме того, депрессия включает депрессивные состояния онкологических больных; при болезни Паркинсона; депрессию после инфаркта миокарда; депрессию бесплодных женщин; педиатрическую депрессию; послеродовую депрессию; а также другие депрессивные состояния, сопровождающие соматические, невралогические и прочие заболевания.
«Заместитель» означает химический радикал, который присоединяется к скэффолду (фрагменту), например, «заместитель алкильный», «заместитель аминогруппы», «заместитель карбамоильный», «заместитель циклической системы», значения которых определено в данном разделе.
«Заместитель аминогруппы» означает заместитель, присоединенный к аминогруппе. Заместитель аминогруппы представляет собой водород, алкил, циклоалкил, арил, гетероарил, гетероциклил, ацил, ароил, алкилсульфонил, арилсульфонил, гетероарилсульфонил, алкиламинокарбонил, ариламинокарбонил, гетероариламинокарбонил, гетероциклиламинокарбонил, алкиламинотиокарбонил, ариламинотиокарбонил, гетероариламинотиокарбонил, гетероциклиламинотиокарбонил, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонилалкил, аралкокси-карбонилалкил, гетероаралкилоксикарбонилалкил.
«Заместитель карбамоильный» означает заместитель, присоединенный к аминокарбонильной группе, значение которой определено в данном разделе. Заместитель карбамоильный представляет собой водород, алкил, циклоалкил, арил, гетероарил, гетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-алкил, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил. Предпочтительными «заместителями карбамоильными» являются алкил, циклоалкил, арил, гетероарил, гетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-алкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Заместитель циклической системы» означает заместитель, присоединенный к ароматической или неароматической циклической системе, включая водород, алкил, алкенил, алкинил, арил, гетероарил, аралкил, гетероаралкил, гидрокси, гидроксиалкил, амино, аминоалкил, алкокси, арилокси, ацил, ароил, галоген, нитро, циано, карбокси, алкоксикарбонил, арилоксикарбонил, аралкоксикарбонил, алкилоксиалкил, арилоксиалкил, гетероциклилоксиалкил, арилалкилоксиалкил, гетероциклилалкил-оксиалкил, алкилсульфонил, арилсульфонил, гетероциклилсульфонил, алкилсульфинил, арилсульфинил, гетероциклилсульфинил, алкилтио, арилтио, гетероциклилтио, алкилсульфонилалкил, арилсульфонилалкил, гетероциклилсульфонилалкил, алкилсульфинилалкил, арилсульфинилалкил, гетероциклилсульфинилалкил, алкилтиоалкил, арилтиоалкил, гетероциклилтиоалкил, арилалкилсульфонилалкил, гетероциклилалкилсульфонилалкил, арилалкилтиоалкил, гетероциклилалкилтиоалкил, циклоалкил, циклоалкенил, гетероциклил, гетероцикленил, амидино, Rk aRk+1 aN-, Rk aN=, Rk aRk+1 aN-алкил-, Rk aRk+1 aNC(=O)- или Rk aRk+1 aSO2, где Rk a и Rk+1 a представляют собой независимо друг от друга «заместители аминогруппы», значение которых определено в данном разделе, например, водород, необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил или необязательно замещенный гетероаралкил, или заместитель Rk aRk+1 aN-, в котором Rk a может быть ацил или ароил, а значение Rk+1 a определено выше, или «заместителем циклической системы» являются Rk aRk+1 aNC(=O)- или Rk a k+1 aNSO2, в котором Rk a и Rk+1 a вместе с атомом азота, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетероцикленил.
«Карбоксил» означает группу -CO2H.
«Когнитивные расстройства или нарушения когнитивных функций (cognitive disorder)» означают нарушение (ослабление) умственных возможностей, включающих внимание, память, мышление, познание, обучение, речевые, мыслительные, исполнительные и творческие способности, ориентацию во времени и пространстве, в частности, когнитивные расстройства, связанные с болезнями Альцгеймера, Паркинсона и Гантингтона; старческое слабоумие; возрастные расстройства памяти (age-associated memory impairment, AAMI); дисметаболические энцефалопатии; психогенные нарушения памяти; амнезия; амнестические расстройства; транзиторная глобальная амнезия; диссоциативная амнезия; васкулярная деменция; легкие (или умеренные) когнитивные нарушения (mild cognitive impairment, MCI); синдром нарушения внимания с гиперактивностью (attention deficit hyperactivity disorder, AD/HD); когнитивные нарушения, сопровождающие психотические заболевания, эпилепсию, делирий, аутизм, психозы, синдром Дауна, биполярные расстройства и депрессию; СПИД-ассоциированная деменция; деменция при гипотиреоидизме; деменция, индуцированная алкоголем, веществами, вызывающими зависимость, и нейротоксинами; деменция, сопровождающая нейродегенеративные заболевания, например, мозжечковую дегенерацию и амиотрофический латеральный склероз; когнитивные расстройства, развивающиеся при инсульте, инфекционных и онкологических заболеваниях головного мозга, а также при черепно-мозговых травмах; нарушения когнитивных функций, ассоциированные с аутоиммунными и эндокринными заболеваниями; и прочие когнитивные расстройства.
«Лекарственное начало» (лекарственная субстанция, лекарственное вещество, drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного средства (препарата).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и др. готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Лиганды» (от латинского ligo - связывать) представляют собой химические вещества (малая молекула, неорганический ион, пептид, белок и прочее), способные взаимодействовать с рецепторами, которые трансформируют это взаимодействие в специфический сигнал.
«Нейродегенеративное заболевание (НЗ)» означает специфическое состояние и заболевание, характеризующиеся повреждением и первичной гибелью популяций нервных клеток в определенных областях центральной нервной системы. Нейродегенеративные заболевания включают, но не ограничивают болезни Альцгеймера и Паркинсона; болезнь (хорею) Хантингтона; рассеянный склероз; мозжечковую дегенерацию; амиотрофический латеральный склероз; деменцию с тельцами Леви; спинальную мускульную атрофию; периферическую нейропатию; губчатый энцефалит («коровье бешенство», Creutzfeld-Jakob Disease); СПИД-ассоциированную деменцию; мультиинфарктную деменцию; лобно-височную деменцию; лейкоэнцефалопатию (болезнь исчезающего белого вещества); хронические нейродегенеративные заболевания; инсульт; ишемическое, реперфузионное и гипоксическое повреждение мозга; эпилепсия; церебральная ишемия; глаукома; черепно-мозговая травма; синдром Дауна; энцефаломиелит; менингит; энцефалит; нейробластома; шизофрения; депрессия. Кроме того, нейродегенеративные заболевания включают патологические состояния и расстройства, развивающиеся при гипоксии, злоупотреблении веществами, вызывающими зависимость, при воздействии нейротоксинов, инфекционных и онкологических заболеваниях головного мозга, а также нейрональные повреждения, ассоциированные с аутоиммунными и эндокринными заболеваниями; и прочие нейродегенеративные процессы.
«Низший алкил» означает линейный или разветвленный алкил с 1-4 атомами углерода.
«Ноотропы» или «ноотропики», они же нейрометаболические стимуляторы - вещества, принимаемые для улучшения умственных способностей.
«Психические расстройства» (психические заболевания) - это болезни или болезненные состояния, связанные с нарушением и/или расстройством психики. Психические расстройства включают аффективные расстройства (биполярные аффективные расстройства, большая депрессия, гипомания, малая депрессия, маниакальный синдром, синдром Котара, циклотимия, шизоаффективное расстройство и др.); интеллектуально-мнестические расстройства, мании (гипомания, графомания, клептомания, магазиномания, мания преследования, мономания, порнографомания, эротомания и др.); расстройство множественной личности, аменцию, белую горячку, бред, бредовый синдром, галлюцинаторный синдром, галлюцинации, галлюциноз, гомицидоманию, делирий, иллюзию, кверулянтство, клиническую ликантропию, макропсию, манихейский бред, микропсию, наркоманию, нервную анорексию, онейроидный синдром, пароноид, паранойю, парафрению, псевдогаллюцинации, психоз, синдром Котара, шизоаффективное расстройство, шизотипическое расстройство, шизофрению, шизофреноподобное расстройство, шизофреноморфное расстройство, синдром Шребера, Даниэль Пауля); фобии (агарофобию, арахнофобию, аутофобию, верминофобию, гидрозофобию, гидрофобию, демофобию, зоофобию, канцерофобию, клаустрофобию, климакофобию, ксенофобию, мизофобию, радиофобию, светобоязнь, сколицефобию, скотофобию, социофобию, тетрафобию, трискаидефобию, эротофобию); алкогольные психозы, алкогольный палимпсест, аллотриофагию, афазию, графоманию, диссоциативные фуги, диссоциативные расстройства, дисфории, Интернет-зависимости, ипохондрию, истерию, копрофемию, манию преследования, меланхолию, мизантропию, обсессию, панические атаки, синдром Аспергера, синдром Капгра, синдром Мюнхгаузена, синдром Ретта, синдром Фреголи, синдром дефицита внимания и гиперактивности, синдром навязчивых состояний, синдром последствий хронической наркотизации, синдром психического автоматизма, синдром раннего детского аутизма, сумашествие, тафофилию, тревожные состояния, синдром Хикикомори, эротографоманию и др.
«Психотические заболевания» это все виды шизофрении; шизофреноподобные заболевания; шизотипические расстройства; шизоаффективные расстройства, включая биполярный и депрессивный типы; бредовые расстройства, включая бред отношения, преследования, величия, ревности, эротомании, а также ипохондрический, соматический, смешанный и недифференцируемый бред; кратковременные психотические расстройства; индуцированные психотические расстройства; индуцированные веществами психотические расстройства; а также другие психотические расстройства.
«Рецепторы» (от латинского recipere - получать, узнавать) представляют собой биологические макромолекулы, расположенные на цитоплазматической мембране клетки или внутриклеточно, способные специфически взаимодействовать с ограниченным набором физиологически активных веществ (лигандов) и трансформировать сигнал об этом взаимодействии в определенный клеточный ответ.
«Терапевтический коктейль» представляет одновременно администрируемую комбинацию двух и более лекарственных препаратов, обладающих различным механизмом фармакологического действия и направленных на различные биомишени, участвующие в патогенезе заболевания.
«Тревожные расстройства» (anxiety) означает генерализованную (неконкретную) тревогу; острое неконтролируемое беспокойство; паническое заболевание; фобии, например, агорафобию (сильная боязнь людных мест) или социальную фобию (сильную боязнь унижения перед другими людьми) или любую конкретную фобию (сильную боязнь конкретных предметов, животных или ситуаций, в виде боязни высоты, медицинских процедур, лифтов, открытого пространства и т.п.); навязчивые состояния (обсессивно-компульсивное расстройство); посттравматическиое стрессовое расстройство и острое стрессовое расстройство. Кроме того, к тревожным расстройствам относятся тревожные состояния, индуцированные алкоголем или веществами; тревога при расстройствах адаптации; а также смешанные формы тревожных расстройств и депрессии.
«Циклоалкил» означает не ароматическую моно- или полициклическую систему, включающую от 3 до 10 атомов углерода. Циклоалкил может иметь один или несколько «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями циклоалкильных групп являются циклопропил, циклобутил, циклопентил, циклогексил, декалин, норборнил, адамант-1-ил и т.п. иклоалкил может быть аннелирован с ароматическим циклом или гетероциклом. Предпочтительными «заместителями циклической системы» являются алкил, аралкокси, гидрокси или Rk aRk+1 aN, значение которых определено в данном разделе.
«Шизофрения» означает все известные типы, формы и варианты заболевания, в том числе: простую, гебефреническую, параноидную, гипертоксическую (фебрильную), кататоническую, шизоаффективную, остаточную или недифференцируемую шизофрению и/или формы шизофрении, определенные в классификации Американской Психиатрической Ассоциации (American Psychiatric Association; in: Diagnostic and Statistical Manual of Mental Disorders, IV Edition, Washington D.C. 2000) или в Международной классификации (International Statistical Classification of Diseases and Related Health Problems) или любые другие известные формы.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение формулы 1 и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие как оливковое масло) и инъекционные органические сложные эфиры (такие как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом может быть введена животным и людям в стандартной форме введения в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения. Фармацевтические композиции, как правило, получают с помощью стандартных процедур, предусматривающих смешение активного соединения с жидким или тонко измельченным твердым носителем.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные. (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
Предметом настоящего изобретения являются новые замещенные 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,б-диамины общей формулы 1 и их фармацевтически приемлемые соли и/или гидраты
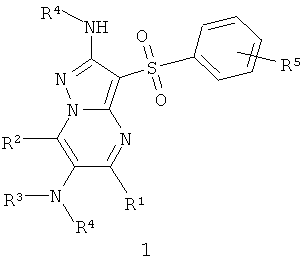
где
R1, R2 и R4 независимо друг от друга представляют собой необязательно одинаковые C1-С3алкил;
R3 и R4 представляют собой необязательно одинаковые атом водорода, необязательно замещенный C1-С3алкил или ацетил;
R5 представляет собой атом водорода, или атом галогена.
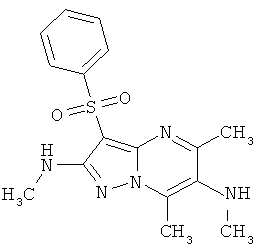
Предпочтительным замещенным 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамином общей формулы 1 является 5,7,N(2)-триметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамины общей формулы 1.1
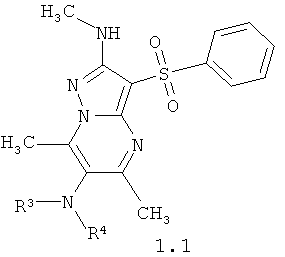
где
R3 и R4 имеют вышеуказанное значение.
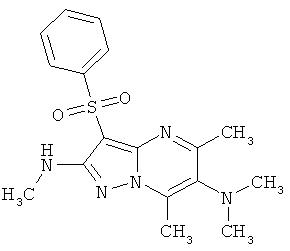
Более предпочтительными 5,7,N(2)-триметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамином общей формулы 1.1 является 5,7N(2)-триметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамин 1.1.1 и 5,7,N(2),N(6),N(6)-пентаметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамин 1.1.2.
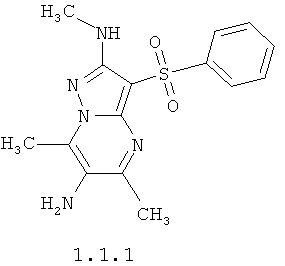
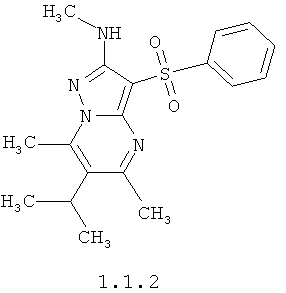
3-Арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамин общей формулы 1 получают по схеме, представленной ниже. В случае, когда в дикетоне 3 Ra и Rb разные алкилы, то образуется смесь двух N(3-арилсульфонил-2-алкиламино)пиразоло[1,5-a]пиримидин-6-ил)ацетамидов 1А, 1В (R3 = Н, R4 = А; Ra и Rb = C1-С3алкил), которую разделяют хроматографически.
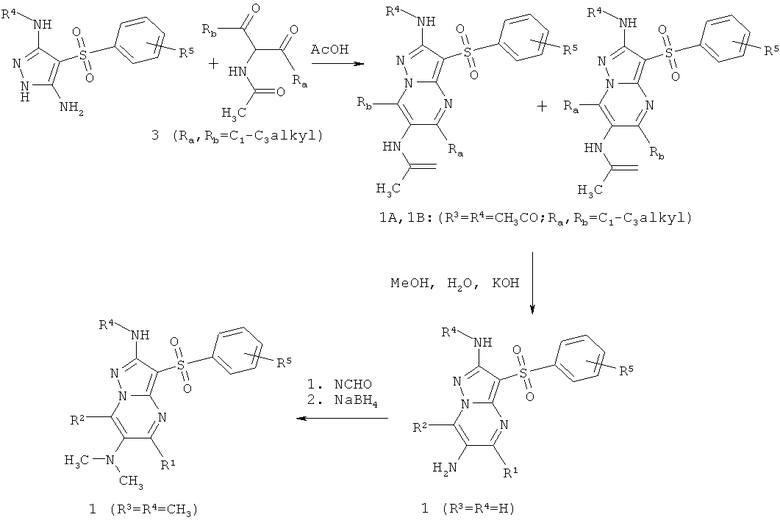
Предметом настоящего изобретения являются также антагонисты серотониновых 5-НТ6 рецепторов, представляющие собой замещенные 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамины общей формулы 1, 1.1, 1.1.1, 1.1.2 и их фармацевтически приемлемые соли и/или гидраты.
Более предпочтительными антагонистом серотониновых 5-НТ6 рецепторов является 5,7,N(2)-триметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамин 1.1.1 и 5,7,N(2),N(6),N(6)-пентаметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамин 1.1.2.
Цель настоящего изобретения заключается в создании новых «молекулярных инструментов» для изучения особенностей взаимодействия с серотониновыми 5-НТ6 рецепторами.
Поставленная цель достигается антагонистами серотониновых 5-НТ6 рецепторов, представляющими собой замещенные 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диаминами общей формулы 1, 1.1, 1.1.1, 1.1.2 и их фармацевтически приемлемыми солями и/или гидратами.
Предметом данного изобретения являются также замещенные 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамины общей формулы 1, 1.1, 1.1.1, 1.1.2 и их фармацевтически приемлемые соли и/или гидраты в качестве лекарственного начала для фармацевтических композиций и лекарственных средств.
Предметом данного изобретения является также фармацевтическая композиция для лечения и предупреждения развития состояний и заболеваний ЦНС людей и теплокровных животных, содержащая фармацевтически эффективное количество нового лекарственного начала, представляющего собой, по крайней мере, одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат.
Фармацевтическая композиция может включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция наряду с лекарственным началом по настоящему изобретению может включать и другие активные ингредиенты при условии, что они не вызывают нежелательных эффектов, например, аллергических реакций.
При необходимости использования фармацевтических композиций по настоящему изобретению в клинической практике они могут смешиваться для изготовления различных форм, при этом они могут включать в свой состав традиционные фармацевтические носители; например, пероральные формы (такие как таблетки, желатиновые капсулы, пилюли, растворы или суспензии); формы для инъекций (такие как растворы или суспензии для инъекций или сухой порошок для инъекций, который требует лишь добавления воды для инъекций перед использованием); местные формы (такие как мази или растворы).
Носители, используемые в фармацевтических композициях по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в том числе: в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, бесцветные агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Предметом данного изобретения является также способ получения новой фармацевтической композиции смешением с инертным наполнителем и/или растворителем лекарственного начала, представляющего собой, по крайней мере, одно из соединений общей формулы 1,1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат.
Предметом данного изобретения является лекарственное средство в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для профилактики и лечения заболеваний центральной нервной системы, патогенез которых связан с 5-НТ6 рецепторами, у теплокровных животных и людей, представляющее собой, по крайней мере одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемаю соль, или фармацевтическую композицию, содержащую новое лекарственное начало.
Более предпочтительным является лекарственное средство в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для профилактики и лечения когнитивных расстройств и нейродегенеративных заболеваний, включающее фармацевтически эффективное количество лекарственнго начала, представляющее собой, по крайней мере, одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат, или фармацевтическую композицию, содержащую новое лекарственное начало.
Более предпочтительным является лекарственное средство в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для профилактики и лечения болезни Альцгеймера, болезни Паркинсона, болезни Гантингтона, включающее фармацевтически эффективное количество нового лекарственного начала, представляющего собой, по крайней мере, одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат, или фармацевтическую композицию, содержащую новое лекарственное начало.
Предметом данного изобретения является также лекарственное средство в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для профилактики и лечения психических расстройств и шизофрении, включающее фармацевтически эффективное количество лекарственного начала, представляющего собой, по крайней мере, одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат, или фармацевтическую композицию, содержащую новое лекарственное начало.
Более предпочтительным является лекарственное средство (анксиолитик или транквилизатор) для профилактики и лечения тревожных расстройств, включающее фармацевтически эффективное количество лекарственного начала, представляющего собой, по крайней мере, одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат, или фармацевтическую композицию, содержащую новое лекарственное начало.
Более предпочтительным является лекарственное средство (ноотропик) для профилактики и лечения гиперкинетических расстройств, в частности для улучшения умственных способностей, включающее фармацевтически эффективное количество лекарственного начала, представляющего собой, по крайней мере одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат, или фармацевтическую композицию, содержащую новое лекарственное начало.
Предметом данного изобретения является также лекарственное средство в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для профилактики и лечения ожирения, включающее фармацевтически эффективное количество лекарственного начала, представляющего собой, по крайней мере, одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат, или фармацевтическую композицию, содержащую новое лекарственное начало.
Предметом данного изобретения является также терапевтический коктейль для профилактики и лечения различных заболеваний, патогенез которых связан с 5-НТ6 рецепторами у животных и людей, включающий лекарственное средство в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, включающее фармацевтически эффективное количество лекарственного начала, представляющего собой, по крайней мере одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат, или фармацевтическую композицию, содержащую новое лекарственное начало.
Предметом данного изобретения является также терапевтический коктейль для профилактики и лечения неврологических расстройств, нейродегенеративных и когнитивных заболеваний у животных и людей, в том числе для профилактики и лечения болезни Альцгеймера, болезни Паркинсона, болезни Гантингтона, психических расстройств и шизофрении, гипоксии-ишемии, гипогликемии, судорожных состояний, мозговых травм, латиризма, бокового амиотрофического склероза, ожирения и инсульта, включающий фармацевтически эффективное количество лекарственного начала, представляющего собой, по крайней мере одно из соединений общей формулы 1, 1.1, 1.1.1, 1.1.2 или его фармацевтически приемлемая соль и/или гидрат, или фармацевтическую композицию, содержащую новое лекарственное начало.
Терапевтические коктейли для профилактики и лечения невралгических расстройств, нейродегенеративных и когнитивных заболеваний у животных и людей, в том числе для профилактики и лечения болезни Альцгеймера, болезни Паркинсона, болезни Гантингтона, психических расстройств и шизофрении, гипоксии-ишемии, гипогликемии, судорожных состояний, мозговых травм, латиризма, бокового амиотрофического склероза, ожирения и инсульта наряду с лекарственными средствами по данному изобретению могут включать другие лекарственные средства, такие как: нестероидные противовоспалительные препараты (Ортофен, Индометацин, Ибупрофен и т.п.); ингибиторы ацетилхолинэстеразы (Такрин, Амиридин, Физостигмин, Арисепт, Phenserine и т.п.); эстрогены (например, Эстрадиол); антагонисты NMDA-рецепторов (например, Мемантин, Neramexane); ноотропные препараты (например, Пирацетам, Фенибут и т.п.); модуляторы АМРА рецепторов (например, Ampalex); антагонисты каннабиноидных рецепторов СВ-1 (например, Rimonabant); ингибиторы моноаминооксидазы МАО-В и/или МАО-А (например, Rasagiline); антиамилоидогенные препараты (например, Tramiprosate); вещества, понижающие нейротоксичность бета-амилоида (например, Индол-3-пропионовая кислота); ингибиторы гамма- и/или бета-Секретазы; агонисты мускариновых рецепторов M1 (например, Cevimeline); хелаторы металлов (например, Clioquinol); антагонисты ГАМК(В) рецепторов (например, CGP-36742); моноклональные антитела (например, Bapineuzumab); антиоксиданты; нейротрофические агенты (например, Церебролизин); антидепрессанты (например, Имипрамин, Сертралин и т.п.) и прочие.
Терапевтический коктейль для понижения избыточного веса и лечения ожирения наряду с лекарственными средствами по данному изобретению включает другие лекарственные средства, такие как анорексические препараты (например, Фепранон, Дезопимон, Мазиндол), гормональные препараты (например, Тиреоидин), гиполипидимические средства, такие как фибраты (например, Фенофибрат), статины (например, Ловастатин, Симвастатин, Правастатин и Пробукол), а также гипогликемические препараты (сульфонилмочевины - например, Бутамид, Глибенкламид; бигуаниды - например, Буформин, Метморфин) и препараты с другим механизмом действия, такие как антагонисты каннабиноидных СВ-1 рецепторов (Rimonabant), ингибиторы обратного захвата норэпинефрина и серотонина (Sibutramine), ингибиторы ферментов синтеза жирных кислот (Orlistat) и прочие наряду с антиоксидантами, пищевыми добавками и т.д.
В соответствии с данным изобретением способ профилактики и лечения различных заболеваний центральной нервной системы, патогенез которых связан с 5-НТ6 рецепторами у животных и людей, заключается во введении фармацевтически эффективного количества нового лекарственного начала, новой фармацевтической композиции, нового лекарственного средства или нового терапевтического коктейля.
Лекарственные средства могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно). Клиническая дозировка лекарственного начала (субстанции), фармацевтической композиции или лекарственного средства, включающих фармацевтически эффективное количество лекарственного начала, у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 10~500 мг, предпочтительно - 50~300 мг. Поэтому во время приготовления фармацевтических композиций по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10~500 мг, предпочтительно - 50~300 мг. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно - от одного до шести раз).
Изобретение поясняется чертежами.
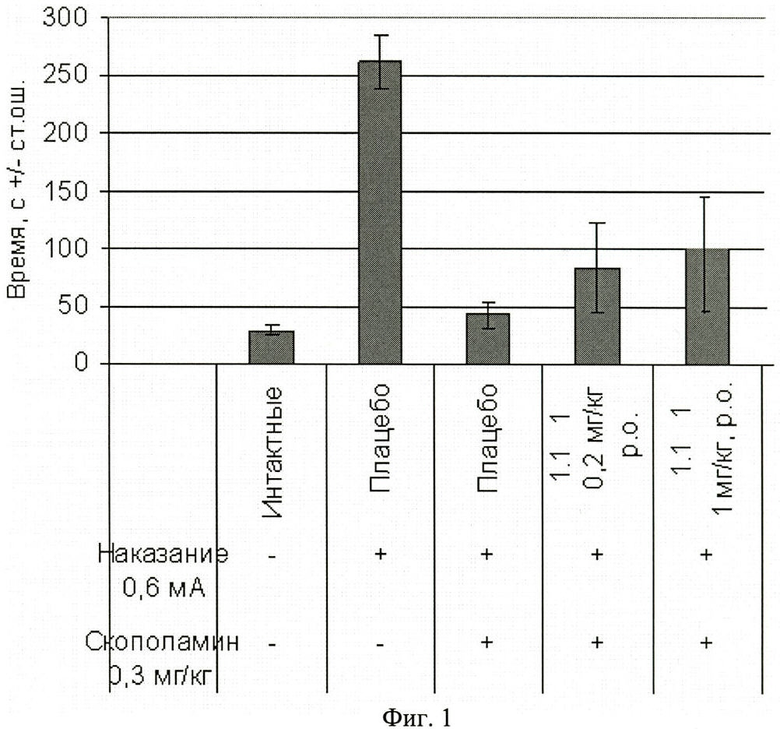
Фиг.1. Латентный период 1-го захода в темный отсек через 24 часа после обучения крыс избеганию темного отсека в челночной камере (средняя величина ± стандартная ошибка). Число в скобках - доза вещества в мг/кг. Изучавшееся вещество 1.1.1 вводили внутрь за 60 минут до опыта. Отличие от группы, получавшей скополамин: * - p<0,05; ** - p<0,01; *** - p<0,001.
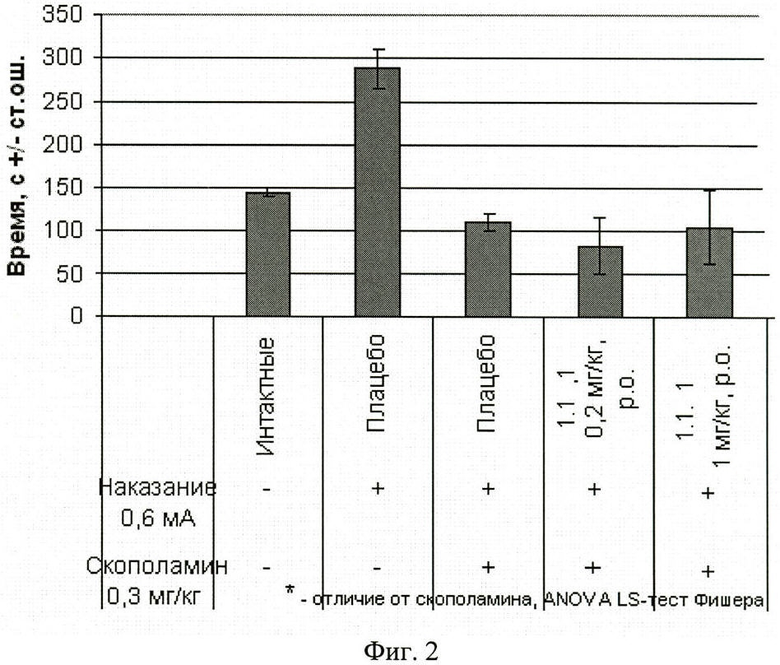
Фиг.2 Продолжительность пребывания в светлом отсеке через 24 часа после обучения крыс избеганию темного отсека в челночной камере (средняя величина ± стандартная ошибка). Число в скобках - доза вещества в мг/кг. Изучавшееся вещество 1.1.1 вводили внутрь за 60 минут до опыта. Отличие от группы, получавшей скополамин: * - p<0,05; ** - p<0,01;*** - p<0,001.
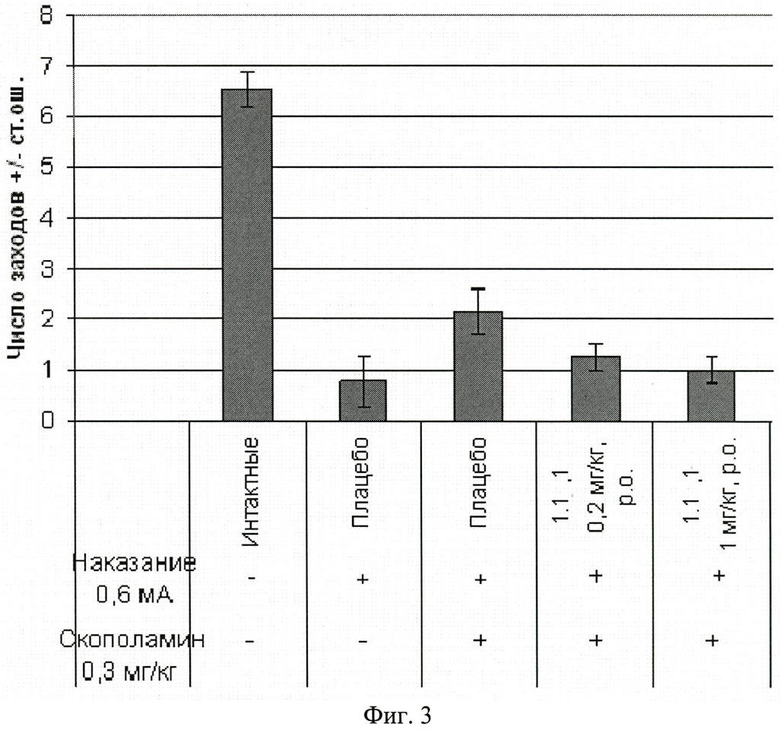
Фиг.3. Число заходов в темный отсек через 24 часа после обучения крыс избеганию темного отсека в челночной камере (средняя величина ± стандартная ошибка). Число в скобках - доза вещества в мг/кг. Изучавшееся вещество 1.1.1 вводили внутрь за 60 минут до опыта. Отличие от группы, получавшей скополамин: * - p<0,05; *** p<0,001.
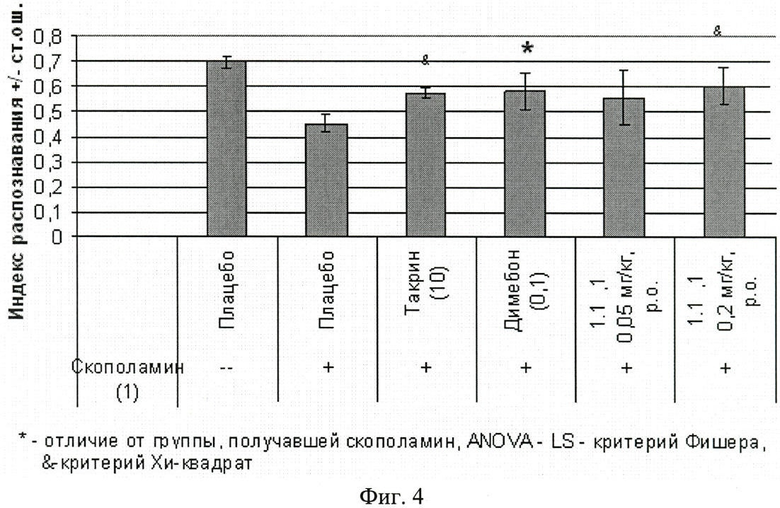
Фиг.4. Результаты теста на распознавание новых объектов на мышах (среднее значение ± стандартная ошибка). В скобках приведены значения доз веществ в мг/кг. Изучавшееся вещество 1.1.1 вводили внутрь за 60 минут до теста. Отличие от группы, которой вводили только скополамин: * - p<0,05 в соответствии с критерием χ2.
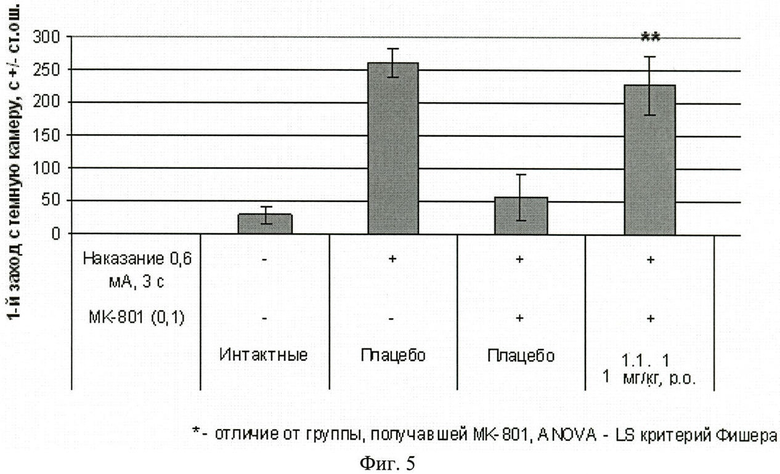
Фиг.5. Латентный период 1-го захода в темный отсек через 24 часа после обучения крыс избеганию темного отсека в челночной камере (средняя величина ± стандартная ошибка). Число в скобках - доза вещества в мг/кг. Изучавшееся вещество 1.1.1 вводили внутрь за 60 минут до опыта. Отличие от группы, получавшей МК-801: * - p<0,05; ** - p<0,01; *** - p<0,001.
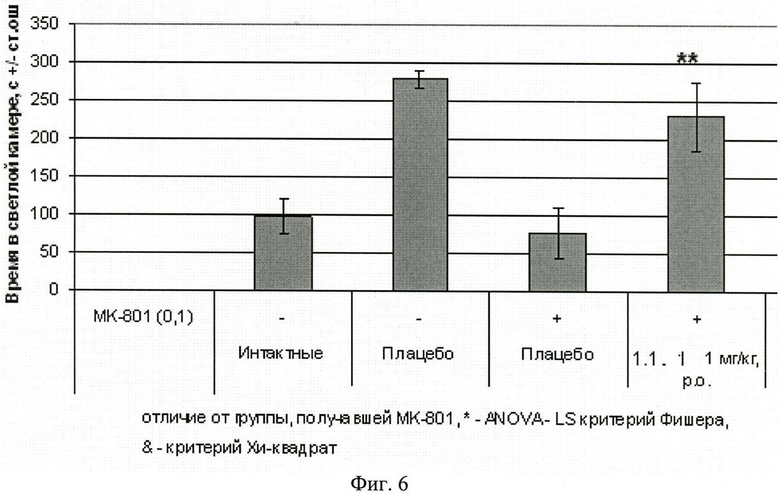
Фиг.6. Продолжительность пребывания в светлом отсеке через 24 часа после обучения крыс избеганию темного отсека в челночной камере (средняя величина ± стандартная ошибка). Число в скобках - доза вещества в мг/кг. Изучавшееся вещество 1.1.1 вводили внутрь за 60 минут до опыта. Отличие от группы, получавшей МК-801: * - p<0,05; ** - p<0,01;*** - p<0,001.
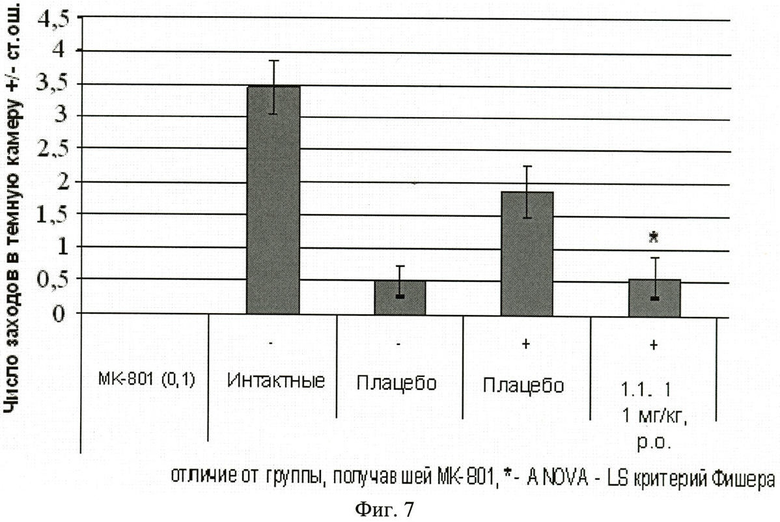
Фиг.7. Число заходов в темный отсек через 24 часа после обучения крыс избеганию
темного отсека в челночной камере (средняя величина ± стандартная ошибка). Число в скобках - доза вещества в мг/кг. Изучавшееся вещество 1.1.1 вводили внутрь за 60 минут до опыта. Отличие от группы, получавшей МК-801: * - p<0,05; *** p<0,001.
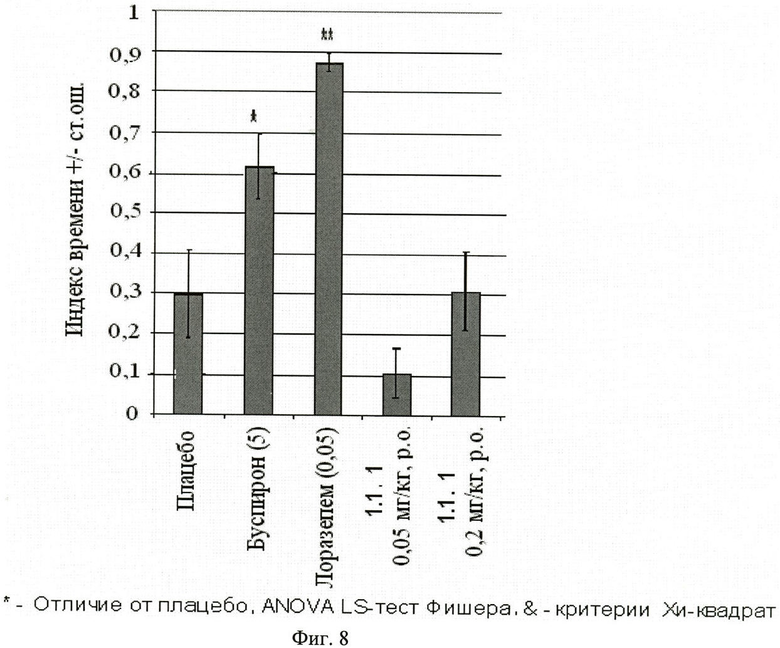
Фиг.8. Отношение времени, проведенного животными в открытых рукавах, к общему времени пребывания в открытых и закрытых рукавах (среднее ± стандартная ошибка). В скобках приведены дозы вещества 1.1.1 (в мг/кг). Отличие от групп, получавших плацебо: * - p<0,05; ** - p<0,01; *** - p<0,001.
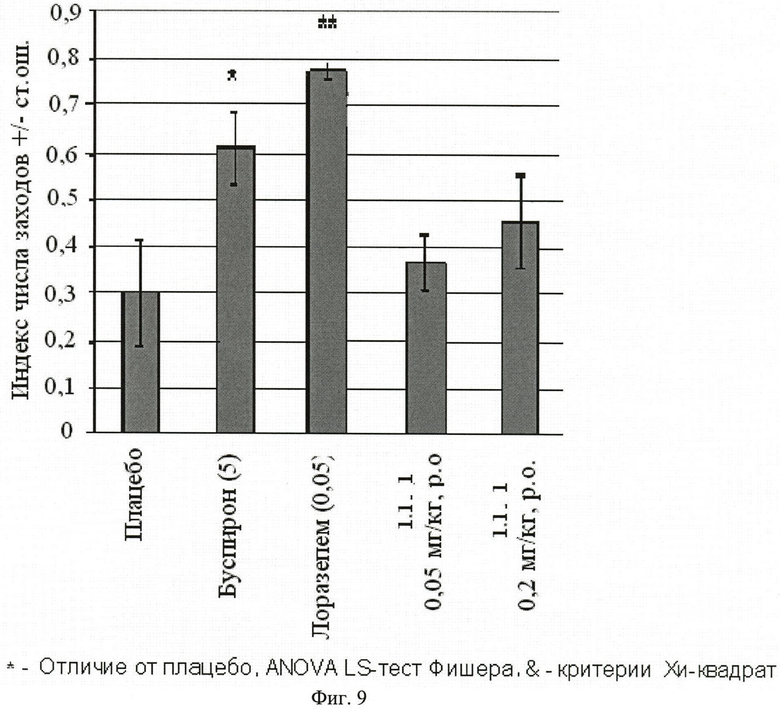
Фиг.9. Отношение числа входов в открытые рукава к общему числу входов в рукава обоих типов (среднее ± стандартная ошибка). В скобках приведены дозы вещества 1.1.1 (в мг/кг). Отличие от групп, получавших плацебо: * - p<0,05; ** - p <0,01; *** - p<0,001.
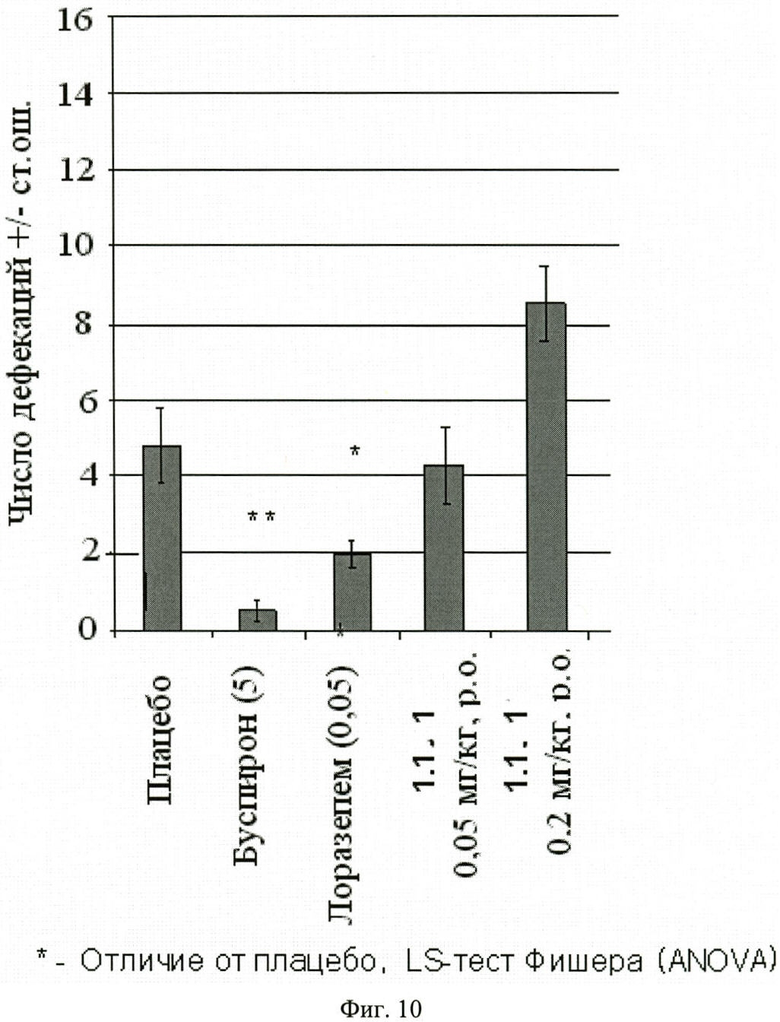
Фиг.10. Число дефекаций в тесте «лабиринт-плюс» (среднее ± стандартная ошибка). В скобках приведены дозы вещества 1.1.1 (в мг/кг). Отличие от групп, получавших плацебо: * - p<0,05; ** - p<0,01; *** - p<0,001.
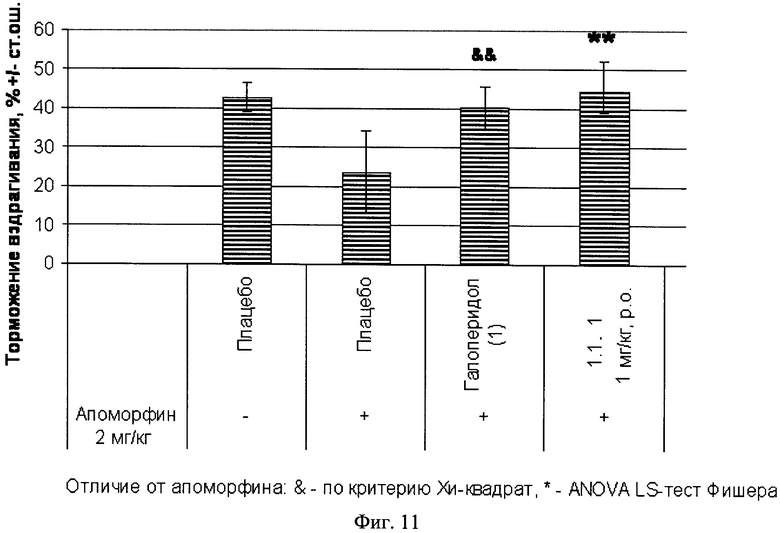
Фиг.11. Результаты теста препульсного торможения вздрагивания у мышей.
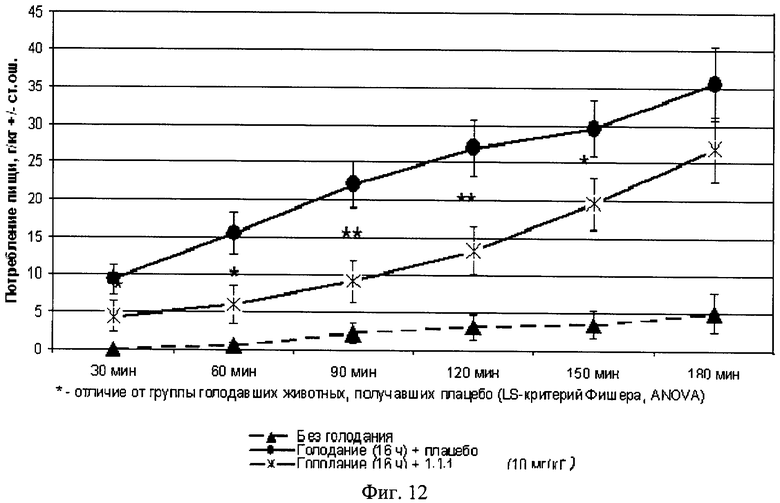
Фиг.12. Результаты теста проверки аппетита у крыс.
Представленные ниже примеры не ограничивают данное изобретение.
Пример 1. Общий способ получения N-(3-арилсульфонил-2-олкиламино)пиразоло[1,5-а]пиримидин-6-ил)ацетамидов общей формулы 1 (R3=Н, R4=Ас). Перемешивают при 100°С 3 часа 0,637 мол. дикетона 3 и 0,606 моль 4-(арилсульфонил)-1H-пиразол-3,5-диамина 2 в 650 мл АсОН. После охлаждения реакционной массы выпавший белый кристаллический осадок отфильтровывают, промывают уксусной кислотой, эфиром и сушат на воздухе. Получают соединения общей формулы 1(R3=Н, R4=Ас) с выходом 80-85%.
Пример 2. Общий способ получения 3-арилсульфонил-N(2)-алкилпиразоло[1,5-а]пиримидин-2,6-диаминов общей формулы 1 (R3=R4=Н). К суспензии 0.29 г N-(3-арилсульфонил2-метиламино)пиразоло[1,5-а]пиримидин-6-ил)ацетамида 1.1 (R3=Н, R4=Ac) в 1350 мл смеси МеОН: Н2О (3:1) добавляют 135 г КОН. Реакционную массу кипятят при перемешивании в течение 72 часов. После окончания реакции (контроль по LC-MS) образовавшийся осадок отфильтровывают и промывают затем водой. Получают соединения общей формулы 1 (R3=R4=Н) с выходом 92-95%.
Пример 3. Общий способ получения 3-арилсульфонил-N(2),N(6),N(6)-триалкил-пиразоло[1,5-д]пиримидин-2,6-диаминов общей формулы 1 (R3=R4=СН3). К суспензии 0.25 мол. 3-арилсульфонил-N(2)-метилпиразоло[1,5-а]пиримидин-2,6-диаминов 1.1 (R3=R4=Н) в 3750 мл этилового спирта добавляют 67 г серной кислоты в 230 мл воды (3М раствор). Полученную суспензию нагревают до 90°С, а затем охдаждают до комнатной температуры, приливают 116,5 г 35%го раствора формалина. Через 30 минут при интенсивном перемешивании постепенно присыпают маленькими порциями 56 г NaBH4, так чтобы температура раствора оставалась не выше 25°С (при необходимости охлаждают водяной баней). После окончания реакции (контроль по LC-MS) осадок отфильтровывают и тщательно промывают водой. Спиртовой маточник упаривают в вакууме, а полученный при этом осадок также промывают водой. Суммарный выход продукта 1 (R3=R4=СН3) составляет 95-97%.
В таблице 2 представлены некоторые примеры новых 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диаминнов общей формулы 1 и данные их LCMS анализов и спектров ЯМР.
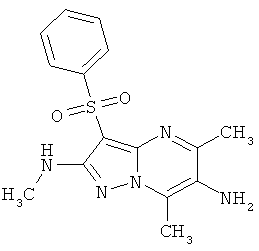
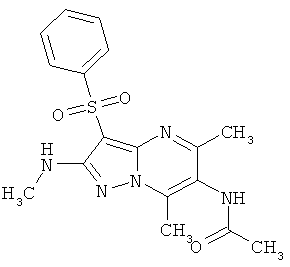
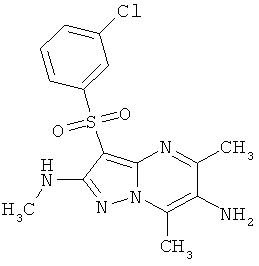
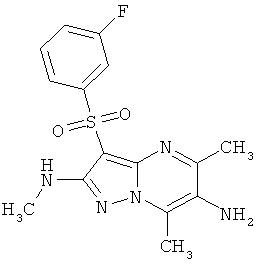
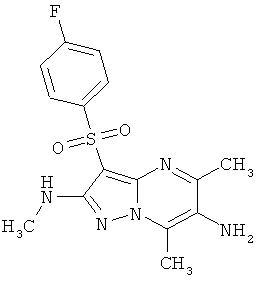
Пример 4. Определение антагонистической активности соединений общей формулы 1 по отношению к 5-НТ6 рецепторам. Соединения общей формулы 1 были испытаны на их способность препятствовать активации 5-НТ6 рецепторов серотонином. Использовали клетки НЕК 293 (клетки почки человеческого эмбриона) с искусственно экспрессированным рецептором 5-НТ6, активация которого серотонином приводит к повышению концентрации внутриклеточного цАМФ. Содержание внутриклеточного цАМФ определяли с помощью реагентного набора LANCE cAMP (PerkinElmer), по методике, описанной производителем набора [http://las.perkinelmer.com/content/Manuals/MAN_LANCEcAMP384K.itUser.pdf]. Эффективность соединений оценивали по их способности снижать содержание внутриклеточного цАМФ, индуцированного серотонином. В таблице 3 представлена антагонистическая активность соединений общей формулы 1 к серотониновым 5-НТ6 рецепторам в условиях функционального эссея, подтверждающая их умеренную или высокую активность.
Пример 5. Определение активности соединений общей формулы 1 в условиях конкурентного связывания с серотониновыми 5-НТ6 рецепторами. Для проведения скрининга веществ на их потенциальную способность взаимодействовать с серотониновым рецептором 5-НТ6 использовали метод радиолигандного связывания. Для этого готовили мембранные препараты из клеток HeLa, экспрессирующих рекомбинантный человеческий 5-НТ6 рецептор, путем гомогенизирования рекомбинантных клеток в стеклянном гомогенизаторе с последующим отделением плазматических мембран от ядер, митохондрий и клеточных обломков путем дифференциального центрифугирования. Определение связывания изучаемых соединений с 5-НТ6 рецептором проводили в соответствии с методикой, описанной в [Monsma FJ Jr, Shen Y, Ward RP, Hamblin MW and Sibley DR, Cloning and expression of a novel serotonin receptor with high affinity for tricyclic psychotropic drugs. Mol Pharmacol. 43:320-327, 1993]. В предпочтительном исполнении мембранные препараты инкубировали с меченым лигандом (1.5 nM [3H] Lysergic acid diethylamide) без и в присутствии исследуемых соединений в течение 120 минут при 37°С в среде, состоящей из 50 mM Tris-HCl, рН 7.4, 150 тМ Nad, 2 тМ Ascorbic Acid, 0.001% BSA. Образцы после инкубации фильтровали под вакуумом на стекломикроволоконных фильтрах G/F (Millipor, USA), фильтры трижды промывали холодным раствором среды и радиоактивность измеряли с помощью сцинтилляционного счетчика MicroBeta 340 (PerkinElmer, USA). Неспецифическое связывание, которое составляло 30% от общего связывания, определяли инкубацией мембранных препаратов с радиолигандом в присутствии 5 цМ Serotonin (5-HT). В качестве положительного контроля использовали Methiothepin. Связывание тестируемых соединений с рецептором определялось по их способности вытеснять радиоактивный лиганд и выражалось в процентах вытеснения. Процент вытеснения определялся по следующей формуле:
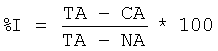 ,
,
где ТА - это общая радиоактивность в присутствии только радиоактивного лиганда, СА - это радиоактивность в присутствии радиолиганда и тестируемого соединения и NA - это радиоактивность в присутствии радиолиганда и серотонина (5 µM).
В таблице 4 представлены результатов испытаний соединений общей формулы 1, свидетельствующие об их высокой активности по отношению к серотониновым 5-НТ6 рецепторам.
Пример 6. Получение лекарственного средства в форме таблеток. Смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг соединения 1.1.1 и спрессовывают в брусок. Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетируют в подходящую форму таблетки весом 560 мг каждая.
Пример 7. Получение лекарственного средства в форме капсул. Тщательно смешивают соединение 1.1.1 с порошком лактозы в соотношении 2:1. Полученную порошкообразную смесь упаковывают по 300 мг в желатиновые капсулы подходящего размера.
Пример 8. Получение лекарственного средства в форме инъекционных композиций для внутримышечных, внутрибрюшинных или подкожных инъекций. Смешивают 500 мг соединения 1.1.1 с 300 мг хлорбутанола, 2 мл пропиленгликоля и 100 мл инъекционной воды. Полученный раствор фильтруют и помещают по 1 мл в ампулы, которые запаивают.
Пример 9. Антиамнестическая активность соединений общей формулы 1 (ноотропное действие).
9.1. Улучшение памяти, нарушенной скополамином.
9.1.1. Ноотропное действие соединений общей формулы 1 в тесте «Пассивное избегание в челночной камере». Эксперименты проводились на взрослых самцах мышей линии BALB/c массой 20-25 г или самцах крыс линии Вистар массой 200-250 г.
В опыте использовалась челночная камера (Ugo Basile, Италия), которая состояла из двух отсеков. Все стенки одного из отсеков были непрозрачными, а второй отсек имел прозрачную крышку. Отсеки соединялись отверстием, которое закрывалось автоматической вертикальной дверцей. Пол темного отсека состоял из поперечных металлических прутьев, на которые могли подаваться импульсы постоянного тока.
В первый день опыта за 30 минут до обучения животным внутрибрюшинно вводили скополамин, который вызывает нарушение памяти. Животным опытной группы дополнительно вводили соединение общей формулы 1, например, соединение 1.1.1, в дозах 0,2 мг/кг. Животные контрольной группы получали инъекцию физиологического раствора. В каждой группе использовалось 8 животных.
Животных помещали в светлый отсек и регистрировали латентный период первого захода в темную камеру. При этом дверцу между камерами закрывали, и животное в течение 3 секунд получало наказание током 0,6 мА. После этого животное возвращали в жилую клетку. Через 24 часа животное вновь помещали в светлый отсек челночной камеры и регистрировали латентный период первого захода в темную камеру, общее время пребывания в светлой камере и число заходов в темную камеру. Продолжительность наблюдения составляла 5 минут.
Животные контрольной группы, получившие наказание в темном отсеке, демонстрировали успешную обучаемость, которая выражалась в увеличении латентного периода захода в темный отсек, длительности пребывания в светлом отсеке и уменьшении числа заходов в темную камеру по сравнению с животными из группы, не получавшей наказания. Скополамин вызывал так называемую антероградную амнезию, которая характеризуется нарушением фиксации в долгосрочной памяти новых событий. Это выражалось в виде статистически значимого увеличения латентного периода захода в темный отсек, уменьшения времени пребывания в светлом отсеке и увеличения числа заходов в темный отсек камеры. Результаты эксперимента, представленные на фиг.1, 2, 3, показали, что в тесте пассивного избегания соединения общей формулы 1, в том числе соединение 1.1.1, обладало способностью уменьшать амнезию (улучшать память), вызванную скополамином.
9.1.2. Ноотропное действие соединений общей формулы 1 в тесте «Распознавание новых объектов».
Эксперимент проводили на взрослых самцах мышей линии SHK. В эксперименте использовали крестообразный плексигласовый лабиринт, который состоял из 4-х тупиковых боковых камер (пронумерованных 1, 2, 3, 4), соединявшихся между собой через пятую центральную камеру. Мышь помещали в центральную камеру и позволяли исследовать лабиринт. Пол очищался после каждого животного. Порядок посещения камер и время визитов регистрировались наблюдателем. Тест заканчивался, когда происходило 13 заходов в тупики. Критерием захода считалось наличие всех четырех лап животного внутри камеры.
Во время обучения животное помещали в лабиринт, в котором в каждой из четырех боковых камер находились по одной одинаковой чашке. Во время теста (спустя 1 час после обучения) две противоположно стоящих чашки были заменены колбами, и животному было позволено исследовать лабиринт. В периоды обучения и тестирования регистрировали время, проведенное животным в каждой боковой камере. Рассчитывали индекс распознавания новых объектов как отношение времени, проведенного в боковых камерах с новыми объектами, к общему времени пребывания в боковых камерах. Появление нового объекта увеличивает время, проведенное животным в камере, по сравнению с фазой обучения (так называемый эффект распознавания новых объектов). Под действием скополамина в дозе 1 мг/кг, введенного внутрибрюшинно за 30 минут до начала обучения, распознавание новых объектов нарушалось, и индекс распознавания снижался. Однако это влияние скополамина удавалось предотвратить внутрибрюшинным введением димебона (0,1 мг/кг) за 5 минут до начала обучения, такрина (10 мг/кг) за 30 мин до начала обучения и соединений общей формулы 1 в дозах 0,05 мг/кг и 0,2 мг/кг за 60 мин до начала обучения.
Из полученных результатов, представленных на фиг.4, следует, что соединение 1.1.1 предупреждает нарушение памяти, вызванное скополамином.
9.2. Улучшение памяти, нарушенной МК-801.
Ноотропное действие соединений общей формулы 1 в тесте «Пассивное избегание в челночной камере».
Эксперимент проводили так же, как описано в примере 10.1.1. В первый день опыта за 30 минут до обучения животным внутрибрюшинно вводили МК-801 (0,1 мг/кг), вызывающий амнезию. Предварительное введение МК-801 значительно снижает эффект обучения, то есть вызывает антероградную амнезию. Параллельно независимым группам мышей до обучения внутрибрюшинно вводили МК-801 в сочетании с исследуемыми соединениями общей формулы 1.
Результаты эксперимента, представленные на фиг.5, 6 и 7, свидетельствуют, что соединение 1.1.1, введенное внутрибрюшинно до начала обучения в дозах 0,2 мг/кг и 1 мг/кг, обладает способностью уменьшать амнезию, вызванную МК-801.
Пример 10. Анксиолитическая активность соединений общей формулы 1 в тесте «Поведение мышей в приподнятом крестообразном лабиринте».
В эксперименте использовали самцов мышей линии BALB/c массой приблизительно 25 г.Животных содержали в клетках (по 5-7 мышей на клетку), обеспечивая свободный доступ к корму и воде. Ни одно из животных не было до этого знакомо с экспериментальной установкой. Каждая экспериментальная группа включала 8 животных.
Использованный метод был ранее описан Листером (Lister R.G. The use of a plus-maze to measure anxiety in the mouse. Psychopharmacology, 1987; 92:180-185). Плексигласовая установка состояла из двух открытых рукавов размером 30×5 см и двух закрытых рукавов размером 30×5×15 см. Боковые рукава были закрыты прозрачным плексигласом и соединялись с центральной площадкой размером 5×5 см. Открытые рукава, центральная платформа и пол были выполнены из черного плексигласа. Аппарат был смонтирован на металлическом основании, которое располагалось над уровнем пола на высоте 38,5 см.
Животным вводили внутрибрюшинно плацебо, буспирон (5 мг/кг за 30 минут до обучения), лоразепам (0,05 мг/кг за 60 минут до обучения) или одно соединений общей формулы 1, например, соединение 1.1.1, в дозе 0,05 мг/кг и 0,2 мг/кг. Буспирон и лоразепам вводили в максимальной эффективной дозе, при которой еще не наблюдалось побочного седативного действия, которое выражалось в виде общего снижения исследовательской активности (число визитов в рукава за время теста).
Каждую мышь помещали в центр лабиринта головой к открытому рукаву. На протяжении 5 минут регистрировали последовательность и продолжительность заходов в рукава с помощи компьютерной программы. Критерием захода считали нахождение всех четырех лап животного в рукаве. Рассчитывали индекс предпочтения как отношение времени, проведенного животным в открытых камерах, а также числа заходов в открытые рукава, к общему времени пребывания в открытых и закрытых рукавах или соответственно к общему числу заходов в рукава обоих типов. Число фекальных болюсов, оставленных мышью, рассматривалось как дополнительный параметр, характеризующий состояние тревоги.
Результаты испытаний, представленные на фиг.8, 9 и 10, показали, что соединения общей формулы 1, в том числе соединение 1.1.1, как и стандарты (буспирон и лоразепам), оказывало выраженное анксиолитическое действие в тесте приподнятого крестообразного лабиринта.
Пример 11. Антипсихотическая активность соединений общей формулы 1 в тесте «Препульсное торможение вздрагивания у мышей». В экспериментах использовали мышей линии SHK массой 24-30 г.Эксперименты проводили в светлое время суточного цикла животных. Апоморфина гидрохлорид и галоперидол были получены от компании Сигма Кемикалз, США. Апоморфина гидрохлорид растворяли в 0,1% растворе аскорбиновой кислоты, приготовленном на стерилизованной воде, и вводили подкожно за 15 минут до теста. Галоперидол растворяли в стерилизованной воде с использованием эмульгатора Твин 80 и вводили внутрибрюшинно за 60 минут до теста. Соединения общей формулы 1 растворяли в стерилизованной воде и вводили подкожно за 60 минут до теста. Объем вводимой жидкости составлял 10 мл/кг. Контрольным животным вводили 0,1% раствор аскорбиновой кислоты, приготовленный на стерилизованной воде с Твином 80. Аппарат состоял из камеры, выполненной из прозрачного плексигласа (производитель - компания Коламбус Инструменте, США), размещенной на платформе, которая находилась внутри звукоизолирующего кабинета. В 2 см от платформы находилась высокочастотная звуковая колонка, через которую передавались звуковые стимулы. При вздрагивании животного возникали колебания платформы, которые улавливались аналоговым преобразователем и регистрировались компьютером. Уровень фонового шума составлял 65 дБ. Животные получали по 4 предъявления одиночного тестирующего («пульсового») стимула длительностью 50 мс и громкостью 105 дБ или предваряющего («пре-пульсового») стимула длительностью 20 мс громкостью 85 дБ, за которым через 30 мс следовал пульсовой стимул длительностью 50 мс громкостью 105 дБ. Интервал между повторными предъявлениями пульсового или пре-пульсового в сочетании с пульсовым стимулов составлял 10 с. Ослабление вздрагивания в ответ на пульсовой стимул при наличии пре-пульсового стимула рассчитывали в процентах по отношению к амплитуде вздрагивания в ответ на изолированный пульсовой стимул. Введение апоморфина, который используется в экспериментах на животных для моделирования психотоподобных состояний, вызывало уменьшение препульсного торможения вздрагивания, что отражает снижение способности ЦНС фильтровать сенсорные стимулы. Результаты эксперимента, представленные на фиг.11, показывают, что галоперидол (1 мг/кг) и изучавшиеся соединения общей формулы 1, в том числе соединение 1.1.1 (1 мг/кг), предупреждало нарушение препульсного торможения вздрагивания при введении апоморфина.
Пример 12. Тест проверки аппетита.
Самцов крыс линии Вистар, весивших 230-360 г, помещали в стандартные жилые клетки, где они имели постоянный свободный доступ к воде и пище за исключением коротких периодов пищевой депривации (16 часов) непосредственно перед тестом аппетита. Тест аппетита проводили в индивидуальных клетках с верхней крышкой из проволоки, в нишу которой помещали порцию пищевых гранул. Массу гранул определяли через каждые 30 минут в течение 3 часов. На основании этих измерений оценивали потребление пищи, которое выражали в граммах корма на килограмм массы тела. Плацебо и соединение 1.1.1. (в дозе 10 мг/кг) вводили внутрибрюшинно за 60 минут до теста. В каждой группе было по 10 крыс. Вещества растворяли в стерильной воде. Объем вводимой жидкости составлял 10 мл/кг. В качестве контрольных групп использовали интактных животных, не подвергавшихся пищевой депривации, и животных после пищевой депривации, которым вводили стерилизованную воду. Результаты эксперимента, представленные на фиг.12, показывают, что изучавшиеся соединения общей формулы 1, в том числе соединение 1.1.1 (10 мг/кг), предупреждало повышение аппетита у крыс.
Данное изобретение относится к новым замещенным 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диаминам общей формулы 1, их фармацевтически приемлемым солям и/или гидратам, которые обладают свойствами антагонистов серотониновых 5-НТ6 рецепторов и могут быть использованы при лечении и предупреждении развития различных заболеваний центральной нервной системы, патогенез которых связан с 5-НТ6 рецепторами, в частности болезни Альцгеймера, болезни Паркинсона, болезни Гангтинтона, шизофрении, других нейродегенеративных заболеваний, когнитивных и тревожных расстройств и ожирения. В общей формуле 1:
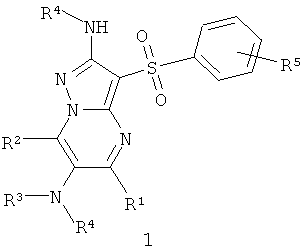
R1, R2 и R4 необязательно одинаковые, независимо друг от друга, представляют собой C1-С3алкил; R3 и R4, необязательно одинаковые, представляют собой: атом водорода, необязательно замещенный C1-С3алкил или ацетил; R5 представляет собой атом водорода или атом галогена. 8 н. и 5 з.п. ф-лы, 12 ил., 4 табл.
1. Замещенные 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамины общей формулы 1 и их фармацевтически приемлемые соли и/или гидраты
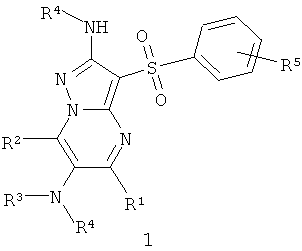
где R1, R2 и R4 необязательно одинаковые независимо друг от друга представляют собой C1-С3алкил;
R3 и R4 необязательно одинаковые представляют собой: атом водорода, необязательно замещенный C1-С3алкил или ацетил;
R5 представляет собой атом водорода или атом галогена.
2. Соединения по п.1, представляющие собой 5,7,N(2)-триметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамины общей формулы 1.1
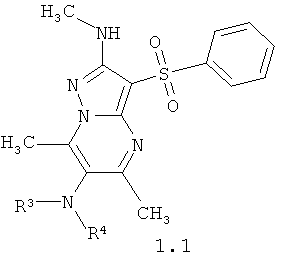
где R3 и R4 имеют вышеуказанное значение.
3. Соединения по любому из пп.1 и 2, представляющие собой 5,7,N(2)-триметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамин 1.1.1 и 5,7,N(2),N(6),N(6)-пентаметил-3-фенилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамин 1.1.2.
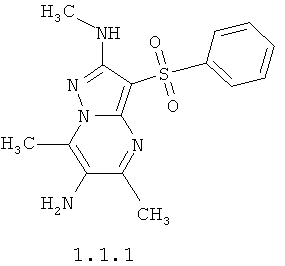
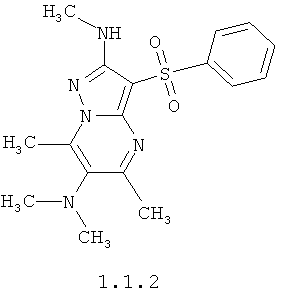
4. Средство, представляющее собой замещенные 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамины по любому из пп.1-3, обладающее свойствами антагонистов серотониновых 5-НТ6 рецепторов.
5. Средство, представляющее собой замещенные 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамины по любому из пп.1-3, для изучения молекулярного механизма взаимодействия с серотониновыми 5-НТ6 рецепторами.
6. Средство, представляющее собой замещенные 3-арилсульфонил-пиразоло[1,5-а]пиримидин-2,6-диамины по любому из пп.1-3, в качестве лекарственного начала для фармацевтических композиций и лекарственных средств.
7. Фармацевтическая композиция, обладающая свойствами антагонистов серотониновых 5-НТ6 рецепторов, пригодная для лечения и предупреждения развития состояний и заболеваний центральной нервной системы, содержащая фармацевтически эффективное количество лекарственного начала по п.6.
8. Способ получения фармацевтической композиции по п.7 смешением с инертным наполнителем и/или растворителем лекарственного начала по п.6.
9. Лекарственное средство в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для профилактики и лечения заболеваний центральной нервной системы, патогенез которых связан с 5-НТ6 рецепторами, включающее фармацевтически эффективное количество лекарственного начала по п.6 или фармацевтической композиции по п.7.
10. Лекарственное средство по п.9 для профилактики и лечения когнитивных расстройств и нейродегенеративных заболеваний.
11. Лекарственное средство по п.9 для профилактики и лечения психических расстройств.
12. Лекарственное средство по п.9, обладающее анксиолитической активностью, для профилактики и лечения тревожных расстройств.
13. Лекарственное средство по п.9, обладающее ноотропной активностью, для улучшения умственных способностей.
14. Лекарственное средство по п.9 для профилактики и лечения ожирения.
15. Способ профилактики и лечения заболеваний центральной нервной системы, патогенез которых связан с 5-НТ6 рецепторами, заключающийся во введении в эффективном количестве лекарственного начала по п.6, или фармацевтической композиции по п.7, или лекарственного средства по любому из пп.9-14.
| WO 2001016111 A2, 08.03.2001 | |||
| KIM HYE; JUNG et al., "New Serotonine 5-HT6 Ligands from Common Feature Pharmacophore Hypotheses" J | |||
| of Chemical Information and Modeling, 2008,48(1), 197-206 | |||
| N-ПИРАЗОЛИЛ-1,2,4-ТРИАЗОЛО-[1,5-С]-ПИРИМИДИН-2-СУЛЬФОНАМИДНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТЬЮ | 1992 |
|
RU2065861C1 |
| 1-N-АЛКИЛ-N-АРИЛПИРИМИДИНАМИНЫ, СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2153494C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИАЗОЛОВ, КОНЕЧНЫЕ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ СПОСОБА | 1996 |
|
RU2156760C2 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| RU 2008139495, 06.10.2008. | |||
Авторы
Даты
2011-06-20—Публикация
2010-02-26—Подача