ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к усовершенствованиям в области доставки лекарственного средства. Более конкретно, это изобретение относится к полипептидам, конъюгатам и фармацевтическим композициям, содержащим полипептиды или конъюгаты согласно изобретению. Настоящее изобретение также относится к применению этих полипептидов и конъюгатов для транспорта соединения или лекарственного средства через гематоэнцефалический барьер млекопитающего и для лечения и диагностики неврологических заболеваний.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
При разработке нового лекарственного средства от патологий головного мозга гематоэнцефалический барьер (ГЭБ) считается основным препятствием для потенциального применения лекарственных средств для лечения нарушений центральной нервной системы (ЦНС). Всемирный рынок лекарственных средств для ЦНС в 1998 году составлял $33 миллиардов, что составляло приблизительно половину глобального рынка лекарственных средств для сердечно-сосудистой системы, несмотря на то, что в США нарушениями ЦНС страдает вдвое больше людей, чем сердечно-сосудистыми заболеваниями. Причина этого несоответствия состоит в том, что более 98% всех потенциальных лекарственных средств для ЦНС не преодолевают гематоэнцефалический барьер. Кроме того, более 99% всемирной разработки лекарственных средств для ЦНС посвящено исключительно изобретению лекарственных средств для ЦНС и менее 1% направлено на доставку лекарственного средства в ЦНС. Это соотношение может объяснить причину отсутствия доступного в настоящее время эффективного лечения основных неврологических заболеваний, таких как опухоли мозга, болезнь Альцгеймера и инсульт.
Головной мозг защищен от потенциально токсических веществ наличием двух барьерных систем: гематоэнцефалического барьера (ГЭБ) и гематоликворного барьера (BCSFB). Полагают, что ГЭБ является основным путем для захвата сывороточных лигандов, поскольку площадь его поверхности приблизительно в 5000 раз выше, чем площадь поверхности BCSFB. Эндотелий головного мозга, который образует ГЭБ, представляет собой основное препятствие для применения потенциальных лекарственных средств против многих нарушений ЦНС. В качестве общего правила, через ГЭБ, т.е. из крови в головной мозг, могут проходить только липофильные молекулы приблизительно менее 500 Дальтон. Однако размер многих лекарственных средств, для которых показаны перспективные результаты в исследованиях в отношении лечения нарушений ЦНС на животных, является значительно более высоким. Таким образом, транспорт пептидных и белковых лекарственных средств из крови в головной мозг главным образом исключен вследствие очень низкой проницаемости клеточной стенки капилляров головного мозга для этих лекарственных средств. Эндотелиальные клетки капилляров головного мозга (BCEC) плотно скреплены посредством плотных межклеточных контактов, они обладают малым количеством отверстий и малым количеством эндоцитозных везикул по сравнению с капиллярами других органов. BCEC окружены внеклеточным матриксом, астроцитами, перицитами и клетками микроглии. Тесная связь эндотелиальных клеток с опорными отростками астроцита и базальной мембраной капилляров важна для развития и поддержания свойств ГЭБ, которые обеспечивают строгий контроль обмена кровь-головной мозг.
В международной публикации WO 2004/060403 описано изобретение авторов изобретения, касающееся молекул для транспорта лекарственного средства через гематоэнцефалический барьер. К настоящему времени не существует иного подхода для доставки лекарственного средства, пригодной для головного мозга. Исследуемые способы доставки пептидного и белкового лекарственного средства в головной мозг можно подразделить на три принципиальных стратегии. Во-первых, инвазивные способы включают в себя прямое внутрижелудочковое введение лекарственных средств посредством хирургической операции и временное повреждение ГЭБ посредством инфузии в сонную артерию гиперосмолярных растворов. Во-вторых, основанная на фармакологии стратегия состоит в упрощении прохождения через ГЭБ посредством повышения растворимости пептидов или белков в липидах. В-третьих, в основанных на физиологии стратегиях используют различные транспортные механизмы в ГЭБ, которые были описаны в последние годы. В этом подходе лекарственные средства присоединяют к белковому вектору, которые функционируют подобно направленному на рецепторы носителю для доставки в ГЭБ. Этот подход является высоко специфичным, и он обеспечивает высокую эффективность и высокую универсальность для клинических целей с неограниченными мишенями. Последний подход изучали и в настоящий момент времени изучают авторы изобретения, которые начинали работу с молекул, описанных в приведенной выше публикации, и молекул согласно изобретению.
В патенте США No. 5807980 описаны ингибиторы на основе ингибитора трипсина бычьей поджелудочной железы (апротинина), а также способ их получения и терапевтического применения. Эти пептиды используют для лечения состояния, характеризующегося аномальной структурой или количеством тканевого фактора и/или фактора VIIIa, такого как аномальный тромбоз.
В патенте США No. 5780265 описаны ингибиторы сериновых протеаз, которые способны ингибировать калликреин плазмы.
В патенте США No.5118668 описаны варианты ингибитора трипсина бычьей поджелудочной железы.
Предоставление усовершенствованных молекул, которые могут выступать в качестве носителей или векторов для транспорта соединения или лекарственного средства через ГЭБ индивидуума, является крайне желательным.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Одной целью настоящего изобретения является осуществление усовершенствования в области доставки лекарственного средства.
Другой целью настоящего изобретения является предоставление неинвазивного и универсального способа и носителя для транспорта соединения или лекарственного средства через гематоэнцефалический барьер индивидуума.
В настоящей заявке описаны новые молекулы, которые могут быть способными, например, транспортировать требуемые соединения через гематоэнцефалический барьер.
В первом аспекте настоящее изобретение относится к биологически активному полипептиду, который способен преодолевать клеточный слой, имитирующий гематоэнцефалический барьер млекопитающего в анализе in vitro, где полипептид может быть выбран, например, из группы, состоящей из
- апротинина (SEQ ID NO:98),
- аналога апротинина,
- фрагмента апротинина, который может содержать (или может по существу состоять из) аминокислотную последовательность, определяемую SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1,
- биологически активного фрагмента SEQ ID NO:1 и
- биологически активного фрагмента аналога SEQ ID NO:1.
Во втором аспекте настоящее изобретение относится к биологически активному полипептиду, который способен преодолевать клеточный слой, имитирующий гематоэнцефалический барьер млекопитающих в анализе in vitro, где полипептид может быть выбран, например, из группы, состоящей из
- фрагмента апротинина, который может содержать аминокислотную последовательность, определяемую SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1,
- биологически активного фрагмента SEQ ID NO:1 и
- биологически активного фрагмента аналога SEQ ID NO:1.
В соответствии с настоящим изобретением фрагмент апротинина может состоять из последовательности, определяемой SEQ ID NO:1. Кроме того, в соответствии с настоящим изобретением фрагмент апротинина может содержать SEQ ID NO:1 и может иметь длину приблизительно от 19 аминокислот до приблизительно 54 аминокислот, например, длину от 10 до 50 аминокислот, длину от 10 до 30 аминокислот и т.д.
В соответствии с настоящим изобретением биологически активный аналог SEQ ID NO:1 может имеет длину приблизительно от 19 аминокислот до приблизительно 54 аминокислот (например, включая, например, от 21 до 23, от 25 до 34, от 36 до 50 и от 52 до 54), или приблизительно от 19 аминокислот до приблизительно 50 аминокислот, или приблизительно от 19 аминокислот до приблизительно 34 аминокислот (например, 19, 20, 21, 22, 23, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34), приблизительно от 19 аминокислот до приблизительно 23 аминокислот или приблизительно 19, 20, 21, 22, 23, 24, 35, 51 аминокислот.
Биологически активный фрагмент полипептида (например, из 19 аминокислот), описанный в настоящем описании, может включать в себя, например, полипептид из приблизительно от 7, 8, 9 или 10 до 18 аминокислот. Таким образом, в соответствии с настоящим изобретением биологически активный фрагмент SEQ ID NO:1 или аналог SEQ ID NO:1 может иметь длину приблизительно от 7 до приблизительно 18 аминокислот или приблизительно от 10 до приблизительно 18.
В патенте США No. 5807980 описан полипептид, который обозначен в настоящем описании как SEQ ID NO:102.
В патенте США No. 5780265 описан полипептид, который обозначен в настоящем описании как SEQ ID NO:103.
Аминокислотная последовательность апротинина (SEQ ID NO:98), аминокислотная последовательность Angiopep-1, а также некоторые последовательности биологически активных аналогов можно найти, например, в международной заявке No. PCT/CA 2004/000011, опубликованной 22 июля 2004 года как международная заявка No. WO 2004/060403. Кроме того, в международной заявке No. WO04/060403 описан полипептид, который обозначен в настоящем описании как SEQ ID NO:104.
В патенте США No.5118668 описаны полипептиды, которые имеют последовательность, представленную в SEQ ID NO:105.
Примеры аналогов апротинина можно найти посредством выполнения protein blast (Genebank: www.ncbi.nlm.nih.gov/BLAST/) для синтетической последовательности апротинина (или ее части), описанной в международной заявке No. PCT/CA 2004/000011. Иллюстративные аналоги апротинина можно найти, например, под регистрационными No. CAA37967 (GI:58005), 1405218C (GI:3604747) и т.д.
В следующем аспекте настоящее изобретение относится к биологически активному полипептиду, который способен преодолевать клеточный слой, имитирующий гематоэнцефалический барьер млекопитающих в анализе in vitro, где полипептид может быть выбран, например, из группы, состоящей из
- фрагмента апротинина длиной от 19 до 54 (например, 19-50) аминокислот, содержащего SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 длиной приблизительно от 19 до 50 аминокислот и
- биологически активного фрагмента SEQ ID NO:1 (от 10 до 18 аминокислот) или биологически активного фрагмента аналога SEQ ID NO:1 (приблизительно от 10 до 18 аминокислот).
В соответствии с настоящим изобретением предусмотрен биологически активный аналог SEQ ID NO:1, который может быть выбран, например, из группы, состоящей из
- аналога SEQ ID NO:1, который может иметь по меньшей мере 35% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 40% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 50% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 60% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 70% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 80% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 90% идентичность аминокислотной последовательности SEQ ID NO:1 и
- аналога SEQ ID NO:1, который может иметь по меньшей мере 95% (т.е. 96%, 97%, 98%, 99% и 100%) идентичность аминокислотной последовательности SEQ ID NO:1.
Например, биологически активный аналог SEQ ID NO:1 может содержать аминокислотную последовательность, выбранную из группы, состоящей из аминокислотной последовательности, определяемой любым из с SEQ ID NO:2 по SEQ ID NO:62, с SEQ ID NO:68 по SEQ ID NO:93, и SEQ ID NO:97, а также 99, 100 и 101. Если полипептид согласно изобретению содержит, например, SEQ ID NO:99, 100 или 101, то полипептид может иметь аминокислотную последовательность длиной из приблизительно от 10 до 50 аминокислот, например от 10 до 30 аминокислот.
Кроме того, в соответствии с настоящим изобретением биологически активный аналог SEQ ID NO:1 может содержать аминокислотную последовательность, определяемую SEQ ID NO:67 (т.е. полипептид No. 67, который представляет собой амидированный вариант SEQ ID NO:67 (Angiopep-1)).
Полипептиды согласно изобретению могут быть амидированными, т.е. они могут иметь амидированную аминокислотную последовательность. Например, может быть амидированным полипептидом SEQ ID NO:67 (полипептид No.67).
Часть соединений согласно изобретению может относиться к полипептидам, определенным в настоящем описании, за исключением полипептидов, определяемых SEQ ID NO:102, 103, 104 и 105, в то время как другая часть соединений согласно изобретению может включать в себя эти пептиды. В качестве неограничивающего примера, настоящее изобретение относится к конъюгатам, содержащим эти пептиды, а также их применению для лечения неврологического заболевания (например, опухоли мозга), способу лечения неврологического заболевания (например, опухоли мозга), фармацевтической композиции для лечения неврологического заболевания и т.д.
В следующем аспекте настоящее изобретение относится к биологически активному полипептиду, который способен преодолевать клеточный слой, имитирующий гематоэнцефалический барьер млекопитающих в анализе in vitro, где полипептид может быть выбран, например, из группы, состоящей из
- фрагмента апротинина длиной от 19 до 54 (например, 19-50) аминокислот, содержащего SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 длиной приблизительно от 19 до 50 аминокислот, при условии, что указанный аналог не является последовательностью SEQ ID NO:102, 103, 104 или 105, и при условии, что если указанный аналог состоит из SEQ ID NO:67, то указанный аналог является амидированным,
- биологически активного фрагмента SEQ ID NO:1 из 10-18 аминокислот и
- биологически активного фрагмента аналога SEQ ID NO:1 приблизительно из 10-18 аминокислот.
Кроме того, в соответствии с настоящим изобретением биологически активный фрагмент SEQ ID NO:1 или биологически активный фрагмент аналога SEQ ID NO:1 может содержать по меньшей мере 9 или по меньшей мере 10 (последовательных или смежных) аминокислот последовательности SEQ ID NO:1 или аналога SEQ ID NO:1.
Полипептиды согласно изобретению могут иметь аминокислотную последовательность, которая может содержать от 1 до 12 аминокислотных замен (т.е. SEQ ID NO:91). Например, количество аминокислотных замен может составлять от 1 до 10 аминокислотных замен или от 1 до 5 аминокислотных замен. В соответствии с настоящим изобретением аминокислотная замена может представлять собой неконсервативную аминокислотную замену или консервативную аминокислотную замену.
Например, если полипептид согласно изобретению содержит аминокислоты, которые идентичны аминокислотам SEQ ID NO:1, и другие аминокислоты, которые не являются идентичными (не идентичны), те аминокислоты, которые являются неидентичными могут представлять собой консервативную аминокислотную замену. Сравнение идентичных и неидентичных аминокислот можно проводить посредством проверки соответствующего положения.
Примеры аналога SEQ ID NO:1, который может иметь по меньшей мере 35% идентичность, включают в себя, например, полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:91 (приблизительно 36,8% идентичность, т.е. 7 аминокислот из 19 аминокислот SEQ ID NO:91 являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:98 (приблизительно 68,4% идентичность, т.е. 13 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:67 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:76 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), и полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:5 (приблизительно 79% идентичность, т.е. 15 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1).
Примеры аналога SEQ ID NO:1, который может иметь по меньшей мере 60% идентичность, включают в себя, например, полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:98 (приблизительно 68,4% идентичность, т.е. 13 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:67 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:76 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1) и полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:5 (приблизительно 79% идентичность, т.е. 15 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1).
Примеры аналога SEQ ID NO:1, который может иметь по меньшей мере 70% идентичность, включают в себя, например, полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:67 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), SEQ ID NO:76 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), SEQ ID NO:5 (приблизительно 79% идентичность, т.е. 15 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1).
В соответствии с настоящим изобретением носитель, более конкретно, может быть выбран из группы, состоящей из пептидов No. 5, 67, 76, 91 и пептида 97 (т.е. SEQ ID NO:5, 67, 76, 91 и 97 (Angiopep-2)). Носитель можно использовать, например, для транспорта присоединенного к нему вещества через гематоэнцефалический барьер. В соответствии с настоящим изобретением носитель может быть способным преодолевать гематоэнцефалический барьер после присоединения вещества и, таким образом, может быть способным транспортировать вещество через гематоэнцефалический барьер.
В соответствии с настоящим изобретением полипептиды могут находиться в выделенной форме или по существу в очищенной форме.
Более конкретно, настоящее изобретение относится к носителю для транспорта присоединенного к нему вещества через гематоэнцефалический барьер, где носитель может быть способным преодолевать гематоэнцефалический барьер после присоединения к веществу и, таким образом, транспортировать вещество через гематоэнцефалический барьер. Носитель может содержать по меньшей мере один полипептид согласно изобретению (при условии, что если указанный полипептид или носитель состоит из SEQ ID NO:67, то указанный полипептид является модифицированным по группе, например амидированным). Например, носитель может быть выбран из класса молекул, относящегося к апротинину.
Активность транспорта, который осуществляют посредством носителя, не влияет на целостность гематоэнцефалического барьера. Транспорт вещества может приводить, например, к доставке вещества в центральную нервную систему (ЦНС) индивидуума.
В рамках настоящего описания следует понимать, что полипептиды согласно изобретению можно синтезировать химически (например, твердофазным синтезом) или их можно получать посредством технологии рекомбинантных ДНК. Кодоны, которые кодируют конкретные аминокислоты, хорошо известны в данной области и описаны, например, в Biochemistry (третье издание; 1988, Lubert Stryer, Stanford University, W. H. Freeman and Company, New-York). Таким образом, в рамках настоящего описания предусмотрена нуклеотидная последовательность, кодирующая носитель согласно изобретению. Более конкретно, настоящее изобретение относится к нуклеотидным последовательностям (дезоксирибонуклеотиды или рибонуклеотиды или их производные), кодирующим полипептид, выбранный из группы, состоящей из любого из с SEQ ID NO:1 по 97. Иллюстративная нуклеотидная последовательность, кодирующая аналог апротинина, представлена в SEQ ID NO:106, и ее можно найти в Gene Bank под регистрационным номером No.X04666. Эта последовательность кодирует аналог апротинина, имеющий лизин в положении 16 (по отношению к аминокислотной последовательности, кодируемой SEQ ID NO:106) вместо валина, который находится в SEQ ID NO:98. В нуклеотидную последовательность SEQ ID NO:106 можно вносить мутацию способами, известными в данной области, для замены продукции на пептид SEQ ID NO:98, имеющий валин в положении 16. Способы, известные в данной области, можно использовать для внесения дополнительных мутаций в нуклеотидную последовательность, чтобы она кодировала аналоги согласно изобретению. Фрагменты можно получать из этой нуклеотидной последовательности посредством ферментативного расщепления или полимеразной цепной реакции, и т.д. Альтернативно требуемую нуклеотидную последовательность можно синтезировать химически известными в данной области способами.
В следующем аспекте настоящее изобретение относится к конъюгату, который может содержать носитель, выбранный из группы, состоящей из любого полипептида согласно изобретению, и вещества, выбранного из группы, состоящей, например, из лекарственного средства (например, низкомолекулярного лекарственного средства, например, антибиотика), медикамента, поддающейся детекции метки, белка (например, фермента), соединения на основе белка (например, белкового комплекса, содержащего одну или несколько полипептидных цепей) и полипептида (пептида). Более конкретно, вещество может представлять собой молекулу, которая является активной на уровне центральной нервной системы. Вещество может представлять собой любое вещество для лечения или выявления неврологического заболевания.
В соответствии с настоящим изобретением носитель, который представляет собой часть конъюгата, может быть выбран, например, из группы, состоящей из
- фрагмента апротинина длиной от 10 до 54 (например, 19-50) аминокислот, содержащего SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 (например, длиной приблизительно от 19 до 50 аминокислот), при условии, что если указанный аналог состоит из SEQ ID NO:67, то указанный аналог является амидированным,
- биологически активного фрагмента SEQ ID NO:1 из 10-18 аминокислот и
- биологически активного фрагмента аналога SEQ ID NO:1 приблизительно из 10-18 аминокислот.
В соответствии с настоящим изобретением вещество может иметь максимальную молекулярную массу приблизительно 160000 Дальтон.
Кроме того, в соответствии с настоящим изобретением транспортной активности можно достигать посредством рецептор-опосредованного трансцитоза или адсорбционно-опосредуемого трансцитоза. Вещество может представлять собой вещество, которое может транспортироваться таким механизмом.
Кроме того, в соответствии с настоящим изобретением конъюгат может находиться в форме слитого белка, который может обладать первой группой, по существу состоящей из носителя согласно изобретению, и второй группой, по существу состоящей из белка или вещества на основе белка.
Иллюстративные неврологические заболевания, которые можно лечить или выявлять с помощью носителя и/или конъюгата, представляют собой заболевания, выбранные, например, из группы, состоящей из опухоли мозга, метастаза в головной мозг, шизофрении, эпилепсии, болезни Альцгеймера, болезни Паркинсона, болезни Гентингтона, инсульта и нарушений функции, связанных с гематоэнцефалическим барьером (например, ожирения).
В соответствии с настоящим изобретением нарушение функции, связанное с гематоэнцефалическим барьером, представляет собой ожирение. Также в соответствии с настоящим изобретением вещество, которое может быть конъюгированным с носителем согласно изобретению, может представлять собой лептин. Конъюгат, содержащий лептин и носитель, можно использовать, например, при лечении ожирения.
В соответствии с настоящим изобретением поддающаяся детекции метка может представлять собой радиовизуализирующее средство. Пример метки, которая может быть конъюгирована с носителем согласно изобретению и которая охватывается настоящим описанием, включает в себя в качестве неограничивающего примера изотоп, флуоресцентную метку (например, родамин), репортерную молекулу (например, биотин) и т.д. Другие примеры поддающихся детекции меток включают в себя, например, зеленый флуоресцирующий белок, биотин, белок histag и β-галактозидазу.
Пример белка или соединения на основе белка, которое можно конъюгировать с носителем согласно изобретению и которое охватывается настоящим описанием, включает в себя в качестве неограничивающего примера антитело, фрагмент антитела (например, связывающий фрагмент антитела, такой как Fv-фрагмент, F(ab)2, F(ab)2' и Fab и т.п.), лекарственное средство на основе пептида или белка (например, положительный фармакологический модулятор (агонист) или фармакологический ингибитор (антагонист)) и т.д. Другие примеры вещества, которое охватывается настоящим описанием, включают в себя клеточные токсины (например, монометилауристатин E (MMAE), токсины из бактериальных эндотоксинов и экзотоксинов; дифтерийные токсины, ботулинические токсины, столбнячные токсины, коклюшные токсины, стафилококковые энтеротоксины, токсин TSST-1 синдрома токсического шока, аденилатциклазный токсин, токсин Шига, холерный энтеротоксин и другие) и антиангиогенные соединения (эндостатин, катехины, нутрицевтики, хемокин IP-10, ингибиторы матриксных металлопротеиназ (MMPI), анастеллин, витронектин, антитромбин, ингибиторы тирозинкиназы, ингибиторы VEGF, антитела против рецептора, герцептин, авастин и панитумумаб и другие).
Также в соответствии с настоящим изобретением вещество может представлять собой низкомолекулярное лекарственное средство, такое как противоопухолевое лекарственное средство (например, для лечения опухоли мозга). Противоопухолевое лекарственное средство, охватываемое настоящим изобретением, может включать в себя, например, лекарственное средство, имеющее группу, обеспечивающую его конъюгацию с носителем согласно изобретению. Примеры противоопухолевого лекарственного средства включают в себя в качестве неограничивающего примера лекарственное средство, которое может быть выбрано из группы, состоящей из паклитаксела (таксол), винбластина, винкристина, этопозида, доксорубицина, циклофосфамида, таксотера, мелфалана, хлорамбуцила и любого сочетания.
Более конкретно, конъюгат согласно изобретению может иметь формулу R-L-M или формулу ее фармацевтически приемлемой соли, где R представляет собой молекулы класса, относящегося к апротинину (например, апротинин, фрагмент апротинина, Angiopep-1, Angiopep-2, аналоги, производные или фрагменты). Например, R может представлять собой носитель, выбранный из молекул класса, относящегося к апротинину, способный преодолевать гематоэнцефалический барьер после присоединения к L-M и, таким образом, транспортировать M через гематоэнцефалический барьер. L может представлять собой линкер или связь (химическую связь). M может представлять собой любое вещество, выбранное из группы, состоящей из лекарственного средства (например, низкомолекулярного лекарственного средства), медикамента, (поддающейся детекции) метки, белка или соединения на основе белка (например, антитела, фрагмента антитела), антибиотика, противоопухолевого средства, антиагиогенного соединения и полипептида или любой молекулы, активной на уровне центральной нервной системы. Следует понимать, что в рамках настоящего описания формула R-L-M не предназначена для того, чтобы ограничиваться конкретным порядком или конкретным соотношением. Как представлено в настоящем описании, M может в несколько раз превышать R.
Например, конъюгаты формулы R-L-M или их фармацевтически приемлемые соли можно использовать для транспорта M через гематоэнцефалический барьер, где R может представлять собой, например, носитель, выбранный из группы, состоящей из пептидов No: 5, 67, 76, 91 и 97, как описано в настоящем описании. Носитель может быть способен преодолевать гематоэнцефалический барьер после присоединения к L-M
и, таким образом, может транспортировать M через гематоэнцефалический барьер.
В соответствии с настоящим изобретением M может представлять собой вещество, пригодное для лечения или диагностики неврологического заболевания.
В рамках настоящего описания следует понимать, что если является доступной или существует более одной области для конъюгации носителя, то с носителем согласно изобретению можно конъюгировать более одного лекарственного средства или молекулы лекарственного средства. Таким образом, конъюгат может содержать одну или несколько молекул лекарственного средства. Может быть активным сам конъюгат, т.е. лекарственное средство может быть активным, даже если оно связано с носителем. Также в соответствии с настоящим изобретением соединение может освобождаться (или может не освобождаться) от носителя, т.е., главным образом, после транспорта через гематоэнцефалический барьер. Таким образом, соединение может высвобождаться из конъюгата (или от носителя) и после этого может становиться активным. Более конкретно, вещество может обладать способностью к освобождению от носителя после транспорта через гематоэнцефалический барьер.
В соответствии с другим вариантом осуществления настоящего изобретения предусмотрен конъюгат для транспорта вещества через гематоэнцефалический барьер, где конъюгат может содержать: (a) носитель и (b) вещество, присоединенное к носителю, где конъюгат способен преодолевать гематоэнцефалический барьер и, таким образом, транспортировать вещество через гематоэнцефалический барьер.
В следующем аспекте настоящее изобретение относится к применению носителя или конъюгата согласно изобретению для транспорта вещества через гематоэнцефалический барьер нуждающегося в этом млекопитающего.
В следующем аспекте настоящее изобретение относится к применению молекул класса, относящегося к апротинину, для транспорта соединения, присоединенного к ним, через гематоэнцефалический барьер пациента.
В дополнительном аспекте настоящее изобретение относится к применению носителя или конъюгата, как описано в настоящем описании для диагностики неврологического заболевания или заболевания центральной нервной системы. Например, носитель или конъюгат можно использовать для выявления неврологического заболевания in vivo.
Носитель может быть выбран, например, из группы, состоящей из (биологически активных)
- апротинина (SEQ ID NO:98),
- фрагмента апротинина, который может содержать аминокислотную последовательность, определяемую SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 и
- биологически активного фрагмента SEQ ID NO:1 или биологически активного фрагмента аналога SEQ ID NO:1.
Более конкретно, носитель может быть выбран, например, из группы, состоящей из (биологически активных)
- фрагмента апротинина, который может содержать аминокислотную последовательность, определяемую SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 и
- биологически активного фрагмента SEQ ID NO:1 или биологически активного фрагмента аналога SEQ ID NO:1.
В соответствии с настоящим изобретением, если этот аналог состоит из SEQ ID NO:67, то указанный аналог является амидированным.
Более конкретно, носитель может быть выбран, например, из группы, состоящей из
- фрагмента апротинина длиной от 10 до 54 (например, 19-50) аминокислот, содержащего SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 (например, длиной приблизительно от 19 до 50 аминокислот), при условии, что если указанный аналог состоит из SEQ ID NO:67, то указанный аналог является амидированным,
- биологически активного фрагмента SEQ ID NO:1 из от 10 до 18 аминокислот и
- биологически активного фрагмента аналога SEQ ID NO:1 из приблизительно от 10 до 18 аминокислот.
В другом аспекте настоящее изобретение относится к применению молекул класса, относящегося к апротинину, для изготовления лекарственного средства.
В соответствии с настоящим изобретением предусмотрено применение молекул класса, относящегося к апротинину, для изготовления лекарственного средства для лечения неврологического заболевания или для лечения нарушения центральной нервной системы.
В другом аспекте настоящее изобретение относится к применению носителя или конъюгата, описанного в настоящем описании, для изготовления лекарственного средства для лечения заболевания головного мозга (ассоциированного с головным мозгом заболевания) или неврологического заболевания, для диагностики заболевания головного мозга или неврологического заболевания или для транспорта вещества через гематоэнцефалический барьер.
В дополнительном аспекте настоящее изобретение относится к применению носителя или конъюгата согласно изобретению для лечения млекопитающего, например, с неврологическим заболеванием или для диагностики неврологического заболевания у нуждающегося в этом млекопитающего.
В соответствии с настоящим изобретением неврологическое заболевание, охватываемое настоящим изобретением, включает в себя в качестве неограничивающего примера опухоль мозга, метастаз в головной мозг, шизофрению, эпилепсию, болезнь Альцгеймера, болезнь Паркинсона, болезнь Гентингтона, инсульт и нарушения функции, связанные с гематоэнцефалическим барьером.
В следующем аспекте настоящее изобретение относится к способу транспорта вещества через гематоэнцефалический барьер млекопитающего (человека, животного), который может включать в себя стадию введения млекопитающему соединения, содержащего вещество, присоединенное к молекулам класса, относящегося к апротинину.
В следующем аспекте настоящее изобретение относится к способу лечения неврологического заболевания у пациента, включающему в себя введение пациенту лекарственного средства, содержащего молекулы класса, относящегося к апротинину, и соединение, адаптированное для лечения заболевания, где соединение присоединено к молекулам класса, относящегося к апротинину.
В дополнительном аспекте предусмотрен способ лечения нарушения центральной нервной системы пациента, включающий в себя введение пациенту лекарственного средства, содержащего молекулы класса, относящегося к апротинину, и соединение, адаптированное для лечения заболевания, где соединение присоединено к апротинину.
В следующем аспекте предусмотрен способ транспорта вещества через гематоэнцефалический барьер, который включает в себя стадию введения индивидууму фармацевтической композиции согласно изобретению.
В следующем аспекте настоящее изобретение также относится к способу лечения млекопитающего (например, пациента), нуждающегося в этом (например, пациента с неврологическим заболеванием). Способ может включать в себя введение млекопитающему носителя, конъюгата и/или фармацевтической композиции согласно изобретению.
Кроме того, настоящее изобретение относится к способу диагностики (т.е. к диагностическому способу) неврологического заболевания у млекопитающего (например, у пациента), нуждающегося в этом. Способ может включать в себя введение носителя, конъюгата и/или фармацевтической композиции согласно изобретению млекопитающему (человеку, пациенту, животному).
В соответствии с настоящим изобретением введение можно проводить внутриартериально, интраназально, внутрибрюшинно, внутривенно, внутримышечно, подкожно, чрескожно или перорально.
В соответствии с настоящим изобретением фармацевтическую композицию можно вводить млекопитающему в терапевтически эффективном количестве.
Нуждающееся млекопитающее (нуждающийся индивидуум) может представлять собой, например, млекопитающее, которое обладает риском неврологического заболевания, заболевания центральной нервной системы, злокачественной опухоли мозга, метастаза в головной мозг и т.д.
В дополнительном аспекте настоящее изобретение относится к фармацевтической композиции, которая может содержать, например:
- носитель (который может быть выбран из группы, состоящей из любого из описанных в настоящем описании полипептидов) или конъюгат согласно изобретению; и
- фармацевтически приемлемый носитель, например, фармацевтически приемлемый эксципиент.
В соответствии с настоящим изобретением фармацевтическую композицию можно применять, например, для лечения неврологического заболевания.
Кроме того, в соответствии с настоящим изобретением фармацевтическую композицию можно применять, например, для диагностики неврологического заболевания.
Также в соответствии с настоящим изобретением фармацевтическую композицию можно использовать, например, для транспорта вещества через гематоэнцефалический барьер.
Также в соответствии с настоящим изобретением фармацевтическую композицию можно применять, например, для доставки вещества в ЦНС индивидуума.
Кроме того, в соответствии с настоящим изобретением фармацевтическую композицию можно использовать, например, для лечения нарушения центральной нервной системы у нуждающегося в этом млекопитающего.
В соответствии с настоящим изобретением фармацевтическую композицию можно использовать для доставки вещества в ЦНС индивидуума.
В рамках настоящего описания следует понимать, что фармацевтически приемлемые соли носителя (полипептида) или конъюгата охватываются настоящим изобретением.
Композиция (фармацевтическая композиция), таким образом, может содержать лекарственное средство, изготовленное, как определено в настоящем описании, совместно с фармацевтически приемлемым эксципиентом.
Для целей настоящего изобретения ниже определены следующие термины.
Подразумевают, что термин "носитель" или "вектор" означает соединение или молекулу, такую как полипептид, которая способна транспортировать соединение. Например, транспорт может происходить через гематоэнцефалический барьер. Носитель может быть соединен (ковалентно или нековалентно) или конъюгирован с другим соединением или веществом и, таким образом, может быть способен транспортировать другое соединение или вещество через гематоэнцефалический барьер. Например, носитель может связываться с рецепторами, находящимися на эндотелиальных клетках головного мозга, и, таким образом, транспортироваться через гематоэнцефалический барьер посредством трансцитоза. Носитель может представлять собой молекулу, для которой могут быть достигнуты высокие уровни трансэндотелиального транспорта без нарушения целостности гематоэнцефалического барьера. Носитель может представлять собой, не ограничиваясь ими, белок, пептид или пептидомиметик, и он может быть природным или полученным путем химического синтеза или посредством рекомбинантной генетической технологии (посредством генетической инженерии).
Подразумевают, что термин "конъюгат" означает сочетание носителя и другого соединения или вещества. Конъюгация может быть химической по своему характеру, такой как конъюгация через линкер, или она может быть генетической по своему характеру, например, посредством рекомбинантной генетической технологии, такой как в слитом белке, например, с репортерной молекулой (например, с зеленым флуоресцирующим белком, β-галактозидазой, Histag и т.д.).
Подразумевают, что выражение "низкомолекулярное лекарственное средство" означает лекарственное средство с молекулярной массой 1000 г/моль или менее.
Подразумевают, что термины "лечение", "проведение лечения" и т.д. означают получение требуемого фармакологического и/или физиологического эффекта, например, ингибирования роста злокачественных клеток, гибели злокачественных клеток или смягчения течения неврологического заболевания или состояния. Эффект может быть профилактическим в виде полного или частичного предотвращения заболевания или его симптома, и/или он может быть терапевтическим в виде частичного или полного излечения заболевания и/или неблагоприятного действия, свойственного заболеванию. В настоящем описании "лечение" охватывает любое лечение заболевания у млекопитающих, в частности у человека, и включает в себя (a) предотвращение возникновения заболевания или состояния (например, предотвращение злокачественной опухоли) у индивидуума, который предрасположен к заболеванию, однако у которого еще не поставлен диагноз как у обладающего этим заболеванием; (b) торможение заболевания (например, остановка его развития) или (c) смягчение течения заболевания (например, снижение симптомов, связанных с заболеванием). В настоящем описании "лечение" охватывает любое введение фармацевтического средства или соединения индивидууму для лечения, исцеления, смягчения, улучшения, ослабления или торможения состояния индивидуума, включая в качестве неограничивающего примера введение индивидууму конъюгата носитель-вещество.
Подразумевают, что термин "злокачественная опухоль" означает любое клеточное злокачественное новообразование, своеобразным признаком которого является утрата нормального контроля, которая приводит к неконтролируемому росту, недостаточной дифференцировке и способности к локальному проникновению в ткани и к метастазированию. Злокачественная опухоль может развиться в любой ткани любого органа. Более конкретно, подразумевают, что злокачественная опухоль включает в себя, не ограничиваясь этим, злокачественную опухоль головного мозга.
Подразумевают, что термин "проведение введения" и "введение" означает способ доставки, включая, но не ограничиваясь этим, внутриартериальную, интраназальную, внутрибрюшинную, внутривенную, внутримышечную, подкожную, трансдермальную или пероральную доставку. Суточную дозировку можно разделять на одну, две или более доз в пригодной форме для введения за один, два или более раз в течение периода времени.
Подразумевают, что термин "терапевтически эффективный" или "эффективное количество" означает количество соединения, достаточное для существенного улучшения какого-либо симптома, ассоциированного с заболеванием или медицинским состоянием. Например, при лечении злокачественной опухоли, или психического состояния, или неврологического заболевания, или заболевания ЦНС, вещество или соединение, которое снижает, предотвращает, замедляет, подавляет или останавливает любой симптом заболевания или состояния, может быть терапевтически эффективным. Терапевтически эффективное количество вещества или соединения не обязательно должно излечивать заболевание или состояние, однако она предусматривает лечение от заболевания или состояния, такое как замедление, задерживание, или предотвращение заболевания или состояния, или ослабление симптомов заболевания или состояния, или изменение продолжительности заболевания или состояния, или, например, снижение тяжести или ускорение выздоровления у индивидуума.
Носитель и конъюгаты согласно изобретению можно использовать в сочетании либо с общепринятыми способами лечения и/или терапии, либо их можно использовать отдельно от общепринятых способов лечения и/или терапии.
В случае, когда конъюгаты согласно изобретению вводят в качестве комбинированной терапии с другими веществами, их можно вводить индивидууму последовательно или одновременно. Альтернативно фармацевтические композиции в соответствии с настоящим изобретением могут включать в себя сочетание конъюгата носитель-вещество согласно изобретению совместно с фармацевтически приемлемым эксципиентом, как описано в настоящем описании, и другим терапевтическим или профилактическим веществом, известным в данной области.
Фармацевтически приемлемые кислотно-аддитивные соли можно получать способами, известными и используемыми в данной области, и они охватываются настоящим изобретением.
Биологически активные полипептиды согласно изобретению включат в себя функциональные производные. Подразумевают, что термин "функциональное производное" означает "химическое производное", "фрагмент" или "вариант" биологически активной последовательности или части носителя, или вещества, или конъюгата и их соли согласно изобретению. Функциональное производное носителя может быть способным к присоединению или конъюгации с другим соединением или веществом и к преодолению гематоэнцефалического барьера и, таким образом, является способным транспортировать другое соединение или вещество через гематоэнцефалический барьер.
Подразумевают, что термин "химическое производное" означает носитель, вещество или конъюгат согласно изобретению, который содержит дополнительные химические группы, не являющиеся частью носителя, вещества или конъюгата носитель-вещество. Ковалентные модификации включены в объем этого изобретения. Химическое производное можно удобно получать посредством прямого химического синтеза с использованием способов, хорошо известных в данной области. Такие модификации, например, можно вносить в белковый или пептидный носитель, вещество или конъюгат носитель-вещество посредством проведения реакции предназначенных для воздействия аминокислотных остатков с органическим приводящим к получению производного веществом, которое способно реагировать с выбранными боковыми цепями или концевыми остатками. Химическое производное носителя является способным к преодолению гематоэнцефалического барьера и к присоединению или конъюгации с другим соединением или веществом, и, таким образом, оно является способным транспортировать другое соединение или вещество через гематоэнцефалический барьер. В предпочтительном варианте осуществления достигают очень высоких уровней трансэндотелиального транспорта через гематоэнцефалический барьер без какого-либо нарушения целостности гематоэнцефалического барьера.
Подразумевают, что термин "вещество" означает без различия антитело, лекарственное средство (такое как медицинское лекарственное средство) или соединение, такое как лекарственное средство или соединение, маркер, метку или соединение для визуализации.
Подразумевают, что термин "лекарственное средство" или "вещество" означает вещество, и/или медикамент, и/или лекарственное средство, используемое для лечения симптомов заболевания, физического или психического состояния, повреждения или инфекции, и включает в себя, не ограничиваясь ими, антибиотики, противоопухолевые средства, антиангиогенные средства и молекулы, активные на уровне центральной нервной системы. Например, для лечения злокачественной опухоли мозга можно внутривенно вводить паклитаксел.
Подразумевают, что термин "состояние" означает любые условия, вызывающие боль, дискомфорт, болезненное состояние, заболевание или нетрудоспособность (психическую или физическую) в индивидууме или у индивидуума, включая неврологическое заболевание, повреждение, инфекцию или хроническую или острую боль. Неврологические заболевания, которые можно лечить посредством настоящего изобретения, включают в себя, но не ограничиваются ими, опухоли мозга, метастазы в головной мозг, шизофрению, эпилепсию, болезнь Альцгеймера, болезнь Паркинсона, болезнь Гентингтона и инсульт.
В настоящем описании "фармацевтическая композиция" означает терапевтически эффективные количества вещества совместно с фармацевтически приемлемыми разбавителями, консервантами, солюбилизаторами, эмульгаторами, адъювантом и/или носителями. "Терапевтически эффективное количество" относится к такому количеству, которое обеспечивает терапевтический эффект для данного состояния и схемы введения. Такие композиции являются жидкими или лиофилизированными или иным образом высушенными составами и включают в себя разбавители с различным буферным составом (например, Tris-HCl, ацетат, фосфат), pH и ионной силой, добавки, такие как альбумин или желатин, для предотвращения адсорбции к поверхностям, детергенты (например, Tween 20, Tween 80, Pluronic F68, соли желчных кислот), солюбилизаторы (например, глицерин, полиэтилен глицерин), антиоксиданты (например, аскорбиновая кислота, натрий метабисульфит), консерванты (например, тимеросал, бензиловый спирт, парабены), вещества для увеличения объема или модификаторы тоничности (например, лактоза, маннит), ковалентное присоединение полимеров, таких как полиэтиленгликоль к белку, образование комплексов с ионами металлов, или добавление вещества в препараты или к препаратам в виде частиц полимерных соединений, таких как полимолочная кислота, полигликолевая кислота, гидрогели и т.д., или в липосомы, микроэмульсии, мицеллы, однослойные или многослойные везикулы, гемолизированные эритроциты или сферопласты. Такие композиции влияют на физическое состояние, растворимость, стабильность, скорость высвобождения in vivo и скорость выведения in vivo. Композиции с контролируемым или замедленным высвобождением включают в себя составы в липофильных веществах замедленного действия (например, жирные кислоты, воски, масла). Также это изобретение относится к композициям в виде частиц, покрытым полимерами (например, полоксамерами или полоксаминами). Другие варианты осуществления композиций согласно изобретению включают в себя защитные покрытия для форм в виде частиц, ингибиторы протеаз или вещества, усиливающие проницаемость, для различных способов введения, включая парентеральный, легочный, назальный, пероральный, вагинальный, ректальный способы. В одном варианте осуществления фармацевтическую композицию вводят парентерально, в область злокачественной опухоли, через слизистую оболочку, трансдермально, внутримышечно, внутривенно, внутрикожно, подкожно, внутрибрюшинно, внутрь желудочков, интракраниально и внутрь опухоли.
Кроме того, в настоящем описании, термины "фармацевтически приемлемый носитель" или "фармацевтический носитель" известны в данной области и включают в себя, но не ограничиваются ими, 0,01-0,1 M или 0,05 M фосфатный буфер или 0,8% физиологический раствор. Кроме того, такие фармацевтически приемлемые носители могут представлять собой водные или неводные растворы, суспензии и эмульсии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и инъецируемые органические сложные эфиры, такие как этилолеат. Водные носители включают в себя воду, спиртовые/водные растворы, эмульсии или суспензии, включая физиологический раствор и буферную среду. Парентеральные носители включают в себя раствор хлорида натрия, раствор Рингера с декстрозой, раствор декстрозы и хлорида натрия, лактированный раствор Рингера или жирные масла. Внутривенные носители включают в себя жидкие и питательные наполнители, электролитные наполнители, такие как наполнители на основе раствора Рингера с декстрозой, и т.п. Консерванты и другие добавки также могут быть представлены, такие, например, как противомикробные средства, антиоксиданты, объединяющие вещества, инертные газы и т.п.
В рамках настоящего описания термин "аналог" следует понимать как полипептид, полученный из исходной последовательности или из части исходной последовательности и который может обладать одной или несколькими модификациями; например, одной или несколькими модификациями аминокислотной последовательности (например, добавление, удаление, вставка, замена аминокислоты и т.д.), одной или несколькими модификациями в остове или боковой цепи одной или нескольких аминокислот, или добавлением группы или другой молекулы к одной или нескольким аминокислотам (боковые цепи или остов). Таким образом, "аналог" следует понимать как молекулу, обладающую биологической активностью и химической структурой (или частью ее структуры), сходными с биологической активностью и химической структурой полипептида, описанного в настоящем описании. Аналог включает в себя полипептид, который может обладать, например, одной или несколькими аминокислотными вставками, либо на одном, либо на обоих концах полипептида и/или внутри аминокислотной последовательности полипептида.
"Аналог" может обладать сходством последовательности и/или идентичностью последовательности с исходной последовательностью или частью исходной последовательности и также может обладать модификацией его структуры, как описано в настоящем описании. Степень сходства между двумя последовательностями основана на процентной доле идентичности (идентичных аминокислот) и консервативных замен.
Сходство или идентичность можно сравнивать, например, на протяжении участка из 2, 3, 4, 5, 10, 19, 20 аминокислот или более (и любого количества между этими количествами). В рамках настоящего описания идентичность может включать в себя аминокислоты, которые являются идентичными исходному пептиду и которые могут занимать одинаковое или сходное положение по сравнению с исходным полипептидом. Аналог, который обладает, например, 50% идентичностью с исходным полипептидом, может включать в себя, например, аналог, содержащий 50% аминокислотной последовательности исходного полипептида и аналогично для других процентных количеств. В рамках настоящего описания следует понимать, что среди аминокислот аналогов, которые являются идентичными или сходными с аминокислотами исходного пептида, могут находиться промежутки. Эти промежутки могут не включать в себя аминокислот, могут включать в себя одну или несколько аминокислот, которые не являются идентичными или сходными с исходным пептидом. При этом предусмотрены биологически активные аналоги носителей (полипептидов) согласно изобретению.
Процентную идентичность можно определять, например, с помощью n алгоритма GAP, BESTFIT или FASTA в Wisconsin Genetics Software Package Release 7,0, с использованием веса разрыва по умолчанию.
Например, аналог может содержать или иметь 50% идентичность с исходной аминокислотной последовательностью, и часть остальных аминокислот, которые занимают аналогичное положение, например, может представлять собой неконсервативную или консервативную аминокислотную замену.
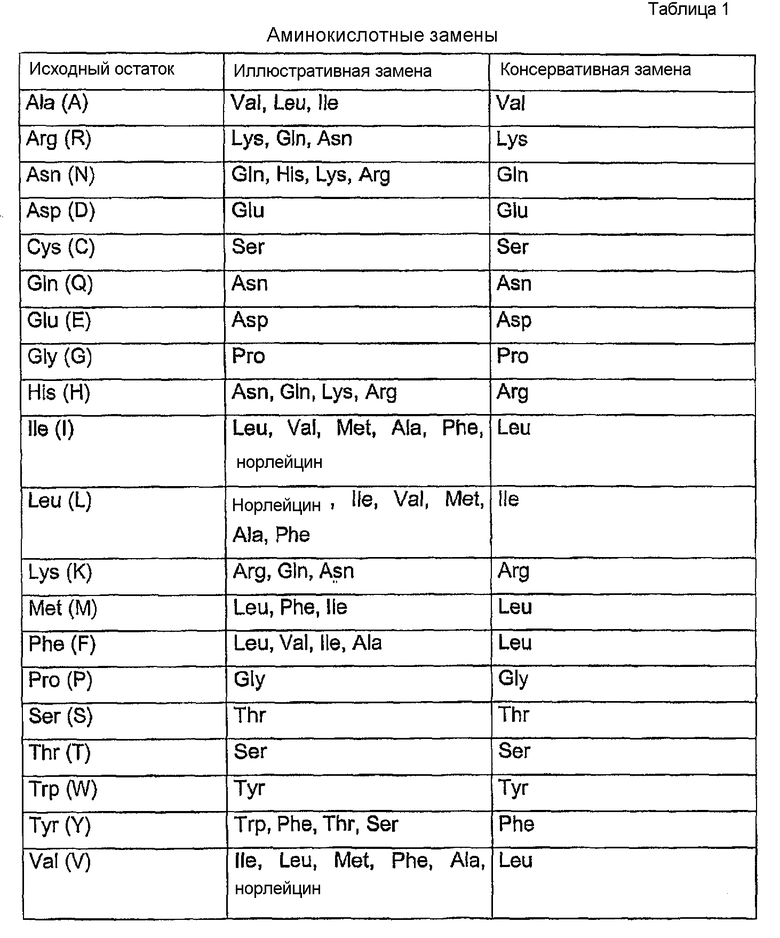
Таким образом, аналоги согласно изобретению также включают в себя аналоги, которые обладают по меньшей мере 90% сходством последовательностей с исходной последовательностью или частью исходной последовательности. "Аналог" может иметь, например, по меньшей мере 35%, 50%, 60%, 70%, 80%, 90% или 95% (96%, 97%, 98%, 99% и 100%) сходство последовательностей с исходной последовательностью или частью исходной последовательности. "Аналог" также может иметь, например, по меньшей мере 35%, 50%, 60%, 70%, 80%, 90% или 95% (96%, 97%, 98%, 99% и 100%) сходство последовательностей с исходной последовательностью в сочетании с одной или несколькими модификациями в остове или боковой цепи аминокислоты или с добавлением группы или другой молекулы и т.д. Иллюстративные аминокислоты, которые считают сходными (консервативные аминокислоты) с другими, известны в данной области и включают в себя, например, аминокислоты, приведенные в таблице 1.
Аналоги согласно изобретению также включают в себя аналоги, которые могут иметь по меньшей мере 35%, 50%, 60%, 70%, 80%, 90% или 95% (96%, 97%, 98%, 99% и 100%) идентичность последовательностей с исходной последовательностью или частью исходной последовательности. Также "аналог" может иметь, например, 35%, 50%, 60%, 70%, 80%, 90% или 95% идентичность (последовательности) с исходной последовательностью (т.е. аналог, который по меньшей мере на 35%, 50%, 60%, 70%, 80%, 90% или 95% является идентичным исходному пептиду) в сочетании с одной или несколькими модификациями остова или боковой цепи аминокислоты или добавлением группы или другой молекулы и т.д.
В рамках настоящего описания "фрагмент" следует понимать как полипептид, образованный из части исходной или основной последовательности или из аналога указанной основной последовательности. Фрагменты включают в себя полипептиды, обладающие укорочением на одну или несколько аминокислот, где укорочение может происходить на амино-конце (N-конце), карбокси-конце (C-конце) или внутри белка. Фрагмент может содержать такую же последовательность, что и соответствующая часть исходной последовательности. Биологически активные фрагменты носителя (полипептида), описанные в настоящем описании, охватываются настоящим изобретением.
Таким образом, биологически активные полипептиды в форме исходных полипептидов, фрагментов (модифицированных или немодифицированных), аналогов (модифицированных или немодифицированных), производных (модифицированных или немодифицированных), гомологов (модифицированных или немодифицированных) носителя, описанного в настоящем описании, охватываются настоящим изобретением.
Таким образом, в рамках настоящего описания охватывается любой полипептид, обладающий модификацией по сравнению с исходным полипептидом, которая не нарушает существенно требуемую биологическую активность. В данной области хорошо известно, что можно проводить ряд модификаций полипептидов согласно изобретению без нарушения их биологической активности. Эти модификации, с другой стороны, могут сохранять или повышать биологическую активность исходного полипептида или могут оптимизировать одно или несколько свойств (например стабильность, биодоступность и т.д.) полипептидов согласно изобретению, которые в некоторых случаях могут быт необходимы или желательны. Полипептиды согласно изобретению включают в себя, например, полипептиды, содержащие аминокислотные последовательности, модифицированные либо посредством природных процессов, таких как посттрансляционный процессинг, либо посредством способов химической модификации, которые известны в данной области. Модификации могут происходить в любой части полипептида, включая полипептидный остов, боковые цепи аминокислот и N-конец или C-конец. Следует учитывать, что такой же тип модификации может быть представлен в такой же или другой степени в нескольких участках данного полипептида. Также данный полипептид может содержать множество типов модификаций. Полипептиды могут быть разветвленными в результате убиквитинилирования, и они могут быть циклическими с ветвлением или без него. Циклические, разветвленные и разветвленные циклические полипептиды могут быть результатом посттрансляционных природных процессов, или их можно получать способами синтеза. Модификации включают в себя в качестве неограничивающего примера пегилирование, ацетилирование, ацилирование, добавление ацетоимидометильной (Acm) группы, АДФ-рибозилирование, алкилирование, амидирование, биотинилирование, карбамоилирование, карбоксиэтилирование, этерификацию, ковалентное присоединение флавина, ковалентное присоединение группы гема, ковалентное присоединение нуклеотида или производного нуклеотида, ковалентное присоединение лекарственного средства, ковалентное присоединение маркера (например, флуоресцентного, радиоактивного и т.д.), ковалентное присоединение липида или производного липида, ковалентное присоединение фосфатидилинозитола, поперечное сшивание, циклизацию, образование дисульфидной связи, деметилирование, образование поперечных связей, образование цистина, образование пироглутамата, формилирование, гамма-карбоксилирование, гликозилирование, образование GPI-якоря, гидроксилирование, йодирование, метилирование, миристоилирование, окисление, протеолитическую обработку, фосфорилирование, пренилирование, рацемизацию, селеноилирование, сульфатацию, опосредуемое транспортной РНК добавление аминокислот к белку, такое как аргинилирование и убиквитинилирование и т.д. В рамках настоящего описания следует понимать, что настоящим изобретением охватывается более одной модификации полипептидов, описанных в настоящем описании, в тех пределах, чтобы биологическая активность была сходной с активностью исходного (основного) полипептида.
Как описано выше, модификация полипептида может включать в себя, например, вставку аминокислоты (т.е. добавление), делецию и замену (т.е. замещение), либо консервативную, либо неконсервативную (например, D-аминокислоты, дезамино кислоты), в полипептидной последовательности, где такие изменения по существу не изменяют суммарную биологическую активность полипептида.
Пример замен может представлять собой замены, которые являются консервативными (т.е. где остаток заменяют другим остатком из того же основного типа или из той же группы) или, при желании, неконсервативными (т.е. где остаток заменяют аминокислотой другого типа). Кроме того, природные аминокислоты можно заменять неприродными аминокислотами (т.е. неприродная консервативная аминокислотная замена или неприродная неконсервативная аминокислотная замена).
Как понятно, природные аминокислоты можно подразделить на кислые, основные, нейтральные и полярные или нейтральные и неполярные. Более того, три из кодируемых аминокислот являются ароматическими. Это можно использовать, чтобы кодируемые полипептиды, отличающиеся от определенного полипептида согласно изобретению, содержали замещенные кодоны для аминокислот, из такого же типа или группы, что и замещенные аминокислоты. Таким образом, в некоторых случаях основные аминокислоты Lys, Arg и His могут быть взаимозаменяемыми; кислые аминокислоты Asp и Glu могут быть взаимозаменяемыми; нейтральные полярные аминокислоты Ser, Thr, Cys, Gln и Asn могут быть взаимозаменяемыми; неполярные алифатические аминокислоты Gly, Ala, Val, Ile и Leu являются взаимозаменяемыми, однако на основании размера Gly и Ala является более сходными и Val, Ile и Leu являются более сходными друг с другом, и ароматические аминокислоты Phe, Trp и Tyr могут быть взаимозаменяемыми.
Кроме того, следует отметить, что если полипептиды получены синтетически, также можно проводить замены аминокислотами, которые не кодируются ДНК в природе (не встречающимися в природе, или неприродными аминокислотами).
В рамках настоящего описания неприродные аминокислоты следует понимать как аминокислоты, которые в природе не продуцируются или не встречаются у млекопитающих. Неприродная аминокислота включает в себя D-аминокислоту, аминокислоту, имеющую ацетиламинометильную группу, присоединенную к атому серы в цистеине, пегилированную аминокислоту и т.д. Включение неприродной аминокислоты в определенную полипептидную последовательность, таким образом, приведет к производному исходного полипептида. Неприродные аминокислоты (остатки) также включают в себя омега-аминокислоты формулы NH2(CH2)nCOOH, где n представляет собой 2-6, нейтральные неполярные аминокислоты, такие как саркозин, трет-бутилаланин, трет-бутилглицин, N-метилизолейцин, норлейцин и т.д. Фенилглицином можно заменять Trp, Tyr или Phe; цитруллин и метионинсульфоксид являются нейтральными неполярными, цистеиновая кислота является кислой, и орнитин является основным. Пролин можно заменять гидроксипролином и сохранять обусловленные конформацией свойства.
В данной области известно, что посредством мутагенеза с заменой можно получать аналоги и сохранять биологическую активность полипептидов согласно изобретению. Эти аналоги обладают по меньшей мере одним удаленным аминокислотным остатком в молекуле белка и встроенным на его место другим остатком. Примеры замен, определяемых как "консервативные замены", представлены в таблице 1. Если такие замены приводят к нежелательным изменениям, тогда вводят другой тип замен, обозначенный в таблице 1 как "иллюстративные замены", или как дополнительно описано в настоящем описании в отношении классов аминокислот, и проводят скрининг продуктов.
В некоторых случаях может представлять интерес модификация биологической активности полипептида посредством аминокислотной замены, вставки или делеции. Например, модификация полипептида может приводить к повышению биологической активности полипептида, может модулировать его токсичность, может приводить к изменению биодоступности или стабильности или может модулировать его иммунологическую активность или иммунологическую идентичность. Существенные модификации функции или иммунологического сходства проводят посредством выбора замен, которые значительно отличаются по своему эффекту на поддержание (a) структуры полипептидного остова в области замены, например, такого как конформация слоя или спирали, (b) заряда или гидрофобности молекулы в предназначенном для воздействия участке или (c) объема боковой цепи. Природные остатки подразделяют на группы, исходя из общих свойств боковых цепей:
(1) гидрофобные: норлейцин, метионин (Met), аланин (Ala), валин (Val), лейцин (Leu), изолейцин (Ile), гистидин (His), триптофан (Trp), тирозин (Tyr), фенилаланин (Phe),
(2) нейтральные гидрофильные: цистеин (Cys), серин (Ser), треонин (Thr),
(3) кислые/отрицательно заряженные: аспарагиновая кислота (Asp), глутаминовая кислота (Glu),
(4) основные: аспарагин (Asn), глутамин (Gln), гистидин (His), лизин (Lys), аргинин (Arg),
(5) остатки, которые влияют на ориентацию цепи: глицин (Gly), пролин (Pro),
(6) ароматические: триптофан (Trp), тирозин (Tyr), фенилаланин (Phe), гистидин (His),
(7) полярные: Ser, Thr, Asn, Gln,
(8) основные положительно заряженные: Arg, Lys, His и
(9) заряженные: Asp, Glu, Arg, Lys, His.
Неконсервативные замены приводят к замене члена из одного из этих классов членом другого класса. Консервативная замена приводит к замене члена одной из этих групп другим членом этих групп. Альтернативно другие консервативные аминокислотные замены приведены в таблице 1.
Биологически активный аналог может представлять собой, например, аналог, имеющий по меньшей мере одну (т.е. неконсервативной или консервативной) аминокислотную замену в исходной последовательности. Биологически активный аналог также может представлять собой, например, аналог, имеющий вставку из одной или нескольких аминокислот.
Другие иллюстративные аналоги включают в себя, например:
- аналог SEQ ID NO:1, который может иметь формулу I: X1-SEQ ID NO:1-X2,
- аналог Angiopep-1, который может иметь формулу II: X1-Angiopep-1-X2 и
- аналог Angiopep-2 может иметь формулу III: X1-Angiopep-2-X2.
X1 и X2 независимо может представлять собой аминокислотную последовательность из от 0 до приблизительно 100 (например, от 0 до приблизительно от 30 до 50) аминокислот. Источником X1 и X2 могут быть последовательные аминокислоты апротинина или аналогов апротинина (гомологичная аминокислотная последовательность), или им может быть любая другая аминокислотная последовательность (гетерологичная аминокислотная последовательность). Соединение любой из формул I, II или III также может содержать аминокислотную замену, делецию или вставку в аминокислотной последовательности Angiopep-1, Angiopep-2 или SEQ ID NO:1. Однако предпочтительно, чтобы аналог был биологически активным, как определяют посредством одного из анализов, описанных в настоящем описании, или посредством сходных или эквивалентных анализов.
Биологически активный полипептид (например, носитель) можно выявлять с использованием одного из анализов или способов, описанных в настоящем описании. Например, потенциальный носитель можно получать посредством общепринятого пептидного синтеза, конъюгировать с таксолом, как описано в настоящем описании, и тестировать в модели in vivo, как описано в настоящем описании. Биологически активный носитель можно выявлять, например, исходя из его эффективности в отношении повышения выживаемости животного, которому инъецировали опухолевые клетки и вводили конъюгат, по сравнению с контролем, в случае которого конъюгат не вводили. Также биологически активный носитель можно выявлять, исходя из его расположения в паренхиме, в анализе перфузии головного мозга in situ.
В рамках настоящего описания следует понимать, что если "диапазон" или "группа объектов" упоминают в отношении конкретной характеристики (например, температуры, концентрации, времени и т.п.) согласно изобретению, то в рамках настоящей заявки настоящее изобретение относится ко всем конкретным членам и сочетанию из поддиапазонов или подгрупп любых из них и прямо включает их в себя. Таким образом, следует понимать, что любой конкретный диапазон или группу следует непосредственно относить ко всем членам диапазона или группы по отдельности, а также ко всем возможным поддиапазонам или подгруппам, охватываемым им, и аналогично в отношении любых поддиапазонов или подгрупп в них. Таким образом, например,
- в отношении длины от 10 до 18 аминокислот I ее следует понимать, как прямо включающую в себя все отдельные длины, например, длину из 18, 17, 15, 10 и любого количества между ними и т.д. Таким образом, если не указано конкретно, каждый диапазон, упомянутый в настоящем описании, следует понимать как являющийся включающим. Например, в выражении "длиной от 5 до 10 аминокислот" диапазон включает в себя 5 и 10;
- и аналогично в отношении других параметров, таких как последовательности, длина, концентрации, элементы и т.д.
В частности, в рамках настоящего описания следует понимать, что все последовательности, области, участки, определенные в настоящем описании, таким образом, включают в себя все описанные отдельные последовательности, области, участки, а также все возможные подпоследовательности, подобласти, подучастки, как в случае, когда такие подпоследовательности, подобласти, подучастки определяют как обязательно включающие в себя конкретные возможности, так и в случае, если они исключают конкретные возможности, или в случае их сочетания; например, исключающее определение для области можно толковать следующим образом: "при условии, что указанный полипептид не короче 4, 5, 6, 7, 8 или 9 аминокислот". Следующий пример отрицательного ограничения является следующим: последовательность, содержащая SEQ ID NO:X, за исключением полипептида SEQ ID NO:Y и т.д. Дополнительный пример отрицательного ограничения является следующим: при условии, что указанный полипептид не представляет собой (не содержит или не состоит из) SEQ ID NO:Z.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На чертежах, которые иллюстрируют иллюстративные варианты осуществления этого изобретения:
на Фиг. 1 представлен пример анализа с использованием трициновых гелей;
на Фиг. 2 представлен способ присоединения вектора или носителя согласно изобретению к паклитакселу;
на Фиг. 3 представлен эффект лечения модели глиобластомы на крысах Льюиса посредством паклитаксела, конъюгированного с апротинином;
на Фиг. 4 представлен эффект лечения модели глиобластомы у мышей nude посредством паклитаксела, конъюгированного с AngioPep-1;
на Фиг. 5 представлен протокол, используемый для конъюгации апротинина с IgG с использованием вещества для поперечного сшивания BS3;
на Фиг. 6 представлен протокол, используемый для конъюгации апротинина IgG с использованием вещества для поперечного сшивания sulfo-EMCS;
на Фиг. 7 представлено проникновение в головной мозг конъюгатов IgG-апротинин;
на Фиг. 9 представлен эффект лечения конъюгатом таксол-Angiopep-2 на выживание мышей (бестимусных, мышей nude) с имплантированной глиобластомой и
на Фиг. 9 представлена структура иллюстративных полипептидов согласно изобретению.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым молекулам, которые могут действовать в качестве векторов или носителей для транспорта вещества, лекарственного средства или другой молекулы в головной мозг и/или центральную нервную систему (ЦНС). Вещества, лекарственные средства или другие молекулы, которые являются неспособными или неэффективными к самостоятельному прохождению через гематоэнцефалический барьер, будут транспортироваться через гематоэнцефалический барьер после присоединения или связывания (конъюгации) с вектором или носителем. Альтернативно для вещества, которое способно самостоятельно преодолевать гематоэнцефалический, также может быть показано повышение транспорта после конъюгации с носителем согласно изобретению. Такие конъюгаты могут находиться в форме композиции, такой как фармацевтическая композиция, для лечения состояния или заболевания.
Создание пригодных в качестве векторов-носителей молекул
В международной заявке No. WO 2004/060403 авторы изобретения описали, что AngioPep-1 (SEQ ID NO:67) и апротинин (SEQ ID NO:98) представляют собой эффективные векторы для транспорта требуемых молекул через гематоэнцефалический барьер. Авторы изобретения в настоящем описании демонстрируют, что для транспорта вещества через гематоэнцефалический барьер в качестве носителей также можно использовать другие молекулы. Следовательно, пептиды, обладающие сходными с апротинином и Angiopep-1 доменами, и модифицированную форму Angiopep-1 (амидированную, пептид No.67), таким образом, рассматривали как возможные векторы-носители. Эти пептиды, являющиеся производными, сходны с апротинином и Angiopep-1, однако они содержат различные аминокислотные вставки и обладают отличающимися зарядами. Таким образом, 96 пептидов, представленных в таблице 2, а также дополнительные пептиды, приведенные в списке последовательностей, тестировали на их возможность выступать в качестве носителя.
В рамках настоящего описания следует понимать, что в следующих экспериментах пептиды были отобраны, исходя из их более высокой по сравнению с другими пептидами активности. Пептиды, которые не были отобраны для дальнейшего экспериментирования, никоим образом не исключаются и не подразумевают, что их считают нефункцональными. Эти пептиды демонстрируют значительную активность и обладают применимостью в качестве (биологически активных) носителей и также охватываются настоящим изобретением.

Отбор посредством модели in vitro
Модель in vitro использовали для скринингового анализа и для изучения механизма транспорта лекарственного средства в головной мозг. Эта эффективная модель гематоэнцефалического барьера in vitro была разработана компанией CELLIAL™ Technologies. Модель in vitro использовали для оценки способности различных носителей достигать головного мозга, получая воспроизводимые результаты. Модель состоит из совместной культуры бычьих эндотелиальных клеток капилляров головного мозга и глиальных клеток крысы. Она отражает ультраструктурные характерные особенности эндотелия головного мозга, включая плотные контакты, отсутствие отверстий, отсутствие трансэндотелиальных каналов, низкую проницаемость для гидрофильных молекул и высокую устойчивость к электричеству. Более того, было показано, что эта модель обладает высоким коэффициентом корреляции между анализом in vitro и in vivo для широкого диапазона тестируемых молекул. К настоящему времени все полученные данные показывают, что эта модель ГЭБ полностью имитирует условия in vivo вследствие воспроизведения некоторых комплексных условий клеточного окружения, которые существуют in vivo, при сохранении экспериментальных преимуществ, обусловленных культурой ткани. Многие исследования подтвердили, что эта клеточная совместная культура является наиболее воспроизводимой моделью ГЭБ in vitro.
Модель ГЭБ in vitro создали с использованием совместной культуры BBCEC и астроцитов. Перед культивированием клеток сменные элементы планшетов (Millicell-PC 3,0 мкМ; диаметр 30 мм) покрывали с верхней стороны коллагеном хвоста крысы. Затем их устанавливали в микропланшеты с шестью лунками, содержащие астроциты, и BBCEC наносили с верхней стороны фильтров в 2 мл среды для совместной культуры. Среду для BBCEC меняли три раза в неделю. При этих условиях дифференцированные BBCEC формировали сплошной монослой через 7 суток. Эксперименты проводили между 5 и 7 сутками после достижения смыкания монослоя. Для проверки проницаемости эндотелия определяли коэффициент проницаемости для сахарозы.
Первичные культуры смешанных астроцитов получали из коры головного мозга новорожденных крыс (Dehouck M.P., Meresse S., Delorme P., Fruchart J.C, Cecchelli, R. An Easier, Reproductible, and Mass-Production Method to Study the Blood-Brain Barrier In Vitro. J.Neurochem, 54, 1798-1801, 1990). В кратком изложении, после удаление мягких мозговых оболочек ткань головного мозга пропускали аккуратно через 82-мкм нейлоновое сито. Астроциты выращивали в микропланшетах с шестью лунками в концентрации 1,2x105 клеток/мл в 2 мл оптимальной культуральной среды (DMEM), дополненной 10% инактивированной нагреванием эмбриональной телячьей сывороткой. Среду меняли дважды в неделю.
Бычьи эндотелиальные клетки капилляров головного мозга (BBCEC) получали от Cellial Technologies. Клетки культивировали в присутствии среды DMEM, дополненной 10% (об./об.) сывороткой лошади и 10% инактивированной нагреванием cывороткой теленка, 2 мМ глутамином, 50 мкг/мл гентамицина и 1 нг/мл основного фактора роста фибробластов, добавляемого раз в двое суток.
Первоначально, на первом уровне отбора, 96 пептидов, как описано в таблице 2, тестировали в качестве носителя с помощью модели ГЭБ in vitro. Каждый пептид добавляли сверху сменных элементов, покрытых или непокрытых эндотелиальными клетками, на 90 минут при 37°C. После инкубации пептиды с нижней стороны камер разделяли посредством электрофореза. Гели для электрофореза для визуализации пептидов окрашивали голубым Кумасси, как представлено для некоторых пептидов (в качестве неограничивающего примера) на Фиг. 1. AngioPep-1 (либо SEQ ID NO:67, либо пептид no.67 (амидированная форма)) часто используют в настоящем описании в качестве ссылки или для целей сравнения. На Фиг. 1 каждый исходный пептид, нанесенный на верхнюю часть фильтров, помещали в гель для электрофореза (ini) в качестве контроля. После 90 минут трансцитоза объем 50 мкл с базолатеральной стороны фильтров, покрытых эндотелиальными клетками (+) или не покрытых (-), помещали в трициновые гели. Для визуализации пептидов гели окрашивали голубым Кумасси.
После первого уровня скрининга пептиды, определенные с нижней стороны камер посредством окрашивания голубым Кумасси (5, 8, 45, 67, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 81, 82, 90 и 91), отбирали для дальнейшего исследования с йодированными пептидами. В кратком изложении, выбранные пептиды йодировали посредством стандартных способов с использованием йодных гранул из Sigma. Для каждого белка использовали две йодные гранулы. Эти гранулы промывали дважды 3 мл фосфатного буфера (PB) на фильтре Whatman™ и ресуспендировали в 60 мкл PB. К суспензии гранул добавляли 125I (1 мКи) из Amersham-Pharmacia biotech на 5 мин при комнатной температуре. Йодирование для каждого пептида начинали посредством добавления 100 мкг (80-100 мкл) суспензии гранул. После инкубации в течение 10 мин при комнатной температуре супернатанты наносили на колонку для обессоливания, предварительно заполненную 5 мл поперечно-сшитого декстрана™ от Pierce, и 125I-белки элюировали посредством 10 мл PBS. Собирали фракции объемом 0,5 мл и измеряли радиоактивность в 5 мкл каждой фракции. Фракции, соответствующие 125I-белкам, собирали и проводили их диализ против буфера Ringer/Hepes, pH 7,4. Эффективность радиоактивного мечения составляла между 0,6-1,0 x 108 cpm/100 мкг белка.
Йодированные пептиды также исследовали посредством модели ГЭБ in vitro. Каждый пептид добавляли на верхнюю сторону сменных элементов, покрытых или не покрытых эндотелиальными клетками, на 90 минут при 37°C. После инкубации пептиды с нижней стороны камер осаждали посредством ТХУ. Результаты выражали в виде соотношений cpm. Для каждого [125I]-пептида количество cpm в нижней части камеры делили на общее число cpm, добавленных на фильтр, покрытый эндотелиальными клетками (+клетки/исходное значение) или непокрытый ими
(-клетки/исходное значение). Также вычисляли соотношение между количеством [125I]-пептида, связанного на дне камеры фильтров, покрытых эндотелиальными клетками или не покрытых ими (+клетки/-клетки). Очень низкое соотношение -клетки/исходное значение указывает на то, что фильтры могут препятствовать пептидам (пептиды 5 и 8). Высокое соотношение +клетки/исходное значение и +клетки/-клетки указывает на более высокое прохождение пептидов через эндотелиальные клетки головного мозга. Результаты для предварительно выбранных 18 пептидов представлены в таблице 3.
Результаты скрининга пептидов после второго уровня скрининга
Исходя из этих результатов, отбирали 12 пептидов с соотношениями +клетки/-клетки, как правило, превышающим 0,35, а именно: 5, 8, 67, 75, 76, 77, 78, 79, 81, 82, 90 и 91. Также для дальнейшего исследования отбирали пептиды #91 и #77 вследствие их соотношений +клетки/-клетки (>0,2).
Затем 12 отобранных пептидов исследовали с использованием модели ГЭБ in vitro посредством оценки их коэффициентов проницаемости. Эффект каждого выбранного пептида при 250 нМ на целостность ГЭБ определяли посредством измерения проницаемости [14C]-сахарозы в модели проницаемости ГЭБ на монослое BBCEC, выращенном на фильтрах в присутствии астроцитов. Для проведения этого теста монослои эндотелиальных клеток головного мозга, выращенные на сменных элементах, переносили в 6-луночные планшеты, содержащие 2 мл Ringer-Hepes на лунку (базолатеральный отдел) на два часа при 37°C. Раствор Ringer-Hepes состоял из 150 мМ NaCl, 5,2 мМ KCl, 2,2 мМ CaCl2, 0,2 мМ MgCl2, 6 мМ NaHCO3, 5 мМ Hepes, 2,8 мМ Hepes, pH 7,4. В каждой верхней камере культуральную среду заменяли на 1 мл Ringer-Hepes, содержащего меченую [14C]-сахарозу. Через различные промежутки времени сменные элементы помещали в другую лунку. Перенос [14C]-сахарозы измеряли при 37°C, на фильтрах без клеток или посредством фильтров, покрытых клетками BBCEC. Пептиды добавляли в начале эксперимента в нулевой момент времени. Результаты наносили на график в качестве зависимости клиренса сахарозы (мкл) от времени (мин).
Клиренс (мкл)=
Концентрация метки на наружной поверхности × Объем наружной камеры/
Концентрация метки на люминальной поверхности
Угловой коэффициент линейного изменения (мкл/мин) представляет собой коэффициент проницаемости сахарозы для фильтра без клеток (Psf) и фильтра, покрытого клетками BBCEC (PSt) в присутствии пептида.
Коэффициент проницаемости (Pe) вычисляли как:
1/Pe = (1/PSt-1/PSf)/площадь фильтра (4,2 см2)
Отбирали пептиды с наиболее высоким Pe: 67, 76, 90, 91, 5, 79, 8 и 78.
В качестве четвертого уровня отбора для отбора наилучших пептидов использовали перфузию головного мозга in situ (у мышей). Этот процесс также позволил отличить соединения, оставшиеся в сосудистой части головного мозга, и соединения, которые прошли через наружную мембрану эндотелия для проникновения в паренхиму головного мозга. Действительно, способ постперфузионной капиллярной элиминации позволяет определить, действительно ли молекула пересекает эндотелий для проникновения в паренхиму головного мозга. С использованием этого способа здесь показано, что определенные пептиды обладают тенденцией к накоплению во фракции паренхимы головного мозга (см. таблица 4).
(мл/100 г)
Для четырех пептидов, а именно 5, 67, 76 и 91, были показаны наивысшие уровни распределения в паренхиме с объемом, превышающим 20 мл/100 г, и для них было показано нахождение по меньшей мере 25% объема в головном мозге в целом (в гомогенате), что таким образом демонстрирует их наибольший потенциал в качестве носителя для применения в качестве векторов для транспорта. Пептид 79 исключили вследствие его более низкого объема распределения в паренхиме головного мозга (18 мл/100 г). Пептид 67 представляет собой амидированную форму Angiopep-1, описанного в предшествующей заявке, которую подали авторы настоящего изобретения. Амидирование пептида влияет на общий заряд пептида. Из таблиц 2 и 3 очевидно, что два пептида, обладающих различным зарядом, не обязательно обладают одинаковой активностью.
Вектор или носитель согласно изобретению, таким образом, можно использовать для способа транспорта вещества через гематоэнцефалический барьер, включающего в себя введение индивидууму вещества, которое содержит активный ингредиент или фармацевтическое средство, присоединенное к носителю, такому как апротинин или его функциональное производное (т.е. аналог апротинина, фрагмент апротинина, производное апротинина, аналог фрагмента апротинина).
Носитель и конъюгат можно вводить пациенту внутриартериально, интраназально, внутрибрюшинно, внутривенно, внутримышечно, подкожно, трансдермально или перорально. Вещество может представлять собой, например, антиангиогенное соединение. Вещество может иметь максимальную массу 160000 Дальтон. Как описано в настоящем описании, вещество может представлять собой маркер или лекарственное средство, такое как низкомолекулярное лекарственное средство, белок, пептид или фермент. Лекарственное средство может быть адаптированным для лечения, например, неврологического заболевания или нарушения центральной нервной системы у пациента. Лекарственное средство может представлять собой цитотоксическое лекарственное средство, а маркер может представлять собой поддающуюся детекции метку, такую как радиоактивная метка, зеленой флуоресцирующий белок, белок histag или β-галактозидазу. Вещество можно доставлять, например, в центральную нервную систему пациента.
В соответствии с другим вариантом осуществления применение, способы, соединения, вещества, лекарственные средства или медикаменты, упомянутые в настоящем описании, не изменяют целостности гематоэнцефалического барьера пациента.
В соответствии со следующим вариантом осуществления настоящего изобретения пептид может быть выбран из группы, состоящей из апротинина, фрагмента апротинина (SEQ ID NO:1) и любого из пептидов, определяемых с SEQ ID NO:1 по 97, 99, 100 или 101.
Например, пептиды 5, 76, 91, 97 и 97, а также пептид 67 можно использовать в соответствии с настоящим изобретением, посредством присоединения их к веществу или соединению для транспорта вещества или соединения через гематоэнцефалический барьер пациента. Вещество или соединение может быть адаптировано для лечения неврологического заболевания или для лечения нарушения центральной нервной системы.
Носитель согласно изобретению, такой, например, как пептиды 5, 76, 91 и 97, а также пептид 67, могут быть связаны с поддающейся детекции меткой или меченными посредством поддающейся детекции метки, такой как радиовизуализирующее вещество, такое как вещества, испускающие излучение, для выявления заболевания или состояния, например, посредством применения конъюгата радиовизуализирующее вещество-антитело-носитель, где антитело связывается со специфичным для заболевания или состояния антигеном. Другие молекулы для связывания, помимо антител, и которые являются известными и которые применяют в данной области, также охватываются настоящим изобретением. Альтернативно носитель или его функциональное производное согласно изобретению или их смеси могут быть связаны с лекарственным средством для лечения заболевания или состояния, или они могут быть связаны с их смесями или меченными посредством их. Лечение можно проводить посредством введения конъюгата носитель-вещество согласно изобретению индивидууму в условиях, которые обеспечивают транспорт вещества через гематоэнцефалический барьер.
В настоящем описании лекарственное средство может представлять собой лекарственное средство, медикамент, вещество, испускающее излучение, клеточный токсин (например, химиотерапевтическое средство), и/или их биологически активный фрагмент, и/или их смесь для обеспечения гибели клеток, или оно может представлять собой вещество для лечения, исцеления, смягчения течения, улучшения, ослабления или торможения заболевания или состояния у индивидуума, подвергаемого лечению. Лекарственное средство может представлять собой синтетический продукт или продукт микроорганизма, относящегося к грибам, бактериям, или другого микроорганизма, такого как микоплазма, вирус и т.д., животного, такого как рептилия, или растительного происхождения. Лекарственное средство и/или его биологически активный фрагмент может представлять собой ферментативно активное вещество и/или его фрагмент, или оно может действовать посредством ингибирования или блокирования важного и/или необходимого клеточного каскада или посредством конкуренции с важным и/или необходимым природным клеточным компонентом.
Примеры радиовизуализирующих веществ, испускающих излучение (поддающиеся детекции радиоактивные метки), которые могут быть пригодны, можно проиллюстрировать с помощью индия-111, технеция-99 или йода-131 в низкой дозе.
Поддающиеся детекции метки, или маркеры, для применения в соответствии с настоящим изобретением могут представлять собой радиоактивную метку, флуоресцентную метку, активную в отношении ядерного магнитного резонанса метку, люминесцентную метку, хромофорную метку, позитронно-активный изотоп для сканнера PET, хемилюминесцентную метку или ферментную метку. Флуоресцентные метки включают в себя, не ограничиваясь ими, зеленый флуоресцирующий белок (GFP), флуоресцеин и родамин. Хемилюминесцентные метки включают в себя, не ограничиваясь ими, люциферазу и β-галактозидазу. Ферментные метки включают в себя, не ограничиваясь ими, пероксидазу и фосфатазу. Также поддающаяся детекции метка может представлять собой histag.
Подразумевается, что вещество может освобождаться от носителя после транспорта через гематоэнцефалический барьер, например посредством ферментативного расщепления или разрушения химической связи между носителем и веществом. Затем высвобожденное вещество может функционировать с предусмотренной для него способностью в отсутствии носителя.
Настоящее изобретение будет более понятным при рассмотрении следующих примеров, которые приведены для иллюстрации этого изобретения, а не для ограничения его объема. Следующие примеры приведены для апротинина. Однако здесь было показано, что молекулы согласно изобретению обладают общими свойствами с апротинином в отношении их потенциала в качестве носителя для транспорта вещества через гематоэнцефалический барьер. Эти примеры, таким образом, распространяются на молекулы согласно изобретению.
ПРИМЕР 1
Стратегии для конъюгации лекарственного средства (паклитаксела)
Для конъюгации паклитаксел (ТАКСОЛ™) обладает 2 основными положениями (положение C2' и C7). На фиг. 2 представлен способ присоединения вектора или носителя согласно изобретению к паклитакселу. В кратком изложении, проводят реакцию паклитаксела с янтарным ангидридом пиридина в течение 3 часов при комнатной температуре для присоединения группы сукцинила в положении 2'. Такой 2'-сукцинилпаклитаксел обладает поддающейся расщеплению сложноэфирной связью в положении 2', при расщеплении которой может легко высвобождаться янтарная кислота. Эту поддающуюся расщеплению сложноэфирную связь при необходимости можно далее использовать для различных модификаций посредством линкеров. Затем проводят реакцию полученного 2'-O-сукцинилпаклитаксела с EDC/NHS в DMSO в течение 9 часов при комнатной температуре, с последующим добавлением носителя или вектора в Ringer/DMSO в течение дополнительного времени реакции, составляющего 4 часа, при комнатной температуре. Мониторинг реакции конъюгации, представленной на Фиг. 2, проводили посредством ВЭЖХ. Каждое промежуточное соединение, такое как паклитаксел, 2'-O-сукцинилпаклитаксел и 2'-O-NHS-сукцинилпаклитаксел, очищали и проверяли с использованием различных подходов, таких как ВЭЖХ, тонкослойная жидкостная хроматография, ЯМР (замена 13C или 1H), температура плавления, масс-спектрометрия. Конечный конъюгат анализировали посредством масс-спектрометрии и SDS-полиакриламидного гель-электрофореза. Это позволяет определение количества конъюгированных молекул паклитаксела на каждом векторе.
Определяли способность к трансцитозу конъюгата апротинин-паклитаксел, и она представлена ниже в таблице 5.
Определение способности конъюгата апротинин-таксол к трансцитозу через ГЭБ
(Ре 10-3 см/мин)
(Ре 10-3 см/мин)
Таксол
0,22
- Целостность барьера также сохраняется.
Как видно из таблицы 5, конъюгация паклитаксела с апротинином сохраняла способность к преодолению гематоэнцефалического барьера в модели in vitro без нарушения целостности сахарозы, таким образом подтверждая, что молекулы (также называемые в настоящем описании как векторы или носители) согласно изобретению, тем не менее, сохраняют их активность при конъюгации с крупными химическими группами, такими как паклитаксел.
Затем проводили исследования выживаемости в модели опухоли мозга крысы для проверки сохранения активности конъюгированного паклитаксела in vivo. Для модели опухоли мозга крысы крысам проводили интрацеребральную имплантацию 50000 клеток глиомы CNS-1. Через трое суток посредством внутривенной инъекции животным проводили введение носителя (апротинина), паклитаксела (5 мг/кг) или паклитаксел-апротинина (5 мг/кг). Затем введение проводили каждую неделю до момента умерщвления животного (см. Фиг. 3). Мониторинг крыс на наличие клинических симптомов и снижение массы проводили каждые сутки. В соответствии с протоколом good animal practice животных умерщвляли, когда снижение массы наблюдали в течение 3 последовательных суток или ранее, если снижение массы составляло более 20% от исходной массы животного.
При использовании указанного экспериментального протокола, при инъецировании отдельно, паклитаксел в максимальной переносимой дозе (54 мг/кг) не был способен повышать выживаемость мышей (Laccabue et al., 2001 Cancer, 92 (12): 3085-92).
Также исследование выживаемости проводили на мышах, которым имплантировали ксенотрансплантат опухоли мозга человека. Для модели опухоли мозга мыши мышам проводили интрацеребральную имплантацию 500000 клеток глиомы человека U87. Через 3 суток после имплантации животным проводили введение паклитаксел-Angiopep1 (5 мг/кг) или носителя посредством внутривенной инъекции. Затем введение проводили каждую неделю до момента умерщвления животного. Мониторинг мышей на наличие клинических симптомов и снижение массы проводили каждые сутки. В соответствии с протоколом good animal practice животных умерщвляли, когда снижение массы наблюдали в течение 3 последовательных суток или ранее, если снижение массы составляло более 20% от исходной массы животного. В данном случае наблюдали, что средняя выживаемость для контрольной группы составляла 19 ± 2 суток. Для статистического анализа в качестве достоверного рассматривали 20% повышение выживаемости. Как можно видеть на Фиг. 4, конъюгат Паклитаксел-AngioPep-1 сохранял свою активность, обладая статистически значимым эффектом. Время выживаемости животных, которым вводили паклитаксел-angioPep1, достоверно повышалось по сравнению с контрольной группой (p<0,05, n=8).
Результаты, полученные в исследованиях выживаемости, показывают, что конъюгация паклитаксела с вектором согласно изобретению повышает выживаемость животных.
ПРИМЕР II
Стратегии для конъюгации антител
Поскольку белки обычно обладают несколькими аминогруппами, доступными для конъюгации, для поперечного сшивания терапевтических антител с векторами (носителями) согласно изобретению используют по аминогруппе с использованием активации посредством sulfo-NHS/EDC. Этот подход был выбран вследствие того, что он представляет собой быстрый, простой и воспроизводимый способ присоединения, вследствие того, что полученный конъюгат является стабильным, сохраняя, тем не менее, биологическую активность антитела, и вследствие того, что он обладает высокой эффективностью конъюгации, которую можно надежно контролировать, и незначительным неспецифичным взаимодействием в ходе процесса присоединения.
Антитела или фрагменты антител (Fab и Fab'2) конъюгировали с вектором согласно изобретению для повышения их доставки в головной мозг. Различные подходы для конъюгации использовали, чтобы сначала конъюгировать IgG с апротинином, показав, что носители согласно изобретению работают точно так же, как и апротинин.
Различные вещества для поперечного сшивания, такие как BS3 [бис(сульфосукцинимидил)суберат], NHS/EDC (N-гидроксисукцинимид и N-этил-N'(диметиламинопропил)карбодимид или Sulfo-EMCS ([N-e-малеимидокапроновая кислота]гидразид) тестировали для конъюгации с IgG. BS3 представляет собой гомобифункциональный сложный эфир N-гидроксисукцинимида, который воздействует на доступные первичные амины. NHS/EDC осуществляет конъюгацию групп первичных аминов карбоксильными группами. Sulfo-EMCS представляют собой гетеробифункциональные реакционно-способные группы (малеимид и NHS-сложный эфир), которые являются реакционно-способными в отношении сульфгидрильных групп и аминогрупп.
Сначала оценивали конъюгацию IgG с апротинином с использованием вещества для поперечного сшивания BS3 (Фиг. 5) или sulfo-EMCS (Фиг. 6).
Затем тестировали транспорт IgG или IgG-конъюгатов через ГЭБ. Захват [125I]-IgG с люминальной стороны капилляров головного мозга мыши определяли с использованием способа перфузии головного мозга in situ, адаптированного в лаборатории авторов изобретения для исследования захвата лекарственного средства в головном мозге мыши (Dagenais et al., 2000, J. Cereb. Blood Flow Metab. 20(2):381-386). Константы транспорта через ГЭБ определяли, как описано ранее Smith (1996, Pharm. Biotechnol. 8:285-307). Захват IgG выражали в качестве объема распределения (Vd) на основе следующего выражения:
Vd=Q*br/C*pf,
где Q*br представляет собой вычисленное количество [125I]-IgG или конъюгата [125I]-IgG-апротинин на грамм правого полушария головного мозга и C*pf представляет собой концентрацию меченого маркера, измеренную в перфузируемой жидкости.
Результаты этого эксперимента показывают, что захват в головном мозге конъюгата [125I]-IgG-апротинин является более высоким, чем захват неконъюгированного [125I]-IgG (см. Фиг. 7).
Конъюгация IgG с апротинином повышает их накопление в паренхиме головного мозга in vivo.
ПРИМЕР III
Эффект конъюгата таксол-Angiopep-2 на выживаемость мышей
Это исследование таксол-Angiopep-2 (обозначаемого в настоящем описании как пептид no. 97 (angiopep2 не является амидированным)) проводили для определения возможности повышения выживаемости мышей посредством конъюгации таксола с Angiopep-2. Структура Angiopep-2 представлена в SEQ ID NO:97. Для этого эксперимента мышам проводили интрацеребральную имплантацию 500000 клеток глиомы человека U87. Через 3 суток после имплантации животным вводили носитель (DMSO/Ringer-Hepes 80:20 об./об. (т.е. контроль)) или конъюгат таксол-Angiopep-2 (3:1, т.е. соотношение 3 молекулы таксола на каждый пептид; TxlAn2 (5 мг/кг)) посредством инъекции в хвостовую вену (Фиг. 8). Мониторинг мышей на наличие клинических симптомов и снижение массы проводили каждые сутки. Введение проводили до момента умерщвления животных. Как представлено в таблице 6, авторы настоящего изобретения выявили, что средняя выживаемость составляла 18 суток для контрольной группы, в то время как средняя выживаемость мышей, которым вводили конъюгат таксол-Angiopep-2, составляла 21 сутки (Фиг. 8). Кривая выживаемости, полученная для мышей, которым вводили конъюгат таксол-Angiopep-2 (красный цвет), показывает, что средняя выживаемость была значительно повышена на 17% (Фиг. 8). Статистический анализ, также представленный в таблице 6, показывает, что введение конъюгата таксол-Angiopep-2 достоверно повышает выживаемость на 17% (значение p = 0,048).
Обобщение результатов исследования выживаемости
Содержание каждой публикации, патента и патентной заявки, упомянутой в настоящей заявке, включено в настоящее описание в качестве ссылки.
Несмотря на то, что настоящее изобретение подробно описано в настоящем описании и проиллюстрировано в прилагаемых рисунках, следует понимать, что это изобретение не ограничивается вариантами осуществления, описанными в настоящем описании, и что различные изменения и модификации можно проводить без отклонения от объема и сущности настоящего изобретения.
Несмотря на то, что это изобретение описано применительно к конкретным вариантам его осуществления, следует понимать, что возможны его дальнейшие модификации и предполагается, что эта заявка охватывает любые варианты, способы применения, и усовершенствования этого изобретения, главным образом, в соответствии с принципами этого изобретения и включает в себя такие отклонения от настоящего описания, которые находятся в пределах известной или общепринятой практики в области, к которой относится это изобретение, и которые можно применять в отношении основных характеристик, указанных выше в настоящем описании, и которые вытекают из объема прилагаемой формулы изобретения.
ПОСЛЕДОВАТЕЛЬНОСТИ:
SEQ ID NO:

Пептид Nо. 5 содержит аминокислотную последовательность, определяемую SEQ ID NO:5, и является амидированным на его С-конце (см., например, Фиг.9).



Пептид по. 67 содержит аминокислотную последовательность, определяемую SEQ ID NO:67 и является амидированным на его С- конце (см., например. Фиг.9)

Пептид по. 76 содержит аминокислотную последовательность, определяемую SEQ ID NO:76 и является амидированным на его С-конце (см., например. Фиг.9)

Пептид по. 91 содержит аминокислотную последовательность, определяемую SEQ ID NO:91 и является амидированным на его С-конце (см., например. Фиг.9).

SEQ ID NO:106

| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИПЕПТИДЫ АПРОТИНИНА ДЛЯ ТРАНСПОРТА СОЕДИНЕНИЯ ЧЕРЕЗ ГЕМАТОЭНЦЕФАЛИЧЕСКИЙ БАРЬЕР | 2010 |
|
RU2611193C2 |
| УСИЛЕНИЕ ДЕЙСТВИЯ ПРОТИВОРАКОВЫХ АГЕНТОВ | 2006 |
|
RU2422143C2 |
| КОНЪЮГАТЫ ЭТОПОЗИДА И ДОКСОРУБИЦИНА ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2009 |
|
RU2531591C2 |
| ШАТТЛ ДЛЯ ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА | 2013 |
|
RU2663120C2 |
| ШАТТЛ ДЛЯ ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА | 2013 |
|
RU2711552C2 |
| БИОЛОГИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ ПЕПТИДА VAPEEHPTLLTEAPLNPK | 2005 |
|
RU2377249C2 |
| ШАТТЛ ДЛЯ ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА | 2019 |
|
RU2754794C2 |
| КОМПОЗИЦИЯ, НА ОСНОВЕ ГИДРОФОБНЫХ АГЕНТОВ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ(ВАРИАНТЫ) | 2009 |
|
RU2518240C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ УЛУЧШЕННОЙ ДОСТАВКИ МАКРОМОЛЕКУЛ | 2009 |
|
RU2522245C2 |
| БИСПЕЦИФИЧНЫЕ АНТИТЕЛА ПРОТИВ ГАПТЕНА/ПРОТИВ РЕЦЕПТОРА ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА, ИХ КОМПЛЕКСЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЧЕЛНОКОВ ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА | 2014 |
|
RU2693438C2 |































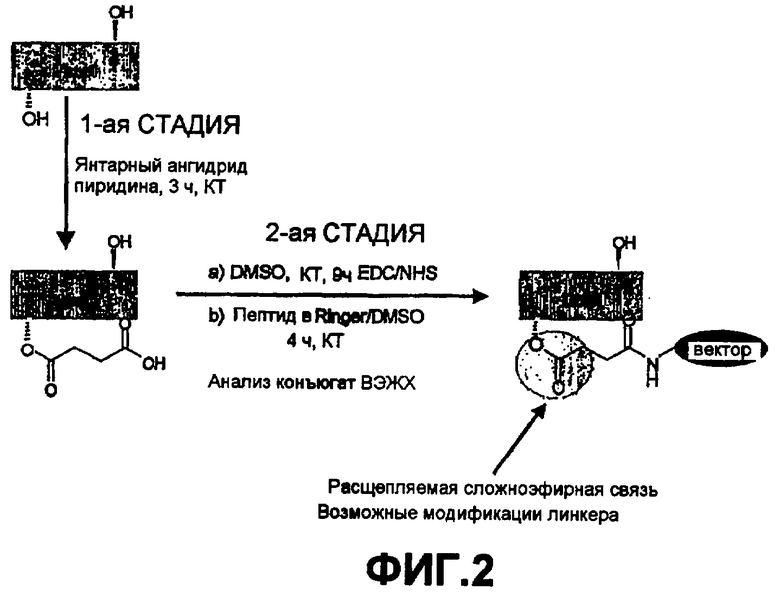
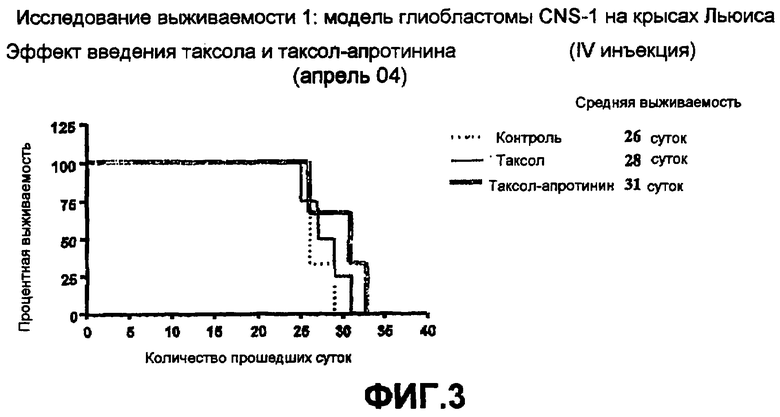

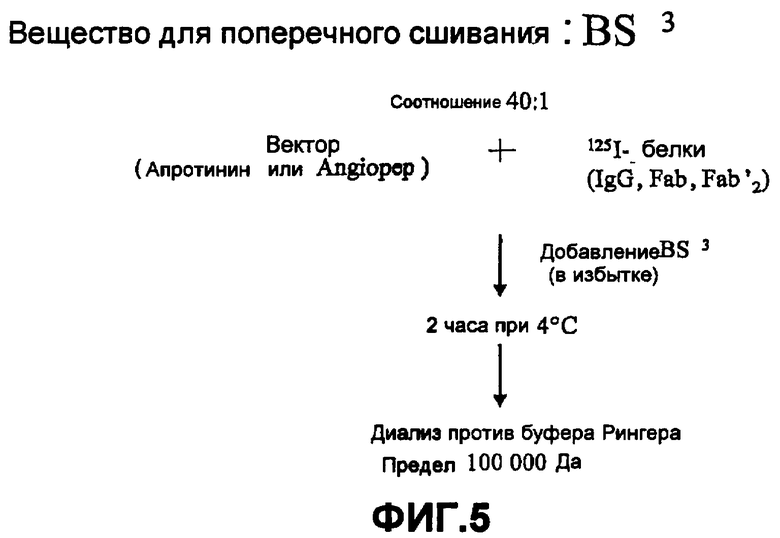
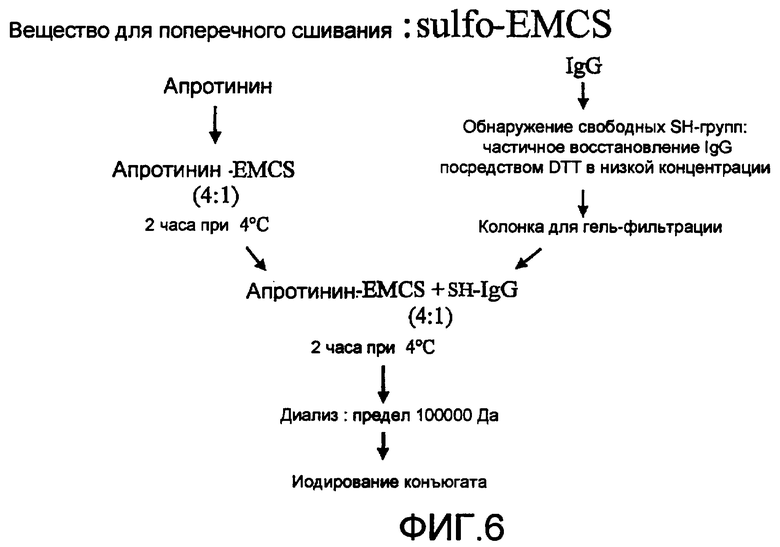
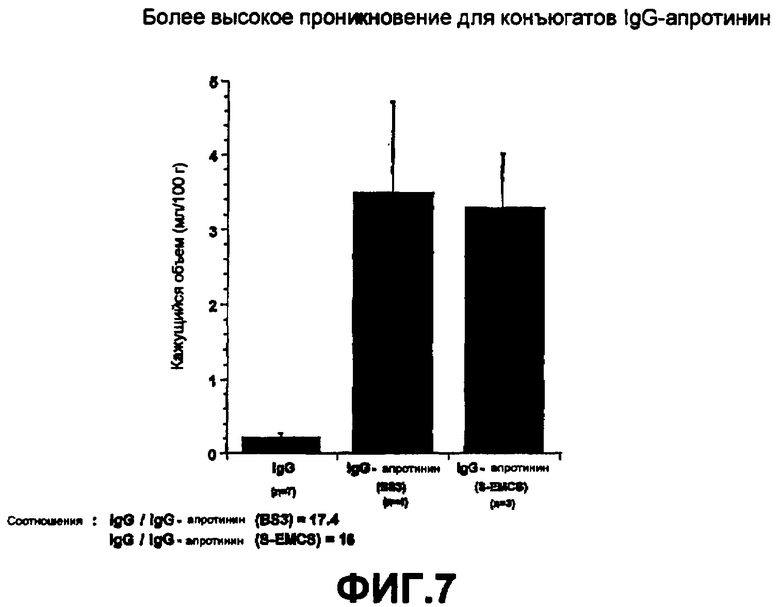
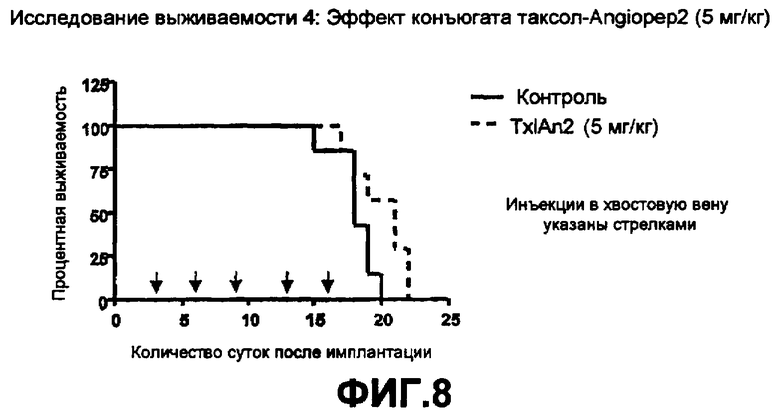
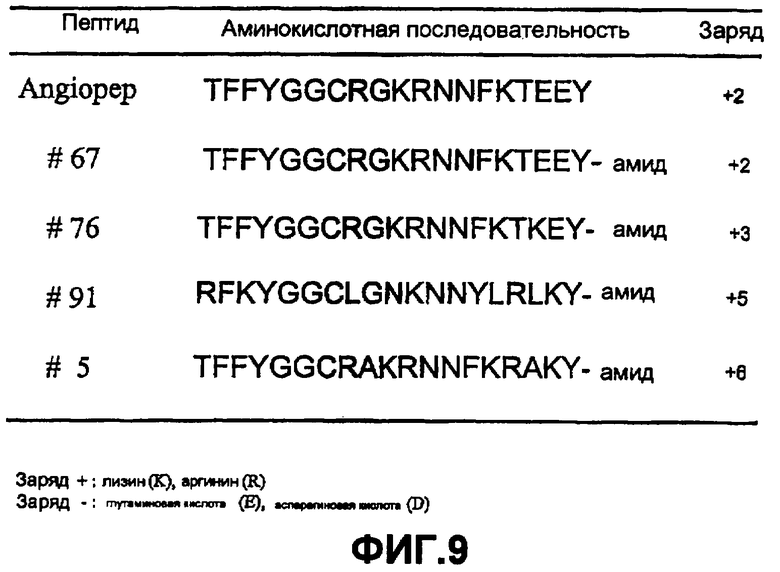
Изобретение относится к области генной инженерии, конкретно к носителям для доставки лекарственного средства, и может быть использовано в медицине. Получают аналог апротинина с последовательностью TFFYGGSRGKRNNFKTEEY, а также конъюгат на его основе. Изобретение позволяет осуществлять доставку соединения или лекарственного средства через гематоэнцефалический барьер млекопитающего. 3 н. и 3 з.п. ф-лы, 9 ил., 6 табл.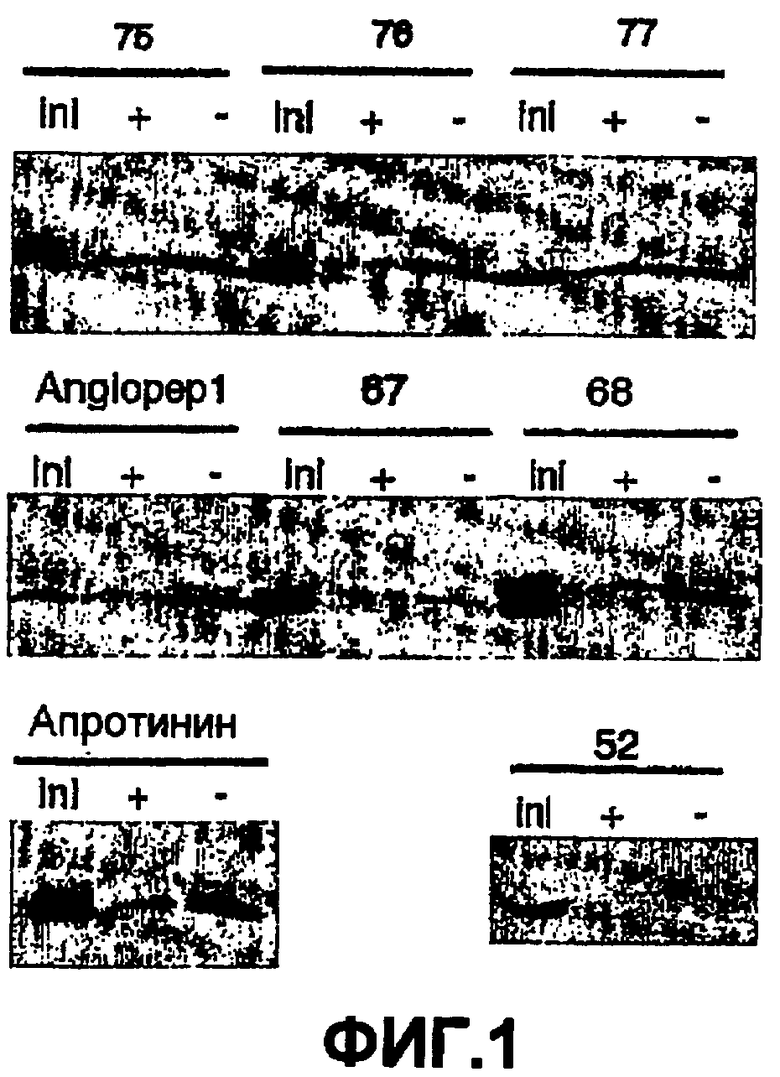
1. Полипептид, способный преодолевать гематоэнцефалический барьер, имеющий аминокислотную последовательность, содержащую последовательность TFFYGGSRGKRNNFKTEEY (SEQ ID NO:70).
2. Полипептид, способный преодолевать гематоэнцефалический барьер, имеющий аминокислотную последовательность, состоящую из последовательности TFFYGGSRGKRNNFKTEEY (SEQ ID NO:70).
3. Конъюгат «носитель-агент», способный преодолевать гематоэнцефалический барьер, где носитель представляет собой полипептид по п.1 или 2, а агент представляет собой лекарственное средство или соединение для визуализации, и конъюгация по своему характеру является химической.
4. Конъюгат по п.3, где конъюгация осуществляется через линкер.
5. Конъюгат по п.3 или 4, где указанный агент выбирают из группы, включающей лекарственное средство, белок, пептид, фермент, противоопухолевое средство, антитело, радиовизуализирующее средство, поддающуюся детекции метку и антиангиогенное соединение.
6. Конъюгат по п.5, где указанное противоопухолевое средство представляет собой паклитаксел.
| WO 2004060403 А2, 22.07.2004 | |||
| 0 |
|
SU393431A1 | |
| RU 97112745 A1, 20.07.1999. | |||
Авторы
Даты
2011-01-10—Публикация
2005-07-21—Подача