Настоящее изобретение относится к фармацевтически стабильным составам наночастиц малорастворимых лекарственных веществ. Настоящее изобретение также относится к способам получения таких составов.
Уровень техники
Основной проблемой приготовления составов из многих биологически активных соединений является их плохая растворимость или нерастворимость в воде. Составы для перорального применения нерастворимых в воде или малорастворимых биологически активных веществ часто демонстрируют низкую и неконтролируемую биодоступность. Следовательно, часто необходимо готовить составы лекарственных препаратов из мелких частиц для увеличения площади поверхности, а значит биодоступности и скорости растворения активного вещества. Составы, содержащие наночастицы лекарственных препаратов, то есть частицы, обычно имеющие средний размер менее 1000 нанометров (нм), во взвесях продемонстрировали успешные результаты в отношении увеличения биодоступности плохо растворимых лекарственных препаратов.
Желательно, чтобы нерастворимое в воде или малорастворимое активное вещество было стабильно при приготовлении состава. Для любой суспензии и для суспензии наночастиц (наносуспензии), в частности, существует два дестабилизирующих процесса, с учетом которых требуется стабилизация суспензии. К этим процессам относится агрегация частиц, или флокуляция, и рост частиц за счет эффекта Оствальда, возникающие в результате изменений в растворимости вследствие колебаний температуры в течение хранения. Чем более чувствительной по отношению к температуре является растворимость лекарственного препарата, тем в большей степени суспензия будет подвержена росту частиц за счет эффекта Оствальда. Обычные наносуспензии (как правило, суспензии в жидких носителях) стабилизируют, чтобы предотвратить агрегацию, добавляя модификаторы поверхности (например, неионогенные поверхностно-активные вещества или полимеры), которые адсорбируются на поверхности частиц лекарственного средства. Такие модификаторы поверхности стабилизируют частицы лекарственного средства за счет отталкивания, возникающего в результате стерического взаимодействия между полимерными цепями модификаторов поверхности, выходящих за пределы поверхности частиц лекарственного средства. Такой эффект зависит от природы, толщины и завершенности адсорбированных на частицах слоев поверхностно-активного вещества/полимера. Модификатор поверхности может также стабилизировать рост кристаллов, при этом полимер или неионогенное поверхностно-активное вещество образует подобную сетке пленку на поверхности кристалла, позволяя кристаллу расти только сквозь отверстия в сетке и, тем самым, замедляя рост кристаллов. Чем более конденсированной и чем менее пористой является пленка, тем лучше ее барьерные свойства и ее способность стабилизировать частицы, препятствуя росту кристаллов. Тем не менее, некоторые составы суспензий наночастиц могут быть чувствительны по отношению к агрегации частиц активного вещества даже в присутствии стабилизатора или модификатора поверхности, например при нагревании состава до температур выше точки помутнения стабилизатора поверхности. При температурах выше их точки помутнения стабилизаторы поверхности диссоциируют с поверхности наночастиц и осаждаются, оставляя наночастицы незащищенными. Незащищенные наночастицы могут затем агрегировать в кластеры частиц. При охлаждении стабилизаторы поверхности могут вновь возвращаться в раствор и покрывать агрегированные частицы, препятствуя их диссоциации на более желательные более мелкие частицы.
Соответственно, целью настоящего изобретения является получение стабильных составов наночастиц, которые не требуют использования стабилизатора или модификатора поверхности.
Краткое описание изобретения
Настоящее изобретение относится к фармацевтически стабильным составам наночастиц, включающих частицы малорастворимых лекарственных средств, имеющих средний размер частиц менее 1000 нм, и твердый или полутвердый дисперсионный носитель.
В представленном изобретении также описываются процессы приготовления стабильных составов наночастиц согласно настоящему изобретению и способы их применения.
Подробное описание изобретения
Основной особенностью составов наночастиц согласно настоящему изобретению является их способность сохранять стабильность в отсутствие модификатора или стабилизатора поверхности адсорбированного на поверхности частиц лекарства. В отличие от традиционных наносуспензий механизмы стабилизации составов согласно настоящему изобретению не включают поверхностных явлений. Твердый или полутвердый носитель действует в качестве стабилизатора агрегации за счет физического воздействия на подвижность частиц лекарственного средства. Когда носитель становится твердым при комнатной температуре или приобретает консистенцию очень вязкого полутвердого вещества, он препятствует или замедляет движение частиц лекарственного средства, а значит препятствует агрегации частиц лекарственного средства. Общеизвестно, что стабильность суспензии возрастает с вязкостью носителя или дисперсионной среды. Твердый или полутвердый носитель также образует физический барьер против роста частиц. Плотно упакованная структура непористой твердой или полутвердой матрицы не оставляет кристаллам пространства для роста. Кроме того, растворимость лекарственного вещества в твердой или полутвердой матрице менее чувствительна к незначительным изменениям температуры по сравнению с растворимостью лекарственного препарата в жидком носителе, а потому полутвердая или твердая суспензия менее чувствительна к росту кристаллов за счет эффекта Оствальда.
В настоящем изобретении под «малорастворимым лекарственным веществом» подразумевается лекарственное вещество, обладающее плохой растворимостью в воде, то есть менее 10 мг/мл при физиологическом рН (2-7,5). Предпочтительно, растворимость в воде лекарственного вещества составляет менее 5 мг/мл, более предпочтительно, менее 1 мг/мл, и наиболее предпочтительно, менее 0,1 мг/мл. Лекарственное вещество суспендируется в дисперсионном носителе или матрице при температурах плавления. Поэтому малорастворимое лекарственное вещество, в соответствии с используемым здесь термином, также обладает плохой растворимостью в дисперсионном носителе при температурах плавления (то есть температурах, равных или выше точки плавления твердого или полутвердого дисперсионного носителя). Предпочтительно, растворимость лекарственного вещества в расплавленной дисперсионной матрице составляет менее 3 мг/г, более предпочтительно, менее 1 мг/г, и наиболее предпочтительно, менее 0,5 мг/г.
В предпочтительном варианте осуществления составы наночастиц согласно настоящему изобретению содержат наночастицы малорастворимого лекарственного вещества, обладающие средним размером частиц менее 1000 нм, предпочтительно, менее 750 нм, более предпочтительно, менее 600 нм и, в частности, менее 500 нм. В другом предпочтительном варианте осуществления составы наночастиц согласно настоящему изобретению содержат малорастворимое лекарственное вещество, в котором по крайней мере 90% и, более предпочтительно, по крайней мере 95% частиц лекарственного средства имеют размер частиц менее 1000 нм.
Количество малорастворимого лекарственного вещества в составе наночастиц согласно настоящему изобретению составляет от приблизительно 0,001% до приблизительно 30% по весу. В предпочтительном варианте осуществления количество малорастворимого лекарственного вещества составляет от приблизительно 1% до приблизительно 20% по весу.
Составы наночастиц согласно настоящему изобретению предпочтительно содержат терапевтически эффективное количество малорастворимого лекарственного вещества (веществ). Используемый в настоящем описании термин «терапевтически эффективное количество» относится к количеству лекарственного препарата, присутствующему во вводимом составе, которого достаточно для предотвращения развития или ослабления до некоторой степени одного или нескольких симптомов заболевания, для лечения которого он применяется. Аналогичным образом, терапевтически эффективным количеством фармацевтического состава наночастиц называется количество такого состава, которого достаточно для предотвращения развития или ослабления до некоторой степени одного или нескольких симптомов заболевания, для лечения которого он применяется. При определении эффективного количества или дозы лечащий медицинский работник рассматривает ряд факторов, в том числе среди прочих, вид млекопитающего, его размер, возраст и общее состояние здоровья; конкретное заболевание, степень поражения или тяжесть заболевания, ответная реакция отдельного пациента, конкретное вводимое соединение, способ введения, характеристики биодоступности вводимого препарата, избранная схема дозировки, использование сопутствующих лекарств и другие важные обстоятельства.
Подходящие лекарственные вещества могут выбираться из ряда известных классов лекарственных средств, в том числе, например, белков, пептидов, нутрицевтиков, противовоспалительных препаратов, НПВП, ингибиторов СОХ-2, аналгетиков, антимускариновых и мускариновых агентов, кортикостероидов, ингибиторов эластазы, средств лечения онкологических заболеваний, противорвотных средств, нейропротекторов, сердечно-сосудистых препаратов, антиагрегатных средств, средств, регулирующих обмен липидов, антикоагулянтов, антигельминтных препаратов, антиаритмических средств, кардиоинотропных препаратов, антигипертензивных препаратов, диуретиков, диагностических средств, диагностических контрастных средств, противовирусных препаратов, противогрибковых препаратов, антибиотиков, антимикобактериальных препаратов, противосудорожных средств, противодиабетических препаратов, противоэпилептических препаратов, антинеопластических препаратов, иммуноактивных препаратов, иммунодепрессантов, антитиреоидных препаратов, тиреоидных препаратов, антидепрессантов, анестетиков, анксиолитиков, гипнотических средств, нейролептиков, вяжущих средств, блокаторов бета-адренорецепторов, дофаминэргических препаратов, гемостатиков, иммунологических препаратов, миорелаксантов, парасимпатомиметиков, паратиреоидного кальцитонина, бифосфонатов, простагландинов, радиофармацевтических препаратов, стероидов, половых гормонов, стимуляторов и аноретиков, симпатомиметиков, антиаллергических препаратов, антигистаминов, противокашлевых препаратов, вазодиляторов и ксантинов. Подробное описание этих и других подходящих лекарственных препаратов можно найти, например, в Martindale, The Extra Pharmacopoeia, 31st Edition (The Pharmaceutical Press, London, 1996), раскрытие которых в силу ссылки на них полностью включено в настоящее описание. Лекарственные средства производятся промышленностью и/или могут быть получены по методикам, известным специалистам в данной области.
Примерами предпочтительных малорастворимых лекарственных средств для целей настоящего изобретения являются 7-хлор-N,N,5-триметил-4-оксо-3-фенил-3,5-дигидро-4H-пиридазино[4,5-b]индол-1-ацетамид, 6-фтор-9-метил-2-фенил-4-(пирролидин-1-илкарбонил)-2,9-дигидро-1H-пиридо[3,4-b]индол-1-он и фумарат изопропил-2-бутил-3-[4-[3-(дибутиламино)пропил]бензоил]-1-бензофуран-5-карбоксилата.
7-Хлор-N,N,5-триметил-4-оксо-3-фенил-3,5-дигидро-4H-пиридазино[4,5-b]индол-1-ацетамид (далее «соединение А») имеет следующую химическую структуру:
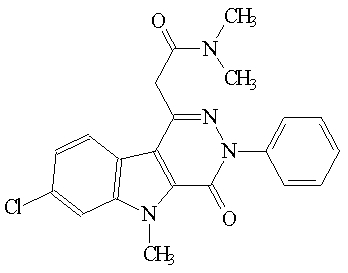
Соединение A
Соединение A используется, например, в качестве нейропротектора для лечения нейродегенеративных заболеваний или в качестве терапии в онкологии для лечения рака и может быть получено в соответствии с основными методами, описанными в патенте США № 6262045 и, в частности, в патенте США № 6395729, которые путем ссылки включены в настоящее описание.
6-Фтор-9-метил-2-фенил-4-(пирролидин-1-илкарбонил)-2,9-дигидро-1H-пиридо[3,4-b]индол-1-он (далее «соединение B») имеет следующую химическую структуру:
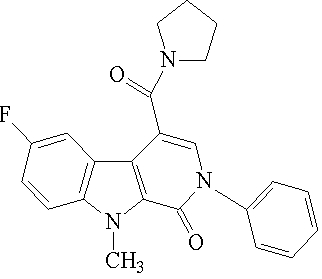
Соединение B
Соединение B может быть использовано в качестве, например, анксиолитика для лечения тревожных состояний или в качестве противосудорожного средства для лечения эпилепсии, мышечной спастичности или миогенной контрактуры; оно может быть получено в соответствии с основными методами, описанными в патенте США № 6075021, который путем ссылки включен в настоящее описание.
Фумарат изопропил-2-бутил-3-[4-[3-(дибутиламино)пропил]бензоил]-1-бензофуран-5-карбоксилата (далее «соединение C») имеет следующую химическую структуру:
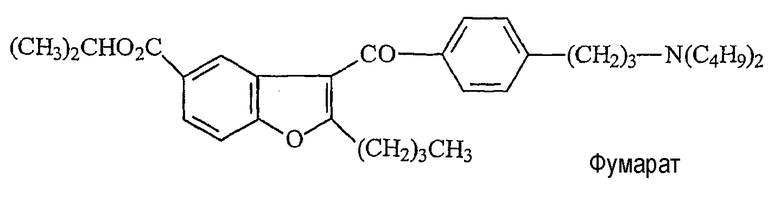
Соединение C
Соединение C используется, например, для лечения или профилактики аритмии или в качестве антиаритмического средства и может быть получено в соответствии с основными методами, описанными в заявке на патент США № 2003/0225100, опубликованной 4 декабря 2003 г., и WO 02/16339, опубликованной 28 февраля 2002 г., которые путем ссылки включены в настоящее описание.
В содержащих наночастицы составах согласно настоящему изобретению лекарственное вещество может присутствовать либо в кристаллической форме, либо в аморфной форме в зависимости от его структуры и концентрации.
Дисперсионный носитель согласно настоящему изобретению представляет собой вещество, не модифицирующее поверхность (то есть не адсорбирующиеся на поверхности частицы лекарства), пригодное для использования в фармацевтических составах, например для перорального и/или топического применения, твердое или полутвердое при комнатной температуре, но плавящееся при температурах выше комнатной. Предпочтительными являются дисперсионные носители, которые плавятся при температуре от приблизительно 30°C до приблизительно 110°C. Другие предпочтительные носители плавятся при температуре от приблизительно 30°C до приблизительно 80°C, а более предпочтительные носители плавятся при температуре от приблизительно 35°C до приблизительно 60°C. Дисперсионный носитель может представлять собой одно вещество с описанными выше свойствами или смесь веществ (такую как, например, растительное масло и воск), которая при смешивании становится твердой или полутвердой при комнатной температуре и плавится, предпочтительно, при температуре ниже 110°C, более предпочтительно - ниже 80°C, и наиболее предпочтительно - ниже 60°C.
Полутвердый дисперсионный носитель, используемый в настоящем изобретении, представляет собой вещество или смесь веществ, которые после смешивания имеют реологические свойства и жидкости, и твердого вещества одновременно. В неподвижном состоянии они имеют плотную консистенцию и не начинают течь, пока к ним не будет приложена сила (например, в результате перемешивания, разравнивания или экструзии), превышающая минимальное значение, называемое «пределом текучести», который является характеристикой полутвердого вещества. После превышения порога текучести полутвердые вещества по свойствам больше похожи на жидкость. Полутвердые вещества текут, в то время как твердые вещества деформируются при приложении напряжения сдвига, превышающего их предел прочности. Вязкость полутвердых веществ зависит от скорости сдвига. Предпочтительными являются полутвердые носители, разжижающиеся при сдвиге, то есть такие, вязкость которых уменьшается с увеличением сдвига. Вязкость также падает с температурой; вещество может быть твердым при комнатной температуре (деформироваться, когда напряжение сдвига превышает предел прочности) и полутвердым при повышенной температуре (течь, когда напряжение сдвига превышает предел текучести), либо полутвердым при комнатной температуре и жидким при повышенной температуре.
Полутвердый дисперсионный носитель по изобретению может дополнительно содержать ряд веществ, позволяющих добиться необходимой консистенции и текстурного профиля. В полутвердых мазеподобных веществах все вещества смешиваются друг с другом (однофазный носитель), как, например, в носителе из минерального масла и вазелина или смешиваемого воска, такого как парафин, который можно использовать, например, в лекарственных формах местного применения. К примерам предпочтительных пероральных полутвердых дисперсионных носителей относятся смеси растительного масла (например, соевого масла) или триглицеридов со средней длиной цепи с одним или несколькими из перечисленных далее веществ: гидрированное растительное масло с высокой температурой плавления (растительный стеарин), сложный эфир или эфиры жирной кислоты или кислот с длинной цепью, такой как эфир глицерина и бегеновой кислоты (имеющейся в продаже под названием Compritol®), и/или съедобный воск, например гидрированное касторовое масло или пчелиный воск.
Другими примерами предпочтительных дисперсионных носителей являются гидрированные растительные масла (такие как Wecobee® S производства компании Stepan Company, Нортфилд, Иллинойс, и HydrokoteTM 112 производства корпорации Abitec, Колумбус, Огайо); триглицериды, например гидрированные глицериды жирных кислот кокосового масла (такие как Softisan® 142 производства компании Sasol Inc.); смешанные глицериды; гидрированные глицериды; синтетические глицериды; эфиры глицерина и фракционированных жирных кислот; не обладающие поверхностной активностью сложные эфиры жирных кислот, например сложные эфиры пропиленгликоля и жирных кислот; жирные кислоты, такие как стеариновая кислота и пальмитиновая кислота; масло какао и заменители масла какао; твердый жир (такой как Softisan® 154 производства компании Sasol Inc.); натуральные и синтетические воски; вазелин.
Содержащие наночастицы составы согласно настоящему изобретению могут также включать дополнительные, не обладающие поверхностной активностью формообразующие вещества, обычно используемые в данной области. Такими формообразующими веществами могут быть один или несколько из следующих веществ: наполнители, заменители сахара, ароматизаторы, красители, консерванты, буферы и другие формообразующие вещества в зависимости от способа введения и дозировки используемой лекарственной формы.
Составы согласно настоящему изобретению обычно вводят пациентам, которыми могут быть, в частности, млекопитающие, например люди, традиционными для данной области способами. Например, эти составы могут вводиться пациентам перорально в виде, например, твердой или мягкой желатиновой капсулы, таблетки, таблетки в виде капсулы или в виде суспензии; ректально или вагинально, например, в форме таблетки, суппозитория или пессария, пасты, мази, примочки или суспензии; или локально, например, в форме пасты, мази, примочки или суспензии.
К предпочтительным осуществлениям настоящего изобретения относятся содержащие наночастицы составы, в которые входит малорастворимое лекарственное вещество и полутвердый дисперсионный носитель для местного применения, в форме мази или пасты.
Настоящее изобретения далее относится к применению содержащих наночастицы составов по изобретению в медицине.
В другом осуществлении изобретение относится к способу лечения пациента, например млекопитающего, такого как человек, с помощью содержащего наночастицы фармацевтического состава по настоящему изобретению, причем способ включает введение пациенту эффективного количества содержащего наночастицы состава по изобретению.
Предпочтительным способом по изобретению является способ лечения нейродегенеративного заболевания или рака, который включает введение пациенту терапевтически эффективного количества содержащего наночастицы состава согласно настоящему изобретению, в котором малорастворимым лекарственным веществом является 7-хлор-N,N,5-триметил-4-оксо-3-фенил-3,5-дигидро-4H-пиридазино[4,5-b]индол-1-ацетамид.
Другим предпочтительным способом по изобретению является способ лечения или профилактики тревожных состояний, эпилепсии, мышечной спастичности или миогенной контрактуры, который включает введение пациенту терапевтически эффективного количества содержащего наночастицы состава согласно настоящему изобретению, в котором малорастворимым лекарственным веществом является 6-фтор-9-метил-2-фенил-4-(пирролидин-1-илкарбонил)-2,9-дигидро-1H-пиридо[3,4-b]индол-1-он.
Еще одним предпочтительным способом по изобретению является способ лечения или профилактики аритмии, который включает введение пациенту терапевтически эффективного количества содержащего наночастицы состава согласно настоящему изобретению, в котором малорастворимым лекарственным веществом является фумарат изопропил-2-бутил-3-[4-[3-(дибутиламино)пропил]бензоил]-1-бензофуран-5-карбоксилата.
Объектом настоящего изобретения является применение содержащего наночастицы состава согласно настоящему изобретению, в котором малорастворимым лекарственным веществом является 7-хлор-N,N,5-триметил-4-оксо-3-фенил-3,5-дигидро-4H-пиридазино[4,5-b]индол-1-ацетамид, в получении медицинских препаратов для лечения нейродегенеративного заболевания или рака.
Еще одним объектом настоящего изобретения является применение содержащего наночастицы состава согласно настоящему изобретению, в котором малорастворимым лекарственным веществом является 6-фтор-9-метил-2-фенил-4-(пирролидин-1-илкарбонил)-2,9-дигидро-1H-пиридо[3,4-b]индол-1-он, в получении медицинских препаратов для лечения тревоги, эпилепсии, мышечной спастичности или миогенной контрактуры.
Еще одним объектом настоящего изобретения является применение содержащего наночастицы состава согласно настоящему изобретению, в котором малорастворимым лекарственным веществом является фумарат изопропил-2-бутил-3-[4-[3-(дибутиламино)пропил]бензоил]-1-бензофуран-5-карбоксилата, в получении медицинских препаратов для лечения аритмии.
В другом варианте осуществления настоящее изобретение относится к лекарственным формам, включающим описанный здесь содержащий наночастицы состав. К лекарственным формам относятся, среди прочих, пилюли, капсулы, таблетки в форме капсулы, таблетки, гранулы, суспензии, мази, примочки, суппозитории и пасты.
Для специалистов в данной области будет очевидным, что составы согласно настоящему изобретению могут вводиться с другими терапевтическими или профилактическими веществами и/или лекарственными средствами, которые не являются несовместимыми с ними, с медицинской точки зрения.
Все компоненты составов по изобретению должны быть фармацевтически приемлемыми. В настоящем описании «фармацевтически приемлемым» компонентом считается компонент, пригодный для использования в лечении человека и/или других животных без нежелательных побочных эффектов (таких как токсичность, раздражение или аллергическая реакция) с соразмерным соотношением пользы и риска.
Настоящее изобретение далее относится к способу получения содержащих наночастицы составов согласно настоящему изобретению, который включает в себя смешивание малорастворимого лекарственного вещества с расплавленным дисперсионным носителем, который является твердым или полутвердым веществом при комнатной температуре, и измельчение полученной смеси в бисерной мельнице для получения состава, содержащего наночастицы.
Предпочтительный способ получения содержащих наночастицы составов согласно настоящему изобретению включает стадии нагревания твердого или полутвердого дисперсионного носителя до температуры его плавления или выше для получения расплавленной формы дисперсионного носителя; смешивания одного или нескольких малорастворимых лекарственных веществ с расплавленным дисперсионным носителем с получением смеси; измельчения смеси с большим количеством мелющих тел с образованием наносуспензии; и охлаждения наносуспензии до температуры ниже температуры плавления дисперсионного носителя.
В одном из наиболее предпочтительных способов получения содержащих наночастицы составов в форме суспензий согласно настоящему изобретению стадию измельчения выполняют при температурах, лишь слегка превышающих температуру плавления дисперсионного носителя. Предпочтительно способ осуществляют при температуре, менее чем на 10°C превышающей температуру плавления дисперсионного носителя, а еще более предпочтительно - при температуре, менее чем на 5°C превышающей температуру плавления дисперсионного носителя.
Еще один аспект настоящего изобретения включает стадию наполнения измельченной наносуспензией капсул перед ее охлаждением до температуры ниже температуры плавления дисперсионного носителя. В еще одном аспекте настоящего изобретения измельченные наносуспензии перед охлаждением гранулируют непосредственно в один или несколько не модифицирующих поверхность фармацевтически приемлемых твердых наполнителей, обычно применяемых в данной области, таких как, например, лактоза, маннитол и кукурузный крахмал, с образованием твердого гранулированного состава без стадии сушки.
Измельчение в бисерных мельницах - процесс получения содержащих наночастицы суспензий, хорошо известный специалистам в данной области. Этот процесс предпочтительно проводят в мельнице, такой как цилиндрический сосуд, имеющий камеру измельчения, в которой находится большое количество мелющих тел, подлежащее измельчению лекарственное вещество и дисперсионный носитель, в котором во взвешенном состоянии присутствуют мелющие тела и лекарственное вещество. В камере измельчения могут также находиться дополнительные формообразующие вещества, не модифицирующие поверхность. Температура камеры поддерживается чуть выше температуры плавления дисперсионного носителя. Содержимое камеры измельчения перемешивают или активируют мешалкой, передающей энергию мелющим телам. Получившие ускорение мелющие тела с силой сталкиваются с лекарственным веществом, посредством чего крошат, расщепляют, дробят или каким-то иным образом уменьшают размер его частиц, что приводит к общему снижению размера частиц и общему уменьшению среднего распределения размера частиц лекарственного вещества. Установленное на выходе сито или сепаратор задерживает мелющие тела.
В одном предпочтительном способе по изобретению мелющие тела, дисперсионный носитель и измельчаемое лекарственное вещество остаются в сосуде, пока размер частиц измельчаемого лекарственного вещества не уменьшится до желаемого или до минимально достижимого. Затем наносуспензии (то есть частицы лекарственного вещества, взвешенные в дисперсионном наполнителе) отделяют от мелющих тел сепаратором или ситом, установленным на выходе камеры измельчения.
В другом предпочтительном способе по изобретению измельчение выполняют в режиме рециркуляции (постоянный режим). Мельница, работающая в режиме рециркуляции, имеет в своем составе сепаратор или сито для удерживания мелющих тел и относительно крупных частиц измельчаемого лекарственного вещества в камере измельчения, сквозь которое могут выходить из камеры более мелкие частицы лекарственного вещества. В режиме рециркуляции суспензия часто движется из камеры измельчения в приемный контейнер и обратно, нередко при помощи насоса. Сепаратор или сито может располагаться на выходе из камеры измельчения.
В третьем предпочтительном способе по изобретению измельчение выполняют в режиме дискретных проходов (дискретный режим). В дискретном режиме смесь лекарственного вещества и дисперсионного наполнителя прокачивается через камеру измельчения, а затем в отдельный приемный контейнер, что составляет один проход. Этот процесс может повторяться до получения требуемого размера частиц.
Мелющие тела, как правило, представляют собой сферический или цилиндрический бисер, которым могут быть многие плотные и твердые материалы, такие как, например, песок, сталь, карбид кремния, керамика, силикат циркония, оксид циркония и иттрия, стекло, окись алюминия, титан, а также определенные полимеры, такие как сшитый полистирол и метилметакрилат. Возможное загрязнение металлическими мелющими телами, такими как цирконий, можно уменьшить посредством предварительной обработки мелющих тел в пустом дисперсионном носителе, при которой начальный износ происходит до добавления в мельницу лекарственного вещества.
Используемый в настоящем описании термин «стабильный» в отношении содержащих наночастицы составов означает состав, в котором частицы лекарства не флокулируют или не агломерируют в значительной степени под действием сил притяжения между частицами или каким-либо иным образом значительно не увеличиваются в размере со временем; а частицы этого состава химически стабильны; и/или физическая структура его частиц не изменяется со временем, например, переходя из аморфной фазы в кристаллическую.
Приведенные далее примеры дополнительно иллюстрируют изобретение, тем не менее, не ограничивая его охват.
ПРИМЕР 1
Соединение A в гидрированном растительном масле
Растворимость соединения A в предлагаемом дисперсионном носителе, Wecobee® S (триглицерид, полученный из растительных масел, температура плавления ~44°C), изначально определяли следующим образом: 5 г гидрированного растительного масла взвешивали, помещали в сцинтилляционный флакон и нагревали до 50°C. Добавляли 5 г соединения A и перемешивали в водяной бане магнитной мешалкой. Лекарственное вещество не растворялось, поэтому постепенно добавляли дополнительное количество гидрированного растительного масла, пока полное количество гидрированного растительного масла не составило 10 г. Смесь оставляли перемешиваться на ночь на водяной бане при 60°C. При этой же температуре смесь отфильтровали (фильтровальную установку нагревали в печи до 60°C), и измеряли растворимость фильтрата для соединения A в гидрированном растительном масле при 60°C, которая оказалась равной 0,48 мг/г.
Для получения суспензии использовали следующий метод: 250 мл 1,0-мм стабилизированных иттрием циркониевых элементов загружали в DynoMill (камера измельчения типа KDL емкостью 0,3 л из нержавеющей стали производства компании Glen Mills). Сначала температура циркуляционной водяной бани (от которой зависит температура в области уплотнения) и температура воды в трубопроводе (от которой зависит температура камеры измельчения) были установлены равными 50°C, чтобы нагреть камеры и бисер. Для начального промывания и предварительной обработки бисера прокачивали соевое масло со скоростью 40 мл/мин при перемешивании со скоростью 3200 об/мин. Через несколько минут температуру циркуляционной водяной бани снижали до 40°C, чтобы температура оставалась ниже 60°C. Температуру воды в трубопроводе также устанавливали равной 45°C. После соевого масла прокачивалось расплавленное гидрированное растительное масло (Wecobee® S) для дополнительной обработки и вымывания жидкого масла. Суммарное время обработки и промывания (соевым маслом и Wecobee® S) составило около одного часа.
Суспензию лекарственного вещества получали диспергированием 150 г соединения A в 700 г расплавленного Wecobee® S при 50°C с помощью расположенного сверху смесителя (марки Lightnin®) на плитке. После слива промывочного носителя из измельчающего оборудования суспензию лекарственного вещества циркулировали со скоростью 400 мл/мин при перемешивании с помощью DynoMillTM со скоростью 3200 об/мин. Суспензию продолжали перемешивать мешалкой, чтобы не допустить осаждения, но не нагревали во время измельчения. Температуру циркуляционной водяной бани и температуру циркулирующей воды в трубопроводе понизили еще больше, чтобы температура упала до примерно 55°C и сохранялась на этом уровне, и чтобы температура продукта сохранялась в пределах от 45°C до 50°C. Такие температуры поддерживались на протяжении всего времени измельчения. Измельчение суспензии продолжалось в сумме 5 часов. По окончании измельчения суспензию переносили в контейнер для хранения и позволяли ей остыть до комнатной температуры.
ПРИМЕР 2
Соединение B в твердом жире
Растворимость соединения B в соевом масле изначально оценивали визуально при постепенном добавлении соевого масла в отвешенное количество лекарственного соединения, пока масло не стало почти прозрачным (визуально). Количество лекарственного вещества в масле оценивали по количеству добавленного масла. Растворимость соединения B в соевом масле была ниже 1 мг/мл, и поэтому был сделан вывод о том, что низкая растворимость соединения B в соевом масле должна означать низкую растворимость и в твердом жире.
Эту суспензию получали при помощи вертикальной мельницы с твердым жиром (Softisan® 154, гидрированное пальмовое масло с диапазоном температур плавления 53-58°C). Твердый жир плавили нагреванием на плитке. 1,0-мм стабилизированный иттрием циркониевый бисер (20 мл) предварительно нагревали в 50-мл пластмассовой пробирке до 50°C. Добавляли 2 г соединения B, а затем 10 мл расплавленного твердого жира. Вокруг верхней части пробирки был обернут ленточный нагревательный элемент, чтобы ее содержимое поддерживалось в расплавленном состоянии. Состав перемешивали со скоростью 2000 об/мин в течение 3 часов при помощи вертикальной мельницы. Из-за относительно высокой температуры плавления твердого жира было необходимо продолжать нагревание при помощи ленточного нагревательного элемента до завершения измельчения. Попытки остановить нагревание приводили к отверждению жира в верхней части пробирки. По завершении измельчения расплавленную суспензию фильтровали, чтобы удалить мелющий бисер.
ПРИМЕР 3
Соединение C в гидрированных глицеридах жирных кислот кокосового масла
Носитель (гидрированные жирные кислоты кокосового масла, имеющиеся в продаже под названием Softisan® 142, с диапазоном температур плавления порядка 42-44°C) нагревали до 50°C на плитке. 2,5 г соединения C, которое обычно плохо растворяется в маслах, взвешивали и помещали в 50-мл центрифужную пробирку и нагревали ее в конвекционной печи до 50°C. В другой пробирке до той же температуры нагревали 20 мл 1-мм циркониевых элементов очень высокой плотности. Элементы добавляли в лекарственное вещество, а затем добавляли 10 мл Softisan® 142. Верхнюю часть пробирки оборачивали ленточным нагревательным элементом, при этом термостат поддерживал низкую температуру. В пробирку вставляли крыльчатку вертикальной мельницы, и состав перемешивали со скоростью 2000 об/мин в течение 3 часов. Добавляли еще 10 мл расплавленного Softisan® 142 и перемешивали стеклянным штабиком. Затем расплавленную суспензию пропускали через сито при 55°C, чтобы удалить мелющий бисер при помощи предварительно нагретой фильтровальной установки.
ПРИМЕР 4
Анализ размеров частиц в примерах 1-3
Анализ размеров частиц в примерах 1-3 проводили с помощью лазерного дифракционного измерителя частиц Horiba LA-920. Сначала порцию весом 200 мг нагревали в водяной бане при 50°C, добавляли 25 мл соевого масла, содержащего дисперсант Aerosol® OT-100 (диоктилсульфосукцинат натрия производства Cytec Industries Inc.), а затем образец перемешивали. Образец переносили в прибор, перемешивали, обрабатывали ультразвуком и анализировали. Результаты измерений размеров частиц в примерах 1-3 представлены ниже в таблицах 1A, 1B и 1C.
Приведенные выше результаты показывают, что способ по настоящему изобретению можно использовать для получения составов, содержащих наночастицы, в которых средний размер частиц лекарственного вещества составляет менее 1000 нм.
ПРИМЕР 5
Физическая стабильность в примере 1
Для определения физической стабильности содержащей наночастицы суспензии, полученной согласно описанию в примере 1, суспензию подвергали механическому напряжению в течение трех месяцев при 40°C и относительной влажности 75%. В конце каждого из трех месяцев анализировали стабильность размеров частиц в образце.
В таблице 2 перечислены параметры размера частиц подвергавшихся напряжению образцов по сравнению с параметрами в начальный момент времени.
ПРИМЕР 6
Физическая стабильность в примере 2
Для определения физической стабильности состава, полученного согласно описанию в примере 2, суспензию подвергали поочередному нагреванию и охлаждению; образец хранили при 50°C в течение одной недели, при 5°C в течение второй недели и при 50°C в течение третьей недели. В конце трехнедельного периода анализировали стабильность размеров частиц в образце.
В таблице 3 показано распределение частиц по размерам в суспензии в примере 2 в начальный момент времени и в конце трехнедельного периода поочередного нагревания и охлаждения.
ПРИМЕР 7
Физическая стабильность в примере 3
Для определения физической стабильности в содержащем наночастицы составе, полученном согласно описанию в примере 3, состав испытывали в течение двух недель при 50°C. В таблице 4 показано распределение частиц по размерам в составе из примера 3 в начальный момент времени и в конце двухнедельного периода испытаний.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛИОФИЛИЗИРОВАННЫЕ ЛЕКАРСТВЕННЫЕ НАНОСУСПЕНЗИИ | 2012 |
|
RU2643062C2 |
| НАНОСУСПЕНЗИЯ, СОДЕРЖАЩАЯ ЧАСТИЦЫ И ЭКСТРАКТ ПРИРОДНЫХ МАТЕРИАЛОВ | 2016 |
|
RU2710952C2 |
| НАНОСУСПЕНЗИИ ПРИРОДНЫХ МАТЕРИАЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2015 |
|
RU2695325C1 |
| СТЕРИЛИЗАЦИЯ ПОД ВЫСОКИМ ДАВЛЕНИЕМ ДЛЯ ЗАКЛЮЧИТЕЛЬНОЙ СТЕРИЛИЗАЦИИ ФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ И МЕДИЦИНСКИХ ИЗДЕЛИЙ | 2004 |
|
RU2392004C2 |
| ПРОТИВООПУХОЛЕВЫЕ НАНОЧАСТИЦЫ С МОДИФИЦИРОВАННОЙ ПОВЕРХНОСТЬЮ И СОДЕРЖАЩАЯ ИХ КОМПОЗИЦИЯ | 1993 |
|
RU2130781C1 |
| ИНЪЕЦИРУЕМЫЕ ПРЕПАРАТИВНЫЕ ФОРМЫ ДЕПО И СПОСОБЫ ОБЕСПЕЧЕНИЯ ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ КОМПОЗИЦИЙ, СОСТОЯЩИХ ИЗ НАНОЧАСТИЦ | 2006 |
|
RU2407529C2 |
| АЭРОЗОЛЬНЫЕ ФТОРХИНОЛОНЫ И ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2603638C2 |
| ТОПИЧЕСКИЙ СОСТАВ, СОДЕРЖАЩИЙ НАНОЧАСТИЦЫ СПИРОНОЛАКТОНА | 2002 |
|
RU2331424C2 |
| ЛЕЧЕНИЕ И ПРЕДУПРЕЖДЕНИЕ ВИЧ-ИНФЕКЦИИ | 2010 |
|
RU2569058C2 |
| ВОДНАЯ СУСПЕНЗИЯ, СОДЕРЖАЩАЯ НАНОЧАСТИЦЫ ГЛЮКОКОРТИКОСТЕРОИДА | 2016 |
|
RU2747803C2 |
Изобретение относится к стабильным фармацевтическим составам наночастиц. Составы содержат малорастворимое лекарственное вещество со средним размером частиц менее 1000 нм, твердый или полутвердый дисперсионный носитель и, при необходимости, не модифицирующий поверхность эксципиент. Указанный состав не содержит модификатора поверхности или стабилизатора. Также описан способ получения составов и их применение. Составы согласно настоящему изобретению характеризуются стабильностью в отсутствие модификатора или стабилизатора поверхности, адсорбированного на поверхности частиц лекарства. 8 н. и 21 з.п. ф-лы, 4 табл.
1. Стабильный фармацевтический состав наночастиц, включающий малорастворимое лекарственное вещество со средним размером частиц менее 1000 нм, твердый или полутвердый дисперсионный носитель и, при желании, не модифицирующий поверхность эксципиент, причем указанный состав не содержит модификатор поверхности или стабилизатор.
2. Состав по п.1, где указанное малорастворимое лекарственное соединение имеет средний размер частиц менее 750 нм.
3. Состав по п.1, где указанное малорастворимое лекарственное соединение имеет средний размер частиц менее 600 нм.
4. Состав по п.1, где по меньшей мере 95% малорастворимого лекарственного соединения имеет размер частиц менее 1000 нм.
5. Состав по п.1, где количество малорастворимого лекарственного соединения в составе составляет от приблизительно 0,01 до приблизительно 30% по весу.
6. Состав по п.5, где количество малорастворимого лекарственного соединения в составе составляет от приблизительно 1 до приблизительно 20% по весу.
7. Состав по п.1, где не модифицирующий поверхность эксципиент представляет собой не модифицирующий поверхность фармацевтически приемлемый твердый наполнитель.
8. Состав по п.1, где указанное малорастворимое лекарственное вещество представляет собой одно или несколько веществ, выбранных из группы, состоящей из белка, пептида, нутрицевтика, противовоспалительного средства, нестероидного противовоспалительного средства, НСПВП, ингибитора СОХ-2, анальгетика, антимускаринового вещества, мускаринового вещества, кортикостероида, ингибитора эластазы, онкологического лекарственного средства, противорвотного средства, нейропротективного средства, лекарственного средства для сердечно-сосудистой системы, противотромбоцитного средства, средства для регуляции липидов, антикоагулянта, антигельминтного вещества, средства против аритмии, инотропного средства для сердца, гипотензивного средства, мочегонного средства, диагностического средства, средства для диагностической визуализации, противовирусного средства, фунгицидного средства, антибиотика, противомикобактериального средства, противосудорожного средства, антидиабетического средства, противоэпилептического средства, антибластомного средства, иммуноактивного средства, иммунодепрессивного средства, антитиреоидного средства, тиреоидного средства, антидепрессанта, обезболивающего средства, анксиолитика, снотворного, нейролептика, вяжущего средства, средства блокировки бета-адренорецептора, допаминергического средства, кровоостанавливающего средства, иммунориологического средства, мышечного релаксанта, парасимпатомиметического средства, кальцитонина для паращитовидной железы, дифосфоната, простагландина, препарата для лучевой терапии, полового гормона, стероида, стимулятора, анорексигенного средства, симпатомиметика, противоаллергического средства, антигистамина, средства от кашля, сосудорасширяющего средства и ксантина.
9. Состав по п.8, где указанным малорастворимым лекарственным веществом является одно или несколько веществ, выбираемых из группы, состоящей из нейропротектора, средства против аритмии, противосудорожного средства и анксиолитического средства.
10. Состав по п.1, где указанное малорастворимое лекарственное вещество выбрано из группы, состоящей из 7-хлор-N,N,5-триметил-4-оксо-3-фенил-3,5-дигидро-4Н-пиридазино[4,5-b]индол-1-ацетамида, 6-фтор-9-метил-2-фенил-4-(пирролидин-1-илкарбонил)-2,9-дигидро-1Н-пиридо[3,4-b]индол-1-она и фумарата изопропил-2-бутил-3-[4-[3-(дибутиламино)пропил]бензоил]-1-бензофуран-5-карбоксилата.
11. Состав по п.10, где указанным малорастворимым лекарственным веществом является 7-хлор-N,N,5-триметил-4-оксо-3-фенил-3,5-дигидро-4Н-пиридазино[4,5-b]индол-1-ацетамид.
12. Состав по п.10, где указанным малорастворимым лекарственным веществом является 6-фтор-9-метил-2-фенил-4-(пирролидин-1-илкарбонил)-2,9-дигидро-1Н-пиридо [3,4-b]индол-1-он.
13. Состав по п.10, где указанным малорастворимым лекарственным веществом является фумарат изопропил-2-бутил-3-[4-[3-(дибутиламино)пропил]бензоил]-1-бензофуран-5-карбоксилата.
14. Состав по п.1, где указанный дисперсионный носитель представляет собой одно или несколько веществ, выбранных из группы, состоящей из гидрированных растительных масел, триглицеридов, гидрированных глицеридов жирных кислот кокосового масла, смешанных глицеридов, гидрированных глицеридов, синтетических глицеридов, сложных эфиров глицерина и фракционированных жирных кислот, не обладающих поверхностной активностью сложных эфиров жирных кислот, жирных кислот, масла какао, заменителей масла какао, твердого жира, натуральных и синтетических восков и вазелина.
15. Состав по п.10, где указанный дисперсионный носитель представляет собой одно или несколько веществ, выбранных из группы, состоящей из гидрированных растительных масел, триглицеридов, гидрированных глицеридов жирных кислот кокосового масла, смешанных глицеридов, гидрированных глицеридов, синтетических глицеридов, сложных эфиров глицерина и фракционированных жирных кислот, сложных диэфиров пропиленгликоля и жирных кислот, других не обладающих поверхностной активностью сложных эфиров жирных кислот, жирных кислот, масла какао, заменителей масла какао, твердого жира, натуральных и синтетических восков и вазелина.
16. Состав по п.15, где указанный дисперсионный носитель представляет собой одно или несколько веществ, выбранных из группы, состоящей из гидрированных растительных масел, твердых жиров и гидрированных глицеридов жирных кислот кокосового масла.
17. Состав по п.11, где указанный дисперсионный носитель представляет собой одно или несколько гидрированных растительных масел.
18. Состав по п.12, где указанный дисперсионный носитель представляет собой один или несколько твердых жиров.
19. Состав по п.13, где указанный дисперсионный носитель представляет собой один или несколько гидрированных глицеридов жирных кислот кокосового масла.
20. Состав по п.1, где указанный твердый или полутвердый дисперсионный носитель представляет собой смесь двух или более веществ.
21. Способ лечения нейродегенеративного заболевания или рака, включающий введение пациенту терапевтически эффективного количества содержащего наночастицы фармацевтического состава по п.11.
22. Способ лечения или профилактики тревожных состояний, эпилепсии, мышечной спастичности или миогенной контрактуры, включающий введение пациенту терапевтически эффективного количества содержащего наночастицы фармацевтического состава по п.12.
23. Способ лечения или профилактики аритмии, включающий введение пациенту терапевтически эффективного количества содержащего наночастицы фармацевтического состава по п.13.
24. Применение содержащего наночастицы фармацевтического состава по п.11 в получении лекарственного средства для лечения нейродегенеративного заболевания или рака.
25. Применение содержащего наночастицы фармацевтического состава по п.12 в получении лекарственного средства для лечения тревоги, эпилепсии, мышечной спастичности или миогенной контрактуры.
26. Применение содержащего наночастицы фармацевтического состава по п.13 в получении лекарственного средства для лечения аритмии.
27. Способ получения содержащего наночастицы фармацевтического состава по п.1, включающий стадии:
(a) смешивания одного или нескольких малорастворимых лекарственных веществ с расплавленным дисперсионным носителем, при комнатной температуре представляющим собой твердое или полутвердое вещество; и
(b) измельчение полученной смеси в бисерной мельнице с целью получения содержащего наночастицы состава.
28. Способ по п.27, включающий стадии:
(a) нагревания твердого или полутвердого дисперсионного носителя до первого температурного диапазона, соответствующего температуре плавления указанного твердого или полутвердого дисперсионного носителя или превышающего ее, с целью образования расплавленного дисперсионного носителя;
(b) смешивания одного или нескольких малорастворимых лекарственных веществ с расплавленным дисперсионным носителем с образованием смеси;
(c) измельчения смеси с большим количеством мелющих тел с образованием наносуспензии и
(d) охлаждения наносуспензии до второго температурного диапазона ниже температуры плавления твердого или полутвердого дисперсионного носителя с образованием содержащего наночастицы состава.
29. Способ по п.27, включающий стадии:
(a) нагревания твердого или полутвердого дисперсионного носителя до первого температурного диапазона, соответствующего температуре плавления указанного твердого или полутвердого дисперсионного носителя или превышающего ее, с целью образования расплавленного дисперсионного носителя;
(b) смешивания одного или нескольких малорастворимых лекарственных веществ с расплавленным дисперсионным носителем с образованием смеси;
(c) измельчения смеси с большим количеством мелющих тел с образованием наносуспензии;
(d) наполнения наносуспензией капсул и
(e) охлаждения капсул до второго температурного диапазона ниже температуры плавления твердого или полутвердого дисперсионного носителя с образованием содержащего наночастицы состава.
30. Способ по п.27, включающий стадии:
(a) нагревания твердого или полутвердого дисперсионного носителя до первого температурного диапазона, соответствующего температуре плавления указанного твердого или полутвердого дисперсионного носителя или превышающего ее, с целью образования расплавленного дисперсионного носителя;
(b) смешивания одного или нескольких малорастворимых лекарственных веществ с расплавленным дисперсионным носителем с образованием смеси;
(c) измельчения смеси с большим количеством мелющих тел с образованием наносуспензии и
(d) гранулирования наносуспензий на не модифицирующий поверхность твердый наполнитель с образованием твердого состава.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| US 5560931 A, 01.10.1996 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2011-01-20—Публикация
2006-05-03—Подача