ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Метформин и его фармацевтически приемлемые соли (например, гидрохлорид метформина, N,N-диметилимидодикарбоимиддиамид гидрохлорид) давно используют для лечения ряда состояний, включая диабет, преддиабет, поликистоз яичников и ожирение. Механизм действия метформина включает снижение уровней глюкозы в плазме (в частности, уровней глюкозы после приема пищи), снижение выработки глюкозы печенью, снижение уровней липидов, повышение чувствительности к инсулину и/или снижение кишечной абсорбции. Более того, метформин оказывает действие, не вызывая гликемии.
В настоящее время применяются пероральные препараты (таблетки) метформина (например, GLUCOPHAGE, Bristol Meyers Squibb Co.). Введение пероральных препаратов метформина может вызвать ряд побочных эффектов. Неблагоприятные события, связанные с пероральными препаратами метформина, часто имеют желудочно-кишечный характер (например, анорексия, тошнота, вздутие живота, рвота, иногда диарея и так далее). Более того, пероральные препараты метформина могут оставлять горький привкус, что может привести к потере аппетита. Эти побочные эффекты часто приводят к отказу пациента принимать лекарство, то есть "проблемам комплаентности" ("compliance issues"). Проблемы комплаентности встречаются среди пациентов всех возрастов, включая детей, которые обычно не хотят принимать лекарства с неприятным вкусом.
Поэтому существует необходимость в препаратах метформина, которые по меньшей мере смягчат одну или несколько из этих проблем, чтобы способствовать согласию пациента принимать лекарство.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Согласно первому аспекту изобретения предложена пероральная трансмукозальная композиция метформина, содержащая фармацевтически приемлемый носитель и эффективное количество фармацевтического агента, состоящего из метформина или его фармацевтически приемлемой соли, находящегося в указанном носителе, причем указанный носитель способен доставить фармацевтически эффективное количество указанного фармацевтического агента к слизистой оболочке рта для абсорбции.
Согласно второму аспекту предложен способ приготовления пероральной трансмукозальной композиции метформина, включающий смешивание эффективного количества фармацевтического агента, состоящего из метформина или его фармацевтически приемлемой соли, с эффективным количеством по меньшей мере одного усилителя абсорбции, выбранного из алкилсульфата щелочного металла, глицерина, желчной кислоты или соли желчной кислоты, лецитина, гиалуроновой кислоты, октилфеноксиполиэтоксиэтанола, гликолевой кислоты, молочной кислоты, экстракта ромашки, экстракта огурца, олеиновой кислоты, линоленовой кислоты, масла бурачника, масла энотеры, полиглицерина, лизина, полилизина, триолеина, моноолеина, моноолеатов, монолауратов, ментола, полидоканол-алкиловых эфиров, хенодезоксихолата, дезоксихолата и их фармацевтически приемлемых солей и аналогов, с образованием препарата. Препарат объединяют с подходящим фармацевтически приемлемым носителем для получения настоящей композиции.
Согласно еще одному аспекту изобретения предложен способ применения и применение композиции для лечения различных состояний, выбранных из диабета, преддиабета, ожирения и синдрома поликистоза яичников. Настоящая композиция может быть полезной для снижения уровней глюкозы в плазме, снижения выработки глюкозы печенью, снижения уровней липидов, повышения чувствительности к инсулину, снижения кишечной абсорбции глюкозы, снижения гипогликемии и снижения аппетита. Способ включает введение субъекту композиции по первому аспекту с целью лечения таких состояний. В изобретении также предложено применение композиции в изготовлении лекарственного средства для лечения тех же состояний. Композицию можно удерживать во рту в течение по меньшей мере 1, 20 или 30 минут. Также композицию можно удерживать во рту от 1 до 30, от 1 до 20 или от 1 до 9 минут.
Согласно еще одному аспекту изобретения предложен препарат для применения в приготовлении композиции согласно первому аспекту. Этот препарат содержит фармацевтический агент, состоящий из метформина или его фармацевтически приемлемой соли, и эффективное количество по меньшей мере одного усилителя абсорбции, выбранного из алкилсульфата щелочного металла, глицерина, желчной кислоты или соли желчной кислоты, лецитина, гиалуроновой кислоты, октилфеноксиполиэтоксиэтанола, гликолевой кислоты, молочной кислоты, экстракта ромашки, экстракта огурца, олеиновой кислоты, линоленовой кислоты, масла бурачника, масла энотеры, полиглицерина, лизина, полилизина, триолеина, моноолеина, моноолеатов, монолауратов, ментола, полидоканол-алкиловых эфиров, хенодезоксихолата, дезоксихолата и их фармацевтически приемлемых солей и аналогов, где фармацевтический агент присутствует в концентрации приблизительно от 5 до 90, от 10 до 80, от 20 до 80 или от 20 до 50 мас./мас.%, и общая концентрация усилителей абсорбции составляет меньше чем приблизительно 30, 20, 10, 7, 5, 2, 1, 0,5 или 0,01 мас./мас.%, все от общей массы препарата.
Настоящее изобретение обладает рядом преимуществ. За счет обхода желудочно-кишечного тракта (ЖК) можно избежать возникновения желудочно-кишечных осложнений и побочных эффектов пероральных препаратов метформина и его солей. В известных препаратах для проглатывания требуется большее количество фармацевтического агента на дозу из-за проблем распада в ЖК тракте. Настоящие композиции, которые доставляют фармацевтический агент через слизистые оболочки рта, могут быть приготовлены в виде препарата с меньшим количеством активного ингредиента. Это приводит к снижению себестоимости и помогает улучшить вкусовой профиль.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Упомянутые выше и другие объекты, признаки и преимущества настоящего изобретения будут понятны из следующего, более конкретного описания предпочтительных воплощений изобретения и сопроводительных графических материалов.
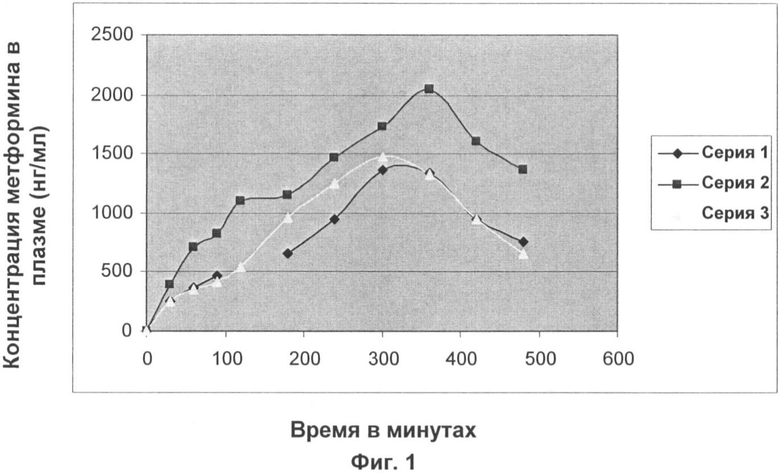
Фиг.1 представляет собой график зависимости концентрации метформина в плазме (нг/мл) от времени. Серия 1 отражает концентрацию метформина в плазме у субъекта, проглотившего таблетку, содержащую 850 мг гидрохлорида метформина. Серии 2 и 3 представляют концентрации метформина в плазме у двух субъектов, которые жевали три подушечки (chiclets) жевательной резинки, каждая из которых содержала 212,5 мг метформина.
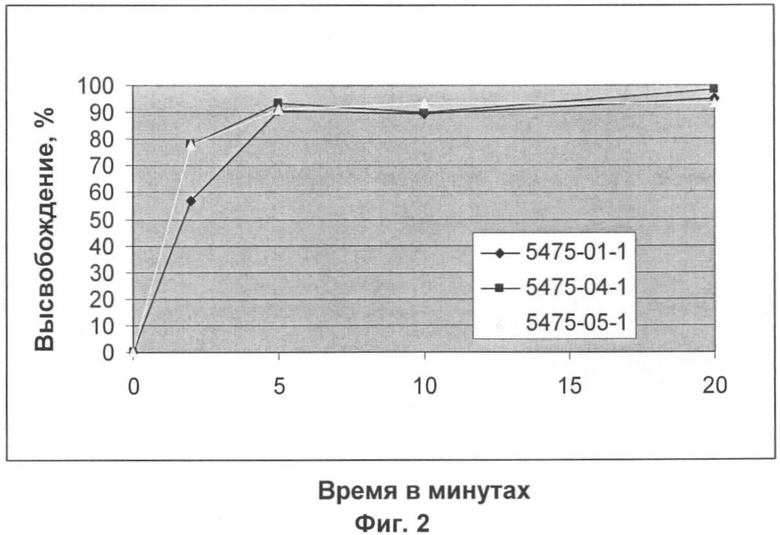
Фиг.2 представляет собой график, изображающий количество метформина, высвободившегося из композиций жевательных резинок согласно настоящему изобретению, в зависимости от времени.
Фиг.3 представляет собой график, сравнивающий концентрации метформина в плазме (млн-1) в зависимости от времени у субъектов, проглотивших таблетку, содержащую 429 мг метформина, и у субъектов, которые жевали жевательную резинку, содержащую 429 мг метформина.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Далее следует описание предпочтительных воплощений изобретения.
Фармацевтические композиции
В одном воплощении изобретение представляет собой пероральную трансмукозальную композицию метформина, содержащую:
эффективное количество фармацевтического агента, состоящего из метформина или его фармацевтически приемлемой соли,
эффективное количество по меньшей мере одного усилителя абсорбции, выбранного из алкилсульфата щелочного металла, глицерина, желчной кислоты или соли желчной кислоты, лецитина, гиалуроновой кислоты, октилфеноксиполиэтоксиэтанола, гликолевой кислоты, молочной кислоты, экстракта ромашки, экстракта огурца, олеиновой кислоты, линоленовой кислоты, масла бурачника, масла энотеры, полиглицерина, лизина, полилизина, триолеина, моноолеина, моноолеатов, монолауратов, ментола, полидоканол-алкиловых эфиров, хенодезоксихолата, дезоксихолата и их фармацевтически приемлемых солей и аналогов, и
фармацевтически приемлемый носитель, способный доставить фармацевтически эффективное количество указанного фармацевтического агента к слизистой оболочке рта для абсорбции.
Фармацевтически приемлемой солью метформина может быть гидрохлорид метформина.
В одном из воплощений фармацевтическая композиция находится в форме жевательной резинки, содержащей гидрохлорид метформина в концентрации приблизительно от 10 до 50 мас./мас.%, лаурилсульфат натрия в концентрации приблизительно от 0,01 до 2 или от 0,01 до 0,5 мас./мас.%, гликохолат натрия в концентрации приблизительно от 0,01 до 2 или от 0,01 до 0,5 мас./мас.%, глицерин в концентрации приблизительно от 2 до 10 или от 2 до 7 мас./мас.% и основу жевательной резинки в концентрации приблизительно от 10 до 90, от 30 до 75 или от 60 до 75 мас./мас.%, все от общей массы композиции. В другом воплощении композиция находится в форме твердого леденца или лепешки.
В другом воплощении изобретение представляет собой способ приготовления пероральной трансмукозальной композиции метформина, включающий:
смешивание (а) эффективного количества фармацевтического агента, состоящего из метформина или его фармацевтически приемлемой соли с (б) эффективным количеством по меньшей мере одного усилителя абсорбции, выбранного из алкилсульфата щелочного металла, глицерина, желчной кислоты или соли желчной кислоты, лецитина, гиалуроновой кислоты, октилфеноксиполиэтоксиэтанола, гликолевой кислоты, молочной кислоты, экстракта ромашки, экстракта огурца, олеиновой кислоты, линоленовой кислоты, масла бурачника, масла энотеры, полиглицерина, лизина, полилизина, триолеина, моноолеина, моноолеатов, монолауратов, ментола, полидоканол-алкиловых эфиров, хенодезоксихолата, дезоксихолата и их фармацевтически приемлемых солей и аналогов, с образованием пасты;
смешивание пасты с основой жевательной резинки; и
формование полученной в результате смеси в таблетки, капсулы, каплеты или подушечки жевательной резинки.
Фармацевтически приемлемые соли и аналоги любого из раскрытых усилителей абсорбции также входят в объем настоящего изобретения, как и смеси или комбинации любого из этих соединений.
Усилители абсорбции представляют собой агенты, которые облегчают доставку фармацевтического агента через слизистые оболочки рта. При использовании здесь, "облегчать" относится к увеличению скорости и/или количества фармацевтического агента, доставленного через слизистую оболочку рта (например, по меньшей мере, приблизительно на 5%, 10%, 20%, 25%, 30%, 35%, 40%, 50%, 60% или 75%) по сравнению с фармацевтической композицией, не содержащей усилителя абсорбции.
Каждый усилитель абсорбции может присутствовать в концентрации вплоть до приблизительно 30, 20, 15, 10, 5, 2, 1, 0,5 или 0,01 мас./мас.% от общей массы композиции. Общее количество усилителей абсорбции составляет менее чем приблизительно 30, предпочтительно менее чем приблизительно 20 и более предпочтительно менее чем приблизительно 10 или 7 мас./мас.% от общей массы композиции.
Усилители абсорбции представляют собой мицеллообразующие соединения, которые служат для инкапсулирования фармацевтического агента и облегчения его доставки через слизистые оболочки рта, когда композиция включена в раствор в ротовой полости.
Как будет понятно специалистам в данной области техники, мицелла представляет собой коллоидный агрегат амфипатических молекул, в котором полярные гиброфильные части молекулы направлены наружу, тогда как неполярные гидрофобные части направлены внутрь. Полагают, что присутствие мицелл в значительной мере способствует абсорбции фармацевтического агента как из-за их улучшенной абсорбционной способности, так и из-за их размера. Кроме того, инкапсулирование фармацевтических агентов в мицеллы защищает агенты от быстрого распада.
Будет понятно, что каждая мицелла может содержать фармацевтический агент и один или более усилителей абсорбции (то есть мицеллообразующих соединений). Предпочтительно, для формирования смешанных мицелл используют по меньшей мере два мицеллообразующих соединения. При использовании здесь, термин "смешанные мицеллы" относится к по меньшей мере двум различным типам мицелл, каждый из которых был образован с использованием различных мицеллообразующих соединений. Например, настоящие композиции могут содержать смесь по меньшей мере двух различных типов мицелл: мицелл, образованных между фармацевтическим агентом и одним из мицеллообразующих соединений (например, алкилсульфатом щелочного металла), и мицелл, образованных между фармацевтическим агентом и по меньшей мере одним дополнительным мицеллообразующим соединением (например, гликохолатом натрия). Будет понятно, что каждая индивидуальная мицелла может быть образована из более чем одного мицеллообразующего соединения.
Размер мицелл составляет предпочтительно больше 6 микрон, но может быть меньше, то есть от приблизительно 1 до приблизительно 10 нанометров, или от приблизительно 1 до приблизительно 5 нанометров. Форма мицелл может меняться и может быть, например, вытянутой, сплющенной или сферической; наиболее типичными являются сферические мицеллы. Полагают, что чрезвычайно малый размер мицелл помогает инкапсулированному фармацевтическому агенту эффективно проникать через слизистые оболочки рта. Таким образом, настоящие композиции предлагают повышенную биодоступность активного лекарственного средства, в частности через слизистые оболочки рта, по сравнению с известными на рынке фармацевтическими препаратами.
В настоящих композициях может быть использован любой алкилсульфат щелочного металла при условии, что нет проблем с совместимостью. Предпочтительно алкил представляет собой С8-С22 алкил, более предпочтительно лаурил (С12). Может быть использован любой щелочной металл, при этом предпочтительным является натрий. В то время как алкилсульфат щелочного обычно присутствует в концентрации вплоть до приблизительно 30 мас./мас.%, предпочтительной является концентрация вплоть до приблизительно 5 мас./мас.% от общей массы композиции. Еще более предпочтительной является концентрация вплоть до приблизительно 1, 0,5 или 0,01 мас./мас.% от общей массы композиции.
При использовании здесь, термин "желчная кислота" включает производные холевой кислоты, такие как холевую, гликохолевую, хенодезоксихолевую, таурохолевую, гликодезоксихолевую и тауродезоксихолевую кислоты, но не ограничивается ими. В композициях по настоящему изобретению могут быть использованы любые желчные кислоты или их соли. Предпочтительным является гликохолат натрия. Так как в настоящем изобретении используют относительно низкие концентрации солей желчных кислот, проблемы с токсичностью, связанной с использованием таких солей, сведены к минимуму, а то и вовсе исключены.
Лецитин может быть насыщенным или ненасыщенным и предпочтительно выбран из фосфатидилхолина, фосфатидилсерина, сфингомиелина, фосфатидилэтаноламина, кефалина и лизолецитина.
Предпочтительные соли гиалуроновой кислоты представляют собой гиалуронаты щелочных металлов, особенно гиалуронат натрия, гиалуронаты щелочно-земельных металлов и гиалуронат алюминия. При использовании гиалуроновой кислоты или ее фармацевтически приемлемых солей в настоящих композициях, концентрация предпочтительно составляет приблизительно от 1 до 5 мас./мас.% от общей масс композиции, наиболее предпочтительно приблизительно от 1,5 до 3,5 мас./мас.%.
Композиция может дополнительно содержать изотонический агент в концентрации вплоть до приблизительно 30, 20, 15, 10 или 6 мас./мас.% от общей массы композиции. Подходящие изотонические агенты включают сахариды, такие как сорбит и маннит, и многоатомные спирты, такие как глицерин, полиглицерин, пропиленгликоль и тому подобное, и двухосновный фосфат натрия, но не ограничиваются ими. Предпочтительным является глицерин. Изотонический агент служит для сохранения мицелл в растворе. Глицерин может служить и как мицеллообразующее соединение, и как изотонический агент; при использовании двухосновного фосфата натрия он также может ингибировать рост бактерий.
Возможно, фармацевтическая композиция может содержать один или более дополнительных терапевтических агентов (например, сульфонмочевины). При использовании здесь, термин "терапевтический агент" относится к агенту, который облегчает заболевание или симптомы, связанные с заболеванием, включая предупреждение или отсрочку появления симптомов заболевания и/или уменьшение их тяжести или частоты. В одном воплощении терапевтический агент применяют для лечения диабета, преддиабета, ожирения или синдрома поликистоза яичников.
В настоящую композицию должно быть включено эффективное количество фармацевтического агента. При использовании здесь, термин "эффективное количество" относится к количеству фармацевтического агента, необходимому для достижения желаемого результата, такого как получение намеченного терапевтического лечения или предупреждение расстройства у пациента, или регулирование физиологического состояния пациента. Поэтому такое количество будет подразумеваться как обладающее терапевтическим и/или профилактическим действием на пациента. Будет понятно, что эффективное количество будет меняться в зависимости от конкретного используемого агента, параметров, установленных для агента, природы и тяжести расстройства, которое лечат, пациента, которого лечат, и характеристик используемого носителя.
"Эффективное количество" также может представлять собой количество, необходимое для того, чтобы пиковые концентрации метформина в плазме были приблизительно равны пиковым концентрациям метформина в плазме у субъекта, которому введена пероральная таблетка гидрохлорида метформина (например, таблетка гидрохлорида метформина, содержащая приблизительно 50, 100, 250, 500, 750, 800 или 1000 мг гидрохлорида метформина). При использовании здесь, "приблизительно равны" означает, что пиковая концентрация метформина в плазме после введения фармацевтической композиции по изобретению (оцененная с помощью измерений на стандартную биодоступность) находится в пределах 10% от пиковой концентрации метформина в плазме после введения пероральной таблетки препарата метформина.
Будет понятно, что любое понижение уровней глюкозы в плазме, выработки глюкозы печенью, уровней липидов, кишечной абсорбции или потеря веса может быть терапевтическим и/или профилактическим, как и любое повышение чувствительности к инсулину. Точный уровень дозировки должен быть определен лечащим врачом или другим медицинским работником и будет зависеть от хорошо известных факторов, включающих возраст, массу тела, пол и общее состояние здоровья субъекта, а также применение сопутствующих терапевтических процедур (или их отсутствие). Конечно, специалисту в данной области техники понятно, что разделенные и частичные дозы также входят в объем настоящего изобретения. Определение эффективного количества находится в пределах компетенции специалиста в данной области техники.
Фармацевтически эффективные дозы могут быть экстраполированы из кривых доза-ответ, полученных на основе in vitro тестов или тест-систем с использованием животных моделей. Они также могут быть определены путем измерения биодоступности известных пероральных препаратов гидрохлорида метформина. Фармацевтическая композиция по изобретению затем может быть изготовлена в виде препарата с дозой, имеющей биодоступность, которая приближается к биодоступности известных пероральных препаратов.
Количество фармацевтического агента может составлять приблизительно от 50 до 850 мг.
Типично, настоящие композиции будут содержать приблизительно от 50 до 500 мг на дозу. В зависимости от режима дозировки, каждая доза может содержать 50, 112,5, 250 мг или 500 мг. Будет понятно, что количество будет изменяться в зависимости от, среди прочего, характеристик высвобождения используемого носителя. Количество активного ингредиента будет подобрано так, чтобы количество высвобождаемого фармацевтического агента оказывало ожидаемое терапевтическое и/или профилактическое действие.
Каждая доза может содержать приблизительно от 5 до 90, более предпочтительно приблизительно от 10 до 80 мас./мас.% и еще более предпочтительно приблизительно от 20 до 80 или от 20 до 50 мас./мас.% фармацевтического агента от общей массы композиции, в зависимости от количества присутствующего носителя.
Настоящие композиции возможно содержат стабилизатор и/или консервант. Фенольные соединения особенно подходят для этих целей, так как они не только стабилизируют композицию, но и защищают от бактериального роста и способствуют абсорбции композиции. Следует понимать, что фенольное соединение относится к соединению, имеющему одну или более гидроксильных групп, присоединенных непосредственно к бензольному кольцу. Предпочтительные фенольные соединения согласно настоящему изобретению включают фенол и метилфенол (также известный как мета-крезол) и их смеси.
Композиции по настоящему изобретению могут дополнительно содержать одно или более из следующего ниже: неорганические соли; антиоксиданты и ингибиторы протеаз. Количество любого из этих возможных ингредиентов для применения в настоящих композициях может быть определено специалистом в данной области техники.
Неорганическая(ие) соль или соли должна(ы) быть такой(ими), которая(ые) может (могут) дополнительно стимулировать высвобождение инсулина. Неограничивающими примерами неорганических солей являются соли натрия, калия, кальция и цинка, особенно хлорид натрия, хлорид калия, хлорид кальция, хлорид цинка и бикарбонат натрия.
Антиоксидант используют для предотвращения разложения и окисления фармацевтически активных ингредиентов. Антиоксидант может быть выбран из токоферола, мезилата детероксима, метилпарабена, этилпарабена, аскорбиновой кислоты и их смесей, а также других антиоксидантов, известных в фармации. Предпочтительным антиоксидантом является токоферол. Парабены также будут обеспечивать консервирующее действие на композицию.
Ингибиторы протеаз служат для ингибирования разложения фармацевтического агента под действием протеолитических ферментов. Когда их используют, ингибиторы протеаз предпочтительно присутствуют в концентрации приблизительно от 1 до 3 мас./мас.% композиции. Может быть использован любой материал, который ингибирует протеолитическую активность и не имеет проблем совместимости. Примеры включают бацитрацин и производные бацитрацина, такие как метилен-дисалицилаты бацитрацина, соевый трипсин и апротинин, но не ограничиваются ими. Бацитрацин и его производные предпочтительно используют в концентрации приблизительно от 1,5 до 2 мас./мас.% от общей массы композиции, тогда как соевый трипсин и апротинин предпочтительно используют в концентрации приблизительно от 1 до 2 мас./мас.% от общей массы композиции.
Специалисту в данной области техники будет понятно, что в композицию также могут быть включены красители, корригенты и нетерапевтические количества других соединений. Когда в качестве одного из мицеллообразующих соединений используется ментол, он также будет придавать композиции аромат.
Корригенты могут представлять собой эфирные масла, эссенции, экстракты, порошки, кислоты и другие вещества, способные влиять на вкусовой профиль. Ароматы, которые можно использовать, включают кокосовый, кофейный, аромат колы, шоколадный, ванильный, грейпфрутовый, ментоловый, лакричный, анисовый, абрикосовый, карамельный, медовый, ананасовый, клубничный, малиновый, аромат тропических фруктов, вишневый, коричный, аромат перечной мяты, аромат гаультерии, аромат мяты колосовой, эвкалиптовый и мятный ароматы, но не ограничиваются ими. В одном воплощении ароматы выбраны из ментолового, карамельного, кофейного и колы.
Красители, которые можно использовать, могут быть природного или синтетического происхождения и должны быть одобрены для использования в пище или лекарственных препаратах.
Носитель может быть изготовлен в виде различных форм, таких как формы животных или звезд, чтобы быть привлекательным для детей.
Композиции по настоящему изобретению могут храниться при комнатной температуре или при низкой температуре.
Фармацевтический агент предназначен для введения через слизистые оболочки рта или "ротовые слизистые оболочки". Они включают оболочки полости рта, горла, гортани и пищевода. Оболочки полости рта являются предпочтительными, в частности слизистая оболочка щек и подъязычная слизистая оболочка. Подъязычная слизистая оболочка включает оболочку вентральной поверхности языка и дна полости рта, а слизистая оболочка щек представляет собой внутреннюю поверхность щек. Подъязычная слизистая оболочка и слизистая оболочка щек являются относительно проницаемыми, обеспечивая быструю абсорбцию и приемлемую биодоступность многих лекарств. Более того, подъязычная слизистая оболочка и слизистая оболочка щек являются близкими, легко доступными и их нельзя избежать. По сравнению с ЖК трактом и другими органами, буккальная среда имеет более низкую ферментативную активность и нейтральное значение рН, что позволяет лекарству оказывать более длительное действие in vivo.
Носитель разработан так, чтобы высвобождать достаточное количество фармацевтического агента и находиться в полости рта в течение достаточного периода времени для абсорбции агента с тем, чтобы обеспечить терапевтический и/или профилактический эффект для пациента. Для лучшей абсорбции носитель предпочтительно является таким, который может двигаться в полости рта так, чтобы контактировать с увеличенной площадью поверхности слизистых оболочек рта. В предпочтительных воплощениях носитель изготовлен в виде пригодного для жевания леденца (например, жевательной резинки или ириски (taffey)) или в виде твердого леденца или лепешки, которые можно жевать или сосать в течение достаточного периода времени, пока леденец двигается около слизистых оболочек рта. Количество высвобожденного фармацевтического агента составляет приблизительно более 50, 60, 70, 80 или 90% за период времени, пока носитель находится в полости рта. Этот период времени составляет приблизительно от 1 до 30, предпочтительно приблизительно от 1 до 20 и более предпочтительно приблизительно от 1 до 10 минут. При высвобождении в полости рта и растворении в слюне фармацевтический агент будет находиться в мицеллярной форме, так как он будет инкапсулирован мицеллообразующими усилителями абсорбции, используемыми здесь. Специалист в данной области техники легко поймет как приготовить подходящие носители на основании данных, раскрытых здесь и известных из литературы.
Способ приготовления композиции
В настоящем изобретении также предложен способ приготовления фармацевтической композиции по настоящему изобретению. Настоящие композиции могут быть получены смешиванием эффективного количества фармацевтического агента, состоящего из метформина или его фармацевтически приемлемой соли, с эффективным количеством по меньшей мере одного усилителя абсорбции, выбранного из алкилсульфата щелочного металла, глицерина, желчной кислоты или соли желчной кислоты, лецитина, гиалуроновой кислоты, октилфеноксиполиэтоксиэтанола, гликолевой кислоты, молочной кислоты, экстракта ромашки, экстракта огурца, олеиновой кислоты, линоленовой кислоты, масла бурачника, масла энотеры, полиглицерина, лизина, полилизина, триолеина, моноолеина, моноолеатов, монолауратов, ментола, полидоканол-алкиловых эфиров, хенодезоксихолата, дезоксихолата и их фармацевтически приемлемых солей и аналогов, с образованием препарата, который объединяют с фармацевтически приемлемым носителем.
Способ может включать стадию добавления одного или более ингредиентов, выбранных из изотонических агентов, стабилизаторов, консервантов, антиоксидантов, ингибиторов протеаз и неорганических солей.
Смешивание может быть осуществлено с использованием высокоскоростного смесителя, такого как профессиональный миксер для лабораторного использования серии HD торговой марки KitchenAid или подобный.
Для приготовления композиции жевательной резинки способ может включать дополнительные стадии:
смешивание препарата с основой жевательной резинки; и
формование полученной в результате смеси в таблетки, капсулы, каплеты или подушечки жевательной резинки.
Конкретные количества ингредиентов могут быть определены специалистом в данной области техники на основе общих указаний, изложенных здесь.
Способ лечения
В изобретении предложен способ лечения состояний, выбранных из диабета, преддиабета, ожирения и синдрома поликистоза яичников, включающий введение субъекту композиции в соответствии с первым аспектом изобретения. Настоящие композиции могут быть полезны для снижения уровней глюкозы в плазме у субъекта (например, уровня глюкозы после приема пищи), снижения выработки глюкозы печенью, снижения уровней липидов, повышения чувствительности к инсулину, снижения кишечной абсорбции глюкозы, снижения гипогликемии, снижения массы тела и/или снижения аппетита.
Если композиция находится в форме пригодного для жевания леденца или твердого леденца или лепешки, способ включает пережевывание и/или сосание леденца в течение периода времени, достаточного для высвобождения и абсорбции фармацевтического агента в мицеллярной форме, с тем, чтобы обеспечить терапевтический и/или профилактический эффект для пациента.
Фармацевтическая композиция может быть представлена в виде однократной дозы (например, один кусочек или одна резинка, или леденец) или может быть представлена в многократных дозах, которые вводят периодически. Частота введения и количество метформина или его соли, принятое за одну дозу, будет определяться предписанием врача на основе природы и тяжести состояния, которое лечат, и других факторов, включая пол, массу тела, здоровье и возраст субъекта, но не ограничиваясь ими.
Способ также может включать стадии введения одного или более терапевтических агентов для лечения диабета, преддиабета, ожирения и/или синдрома поликистоза яичников и/или снижения массы тела. Терапевтические агенты для вышеуказанных состояний известны из уровня техники, а режим дозирования комбинированной терапии может быть определен врачом или практикующим медицинским работником. Например, фармацевтическая композиция по изобретению может быть введена одновременно в другим(и) терапевтическим(и) агентом(ами), или, альтернативно, в разное время суток. В частности, фармацевтическая композиция по изобретению может быть введена в комбинации с инсулином для лечения диабета. Когда фармацевтические композиции по изобретению используют в комбинации с инсулином, количество инсулина, необходимое для контроля диабета, может быть снижено.
При использовании здесь, "диабет" или "сахарный диабет" относится к состоянию, характеризуемому гипергликемией. Гипергликемия может являться результатом абсолютного или относительного ухудшения секреции инсулина и/или действия инсулина. Способы обнаружения гипергликемии известны из уровня техники и обычно включают в себя измерение уровней глюкозы в плазме. У пациентов, не обнаруживающих симптомов заболевания, диабет можно диагностировать, когда имеет место диагностический критерий для гипергликемии натощак: уровень глюкозы в плазме (или сыворотке)>=140 мг/дал (>=7,77 ммоль/л) (рекомендован Национальной группой по изучению диабета (National Diabetes Data Group (NDDG))) после ночного голодания в двух случаях у взрослого или ребенка; или когда субъект имеет уровни глюкозы в плазме натощак более 126 мг/дал (>6,99 ммоль/л) (рекомендован американской диабетической ассоциацией (American Diabetes Association)). Диабет включает диабет 1 типа (инсулинозависимый сахарный диабет), при котором у субъекта образуется очень мало инсулина или совсем не образуется, и диабет 2 типа (инсулинонезависимый сахарный диабет), при котором гипергликемия является результатом как нарушенного инсулин-секреторного ответа на глюкозу, так и/или пониженной эффективности инсулина в стимулировании усвоения глюкозы скелетными мышцами и в сдерживании образования глюкозы печенью (инсулинорезистентность).
При использовании здесь, "преддиабет" (также называемый как нарушенная толерантность к глюкозе, то есть IGT) относится к состоянию, которое имеет место, когда уровень глюкозы в плазме у субъекта после приема пищи выше нормы, но недостаточно высок для диагноза диабет 2 типа. Способы измерения уровней глюкозы в плазме известны из уровня техники.
При использовании здесь, "синдром поликистоза яичников" или "гиперандрогенная хроническая ановуляция" представляет собой состояние, которое может быть причиной аменореи, но обычно характеризуется нерегулярными менструациями, легкой степенью ожирения и гирсутизмом, обычно начинающимся в пубертатном возрасте и ухудшающимся со временем. Большинство пациентов имеет обильную шеечную слизь при исследовании и повышенный уровень свободных эстрогенов. Уровни большинства циркулирующих андрогенов имеют тенденцию к небольшому повышению. Яичники могут быть увеличены с гладкими, утолщенными капсулами или могут быть нормальными по размеру. Типично, яичники содержат много 2-6 мм фолликулярных кист, и капсульная гиперплазия окружает зернистые клетки. Могут присутствовать большие кисты, содержащие атретические клетки.
При использовании здесь, "ожирение" относится к обладанию массой тела, которая более чем приблизительно на 30% больше идеальной массы тела, как определено специалистом-медиком, и/или к обладанию индексом массы тела, который больше чем приблизительно 27, как определено специалистом-медиком.
Термины "терапевтический," "лечение" и "лечить" при использовании здесь относятся к улучшению заболевания или симптомов, связанных с заболеванием, включая предупреждение или отсрочку появления симптомов заболевания и/или уменьшение тяжести или частоты симптомов заболевания.
Симптомы диабета и преддиабета включают дислипидемию, ожирение, артериальную гипертензию и микрососудистые и макрососудистые осложнения, например атеросклероз, ретинопатии, нефропатии и невропатии, но не ограничиваются ими. Симптомы ожирения включают диабет (например, диабет 2 типа), заболевание коронарных артерий, окклюзионное заболевание периферических артерий, инфаркт миокарда, дислипидемии (например, гиперлипидемию), удар, хронические венозные патологии, ортопедические проблемы, синдромы апноэ во сне, эзофагеальный рефлюкс, гипертензию, артрит, бесплодие, прерывания беременности и рак (например, колоректальный рак, рак молочной железы), но не ограничиваются ими.
ПРИМЕРЫ
Приготовление пастообразного препарата
Препарат для применения в приготовлении композиции по настоящему изобретению готовили следующим образом.
Пример 1
Порошкообразный гидрохлорид метформина (доступный от Spectrum Chemicals), порошкообразный гликохолат натрия (доступный от NutriScience Innovations, LLC) и порошкообразный лаурилсульфат натрия (доступный от Charles Tennant and Bioshop) пропускали через сито 100 меш, и частицы, прошедшие сквозь сито, использовали для приготовления препарата.
При комнатной температуре и относительной влажности от 25 до 65%, 123,51 г жидкого глицерина (доступного от Canada Colors and Chemicals Ltd.) медленно вливали в высокоскоростной смеситель и перемешивали в течение приблизительно от двух до трех минут. К смеси добавляли 4,83 г порошкообразного гликохолата натрия, и два ингредиента перемешивали в течение дополнительных двух-трех минут. Затем добавляли 4,82 г порошкообразного лаурилсульфата натрия, и смесь перемешивали в течение еще двух-трех минут с получением непрозрачного раствора. Затем добавляли 1000 г порошкообразного гидрохлорида метформина, продолжая перемешивание в течение еще 15-20 минут с получением гомогенной пасты тестообразной консистенции.
Полученная таким образом паста соответствует настоящему изобретению и содержала гидрохлорид метформина в концентрации 88,25 мас./мас.%, глицерин в концентрации 10,90 мас./мас.%, гликохолат натрия в концентрации 0,43 мас./мас.% и лаурилсульфат натрия в концентрации 0,43 мас./мас.%, все от общей массы пастообразного препарата.
Пример 2
Протокол Примера 1 повторяли со слегка измененными количествами исходных ингредиентов с получением пасты по настоящему изобретению, содержащей гидрохлорид метформина в концентрации 76,98 мас./мас.%, глицерин в концентрации 22,28 мас./мас.%, гликохолат натрия в концентрации 0,37 мас./мас.% и лаурилсульфат натрия в концентрации 0,37 мас./мас.%, все от общей массы пастообразного препарата.
В Примерах 1 и 2 количество глицерина, используемого для приготовления пасты, может быть уменьшено с тем, чтобы получить пасту, содержащую до 10 мас./мас.% глицерина от общей массы пасты. Пастообразный препарат можно объединять с подходящим фармацевтически приемлемым носителем для получения композиции по настоящему изобретению.
Приготовление композиции жевательной резинки
Пример 3
Пасту Примера 2 превращали в композицию жевательной резинки (подушечки) согласно другому аспекту изобретения. Каждая подушечка содержала гидрохлорид метформина в концентрации 212,5 мас./мас.%, глицерин в концентрации 6,15 мас./мас.%, гликохолат натрия в концентрации 0,10 мас./мас.% и лаурилсульфат натрия в концентрации 0,10 мас./мас.%, все от общей массы композиции подушечки. Остальная часть каждой подушечки состояла из основы резинки.
Несмотря на то, что жевательная резинка по этому примеру содержала глицерин в концентрации 6,15 мас./мас.%, исходное количество глицерина, используемое для приготовления пасты, может быть снижено для получения жевательной резинки, содержащей до 3 мас./мас.% глицерина от общей массы резинки.
Пример 4
Количество ингредиентов, используемых в Примере 3 для приготовления пасты, корректировали с тем, чтобы получить композицию резинки, содержащую 850 мг гидрохлорида метформина, 246 мг глицерина, 4 мг гликохолата натрия и 4 мг лаурилсульфата натрия.
В обоих Примерах 3 и 4 жевательную резинку готовили согласно известному способу следующим образом. Материал матрицы, состоящий из эластомеров, эмульгаторов и восков, измельчали и помещали в традиционный смеситель для жевательной резинки. Затем добавляли дополнительные ингредиенты (подсластители, корригенты и красители) для образования приятной основы резинки. Затем к основе резинки добавляли пасту в соотношении приблизительно 276 частей пасты на 1000 частей основы резинки и смешивали все ингредиенты до образования гомогенной массы жевательной резинки. Теплую массу резинки затем удаляли из смесителя и с использованием обычных систем и устройств формовали кусочки жевательной резинки. Кусочки резинки оставляли для затвердения и покрывали подходящим покрытием драже, которое содержало дополнительные красители и корригенты.
Композиции жевательной резинки по настоящему изобретению могут быть приготовлены с использованием других известных способов, таких как те, которые описаны в патентах US №5487902, 6344222, 6432383 и 5470566, содержания которых включены здесь посредством ссылки.
Приготовление твердых леденцов и лепешек
Пасту можно сформовать, например, в твердые леденцы и лепешки с использованием известных способов, таких как способы, раскрытые, например, в патенте US №5470566, содержания которых включены здесь посредством ссылки.
Ее также можно использовать для приготовления жевательных капсул, как описано, например, в публикации заявки на патент US №2003/0095925 А1, содержание которой включено здесь посредством ссылки.
Тесты, включающие введение резинки метформина
Жевательную резинку Примера 3, описанную выше, содержащую 212,5 мг гидрохлорида метформина на каждую подушечку, давали двум субъектам, лицам А и В. Субъекты не получали пищи в течение ночи, а на следующее утро им давали одну подушечку в момент времени 0, которую они жевали в течение 30 минут, а затем выплевывали. Через 10 минут ожидания субъектам давали другую подушечку для жевания в течение еще 30 минут. Затем субъекты находились в состоянии четырехчасового ожидания и жевали третью подушечку в течение приблизительно 30-40 минут перед первым приемом пищи за день. Концентрацию метформина в плазме у лиц А и В (в нг/мл) измеряли, начиная с момента времени 0, и отражали на графике фиг.1. Серия 2 представляет концентрацию метформина в плазме для лица А. Серия 3 представляет концентрацию метформина в плазме для лица В.
За неделю до этого, лицу В давали 850 мг таблетку гидрохлорида метформина, проданную под товарным знаком GLUCOPHAGE от Bristol-Meyers Squib Со. Таблетка была проглочена утром в момент времени 0 после ночного воздержания от пищи. Концентрацию метформина в плазме лица В (в нг/мл) измеряли, начиная от момента времени 0, и отражали на графике фиг.1 (см. Серию 1).
Пиковые концентрации метформина в плазме имели место после приблизительно 300 минут у контрольного субъекта, получившего GLUCOPHAGE, и у одного из субъектов, получивших резинку метформина. Пиковая концентрация метформина в плазме у второго субъекта, получившего резинку метформина, имела место приблизительно после 360 минут. У одного из лиц, получивших резинку, пиковая концентрация в плазме составляла выше 2000 нг/мл по сравнению с пиковой концентрацией ниже 1500 нг/мл у субъекта, получившего таблетку GLUCOPHAGE. Эти результаты указывают на то, что резинка является такой же эффективной или более эффективной, чем таблетки, при доставке гидрохлорида метформина в кровоток человека, несмотря на то, что концентрации гидрохлорида метформина в дозе из трех подушечек гораздо ниже.
Высвобождение гидрохлорида метформина из жевательной резинки
Пастообразный препарат Примера 2 приготавливали для трех различных композиций жевательной резинки с использованием известного способа, описанного выше. Использовали ароматизированные основы резинок. Серийные номера, используемые для идентификации каждой основы резинки, и композиция жевательной резинки, полученная с использованием каждой основы, представлены ниже.
Композиция жевательной резинки 5475-01-1, сделанная с использованием основы резинки с ароматом колы 25084;
композиция жевательной резинки 5475-04-1, сделанная с использованием основы резинки с ароматом карамели 25046; и
композиция жевательной резинки 5475-05-1, сделанная с использованием основы резинки с ароматом кофейной карамели 25046.
Композиции жевательных резинок были в виде подушечек массой один грамм. Подушечки содержали приблизительно 210, 217 и 214 мг гидрохлорида метформина соответственно. Следует понимать, что истинное количество гидрохлорида метформина может меняться в обе стороны в пределах до 5%.
Каждую подушечку помещали в устройство для жевания, содержащее буферный раствор. Подушечку жевали со скоростью 60 жевательных движений в минуту в течение 20 минут. Количество гидрохлорида метформина, высвобожденное в буферный раствор, измеряли, используя высокоэффективную жидкостную хроматографию (ВЭЖХ) в моменты времени 2, 5, 10 и 20 минут в виде процентного содержания высвобожденного гидрохлорида метформина. Результаты суммированы в Таблице 1 ниже, и процентное содержание высвобожденного лекарства отражено на графике (см. фиг.2).
Начальная скорость высвобождения для композиции резинки 5475-01-1 ниже, чем для других композиций по причине использования основы резинки с более медленным высвобождением.
Суммарные результаты показывают, что высвобождение гидрохлорида метформина происходит довольно быстро во всех композициях, при этом по меньшей мере 90% фармацевтического агента высвобождается всего через пять минут жевания.
Пример 5
Тесты, сравнивающие резинку с метформином и таблетки метформина при одинаковом уровне доз
Жевательную резинку с композицией, идентичной композиции Примера 3, за исключением того, что количество гидрохлорида метформина составляло 214,5 мг на подушечку (в отличие от 212,5 мг), давали группе из десяти здоровых добровольцев (6 мужчин, 4 женщины), средний возраст которых составлял 30 и 29,8 лет, соответственно, и имеющих средний индекс массы тела (ИМТ) 23,9 и 21,49 соответственно. В момент времени 0 каждому субъекту дали две подушечки для жевания с общей дозой 429 мг гидрохлорида метформина.
В качестве контроля, на следующий день той же группе субъектов давали 429 мг таблетку гидрохлорида метформина, проданную под товарным знаком GLUCOPHAGE от Bristol-Meyers Squib Co.
Образцы плазмы (300 микролитров), полученные от субъектов, подвергали твердофазной экстракции (spe) со слабым катионным обменом перед анализом с помощью ВЭЖХ.
Концентрацию метформина в плазме субъектов (в млн-1) измеряли, начиная с момента времени 0 минут; дополнительный отбор проб осуществляли через 5, 15, 30, 45, 60, 90, 120, 150, 180, 210, 240, 300, 360, 540, 720, 1440 минут (24 часа). Результаты представлены на графике фиг.3.
Анализы соответствующих площадей под кривой (AUC) с помощью ANOVA (f-тест) и парного t-теста показали, что не было существенного различия между концентрациями в плазме у субъектов, получивших резинку, по сравнению с субъектами, получившими таблетку GLUCOPHAGE, хотя концентрации в плазме после резинки имеют тенденцию к тому, чтобы быть выше. Пиковые концентрации метформина в плазме имели место приблизительно через 200 минут в обеих группах субъектов, при этом пиковая концентрация в плазме составила почти 0,8 млн-1 у субъектов, получивших резинку, по сравнению с почти 0,6 млн-1 у субъектов, получивших таблетку GLUCOPHAGE.
Эти результаты указывают на то, что жевательная резинка является по меньшей мере такой же эффективной, как и таблетки, при доставке гидрохлорида метформина в кровоток человека.
Хотя это изобретение было подробно продемонстрировано и описано со ссылками на его предпочтительные воплощения, специалисту в данной области техники будет понятно, что в пределах объема данного изобретения, охватываемого прилагаемой формулой изобретения, могут быть сделаны различные изменения по форме и в деталях.
Изобретение относится к химико-фармацевтической промышленности и касается пероральных трансмукозальных фармацевтических композиций, содержащих метформин или его фармацевтически приемлемую соль, в присутствии по меньшей мере одного усилителя абсорбции, выбранного из алкилсульфата щелочного металла, глицерина, желчной кислоты или соли желчной кислоты, а также к способам применения таких композиций для лечения диабета у субъекта, к способу приготовления композиций. Заявленная композиция обеспечивает высокую биодоступность метформина у субъекта и быстрое наступление терапевтического эффекта. 5 н. и 19 з.п. ф-лы, 1 табл., 3 ил.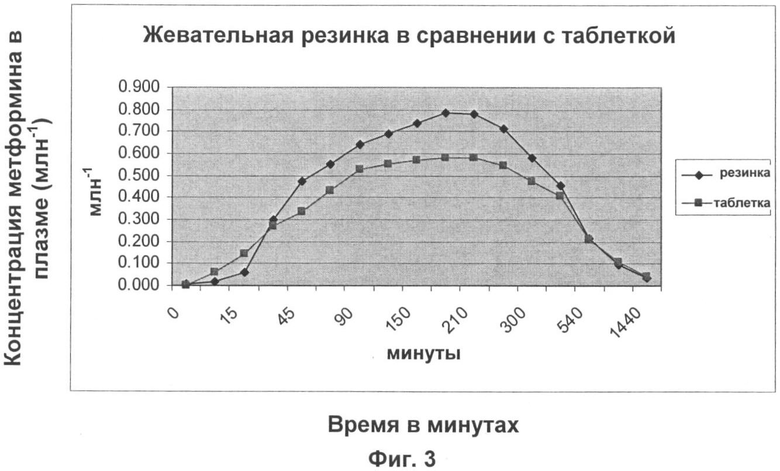
1. Пероральная трансмукозальная фармацевтическая композиция для доставки фармацевтически эффективного количества метформина или его фармацевтически приемлемой соли через слизистую оболочку рта субъекта, содержащая:
эффективное количество метформина или его фармацевтически приемлемой соли,
эффективное количество по меньшей мере одного усилителя абсорбции, выбранного из алкилсульфата щелочного металла, глицерина, желчной кислоты или соли желчной кислоты, и
фармацевтически приемлемый носитель в форме твердого леденца, лепешки, жевательной резинки или жевательной таблетки;
где фармацевтический агент присутствует в концентрации от 5 до 90 мас./мас.% от общей массы препарата.
2. Композиция по п.1, где каждый усилитель абсорбции присутствует в концентрации вплоть до приблизительно 30 мас./мас.% от общей массы композиции, и общая концентрация усилителей абсорбции составляет менее чем приблизительно 30 мас./мас.% от общей массы композиции.
3. Композиция по п.1, где каждый усилитель абсорбции присутствует в концентрации менее чем приблизительно 7 мас./мас.% от общей массы композиции.
4. Композиция по п.1, где алкилсульфат щелочного металла представляет собой С8-С22 алкилсульфат щелочного металла.
5. Композиция по п.1, содержащая лаурилсульфат натрия.
6. Композиция по п.1, содержащая глицерин.
7. Композиция по п.1, содержащая гликохолат натрия.
8. Композиция по п.1, где фармацевтически приемлемая соль метформина представляет собой гидрохлорид метформина.
9. Композиция по п.1, где количество метформина или его фармацевтически приемлемой соли составляет от 100 до 850 миллиграмм на дозу.
10. Композиция по п.1, где количество метформина или его фармацевтически приемлемой соли от 100 до 500 миллиграмм на дозу.
11. Композиция по п.1, где количество метформина или его фармацевтически приемлемой соли от 250 до 500 миллиграмм на дозу.
12. Фармацевтическая композиция по п.1 в форме жевательной резинки, содержащая гидрохлорид метформина в концентрации приблизительно от 10 до 50 мас./мас.%, лаурилсульфат натрия в концентрации приблизительно от 0,01 до 2 мас./мас.%, гликохолат натрия в концентрации приблизительно от 0,01 до 2 мас./мас.%, глицерин в концентрации приблизительно от 2 до 10 мас./мас.% и основу жевательной резинки в концентрации приблизительно от 10 до 90 мас./мас.%, все от общей массы композиции.
13. Композиция по п.1, где оболочка представляет собой оболочку щек.
14. Способ приготовления пероральной трансмукозальной композиции метформина, включающий:
смешивание (а) эффективного количества фармацевтического агента, состоящего из метформина или его фармацевтически приемлемой соли с (б) эффективным количеством по меньшей мере одного усилителя абсорбции, выбранного из алкилсульфата щелочного металла, глицерина, желчной кислоты или соли желчной кислоты с образованием пасты;
смешивание пасты с основой жевательной резинки; и
формование полученной в результате смеси в твердый леденец, лепешку, жевательную резинку или жевательную таблетку.
15. Композиция по любому из пп.1-13 для применения в лечении диабета у субъекта.
16. Применение композиции по любому из пп.1-13 в лечении диабета у субъекта.
17. Применение композиции по любому из пп.1-13 в изготовлении лекарственного средства для лечения диабета.
18. Способ лечения диабета, включающий введение субъекту композиции по любому из пп.1-13.
19. Способ по п.18, где композицию удерживают во рту в течение по меньшей мере 1 мин.
20. Способ по п.19, где композицию удерживают во рту в течение от 1 до 30 мин.
21. Способ по п.20, где композицию удерживают во рту в течение от 1 до 20 мин.
22. Способ по п.21, где композицию удерживают во рту в течение от 1 до 9 мин.
23. Способ по п.19, где композицию удерживают во рту в течение по меньшей мере 30 мин.
24. Способ по п.19, где композицию удерживают во рту в течение по меньшей мере 20 мин.
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Огнетушитель | 0 |
|
SU91A1 |
| US 6432383 B1, 13.02.2002 | |||
| Регистр Лекарственных Средств РЛС-Аптекарь, ООО "РЛС-2003", вып.5, 2003, с.650-651. | |||
Авторы
Даты
2011-01-20—Публикация
2006-03-30—Подача