Уровень техники
Клетки позвоночных содержат филаменты, из которых одна группа состоит из кератинов. К этим кератинам, которые встречаются также в волосах, коже и ногтях, присоединены специфические белки, такие как, например, десмоплакин, посредством специального фрагмента последовательности, так называемого кератинсвязывающего домена (Fontao L, Favre В, Riou S, Geerts D, Jaunin F, Saurat JH, Green KJ, Sonnenberg A, Borradori L., Interaction of the bullous pemphigoid antigen 1 (BP230) and desmoplakin with intermediate filaments is mediated by distinct sequences within their COOH terminus., Mol Biol Cell. 2003 May; 14(5):1978-92. Epub 2003 Jan 26; Hopkinson SB, Jones JC., The N terminus of the transmembrane protein BP180 interacts with the N-terminal domain of BP230, there by mediating keratin cytoskeleton anchorage to the cell surface at the site of the hemidesmosome, Mol Biol Cell. 2000 Jan; 11(1):277-86).
Постановка задачи
Задачей данного изобретения была разработка новых полипептидов, имеющих высокое сродство с кератином, соответственно кератинсодержащими тканями, такими как кожа или волосы. Такие полипептиды пригодны для косметической или фармацевтической обработки кератинсодержащих структур, в частности волос и кожи.
Описание изобретения
Объектом изобретения являются косметические композиции для обработки кератинсодержащих материалов, содержащих, по меньшей мере, одну кератинсвязывающую полипептидную последовательность (i) в косметически переносимой среде.
Полипептидные последовательности (i)
Пептидная последовательность (i) обладает связывающим сродством с кератином. Связывание полипептидной последовательности (i) с кератином может быть протестировано в условиях, описанных в примерах 8, 9 и 10.
Особенно хорошо пригодными кератинсвязывающими полипептидами являются последовательности, содержащиеся в десмоплакине человека или полученные из него путем изменений полипептидных последовательностей десмоплакина человека, таких как инсерция, замещение или делеция аминокислот.
Полипептидная последовательность десмоплакина человека представлена в SEQ ID NO:1. Пригодным кератинсвязывающим доменом (домен В) является полипептидная последовательность SEQ ID NO:1, положение 2193-2481, а также ее функциональные эквиваленты. Следующим кератинсвязывающим доменом (домен С) является полипептидная последовательность SEQ ID NO:1, положение 2606-2871, а также ее функциональные эквиваленты.
Кератинсвязывающие домены представлены на фиг.1.
Предпочтительные полипептидные последовательности (i) содержат аминокислотную последовательность согласно SEQ ID NO:1.
Изобретением охвачены также «функциональные эквиваленты» конкретно раскрытых полипептидных последовательностей (i), а также их применение в способе согласно изобретению.
«Функциональными эквивалентами» или аналогами конкретно раскрытых полипептидов (i) являются в рамках данного изобретения различные полипептиды, имеющие желаемую биологическую активность, например связывание с кератином. Так, например, под «функциональными эквивалентами» понимают полипептидные последовательности, которые согласно одному из примеров 9 или 10 описанного теста связывания имеют связывание по меньшей мере 10%, предпочтительно по меньшей мере 50%, особенно предпочтительно по меньшей мере 75%, совершенно предпочтительно 90% относительно связывания, продемонстрированного полипептидом с доменом В или с доменом С последовательности SEQ ID NO:1 в тесте связывания согласно примеру 9 или 10.
Примеры пригодных аминокислотных заместителей можно взять из следующей таблицы:
Известно, что в последовательности SEQ ID NO:1 расположенный обычно в положении 2849 серин может быть заменен глицином, чтобы избежать фосфорилирования в этом положении (Fontao L, Favre В, Riou S, Geerts D, Jaunin F, Saurat JH, Green KJ, Sonnenberg A, Borradori L., Interaction of the bullous pemphigoid antigen 1 (BP230) and desmoplakin with intermediate filaments is mediated by distinct sequences within their COOH terminus, Mol Biol Cell. 2003 May; 14(5):1978-92. Epub 2003 Jan 26).
Под «функциональными эквивалентами» понимают согласно изобретению в частности также мутеины, которые в по меньшей мере одном положении указанных выше аминокислотных последовательностей имеют отличную от конкретно указанной аминокислоту, но, несмотря на это, обладают одной из указанных выше активностей. Таким образом, «функциональные эквиваленты» охватывают мутеины, получаемые путем одного или нескольких присоединений, замещений, делеций и/или инверсий аминокислот, причем указанные изменения могут возникать в любом положении последовательности, пока они ведут к образованию мутеина с соответствующим изобретению профилем свойств.
«Функциональными эквивалентами» в указанном выше смысле являются также «прекурсоры»(предшественники) описанных полипептидов, а также «функциональные производные» и «соли» полипептидов.
При этом «прекурсорами» являются природные или синтетические предшественники полипептидов, имеющие или не имеющие желаемую биологическую активность.
Под термином «соли» понимают как соли карбоксильных групп, так и кислотоаддитивные соли аминогрупп соответствующих изобретению молекул белков. Соли карбоксильных групп могут быть получены известным способом и охватывают неорганические соли, такие как соли натрия, кальция, аммония, железа и цинка, а также соли органических оснований, например аминов, такие как триэтаноламин, аргинин, лизин, пиперидин и им подобные. Кислотоаддитивные соли, например соли с минеральными кислотами, такими как соляная кислота или серная кислота, и соли с органическими кислотами, такие как уксусная кислота и щавелевая кислота, также являются предметом данного изобретения.
«Функциональные производные» соответствующих изобретению полипептидов также могут быть получены на функциональных аминокислотных боковых группах или на их N- или С-терминальных концах с помощью известных технологий. Такие производные охватывают, например, сложные эфиры или сложные тиоэфиры групп карбоновых кислот, амиды групп карбоновых кислот, получаемые путем реакции с аммиаком или первичным или вторичным амином; N-ацильные производные свободных аминогрупп, полученные путем реакции с ацилирующими средствами; N-алкильные производные свободных аминогрупп, полученные путем реакции с алкилирующими средствами; S-ацильные производные свободных меркаптогрупп, полученные путем реакции с ацилирующими средствами; простые тиоэфиры, полученные путем реакции свободных меркаптогрупп с алкилирующими средствами; дисульфиды, полученные путем реакции свободных меркаптогрупп, например, с тиолами; O-ацильные производные свободных гидроксильных групп, полученные путем реакции с ацилирующими средствами; или простые эфиры, полученные путем реакции свободных гидроксильных групп с алкилирующими средствами.
«Функциональные эквиваленты» охватывают, естественно, также полипептиды, доступные из других организмов, а также естественно встречающиеся варианты. Например, можно путем сравнения последовательностей установить зоны гомологичных фрагментов последовательностей и в соответствии с конкретными предписаниями изобретения определить эквивалентные ферменты.
«Функциональные эквиваленты» включают также фрагменты, преимущественно отдельные домены или фрагменты последовательностей, соответствующих изобретению полипептидов, обладающих желаемыми биологическими функциями. Кроме того, «функциональными эквивалентами» являются фузионные белки, которые содержат одну или несколько указанных выше полипептидных последовательностей или производных от них функциональных эквивалентов и, по меньшей мере, еще одну, функционально от нее отличную гетерологическую последовательность в функциональной N- или С-терминальной связи (то есть без существенного взаимного функционального влияния фузионных белков). Не ограничивающими примерами таких гетерологичных последовательностей являются, например, сигнальные пептиды или ферменты.
Соответствующие изобретению «функциональные эквиваленты» являются гомологами конкретно описанных белков. Они имеют по меньшей мере 50%, предпочтительно по меньшей мере 75%, в частности по меньшей мере 85%, например 90%, 95% или 99% гомологии к конкретно описанным аминокислотным последовательностям, исчисленной по алгоритму Пирсона и Липмана (Pearson, Lipman, Proc. Natl. Acad. Sci. (USA) 85 (8), 1988, 2444-2448). Процентная гомология соответствующего изобретению гомологичного полипептида означает, в частности, процентную идентичность аминокислотного остатка относительно общей длины одной из конкретно описанных здесь аминокислотных последовательностей.
В случае возможного гликозилирования белков соответствующие изобретению «функциональные эквиваленты» охватывают белки описанного выше типа в гликозилированной или дегликозилированной форме, а также модифицированные формы, полученные путем изменения шаблона гликозилирования.
В случае возможного фосфорилирования белков соответствующие изобретению «функциональные эквиваленты» охватывают белки описанного выше типа в фосфорилированной или дефосфорилированной форме, а также модифицированные формы, полученные путем изменения шаблона фосфорилирования.
Гомологи соответствующих изобретению полипептидов (i) могут быть получены путем мутагенеза, например точечной мутации или усечения белка.
Гомологи соответствующих изобретению полипептидов могут быть идентифицированы путем скрининга комбинаторных банков мутантов, таких как мутанты укорачивания. Например, может быть создан банк вариантов белка путем комбинаторного мутагенеза на уровне нуклеиновой кислоты, например, путем ферментного легирования смеси синтетических олигонуклеотидов. Имеется большое количество способов, которые могут быть использованы для создания банков потенциальных гомологов из дегенерированной олигонуклеотидной последовательности. Химический синтез дегенерированной генной последовательности может быть осуществлен в автомате для синтеза ДНК, а синтетический ген потом может быть легирован в подходящий вектор экспрессии. Использование дегенерированного генного набора делает возможным приготовление всех последовательностей в смеси, которые кодируют желаемый набор потенциальных белковых последовательностей. Способы синтеза дегенерированных олигонуклеотидов известны специалисту (например, Narang, S.A. (1983) Tetrahedron 39:3; Itakura et al. (1984) Annu. Rev. Biochem. 53:323; Itakura et al., (1984) Science 198:1056; Ike et al. (1983) Nucleic Acids Res. 11:477).
В уровне техники известны несколько технологий скрининга генных продуктов комбинаторных банков, созданных путем точечной мутации или укорачивания, и для скрининга банков кДНК на наличие генных продуктов с выбранными свойствами. Эти технологии могут быть приспособлены для быстрого скрининга генных банков, созданных путем комбинаторного мутагенеза соответствующих изобретению гомологов. Наиболее часто используемые технологии скрининга больших генных банков, подлежащих анализу с большой производительностью, включают клонирование генного банка в воспроизводимых векторах экспрессии, трансформацию подходящих клеток с помощью результирующего банка векторов и экспрессию комбинаторных генов в условиях, в которых облегчается подтверждение желаемой активности, изоляция вектора, кодирующего ген, продукт которого должен быть подтвержден. Рекурсивный множественный мутагенез (Recursive-Ensemble-Mutagenese; REM)) - технология, увеличивающая частоту функциональных мутантов в банках, может быть использован в комбинации со скрининг-тестом для идентификации гомологов (Arkin und Yourvan (1992) PNAS 89:7811-7815; Delgrave et al. (1993) Protein Engineering 6(3):327-331).
Особенно целесообразной формой осуществления изобретения являются полипептидные последовательности (i), включающие по меньшей мере такие последовательности:
a) полипептидная последовательность SEQ ID NO:1, положение 2193-2481 (домен В),
b) полипептидная последовательность SEQ ID NO:1, положение 2606-2871 (домен С),
c) полипептидная последовательность, в которой по сравнению с последовательностью (а) изменено до 60% аминокислот,
d) полипептидная последовательность, в которой по сравнению с последовательностью (b) изменено до 50% аминокислот,
с оговоркой, что последовательности (с) или (d) имеют связывание кератина, составляющее по меньшей мере 10% значения, которое имеют полипептидные последовательности (а) или (b), при измерении в тесте согласно примерам 9 или 10. Здесь под доменами В и С имеются в виду описанные выше кератинсвязывающие домены десмоплакина человека (SEQ ID NO:1). Под изменением аминокислот здесь имеются в виду замещение, инсерция и делеция или любая комбинация этих трех возможностей.
Используют преимущественно полипептидные последовательности (i), которые для желаемого организма имеют высокоспецифичное сродство. В соответствии с этим в косметике для кожи используют предпочтительно полипептидные последовательности (i), имеющие особенно высокое сродство с кератином кожи человека. В косметике для волос предпочтение имеют полипептидные последовательности, имеющие особенно высокое сродство с кератином волос человека.
Соответственно для использования для домашних животных наряду с описанными полипептидными последовательностями (SEQ ID NO:1) преимущество имеют такие полипептидные последовательности (i), которые имеют особенно высокое сродство с соответствующим кератином, например кератином собак или кератином кошек.
Однако в соответствующей изобретению эффекторной молекуле могут быть использованы также более чем одна полипептидная последовательность (i), например последовательность (i), обладающая высоким связывающим сродством с кератином кожи человека, в сочетании с последовательностью (i), обладающей высоким связывающим сродством с кератином волос человека. Для достижения более высокого связывания могут быть соединены последовательно и другие копии подобных полипептидных последовательностей (i).
Подходящие кератинсвязывающие полипептидные последовательности (i) известны. Например, десмоплакины и плектины содержат кератинсвязывающие домены (Fontao L, Favre В, Riou S, Geerts D, Jaunin F, Saurat JH, Green KJ, Sonnenberg A, Borradori L, Interaction of the bullous pemphigoid antigen 1 (BP230) and desmoplakin with intermediate filaments is mediated by distinct sequences within their COOH terminus, Mol Biol Cell. 2003 May; 14(5): 1978-92. Epub 2003 Jan 26; Hopkinson SB, Jones JC., The N terminus of the transmembrane protein BP180 interacts with the N-terminal domain of BP230, thereby mediating keratin cytoskeleton anchorage to the cell surface at the site of the hemidesmosome, Mol Biol Cell. 2000 Jan; 11(1):277-86).
Путем сравнения таких известных белковых последовательностей, например, с помощью компьютерной программы, такой как Vector NTI 8 (версия от 25 сентября 2002) фирмы InforMax Inc., такие зоны могут быть картированы и идентифицированы.
Другими подходящими полипептидными последовательностями (i) с хорошим связыванием с кератином человека являются зоны последовательностей, которые в сравнении имеют высокую гомологию или идентичность с последовательностями или могут быть охарактеризованы как консенсусные последовательности кератинсвязывающих доменов.
Среди этих зон последовательностей особенно предпочтительными являются:
Домен В (KBD-B): полипептидная последовательность SEQ ID NO:1, положение 2193-2448
Домен В (KBD-B): полипептидная последовательность SEQ ID NO:1, положение 2209-2448
Домен С (KBD-С): полипептидная последовательность SEQ ID NO:1, положение 2606-2871
Домен С (KBD-С): полипептидная последовательность SEQ ID NO:1, положение 2616-2871
Домен С (KBD-С): полипептидная последовательность SEQ ID NO:1, положение 2616-2811
Домен С (KBD-С): полипептидная последовательность SEQ ID NO:1, положение 2606-2871
Известно, что в SEQ ID NO:1 серин, природно имеющийся в положении 2849, может быть заменен, например, глицином, чтобы избежать фосфорилирования в этом положении и тем самым обеспечить связывание домена C с соответствующим кератином (Fontao L, Favre В, Riou S, Geerts D, Jaunin F, Saurat JH, Green KJ, Sonnenberg A, Borradori L., Interaction of the bullous pemphigoid antigen 1 (BP230) and desmoplakin with intermediate filaments is mediated by distinct sequences within their COOH terminus, Mol Biol Cell. 2003 May; 14(5):1978-92. Epub 2003 Jan 26).
При желании достичь особенно хорошего связывания полипептидных последовательностей (i) с кератином из организма, не принадлежащего человеку, в качестве подходящих фрагментов последовательностей выбирают таковые из кератинсвязывающего белка, например десмоплакина или плектина, соответствующего организма.
На фиг.2 изображено сравнение кератинсвязывающих молекул.
Соответствующие изобретению кератинсвязывающие полипептиды (i) могут быть также - по желанию - снова легко отделены от кератина. Для этого может быть применено, например, промывание кератином, вследствие чего кератинсвязывающие полипептиды (i) вытесняются к кератину и насыщаются кератином из промывного средства. Альтернативно может быть осуществлено промывание раствором с большим количеством моющего средства (например, додецилсульфата натрия (SDS)) для вымывания.
Соответствующие изобретению кератинсвязывающие полипептиды (i) имеют широкую область применения в косметике для человека, в частности в средствах для ухода за кожей, ногтями и волосами, для ухода за животными, для ухода за кожаными изделиями и для обработки кожи.
Соответствующие изобретению кератинсвязывающие полипептиды (i) используются преимущественно в косметических средствах для кожи. Они обеспечивают высокую концентрацию и длительное действие активных веществ для ухода за кожей и для защиты кожи.
Подходящие вспомогательные и дополнительные материалы для изготовления косметических препаратов для ухода за волосами, ногтями и кожей известны специалисту и могут быть взяты из справочников по косметике, например, Шрадер, «Основы и рецептура косметики», издательство Huthig Verlag, Хайдельберг, 1989 (Schrader, Grundlagen und Rezepturen der Kosmetika, Huthig Verlag, Heidelberg, 1989, ISBN 3-7785-1491-1).
В случае соответствующих изобретению косметических средств речь может идти о косметических средствах для ухода за кожей, ногтями и волосами, дерматологических, гигиенических или фармацевтических средствах.
Соответствующие изобретению средства могут быть изготовлены в форме геля, пены, спрея, мази, крема, эмульсии, суспензии, лосьона, молочка или пасты. При желании могут быть использованы также липосомы или микросферы.
Соответствующие изобретению косметически или фармацевтически активные средства дополнительно могут содержать косметически и/или дерматологически активные вещества, а также вспомогательные вещества.
Соответствующие изобретению косметические средства содержат преимущественно по меньшей мере одну определенную выше кератинсвязывающую последовательность (i) и по меньшей мере одну отличную от нее составляющую, выбранную среди косметически активных веществ, эмульгаторов, поверхностно-активных веществ, консервирующих средств, парфюмерных масел, сгустителей, полимеров для волос, кондиционеров для волос и кожи, привитых сополимеров, водорастворимых или диспергируемых силиконсодержащих полимеров, светозащитных средств, отбеливателей, гелеобразователей, средств для ухода, красящих средств, тональных средств, средств для загара, красителей, пигментов, средств для придания консистентности, влагоудерживающих средств, восстановителей жирности, коллагенов, гидролизатов белка, липидов, антиоксидантов, противовспенивателей, антистатиков, умягчителей и размягчителей. Кератинсвязывающие полипептидные активные вещества могут также содержаться в капсулированной форме в косметических препаратах.
Антиоксиданты выбирают предпочтительно из группы, содержащей аминокислоты (например, глицин, гистидин, тирозин, триптофан) и их производные, имидазолы (например, урокаминовую кислоту) и их производны, пептиды, такие как D,L-карнозин, D-карнозин, L-карнозин и их производные (например, ансерин), каротиноиды, каротины (например, β-каротин, ликопин) и их производные, хлорогенная кислота и ее производные, липоновая кислота и ее производные (например, дигидролипоновая кислота), ауротиоглюкоза, пропилтиоурацил и другие тиолы (например, тиородоксин, глютатион, цистеин, цистин, цистамин и их гликозиловые, N-ацетиловые, метиловые, этиловые, пропиловые, амиловые, бутиловые, и лауриловые, пальмитоиловые, олеиловые, γ-линолеиловые, холестериловые и глицериловые эстеры), а также их соли, дилаурилтиодипропионат, дистеарилтиодипропионат, тиодипропионовая кислота и ее производные (сложные эфиры, простые эфиры, пептиды, липиды, нуклеотиды, нуклеозиды и соли), а также сульфоксиминовые соединения (например, бутионинсульфоксимины, гомоцистеинсульфоксимины, бутионинсульфоны пента-, гекса-, гептатионинсульфоксимин) в очень малых дозировках (например, от пикомоль до микромоль на килограмм), кроме того (металл)-хелаторы (например, α-гидроксижирные кислоты, пальмитиновая кислота, фитиновая кислота, лактофиеррин), α-гидроксильные кислоты (например, лимонная кислота, молочная кислота, яблочная кислота), гуминовая кислота, желчная кислота, экстракты желчи, билирубин, биливердин, этилендиаминтетрауксусная кислота (EDTA) и ее производные, ненасыщенные жирные кислоты и их производные (например, γ-линоленовая кислота, линолевая кислота, масляная кислота), фолиевая кислота и ее производные, убихинон и убихинол и их производные, витамин С и его производные (например, аскорбат натрия, аскорбилпальмитат, магний-аскорбилфосфат, аскорбилацетат), токоферол и производные (например, ацетат витамина Е, токотриенол), витамин А и производные (пальмитат витамина А), а также кониферилбензоат бензойной смолы, рутиновая кислота и ее производные, α-гликозилрутин, феруловая кислота, фурфурилиденглюцитол, карнозин, бутилгидрокситолуол, бутилгидроксианизол, кислота нордигидрогваяковой смолы, тригидроксибутирофенон, мочевая кислота и ее производные, манноза и ее производные, цинк и его производные (например, ZnO, ZnSO4), селен и его производные (например, селенметионин), стильбен и его производные (например, оксид стильбена, трансоксид стильбена).
Обычными сгустителями в таких композициях являются сетчатые полиакриловые кислоты и их производные, полисахариды и их производные, такие как ксантановая смола, агар-агар, альгинаты или тилозы, производные целлюлозы, например карбоксиметилцеллюлоза или гидроксикарбоксиметилцеллюлоза, жирные спирты, моноглицериды и жирные кислоты, поливиниловый спирт и поливинилпирролидон. Предпочтение отдают неионным сгустителям.
Пригодными косметически и/или дерматологически активными веществами являются, например, красящие вещества, пигментные вещества для кожи и волос, тональные средства, средства для загара, отбеливатели, отвердители кератина, светофильтрующие вещества, репелленты, гиперемически действующие вещества, кератолитически и кератопластически действующие вещества, вещества против перхоти, противовоспалительные вещества, кератинизирующе действующие вещества, антиоксиданты или ловушки радикалов, увлажнители кожи или удержатели влаги, восстановители жирности, анатиэритематозные или противоаллергические вещества, разветвленные жирные кислоты, такие как 18-метилэйкозановая кислота, и их смеси.
Веществами для искусственного загара, пригодными для придания коже коричневого цвета без применения природного или искусственного облучения ультрафиолетовыми (УФ) лучами, являются, например, дигидроксиацетон, алло-ксан и экстракт скорлупы грецкого ореха. Пригодными кератинотверждающими веществами являются, как правило, вещества, используемые также в средствах против пота, такие как калий-алюминий-сульфат, гидроксихлорид алюминия, лактат алюминия и т.п.
Антимикробные биологически действующие вещества применяются для уничтожения или для сдерживания роста микроорганизмов и служат таким образом как в качестве консервантов, так и в качестве дезодорантов, которые ослабляют возникновение или интенсивность запаха тела. К ним принадлежат, например, обычные, известные специалисту консервирующие средства, такие как сложный эфир р-гидроксибензойной кислоты, имидазолидинил-карбамид, формальдегид, сорбиновая кислота, бензойная кислота, салициловая кислота и т.п. Такими дезодорирующими веществами являются, например, цинкрицинолеат, триклозан, алкилоламид ундециленовой кислоты, сложный 2-триэтиловый эфир лимонной кислоты, хлоргексидин и т.д.
Согласно изобретению в качестве консервирующих средств следует применять вещества, указанные ниже вместе с их Е-номером:
Кроме того, согласно изобретению пригодны используемые в косметике консервирующие средства или консервирующие вспомогательные вещества: дибромдицианобутан (2-бром-2-бромметилглютародинитрил), 3-иод-2-пропинилбутилкарбамат, 2-бром-2-нитропропан-1,3-диол, имидазолидинилкарбамид, 5-хлор-2-метил-4-изотиазолин-3-он, 2-хлорацетамид, хлорид бензалкония, бензиловый спирт + отщепитель формальдегида.
Кроме того, в качестве консервирующих средств пригодны простые фенилгидроксиалкиловые эфиры, в частности соединение, известное под названием феноксиэтанол, благодаря его бактерицидному и фунгицидному действию на ряд микроорганизмов.
Пригодны также другие ингибиторы роста бактерий, в которые могут быть введены соответствующие изобретению препараты. Предпочтительными веществами являются, например: простой 2,4,4'-трихлор-2'-гидроксидифениловый эфир (иргазан), 1,6-ди-(4-хлорфенилбигуанидо)-гексан (хлоргексидин), 3,4,4'- трихлоркарбанилид, четвертичные соединения аммония, гвоздичное масло, мятное масло, тимьяновое масло, триэтилцитрат, фарнезол (3,7,11-триметил-2,6,10-додекатриен-1-он), а также активные вещества и комбинации активных веществ, описанные в выложенных описаниях изобретений к заявкам DE-37 40 186, DE-39 38 140, DE-42 04 321, DE-42 29 707, DE-43 09 372, DE-44 11 664, DE-195 41 967, DE-195 43 695, DE-195 43 696, DE-195 47 160, DE-196 02 108, DE-196 02 110, DE-196 02 111, DE-196 31 003, DE-196 31 004 и DE-196 34 019 и в описаниях изобретений к патентам DE-42 29 737, DE-42 37 081, DE-43 24 219, DE-44 29 467, DE-44 23 410 и DE-195 16 705. Целесообразно также использование гидрокарбоната натрия. Могут быть использованы также антимикробные полипептиды.
Пригодными светофильтрующими веществами являются вещества, способные абсорбировать ультрафиолетовые лучи в диапазоне В и/или А. Пригодными ультрафиолетовыми фильтрами являются, например, 2,4,6-триарил-1,3,5-триазины, в которых арильные группы могут содержать по меньшей мере один заместитель, выбранный предпочтительно среди гидроксильной, алкоксильной, особенно метоксильной, алкоксикарбонильной, особенно метоксикарбонильной и этоксикарбонильной групп и их смесей. Кроме того, пригодны сложные эфиры р-аминобензойной кислоты, эфиры коричной кислоты, бензофеноны, производные камфары, а также пигменты, задерживающие ультрафиолетовые лучи, такие как диоксид титана, тальк и оксид цинка.
В качестве веществ, фильтрующих ультрафиолетовое излучение, могут быть использованы любые УФ-А- и УФ-В-фильтрующие вещества. Примерами таких веществ являются:
Сложный 1-глицериловый эфир 4-аминобензойной кислоты
Кроме того, соответствующие изобретению косметические и дерматологические препараты могут содержать задерживающие ультрафиолетовое излучение неорганические пигменты на основе оксидов металлов и/или других труднорастворимых или нерастворимых в воде соединений металлов, выбранных из группы, включающей: оксиды цинка (ZnO), титана (TiO2), железа (например, Fe2O3), циркония (ZrO2), кремния (SiO2), марганца (например, MnO), алюминия (Al2O3), церия (например, Се2О3), смешанные оксиды соответствующих металлов, а также смеси таких оксидов.
При этом неорганические пигменты могут иметь покрытие, то есть могут быть подвергнуты поверхностной обработке. Эта поверхностная обработка может состоять в том, что на пигменты известным способом, например, описанным в DE-A-33 14 742, наносят тонкий гидрофобный слой.
Пригодными репеллентами являются соединения, которые в состоянии удерживать на расстоянии от человека или отгонять определенных животных, в частности насекомых. К ним относятся, например, 2-этил-1-3-гексанол, N,N-диэтил-m-толуамид и т.п.
Пригодными гиперемически действующими веществами, стимулирующими кровоснабжение кожи, являются, например, эфирные масла, такие как экстракт горной сосны, экстракт лаванды, экстракт розмарина, экстракт можжевельника, экстракт конского каштана, экстракт березовых листьев, экстракт лекарственных трав, этилацетат, камфара, ментол, мятное масло, экстракт розмарина, масло эвкалипта и т.д.
Пригодными кератолитически и кератопластически действующими веществами являются, например, салициловая кислота, тиогликолат кальция, тиогликолевая кислота и ее соли, сера и т.д.
Пригодными средствами против перхоти являются, например, сера, серополиэтиленгликольсорбитанмоноолеат, серорицинолполиэтоксилат, цинкпиритион, алюминий-пиритион и т.д.
Пригодными противовоспалительными средствами, противодействующими раздражению кожи, являются, например, аллантоин, бисаболол, драгосантол, экстракт ромашки, пантенол и т.д.
Соответствующие изобретению косметические средства в качестве косметического и/или фармацевтического активного вещества (а также в зависимости от обстоятельств - в качестве вспомогательного вещества) могут содержать по меньшей мере один косметически или фармацевтически приемлемый полимер, отличающийся от полимеров, образующих соответствующий изобретению полиэлектролитный комплекс. К ним относятся целиком катионные, амфотерные и нейтральные полимеры.
Пригодными полимерами являются, например, катионные полимеры, имеющие название Polyquaternium согласно Международной номенклатуре косметических ингредиентов (International Nomenclature of Cosmetic Ingredients=INCI), например сополимеры винилпирролидон/солей N-винилимидазола (Luviquat FC, Luviquat HM, Luviquat MS, Luviquat&commat, Care) сополимеры N-винилпирролидон/диметиламиноэтилметакрилат, кватернизированный диэтилсульфатом (Luviquat PQ 11), сополимеры N-винилкапролактама/N-винилпирролидона/солей N-винилимидазола (Luviquat E Hold), катионные производные целлюлозы (Polyquaternium-4 и -10), акриламидные сополимеры (Polyquaternium-7) и хитозан.
Пригодными катионными (кватернизированными) полимерами являются также Merquat (полимер на основе хлорида диметилдиаллиламмония), Gafquat (четвертичные полимеры, получаемые путем реакции поливинилпирролидона с четвертичными соединениями аммония), полимер JR (гидроксиэтилцеллюлоза с катионными группами) и катионные полимеры на растительной основе, например гуаровые полимеры, такие как полимеры марки Jaguar фирмы Rhodia.
Следующими пригодными полимерами являются также нейтральные полимеры, такие как поливинилпирролидоны, сополимеры N-вилинпирролидона и винилацетата и/или винилпропионата, полисилоксаны, поливинилкапролактам и другие сополимеры с N-винилпирролидон, полиэтиленимины и их соли, поливиниламины и их соли, производные целлюлозы, соли полиаспаргиновой кислоты и производные. К ним относятся, например Luviflex 0 Swing (частично омыленный сополимеризат поливинилацетата и полиэтиленгликоля, фирма BASF).
Пригодными полимерами являются также неионные, водорастворимые или вододиспергируемые полимеры или олигомеры, такие как поливинилкапролактам, например Luviskol 0 Plus (BASF), или поливинилпирролидон и его сополимеры, в частности со сложными виниловыми эфирами, такими как винилацетат, например Luviskol 0 VA 37 (BASF), полиамиды, например, на основе итаконовой кислоты и алифатических диаминов, например, описанные в DE-A-43 33 238.
Пригодными полимерами являются также амфотерные или цвиттер-ионные полимеры, такие как получаемые под названием амфомер (National Starch) сополимеры октилакриламид/метилметакрилат/трет-бутиламиноэтилметакрилат-гидроксипропилметакрилат, а также цвиттер-ионные полимеры, такие как описанные в немецких патентных заявках DE 39 29 973, DE 21 50 557, DE 28 17 369 и DE 3708 451. Сополимеризаты хлорида акриламидопропилтриметиламмония/акриловой или метакриловой кислоты и их щелочные и аммониевые соли являются предпочтительными цвиттер-ионными полимерами. Кроме того, пригодными цвиттер-ионными полимерами являются сополимеры метакроилэтилбентаин/метакрилат, имеющиеся в продаже под названием амерсет {AMERCHOL), и сополимеры из гидро-ксиэтилметакрилата, метилметакрилата, N,N-диметиламиноэтилметакрилата и акриловой кислоты (Jordapon (D)).
Пригодными полимерами являются также неионные, силоксансодержащие, водорастворимые или вододиспергируемые полимеры, например полиэфирсилоксаны, такие как Tegopren 0 (фирма Goldschmidt) или Besi&commat (фирма Wacker). Основа соответствующих изобретению фармацевтических средств содержит предпочтительно фармацевтически приемлемые вспомогательные материалы. Фармацевтически приемлемыми являются обычно используемые в пищевой промышленности и прилегающих к ней отраслях вспомогательные вещества, в частности вещества, внесенные в фармацевтические книги (например, DAB Ph. Eur. BP NF), а также другие вспомогательные вещества, свойства которых не препятствуют физиологическому применению.
Пригодными вспомогательными веществами могут быть: смазывающие средства, смачивающие средства, эмульгирующие и суспендирующие средства, консервирующие средства, антиоксиданты, противораздражающие средства, хелатирующие агенты, стабилизаторы эмульсии, пленкообразующие средства, гелеобразующие средства, средства, маскирующие запах, смолы, гидроколлоиды, растворители, агенты растворения, нейтрализирующие средства, ускорители проникновения, пигменты, четвертичные соединения аммония, восстановители жирности и пережиривающие средства, основные вещества мазей, кремов и масел, производные силикона, стабилизаторы, стерилизаторы, разрыхлители, осушители, омутнители, загустители, воски, умягчители, белое масло. Соответствующая форма является предметом профессионального знания, изложенного, например, в книге Фидлера Х.П. «Лексикон вспомогательных средств для фармакологии, косметики и граничащих отраслей», 4-е издание, издательство Aulendorf: ECV-Editio-Kantor, 1996 (Fiedler, H.P. Lexikon der Hilfsstoffe fur Pharmazie, Kosmetik und angrenzende Gebiete, 4. Aufl., Aulendorf: ECV-Editio-Kantor-Verlag, 1996).
Для изготовления соответствующих изобретению дерматологических средств активные вещества могут быть смешаны с пригодными вспомогательными средствами (наполнителями) или разведены ними. Наполнители могут быть твердыми, полутвердыми или жидкими материалами, которые могут служить в качестве лекарственной основы, носителя или среды для активных веществ. Примешивание других вспомогательных веществ осуществляют при желании известным специалисту образом. Кроме того, в фармации в качестве вспомогательных веществ пригодны полимеры и дисперсии, преимущественно в качестве материалов покрытия или вяжущих веществ для твердых лекарственных форм. Они могут быть использованы также в кремах и в качестве покрытий таблеток и вяжущих веществ для таблеток.
В предпочтительной форме осуществления изобретения соответствующие изобретению средства являются средствами для очистки кожи.
Предпочтительными средствами для очистки кожи являются мыла в консистенции от жидкой до гелеобразной, такие как прозрачные мыло, мыло класса «люкс», мыло-дезодорант, крем-мыло, детское мыло, мыло для защиты кожи, абразивное мыло и синдеты (Syndet), пастоподобное мыло, жидкое мыло и паста для мытья, мыло против шелушения, увлажнительные салфетки, жидкие препараты для мытья, душа и ванны, такие как моющие лосьоны, растворы и гели для душа, пена для ванны, масляные ванны и препараты для чистки, пены, лосьоны и кремы для бритья.
Согласно другой предпочтительной форме осуществления соответствующие изобретению средства являются косметическими средствами для ухода и защиты кожи и волос, средства для ухода за ногтями или препараты для декоративной косметики.
Пригодными косметическими средствами для кожи являются, например, туалетная вода для лица, дезодоранты и другие косметические лосьоны. Средства для использования в декоративной косметике включают карандаши, театральные краски, тени для век, помады, каяловый карандаш, карандаши для подведения глаз, румяна, пудры и карандаши для бровей.
Кроме того, полипептидные последовательности (i) могут быть использованы в полосках для очистки пор, в средствах против угрей, репеллентах, средствах для бритья, средствах для ухода за кожей до и после бритья, средства для ухода за кожей после солнечных процедур, средствах для удаления волос, средствах для окраски волос, средствах для интимного ухода, средствах для ухода за ногами, а также средствах для ухода за детьми.
Соответствующими изобретению средствами для ухода за кожей являются, в частности, кремы для кожи на основании эмульсий «вода-в-масле» или «масло-в-воде», дневные и ночные кремы, кремы для глаз, кремы для лица, кремы против морщин, солнцезащитные кремы, влагоудерживающие кремы, осветляющие кремы, кремы для загара, витаминные кремы, лосьоны для кожи, лосьоны для ухода за кожей и влагоудерживающие лосьоны.
Косметические и дерматологические средства на основе указанных выше полиэлектролитных комплексов проявили хорошее действие. Полимеры могут, кроме прочего, содействовать удержанию влаги и кондиционированию кожи и улучшению кожной чувствительности. Полимеры могут действовать в препаративных формах в качестве сгустителей. Путем добавления соответствующих изобретению полимеров к определенным препаративным формам может быть достигнуто существенное улучшение переносимости препарата кожей.
Косметические и дерматологические средства содержат по меньшей мере одну полипептидную последовательность (i) в количестве от 0,001 до 30 мас.%, предпочтительно от 0,01 до 20 мас.%, особенно предпочтительно от 0,1 до 12 мас.% относительно общей массы средства.
Светозащитные средства на основе полипептидных последовательностей (i) обладают свойством увеличения времени действия составляющих, абсорбирующих ультрафиолетовое излучение, по сравнению с обычными вспомогательными средствами.
В зависимости от области применения соответствующие изобретению средства могут быть изготовлены в пригодной для ухода за кожей форме, такой, например, как крем, пена, гель, карандаш, мусс, молочко, спрей (с насосом или с пропеллентом) или лосьон.
Косметические препараты для кожи наряду с полипептидными последовательностями (i) и пригодными наполнителями могут содержать также и другие принятые в косметике для кожи активные вещества и вспомогательные материалы, описанные выше. К ним относятся предпочтительно эмульгаторы, консерванты, косметические масла, косметические активные вещества, такие как фитантриол, витамины А, Е и С, ретинол, бисаболол, пантенол, светозащитные средства, отбеливающие агенты, красители, тональные вещества, средства для загара, коллагены, гидролизаты белка, стабилизаторы, регуляторы значения рН, соли, сгустители, гелеобразователи, средства для придания консистентности, силиконы, увлажнители, восстановители жирности и другие обычные добавки.
Предпочтительными масляными и консистентными компонентами косметических и дерматологических средств являются названные выше минеральные и синтетические масла, такие как парафины, силиконовые масла и алифатические углеводородные соединения с количеством атомов углерода более 8, животные и растительные масла, такие как подсолнечное масло, кокосовое масло, масло авокадо, оливковое масло, ланолин, или воски, жирные кислоты, сложные эфиры жирных кислот, вазелины, гидрированный ланолин и ацетилированный ланолин, а также их смеси.
Соответствующие изобретению полипептидные последовательности (i) могут быть также смешаны с обычными полимерами с целью получения специальных свойств.
Для установления определенных свойств, таких как улучшение ощущения на ощупь, растекаемости, водостойкости и/или связывания активных и вспомогательных веществ, таких как пигменты, косметические и дерматологические препараты дополнительно могут содержать также кондиционирующие вещества на основе силиконовых соединений.
Пригодными силиконовыми соединениями являются, например, полиалкилсилоксаны, полиарилсилоксаны, полиарилалкилсилоксаны, полиэфирсилоксаны или силиконовые смолы.
Изготовление косметических и дерматологических препаратов осуществляют обычными, известными специалисту методами.
Косметические и дерматологические средства имею предпочтительно форму эмульсий, в частности эмульсий «вода-в-масле» или «масло-в-воде».
Однако могут быть выбраны также иные препаративные формы, например гели, масла, масляные гели, сложные эмульсии, например в форме эмульсий «вода-в-масле» или «масло-в-воде», безводные мази или основы мазей и т.д. Выгодными формами осуществления являются также безэмульгаторные препаративные формы, такие как гидродисперсии, гидрогели или эмульсии Пиккеринга (Pickering).
Изготовление эмульсий осуществляют известными методами. Эмульсии наряду с по меньшей мере одной полипептидной последовательностью (i) содержат, как правило, обычные составляющие, такие как жирные спирты, сложные эфиры жирных спиртов и особенно триглицериды жирных спиртов, жирные кислоты, ланолин и их производные, природные и синтетические масла или воски и эмульгаторы в присутствии воды. Выбор добавок, специфических для данного типа эмульсии, и изготовление эмульсий описаны, например, в книге Шрадера «Основы и рецептура косметики», издательство Huthig Buch Verlag, Хайдельберг, 2-издание, 1989, третья часть (Schrader, Grundlagen und Rezepturen der Kosmetika, Huthig Buch Verlag, Heidelberg, 1989), на которую этим упоминанием дается ссылка.
Пригодная эмульсия в форме «вода-в-масле», например для крема для кожи, содержит в общем случае водную фазу, которая с помощью пригодной эмульгаторной системы переведена в масляную или консистентную фазу. Для приготовления водной фазы может быть использован полиэлектролитный комплекс. Предпочтительными консистентными компонентами, которые могут содержаться в консистентной фазе эмульсий, являются: углеводородные масла, такие как парафиновое масло, пурцеллиновое масло, пергидросквален и растворы микрокристаллических восков в этих маслах; животные или растительные масла, такие как миндальное масло, масло авокадо, калофиловое масло, ланолин и их производные, рициновое масло, кунжутное масло, оливковое масло, масло жожоба, масло семян «масляного дерева», масло хоплостетуса, минеральные масла, дистилляция которых начинается при атмосферном давлении при температуре около 250°С, а температура дистилляции составляет около 400°С, такие как вазелиновое масло, сложные эфиры насыщенных и ненасыщенных жирных кислот, такие как алкилмиристаты, например, i-пропил-, бутил- или цетилмиристат, гексадецилстеарат, этил- или пропилпальмитат, триглицериды октановой или декановой кислоты и цетилрицинолеат.
Консистентная фаза может содержать также растворимые в других маслах силиконовые масла, такие какдиметилполисилоксан, метилфенилполисилоксан и силиконгликолевый сополимер, жирные кислоты и жирные спирты.
Наряду с полипептидными последовательностями (i) могут быть использованы также воски, такие как карнаубский воск, воск кандилилы, пчелиный воск, микрокристаллический воск, озокеритовый воск, и олеаты, миристаты, линолеаты и стеараты кальция, магния и алюминия.
Кроме того, соответствующая изобретению эмульсия может быть изготовлена в форме «масло-в-воде». Такая эмульсия содержит обычно масляную фазу, емульгаторы, стабилизирующие масляную фазу в водной фазе, и водную фазу, обычно в концентрированном виде. В качестве эмульгаторов используют предпочтительно эмульгаторы «масло-в-воде», такие как сложный полиглицериновый эфир, сложный сорбитановый эфир или частично этерифицированные глицериды.
Согласно следующей предпочтительной форме осуществления соответствующие изобретению средства являются гелем для душа, шампунем или препаратом для ванны.
Такие препаративные формы содержат по меньшей мере одну полипептидную последовательность (i), а также обычно анионные основные поверхностно-активные вещества и амфотерные и/или неионные дополнительные поверхностно-активные вещества. Другими пригодными активными и/или вспомогательными веществами являются в общем случае липиды, парфюмерные масла, красители, органические кислоты, консерванты и антиоксиданты, а также сгустители/гелеобразователи, средства для кондиционирования и увлажнения кожи.
Эти препаративные формы содержат предпочтительно от 2 до 50 мас.%, преимущественно от 5 до 40 мас.%, особенно преимущественно от 8 до 30 мас.% поверхностно-активных веществ относительно общей массы препаративной формы.
В препаратах для мытья, душа и ванны могут быть использованы все анионные, нейтральные, амфотерные или катионные поверхностно-активные вещества, обычные для средств для очистки тела.
Пригодными анионными поверхностно-активными веществами являются, например, алкилсульфаты, алкилэтерсульфаты, алкилсульфонаты, алкиларилсульфонаты, алкилсукцинаты, алкилсульфосукцинаты, N-алкоилсаркозинаты, ацилтаураты, ацилизотионаты, алкилфосфаты, алкилэтерфосфаты, алкилэтеркарбоксилаты, альфа-олефинсульфонаты, в частности соли щелочных и щелочно-земельных металлов, таких как натрий, калий, магний, кальций, а также аммониевые и триэтаноламиновые соли. Алкилэтерсульфаты, алкилэтерфосфаты и алкилэтеркарбоксилаты могут содержать от 1 до 10 этиленоксидных или пропиленоксидных единиц, предпочтительно от 1 до 3 этиленоксидных единиц в молекуле.
К ним относятся, например, лаурилсульфат натрия, лаурилсульфат аммония, лаурилэтерсульфат натрия, лаурилэтерсульфат аммония, лаурилсаркозинат натрия, олеилсукцинат натрия, лаурилсульфосукцинат аммония, додецилбензолсульфонат натрия, триэтаноламиндодецилбензолсульфонат.
Пригодными амфотерными поверхностно-активными веществами являются, например, алкилбетаины, алкиламидопропилбетаины, алкилсульфобетаины, алкилглицинаты, алкилкарбоксиглицинаты, алкиламфоацетаты или -пропионаты, алкиламфодиацетаты или -дипропионаты.
Могут быть использованы, например, кокодиметилсульфопропилбетаин, лаурилбетаин, кокамидпропилбетаин или кокамфопропионат натрия.
В качестве поверхностно-активных веществ пригодны продукты реакции алифатических спиртов или алкилфенолов, имеющих 6-20 атомов углерода в алкильной цепи, которые могут быть линейными или разветвленными, с этиленоксидом и/или пропиленоксидом. Количество алкиленоксида составляет от 6 до 60 моль на один моль спирта. Кроме того, пригодны алкиламиноксиды, моно- или диалкилалканоламиды, сложные эфиры жирных кислот полиэтиленгликолей, этоксилированные амиды жирных кислот, алкилполигликозиды или сорбитанэтерэфиры.
Кроме того, препараты для мытья, душа или ванной могут содержать обычные катионные поверхностно-активные вещества, такие как четвертичные соединения аммония, например хлорид цетилтриметиламмония.
Кроме того, душ-гели/шампуни могут содержать сгустители, такие как поваренная соль, PEG-55, пропиленгликоль-олеат, диолеат PEG-120-метилглюмозы и другие, а также консерванты, другие активные и вспомогательные вещества и воду.
Согласно другой предпочтительной форме осуществления соответствующие изобретению средства являются средствами для ухода за волосами.
Соответствующие изобретению средства для ухода за волосами содержат по меньшей мере одну полипептидную последовательность (i) в количестве от 0,01 до 30 мас.%, предпочтительно от 0,5 до 20 мас.% относительно общей массы средства.
Соответствующие изобретению средства для ухода за волосами могут быть изготовлены в форме уплотнителя пены, мусса, геля, шампуни, спрея, пены, выравнивателя для длительной завивки, красителя и отбеливателя или "Hot-Oil-Treatments". В зависимости от области применения косметические препараты для волос могут применяться в виде (аэрозольного) спрея, (аэрозольной) пены, геля, гель/спрея, крема, лосьона или воска. При этом спреи для волос включают как аэрозольные спреи, так и насосные спреи без пропеллента. Пены для волос включают как аэрозольные пены, так и насосные пены без пропеллента. Спреи и пены для волос включают преимущественно или исключительно водорастворимые или вододиспергируемые компоненты. Если соединения, используемые в соответствующих изобретению спреях и пенах для волос, вододиспергируемы, они могут быть применены в форме водных микродисперсий с диаметрами частичек от 1 до 350 нм, предпочтительно от 1 до 250 нм. При этом содержание твердых веществ в этих препаратах лежит в диапазоне от 0,5 до 20 мас.%. Эти микродисперсии, как правило, не нуждаются в эмульгаторах для их стабилизации.
Соответствующие изобретению косметические препаративные формы для волос в предпочтительной форме осуществления содержат
а) от 0,01 до 30 мас.% по меньшей мере одной полипептидной последовательности (i),
b) от 20 до 99,95 мас.% воды и/или спирта,
c) от 0 до 50 мас.% по меньшей мере одного пропеллента,
d) от 0 до 5 мас.% по меньшей мере одного эмульгатора,
е) от 0 до 3 мас.% по меньшей мере одного сгустителя,
а также до 25 мас.% других составляющих.
Под спиртом следует понимать все обычные в косметике спирты, например, этанол, изопропанол, n-пропанол.
Под другими составляющими следует понимать обычные в косметике добавки, например наполнители, противовспениватели, поверхностно-активные соединения, эмульгаторы, пенообразователи и солюбилизаторы. Используемые поверхностно-активные вещества могут быть анионными, катионными, амфотерными или нейтральными. Кроме того, другими обычными составляющими могут быть консерванты, парфюмерные масла, помутнители, активные вещества, ультрафиолетовые фильтры, вещества для ухода, такие как пантенол, коллаген, витамины, гидролизаты белка, альфа- и бета-гидроксикарбоновые кислоты, стабилизаторы, регуляторы значения рН, красители, регуляторы вязкости, гелеобразователи, соли, средства для удерживания влаги, восстановители жирности, комплексообразователи и другие обычные добавки.
Кроме того, к ним причисляются все известные в косметике модельные и кондиционирующие полимеры, которые в случае необходимости получения совершенно специальных свойств могут быть использованы в комбинации с соответствующими изобретению полипептидными последовательностями (i).
В качестве обычных полимеров для косметики для волос пригодны все названные выше катионные, анионные, нейтральные, неионные и амфотерные полимеры, на которые здесь дается ссылка.
Для установления определенных свойств препараты дополнительно могут содержать также кондиционирующие вещества на основе силиконовых соединений. Пригодными силиконовыми соединениями являются, например, полиалкилсилоксаны, полиарилсилоксаны, полиарилалкилсилоксаны, полиэтерсилоксаны, силиконовые смолы или диметикон сополиолы (CTFA) и аминофункциональные силиконовые соединения, такие как амодиметиконы (CTFA).
Соответствующие изобретению полимеризаты особенно пригодны в качестве материалов для изготовления препаратов для модельного оформления волос, в частности спреев для волос (аэрозольные спреи и насосные спреи без пропеллента) и пен для волос (аэрозольные пены и насосные пены без пропеллента).
В предпочтительной форме исполнения спрейные препараты содержат:
a) от 0,01 до 30 мас.% по меньшей мере одной полипептидной последовательности (i),
b) от 20 до 99,9 мас.% воды и/или спирта,
c) от 0 до 70 мас.% по меньшей мере одного пропеллента,
d) от 0 до 20 мас.% других составляющих.
В качестве пропеллента используют преимущественно обычные для спреев или пен для волос смеси: пропан/бутан, пентан, диметилэтер, 1,1-дифторэтан (HFC-152 а), двуокись углерода, азот или сжатый воздух.
Соответствующая изобретению аэрозольная пена для волос содержит предпочтительно:
a) от 0,01 до 30 мас.% по меньшей мере одной полипептидной последовательности (i),
b) от 55 до 99,8 мас.% воды и/или спирта,
c) от 5 до 20 мас.% пропеллента,
d) от 0,1 до 5 мас.% эмульгатора,
e) от 0 до 10 мас.% других составляющих.
В качестве эмульгаторов могут быть использованы все обычные в пенах для волос эмульгаторы. Пригодные эмульгаторы могут быть неионными, катионными или анионными или амфотерными.
Примерами неионных эмульгаторов (номенклатура INCI) являются лауреты, например лаурет-4 (Laureth-4); цететы, например цетет-1 (Cetheth-1); простой цетиловый эфир полиэтиленгликоля, цетеареты, например, цетеарет-25 (Cetheareth-25), глицериды полигликольжирных кислот, гидроксилированный лецитин, лактиловые сложные эфиры жирных кислот, алкилполигликозиды.
Примерами катионных эмульгаторов являются гидрофосфат цетилдиметил-2-гидроксиэтиламмония, хлорид цетилтриммония, бромид цетилтриммония, метилсульфат кокотриммония, Quaternium-1-x (INCI).
Анионные эмульгаторы могут быть выбраны из группы, включающей алкилсульфаты, алкилэтерсульфаты, алкилсульфонаты, алкиларилсульфонаты, алкилсукцинаты, алкилсульфосукцинаты, N-алкоилсаркозинаты, ацилтаураты, ацилизетионаты, алкилфосфаты, алкилэтерфосфаты, алкилетеркарбоксилаты, альфа-олефинсульфонаты, в частности соли щелочных и щелочноземельных металлов, например натрия, калия, магния, кальция, а также аммониевые и триэтаноаминовые соли. Алкилэтерсульфаты, алкилэтерфосфаты и алкилетеркарбоксилаты могут иметь в молекуле от 1 до 10 этиленоксидных или пропиленоксидных единиц, предпочтительно от 1 до 3 этиленоксидных единиц.
Препарат, в соответствии с изобретением пригодный для изготовления модельного геля, может иметь такой состав:
a) 0,01-30 мас.% по меньшей мере одной полипептидной последовательности (i),
b) 80-99,85 мас.% воды и/или спирта,
c) 0-3 мас.%, предпочтительно 0,05-2 мас.%, гелеобразователя,
d) 0-20 мас.% других составляющих.
В общем случае соответствующие изобретению полипептидные последовательности (i) являются «самосгущающимися», поэтому во многих случаях при изготовлении гелей можно отказаться от использования гелеобразователей. Однако их использование может быть целесообразным для придания гелям специальных реологических или других прикладных свойств. В качестве гелеобразователей могут быть использованы все обычные для косметики гелеобразователи. К ним относятся легко сшиваемые полиакриловые кислоты, например карбомер (INCI), производные целлюлозы, например гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза, катионно модифицированная целлюлоза, полисахариды, например ксантановая смола, каприл/каприн-триглицерид, сополимеры акрилата натрия, Polyquaternium-32 (и) жидкий парафин (Paraffinum Liquidum (INCI)], сополимеры акрилата натрия (и) жидкий парафин (и) PPG-1 Trideceth-6, сополимеры хлорид акрила-мидопропилтримония/акриламид, простой аллиловый эфир Steareth-10, сополимеры акрилата, Polyquaternium-37 (и) жидкий парафин (и) PPG-1 Trideceth-6, Polyquaternium-37 (и) пропиленглигольдикапрат/дикаприлат (и) PPG-1 Trideceth-6, Polyquaternium-7, Polyquaternium-44.
Соответствующие изобретению полипептидные последовательности (i) могут быть использованы в косметических препаратах в качестве кондиционирующих средств.
Препарат, содержащий соответствующую изобретению полипептидную последовательность (i), может быть использован в шампунях в качестве укрепляющего или кондиционирующего средства. Предпочтительные составы шампуней содержат:
a) 0,01-30 мас.% по меньшей мере одной полипептидной последовательности (i),
b) 25-94,95 мас.% воды,
c) 5-50 мас.% поверхностно-активного вещества,
c) 0-5 мас.% другого кондиционирующего средства,
d) 0-10 мас.% других косметических составляющих.
В композициях шампуни могут быть использованы все обычно применяемые анионные, нейтральные, амфотерные или катионные поверхностно-активные вещества.
Пригодными поверхностно-активными веществами являются, например, алкилсульфаты, алкилэтерсульфаты, алкилсульфонаты, алкиларилсульфонаты, алкилсукцинаты, алкилсульфонсукцинаты, N-алкоилсаркозинаты, ацилтаураты, ацилизотионаты, алкилфосфаты, алкилэтерфосфаты, алкилэтеркарбоксилаты, альфа-олефинсульфонаты, в частности соли щелочных и щелочноземельных металлов, например натрия, калия, магния, кальция, а также аммониевые и триэтаноламиновые соли. Алкилэтерсульфаты, алкилэтерфосфаты и алкилетеркарбоксилаты могут иметь в молекуле от 1 до 10 этиленоксидных или пропиленоксидных единиц, предпочтительно от 1 до 3 этиленоксидных единиц.
Пригодными являются, например, лаурилсульфат натрия, лакрилсульфат аммония, лаурилэтерсульфат натрия, лаурилэтерсульфат аммония, лауроилсаркозинат натрия, олеилсукцинат натрия, лаурилсульфосукцинат аммония, додецилбензолсульфонат натрия, триэтаноламиндодецилбензолсульфонат.
Пригодными амфотерными поверхностно-активными веществами являются, например, алкилбетаины, алкиламидопропилбетаины, алкилсульфобетаины, алкилглицинаты, алкилкарбоксиглицинаты, алкиламфоацетаты или -пропионаты, алкиламфодиацетаты или -дипропионаты.
Например, могут быть использованы кокодиметилсульфопропилбетаин, лаурилбетаин, кокамидопропилбетаин или кокамфопропионат натрия.
В качестве неионных поверхностно-активных веществ пригодны, например, продукты реакции алифатических спиртов или алкилфенолов с 6-2- атомами углерода в алкильной цепи, которые могут быть линейными или разветвленными, с элитеноксидом и/или пропиленоксидом. Количество алкиленоксида составляет от 6 до 60 моль на один моль спирта. Кроме того, пригодными являются алкиламидоксиды, моно- или диалкилалканоламиды, сложные эфиры жирных кислот полиэтиленгликолей, алкилполигликозиды или сорбитанэтерэфиры.
Кроме того, композиции шампуней могут содержать обычные катионные поверхностно-активные вещества, такие как четвертичные аммониевые соединения, например хлорид цетилтриметиламмония.
Кроме того, в составе шампуней для достижения определенного эффекта могут быть использованы обычные кондиционирующие средства в комбинации с полипептидными последовательностями (i).
К ним относятся, например, указанные выше катионные полимеры с наименованием Polyquaternium согласно INCI, в частности сополимеры винилпирролидона/солей N-винилимидазола (Luviquat FC, Luviquat&commat, HM, Luviquat MS, Luviquat Care), сополимеры N-винилпирролидона/диметиламиноэтилметаклирата, кватернизированного диэтилсульфатом (Luviquat D PQ 11), сополимеры N-винилкапролактама/N-винилпирролидона/солей N-винилимидазола (Luviquat D Hold), катионные производные целлюлозы (Polyquaternium-4 и Polyquaternium-10), акриламидные сополимеры (Polyquaternium-7). Кроме того, могут быть использованы гидролизаты белка, а также кондиционирующие вещества на основе силиконовых соединений, например, полиалкилсилоксаны, полиарилсилоксаны, полиарилалкилсилоксаны, полиэтерсилоксаны или силиконовые смолы. Другими пригодными силиконовыми соединениями являются диметикон сополиол (Dimeticon Copolyole (CTFA)) и аминофункциональные силиконовые соединения, такие как амодиметиконы (CTFA). Кроме того, могут быть использованы катионные производные гуара, такие как хлорид гуаргидроксипропилтримония (INCI).
Следующим предметом изобретения являются эффекторные молекулы, состоящие из
(i) по меньшей мере одной полипептидной последовательности (i), обладающей связывающим сродством с кератином,
(ii) эффекторной молекулы, природным образом не связанной с полипептидной последовательностью (i).
Пригодные полипептидные последовательности (i) описаны выше.
Особенно предпочтительным исполнением являются кератинсвязывающие эффекторные молекулы, причем полипептидная последовательность (i) содержит по меньшей мере одну из следующих полипептидных последовательностей:
i) полипептидная последовательность (домен В),
ii) полипептидная последовательность (домен С),
iii) полипептидная последовательность, в которой по отношению к (а) изменено до 70% аминокислот,
iv) полипептидная последовательность, в которой по отношению к (b) изменено до 70% аминокислот,
с оговоркой, что последовательности (с) или (d) имеют связывание кератина, составляющее по меньшей мере 10% значения, которое имеют полипептидные последовательности (а) или (b), при измерении в тесте согласно примерам 9 или 10. Здесь под доменами В и С имеются в виду описанные выше кератинсвязывающие домены десмоплакина человека (SEQ ID NO:1). Под изменением аминокислот здесь имеются в виду замещение, инсерция и делеция или любая комбинация этих трех возможностей.
Используют преимущественно полипептидные последовательности (i), обладающие для желаемого организма высокоспецифическим сродством. В соответствии с этим для косметики для кожи используют предпочтительно полипептидные последовательности (i), имеющие особенно высокое сродство с кератином кожи человека. Для применения в косметике для волос предпочтительными являются полипептидные последовательности, имеющие особенно высокое сродство с кератином волос человека.
Для применений в области ухода за животными предпочтительными являются полипептидные последовательности, имеющие особенно высокое сродство с соответствующим кератином, например кератином собак или кератином кошек.
Однако в соответствующей изобретению эффекторной молекуле может быть использована более чем одна полипептидная последовательность, например последовательность (i), имеющая высокое связывающее сродство с кератином кожи человека, в сочетании с последовательностью (i), имеющей высокое сродство с кератином волос человека. Для достижения более высокого связывания могут быть последовательно соединены несколько копий одной и той же полипептидной последовательности (i).
Пригодные кератинсвязывающие полипептидные последовательности (i) известны. Кератинсвязывающие домены (далее: «КСД») содержат, например, десмоплакины и плектины. (Fontao L, Favre В, Riou S, Geerts D, Jaunin F, SauratJH, Green KJ, Sonnenberg A, Borradori L., Interaction of the bullous pemphigoid antigen 1 (BP230) and desmoplakin with intermediate filaments is mediated by distinct sequences within their COOH terminus., Mol Biol Cell. 2003 May; 14(5): 1978-92. Epub 2003 Jan 26; Hopkinson SB, Jones JC., The N terminus of the transmembrane protein BP180 interacts with the N-terminal domain of BP230, thereby mediating keratin cytoskeleton anchorage to the cell surface at the site of the hemidesmosome, Mol Biol Cell. 2000 Jan; 11(1):277-86).
Путем сравнения таких известных полипептидных последовательностей, например, с помощью такой компьютерной программы, как Vector NTI 8 (версия от 25 сентября 2002 года) фирмы InforMax Inc., такие зоны могут быть картированы и идентифицированы.
Другими пригодными полипептидными последовательностями (i) с хорошим связыванием с кератином человека являются зоны последовательностей, которые в сравнении имеют высокую гомологию или идентичность к последовательности и могут быть выделены как консенсусные последовательности кератинсвязывающих доменов.
Среди них особенно предпочтительными являются:
Домен В (КСД-В): полипептидная последовательность SEQ ID NO:1, положение 2193-2448
Домен В (КСД-В): полипептидная последовательность SEQ ID NO:1, положение 2209-2448
Домен С (КСД-С): полипептидная последовательность SEQ ID NO:1, положение 2606-2871
Домен С (КСД-С): полипептидная последовательность SEQ ID NO:1, положение 2616-2871
Домен С (КСД-С): полипептидная последовательность SEQ ID NO:1, положение 2616-2811
Домен С (КСД-С): полипептидная последовательность SEQ ID NO:1, положение 2606-2871
При желании достижения особенно высокого связывания полипептидных последовательностей (i) с кератином, не принадлежащим человеческому организму, в качестве пригодных фрагментов последовательностей выбирают предпочтительно последовательности из кератинсвязывающего белка, например десмоплакина или плектина, соответствующего организма.
На фиг.2 изображено сравнение кератинсвязывающих молекул.
Эффекторные молекулы (ii)
Под эффекторными молекулами (ii) ниже имеются в виду молекулы, имеющие определенное, предсказуемое действие.
Среди белковых эффекторных молекул предпочтительными являются ферменты и антитела.
Среди ферментов в качестве эффекторных молекул (ii) предпочтительными являются: оксидазы, пероксидазы, протеазы, глюконазы, мутаназы, тирозиназы, лактазы, металлсвязывающие ферменты, лактопероксидаза, лизозим, амилогилкозидаза, глюкозооксидаза, супероксиддизмутаза, фотолиаза, Т4 эндонуклеаза, каталаза, тиоредоксин, тиоредоксин-редуктаза.
Среди белковых, но не ферментно действующих, эффекторных молекул в качестве эффекторных молекул (ii) предпочтительными являются: антимикробные пептиды, шелковичные белки, гидрофобины, коллагены, каротеноидсвязывающие белки, белки, связывающие тяжелые металлы, белки, связывающие одоранты.
Пригодными в качестве белковых эффекторных молекул (ii) являются также гидролизаты белков растительного и животного происхождения, например гидролизаты белков морского происхождения или гидролизаты шелка.
Среди небелковых эффекторных молекул (ii) предпочтительными являются красители, например красители для пищевых продуктов, полуперманентные красители, реакционноспособные или окислительные красители. В случае окислительных красителей целесообразно одну компоненту в качестве эффекторной молекулы (ii) слить с кератинсвязывающей полипептидной последовательностью (i), а затем после связывания с волосами окислительно связать со второй компонентой красителя. Кроме того, в случае окислительных красителей предпочтительно соединение красительных компонентов осуществлять перед связыванием с полипептидной последовательностью (i).
Кроме того, реакционноспособные красители в качестве компоненты в качестве эффекторной молекулы (ii) могут быть соединены с кератинсвязывающей полипептидной последовательностью (i), а затем связаны с волосами. Кроме того, такие красители, которые в качестве эффекторных молекул (ii) с кератинсвязывающей полипептидной последовательностью (i) путем связывания соединены с ногтями или кожей, могут быть использованы в декоративной косметике.
В качестве красителей для соответствующих изобретению молекул пригодны все обычные красители для волос. Пригодные красители известны специалисту из справочников по косметике, например из книги Шрадера, «Основы и рецептура косметики», издательство Hüthig Verlag, Хайдельберг, 1989 (Schrader, Grundlagen und Rezepturen der Kosmetika, Hüthig Verlag, Heidelberg, 1989, ISBN 3-7785-1491-1).
Особенно предпочтительные красители указаны в приведенном ниже перечне. Регистрационный номер красителя (Colour Index Nummern (CIN)) можно взять из публикации Rowe Colour Index, 3. Auflage, Society of Dyers and Colourists, Bradford, England, 1971.
В качестве красителей для волос могут быть использованы также пищевые красители.
Указанные выше красители могут быть использованы также в качестве эффекторных молекул (ii) в связываемой с кожей или ногтями полипептидной последовательности (i) для окрашивания кожи или ногтей, например, при татуировании.
Соответствующие изобретению эффекторные молекулы (ii), соединенные с кератинсвязывающей полипептидной последовательностью (i), при необходимости могут быть снова легко отделены от кератина в коже, волосах или ногтях. Для этого может быть применено промывание кератином, вследствие чего эффекторные молекулы (ii), соединенные с кератинсвязывающей полипептидной последовательностью (i), вытесняются из имеющейся связи с кератином и насыщаются кератином из промывного средства. Альтернативно для вымывания может быть применено также промывное средство с высокой долей моющего средства (например, додецилсульфата натрия (SDS)).
Другими предпочтительными эффекторными молекулами (ii) являются жирные кислоты, в частности насыщенные жирные кислоты, имеющие алкильное разветвление, особенно предпочтительно разветвленные эйкозановые кислоты, такие как 19-метил-эйкозановая кислота.
Другими предпочтительными эффекторными молекулами (ii) являются каротиноиды. Под каротиноидами согласно изобретению следует понимать следующие соединения, а также их этеризированные или гликозилированные производные: β-каротин, ликопин, лютеин, астаксантин, зеаксантин, криптоксантин, цитранаксантин, кантаксантин, биксин, β-апо-4-каротинал, β-апо-8-каротинал, сложный эфир β-апо-8-каротиновой кислоты, нейроспорен, эхиненон, адонирубин, виолаксантин, торулен, торулародин, отдельно или в смеси. Предпочтительно используемыми каротиноидами являются β-каротин, ликопин, лютеин, астаксантин, зеаксантин, цитранаксантин, кантаксантин.
Другими предпочтительными эффекторными молекулами (ii) являются витамины, в частности витамин А, и их сложные эфиры.
Под ретиноидами в рамках настоящего изобретения понимаются витамин А спирт (ретинол) и его производные, такие как витамин А альдегид (ретинал), витамин А кислота (ретиновая кислота) и витамин А сложный эфир (например, ретинилацетат, ретилинпропионат и ретинилпальмитат). При этом термин ретиновая кислота охватывает как полностью транс-ретиновую кислоту, так и 13-цис-ретиновую кислоту. Термины ретинол и ретинал охватывают предпочтительно полностью транссоединения. В качестве предпочтительного ретиноида используют для соответствующих изобретению суспензий полностью транс-ретинол, в последующем называемый ретинолом.
Другими предпочтительными эффекторными молекулами (ii) являются витамины и провитамины из групп А, С, Е и F, в частности 3,4-дидегидроретинол, β-каротин (провитамин витамина А), аскорбиновая кислота (витамин С), а также сложные эфиры пальмитиновой кислоты, глюкозиды или фосфаты аскорбиновой кислоты, токоферолы, в частности α-токоферол, а также его сложные эфиры, например ацетат, никотинат, фосфат и сукцинат; кроме того, витамин F, в частности эссенциальные жирные кислоты, особенно линолевая кислота, линоленовая кислота и арахидоновая кислота.
К предпочтительно используемым согласно изобретению провитаминам или предшественникам витаминов В-группы или их производным, а также производным 2-фуранона относятся среди прочих следующие.
Витамин B1, тривиальное название: тиамин, химическое название: хлорид 3-[(4'-амино-2'-метил-5'-пиримидинил)метил]-5-(2-гидроксиэтил)-4-метилтиазола.
Витамин В2, тривиальное название: рибофлавин, химическое название: 7,8-диметил-10-(1-D-рибитил)-бензо[g]птеридин-2,4(3Н,10Н)-дион. В свободной форме рибофлавин встречается в молочной сыворотке, другие производные рибофлавина можно изолировать из бактерий и дрожжей. Пригодным согласно изобретению стереоизомером рибофлавина является изолируемый из рыбной муки или печени ликсофлавин, который вместо D-рибитила содержит D-арабитиловый остаток.
Витамин В3. Под этим названием часто используют соединения никотиновой кислоты и амида никотиновой кислоты (ниацинамид). Предпочтительным согласно изобретению является амид никотиновой кислоты.
Витамин В5 (пантотеновая кислота и пантенол). Используют предпочтительно пантенол. Используемыми согласно изобретению производными пантенола являются, в частности, простые и сложные эфиры пантенола, а также катионно произведенные пантенолы. В следующей предпочтительной форме осуществления изобретения дополнительно к пантотеновой кислоте или пантенолу могут быть использованы также производные 2-фуранона. Особенно предпочтительными производными являются имеющиеся в торговле вещества: дигидро-3 гидрокси-4,4-диметил-2(3Н)-фуранон с тривиальным названием пантолактон (Merck), 4 гидроксиметил-γ-бутиролактон (Merck), 3,3-диметил-2-гидрокси-γ-бутиролактон (Aldrich) и 2,5-дигидро-5-метокси-2-фуранон (Merck), причем определенно включены все стереоизомеры.
Эти соединения придают соответствующим изобретению кератинсвязывающим эффекторным молекулам влагосохраняющее и успокаивающее свойства.
Витамин B6, причем под этим имеется в виду не единое вещество, а известные под тривиальными названиями пиридоксин, пиридоксамин и пиридоксал производные 5-гидроксиметил-2-метилпиридин-3-ола.
Витамин B7 (биотин), называется также витамином Н или «кожным витамином». Биотин является (3aS,4S,6aR)-2-оксогексагидротиенол[3,4-d]имидазол-4-валериановой кислотой.
Согласно изобретению совершенно предпочтительными являются пантенол, пантолактон, амид никотиновой кислоты, а также биотин.
Согласно изобретению могут быть использованы пригодные производные (соли, сложные эфиры, сахара, нуклеотиды, нуклеозиды, пептиды и липиды). В качестве актиоксидантов предпочтительными из этой группы являются токоферол и его производные, сложные эфиры галловой кислоты, флавоноиды и каротиноиды, а также бутилгидрокситолуол/анизол. В качестве водорастворимых антиоксидантов предпочтительными являются аминокислоты, например тирозин и цистеин и их производные, а также дубильные вещества, в частности таковые растительного происхождения.
Тритерпены, в частности тритерпеновые кислоты, такие как урзоловая кислота, розмариновая кислота, бетулиновая кислота, босвелиевая кислота и брионоловая кислота.
Кроме того, предпочтительной эффекторной молекулой (ii) является липоновая кислота и ее пригодные производные (соли, сложные эфиры, сахара, нуклеотиды, нуклеозиды, пептиды и липиды).
Следующими предпочтительными эффекторными молекулами (ii) являются ультрафиолетовые защитные фильтры. Под ними следует понимать органические вещества, способные абсорбировать ультрафиолетовые лучи и отдавать принятую энергию в форме более длинноволнового излучения, например тепла. Органические вещества могут быть растворимыми в масле или в воде.
В качестве маслорастворимых ультрафиолетовых фильтров могут быть использованы, например:
3-бензилиденкамфара и ее производные, например 3-(4-метилбензилиден)камфара;
производные 4-аминобензойной кислоты, предпочтительно 2-этилгексиловый сложный эфир 4-(диметиламино)-бензойной кислоты-, сложный 2-октиловый эфир 4-(диметиламино)бензойной кислоты и сложный амиловый эфир 4-(диметиламино)-бензойной кислоты;
сложные эфиры коричной кислоты, предпочтительно сложный 2-этилгексиловый эфир 4-метоксикоричной кислоты, сложный пропиловый эфир 4-метоксикоричной кислоты, сложный изоамиловый эфир 4-метоксикоричной кислоты, сложный изопентиловый эфир 4-метоксикоричной кислоты, сложный 2-этилгексиловый эфир 2-циано-3-фенил-коричной кислоты (октокрилен);
сложные эфиры салициловой кислоты, предпочтительно сложный 2-этилгексиловый эфир салициловой кислоты, сложный 4-изопропилбензиловый эфир салициловой кислоты, сложный гомоментиловый эфир салициловой кислоты
производные бензофенона, предпочтительно 2-гидрокси-4-метоксибензофенон, 2-гидрокси-4-метокси-4'-метилбензофенон, 2,2'-дигидрокси-4-метоксибензофенон;
эфиры бензальмалоновой кислоты, предпочтительно сложный ди-2-этилгексиловый эфир 4-метоксибензмалоновой кислоты;
производные триазина, такие как 2,4,6-трианилино-(р-карбо-2'-этил-1'-гексилокси)-1,3,5-триазин (октилтриазон) и диоктил бутамино триазон (Uvasorb® HEB);
пропан-1,3-дионы, такие как 1-(4-трет-бутилфенил)-3-(4'-метоксифенил)пропан-1,3-дион.
В качестве водорастворимых веществ могут быть использованы:
2-фенилбензимидазол-5-сульфоновая кислота и ее щелочные, щелочно-земельные, аммониевые, алкиламмониевые, алканоламмониевые и глюкаммониевые соли;
производные сульфоновой кислоты от бензофенонов, предпочтительно 2-гидрокси-4-метоксибензофенон-5-сульфоновая кислота и ее соли;
производные сульфоновой кислоты 3-бензилиденкамфары, такие как 4-(2-оксо-3-борнилиденметил)бензолсульфоновая кислота и 2-метил-5-(2-оксо-3-борнилиден)сульфоновая кислота и их соли.
Особенно предпочтительным является использование эфиров коричной кислоты, таких как сложный 2-этилгексиловый эфир 4-метоксикоричной кислоты, сложный изопентиловый эфир 4-метоксикоричной кислоты, сложный 2-этилгексиловый эфир 2-циано-3-фенил-коричной кислоты (октокрилен).
Кроме того, предпочтительным является использование производных бензофенона, в частности 2-гидрокси-4-метоксибензофенона, 2-гидрокси-4-метокси-4'-метилбензофенона, 2,2'-дигидрокси-4-метоксибензофенона, а также пропан-1,3-дионов, таких как 1-(4-трет-бутилфенил)-3-(4-метоксифенил)пропан-1,3-дион.
Типичными УФ-А-фильтрами являются:
производные бензоилметана, такие как 1-(4'-трет-бутилфенил)-3-(4'-метоксифенил)пропан-1,3-дион, 4-трет-бутил-4'-метоксидибензоилметан или 1-фенил-3-(4'-изопропилфенил)-пропан-1,3-дион;
амино-гидрокси-замеиценные производные бензофенонов, такие как N,N-диэтиламино-гидроксибензоил-n-гексилбензоат.
Само собой разумеется, что УФ-А- и УФ-В-фильтры могут быть использованы также в смесях.
Пригодные УФ-фильтрующие вещества приведены в таблице:
Наряду с обеими приведенными выше группами первичных светозащитных веществ могут быть использованы также вторичные светозащитные средства типа антиоксидантов, прерывающие цепь реакций, возбуждаемых при проникновении ультрафиолетового излучения в кожу. Типичными примерами являются супероксид-дисмутаза, каталаза, токоферол (витамин Е) и аскорбиновая кислота (витамин С).
Следующей группой являются противораздражители, обладающие противовоспалительным действием на поврежденную УФ-излучением кожу. Такими веществами являются, например, бизаболол, фитол и фитантриол.
Соединение эффекторных молекул (ii) с кератинсвязывающей полипептидной последовательностью (i)
Эффекторные молекулы (ii) соединены с полипептидной последовательностью (i), обладающей связывающим сродством с кератином. Соединение между (i) и (ii) может быть осуществлено как за счет ковалентной связи, так и за счет ионных или Ван-дер-Ваальсовых взаимодействий.
Предпочтительным является ковалентное соединение. Оно может быть осуществлено, например, через боковые цепочки полипептидной последовательности (i), в частности через аминные, или гидроксильные, или карбоксилатные, или тиоловые функции, предпочтительным является соединение через аминофункции одного или нескольких лизиновых остатков, одной или нескольких тиоловых групп цистеиновых остатков или через N-терминальную или С-терминальную функцию полипептида (i). Кроме имеющихся в полипептидной последовательности (i) аминокислотных функций к последовательности могут приобщиться также аминокислоты с пригодными функциями (например, цистеины, лизины, аспартаты, глютаматы), или аминокислоты полипептидной последовательности (i) могут быть замещены такими аминокислотными функциями.
Соединение эффекторных молекул (ii) с полипептидной последовательностью (i) может быть осуществлено или непосредственно, то есть как ковалентная связь двух уже имеющихся в (i) и (ii) химических функций, например аминофункция последовательности (i) соединяется с карбоксилатной функцией молекулы (ii) в амид кислоты, или же через так называемый линкер, то есть по меньшей мере бифункциональную молекулу, которая одной функцией вступает в связь с последовательностью (i), а одной или несколькими другими функциями соединяется с молекулой (ii).
В случае, когда эффекторная молекула (ii) также состоит из полипептидных последовательностей, соединение (i) и (ii) может быть осуществлено в форме так называемого белка слияния, то есть сплошной полипептидной последовательности, которая состоит из обеих частичных последовательностей (i) и (ii).
Между (i) и (ii) могут быть также встроены так называемые спейсерные элементы, например полипептидные последовательности, имеющие потенциальные пробельные места для протеазы, липазы, эфиразы, фосфатазы, гидролазы, или олиго- и полипептидные последовательности, которые позволяют осуществлять легкую очистку фузионного белка, например так называемые «His-tags», то есть олигогистидиновые метки.
Кроме того, спейсерные элементы могут состоять из алкильных цепочек, этиленгликоля и полиэтиленгликолей.
Особенно предпочтительными являются линкерные и/или спейсерные элементы, которые обладают потенциальными пробельными местами для протеазы, липазы, эфиразы, фосфатазы, гидролазы, то есть являются ферментативно расщепляемыми.
Примерами ферментативно расщепляемых линкеров, которые могут быть использованы в соответствующих изобретению молекулах, являются, например, линкеры, известные из публикации WO 98/01406, на полный объем которой этим делается ссылка.
Особенно предпочтительными являются термо- и светорасщепляемые линкеры и спейсеры. Соответствующие химические структуры известны специалисту и интегрируются между частями (i) и (ii) молекулы.
Соединение в случае небелковой эффекторной молекулы с полипептидной последовательностью (i) осуществляется предпочтительно посредством функционализируемых остатков (боковые группы, С- или N-конец) в полипептиде (i), которые вступают в ковалентную связь с химической функцией эффекторной молекулы.
Предпочтительным здесь является соединение через амино-, тиольную или гидроксильную функцию полипептида (i), которая может создавать с карбоксильной функцией эффекторной молекулы (ii) - при необходимости после активизации - соответствующую амидную, тиоэфирную или эфирную связь.
Следующим предпочтительным способом соединения полипептидной последовательности (i) с эффекторной молекулой (ii) является применение линкера, подготовленного по потребности. Такой линкер имеет две или более так называемых анкерные группы, с которыми он может соединять полипептидную последовательность (i) и одну или несколько эффекторных молекул (ii). Например, анкерная группа для (i) может быть тиольной функцией, с помощью которой линкер может образовывать дисульфидную связь с цистеиновым остатком полипептида (i). Анкерная группа для (ii) может быть, например, карбоксильной функцией, с помощью которой линкер может образовывать эфирную связь с гидроксильной функцией эффекторной молекулы (ii).
Применение такого, подготовленного по потребности, линкера позволяет осуществлять точное согласование соединения с желаемой эффекторной молекулой. Кроме того, благодаря этому имеется возможность определенно соединить с полипептидной последовательностью (i) несколько эффекторных молекул.
Используемый линкер готовится в зависимости от подлежащей соединению функциональности. Пригодны, например, молекулы, которые присоединяются к полипептидам (i) посредством сульфгидрил-реактивных групп, например малеимиды, пиридилдисульфиды, α-галоацетилы, винилсульфоны, сульфатоалкилсульфоны (предпочтительно сульфатоэтилсульфоны), а к эффекторным молекулам (ii) посредством
- сульфгидрил-реактивных групп (например, малеимиды, пиридилдисульфиды, α-галоацетилы, винилсульфоны, сульфатоалкилсульфоны (предпочтительно сульфатоэтилсульфоны)),
- амин-реактивных групп (например, сукцинимидилэфиры, карбодиимиды, гидроксиметил-фосфин, имидоэфир, эфир PFP и т.д.),
- сахара или оксидированные сахаро-реактивные группы (например, гидразиды и т.д.),
- карбокси-реактивные группы (например, карбоксидиимиды и т.д.),
- гидроксильно-реактивные группы (например, изоцианаты и т.д.),
- тимин-реактивные группы (например, псоралы и т.д.),
- неселективные группы (например, арилазиды и т.д.),
- светоактивируемые группы (например, перфторфенилазид и т.д.),
- металлкомплексирующие группы (например, EDTA, гексагис, ферритин),
- антитела и -фрагменты (например, однонитевые антитела, F(ab)-фрагменты антител, каталитические антитела).
Альтернативно непосредственное соединение между действующим/эффекторным веществом и кератинсвязывающим доменом может быть осуществлено, например, посредством карбодиимидов, глютардиальдегида, перечисленных выше или других, известных специалисту кросслинкеров.
Соответствующие изобретению кератинсвязывающие эффекторные молекулы могут быть также - при желании - легко отделены от кератина. Для этого может быть применено, например, промывание кератином, в результате которого кератинсвязывающие молекулы вытесняются из их имеющейся связи с кератином и насыщаются кератином из промывного раствора. Таким образом возможно обратимое присоединение большого количества эффекторных молекул к кератину. Альтернативно может быть осуществлено промывание раствором с большим количеством моющего средства (например, додецилсульфата натрия (SDS)) для вымывания.
Соответствующие изобретению кератинсвязывающие эффекторные молекулы имеют широкую область применения в косметике для человека, в частности для ухода за кожей и волосами, а также для ухода за животными, для ухода за (выделанной) кожей и для обработки (выделанной) кожи.
Соответствующие изобретению кератинсвязывающие эффекторные молекулы используются предпочтительно для косметики для кожи, ногтей и волос. Они позволяют создавать высокую концентрацию и длительное действие эффекторных веществ для ухода или защиты кожи, ногтей и волос.
Пригодные вспомогательные и дополнительные материалы для изготовления косметических препаратов для волос и кожи известны специалисту и могут быть взяты из косметических справочников, например, Шрадер, «Основы и рецептура косметики», издательство Huthig Verlag, Хайдельберг, 1989 (Schrader, Grundlagen und Rezepturen der Kosmetika, Huthig Verlag, Heidelberg, 1989, ISBN 3-7785-1491-1).
Согласно следующей форме осуществления изобретения этот косметический препарат служит для ухода или защиты кожи или волос в форме эмульсии, дисперсии, суспензии, водного поверхностно-активного препарата, молочка, лосьона, крема, бальзама, мази, геля, гранулята, пудры, карандаша, например губной помады, пены, аэрозоля или спрея. Такие препаративные формы хорошо пригодны для локального применения. Эмульсии могут быть в форме масло-в-воде и вода-в-масле или в форме микроэмульсий.
Как правило, косметические препараты для волос или для кожи используются для местного нанесения на кожу или волосы. При этом под препаратами местного применения понимают препараты, пригодные для нанесения активного вещества в тонком разведении и пребывающие в форме, пригодной для поглощения кожей. Для этого пригодны, например, водные и водно-спиртовые растворы, спреи, пены, пенные аэрозоли, мази, водные гели, эмульсии типов масло-в-воде или вода-в-масле, микроэмульсии или косметические карандаши.
Согласно предпочтительной форме исполнения соответствующего изобретению косметического средства оно содержит носитель. Предпочтительными носителями являются: вода, газ, жидкости на основе воды, масло, гель, эмульсия или микроэмульсия, дисперсия или их смесь. Указанные носители имеют хорошую переносимость кожей. Особенно предпочтительными для локального применения являются водные гели, эмульсии или микроэмульсии.
В качестве эмульгаторов могут быть использованы неионные поверхностно-активные вещества, цвиттер-ионные поверхностно-активные вещества, амфолитические поверхностно-активные вещества или анионные эмульгаторы. В соответствующей изобретению композиции эмульгаторы могут содержаться в количестве от 0,1 до 10, предпочтительно от 1 до 5 мас.% относительно массы композиции.
В качестве неионного поверхностно-активного вещества может быть использовано вещество из по меньшей мере одной из групп:
продукты присоединения от 2 до 30 молей этиленоксида и/или от 0 до 5 моль пропиленоксида к линейным жирным спиртам, содержащим от 8 до 22 атомов углерода, к жирным кислотам, содержащим от 12 до 22 атомов углерода и к алкилфенолам, содержащим от 8 до 15 атомов углерода в алкильной группе;
моно- и диэфиры С12/18-жирных кислот продуктов присоединения от 1 до 30 моль этиленоксида к глицерину;
глицеринмоно- и диэфиры и сорбитанмоно- и диэфиры насыщенных и ненасыщенных жирных кислот, содержащих 6-22 атомов углерода, и продукты их присоединения к этиленоксиду;
алкилмоно- и олигогликозиды, содержащие 8-22 атомов углерода в алкильном остатке, и их этоксилированные аналоги;
продукты присоединения от 15 до 60 моль этиленоксида к рициновому маслу и/или отвержденному рициновому маслу;
полиолевые и, в частности, полиглицериновые эфиры, такие как полиглицерирполирицинолеат, полиглицеринполи-12-гидроксистеарат или полиглицериндимерат. Пригодны также смеси соединений из нескольких этих классов веществ;
продукты присоединения от 2 до 15 моль этиленоксида к рициновому маслу и/или отвержденному рициновому маслу;
парциальные эфиры на основе линейных, разветвленных, ненасыщенных или насыщенных С6/22-жирных кислот, рициновая кислота, а также 12-гидроксистеариновая кислота и глицерин, полиглицерин, пентаэритрит, дипентаэритрит, сахарные спирты (например, сорбит), алкилгликозиды (например, метилглюкозид, бутилглюкозид, лаурилглюкозид), а также полиглюкозиды (например, целлюлоза);
моно-, ди- и триалкилфосфаты, а также моно-, ди- и/или три-PEG-алкилфосфаты и их соли;
шерстяно-восковые спирты;
сополимеры полисилоксан-полиалкил-полиэфир и соответствующие производные;
смешанные эфиры из пентаэтитрита, жирных кислот, лимонной кислоты и жирного спирта согласно описанию к патенту DE 1165574 и/или смешанные эфиры жирных кислот с 6-22 атомами углерода, метилглюкозы и полиолей, предпочтительно глицерин или полиглицерин, а также
полиалкиленгликоли;
бентаины.
Кроме того, в качестве эмульгаторов могут быть использованы цвиттер-ионные поверхностно-активные вещества. Цвиттер-ионными поверхностно-активными веществами называют соединения, содержащие в молекуле по меньшей мере одну четвертичную аммониевую группу и по меньшей мере одну карбоксилатную или сульфонатную группу. Особенно пригодными цвиттер-ионными поверхностно-активными веществами являются так называемые бентаины, такие как N-алкил-N,N-диметиламмонийглицинаты, например кокосалкилдиметиламмонийглицинат, N-ациламино-пропил-N,N диметиламмонийглицинаты, например кокосациламинопропилдиметиламмонийглицинат, и 2-алкил-3-карбоксилметил-3-гидроксиэтилимидазолины, содержащие 8-18 атомов углерода в алкильной или ацильной группе, а также кокосациламиноэтилгидроксиэтил-карбоксиметилглицинат. Особенно предпочтительной является амидная производная жирной кислоты, известная под CTFA-названием кокамидопропил бентаин.
Пригодными эмульгаторами являются также амфолитические поверхностно-активные вещества. Под амфолитическими поверхностно-активными веществами понимают такие соединения, которые кроме С8,18-алкильной или -ацильной группы в молекуле содержат по меньшей мере одну свободную аминогруппу и по меньшей мере одну группу -СООН- или -SO3H- и способны к образованию внутренних солей. Примерами пригодных амфолитических поверхностно-активных веществ являются N-алкилглицины, N-алкилпропионовые кислоты, N-алкиламиномасляные кислоты, N-алкилиминодипропионовые кислоты, N-гидроксиэтил-N-алкиламидопропилглицины, N-алкилтаурины, N-алкилсаркозины, 2-алкиламинопропионовые кислоты и алкиламинооцтовые кислоты, каждое с 8-18 атомами углерода в алкильной группе.
Особенно предпочтительными амфолитическими поверхностно-активными веществами являются N-кокосалкиламинопропионат, кокосациламиноэтиламинопропионат и С12/18-ацилсаркозин. Наряду с амфолитическими могут быть использованы также четвертичные эмульгаторы, причем преимущественными являются таковые типа эфиркватов, например метил-кватернированные соли триэтаноламинового эфира дижирных кислот. Кроме того, в качестве анионных эмульгаторов могут быть использованы сульфаты алкилового эфира, сульфаты моноглицерида, сульфаты жирных кислот, сульфосукцинаты и/или эфиркарбоновые кислоты.
В качестве масляного тельца могут быть использованы спирты Гербе с 6-18, предпочтительно 8-10 атомами углерода, эфиры линейных С6-С22-жирных кислот с линейными С6-С22-жирными спиртами, эфиры разветвленных С6-С13-карбоновых кислот с линейными С6-С22-жирными спиртами, эфиры линейных С6-С22-жирных кислот с разветвленными спиртами, в частности 2-этилгексанол, эфиры линейных и/или разветвленных жирных кислот с многовалентными спиртами (такими как пропиленгликоль, димердиол или тримертриол) и/или спиртами Гербе, триглицериды на основе С6-С10-жирных кислот, жидкие моно-/ди-, триглицеридные смеси на основе С6-С18-жирных кислот, эфиры С6-С22-жирных спиртов и/или спиртов Гербе с ароматическими карбоновыми кислотами, в частности бензойной кислотой, эфиры С2-С12-дикарбоновых кислот с линейными или разветвленными спиртами с 1-22 атомами углерода или полиолями с 2-10 атомами углерода и 2-6 гидроксильными группами, растительные масла, разветвленные первичные спирты, замещенные циклогексаны, линейные карбонаты С6-С22-жирных спиртов, карбонаты Гербе, эфиры бензойной кислоты с линейными и/или разветвленными С6-С22-спиртами (например, Finsolv® TN), диалкиловые эфиры, обладающие раскрытыми кольцами продукты эпоксидированных эфиров жирных кислот с полиолями, силиконовые масла и/или алифатические или нафтеновые углеводороды. Кроме того, в качестве масляных телец могут быть также использованы, например, диметилполисилоксаны, метилфенилполисилоксаны, циклические силиконы, а также амино-, жирнокислотно-, спирто-, полиэфирно-, эпокси-, фтор-, алкил- и/или гликозидмодифицированные силиконовые соединения, которые при комнатной температуре могут пребывать как в жидком, так и в смолообразном состоянии. Масляные тельца могут содержаться в соответствующих изобретению средствах в количестве от 1 до 90, предпочтительно от 5 до 80, в частности от 10 до 50 мас.% относительно общей массы композиции.
Путем присоединения соответствующих соединений к кератинсвязывающему полипептиду (i) может быть значительно увеличен срок действия на кожу. Присоединение осуществляют описанным выше способом, изготовление и применение осуществляют известными специалисту методами. В частности для деодорантов пригодными эффекторными молекулами (ii) являются: парфюмерные масла, циклодекстрины, ионообменники, цинк-рицинолеат, ингибиторы роста растений/бактериостатические соединения (например, DCMX, Irgasan DP 300, ТСС).
В качестве средств против потоотделения пригодны: танины и цинковые/алюминиевые мази.
Следующей областью применения соответствующих изобретению веществ является терапевтическое или профилактическое применение при определенных заболеваниях кожи и слизистых оболочек. В частности, в случае ротовой, горловой и носовой полости для лечения/профилактики целесообразным является усиление и продление действия активных веществ с помощью кератинсвязывающих доменов. Областями применения, в частности, являются;
- вирусные заболевания (например, герпес, коксаки, Varicella zoster, вирус цитомегалии и т.д.),
- бактериальные заболевания (например, туберкулез, сифилис и т.д.),
- грибковые заболевания (например, кандида, криптококк, гистоплазмоз, аспергиллез, мукормикоз и т.д.),
- опухолевые заболевания (например, меланома, аденома и т.д.),
- аутоимунные заболевания (например, обыкновенная пузырчатка (pemphigus vulgaris), буллезный пемфигоид (bullous pemphigoid}, системная красная волчанка (systemic lupus erythematosis) и т.д.),
- солнечные ожоги,
- поражение паразитами (например, клещи, блохи и т.д.),
- укусы насекомых (например, кровососущие насекомые, такие как малярийный комар обыкновенный и т.д.).
Вещества, пригодные для лечения или профилактики (например, кортикоиды, иммуностимулирующие соединения, антибиотики, противогрибковые средства, противовирусные соединения, средства, отпугивающие насекомых и т.д.), могут быть с помощью описанных выше линкеров (в зависимости от подключаемой функциональности соответствующий оптимирующий линкер) подсоединены к кератинсвязывающим полипептидам (i).
Пример 1: Векторы экспрессии и продуктивные штаммы
Были протестированы различные векторы для экспрессии кератинсвязывающих доменов (КСД). При этом были использованы различные промоторы (например, IPTG-индуцируемый, рамнозо-индуцируемый, арабиндозо-индуцируемый, метанол-индуцируемый, конститутивные промоторы и другие). Также были протестированы конструкты, в которых кератинсвязывающие домены были экспрессированы как фузионные белки (например, как слияние с тиоредоксином, или eGFP, или YaaD [В.subtilis, SWISS-PROT: P37527, PDX1] и т.д.). При этом с использованием различных систем экспрессии были экспрессированы как описанные кератинсвязывающие домены В (КСД-В), так и кератинсвязывающие домены С (КСД-С), а также комбинация обоих доменов (КСД-ВС). Упомянутые конструкции векторов не являются ограничивающим перечнем.
В качестве примера приведена векторная карта IPTG-индуцируемого вектора pQE30-KBD-B (фиг.3), метанол-индуцируемых векторов pLib15 (фиг.4) и pLib16 (фиг.5), а также индуцируемого вектора pLib19 (фиг.6). Аналогично описанным векторным конструкциям и экспрессиям может быть осуществлен подход и к КСД-С.
Для экспрессии КСД были использованы различные продуктивные хозяева, такие как штаммы Е.Coli (смотри пример 2; например, XL10-Gold [фирма Stratagene], BL21-CodonPlus [фирма Stratagene] и другие). Однако были использованы и другие продуктивные хозяева, такие как Bacillus megaterium или Bacillus subtilis. КСД-экспрессию в В.megaterium осуществляли согласно публикации Barg, H., Malten, М. & Jahn, D. (2005). Protein and vitamin production in Bacillus megaterium. In Methods in Bio-technology-Micobial Products and Biotransformations (Barredo, J.-L., ed.).
В качестве продуктивных штаммов использовали Pichia pastoris (смотри пример 3; например, GS115 и КМ71 [оба: фирма Invitrogen] и другие) и Aspergillus nidulans (смотри пример 4; например, RMS011 [Stringer, MA, Dean, RA, Sewall, TC, Timberlake, WE (1991) Rodletless, a new Aspergillus developmental mutant induced by direct gene activation. Genes Dev 5:1161-1171] и SRF200 [Karos, М, Fischer, R. (1999) Molecular characterization of HymA, an evolutionarily highly conserved and highly expressed protein of Aspergillus nidulans. Mol Genet Genomics 260:510-521] и другие). Однако для КСД-экспрессии могут быть использованы и другие грибковые продуктивные хозяева, например Aspergillus niger (КСД-экспрессия аналогично ЕР 0635574 А1 и/или WO 98/46772).
Пример 2: КСД-экспрессия в штаммах E.Coli с помощью IPTG-индуцируемых промоторов, например с помощью экспрессионной плазмиды pQE30-KBD-B
Для экспрессии были использованы различные продуктивные хозяева, такие как различные штаммы Е.coli (например, XL10-Gold [фирма Stratagene], BL21-CodonPlus [фирма Stratagene] и другие), Bacillus megaterium, Bacillus subtilis и другие.
Здесь - в качестве примера - описано клонирование и экспрессия КСД-В с помощью Е.coli, трансформированную вектором pQE30-KBD-B.
Клонирование pQESO-KBD-В
- Получали Lambda-MaxiDNA (DNA-Lambda Maxi Kit, фирма Qiagen) из банка кДНК кератинозитов человека (фирма BD Bioscience, Clontech, Human Keratinocyte cDNA, foreskin, primary culture in log phase, Vektor: λgt11).
Полимеразную цепную реакцию (ПЦР) осуществляли с использованием следующих олигонуклеотидов:
Bag 43 (5'-GGTCAGTTACGTGCAGCTGAAGG-3') и
Bag 44 (5' GCTGAGGCTGCCGGATCG-3').
- Полученный продукт полимеразной цепной реакции длиной около 1102 пар основ выделяли из агарозного геля и очищали.
- С очищенным продуктом полимеразной цепной реакции в качестве шаблона осуществляли вторую полимеразную цепную реакцию.
Используемые олигонуклеотиды:
Bag 53: (5'-CGCGCCTCGAGCCACATACTGGTCTGC-3') и
Bag 51 (5'-GCTTAGCTGAGGCTGCCGGATCG-3').
- Полученный продукт полимеразной цепной реакции длиной почти 1073 пар основ выделяли из агарозного геля, очищали и клонировали следующим вектором: pCR2.1-TOPO (фирма Invitrogen).
- После этого полученный вектор pCR2.1-TOPO+KBD-B (5027 пар основ) трансформировали, амплифицировали в Е.Coli, затем вырезали с помощью XhoI и EcoRI и полученный фрагмент КСД-В клонировали в pBAD/HisA (фирма Invitrogen; также вырезаннном с помощью XhoI и EcoRI).
- Новый полученный вектор pBAD/HisA+KBD-B (5171 пар основ) снова разрезали с помощью SacI и StuI и полученный КСД-фрагмент клонировали в pQE30 (фирма Qiagen; вырезанном с помощью SacI и Smal). Полученный в результате вектор экспрессии pQE30-KBD-B (4321 пар основ; смотри также фиг.3) был использован для следующих экспрессии КСД-В.
Кератинсвязывающий домен В, экспрессированный вектором pQE30-KBD-B в Е.Coli, дополнительно наряду с полипептидной последовательностью SEQ ID NO:1 положения 2193-2481 содержал на N-конце аминокислоты MRGSHHHHHHGSACEL, а также на С-конце аминокислоты GVDLQPSLIS.
Экспрессия КСД-В вектором pQESO-KBD-B в Е.coli
- Исходные культуры из пластины или в культуре глицерина инфицировали штаммами Е.Coli (например, XL10-Gold [фирма Stratagene]), трансформированными вектором pQE30-KBD-B. В зависимости от размера основной культуры инфицирование осуществляли в трубочке или в маленькой колбе с LB-средой (около 1:100).
- Антибиотики применяли в зависимости от используемого штамма (для pQE30-KBD-В ампициллин 100 мкг/мл).
- Инкубировали при скорости вращения 250 оборотов в минуту и температуре 37°С.
- Основную культуру инфицировали исходной культурой в соотношении около 1:100. Основная культура: LB-среда или пригодная минимальная среда с соответствующим антибиотиком. Инкубирование при скорости вращения 250 оборотов в минуту и температуре 37°С.
- Индукцию осуществляли с помощью 1 мМ IPTG, начиная от оптической плотности OD (600 нм) 0,5.
- После 4 часов индукции клетки отделяли центрифугированием.
В ферментаторах действовали аналогичным образом, однако индукцию осуществляли при значительно более высоких значениях оптической плотности, и поэтому выход клеток и белка был значительно большим.
Пример 3: Внутриклеточная и секреторная экспрессия КСД посредством штаммов Pichia pastoris с использованием метанол-индуцируемых промоторов, например экспрессионными плазмидами pLib 15 и pLib 16 (качающаяся колба)
Для КСД-экспрессии были использованы различные штаммы Pichia pastoris, например GS115 и КМ71 (Pichia Expression Kit, Version M; Invitrogen Life Technologies).
Ниже - в качестве примера - описана экспрессия КСД-В с помощью Р. pastoris, трансформированного промоторами pLib15 (внутриклеточная экспрессия, вектор - смотри фиг.4) или pLib16 (секреторная экспрессия, вектор - смотри фиг.5).
- Для конструирования pLib15 в качестве шаблона был использован КСД-В-кодирующий фрагмент ДНК размером 930 пар основ, амплифицированный посредством полимеразной цепной реакции с использованием олигонуклеотидов Lib148 (5'-GCTAAGGAATTCACCATGCATCACCATCACCATCACGAGCCACATACTGGTCTGCT-3') и Lib149 (5'-GCTGGAGAATTCTCAGCTAATTAAGCTTGGCTGCA-3'), а также вектора pQE30-KBD-B (пример 2, фиг.3). При этом на обоих концах продукта полимеразной цепной реакции были размещены рестрикционные EcoRI-сайты.
- Для конструирования pLib16 в качестве шаблона был использован КСД-В-кодирующий фрагмент ДНК размером 930 пар основ, амплифицированный посредством полимеразной цепной реакции с использованием олигонуклеотидов Lib149 (5'-GCTGGAGAATTCTCAGCTAATTAAGCTTGGCTGCA-3') и Lib150 (5'-GCTAAGGAATTCCATCACCATCACCATCACGAGCCACATACTGGTCTGCT-3'), a также вектора pQE30-KBD-B (пример 2, фиг.3). При этом на обоих концах продукта полимеразной цепной реакции были размещены рестрикционные EcoRI-сайты.
- ПЦР-продукт, амплифицированный олигонуклеотидами Lib148/Lib149, перетравливали EcoRI и лигировали в разрезанный с помощью EcoRI вектор pPIC3.5 (Pichia Expression Kit, Version M, фирма Invitrogen). Корректное амплифицирование КСД-В проверяли путем секвенирования результирующего из лигирования вектора pLib15 (фиг.4).
- ПЦР-продукт, амплифицированный олигонуклеотидами Lib149/Lib150, перетравливали EcoRI и лигировали в разрезанный с помощью EcoRI вектор рР1С9 (Pichia Expression Kit, Version M, фирма Invitrogen). Корректное амплифицирование КСД-В проверяли путем секвенирования результирующего из лигирования вектора pLib16 (фиг.5).
- Электрокомпетентные клетки и сферопласты штаммов Р.pastoris трансформировали циркулярными и линеаризованными векторами pLib15 и pLib16.
- Анализ трансформантов осуществляли посредством ПЦР и Southern Blot с использованием хромосомных ДНК.
- Для получения начальной культуры КСД-В-экспресующие трансформанты Р.pastoris инфицировали из пластины или глицериновой культуры. В зависимости от размера основной культуры инфицировали трубочку или маленькую колбу с MGY-, BMG- или BMGY-средой (Pichia-Expression-Kit, Version M, фирма Invitrogen) (около 1:100).
- Культуру инкубировали при частоте вращения 250-300 оборотов в минуту и температуре 30°С до OD600=2-6.
- Клетки собирали путем центрифугирования при 1500-3000×g в течение 5 минут при комнатной температуре.
- Для получения главной культуры собранный центрифугат разводили до OD600=1 в метанолсодержащей mM-, BMM- или BMMY-среде с тем, чтобы индуцировать экспрессию.
- Инкубирование главной культуры осуществляли при скорости вращения 250-300 об/мин и температуре 30°С в течение 1-96 часов.
- Поддержание индукции осуществляли путем добавления 100% метанола каждые 24 часа при конечной концентрации метанола 0,5%.
- При внутриклеточной экспрессии собирание и подготовку клеток осуществляли после главной культуры посредством Menton-Gaulin.
- При секреторной экспрессии собирали надосадочную жидкость культуры и КСД-В очищали непосредственно из нее.
- КСД-В (pLib15), внутриклеточно экспрессированный в Р.pastoris, наряду с полипептидной последовательностью SEQ ID NO:1 положение 2193-2481 дополнительно содержал на N-конце аминокислоты МНННННН, а также на С-конце аминокислоты GVDLQPLIS.
- КСД-В (pLib16), секреторно экспрессированный в Р.pastoris, перед процессированием наряду с полипептидной последовательностью SEQ ID NO:1 положение 2193-2481 дополнительно содержал на N-конце аминокислоты MRFPSIFTAVLFAASSALAAPVNTTTEDETAQIPAEAVIGYSDLEGDFDVAVLPFSNSTNN GLLFINTTIASIAAKEEGVSLEKREAEAYVEFHHHHHH, а также на С-конце аминокислоты GVDLQPLIS. С помощью Р.pastoris выделенный и процессированный КСД-В (pLib16) наряду с полипептидной последовательностью SEQ ID NO:1 положение 2193-2481 дополнительно содержал на N-конце аминокислоты YVEFHHHHHH, а также на С-конце аминокислоты GVDLQPLIS.
Пример 4: Экспрессия КСД посредством штаммов Aspergillus nidulans с использованием индуцируемого промотора alcaA, например, с помощью экспрессионного плазмида pLib 19 (качающаяся колба)
Для экспрессии использовали дикие типы штаммов A.nidulans, такие как RMS011 или SRF200. Ниже - в качестве примера - описана экспрессия КСД-В с помощью штамма A.nidulans, трансформированного pLib19 (фиг.6).
- Для конструирования pLib19 в качестве шаблона был использован КСД-В-кодирующий фрагмент ДНК размером 900 пар основ, амплифицированный посредством полимеразной цепной реакции с использованием олигонуклеотидов Lib151 (5'-CACCATGCATCACCATCACCATCACGAGCCACATACTGGTCTGCT-3') и Lib152 (5'- GCTAATTAAGCTTGGCTGCA-3'), а также вектора pQE30-KBD-B (пример 2, фиг.3). ПЦР-продукт был легирован в вектор pENTR/D (pENTR™ Directional ТОРО® Cloning Kit, Version E, фирма Invitrogen). Корректную КСД-В-амплификацию проверяли путем секвенирования.
- Рекомбинацию КСД-В-кодирующего фрагмента ДНК осуществляли в вектор рМТ-OvE (Toews MW, Warmbold J, Konzack S, Rischitor P, Veith D, Vienken K, Vinuesa C, Wei H, Fischer R; Establishment of mRFP1 as a fluorescent marker in Aspergillus nidulans and construction of expression vectors for high-throughput protein tagging using recombination in vitro (GATEWAY). (2004) Curr Genet 45: 383-389) с использованием „Gateway® LR clonase™ enzyme mix" (фирма Invitrogen). При этом образовывался вектор pLib19 (фиг.6).
- Протопласты диких типов штаммов A.nidulans трансформировали циркулярным вектором pLib19. Анализ трансформантов осуществляли посредством ПЦР и Southern Blot с использованием хромосомных ДНК.
- Для получения начальной культуры КСД-В-экспресующих трансформантов А.nidulans 100 мл минимальной среды (0,6% NaNO3; 0,152% KH2PO4; 0,052% KCl [pH 6,5]; 0,8% глюкозы; 0,05% MgSO4; 1 мл раствора микроэлементов [1 г/л FeSO4×7H2O; 8,8 г/л ZnSO4×7H2O; 0,4 г/л CuSO4×5H2O; 0,15 г/л MnSO4×4H2O; 0,1 г/л Na2B4O7×10H2O; 0,05 г/л (NH4)6Mo7O24×4H2O] + штамм-специфическое дополнение) или 100 мл комплексной среды (2% солодового экстракта; 0,1% пептона; 2% глюкозы; + штамм-специфическое дополнение) инфицировали в колбе объемом 500 мл спорами в количестве 106-107 и инкубировали в течение 16-24 часов при скорости вращения 200-250 об/мин и температуре 37°С.
- После начальной культуры путем фильтрования собирали мицелий, промывали дистиллированной водой и помещали в колбу с 100-500 мл свежей минимальной среды. В этой среде главной культуры в качестве источника углерода использовали 0,1% фруктозу вместо глюкозы. Для индукции экспрессии КСД-В в среду дополнительно добавляли этанол (конечная концентрация 1%), или глицерол (50 мМ), или ацетат натрия (50 мМ), или этиламин, или треонин. Указанные добавки для индукции экспрессии не являются ограничивающими для объема прав. Главную культуру инкубировали в течение 5-48 часов при скорости вращения 200-250 об/мин и температуре 37°С.
- После получения культуры собирали мицелий путем центрифугирования при 1500-3000×g в течение 5 минут при комнатной температуре и обрабатывали посредством Menton-Gaulin.
- КСД-В (pLib19), экспрессированный в A.nidulans, наряду с полипептидной последовательностью SEQ ID NO:1 положение 2193-2481 дополнительно содержал на N-конце аминокислоты МНННННН, а также на С-конце аминокислоты KGGRADPAFLYKVVMIRLLTKPERKLLEGGPGTQLLFPLVRVNCALGVIMVIAVSCVKLL SAHNSTQHTSRKHKV.
Пример 5: Отделение клеток и очистка включений (pQE30-KBD-B)
Растворимо экспрессованный КСД после очистки может быть использован непосредственно. Нерастворимо экспрессованный КСД (например, в тельцах включений) очищали следующим образом.
- Ферментер центрифугировали, центрифугат суспендировали в 20 мМ фосфатного буферного раствора с рН=7,4 и с помощью Menton-Gaulin.
- Раствор снова центрифугировали (15000g), центрифугат смешивали с 20 мМ фосфата, 500 мМ NaCl и 8 М карбамида и перемешивали (растворение телец включений).
- Значение рН надосадочной жидкости устанавливали 7,5.
- После этого еще раз центрифугировали и надосадочную жидкость подавали на Ni-хелат-сефарозную колонку.
Пример 6: Очистка кератинсвязывающего домена В Ni-хелат-сефарозной колонкой
Очистка КСД может быть осуществлена путем хроматографии на Ni-колонке через подвешенные гистаминовые метки.
Материал колонки: Ni-Sepharose High Performance фирма Amersham Biosciences Номер для заказа: 17-5268-02.
Материалом набивали колонку (например, диаметр 2,6 см, высота 5 см) и уравновешивали буфером А+4% буфера В (соответствует 20 мМ имидазола).
Белковый экстракт (смотри растворение клеток и очистка телец включений) с рН 7,5 через суперпетлю (АКТА-система) подавали на колонку (поток около 5 мл/мин).
После подачи промывали буфером А+20 мМ имидазола.
Элюирование осуществляли буфером В (500 мМ имидазола в буфере А).
Элюат фракционно улавливали фракционным сборником.
Пример 7: Восстановление кератинсвязывающего домена В
Нерастворимо экспрессованный кератинсвязывающий домен (например, из телец включений) может быть восстановлен и тем самым активизирован следующим образом:
Метод 1: Дискретный диализ
К 6,5 мл КСД-В с тельцами включений в 8 М карбамида (Ni-хелатный элюат, HiTrap) добавляли 6,5 мл Cellytic IB (фирма Sigma, номер для заказа С5236) и 5 мМ DTT. После этого подлежащий восстановлению раствор подавали в диализный мешок (фирма Spectrum: Spectra Por MWCO:12-14 kD).
Диализ осуществляли в течение 12 часов против 1 л 6 М раствора карбамида при температуре 4°С с осторожным перемешиванием.
Добавляли 500 мл 25 мМ трис/HCl рН=7,50 и подвергали диализу в течение 9 часов при температуре 4°С. Затем добавляли еще 250 мл трис/буфера (см. выше) и подвергали диализу в течение следующих 12 часов.
Затем добавляли 500 мл 25 мМ трис/HCl рН=7,50 и подвергали диализу в течение 9 часов при температуре 4°С. Затем добавляли еще 250 мл трис/буфера (см. выше) и подвергали диализу в течение следующих 12 часов.
Затем добавляли 500 мл 25 мМ трис/HCl рН=7,50 и подвергали диализу в течение 9 часов при температуре 4°С. После этого в диализный мешок подавали диализат в 2 л: 25 мМ трис + 150 мМ NaCl pH=7,50. Снова подвергали диализу в течение 12 часов при температуре 4°С.
После этого изымали содержимое диализного мешка.
Метод 2: Непрерывный диализ
6,5 мл КСД-В с тельцами включений в 8 М карбамида (Ni-хелатный элюат, HiTrap) смешивали с 6,5 мл Cellytic IB (фирма Sigma, номер для заказа С5236) и 5 мМ DTT. После этого раствор помещали в диализную камеру: Slide-A-Lyzer Dialyses Cassette фирма PIERCE, MWCO: 10 kD. Номер для заказа: 66830.
Диализ осуществляли в течение 1 часа против 1 л 6 М раствора карбамида при температуре 4°С.
После этого в течение 48 часов непрерывно подавали шланговым насосом 2 л буферного раствора: 25 мМ трис/HCl рН=7,5.
Затем диализный мешок с диализатом помещали в 2 л конечного буферного раствора: 25 мМ трис + 150 мМ NaCl рН=7,50 и подвергали диализу в течение 12 часов при температуре 4°С.
После этого извлекали содержимое диализного мешка.
Пример 8: Связывание с кожей 1 (качественный анализ)
Был разработан визуальный качественный тест для проверки связывания КСД с кожей.
Используемые растворы:
Блокирующий раствор: DIG Wash + Bufferset 1585762 Boehringer MA (10xLsg), разведенный в TBS.
TBS: 20 мМ трис; 150 мМ NaCl pH 7,5.
TTBS: TBS + 0,05% Tween 20.
Первой стадией являлось перенесение внешнего слоя кератина с кожи на стабильный носитель. Для этого на кожу человека, с которой удалили волосы, наносили полоску прозрачного клея, а затем снова удаляли. Тест можно осуществлять непосредственно на прозрачной полоске клея или перенести приклеившийся слой кератина на предметное стекло. Подтверждение связывания осуществляли следующим образом.
- Помещение в пробирку Фалькона для инкубирования с различными реагентами.
- При необходимости - добавление этанола для обезжиривания, удаление этанола и сушка предметного стекла.
- Инкубирование в течение 1 часа при комнатной температуре с блокирующим раствором.
- Промывание TTBS 2 раза по 5 мин.
- Промывание TBS 1 раз в течение 5 мин.
- Инкубирование с тестируемым КСД (присоединенным метке - например, His6, НА и т.д.) или с контрольным белком в TBS/0,05% Tween 20 в течение 2-4 часов при комнатной температуре.
- Удаление надосадочной жидкости.
- 3-Разовое промывание с помощью TBS.
- Инкубирование в течение 1 часа с моноклональным анти-гистидиновым антителом, разведенным в соотношении 1:2000 в TBS+0,01% блокирующий раствор.
- Промывание TTBS 2 раза по 5 мин.
- Промывание TBS 1 раз в течение 5 мин.
- Инкубирование в течение 1 часа при комнатной температуре с анти-мышиным IgG щелочно-фосфатазным конъюгатом, разведенным в соотношении 1:5000 в TBS+0,01% блокирующий раствор.
- Промывание TTBS 2 раза по 5 мин.
- Промывание TBS 1 раз в течение 5 мин.
- Добавление фосфатазного субстрата (NBT-BCIP; Boehringer MA 1 таблетка/40 мл воды 2,5 мин; остановка: водой).
- Визуальная оценка цветного осадка невооруженным глазом или через микроскоп. Синий цвет осадка свидетельствует, что КСД связан с кожей.
Пример 9: Связывание с кожей (количественный анализ)
Был разработан количественный тест, позволяющий сравнить силу связи с кожей/волосами кератинсвязывающих доменов и неспецифических белков.
Из размороженного сухого кусочка кожи (человека или свиньи) с помощью сверла для пробок был высверлен образец 5 мм (или в случае поверхностного теста кусочек кожи согласовывали с крышкой пробирки Фалькона). Пробу кожи доводили до толщины 2-3 мм, чтобы удалить возможно имеющуюся ткань. Затем пробу кожи помещали в сосуд Эппендорфа для проведения анализа на подтверждение связывания (смотри также фиг.7).
- 2-разовое промывание PBS/0,05% Tween 20.
- Добавление 1 мл 1% BSA в PBS и инкубирование в течение 1 часа при комнатной температуре и легком покачивании (900 об/мин).
- Удаление надосадочной жидкости.
- Добавление 100 мкг КСД в PBS+0,05% Tween 20; инкубирование в течение 2 часов при комнатной температуре и легком покачивании (900 об/мин).
- Удаление надосадочной жидкости.
- 3-разовое промывание PBS/0,05% Tween 20.
- Инкубирование с 1 мл моноклинального мышиного анти-метка-(His6 или НА или специфический КСД)-антитела с пероксидазным конъюгатом (1:2000 в PBS/0,05% Tween 20) [Monoclonal AntipolyHistidin Peroxidase Conjugate, produced in mouse, lyophilized powder, фирма Sigma] в течение 2-4 часов при комнатной температуре и легком покачивании (900 об/мин).
- 3-разовое промывание PBS/0,05% Tween 20.
- Добавление пероксидазного субстрата (1 мл/сосуд Эппендорфа; состав смотри ниже).
- Проведение реакции до появления синего цвета (около 1:30 мин).
- Остановка реакции с помощью 100 мкл 2 М H2SO4.
- Измерение абсорбции на длине волны 405 нм.
Пероксидазный субстрат (использованный немного выше по тексту):
0,1 мл ТМВ-раствора (42 мМ ТМВ в DMSO)
+10 мл субстратного буфера (0,1 М ацетат натрия рН 4,9)
+14,7 мкл H2O2 3%
Пример 10: Связывание с волосами (количественный анализ)
Для подтверждения силы связи кератинсвязывающих доменов с волосами в сравнении с другими белками был разработан метод количественного анализа (смотри также фиг.7). Согласно этому тесту сначала волосы инкубируют с КСД и лишний КСД вымывают. Затем через гистидиновую метку к КСД присоединяют антительный пероксидазный конъюгат. Не связанный антительный пероксидазный конъюгат снова вымывают. Связанный антительный пероксидазный конъюгат [Monoclonal AntipolyHistidin Peroxidase Conjugate, produced in mouse, lyophilized powder, фирма Sigma] может преобразовать бесцветный субстрат (ТМВ) в цветной продукт, который измеряют фотометрическим методом на длине волны 405 нм. Интенсивность абсорбции свидетельствует о количестве связанного кератинсвязывающего домена или сравнительного белка. В качестве сравнительного белка был выбран YaaD из В.subtilis, который также - как требуется для этого теста - имеет гистидиновую метку, пригодную для выявления. Вместо гистидиновой метки могут быть использованы также другие специфические антитела, конъюгированные с пероксидазой.
5 мг волос (человека) нарезали отрезками длиной 5 мм и помещали в сосуд Эппендорфа для проведения теста:
- Добавление 1 мл этанола для обезжиривания
- Центрифугирование, удаление этанола и промывка волос водой
- Добавление 1 мл 1% BSA в PBS и инкубирование в течение 1 часа при комнатной температуре и легком покачивании
- Центрифугирование, удаление надосадочной жидкости
- Добавление тестируемого кератинсвязывающего домена (присоединенного к метке - например, His6, НА и т.д.) или контрольного белка в 1 мл PBS/0,05% Tween 20; инкубирование в течение 16 часов при температуре 4°С (или по меньшей мере 2 часа при комнатной температуре) при легком покачивании.
- Центрифугирование, удаление надосадочной жидкости
- 3-разовое промывание PBS/0,05% Tween 20
- Инкубирование с 1 мл моноклонального мышиного анти-метка-(His6 или НА)-антитела с пероксидазным конъюгатом (1:2000 in PBS/0,05% Tween 20) [Monoclonal AntipolyHistidin Peroxidase Conjugate, produced in mouse, lyophilized powder, фирма Sigma] в течение 2-4 часов при комнатной температуре и легком покачивании
- 3-разовое промывание PBS/0,05% Tween 20
- Добавление пероксидазного субстрата (1 мл/сосуд Эппендорфа)
- Проведение реакции до появления синего цвета (около 2 минут)
- Остановка реакции с помощью 100 мкл 2 М H2SO4
- Измерение абсорбции при длине волны 405 нм.
Пероксидазный субстрат (использованный немного выше по тексту):
0,1 мл ТМВ-раствора (42 мМ ТМВ в DMSO)
+10 мл субстратный буфер (0,1 М ацетат натрия рН 4,9)
+14,7 мкл Н2О2 3%
Обозначения:
BSA = Bovine serum albumin = Бычий сывороточный альбумин
PBS = Фосфатный буферный солевой раствор
Tween 20 = Полиоксиэтилен сорбитан монолауреат, n около 20
ТМВ = 3,5,3,'5'-тетраметилбензидин
В качестве примера осуществленный тест на связывание с волосами показал значительное превосходство связывания КСД-В с волосами по сравнению со значительно худшим связыванием сравнительного белка YaaD:
Пример 10а: Слияние красителя с КСД-В
Для слияния флюоресцентного красителя (Alexa Fluor 532, фирма Molecular Probes/Invitrogen) к белку КСД-В краситель был с помощью линкера (диимид малеиновой кислоты) присоединен к цистеинтиольной группе согласно приведенному ниже протоколу. Реакция изображена на фиг.8.
- 1 мг красителя Alexa Fluor 532 растворяли в 150 мкл PBS, рН 7.0; кратковременно центрифугировали для отделения возможно не растворившихся составляющих.
- К 100 мкг КСД-В (1 мг/мл) добавляли 10 мкл растворенного красителя.
- Смесь накрывали алюминиевой фольгой и в течение 1 часа инкубировали при температуре 24°С и скорости качания 450 об/мин.
- Добавляли 10 мкл 1 М DTT, чтобы инактивировать малеиндиимидную функцию не прореагировавшего красителя Alexa Fluor 532.
- Затем накрывали алюминиевой фольгой и инкубировали в течение 30 минут при температуре 24°С и скорости качания 450 об/мин.
Связывание КСД-В с присоединенным красителем Alexa Fluor 532 с кожей/волосами может быть определено с помощью теста активности (примеры 9 и 10). Действие связанного в соответствии с примерами 9 или 10 с кожей, или волосами КСД-В с присоединенным красителем Alexa Fluor 532 очень хорошо можно подтвердить с помощью флуоресцентного микроскопа (абсорбция: 532 нм/эмиссия: 590 нм), или даже невооруженным глазом на светлых волосах.
Пример 11: Применение кератинсвязывающего домена в эмульсии для дневного ухода - тип масло-в-воде


Изготовление: Фазы А и В отдельно одну от другой нагреть до температуры около 80°С. Фазу В при помешивании добавлять к фазе А и гомогенизировать. Фазу С при помешивании добавить к комбинированным фазам А и В и снова гомогенизировать. При помешивании охладить до температуры около 40°С, добавить фазу D, значение рН фазой Е установить около 6,5, гомогенизировать и при помешивании охладить до комнатной температуры.
Примечания: Препарат изготовляется без защитного газа. Заполнять следует в кислородонепроницаемую упаковку, например в алюминиевые тубы.
Пример 12: Применение кератинсвязывающего домена в защитном дневном креме тип масло-в-воде
Активного вещества 1%:


Изготовление: Фазы А и В отдельно одну от другой нагреть до температуры около 80°С. Фазу В при помешивании добавлять к фазе А и гомогенизировать. Фазу С при помешивании добавить к комбинированным фазам А и В и снова гомогенизировать. При помешивании охладить до температуры около 40°С, добавить фазу D, значение рН фазой Е установить около 6,5, гомогенизировать. При помешивании охладить до комнатной температуры.
Пример 13: Применение КСД в лосьоне для очистки лица - тип масло-в-воде
Активного вещества 1%:


Изготовление: Растворить фазу А. Фазу В при помешивании добавить в фазу А; фазу С примешать к фазам А и В. Растворить фазу D, при помешивании добавить в комбинированные фазы А, В и С и гомогенизировать. Перемешивать в течение 15 минут.
Пример 14: Применение КСД в дневном спрее для тела


Изготовление: Компоненты фазы А взвесить и растворить.
Пример 15: Применение КСД в геле для ухода за кожей

Изготовление: Фазу А растворить. Дать набухнуть фазе В и нейтрализовать фазой С. Фазу А добавить к гомогенизированной фазу В и гомогенизировать.
Пример 16: Применение КСД в лосьоне после бритья


Изготовление: Смешать компоненты фазы А. Растворить фазу В, добавить в фазу А и гомогенизировать.
Пример 17: Применение КСД в лосьоне после загара
Активного вещества 1%:


Изготовление: Смешать компоненты фазы А. Фазу В при помешивании добавить в фазу А. нейтрализовать фазой С и снова гомогенизировать.
Пример 18: Применение КСД в солнцезащитном лосьоне


Изготовление: Компоненты фаз А и В отдельно друг от друга нагреть до температуры около 80°С. Фазу В при помешивании добавить в фазу А и гомогенизировать. Фазу С нагреть до температуры около 80°С и при помешивании добавить в комбинированные фазы А и В. При помешивании охладить до температуры около 40°С, добавить фазу D и еще раз гомогенизировать.
Пример 19: Применение КСД в солнцезащитном лосьоне - тип масло-в-воде


Изготовление: Фазу А нагреть до температуры около 80°С, при помешивании добавить фазу В и гомогенизировать в течение 3 минут. Фазу С также нагреть до температуры 80°С и при помешивании добавить в комбинированные фазы А и В. Охладить до температуры около 40°С, при помешивании добавить фазу D и еще раз гомогенизировать.
Пример 20: Применение КСД в лосьоне для защиты от солнца - тип масло-в-воде


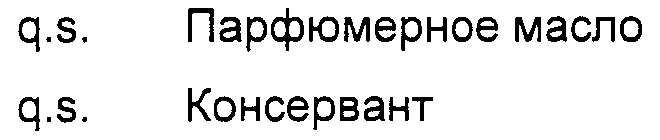
Изготовление: Фазу А нагреть до температуры около 80°С, при помешивании добавить фазу В и гомогенизировать в течение 3 минут. Фазу С также нагреть до температуры 80°С и при помешивании добавить в комбинированные фазы А и В. Охладить до температуры около 40°С, при помешивании добавить фазу D и еще раз гомогенизировать.
Пример 21: Применение КСД в бальзаме для ног


Изготовление: Компоненты фаз А и В отдельно друг от друга нагреть до температуры около 80°С, Фазу В при помешивании добавить в фазу А и гомогенизировать. При помешивании охладить до температуры около 40°С, добавить фазы С и D и кратковременно гомогенизировать. При помешивании охладить до комнатной температуры.
Пример 22: Применение КСД в эмульсии вода-в-масле с бисабололом


Изготовление: Фазы А и В отдельно друг от друга нагреть до температуры около 85°С. Фазу В при помешивании добавить в фазу А и гомогенизировать. При помешивании охладить до температуры около 40°С, добавить фазу С и еще раз кратковременно гомогенизировать. При помешивании охладить до комнатной температуры.
Составление рецептур для патента кератинсвязывающий домен
Пример 23: Пенокондиционер с фиксатором


Изготовление: Компоненты А взвесить, перемешивать до полного растворения и расфасовать.
Пример 24: Пенокондиционер


Изготовление: Компоненты А взвесить, перемешивать до полного растворения и расфасовать.
Пример 25: Пенокондиционер

Изготовление: Компоненты А взвесить, перемешивать до полного растворения и расфасовать.
Пример 26: Модельная пена

Изготовление: Смешать компоненты фазы А. Последовательно добавлять компоненты В и растворить. Расфасовать с фазой С.
Пример 27: Модельная пена


Изготовление: Смешать компоненты фазы А. Последовательно добавлять компоненты В и растворить. Расфасовать с фазой С.
Пример 28: Модельная пена

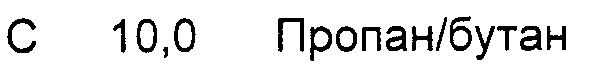
Изготовление: Смешать компоненты фазы А. Компоненты фазы В растворить, затем фазу В при помешивании добавить в фазу А. Установить значение рН 6-7, расфасовать с фазой С.
Пример 29: Модельная пена


Изготовление: Смешать компоненты фазы А. Последовательно добавлять компоненты В и растворить. Фазу С растворить в смеси фаз А и В, затем установить значение рН 6-7. Расфасовать с фазой D
Пример 30: Модельная пена


Изготовление: Смешать компоненты фазы А. Последовательно добавлять компоненты В и растворить. Фазу С растворить в смеси фаз А и В, затем установить значение рН 6-7. Расфасовать с фазой D.
Пример 31: Модельная пена


Изготовление: Солюбилизировать фазу А. Фазу В добавить в фазу А и добиться растворения. Установить значение рН 6-7, расфасовать с фазой С.
Пример 32: Модельная пена


Изготовление: Солюбилизировать фазу А. Фазу В добавить в фазу А и добиться растворения. Установить значение рН 6-7, расфасовать с фазой С.
Пример 32: Модельная пена


Изготовление: Солюбилизировать фазу А. Фазу В добавить в фазу А и добиться растворения. Установить значение рН 6-7, расфасовать с фазой С.
Пример 33: Модельная пена


Изготовление: Смешать компоненты фазы А. Последовательно добавлять компоненты В и растворить. Расфасовать с фазой С.
Пример 34: Шампунь для ухода


Изготовление: Компоненты фазы А смешать и растворить. Лимонной кислотой установить значение рН 6-7.
Пример 35: Гель для душа


Изготовление: Компоненты фазы А смешать и растворить. Лимонной кислотой установить значение рН 6-7.
Пример 36: Шампунь


Изготовление: Компоненты фазы А смешать и растворить. Лимонной кислотой установить значение рН 6-7.
Пример 37: Шампунь


Изготовление: Компоненты фазы А отвесить и растворить. Установить значение рН 6-7. Добавить фазу В и нагреть до температуры около 50°С. При помешивании охладить до комнатной температуры.
Пример 38: Увлажняющий крем для ухода за телом


Изготовление: Фазы А и В отдельно нагреть до температуры около 80°С. Фазу В кратковременно предварительно гомогенизировать, затем фазу В при помешивании добавить в А и снова гомогенизировать. Охладить до температуры около 40°С, добавить фазу С и еще раз хорошенько гомогенизировать. Лимонной кислотой установить значение рН 6-7.
Пример 39: Увлажняющий крем для ухода за телом


Изготовление: Фазы А и В отдельно нагреть до температуры около 80°С. Фазу В при помешивании добавить в фазу А и гомогенизировать. При помешивании охладить до температуры около 40°С, добавить фазу С и снова гомогенизировать. При помешивании дать остыть до комнатной температуры.
Пример 40: Жидкое средство для снятия косметики - тип масло-в-воде


Изготовление: Фазы А и В отдельно нагреть до температуры около 80°С. Фазу В при помешивании добавить в фазу А и гомогенизировать. При помешивании охладить до температуры около 40°С, добавить фазы С и D и еще раз основательно гомогенизировать. При помешивании дать остыть до комнатной температуры.
Пример 41
В приведенных ниже рецептурах в качестве биологически активного вещества был использован 5-процентный водный раствор кератинсвязывающего домена или кератинсвязывающей эффекторной молекулы. Указанные данные являются массовыми частями.
Прозрачный шампунь
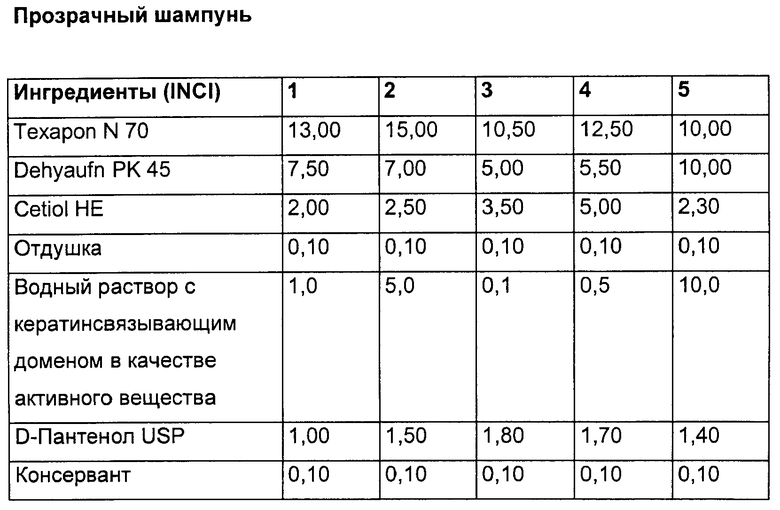
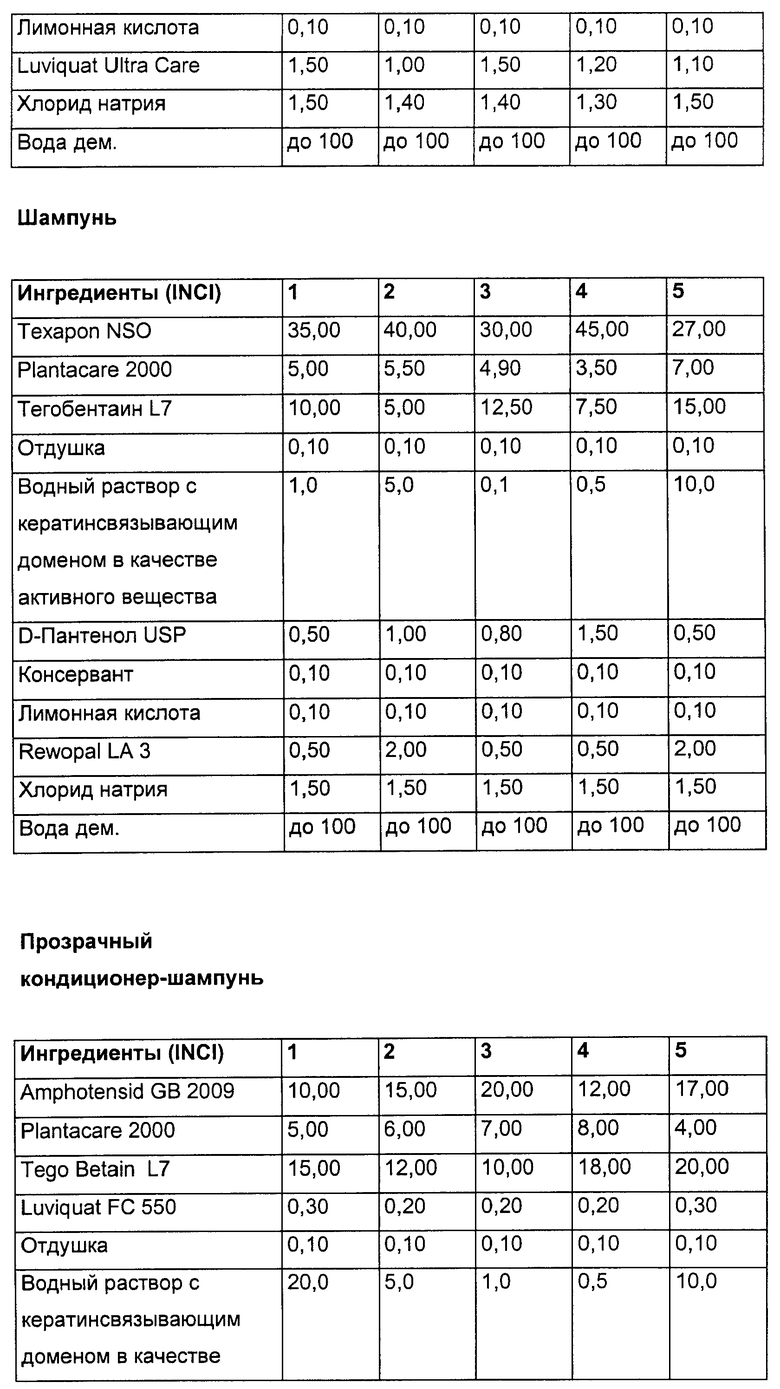
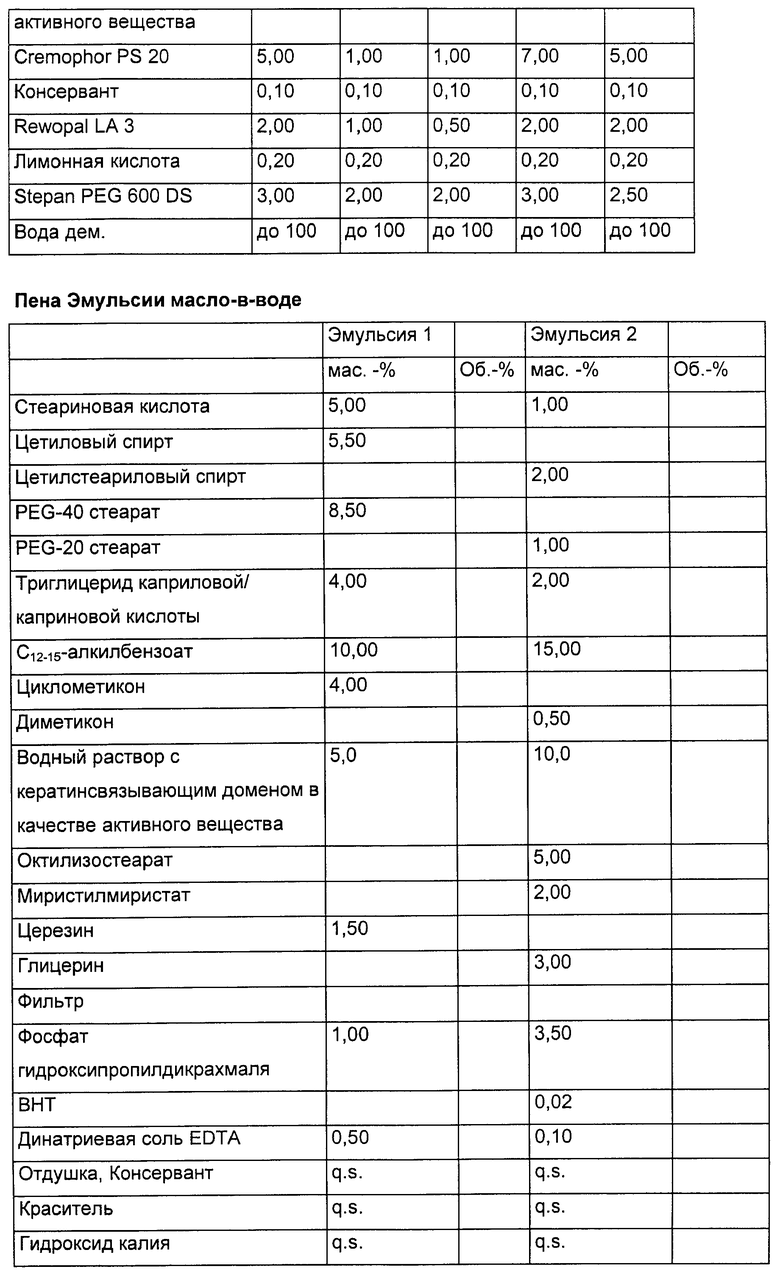
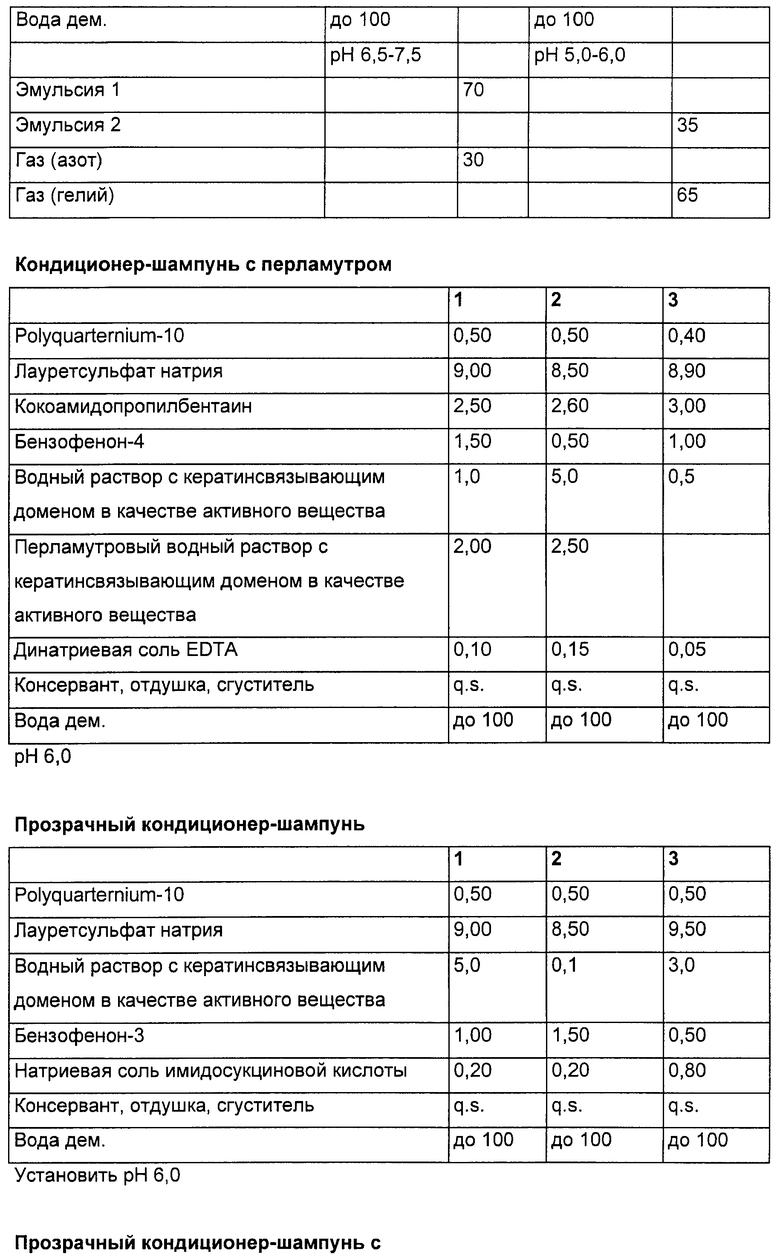
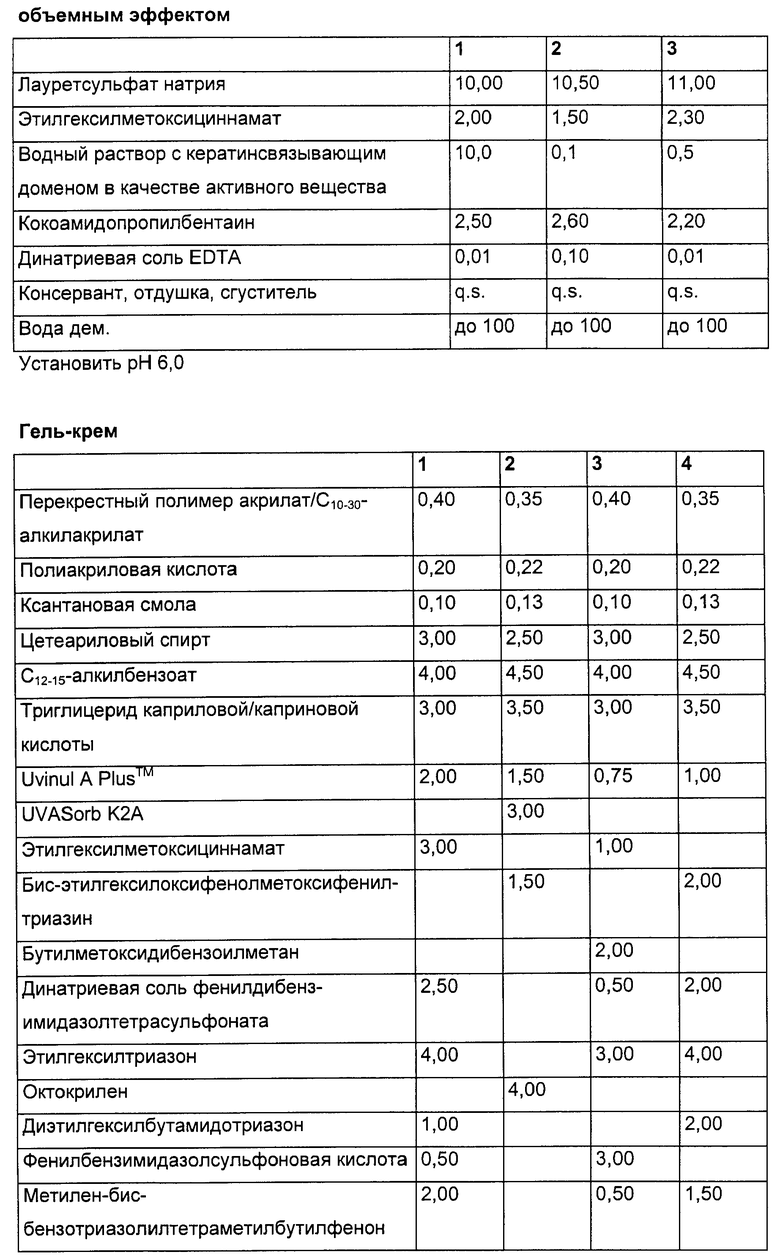
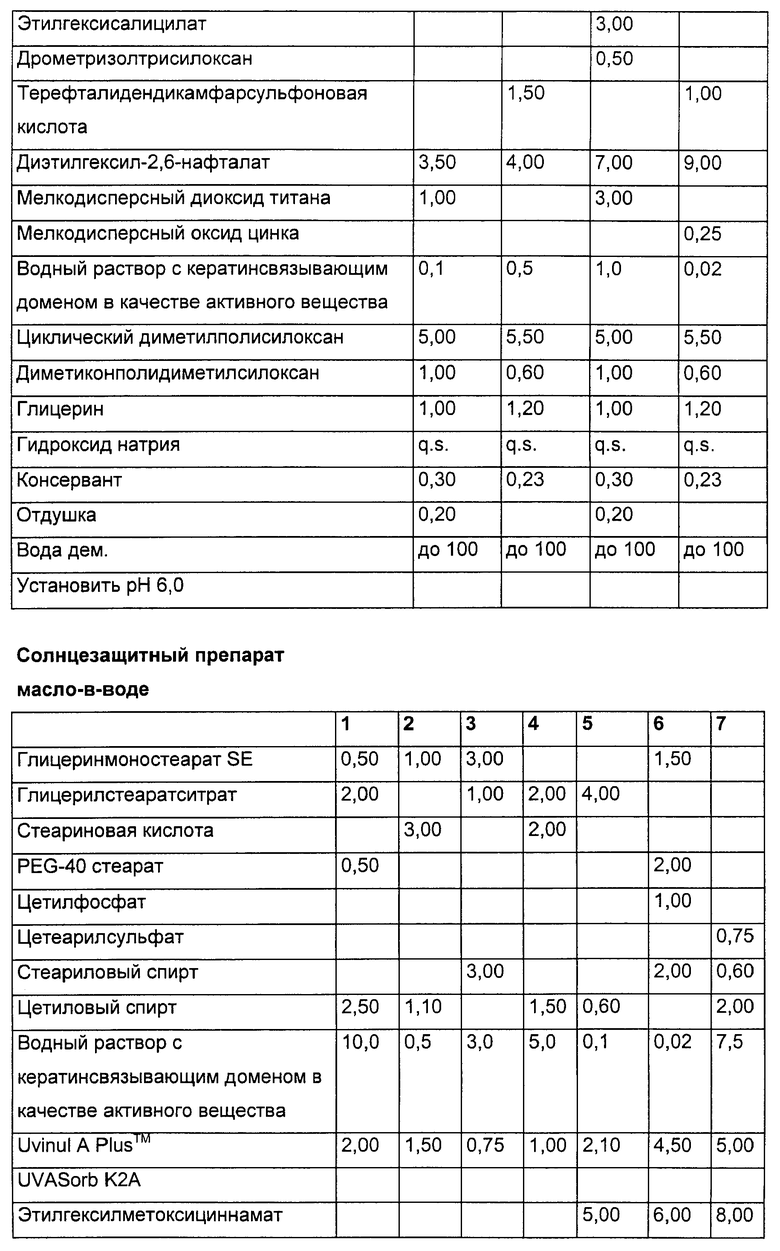
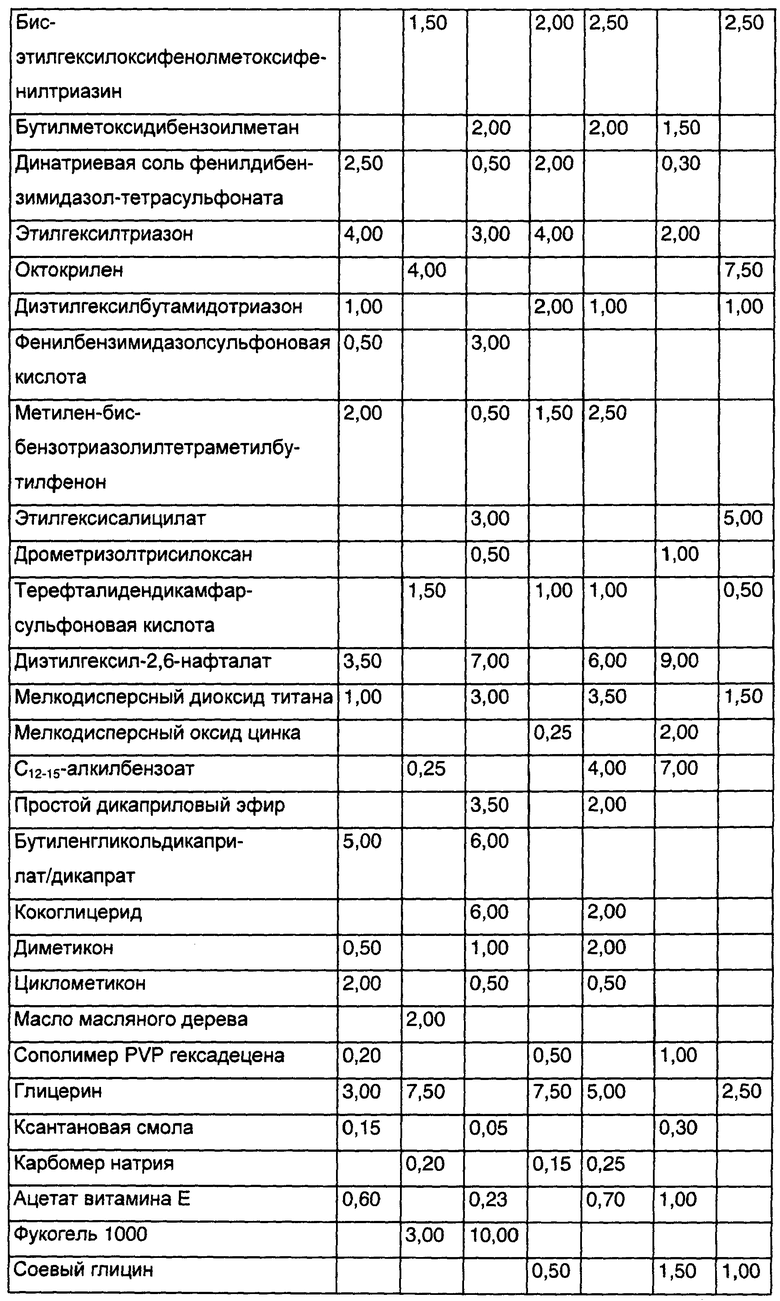
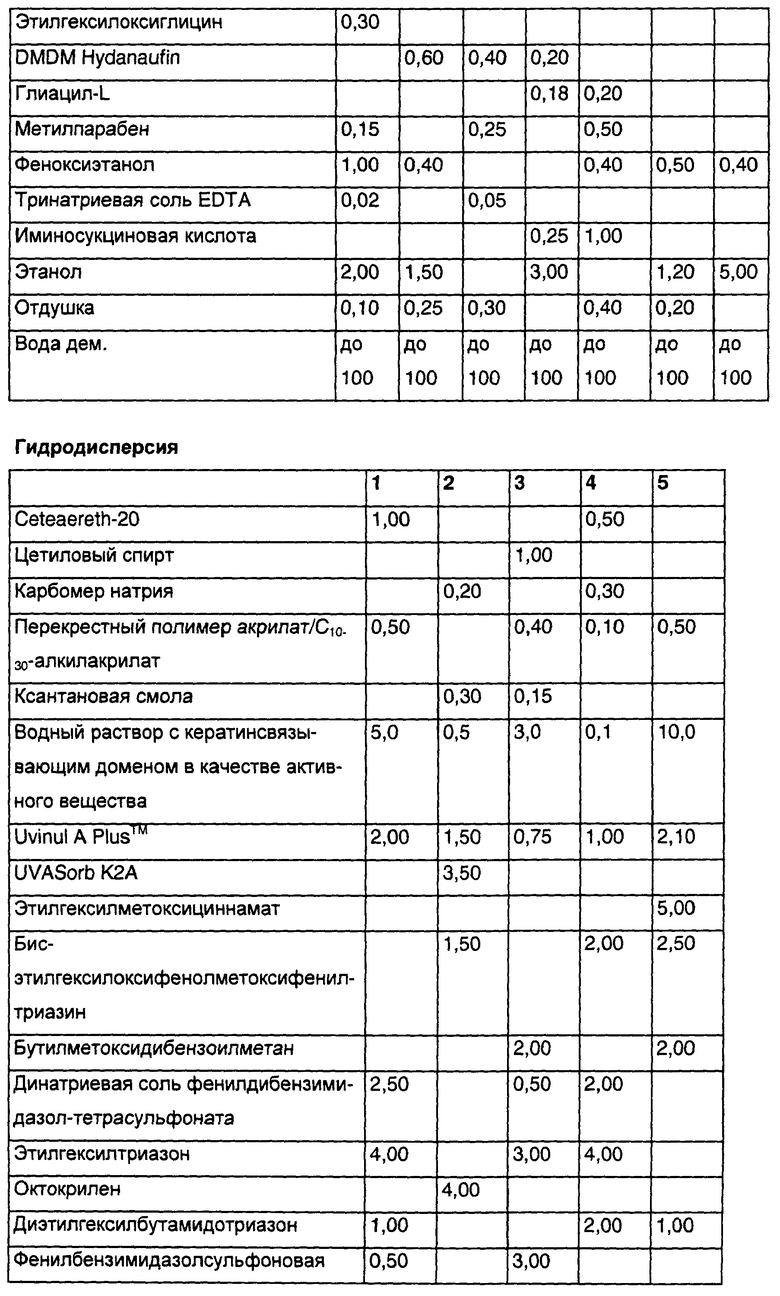
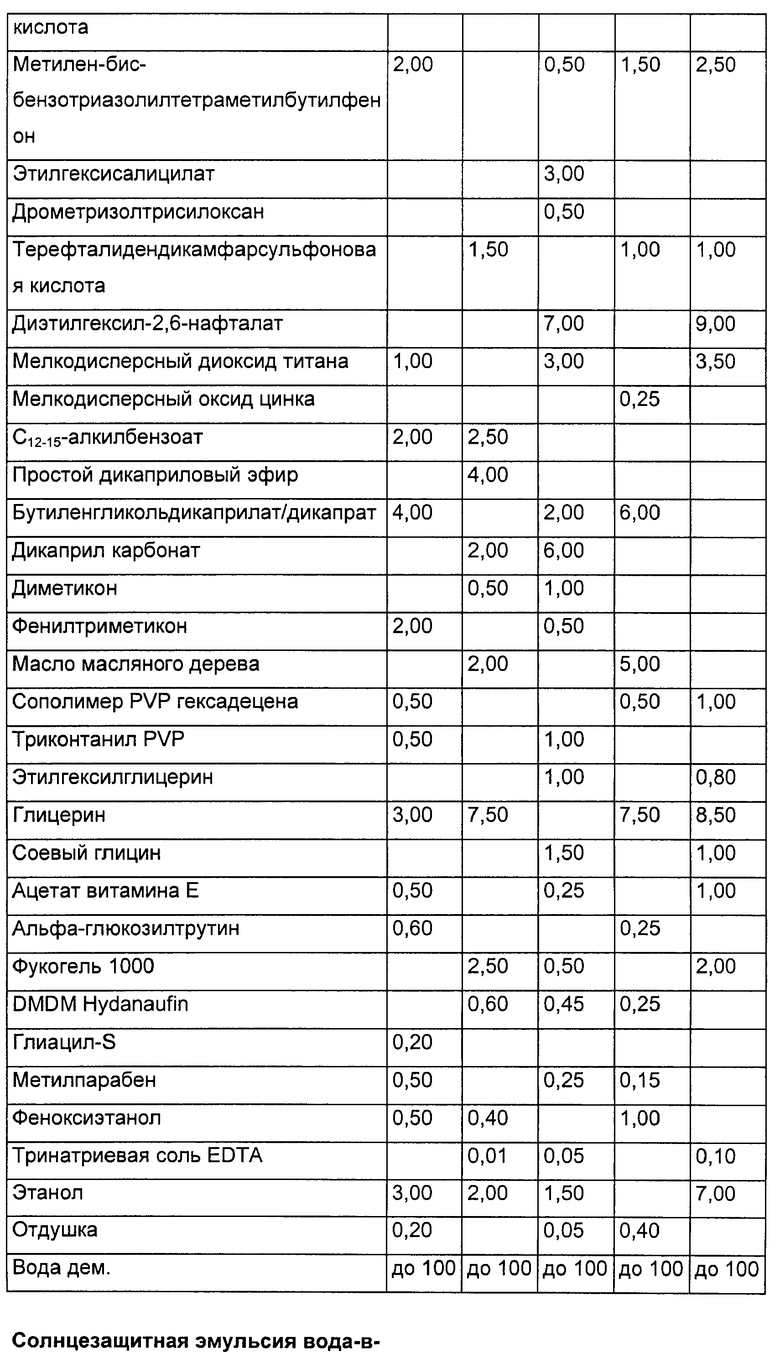
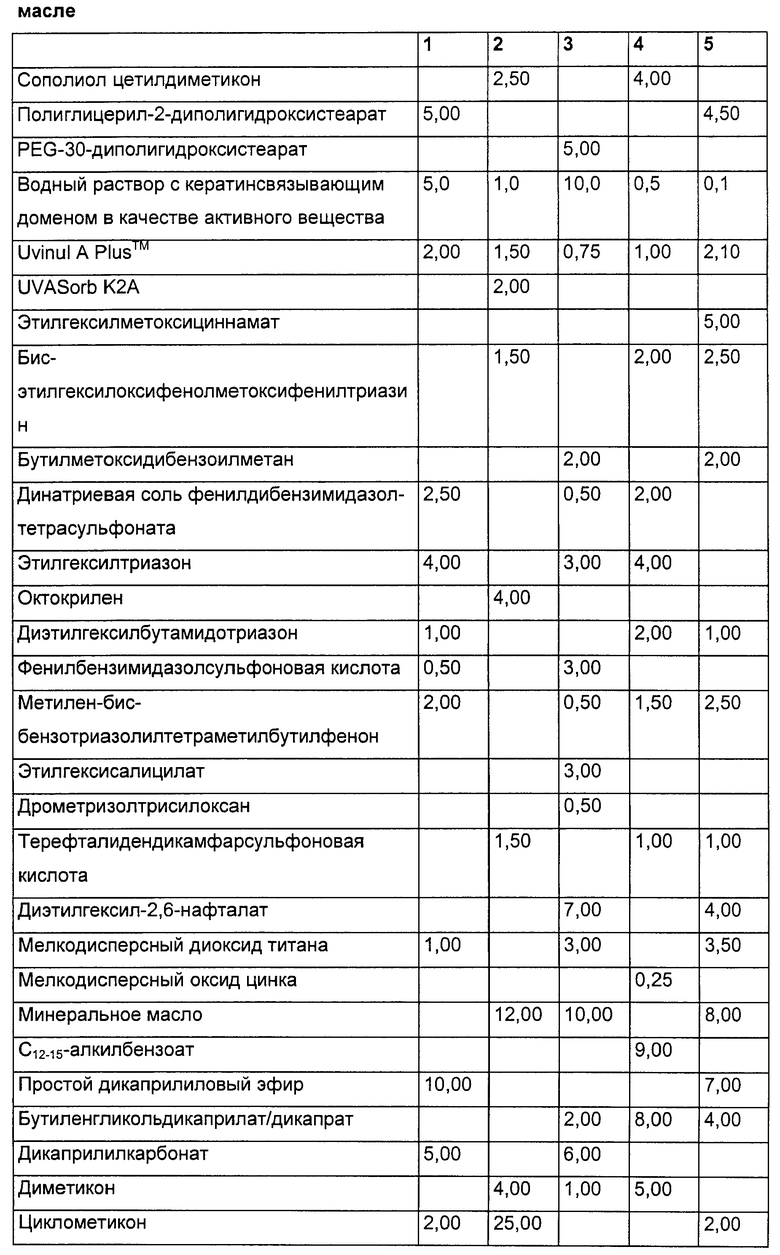
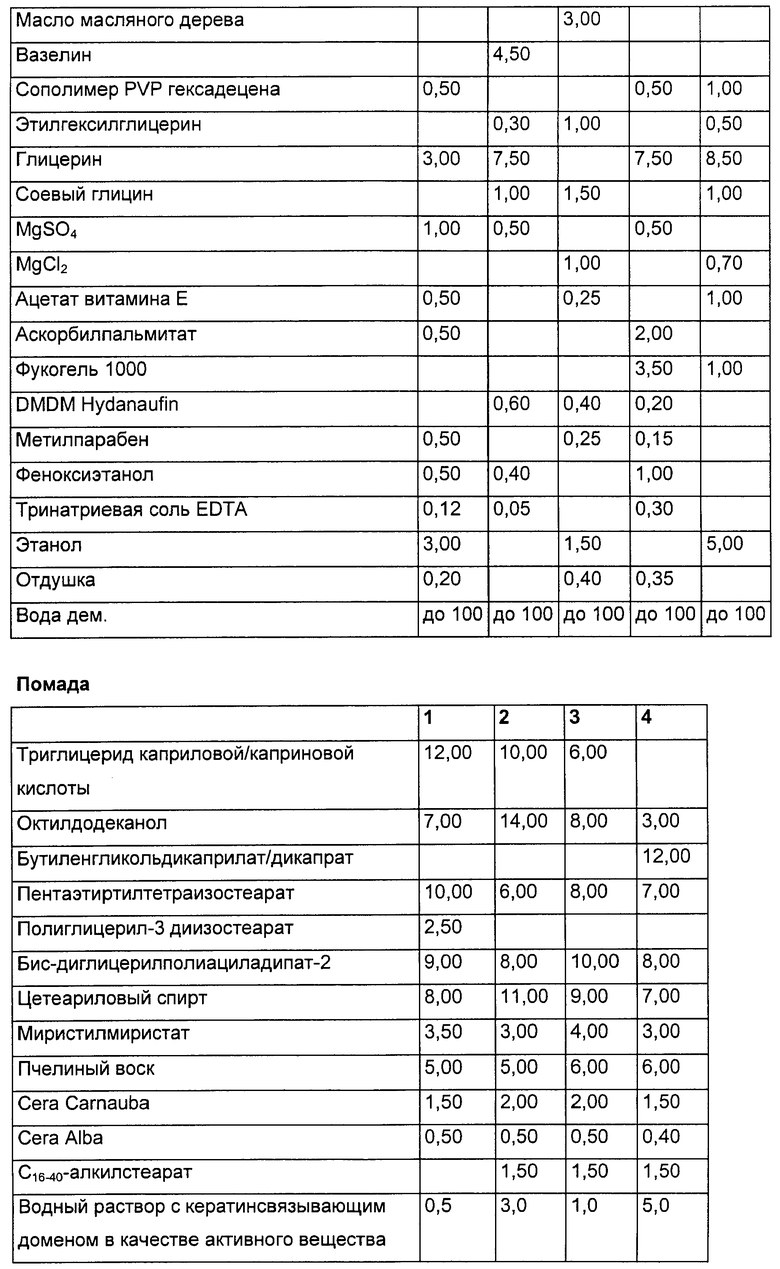
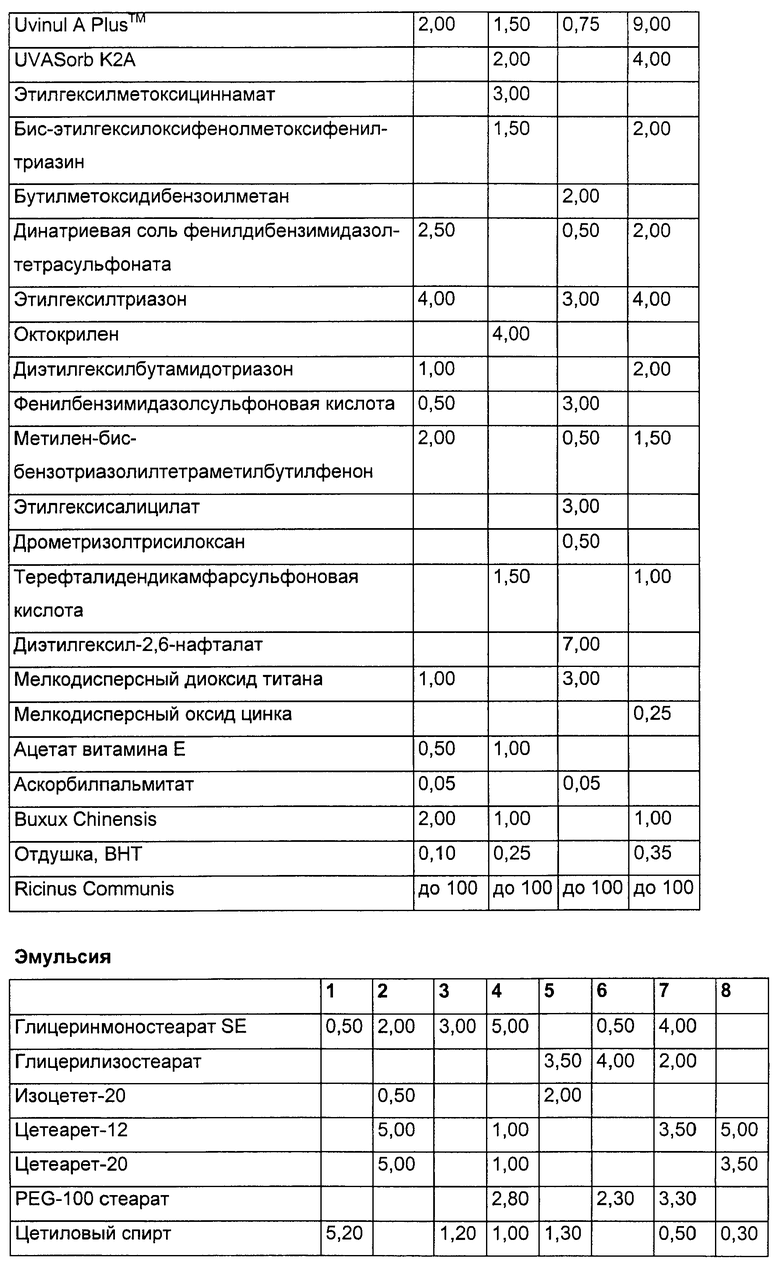
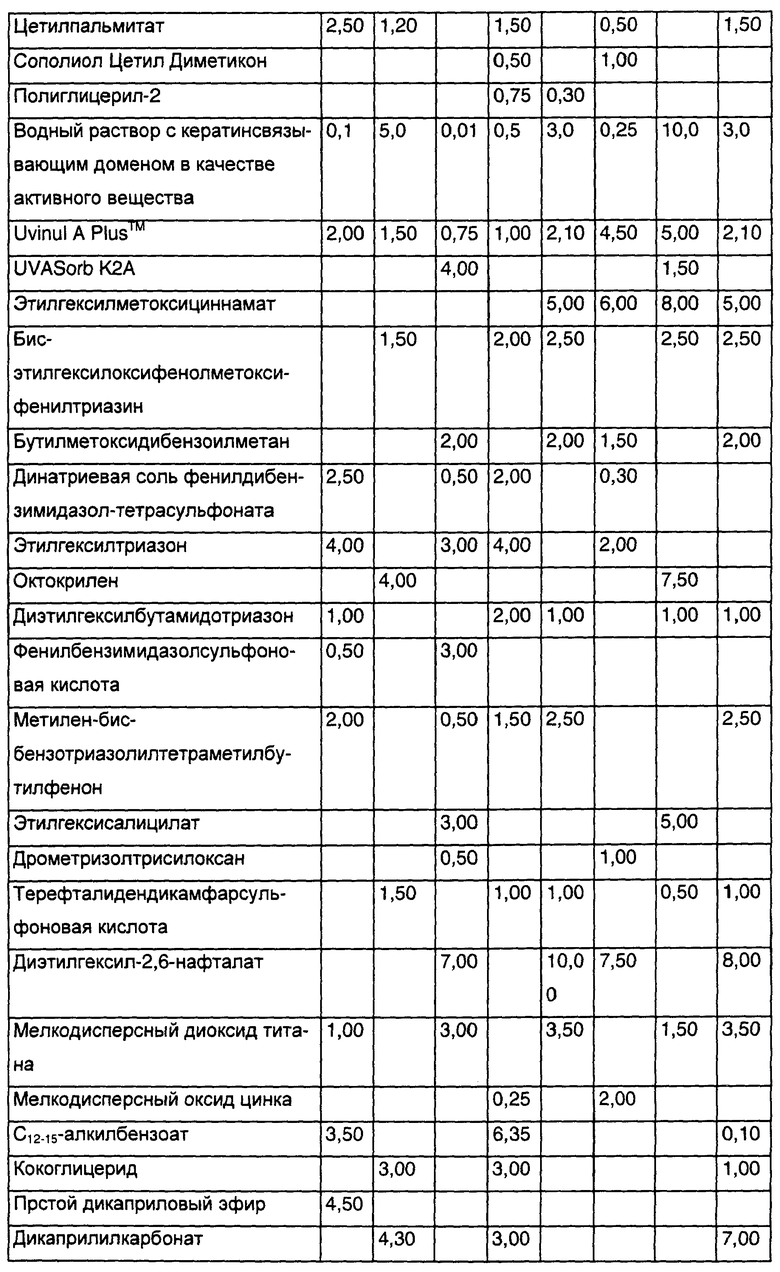
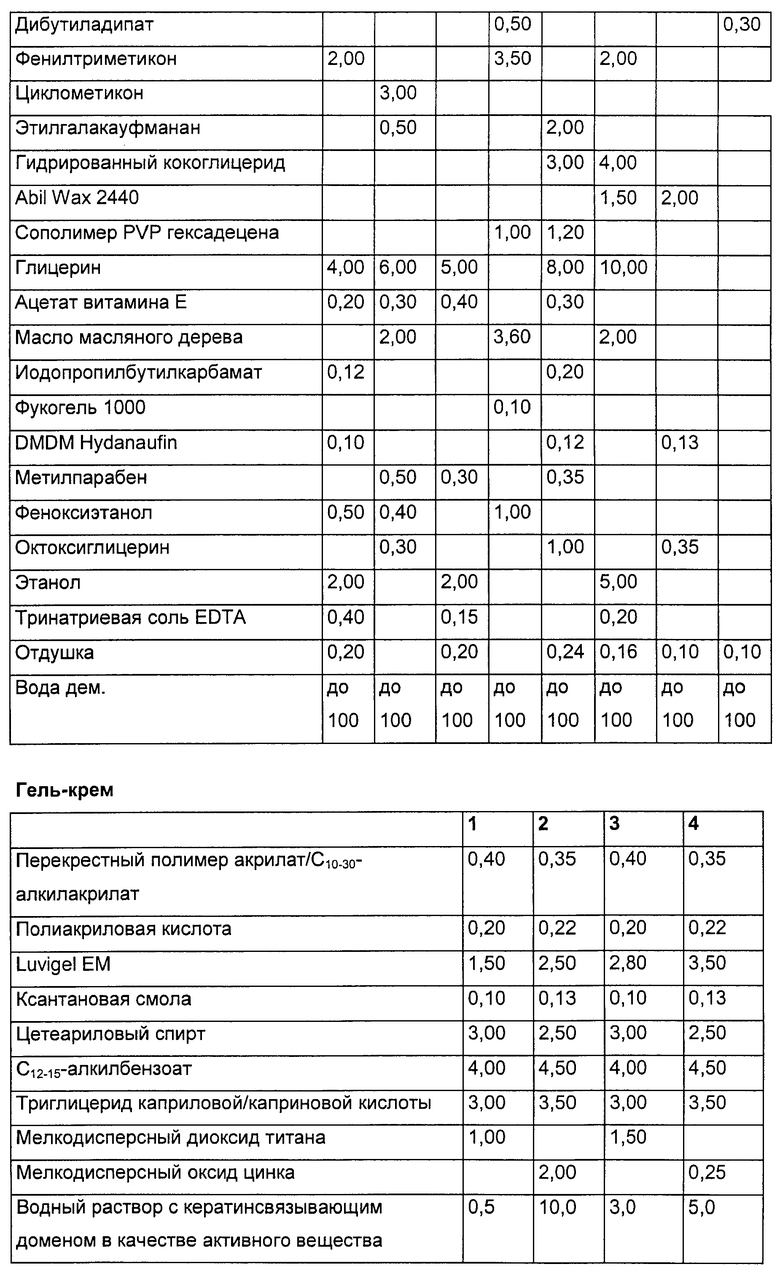
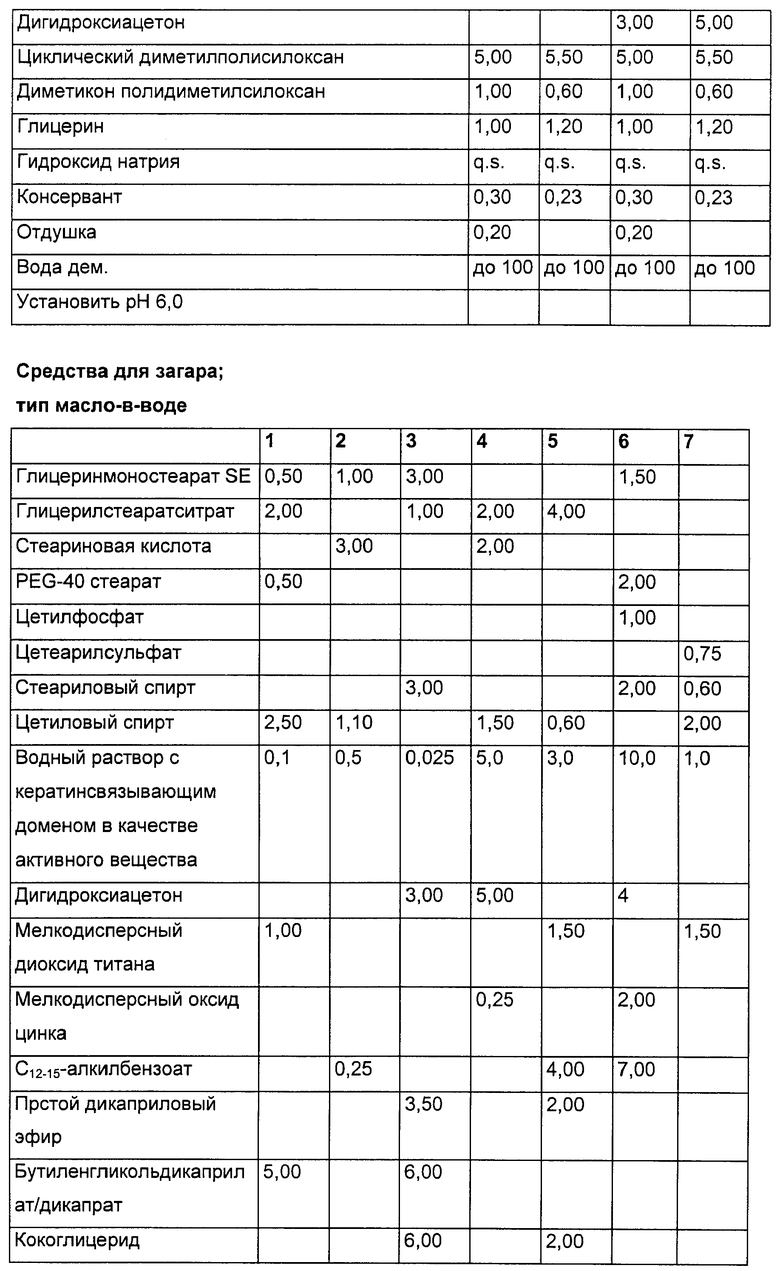
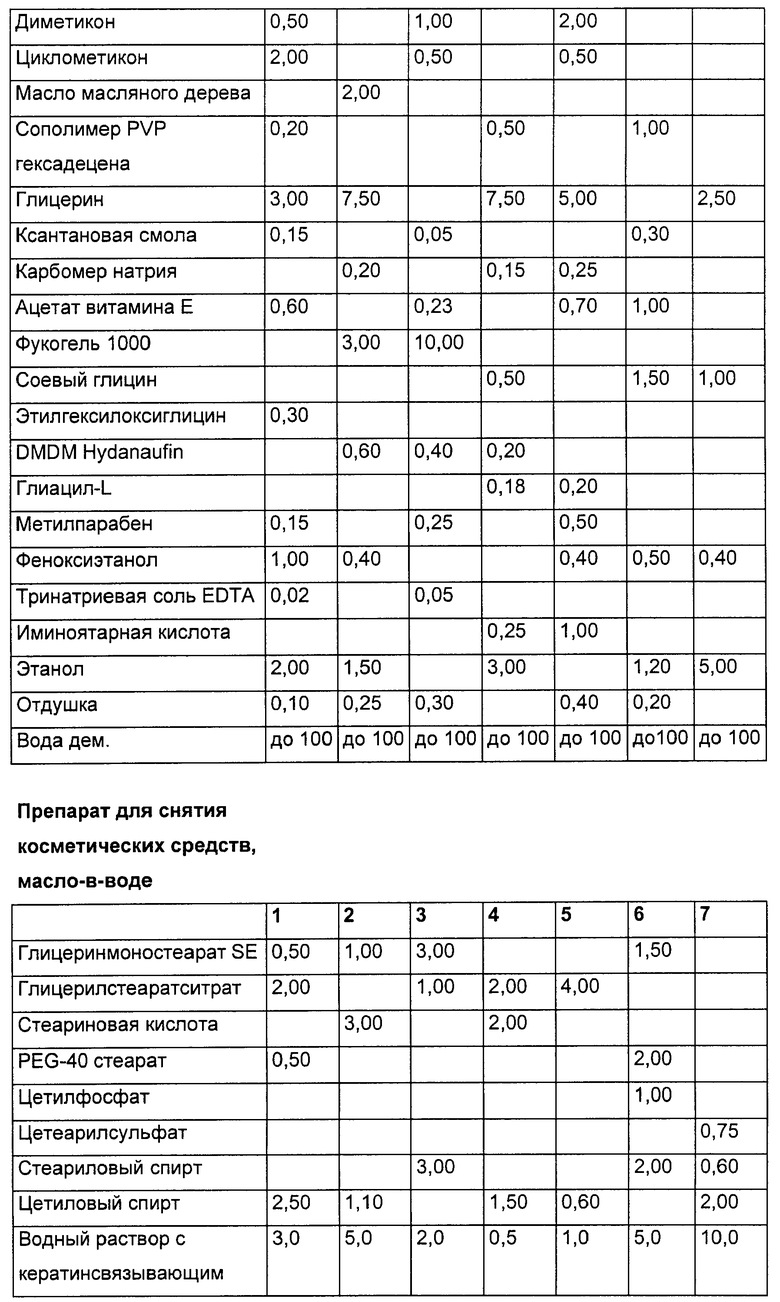
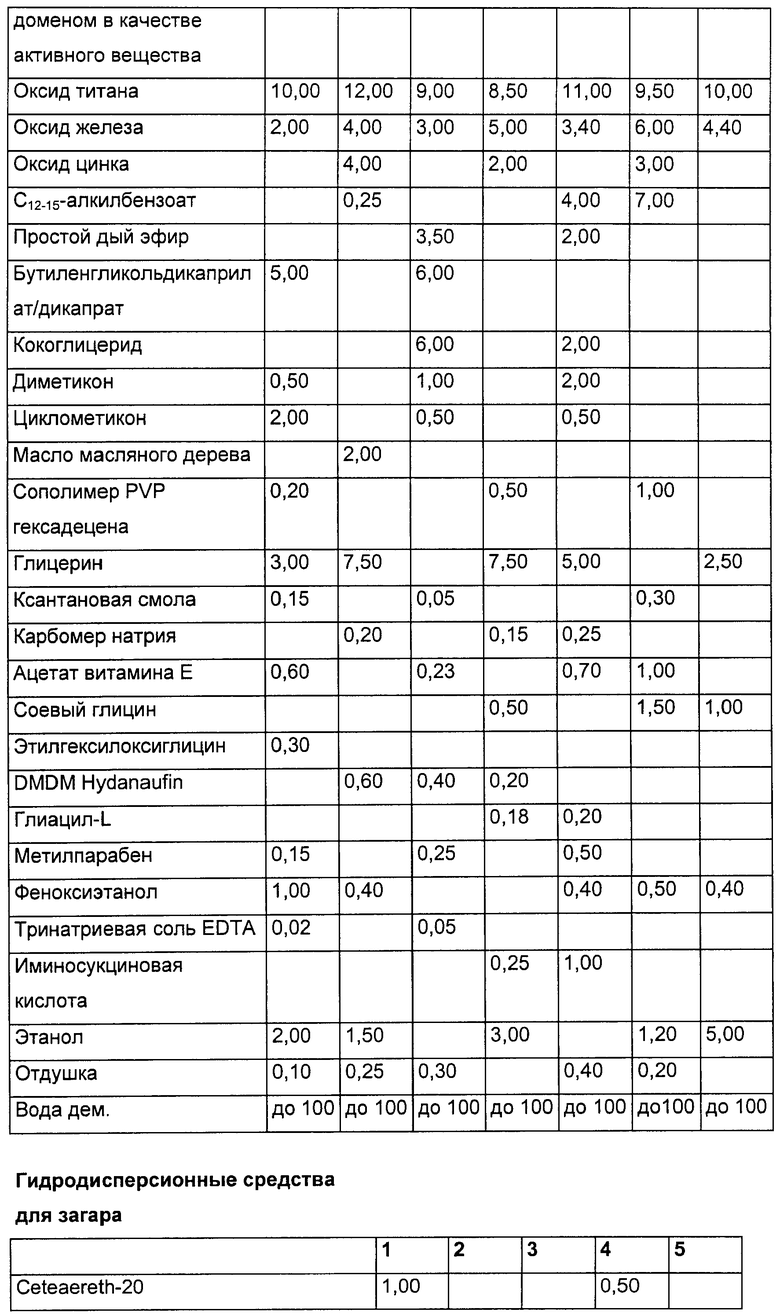
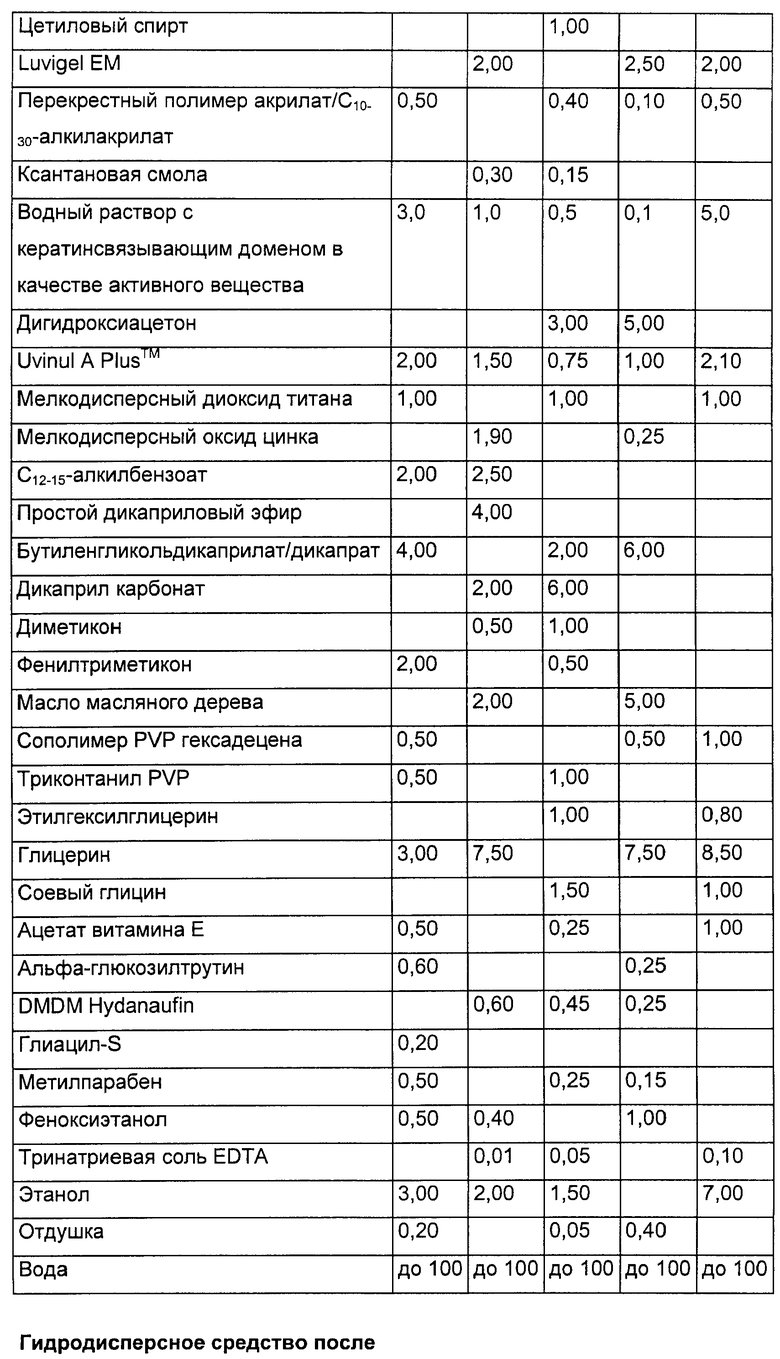
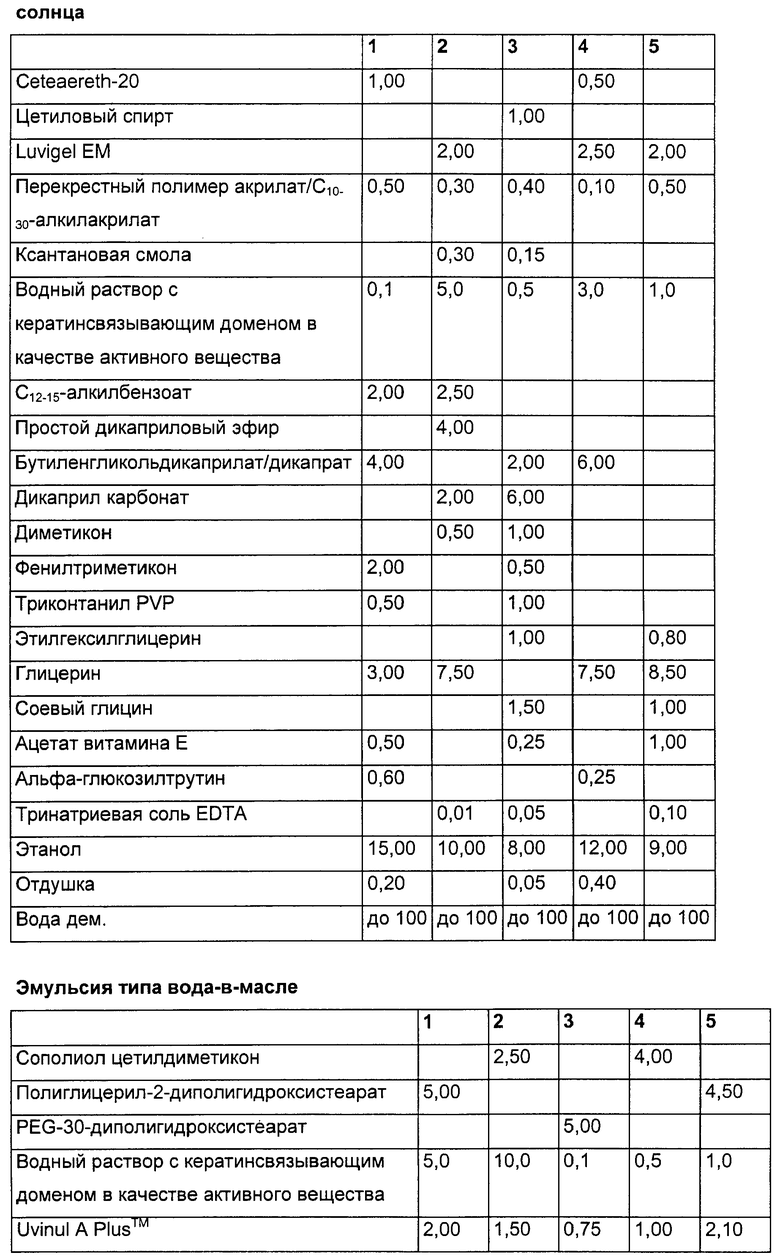
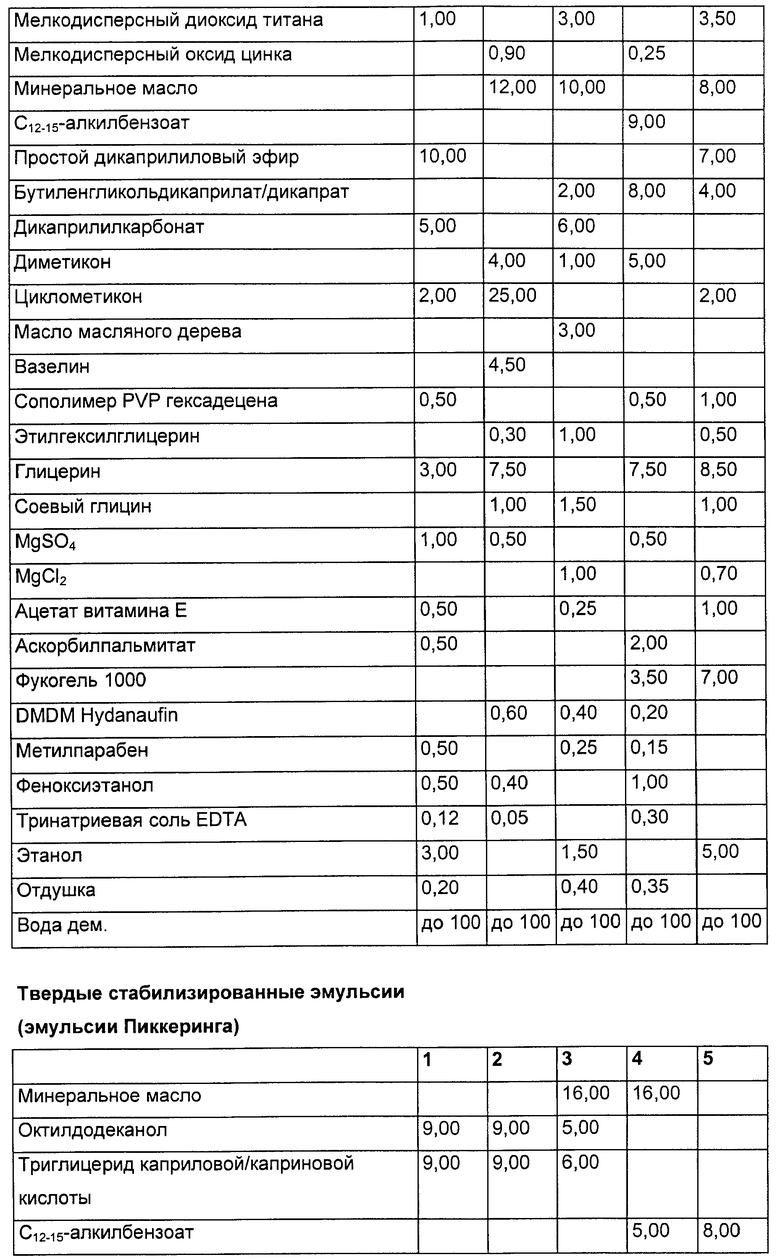
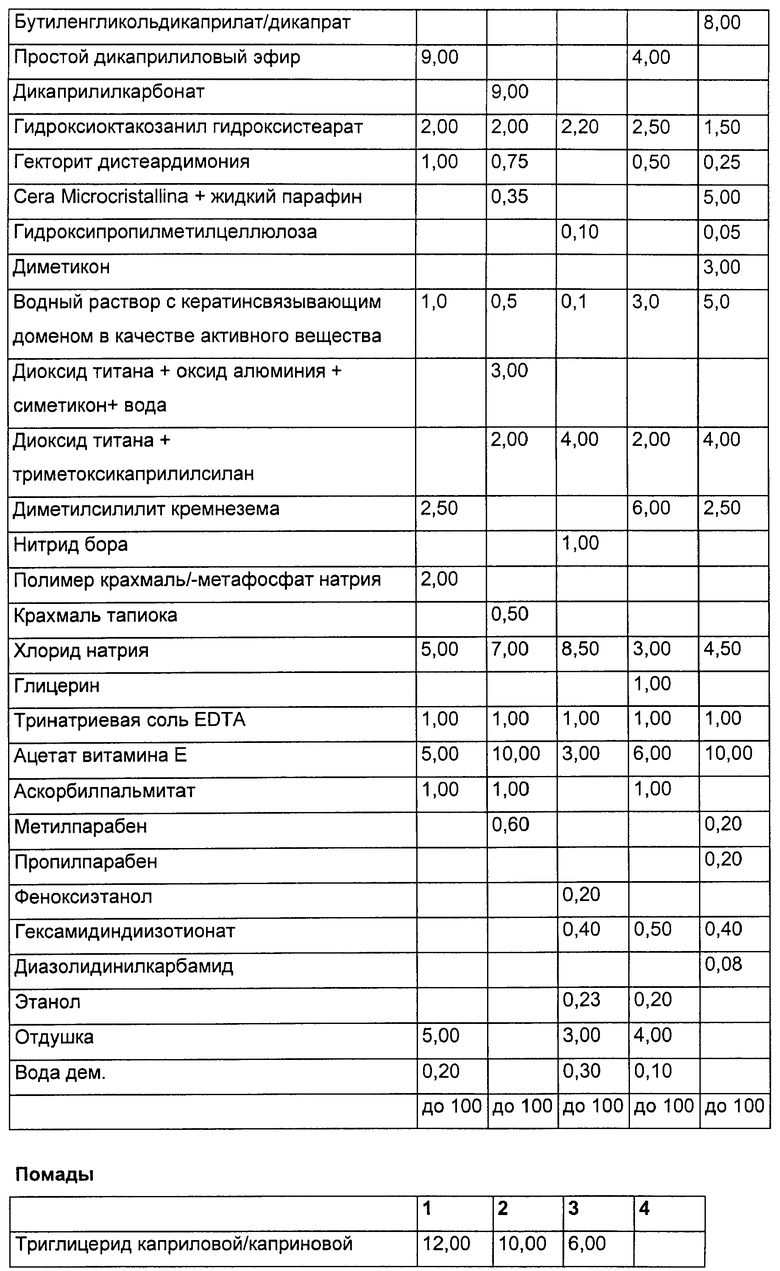
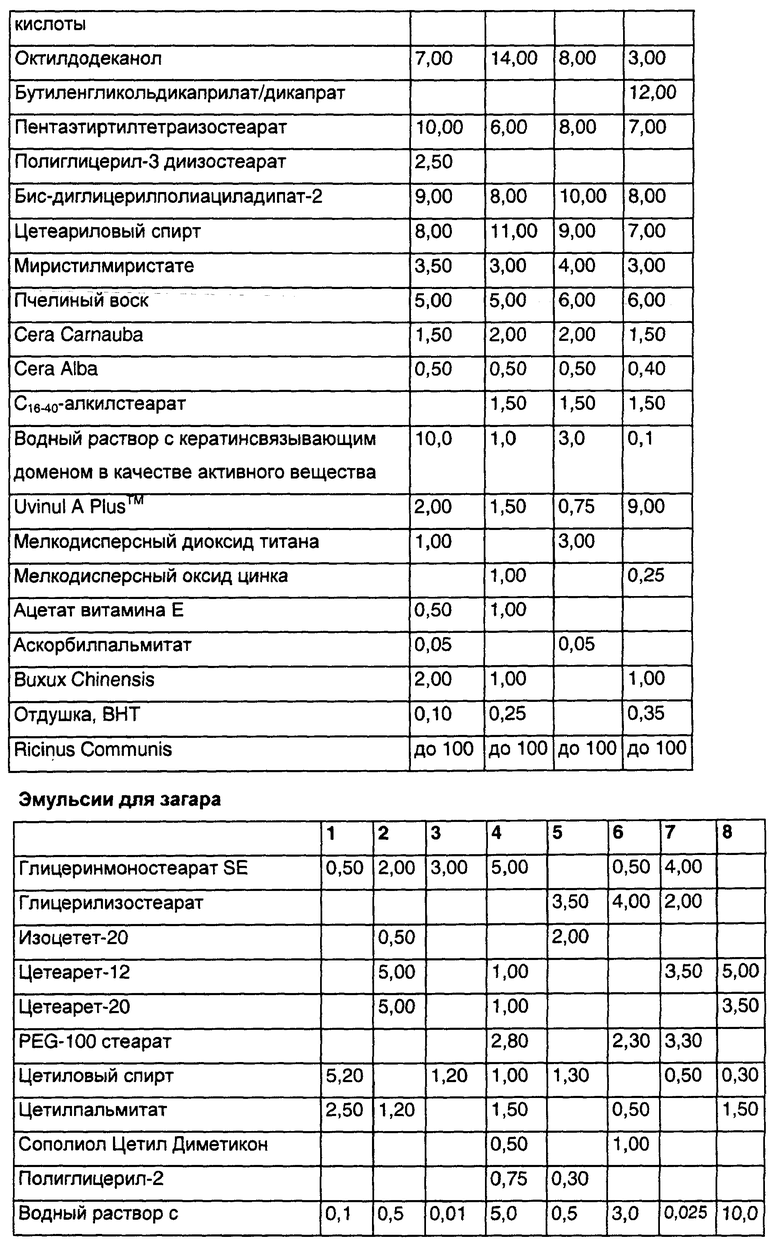
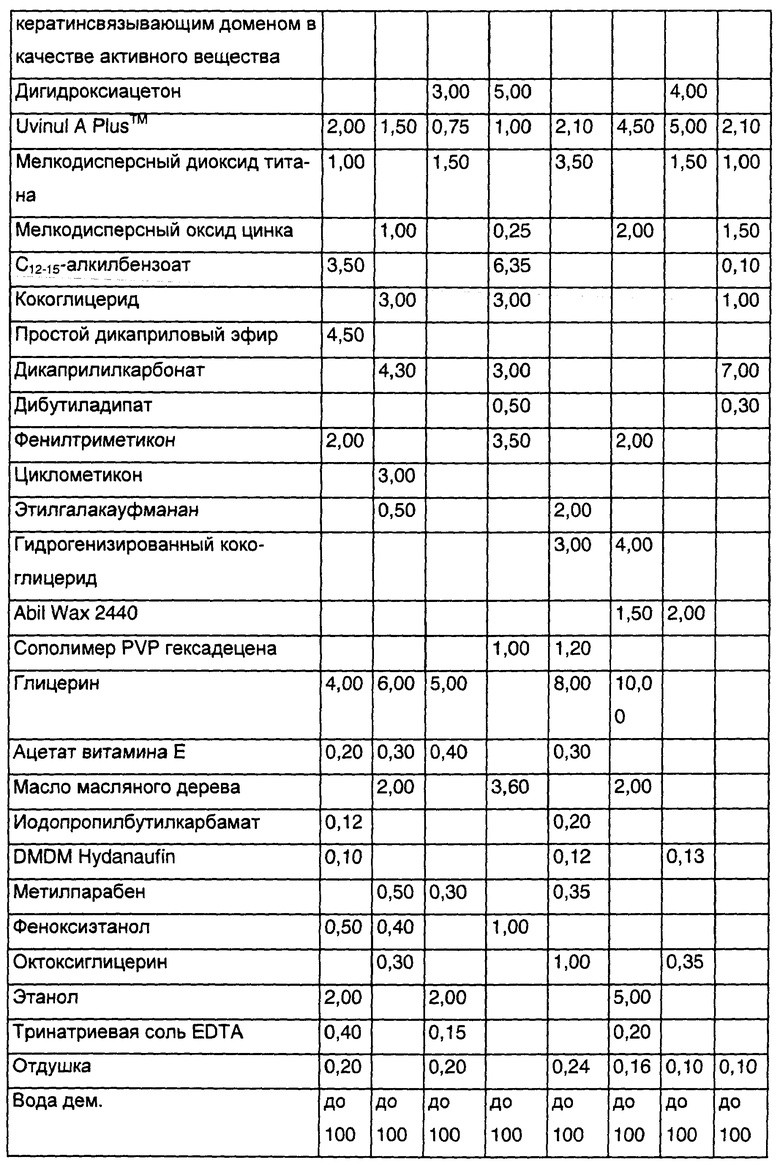
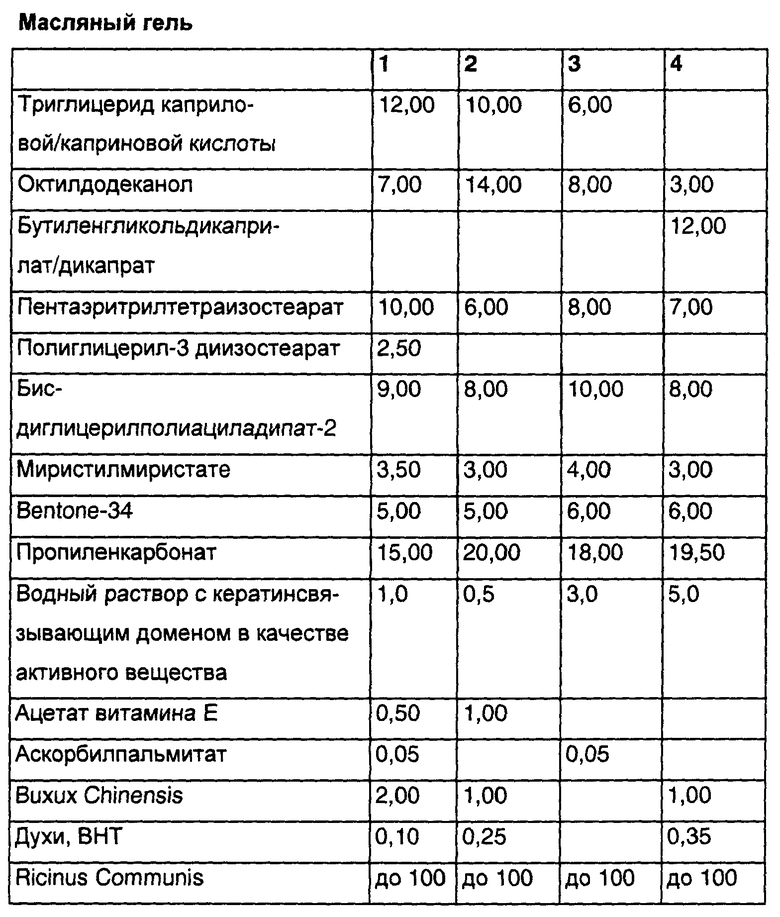


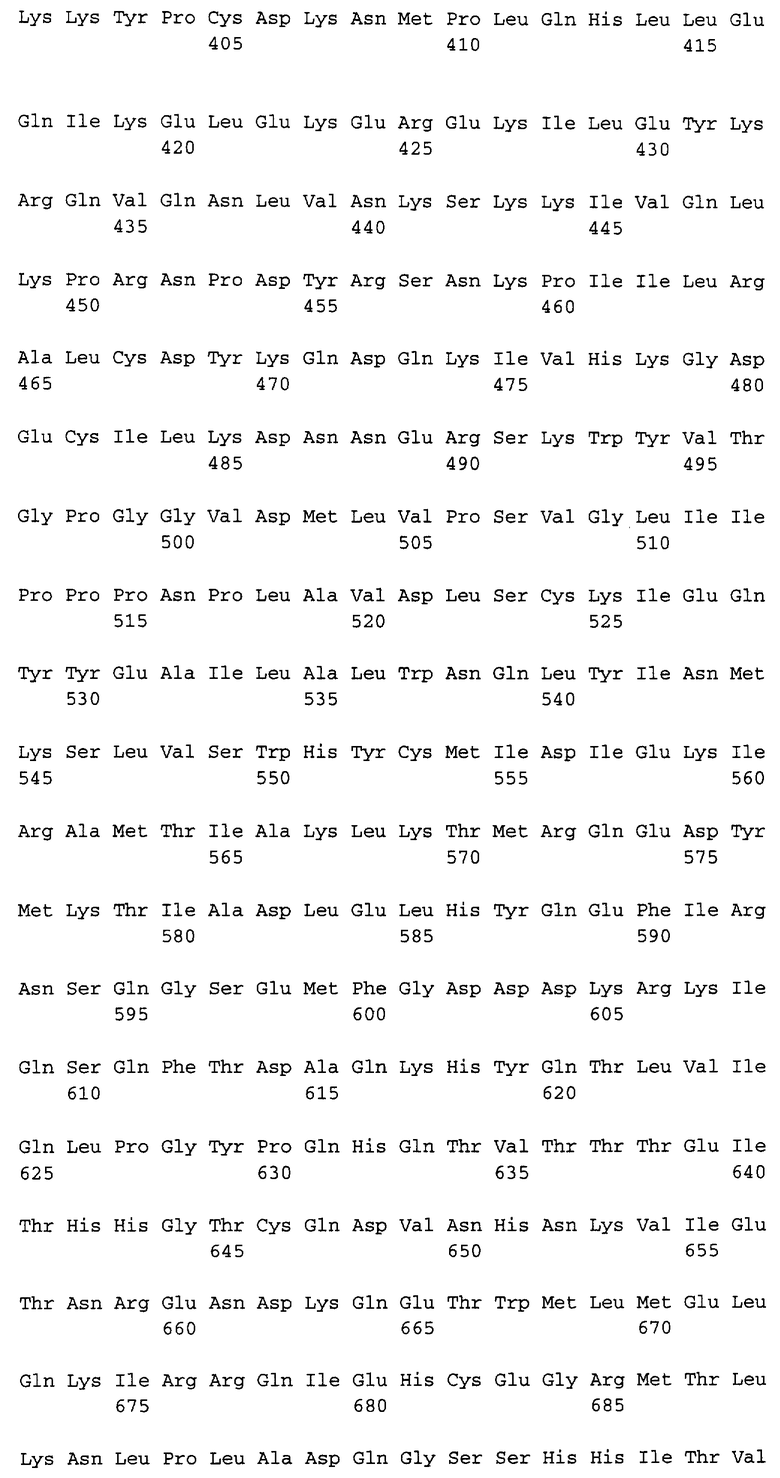

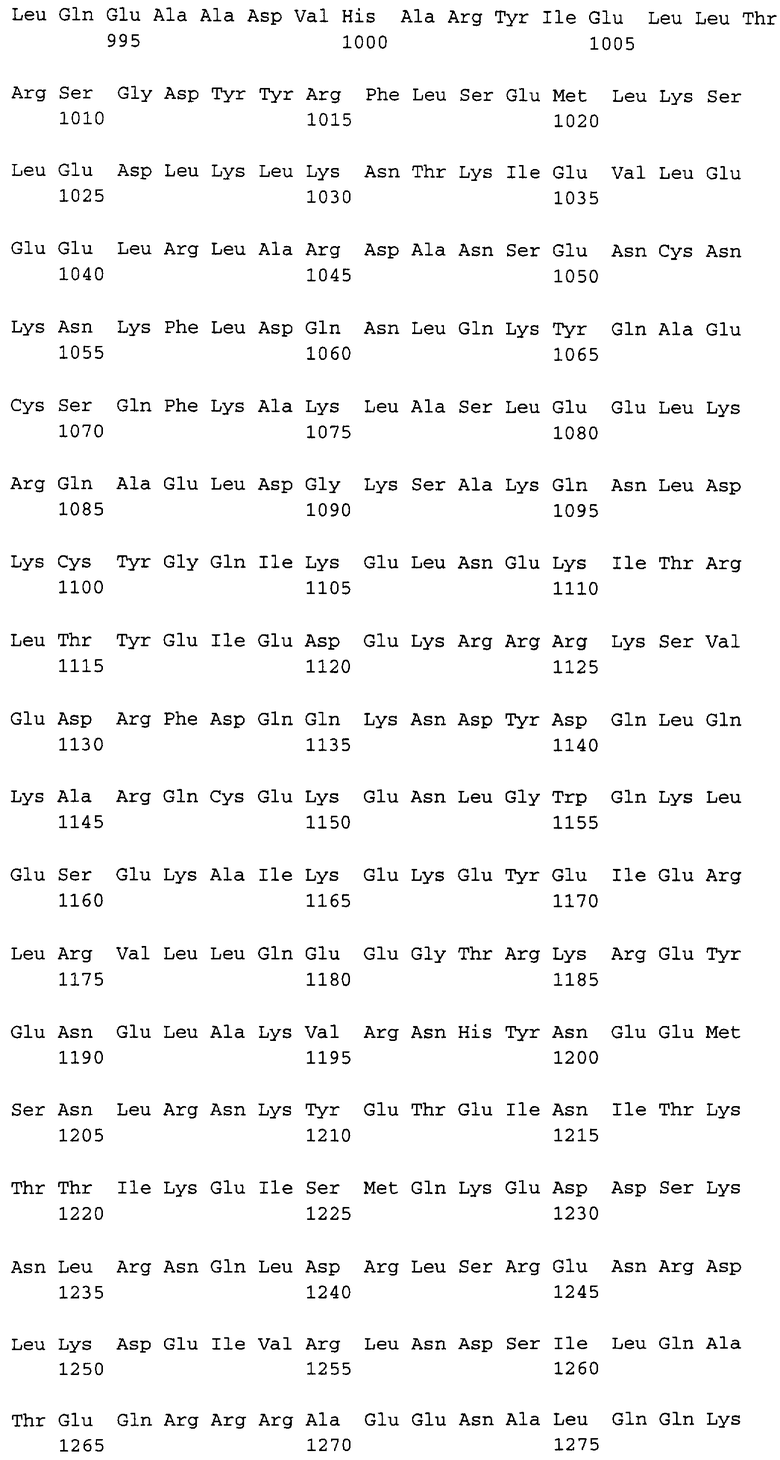
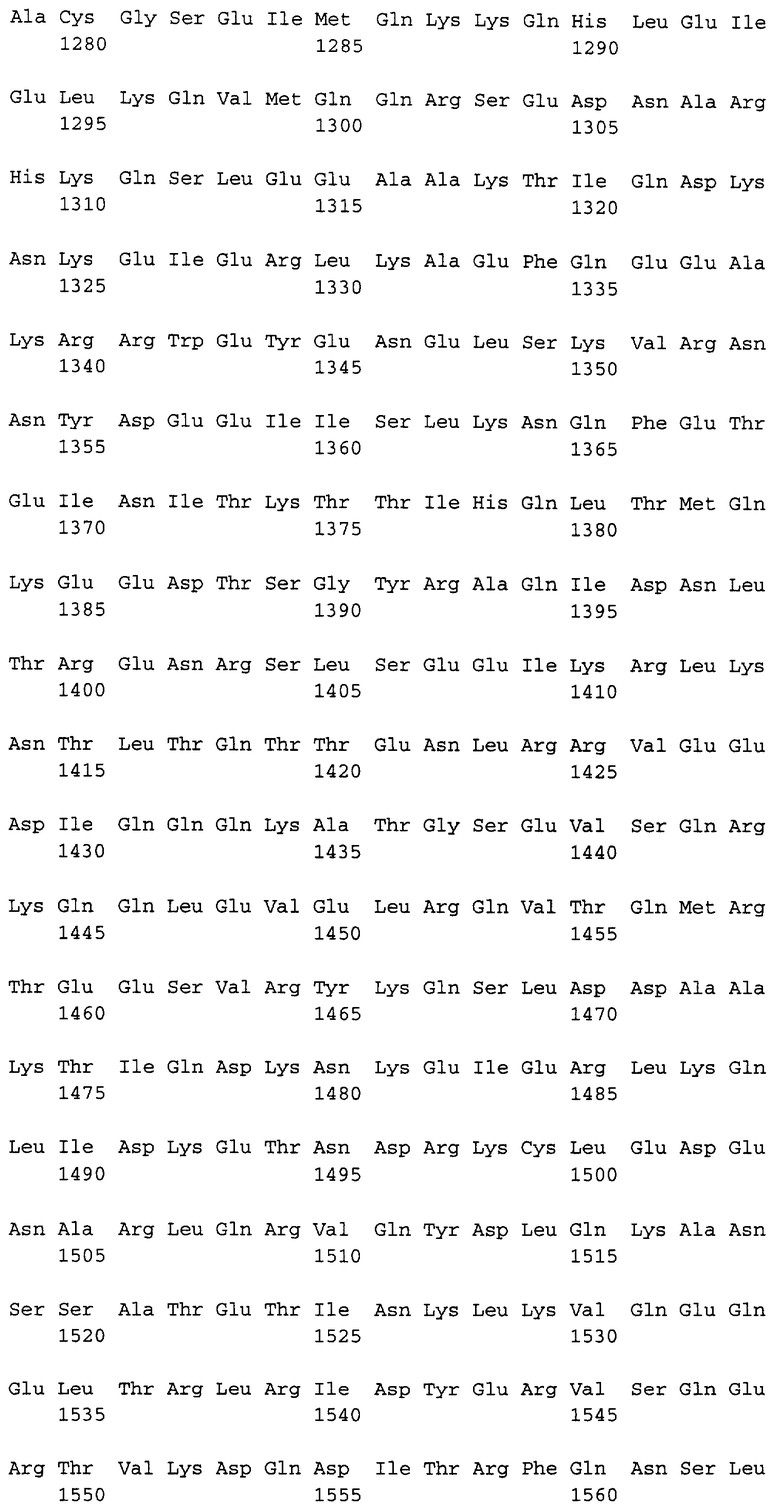
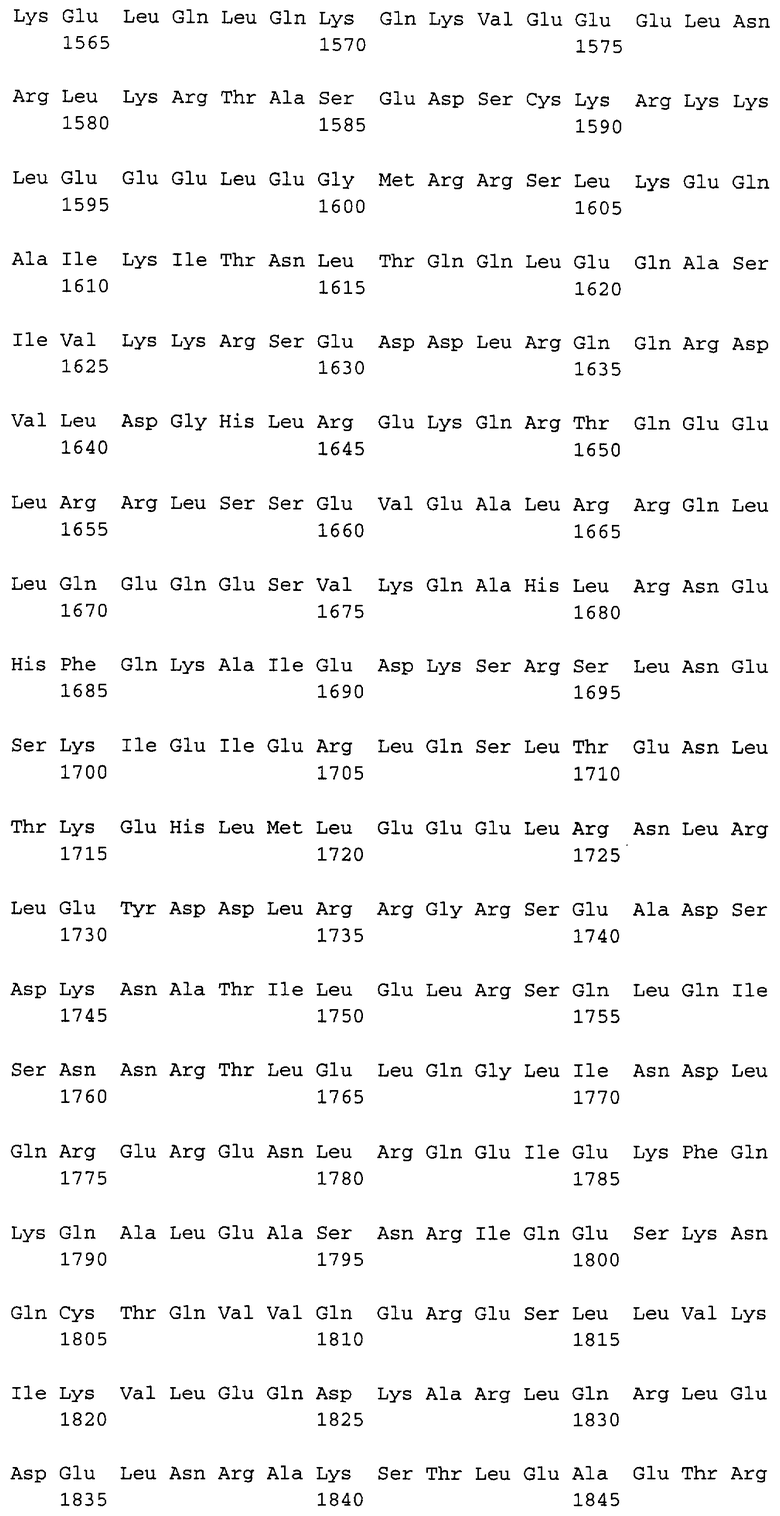
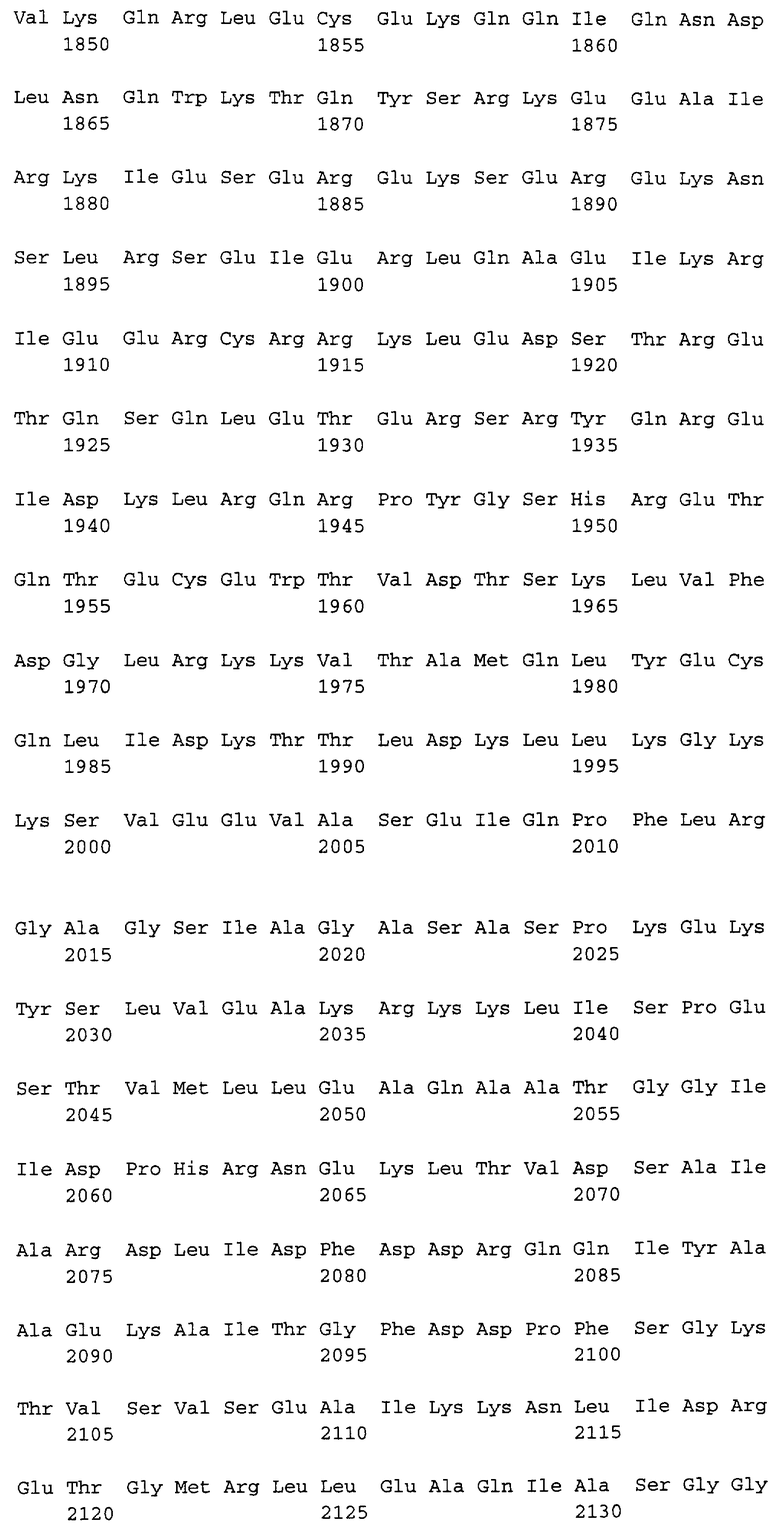
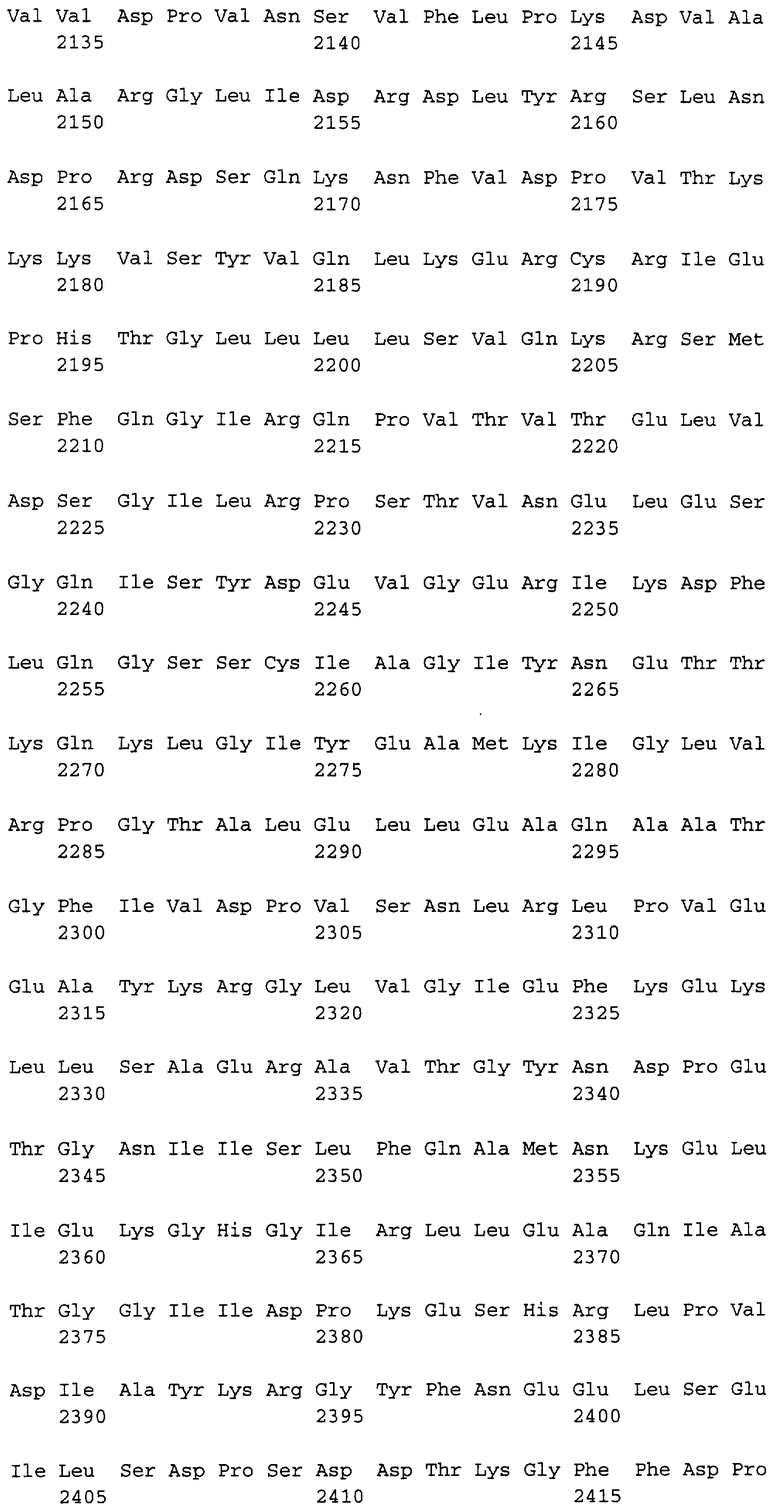
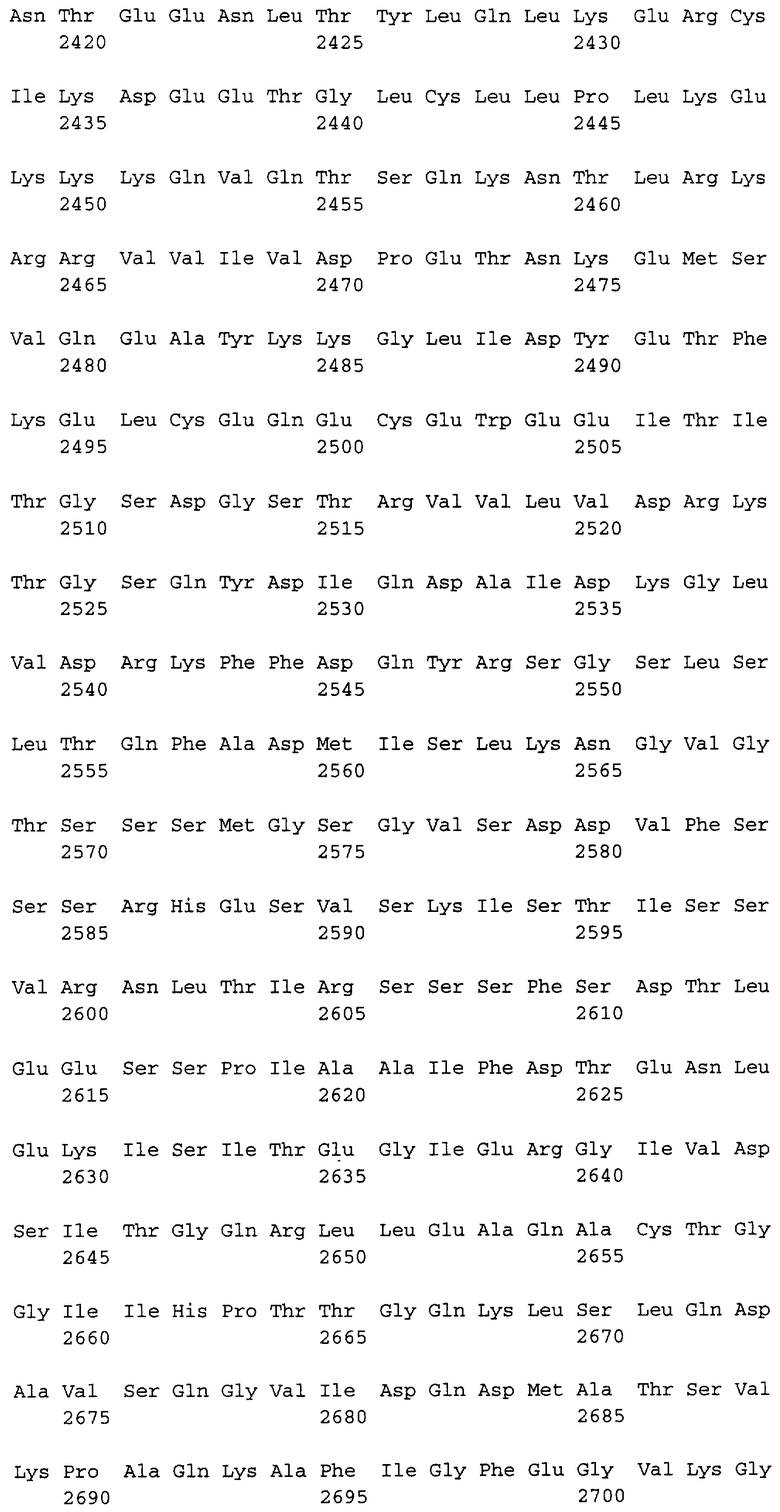

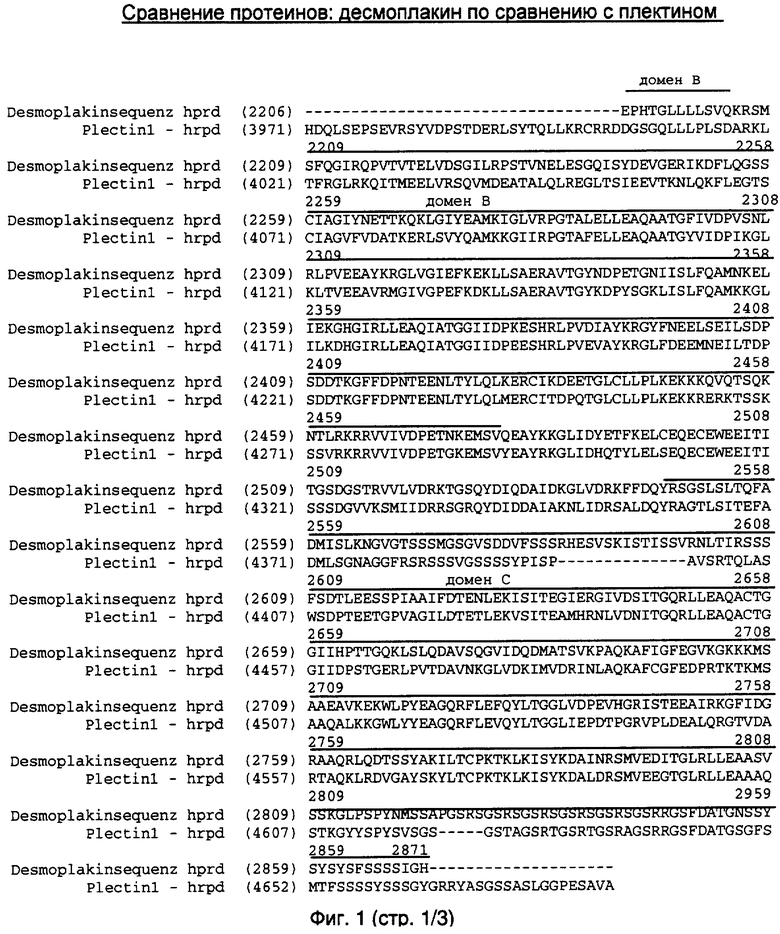
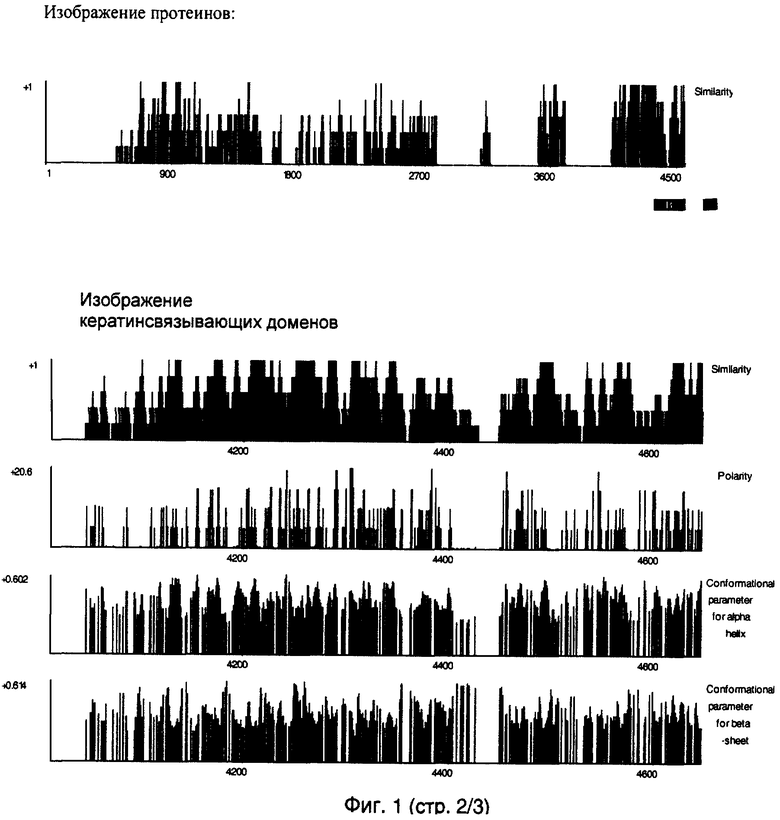
















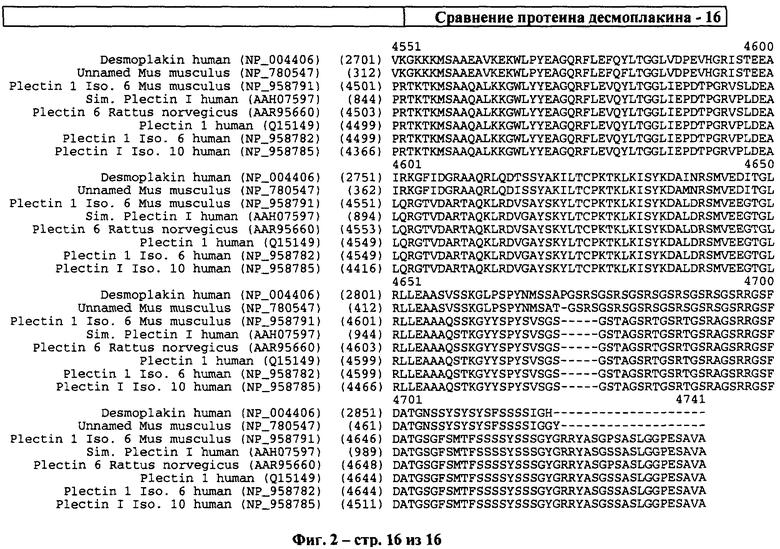
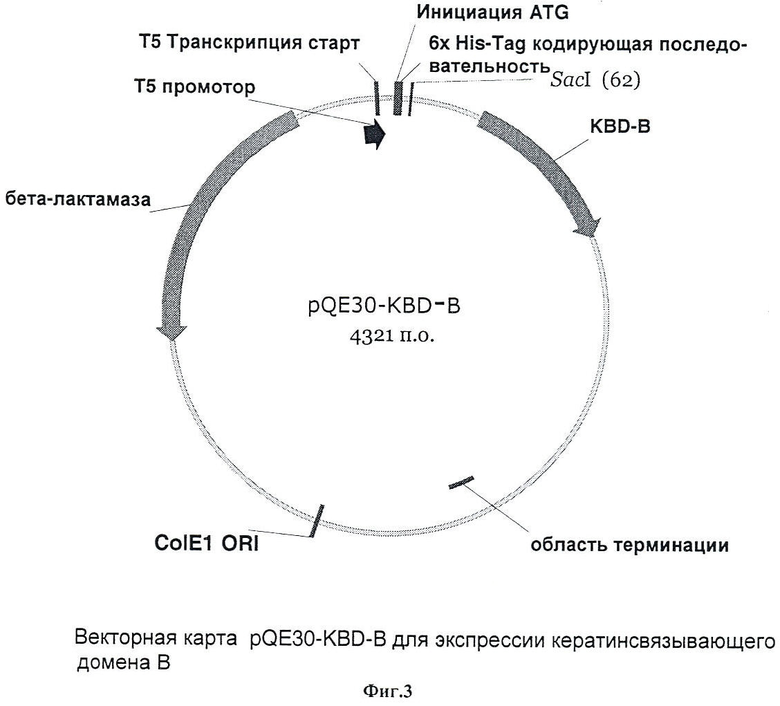
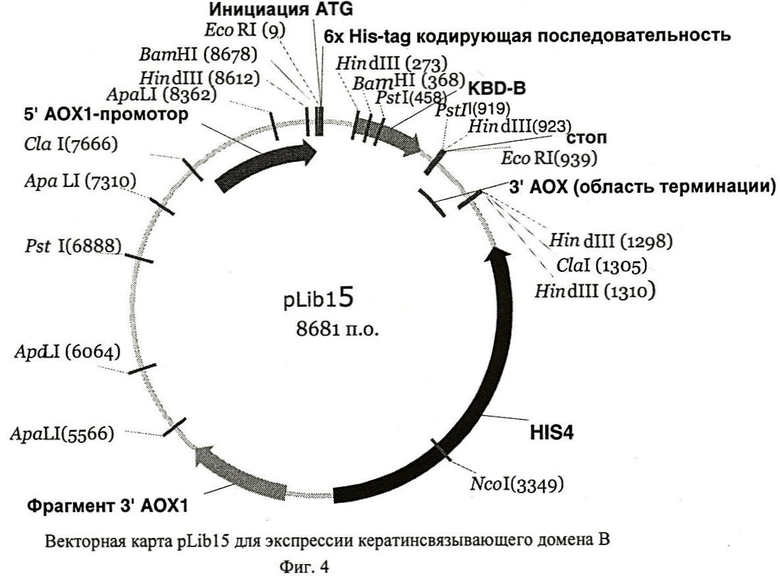
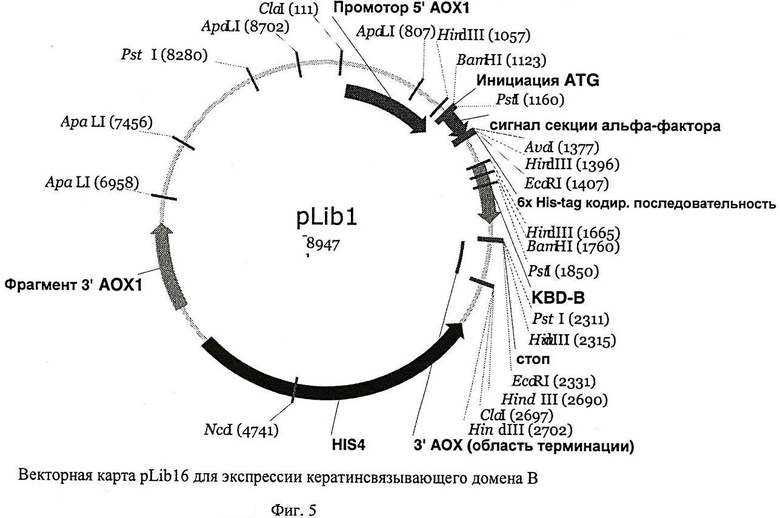
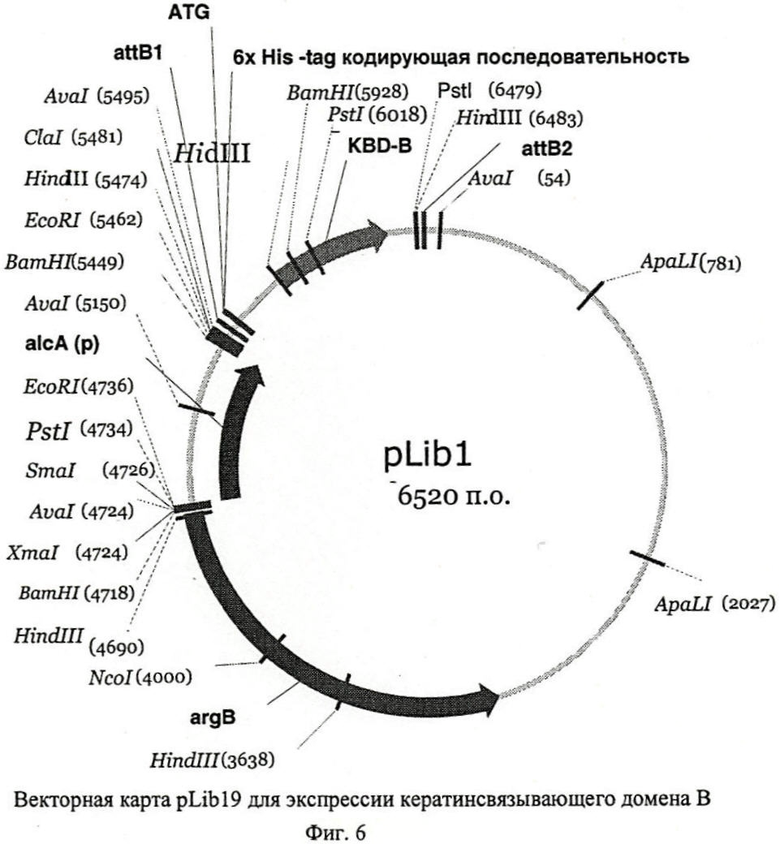
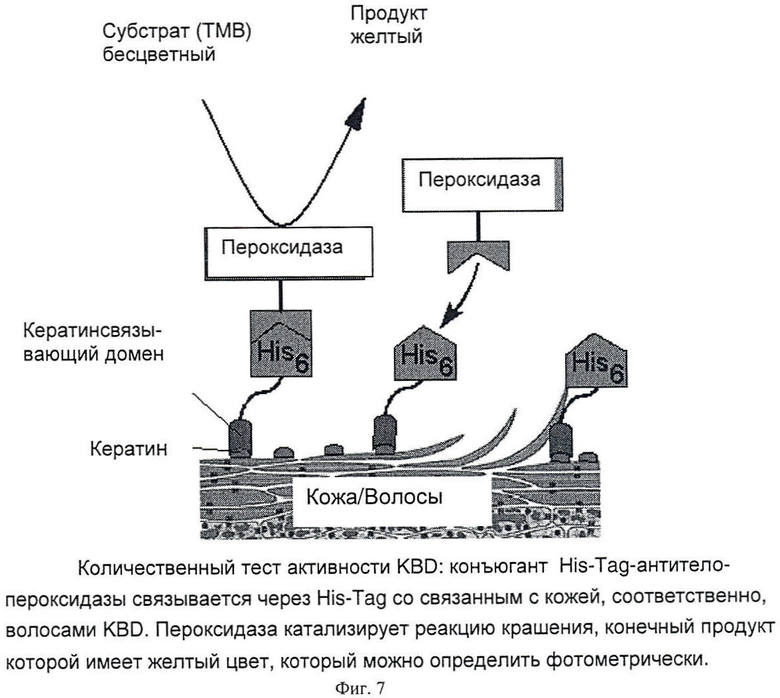
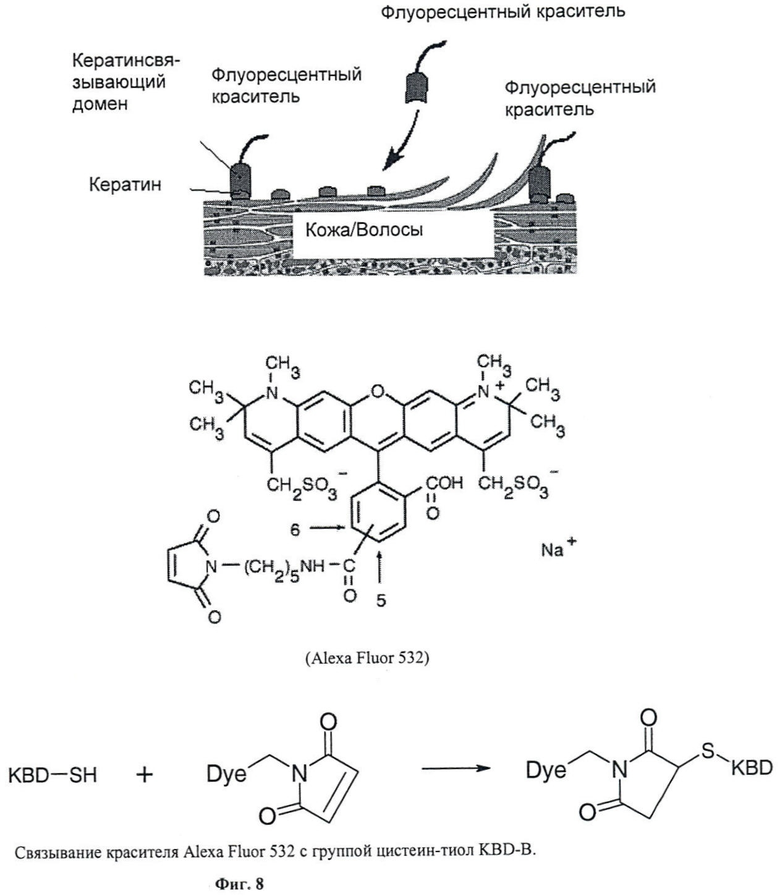
Настоящее изобретение относится к новой кератинсвязывающей эффекторной молекуле, содержащей полипептидные последовательности, которые имеют связывающее сродство с кератином, к их получению и применению. Пригодным кератинсвязывающим доменом (домен В) является полипептидная последовательность SEQ ID NO:1, положение 2193-2481, а также ее функциональные эквиваленты. Дальнейшим кератинсвязывающим доменом (домен С) является полипептидная последовательность SEQ ID NO:1, положение 2606-2871, а также ее функциональные эквиваленты, под доменами имеются в виду домены десмоплакина человека. Изобретение обеспечивает высокоспецифическое сродство с кератином кожи субъекта. 4 н. и 13 з.п. ф-лы, 8 ил., 1 табл.
1. Кератинсвязывающая эффекторная молекула для обработки кератинсодержащих материалов, состоящая из
(i) по меньшей мере, одной полипептидной последовательности, которая имеет связывающее сродство с кератином,
(ii) эффекторную молекулу, которая связана с полипептидной последовательностью (i), причем связь не является природного происхождения,
причем
полипептидная последовательность (i) включает, по меньшей мере, одну из следующих полипептидных последовательностей:
(a) полипептидную последовательность SEQ ID NO:1 положение 2269 до 2508,
(b) полипептидную последовательность SEQ ID NO:1 положение 2606 до 2871,
а
эффекторная молекула (ii) является красителем или компонентом красителя.
2. Кератинсвязывающая эффекторная молекула по п.1, отличающаяся тем, что полипептидная последовательность (i) имеет связывающее сродство с кератином волос, ногтей и кожи человека.
3. Кератинсвязывающая эффекторная молекула по п.1, отличающаяся тем, что эффекторная молекула (ii) включает полипептидную последовательность.
4. Кератинсвязывающая эффекторная молекула по любому из пп.1-3, отличающаяся тем, что эффекторная молекула (ii) связана через ковалентные связи с полипептидной последовательностью (i).
5. Кератинсвязывающая эффекторная молекула по п.4, отличающаяся тем, что эффекторная молекула (ii) при использовании двух уже имеющихся в (i) и (ii) химических функций ковалентно связана с функциональными группами боковой цепи, С- или N-концами полипептида (i).
6. Кератинсвязывающая эффекторная молекула по п.4, отличающаяся тем, что эффекторная молекула (ii) ковалентно связана через, по меньшей мере, бифункциональный линкер с функциональными группами боковой цепи, С- или N-концами полипептида (i).
7. Кератинсвязывающая эффекторная молекула по любому из пп.1-3, или 6, отличающаяся тем, что между эффекторной молекулой (ii) и полипептидом (i) встроены спейсерные элементы.
8. Кератинсвязывающая эффекторная молекула по п.6, отличающаяся тем, что имеет между эффекторной молекулой (ii) и полипептидом (i) потенциальное место расщепления для протеазы, липазы, эстеразы, фосфатазы или гидролазы.
9. Кератинсвязывающая эффекторная молекула по п.7, отличающаяся тем, что имеет между эффекторной молекулой (ii) и полипептидом (i) потенциальное место расщепления для протеазы, липазы, эстеразы, фосфатазы или гидролазы.
10. Кератинсвязывающая эффекторная молекула по п.8 или 9, отличающаяся тем, что между эффекторной молекулой (ii) и полипептидом (i) имеет еще одну полипептидную последовательность, которая обеспечивает легкую очистку протеина слияния.
11. Кератинсвязывающая эффекторная молекула по п.7, отличающаяся тем, что между эффекторной молекулой (ii) и полипептидом (i) имеет еще одну полипептидную последовательность, которая обеспечивает легкую очистку протеина слияния.
12. Применение кератинсвязывающей эффекторной молекулы по п.1 для получения композиций для косметики кожи, ногтей и волос.
13. Косметическая композиция для обработки кератинсодержащих материалов, содержащая, по меньшей мере, одну кератинсвязывающую полипептидную последовательность (i) в косметически переносимой среде, причем полипептидная последовательность (i) включает, по меньшей мере, одну из следующих полипептидных последовательностей:
(a) полипептидную последовательность SEQ ID NO:1 положение 2193 до 2481 и
(b) полипептидную последовательность SEQ ID NO:1 положение 2606 до 2871,
и,
по меньшей мере, одно косметическое действующее вещество, причем косметическое действующее вещество связано с полипептидной последовательностью (i) с образованием кератинсвязывающей эффекторной молекулы, как определенной в п.1.
14. Косметическая композиция по п.13, отличающаяся тем, что полипептидная последовательность (i) имеет связывающее сродство с кератином волос, ногтей или кожи человека.
15. Косметическая композиция по п.13, отличающаяся тем, что она содержит полипептидную последовательность (i) в количестве от 0,01 до 30 вес.%.
16. Косметическая композиция по п.13, отличающаяся тем, что косметическое действующее вещество выбрано из группы, включающей естественные или синтетические полимеры, пигменты, средства удержания влажности, масла, воски, ферменты, минералы, витамины, средства защиты от солнца, красители, душистые вещества, антиокислители и консерванты.
17. Применение косметических композиций по любому из пп.13-15 для получения композиций для косметики волос, ногтей и кожи.
| 0 |
|
SU293837A1 | |
| Fontao L et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Mol Biol Cell | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Овчинников Ю.А | |||
| Биоорганическая химия | |||
| - М.: Просвещение, 1987, | |||
Авторы
Даты
2011-02-10—Публикация
2005-05-24—Подача