Изобретение относится к технологии переработки природных объектов и касается способа получения пигмента спинохрома Е из отходов переработки промысловых морских ежей Strongylocentrotus nudus.
Полигидроксинафтохинон - 2,3,6,7-тетрагидроксинафтазарин (спинохром Е) впервые обнаружен Ледерером [Lederer Е., Glaser R. // C.r.Acad. Sci, v.2007, p.454-456, 1938.]. Структура и свойства этого пигмента установлены Смитом и Томсоном [Smith J., Thomson R.H. // J.Chem. Soc., №3, p.1008-1012, 1961].
Известно, что нафтохиноновые пигменты являются эффективными антиоксидантами [Кольцова Е.А., Максимов О.Б., Уткина Н.К., Щедрин А.П. // Хиноидные пигменты иглокожих // Рукопись деп. ВИНИТИ, №106, с.74, 1974].
В основе патогенеза ряда заболеваний (инфаркты, инсульты, язвенная болезнь, диабет, онкологические, воспалительные, инфекционные и др.) лежит активация перекисных и других свободно-радикальных процессов, так называемая «свободно-радикальная патология». Лекарственное коррегирование подобных нарушений, т.е. антиоксидантотерапия, стало одним из ведущих направлений современных фармакологических разработок [Мищенко Н.П., Федореев С.А., Багирова В.Л. // Хим. - фарм. журнал, т.37, вып. 8, с.49-53, 2003; Карпов Р.С., Дудко В.А. // Атеросклероз: патогенез, клиника, функциональная диагностика и лечение // Томск, СТТ, с.656, 1998].
Известен и применяется в медицине природный полигидроксинафтохинон - эхинохром А, обладающий противоишемической и противоинфарктной активностью [Мищенко Н.П., Федореев С.А., Багирова В.Л. // Хим. - фарм. журнал, т. 37, вып. 8, с.49-53, 2003]. Аналогичную активность проявляют и другие полигидроксинафтохиноны, входящие в состав оболочных клеток панцирей и игл морских ежей, так называемые спинохромы. Антиоксидантные свойства спинохромов были изучены на моделях инициированного окисления алкибензолов, термического окисления метиленолеата и окисления минеральных и растительных масел [Кольцова Е.А., Максимов О.Б., Уткина Н.К., Щедрин А.П. // Хиноидные пигменты иглокожих // Рукопись деп. ВИНИТИ, №106, с.74, 1974]. Константа взаимодействия спинохромов с перекисными радикалами существенно превышает константу ионола [Вопросы медицинской химиии, т. 45, с.123-130, 1999] и природного антиоксиданта токоферола [Карпов Р.С., Дудко В.А. // Атеросклероз: патогенез, клиника, функциональная диагностика и лечение // Томск, СТТ, с.656, 1998]. Помимо этого 1,4-нафтохиноны проявляют цитотоксическую активность в отношении различных линий опухолевых клеток [Tomson R.H. // Spinochromes. Naturally Occuring Quinones. 1971, - 2 ed., - L. N-Y: Acad. Press., p 257-276.].
Сравнительный анализ антиоксидантной активности спинохромов показал, что антиоксидантная активность растет в зависимости от степени гидроксилирования нафтохинонового цикла. Наибольшую степень гидроксилирования среди этих соединений имеет спинохром Е, что, вероятно, и определяет его высокую антиоксидантную активность [Лебедев А.В., Иванова М.В. и др. // Вопросы медицинской химиии, т. 45, с.123-130, 1999]. В то же время спинохром Е, содержащий гидроксилы во 2, 3, 5, 6, 7 и 8-м положениях, наименее устойчив в нейтральных и щелочных водных растворах. Поэтому возникла необходимость в разработке способа получения спинохрома Е, исключающего деструкцию целевого продукта.
Известен способ получения спинохромов из морских ежей Arbacia punetulata путем растворения игл в концентрированной соляной кислоте, фильтрации, нейтрализации кислого раствора бикарбонатом натрия, удаления липидов эфиром, подкисления эфирного слоя кислотой, высушивания над безводным сульфатом натрия, фильтрации, упаривания и последующей хроматографии с использованием обработанного кислотой силикагеля в системе 5% метанол-хлороформ, элюирования этилацетатом, фильтрации и упаривания досуха [Chang C.W.J., Moore J.C. // Journal of Chemical Education, v.50, p.102, 1973].
Однако известный способ является лабораторно-аналитическим. Спинохром Е был выделен в виде индивидуального вещества только методом тонкослойной хроматографии с целью его идентификации.
В качестве прототипа выбран способ получения суммы хиноидных пигментов из панцирей с иглами и внутренностей морских ежей вида Strongylocentrotus nudus, включающий разложение сырья кислотой, фильтрацию полученного раствора, последующую эфирную экстракцию, выделение из экстракта суммы хиноидных пигментов хроматографией на силикагеле, отмывку и сушку выделенных пигментов [Кольцова Е.А., Максимов О.Б., Уткина Н.К., Щедрин А.П. // Хиноидные пигменты иглокожих // Рукопись деп. ВИНИТИ, №106, с.74, 1974].
Однако данный способ не обеспечивает получения индивидуального пигмента спинохрома Е. Он относится к лабораторно-аналитическим способам получения суммы хиноидных пигментов и непригоден для технологических целей.
Технический результат, обеспечиваемый изобретением, заключается в расширении спектра биологически активных веществ, получаемых из отходов промышленной переработки промысловых морских ежей. В результате осуществления изобретения получают индивидуальное соединение - спинохром Е, являющееся эффективным антиоксидантом.
Заявляемый способ получения 2,3,6,7-тетрагидроксинафтазарина (спинохрома Е) заключается в следующем.
Панцири с иглами промысловых морских ежей Strongylocentrotus nudus, оставшиеся после извлечения икры, свежие, дефростированные или законсервированные, промывают водой для удаления механических примесей и морских солей. При использовании консервированного сырья консервант предварительно отделяют декантацией. Содержащиеся в сырье вещества липидной природы удаляют экстракционной промывкой 96% этанолом с последующей регенерацией этанола.
Обезжиренное сырье экстрагируют трехкратно 96% этиловым спиртом с добавлением фосфорной кислоты. Соотношение сырье:экстрагент 1,0:(1,0-1,2). Экстракцию осуществляют в течение 12-24 часов при комнатной температуре. Полученный спиртовый экстракт имеет pH 3-3,5.
Суммарный пигментный комплекс очищают от посторонних примесей на хитозане. Для этого спиртовые экстракты объединяют и пропускают через хроматографическую колонку, заполненную хитозаном. Колонку с адсорбированными на хитозане пигментами промывают 96% этиловым спиртом. Пигменты элюируют с колонки 96% этиловьм спиртом с добавлением соляной кислоты (pH 2-4).
Спинохром Е выделяют из пигментного комплекса на гидрофобном сорбенте полихром-1. Для этого элюат, полученный на предыдущей стадии, пропускают через хроматографическую колонку с полихромом-1. Адсорбированные компоненты отмывают от кислоты дистиллированной водой. Элюирование спинохрома Е осуществляют 40-50% этиловым спиртом. Этиловый спирт удаляют концентрированием в вакууме. Концентрат лиофилизуют.
С целью дополнительной очистки возможна кристаллизация спинохрома Е из этанола или возгонка в вакууме при температуре 195-200°С.
Для подтверждения чистоты продукта проведен анализ образцов спинохрома Е методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
ВЭЖХ проводили на хроматографе "LaChrom" (Merck Hitachi), снабженном УФ детектором L-7400, насосом L-7100, термостатом L-7300, интегратором D-7500 и колонкой Agilent Technologies Zorbax Eclipse XDB-C18, 3.5 µm (75 мм × 4.6 мм) с защитной колонкой Hypersil ODS, 5 µm (4.0 мм × 4.0 мм). Колонку термостатировали при 30°С. Разделение примесей проводили смесью растворителей - А (вода +1% ледяной уксусной кислоты) и В (ацетонитрил +1% ледяной уксусной кислоты) в следующем режиме: 0-5 мин - изократический, 90% А, 10% В; 5-35 мин градиентный, 90-10% А, 10-90% В. Скорость подачи растворителей - 1 мл/мин. Детектирование проводили при 270 нм.
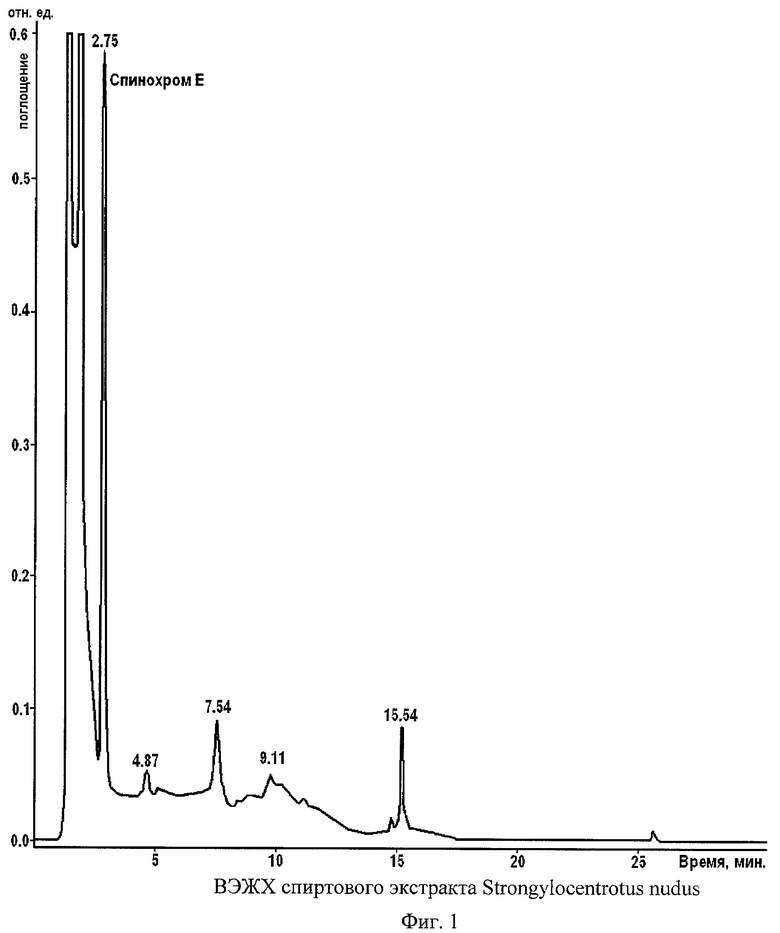
На фиг.1 представлена ВЭЖХ спиртового экстракта морских ежей S. Nudus.
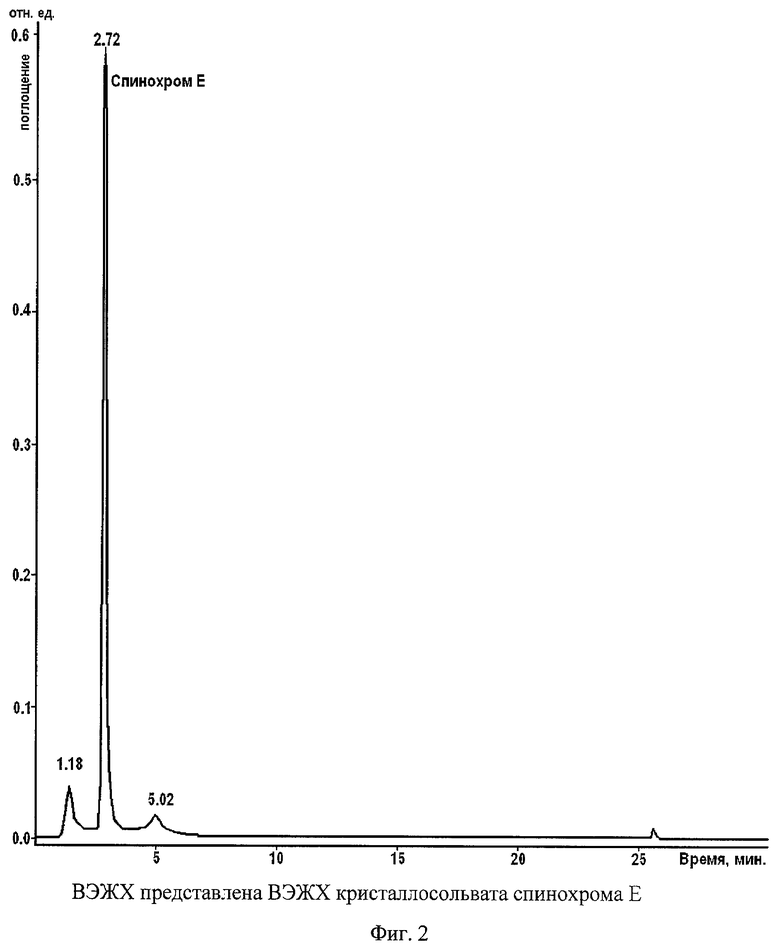
На фиг.2 представлена ВЭЖХ кристаллосольвата спинохрома Е.
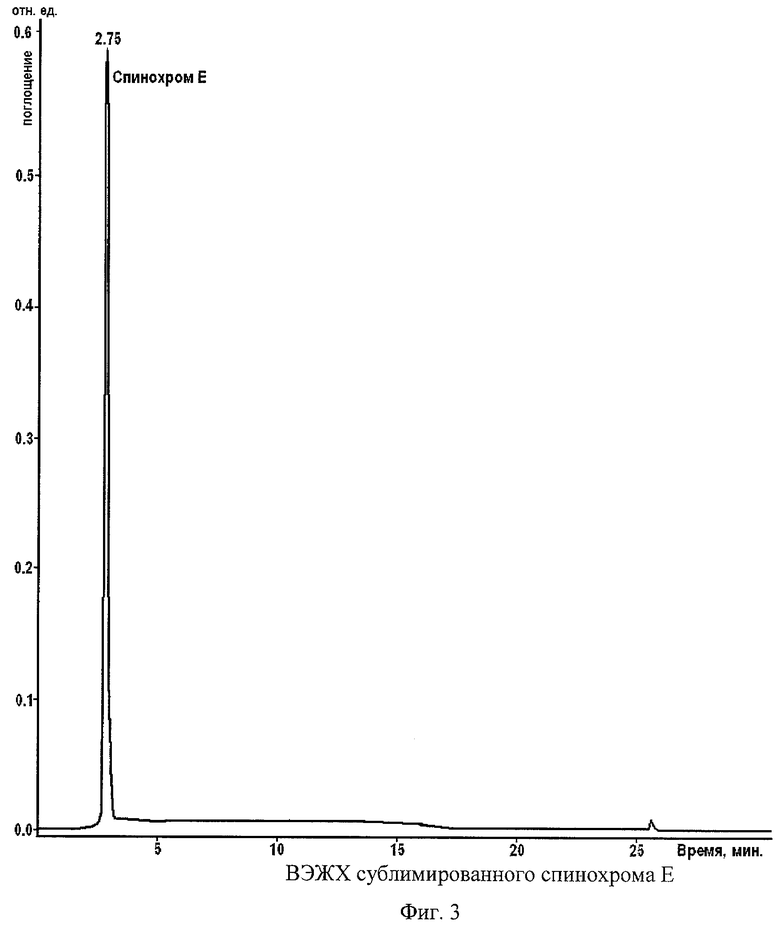
На фиг.3 представлена ВЭЖХ сублимированного спинохрома Е.
Изобретение иллюстрируется следующими примерами.
Пример 1
Панцири с иглами морских ежей Strongylocentrotus nudus, оставшиеся после извлечения икры, свежие или дефростированные, в количестве 100 кг промывают водой питьевой для удаления механических примесей, морских солей и измельчают.
Сырье загружают в реактор-экстрактор и экстрагируют 100 л 96% этилового спирта до полного удаления веществ липидной природы. Этиловый спирт регенерируют. Обезжиренное сырье экстрагируют 117 л 96% этилового спирта с добавлением 7 л 20% фосфорной кислоты Соотношение сырье:экстрагент 1:1. Экстракцию проводят трехкратно в течение 12 часов при комнатной температуре. Экстракты объединяют, фильтруют через тканевый фильтр и центрифугируют. Полученный спиртовый экстракт имеет pH 3,0.
После этого экстракт пропускают через колонку с 5 кг измельченного хитозана. Обедненный экстракт регенерируют перегонкой и этанол возвращают в технологический процесс. Колонку с адсорбированными на хитозане пигментами промывают 10 л 96% этилового спирта. Пигменты элюируют с колонки 10 л 96% этанола с добавлением 300 мл 18% соляной кислоты до pH 4,0.
Регенерация колонки - хитозан промывают 20 л 96% этилового спирта.
Элюат пропускают через колонку с 3 кг полихрома-1. При этом пигменты адсорбируются на полихроме-1. Адсорбированные пигменты отмывают от кислоты 12 л дистиллированной воды. Спинохром Е элюируют с колонки 6 л 40% водного раствора этилового спирта. Водный остаток в количестве 2,5-3 л лиофилизуют. После сублимации в вакууме при 195-200°С получают спинохром Е в виде красно-коричневого порошка.
Выход составляет 19 г (0,019% от веса исходного сырья).
Пример 2
Консервированное сырье - морские ежи вида S. nudus, в количестве 100 кг загружают в реактор, консервант сливают. Расконсервированных морских ежей экстрагируют 96% этиловым спиртом с добавлением фосфорной кислоты (соотношение сырье:экстрагент 1:1,2). Экстрагент получают смешиванием 140 л этанола и 9 л 20% фосфорной кислоты. Экстракцию проводят трехкратно в течение 24 часов при комнатной температуре. Затем экстракты объединяют, фильтруют через тканевый фильтр, центрифугируют. Полученный спиртовый экстракт имеет рН 3,5.
Затем экстракт пропускают через колонку с 5 кг хитозана, упаривают и этанол возвращают в технологический процесс.
Колонку с адсорбированной суммой пигментов промывают 10 л 96% этилового спирта. Пигменты элюируют с колонки 10 л 96% этилового спирта с добавлением 340 мл 18% соляной кислоты до pH 2,0.
Регенерация колонки - хитозан промывают 20 л 96% этилового спирта.
Полученный элюат пропускают через колонку с 3 кг полихрома-1 в воде. Адсорбированные пигменты отмывают от кислоты 12 л дистиллированной воды. Спинохром Е элюируют с колонки 6 л 50% водного раствора этилового спирта. Этанольный раствор упаривают досуха на роторном испарителе в вакууме. Остаток растворяют в минимальном количестве кипящего этанола, фильтруют и охлаждают. Выпавшие кристаллы промывают охлажденным ацетоном и высушивают в вакууме. Получают 24 г кристаллосольвата спинохрома Е (0,024% от веса исходного сырья).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,3,7-ТРИОКСИЮГЛОНА (СПИНОХРОМА В) | 2014 |
|
RU2568604C1 |
| СПОСОБ ПОЛУЧЕНИЯ СПИНОХРОМА А И БЕЛКА МОРСКИХ ЕЖЕЙ, ВЗАИМОДЕЙСТВУЮЩЕГО С ПОЛИГИДРОКСИНАФТОХИНОНОМ | 2008 |
|
RU2362573C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИГМЕНТНОГО КОМПЛЕКСА БИСНАФТАЗАРИНОВ | 2014 |
|
RU2545692C1 |
| СПОСОБ ПОЛУЧЕНИЯ СПИНОХРОМА Е | 2014 |
|
RU2561280C1 |
| Способ получения нафтохинонов из морских ежей | 2016 |
|
RU2645077C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАГИДРОКСИЭТИЛНАФТОХИНОНА (ЭХИНОХРОМА А) | 2015 |
|
RU2581055C1 |
| СПОСОБ ПЕРЕРАБОТКИ ПАНЦИРЯ МОРСКИХ ЕЖЕЙ | 2010 |
|
RU2441661C1 |
| Способ получения кальцийсодержащей композиции из панциря морских ежей | 2015 |
|
RU2611847C1 |
| Способ получения водорастворимой солевой формы эхинохрома А, пригодной для использования в фармакологической и пищевой промышленности | 2019 |
|
RU2697197C1 |
| Композиция ингредиентов для функциональных пищевых продуктов | 2016 |
|
RU2644957C1 |
Изобретение относится к технологии переработки природных объектов. Для получения 2,3,6,7-тетрагидроксинафтазарина (спинохрома Е) в качестве сырья используют отходы переработки промысловых морских ежей Strongylocentrotus nudus, которое дефростируют или отделяют от консерванта декантацией. Промывают водой, обезжиривают 96% этиловьм спиртом, затем экстрагируют трехкратно 96% этиловым спиртом с добавлением фосфорной кислоты (рН 3,0-3,5) при соотношении сырье: экстрагент 1,0:(1,0-1,2) в течение 12-24 час. Полученный экстракт пропускают через колонку с хитозаном, промывают колонку 96% этиловым спиртом, затем элюируют пигменты 96% этиловым спиртом с добавлением соляной кислоты (рН 2-4). Далее элюат пропускают через колонку с полихромом-1, промывают колонку дистиллированной водой, затем элюируют целевой продукт 40-50% водным раствором этилового спирта, отгоняют растворитель в вакууме, водный остаток лиофилизуют. Затем спинохром Е сублимируют при 195-200°С или перекристаллизовывают из этилового спирта. Способ позволяет расширить спектр биологически активных веществ, получаемых из отходов промышленной переработки промысловых морских ежей. 3 ил.
Способ получения 2,3,6,7-тетрагидроксинафтазарина из морских ежей Strongylocentrotus nudus, заключающийся в том, что сырье дефростируют или отделяют от консерванта декантацией, промывают водой, обезжиривают 96%-ным этиловым спиртом, затем экстрагируют трехкратно 96%-ным этиловым спиртом с добавлением фосфорной кислоты (pH 3,0-3,5) при соотношении сырье : экстрагент 1,0:(1,0-1,2) в течение 12-24 ч, полученный экстракт пропускают через колонку с хитозаном, промывают колонку 96%-ным этиловым спиртом, затем элюируют пигменты 96%-ным этиловым спиртом с добавлением соляной кислоты (pH 2-4), далее элюат пропускают через колонку с полихромом-1, промывают колонку дистиллированной водой, затем элюируют целевой продукт 40-50%-ным водным раствором этилового спирта, отгоняют растворитель в вакууме, водный остаток лиофилизуют, затем спинохром Е сублимируют при 195-200°С или перекристаллизовывают из этилового спирта.
| КОЛЬЦОВА Е.А | |||
| и др | |||
| Хиноидные пигменты иглокожих | |||
| Главные пигменты некоторых япономорских морских ежей | |||
| Деп | |||
| ВИНИТИ, 1974, №106, с.74 | |||
| СПОСОБ ПОЛУЧЕНИЯ 2,3,5,7,8-ПЕНТАГИДРОКСИ-6-ЭТИЛ-1,4-НАФТОХИНОНА | 2005 |
|
RU2283298C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 2,3,5,8-ТЕТРАГИДРОКСИ-1,4-НАФТАХИНОНОВ | 1990 |
|
RU2022959C1 |
| SU 1401828 А1, 27.07.1996 | |||
| ROKHILO ND et al | |||
| Synthesis of echinamines A and B, the first aminated hydroxynaphazarins produced by the sea urchin | |||
Авторы
Даты
2011-02-20—Публикация
2009-07-13—Подача