Панцирь и иглы морского ежа являются побочным продуктом при получении съедобных гонад и представляют собой известковое образование. Содержание карбоната кальция по разным данным составляет от 70% до 95%. Основными ценными минорными компонентами панцирей и игл морских ежей являются придающие окраску пигменты полигидроксинафтохинонового ряда - эхинохром А и спинохромы, проявляющие антиоксидантные свойства [Lebedev AV et al., 2008; Kuwahara R. et al., 2009].
В России зарегистрирован антиоксидантный препарат Гистохром®, содержащий в качестве активного вещества натриевые соли пентагидроксиэтилнафтохинона (эхинохрома А) в концентрации 0,2 мг/мл (раствор для инъекций) и 10 мг/мл (раствор для внутривенного введения) [RU 2137472 С1, 10.08.99; RU 2134107 С1, 20.09.99; Мищенко Н.П. и др., 2004]. Эхинохром А также входит в состав некоторых биологически активных добавок (БАД) к пище (например, Тимарин, Золотой рог, экстракт морского ежа и др.).
Известен способ получения эхинохрома А из плоских морских ежей, включающий экстракцию морских ежей растворами серной кислоты в спирте этиловом с последующей жидкостной экстракцией хлороформом в смеси с водой (1:1) и перекристаллизацией целевого продукта из смеси диоксан-гексан [SU 1508535 A3, 27.08.1996]. Данный способ обеспечивает выход эхинохрома А 0,05-0,06%.
Недостатками данного способа являются использование токсичной неорганической серной кислоты, низкий выход целевого продукта и его низкая чистота.
Известны способы получения эхинохрома А с чистотой не менее 98% (методом ВЭЖХ). 1-ый способ заключается в последовательной обработке свежевыловленных или дефростированных морских ежей органическим растворителем, смешивающимся с водой (этиловый спирт, ацетон), а затем несмешивающимся с водой (гексан, хлороформ), экстракции сырья раствором неорганической кислоты (серной или соляной) в этиловом спирте, жидкостной экстракции хлороформом, перекристаллизации целевого продукта из диоксана и очистки эхинохрома А сублимацией при температуре около 220°С [RU 2283298 С1, 10.09.2006]. 2-ой способ заключается в экстракции консервированных плоских морских ежей раствором неорганической кислоты (соляной, фосфорной) в спирте с последующей хроматографической очисткой экстракта на колонке с хитозаном в ОН форме, элюировании эхинохрома А подкисленным этиловым спиртом, нейтрализации элюата, удалении растворителя, перерастворении остатка в хлороформе или ацетоне, перекристаллизации из этилового спирта и сушке продукта [RU 2352554 С1, 20.04.2007]. Эти способы обеспечивают выход эхинохрома А от 0,3 до 1,5% от массы загруженного сырья.
Известен способ получения спинохрома А из панциря и игл промыслового морского ежа Strongylocentrotus nudus, заключающийся в обработке сырья этиловым спиртом, деминерализации панцирей и игл 20% фосфорной кислотой, фильтрации и хроматографической очистке полученной вытяжки с применением сорбента полихром 1 (политетрафторэтилен), элюировании ферментно-пигментного комплекса водно-спиртовыми смесями, концентрировании и сушке остатка, повторном растворении остатка в воде, осаждении белковых компонентов этиловым спиртом, хроматографическом отделении спинохрома А с использованием сефадекса LH-20 и перекристаллизации его из ацетона [RU 2362573 С1, 27.07.2009].
Известен инкапсулированный пищевой краситель, представляющий собой сумму хиноидных пигментов, выделенных из панциря с иглами и внутренностей морских ежей Strongylocentrotus nudus или Strongylocentrotus intermedius, заключенный в оболочку из пищевого материала и способ его получения, включающий разложение панцирей с иглами и внутренностей морских ежей кислотой, фильтрацию раствора с последующей экстракцией пигментов эфиром, отмывку, сушку и концентрирование выделенных пигментов с последующим заключением их в липосомную оболочку, состоящую из фосфолипидов сои, стабилизированных α-токоферолом и холестерином [RU 2004124260 А, 27.01.2006].
Недостатками перечисленных способов получения пигментов является использование растворов сильных и средних минеральных кислот для деминерализации панциря, длительность экстракционных процедур (до 24 часов), большие потери целевых продуктов при хроматографировании, жидкостной экстракции и предварительной очистке сырья, а также потеря минеральной составляющей панциря и игл морских ежей.
Обработка панциря и игл растворами кислот необходима для разрушения минерально-пигментных комплексов-фенолятов. Панцирь и иглы морских ежей представляют собой известковое образование. Карбонатный скелет морских ежей легко нейтрализуется с разложением и растворами органических кислот. Получающиеся при нейтрализации карбонатного скелета кальциевые соли органических кислот могут находить широкое применение в пищевой и фармацевтической промышленности. Например, кальциевые соли молочной, лимонной, винной кислот являются разрешенными в РФ пищевыми добавками, кальциевая соль аскорбиновой кислоты является источником витамина С. Кроме того, было показано, что абсорбция кальция, изученная в условиях in vivo на крысах, при применении лактата кальция из панцирей морских ежей Hemicentrotus pulcherrimus превышала абсорбцию кальция из синтетического лактата кальция [US 6203827 B1, 20.03.2001].
Известны методы получения кальциевой составляющей панцирей морских ежей путем их термической обработки при температуре 700-1100°С, последующей обработки органическими кислотами [US 6203827 В1, 20.03.2001; KR 20070077756 А, 27.07.2007] или без кислотной обработки [JP 2009126777 А, 11.06.2009].
Известна антимикробная композиция для применения в фармацевтической или пищевой промышленности, содержащая кальций из панциря морских ежей Strongylocentrotus nudus и Anthocidaris crassispina, получаемая нагреванием лиофильно высушенных панцирей при температуре 600-1100°С [KR 20030020066 А, 08.03.2003].
Недостатком описанных способов получения кальциевой составляющей панцирей морских ежей является необратимая потеря других биологически активных веществ панциря.
Наиболее близким к заявляемому способу является способ комплексной переработки плоских морских ежей [RU 2305548 С1, 10.09.2007], заключающийся в последовательной обработке сырья - свежевыловленных или замороженных цельных морских ежей водным раствором органического комплексообразователя, водным раствором щелочи, спиртовым раствором органического комплексообразователя, разбавленным спиртовым раствором серной кислоты с последующим концентрированием и очисткой полученных экстрактов. В результате переработки плоских морских ежей по данному способу получают белковую кормовую добавку, фракцию ганглиозидов, эхинохром А чистотой 78% и минеральную муку. Экстракция эхинохрома А из сырья по этому способу осуществляется с применением разбавленной серной кислоты. Получение минеральной муки возможно в случае неполной деминерализации панциря, что заведомо снижает выход пигментов. Используемый в качестве сырья плоский морской еж богат эхинохромом А. Однако из опубликованных литературных данных известно, что структурные аналоги эхинохрома А, спинохромы, также обладают антирадикальными и железохелатирующей активностями, а значит, проявляют антиоксидантные свойства [Lebedev AV et al., 2008].
Отличительной особенностью настоящего изобретения является:
- использование только панцирей с иглами морских промысловых ежей любых видов, кроме плоских морских ежей;
- быстрая экстракция пигментов растворами органических кислот;
- получение в конечном итоге продукта, представляющего собой комплекс пигментов, не содержащий эхинохрома А, обладающих антиоксидантной активностью;
- получение минеральной составляющей панциря в виде водорастворимых солей органических кислот.
Настоящее изобретение решает задачу одновременного получения пигментного антиоксидантного комплекса и минеральной составляющей панциря и игл морских ежей в виде солей органических кислот, растворимых в воде.
Задача решена тем, что панцири с иглами морских ежей промывают от остатков внутренностей, высушивают при температуре 5-8°С или 40-50°С, измельчают.
Измельченный панцирь деминерализуют при температуре 40-90°С (предпочтительно 60°С) небольшим стехиометрическим избытком слабой органической кислоты, используя 10-80% (предпочтительно 50%) водный раствор кислоты, выбранной из ряда: молочная, уксусная, муравьиная, винная, аскорбиновая, лимонная. Реакционную смесь центрифугируют для удаления нерастворившихся частиц.
Соли органической кислоты осаждают добавлением органического растворителя, смешивающегося с водой, например: этиловый спирт, ацетон, ацетонитрил. Отделяют от реакционной смеси, промывают, при необходимости перекристаллизовывают из подходящего растворителя.
Кислую вытяжку нейтрализуют до pH 4-7 добавлением водорастворимых солей натрия, калия или подобных, предпочтительно карбоната натрия, фильтруют, концентрируют под вакуумом при температуре не выше 60°С, лиофильно высушивают. Продукт растворяют в органическом растворителе, смешивающемся с водой, например: этиловом спирте, ацетоне, ацетонитриле, фильтруют, высушивают.
Изобретение иллюстрируется следующими примерами.
Пример 1
20 г промытых, высушенных, измельченных панцирей с иглами морских ежей деминерализуют 100 мл 50% водного раствора молочной кислоты при температуре 80°С. Полученный раствор центрифугируют для удаления нерастворенных мелких частиц. К супернатанту приливают 50 мл 95% этилового спирта, перемешивают, раствор, оставляют на холоде (2-8°С) для выпадения осадка лактата кальция. Выпавший осадок отфильтровывают, промывают холодной водой до нейтральной реакции, при необходимости перекристаллизовывают из воды, высушивают. Полученный фильтрат нейтрализуют карбонатом натрия до pH 4-7, фильтруют, концентрируют в вакууме при температуре 40°С до объема около 20 мл, лиофилизируют. Сухой остаток (около 1 г) перерастворяют в 5 мл этилового спирта, фильтруют, высушивают. Выход пигментного комплекса составляет 0,5 г, выход кальция лактата 35 г.
Пример 2
Аналогично примеру 1, только сырье деминерализуют 100 мл 80% молочной кислоты.
Пример 3
Аналогично примеру 1 и 2, только к супернатанту приливают 40 мл ацетона.
Пример 3
Аналогично примеру 1, только для деминерализации панцирей и игл используют 30% водный раствор винной кислоты.
Пример 4
Аналогично примеру 1, только для деминерализации панцирей и игл используют 20% водный раствор лимонной кислоты.
Пример 5
Аналогично примеру 4, только для деминерализации панцирей и игл используют водный раствор аскорбиновой кислоты.
Пример 6
Аналогично примеру 1, только для деминерализации панцирей и игл используют водный раствор уксусной кислоты.
Пример 7
Аналогично примеру 2, только для деминерализации панцирей и игл используют водный раствор муравьиной кислоты.
Пример 8
Оценка антиоксидантной активности пигментного комплекса панцирей и игл морских ежей.
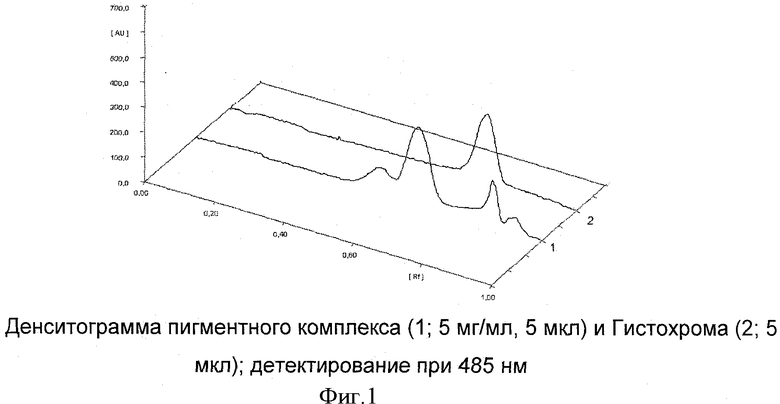
Об антиоксидантной активности пигментного комплекса судили по наличию антирадикальной активности (АРА) по отношению к радикалу 2,2-дифенил-1-пикрилгидразила (DPPH радикалу). Антирадикальную активность оценивали с применением метода тонкослойной хроматографии (ТСХ). Такой подход сочетает в себе хроматографическое разделение многокомпонентной смеси и оценку антирадикальной активности каждого компонента [Pozharitskaya ON et al., 2007]. Разделение пигментного комплекса методом ТСХ проводили на пластинах Silica gel 60 F254 (Merck, Германия), импрегнированных спиртовым раствором щавелевой кислоты. Пигментный комплекс, полученный по п.1 из панцирей и игл ежа Strongylocentrotus droebachiensis растворяли в 1% спиртовом растворе соляной кислоты в концентрации 1-10 мг/мл и наносили на пластину в количестве 2-20 мкл. Пластину элюировали восходящим способом в системе растворителей метанол/хлороформ/уксусная кислота/вода (11/50/5/2 по объему) на высоту 80 мм. По окончании процесса элюирования пластину высушивали до отсутствия запаха растворителей, детектировали при 485 нм (сканирующий спектроденситометр). Антирадикальную активность пигментов оценивали после погружения пластин в 0,5 мМ метанольный раствор 2,2-дифенил-1-пикрилгидразила по гашению окраски фиолетового фона пластины. Для количественных расчетов АРА по DPPH радикалу пластину детектировали при 520 нм (сканирующий спектроденситометр), для оценки АРА пигментов рассчитывали их ID50 - количество компонента, обеспечивающие связывание половинного количества DPPH радикалов с применением сигмоидальной регрессии на линейном участке кривой зависимости интенсивности гашения фона пластины от количества образца.
В качестве препарата сравнения использовали Гистохром® раствор для инъекций.
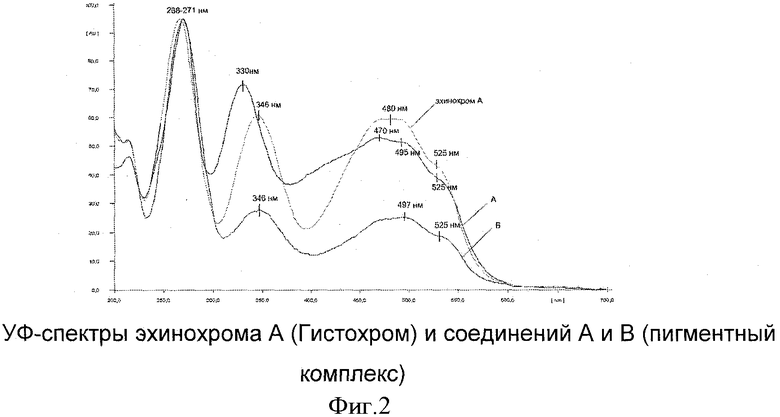
В составе пигментного комплекса обнаружено 4 превалирующих соединения (фиг.1), УФ-спектры двух соединений (А и В) однозначно позволяют отнести их к классу полигидроксинафтохиноновых соединений (фиг.2).
Получаемый по описываемому способу пигментный комплекс не содержит эхинохрома А. Все соединения пигментного комплекса проявляют антирадикальную активность по отношению к DPPH радикалу (фиг.3).
Антирадикальная активность соединений А и В в данной модели оказалась выше, чем у эхинохрома А, значения ID50 этих соединений: 0,057 мкг для соединения А, 0,043 мкг для соединения В и 0,134 мкг для эхинохрома А.
Технический результат изобретения заключается в возможности быстрого, простого и безопасного получения 2-х целевых продуктов из панциря морских ежей: антиоксидантного пигментного комплекса, компоненты которого активнее эхинохрома А в отношении DPPH радикала и водорастворимых кальциевых солей органических кислот.
Источники информации
1. Lebedev AV, Ivanova MV, Levitsky DO. Iron chelators and free radical scavengers in naturally occurring polyhydroxylated 1,4-naphthoquinones // Hemoglobin, 2008. - 32(1-2). - P.165-179.
2. Kuwahara R, Hatate H, Yuki T et al. Antioxidant property of polyhydroxylated naphthoquinone pigments from shells of purple sea urchin Anthocidaris crassispina // LWT - Food Science and Technology, 2009. - 42. - P.1296-1300.
3. Pozharitskaya O.N., Ivanova S.A., Shikov A.N., Makarov V.G., Galambosi B. Separation and evaluation of free radical-scavenging activity of phenol components of green, brown, and black leaves of Bergenia crassifolia by using HPTLC-DPPH* method. / J Sep Sci. - 2007. - 30(15). - P.2447-2451.
4. Мищенко Н.П., Федореев C.A., Глазунов В.П. и др. Выделение и идентификация примесей в субстанции эхинохром и препарате гистохром // Хим-фармац. журн. - 2004. - 38(1). - С.50-53.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПИГМЕНТНОГО КОМПЛЕКСА БИСНАФТАЗАРИНОВ | 2014 |
|
RU2545692C1 |
| СПОСОБ ПОЛУЧЕНИЯ СПИНОХРОМА А И БЕЛКА МОРСКИХ ЕЖЕЙ, ВЗАИМОДЕЙСТВУЮЩЕГО С ПОЛИГИДРОКСИНАФТОХИНОНОМ | 2008 |
|
RU2362573C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,7-ТРИОКСИЮГЛОНА (СПИНОХРОМА В) | 2014 |
|
RU2568604C1 |
| Способ получения нафтохинонов из морских ежей | 2016 |
|
RU2645077C1 |
| Способ получения кальцийсодержащей композиции из панциря морских ежей | 2015 |
|
RU2611847C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ МОРСКИХ ЕЖЕЙ | 2010 |
|
RU2432956C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,6,7-ТЕТРАГИДРОКСИНАФТАЗАРИНА | 2009 |
|
RU2411939C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ И ПРОТИВОАЛЛЕРГИЧЕСКИМ ДЕЙСТВИЕМ | 2012 |
|
RU2488402C1 |
| СРЕДСТВО НА ОСНОВЕ БИСНАФТАЗАРИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2669374C2 |
| Способ получения водорастворимой солевой формы эхинохрома А, пригодной для использования в фармакологической и пищевой промышленности | 2019 |
|
RU2697197C1 |

Изобретение относится к фармацевтической промышленности и касается способа переработки панциря морского ежа. Способ переработки панциря морского ежа, заключается в том, что панцири с иглами морских ежей промывают, высушивают, измельчают, деминерализуют слабой органической кислотой, центрифугируют, соль органической кислоты осаждают добавлением органического растворителя, смешивающегося с водой, отфильтровывают, фильтрат концентрируют, нейтрализуют, концентрируют под вакуумом, лиофильно высушивают, антиоксидантный пигментный комплекс перерастворяют из органического растворителя, при определенных условиях. Способ позволяет осуществлять безотходную переработку панцирей и игл морского ежа и обеспечивает расширение спектра биологически активных веществ. 1 з.п. ф-лы, 3 ил.
1. Способ переработки панциря морского ежа, характеризующийся тем, что панцири с иглами морских ежей промывают от остатков внутренностей, высушивают при температуре 5-8°С или 40-50°С, измельчают, деминерализуют при температуре 40-90°С небольшим стехиометрическим избытком слабой органической кислоты, используя 10-80%-ный водный раствор кислоты, полученную смесь центрифугируют, соль органической кислоты осаждают добавлением органического растворителя, смешивающегося с водой, отфильтровывают, фильтрат концентрируют, нейтрализуют до pH 4-7 добавлением водорастворимых солей натрия, калия или подобных, концентрируют под вакуумом при температуре не выше 60°С, лиофильно высушивают, антиоксидантный пигментный комплекс перерастворяют из органического растворителя.
2. Способ по п.1, где в качестве слабой органической кислоты используют молочную, уксусную, муравьиную, винную, аскорбиновую или лимонную кислоту, а в качестве органического растворителя используют этиловый спирт, ацетон, ацетонитрил.
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ ПЛОСКИХ МОРСКИХ ЕЖЕЙ | 2006 |
|
RU2305548C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,5,7,8-ПЕНТАГИДРОКСИ-6-ЭТИЛ-1,4-НАФТОХИНОНА | 2005 |
|
RU2283298C1 |
| KR 20020000660 A, 05.01.2002. | |||
Авторы
Даты
2012-02-10—Публикация
2010-12-24—Подача