Изобретение относится к медицине и может быть использовано в кардиологии или терапии.
Известны способы разделения на фракции липопротеинов крови методом аналитического ультрацентрифугирования (А.Н.Климов, Н.Г.Никульчева. Липиды, липопротеины и атеросклероз. - Питер, пресс, с.98-102).
Известен способ разделения на фракции ЛП в полиакриламидном геле (Н.Н.Шацкая. Биохимические исследования в оценке состояния сердечно-сосудистой системы. В кн. "Методы исследований в профпатологии", М., 1988, с.95-97).
Известны также способы разделения на фракции ЛП путем электрофореза в геле агарозы (Лаб. Методы исследования / Под редакцией В.В.Меньшикова. М.: Медицина, 1987, с.248-249), SU 1720015 А, 15.03.1992. RU 2063040 C1, 27.06.1996. RU 2115121 C1, 10.07.1998. RU 2097038 C1, 27.11.1997. RU 2060034 C1, 20.05.1996. EP 0074610 A, 23.03.1983.
Недостатком данных способов является то, что они не позволяют выявить все фракции ЛП крови, включая хиломикроны (ХМ), липопротеины высокой плотности (ЛПВП), липопротеины низкой плотности (ЛПНП), липопротеины очень низкой плотности (ЛПОНП) и ЛП(а), а служат для разделения на фракции ХМ, ЛПВП, ЛПНП, ЛПОНП от комплекса альбумина с неэтерифицированными жирными кислотами, а также не позволяют выявить минорные фракции модифицированных липопротеинов крови, а именно модифицированных Lipoprotein abnormal (Lp(a) или ЛП(а)).
Известен способ определения фракций липопротеинов крови авторов Канской Н.В., Федоровой Н.А., Перовой Н.В., Гарганеевой Н.П., Кожановой А.А., Байкова А.Н., Канского А.В., Похряева Е.Н. RU 2210079 С2 G01N 33/92, 10.08.2003 Бюл. №22.
Данный способ является наиболее близким к предлагаемому по технической сущности и достигаемому результату и выбран в качестве прототипа.
Недостатком данного способа является то, что он не позволяет выявить минорные фракции модифицированных ЛП(а). Это связано с тем, что минорная фракция ЛП(а) является наиболее атерогенной. Поэтому для ранней диагностики заболевания особенно важно выявление минорной фракции ЛП(а) наряду с максимально полным определением фракций других ЛП крови.
Целью предлагаемого изобретения является повышение точности способа.
Указанная цель достигается тем, что сыворотку крови обрабатывают 7% раствором ПЭГ 6000, а затем инкубируют ПЭГ 6000 - преципитат сыворотки крови с красителем Суданом Б при 40°С в темном термостате в течение 1 ч и вносят для электрофоретического исследования в увеличенную в 2 раза по объему лунку геля агарозы. Перед обработкой сыворотки крови 7% ПЭГ 6000 к 0,6 мл пробы добавляют 0,2 мл 0,1% раствора тритон Х-100 и инкубируют при 20°С в течение 15 мин, перемешиванием смеси методом встряхивания 120 раз в 1 мин и выявляют минорные фракции модифицированных липопротеинов крови.
Новым в данном способе является то, что пробу сыворотки крови пациента обрабатывают детергентом тритон Х-100, инкубируют 15 мин при 20°С, перемешивают смесь методом встряхивания 120 раз в 1 мин, что позволяет дополнительно выявлять интенсивные минорные фракции модифицированных липопротеинов крови.
Следовательно, только комплексная модернизация способа-прототипа позволяет получить желаемый результат.
Для получения ПЭГ-6000 преципитата сыворотки крови использовался 7%-ный раствор ПЭГ-6000. Известно, что 7%-ный ПЭГ-6000 является предельной концентрацией для получения преципитатов сыворотки крови, содержащих иммунные комплексы и не содержащих грубодисперсных белков сыворотки крови. Применение 6%-ного раствора ПЭГ-6000 не позволяет полностью осадить иммунные комплексы сыворотки крови. Поэтому для повышения точности способа экспериментальным путем была выбрана 7%-ная концентрация ПЭГ-6000, позволяющая, с одной стороны, полностью осадить иммунные комплексы из сыворотки крови с гарантией отсутствия грубодисперсных (высокомолекулярных) белков сыворотки крови, а с другой стороны, позволяющая полностью осадить циркулирующие иммунные комплексы (ЦИК), присутствующие в сыворотке крови. Так, в случае концентрации ЦИК в сыворотке крови, равной 2,5 г/л, эта же концентрация ЦИК выявлена в 7%-ных преципитатах сыворотки крови (с результатом +3%), что связано с увеличением числа манипуляций, а не изменением концентрации ЦИК в преципитатах сыворотки крови.
Инкубация 7% ПЭГ-6000 преципитата исследуемой сыворотки крови с красителем судана Б повышает сродство красителя к ЛП преципитатов крови, а большой объем взятого для исследований образца крови позволяет выявить модифицированные ЛП(а), содержащиеся в крови больных ишемической болезнью сердца (ИБС) в очень низких концентрациях. Дополнительная обработка сыворотки крови тритоном Х-100 с перемешиванием смеси методом встряхивания 120 раз в 1 мин позволяет повысить точность способа и получить желаемый результат. Предлагаемый способ позволяет выявлять следующие минорные фракции модифицированных ЛП: ЛПВП, ЛПНП, ЛПОНП и ЛП(а).
Каждый вновь введенный в формулу изобретения признак выполняет функцию повышения точности и эффективности способа: обработка 0,6 мл пробы сыворотки крови пациента 0,2 мл 0,1% раствора тритон Х-100, инкубация пробы при 20°С в течение 15 мин, перемешиванием смеси методом встряхивания 120 раз в 1 мин и дополнительное выявление минорных фракций модифицированных липопротеинов.
Исследование ЛП разных классов при диагностике ишемической болезни сердца (ИБС) рекомендовано Всероссийским научным обществом кардиологов согласно положению рекомендаций Европейского общества по изучению атеросклероза- «Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза» (г.Москва, 2005 г.; Клиническая лабораторная диагностика, №10, 2008., с.21-32).
В настоящее время перспективными являются методы исследования липидов с детергентами /Тритон Х-100 и др./. В лабораторной практике все больше используются прямые или гомогенные методы определения липопротеинов (ЛП) и их липидов. Такие методы основаны на использовании различных детергентов, способных блокировать или солюбилизировать классы ЛП для специфического выделения ЛПВП, ЛПНП и других фракций ЛП.
При использовании таких методов изоляция других классов ЛП не требует дополнительных операций и концентрацию холестерина (ХС) в классах ЛП можно определить напрямую в сыворотке крови общепринятыми ферментными методами в той же кювете («Клиническая лабораторная диагностика, №10, 2008., с.21-32).
Увеличение концентрации ЛП abnormal или ЛП (а) в крови считают независимым фактором риска атеросклероза. При содержании в крови ЛП(а) более 300 мкг/мл при норме 0-300 мкг/мл риск возникновения коронарного атеросклероза увеличивается вдвое, а при одновременном повышении уровня ЛП(а) ХС и ХС ЛПНП - в 5 раз (J.A. M.A. - 2001. - Vol.285, - p.2486-2497, Eur. Heart. J. - 2003. - Vol.24, - p.1601-1610).
В настоящее время особое внимание уделяется исследованию минорных фракций модифицированных ЛП(а), в связи с чем разрабатываются способы лабораторной диагностики, позволяющие исследовать этот липопротеин крови. Он относится к апо-В-содержащим липопротеинам, богатым холестеролом (ХС). ЛП(а) идентичен "тонущим" пре-β-ЛП (sinking pre-β-Lp), имеющим при электрофорезе подвижность пре-β-ЛП. ЛП(а) содержат 27% белка, 8% углеводов и 65% липидов, из которых ЭХС составляют 59%, НЭХС 14%, ФЛ 14%.
Белковым компонентом ЛП(а) является высокогликозилированный полипептид-апо(а), имеющий близкое структурное сродство к плазминогену - одному из факторов системы свертывания - противосвертывания крови. При росте концентрации как ЛП(а), так и его модифицированных форм в крови нарушаются процессы микроциркуляции в кровеносных артериях с возможным образованием микротромбов.
Благодаря наличию в структуре апо(а) сиаловых кислот ЛП(а) более отрицательно заряжен по сравнению с β-ЛП в электрическом поле, лучше растворим в воде, может взаимодействовать с ионами металлов (кальция). Этот липопротеин и его модифицированные формы гетерогенны. Все это свидетельствует об особой роли ЛП(а) и модифицированных ЛП(а) в атерогенезе.
ЛП(а) может взаимодействовать с ЛПНП-рецепторами, оказывая слабое влияние на активность ГМК-КоА редуктазы, на этерификацию ХС. Период полураспада ЛП(а) длиннее, чем у ЛПНП и составляет 3,3 суток. Содержание ЛП(а) в крови в норме не превышает 30 мг/л. При высокой концентрации в крови ЛП(а) выявляется в местах поражения сосудов в области скопления фибриногена. Повышенная концентрация ЛП(а) часто сочетается с IIa, IIб типами гиперлипопротеинемий, при которых часто выявляются модифицированные ЛП. Поэтому в клинической практике крайне важно определение ЛП(а) одновременно с определением белков острой фазы воспаления. Установлено, что большинство гиполипидемических препаратов не влияет на повышенный уровень ЛП(а).
Фракция ЛП(а) гетерогенна. Установлено, что при электрофорезе ЛП(а) находятся в области β-глобулинов, но до 5% ЛП(а) при этом могут выявляться в области α-глобулинов. По причине такой выраженной гетерогенности достаточно сложно оценить при электрофорезе всю фракцию ЛП(а), а тем более ее минорные фракции, которые могут оставаться на линии старта, если размер их частиц достаточно велик. Поэтому использование общепринятого в исследованиях последнего пятидесятилетия детергента тритон Х-100 для обработки сыворотки крови, а именно липопротеинов крови, ведущее к частичной делипидизации ЛП и увеличению их подвижности при электрофорезе позволяет выявлять минорные фракции ЛП(а). В химической промышлености используются различные детергенты (при изготовлнении стирального порошка, моющих средств и т.д.), но при работе с биологическим материалом используется преимущественно ТритонХ-100. Режим обработки пробы Тритоном Х-100 подбирался на основе экспериментальных исследований эмпирическим путем. Для этого использовали различные разведения Тритона Х-100, различную температуру и различную экспозицию в минутах. При использовании различных концентраций раствора Тритон Х-100 малые концентрации (ниже 0,1%) не увеличивали выделения минорных фракций ЛП, в том числе ЛП (а), а высокие концентрации (больше 0,1%) вели к полной делипидизации и разрушению структуры ЛП. Результат проведенного исследования представлен в таблице 1.
Обработка 0,3 мл сыворотки крови для исследования липопротеинов разными концентрациями раствора Тритон Х-100 в течение различного времени инкубации пробы при разной температуре.
Следовательно, оптимальными условиями обработки сыворотки крови раствором Тритон Х-100 является концентрация 0,1% в объеме 0,1 мл, при температуре 20 градусов Цельсия в течение 15 минут.
Усовершенствование способа касается механического встряхивания пробы с частотой 120 раз в 1 мин на лабораторном встряхивателе для приготовления реактивов. Более частое или длительное встряхивание ведет к повышению температуры пробы и появлению ремнантных форм липопротеинов крови, что препятствует дальнейшему проведению исследования и искажает результат электрофоретического анализа пробы. Менее короткий период встряхивания, равный 30 сек, не позволяет улучшить результат исследования.
Поскольку ЛП(а) наиболее атерогенен, очень важно на ранних стадиях заболевания выявлять максимальное содержание ЛП(а) в крови каждого пациента. Это позволяет диагностировать ишемическую болезнь сердца еще до стадии значительных изменений других клинико-лабораторных показателей, повышает точность диагностики заболевания. В свою очередь таким пациентам рано назначается патогенетически обоснованная терапия. Не менее важно выявление минорных фракций ЛП(а) для оценки эффективности терапии заболевания и прогнозирования течения ишемической болезни сердца.
Все сказанное свидетельствует о крайней важности разработки способов лабораторной диагностики, позволяющих наиболее полно выявлять ЛП(а), его модифицированные формы и их минорные фракции.
В настоящее время в широкой клинической лабораторной практике недостаточно используют способы определения ЛП(а). В то же время популярность способа электрофоретического разделения на фракции ЛП крови в геле агарозы обусловлена его высокой чувствительностью, простотой осуществления и достаточной адекватностью получаемых результатов (Лаб. дело, 1980, №5, с.287-290, Клиническая лабораторная диагностика №10, 2008, с.21-32).
Существенные признаки, характеризующие изобретение, проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не являются очевидными для специалиста.
Идентичной совокупности признаков не обнаружено при изучении патентной и научно-медицинской литературы.
Данное изобретение может быть использовано в медицинской практике для повышения точности диагностики степени атеросклероза при ишемической болезни сердца.
Таким образом, следует считать предлагаемое изобретение соответствующим условиям патентоспособности: «новизна», «изобретательский уровень», «промышленная применимость».
Метод основан на электрофоретической подвижности модифицированных липопротеинов крови.
Изобретение будет понятно из следующего описания приложенных чертежей.
На фиг.1 представлены результаты электрофоретического разделения на фракции ЛП сыворотки крови: а - в группе контроля способом-прототипом; б - в группе контроля предлагаемым способом;
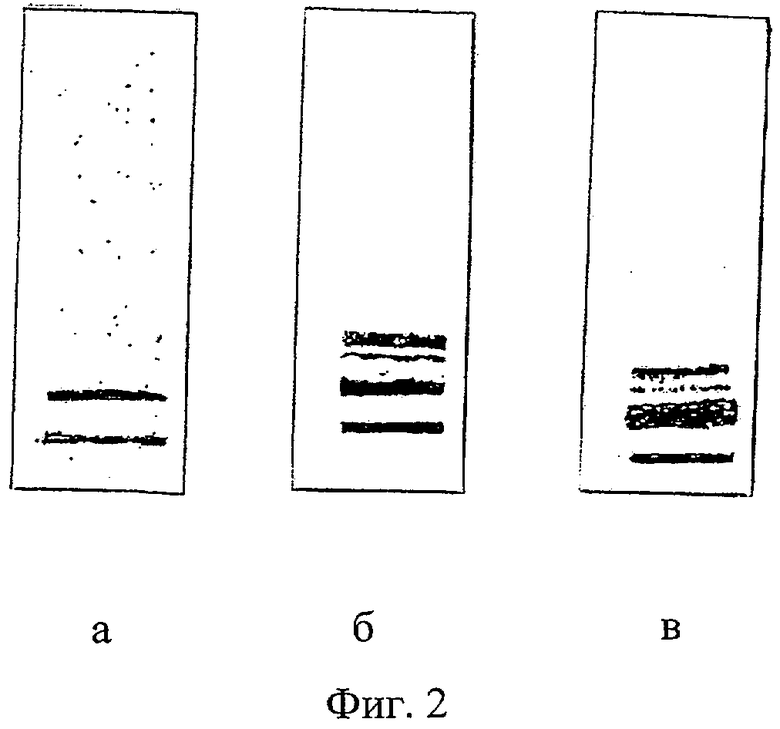
На фиг.2 а, б, в представлены результаты электрофоретического разделения на фракции ЛП сыворотки крови в группе больных ИБС способом-прототипом;
На фиг.3 представлены результаты электрофоретического разделения на фракции ЛП сыворотки крови больного Б: а - способом-прототипом; б - предлагаемым способом.
Способ осуществляется следующим образом поэтапно:
1) приготовление раствора судана Б: 400 мг судана Б растворяют в 20 мг этиленгликоля на кипящей водяной бане в течение 50 минут, фильтруют, хранят в стеклянной посуде;
2) приготовление геля агарозы: 320 мг агарозы А фирмы "Sigma" растворяют в 20 мл воды при кипячении, затем помещают в термостат при 55°С; добавляют 20 мл раствора альбумина (1 г альбумина в 200 мл веронал-мединалового буфера, pH 8,6). 3 мл геля агарозы наносят на обезжиренное горизонтально установленное предметное стекло, помещают металлический стальной стержень-брусок 20×4 мм (высотой 10 мм), который после застывания геля убирают магнитом;
3) к 0,6 мл пробы сыворотки крови пациента добавляют 0,2 мл 0,1% раствора тритон Х-100, инкубируют 15 мин при 20°С, перемешивают смесь методом встряхивания 120 раз в 1 мин, затем добавляют 40 мл 7% полиэтиленгликоля (ПЭГ)-6000 и инкубируют 1 ч при 20°С, центрифугируют 40 мин при 25000 g. Осадок дважды промывают.
4) 0,25 мл раствора преципитата используют для электрофоретического исследования. К 0,25 мл преципитата сыворотки крови добавляют 0,15 мл раствора Судана Б, помещают на 1 ч в темный термостат при 40°С, затем добавляют 0,2 мл горячего раствора геля агарозы, смешивают, подогревают при 55°С и подогретым вносят в желобок геля агарозы;
5) предметное стекло помещают в камеру для электрофореза слоем агарозы вниз, электрофорез проводят в течение часа в холодильной камере при температуре 4°С при напряжении 100 В и силе тока 40-45 мА;
6) электрофореграмму фиксируют в 5% растворе уксусной кислоты в течение одного часа, затем высушивают между листами фильтровальной бумаги, непрерывно смачивая 96% этиловым спиртом;
7) денситометрию проводят на микрофотометре МФ-4.
Для подтверждения работоспособности предлагаемого способа и достижения технического результата были обследованы группа контроля (n=12) и группа больных ИБС (n=24). Обе группы обследованы с помощью предлагаемого способа и способа-прототипа.
В группе контроля в 7% ПЭГ-6000 преципитатах сыворотки крови в случае использования способа-прототипа и предлагаемого способа ЛП не выявлены (фиг.1а, б).
В группе больных ИБС в 7% ПЭГ-6000 преципитатах сыворотки крови, с помощью способа-прототипа, выявлены ЛПНП и ЛПОНП и следы ЛП(а) (фиг.2а, б, в).
В группе больных ИБС в 7% ПЭГ-6000 преципитатах сыворотки крови предлагаемым в качестве изобретения способом, кроме фракций ЛПНП, ЛПОНП в зоне между ЛПНП и ЛПОНП, выявлены минорные фракции модифицированных ЛП(а) у 18 пациентов, а у 6 пациентов этой группы фракция ЛП(а) выявлена в виде низких концентраций.
Пример
Пациент Г., 55 лет. История болезни №194. Поступил в отделение ИБС и атеросклероза НИИ кардиологии ТНЦ СО РАМН с жалобами на боли за грудиной и в области сердца, возникающие при физической нагрузке; боли купируются нитроглицеролом. Больного беспокоит одышка при физической нагрузке. АД 160/90 мм рт.ст., пульс в покое 66 ударов в минуту.
Диагноз: ишемическая болезнь сердца, стенокардия напряжения ФК II.
Результаты лабораторных исследований: ХС общий 8,8 ммоль/л; триацилглицерол 1,6 ммоль/л; ХС ЛПВП 0,9 ммоль/л.
Результаты электрофоретического исследования ЛП крови данного больного по способу-прототипу представлены на (фиг.3а), а по предлагаемому способу на (фиг.3б). Выявлены модифицированные ЛПНП, ЛПВП, ЛПОНП, ЛП(а) в низкой концентрации.
Предлагаемый способ позволяет выявить у больных ИБС с выраженной гиперхолестеролемией наличие минорных фракций модифицированных ЛП(а) (м ЛП(а)) способом электрофореза ЛП в геле агарозы.
Применение предлагаемого способа разделения на фракции ЛП крови в отличие от способа-прототипа позволило выявить дополнительную интенсивную минорную фракцию модифицированных ЛП(а), что повышает точность способа.
При этом предлагаемый способ прост в использовании и интерпретации полученных результатов.
Приложение
Таблица 1. Исследование влияния детергента Тритон Х-100 на выявление фракций липопротеидов при разном времени инкубации и разной температуре, то есть определение оптимальных условий;
Фиг.1. Представлены результаты электрофоретического разделения на фракции ЛП сыворотки крови: а - в группе контроля способом-прототипом; б - в группе контроля предлагаемым способом;
Фиг.2 (а, б, в). Представлены результаты электрофоретического разделения на фракции ЛП сыворотки крови в группе больных ИБС способом-прототипом;
Фиг.3. Представлены результаты электрофоретического разделения на фракции ЛП сыворотки крови больного Б: а - способом-прототипом;
б - предлагаемым способом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ФРАКЦИЙ МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИНОВ КРОВИ | 2010 |
|
RU2428698C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2010 |
|
RU2439581C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2011 |
|
RU2462722C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2009 |
|
RU2396567C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2012 |
|
RU2507518C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2010 |
|
RU2439582C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2009 |
|
RU2398239C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2011 |
|
RU2470294C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФРАКЦИЙ МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИНОВ КРОВИ | 2007 |
|
RU2364873C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 2012 |
|
RU2520755C1 |


Изобретение относится к медицине и касается способа определения фракций модифицированных липопротеинов крови. Сущность способа заключается в том, что сыворотку крови пациента обрабатывают 7% раствором полиэтиленгликоля-6000, инкубируют и с красителем Суданом Б при 40°С в течение 1 ч, разделяют электрофоретически в геле агарозы. Далее дополнительно перед обработкой сыворотки крови 7% ПЭГ-6000 к 0,6 мл пробы добавляют 0,2 мл 0,1% раствора тритона Х-100, инкубируют 15 мин при 20°С и затем перемешивают смесь методом встряхивания 120 раз в 1 мин. Использование способа позволяет выявить дополнительную интенсивную минорную фракцию модифицированных ЛП(а), что повышает точность диагностики. 3 ил., 1 табл.
Способ определения фракций модифицированных липопротеинов крови путем обработки сыворотки крови 7%-ным раствором полиэтиленгликоля-6000, инкубации с красителем Судан Б при 40°С в течение 1 ч с последующим электрофоретическим разделением в геле агарозы, отличающийся тем, что дополнительно перед обработкой сыворотки крови 7% ПЭГ-6000 к 0,6 мл пробы добавляют 0,2 мл 0,1%-ного раствора тритона Х-100, инкубируют 15 мин при 20°С и затем перемешивают смесь методом встряхивания 120 раз в 1 мин.
| СПОСОБ ОПРЕДЕЛЕНИЯ ФРАКЦИЙ МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИНОВ КРОВИ | 2000 |
|
RU2210079C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФРАКЦИЙ ЛИПОПРОТЕИДОВ КРОВИ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2000 |
|
RU2200950C2 |
| Способ определения модифицированных липопротеидов крови | 1989 |
|
SU1720015A1 |
| CN 101051051 A, 10.10.2007 | |||
| SOLLER M | |||
| et al | |||
| Isolation and characterization of soluble acidic lipoproteins from rat brain synaptic vesicles | |||
| Journal of Neurochemistry, 1973, vol.21, pp.557 to 572 | |||
| Pergamon Press | |||
| Printed in Great Britain | |||
| PATSY M | |||
| NISHINA et al. | |||
Авторы
Даты
2011-03-10—Публикация
2009-02-02—Подача