Предлагаемое изобретение относится к области органической химии, а именно к способу синтеза N-(1,3,5-дитиазинан-5-ил)-тиомочевины формулы
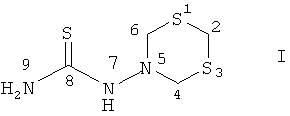
Представленное соединение может найти применение в качестве модифицированного селективного сорбента благородных и драгоценных металлов [Муринов Ю.И., Майстренко В.Н., Афзалетдинова Н.Г. Экстракция металлов S,N-органическими соединениями, М., Наука, 1993, с 192] и как низкомолекулярный биорегулятор (инсектицид, гербицид, биоцид) [Harvey M. Loux., Patent U.S. №3.466.280, 9, 1969].
Синтез N-(1,3,5-дитиазинан-5-ил)-тиомочевины в литературе не описан.
В литературе описан синтез соответствующих 4,6-диимино-1,3,5-дитиазинанов (IV, V) в реакциях взаимодействия 1,5-дифенилтиобиурета (II) с бромистым метиленом [Underwood H.G., Dains F.B. The Actions of Perthiocyanic Acid on Amines // J. Am. Chem. Soc, 1935, V.57, p.1768-1771] или (II) с 1-ароил-2-фенилацетиленами (III) в присутствии BF3*Et2O [Глотова Т.Е., Процук Н.И., Албанов А.И. и др. Синтез новых производных 1,3,5-дитиазинана. // ЖОХ, 2003, т.73, вып.5, с 834-838].

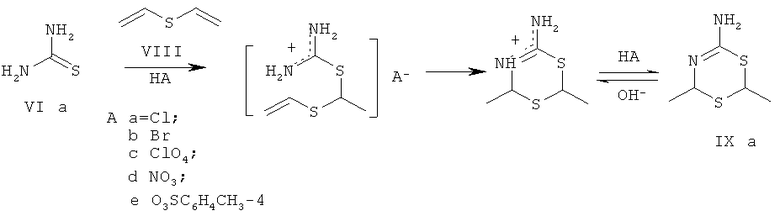
Известен способ получения гидробромидов 4,6-диимино-1,3,5-дитиазина (VIIa-г) при взаимодействии тиомочевины (VIa-г) с бромистым метиленом в EtOH [Grogan C.H., Rice L.M. Dithiazanes or Methylenediisothiuronium Salts // J. Org. Chem. 1963, V.28, №9, p.2486-2487], тогда как в реакции тиомочевины (VIa) с дивинилсульфидом (VIII) в присутствии сильных кислот происходит образование ненасыщенного 1,3,5-дитиазинана (IX) [Трофимов Б.А., Гаврилова Г.М., Калабин Г.А., Баиров В.В, Амосова С.В. Циклоприсоединение дивинилсульфида к тиомочевине // Химия гетероциклических соединений, 1979, №11, с.1466-1469].

Из литературных данных известно, что алифатические амиды (Ха-д), вступая в реакцию циклотиометилирования в присутствии BuONa/BuOH, образуют N-ацил-1,3,5-дитиазинаны (XIa-д) [В.Р.Ахметова, P.P.Хайруллина, Г.Р.Надыргулова, Р.В.Кунакова, У.М.Джемилев. Мультикомпонентная гетероциклизация амидов карбоновых кислот с H2S и CH2O. Журнал органической химии, 2008, т.44, №21, с 200-206].

Перечисленными выше способами не может быть получена N-(1,3,5-дитиазинан-5-ил)-тиомочевина.
Задачей изобретения является получение N-(1,3,5-дитиазинан-5-ил)-тиомочевины однореакторной конденсацией гидразинкарботиоамида (тиосемикарбазида) с формальдегидом и сероводородом.
Предлагаемый нами способ синтеза 1,3,5-дитиазинанов заключается во взаимодействии насыщенного сероводородом формальдегида со свежеприготовленной смесью тиосемикарбазид-BuONa/BuOH (pH>11.5) при соотношении тиосемикарбазид:BuONa/BuOH, равном 1:3. Реакция осуществляется при соотношении тиосемикарбазид:формальдегид:сероводород, равном 1:3:2. Реакционную смесь перемешивают 7 ч, поддерживая заданную температуру (40°C), затем нейтрализуют расчетным количеством разбавленной HCl. Образующуюся N-(1,3,5-дитиазинан-5-ил)-тиомочевину отфильтровывают и промывают EtOH. Реакция протекает по схеме:

Преимущества предлагаемого способа
На основании предложенного способа можно селективно получать N-(1,3,5-дитиазинан-5-ил)-тиомочевину, синтез которой в литературе ранее не описан. Предлагаемый способ препаративно прост, в качестве растворителя используется н-бутиловый спирт, процесс не требует больших энергозатрат, и не образуются токсичные отходы.
Способ поясняется примерами
ПРИМЕР. В стеклянный реактор, снабженный магнитной мешалкой, обратным холодильником, газопроводящей трубкой и капельной воронкой, при 40°C помещали 3 моля формальдегида, барботированием насыщали его сероводородом в течение 20 мин. В другом реакторе при комнатной температуре (20°C) смешивали тиосемикарбазид с BuONa/BuOH при соотношении 1:3 (pH>11.5) и прибавляли по каплям в раствор, полученный барботированием газообразного H2S в формальдегид. Реакционную смесь перемешивали 7 ч, поддерживая заданную температуру (40°C), затем нейтрализовали расчетным количеством разбавленной HCl. Образующуюся N-(1,3,5-дитиазинан-5-ил)-тиомочевину отфильтровывали и промывали EtOH. Выход составил 92%.
Спектральные характеристики
N-(1,3,5-дитиазинан-5-ил)-тиомочевины

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N-(1,3,5-ДИТИАЗИНАН-5-ИЛ)-ИЗОНИКОТИНАМИДА И N-(2,4,6-ТРИМЕТИЛ-1,3,5-ДИТИАЗИНАН-5-ИЛ)-ИЗОНИКОТИНАМИДА | 2010 |
|
RU2447072C2 |
| СПОСОБ ПОЭТАПНОГО ПОЛУЧЕНИЯ 1,7,13,19,25,31,37,43-ОКТАТИА-3,5,9,11,15, 17,21,23,27,29,33,35,39,41,45,47-ГЕКСАДЕКААЗАЦИКЛООКТАТЕТРАКОНТАН-4,10,16,22,28,34,40,46-ОКТАТИОНА И 5,6-ДИГИДРО-2Н-ТИАДИАЗИН ГИДРОЙОДИДА | 2010 |
|
RU2490264C2 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 2-, 3- И 4-(1,3,5-ДИТИАЗИНАН-5-ИЛ) ТИОФЕНОЛОВ | 2009 |
|
RU2425039C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ФЕНИЛ(БЕНЗИЛ)-(1,3,5-ДИТИАЗИНАН-5-ИЛ)АМИНОВ | 2010 |
|
RU2443692C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АРИЛ-1,3,5-ДИТИАЗИНАНОВ | 2010 |
|
RU2443694C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОНО-(ДИ-, ТЕТРА-)МЕТИЛ-1,2-БИС-(1,3,5-ДИТИАЗИНАН-5-ИЛ)ЭТАНОВ | 2010 |
|
RU2443702C2 |
| СПОСОБ ПОЛУЧЕНИЯ 5-[4-(1,3,5-ДИТИАЗИНАН-5-СУЛЬФОНИЛ)-ФЕНИЛ]-1,3,5-ДИТИАЗИНАНА | 2007 |
|
RU2342369C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-[4-НИТРО(2,4-ДИНИТРО)ФЕНИЛ]-1,3,5-ДИТИАЗИНАН-5-АМИНОВ | 2010 |
|
RU2434857C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АРИЛ(БЕНЗИЛ)-(1,3,5-ДИТИАЗИАН-5-ИЛ)АМИНОВ | 2010 |
|
RU2464265C2 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСИ 3-ТИА-1,5-ДИАЗАБИЦИКЛО[4.3.1]ДЕКАНА И 5-[4-(1,3,5-ДИТИАЗИНАН-5-ИЛ)БУТИЛ]1,3,5-ДИТИАЗИНАНА | 2006 |
|
RU2323933C1 |
Изобретение относится к области органического синтеза. Полученная предлагаемым способом N-(1,3,5-дитиазинан-5-ил)-тиомочевина может найти применение в качестве селективных сорбентов и экстрагентов благородных и драгоценных металлов. Сущность способа заключается во взаимодействии насыщенного сероводородом формальдегида с предварительно приготовленной смесью тиосемикарбазид-BuONa/BuOH (pH>11.5) при соотношении тиосемикарбазид:BuONa/BuOH: CH2O:H2S, равном 1:3:3:2, в течение 7 ч (40°С) с последующей нейтрализацией расчетным количеством разбавленной HCl. Выход целевой N-(1,3,5-дитиазинан-5-ил)-тиомочевины составил 92%.
Способ получения N-(1,3,5-дитиазинан-5-ил)-тиомочевины формулы:

отличающийся тем, что насыщенный сероводородом формальдегид взаимодействует с предварительно приготовленной смесью тиосемикарбазид - BuONa/BuOH (pH>11.5) при соотношении тиосемикарбазид: BuONa/BuOH: CH2O: H2S, равном 1:3:3:2, температуре 40°С в течение 7 ч с последующей нейтрализацией расчетным количеством разбавленной HCl.
| US 3466280, 09.09.1969 | |||
| СПОСОБ ПОЛУЧЕНИЯ 5-АЦИЛ-ПЕРГИДРО-1,3,5-ДИТИАЗИНОВ | 2005 |
|
RU2291150C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-[1',3',5'-ДИТИАЗИНАН-5'-ИЛ-КАРБОНИЛ]-1,3,5-ДИТИАЗИНАН-5-КАРБОКСАМИДА | 2007 |
|
RU2342370C1 |
Авторы
Даты
2011-03-20—Публикация
2009-09-24—Подача