Изобретение относится к медицине, в частности к молекулярно-генетическим исследованиям, а именно к области диагностики генетической предрасположенности к различным видам физических нагрузок и особенностей тренировочного процесса.
Известен способ определения физической работоспособности, основанный на анализе мутаций в генах ACTN3, AMPD1, ACE. Для реализации данного способа используется метод анализа мутаций в генах ACTN3 (R577X) при помощи ПЦР-амплификации интересующего фрагмента данного гена, с использованием оригинальных праймеров, и его последующее расщепление соответствующей эндонуклеазой рестрикции. В дальнейшем результат регистрируется с помощью гель-электорофореза. Исследование мутаций в генах AMPD1 (С34Т) и ACE (17I/D) проводится по аналогичной методике, для каждого из генов в отдельности (В.А.Рогозкин, И.В.Астратенкова, A.M.Дружевская, О.Н.Федоровская // Гены-маркеры предрасположенности к скоростно-силовым видам спорта // Теория и практика физической культуры 2005, с.5-8).
При наличии С-аллели гена ACTN3 считают, что индивидууму целесообразней заниматься скоростно-силовыми видами спорта, а при наличии T-аллели предпочтительнее виды спорта на выносливость. Наличие C-аллели гена AMPD1 указывает на предрасположенность к скоростно-силовым видам спорта, а T-аллели - к видам на выносливость. При наличии I-аллели гена ACE считают, что индивидууму целесообразней заниматься видами спорта на выносливость, а при наличии D-аллели предпочтительнее скоростно-силовые виды спорта.
Недостатком данного метода являются трудоемкость проведения анализа и дороговизна вследствие повышенного использование расходного материала, в связи с тем, что каждый из генов исследуется отдельно, а также разноплановость функционального значения продуктов исследуемых генов без последующей интерпретации и рекомендаций с учетом полученных результатов.
Известен метод исследования делеции пяти пар нуклеотидных оснований в промотерной зоне гена CNB и его ассоциация с гипертрофией левого желудочка. Продукт гена CNB входит в состав регуляторной субъединицы Ca2+-модулинфосфотазы, являющейся одним из основных регуляторов концентрации ионов Ca в организме. В результате замены происходит активация транскрипции генов приводящих к развитию различных форм гипертрофии левого желудочка сердца, что в дальнейшем влияет на снижение физической работоспособности и ограничение переносимых физических нагрузок (Weihong Tang, Donna К. Arnett, Richard В. Devereux, Demetrios Panagiotou, Michael A. Province, Michael B. Miller, Giovanni de Simone, Charles Gu // Identification of a novel 5-base pair deletion in calcineurin B (PPP3R1) promoter region and its association with left ventricular hypertrophy, c.845-851).
Существует метод анализа полиморфизма 5I/5D в гене CNB (PPP3R1), который заключается в ПЦР-амплификации интересующего фрагмента гена, с использованием оригинальных подобранных праймеров с его последующим расщеплением соответствующей эндонуклеазой рестрикции, в дальнейшем результат регистрируется методом гель-электрофореза. Полученные результаты рассматривают в аспекте развития патологий сердечно-сосудистой системы.
Наличие D-аллели гена CNB связывают с риском развития патологической гипертрофии левого желудочка, что негативно сказывается на физической работоспособности и ведет к снижению переносимости физических нагрузок.
Недостатком данного метода являются время и трудоемкость проведения анализа, дороговизна вследствие повышенного использование расходного материала, а также изучение данного полиморфизма исключительно только с клинико-морфологической точки зрения и малая информативность применительно к физической работоспособности в связи с узким спектром исследуемых генов.
Известен метод исследования генетической и другой активности AMPD в скелетных мышцах здоровых людей. Скелетно-мышечная аденозинмонофосфатдезаминаза (M-изоформа) участвует в ряде биохимических процессов (в основном азотистого обмена). Играет основную роль в регуляции энергетических процессов в скелетной мускулатуре, повышает эффективность синтеза АТФ и оказывает непосредственное влияние на физическую работоспособность человека (В.Norman, D.К.Mahnke-Zizelman, R.L.Sabina. // Genetic and other determinants of AMP deaminase activity in healthy adult skeletal muscle // Journal of Applied Physiology, 85: 1273-1278, 1998).
Существует способ анализа мутации гена AMPD1 (С34Т), который проводится методом ПЦР-амплификации искомого фрагмента гена, с его последующим расщеплением соответствующей эндонуклеазой рестрикции, в дальнейшем результат регистрируется методом гель-электрофореза. После рестрикции и электрофореза продуктов амплификации геномной ДНК у индивидуумов, не содержащих данную мутацию, на электрофореграмме присутствует один гидролизированный фрагмент, у гетерозигот - два дополнительных фрагмента, соответствующих по длине гидролизированным фрагментам ДНК, и у гомозигот по мутации выявляют только эти два фрагмента. Полученные результаты анализируют методами статистики.
Согласно статистическим данным, наличие C-аллели гена AMPD1 определяет для индивидуума предпочтение к скоростно-силовым видам спорта, а T-аллели - к видам спорта на выносливость.
Недостатком данного метода являются время и трудоемкость проведения анализа, исследование только одного гена по отношению к функциональному состоянию мускулатуры и особенностям эффективности тренировочного процесса, а также невозможность одновременной и быстрой диагностики большого количества мутаций для одного или разных генов.
Для оценки физической работоспособности на основе определения значения гена ACTN3 используют метод, который заключается в том, что анализ мутации гена ACTN3 (R577X) проводят методом ПЦР-амплификации искомого фрагмента гена, с его последующим расщеплением соответствующей эндонуклеазой рестрикции, в дальнейшем результат регистрируют методом гель-электрофореза. Полученные результаты статистически обработывают и делают вывод о значимости влияния генотипа гена ACTN3 на физическую работоспособность человека (North Kathryn Nance (AU) // ACTN3 genotype screen for athletic performance // Australian Provisional Patent Application № 2002951411 // 25.03.2004).
Недостатком данного метода являются трудоемкость проведения анализа, рассмотрение и изучение значения только одного гена, ассоциированного с физической работоспособностью, а также невозможность одновременной и быстрой диагностики большого количества мутаций для одного или разных генов.
Наиболее близким к предлагаемому изобретению является способ диагностики сердечно-сосудистых заболеваний и диагностический набор для его осуществления.
Диагностика в этом методе проводится методом анализа полиморфизма генов ACE, AGTR1, ENOS, MTHFR, MTRR, АРОЕ методом мультиплексной полимеразной цепной реакции (ПЦР), осуществляемой путем смешивания компонент и добавления в набор широкой группы олигопраймеров, с последующим анализом полиморфизма длин рестрикционных фрагментов (ПДРФ) и визуализацией в полиакриламидном геле (Глотов О.С. и др. // Исследование функционально-значимых полиморфизмов ACE, AGTR1, ENOS, MTHFR, MTRR и APOE генов в популяции Северо-Западного региона России. // Экологическая генетика, 2004 г. // TII, выпуск 3, стр.32-35).
Преимуществом данного метода являются простота и удобство в применении, высокая скорость анализа (за счет стандартизации протокола анализа), снижение затрат на диагностические операции и расходный материал.
Недостатком данного способа является неприменимость конкретного метода для диагностики мутаций и генов, связанных с физической работоспособностью.
В основу изобретения положена задача создания простого, недорогого, специфичного метода, позволяющего выявлять функционально-значимые полиморфные локусы, а также "наращивать" число анализируемых генов с целью дальнейшего внедрения в любую стандартную клиническую лабораторию. Это обеспечивается за счет проведения мультиплексной полимеразной цепной реакции (ПЦР) в одну стадию с использованием уникального набора праймеров, продукт которой в дальнейшем анализируют методом анализа полиморфизма длины рестрикционных фрагментов (ПДРФ).
Решение поставленной задачи обеспечивается тем, что в способе определения физической работоспособности человека посредством анализа полиморфизма генов методом мультиплексной полимеразной цепной реакции, осуществляемой путем смешивания компонент и добавления олигопраймеров, с последующим анализом полиморфизма длин рестрикционных фрагментов и визуализацией электрофореграммы в полиакриламидном геле, генетическую предрасположенность определяют путем анализа полиморфизма генов ACTN3 (R577X), CNB (5I/5D), AMPD1 (C34T) методом мультиплексной полимеразной цепной реакции с использованием набора праймеров, при этом для гена ACTN3 (R577X или 1747C/TJ используют праймеры: 5'-ACTGCTGCCCTTTCTGTTGCCT-3' и 5'-CTGCAGGTGGCACTGACCATA-3', для гена CNB (5I/5D) используют праймеры: 5'-GGAGTTTAAAAGCCAGCCAGTCATACTA-3' и 5'-TGGAAGATCACACCATTTGATTAGCAGT-3', для гена AMPD1 (С34Т) используют праймеры: 5'-GCAATCTACATGTGTCTACCCCAAAG-3' и 5'-CACTGCTGAAAAATAGCCATGTTTCTG-3', при этом в одну пробирку объединяют три пары праймеров, подобранных со средней температурой плавления 58-59°C при стандартных условиях, и на основании результата анализа электрофореграммы составляют клиническую интерпретацию, включающую в себя рекомендации по особенностям тренировочного процесса и интенсивности физических тренировок.
Продукт полимеразной цепной реакции гена ACTN3 подвергают гидролизу эндонуклеазами рестрикции BstDEI (CCCGAGGCTGACTGAGAGCGAG).
Продукт полимеразной цепной реакции гена CNB подвергают гидролизу эндонуклеазами рестрикции Vsp1 (GTTAATTGTACACTTAAATTAATAGCAACTGTATACT).
Продукт полимеразной цепной реакции гена AMPD1 подвергают гидролизу эндонуклеазами рестрикции Tail (TACAGCTGAAGAGAAACGTGAGTATTGCATT).
При составлении рекомендаций наличие генотипа C/C по гену ACTN3 интерпретируют как предрасположенность к скоростно-силовым видам спорта, генотипа C/T - как предрасположенность к силовым видам спорта, но требующим выносливости, и генотипа T/T - как предрасположенность к видам спорта, требующим выносливости.
При составлении рекомендаций наличие генотипов I/I или I/D по гену CNB интерпретируют как предрасположенность к занятию любым видом спорта без ограничений по времени и интенсивности нагрузок, и генотипа D/D - как предрасположенность к риску развития гипертрофии, и носителю этого генотипа рекомендуют ограничение тренировок по времени и интенсивности.
При составлении рекомендаций наличие генотипов C/C и C/T по гену AMPD1 интерпретируют как предрасположенность к занятию любым видом спорта без ограничений по времени и интенсивности нагрузок, а генотипа T/T - как возможность занятия спортом с ограничением тренировок по времени и интенсивности.
В качестве клинического образца преимущественно используют образцы ДНК, выделенные из лимфоцитов периферической крови и других материалов, полученных от обследуемого индивидуума.
Предлагаемый метод технически прост, обеспечивает существенное снижение времени и материальных затрат на проведения анализа. Предложенная схема проведения мультиплексной ПЦР на основе анализа генов ACTN3, CNB, AMPD1 непосредственно в клиническом образце методом мультиплексной полимеразной цепной реакции (ПЦР) с последующим анализом полиморфизма длины рестрикционных фрагментов (ПДРФ) и интерпретацией полученных результатов может быть использована с целью диагностики предрасположенности к различным видам физической нагрузки, определения особенностей тренировочного процесса.
Предлагаемое изобретение поясняется с помощью фиг.1, 2. На фиг.1 приведена электрофореграмма продукта мультиплексной ПЦР, где дорожка 1 - продукт мультиплексной ПЦР генов ACTN3, CNB, AMPDV, дорожка 2 - продукт мультиплексной ПЦР генов ACTN3, CNB, AMPD1; дорожка 3 - продукт мультиплексной ПЦР генов ACTN3, CNB, AMPD1 (длины ПЦР продуктов приведены в п.о.). На фиг.2 показана электрофореограмма ПЦР-продуктов генов диагностического набора после ферментативного гидролиза (длины ПЦР продуктов приведены в п.о.), где дорожка 1 - λ-Pst; дорожка 2 -продукт ПЦР генов ACTN3, CNB, AMPD1; дорожка 3 - продукт ферментативного гидролиза (энзиматической рестрикции).
Во время проведения мультиплексной полимеразной цепной реакции (ПЦР) с использованием уникального набора праймеров, указанных в таблице 1, происходит амплификация искомого участка гена. Наличие продуктов мультиплексной ПЦР анализируют путем электрофоретического разделения в 6% полиакриламидном геле. Продукты мультиплексной ПЦР-амплификации подвергают гидролизу соответствующими эндонуклеазами рестрикции, каждая из которых специфична для изучаемых полиморфизмов в данных генах.

В качестве клинического образца используют образцы ДНК, выделенные из лимфоцитов периферической крови, и других материалов, полученных от обследуемого индивидуума.
Существенным фактором является состав и набор праймеров для амплификации полиморфных фрагментов генов, используемый в способе экспресс-анализа генетического полиморфизма настоящего изобретения. Последовательности праймеров приведены в перечне последовательностей (Таблица 1). Подбор праймеров осуществляется согласно следующим критериям:
- отсутствие внутренней вторичной структуры;
- отсутствие комплементарности между 3'-концами, что может быть причиной образования димеров праймеров;
- наличие единой температуры плавления (разброс температур плавления праймеров не более 1°C от среднего значения).
Праймеры под номерами 1, 2 используются для идентификации мутации R577X в гене ACTN3. Праймеры под номерами 3, 4 используются для идентификации мутации 5I/5D в гене CNB. Праймеры под номерами 5, 6 используются для идентификации мутаций С34Т в гене AMPD1.
Основными характеристиками предлагаемого нами метода являются следующие:
- амплификация проводится в один раунд;
- размеры ПЦР продуктов для первого раунда составляют 200-400 п.н
- в реакции используется не более 3-х пар праймеров в одной мультиплексной смеси (для надежной воспроизводимости результатов).
В предпочтительной вариации данного способа, обеспечивающей удобство клинического применения настоящего изобретения, наличие альтернативных генетических вариантов определяют, используя образцы ДНК, выделенные из лимфоцитов периферической крови, полученные от пациента.
Полимеразная цепная реакция может быть проведена с использованием любого вида термостабильной полимеразы, работающей в соответствующем буфере. Для построения новой цепи в буфер добавляется смесь дНТФ (дАТФ, дГТФ, дЦТФ, дТТФ) в принятых концентрациях, но вместо дТТФ может быть использован дУТФ. Для проведения ПЦР могут быть использованы готовые коммерчески доступные наборы, содержащие все необходимые компоненты, за исключением праймеров.
В качестве праймеров для проведения мультиплексной полимеразной цепной реакции используют праймеры, приведенные в Таблице 1. Используются праймеры с номерами 1, 2, 3, 4, 5, 6. Существуют разнообразные химические подходы к синтезу олигонуклеотидных праймеров, например, фосфодиэфирный метод, гидрофосфорильный метод и т.д., но наибольшее распространение в настоящее время имеет фосфорамидитный метод. Синтез праймеров осуществляют, используя автоматические ДНК/РНК синтезаторы, например, (без ограничения) производства фирмы Applied Biosystems (США).
Подтверждением результата прохождения мультиплексной амплификации служат наличие соответствующих бэндов (полос) на фиг.1.
После амплификации продукты мультиплексной ПЦР подвергают ферментативному гидролизу, чтобы расщепить ПЦР продукт по следующим сайтам:
1) Ген ACTN3 - BstDEI (CCCGAGGCTGACTGAGAGCGAG)
2) Ген CNB - Vsp1 (GTTAATTGTACACTTAAATTAATAGCAACTGTATACT)
3) Ген AMPD1 - Tail (TACAGCTGAAGAGAAACGTGAGTATTGCATT).
Подтверждением результата прохождения ферментативного гидролиза служит наличие соответствующих бэндов (полос) на фиг.2. Заключительным этапом является составление рекомендаций, полученных в результате анализа данных.
Способ экономичен, не требует дорогостоящего оборудования и может быть введен в повсеместную клиническую практику. Данные, полученные с помощью способа настоящего изобретения, могут быть использованы для выявления носительства 3-х значимых мутаций в генах ACTN3, CNB, AMPD1, которые оказывают непосредственное влияние на физическую работоспособность и выносливость человека, что тем или иным образом определяет особенности тренировочного процесса. На основании анализа полученных данных и разработанных интерпретаций можно повысить эффективность получаемых результатов во время тренировок.
Изобретение иллюстрируется примерами конкретного осуществления способа экспресс-анализа генетически обусловленной физической работоспособности с дальнейшей интерпретацией полученных результатов и набором рекомендаций по проведению тренировочного процесса.
Пример 1. Использование предложенного метода для составления рекомендаций по оптимизации тренировочного процесса.
У исследуемого человека берут кровь, из которой стандартным методом выделяют ДНК. Затем методом мультиплексной ПЦР исследуют фрагменты генов ACTN3, CNB, AMPD1 в образце ДНК.
Готовят ПЦР смесь в пробирке объемом 25 мкл. Состав смеси следующий: 67 мМ трис-HCl, pH 8,8 при 250 С; 16,6 мМ (NH4)2SO4; 6,7 мМ MgCl2; 6,7 мкм ЭДТА; 10 мМ 2-меркаптоэтанола, 170 мкг БСА, смесь четырех основных αNTP в концентрации 0,8 мМ каждого, термостабильная ДНК-полимераза 0,5 ед/мкл и 6 праймеров 1, 2, 3, 4, 5 и 6 по 10 пмоль каждого.
В каждую пробирку вносят 1 мкл образца ДНК. Затем проводят 35 циклов амплификации по следующей схеме:
1 цикл 95° - 5 мин
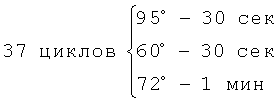
Элонгация 72° - 5 мин 30 сек
Затем проводят регистрацию результатов мультиплексной ПЦР. Анализ выполняют, используя электрофоретическое разделение в 8% полиакриламидном геле (ПААГ), приготовленном на десятикратном трис-боратном буфере в аппарате для вертикального электрофореза с длиной стекла 20-22 см.
Для приготовления 40 мл 8% геля смешивают: 9 мл 30% р-р акриламида (29 г акриламида; 1 г N,N метилен-бисакриламида на 100 мл водного раствора), 4,5 мл 10× ТБЕ (89 мМ трис-борат (pH 8,3-8,6), 2 мМ ЭДТА), 26,5 мл дистиллированной воды, 40 мкл тетраэтилендиамина (TEMED), 400 мкл персульфата аммония (PSA). Перед заливкой раствор тщательно перемешивают. После амплификации непосредственно к аликвотам реакционной смеси (~5 мкл) добавляют буфер для нанесения проб (~2 мкл) и проводят электрофорез (шестикратный буфер для нанесения проб состоит из 0,25% бромфенола, 0,25% ксилен-цианола и 15% фикола).
Электрофорез проводят при напряжении 100 B до тех пор, пока образец не входит в гель и не проходит около 1 см от начала лунок. В дальнейшем напряжение увеличивают до 300 B. Остановку электрофореза проводят за 1 см до выхода бромфенола из геля.
Затем гель окрашивают в водном растворе этидиум-бромида (0,5 мкг/мл), а визуализацию результатов проводят в проходящем ультрафиолетовом свете на трансиллюминаторе.
При подтверждении результата прохождения мультиплексной амплификации, по наличию соответствующих бэндов (полос) на фиг.1, получившийся продукт ПЦР подвергают ферментативному гидролизу, по схеме (на одно исследование):
А) в пробирку №1
- 0,5 мкл эндонуклеазы рестрикции Tae 1
(Fermentas)
- 1,5 мкл буфер R (Fermentas)
- 9 мкл воды
- 4 мкл продукта мультиплексной ПЦР.
Б) в пробирку №2
- 0,5 эндонуклеазы рестрикции мкл Vsp 1 (Sibenzyme)
0,3 эндонуклеазы рестрикции мкл
BstDEI (Sibenzyme)
- 1,5 мкл буфер W (Sibenzyme)
- 8,7 мкл воды
- 4 мкл продукта мультиплексной ПЦР.
Гидролиз проводят в течение 12 часов, при температуре 37°C. Данные эндонуклеазы рестрикции расщепляют специфическую последовательность ДНК или же этого не происходит. Эндонуклеаза рестрикции BstDE1 специфична для гена ACTN3, эндонуклеаза рестрикции Vsp1 специфична для гена CNB, эндонуклеаза рестрикции Tail специфична для гена AMPD1.
Затем проводят электрофорез в 8% полиакриламидном геле. Определяемые мутации, количество и размер визуализируемых фрагментов приведены в таблицах 2 и 3.
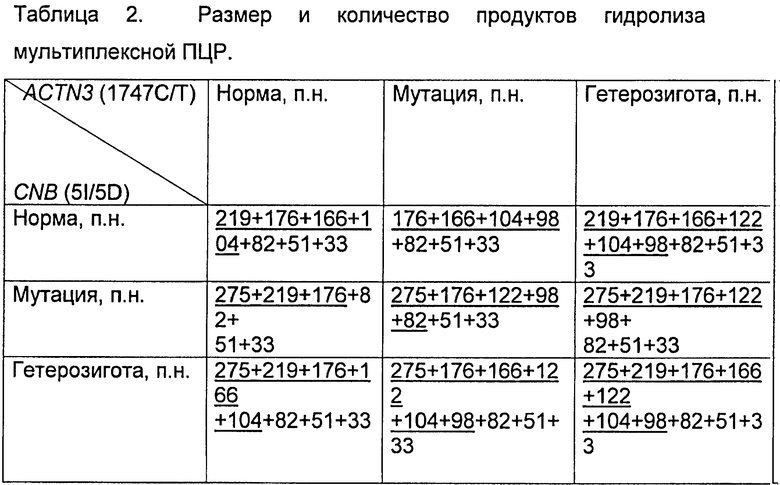
В результате анализа мутаций в генах ACTN3, CNB, AMPD1, пациенту могут быть даны следующие рекомендации (фиг.2): продукт гена ACTN3 отвечает за синтез α-актина-3, являющегося основным компонентом Z-линий мышечных саркомеров, который

определяет развитие быстрых мышечных волокон II типа. Он выполняет статическую функцию в организации работы тонких филаментов и взаимодействия между саркомерным цитоскелетом и саркоплазмой, тем самым обеспечивая упорядочение массива миофибрилл. При наличии генотипа C/C по гену ACTN3 образование стоп-кодона не происходит и синтез α-актина-3 проходит полноценно. Это обуславливает предпочтение для данного индивидуума скоростно-силовых видов спорта.
Продуктом гена AMPD1 является специфическая скелетно-мышечная аденозинмонофосфатдезаминаза (M-изоформа), участвующая в ряде биохимических процессов (азотистого обмена). Данный фермент играет основную роль в регуляции энергетических процессов в скелетной мускулатуре, повышает эффективность синтеза АТФ. При наличии генотипа C/C по гену AMPD1 синтезируется нормальное количество продукта данного гена, что не приводит к повышенному риску развития метаболической и вызванной физическими упражнениями миопатий у человека. Таких индивидуумов не беспокоит слабость, быстрая утомляемость или мышечные судороги после средней по интенсивности физической нагрузки. Для данного пациента существенных ограничений по времени и интенсивности тренировок нет.
Продукт гена CNB входит в состав регуляторной субъединицы Са2+-модулинфосфотазы, являющейся одним из основных регуляторов концентрации ионов Са2+ в организме, а также является одним из факторов активации транскрипции ряда генов, приводящих к развитию врожденных форм гипертрофии левого желудочка сердца. При наличии генотипа I/I по гену CNB активации транскрипции генов, проводящих к врожденной гипертрофии левого желудочка сердца не происходит, вследствие чего риск развития патологий сердечно-сосудистых осложнений, обусловленных физическими нагрузками, существенно снижен. Развитие гипертрофии возможно только при целенаправленных длительных систематических тренировках и будет носить физиологически обусловленный приспособительный характер. На основании анализа этого гена для данного индивидуума существенных ограничений по времени и интенсивности тренировок не существует.
С учетом общего анализа генотипов по генам ACTN3, AMPD1, CNB данному пациенту для достижения максимальных результатов будут рекомендованы силовые тренировки, без существенных ограничений по времени и интенсивности.
Таким образом, предлагаемое изобретение обеспечивает способ подготовки материала к диагностике 3-х значимых мутаций в генах ACTN3, CNB, AMPD1 непосредственно в клиническом образце методом мультиплексной полимеразной цепной реакции (ПЦР) с последующим анализом полиморфизма длины рестрикционных фрагментов (ПДРФ) и интерпретацию полученных результатов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫЯВЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ К ДЛИТЕЛЬНЫМ ФИЗИЧЕСКИМ НАГРУЗКАМ | 2011 |
|
RU2468086C1 |
| СПОСОБ ДИАГНОСТИКИ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ И ДИАГНОСТИЧЕСКИЙ НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2005 |
|
RU2304775C2 |
| ГЕНЕТИЧЕСКАЯ ПАНЕЛЬ И СПОСОБ ОПРЕДЕЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ ЧЕЛОВЕКА К РАЗЛИЧНЫМ ВИДАМ ФИЗИЧЕСКОЙ РАБОТОСПОСОБНОСТИ | 2006 |
|
RU2339701C2 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА У ДЕТЕЙ НА ОСНОВЕ ГЕНЕТИЧЕСКИХ И БИОХИМИЧЕСКИХ МАРКЕРОВ | 2012 |
|
RU2492485C1 |
| Способ профессионального отбора сотрудников силовых ведомств РФ и лиц, деятельность которых связана с высокой опасностью для жизни и здоровья, для эффективного выполнения служебной деятельности в экстремальных условиях | 2019 |
|
RU2741342C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ГЕСТОЗА НА ОСНОВЕ ГЕНЕТИЧЕСКИХ МАРКЕРОВ | 2010 |
|
RU2431842C1 |
| СПОСОБ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА ДЛЯ ПРОВЕДЕНИЯ ПОСТНАТАЛЬНОЙ ДНК-ДИАГНОСТИКИ МУКОВИСЦИДОЗА | 2008 |
|
RU2412247C2 |
| СПОСОБ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА, ОПРЕДЕЛЯЮЩЕГО ПРЕДРАСПОЛОЖЕННОСТЬ К ОНКОЛОГИЧЕСКИМ ЗАБОЛЕВАНИЯМ И ИНДИВИДУАЛЬНУЮ ЧУВСТВИТЕЛЬНОСТЬ К ФАРМАЦЕВТИЧЕСКИМ ПРЕПАРАТАМ С ИСПОЛЬЗОВАНИЕМ ОЛИГОНУКЛЕОТИДНОГО БИОЛОГИЧЕСКОГО МИКРОЧИПА (БИОЧИПА) | 2005 |
|
RU2303634C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ДЛИНЫ ТЕЛА ЧЕЛОВЕКА НА ОСНОВАНИИ ИССЛЕДОВАНИЯ ДНК В РАМКАХ РУССКОЙ ПОПУЛЯЦИИ | 2012 |
|
RU2531341C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ К ОНКОЛОГИЧЕСКИМ ЗАБОЛЕВАНИЯМ И ДИАГНОСТИЧЕСКИЙ НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2005 |
|
RU2296328C1 |
Изобретение относится к области биотехнологии, в частности к молекулярно-генетическим исследованиям, а именно к области диагностики генетической предрасположенности к различным видам физических нагрузок и особенностей тренировочного процесса. Генетическую предрасположенность определяют путем анализа полиморфизма генов ACTN3 (R577X), CNB (5I/5D), AMPD1 (С34Т) методом мультиплексной полимеразной цепной реакции. Для этого используют набор праймеров, при этом для гена ACTN3 (R577X) используют праймеры 5'-ACTGCTGCCCTTTCTGTTGCCT-3' и 5'-CTGCAGGTGGCACTGACCАТА-3', для гена CNB (5I/5D) используют праймеры 5'-GG AGTTTAAAAGCCAGCCAGTCАТАСТА-3' и 5'-TGGAAGATCACACCATTTGATTAGCAGT-3', для гена AMPD1 (С34Т) используют праймеры 5'-GCAATCTACATGTGTCTACCCCAAAG-3' и 5'-СACTGCTGAAAAATAGCCATGTTTCTG-3'. После чего в одну пробирку объединяют 3 пары праймеров, подобранных со средней температурой плавления 58-59°С при стандартных условиях. Затем осуществляют анализ продукта реакции методом анализа полиморфизма длины рестрикционных фрагментов. Предложенное изобретение позволяет создать простой, недорогой, специфичный метод, позволяющий выявлять функционально-значимые полиморфные локусы, а также "наращивать" число анализируемых генов с целью дальнейшего внедрения в любую стандартную клиническую лабораторию. 1 з.п. ф-лы, 2 ил., 3 табл.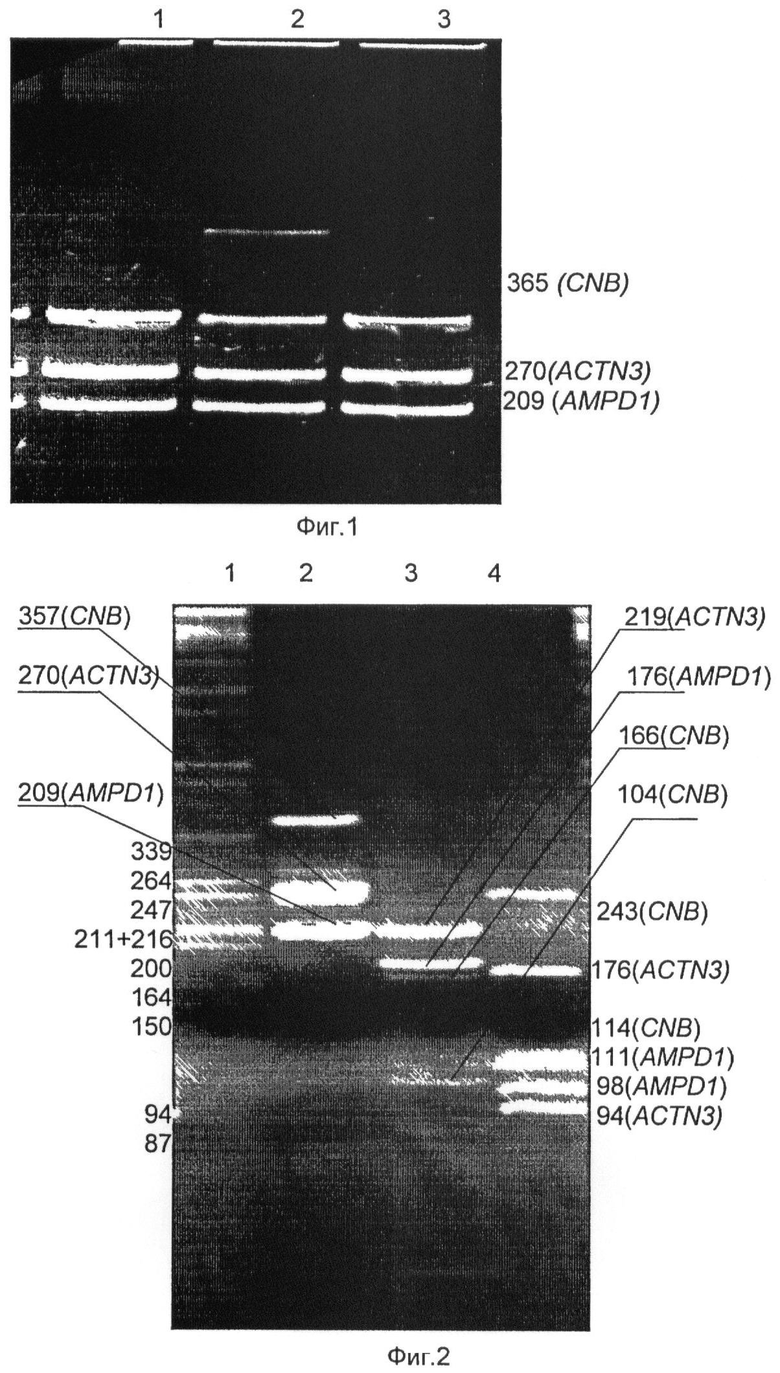
1. Способ определения физической работоспособности человека посредством анализа полиморфизма (мутаций) генов методом мультиплексной полимеразной цепной реакции, осуществляемой путем смешивания компонент и добавления олигопраймеров, с последующим анализом полиморфизма длин рестрикционных фрагментов и визуализацией электрофореграммы в полиакриламидном геле, отличающийся тем, что генетическую предрасположенность определяют путем анализа полиморфизма генов ACTN3 (R577X), CNB (5I/5D), AMPD1 (С34Т) методом мультиплексной полимеразной цепной реакции с использованием набора праймеров, при этом для гена ACTN3 (R577X) используют праймеры 5'-ACTGCTGCCCTTTCTGTTGCCT-3' и 5'-CTGCAGGTGGCACTGACCATA-3', для гена CNB (5I/5D) используют праймеры 5'-GGAGTTTAAAAGCCAGCCAGTCАТАСТА-3' и 5'-TGGAAGATCACACCATTTGATTAGCAGT-3', для гена AMPD1 (С34Т) используют праймеры 5'-GCААТСТАСATGTGTCTACCCCAAAG-3' и 5'-CACTGCTGAAAAATAGCCATGTTTCTG-3', при этом в одну пробирку объединяют 3 пары праймеров, подобранных со средней температурой плавления 58-59°С при стандартных условиях, продукт мультиплексной полимеразной цепной реакции подвергают гидролизу эндонуклеазами рестрикции BstDEl (ген ACTN3) (CCCGAGGCTGACTGAGAGCGAG), Vspl (ген CNB) (GTTAATTGTACACTTAAATTAATAGCAACTGTATACT), Tail (ген AMPD1) (TACAGCTGAAGAGAAACGTGAGTATTGCATT) и на основании результата анализа электрофореграммы составляют клиническую интерпретацию, включающую в себя рекомендации по особенностям тренировочного процесса и интенсивности физических тренировок, а при составлении рекомендаций наличие генотипа С/С по гену ACTN3 интерпретируют как предрасположенность к скоростно-силовым видам спорта, генотипа С/Т - как предрасположенность к силовым видам спорта, но требующим выносливости, и генотипа Т/Т - как предрасположенность к видам спорта, требующим выносливости, наличие генотипов I/I или I/D по гену CNB интерпретируют как предрасположенность к занятию любым видом спорта без ограничений по времени и интенсивности нагрузок, и генотипа D/D - как предрасположенность к риску развития гипертрофии, и носителю этого генотипа рекомендуют ограничение тренировок по времени и интенсивности, наличие генотипов С/С и С/Т по гену AMPD1 интерпретируют как предрасположенность к занятию любым видом спорта без ограничений по времени и интенсивности нагрузок, а генотипа Т/Т - как возможность занятия спортом с ограничением тренировок по времени и интенсивности.
2. Способ по п.1, отличающийся тем, что в качестве клинического образца преимущественно используют образцы ДНК, выделенные из лимфоцитов периферической крови, и других материалов, полученных от обследуемого индивидуума, например, буккального эпителия или слюны.
| ГЛОТОВ О.С | |||
| и др | |||
| Исследование функционально-значимых полиморфизмов АСЕ, AGTR1, ENOS, MTHFR, MTRR и АРОЕ генов в популяции Северо-Западного региона России | |||
| - Экологическая генетика, 2004 г., т.2, выпуск 3, с.32-35. | |||
| РОГОЗКИН В.А | |||
| и др | |||
| Гены-маркеры предрасположенности к скоростно-силовым видам спорта | |||
| - Теория и практика физической культуры, 2005 |
Авторы
Даты
2011-03-20—Публикация
2008-12-09—Подача