Область техники, к которой относится изобретение
Настоящее изобретение связано с диагностикой неврологических заболеваний, в особенности с диагностикой болезни Альцгеймера с помощью антитела, которое способно взаимодействовать со специфическими пептидами, ассоциированными с указанным заболеванием.
Уровень техники
Болезнь Альцгеймера (БА) - это неврологическое заболевание, которое вызывает гибель нейронов в мозге. Как правило, оно прогрессирует медленно, начинаясь после 50 лет, и его первые симптомы могут быть объяснены старческим возрастом или обычной забывчивостью. По мере того как заболевание прогрессирует, появляется постепенное ухудшение когнитивных способностей, включая способность принимать решения и выполнять повседневные задачи, и могут иметь место изменения личности, а также проблемы в поведении. На поздних стадиях БА приводит к деменции и в конце концов - к смерти. В настоящее время заболевание является неизлечимым и составляет основную причину смертности.
В настоящее время болезнь Альцгеймера обычно диагностируется по клинической картине, хотя окончательный диагноз может основываться только на гистологическом исследовании образцов мозга (аутопсии или биопсии), выявляющем присутствие характерных признаков в ткани мозга. Принимая во внимание риск, связанный с биопсией мозга у живых пациентов, эта процедура применяется очень редко, и, соответственно, считается, что частота появления ошибок при диагностике данного заболевания in vivo составляет около 20-30%.
В мозге индивидуумов с болезнью Альцгеймера выявляется два принципиальных патологических маркера: нейрофибриллярная дегенерация (которая идентифицируется по присутствию нейрофибриллярных клубков, дистрофических нейритов и нитей нейропилей) и отложения амилоидного вещества (то есть отложения так называемого β-амилоидного пептида, обычно сокращаемого до Аβ), причем и тот, и другой представлены в виде бляшек (диффузные бляшки и нейритные бляшки, эти последние приведенные формы являются характерными чертами заболевания и определяются, как только они появляются между нейронами и внутри них) и в виде отложений в сосудах (встречаются в стенках кровеносных сосудов головного мозга). И нейрофибриллярная дегенерация, и амилоидные отложения представляют собой дегенеративные процессы, которые связаны также и с нормальным старением мозга. У пожилых людей, которые не страдают деменцией, пептид Аβ откладывается преимущественно в виде диффузных бляшек. Этот тип отложения чрезвычайно выражен у некоторых субъектов с нормальными когнитивными способностями и, согласно некоторым авторам, связан с процессом «патологического старения», который рассматривается как промежуточное состояние между нормальным процессом старения мозга и БА [1]. Особенно интенсивное раннее развитие диффузных бляшек за несколько лет до появления нейритных бляшек имеет место также и при синдроме Дауна (СД) вследствие трисомии 21 хромосомы, которая приводит к гиперэкспрессии белка амилоидного предшественника (β-АРР). Хотя небольшое количество нейритных бляшек может наблюдаться и в мозге субъектов с нормальными когнитивными способностями, мозг, пораженный БА, так же как и при поражении СД, в старшем возрасте отличается развитием большого количества зрелых нейритных бляшек [2, 3]. В отличие от диффузных бляшек, которые содержат нефибриллярную форму Аβ (обозначенную как «преамилоид») [4], и сосудистые амилоидные отложения, и нейритные бляшки содержат пептид Аβ в фибриллярной форме и взаимодействуют с красителями для амилоидного вещества, такими как Конго Красный и Тиофлавин Т.
Когнитивное ухудшение при БА линейно коррелирует с прогрессией нейрофибриллярных изменений и утратой кортикальных синапсов [5]. Не было обнаружено локальной утраты синапсов, связанной с диффузными бляшками [6]. В противовес этому, нейритные бляшки ассоциированы с потерей синаптической плотности, нейрофибриллярными изменениями и активацией микроглии [7]. И чистые нейрофибриллярные изменения, и отложение Аβ следуют за четко устанавливаемыми последовательными чертами прогрессии БА [8, 9]. Однако хотя степень когнитивного угасания лучше коррелирует с последовательностью стадий, определяющихся нейрофибриллярными изменениями [5], тем не менее окончательный нейропатологический диагноз при БА основан на гистологической демонстрации значительно более высокой плотности нейритных бляшек в ассоциативных неокортикальных областях по сравнению с таковой, ожидаемой в соответствии с возрастной группой пациента, в пределах клинической картины деменции (критерии согласования CERAD: Консорциума по Учреждению Регистрации Болезни Альцгеймера) [10]. Формирование нейритных бляшек составляет основной патогенный процесс при БА, и молекулярный состав этих отложений β-амилоида, и отличия от диффузных бляшек в отношении указанного состава являются соответственно одной из основных областей интереса в современных исследованиях БА.
Знания о молекулярном составе отложений β-амилоида в ткани мозга пациентов с болезнью Альцгеймера радикально изменились в течение последних лет. Различные исследования с применением биохимических и иммуногистохимических методов с целью выявления различных форм пептида Аβ обеспечили довольно последовательную картину, которая дает возможность молекулярной интерпретации классических морфологических данных. Это были те исследования, которые обеспечили основу для унифицированной патогенной теории заболевания, именуемой амилоидной гипотезой [11], хотя в последнее время исходная гипотеза была переформулирована, с тем, чтобы учесть новую роль растворимых олигомеров Аβ в качестве основных агентов, вызывающих заболевание [12]. Принятие центральной и первичной патогенной роли пептидов Аβ при БА в настоящее время приводит к новым стратегиям лечения, направленным на предупреждение возникновения этих отложений или их удаление.
Топографическое распространение и временная последовательность отложения пептидов Аβ, характерных для мозга, пораженного БА, было выявлено с помощью антител, ориентированных на карбоксильный конец, N-конец или на внутренние части молекулы Аβ, наряду с выделением и очисткой изоформ Аβ биохимическими методами. Распределение пептидов, охарактеризованных по особенностям их карбоксильных концов, в ткани демонстрирует довольно правильную, четкую картину. Тогда как Аβх-40 является преобладающей формой в сосудистых отложениях и основной формой, встречающейся в CSF (спинномозговая жидкость), Аβх-42 является основной формой, обнаруживаемой в отложениях в ткани мозга (диффузные бляшки и нейритные бляшки) [13]. При БА, синдроме Дауна (СД) [13, 14] и нормальном старении [1] Аβх-42 является единственным компонентом диффузных бляшек и основным компонентом нейритных бляшек. Последние также могут содержать Аβх-40, преимущественно в районе их основного ядра. Также было установлено, что Аβх-42 является формой, которая откладывается на начальных стадиях.
Хотя изначально считалось, что Аβх-40 и Аβх-42 почти всегда начинаются с аминокислоты Asp1, иммуногистохимически и биохимически было четко показано, что большое количество гетерогенных изоформ пептида Аβ, модифицированных и укороченных на N-конце, входит в состав и диффузных, и нейритных бляшек [15]. Эти изоформы также проявляют тенденцию к регулярному распределению между диффузными и нейритными бляшками, так что полная картина топографического распространения различных пептидов Аβ, наконец, начинает проясняться. Тем не менее существуют некоторые несоответствия между стадиями, особенно в отношении свойств N-конца пептидов, которые образуют диффузные бляшки, и сравнительным количеством отложений амилоида, представляющего каждую из них.
Эти несоответствия касаются, в частности, пептида р3 (Aβ17-42). Тогда как предполагается, что на некоторых стадиях Aβ17-42 может быть главным компонентом диффузных бляшек [16], на остальных стадиях при этом обнаруживаются относительно большие количества более длинных форм (начинающихся с Asp1 или укороченных с N-конца или других модифицированных изоформ) [15]. Поскольку Aβ17-42 образуется при расщеплении β-АРР α-секретазой (так называемый неамилоидогенный путь) и проявляет физико-химические свойства, совершенно отличные от свойств более длинных изоформ Аβ (последние образуются при расщеплении β-АРР γ-секретазой), его избирательное присутствие в диффузных бляшках может иметь критическое патогенное значение в развитии бляшек.
Gowing и др. [17] впервые выделили пептид Aβ17-42 в качестве преобладающей формы, полученной из образцов мозга, пораженного БА, богатого диффузными бляшками. Это отложение не было обнаружено в сосудистых амилоидных отложениях или в нейритных бляшках. Коммерческие моноклональные антитела 6Е10, которые распознают Aβ1-17, в сериях мозга, пораженного БА и СД, не дают иммуноокрашивания диффузных бляшек, ни неокортикальных, ни мозжечковых, [18]. Однако в полосатом теле, где в большом количестве присутствуют диффузные бляшки при отсутствии нейритных бляшек, обнаружилось некоторое количество бляшек, которые являются положительными в отношении антител 6Е10. Используя HPLC и иммуногистохимическое распознавание, Lalowski и др. [19] показали, что Aβ17-42 составляет 70% от общего содержания амилоида в диффузных бляшках мозжечка, тогда как Aβ1-42 составляет 12%, и другие укороченные формы Аβх-42 составляют 5% или менее. В мозге пожилых людей, больных СД, Saido и др. [20] обнаружили большее окрашивание диффузных бляшек специфическими антителами против Аβ N3 (pyroGlu), чем антителами против Aβ N(1). Iwatsubo и др. [15] исследовали диффузные бляшки в сериях мозга пожилых людей, больных БА и больных СД, с помощью групп антител, направленных на распознавание форм Аβ, укороченного и модифицированного с N-конца. Это исследование уникально тем, что ткань мозга, использованная для иммуногистохимического исследования, была фиксирована либо в 70% спирте, либо в 4% формальдегиде, с тем, чтобы иметь возможность проверить влияние обычной фиксации формальдегидом на появление артефактов. Во всех образцах ткани, фиксированных в 70% спирте, диффузные бляшки окрашивались интенсивнее при наличии Аβ N1 (L-Asp), Aβ N1 (L-isoAsp), Aβ N1 (D-Asp), Aβ N3 (pyroGlu) и Аβ Х-42. Слабое иммуноокрашивание получали с Аβ N11 (pyroGlu) и Аβ N17. Однако в материале, фиксированном в формальдегиде, некоторые диффузные бляшки окрашивались с Аβ N1 (L-Asp) и не окрашивались с Аβ N1 (L-isoAsp) или Аβ N1 (D-Asp), тогда как участок окрашивания на карбоксильном конце был неизмененным. Хотя авторы показали, что модификация N-конца может влиять на результат иммуноокрашивания в тканях, фиксированных в формальдегиде, они получили слабую реактивность для Аβ N17 даже в материале, фиксированном в спирте. Применяя моноклональное антитело, специфичное в отношении р3 (Aβ17-42) [16], они обнаружили, что отложение этого пептида в значительной степени ограничивалось диффузными бляшками, дистрофическими нейритами и верхними частями нейритных бляшек в области миндалин, гиппокампа и парагиппокампа. Авторы высказали мнение о специфической роли р3 в начальном отложении амилоидной массы и возникновении нейритных бляшек. Tekirian и др. [21] показали в сериях мозга больных БА и контрольной группы присутствие Аβ N3 (пептид)>Аβ N1 (D)>Aβ N17 (L)>Aβ N1 (rD) в диффузных бляшках.
Что касается вариабельности карбокси-конца, в исследовании с использованием антител против Аβх-40, Аβх-42 или Aβx-43, Parvathy и др. [22] обнаружили подгруппу нейритных бляшек, которые реагируют только с антителами Аβ С40, и большую подгруппу бляшек, которые реагируют и с Аβ С40, и с Аβ С42.
Таким образом, в более ранних исследованиях установлено, что диффузные бляшки обнаруживают профиль Аβ, который является высокоспецифичным на карбоксильном конце, и профиль, который довольно специфичен на N-конце, последний зависит от некоторой гетерогенности между пациентами и между различными участками мозга. Присутствие Aβ17-42 в значительной степени ограничивается диффузными бляшками, хотя существует большое различие между стадиями в отношении относительного содержания в них этого более короткого пептида. В исследованиях под руководством Kida и других [18] не было выявлено окрашивания для пептидов Аβ, которые содержат последовательность 12-16 в диффузных бляшках кортикального или субкортикального участков.
С учетом всех результатов, полученных в данной области, можно заключить, что, как было предложено Larner [23], формы пептида Аβ, которые являются специфичными в области своего N-конца, могут играть существенную роль в развитии диффузных бляшек, превращая их в нейритные бляшки. Следовательно, антитела, способные специфически детектировать формы с укороченным N-концом и, соответственно, четко дифференцировать диффузные бляшки и нейритные бляшки, являются чрезвычайно полезными в качестве инструментов в диагностике болезни Альцгеймера. К ним относятся антитела, способные дифференцировать подгруппы нейритных бляшек в соответствии с соотношением различных форм амилоидного пептида, различающихся по аминокислоте, которой заканчивается карбоксильный конец, и именно такие антитела будут особенно пригодными, особенно если их можно будет использовать для определения подгрупп бляшек, которые являются специфическим маркером заболевания. Моноклональное антитело согласно изобретению, направленное против последовательности, состоящей из аминокислот 12-16 β-амилоидного пептида и обладающее большей аффинностью в отношении формы Аβ42, чем формы Аβ40, удовлетворяет обеим характеристикам.
Другим аспектом, в соответствии с которым антитела, способные детектировать формы β-амилоидного пептида, были бы чрезвычайно пригодны в диагностике болезни Альцгеймера при помощи оценки концентрации различных форм этого пептида в биологических жидкостях, является аспект, который исследуется и для облегчения диагностики на основе биохимических параметров, и даже с целью распознавания доклинических случаев или случаев с особым риском развития заболевания, и для наблюдения пациентов, участвующих в клинических исследованиях. Для этого многие исследования сфокусированы на спинномозговой жидкости (CSF) с намерением выявить, есть ли изменения в концентрациях растворимых форм β-амилоидного пептида, присутствующего в этой жидкости, что дало бы возможность отличать больных от здоровой контрольной группы. Однако маловероятно, что исследование CSF, которое включает в себя применение инвазивной технологии, люмбарную пункцию, могло бы быть применимо для диагностики и стандартного наблюдения пациентов с болезнью Альцгеймера в клинической практике. Поэтому другие направления исследования сфокусированы на изучении различий в концентрации биологических маркеров в крови и моче (каковые включают в себя растворимые формы β-амилоидного пептида), которые могли бы коррелировать с появлением и развитием заболевания, хотя некоторые исследования и опубликованы к настоящему времени. Соответственно, обнаруживается, что уровни Аβх-42 и Аβх-40 в плазме возрастают при синдроме Дауна, и также они увеличиваются с возрастом у здоровых людей. Уровни в плазме Аβх-42, но не Аβх-40, повышаются у больных с болезнью Альцгеймера, и снижаются, если заболевание развивается [28, 29], хотя измерение концентрации этих веществ в плазме в настоящее время не может быть использовано для диагностики. Присутствие растворимых форм β-амилоидного пептида также детектировали в моче [30], хотя сравнительное исследование между больными и контрольной группой еще не доведено до конца. Хотя порядок величины концентраций β-амилоидного пептида, которые детектируются в плазме и моче, осложняет определение профилей, соответствующих здоровым индивидуумам и больным на разных стадиях заболевания, и возможная связь растворимых форм β-амилоидного пептида с другими белками, присутствующими в указанных биологических жидкостях, является еще одним препятствием, которое придется преодолеть, этот подход активно рассматривается, поскольку моноклональные антитела, которые могут взаимодействовать с формами β-амилоидного пептида, присутствующими в биологических жидкостях, дают возможность их детекции и могут представлять собой очень удобный способ диагностики болезни Альцгеймера. Антитело согласно изобретению, которое способно взаимодействовать с растворимыми формами β-амилоидного пептида и обнаруживать их присутствие в биологических жидкостях, таких как моча, является одним из антител, которые могут использоваться для реализации этих диагностических технологий. Кроме того, то обстоятельство, что оно специфически направлено против участка вблизи амино-конца β-амилоидного пептида, является свойством, представляющим интерес при разделении форм β-амилоидного пептида, в которых сохраняется амино-конец, и тех форм, в которых указанный конец укорочен.
Описаны другие моноклональные антитела, ориентированные специфически против участка вблизи N-конца β-амилоидного пептида, а также их применение в диагностических методах, связанных с БА. Например, в патенте США US-4666829 описано получение моноклонального антитела, выработанного против части амилоидного пептида, наиболее близкой к N-концу. Конкретно: был получен синтетический пептид, содержащий первые десять остатков указанного пептида (Asp-Ala-Glu-Phe-Arg-His-Asp-Ser-Gly-Tyr), представленный в SEQ ID NO:1. Эпитоп, распознанный этим антителом, будет содержать эти аминокислоты 1-10, тогда как антитело, заявленное в настоящем изобретении, распознает по меньшей мере эпитоп, который содержит аминокислоты 12-16. Также существует различие в специфической последовательности, которую распознает это моноклональное антитело, в сравнении с таковым согласно настоящему изобретению; разработка предложенной диагностической технологии также отличается, поскольку то, что определяется, является исключительно связыванием антител, применяемых в отношении того, что рассматривается в указанном патенте, то есть пептида, который характерен для болезни Альцгеймера и образован 1-28 аминокислотами амилоидного пептида, без учета связывания с другими формами пептида различных длин и/или с вариациями в амино- и карбокси-концах. Более того, не было представлено экспериментального подтверждения, которое служило бы доказательством его возможности детектировать формы амилоидного пептида, присутствующего в биологических жидкостях.
Кроме того, в патентной заявке РСТ WO 90/12871 описано получение моноклонального антитела, обозначенного SV17-6E10. Это антитело получают посредством иммунизации пептидом с последовательностью Asp-Ala-Glu-Phe-Arg-His-Asp-Ser-Gly-Tyr-Gln-Val-His-His-Gln-Lys-Leu, представленной в SEQ ID NO:2, которая могла считаться эквивалентной аминокислотной последовательности 1-17 аминокислот амилоидного пептида. Другое моноклональное антитело, направленное на участок, который содержит аминокислоты 1-17 - это указанное коммерческое моноклональное антитело 6Е10, которое, как указано в описании спецификации, соответствующей продукту, http://www.alexis_corp.com/monoclonal:antibodies-SIG-9320/opfa.1.1.SIG-9320.386.4.1.html, специфически, в пределах с 1 по 17 аминокислоты β-амилоидного пептида, распознает эпитоп, заключенный между аминокислотами 3-8. Этот эпитоп соответствует другому участку, расположенному ближе к N-концу, чем таковой в моноклональном антителе ЕМ5 согласно изобретению. Хотя оно способно давать дифференциальное окрашивание нейритных бляшек и сосудистых отложений без окрашивания диффузных бляшек, это антитело не проявляет различий в аффинности в отношении пептидов AR42 и Ар40.
Таким образом, моноклональное антитело согласно изобретению, которое было обозначено ЕМ5, представляет собой новый инструмент, поскольку оно распознает по меньшей мере один эпитоп в последовательности β-амилоидного пептида, который не распознается ни одним антителом, описанным в настоящее время в данной области науки. Следовательно, антитело согласно изобретению является пригодным для применения в диагностике болезни Альцгеймера. Оно специфически распознает нейритные бляшки, без обнаружения диффузных бляшек, которые не являются специфически ассоциированными с заболеванием. Среди нейритных бляшек моноклональное антитело согласно изобретению дает возможность обнаруживать подгруппу нейритных бляшек, различающихся по их молекулярному составу относительно отложений β-амилоидного пептида. Кроме того, моноклональное антитело согласно изобретению способно связываться с формами β-амилоидного пептида, присутствующими в растворе, создавая возможность для последующего детектирования и определения количества указанных пептидов, включая те случаи, когда раствор является биологической жидкостью, такой как моча.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение связано с моноклональным антителом, которое распознает в β-амилоидном пептиде эпитоп, соответствующий последовательности:
Val-His-His-Gln-Lys (SEQ ID NO:3),
и способно связываться с изоформами β-амилоидного пептида, которые содержат указанную последовательность, независимо от того, находится ли пептид в растворимой форме, агрегированной форме или денатурирован с помощью SDS, хотя проявляет большую аффинность к изоформе Аβ 42, чем к изоформе Аβ 40.
Данное изобретение относится также к фрагментам указанного антитела, которые также способны связываться с изоформами β-амилоидного пептида, содержащего указанную последовательность SEQ ID NO:3.
В данном изобретении описана также гибридомная клеточная линия, способная продуцировать ранее охарактеризованное моноклональное антитело, и способ получения указанного антитела с помощью указанной гибридомной линии клеток, и выращивание указанной клеточной линии в условиях, которые позволяют получать моноклональное антитело.
Дополнительно в данном изобретении описана композиция, содержащая антитело согласно изобретению или по меньшей мере один его фрагмент, способный связываться с SEQ ID NO:3. Возможным вариантом осуществления композиции согласно изобретению является тот, в котором антитело или его фрагмент соединяется с веществом, которое позволяет его детектировать; указанное вещество является вторым антителом, способным связываться с антителом согласно изобретению или с его фрагментом, и соединено с веществом, которое может позволить его детектировать, как, например фермент, способный катализировать превращение данного вещества в другое, которое можно детектировать, например, хромогенное вещество. Другим возможным вариантом осуществления композиции согласно изобретению является вариант, в котором антитело или его фрагмент соединены с неким веществом или частицей, которая способствует выделению присутствующих в растворе изоформ β-амилоидного пептида, как, например, магнитная частица, которая позволит разделить в растворе комплексы антиген-антитело или антиген-фрагмент антитела, образующиеся при наложении магнитного поля, таким образом делая возможным концентрирование изоформы β-амилоидного пептида, присутствующие в указанном растворе, и облегчать их последующую детекцию, идентификацию и/или количественную оценку.
Данное изобретение относится также к применению моноклонального антитела согласно изобретению или по меньшей мере одного его фрагмента, способного связываться с последовательностью SEQ ID NO:3, для детекции изоформ β-амилоидного пептида, которые содержат SEQ ID NO:3. Изоформы β-амилоидного пептида, которые следует детектировать, могут присутствовать в образце ткани мозга, взятой от человека, в растворе, таком как образец биологической жидкости или полученный из нее раствор, или даже может содержаться в некоторых других образцах небиологического типа, в которых также желательно детектировать возможное присутствие изоформ β-амилоидного пептида.
В заключение данное изобретение относится к способу диагностики болезни Альцгеймера in vitro, основанному на детекции изоформ β-амилоидного пептида посредством применения антитела согласно изобретению или по меньшей мере одного его фрагмента, способного связываться с SEQ ID NO:3. В предпочтительном варианте осуществления изобретения изоформы β-амилоидного пептида детектируются в образце ткани мозга, взятом у индивидуума. В этом случае особенно пригодными могут быть композиции согласно изобретению, в которых антитело или его фрагмент соединяется с веществом, которое может позволить детектировать их, при этом указанное вещество может быть вторым антителом, способным связываться с антителом согласно изобретению или с его фрагментом, и соединяется с еще одним веществом, которое может позволить детектировать его.
В другом предпочтительном варианте осуществления диагностической технологии согласно изобретению изоформы β-амилоидного пептида детектируются в растворе, предпочтительно в образце биологической жидкости, например, в спинномозговой жидкости, моче или крови, или даже в растворе, полученном из биологической жидкости, таком как плазма. В этом втором варианте осуществления изобретения предпочтительно использовать композиции согласно изобретению, в которых антитело или его фрагмент соединено с неким веществом или частицей, которая способствует выделению изоформ β-амилоидного пептида, присутствующих в растворе, например, с магнитной частицей, которая способствует разделению комплексов антиген-антитело или антиген-фрагмент антитела, образующихся в растворе под действием магнитного поля, таким образом создавая возможность концентрировать изоформы β-амилоидного пептида, присутствующие в растворе, и способствуя их последующей детекции, идентификации и/или количественной оценке. Таким образом, способ диагностики согласно изобретению включает в себя следующие стадии:
a) добавление композиции, которая содержит антитело согласно изобретению или по меньшей мере один его фрагмент, способный связываться с SEQ ID NO:3, соединенное с магнитной частицей, к образцу биологической жидкости или полученному из нее раствора;
b) выжидание в течение времени, достаточного для формирования комплексов антиген-антитело или антиген-фрагмент антитела между по меньшей мере одной изоформой β-амилоидного пептида и антителом или фрагментом антитела, содержащимися в композиции;
c) наложение магнитного поля для выделения из раствора комплексов антиген-антитело или антиген-фрагмент антитела;
d) удаление раствора;
e) разделение антитела или фрагмента антитела и молекул β-амилоидного пептида;
f) идентификацию и количественную оценку изоформ β-амилоидного пептида, выделенных из образца биологической жидкости или из полученного из нее раствора.
Предпочтительно, чтобы раствор, из которого экстрагируются изоформы β-амилоидного пептида, был образцом крови или мочи, поскольку их легче получить, чем в случае с образцами спинномозговой жидкости, или - альтернативно - образцом плазмы, полученным из образца крови. Особенно предпочтительно, чтобы из крови или плазмы, или мочи образец биологической жидкости был образцом мочи, который может быть получен без применения инвазивных методов. Однако в таком случае необходимо использовать очень чувствительный метод для идентификации и количественной оценки изоформ β-амилоидного пептида, такой как масс-спектрометрия MALDI-TOF.
Поликлональные антитела ЕМ2 и ЕМ3, которые также были получены авторами настоящего изобретения, также могут применяться в качестве дополнительного инструмента в способе диагностики согласно изобретению.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
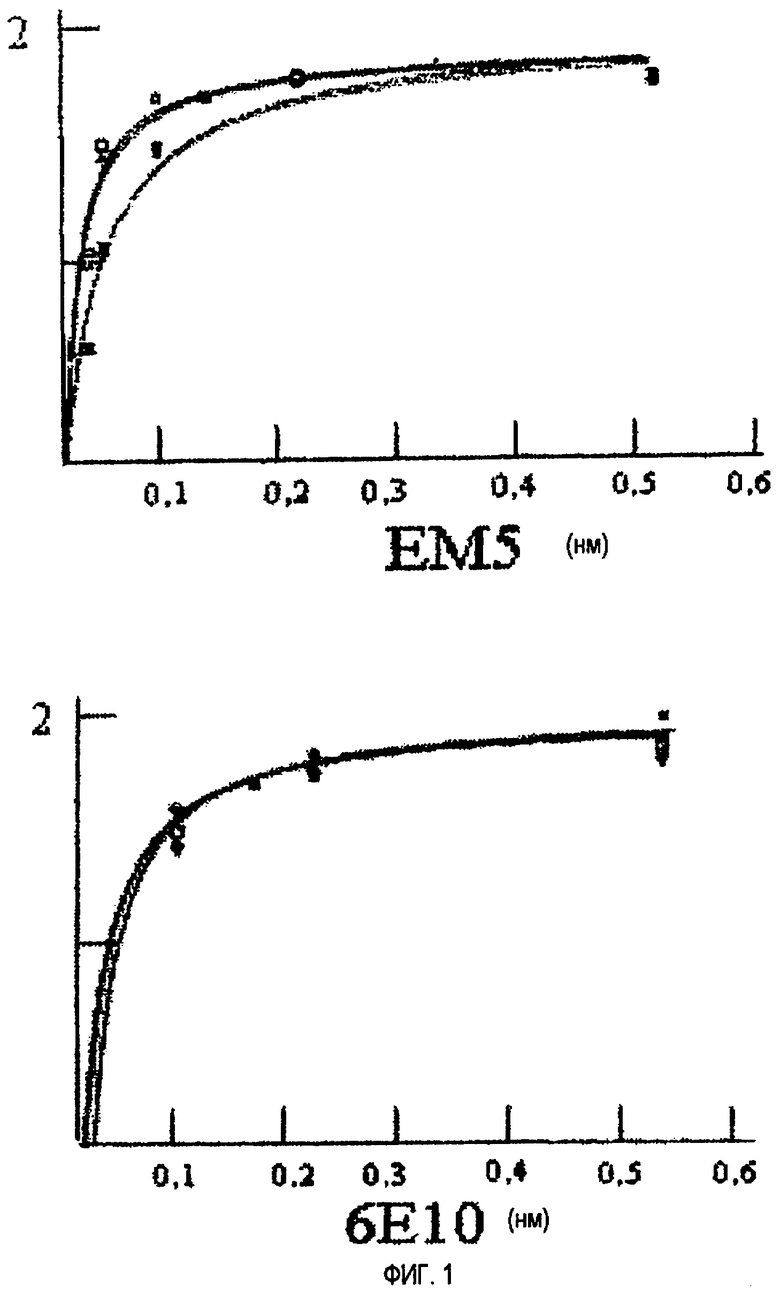
На фиг.1 приведены кривые связывания антител ЕМ5 (верхняя часть) и 6Е10 (нижняя часть) с иммобилизованными пептидами Аβ. Здесь приведены результаты, соответствующие различным концентрациям антител (абсцисса; концентрация в нМ) с обоими пептидами: Аβ 40 (заполненные значки) и Аβ 42 (пустые значки), в обоих случаях агрегированные (Δ) или не агрегированные (□). Каждая точка соответствует среднему значению экспериментов, проведенных в трех параллельных пробах. Оптическая плотность (O.D.) при 450 нм показана на оси ординат.
На фиг.2 показан результат изучения иммунного переноса антител ЕМ2, ЕМ3 и ЕМ5 относительно синтетических пептидов Аβ 1-40 и Аβ 1-42.
На фиг.3 приведена (в верхней части) гистограмма реактивности ЕМ5 к сериям синтетических пептидов Аβ, оцененной при помощи ELISA, со значениями оптической плотности (O.D. при 450 нм), соответствующими 20 мг/мл антител. Нижняя часть соответствует локализации эпитопа, распознанного ЕМ5, согласно результатам ELISA. 1-28R=Aβ1-28 грызуна. В круглых скобках указаны различные мутации.
На фиг.4 показана локализация эпитопа пептида Аβ, распознанного моноклональным антителом ЕМ5, согласно масс-спектрометрическому анализу иммунопреципитированного β-амилоидного пептида, обработанного различными протеолитическими ферментами, приведенными в таблице в описании (пептиды 1-5). Последовательность 6 соответствует β-амилоидному пептиду без ферментативного гидролиза.
На фиг.5 приведены фотографические снимки иммуноокрашивания ткани мозга, пораженного болезнью Альцгеймера, с применением ЕМ2, ЕМ3, ЕМ5 и комбинаций ЕМ5 с каждым указанным вариантом. Окрашенные структуры помечены как V (сосуды), DP (диффузные бляшки) и NP (нейритные бляшки). Фотографические снимки соответствуют
- (А) и (В): Последовательным серийным срезам одной и той же зоны затылочной части коры головного мозга после иммуноокрашивания с ЕМ5 (А) и ЕМ3 (В) в качестве первого антитела, с применением нитросинего тетразолиевого (NBT) в качестве хромогенного вещества.
- (С): Микрофотографии при большом увеличении с технологией двойного иммуноокрашивания с применением ЕМ3 (хромогенное вещество: NBT) и ЕМ5 (хромогенное вещество: DAB) в качестве первых антител.
(D) и (Е): Последовательным серийным срезам одной и той же области затылочной части коры головного мозга, после иммуноокрашивания с либо ЕМ5 (D), либо с ЕМ2 (Е).
- (F): Микрофотографии при большом увеличении с технологией двойного иммуноокрашивания с применением ЕМ2 (хромогенное вещество: нитросиний тетразолиевый, NBT) и ЕМ5 (хромогенное вещество: диаминобензидин, DAB).
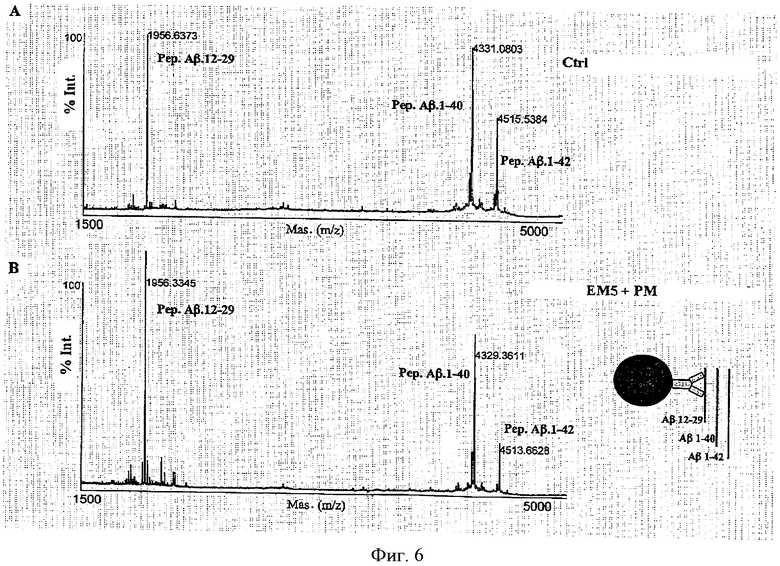
На фиг.6 приведены графики, полученные после масс-спектрометрического исследования MALDI-TOF форм β-амилоидного пептида различной длины. В каждом случае на оси ординат указана интенсивность, выраженная в процентах (% Int.), соответствующая каждому из пиков различных масс (Mas.), выведенному из соотношения масса/заряд (m/z). Верхний график, отмеченный буквой А и маркированный «Ctrl.» справа, был получен для раствора, который содержал пептиды, включающие в себя аминокислоты β-амилоидного пептида с 12 по 29 (Pep. Аβ. 12-29), с 1 по 40 (Pep. Аβ. 1-40) и с 1 по 42 (Pep. Аβ 1-42). Нижний график, отмеченный буквой В и маркированный «ЕМ5+РМ» справа, был получен после концентрирования пептидов из содержащего их раствора с применением антитела ЕМ5, ковалентно связанного с магнитными частицами, и разделения комплексов, образовавшихся при наложении магнитного поля. На чертеже справа внизу изображен участок связывания антитела с каждым из рассматриваемых пептидов.
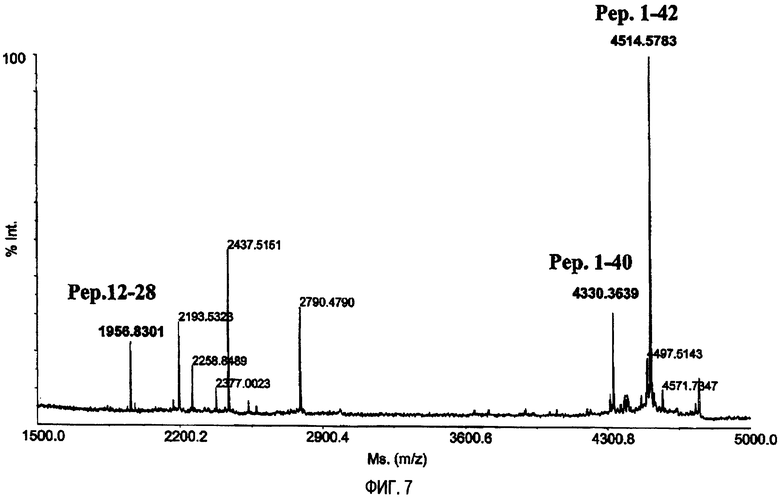
На фиг.7 приведен график, полученный в результате масс-спектрометрического исследования MALDI-TOF образца мочи здорового человека, к которому были добавлены дополнительные количества пептидов, содержащие аминокислоты β-амилоидного пептида с 12 по 28 (пик, маркированный как Pep. 12-28), с 1 по 40 (пик, маркированный как Pep. 1-40) и 1-42 (пик, маркированный Pep. 1-42), после чего образец был обработан антителом ЕМ5, ковалентно связанным с магнитными частицами, и образовавшиеся комплексы были разделены под действием магнитного поля. Ордината отображает интенсивность в процентах (% Int.), соответствующую каждому из пиков различных масс (Ms.), выведенному из соотношения масса/заряд (m/z). Указаны пики, соответствующие каждой из форм β-амилоидного пептида, добавленной к образцу мочи.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Как уже отмечалось, в данном изобретении описано моноклональное антитело ЕМ5, которое распознает в β-амилоидном пептиде эпитоп, соответствующий последовательности:
Val-His-His-Gln-Lys (SEQ ID NO:3)
Эта последовательность соответствует последовательности остатков 12-16 β-амилоидного пептида человека. Следовательно, есть основания предполагать, что указанное антитело будет связываться с изоформами β-амилоидного пептида, которые содержат указанную последовательность, без распознавания тех форм, которые ее не содержат, например, так называемого пептида р3 (Aβ17-42) и других форм с укороченным N-концом (Aβ17-x). В характеристике моноклонального антитела, которое подробно описано в приведенных ниже примерах, показано, что ЕМ5 связывается с любым пептидом, содержащим остатки 12-16, последовательности человеческого Аβ, даже несмотря на то, что он имеет модификации вне этого участка, и оно не распознает пептиды, у которых нет указанного участка. Если данный участок модифицирован, как в случае с пептидом Aβ1-28 (грызун), у которого заменена аминокислота в положении 13, так же как и в положении 5 и 10, то данный пептид больше не распознается ЕМ5.
Более того, исследования показали, что антитело способно связываться с изоформами пептида Аβ, содержащими остатки 12-16, независимо от того, находятся ли они в растворимой форме, агрегированной форме или денатурированы (в SDS). В частности, тесты, описанные в представленных ниже примерах, показывают, что антитело согласно изобретению связывается как с изоформами β-амилоидного пептида, которые агрегируют, образуя часть бляшек, присутствующих в образцах ткани мозга, так и с изоформами β-амилоидного пептида, которые находятся в растворе, включая и случаи, когда раствор представляет собой образец биологической жидкости, такой как моча. Поэтому другой аспект изобретения связан с композицией, которая содержит антитело согласно изобретению или по меньшей мере один его фрагмент, способный связываться с последовательностью SEQ ID NO:3, объединенной с веществом, которое позволяет его детектировать и/или концентрировать, и связан с его применением в диагностике болезни Альцгеймера.
Когда антитело согласно изобретению или его фрагмент объединено с веществом, позволяющим его детектировать, детекция присутствия изоформ β-амилоидного пептида, которые связались с антителом или его фрагментом, и/или их количественная оценка становится возможной посредством детекции и/или количественной оценки антитела или его фрагмента, связавшегося с изоформами β-амилоидного пептида, которые содержат специфическую последовательность, распознаваемую антителом согласно изобретению. В предпочтительном варианте осуществления данного изобретения вещество, с которым связывается антитело или его фрагмент, способный связываться с SEQ ID NO:3, объединено со вторым антителом, способным связываться с моноклональным антителом согласно изобретению, второе антитело связано с ферментом, способным катализировать превращение данного вещества в другое, которое обладает характеристиками, которые способствуют детекции его присутствия. В особенно предпочтительном варианте осуществления изобретения второе антитело, связанное с ферментом, является частью системы Envision от Dako Laboratories, вещество, превращение которого катализируется ферментом, является хромогенным веществом, и фермент, который катализирует реакцию, является либо щелочной фосфатазой (в том случае, когда в качестве хромогенного вещества используется нитросиний тетразолиевый), либо пероксидазой хрена (в том случае, когда в качестве хромогенного вещества используется диаминобензидин).
В другом варианте антитело согласно изобретению или его фрагмент связан с веществом или частицей, которая способствует концентрированию изоформ β-амилоидного пептида, которые связались с указанным антителом или его фрагментом. Этот вариант осуществления является предпочтительным, если композиция согласно изобретению используется для детекции и/или количественной оценки изоформ β-амилоидного пептида, которые присутствуют в растворе, особенно в растворе, в котором их концентрация низка, например, в крови или плазме, моче или спинномозговой жидкости. Вещество или частица должны быть такими, чтобы можно было легко разделить комплекс антиген-антитело в указанном растворе, например, при помощи иммунопреципитации. Предпочтительными примерами указанных частиц являются магнитные частицы, которые, когда соединены с антителом согласно изобретению или с его фрагментом, способным связываться с изоформами β-амилоидного пептида, которые содержат специфическую последовательность, распознаваемую антителом согласно изобретению, дадут возможность выделить из раствора изоформы β-амилоидного пептида, связанные с антителом или с его фрагментом, под действием соответствующего магнитного поля. Впоследствии изоформы β-амилоидного пептида могут отделяться от антитела или его фрагмента и затем могут детектироваться, идентифицироваться и/или количественно оцениваться. Подходящим методом является масс-спектрометрия, особенно та, что известна под названием MALDI-TOF (времяпролетная матрично-активированная лазерная десорбция/ионизация).
Как уже упоминалось, антитело согласно изобретению или его фрагмент, способные связываться с изоформами β-амилоидного пептида, которые содержат специфическую последовательность, распознаваемую антителом согласно изобретению, так же как композиции, включающие в себя по меньшей мере одну из них, могут использоваться для диагностики болезни Альцгеймера in vitro. Способы диагностики болезни Альцгеймера in vitro с применением антитела согласно изобретению или его фрагмента, связывающихся с изоформами β-амилоидного пептида, которые содержат специфическую последовательность, распознаваемую антителом согласно изобретению, так же как и с применением композиций, которые содержат указанное антитело или указанный фрагмент, входят в объем данного изобретения. Указанная диагностика может производиться на ткани мозга, в которой избирательно обнаруживается присутствие отложений с преобладанием изоформ амилоидного пептида, содержащих последовательности, распознаваемые моноклональным антителом согласно изобретению (нейритные бляшки и сосудистые отложения, отложения, которые являются характерными для развития болезни Альцгеймера), обнаруживая существование связывания с указанными отложениями моноклонального антитела согласно изобретению или его фрагмента, способного связываться со специфической последовательностью, распознаваемой указанным антителом, в отличие от того, что будет наблюдаться в отложениях, в которых преобладающими изоформами являются те, в которых отсутствует последовательность, распознаваемая моноклональным антителом согласно изобретению (диффузные бляшки), как изоформы Aβ17-x, которые не будут обнаруживать связывания моноклонального антитела или его фрагментов. Связывание антитела с нейритными бляшками и сосудистыми отложениями выявляется при посредстве композиции, такой как одна из тех, что содержат, помимо антитела согласно изобретению или его фрагмента, второе антитело, способное связываться с моноклональным антителом согласно изобретению, где второе антитело связано с ферментом, таким как хромогенное вещество, способным катализировать переход описанного вещества в другое, которое обладает характеристиками, которые способствуют детекции ее присутствия. В наиболее предпочтительном варианте осуществления диагностической технологии согласно изобретению на ткани мозга способ диагностики дополняется применением поликлональных антител ЕМ2 и ЕМ3, которые распознают или Аβх-42 (ЕМ3), или Аβх-40 (ЕМ2), причем оба этих антитела также были получены ранее группой авторов данного изобретения [24].
Другой вариант осуществления способа диагностики согласно изобретению выполняется на биологической жидкости, о которой известно, что она содержит изоформы β-амилоидного пептида, например, на спинномозговой жидкости, моче или крови, или, в последнем случае, на плазме, полученной из крови. Поскольку для получения спинномозговой жидкости требуется проведение пункции, предпочтительно использовать плазму или мочу, в особенности последнюю, которая может быть получена без применения инвазивных технологий. Также предпочтительно, чтобы в способе диагностики согласно изобретению применялись композиции, которые содержат антитело согласно изобретению или его фрагмент, связанные с неким веществом или частицей, которая способствует концентрации изоформ β-амилоидного пептида, которые связываются с указанным антителом или его фрагментом. Как уже упоминалось, предпочтительно, чтобы частицы, которые помогают концентрировать изоформы β-амилоидного пептида, были магнитными частицами, соединенными с антителом или с его фрагментом, так, что когда раствор, который содержит комплексы, образованные изоформами β-амилоидного пептида, подвергаются действию магнитного поля, последние могут быть выделены из раствора, который может беспрепятственно сбрасываться с использованием метода, такого как аспирация. В случае, когда используется полное антитело, особенно предпочтительной для соединения антитела с магнитной частицей является ковалентная связь, чтобы увеличить его стабильность, но образование указанной ковалентной связи должно быть таким, чтобы освободить, насколько возможно, место связывания антигена, чтобы не уменьшить способность антитела к связыванию, поэтому предпочтительными являются методы, в которых связывание имеет место предпочтительно в богатом гистидином районе Fc-фрагмента антитела или в гликозидных цепях указанного района. В связи с этим метод связывания антител с магнитными частицами, описанный Fuentes и др. [26], является особенно предпочтительным.
Однократно связывающие комплексы изоформ β-амилоидного пептида выделялись из раствора, разделение указанных изоформ и антител или их фрагментов предпочтительно проводить раньше детекции и/или количественной оценки выделенных изоформ β-амилоидного пептида, для чего может использоваться ацетонитрил или трифторуксусная кислота. Поскольку обычно концентрация изоформ β-амилоидного пептида в моче является довольно низкой, предпочтительно, чтобы детекция и/или количественная оценка осуществлялись с использованием очень чувствительного метода, как, например, масс-спектрометрия MALDI-TOF.
В другом аспекте данного изобретения рассматривается гибридомная клеточная линия, способная продуцировать моноклональное антитело согласно изобретению. В предпочтительном варианте осуществления изобретения указанная клеточная линия получена путем слияния линии мышиной миеломы Р3/Х63-Ag.653 с клетками селезенки мышей BALB/c, иммунизированных пептидом Aβ1-40, соединенным с KLH (гемоцианин моллюска Keyhole limpet).
В заключение, еще одной стороной данного изобретения является метод получения и очистки моноклонального антитела согласно изобретению, начинающегося с гибридомных клеток. В предпочтительном варианте осуществления изобретения метод включает в себя получение гибридомной клеточной линии, как описано ранее, и ее выращивание как асцитной жидкости в мышах линии BALB/c, предварительно пролеченных Пристаном. Моноклональное антитело очищено от этой асцитной жидкости при помощи аффинной хроматографии на колонке Protein A-Sepharose (Pharmacia). В особенно предпочтительном варианте осуществления изобретения применявшиеся гибридомные клетки являются клетками линии, обозначенной «ЕМ5 клон А», депонирование которой было запрошено 1 марта 2006 в Европейской Коллекции Культур Клеток (ЕСАСС), CAMR, Porton Down, Солсбери, Уилтшир, Соединенное Королевство и которой был дан номер доступа 06030101.
Данное изобретение и его предпочтительные варианты осуществления теперь описываются более подробно с использованием следующих примеров.
Примеры
Пример 1. - Получение антител
Поликлональные антитела ЕМ2 и ЕМ5, примененные в этом исследовании, были получены способом, описанным ранее [24].
Для получения моноклонального антитела ЕМ5 были предприняты следующие шаги.
Получение гибридом
Мышам BALB/c подкожно вводилось 40 мкг пептида Aβ1-40, соединенного с KLH (гемоцианин моллюска Keyhole limpet) и растворенного в фосфатно-солевом буфере (PBS), и эмульгированного с равным объемом полного адъюванта Фрейнда. Мыши получили три введения, повторявшихся каждую вторую неделю, с неполным адъювантом Фрейнда. За три дня до слияния, мышам проводили внутрибрюшинное введение 25 мкг Aβ1-40-KLH в PBS. В день слияния клетки селезенки животных, иммунизированных линией мышиной миеломы Р3/Х63-Ag.653, были слиты с применением полиэтиленгликоля 1400 (Sigma), следуя принятой методике [25]. Слитые клетки были распределены в стерильные 96-луночные планшеты при плотности 105 клеток на лунку и селектировались в среде, содержащей гипоксантин, тимидин и аминоптерин. Гибридомы, продуцирующие антитела, идентифицировали посредством метода ELISA, описанного далее.
Отбор гибридом
Полистирольные чашки для микротитрования (Maxisorb, Nunc) покрывали пептидом Aβ1-40 с концентрацией 5 мкг/мл в 50 мМ карбонатном буфере, pH 9,6 (покрывающий буфер) в течение ночи при 4°С. Чашки промывали 0,05% Tween 20 в PBS (PBS-T), и сайты неспецифического связывания блокировали 2% бычьим сывороточным альбумином (BSA) в PBS-T (блокирующий раствор) в течение 1 часа при 37°С. После отмывки чашки инкубировали 1 час с супернатантом культуры ткани, разведенным вдвое блокирующим раствором. Чашки снова отмывали и инкубировали с козьим антимышиным IgG, конъюгированным с пероксидазой хрена (Sigma), в течение 1 часа при 37°С. После отмывки к раствору добавляли субстрат (0,05% о-фенилендиамин и 0,015% перекись водорода в 100 мМ цитратном буфере, pH 5,0). Реакцию останавливали через 10 минут 2,5 М серной кислотой, и определяли поглощение при 492 нм в считывающем устройстве для микрочашек. Отбирались гибридомы, супернатанты которых давали значение оптической плотности по меньшей мере вдвое больше, чем полученные с супернатантом независимых гибридом (антитела против глиадина). Гибридомы, которые продуцировали специфические антитела, повторно клонировали, применяя предельное разведение, и изотипы моноклональных антител были определены в супернатанте культуры клеток, концентрированном гель-иммунопреципитацией с применением специфической антисыворотки (Sigma). Отобранные гибридомы выращивали как асцитную жидкость в линии мышей BALB/c, предварительно пролеченных Пристаном.
Очистка моноклональных антител
Моноклональное антитело ЕМ5 очищали от асцитной жидкости посредством аффинной хроматографии на колонке Protein А-Sepharose (Pharmacia). Очищенные антитела тщательно диализировали в PBS и хранили при -85°С до тех пор пока они не использовались.
Пример 2. - Подсчет средней константы диссоциации: аффинность к пептидам Аβ1-40 и Аβ1-42
Для изучения аффинности моноклональных антител ЕМ5 и 6Е10 применялась ELISA с использованием недавно растворенных, иммобилизованных пептидов Aβ1-40 и Aβ1-42, которые были синтезированы в WM Keck plant Йельского Университета с применением N-t-бутилоксикарбонильной методики.
Полистирольные чашки для микротитрования (Immulon 2, Dynex Technology Inc., Chantilly, VA) покрывали 0,5 мкг пептида Aβ1-40 или Aβ1-42, недавно растворенного или агрегированного в карбонатном/бикарбонатном буфере с pH 9,6 в течение 16 часов при 4°С. После блокирования с Superblock (Pierce Chemical Co.), возрастающие концентрации очищенного ЕМ5 (0-0,5 нМ в TBS-T, 100 микролитров на лунку) добавляли в лунки, покрытые Аβ, инкубируя в течение 3 часов при 37°С. Связанное ЕМ5 детектировали с помощью фрагмента F(ab')2 козьего антимышиного IgG, конъюгированного с пероксидазой хрена (1:3000, Amersham). Реакция с 3,3',5,5'-тетраметилбензидином (TMB) (BioRad, Hercules, CA.) развивалась в течение 15 минут, ее останавливали 2М серной кислотой и проводили количественную оценку в считывающем устройстве для микрочашек (Cambridge Technology, Watertown, MA) при 450 нм. Аффинность коммерчески доступного антитела 6Е10 (Senetek, PLC) оценивалась согласно аналогичному протоколу при использовании препаратов очищенных антител IgG. Нелинейный регрессионный анализ, оценка средних констант диссоциации и сравнение данных по связыванию белка с целью нахождения статистической значимости путем подсчета коэффициентов F проводились при использовании программы Prism software от GraphPad (GraphPad, San Diego, CA).
Фиг.1 отображает кривые насыщения, соответствующие связыванию моноклональных антител ЕМ5 и 6Е10 в ELISA с недавно растворенными и агрегированными пептидами Аβ. Высокая аффинность наблюдалась во всех случаях, со средними константами диссоциации в пикомолярном диапазоне. Ни одно из этих антител не показало различной аффинности по отношению к недавно приготовленным или агрегированным формам Аβ. Интересно, что несмотря на то, что 6Е10 показали равнозначную аффинность по отношению к Aβ1-40 и Aβ1-42, ЕМ5 проявили большую аффинность к Аβ 42, чем к Аβ 40 (p<0,01) (13,7 пМ и 15,5 пМ для недавно подготовленных и агрегированных Аβ 42 соответственно; и 37,5 пМ и 37,0 пМ для недавно подготовленных и агрегированных Аβ 40 соответственно).
Пример 3. - Исследование с применением иммунного переноса
Было изучено специфическое распознавание Aβ1-40 и Aβ1-42 антителами ЕМ5 и проведено его сравнение с поликлональными антителами ЕМ2 и ЕМ3 посредством иммунного переноса. Для этого был проведен PAGE электрофорез с пептидами Аβ (0,5 мкг на одну дорожку) в 16% акриламиде, трис-трицин-SDS. Пептиды переносили электрофоретически в течение 1 часа при 400 мА и 4°С на мембраны из поливинилиденфторида (Immobilon-P, Millipore), используя 3-циклогексиламино-1-пропансерную кислоту с pH 11, содержащую 10% метанол. Мембраны блокировали 16 часов при 4°С в TBS-T, содержащем 5% порошкообразное обезжиренное молоко, и затем инкубировали в течение 1 часа при комнатной температуре с 2 мкг/мл иммуноглобулинов G (IgG) ЕМ2, ЕМ3 или ЕМ5. Козий антикроличий IgG (ЕМ2 и ЕМ3) или козий антимышиный IgG (ЕМ5), соединенный с пероксидазой хрена (Amersham) и разведенный 1:2000, использовался в качестве второго антитела. Иммунный перенос визуализировали посредством хемолюминесценции (Amersham), следуя инструкциям производителя.
Данные результаты показаны на Фиг.2, где можно видеть, что в экспериментах по иммунному переносу ЕМ5 проявляло иммунореактивность в отношении обоих пептидов Aβ1-40 и Aβ1-42 (подтверждаемую результатами, полученными в ELISA), тогда как антитела ЕМ2 и ЕМ3 могли распознавать только пептиды Aβ1-40 и Aβ1-42, соответственно, как описано ранее [24]. Эти результаты подтверждают идею о том, что моноклональное антитело ЕМ5 связывается со специфическим линейным эпитопом, общим для обоих пептидов, который сохраняется в образцах, обработанных SDS. В целом наши результаты показывают, что ЕМ5 способно распознавать пептиды Аβ в растворимой форме, агрегированной форме и денатурированной форме (в SDS), с незначительным предпочтением связываясь с Аβ 42, возможно, ввиду возрастания гидрофобности пептида.
Пример 4. - Локализация эпитопа
Для определения точной локализации эпитопа, распознаваемого антителом ЕМ5, было исследовано связывание антитела с сериями синтетических пептидов Аβ. Пептиды Aβ1-16, Aβ1-28 и Аβ25-35 были получены от Sigma (San Luis, МО); пептиды Aβ1-42, Aβ1-42 (E22Q), Aβ1-40, Aβ1-40 (E22G), Aβ1-40 (E22Q), Aβ1-28 (грызун), Aβ1-28 (E22Q), Aβ17-40, Aβ16-42 и Аβ25-35 были синтезированы в WM Keck plant Йельского Университета с применением N-трет-бутилоксикарбонильной методики; Aβ21-28, Aβ21-28 (E22Q), Аβ37-41 и Аβ37-40 синтезировались в Peptide Synthesis Unit (National Biotechnology Center, Madrid) с применением обычной методики Fmoc. Дизайн пептидов Аβ37-42 и Аβ37-49 включал в себя хвост с N-конца с остатком цистеина для их соединения, который имел последовательность CSGGSGGG (SEQ ID NO:4). Все пептиды очищались посредством высокоэффективной жидкостной хроматографии обратно-фазовым способом, и их чистота оценивалась посредством масс-спектрометрии MALDI-TOF.
a) ELISA - захват антител
Чтобы провести исследование, плоскодонные полистирольные чашки для микротитрования (Immulon 2, Dynex Technology Inc., Chantilly, VA) покрывали 1 мкг на лунку соответствующего пептида Аβ в 0,1 М карбонатно-бикарбонатном буфере, pH 9,6 в течение 16 часов при 4°С. После блокирования с 150 мМ NaCl, 20 мМ Tris, 0,05% Tween-20, pH 7,4 (TBST), содержащем 2% BSA, серийные разведения антитела ЕМ5 (от 20 до 0,02 мг/мл фракции IgG) инкубировали в течение 1 часа при 37°С. Затем антимышиный IgG, соединенный с пероксидазой (Sigma, San Luis, МО) и разведенный 1:2000, применялся в течение 30 минут при 37°С. Реакция развивалась в ТМВ (BioRad, СА), останавливалась 2М серной кислотой и количественно оценивалась при 450 нм. Неспецифическое связывание было предотвращено, минуя первичные антитела.
Данные результаты представлены на Фиг.3, верхняя часть которой отображает гистограмму, соответствующую значениям оптической плотности, полученной соответственно при инкубации 20 мкг/мл антитела с каждым из пептидов. Было показано, что ЕМ5 связывалось с любым пептидом, который содержал остатки последовательности Аβ человека 12-16, и было не в состоянии распознать пептиды без этого участка. Более того, мутантные варианты с модификациями вне этого участка (Aβ1-42 (E22Q), Aβ1-40 (A21G), Aβ1-40 (E22G), Aβ1-40 (E22Q)) проявили схожее связывание при сравнении с пептидом дикого типа, тогда как пептид Aβ1-28 (грызун), который обнаруживает три аминокислотные замены в позициях 5, 10 и 13, не был распознан ЕМ5.
b) Масс-спектрометрический анализ гидролизованного и иммунопреципитированного β-амилоидного пептида
Для подтверждения результатов было проведено дополнительное исследование, в котором серию пептидов, производных Aβ1-42, полученных посредством гидролиза с трипсином или α-химотрипсином, приводили в контакт с магнитными частицами, покрытыми антителом ЕМ5, выполняя следующие шаги.
Для ферментативного гидролиза пептида добавлялось 0,5 мкл трипсина или α-химотрипсина, содержащего 0,025 мкг фермента, к аликвоте β-амилоидного пептида объемом 10 мкл в 50 мМ бикарбонате аммония, содержащей 1 мкг пептида. Инкубация проводилась в течение 2 часов при 37°С. Результаты проведенного ферментативного гидролиза схематически показаны в Таблице I.
Для иммобилизации моноклонального антитела ЕМ5 на магнитных частицах аликвоту ЕМ5 объемом 5 мкл (1,1 мг/мл) инкубировали при комнатной температуре в течение 2 часов с 50 мкл Dynabeads M450, покрытыми козлиным антимышиным IgG. Комплекс отмывали 4 раза в PBS двунаправленным перемешиванием (в роторе).
Чтобы произвести иммунопреципитацию, 10 мкл аликвоты β-амилоидного пептида, обработанного трипсином (или α-химотрипсином), инкубировали в роторе в течение 1 часа при 37°С с 50 мкл ЕМ5, иммобилизованного на магнитных частицах. Магнитно-иммунопреципитационный комплекс отмывали 4 раза в PBS в том же роторе, и супернатанты удаляли и выбрасывали.
Для масс-спектрометрического анализа гидролизованного иммунопреципитированного β-амилоидного пептида иммунопреципированные пептиды, содержащиеся в магнитных комплексах, высвобождали с применением 20 мкл смеси 50% ацетонитрила и 0,3% трифторуксусной кислоты. 5 мкл этого раствора смешивали с 5 мкл насыщенной α-циано-4-гидроксикоричной кислоты в 0,1% смеси трифторуксусной кислоты и ацетонитрила (2:1). Затем 0,5 мкл этого раствора помещали в остроконечный датчик из нержавеющей стали и оставляли сохнуть при комнатной температуре. Образцы измеряли в масс-спектрометре MALDI-TOF Reflex II от Bruker, оснащенном ионным источником с оптической системой визуализации и лазером N2 (337 нм). Масс-спектры записывали в позитивном линейном виде при ускоряющем напряжении 28,5 кВ и 1,5 кВ в линейном детекторе, накапливающем 200 лазерных однократных спектров ниже порога плотности облучения. Учитывали только масс-сигналы с хорошим разрешением, с высокой интенсивностью, испускаемые из 3-5 отобранных точек в зоне действия. Все спектры MALDI калибровали внешне, пользуясь стандартизованной смесью пептидов [ангиотензин II (1047,2), фрагмент 18-39 адренокортикотропного гормона 2466,7) и инсулин (5734,6); Sigma].
Рассмотренные свойства пептидов, а также полученные данные суммированы и приведены в следующей Таблице I:
Последовательности каждого из этих пептидов (1-5) и последовательность негидролизованного пептида (6) представлены на Фиг.4, где затенена область, которая фигурирует, как соответствующая эпитопу, распознаваемому антителом ЕМ5 согласно результатам масс-спектроскопии MALDI-TOF иммунопреципитированного материала.
Как можно видеть на указанной Фиг.4, исследование иммунопреципитированного материала при помощи масс-спектроскопии MALDI-TOF показало, что ЕМ5 было способно выделять из гидролизованной смеси каждый фрагмент пептида, который содержал остатки 11-16 (затененные участки). Фрагменты пептида вне этого участка не восстанавливались из раствора. Эти результаты подтверждают данные, полученные посредством метода ELISA и иммунного переноса.
В заключение стоит сказать, что различная реактивность антитела в отношении серий пептидов Аβ показывает, что ЕМ5 распознает остатки 11-16 пептидов Аβ. Среди них участие остатков 12-16 является основным, что иллюстрирует тот факт, что мутация остатка 12 в пептиде Aβ1-28 грызуна (1-28 R) препятствует его распознаванию антителом; частичное участие остатка 11 (Е) в формировании конформации эпитопа нельзя исключить, хотя и полученные данные не вполне это подтверждают.
Пример 5. - Иммуногистохимия: реактивность антител в отношении ткани
Чтобы продемонстрировать обоснованность применения антитела ЕМ5 для обнаружения отложений, которые являются отличительными чертами болезни Альцгеймера (нейритные бляшки и сосудистые отложения) в отличие от диффузных бляшек, проводили иммуноокрашивание срезов ткани мозга, пораженного болезнью Альцгеймера, с применением антител ЕМ2 (поликлональное антитело, направленное на карбоксильный конец пептида Аβ 40), ЕМ3 (поликлональное антитело, направленное на карбоксильный конец пептида Аβ 42) и ЕМ5 (моноклональное антитело с показанной специфичностью к остаткам 12-16 пептида Аβ). И ЕМ2, и ЕМ3 применялись в более ранних исследованиях [24].
Обработка ткани мозга и зон, выбранных для иммуногистохимии
Ткань мозга была поставлена Tissue Bank for Neurological Investigations, Мадрид. Шесть человек, 3 мужчины и 3 женщины, однозначно с БА было включено в исследование. Их возраст был в пределах от 68 до 75 лет. Во всех случаях диагноз БА основывался на клинических патологических нормативах CERAD (Консорциума по Учреждению Регистрации Болезни Альцгеймера) [10]. Ни один из больных не имел других существенных нейропатологических отклонений, например, болезни Паркинсона или значительных сосудистых изменений. Все экземпляры мозга обрабатывали для гистологической оценки, следуя протоколам Brain Bank для нарезания, фиксации и закладки. Периоды post mortem варьировали от 10 до 18 часов. Сразу же после аутопсии одна половина мозга (полученная при медио-сагиттальном срезе полушарий мозга, мозжечка и ствола мозга) фиксировалась в формальдегиде, забуференном 4% фосфатом. После фиксации в течение 3-4 недель были получены блоки ткани из всех кортикальных и субкортикальных зон, принимающих значительное участие в БА, и после постепенной дегидратации в этаноле и осветления ткани ксилолом они были заложены в парафин. Во всех случаях срезы ткани 5 мкМ, соответствующие теменно-затылочной латеральной части коры головного мозга, височной латеральной части коры головного мозга (эти две последние зоны рекомендованы в нормативах CERAD [10]), гиппокампу, caudatum - putamen (в передней части хвостатого ядра) и коре полушарий мозжечка, были получены из исходных парафиновых блоков для иммуногистохимического исследования. В качестве контроля неспецифического окрашивания амилоида проводилось окрашивание модифицированным методом метенамин серебро на срезах, соседних с теми, что обработаны для иммуногистохимического исследования амилоида.
Антитела и протоколы иммуноокрашивания
Применявшимися первичными антителами были ЕМ2, ЕМ3 и ЕМ5. И ЕМ2, и ЕМ3 использовались в более ранних исследованиях [24]. Срезы инкубировали с первичными антителами при комнатной температуре в течение 30 минут. Поликлональные антитела детектировали с помощью системы Envision (Dako Laboratories) с щелочной фосфатазой (APh), используя нитросиний тетразолиевый (NBT) в качестве хромогенного вещества, и ЕМ5 детектировали либо с помощью ранее указанной системы, либо с помощью системы Envision (Dako Laboratories) с пероксидазой хрена (HRP), применяя диаминобензидин (DAB) в качестве хромогенного вещества. В случае использования методов совместной локализации поликлональные антитела всегда детектировали с помощью системы Envision с APh (применяя NBT в качестве хромогенного вещества), тогда как ЕМ5 детектировали с помощью системы Envision с HRP (используя DAB в качестве хромогенного вещества).
Двойное и одиночное иммуноокрашивание
Методы двойного иммуноокрашивания с использованием ЕМ5 в качестве первого первичного антитела и ЕМ2 или ЕМ3 в качестве второго первичного антитела применялись как предварительное действие с целью установления степени совместной локализации каждой пары антител и оптимального рабочего разведения каждого из них. Во время этой фазы исследования, которая ограничивалась срезами ткани теменно-затылочной части коры головного мозга двух больных, было установлено, что использование ЕМ5 в качестве первого первичного антитела исключало эффект маскировки двух других антител, если они применялись в качестве первого антитела во время двойного иммуноокрашивания. В серийных срезах обоих отобранных парафиновых блоков возрастающие разведения ЕМ5 (1:50, 1:100, 1:500, 1:1000 и 1:2000) совместно локализовались с уменьшающимися разведениями ЕМ2 или ЕМ3 (1:2000, 1:1000, 1:500, 1:100 и 1:50). Поскольку было обнаружено, что антитело ЕМ2 с высокой степенью совместно локализовалось с ЕМ5, остальная часть исследования была направлена на то, чтобы показать характерные участки реактивности, проявляемой ЕМ5 и ЕМ3. С этой целью последующее двойное иммуноокрашивание срезов всех выбранных зон ограничивалось во всех случаях использованием ЕМ5 (с разведением 1:1000) в качестве первого первичного антитела и ЕМ3 (с разведением 1:1000) в качестве второго первичного антитела. В дополнение для более точной визуализации участков реактивности, проявляемой каждым антителом в одной и той же ткани, одиночное иммуноокрашивание проводилось на серийных срезах каждого блока с применением ЕМ5, ЕМ2 или ЕМ3 в качестве первичного антитела. Поскольку основной целью этой части исследования является качественное сравнение различных участков иммунной реактивности, что предпочтительнее, чем сравнение количественных различий между антителами, результаты окрашиваний не были оценены количественно.
Результаты
Результаты по одному из случаев заболевания можно видеть на Фиг.5, представленной с ранее приведенным распределением, а именно:
- (А) и (В): Последовательные серийные срезы одной и той же области затылочной части коры головного мозга, после иммуноокрашивания с ЕМ5 (А) и ЕМ3 (В) в качестве первичного антитела, с использованием NBT в качестве хромогенного вещества. Сосуды (V) отмечены, с тем, чтобы облегчить нахождение бляшек. Тогда как ЕМ3 (В) выявляет и диффузные бляшки (DP), и нейритные бляшки (NP), так же как и отложения в кровеносных сосудах (V), ЕМ5 (А) дает более интенсивное окрашивание и кровеносных сосудов, и некоторых нейритных бляшек, хотя не окрашивает диффузные бляшки.
(С) Микрофотография при большом увеличении техники двойного иммуноокрашивания с использованием ЕМ3 (применяя NBT - синее окрашивание - в качестве хромогенного вещества) и ЕМ5 (применяя DAB - коричневое окрашивание - в качестве хромогенного вещества) в качестве первичных антител. Наблюдается двойное иммуноокрашивание нейритных бляшек и стенки сосудов.
- (D) и (Е): Последовательные серийные срезы одной и той же области затылочной части коры головного мозга после иммуноокрашивания либо с ЕМ5 (D), либо с ЕМ2 (Е). Вновь сосуды (V) отметили, чтобы это способствовало распознаванию бляшек. Можно видеть, что и сосуды, и нейритные бляшки взаимодействуют с обоими антителами. Меньшее количество нейритных бляшек окрашивается с ЕМ2, нежели с ЕМ5, и ни одна диффузная бляшка не взаимодействует с любым из них.
(F) Микрофотография при большом увеличении техники двойного иммуноокрашивания с использованием ЕМ2 (применяя NBT - синее окрашивание - в качестве хромогенного вещества) и ЕМ5 (применяя DAB - коричневое окрашивание - в качестве хромогенного вещества) в качестве первичных антител того же среза ткани затылочной части коры головного мозга. Наблюдалась четкая совместная локализация активности обоих антител в стенке сосуда и нейритных бляшках.
Во всех случаях заболевания, кроме одного, обнаруживаются резко выраженные лептоменингеальные и интракортикальные сосудистые амилоидные отложения, которые взаимодействовали со всеми испытываемыми антителами. Во всех достоверных случаях иммунореактивность сосудистых амилоидных отложений была более резко выражена (более обширно и более интенсивно) с ЕМ2 (Фиг.(5Е)) и с ЕМ5 (Фиг.(5А) и (5D)), чем с ЕМ3 (Фиг.(5В)). В этом случае наиболее четко совместно локализовались ЕМ2 и ЕМ5 (Фиг.(5F)). Как ожидалось, в неокортикальных областях и гиппокампе была обнаружена высокая плотность диффузных и нейритных бляшек, тогда как в коре мозжечка и полосатом теле были продемонстрированы только диффузные отложения амилоида. Срезы инкубировали с антителом ЕМЗ, проявляющим активность по отношению к диффузным и нейритным бляшкам (Фиг.(5В)). Когда их сравнили с последующими срезами, окрашенными с применением модифицированного метода метенамин-серебро, то обнаружили, что ЕМЗ окрасило все бляшки, присутствующие в каждом срезе. Дополнительно антитело ЕМ3 окрасило некоторые тела нейронов. И ЕМ2, и ЕМ5 окрашивали незрелые нейритные бляшки (без ядра) и зрелые нейритные бляшки (с ядром), снова с высокой степенью совместной локализации (Фиг.(5F)). ЕМ2 не взаимодействовало ни с какими диффузными бляшками, ни в кортикальной зоне, ни в субкортикальной зоне (Фиг.(3Е)). Двойное иммуноокрашивание с ЕМ5 и ЕМ3 показывает совместную локализацию обоих антител в некоторых нейритных бляшках, но не в диффузных бляшках (Фиг.(5С)), хотя в этом случае была обнаружена некая совместная локализация, когда ЕМ5 инкубировали при очень незначительном разведении (1:50). Только в одном случае заболевания, который продемонстрировал множество ЕМ3-положительных диффузных бляшек на срезах полосатого тела, некоторые из них окрашивались очень слабо с ЕМ5 при рабочем разведении (1:500). Этот же самый образец не показал какой-либо реактивности в диффузных бляшках, как, например, ЕМ5 в коре мозжечка. Во всех остальных случаях на срезах полосатого тела и на срезах мозжечка было показано переменное количество диффузных бляшек, ни одна из них не взаимодействовала с антителом ЕМ5. Ни ЕМ2, ни ЕМ5 не обнаружили окрашивания всех присутствующих нейритных бляшек (см. Фиг.(5А, D)). Однако, как было обнаружено в случае с иммунореактивностью сосудистых амилоидных отложений, нейритные бляшки, реактивные к ЕМ2 или ЕМ5, окрашивались более интенсивно, чем с ЕМ3. Не считая негативного ответа сосудов по отношению ко всем антителам в единственном случае и незначительного позитивного ответа некоторых диффузных бляшек полосатого тела в том же образце мозга, можно считать, что все случаи показывают сходные участки окрашивания для каждого исследуемого антитела.
Таким образом, в отличие от более равномерных участков окрашивания, наблюдаемых в диффузных бляшках, панель антител выявила гетерогенность среди нейритных бляшек, что подтверждает уместность отображения реальных стадий в процессе развития диффузных бляшек и их трансформации в нейритные бляшки. Антитело ЕМ5 дает интенсивное окрашивание всех структур (нейритных бляшек и стенок сосудов), окрашенных с ЕМ2 и окрашенных в разной степенью ЕМ3. Было обнаружено, что в подгруппе нейритных бляшек имеется паттерн, окрашивающийся идентично сосудистому амилоиду, с высокой степенью совместной локализации реактивности к ЕМ2 и ЕМ5. Данное изобретение демонстрирует, что ЕМ5 должно реагировать со всеми структурами, которые имеют в своем составе либо Аβ<11-40, либо Aβ<11-42. В действительности результаты ELISA, представленные здесь, показывают, что антитело ЕМ5 распознает и недавно растворенные, и агрегированные формы пептида Аβ. Несмотря на это, на срезах ткани была обнаружена большая вариабельность окрашивания с ЕМ5 среди нейритных бляшек, чем с поликлональными антителами, наряду с высокой степенью совместной локализации интенсивной реактивности в отношении ЕМ5 с ЕМ2 (Аβ С40). Относительно более интенсивное окрашивание в этих позитивных бляшках может выявить подгруппу нейритных бляшек либо с чрезвычайно высоким содержанием длинных пептидов Аβ, либо с избирательно высоким содержанием Аβ С40, или даже исключительную доступность эпитопа, распознаваемого ЕМ5 в структурах (в сосудах или бляшках), в которых обнаружено совместное отложение Аβ<11-40 и Аβ<11-42. Возможно, что антитело согласно изобретению детектирует ту же подгруппу нейритных бляшек Аβ С40 (+), которую детектировали ранее Parvathy и др. [22]. Эта подгруппа нейритных бляшек с особенно высоким содержанием длинных пептидов Аβ может представлять собой важные этапы в прогрессии амилоидных поражений при БА, что способно детектировать моноклональное антитело согласно изобретению. Следовательно, применение ЕМ5 может позволить охарактеризовать подгруппы бляшек, которые служат специфическим маркером стадий при прогрессии заболевания.
Пример 6. - Способность антител взаимодействовать с формами пептида β-амилоид в моче
Чтобы продемонстрировать обоснованность использования антитела ЕМ5 для выявления присутствия форм β-амилоидного пептида в биологических жидкостях, было проведено исследование по детекции их в образцах мочи здоровых пациентов, к которым после того, как образцы были получены, добавляли смесь синтетических пептидов, соответствующих формам различной длины β-амилоидного пептида. Для этого моноклональное антитело, связанное с магнитными частицами, добавляли к образцам мочи, и связанные пептиды детектировали, применяя масс-спектрометрию MALDI-TOF. Детали применявшегося метода представлены ниже.
Связывание антитела с магнитными частицами
Магнитные частицы, соединенные с антителом ЕМ5, готовили, следуя методу, описанному Fuentes и др. [26], основанному на мягком окислении гликозидных остатков иммуноглобулинов для получения альдегидных групп, взаимодействующих с магнитными частицами, на поверхности которых посредством модифицирования с этилендиамином сформированы аминогруппы. Кратко: окисление антитела ЕМ5 вызывали посредством инкубации с 10 мМ периодатом натрия в течение 2 часов, после чего окисленное антитело диализировали в дистиллированной воде при 4°С. Магнитные частицы ЕМ/100-30 (Merck Co, Франция), на поверхности которых имеются карбоксильные группы, модифицировали посредством инкубации, при концентрации 10 мг/мл, с 1М этилендиамином pH 4,75 в течение 90 минут, после чего добавляли твердый EDCI (1-этил-3-(3'-диметиламинопропил)карбодиимида гидрохлорид) до конечной концентрации 10 мМ и оставляли для взаимодействия на 90 минут, перед тщательной промывкой дистиллированной водой.
Антитело иммобилизовывали на магнитных частицах после добавления 10 мг окисленного антитела ЕМ5, растворенного в 150 мМ фосфатно-натриевом буфере с pH 7,5, к 2 мл магнитных частиц (10 мг/мл) с аминогруппами на их поверхности и инкубировали при 4°С в течение ночи. Образовывались основания Шиффа, и непрореагировавшие альдегидные группы устранялись при добавлении борогидрида натрия до достижения концентрации 1 мг/мл при pH 8,5 и 4°С. Препарат обильно промывали дистиллированной водой. Количество иммобилизованного антитела определяли посредством количественной оценки различия в концентрации белков в супернатанте до и после иммобилизации, используя метод Бредфорда [27].
Детекция β-амилоидного пептида в растворе
Перед проверкой обоснованности применения антитела согласно изобретению для связывания с изоформами β-амилоидного пептида, присутствующими в образцах биологических жидкостей, как например в моче, авторы проверили его способность к связыванию с формами β-амилоидного пептида в растворе, и если антитела, связанные с магнитными частицами, делали возможным выделение форм β-амилоидного пептида из растворов, в которых они встречались, продолжали их последующую идентификацию и/или количественную оценку. Поэтому синтетические пептиды, которые соответствовали формам β-амилоидного пептида Aβ12-29, Aβ1-40 и Aβ1-42, растворенные в дистиллированной воде, смешивали друг с другом в дистиллированной воде, чтобы произвести смесь с конечными концентрациями 0,44 мкг/мкл Aβ12-29 и Aβ1-42 и 0,11 мкг/мкл Aβ1-40. 4 мкл этой смеси пептидов добавляли к 981 мкл воды.
Затем формы β-амилоидного пептида, присутствующие в растворе в воде, разделяли, применяя антитело согласно изобретению, соединенное с магнитными частицами. Результаты масс-спектрометрометрического исследования смесей пептидов, выделенных из раствора, представлены на Фиг.6, где часть А соответствует исследованию раствора без предварительной обработки антителами (Ctrl.) и часть В соответствует применению антитела, связанного с магнитными частицами (ЕМ5+РМ). Как можно видеть, антитело способно связываться с формами β-амилоидного пептида в растворе и образовывать с ними комплексы, так что они могут быть отделены от указанного раствора.
Подготовка образца мочи
В дни разделения образцы мочи объемом 10 мл собирались у здорового индивидуума и центрифугировались при 3500 об/мин при комнатной температуре в течение 5 минут. Мочу нейтрализовали до pH 7,0, применяя 1 М NaOH в буфере PBS.
Синтетические пептиды, которые соответствовали формам (3-амилоидного пептида Aβ12-28, Aβ1-40 и Aβ1-42, смешивали друг с другом в дистиллированной воде, чтобы произвести смесь с конечными концентрациями 0,44 мкг/мкл Aβ12-28 и Aβ1-42 и 0,11 мкг/мкл Aβ1-40. 4 мкл этой смеси пептидов добавляли к 981 мкл мочи.
Конечная концентрация форм β-амилоидного пептида в моче составляла 1,76 мкг/мл в случае с Aβ12-28 и Aβ1-42 и 0,44 мкг/мл в случае с Aβ1-40.
Иммунопреципитация
15 мкл магнитных частиц, покрытых моноклональным антителом ЕМ5 (разведенным 1:4 в буфер PBS), инкубировали в течение 1 часа при 37°С с 981 мкл образца мочи, описанного выше, который содержал три β-амилоидных пептида (Aβ12-18, Aβ1-40 и Aβ1-42).
После инкубации пробирка помещалась в намагниченный сепаратор для магнитных частиц, и моча аккуратно удалялась при помощи пипетки.
Магнитные частицы со связавшимися с ними пептидами, удерживаемые под действием магнитного поля сепаратора, 3 раза промывались водой.
Пептиды, связанные с ними, отделялись от магнитных частиц с помощью 12 мкл раствора смеси α-циано-4-гидроксикоричной кислоты в 30% (v/v) водном ацетонитриле, содержащем 0,1% (v/v) трифторуксусной кислоты (TFA), и были исследованы посредством масс-спектрометрии MALDI-TOF.
Детекция иммунопреципитированных пептидов посредством масс-спектрометрии
1,5 мкл смеси образцов, полученной при иммунопреципитации на матрице α-циано-4-гидроксикоричной кислоты, помещали в датчик из нержавеющей стали вместимостью 100 образцов и оставляли сохнуть при комнатной температуре на 5 минут.
Образцы оценивали в автоматизированном рабочем месте Voyager DE-PRO для масс-спектрометрии MALDI-TOF от РЕ Biosystems, используя стандартную конфигурацию измерительного прибора. Масс-спектры записывали в позитивном отражающем виде при ускоряющем напряжении 20 кВ и 75% напряжения в коллектор, при 0,002% направляющей нити накала и времени запаздывания 150 наносекунд, накапливая 200 спектров для отдельного возбуждения лазера ниже порога плотности облучения. Учитывали только масс-сигналы с хорошим разрешением, с высокой интенсивностью, испускаемые из 3-5 отобранных точек в зоне действия. Оборудование калибровали внешне, пользуясь калибровочной смесью 2, предоставляемой Applied Biosystems (Tres Cantos, Мадрид, Испания), состоящей из ангиотензина (1297 Да), АСТН 1-17 (2094 Да), АСТН 18-39 (2466 Да), АСТН 7-38 (3660 Да) и бычьего инсулина (2867 Да).
На Фиг.7 показан типичный график, полученный для одного из образцов. Видны пики, соответствующие пептидам, добавленным к образцу мочи, которые демонстрируют способность антитела согласно изобретению связываться с ними в образцах мочи. Как показало исследование образца биологической жидкости, также могут быть видны другие пики, соответствующие другим молекулам, от природы присутствующим в данном образце, которые также связывались с антителом, соединенным с магнитными частицами.
Депонирование гибридом
Гибридома, продуцирующая антитело ЕМ5, была депонирована в Европейской Коллекции Культур Клеток (ЕСАСС), CAMR, Солсбери, Уилтшир, Соединенное Королевство. Дата депонирования и номер доступа следующие:
Как отмечалось ранее, эти гибридомные клетки были получены посредством слияния двух типов клеток: а) лимфоциты селезенки мыши линии BALB/c, полученные после иммунизации мышей с использованием в качестве иммуногена формы β-амилоидного пептида, обозначенной Aβ1-40, содержащей 1-40 аминокислоту указанного пептида, соединенного с KLH (гемоцианин моллюска Keyhole limpet); b) клетки линии мышиной миеломы Р3/Х63-Ag653, которая играла иммортализующую роль в слиянии. Были получены различные клоны, из которых мы отобрали клон, названный «ЕМ5 клон А», который продуцирует моноклональное антитело, названное «ЕМ5», антитело типа IgG1, способное специфически распознавать антиген, использованный для иммунизации - пептид Aβ1-40, что подтвердили тесты ELISA по захвату антител. Этот клон растили на культуральной среде RPMI 1640 с 10% эмбриональной телячьей сыворотки, 10% DMSO, 2 мМ глутамином и 1 мМ пируватом натрия при 37°С и в атмосфере, содержащей 5% CO2, в условиях, при которых 95% клеток росли в суспензии и остальные 5% прикреплялись к культуральной бутыли. Клетки клонировали дважды посредством предельных разведений, после чего аликвоты 4×106 клеток брали и помещали во флаконы. После проверки на отсутствие бактерий, отсутствие микоплазм и отсутствие грибов несколько из этих флаконов было отправлено в Европейскую Коллекцию Культур Клеток (ЕСАСС) с запросом на разрешение для их депонирования.










Изобретение относится к области биотехнологии и иммунологии. Предложены варианты моноклонального антитела, которое распознает в β-амилоидном пептиде эпитоп с последовательностью VHHQK. Описана гибридома, продуцирующая указанное антитело (ЕСАСС 06030101), а также варианты композиций на основе антитела. Предложены варианты способа in vitro-диагностики на основе антител и варианты использования антитела в in vitro-диагностике болезни Альцгеймера с помощью моноклонального антитела и композиции на его основе. Связывание антитела с аминокислотами 12-16 β-амилоидного пептида специфически детектирует нейритные бляшки, которые являются характерными чертами болезни Альцгеймера, без детекции диффузных бляшек, которые не являются показателями заболевания. С помощью моноклонального антитела можно осуществлять детекцию подгруппы среди нейритных бляшек, отличающейся по составу отложений изоформ β-амилоидного пептида, которая связана со стадией прогрессии заболевания. Антитело способно связываться с изоформами β-амилоидного пептида в биологической жидкости, такой как моча, плазма, кровь, спинномозговая жидкость. Указанные свойства могут найти применение в in vitro-диагностике болезни Альцгеймера при определении стадии прогрессии заболевания. 10 н. и 40 з.п. ф-лы, 7 ил., 1 табл.
1. Моноклональное антитело, продуцируемое гибридомной клеточной линией ЕСАСС 06030101, которое распознает в β-амилоидном пептиде (Ар) эпитоп, соответствующий последовательности
Val-His-His-Gln-Lys (SEQ ID NO:3),
и которое способно связываться с изоформами человеческого β-амилоидного пептида, содержащими указанную последовательность.
2. Моноклональное антитело по п.1, аффинность связывания которого с Aβ1-42 больше, чем его аффинность связывания с Aβ1-40, причем обе аффинности связывания измерены посредством ELISA.
3. Моноклональное антитело по п.2, связывающееся с отложениями человеческого β-амилоидного пептида в ткани мозга индивидуумов, страдающих болезнью Альцгеймера.
4. Моноклональное антитело по п.3, избирательно связывающееся с нейритными бляшками и сосудистыми отложениями амилоида.
5. Моноклональное антитело по п.4, проявляющее большую аффинность связывания в отношении подгруппы нейритных бляшек, состав которых подобен составу сосудистых отложений амилоида.
6. Гибридомная клеточная линия ЕСАСС 06030101, продуцирующая моноклональное антитело по любому из пп.1-5.
7. Гибридомная клеточная линия по п.6, полученная посредством слияния линии клеток мышиной миеломы P3/X63-Ag.653 с клетками селезенки мышей линии BALB/c, иммунизированных β-амилоидным пептидом, который содержит последовательность Val-His-His-Gln-Lys (SEQ ID NO:3).
8. Гибридомная клеточная линия по п.6, полученная посредством слияния линии клеток мышиной миеломы P3/X63-Ag.653 с клетками селезенки мышей линии BALB/c, иммунизированных пептидом Aβ1-40.
9. Гибридомная клеточная линия по п.8, полученная посредством слияния линии мышиной миеломы P3/X63-Ag.653 с клетками селезенки мышей линии BALB/c, иммунизированных пептидом Aβ1-40, соединенным с KLH.
10. Гибридомная клеточная линия по п.9, которая содержит, по существу, чистый образец ЕСАСС 06030101.
11. Применение моноклонального антитела по любому из пп.1-5 в in vitro-диагностике болезни Альцгеймера в образце ткани мозга, взятой у индивидуума, страдающего указанным заболеванием.
12. Применение по п.11, где стадия прогрессии заболевания коррелирует с присутствием в образце подгруппы нейритных бляшек, обнаруженных благодаря их связыванию с моноклональным антителом.
13. Композиция для применения в диагностике неврологических заболеваний, которая содержит эффективное количество моноклонального антитела по любому из пп.1-5, связанного с веществом, которое позволяет детектировать указанное антитело или его фрагмент.
14. Композиция по п.13, где вещество, с которым соединено моноклональное антитело, является вторым антителом, способным связываться с указанным первым антителом, при этом указанное второе антитело связано с ферментом, способным катализировать превращение особого вещества в другое, которое можно детектировать.
15. Композиция по п.14, где вещество, превращение которого катализируется ферментом, является хромогенным веществом.
16. Композиция по п.15, где второе антитело связано с щелочной фосфатазой, а используемым хромогенным веществом является нитросиний тетразолиевый.
17. Композиция по п.15, где второе антитело связано с пероксидазой хрена, а используемым хромогенным веществом является диаминобензидин.
18. Композиция по любому из пп.13-17, которая содержит по меньшей мере одно иное антитело, специфичное по меньшей мере в отношении одного участка последовательности, отличающегося от β-амилоидного пептида.
19. Композиция по п.18, которая содержит моноклональное антитело по любому из пп.1-5, соединенное с веществом, которое можно детектировать, и еще одно антитело или другие антитела, специфичные в отношении одного или более различных участков последовательности β-амилоидного пептида, соединенные с различными веществами, которые также можно детектировать.
20. Композиция по п.19, где вторым антителом против другого участка последовательности β-амилоидного пептида является антитело ЕМ2.
21. Композиция по п.20, где моноклональное антитело по любому из пп.1-5 соединено со вторым антителом, связанным с пероксидазой хрена, и хромогенное вещество диаминобензидин (DAB) используется в качестве вещества для превращения, которое можно детектировать, тогда как антитело ЕМ2 соединяется со вторым антителом, связанным с щелочной фосфатазой, и хромогенное вещество нитросиний тетразолиевый используется в качестве вещества для превращения, которое можно детектировать.
22. Композиция по п.19, где вторым антителом против другого участка последовательности β-амилоидного пептида является антитело ЕМ3.
23. Композиция по п.22, где моноклональное антитело по любому из пп.1-5 соединяется со вторым антителом, связанным с пероксидазой хрена, и хромогенное вещество диаминобензидин (DAB) используется в качестве вещества для превращения, которое можно детектировать, тогда как антитело ЕМ3 соединено со вторым антителом, связанным с щелочной фосфатазой, и хромогенное вещество нитросиний тетразолиевый используется в качестве вещества для превращения, которое можно детектировать.
24. Применение композиции по любому из пп.13-23 в диагностике болезни Альцгеймера по образцу ткани мозга, взятой у индивидуума, имеющего указанное заболевание.
25. Способ in vitro-диагностики болезни Альцгеймера в образце ткани мозга, взятой у индивидуума, страдающего указанным заболеванием, включающий в себя детектирование присутствия в указанном образце нейритных бляшек и сосудистых отложений амилоида вследствие связывания моноклонального антитела по любому из пп.1-5 по меньшей мере с одной изоформой β-амилоидного пептида, которая содержит по меньшей мере последовательность Val-His-His-Gln-Lys (SEQ ID NO:3) и которая присутствует в нейритных бляшках и/или сосудистых отложениях амилоида.
26. Способ по п.25, где моноклональное антитело содержится в композиции по любому из пп.13-17.
27. Способ по п.25, где присутствие нейритных бляшек, детектируемых посредством моноклонального антитела по любому из пп.1-5, коррелирует со стадией прогрессии заболевания.
28. Способ по любому из пп.25-27, где присутствие изоформы Aβ1-40 пептида β-амилоида в нейритных бляшках, детектируемых посредством моноклонального антитела, подтверждается вследствие связывания антитела, специфичного в отношении карбокси-конца изоформы Аβ1-40 β-амилоидного пептида.
29. Способ по п.28, где антителом, специфичным в отношении карбокси-конца изоформы Aβ1-40 β-амилоидного пептида, является ЕМ2.
30. Способ по п.29, где присутствие дополнительных нейритных бляшек и/или диффузных бляшек детектируется вследствие связывания с антителом, специфичным в отношении карбокси-конца изоформы Аβ1-42 β-амилоидного пептида.
31. Способ по п.30, где антителом, специфичным в отношении карбокси-конца изоформы Aβ1-42 β-амилоидного пептида, является ЕМ3.
32. Моноклональное антитело, которое распознает в β-амилоидном пептиде (Аβ) эпитоп, соответствующий последовательности Val-His-His-Gln-Lys (SEQ ID NO:3), и связывается с растворимыми формами человеческого β-амилоидного пептида в образцах биологических жидкостей или полученных из них растворов, выбранных из группы, состоящей из спинно-мозговой жидкости, крови, плазмы и мочи.
33. Моноклональное антитело по п.32, связывающееся с растворимыми формами человеческого пептида β-амилоида в образцах мочи.
34. Композиция, содержащая моноклональное антитело по п.32 или 33, где антитело соединено с веществом или частицей, которая способствует выделению комплексов антиген-фрагмент антитела из раствора, в котором они присутствуют.
35. Композиция по п.34, где веществом или частицей, способствующей выделению комплексов антиген-фрагмент антитела из раствора, в котором они присутствуют, является магнитная частица.
36. Композиция по п.35, где связью между антителом и магнитной частицей является ковалентная связь.
37. Применение моноклонального антитела по п.32 или 33 в in vitro-диагностике болезни Альцгеймера в образце биологической жидкости или полученного из нее раствора.
38. Применение по п.37, где моноклональное антитело содержится в композиции по любому из пп.34-36.
39. Применение по п.38, где моноклональное антитело содержится в композиции по п.36.
40. Применение по п.39, где композицию по п.36 добавляют к образцу биологической жидкости или к полученному из нее раствору с тем, чтобы сформировался комплекс антиген-антитело с формами β-амилоидного пептида, присутствующими в образце биологической жидкости или полученного из нее раствора.
41. Применение по п.40, где выделение образующихся комплексов антиген-антитело из биологической жидкости или раствора, в котором они встречаются, осуществляется посредством использования магнитного поля.
42. Применение по п.41, где формы β-амилоидного пептида, выделенные из биологической жидкости или полученного из нее раствора в виде комплексов антиген-антитело, отделяют от антитела после их выделения из биологической жидкости или раствора, в которых они присутствуют, и перед их идентификацией и/или количественной оценкой.
43. Применение по п.42, где формы β-амилоидного пептида идентифицируют и/или количественно оценивают посредством масс-спектрометрии MALDI-TOF.
44. Применение по любому из пп.37-43, где образцом биологической жидкости является образец мочи.
45. Применение по п.42, где стадия прогрессии болезни Альцгеймера коррелирует с концентрацией изоформы Aβ1-42 в образце.
46. Способ in vitro-диагностики болезни Альцгеймера в образце биологической жидкости или полученного из нее раствора, который включает в себя детектирование в указанном образце по меньшей мере одной изоформы β-амилоидного пептида, который содержит по меньшей мере последовательность Val-His-His-Gln-Lys (SEQ ID NO:3), вследствие ее связывания с моноклональным антителом по п.32 или 33, включающий в себя следующие стадии:
a) добавление композиции по п.35 или 36 к образцу биологической жидкости или полученного из нее раствора;
b) выжидание в течение времени, достаточного для образования комплексов антиген-антитело между по меньшей мере одной изоформой β-амилоидного пептида и антителом, содержащимися в композиции;
c) наложение магнитного поля для выделения комплексов антиген-антитело из раствора;
d) удаление раствора;
e) отделение антитела от молекул β-амилоидного пептида;
f) идентификацию и количественную оценку изоформ β-амилоидного пептида, выделенных из образца биологической жидкости или полученного из нее раствора.
47. Способ in vitro-диагностики болезни Альцгеймера по п.46, где образцом биологической жидкости является образец мочи.
48. Способ in vitro-диагностики болезни Альцгеймера по п.47, где композиция, добавляемая на стадии а), содержит моноклональное антитело по п.32, ковалентно связанное с соответствующими магнитными частицами посредством модификации одного или более остатков, присутствующих в Fc-области указанного антитела.
49. Способ in vitro-диагностики болезни Альцгеймера по п.48, где идентификацию и количественную оценку изоформ β-амилоидного пептида, выделенного из образца мочи, осуществляют посредством масс-спектрометрии MALDI-TOF.
50. Способ in vitro-диагностики болезни Альцгеймера по п.49, где стадию е) отделения антитела или фрагмента антитела от молекул β-амилоидного пептида осуществляют в α-циано-4-гидроксикоричной кислоте в водном ацетонитриле, содержащем трифторуксусную кислоту.
Приоритет по пунктам:
09.03.2006 по пп.1-31;
09.03.2005 по пп.32-50.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| FURUKAWA et al., Increased activity-regulating and neuroprotective efficacy of α-secretase-derived secreted amyloid precursor protein conferred by a C-teminal heparin-binding domain, Journal of Neurochemistry, 67, стр.1882-1896, 1996 | |||
| RU 2000132207/14 A, 21.05.1999. | |||
Авторы
Даты
2011-04-20—Публикация
2006-03-09—Подача