Изобретение относится к области медицины, в частности гепатологии и инфекционным болезням, и может использоваться для оценки фиброза печени на фоне хронического вирусного гепатита C с целью регистрации предцирротической стадии фиброза и перехода ее в цирроз печени путем исследования пробы венозной крови.
Более 175 миллионов жителей нашей планеты (3% населения) инфицировано вирусом гепатита С (ВГС), что позволяет причислять его к разряду глобальных пандемических агентов. Каждый год число страдающих ВГС-инфекцией возрастает на 3-4 миллиона, в России только число ежегодно выявляемых ВГС-инфицированных субъектов составляет примерно 220 тысяч человек [1, 2]. В 70-90% случаев заболевание принимает хроническое течение, которое сопровождается прогрессирующим поражением печени с развитием цирроза или гепатоклеточной карциномы. Так, частота перехода заболевания в цирроз печени составляет по прошествии 1-2 десятилетий около 20% с развитием осложнений, несовместимых с жизнью [3].
Существуют определенные трудности в прогнозировании прогрессирующего течения фиброза и развития цирроза печени. В настоящее время золотым стандартом определения степени фиброзных изменений в печени является пункционная биопсия с последующим гистологическим определением стадии фиброза [4, 5], однако этот метод, относящийся к числу высоко инвазивных, не всегда позволяет достаточно точно получить тканевой материал из участка максимальной выраженности фиброзных изменений, а его использование иногда приводит к серьезным осложнениям, угрожающим жизни пациента. В связи с последним обстоятельством пункционную биопсию рекомендуют производить не чаще 1 раза в 5 лет, что заставляет продолжать поиск менее инвазивных способов определения критериев цирроза, позволяющих проводить мониторинг прогрессирования фиброзных изменений в печени на фоне хронического вирусного гепатита С (ХВГС) по косвенным признакам [6].
Ввиду того что определяющую роль в развитии и прогрессировании хронического гепатита С играет иммунная система, а ВГС-индуцированное поражение печени в большей степени опосредовано иммунными механизмами, чем прямыми цитопатическими эффектами самого вируса [7], одним из критериев прогрессирования фиброза и, в конечном итоге, развития цирроза печени может служить характер иммунного ответа на ВГС с участием естественных киллеров (ЕК) и ЕКТ - CD56+ клеток иммунной системы, которые широко представлены в печеночной ткани и за которыми в настоящее время признается ведущая роль в элиминации ВГС [8, 9].
Наиболее близкий аналог заявляемого изобретения - способ мониторинга фиброза печени у больных хроническим гепатитом С (ХГС) [Патент РФ 2309406, опубл. 2007]. Способ основан на определении в сыворотке крови содержания цитокинов ИЛ-4, ИЛ-10, ИЛ-12р70, ФНО-альфа. При ИЛ-4 выше 5,6 пг/мл, ИЛ-10 выше 35 пг/мл, ФНО-альфа выше 14 пг/мл и ИЛ-12р70 выше 8,5 пг/мл устанавливается наличие выраженного фиброза печени. Изобретение позволяет провести эффективную диагностику фиброза печени у больных хроническим гепатитом С.
Основным недостатком аналога следует считать неточность получаемого результата, не позволяющего определить четкие показания для смены врачебной тактики и перехода к интенсивным лечебным мероприятиям по предупреждению цирроза печени.
Задача настоящего изобретения заключается в разработке эффективного способа оценки фиброза печени на стадиях предцирротических и цирротических изменений и, таким образом, прогноза цирроза печени при ХВГС с использованием фенотипирования CD56+ лимфоцитов крови.
Поставленная задача решается следующим образом.
Предложен способ оценки фиброза печени у больных хроническим вирусным гепатитом С, включающий проведение исследований фенотипа CD56+ лимфоцитов крови, при этом определяют процентное содержание CD3+/CD56+, CD3+/CD56+/CD4+, CD3+/CD56+/CD8+, CD56+/CD94+, CD56+/NKG2D+, CD56+/CD107a+ клеток и при изменении содержания в крови CD3+/CD56+ клеток выше 3,7%, CD3+/CD56+/CD4+ клеток выше 23,8%, CD3+/CD56+/CD8+ клеток ниже 47,6%, CD56+/CD94+ клеток ниже 46,7%, CD56+/NKG2D+ клеток выше 98,4%, и CD56+/CD107a+ клеток ниже 98,2% устанавливают наличие третьей стадии (предцирротической) фиброза печени, а изменение содержания в крови 5 из 6 параметров: CD3+/CD56+ клеток ниже 4,3%, CD3+/CD56+/CD4+ клеток ниже 24%, CD3+/CD56+/CD8+ клеток выше 27,7%, CD56+/CD94+ клеток ниже 31,6% или выше 41,6%, CD56+/NKG2D+ клеток ниже 98,5%, и CD56+/CD107a+ клеток выше 58,9% расценивают как переход заболевания в цирроз печени.
Больные ХВГС были разделены на 4 подгруппы в соответствии со стадией фиброзных изменений печени по шкале METAVIR: 1-я подгруппа (стадия фиброза 1) - 16 человек; 2-я подгруппа (стадия фиброза 2) - 6 человек; 3-я подгруппа (стадия фиброза 3) - 8 человек; 4-я подгруппа (стадия фиброза 4) - 11 человек. Всем больным последней подгруппы был поставлен диагноз цирроза печени на основании анамнеза, клинических проявлений, результатов биохимических и физикальных исследований, данных ультразвукового исследования органов брюшной полости и эзофагогастродуоденоскопии.
Материалом для исследования являлась венозная кровь. Забор крови проводился у пациентов утром натощак в количестве 5 мл в пробирки Vacuum Tube EDTA.K3 (цельная кровь). Исследование крови осуществлялось в течение 2-х часов после забора. Изучение клеточных факторов иммунной системы проводилось с использованием проточного цитофлуориметра BD FACSCanto II (Becton Dickinson, США) после автоматизированной пробоподготовки цельной крови с помощью станции автоматической пробоподготовки BD FACS Sample Prep Assistant II (Becton Dickinson, США) в соответствии с инструкцией по применению приборов и моноклональных антител и включало типовое фенотипирование лимфоцитов крови, а также исследование субпопуляционного состава и функциональной активности CD56+ клеток в крови.
При типовом фенотипировании лимфоцитов использовался стандартизированный комплект моноклональных антител (МКАТ) BD Multitest 6-Color TBNK Reagent (BD Biosciences), содержащий меченные PerCP-Су5.5 anti-CD45 МКАТ, меченные FITC anti-CD3 МКАТ, меченные PE-Су7 anti-CD4 МКАТ, меченные АРС-Су7 anti-CD8 МКАТ, меченные АРС anti-CD19 МКАТ, меченные РЕ anti-CD 16/anti-CD56 МКАТ. При этом регистрировались следующие показатели: абсолютное и относительное число CD3+ клеток; абсолютное и относительное число CD3+/CD4+/CD8+ клеток; абсолютное и относительное число CD3+/CD4+ клеток; абсолютное и относительное число CD3+/CD8+ клеток; иммунорегуляторный индекс (ИРИ); абсолютное и относительное число CD3+/CD16+/CD56+ клеток (ЕКТ); абсолютное и относительное число CD19+клеток; абсолютное и относительное число CD3-/CD16+/CD56+ клеток (ЕК).
Для ЕКТ определялась доля отдельных субпопуляций среди общего числа ЕКТ с использованием комплекта МКАТ BD Multitest 6-Color TBNK Reagent (BD Biosciences): относительное число CD3+/CD56+/CD4+ клеток; относительное число CD3+/CD56+/CD8+ клеток; относительное число CD3+/CD56+/CD8-/CD4- (DN) клеток. Для естественных киллеров проводился расчет доли двух субпопуляций среди ЕК крови: CD56bright и CD56dim на основе гистограмм по пикам «яркого» и «тусклого» свечения проб с меченными РЕ-Су5 anti-CD56 МКАТ (IOTest, Beckman Coulter).
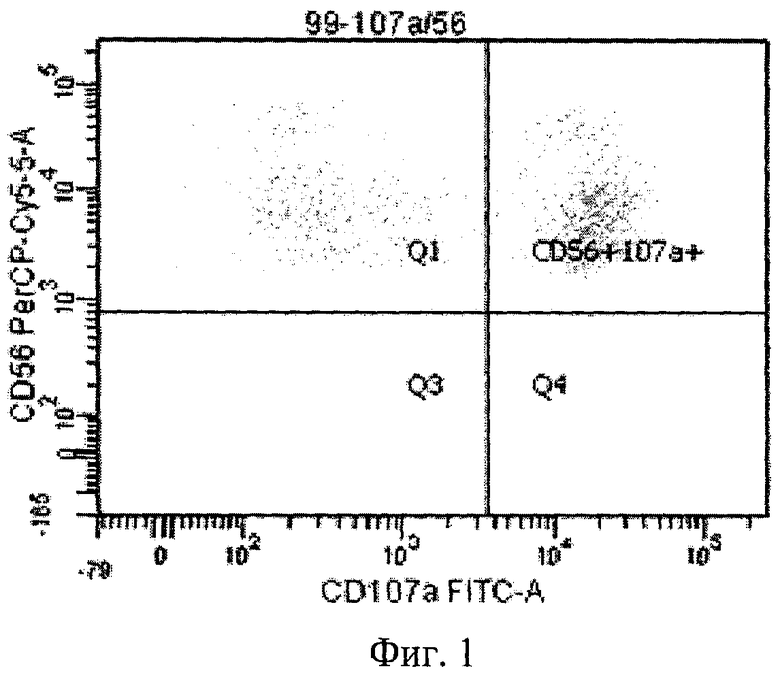
Для анализа функциональной активности CD56+ клеток регистрировались уровни экспрессии на их мембране таких маркеров, как: 1) киллингингибирующих рецепторов (KIR) из суперсемейства иммуноглобулинов (CD158a,h); 2) ингибирующих рецепторов суперсемейства лектинов С-типа (CD94); 3) активирующих рецепторов суперсемейства пектинов С-типа (NKG2D); 4) гликопротеидов, ассоциированных с мембраной лизосом и отражающих состояние гранулярного аппарата клетки (CD107a); 5) рецепторов естественной цитотоксичности (NKp46); 6) CD16 - рецепторов, опосредующих механизм антителозависимой цитотоксичности (АЗКЦТ). Определение относительного количества CD56+/CD158a,h, CD56+/CD94+, CD56+/NKG2D+, CD56+/NKp46+, CD56+/CD16+ клеток (от всех CD56+ клеток) проводилось в раздельной пробе крови; в каждом случае использовался комплект из двух моноклональных антител: меченные РЕ-Су5 anti-CD56 MKAT (IOTest, Beckman Coulter) и меченные РЕ anti-CD158a,h МКАТ (IOTest, Beckman Coulter); меченные РЕ-Су5 anti-CD56 MKAT (IOTest, Beckman Coulter) и меченные РЕ anti-CD94 MKAT (Immunotech); меченные РЕ-Су5 anti-CD56 MKAT (IOTest, Beckman Coulter) и меченные РЕ anti-NKG2D MKAT (IOTest, Beckman Coulter); меченные FITC anti-NKp46 MKAT (BD Biosciences) и меченные РЕ-Су5 anti-CD56 MKAT (IOTest, Beckman Coulter); меченные FITC anti-CD 16 MKAT (IOTest, Beckman Coulter) и меченные РЕ-Су5 anti-CD56 MKAT (IOTest, Beckman Coulter). Для регистрации CD56+ клеток, несущих маркер CD107a, производилось внутриклеточное определение данного рецептора с использованием пермобилизирующих компонентов фирмы Beckman Coulter и комплекта из двух моноклональных антител: меченных FITC anti-CD107a MKAT (BD Biosciences) и меченные PerCP-Су5-5 anti-CD56 MKAT (BD Biosciences) (фиг.1).
Для статистической обработки данных применялись методы непараметрической статистики с использованием критериев Манна-Уитни и Колмагорова-Смирнова (данные не давали нормального распределения). На основании полученных лабораторных данных проводился дискриминантный анализ, который использовался для отбора наиболее информативных критериальных значений. Статистическая обработка данных проводилась при помощи пакета статистических программ SPSS 17.0 (допустимая ошибка Е=5%).
После тестирования клеточного состава в каждой подгруппе по стадиям фиброза печени с помощью статистического сопоставления средних величин, диапазонов значений показателей (минимум-максимум), дискриминантного анализа определялся набор наиболее информативных показателей и выявлялись диапазоны их значений соответственно каждой стадии фиброзных изменений в печени.
Было установлено, что в набор информативных показателей вошли только 6 параметров, характеризующих по фенотипу субпопуляционный состав и функциональное состояние CD56+ клеток. Диапазоны значений шести информативных показателей в соответствии со стадией фиброза печени у больных ХВГС и в контрольной группе представлены в таблице 1.
На первой и второй стадиях фиброзных изменений в печени при ХВГС отклонения диапазонов значений информативных показателей от показателей предыдущей стадии или показателей здоровых людей не были уникальными, в то время как переход со второй на третью стадию фиброза печени сопровождался характерным сдвигом диапазонов значений всех 6 информативных показателей у всех без исключения больных ХВГС. Этот факт является прогностически очень важным, так как третья стадия - это этап предцирротических изменений в печени, когда с помощью расширения спектра лечебных мероприятий еще можно повлиять на интенсивность прогрессирования заболевания и отсрочить формирование цирроза печени.
При переходе с третьей стадии фиброза в цирроз печени у больных ХВГС набор информативных показателей опять меняет диапазон значений в 72,7-100% случаев, что позволяет констатировать переход в цирроз печени.
Контроль специфичности отобранных критериев для стадии 3 фиброза печени и стадии цирроза у больных ХВГС проводился путем сравнения полученных результатов по отобранным признакам в группах сопоставления - у здоровых людей и у больных хроническим вирусным гепатитом В. Сводные данные по диагностической значимости отобранных критериальных признаков на третьей стадии фиброзных изменений представлены в таблице 2, на четвертой стадии в таблице 3 и в целом - на чертежах (фиг.2-7).
Можно констатировать, что на третьей стадии фиброзных изменений печени (предцирротической) из 6 установленных критериальных признаков в наших исследованиях у всех больных ХВГС регистрировались все 6 признаков. Ни при ХВГВ, ни у здоровых людей более 3-х признаков ни разу отмечено не было. Таким образом, в процессе мониторинга крови больного при наличии шести признаков из шести отобранных критериев у больного ХВГС можно определить третью стадию фиброза печени, которая служит для него прогностическим критерием угрозы перехода хронического вирусного гепатита С в цирроз печени.
Что касается развития цирроза печени на фоне ХВГС, то наличие 5 из 6 отобранных нами критериальных признаков позволяет поставить диагноз цирроза печени, но этот результат неспецифичен для ХВГС, поскольку может регистрироваться при циррозе печени другой этиологии (алкогольном, на фоне ХВГВ). Обозначенные критерии приобретают выраженное диагностическое значение только при иммунологическом мониторинге больных, когда изменения критериальных признаков, характерных для стадии фиброза 3, меняют диапазон значений на таковой, присущий стадии 4. Поскольку в наших исследованиях диапазоны значений показателей, характерные для стадии 4, ни разу не были зарегистрированы на стадии 3, то такое изменение диапазона значений позволяет констатировать цирроз печени на фоне хронического вирусного гепатита С.
Таким образом, использование для мониторинга больных набора критериальных признаков, характеризующих субпопуляционный состав ЕКТ и функциональное состояние CD56+ клеток крови по их фенотипу и в определенных диапазонах значений, позволяет четко и специфично для ХВГС установить стадию предцирротических изменений в печени и прогнозировать угрозу развития цирроза печени, отнеся больного в группу риска, а также определить переход заболевания на стадию цирроза печени.
Способ иллюстрируется следующими чертежами.
Фиг.1. Определение относительного количества CD56+/CD107a+ клеток крови методом проточной цитофлуориметрии.
Фиг.2. Диапазон индивидуальных значений процентного содержания CD3+/CD56+ клеток в крови больных ХВГС в динамике, больных ХВГВ на стадии цирроза и алкогольным циррозом.
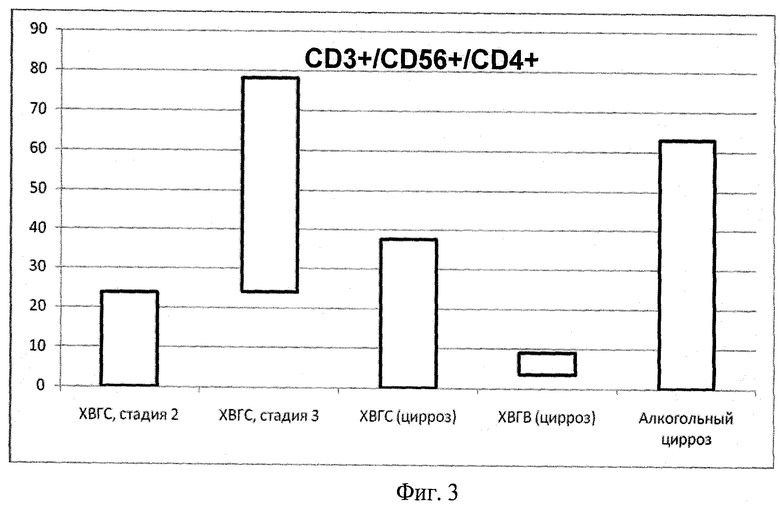
Фиг.3. Диапазон индивидуальных значений процентного содержания CD3+/CD56+/CD4+ ЕКТ в крови больных ХВГС в динамике, больных ХВГВ на стадии цирроза и больных алкогольным циррозом.
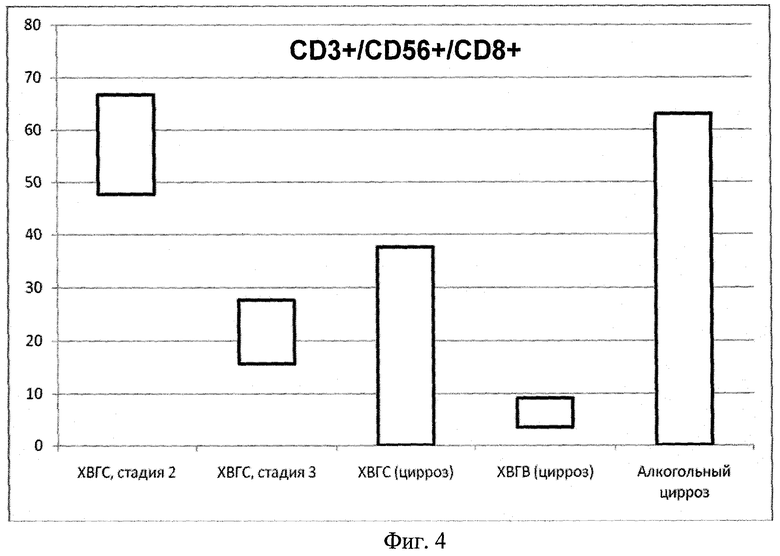
Фиг.4. Диапазон индивидуальных значений процентного содержания CD3+/CD56+/CD8+ ЕКТ в крови больных ХВГС в динамике, больных ХВГВ на стадии цирроза и больных алкогольным циррозом.
Фиг.5. Диапазон индивидуальных значений процентного содержания CD56+/CD94+ клеток в крови больных ХВГС в динамике, больных ХВГВ на стадии цирроза и больных алкогольным циррозом.
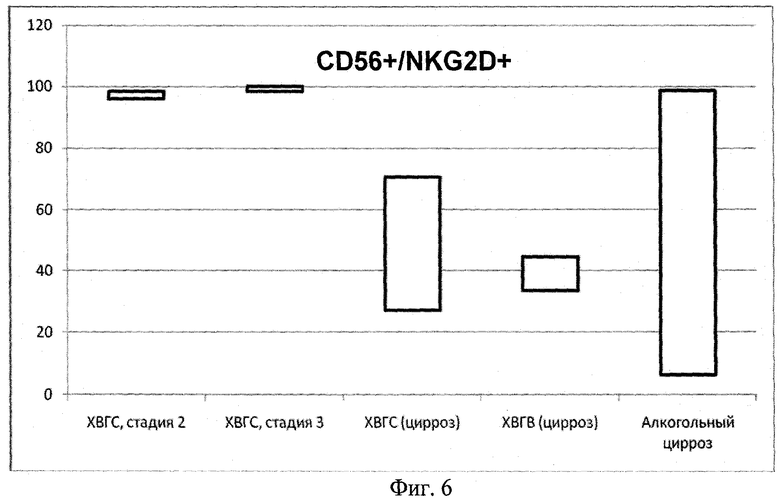
Фиг.6. Диапазон индивидуальных значений процентного содержания CD56+/NKG2D+ клеток в крови больных ХВГС в динамике, больных ХВГВ на стадии цирроза и больных алкогольным циррозом.
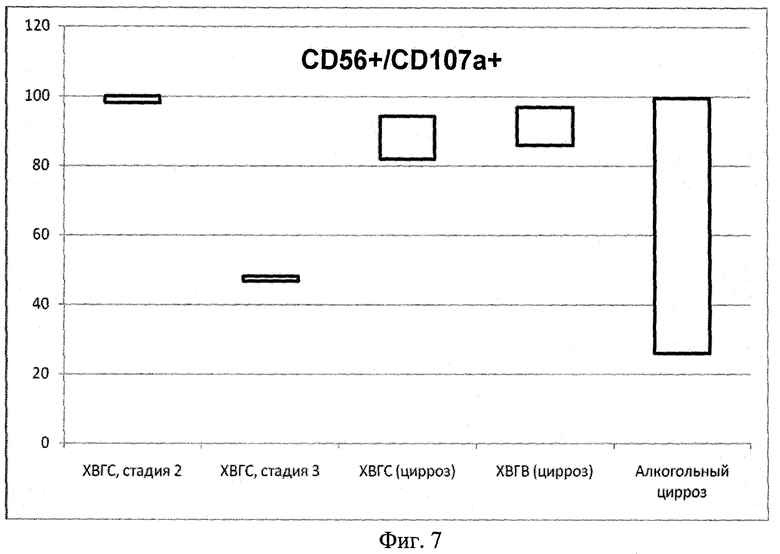
Фиг.7. Диапазон индивидуальных значений процентного содержания CD56+/CD107a+ клеток в крови больных ХВГС в динамике, больных ХВГВ на стадии цирроза и больных алкогольным циррозом.
Способ подтверждается следующими клиническими примерами.
Пример 1. Больной В., 51 год, наблюдается амбулаторно в гепатологическом центре при Инфекционной клинической больнице №1 с диагнозом: «Хронический вирусный гепатит С, умеренная активность, тяжелый фиброз. Сопутствующий диагноз: хронический простатит, гипертоническая болезнь».
Из анамнеза известно, что впервые гиперферментемия выявлена в 1998 году. Антитела к вирусу гепатита С обнаружены в 2002 году. Противовирусную терапию не получал. В декабре 2008 года впервые произведена пункционная биопсия печени, при гистологическом исследовании которой был выявлен фиброз печени стадии 3 по шкале METAVIR.
Проходил всестороннее обследование в феврале 2009 года. При физикальном осмотре обращало на себя внимание увеличение печени, которая пальпировалась на 1 см ниже края реберной дуги, в остальном без особенностей. Общий анализ крови: эритроциты - 5,77·1012/л; гемоглобин - 186 г/л; гематокрит - 52,4%; тромбоциты - 126·109/л; лейкоциты - 7,4·109/л; моноциты - 5% (0,37·109/л); гранулоциты - 73,9% (5,47·109/л); лимфоциты - 21,1% (1,56·109/л). Биохимический анализ крови: общий белок - 71 г/л; альбумины - 62,2%; альфа1-глобулины - 3,2%; альфа2-глобулины - 10,8%; бета-глобулины - 9,4%; гамма-глобулины - 14,4%; аспартатаминотрансфераза - 99 ME; аланинаминотрансфераза - 67 ME.
Критериальные иммунологические параметры: CD3+/CD56+ - 9,6%; CD3+/CD56+/CD4+ - 24%; CD3+/CD56+/CD8+ - 27,7%; CD56+/CD94+ - 31,6%; CD56+/NKG2D+ - 99,1%; CD56+/CD107a+ - 46,6%.
Таким образом, у больного определено соответствие величин всех 6 критериальных параметров таковым для стадии 3, что полностью совпадает с данными гистологических исследований и позволяет отнести больного в группу риска по развитию цирроза печени.
Пример 2. Больной Ч., 59 лет, находится на учете в консультативном гепатологическом центре при Инфекционной клинической больнице №1 с диагнозом: «Хронический вирусный гепатит С, цирроз печени, портальная гипертензия. Сопутствующий диагноз: коксартроз, гипертоническая болезнь».
Из анамнеза известно, что впервые антитела к вирусу гепатита С и РНК ВГС выявлены в 1995 году при плановом обследовании. В 1996 году получал интерфероновую терапию в течение года без эффекта. В 1995 году впервые была произведена пункционная биопсия печени, гистологическая картина биоптата соответствовала хроническому гепатиту умеренной активности, с формированием цирроза печени. В 2000 году была сделана повторная биопсия печени, в результате которой был выявлен гепатит умеренной активности, тяжелый фиброз (формирование монолобулярного цирроза печени).
Результаты последних инструментальных исследований: эзофагогастродуоденоскопия (27.05.2009) - расширение варикозных вен пищевода 1-я стадия; ультразвуковое исследование органов брюшной полости (09.06.2009) - печень: контур четкий, неровный, местами волнистый; размеры печени увеличены: левая доля - 126 мм, толщина - 52 мм, хвостатая доля - 25 мм, правая доля - 170 мм, толщина - 89 мм; эхогенность незначительно повышена; сосудистый рисунок обеднен умеренно; структура паренхимы неоднородная, определяются цирротические изменения; внутрипеченочные протоки не расширены; воротная вена 13,5 мм; желчный пузырь увеличен, обнаруживается полип стенки 4×5 мм; холедох 5 мм; поджелудочная железа - диффузные изменения; селезенка не увеличена, селезеночная вена не расширена - 8,2 мм; свободной жидкости в брюшной полости нет. Биохимический анализ крови (30.04.2009): общий белок - 88 г/л; альбумины - 41,8%; альфа1 - глобулины - 3%; альфа2-глобулины - 14,5%; бета-глобулины - 13,5%; гамма-глобулины - 27,3%.
В июне 2009 года пациент Ч. дал согласие на участие в исследованиях. При физикальном обследовании обращает на себя внимание увеличение печени, которая выступает из-под реберной дуги на 2 см, в остальном без особенностей. Общий анализ крови: эритроциты - 4,06·1012/л; гемоглобин - 132 г/л; гематокрит - 37,1%; тромбоциты - 117·109/л; лейкоциты - 4,3·109/л; моноциты - 8,1% (0,35·109/л); гранулоциты - 58% (2,5·109/л); лимфоциты - 33,9% (1,46·109/л). Биохимический анализ крови: аспартатаминотрансфераза - 301 ME; аланинаминотрансфераза - 275 ME; биллирубин общий - 16 мкмоль/л; биллирубин прямой - 4 мкмоль/л; билирубин непрямой - 12 мкмоль/л.
Критериальные иммунологические параметры: CD3+/CD56+ - 0,4%; CD3+/CD56+/CD4+ - 44,4%; CD3+/CD56+/CD8+ - 55,6%; CD56+/CD94+ - 52,1%; CD56+/NKG2D+ - 98,1%; CD56+/CD107a+ - 82%.
Таким образом, по результатам исследования критериальных иммунологических параметров определено 5 признаков из 6, характерных для цирроза печени, что соответствует диагнозу и другим клинико-лабораторным признакам цирроза печени у данного больного.
Пример 3. Больной К., 52 года, находится на учете в гепатологическом центре при Инфекционной клинической больнице №1 с 2000 года с диагнозом: «Хронический вирусный гепатит С. Сопутствующий диагноз: тиреотоксикоз, язвенная болезнь желудка».
Из анамнеза известно, что в 1992 году впервые обследован на HBsAg при отрицательном результате, биохимический анализ крови - норма. В этом же году проходил лечение в стационаре с диагнозом: «Диффузный токсический зоб III стадии», где была проведена субтотальная резекция щитовидной железы. В 1993 году впервые отмечено повышение аланинаминотрансферазы, был поставлен диагноз - токсический гепатит. В 1998 году впервые обследован на антитела к ВГС, результат положительный. В этом же году был проведен курс терапии Интроном А 3 млн.ед. 3 раза в неделю, 6 месяцев. После лечения сохранялась гиперферментимия до 90 ME. Повторные курсы этиотропной терапии не проводились ввиду тяжелой сопутствующей патологии. В 2001 году впервые была произведена пункционная биопсия печени, в результате которой был определена 1 стадия фиброза по METAVIR. Повторная биопсия печени была сделана в декабре 2007 года, по результатам которой также выявлена 1 стадия фиброза по METAVIR (биоптат просмотрен дважды в двух независимых лабораториях).
Ввиду того что постоянно стоял вопрос о проведении повторного курса этиотропной терапии, в октябре 2007 года пациент был обследован методом непрямой транзиентной эластографии печени на приборе «FibroScan», который показал результат, соответствующий 3 стадии фиброзных изменений печени по METAVIR. Также в декабре 2008 года больному было предложено провести исследование венозной крови на специфические маркеры повреждения ткани печени. Результат FibroTest показал 4 стадию фиброза печени, a ActiTest выявил третью степень активности некрозовоспалительного процесса в ткани печени.
Определение вирусной нагрузки (13.01.2009): РНК ВГС - 3,1·106 МЕ/мл, 1,2·107 копий/мл. Генотип 1b. Ультразвуковое исследование органов брюшной полости (22.01.2009): увеличение размеров печени (+0,4; +0,7), диффузные изменения. Эластогастродуоденоскопия (26.01.2009): расширение варикозных вен пищевода 1 стадии. Исследование гуморального иммунитета (13.01.2009): ревматоидный фактор - отрицательно; С3 коплемента - 174 мг/дл; С4 комплемента - 31 мг/дл; IgA - 2,59 г/л; IgG - 18 г/л; IgM - 0,8 г/л. В конце января 2009 года пациент К. дал согласие на участие в исследованиях. Пациент не вошел в анализированную группу ввиду тяжелой сопутствующей патологии и неоднозначности результатов определения степени фиброза печени. Общий анализ крови: эритроциты - 4,78·1012/л; гемоглобин - 157 г/л; гематокрит - 43,5%; тромбоциты - 207·109/л; лейкоциты - 5,8·109/л; моноциты - 6,8% (0,39·109/л); гранулоциты - 55,3% (3,21·109/л); лимфоциты - 37,9% (2,2·109/л). Биохимический анализ крови: общий белок - 70 г/л; альбумины - 61,8%; альфа1-глобулины - 2,6%; альфа2-глобулины - 9,4%; бета-глобулины - 8,8%; гамма-глобулины - 17,4%; аспартатаминотрансфераза - 45 ME; аланинаминотрансфераза - 86 ME; коэффициент 0,5; биллирубин менее 9 мкмоль/л; α-фетопротеин - 3,02.
Критериальные иммунологические параметры: CD3+/CD56+ - 3,7%; CD3+/CD56+/CD4+ - 0%; CD3+/CD56+/CD8+ - 56,9%; CD56+/CD94+ - 65,1%; CD56+/NKG2D+ - 98,4%; CD56+/CD107a+ - 98,2%.
Таким образом, на основании пункционной биопсии, выполненной 2 года назад, была определена стадия фиброза 1, уже на следующий год инструментальные методы исследования позволили выявить стадию фиброза 3, а биохимические (FibroTest) - стадию 4. Такая противоречивость данных создала трудности диагностики в связи с низкой вероятностью сочетания результатов, полученных разными методами. Еще через год на момент иммунологического обследования у больного были зарегистрированы некоторые признаки начинающегося цирроза печени, в частности расширение варикозных вен пищевода. Исследование, выполненное с определением иммунологических критериев, позволяет констатировать стадию цирроза печени (4) по 6 признакам. Иными словами, пункционная биопсия показала неточный результат, в то время как иммунологическое исследование дало более достоверную информацию, поскольку она сочеталась с результатами других (непункционных) методов исследования.
Данный способ позволяет выявлять четкое соответствие иммунологических сдвигов в крови третьей и четвертой стадии фиброзных изменений в печени. Кроме того, способ позволяет определять выраженные фиброзные изменения в печени по концентрациям цитокинов в сыворотке крови и регистрировать предцирротическую и цирротическую стадию фиброза в печени по содержанию в крови лимфоцитов определенного фенотипа как способа прогнозирования реальной угрозы цирроза печени.
В таблице 1 представлен диапазон значений информативных показателей CD56+ клеток в контроле и у больных ХВГС на разных стадиях фиброза печени.
В таблице 2 представлена сводная таблица сведений по способам иммунологической индикации стадии фиброза 3 у больных хроническим гепатитом С
При ХВГС, 2 стадия: 0 признаков - 100%
При ХВГС, 4 стадия: 0 признаков - 100%
При ХВГВ:
В таблице 3 представлена сводная таблица сведений по способам иммунологической индикации стадии фиброза 4 у больных хроническим гепатитом С.
При ХВГС, 3 стадия: 0 признаков - 100% При ХВГВ, 4 стадия:
Литература
1. Шаханина И.Л., Радуто О.И. Вирусные гепатиты в России: официальная статистика и экономические потери // Вакцинация. Вирусные гепатиты. - 2001. - Т.6. - №18.
2. Lang К., Weiner D.B. Immunotherapy for HCV infection: next steps // Expert Rev. Vaccines. - 2008. - Vol.7. - №7. - P.915-923.
3. Майер К.-П. Гепатит и последствия гепатита. М.: ГЭОТАР-МЕД. - 2004. - 720 С.
4. Leftkowich J.H. Liver biopsy assessment in chronic hepatitis // Arch. Med. Res. - 2007. - Vol.38. - №6. - P.634-643.
5. Mysorekar V.V., Rao S.G., Mahadeva K.C. Liver histology in patients on hemodialysis with chronic hepatitis С viral infection // Indian. J. Pathol. Microbiol. - 2008. - Vol.51. - №2. - P.182-185.
6. Yeshua H., Oren R. Non invasive assessment of liver fibrosis // Ann. Transplant. - 2008. - Vol.13. - №2. - P.5-11.
7. Bode J.G., Brenndorfer E.D., Haussinger D. Hepatitis С virus (HCV) employs multiple strategies to subvert the host innate antiviral response // Biol. Chem. - 2008. - Vol.389. - №10. - P.1283-1298.
8. Chang K.M. Immunopathogenesis of hepatitis С virus infection // Clin. Liver Dis. - 2003. - Vol.7. - №1. - P.89-105.
9. Kanto Т. Virus associated innate immunity in liver // Front. Biosci. - 2008. - Vol.13. - P.6183-6192.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ СТАДИИ ФИБРОЗА ПЕЧЕНИ У ПАЦИЕНТОВ С ХРОНИЧЕСКИМ ВИРУСНЫМ ГЕПАТИТОМ С | 2019 |
|
RU2709507C1 |
| СПОСОБ ДИАГНОСТИКИ ФИБРОЗА ПЕЧЕНИ ПРИ ХРОНИЧЕСКОМ ВИРУСНОМ ГЕПАТИТЕ С | 2014 |
|
RU2557927C1 |
| Способ диагностики цирроза печени (стадии F4) в исходе хронического вирусного гепатита С | 2019 |
|
RU2724595C1 |
| СПОСОБ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ СТАДИИ ФИБРОЗА ПЕЧЕНИ ПРИ ХРОНИЧЕСКОМ ВИРУСНОМ ГЕПАТИТЕ С | 2015 |
|
RU2583939C1 |
| Способ прогнозирования формирования цирроза печени микст (ВГС+алкоголь) этиологии | 2016 |
|
RU2618418C1 |
| Способ диагностики выраженного фиброза печени у больных хроническим гепатитом С с 1 генотипом | 2017 |
|
RU2639480C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ БЫСТРОГО ВИРУСОЛОГИЧЕСКОГО ОТВЕТА У БОЛЬНЫХ ХРОНИЧЕСКИМ ГЕПАТИТОМ С | 2013 |
|
RU2563812C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ПРОТИВОВИРУСНОЙ ТЕРАПИИ У ВЗРОСЛЫХ БОЛЬНЫХ ХРОНИЧЕСКИМ ГЕПАТИТОМ С С ГЕНОТИПОМ 1b | 2012 |
|
RU2522500C1 |
| Способ прогноза отсутствия регресса фиброза печени у больных хроническим гепатитом С | 2019 |
|
RU2723387C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ХРОНИЧЕСКИМ ВИРУСНЫМ ГЕПАТИТОМ С, ГЕНОТИПОМ 3а | 2009 |
|
RU2400229C1 |


Изобретение относится к области медицины, в частности гепатологии и инфекционным болезням. Способ оценки фиброза печени у больных хроническим вирусным гепатитом С, заключающийся в определении фенотипа СD56+лимфоцитов крови и по диапазону значений процентного содержания CD3+/CD56+, CD3+/CD56+/CD4+, CD3+/CD56+/CD8+, CD56+/CD94+, CD56+/NKG2D+, CD56+/CD107a+ клеток в крови устанавливают третью стадию фиброза (предцирротическую) или цирроз печени. Вышеописанный способ позволяет повысить точность диагностики фиброзных изменений печени. 7 ил., 3 табл.
Способ оценки фиброза печени у больных хроническим вирусным гепатитом С, включающий проведение исследований фенотипа CD56+лимфоцитов крови, отличающийся тем, что определяют процентное содержание CD3+/CD56+, CD3+/CD56+/CD4+, CD3+/CD56+/CD8+, CD56+/CD94+, CD56+/NKG2D+, СD56+/СD107а+клеток и при изменении содержания в крови СD3+/СD56+клеток выше 3,7%, CD3+/CD56+/CD4+клеток выше 23,8%, CD3+/CD56+/CD8+клеток ниже 47,6%, CD56+/CD94+ клеток ниже 46,7%, CD56+/NKG2D+ клеток выше 98,4%, и CD56+/CD107a+ клеток ниже 98,2% устанавливают наличие третьей стадии (предцирротической) фиброза печени, а изменение содержания в крови 5 из 6 параметров: CD3+/CD56+ клеток ниже 4,3%, CD3+/CD56+/CD4+ клеток ниже 24%, CD3+/CD56+/CD8+ клеток выше 27,7%, CD56+/CD94+ клеток ниже 31,6% или выше 41,6%, CD56+/NKG2D+ клеток ниже 98,5%, и CD56+/CD107a+ клеток выше 58,9% расценивают как переход заболевания в цирроз печени.
| СПОСОБ МОНИТОРИНГА ФИБРОЗА ПЕЧЕНИ У БОЛЬНЫХ ХРОНИЧЕСКИМ ГЕПАТИТОМ С (ХГС) | 2005 |
|
RU2309406C2 |
| СПОСОБ ПРОГНОЗА БЫСТРОГО ПРОГРЕССИРОВАНИЯ ЗАБОЛЕВАНИЯ У БОЛЬНЫХ ХРОНИЧЕСКИМ ГЕПАТИТОМ С | 2007 |
|
RU2354975C1 |
| Павлов Ч.С.и др | |||
| Современные возможности эластометрии, фибро- и акти-теста в диагностике фиброза печени// Российский журнал гастроэнтерологии, гепатологии, колопроктологии, 2008, том XVIII, №4, с.43-52. | |||
Авторы
Даты
2011-04-20—Публикация
2009-11-30—Подача