Область техники
Изобретение относится к применению известных производных индолов в качестве ингибиторов протеинкиназы С.
Предшествующий уровень техники
Протеинкиназа С (ПКС) или Ser/Thr-специфическая протеинкиназа - это общее название семейства родственных ферментов, которые осуществляют фосфорилирование по остаткам серина и треонина. Для активации протеинкиназы необходимы кальций и фосфолипиды (J. Biol. Chem. 1977. 252, 7603-7609; J. Biol. Chem. 1977. 252, 7610-7616). Дополнительная стимуляция ПКС происходит под действием диацилглицерина, который играет роль химического сигнала, активирующего ПКС in vivo (J. Biol. Chem. 1979. 254, 3692-3695; Nature. 1984, vol.308. P.693-698).
Протеинкиназа C экспрессируется практически во всех клетках млекопитающих и является одним из важнейших элементов клеточной системы передачи сигналов, экспрессии генов и регуляции дифференцировки и роста клеток. В настоящее время известно порядка двенадцати изозимов (изоферментов) ПКС, которые различаются по ферментативной специфичности, распределению в тканях, а также процессам регуляции.
Известно, что нарушения в функционировании сети сигнал-трансдуцирующих ферментов клетки, в которых участвуют серин-треониновые протеинкиназы, играют ключевую роль в развитии значительного числа болезней, включая воспалительные заболевания, диабет, расстройства центральной нервной системы, сердечно-сосудистые заболевания, различные виды опухолей, нарушения иммунитета, дерматологические заболевания.
Например, в работе Mulqueen M.J. с сотр. (Agents Actions. 1992 Sep; 37(l-2): 85-9) показано, что ингибиторы ПКС блокируют отрицательную регуляцию CD3 в Т-лимфоцитах. В работе Twomyy B. (Biochem Biophys Res Commun. 1990 Sep 28; 171(3): 1087-92) продемонстрировано, что ингибиторы ПКС оказывают влияние на окислительный выброс нейтрофилов. Следовательно, соединения, проявляющие свойства ингибиторов ПКС, могут быть применены в лечении воспаления.
Следствием ингибирования окислительного выброса нейтрофилов является тот факт, что ингибиторы ПКС также применимы в лечении сердечно-сосудистой ишемии, как показано в in vivo исследовании, проведенном на собаках, в работе Sonoki Н. (Kokyu То Junkan. 1989 Jun; 37(6): 669-74).
В исследовании Наrа Н. (J Cereb Blood Flow Metab. 1990 Sep; 10(5): 646-53), сделанном на крысиной модели ишемии, обнаружено, что ингибиторы протеинкиназы С предотвращают нейрональные повреждения, наблюдаемые при ишемическом инсульте.
В нескольких работах (Biochem Biophys Res Commun. 1989 Jan 16; 158(l): 105-9; Biochem Biophys Res Commun. 1990 Dec 31; 173(3): 976-81) было показано, что ингибиторы протеинкиназы С блокируют индуцируемую агонистами пролиферацию клеток гладких мышц, что позволяет рассматривать их как потенциальные терапевтические агенты для лечения сердечно-сосудистых заболеваний.
Много работ посвящено активности ПКС, связанной с пролиферацией, дифференциацией, апоптозом и ростом клеток, в том числе влиянием на рост опухолей, и применению при онкологических заболеваниях (например, Semin Oncol. 2006 Aug; 33(4): 466-78; Int J Cancer. 1989 May 15; 43(5): 851-6; Cancer Res. 1991 Sep 15; 51(18): 4888-92, и т.д.).
Было показано, что ингибиторы протеинкиназы С сокращают количество цитокинов, ингибируют активацию периферальных Т-клеток и пролиферацию кератиноцитов, тем самым оказывая положительный эффект на такие дерматологические расстройства, как контактный дерматит и псориаз (J Clin Invest. 2008 Sep; 118(9): 3151-9; Arch Dermatol Res. 1992; 284(3): 179-83, и Arch Dermatol Res. 1991; 283(7): 456-60).
Протеинкиназу С связывают также с различными аспектами диабета, в частности с диабетической ретинопатией, нефропатией и кардиоваскулярными заболеваниями (Pharmacol Res. 2007 Jun; 55(6): 498-510).
Известно, что протеинкиназа С, в том числе протеинкиназа С альфа, напрямую участвует в сигнальных каскадах, происходящих при астме. Количество ПКС повышено в гладкой мускулатуре дыхательных путей у больных астмой. При этом предполагается, что активация ПКС приводит к пролиферации клеток гладкой мускулатуры дыхательных путей и, как следствие, ремоделированию и повреждению тканей при астме (Experimental and Molecular Medicine, vol.39, №1, стр.97-105; Chin Med J 2008, 121(20): 2070-2076). Активация ПКС также является необходимым этапом в воспалительном каскаде лейкотриенового рецептора (JPET, 2008, 325(3), стр.1024-1030), принимающего активное участие в патологии астмы.
Таким образом, соединения, проявляющие свойства ингибиторов протеинкиназы С, применимы в лечении состояний, в которых протеинкиназа С так или иначе влияет на патологический процесс. Состояниями, для которых такое влияние подтверждено проведенными исследованиями, являются: воспалительные заболевания, сахарный диабет, астма, ишемия, сердечно-сосудистые заболевания, дерматологические заболевания.
Важнейшая роль ПКС в физиологии обуславливает растущий в настоящее время интерес к получению соединений, которые проявляют активность в качестве ингибиторов ПКС. Такие соединения, проявляя избирательное действие в отношении ПКС или ее изозимов, могут стать эффективными терапевтическими агентами. Однако наряду с эффективностью не менее важным условием для потенциального терапевтического агента является низкая токсичность.
Известен сильный ингибитор ПКС - стауроспорин, микробный индолкарбазол (Biochem. Biophys. Res. Commun. 135: 397-402 (1986); Biochem. Pharmacol. 40: 343-350 (1990)). Однако его использование ограничено в силу присущей данному соединению неприемлемой токсичности. Стауроспорин стал своего рода отправной точкой в синтезе ингибиторов протеинкиназ, и большинство дальнейших работ было направлено на то, чтобы создать близкий структурный аналог стауроспорина, обладающий меньшими токсическими свойствами. Примерами таких аналогов являются, в частности: сотрастаурин - международная заявка WO-00238561, цефалон - международная заявка WO-09721677, ингибиторы ПКС, описанные в международной заявке WO-09741127, ингибиторы ПКС, описанные в евразийском патенте 000598, патенте РФ 2191175.
К сожалению, большая часть потенциальных лекарственных средств, представляющих собой ингибиторы ПКС, не проходят даже вторую фазу клинических испытаний (Nat Rev Cancer. 2007 Jul; 7(7): 554-62). Поэтому, несмотря на многочисленные исследования, создание эффективных и низкотоксичных ингибиторов ПКС остается актуальной потребностью.
Задачей настоящего изобретения является расширение арсенала лекарственных средств, применимых в лечении состояний, в которых протеинкиназа С играет роль в патологии, в частности, связанных с воспалительными заболеваниями, астмой, ишемией, сердечно-сосудистыми заболеваниями, дерматологическими болезнями.
Данное изобретение относится к ингибиторам протеинкиназы С, имеющим структуру, принципиально отличную от структуры аналогов стауроспорина. Соединения данного изобретения являются, совершенно неожиданно, эффективными ингибиторами ПКС, а также изозима ПКС-альфа. Раскрытие изобретения
Техническим результатом настоящего изобретения является применение производных индолов, обладающих свойствами ингибиторов протеинкиназы С, для создания лекарственного средства для лечения состояний, в которых протеинкиназа С играет роль в патологии, в частности, связанных с воспалительными заболеваниями, ишемией, сердечно-сосудистыми заболеваниями, дерматологическими болезнями, что позволит расширить арсенал лекарственных средств для лечения указанных заболеваний. Производные индолов, предлагаемые в настоящем изобретении, обладают низкой токсичностью и хорошей переносимостью.
Указанный результат достигается применением производных индола для создания фармацевтической композиции, активным началом которой являются соединения общей формулы (I):
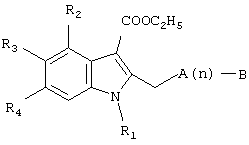
где R1 представляет собой заместитель, выбранный из необязательно замещенных алкила, оксиалкила или циклоалкила; необязательно замещенного гетероциклила или необязательно замещенного арила, при этом в качестве заместителей могут использоваться низший алкил, галоген, оксиалкил, гидроксигруппа, аминогруппа или несколько из перечисленных заместителей одновременно,
R2 - Н, -CH2N(R'R'')2, где R' и R'' независимо друг от друга представляют собой заместитель аминогруппы, выбранный из водорода или необязательно замещенного алкила,
R3 - алкоксигруппа или OH,
R4 - представляет собой заместитель, выбранный из водорода, галогена, цианогруппы, NO2-группы, трифторметила, необязательно замещенного арила или необязательно замещенного гетероциклила;
A - S, SO, SO2,
B - (CH2)k-R5, где R5 - необязательно замещенный арил, необязательно замещенный алкен, необязательно замещенный алкил или оксиалкил, необязательно замещенный гетероциклил;
n=0-1; k=0-2,
или гидраты и фармацевтически приемлемые соли соединения формулы I, обладающие активностью ингибиторов протеинкиназы С, а также фармацевтически приемлемый носитель и/или вспомогательное вещество. Данная фармацевтическая композиция может применяться для приготовления лекарственных препаратов в форме таблеток, гранул, капсул, суспензий, растворов или инъекций.
Упомянутые соединения, соответствующие формуле I, в том числе их синтез и физико-химические свойства, описаны в литературе (Химико-фармацевтический журнал, №1, 1995, с.51-53, Химико-фармацевтический журнал; №2; 1995, с.5-8, Химико-фармацевтический журнал, №1, 1998, с.565-569; Bioorg. Med. Chem., №14, 2006, стр.911-917), а также в международной заявке PCT/RU 2007/000246. Все конечные химические соединения по настоящему изобретению получены по способам, описанным в приведенной литературе, либо могут быть получены аналогичными способами, при этом данные способы известны обычным специалистам в области органической химии.
Наши предшествующие исследования показали, что соединения, описываемые формулой I, могут быть полезными при лечении вирусных заболеваний, таких как грипп A и B (патент РФ 2008004), атипичная пневмония (патент РФ №2256451), ротавирусная инфекция (патент РФ 2266742), диабет (патент РФ №2361581), астма (заявка РФ №2008147222).
Однако до настоящего времени не было известно о том, что соединения, соответствующие формуле I, проявляют активность в качестве ингибиторов протеинкиназы C, что впервые было показано авторами настоящего изобретения.
Наиболее предпочтительно использование в качестве активного компонента следующих соединений (химические формулы и краткие обозначения приведены в таблице 1 для удобства использования в дальнейшем тексте описания и формулы изобретения).
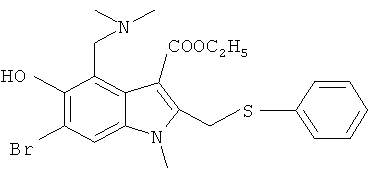
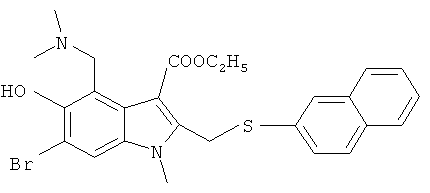
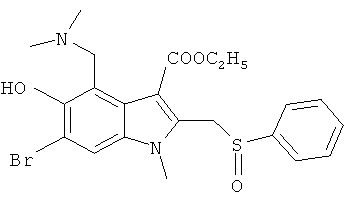
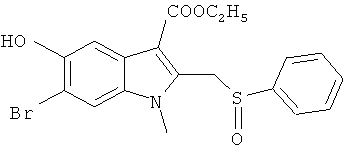
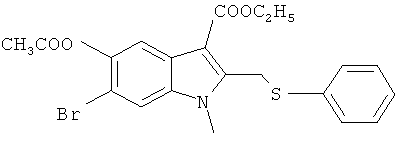
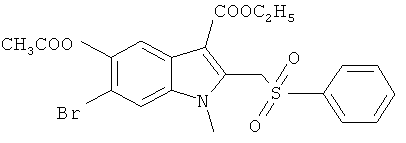
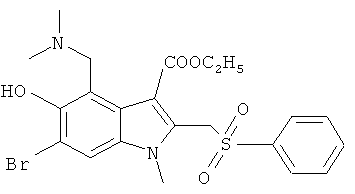
Мы изучили активность нескольких соединений на in vitro моделях.
Предлагаемые соединения ингибируют ПКС с величиной IC50 ниже 50 мкм. Кроме того, соединения данного изобретения селективно ингибируют альфа изозим протеинкиназы C и имеют величину IC50 относительно этого изозима ниже 10 мкм.
Еще одним вариантом данного изобретения является фармацевтическая готовая форма, содержащая соединение формулы I и один или несколько фармацевтически приемлемых носителей, разбавителей или наполнителей. Данные фармацевтические готовые формы готовят известными способами. Готовые композиции могут быть в форме таблеток, порошков, капсул, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей, растворов для инъекций.
Композиции данного изобретения могут быть приготовлены таким образом, чтобы обеспечивать быстрое или пролонгированное высвобождение активного ингредиента после введения пациенту. Композиции предпочтительно готовят в форме стандартной дозы, причем каждая доза содержит от ~50 до ~1000 мг, предпочтительно 100-500 мг активного ингредиента. Вводимая терапевтическая доза должна определяться врачом в зависимости от состояния, которое должно быть подвергнуто лечению, выбору вводимого соединения и избранного способа введения, поэтому указанный выше диапазон доз не предполагает ограничения объема данного изобретения. Кроме того, ингибиторы ПКС, как правило, взаимодействуют не только с ПКС, но и с другими компонентами клетки, что может сказываться на их суммарном эффекте.
Кроме указанных выше готовых форм, соединения данного изобретения можно вводить местно. Готовые формы для местного введения представляют собой мази, кремы и гели.
Обычное количество препарата для местного нанесения, которое должно быть нанесено на пораженную ткань, будет зависеть от размера пораженной ткани и концентрации соединения в препарате. Как правило, готовую форму наносят на пораженную ткань в количестве, доставляющем от ~0,05 до ~100 мг соединения на см2 пораженной ткани. Предпочтительно наносимое количество соединения должно находиться в диапазоне от ~1 до ~10 мг/см2.
Пример 1. Ингибирование протеинкиназы C (ПКС)
Соединения оценивали по их способности ингибировать протеинкиназу С согласно известным методикам (Biotechnology, 1990, №8, 732-735; Biochem J., 1993, 294: 335-337). Для этого в реакционный буфер (20 мМ Трис-HCl, pH=7,4; 10 мМ MgCl2, 0,1 мМ CaCl2; 8,7 мг/мл фосфатидилсерина, 5,9 мг/мл диацилглицерина) добавляли ПКС, исследуемое соединение (10 мкМ) и гистон H3 (370 мг/мл) и инкубировали 15 мин при 25°C. Затем добавляли в смесь [γ-32P]АТФ (10 мкМ) и инкубировали 15 мин при 25°C. Реакционную смесь наносили на фильтры, отмывали ортофосфорной кислотой (75 мМ), переносили в сцинцилляционные флаконы и определяли включение 32Р (имп/мин) на сцинцилляционном счетчике. Для каждой реакционной смеси рассчитывали процент ингибирования. Соединения анализировали в двух повторах. Полученные результаты суммированы в таблице 2.
Пример 2. Определение IC50 для ПКС
Для соединений, продемонстрировавших наиболее сильные ингибиторные свойства, определяли стандартный параметр IC50 - концентрацию вещества, при которой достигается 50% ингибирование фермента. Реакцию ингибирования проводили в условиях, аналогичных таковым в примере 1. Для анализа использовали концентрации в диапазоне от 0,03 до 100 мкМ. Полученные значения IC50 суммированы в таблице 3.
Пример 3. Ингибирование протеинкиназы Cα (ПКСα)
Кроме исследования ПКС, представляющей из себя смесь изоферментов, была проанализирована способность нескольких соединений этого класса ингибировать активность протеинкиназы Cα по известной методике (Biochem Biophys Res Comm., 1986, 135: 397-402). Для этого в реакционный буфер (20 мМ HEPES; 8 мМ MgCl2, 0,08 мМ CaCl2; 100 мкг/мл фосфатидилсерина, 20 мкг/мл диацилглицерина) добавляли ПКСα, исследуемое соединение и гистон (250 мг/мл) и инкубировали 15 мин при 25°C. Затем добавляли в смесь [γ-32P]АТФ (10 мкМ) и инкубировали 10 мин при 25°C. Реакционную смесь наносили на фильтры, отмывали ортофосфорной кислотой (75 мМ), переносили в сцинцилляционные флаконы и определяли включение 32P (имп/мин) на сцинцилляционном счетчике. Были получены следующие данные:
Приведенные выше примеры доказывают, что соединения по настоящему изобретению ингибируют активность протеинкиназы C, а также протеинкиназы Cα. С учетом известных из уровня техники закономерностей, можно ожидать, что такие соединения найдут применение при лечении связанных с протеинкиназой C заболеваний.
Настоящее изобретение относится к области медицины, а именно к новому применению известных производных индола для приготовления лекарственного средства, обладающего свойствами ингибитора протеинкиназы С. Предпочтительным производным индола является 1-метил-2-фенилтиометил-3-карбэтокси-4-диметиламинометил-5-окси-6-броминдола гидрохлорид. Указанные соединения являются эффективными ингибиторами протеинкиназы С, что позволяет использовать их при лечении воспалительных заболеваний, ишемии, сердечно-сосудистых заболеваний, дерматологических заболеваний, астмы, диабета. 2 з.п. ф-лы, 3 табл.
1. Применение замещенного индола общей формулы (I):

где R1 представляет собой замещенный или незамещенный алкил, оксиалкил, циклоалкил, гетероциклил или арил, при этом в качестве заместителей могут использоваться низший алкил, галоген, оксиалкил, гидроксигруппа, аминогруппа или несколько из перечисленных заместителей одновременно;
R2 - H, -CH2N(R'R")2, где R' и R" независимо друг от друга представляют собой заместитель, выбранный из водорода или необязательно замещенного алкила,
R3 - алкоксигруппа или ОН;
R4 - представляет собой заместитель, выбранный из водорода, галогена, цианогруппы, NO2-группы, трифторметила, необязательно замещенного арила или необязательно замещенного гетероциклила;
A - S, SO, SO2;
В - (CH2)k-R5, где R5 - необязательно замещенный арил, необязательно замещенный алкен, необязательно замещенный алкил или оксиалкил, необязательно замещенный гетероциклил;
n=0-1; k=0-2,
или его гидратов и/или фармацевтически приемлемых солей для приготовления лекарственного средства, обладающего свойствами ингибитора протеинкиназы С.
2. Применение по п.1, отличающееся тем, что в качестве замещенного индола используется 1-метил-2-фенилтиометил-3-карбэтокси-4-диметиламинометил-5-окси-6-броминдола гидрохлорид.
3. Применение по п.1, отличающееся тем, что замещенный индол используют для приготовления лекарственного средства, предназначенного для лечения заболевания, выбранного из группы: воспалительное заболевание, дерматологическое заболевание, сердечно-сосудистое заболевание, диабет, ишемия, астма.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОДИАБЕТИЧЕСКОЙ, ГИПОЛИПИДЕМИЧЕСКОЙ, ГИПОГЛИКЕМИЧЕСКОЙ И ГИПОХОЛЕСТЕРИНЕМИЧЕСКОЙ АКТИВНОСТЬЮ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБЫ ЛЕЧЕНИЯ УКАЗАННЫХ ЗАБОЛЕВАНИЙ | 2007 |
|
RU2361581C2 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| ЗАМЕЩЕННЫЕ ЭФИРЫ 1Н-ИНДОЛ-3-КАРБОНОВОЙ КИСЛОТЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2006 |
|
RU2323210C9 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИНТЕРФЕРОНИНДУЦИРУЮЩЕЙ И ИММУНОМОДУЛИРУЮЩЕЙ (ИММУНОСТИМУЛИРУЮЩЕЙ) АКТИВНОСТЬЮ | 1987 |
|
RU2033157C1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2011-06-20—Публикация
2009-11-19—Подача