Изобретение относится к области медицины, а именно к группе лекарственных средств, обладающих интерфероногенным и иммуномодулирующим действием, и касается известного лекарственного средства арбидола.
В настоящее время уделяется много внимания поиску и изучению лекарственных средств, способных модулировать (стимулировать или подавлять) иммунные реакции организма-иммуномодуляторов.
Иммуностимуляторы повышают общую сопротивляемость организма, влияя на специфические иммунные реакции и неспецифические факторы защиты, в том числе на синтез эндогенного интерферона. Они находят применение для лечения заболеваний, в патогенезе которых важную роль играют нарушения иммунного статуса организма первичных и вторичных иммунодефицитных состояний, включая злокачественные новообразования, а также хронические и рецидивирующие вирусные инфекции [1]
Среди немногих синтетических химических препаратов, используемых в качестве иммуностимуляторов, наиболее активным и широко применяемым в медицинской практике является левамизол 2,3,5,6-тетрагидро-6-фенилимидазо-[2,1-b] -тиазола гидрохлорид [2] Первоначально этот препарат применялся в качестве противоглистного средства. Как иммуностимулятор левамизол используется в комплексной терапии различных заболеваний, связанных с иммунодефицитными состояниями. Известно применение левамизола при лечении тяжелых рецидивирующих форм герпесвирусной инфекции [3]
Левамизол, как и другие некоторые иммуномодуляторы, стимулирует синтез сыворотного интерферона в организме. Титры интерферона, синтезированного под действием левамизола, не превышают 80-160 ед/мл в культуре клеток; 160-320 ед/мл в сыворотке крови мышей и 40-80 ед/мл в сыворотке крови людей [4,5] Однако левамизол высоко токсичен и может вызвать различные побочные явления: головную боль, нарушения сна, повышение температуры, изменение вкусовых ощущений, диспепсические явления, обонятельные галлюцинации (изменение запахов), аллергические кожные реакции, уртикарию, гриппо-подобные и неврологические симптомы. Наиболее опасным побочным явлением, которое может иметь место при терапии левамизолом в качестве иммуностимулятора, является агранулоцитоз уменьшение нейтрофильных гранулоцитов ниже 25% Поэтому в процессе лечения левамизолом следует систематически проводить анализы крови.
Левамизол поставляет в СССР ВНР (производство химический завод Гедеон Рихтер А.О. Будапешт).
Цель изобретения лекарственное средство, обладающее выраженным интерфероногенным и иммуностимулирующим действием и не оказывающее нежелательных побочных эффектов.
Поставленная цель достигается применением 1-метил-2-фенилтиометил-3-карбэтокси-4-диметиламинометил-5-окси-6- броминдола гидрохлорида, моногидрата формулы (I) (условно арбидол)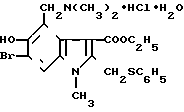 по новому назначению, а именно в качестве интерфероноиндуцирующего и иммуномодулирующего (иммуностимулирующего) средства.
по новому назначению, а именно в качестве интерфероноиндуцирующего и иммуномодулирующего (иммуностимулирующего) средства.
Арбидол прошел клиническое изучение и рекомендован ФК МЗ СССР к медицинскому применению в качестве лечебного средства при гриппе в виде таблеток для приема внутрь [6,7]
Арбидол не токсичен, хорошо переносится и не оказывает побочного действия как у здоровых, так и у больных гриппом людей.
Интерферониндуцирующая и иммуностимулирующая активность арбидола изучена в экспериментальных исследованиях на животных и частично на людях (на добровольцах в условиях клиники).
Изучение интерферониндуцирующей активности арбидола.
Изучено влияние арбидола на неспецифические факторы защиты, в частности на его способность индуцировать интерферон.
Изучение интерферониндуцирующей активности арбидола проведено в опытах in vitro (на первично-трипсинизированной культуре клеток фибробластов куриного эмбриона ФЭК), в опытах in vivo на 340 неинбредных белых мышах с массой тела 18-20 г и на 25 добровольцах (здоровые молодые люди обоего пола в возрасте от 18 до 30 лет).
С целью индуцирования интерферона в культуру клеток ФЭК вносили различные дозы арбидола с 2% ДЕАЕ dextran в соотношении 1:4 по 0,2 мл на пробирку с монослоем клеток. Инкубацию обработанных клеток проводили при 37оС в течение 1 ч. Затем клетки отмывали от препарата средой N 199 и заливали 1 мл среды N 199 без добавления сыворотки крови крупного рогатого скота. Через 8, 24 и 48 ч инкубирования при 37оС культуральную жидкость собирали и титровали на наличие интерферона в культуре клеток ФЭК с вирусом венесуэльского энцефаломиелита по общепринятой методике [8]
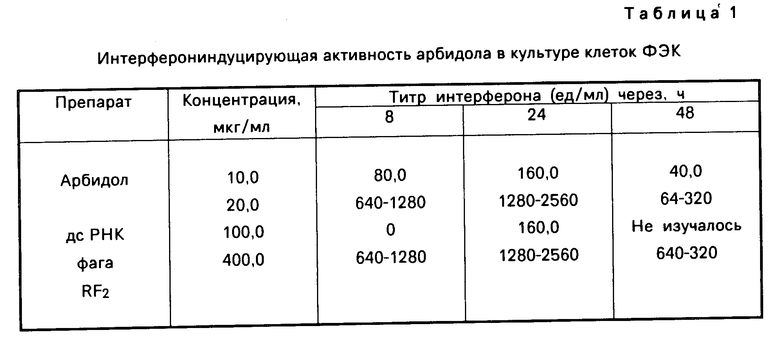
Результаты титрования представлены в табл.1.
В качестве стандартного препарата сравнения при изучении интерферониндуцирующей активности арбидола использован высокоактивный индуктор интерферона дс РНК фага RF2 (двуспиральная рибонуклеиновая кислота фага RF2) [4]
Результаты, представленные в табл.1, позволяют сделать вывод арбидол является высокоактивным индуктором интерферона в культуре клеток ФЭК. В концентрации 20 мкг/мл арбидол индуцирует интерферон уже через 8 ч (титр 640-1280 ед/мл, максимальный титр 2560 ед/мл определяется через 24 ч, к 48 ч титр интерферона снижается до 320 ед/мл).
Установлен дозозависимый эффект индукции интерферона в культуре клеток ФЭК под влиянием арбидола. Снижение концентрации арбидола в 2 раза (до 10 мкг/мл) приводит к уменьшению индукции интерферона примерно в 8 раз, однако динамика остается той же.
Сравнительное изучение индукции интерферона под влиянием арбидола и эталонного высокоактивного индуктора интерферона дс РНК фага RF2 выявило сходную динамику индукции и близкие титры интерферона, однако при этом дс РНК фага RF2 требовалось в 20 раз больше (400 мкг/мл), концентрация 100 мкг/мл вызывала слабую индукцию интерферона.
В следующей серии экспериментов изучена способность арбидола индуцировать интерферон в сыворотке крови экспериментальных животных.
Арбидол в дозах 250, 125 и 62,5 мг/кг вводили мышам per os однократно (3 группы мышей по 100 штук) и через 16, 24, 48 и 72 ч получали сыворотку крови, которую использовали для титрования интерферона в перевиваемой линии мышиных клеток L в отношении тест-вируса везикулярного стоматита. Кроме того, группе из 20 мышей арбидол был введен внутрибрюшинно (в/б) в дозе 10 мг/кг однократно и через 24 ч получена сыворотка крови, в которой также был определен титр интерферона.
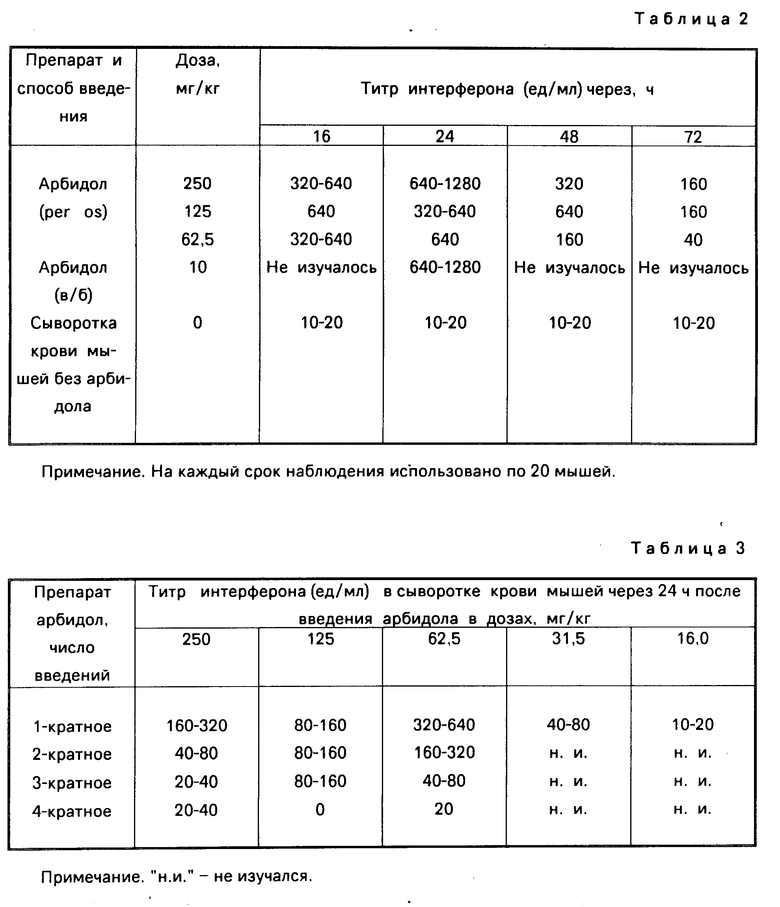
Результаты представлены в табл.2.
Результаты, представленные в табл. 2, свидетельствуют о том, что под влиянием арбидола, введенного per os, происходит индукция интерферона в сыворотке крови мышей. Эффект характеризуется дозозависимостью и наиболее выражен в диапазоне доз от 250 до 62,5 мг/кг массы тела животного. Высокие титры интерферона (640 ед/мл) выявляются в сыворотке крови мышей через 16 ч и наблюдаются до 48 ч. Арбидол стимулирует индукцию интерферона в сыворотке крови мышей также при внутрибрюшинном введении (см. табл.2).
При многократном введении арбидола мышам с целью индукции интерферона у мышей наступает состояние гипореактивности, которое выражается в снижении титров интерферона в сыворотке крови. Состояние гипореактивности характерное явление для индукторов интерферона [9] В табл.3 суммированы результаты опытов, проведенные на 400 мышах по изучению состояния гипореактивности после многократного введения арбидола.
На основании полученных данных (табл.3) можно заключить, что при многократном введении арбидола у мышей наступает состояние гипореактивности, которое выражается в снижении титров интерферона в сыворотке крови, особенно резком после 3-4-го последовательных введений препарата: с 320-640 до 20-0 ед/мл.
Арбидол как индуктор интерферона оказывает профилактическое действие при экспериментальных вирусных инфекциях. Профилактическую активность арбидола изучали при гриппозной пневмонии мышей, вызванной интраназальным заражением животных вирусом гриппа А/Бетезда/63 (H2N2), и при генерализованном герпесе мышей, вызванном интраназальным заражением их вирусом герпеса простого 1-го антигенного типа штамма Л2.
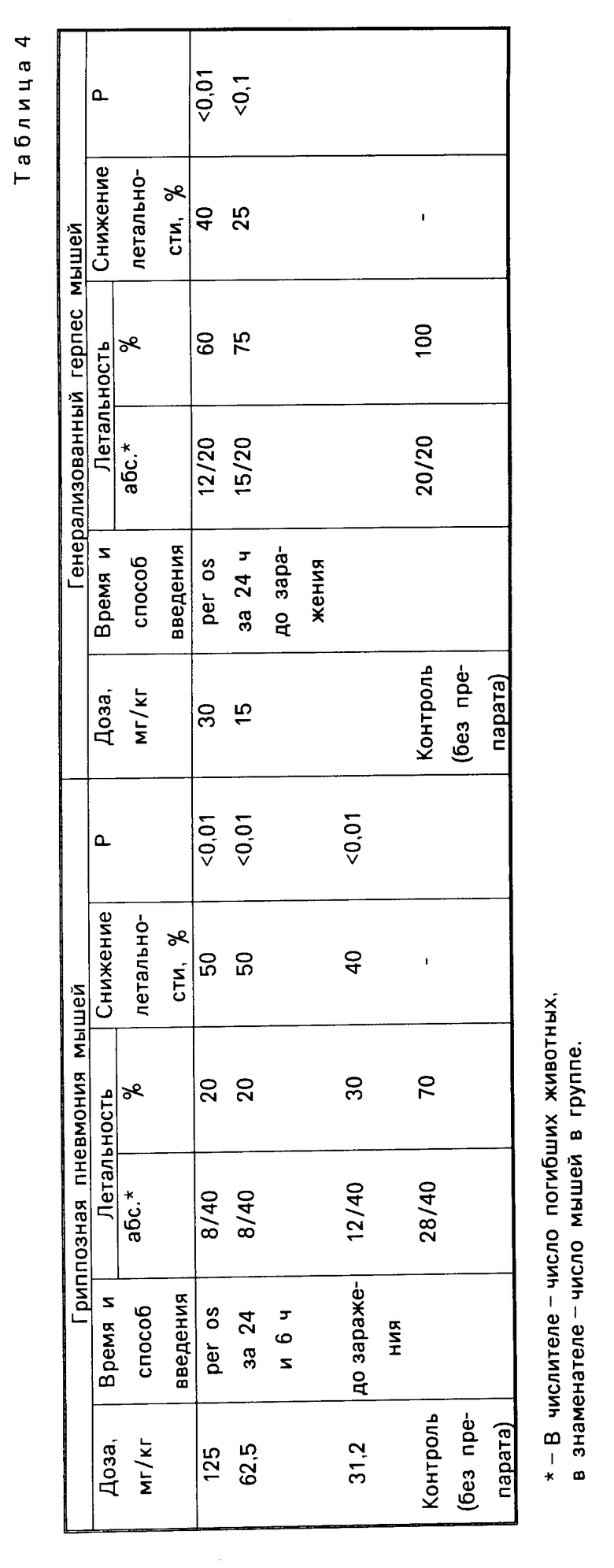
Результаты представлены в табл.4.
Арбидол при профилактическом введении за 24 и 6 ч до заражения per os в дозах от 31,2 до 125 мг/кг снижает гибель мышей от гриппозной пневмонии на 40-50% по сравнению с контролем. Введение арбидола в дозе 30 мг/кг per os однократно за 24 ч до заражения предохраняет от гибели 40% животных с генерализованной герпетической инфекцией.
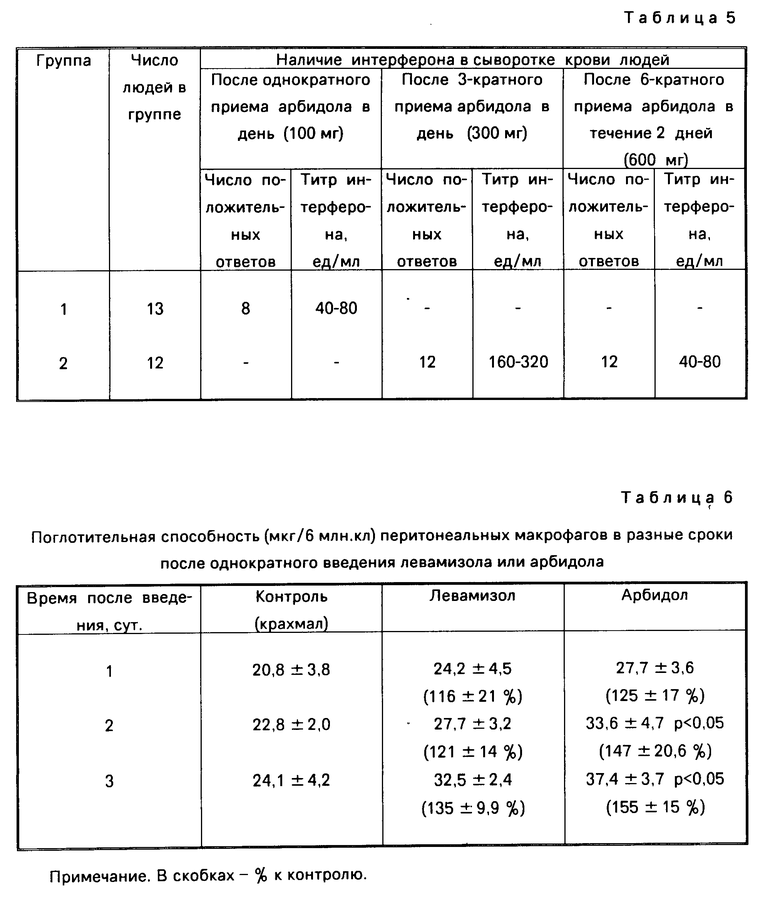
Интерферониндуцирующая активность арбидола изучена также у людей. Сыворотки крови людей, получавших per os таблетки арбидола (0,1 г) по различным схемам, исследовали на наличие сывороточного интерферона. Титрование сывороток проводили по общепринятой методике, используя культуру человеческих диплоидных клеток М-22, и тест-вирусом энцефаломиокардита мышей. Результаты представлены в табл.5.
Установлено, что однократный прием арбидола в дозе 100 мг per os вызывает индукцию сывороточного интерферона в титрах 40-80 ед/мл у 8 из 13 (61,5%) добровольцев.
3-кратный прием по 1 таблетке арбидола (300 мг) в течение дня приводил к резкому возрастанию индукции интерферона: интерферон определялся в сыворотке крови у всех 12 добровольцев (100%) в титрах, достигающих 160-320 ед/мл. При дальнейшем увеличении дозы до 600 мг в течение 2 дней (по 3 таблетки в день) наблюдалось резкое снижение индукции интерферона: титр интерферона в сыворотке крови не превышал 40-80 ед/мл.
Полученные результаты свидетельствуют о выраженной интерферониндуцирующей активности арбидола у людей при приеме его per os. Максимальное количество интерферона в сыворотке крови людей определяется после приема 300 мг арбидола (по 100 мг 3 раза в день). Увеличение дозы и длительности приема арбидола приводило к развитию у людей состояния гипореактивности, что характеризовалось резким снижением титров сывороточного интерферона.
Изучение иммуномодулирующей (иммуностимулирующей) активности арбидола.
Изучено влияние арбидола на функции системы иммунитета.
Функция фагоцитирующих клеток под влиянием арбидола изучена у половозрелых мышей-самок гибрида (CBA/C 57 BL6)F. Арбидол вводили per os в дозе 125 мг/кг однократно и в течение 5 дней по 1 разу в день. В качестве препарата сравнения был использован левамизол, который вводили по той же схеме в дозе 50 мкг/мышь. В разные сроки после введения препаратов у мышей выделяли перитонеальные макрофаги, поглотительную способность которых определяли по поглощению нейтрального красного и количественно определяли по калибровочной кривой спектрофотометрически при 530 нм.
Результаты представлены в табл.6.
Введение арбидола или левамизола не влияло на количество вымываемых из брюшной полости макрофагов, но стимулировало их поглотительную способность. Так, к 2-3 суткам после однократного введения поглотительная способность макрофагов у мышей, получавших арбидол, возрастала до 155% а у мышей, получавших левамизол, до 135% (p < 0,05).
После ежедневного введения препаратов в тех же дозах в течение 5 дней поглотительная способность макрофагов сохранялась на том же уровне 164 ± 13% (p < 0,05) и 13,8 ± 11% (p < 0,05) соответственно.
Таким образом, введение арбидола in vivo стимулирует поглотительную способность макрофагов в большей степени, чем введение левамизола.
Влияние арбидола на антителогенез изучено сравнительно с левамизолом и дс РНК F2. Использованы 2 линии мышей: CBA/C 57 BL6)F, а также животные-опухоленосители (карцинома молочной железы, привитая подкожно в бедро), интактные и облученные тотально 2 Гр.
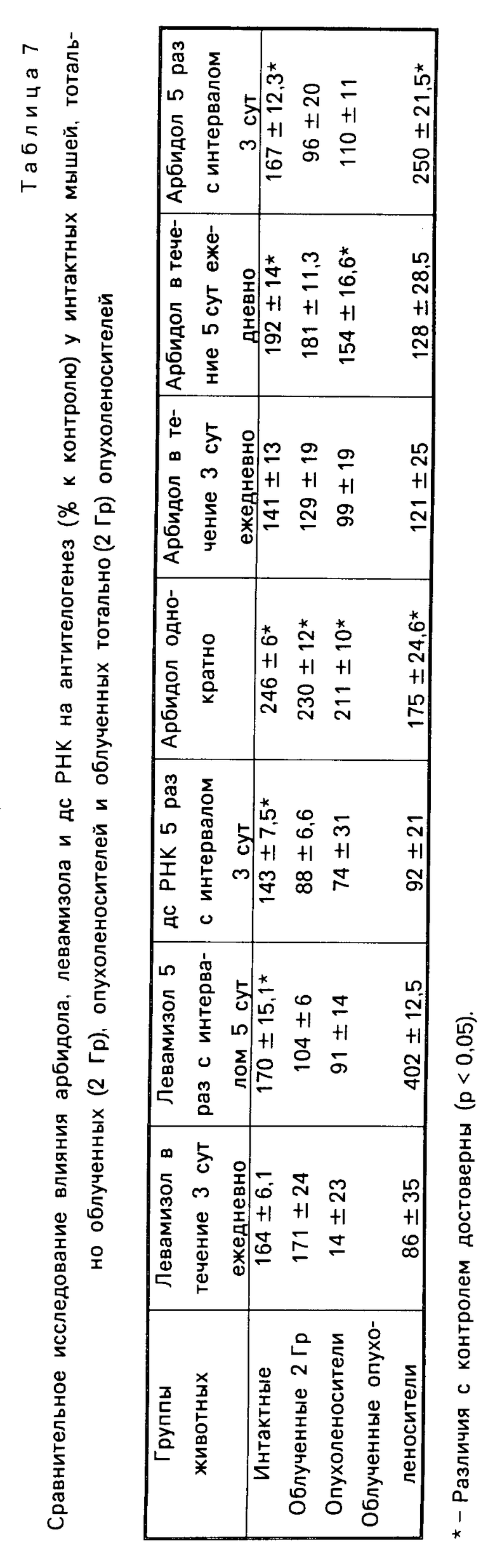
Антителогенез изучен по отношению к эритроцитам барана при иммунизации внутрибрюшинно в дозе 1 х 10 8 кл. Через 5 сут после иммунизации животных забивали декапитацией и определяли содержание антителообразующих клеток (АОК) в селезенке по методике Канингейма. Результаты опытов суммированы в табл.7.
Арбидол повышал количество АОК при различных схемах введения до 167-246% левамизол и дс РНК фага RF2 в пределах 143-170%
Выраженным иммуностимулирующим действием по отношению к облученным животным обладал только арбидол, причем в наибольшей степени при введении за 3 сут до облучения: иммунный ответ сразу после облучения составлял 230% по отношению к контролю. Левамизол у этих животных малоэффективен, дс РНК фага RF2 неэффективен.
Арбидол оказывал также иммуностимулирующее действие по отношению к животным-опухоленосителям (7-17 сут роста опухоли) после однократного (иммунизация через 3 сут) или пятикратного ежедневного введения. Левамизол и дс РНК в этих экспериментах неэффективны.
Арбидол активен у тотально облученных животных-опухоленосителей и оказывал выраженное иммуностимулирующее действие даже тогда, когда уровень антителогенеза был снижен примерно в 50 раз по сравнению с интактными животными. Левамизол также обладал иммуностимулирующим действием по отношению к этим животным; дс РНК была неэффективна.
Таким образом, арбидол обладает способностью стимулировать антителогенез у всех изученных линий мышей, как интактных, так и облученных, и по эффективности превосходит препараты сравнения левамизол и дс РНК фага RF2.
Влияние арбидола на реакции клеточного иммунитета, тестируемые по реакции трансплантат против хозяина (РТПХ) изучены известным методом [10]
Мышей-гибридов (CBA x С 57 BL/6)F1, самцов в возрасте 3 месяцев облучали в дозе 5 Гр (аппарат "Луч", мощность дозы около 0,8 Гр/мин) для стимуляции эндогенного колониеобразования селезенки, выживающим после облучения кроветворными колониеобразующими единицами (КОЕ-С).
Через 1 сут после облучения им внутривенно вводили лимфоциты, полученные из брыжеечных лимфоузлов родительской линии CBA в возрасте 3 мес в концентрациях 1,25, 2,5 и 5,0 миллионов кариоцитов. В опытных группах сразу после внутривенного введения лимфоцитов перорально вводили арбидол из расчета 100 мг/кг массы тела или левамизол из расчета 5 мг/кг в 2%-ном растворе крахмала. В каждой группе было по 15 мышей. Через 8 сут после облучения мышей забивали, селезенки фиксировали и подсчитывали число колоний диаметром не менее 0,2 мм.
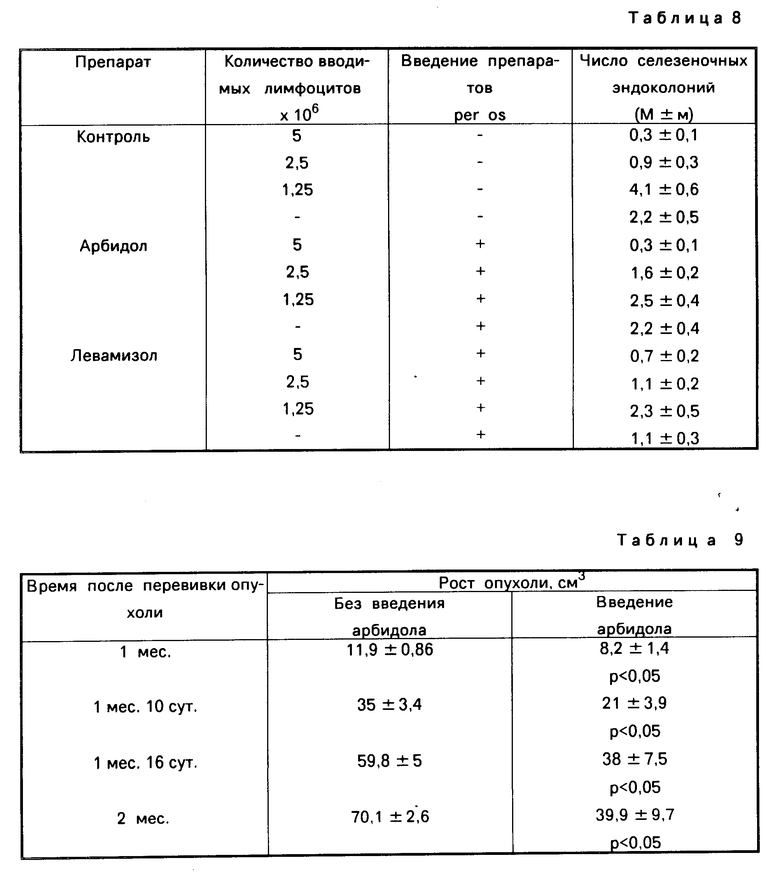
Полученные данные сведены в табл.8. Введение аллогенных лимфоцитов в больших дозах (2,5 и 5 миллионов) приводит в контроле к уменьшению выхода селезеночных колоний, а при наименьшей использованной дозе (1,25˙106) несколько повышает выход селезеночных колоний. Введение арбидола уменьшает оба наблюдаемых отклонения к значению контроля, если только доза введенных клеток не самая большая (5˙106). Левамизол обладает сходным, но менее выраженным действием. Кроме того, в том случае, когда аллогенные лимфоциты не вводятся, левамизол несколько уменьшает выход селезеночных колоний, а арбидол такого эффекта не оказывает.
Таким образом, введение арбидола в условиях индуцированной РТПХ нормализует пролиферативную активность "клеток-мишеней" и способность их дать жизнеспособную колонию как в случае торможения (при больших дозах лимфоцитов), так и в случае стимуляции (меньшие дозы лимфоцитов). По своей эффективности арбидол превосходит стандартный препарат левамизол.
В качестве иммуностимулирующего средства изучено влияние арбидола на рост перевиваемой опухоли и термическое повреждение кожи.
Исследовали влияние арбидола на рост саркомы-45, прививаемой подкожно в правое бедро половозрелым крысам самцам линии Вистар. Арбидол вводили внутрижелудочно в виде суспензии в 1%-ном растворе крахмала в дозе 125 мг/кг в течение 5 дней ежедневно через две недели после прививки опухоли. Контрольным животным вводили только раствор крахмала. Динамику роста опухоли контролировали прижизненным измерением ее объема.
Результаты. При наблюдении в течение двух месяцев обнаружено торможение роста опухоли в группе (10 животных), получавших арбидол (табл.9).
Таким образом, арбидол оказывает угнетающее действие на рост солидной перевиваемой экспериментальной опухоли, возможно опосредованно через стимуляцию иммунологической реактивности.
В связи с тем, что арбидол предназначается использовать не только при чисто лучевом воздействии на опухоль, но и при термолучевой терапии, представляло интерес оценить влияние этого препарата на термочувствительность кожи мышей. Ранее проводимые исследования показали, что эталонный препарат левамизол не оказывал какого-либо влияния на термочувствительность кожи.
Опыты проведены на белых нелинейных мышах-самцах в возрасте 3 месяцев. У наркотизированных животных (нембутал 70 мг/кг массы тела) в водяном термостате нагревали хвост при температуре 45оС в течение различного периода времени (11-23 мин). Затем в течение 2 недель учитывали частоту развития некроза. В каждой группе было 25-70 мышей. Арбидол вводили за сутки до гипертермического воздействия перорально на 2% крахмальном растворе из расчета 100 мг/кг массы тела.
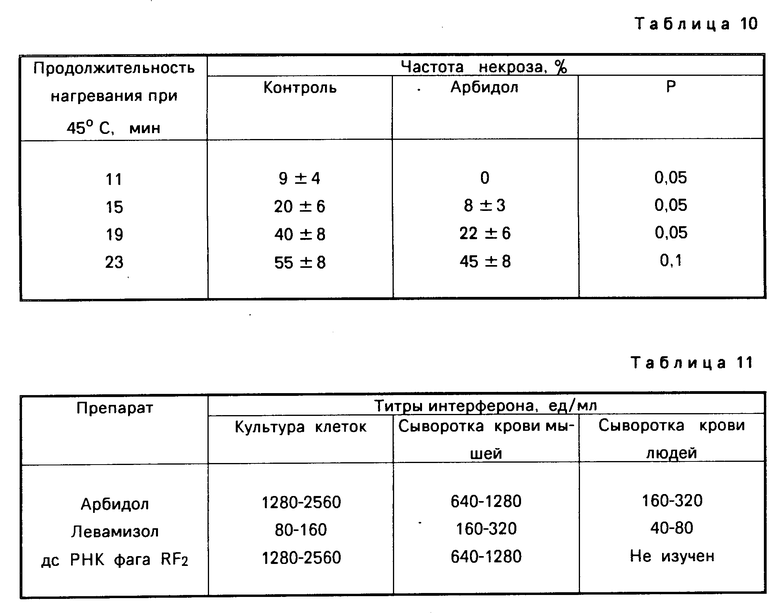
Результаты опыта приведены в табл.10. Арбидол обладает невысоким термозащитным эффектом, а различия при большинстве изученных продолжительностей воздействия статистически значимы.
Таким образом, можно рекомендовать использовать арбидол и при термолучевом лечении опухолей на коже, так как он оказывает теплозащитное действие.
Изучено влияние арбидола на иммунологический статус людей.
Под наблюдением находились здоровые молодые люди (добровольцы) от 18 до 30 лет (25 человек).
О состоянии иммунологического статуса судили на основании исследования Т-клеточного иммунитета: состояния лимфоцитов в периферической крови, абсолютное и относительное содержание Т-клеток (по методу Джондала), состоянию стабильности рецепторов на поверхностной мембране лимфоцитов.
Под влиянием различных доз арбидола изучен иммунологический статус здоровых молодых людей без предварительной антигенной стимуляции и при вакцинальной гриппозной инфекции, которую создавали путем вакцинации коммерческой гриппозной вакциной типа А, производства Одесского предприятия по производству вакцинных препаратов МЗ СССР, интраназально в разведении 1:1 в объеме 10 мл.
Исследование проведено методом двойного слепого контроля, наряду с таблетками арбидола по 100 мг использовали аналогичное по виду плацебо. Результаты обработаны статистически.
Полученные данные свидетельствуют о том, что арбидол при однократном приеме 100 мг внутрь и суточной дозе 300 мг (по 100 мг 3 раза в день) не изменяет численность Т-популяции, но приводит к изменению связи рецепторов с поверхностной мембраной лимфоцитов, которое сохраняется в течение 14 дней (срок наблюдения).
Вакцинация, проводимая через сутки после введения препарата, не влияла на характер изменений связи рецепторов с мембраной лимфоцитов.
Изменение поверхностных свойств мембраны лимфоцитов под действием арбидола, вероятно, сказывается на изменении функциональных свойств этих клеток, приводящему к усилению функции системы иммунитета, о чем свидетельствует наблюдаемый защитный эффект арбидола в отношении развития гриппозной инфекции. Арбидол предупреждает развитие постгриппозных осложнений и существенно снижает частоту обострений хронических заболеваний у переболевших гриппом людей.
Проведенные экспериментальные и клинические исследования свидетельствуют о том, что арбидол является активным интерфероногеном и весьма перспективным иммуностимулятором.
Арбидол стимулирует синтез интерферона как in vitro (в культуре клеток), так и in vivo (животные, люди).
По выраженности интерферониндуцирующей активности в эксперименте арбидол превосходит левамизол и близок к известному интерфероногену дс РНК фага RF2 [4] Следует отметить, что наличие интерферона в сыворотке крови людей для дс РНК фага RF2 не установлено (см. табл.11).
Изучение арбидола в качестве иммуномодулятора показало, что он способен стимулировать различные функции системы иммунитета, что повышает резистентность организма к росту перевиваемой опухоли. Эффект арбидола проявляется и в облученном организме, что показано на примере влияния препарата на проявления РТПХ. По большинству изученных тестов арбидол превосходит или, по крайней мере, не уступает по эффективности левамизолу (или дс РНК), использованным в качестве эталонных соединений. Кроме того, выявлено, что арбидол способен несколько уменьшить термическое повреждение кожи. Все эти данные свидетельствуют о перспективности проведения клинических испытаний арбидола в качестве иммуностимулятора при лучевом или термолучевом лечении онкологических больных.
Известно, что такое лечение в настоящее время обладает значительным иммуносупрессивным эффектом. Поэтому на фоне выраженной первичной регрессии опухоли в дальнейшем могут развиваться рецидивы и отдаленные метастазы. Современные представления о стратегии лечения онкологических больных предполагают обязательную коррекцию иммунологических функций организма-опухоленосителя после (или в процессе) интенсивной цитостатической и цитотоксической терапии. В этом отношении использование арбидола представляется весьма перспективным. Следует отметить, что наличие у арбидола выраженной интерфероногенной активности также свидетельствует о перспективности его включения в схему лечения онкологических больных. В настоящее время накоплен определенный опыт использования интерферонов при лечении рака и показана перспективность сочетания при этом интерферона с химиопрепаратами, гипертермией и ионизирующей радиацией.
При клиническом изучении эффективности арбидола при гриппе показано, что препарат практически не токсичен, хорошо переносится здоровыми и больными гриппом людьми. Это большое преимущество арбидола перед левамизолом, который является высокотоксичным препаратом.
Для разработки оптимальных схем применения арбидола в качестве иммуностимулятора проведен синтез и изучение меченного арбидола 14С. Полученные результаты показывают, что препарат быстро выводится, что позволяет не опасаться возможной кумуляции его в организме.
Совокупность полученных данных позволяет считать арбидол эффективным интерфероногеном и иммуностимулятором, не обладающим токсическим и побочными действиями на организм. Арбидол может быть рекомендован для клинического изучения в качестве иммуностимулятора при вторичных иммунодефицитных состояниях, в том числе при лучевом и термолучевом лечении онкологических больных, а также хронических и рецидивирующих вирусных инфекциях. Литература. 1. Петров Р.В. Иммунология. М. Медицина, 1987, с.379-389.
2. Машковский М. Д. Лекарственные средства, ч.2. М. Медицина, 1984, с. 169-171.
3. Каспаров А. А. и др. Индукторы интерферона. М. Медицина, 1982, с. 155-160.
5. Ершов Ф.И. и Жданов В.М. Индукторы интерферона. М. Медицина, 1982, с. 7-18.
5. Hadden J.W. Yopez C. O'Reily R.J.O. Hadden E. In: Third Conference on Antiviral Substances. Annals of the New York Academy of Sciences, 1977, 284, p.139-152.
6. Заявка ВНИХФИ N 2.078.859/23-4, 1974.
7. Заявка ВНИХФИ N 4106938/14, 1986.
8. Фомина А. Н. и др. Биологическая активность нового отечественного природного индуктора двунитевого РНК. Антибиотики, 1980, N 1, с.28-32.
9. Ершов Ф. И. и Новохатский А.С. Интерферон и его индукторы. М. Медицина, 1980, с.40-41.
10. Петров Р.В. и др. Радиобиология, 1970, т.70, N 4, с.532-535.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ДЕЙСТВИЕМ ПРОТИВ ИНФЕКЦИОННЫХ АГЕНТОВ | 1994 |
|
RU2092177C1 |
| ИНДУКТОР ИНТЕРФЕРОНА ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 1999 |
|
RU2172631C2 |
| ИНДУКТОР ИНТЕРФЕРОНА | 1998 |
|
RU2132681C1 |
| ИНТЕРФЕРОНИНДУЦИРУЮЩЕЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОСТРЫХ РЕСПИРАТОРНЫХ ВИРУСНЫХ ИНФЕКЦИЙ (ОРВИ) | 2010 |
|
RU2470634C2 |
| ИММУНОСТИМУЛЯТОР | 1993 |
|
RU2077339C1 |
| ИНТЕРФЕРОНИНДУЦИРУЮЩЕЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОСТРЫХ РЕСПИРАТОРНЫХ ВИРУСНЫХ ИНФЕКЦИЙ (ОРВИ) | 2010 |
|
RU2445094C1 |
| ИНДУКТОР ИНТЕРФЕРОНА РИДОСТИН | 1993 |
|
RU2083221C1 |
| Индуктор интерферона | 1985 |
|
SU1701322A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2008 |
|
RU2406517C2 |
| N-МЕТИЛ-N-( α,D -ГЛЮКОПИРАНОЗИЛ) АММОНИЯ-2-(АКРИДОН-9-ОН-10-ИЛ)АЦЕТАТ(ЦИКЛОФЕРОН), ОБЛАДАЮЩИЙ ИНТЕРФЕРОНОГЕННОЙ, ПРОТИВОВИРУСНОЙ, В ТОМ ЧИСЛЕ АНТИВИЧ, АНТИПАРАЗИТАРНОЙ, АНТИПРОМОТОРНОЙ И РАДИОПРОТЕКТИВНОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2036198C1 |
Изобретение относится к области медицины, а именно к фармакологии и созданию лекарственных средств, обладающих интерфероногенным и иммуномодулирующим действием. Цель изобретения - изыскание лекарств, обладающих выраженным интерфероногенным и иммуностимулирующим действием и не оказывающих нежелательные побочные эффекты. Поставленная цель достигается использованием 1-метил-2-фенилтиометил-3-карбэтокси-4-диметиламинометил-5-окси-6-броминдола моногидрата гидрохлорида (условно назван арбидол) по новому назначению, а именно в качестве интерферониндуцирующего и иммуномодулирующего (иммуностимулирующего) средства. 11 табл.
СРЕДСТВО, ОБЛАДАЮЩЕЕ ИНТЕРФЕРОНИНДУЦИРУЮЩЕЙ И ИММУНОМОДУЛИРУЮЩЕЙ (ИММУНОСТИМУЛИРУЮЩЕЙ) АКТИВНОСТЬЮ, отличающееся тем, что оно представляет собой 1-метил-2-фенилтиометил-3-карбэтокси-4-диметиламинометил-5-окси-6-броминдола гидрохлорид моногидрат формулы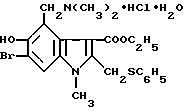
| Машковский М.Д | |||
| Лекарственные средства | |||
| М., 1985, ч.2, с.169-171. |
Авторы
Даты
1995-04-20—Публикация
1987-12-16—Подача