Настоящее изобретение относится к индолилмалеимидным производным, способу их получения и содержащим их фармацевтическим композициям.
В частности, в настоящем изобретении представлено соединение формулы I
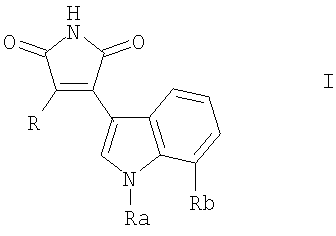
в которой
Ra обозначает Н, СН3, СН2-СН3 или изопропил,
Rb обозначает Н, галоген, С1-6алкокосигруппу или С1-6алкил и либо
I. R представляет собой радикал формулы (а)
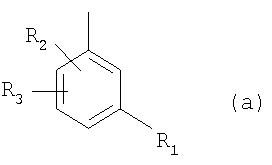
в которой
R1 обозначает пиперазин-1-ил, необязательно замещенный СН3 в положении 3 или 4, или 4,7-диаза-спиро[2,5]окт-7-ил,
R2 обозначает Cl, Br, CF3 или СН3, и
R3 обозначает Н, СН3 или CF3; R2 отлично от СН3 или Cl, когда R3 обозначает Н,
Ra обозначает Н или СН3, Rb обозначает Н, и R1 обозначает 4-метил-1-пиперазинил; либо
II. Ra обозначает радикал формулы (б)
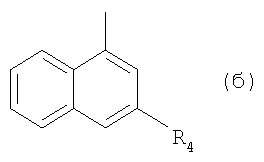
в которой
R4 обозначает 1-пиперазинил, замещенный СН3 в положениях 3 и/или 4, или
4,7-диаза-спиро[2,5]окт-7-ил, Ra отлично от Н или СН3, когда R4 обозначает 4-метил-1-пиперазинил; либо
III. R обозначает остаток формулы (в)
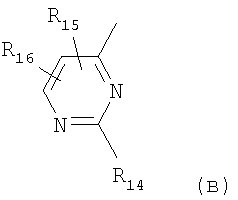
в которой
R14 обозначает 1-пиперазинил, необязательно замещенный СН3 в положении 3 и/или 4 или в положении 3 этилом, фенил-С1-4-алкилом, С1-4алкокси-С1-4алкилом или галоген-С1-4алкилом; или 4,7-диаза-спиро[2,5]окт-7-ил,
R15 обозначает галоген, CF3 или СН3, R15 отлично от СН3, когда R16 обозначает СН3, Ra обозначает Н или СН3, Rb обозначает Н, и R14 обозначает 4-метил-1-пиперазинил, и
R16 обозначает Н, СН3, СН2-СН3 или CF3, R16 отлично от Н, когда R15
обозначает Cl, Ra обозначает Н или СН3, Rb обозначает Н, и R14 обозначает 4-метил-1-пиперазинил, либо
IV. R представляет собой радикал формулы (г)
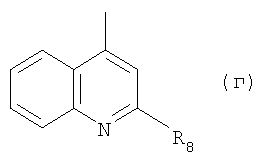
в которой R8 обозначает 1-пиперазинил, 3-метил-пиперазин-1-ил или 4-бензил-пиперазин-1-ил, либо
V. R представляет собой радикал формулы (д)
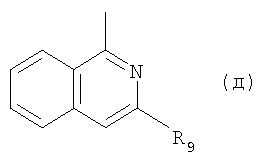
в которой R9 обозначает 4,7-диаза-спиро[2,5]окт-7-ил или пиперазин-1-ил, замещенный в положении 3 метилом или этилом и необязательно метилом в положении 4.
Соединения формулы I могут существовать в свободной форме или в форме солей, например аддитивных солей, образованных, например, с органическими или неорганическими кислотами, например хлористо-водородной кислотой, уксусной кислотой, трифторуксусной кислотой.
Следует принять во внимание, что соединения формулы I могут существовать в форме оптических изомеров, рацематов или диастереомеров. Например, атом углерода цикла, несущий заместитель в положении 3 остатка пиперазинила, является асимметричным и может иметь R- или S-конфигурации. Следует иметь в виду, что настоящее изобретение охватывает все энантиомеры и их смеси. Энантиомеры являются более предпочтительными, чем рацематы. Как отмечено выше, аналогичные соображения относятся к исходным материалам, имеющим асимметричные атомы углерода. Алкил или алкоксигруппа могут быть неразветвленными или разветвленными. Фенил-С1-4алкил предпочтительно представляет собой бензил или фенетил. В С1-4алкокси-С1-4алкиле часть алкоксигруппы предпочтительно представляет собой метокси- или этоксигруппу, и алкильная часть предпочтительно представляет собой метил или этил, подходящим примером является, например, 2-метоксиэтил. Галоген может представлять собой F, Cl, Br или I, предпочтительно F, Cl или Br. Галоген-С1-4алкил представляет собой алкил, в котором один или более атомов Н замещены галогеном, например Cl или F, например CH2Cl, CH2F или CF3.
R предпочтительно обозначает радикал формулы (а), (в) или (г), предпочтительно (д).
В радикале формулы (а) или (в), R2 или R15 предпочтительно находятся в пара-положении относительно R1 или R14 соответственно. R3 находится предпочтительно в мета-положении относительно R1. В радикале или формуле (г) R9 предпочтительно обозначает 4,7-диаза-спиро[2,5]окт-7-ил; когда R9 представляет собой пиперазинил, замещенный в положении 3, он имеет R- или S-конфигурацию.
Настоящее изобретение включает также способ получения соединения формулы I, который включает реакцию соединения формулы II
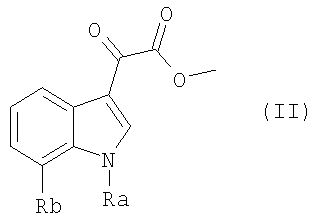
в котором Ra и Rb такие, как определено выше, с соединением формулы III
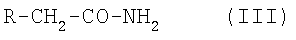
в котором R такое, как определено выше,
и, если требуется, превращение конечного соединения формулы I, полученного в свободной форме, в солевую форму или наоборот, по необходимости.
Способ можно подходящим образом осуществить в присутствии сильного основания, например трет-BuOK, например, как описано в Международной заявке WO 02/38561, содержание которой включено в данном контексте в виде ссылки, и как показано в Примерах.
Соединения формул II и III могут быть получены в соответствии с известными способами, например, как описано в Международной заявке WO 02/38561, содержание которой включено в данном контексте в виде ссылки, и как показано в Примерах.
В том случае, если получение исходных продуктов подробно не описано, соединения являются известными или могут быть получены аналогично методам, известным в области техники или как описано далее.
Следующие примеры иллюстрируют изобретение без каких-либо ограничений.
КТ = комнатная температура
ТГФ = тетрагидрофуран
УКХ = ускоренная колоночная хроматография
ФТБ = фторид тетрабутиламмония
BINAP = 2,2'-бис(дифенилфосфин)-1,1'-бинафтил
Pd2(dba)3 = Pd(0)-бис(дибензилиденацетон)
Пример 1: 3-[2-Хлор-3-метил-5-(4-метил-пиперазин-1-ил)-фенил]-4-(1Н-индол-3-ил)-пиррол-2,5-дион
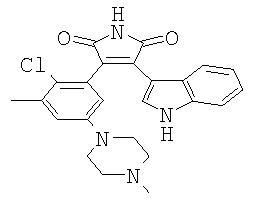
2-[2-Хлор-3-метил-5-(4-метил-пиперазин-1-ил)-фенил]-ацетамид (211 мг, 0,75 ммоль) и 3-индолглиоксилат (270 мг, 1,35 ммоль) растворяют в ТГФ (5 мл). Добавляют раствор 1,0 М трет-BuOK в ТГФ (2,98 мл, 4 экв.) и перемешивают смесь при температуре 35°С в течение ночи. Реакцию разводят AcOEt (20 мл) и промывают Н2О (20 мл) и соляным раствором (10 мл). Органическую фазу сушат над Na2SO4 и выпаривают растворитель. Остаток очищают с помощью УКХ (AcOEt/AcOH/H2O 7:1:1), что дает титульное соединение в форме соли уксусной кислоты. Данные 1H ЯМР-спектроскопии (ДМСО, 400 МГц) δ 2,16 (s, 3H), 2,31 (s, 3H), 2,32-2,38 (m, 4Н), 2,97-3,10 (m, 4H), 6,61 (d, J=8,0 Гц, 1Н), 6,71-6,77 (m, 2Н), 7,04 (d, J=2,8 Гц, 1Н), 7,08 (dd, J=7,4, 7,2 Гц, 1H), 7,41 (d, J=8,2 Гц, 1Н), 7,98 (d, J=1,5 Гц, 1H), 11,05 (br s, 1H), 11,90 (br s, 1H); ES-MS: 435 [M+H]+.
2-[2-Хлор-3-метил-5-(4-метил-пиперазин-1-ил)-фенил]-ацетамид,
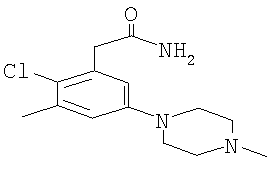
используемый как исходный материал, может быть получен следующим образом:
метиловый эфир (5-бром-2-хлор-3-метил-фенил)-уксусной кислоты (2,0 г, 7,2 ммоль), N-метилпиперазин (960 мкл, 8,6 ммоль) и Cs2СО3 (3,3 г, 10,1 ммоль) суспендируют в толуоле (80 мл). Добавляют Pd(OAc)2 (81 мг, 0,36 ммоль) и BINAP (224 мг, 0,36 ммоль) и перемешивают реакцию при температуре 100°С в течение ночи. Смесь фильтруют через целит и выпаривают растворитель. Остаток очищают с помощью УКХ (AcOEt/AcOH/H2O 60:15:15), что дает метиловый эфир 2-[2-хлор-3-метил-5-(4-метил-пиперазин-1-ил)-фенил]-уксусной кислоты. Данный эфир суспендируют в 25% NH4OH (60 мл). Смесь перемешивают в течение ночи при КТ, и отфильтровывают осадок, получая амид. Данные 1H ЯМР-спектрометрии (ДМСО, 400 МГц) δ 2,20 (s, 3Н), 2,27 (s, 3Н), 2,40-2,45 (m, 4Н), 3,07-3,13 (m, 4H), 3,48 (s, 2Н), 6,78 (s, 1H), 6,82 (s, 1H), 6,91 (brs, 1H), 7,34 (br s, 1H).
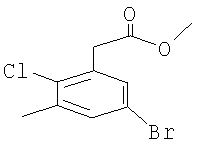
CuCl2 (8,0 г, 0,06 моль) и трет-бутилнитрил (8,9 мл, 0,074 моль) суспендируют в ацетонитриле (60 мл). 1,1-дихлорэтилен добавляют по каплям при температуре 20°С. Добавляют 5-бром-2-хлор-3-метил-фениламин (11,0 г, 0,05 моль), растворенный в ацетонитриле (60 мл), и перемешивают реакцию при КТ в течение 3 ч. Смесь выливают в водную 20% HCl (150 мл) и экстрагируют водную фазу с использованием CH2Cl2 (2×150 мл). Органическую фазу сушат над Na2SO4 и выпаривают растворитель. Остаток очищают с помощью УКХ (гексан/СН2Cl2 9:1), что дает 5-бром-2-хлор-1-метил-3-(2,2,2-трихлор-этил)-бензол. Промежуточный продукт перерастворяют в МеОН (80 мл) и нагревают до температуры 70°С. Раствор 5,4 M NaOMe в МеОН (28,4 мл) добавляют по каплям и перемешивают реакцию при температуре 70°С в течение 3 ч. Реакцию охлаждают до КТ и добавляют концентрированную H2SO4 (10 мл). Реакцию перемешивают при нагревании с обратным холодильником в течение 1 ч. Смесь разводят H2O (200 мл) и экстрагируют СН2Cl2 (2×200 мл). Объединенные органические фазы сушат над Na2SO4 и выпаривают растворитель. Остаток очищают помощью УКХ (гексан/СН2Cl2 9:1-1:1), что приводит к получению метилового эфира (5-бром-2-хлор-3-метил-фенил)-уксусной кислоты. Данные 1Н ЯМР-спектрометрии (CDCl3, 400 МГц) δ 2,26 (s, 3Н), 3,61 (s, 3Н), 3,63 (s, 2Н), 7,15 (s, 1H), 7,21 (s, 1H).
Согласно процедуре, представленной в Примере 1, но при использовании соответствующих исходных материалов можно получить соединения формулы I, в которых R представляет собой остаток формулы (а), как указано в Таблице 1 ниже.
Пример 20: 3-[3-(4,7-Диаза-спиро[2.5]окт-7-ил)-нафталин-1-ил]-4-(1-метил-1Н-индол-3-ил)-пиррол-2,5-дион
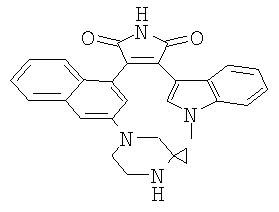
Из 2-[3-(4,7-Диаза-спиро[2.5]окт-7-ил)-нафталин-1-ил]-ацетамида (100 мг, 0,30 ммоль) и метилового эфира (1-метил-1Н-индол-3-ил)-оксо-уксусной кислоты (97 мг, 0,44 ммоль) трижды получают азеотропную смесь с сухим ТГФ, а затем растворяют в сухом ТГФ (3 мл). Раствор 1,0 М KOtBu в ТГФ (1,2 мл) добавляют по каплям в течение 20 мин при КТ. Через 5 минут анализ с помощью ТСХ (тонкослойной хроматографии) показывает полное превращение исходных материалов. Реакцию гасят добавлением воды (5 мл). Смесь разводят EtOAc и дважды промывают насыщенным водным раствором NH4Cl Водные слои дважды подвергают обратной экстракции EtOAc. Объединенные органические слои сушат над Na2SO4 и выпаривают растворитель. Остаток очищают с помощью УКХ (EtOAc/АсОН/Н2О 800:55:45), что приводит к получению титульного соединения в виде его соли ацетата. Соединение растворяют в МеОН/ТФК (трифторуксусная кислота) и удаляют растворитель, получая титульное соединение в виде его соли трифторацетата. Данные 1H ЯМР-спектрометрии (ДМСО, 400 МГц) δ 0,95 (М, 4Н), 3,39 (br, 4H), 3,49 (br, 2H), 3,86 (s, 3Н), 6,16 (d, J=7,9 Гц, 1Н), 6,46 (dd, J=6,6/7,9 Гц, 1Н), 7,00 (dd, J=6,6/7,9 Гц, 1Н), 7,13 (dd, J=7,6/7,6 Гц, 1H), 7,40 (m, 4Н), 7,55 (d, J=8,5 Гц, 1H), 7,78 (d, J=7,6 Гц, 1H), 8,14 (s, 1H), 9,10 (br, 2H), 11,17 (s, 1H); ES-MS: 463 [M+H]+.
2-[3-(4,7-Диаза-спиро[2.5]окт-7-ил)-нафталин-1-ил]-ацетамид, используемый как исходный материал, может быть получен следующим образом:
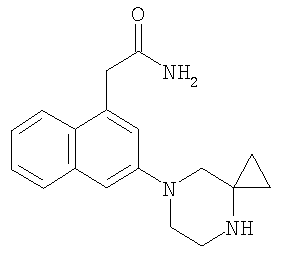
а) Из 2-[3-(4-бензил-4,7-диаза-спиро[2.5]окт-7-ил)-нафталин-1-ил]-ацетамида (280 мг, 0.73 ммоль) дважды получают азеотропную смесь с 1,25 М раствором HCl в МеОН. Остаток растворяют в EtOH (10 мл). Добавляют палладий на угле (10%, 77 мг) и перемешивают смесь в атмосфере водорода (1 атм) при КТ в течение 14 ч и при температуре 50°С в течение 2 ч. Смесь фильтруют и концентрируют фильтрат. Остаток очищают с помощью УКХ (EtOAc/АсОН/Н2О 750:83:68-600:150:150), получая титульное соединение, содержащее 0,7 экв. АсОН. Данные 1Н ЯМР-спектрометрии (ДМСО, 400 МГц) δ 0,53 (m, 4H), 1,78 (s, АсОН), 2,93 (ddd, 2H), 3,04 (s, 2H), 3,16 (ddd, 2H), 3,76 (s, 2H), 6,94 (br, 1H), 6,99 (s, 1H), 7,25 (dd, 1H), 7,26 (s, 1H), 7,35 (dd, J=6,7/7,8, 1H), 7,49 (br, 1H), 7,69 (d, J=7,8, 1H), 7,88 (d, J=10,0, 1H); ES-MS: 296 [M+H]+.
б) 2-[3-(4-бензил-4,7-диаза-спиро[2.5]окт-7-ил)-нафталин-1-ил]-ацетамид
Этиловый эфир [3-(4-бензил-4,7-диаза-спиро[2.5]окт-7-ил)-нафталин-1-ил]-уксусной кислоты (347 мг, 0,84 ммоль) и формамид (126 мг, 2,80 ммоль) растворяют в атмосфере аргона в ДМФ (диметилформамиде) (1 мл). Раствор нагревают до температуры 105°С и по каплям добавляют NaOMe (155 мкл 5,4 M раствора в МеОН, 45 мг, 0,84 ммоль) в течение 15 мин. Через 30 мин выдерживания при температуре 105°С, анализ с помощью ТСХ показывает, что исходный материал полностью использован. Реакционную смесь охлаждают до КТ, разводят водой и экстрагируют EtOAc. Слои EtOAc дважды промывают водой. При удалении растворителя и очистке с помощью УКХ (EtOAc/MeOH 98:2 до 96:4 до 90:10) получают титульное соединение. Данные 1Н ЯМР-спектрометрии (CDCl3, 400 МГц) δ 0,71 (ddd, 2H), 0,89 (ddd, 2H), 3,10 (ddd, 2H), 3,16 (s, 2H), 3,31 (ddd, 2H), 3,93 (s, 2H), 3,99 (s, 2H), 5,33 (br, 1H), 5,42 (br, 1H), 7,11 (s, 1H), 7,23 (d, J=2,0, 1H), 7,32 (m, 5H), 7,37 (dd, J=6,7 Гц, 1H), 7,45 (dd, J=6,7 Гц, 1H), 7,73 (d, J=8,9 Гц, 1H), 7,85 (d, J=8,9 Гц, 1H); ES-MS: 386 [М+Н]+.
в) Этиловый эфир [3-(4-Бензил-4,7-диаза-спиро[2.5]окт-7-ил)-нафталин-1-ил]-уксусной кислоты
Этиловый эфир (3-трифторметансульфонилокси-нафталин-1-ил)-уксусной кислоты (500 мг, 1,38 ммоль) растворяют в атмосфере аргона в сухом ТГФ (10 мл). Добавляют 4-бензил-4,7-диаза-спиро[2.5]октан (325 мг, 1,61 ммоль) с последующим добавлением К3PO4 (410 мг, 1,93 ммоль), Pd2(dba)3 (62 мг, 0,069 ммоль) и бифенил-2-ил-ди-трет-бутил-фосфана (21 мг, 0,069 ммоль). Реакционную смесь нагревают до температуры 80°С. Через 4 ч анализ с помощью ТСХ показывает, что исходный материал полностью использован. Реакционную смесь охлаждают до КТ, фильтруют и концентрируют. Остаток очищают УКХ (гексаны/EtOAc 100:0 до 90:10, до 80:20, до 70:30, до 0:100), что дает титульное соединение. Данные 1Н ЯМР-спектрометрии (CDCl3, 400 МГц) δ 0,69 (ddd, 2Н), 0,86 (ddd, 2H), 1,24 (t, J=7,0 Гц, 3Н), 3,09 (ddd, 2Н), 3,19 (s, 2H), 3,31 (ddd, 2H), 3,93 (s, 2H), 4,02 (s, 2H), 4,17 (q, J=7,0 Гц, 2H), 7,08 (s, 1H), 7,21 (s, 1H), 7,33 (m, 6H), 7,42 (dd, J=8,8 Гц, 1H), 7,71 (d, J=8,8 Гц, 1H), 7,88 (d, J=8,8 Гц, 1H); ES-MS: 415 [M+H]+.
г) Этиловый эфир (3-трифторметансульфонилокси-нафталин-1-ил)-уксусной кислоты
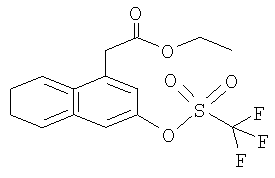
Этиловый эфир (3-гидрокси-нафталин-1-ил)-уксусной кислоты (1,67 г, 7,25 ммоль) растворяют в CH2Cl2 (20 мл) в атмосфере аргона. Добавляют пиридин (1,17 мл, 1,15 г, 14,50 ммоль) и охлаждают реакционную смесь до 0°С, после чего по каплям добавляют трифторметансульфоновый ангидрид (1,79 мл, 3,07 г, 10,88 ммоль). Реакционную смесь нагревают до КТ, и через 1 ч выдерживания при КТ анализ с помощью ТСХ показывает, что исходный материал полностью использован. Реакционную смесь разводят EtOAc и дважды промывают Н2О. Объединенные органические слои сушат над Na2SO4, растворитель удаляют и остаток очищают с помощью УКХ (гексаны/EtOAc 100:0 до 97:3, до 95:5, до 93:7, до 90:10), что приводит к получению титульного соединения. Данные 1Н ЯМР-спектрометрии (ДМСО, 400 МГц) δ 1,19 (t, J=7,2 Гц, 3Н), 4,11 (q, J=7,2 Гц, 2Н), 4,38 (s, 2Н), 7,60 (d, J=3,0 Гц, 1H), 7,70 (m, 2H), 8,03 (m, 1H), 8,12 (m, 2H); ES-MS: 362 [M+H]+.
д) Этиловый эфир (3-гидрокси-нафталин-1-ил)-уксусной кислоты
Этиловый эфир (3-бензилокси-нафталин-1-ил)-уксусной кислоты (2,43 г, 7,58 ммоль) растворяют в МеОН (50 мл). Добавляют палладий на угле (807 мг) и перемешивают реакционную смесь при КТ в атмосфере водорода (1 атм) в течение 14 ч. Реакционную смесь фильтруют. При концентрировании получают чистое титульное соединение. Данные 1Н ЯМР-спектрометрии (CDCl3, 400 МГц) δ 1,18 (t, J=7,2 Гц, 3Н), 4,05 (s, 2H), 4,10 (q, J=7,2 Гц, 2H), 7,04 (d, J=1,8 Гц, 1H), 7,06 (d, J=1,8, 1H), 7,30 (t, J=7,8, 1H), 7,40 (t, J=7,8, 1H), 7,70 (d, J=7,8, 1H), 7,80 (d, J=7,8 Гц, 1H); ES-MS: 230 [М+Н]+.
е) Этиловый эфир (3-бензилокси-нафталин-1-ил)-уксусной кислоты
3-бензилокси-1-бром-нафталин (5,64 г, 18,01 ммоль) растворяют в атмосфере аргона в сухом ДМФ (диметилформамиде) (100 мл). Добавляют этиловый эфир трибутилстаннанил-уксусной кислоты (7,47 г, 19,81 ммоль), а также дихлорид [бис(три-орто-толил-фосфин)]палладия (II) (2,83 г, 3,60 ммоль) и бромид цинка (II) (5,27 г, 23,41 ммоль). Реакционную смесь нагревают до температуры 80°С в течение 3 ч. Реакционную смесь разводят EtOAc и дважды промывают разбавленным соляным раствором (обратная экстракция). Объединенные органические слои сушат над Na2SO4, растворитель удаляют и остаток очищают с помощью УКХ (гексан/EtOAc 100:0 до 97,5:2,5, до 95:5, до 90:10). Полученное в результате масло, еще содержащее примеси олова, перемешивают в смеси 1:1 EtOAc/1 н. NaOH (200 мл) в течение 1 час. Смесь дважды экстрагируют EtOAc. Объединенные органические слои дважды промывают Н2О (обратная экстракция), сушат над Na2SO4 и концентрируют. Остаток очищают с помощью УКХ (гексан/EtOAc 100:0 до 97:3, до 95:5, до 93:7, до 92:8, до 90:10), получая титульное соединение. Данные 1Н ЯМР-спектрометрии (ДМСО, 400 МГц) δ 1,18 (t, J=7,2 Гц, 3Н), 4,10 (q, J=7,2 Гц, 2H), 4,11 (s, 2H), 5,25 (s, 2H), 7,21 (d, J=3,0 Гц, 1H), 7,41 (m, 8H), 7,53 (d, J=6,6 Гц, 1H), 7,84 (dd, J=7,2 Гц, 1H); ES-MS: 320 [М+Н]+.
ж) 3-Бензилокси-1-бром-нафталин
4-бром-нафталин-2-ол (5,0 г, 22,41 ммоль) растворяют в сухом ДМФ (50 мл) в атмосфере аргона. Добавляют гидрид натрия (986 мг 60% суспензии с минеральном масле, 592 мг, 24,65 ммоль) и смесь перемешивают при температуре 50°С в течение 1 ч. После вторичного охлаждения до КТ добавляют бензилбромид (3,46 мл, 4,98 г, 29,14 ммоль) и йодид тетрабутиламмония (828 мг, 2,24 ммоль). После выдерживания в течение 16 ч при КТ реакционную смесь разводят EtOAc. Раствор дважды промывают полуконцентрированным соляным раствором (обратная экстракция).
Объединенные органические слои сушат над Na2SO4, удаляют растворитель и очищают остаток с помощью УКХ (гексан/EtOAc 100:0 до 95:5, до 90:10), получая титульное соединение. Данные 1Н ЯМР-спектрометрии (CDCl3, 400 МГц) δ 5,22 (s, 2H), 7,25 (d, J=1,5 Гц, 1Н), 7,45 (m, 7Н), 7,64 (d, J=2,4, 1H), 7,75 (d, J=7,8, 1H), 8,17 (d, J=7,8, 1H); ES-MS: 312 [M+H]+.
Согласно процедуре, соответствующей Примеру 20, могут быть получены соединения формулы I, в которой R представляет собой остаток формулы (б), как показано в Таблице 2.
Согласно процедуре, как описано выше или в Примере 56 Международной заявки WO 02/38561, но при использовании соответствующих исходных материалов могут быть получены соединения формулы I, в которой R представляет собой остаток формулы (с), как показано ниже в Таблице 3.
Согласно процедуре, как описано выше или в примере 163 Международной заявки WO 02/38561, но при использовании соответствующих исходных материалов могут быть получены соединения формулы I, в которой R представляет собой остаток формулы (г), как показано в таблице 4.
Пример 69: 3-[3-(4,7-Диаза-спиро[2.5]окт-7-ил)-изохинолин-1-ил]-4-(7-метил-1Н-индол-3-ил)-пиррол-2,5-дион
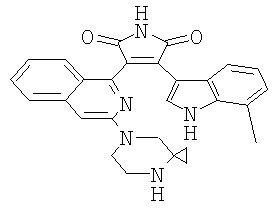
Из 2-[3-(4,7-диаза-спиро[2.5]окт-7-ил)-изохинолин-1-ил]-ацетамида (4,95 г, 16,70 ммоль) и метилового эфира (7-метил-1Н-индол-3-ил)-оксо-уксусной кислоты (5,44 г, 25,05 ммоль) дважды получают азеотропную смесь с сухим ТГФ. Затем добавляют сухой ТГФ (100 мл) и в атмосфере аргона по каплям вводят KOtBu (1,0 М в ТГФ, 50 мл, 50 ммоль) в течение 20 мин. Через дополнительные 90 мин анализ с помощью ТСХ показывает полное превращение исходных материалов. Реакционную смесь разводят водой и дважды экстрагируют EtOAc. Объединенные органические слои дважды промывают насыщенным водным раствором NH4Cl (обратная экстракция), сушат над Na2SO4 и концентрируют. Очистка с помощью УКХ (CH2Cl2/MeOH 100:0 до 98:2, до 96:4, до 94:6, до 92:8, до 90:10) дает титульное соединение, которое превращают в его соль уксусной кислоты путем концентрирования раствора EtOH/АсОН. Данные 1H ЯМР-спектрометрии (ДМСО, 400 МГц) δ 0,26-0,53 (br, 4Н), 1,89 (s, 3H, СН3СООН), 2,36 (s, 3H), 2,80 (br m, 2Н), 3,15 - 3,48 (br m, 2H), 6,14 (d, J=8,2 Гц, 1Н), 6,44 (dd, J=8,2/7,4 Гц, 1Н), 6,75 (d, J=7,4 Гц, 1Н), 7,00 (s, 1H), 7,02 (dd, J=8,2/8,2 Гц, 1Н), 7,40 (dd, J=8,2/8,2 Гц, 1Н), 7,59 (d, J=8,2 Гц, 1H), 7,63 (d, J=8,2 Гц, 1H), 7,63 (d, J=8,2 Гц, 1H), 7,97 (d, J=2,9 Гц, 1H), 11,04-11,21 (br, 1H), 11,86 (d, J=2,9 Гц, 1H); ES-MS: 464 [M+H]+.
2-[3-(4,7-Диаза-спиро[2.5]окт-7-ил)-изохинолин-1-ил]-ацетамид, используемый в качестве исходного материала, может быть приготовлен следующим образом:
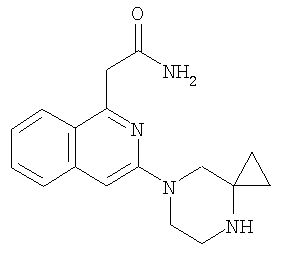
а) 2-[3-(4-Бензил-4,7-диаза-спиро[2.5]окт-7-ил)-изохинолин-1-ил]-ацетамид (490 мг, 1,27 ммоль) растворяют в абсолютном МеОН (5 мл). Добавляют Pd на угле (140 мг), а также формиат аммония (200 мг, 3,17 ммоль). После нагревания с обратным холодильником в течение 1 ч (Т=75°С) добавляют дополнительную порцию формиата аммония (200 мг, 3,17 ммоль). Через 1 ч анализ с помощью ТСХ показывает полное превращение исходных материалов. После фильтрации и концентрирования остаток помещают в CH2Cl2 и промывают водой (рН 10 получают при добавлении 2 н. NaOH). Органический слой сушат над Na2SO4 и удаляют растворитель. Очистка с помощью УКХ (EtOAc/АсОН/Н2О 750:83:68 до 700:110:90, до 650:130:120, до 600:150:150) приводит к получению титульного соединения в виде его бисацетатной соли. Данные 1Н ЯМР-спектрометрии (ДМСО, 400 МГц) δ 0,46-0,52 (m, 4H), 2,88 (t, J=5,5, 2H), 3,35 (s, 2H), 3,49 (t, J=5,5, 2H), 3,94 (s, 2H), 6,77 (s, 1H), 7,00 (br s, 1H), 7,18-7,25 (m, 1H), 7,45-7,56 (m, 2H), 7,60-7,65 (m, 1H), 7,95 (d, J=9,9, 1H), ES-MS: 297 [М+Н]+.
б) 2-[3-(4-Бензил-4,7-диаза-спиро[2.5]окт-7-ил)-изохинолин-1-ил]-ацетамид
Этиловый эфир [3-(4-бензил-4,7-диаза-спиро[2.5]окт-7-ил)-изохинолин-1-ил]-уксусной кислоты (700 мг, 1,68 ммоль) растворяют в сухом ДМФ в атмосфере аргона. Добавляют формамид (224 мкл, 254 мг, 5,64 ммоль) и нагревают реакционную смесь до температуры 105°С. При данной температуре по каплям добавляют NaOMe (312 мкг 5,4 М раствора в МеОН, 91 мг, 1,68 ммоль) в течение 20 мин. После выдерживания в течение 30 мин при температуре 105°С анализ с помощью ТСХ показывает полное превращение исходного материала. После охлаждения реакционной смеси до КТ добавляют воду и проводят экстракцию с использованием EtOAc. Органические слои промывают Н2О (два раза), сушат над Na2SO4 и концентрируют. Остаток очищают с помощью УКХ (гексан/EtOAc 1:1 до 1:3, до 0:100 до EtOAc/МеОН 98:2) для получения титульного соединения. Данные 1Н ЯМР-спектрометрии (ДМСО, 400 МГц) δ 0,68-0,70 (m, 2Н), 0,82-0,88 (m, 2Н), 3,08 (t, J=4,4, 2H), 3,45 (s, 2H), 3,58 (t, J=4,4, 2H), 3,96 (s, 2H), 4,27 (s, 2H), 5,3 - 5,5 (br, 1H), 6,55-6,7 (br, 1H), 6,72 (s, 1H), 7,26-7,36 (m, 6H), 7,51 (t, J=8,8, 1H), 7,60 (d, J=9,9, 1H), 8,02 (d, J=9,9, 1H); ES-MS: 387 [М+Н]+.
в) Этиловый эфир [3-(4-бензил-4,7-диаза-спиро[2.5]окт-7-ил)-изохинолин-1-ил]-уксусной кислоты
Этиловый эфир (3-хлор-изохинолин-1-ил)-уксусной кислоты (2,50 г, 10,01 ммоль), 4-бензил-4,7-диаза-спиро[2.5]октан (2,23 г, 11,01 ммоль), NaOtBu (1,06 г, 11,01 ммоль), BINAP (249 мг, 0,40 ммоль) и ацетат палладия(II) (180 мг, 0,80 ммоль) смешивают под аргоном. После добавления дегазированного сухого диоксана (36 мл) суспензию нагревают до температуры 85°С. После выдерживания в течение 25 мин при температуре 85°С анализ ВЭЖХ (высокоэффективная жидкостная хроматография) показывает превращение на 71%. Смесь охлаждают до КТ, разводят EtOAc и промывают Н2О и насыщенным водным раствором NH4Cl (обратная экстракция). Объединенные органические слои сушат над Na2SO4, растворитель удаляют и остаток очищают с помощью УКХ (гексан/EtOAc 100:0 до 96:4, до 93:7, до 90:10, до 85:15) для получения титульного соединения. Данные 1Н ЯМР-спектрометрии (ДМСО, 400 МГц) δ 0,58-0,61 (m, 2H), 0,70-0,73 (m, 2H), 1,18 (t, J=8,8, 3Н), 2,98 (t, J=5,5, 2H), 3,39 (s, 2H), 3,49 (t, J=5,5, 2H), 3,86 (s, 2H), 4,12 (s, 2H), 4,12 (q, J=8,8, 2H), 5,59 (s, 1H), 7,14-7,19 (m, 6H), 7,39 (t, J=8,8, 1H), 7,51 (d, J=9,9, 1H), 7,78 (d, J=9,9, 1H); ES-MS: 417 [M+H]+.
г) Этиловый эфир (3-хлор-изохинолин-1-ил)-уксусной кислоты
1,1,1,3,3,3-гексаметил-дисилазан (27,4 мл, 20,37 г, 126,2 ммоль) растворяют в сухом толуоле (150 мл). После охлаждения до температуры -78°С медленно добавляют н-BuLi (79 мл 1,6 М раствора в гексанах, 126,2 ммоль) в течение 20 мин. Суспензию белого цвета перемешивают при температуре -78°С в течение 15 мин и при КТ в течение 15 мин, через указанный период времени получают прозрачный раствор светло-желтого цвета. Данный раствор канюлей переносят во вторую двугорлую колбу, содержащую Pd2(dba)3 (1,39 г, 1,51 ммоль) и (2'-дициклогексилфосфанил-бифенил-2-ил)-диметил-амин (1,25 г, 3,18 ммоль). После перемешивания при КТ в течение 10 мин прозрачный раствор темно-красного цвета охлаждают до температуры -10°С. Трет-бутиловый эфир уксусной кислоты (15,7 мл, 13,5 г, 116,1 ммоль) добавляют в течение 5 мин. После выдерживания в течение 10 мин при температуре -10°С добавляют 1,3-дихлор-изохинолин (10,0 г, 50,49 ммоль) в одной порции. Раствору темно-красного цвета дают нагреться до КТ. Через 30 мин выдерживания при КТ анализ с помощью ТСХ показывает полное превращение исходного материала. Реакционную смесь фильтруют через слой оксида кремния толщиной 2 см, который промывают EtOAc/MeOH 98:2. После концентрирования остаток очищают с помощью УКХ (толуол/CH2Cl2 2:1 до толуол/EtOAc 100:0 до 99:1, до 98:2, до 97:3, до 96:4, до 94:6, до 90:10) для получения трет-бутилового эфира (3-хлор-изохинолин-1-ил)-уксусной кислоты. Данное соединение растворяют в насыщенном этаноловом растворе HCl (200 мл) и нагревают с обратным холодильником в течение 15 мин. Концентрирование приводит к получению титульного соединения с количественным выходом. Данные 1Н ЯМР-спектрометрии (ДМСО, 400 МГц) δ 1,17 (t, J=8,8, 3Н), 4,11 (q, J=8,8, 2Н), 4,28 (s, 2H), 7,51-7,57 (m, 1H), 7,61 (s, 1H), 7,61-7,66 (m, 1H), 7,72 (d, J=8,8, 1H), 7,98 (d, J=8,8, 1H); ES-MS: 250 [М+Н]+.
Согласно процедуре, соответствующей примеру 163, но при использовании соответствующих исходных материалов могут быть получены соединения формулы I, в которой R представляет собой остаток формулы (д), как показано в таблице 5.
Соединения формулы I в свободной форме или в форме фармацевтически приемлемой соли проявляют ценные фармакологические свойства, например ингибируют активность протеинкиназы С (ПКС), например изоформ ПКС, таких как α, β, δ, ε, η или θ, подавляют активацию и пролиферацию Т-клеток, например путем ингибирования продукции Т-клеток или цитокинов, например ИЛ-2, посредством подавления пролиферативного ответа Т-клеток или цитокинов, например ИЛ-2, например, как показано в тестах in vitro и in vivo, и на основании этого предложено их терапевтическое применение.
A. In vitro
1. Анализ с использованием протеинкиназы С
Соединения формулы I тестируют на активность в отношении различных изоформ ПКС согласно опубликованному методу (см. D. Geiges et al., Biochem. Pharmacol., 1997, 53:865-875). Анализ проводят в 96-луночной полипропиленовой плате для микротитрования (Costar 3794), которую предварительно силиконизируют с использованием Sigmacote® (Sigma SL-2). Реакционная смесь (50 мкл) содержит 10 мкл соответствующего изомера ПКС, а также 25 мкл тест-соединения и 15 мкл смешанного раствора, который содержит 200 мг/мл сульфата протамина, 10 мМ Mg(NO3)2, 10 мкМ АТФ (Boehringer 519987) и 3750 Бк 33Р-АТФ (Hartmann Analytic SFC301, 110 ТБк/ммоль) в 20 мМ Трис-буфере рН 7,4+0,1% БСА (бычьего сывороточного альбумина). Инкубирование проводят в течение 15 мин при температуре 32°С в термостате со встряхиванием для плат для микротитрования (Biolabo Scientific Instruments). Реакцию останавливают добавлением 10 мкл 0,5 М Na2ЭДТК (этилендиаминтетрауксусной кислоты), рН 7,4. 50 мкл смеси пипеткой наносят на предварительно увлажненную фосфоцеллюлозную бумагу (Whatmann 3698-915) при осторожном надавливании. Неинкорпорированную АТФ отмывают с использованием 100 мкл бидистиллированной H2O. Бумагу дважды промывают в 0,5% Н3PO4 в течение 15 мин, а затем в течение 5 мин в EtOH. После этого бумагу сушат и помещают в универсальный фильтр (Packard 6005219) и накрывают слоем Microscint-O (Packard 6013611) в количестве 10 мл/лунку перед подсчетом в счетчике радиоактивности Topcount (Packard). Измерение IC50 (50% подавляющей или ингибирующей концентрации) проводят на рутинной основе путем инкубирования серийного разведения ингибитора в концентрациях, лежащих в интервале от 1 до 1000 мкМ согласно нижеописанному методу. Значения IC50 рассчитывают с помощью графика в виде эмпирической сигмоидальной кривой.
2. Анализ протеинкиназы С θ
Человеческую рекомбинантную ПКС θ используют в условиях анализа, как описано выше. В данном анализе соединения формулы I ингибируют ПКС θ с IC50≤1 мкМ. Соединение, соответствующее Примерам 33 и 69, ингибирует ПКС θ в данном анализе с IC50 6,8 и 12,1 нМ, соответственно.
3. Анализ протеинкиназы Сα
Человеческую рекомбинантную ПКСα получают из фирмы Oxford Biomedical Research и используют в условиях анализа, как описано выше в Разделе A.1. В данном анализе соединения формулы I ингибируют ПКСα с IC50≤1 мкМ. Соединение, соответствующее примеру 29, ингибирует ПКСα в данном анализе с IC50 4,3 нМ.
4. Анализ протеинкиназы С β1
Человеческую рекомбинантную ПКСβ1 получают из фирмы Oxford Biomedical Research и используют в условиях анализа, как описано выше в Разделе A.1. В данном анализе соединения формулы I ингибируют ПКСβ1 с IC50≤1 мкМ. Соединение, соответствующее Примеру 33, ингибирует ПКСβ1 в данном анализе с IC50 19,6 нМ.
5. Анализ протеинкиназы Сδ
Человеческую рекомбинантную ПКСδ получают из фирмы Oxford Biomedical Research и используют в условиях анализа, как описано выше в Разделе A.1. В данном анализе соединения формулы I ингибируют ПКСδ с IC50≤1 мкМ. Соединение, соответствующее Примеру 29, ингибирует ПКСδ в данном анализе с IC50 20 нМ.
6. Анализ протеинкиназы Cε
Человеческую рекомбинантную ПКСε получают из фирмы Oxford Biomedical Research и используют в условиях анализа, как описано выше в Разделе A.1. В данном анализе соединения формулы I ингибируют ПКСε с IC50≤1 мкМ. Соединение, соответствующее Примеру 69, ингибирует ПКСε в данном анализе с IC50 18 нМ.
7. Анализ протеинкиназы Cη
Человеческую рекомбинантную ПКСη получают из фирмы PanVera и используют в условиях анализа, как описано выше в Разделе А.1. В данном анализе соединения формулы I ингибируют ПКСη с IC50≤1 мкМ. Соединение, соответствующее примеру 29, ингибирует ПКСη в данном анализе с IC50 27,4 нМ.
8. Анализ костимуляции CD28
Анализ проводят на клетках Jurkat, трансфицированных конструкцией промотора/сигнального гена интерлейкина-2 человека, как описано в статье Baumann G et al. (см. Transplant.Proc. 1992; 24:43-8), причем сигнальный ген β-галактозидазы замещают геном люциферазы (см. статью de Wet J., et al., Mol. Cell Biol. 1987, 7(2), 725-737). Клетки стимулируют связанными с твердой фазой антителами или форболмиристат ацетатом (ФМА) и ионофором Са++ иономицином следующим образом. Для опосредованной антителом стимуляции планшеты для микротитрования Microlite TM1 (Dynatech) покрывают козьими антителами IgG Fc против мыши (Jackson) в концентрации 3 мкг/мл в 55 мкл забуференного фосфатом солевого раствора (PBS)/лунку в течение трех часов при КТ. После удаления антитела планшеты блокируют инкубированием с 2% бычьим сывороточным альбумином (БСА) в PBS (300 мкл/лунку) в течение 2 ч при КТ. После трехкратного промывания с помощью 300 мкл PBS/лунку добавляют 10 нг/мл антител против Т-клеточного рецептора (WT31, Becton & Dickinson) и 300 нг/мл антител против CD28 (15Е8) в 50 мкл 2% БСА/PBS в качестве стимулирующих антител и инкубируют в течение ночи при температуре 4°С. Наконец, планшеты три раза промывают 300 мкл PBS/лунку. В отдельных планшетах готовят семь трехкратных серийных разведений тест-соединений в повторностях в среде для анализа (RPMI 1640/10% сыворотка телячьих эмбрионов (FCS), содержащая 50 мкМ 2-меркаптоэтанол, 100 ед./мл пенициллина и 100 мкг/мл стрептомицина), смешивают с трансфицированными клетками Jurkat cells (клон К22 290_Н23) и инкубируют в течение 30 мин при температуре 37°С в 5% СО2. Затем 100 мкл данной смеси, содержащей 1×105 клеток, переносят в планшеты для анализа, покрытые антителом. Параллельно 100 мкл инкубируют с 40 нг/мл ФМА и 2 мкМ иономицина. После инкубирования в течение 5,5 ч при температуре 37°С в 5% CO2, определяют уровень люциферазы путем измерения биолюминесценции. Планшеты центрифугируют в течение 10 мин при 500 g и удаляют супернатант резким движением. Добавляют лизирующий буфер, содержащий 25 мМ Трис-фосфата, рН 7,8, 2 мМ ДТТ (дитиотреитол), 2 мМ 1,2-диаминоциклогексан-N,N,N',N-тетрауксусную кислоту, 10% (об/об) глицерин и 1% (об/об) Тритон Х-100 (20 мкл/лунку). Планшеты инкубируют при КТ в течение 10 мин при постоянном встряхивании. Активность люциферазы анализируют с помощью биолюминесцентного ридера (Labsystem, Helsinki, Finland) после автоматизированного добавления 50 мкл/лунку буфера для реакции люциферазы, содержащего 20 мМ Трицин, 1,07 мМ (MgCO3)4Mg(OH)2×5H2O, 2,67 мМ MgSO4, 0,1 мМ ЭДТА (этилендиаминтетрауксусная кислота), 33,3 мМ ДТТ, 270 мкМ кофермента А, 470 мкМ люциферина (Chemie Brunschwig AG), 530 мкМ АТФ, рН 7,8. Время запаздывания составляет 0,5 с, общее время измерения составляет 1 или 2 с. Контрольные значения нижнего уровня представляют собой световые единицы от клеток, стимулированных антителом против Т-клеточного рецептора или ФМА, контрольные значения высокого уровня получают от клеток, стимулированных антителами против Т-клеточного рецептора/антителами против CD28 или ФМА/иономицином без добавления какого-либо тест-образца. Контрольные значения нижнего уровня вычитают из всех значений. Ингибирование, полученное в присутствии тест-соединения, рассчитывают как процент ингибирования контрольного значения высокого уровня. Концентрацию тест-соединений, в результате приводящую к 50% ингибированию (IC50), определяют по кривым зависимости от дозы. В данном анализе соединения формулы I подавляют клетки Jurkat, стимулированные антителом против Т-клеточного рецептора/антителом против CD28 и ФМА/иономицином с IC50≤1 мкМ. Соединение, соответствующее Примеру 29, в данном анализе имеет IC50 20 нМ.
9. Реакция аллогенной смешанной культуры лейкоцитов (РСКЛ или СКЛ-реакция)
СКЛ-реакцию двух типов проводят согласно стандартным методикам (см. J. Immunol. Methods, 1973, 2, 279 и Мео Т. et al., Immunological Methods, New York, Academic Press, 1979, 227-39). Вкратце, клетки селезенки мышей СВА и BALB/c (1,6×10 клеток каждой линии/лунку в плоскодонных планшетах для микротитрования для тканевых культур, в целом 3,2×105) инкубируют в среде RPMI, содержащей 10% FCS, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина (Gibco BRL, Basel, Switzerland), 50 мкМ 2-меркаптоэтанола (Fluka, Buchs, Switzerland) и соединения в серийных разведениях. Делают семь трехкратных разведений в повторностях на тест-соединение. Через четверо суток инкубирования добавляют 1мкКи 3Н-тимидин. Клетки собирают через дополнительный четырехчасовой период инкубирования и определяют включенный 3Н-тимидин согласно стандартным методикам. Фоновые значения (контроль нижнего уровня) СКЛ-реакции представляют собой данные по пролиферации монокультуры клеток BALB/c. Значения контроля нижнего уровня вычитают из всех значений. Контрольные значения высокого уровня без содержания какого-либо образца принимают за 100% пролиферацию. Вычисляют процент подавления образцами и определяют концентрации, требующиеся для 50% подавления (значения IC50). В данном анализе соединение, соответствующее Примеру 29, имеет IC50 28 нМ. Соединения формулы I также демонстрируют значения IC50 в наномолярном (нМ) диапазоне при тестировании в СКЛ-реакции с использованием лейкоцитов человека.
10. Ингибирование GSK-3β
Анализ связывания GSK-3β проводят реакциях объемом 50 мкл в 96-луночных полипропиленовых планшетах, причем каждая реакция содержит 20 мМ хлорида магния, 40 мкМ АТФ, 2 мМ ДТТ, 88,5 мкМ биотинилированного и фосфорилированного CREB-пептидного субстрата (биотин-KRREILSRRPS(PO4)YR-OH; Q.M. Wang et al., J.Biol.Chem. 269, 14566-14574, 1994), [γ-33Р]АТФ (1 мкКи) и 2 мкл тестируемого соединения ДМСО (диметилсульфоксид) (в различных концентрациях). Добавляют 15 мкл GSK-3β (в различных концентрациях) и инкубируют смесь при температуре 30°С в течение 1 ч. Реакцию останавливают перенесением 25 мкл смеси на фосфоцеллюлозную пластинку, содержащую 130 мкл 1,85% фосфорной кислоты. Свободные радионуклиды в мембране отмывают под вакуумом 1,85% фосфорной кислотой (5 раз). После последнего промывания пластинку переносят на переходную плату, добавляют 50 мкл сцинтиляционной смеси (Microscint-20, Packard, cat. №20-133) в каждую лунку и подсчитывают уровень радиоактивности с помощью счетчика (top counter). Соединения формулы I проявляют активность в данном анализе. Соединения формулы I можно также тестировать с помощью других стандартных анализов связывания GSK-3β при использовании других субстратов, например, таких как имеющиеся в продаже.
В. In vivo
Трансплантация сердца у крыс
Используют комбинацию линий: самцы Lewis (RT1 гаплотип) и BN (гаплотип RT1). Животным проводят анестезию с использованием ингаляционного изофлуорана. После гепаринизации крысы-донора через брюшной отдел нижней полой вены при одновременном обескровливании через аорту вскрывают грудную клетку и быстро охлаждают сердце. Аорту лигируют и отделяют дистально по отношению к первой ветви и плечеголовной ствол отделяют на уровне первого разветвления. Левую легочную артерию лигируют и отделяют, правую сторону отделяют, но оставляют открытой. Все остальные сосуды препарируют, лигируют и отделяют, и сердце донора удаляют для помещения в ледяной физиологический раствор.
Подготовку реципиента осуществляют путем препарирования и пережатия подпочечной брюшной аорты и полой вены. Трансплантат имплантируют с помощью анастомозов типа "конец в бок" при использовании одноволоконного шовного материала 10/0 между плечеголовным стволом донора и аортой реципиента и правой легочной артерии донора к полой вене реципиента. Зажимы снимают, трансплантат соединяют ретроабдоминально, содержимое брюшной полости промывают теплым физиологическим раствором и животное зашивают и дают ему восстановиться под нагревательной лампой. Выживаемость трансплантата мониторируют путем ежедневной пальпации сокращений сердца донора через брюшную полость. Отторжение считают полным, когда сердце перестает сокращаться. Повышение выживаемости трансплантата получают у животных, которых лечат соединением формулы I, которое вводят перорально при суточной дозе от 1 до 30 мг/кг при приеме дважды в день.
Модель трансплантат против хозяина
Клетки селезенки (2×107) крыс Wistar/F вводят подкожной инъекцией в подушечку на подошве правой задней лапы гибридных крыс (Wistar/F x Fischer 344)F1. Подушечку задней левой лапы оставляют нелеченой. Животных лечат тест-соединениями в течение 4 последующих дней (0-3). В день 7 удаляют подколенные лимфатические узлы и определяют разницу в массе между двумя соответствующими лимфатическими узлами. Результаты выражают как подавление увеличения лимфатических узлов (приводят в процентах), сравнивая разницу в массах лимфатических узлов в экспериментальных группах с разницей в массах между соответствующими лимфатическим узлами групп животных, оставшихся нелечеными тест-соединением. В данном анализе подавление 100% получают при использовании соединения, соответствующего примеру 29, при введении в дозе 30 мг/кг/два раза в день.
Вследствие этого соединения формулы I эффективны для лечения и/или профилактики заболеваний или состояний, опосредуемых Т-лимфоцитами и/или ПКС, например, острого или хронического отторжения алло- или ксенотрансплантатов органов или тканей, болезней трансплантат против хозяина, атеросклероза, закупорки сосудов вследствие повреждения сосудов, такого как при ангиопластике, рестеноза, ожирения, синдрома X, нарушения толерантности к глюкозе, синдрома поликистоза яичников, гипертензии, сердечной недостаточности, хронической обструктивной легочной болезни, заболеваний ЦНС, таких как болезнь Альцгеймера или боковой амиотрофический склероз, рака, инфекционных заболеваний, таких как СПИД, септический шок или респираторный дистресс-синдром взрослых, ишемических/реперфузионных повреждений, например инфаркта миокарда, инсульта, ишемии кишки, почечной недостаточности или геморрагического шока, либо травматического шока, например травматического повреждения головного мозга. Соединения формулы I используют также для лечения и/или профилактики опосредованных Т-клетками острых или хронических воспалительных заболеваний или нарушений, либо аутоиммунных заболеваний, например ревматоидного артрита, остеоартрита, системной красной волчанки, тироидоза Хашимото, рассеянного склероза, злокачественной миастении, диабета типа I или II и связанных с ним нарушений, например ангиопатии, диабетической пролиферативной ретинопатии, диабетического макулярного отека, нефропатии, невропатии и синдрома Дауна, респираторных заболеваний, таких как астма или воспалительное повреждение легкого, воспалительных повреждений печени, воспалительных гломерулярных повреждений, кожных проявлений иммунологически опосредованных нарушений или болезней, воспалительных и гиперпролиферативных кожных заболеваний (таких как псориаз, атопический дерматит, аллергический контактный дерматит, контактный дерматит, вызываемый раздражающими веществами, и другие экзематозные дерматиты, себорейная экзема), воспалительных глазных заболеваний, например синдрома Шегрена, кератоконъюнктивита или увеита, воспалительной болезни кишки, болезни Крона или язвенного колита. Для вышеуказанных применений необходимая доза, конечно, будет варьироваться в зависимости от способа введения, конкретного состояния, лечение которого предусматривают, и необходимого эффекта. В общем, как показано, удовлетворительные результаты системно получают при суточных дозировках от приблизительно 0,1 до приблизительно 100 мг/кг массы тела. Необходимую суточную дозу для более крупного млекопитающего, например человека, которая лежит в интервале от приблизительно 0,5 мг до приблизительно 2000 мг, рекомендуют вводить, например, в разделенных дозах до четырех раз в сутки или в форме с пролонгированным действием.
Соединения формулы I можно ввести любым принятым образом, в частности энтерально, например перорально, например, в форме таблеток или капсул, или парентерально, например, в форме инъекционных растворов или суспензий, местно, например, в форме лосьонов, гелей, мазей или кремов, или в назальной форме, или в форме суппозиториев. Фармацевтические композиции, содержащие соединение формулы I в свободной форме или в форме фармацевтически приемлемой соли в сочетании с по меньшей мере одним фармацевтически приемлемым носителем или разбавителем, можно приготовить принятым образом посредством смешивания с фармацевтически приемлемым носителем или разбавителем. Унифицированные дозированные формы для перорального применения содержат, например, от приблизительно 0,1 мг до приблизительно 500 мг активной субстанции.
Наружное нанесение осуществляют, например, на кожу. Другой формой наружного применения является нанесение на глаз.
Соединения формулы I можно применять в свободной форме или в форме фармацевтически приемлемой соли, например, как указано выше. Данные соли могут быть получены принятым путем и иметь такой же порядок активности, что и свободные соединения.
В соответствии с вышеизложенным данное изобретение далее представляет:
1.1. Способ профилактики или лечения нарушений или заболеваний, опосредованных Т-лимфоцитами и/или ПКС либо GSK-3β, например, как указано выше, у субъекта, нуждающегося в таком лечении, причем способ включает введение субъекту эффективного количества соединения формулы I или его фармацевтически приемлемой соли.
1.2. Способ профилактики или лечения острого или хронического отторжения трансплантата или опосредованных Т-клетками воспалительных или аутоиммунных заболеваний, например, как указано выше, у субъекта, нуждающегося в таком лечении, причем способ включает введение субъекту эффективного количества соединения формулы I или его фармацевтически приемлемой соли.
2. Соединение формулы I в свободной форме или в форме фармацевтически приемлемой соли для применения в качестве фармацевтического препарата, например, в любом из способов, как указано в пунктах 1.1 и 1.2 выше.
3. Фармацевтическую композицию, например, для применения в любом из способов, как в пунктах 1.1 и 1.2 выше, включающую соединение формулы I в свободной форме или в форме фармацевтически приемлемой соли в сочетании с его фармацевтически приемлемым разбавителем или носителем.
4. Соединение формулы I или его фармацевтически приемлемую соль для использования при приготовлении фармацевтической композиции для применения в любом из способов, как указано в пунктах 1.1 и 1.2 выше.
Соединения формулы I могут применяться в виде монокомпонентного активного ингредиента или в комбинации с другими лекарственными препаратами в схемах иммуномодуляции или с другими противовоспалительными агентами, например, для лечения или профилактики острого или хронического отторжения алло- или ксенотрансплантата или воспалительных либо аутоиммунных нарушений. Например, их можно использовать в комбинации с циклоспоринами или аскомицинами или их аналогами либо производными, обладающими иммунодепрессивными свойствами, например циклоспорином A, ISA T×247, FK-506, ABT-281, ASM 981, с ингибитором mTOR, например рапамицином, 40-O-(2-гидрокси)этилрапамицином, CCI779, АВТ578 или рапалогом, например АР23573 и т.п., с кортикостероидами, циклофосфамидом, азатиопреном, метотрексатом, агонистом рецептора EDG, обладающим свойствами ускорения хоминга лимфоцитов, например FTY 720 или его аналогом; лефлуномидом или его аналогами, мизорибином, микофеноловой кислотой, мофетилмикофенолятом, 15-дозоксиспергуалином или его аналогами, иммунодепрессивными моноклональными антителами, например, моноклональными антителами к рецепторам лейкоцитов, например МНС, CD2, CD3, CD4, CD 11a/CD18, CD7, CD25, CD 27, В7, CD40, CD45, CD58, CD 137, ICOS, CD150 (SLAM), OХ40, 4-1BB и их лигандам, например CD154, или другими иммуномодулирующими соединениями, например рекомбинантными связывающими молекулами, включающими по меньшей мере часть экстрацеллюларного домена CTLA4 или его мутанта, например по меньшей мере экстрацеллюларную часть CTLA4 или его мутанта, связанную с последовательностью белка не-CTLA4, например CTLA4Ig (например обозначаемую АТСС 68629) или его мутанта, например LEA29Y, либо другими ингибиторами молекулы адгезии, например mAbs (моноклональными антителами) или низкомолекулярными ингибиторами, включая антагонисты LFA-1, антагонисты селектина и антагонисты VLA-4. Соединения формулы I могут также применяться вместе с антипролиферативным лекарственным препаратом, например химиотерапевтическим лекарственным препаратом, например таким, как используют при лечении рака, включая без ограничения перечисленным ингибиторы ароматазы, антиэстрогены, ингибиторы топоизомеразы I, ингибиторы топоизомеразы II, агенты, активные в отношении микротрубочек, алкилирующие агенты, ингибиторы гистондезацетилазы, ингибиторы фарнезилтрансферазы, ингибиторы СОХ-2, ингибиторы ММР, ингибиторы mTOR, противоопухолевые антиметаболиты, соединения платины, соединения, снижающие активность протеинкиназы, и другие антиангиогенные соединения, агонисты гонадорелина, антиандрогены, бенгамиды, бисфосфонаты, антипродиферативные антитела и темозоламид, или с антидиабетическим лекарственным препаратом, стимулятором секреции инсулина или соединением, усиливающим секрецию инсулина, например сульфонилмочевиной, например толбутамидом, хлорпропамидом, толазамидом, ацетогексамидом, 4-хлор-N-[(1-пиролидиниламино)карбонил]-бензолсульфонамидом (гликопирамидом), глибенкламидом (глибуридом), гликлазидом, 1-бутил-3-метанилилмочевиной, карбутамидом, глибонуридом, глипизидом, глисоксепидом, глибутиазолом, глибузолом, глигексамидом, глимидином, глипинамидом, фенбутамидом или толилцикламидом, пероральным производным инсулинотропного агента, например быстродействующим стимулятором инсулина, например меглитинидом, репаглинидом, производным фенилуксусной кислоты, например натеглинидом, ингибитором DPP IV, например 1-{2-[(5-цианопиридин-2-ил)амино]этиламино}ацетил-(2S)-циано-пирролидин дигидрохлоридом, LAF237, GLP-1 или аналогом агониста GLP-1, либо агентом, повышающим чувствительность к инсулину, например агонистом активируемого пероксисомным пролифератором рецептора γ (PPARγ), например глитазоном, агентом неглитазонового типа, таким как аналог N-(2-бензоилфенил)-L-тирозина, например GI-262570, или оксолидиндионом, например JTT501, двойным агонистом PPARγ/PPARα, например DRF-554158, NC-2100 или NN-622, агонистом рецептора ретиноида Х или рексиноидом, например 2-[1-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтил)-циклопропил]-пиридин-5-карбоновой кислотой, 4-[(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтил)-2-карбонил]-бензойной кислотой, 9-цис-ретиноевой кислотой или их аналогом, производным или фармацевтически приемлемой солью, при лечении диабета.
Согласно вышеизложенному, настоящее изобретение представлено в еще одном аспекте:
5. Способ, как определено выше, включающий совместное применение, например одновременное или последовательное, терапевтически эффективного количества ингибитора GSK-3β, ПКС или активации и пролиферации Т-клеток, например соединения формулы I в свободной форме или в форме фармацевтически приемлемой соли, и второй лекарственной субстанции, причем вторая лекарственная субстанция представляет собой иммунодепрессант, иммуномодулирующий, противовоспалительный, антипролиферативный или антидиабетический лекарственный препарат, например такой, как указано выше.
6. Терапевтическая комбинация, например набор, включающий а) ингибитор GSK-3β, ПКС или активации и пролиферации Т-клеток, например соединение формулы I в свободной форме или в форме фармацевтически приемлемой соли, и б) по меньшей мере один второй агент, выбранный из иммунодепрессанта, иммуномодулирующего, противовоспалительного, антипролиферативного и антидиабетического лекарственного препарата. Компонент а) и компонент б) могут быть использованы одновременно или последовательно. Набор может включать инструкции по применению.
Когда ингибитор GSK-3β, ПКС или активации и пролиферации Т-клеток, например соединение формулы I, вводят в сочетании с другим иммунодепрессантом/иммуномодулирующим, противовоспалительным, антипролиферативным или антидиабетическим терапевтическим препаратом, например, с целью профилактики или лечения острого или хронического отторжения трансплантата или воспалительных либо аутоиммунных нарушений, таких как определены выше в данном контексте, дозировки совместно применяемого иммунодепрессанта, иммуномодулирующего, противовоспалительного, антипролиферативного или антидиабетического соединения обязательно будут варьироваться в зависимости от типа используемого для совместного введения лекарственного препарата, например от того, является ли он стероидом или циклоспорином, от конкретного лекарственного препарата, который используют, от состояния, которое лечат, и т.д.
Соединения формулы I имеют интересный фармакокинетический профиль и интересные активности in vitro и in vivo.
| название | год | авторы | номер документа |
|---|---|---|---|
| Замещенные N2-(4-амино-2-метоксифенил)-N4-[2-(диметилфосфорил)-фенил]-5-хлор-пиримидин-2,4-диамины в качестве модуляторов ALK и EGFR, предназначенные для лечения рака | 2015 |
|
RU2607371C1 |
| ИЗОИНДОЛИНОНОВЫЕ ИНГИБИТОРЫ ВЗАИМОДЕЙСТВИЯ MDM2-P53, ОБЛАДАЮЩИЕ ПРОТИВОРАКОВОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2794333C1 |
| ХИНОЛИНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ SMO | 2015 |
|
RU2695815C2 |
| НОВЫЕ СОЕДИНЕНИЯ - АНТАГОНИСТЫ РЕЦЕПТОРА НЕЙРОКИНИНА 1 | 2013 |
|
RU2631319C2 |
| ТРИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, ОБЕСПЕЧИВАЮЩИЕ РАЗРУШЕНИЕ БЕЛКА IKAROS И БЕЛКА AIOLOS | 2020 |
|
RU2833608C2 |
| БЕНЗОКСАЗЕПИНОВЫЕ ИНГИБИТОРЫ PI3 И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2654068C1 |
| БЕНЗОКСАЗЕПИНОВЫЕ ИНГИБИТОРЫ PI3K И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2600927C2 |
| АНАЛОГИ СОЕДИНЕНИЙ 4Н-ПИРАЗОЛО[1,5-А]БЕНЗИМИДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ PARP | 2015 |
|
RU2672722C2 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКИХ АМИНОВ В КАЧЕСТВЕ АНТАГОНИСТОВ РЕЦЕПТОРА ЕР4 | 2011 |
|
RU2565596C2 |
| ДИАРИЛГИДАНТОИНЫ | 2011 |
|
RU2638833C2 |
Изобретение относится к соединениям формулы (I),
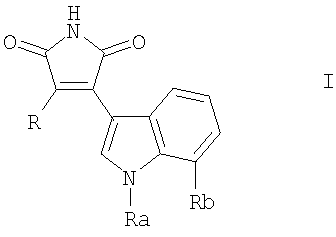
в которой Ra обозначает Н, СН3 или изопропил, Rb обозначает Н, галоген, C1-6алкокосигруппу или С1-6алкил, и либо
I. R обозначает радикал формулы (б)
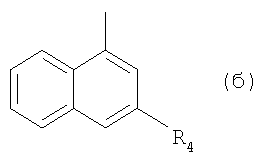
R4 обозначает 1-пиперазинил, замещенный СН3 в положениях 3 и/или 4, Ra отлично от Н или СН3, когда R4 обозначает 4-метил-1-пиперазинил; либо
III. R обозначает остаток формулы (в)
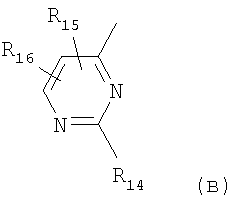
в которой R14 обозначает 1-пиперазинил, необязательно замещенный СН3 в положении 3; или 4,7-диаза-спиро[2.5]окт-7-ил, R15 обозначает галоген, CF3 или СН3, R15 отлично от СН3, когда R16 обозначает СН3, Ra обозначает Н или СН3, Rb обозначает Н, и R14 обозначает 4-метил-1-пиперазинил, и R16 обозначает Н, СН3 или CF3, R16 отлично от Н, когда R15 обозначает Cl, Ra обозначает Н или СН3, Rb обозначает Н, и R14 обозначает 4-метил-1-пиперазинил, либо
IV. R представляет собой радикал формулы (г)
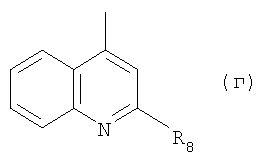
в которой R8 обозначает 1-пиперазинил, 3-метил-пиперазин-1-ил или 4-бензил-пиперазин-1-ил, либо
V. R представляет собой радикал формулы (д)
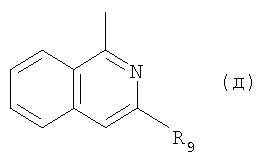
в которой R9 обозначает 4,7-диаза-спиро[2,5]окт-7-ил или пиперазин-1-ил, замещенный в положении 3- этилом, или его соль, способу их получения, фармацевтической композиции на их основе и применению для получения лекарственного средства для лечения и/или профилактики заболеваний либо нарушений, опосредованных Т-лимфоцитами и/или ПКС. 4 н. и 8 з.п. ф-лы, 5 табл.
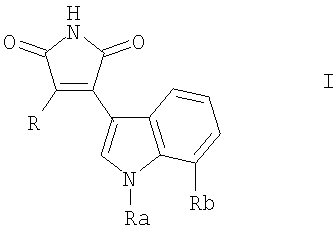
в которой Ra обозначает Н, СН3 или изопропил,
Rb обозначает Н, галоген, C1-6алкокосигруппу или C1-6алкил, и либо
I. R обозначает радикал формулы (б)

в которой R4 обозначает 1-пиперазинил, замещенный СН3 в положениях 3 и/или 4, Ra отлично от Н или СН3, когда R4 обозначает 4-метил- 1-пиперазинил; либо
III. R обозначает остаток формулы (в)
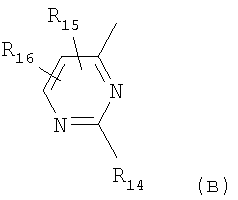
в которой R14 обозначает 1-пиперазинил, необязательно замещенный СН3 в положении 3; или 4,7-диаза-спиро [2.5]окт-7-ил,
R15 обозначает галоген, CF3 или СН3, R15 отлично от СН3, когда R16 обозначает СН3, Ra обозначает Н или СН3, Rb обозначает Н, и R14 обозначает 4-метил-1-пиперазинил, и
R16 обозначает Н, СН3 или CF3, R16 отлично от Н, когда R15 обозначает Cl, Ra обозначает Н или СН3, Rb обозначает Н, и R14 обозначает 4-метил-1-пиперазинил, либо
IV. R представляет собой радикал формулы (г)
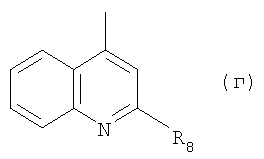
в которой R8 обозначает 1-пиперазинил, 3-метил-пиперазин-1-ил или 4-бензил-пиперазин-1-ил, либо
V. R представляет собой радикал формулы (д)
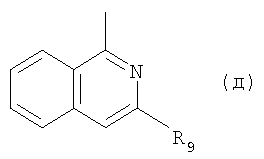
в которой R9 обозначает 4,7-диаза-спиро[2,5]окт-7-ил или пиперазин-1-ил, замещенный в положении 3-этилом, или его соль.

в котором Ra и Rb имеют значения, как определено в п.1, с соединением формулы III
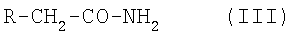
в котором R имеет значения, как определено в п.1,
и, в случае необходимости, превращение конечного соединения формулы I, полученного в свободной форме, в форму соли или наоборот.
Приоритет по пунктам:
| СПОСОБ ПОЛУЧЕНИЯ ТРИМЕТИЛХЛОРСИЛАНА | 0 |
|
SU210158A1 |
| 0 |
|
SU328026A1 | |
| Контактор устройства регулирования напряжения под нагрузкой | 1982 |
|
SU1120414A1 |
| Установка для пастеризации молока | 1961 |
|
SU146178A1 |
| ЗАМЕЩЕННЫЕ ПИРРОЛЫ И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1990 |
|
RU2142460C1 |
Авторы
Даты
2008-12-10—Публикация
2003-04-02—Подача