Изобретение относится к медицине, а именно к фармакологии и кардиологии, и может быть использовано для лечения дислипидемии.
В настоящее время в клинической практике используется ряд препаратов различного механизма действия, направленных на коррекцию нарушений липидного обмена с целью профилактики и лечения атеросклероза - ингибиторы ГМГ-КоА редуктазы (статины), ингибитор абсорбции холестерина в кишечнике (эзетимиб), секвестранты желчных кислот (ионно-обменные смолы), производные фиброевой кислоты (фибраты), никотиновая кислота, ω-3 полиненасыщенные жирные кислоты. У больных ишемической болезнью сердца, сахарным диабетом с гиперлипидемией препаратами выбора для медикаментозной терапии являются статины (Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. // Приложение 3 к журналу «Кардиоваскулярная терапия и профилактика». 2007, №6(6), с.41).
У больных ишемической болезнью сердца и сахарным диабетом с нарушениями липидного обмена препаратами выбора для медикаментозной терапии являются статины (Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Краткие Российские рекомендации. Разработаны группой экспертов секции атеросклероза ВНОК. // Приложение 3 к журналу «Кардиоваскулярная терапия и профилактика», 2007, №6(6), с.41).
Проведенные исследования показали, что статины в Российской Федерации в течение 3 лет принимают менее 6% больных. В то время как для достижения реального эффекта терапия должна продолжаться длительно, по сути, пожизненно. Однако низкая приверженность пациентов к лечению или внезапное прекращение приема лекарственных препаратов может явиться самостоятельным патогенетическим фактором, усугубляющим имевшиеся ранее нарушения, что способно оказать значительное влияние на течение атеросклеротического процесса.
Технический результат заключается в пролонгировании гиполипидемического эффекта ловастатина.
Сущность изобретения заключается в том, что в способе профилактики нарушений липидного обмена, включающем прием перорально ловастатина, дополнительно вводят 3-окси-6-метил-2-этил-пиридина сукцинат в дозе 0,7 мг/кг внутримышечно ежедневно 1 раз в сутки в течение 10 дней.
3-окси-6-метил-2-этил-пиридина сукцинат (мексидол) широко применяется в различных областях медицины. Благодаря своему механизму действия и широкому спектру фармокологических эффектов 3-окси-6-метил-2-этил-пиридина сукцинат оказывает влияние на основные звенья патогенеза различных заболеваний, связанных с процессами свободно-радикального окисления.
Способ осуществляют следующим образом. На фоне введения ловастатина в среднетерапевтической дозе дополнительно внутримышечно вводят 3-окси-6-метил-2-этил-пиридина сукцинат также в среднетерапевтической дозе, равной 0,7 мг/кг, ежедневно 1 раз в сутки в течение 10 дней.
Предложенные свойства 3-окси-6-метил-2-этил-пиридина сукцината иллюстрируются следующими примерами.
Пример 1
Использовалась модель дислипидемии осуществленная путем ежедневного введения масляного раствора холестерина в дозе 40 мг/кг/сут и, в качестве прооксиданта, витамина D2 в дозе 25000 МЕ/кг в течение 40 суток per os. Контрольную группу составили 10 животных, не получавших фармакологическую коррекцию. Животным 1-й группы (n1=10) с 21-х по 30-е сутки эксперимента вводили ловастатин в дозе 3,5 мг/кг перорально ежедневно 1 раз в сутки. Доза ловастатина рассчитывалась исходя из среднетерапевтической (40 мг в сутки на человека) с учетом межвидового переноса доз (Freireich E.J., Lehan Е., Rall D. et al, 1966).
Во 2-й опытной группе (n2=10) проводилось комбинированное введение 3-окси-6-метил-2-этил-пиридина сукцината (мексидола) (внутримышечно 5 мг/кг ежедневно 1 раз в сутки, что соответствует дозе 0,7 мг/кг для человека с учетом межвидового переноса доз) и ловастатина (в указанной выше дозе, соответствующей средней терапевтической). Животные выводились из эксперимента на 41-е сутки. Исследовали содержание общего холестерина (ОХС) в сыворотке крови - по методу Илька; холестерина липопротеидов низкой плотности (ХС ЛПНП) - по методу Бурштейна; холестерина липопротеидов высокой плотности (ХС ЛПВП) - по методу Абель после гепарин-марганцевой преципитации и осаждения из сыворотки липопротеидов низкой плотности (ЛПНП); содержание триглицеридов (ТГ) определяли при помощи диагностических наборов «Лахема» (Чехия); индекс атерогенности рассчитывали по формуле [ИА=(ОХС-ХС ЛПВП)/ХС ЛПВП (усл.ед.)], содержание холестерин липопротеидов очень низкой плотности рассчитывали по формуле [ХС ЛПОНП=ТГ/2,2].
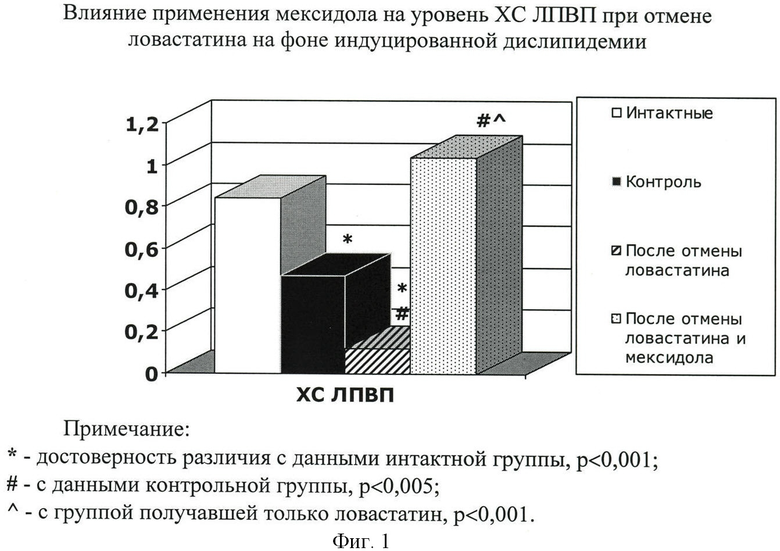
В результате эксперимента, при моделировании холестериновой дислипидемии, в контрольной группе на 41-е сутки содержание общего холестерина не было повышено по сравнению с данными животных интактной группы (0,97±0,08 и 1,13±0,07 ммоль/л, p>0,05). При этом значительного увеличения содержания ХС ЛПНП (0,40±0,04 и 0,49±0,04 ммоль/л, p>0,05) и ХС ЛПОНП (0,19±0,09 и 0,23±0,04, p>0,05) не зарегистрировано. Содержание триглицеридов к 41-м суткам эксперимента не отличалось от показателей животных интактной группы (0,43±0,20 и 0,52±0,08 ммоль/л, p>0,05). Снижение содержания ХС ЛПВП было достоверным (0,84±0,05 ммоль/л у интактных животных и 0,47±0,04 ммоль/л в контрольной группе, p<0,001). Расчетный индекс атерогенности возрос при этом в 9,7 раза (с 0,15±0,06 до 1,45±0,16 усл.ед., p<0,001).
В группе, получавшей только ловастатин, на десятые сутки после отмены препарата содержание общего холестерина не отличалось от контрольной группы (1,13±0,07 и 1,15±0,05 ммоль/л, р>0,05). Содержание ХС ЛПНП не менялось по сравнению с контролем (0,49±0,04 и 0,52±0,02 ммоль/л, р>0,05), но увеличивалось по сравнению с интактной группой (0,40±0,04 и 0,52±0,02 ммоль/л, р<0,05). Показатель ХС ЛПОНП увеличивался по сравнению с контрольной группой (с 0,23±0,04 до 0,35±0,03, р<0,05). Уровень триглицеридов превышал показатели интактной (0,43±0,20 по сравнению с 0,77±0,06 ммоль/л, р>0,05) и контрольной (с 0,52±0,08 до 0,77±0,06 ммоль/л, р<0,05) групп. Наблюдалось значительное снижение ХС ЛПВП - на 75% относительно контроля (с 0,47±0,04 до 0,12±0,01 ммоль/л, р<0,001). Индекс атерогенности резко возрос в 6,4 раза по сравнению с контрольной группой (с 1,45±0,16 по 9,34±0,83 усл.ед., р<0,001).
На десятые сутки после отмены мексидола и ловастатина содержание общего холестерина (1,29±0,11 ммоль/л) значительно не отличалось от контрольной группы (1,13±0,13 ммоль/л, р>0,05) и группы, получавшей только ловастатин (1,15±0,05 ммоль/л, р>0,05). Содержание холестерин липопротеидов низкой плотности также не менялось (0,58±0,07 ммоль/л) по сравнению с контрольной группой (0,49±0,04 ммоль/л, р>0,05) и с группой, получавшей только ловастатин (0,52±0,02 ммоль/л, р>0,05). Уровень ХС ЛПОНП (0,27±0,03) не отличался от показателей контрольной (0,23±0,04, р>0,05) и группы ловастатина (0,35±0,03, р>0,05). Содержание триглицеридов (0,59±0,07 ммоль/л) не отличалось от показателей животных контрольной группы (0,52±0,08 ммоль/л, р>0,05) и группы, получавшей только ловастатин (0,77±0,06 ммоль/л, р>0,05). Отмечался значительный рост содержания ХС ЛПВП (1,04±0,12 ммоль/л) по сравнению как с контрольной группой (0,47±0,04 ммоль/л, р<0,005), так и с группой, получавшей только ловастатин (0,12±0,01 ммоль/л, р<0,001). Это привело к снижению индекса атерогенности (до 0,29±0,04 усл.ед.) в 32,2 раза по сравнению группой, получавшей только ловастатин (9,34±0,83 усл.ед., р<0,001) и на 80% с контрольной группой (1,45±0,16 усл.ед., р<0,001)(табл.1, фиг.1, 2).
Таким образом, проведенные исследования выявили, что отмена ловастатина приводит к прогрессированию проатерогенных изменений сыворотки крови, наблюдающихся в условиях моделирования дислипидемии и проявляющихся в снижении антиатерогенных фракций холестерина, и значительном увеличении индекса атерогенности по сравнению с контрольной группой животных, не получавших какую-либо фармакологическую коррекцию. Дополнительное применение мексидола на фоне курсового введения ловастатина позволяет предотвратить прогрессирование нарушений липидного обмена, развивающееся на фоне отмены гиполипидемической терапии.
Пример 2
Исследование влияния мексидола на фоне сочетанной модели осуществлялось путем введения аллоксана в дозе 135 мг/кг внутрибрюшинно однократно и последующей ежедневной нагрузкой холестерином в дозе 40 мг/кг. Животные были распределены по опытным группам. Контрольную группу составило 10 животных, не получавших фармакологическую коррекцию. Животным 1-й группы (n1=10) с 21-х по 30-е сутки эксперимента вводили ловастатин в дозе 3,5 мг/кг перорально ежедневно 1 раз в сутки. Во 2-й опытной группе (n2=10) проводилось комбинированное введение мексидола (внутримышечно 5 мг/кг ежедневно 1 р/сут.) и ловастатина (в указанной выше дозе). Животные выводились из эксперимента на 41-е сутки. Исследовали содержание ОХС, ХС ЛПНП, ХС ЛПВП, ТГ; рассчитывали ИА и ХС ЛПОНП.
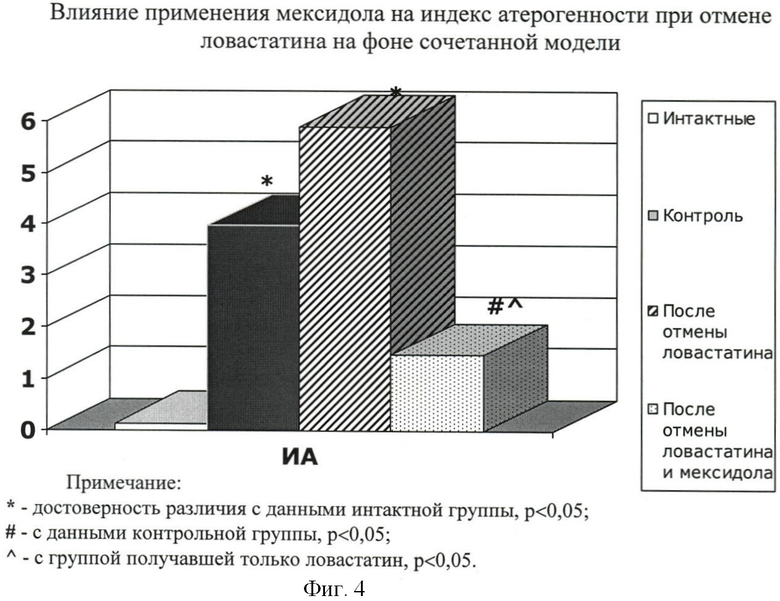
В результате эксперимента в контрольной группе животных на 41-е сутки содержание глюкозы было повышенно по сравнению с данными интактной группы в 3,1 раза (с 7,07±0,22 до 22,13±2,67 ммоль/л, р<0,005). ОХС превышал показатели интактной группы в 1,9 раза (с 0,97±0,08 до 1,84±0,06 ммоль/л, р<0,001). Уровень ХС ЛПВП снижался в 2,2 раза (с 0,84±0,05 до 0,39±0,05 ммоль/л, р<0,01). Содержание ХС ЛПНП, ХС ЛПОНП и ТГ превышали показатели интактной группы в 2,2, 2,6 и 2,8 раза соответственно (с 0,40±0,04 до 0,89±0,08 ммоль/л, р<0,01; с 0,11±0,03 до 0,29±0,03 ммоль/л, р<0,05 и с 0,23±0,07 до 0,64±0,06 ммоль/л, р<0,05). ИА увеличился в 26 раз (с 0,15±0,06 до 3,98±0,79 усл.ед., р<0,05).
В 1-й опытной группе на десятые сутки после отмены ловастатина содержание глюкозы не отличалось от контрольной группы (17,62±4,71 ммоль/л, р>0,05). Содержание ОХС не менялось по сравнению с контролем (1,19±0,05 ммоль/л, р>0,05). Уровень ТГ и ХС ЛПОНП превышал показатели интактной группы (0,61±0,09 ммоль/л по сравнению с 0,23±0,07 ммоль/л и 0,28±0,04 ммоль/л по сравнению с 0,11±0,03 ммоль/л; р<0,05), но не отличался от контрольной (р>0,05) группы. Наблюдалось снижение ХС ЛПВП - на 54% относительно контроля (до 0,18±0,03 ммоль/л, р<0,05) и ХС ЛПНП - на 37% (до 0,56±0,06 ммоль/л, р<0,05). Индекс атерогенности превышал показатели контрольной группы в 1,5 раза (с 3,98±0,79 до 5,903±0,869 усл.ед., p>0,05).
Во второй опытной группе на 10-е сутки после отмены мексидола и ловастатина содержание глюкозы (20,50±5,11 ммоль/л) и ОХС (1,63±0,49 ммоль/л) не отличалось от контрольной группы (p>0,05) и группы, получавшей только ловастатин (р>0,05). Содержание ХС ЛПНП, ТГ и ХС ЛПОНП не менялось по сравнению с контрольной группой (р>0,05) и с 1-ой опытной группой (р>0,05). Отмечался значительный рост содержания ХС ЛПВП (0,663±0,088 ммоль/л) по сравнению как с контрольной группой (на 70%, р<0,05), так и с 1-й опытной группой (в 3,7 раза, р<0,001). Это привело к снижению индекса атерогенности (1,47±0,45 ммоль/л) в 4 раза по сравнению с 1-й опытной группой (р<0,05) и на 63% с контрольной группой (р<0,05) (таб.2, рис.3, 4).
Таким образом, отмена ловастатина приводит к прогрессированию проатерогенных изменений сыворотки крови, наблюдающихся в условиях сочетанного моделирования дислипидемии и аллоксанового диабета, что проявляется в виде снижения антиатерогенных фракций холестерина и увеличении индекса атерогенности по сравнению с контрольной группой животных, не получавших какую-либо фармакологическую коррекцию.
По сравнению с известными решениями дополнительное введение 3-окси-6-метил-2-этил-пиридина сукцината на фоне курсового введения ловастатина позволяет предотвратить прогрессирование нарушений липидного обмена, развивающееся на фоне отмены гиполипидемической терапии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ НЕМЕДИКАМЕНТОЗНОГО СНИЖЕНИЯ ГИПЕРЛИПИДЕМИИ | 2010 |
|
RU2454973C1 |
| СПОСОБ НЕМЕДИКАМЕНТОЗНОГО СНИЖЕНИЯ ГИПЕРЛИПИДЕМИИ | 2012 |
|
RU2494747C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГИПОЛИПИДЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2004 |
|
RU2268714C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА У КРЫС | 2009 |
|
RU2394281C1 |
| СПОСОБ ПОСТАДИЙНОГО МОДЕЛИРОВАНИЯ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ У КРЫС | 2021 |
|
RU2770555C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ СТАБИЛЬНОЙ СТЕНОКАРДИЕЙ НАПРЯЖЕНИЯ | 2009 |
|
RU2401138C1 |
| Применение производного роданина 3-(2-фенилэтил)-2-тиоксо-1,3 тиазолидин-4-она для нормализации обмена веществ, повышения неспецифической резистентности, роста и развития животных | 2019 |
|
RU2768456C2 |
| СПОСОБ КОРРЕКЦИИ ЛИПОПЕРОКСИДАЦИИ ПРИ ГИПОЛИПИДЕМИЧЕСКОЙ ТЕРАПИИ ПАЦИЕНТОВ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ | 2011 |
|
RU2458687C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА У БОЛЬНЫХ ХРОНИЧЕСКИМ ХОЛЕЦИСТИТОМ | 2009 |
|
RU2403868C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПОЛИОРГАННОЙ ПАТОЛОГИИ У КРЫС | 2011 |
|
RU2453002C1 |


Изобретение относится к медицине, а именно к фармакологии и кардиологии, и касается профилактики нарушений липидного обмена. Для этого на фоне введения ловастатина в среднетерапевтической дозе дополнительно внутримышечно вводят 3-окси-6-метил-2-этил-пиридина сукцинат также в дозе 0,7 мг/кг ежедневно 1 раз в сутки в течение 10 дней. Способ обеспечивает пролонгацию гиполипидемического эффекта ловастатина после его отмены. 2 табл., 4 ил.
Способ профилактики нарушений липидного обмена при отмене ловастатина, включающий перед отменой прием перорально ловастатина в терапевтической дозе и 3-окси-6-метил-2-этил-пиридина сукцината внутримышечно в дозе 0,7 мг/кг ежедневно 1 раз в сутки в течение 10 дней.
| СРЕДСТВО ДЛЯ КОРРЕКЦИИ ИНСУЛИНОВОЙ РЕЗИСТЕНТНОСТИ | 1999 |
|
RU2158590C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГИПОЛИПИДЕМИЧЕСКИМ, АНТИОКСИДАНТНЫМ И ГИПОГЛИКЕМИЧЕСКИМ ДЕЙСТВИЕМ, ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО- СОСУДИСТЫХ И ЭНДОКРИННЫХ ЗАБОЛЕВАНИЙ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2003 |
|
RU2246964C1 |
| WO 2009070974 A1, 11.06.2009 | |||
| Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза | |||
| Краткие Российские рекомендации | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| EREN M | |||
| et | |||
Авторы
Даты
2011-07-10—Публикация
2009-10-26—Подача