Настоящее изобретение относится к лекарственному средству, более конкретно к новому ариламидразоновому производному, обладающему антагонистическим действием в отношении S1P3 рецепторов, и к лекарственному средству, содержащему такое соединение в качестве активного ингредиента.
Предпосылки изобретения
Как известно, S1P рецепторы, лигандом которых является сфингозин 1-фосфат (далее сокращенно указан как "S1P"), представляют собой тип рецепторов, связанных с G-белком, и играют важную роль in vivo. В настоящее время S1P рецепторы классифицированы на 5 подтипов (S1P1, S1P2, S1P3, S1P4 и S1P5).
S1P3 рецепторы экспрессируются в сосудистых эндотелиальных клетках или клетках гладкой мускулатуры сосудов в сердечно-сосудистой системе, и известно, что они воспринимают стимулирующее действие внеклеточного S1P и связываются с Gi, активируя MAPK (митоген-активируемая протеинкиназа), такую как ERK (регулируемая внеклеточным сигналом киназа), или с Gq/G12, активируя Rho (гомолог Ras). Таким образом, было сделано предположение, что S1P3 рецепторы связаны с развитием артериосклероза, утолщения интимы или сосудистых пролиферативных заболеваний, таких как солидные опухоли, диабетическая ретинопатия и т.п. Действительно, оказалось, что сурамин, который специфическим образом ингибирует S1P3 рецепторы, является эффективным для лечения в модели заболевания артериосклерозом. Таким образом, предполагается, что S1P3 рецептор-специфический антагонист является полезным в качестве профилактического или терапевтического средства в отношении этого заболевания (см. Непатентные Документы 1-8).
Кроме того, S1P3 рецепторы, как наблюдалось, также экспрессируются в клетках сердечной мышцы человека. S1P3 рецепторы индуцируют образование инозит 3-фосфата (IP3) через действие Gq, тогда как считается, что IP3 в клетках сердечной мышцы, который индуцируется при стимуляции рецептора ангиотензина II, влияет на развитие или прогрессирование гипертрофии сердца. Поэтому существует возможность того, что S1P3 рецепторы могут также влиять на гипертрофию сердца. Более того, поскольку продуцирование S1P увеличивается при гипоксическом стрессе, вызванном ишемией при остром инфаркте миокарда, есть предположение, что ишемическое реперфузионное расстройство может быть вызвано чрезмерной нагрузкой Ca2+ с вовлечением S1P3 рецепторов. Поэтому считают, что антагонист S1P3 рецептора будет полезным в качестве профилактического или терапевтического средства при гипертрофии сердца или ишемическом реперфузионном расстройстве после острого инфаркта миокарда (см. Непатентные Документы 9 и 10).
В то же время, поскольку S1P3 рецепторы специфически экспрессируются в клетках гладких мышц в базилярной артерии крыс или коронарных сосудов человека, исследования были сфокусированы на роли S1P3 рецепторов в этих органах. В экспериментах с использованием фронтальной базилярной артерии или коронарной артерии собаки S1P показал доза-зависимый сосудосуживающий эффект через действие Rho, что дает основание предположить, что S1P может представлять собой новое сосудосуживающее вещество или индуцирующее спазм вещество, которое действует через S1P3 рецепторы. Действительно, сосудосуживающее действие S1P в фронтальной базилярной артерии собаки ингибировалось сурамином или антисмысловым антителом к S1P3 рецептору. Поэтому следует отметить, что антагонист S1P3 рецептора является полезным в качестве профилактического или терапевтического средства при цереброваскулярном спазме после субарахноидального кровоизлияния, стенокардии или инфаркта миокарда, вызванного коронарным спазмом, или в качестве сосудорасширяющего средства (см. Непатентные Документы 10-14).
Также есть предположение, что S1P3 рецепторы возможно связаны с доза-зависимым сосудосуживающим эффектoм сфингозилфосфорилхолина в почечных капиллярах крысы или с пролиферацией мезангиальных клеток и, таким образом, могут играть важную роль в почечных заболеваниях, таких как гломерулонефрит. Поэтому также предполагается, что антагонист S1P3 рецептора является полезным для предотвращения развития прогрессирующего почечного расстройства (см. Непатентные Документы 15-18).
Однако хотя и сообщалось, что S1P промотирует экспрессию тканевого фактора (TF) в эндотелиальных клетках через действие ERK, S1P вместе с тромбином также индуцирует экспрессию S1P3 рецепторов, и, таким образом, предполагается, что S1P и S1P3 рецепторы действуют как положительный механизм обратной связи для промотирования экспрессии TF. Поэтому есть предположения, что S1P3 рецепторы также могут быть вовлечены в образование тромба при тромбозе (см. Непатентный Документ 19).
Более того, известна также взаимосвязь между S1P3 рецепторами и легочными заболеваниями, фибрилляцией предсердия или брадикардией. Например, поскольку S1P нарастающим образом продуцируется в трахее под действием воспалительных цитокинов, S1P при введении через трахею мышам синергически воздействует с TNF, вызывая отек легкого, который вызывается быстрым раскрытием плотного соединения через функцию S1P3 рецептора, как показано в эксперименте с использованием мышей с “выключенным” S1P3 рецептором. Поэтому есть предположения, что антагонист S1P3 рецептора является полезным в качестве профилактического или терапевтического средства от легочных заболеваний, вызванных отеком легких (респираторный дистресс-синдром взрослых (ARDS) и т.п.) (см. Непатентный Документ 20).
В другом эксперименте с использованием мышей с “выключенным” S1P3 рецептором также предполагалось, что S1P возможно активирует ацетилхолин-чувствительный поток K+ (IK, ACh) через действие S1P3 рецепторов, вызывая задержку водителя ритма синусно-предсердного узла, приводя, таким образом, к брадикардии. Кроме того, активация IK, ACh ведет к парасимпатетически-опосредованной фибрилляции предсердия, и, таким образом, предполагается, что антагонист S1P3 рецептора является полезным в качестве профилактического или терапевтического средства при брадикардии или парасимпатетически-опосредованной фибрилляции предсердия (см. Непатентный Документ 21).
Как можно видеть из вышесказанного, антагонист S1P3 рецептора является полезным в качестве профилактического или терапевтического средства при артериосклерозе; утолщении интимы; сосудистых пролиферативных заболеваниях, таких как солидные опухоли, диабетическая ретинопатия и т.п., сердечной недостаточности; ишемическом реперфузионном расстройстве; цереброваскулярном спазме после субарахноидального кровоизлияния; стенокардии или инфаркте миокарда, вызванном коронарным спазмом; прогрессирующих почечных заболеваний, таких как гломерулонефрит; тромбозе; легочных заболеваниях, вызванных отеком легких (ARDS и т.п.); брадикардии; парасимпатетически-опосредованной фибрилляции предсердия и т.п. или в качестве сосудорасширяющего средства.
Антагонист S1P3 рецепторов включает сурамин или антисмысловое антитело к S1P3, как описано выше.
Однако сурамин имеет молекулярную массу более чем 1200 и, таким образом, может иметь низкую пероральную абсорбцию. Антисмысловое антитело проблематично для крупномасштабного изготовления, и эффективность его включения для фармацевтического применения еще недостаточна. Фенилхинолинкарбоксамидные производные (см. Патентный Документ 1) и производные аминофенилпропионовой кислоты (см. Патентный Документ 2) раскрыты как низкомолекулярные антагонисты S1P3 рецепторов. Тиазолидиновые производные и тиазинановые производные (см. Патентный Документ 3), и ариламидные производные (см. Патентный Документ 12) также раскрыты как соединения, обладающие антагонистической функцией против S1P1 и S1P3 рецепторов. Однако эти соединения до настоящего времени не использовали для клинического применения. Были раскрыты другие соединения, демонстрирующие неселективное антагонистическое действие в отношении S1P рецепторов (см. Непатентные Документы 4-7); однако эффект этих соединений на S1P3 рецепторы неизвестен. Как обсуждалось выше, к настоящему времени существует потребность в S1P3 рецептор-селективном антагонисте, который является клинически применимым.
В то же время, что касается примеров соединения, имеющего ариламидразоновый скелет, как соединение по настоящему изобретению, Патентный Документ 8 раскрывает соединение, представленное приведенной ниже формулой (A):
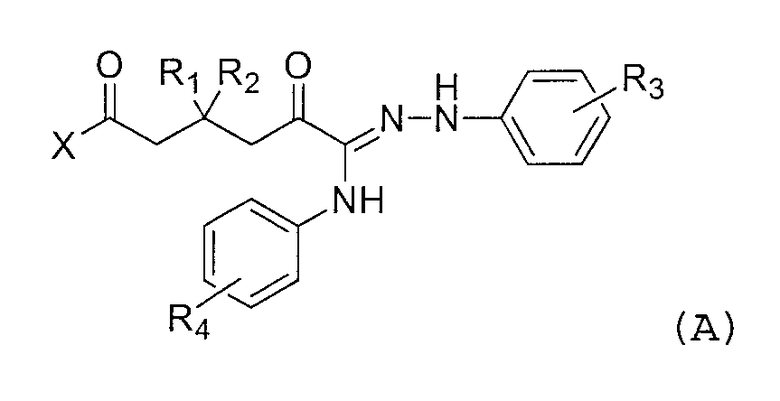
где R1 и R2, которые являются отличными друг от друга, каждый представляет собой атом водорода, метильную группу или т.п.; R3 представляет собой атом водорода, атом галогена или т.п.; R4 представляет собой атом водорода, атом галогена, нитрогруппу или т.п.; и X представляет собой алкоксигруппу, аминогруппу или т.п. Кроме того, Патентный Документ 9 раскрывает соединение, представленное приведенной ниже формулой (B):
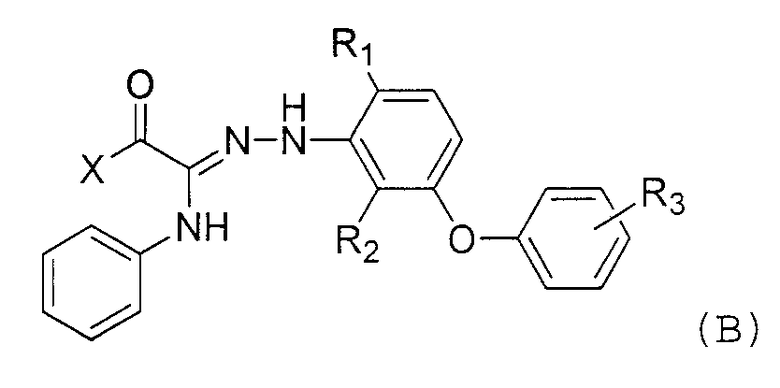
где R1 представляет собой атом водорода, алкильную группу или т.п.; R2 представляет собой атом водорода, нитрогруппу или т.п.; R3 представляет собой атом водорода, атом галогена или т.п.; и X представляет собой метильную группу, алкоксигруппу, аминогруппу или т.п. Непатентный Документ 22 раскрывает соединение, представленное приведенной ниже формулой (C):
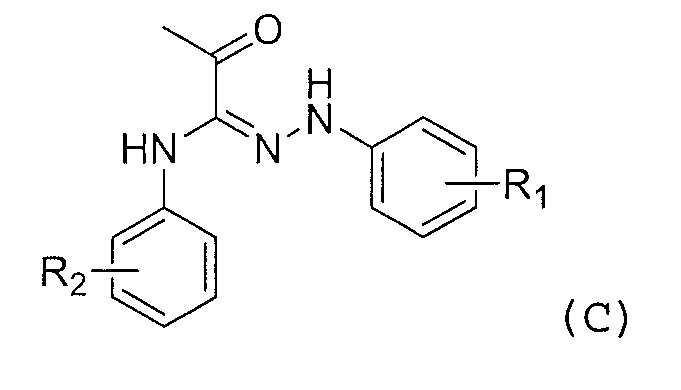
где R1 представляет собой атом галогена, метильную группу или т.п.; и R2 представляет собой атом водорода, атом галогена или т.п. Однако ни один из указанных выше документов не раскрывает данные, показывающие специфическое антагонистическое действие в отношении S1P3 рецепторов, как показано в настоящей заявке. Более того, Непатентный Документ 23 раскрывает соединение, представленное приведенной ниже формулой (D):
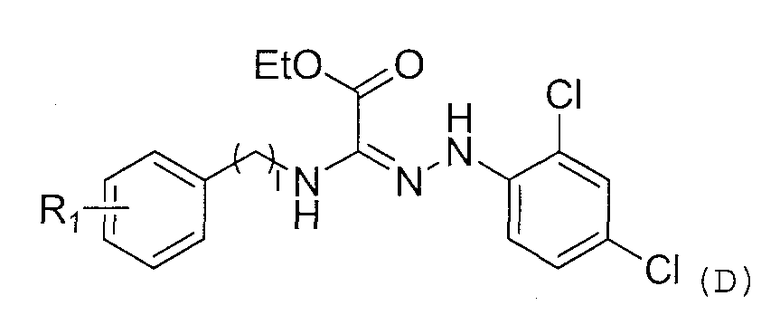
где l представляет собой целое число, имеющее значение 0 или 1; когда l имеет значение 0, R1 представляет собой атом водорода, 2-метильную группу, 4-метильную группу, 4-метоксигруппу или 4-этоксигруппу; и когда l имеет значение 1, R1 представляет собой атом водорода. Однако этот документ раскрывает только способ синтеза гидразидинового производного из этилацетоацетата, а соединение (D) описано только в Препаративном Примере, без какого-либо указания, какой эффект соединение будет оказывать на S1P3 рецепторы.
Кроме того, Патентные Документы 10 и 11 описывают соединение, имеющее ариламидразоновый скелет, в качестве промежуточного соединения для получения целевого вещества, но эти документы не раскрывают никакие данные, предполагающие специфическое антагонистическое действие на S1P3 рецепторы, как показано в настоящей заявке.
[Патентный Документ 1] JP-A-2002-332278
[Патентный Документ 2] JP-A-2005-247691
[Патентный Документ 3] WO 03/062392
[Патентный Документ 4] JP-A-2002-212070
[Патентный Документ 5] JP-A-2003-137894
[Патентный Документ 6] WO 03/040097
[Патентный Документ 7] WO 02/064616
[Патентный Документ 8] WO 92/19588
[Патентный Документ 9] JP-A-62-45568
[Патентный Документ 10] JP-A-54-3071
[Патентный Документ 11] DE 2724819 A
[Патентный Документ 12] WO 2006/063033
[Непатентный Документ 1] Cell, published by Cell Press, Vol. 99, p. 301-312 (1999)
[Непатентный Документ 2] Pharmacology & Therapeutics, published by Elsevier, USA, Vol. 88, p. 115-131 (2000)
[Непатентный Документ 3] Journal of Biological Chemistry, published by the American Society of Biochemistry and Molecular Biology, USA, vol. 276, p. 11830-11837 (2001)
[Непатентный Документ 4] American Journal of Respiratory Cell and Molecular Biology, published by the American Thoracic Society, USA, vol. 46, p. 711-719 (2001)
[Непатентный Документ 5] Blood, published by the American Society of Hematology, USA, vol. 102, p. 2099-2107 (2003)
[Непатентный Документ 6] Biochimica et Biophysica Acta, published by Elsevier, USA, vol. 1582, p. 190-196 (2002)
[Непатентный Документ 7] Circulation, published by the American Heart Association, USA, vol. 100, p. 861 (1999)
[Непатентный Документ 8] Cardiovascular Research, published by Elsevier, USA, vol. 28, p. 1166 (1994)
[Непатентный Документ 9] European Journal of Biochemistry, published by Blackwell Publishing, Inc., UK, vol. 267, p. 5679-5686 (2000)
[Непатентный Документ 10] The Journal of Histochemistry и Cytochemistry, published by the Histochemical Society, USA, vol. 50, p. 661-670 (2002)
[Непатентный Документ 11] Circulation Research, published by the American Heart Association, USA, vol. 91, p. 151-157 (2002)
[Непатентный Документ 12] Stroke, published by the American Heart Association, USA, vol. 32, p. 2913-2919 (2001)
[Непатентный Документ 13] European Journal of Biochemistry, published by Blackwell Publishing, Inc., UK, vol. 469, p. 125-134 (2003)
[Непатентный Документ 14] Arteriosclerosis, Thrombosis and Vascular Biology, published by the American Heart Association, USA, vol. 24, p. 918-922 (2004)
[Непатентный Документ 15] Biochemical and Biophysical Research Communications, published by Elsevier, USA, vol. 260, p. 203-208 (1999)
[Непатентный Документ 16] British Journal of Pharmacology, published by Nature Publishing Групп, UK, vol. 130, p. 1871-1877 (2000)
[Непатентный Документ 17] Genes Cells, published by Blackwell Publishing, Inc., UK, vol. 7, p. 1217-1230 (2002)
[Непатентный Документ 18] The 29th Eastern Regional Meeting of the Japanese Society of Nephrology, Abstract, p. 614
[Непатентный Документ 19] Blood, published by the American Society of Hematology, USA, vol. 102, p. 1693-1700 (2003)
[Непатентный Документ 20] Proceedings of the National Academy of Sciences of the United States of America, published by the National Academy of Sciences, USA, vol. 102, p. 9270-9275 (2005)
[Непатентный Документ 21] The Journal of Pharmacology и Experimental Therapeutics, published by the American Society for Pharmacology и Experimental Therapeutics, USA, vol. 309, p. 758-768 (2004)
[Непатентный Документ 22] Journal of Medicinal Chemistry, published by the American Chemical Society, USA, vol. 45, p. 2123-2126 (2002)
[Непатентный Документ 23] Berichte der Deutschen Chemischen Gesellschaft, published by Ferd. Dummler's Verlagsbuchhandlung, vol. 50, p. 1478-1496 (1917)
Раскрытие изобретения
Задачи, решаемые настоящим изобретением
Задача настоящего изобретения состоит в обеспечении низкомолекулярного соединения, которое обладает антагонистическим действием на S1P3 рецепторы и, таким образом, является полезным в качестве фармацевтического продукта.
Средства решения задач
Принимая во внимание указанные выше обстоятельства, авторы настоящего изобретения предприняли попытку разработки антагониста рецептора S1P3 как фармацевтического продукта и осуществили поиск низкомолекулярных соединений, обладающих антагонистическим действием против S1P3 рецепторов. Авторы настоящего изобретения в результате обнаружили, что ариламидразоновое производное, представленное приведенной ниже формулой (1), или его фармацевтически приемлемая соль обладают отличной антагонистической активностью против S1P3 рецепторов.
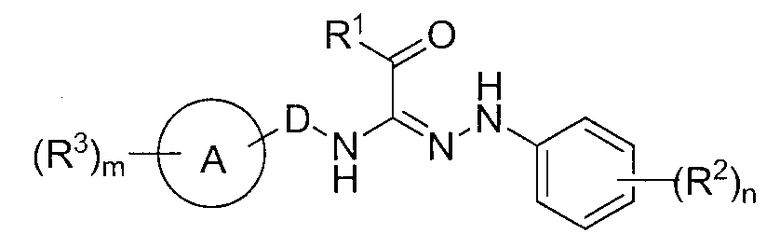
Таким образом, настоящее изобретение обеспечивает ариламидразоновое производное, представленное приведенной ниже формулой (1):
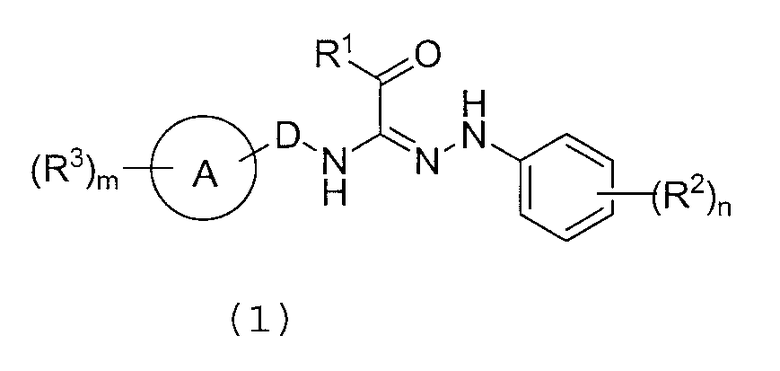
где R1 представляет собой C2-C8 алкильную группу, которая может быть замещена, фенильную группу, которая может быть замещена, ароматическую гетероциклическую группу, которая может быть замещена, C2-C8 алкоксигруппу, которая может быть замещена, или -NR4R5 (где R4 и R5, которые являются одинаковыми или отличными друг от друга, каждый представляет собой атом водорода или низшую алкильную группу, которая может быть замещена, или R4 и R5 могут объединяться со смежным атомом азота с образованием азот-содержащего гетероциклического кольца, которое может быть замещено);
R2 и R3, которые являются одинаковыми или отличными друг от друга, каждый представляет собой атом водорода, атом галогена, галоген-низшую алкильную группу, низшую алкильную группу, низшую алкинильную группу, низшую алкоксигруппу, цианогруппу, низшую алканоильную группу или низшую алкилсульфонильную группу;
A представляет собой бензольное кольцо или гетероциклическое кольцо;
D представляет собой простую связь или метилен;
m представляет собой целое число, имеющее значение от 1 до 3, и n представляет собой целое число, имеющее значение от 1 до 5 (при условии исключения соединений, характеризующихся нижеследующими условиями: когда R1 представляет собой этоксигруппу, R2 представляет собой 2,4-дихлоргруппу, R3 представляет собой атом водорода, А представляет собой бензольное кольцо и D представляет собой метилен; и случай, когда R1 представляет собой этоксигруппу, R2 представляет собой 2,4-дихлоргруппу, R3 представляет собой атом водорода, 2-метильную группу, 4-метильную группу, 4-метоксигруппу или 4-этоксигруппу, А представляет собой бензольное кольцо и D представляет собой простую связь),
или его фармацевтически приемлемую соль.
Кроме того, настоящее изобретение обеспечивает лекарственное средство, содержащее ариламидразоновое производное, представленное выше формулой (1), или его фармацевтически приемлемую соль в качестве активного ингредиента.
Настоящее изобретение обеспечивает фармацевтическую композицию, содержащую ариламидразоновое производное, представленное выше формулой (1), или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
Настоящее изобретение обеспечивает применение ариламидразонового производного, представленного выше формулой (1), или его фармацевтически приемлемой соли для получения лекарственного средства.
Кроме того, настоящее изобретение обеспечивает способ лечения артериосклероза, утолщения интимы, солидных опухолей, диабетической ретинопатии, сердечной недостаточности, ишемического реперфузионного расстройства, цереброваскулярного спазма после субарахноидального кровоизлияния, стенокардии или инфаркта миокарда, вызванного коронарным спазмом, гломерулонефрита, тромбоза, легочных заболеваний, вызванных отеком легких (ARDS), брадикардии и парасимпатетически-опосредованной фибрилляции предсердия, при этом способ включает введение ариламидразонового производного, представленного выше формулой (1), или его фармацевтически приемлемой соли.
Эффекты изобретения
Ариламидразоновое производное, представленное формулой (1) по настоящему изобретению, или его фармацевтически приемлемая соль обладают антагонистическим действием против S1P3 рецепторов и, таким образом, являются полезными в качестве профилактического или терапевтического средства при различных заболеваниях, вызванных стимуляцией S1P3 рецептора, например, артериосклерозе, утолщении интимы, сосудистых пролиферативных заболеваниях (солидных опухолей, диабетической ретинопатии и т.п.), сердечной недостаточности, ишемическом реперфузионном расстройстве, цереброваскулярном спазме после субарахноидального кровоизлияния, стенокардии или инфаркте миокарда, вызванного коронарным спазмом, прогрессирующих почечных расстройствах, таких как гломерулонефрит, тромбозе, легочных заболеваниях, вызванных отеком легких (ARDS и т.п.), брадикардии и парасимпатетически-опосредованной фибрилляции предсердия или т.п., или в качестве сосудорасширяющего средства.
Наиболее предпочтительный способ осуществления изобретения
В ариламидразоновом производном, представленном формулой (1), R1 представляет собой C2-C8 алкильную группу, которая может быть замещена, фенильную группу, которая может быть замещена, ароматическую гетероциклическую группу, которая может быть замещена, C2-C8 алкоксигруппу, которая может быть замещена, или -NR4R5.
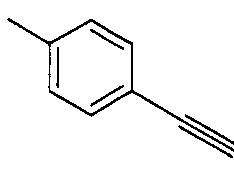
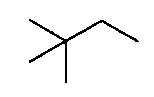
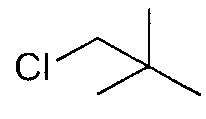
C2-C8 алкильная группа, которая может быть замещена, представленная как R1, включает линейную или разветвленную алкильную группу, содержащую от 2 до 8 атомов углерода, и циклическую алкильную группу, содержащую от 3 до 7 атомов углерода, такую как этильная группа, н-пропильная группа, изопропильная группа, 1-этилпропильная группа, 2,2-диметилпропильная группа, н-бутильная группа, изобутильная группа, втор-бутильная группа, трет-бутильная группп, н-пентильная группа, 2-пропилпентильная группа, н-гексильная группа, циклопентильная группа, циклогексильная группа и т.п. Из них линейная или разветвленная алкильная группа, содержащая от 2 до 6 атомов углерода, является предпочтительной, и линейная или разветвленная алкильная группа, содержащая от 2 до 4 атомов углерода, является более предпочтительной, при этом н-бутильная группа, трет-бутильная группа, 1-этилпропильная группа и 2,2-диметилпропильная группа являются еще более предпочтительными.
В данном случае, группа, которая может быть заместителем в C2-C8 алкильной группе, включает атом галогена, низшую алкоксигруппу и т.п.
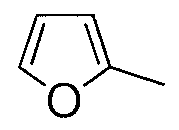
Фенильная группа, которая может быть замещена, и ароматическая гетероциклическая группа, которая может быть замещена, представленные как R1, включают фенильную группу и ароматическую гетероциклическую группу, незамещенную или замещенную 1-3 заместителями, расположенными в любых произвольных положениях. В данном случае, ароматическая гетероциклическая группа представляет собой 5-7-членное ароматическое кольцо, содержащее один или два атома кислорода, азота, серы или другие атомы, и конкретные примеры включают фурильную группу, тиенильную группу, пирролильную группу, пиридильную группу, пиримидильную группу и т.п., при этом фурильная группа, тиенильная группа и пиридильная группа являются предпочтительными. В качестве фенильной группы, которая может быть замещена, или ароматической гетероциклической группы, которая может быть замещена, фурильная группа, которая может быть замещена, является более предпочтительной. В данном случае, группа, которая может быть заместителем в фенильной группе или ароматической гетероциклической группе, включает атом галогена, низшую алкильную группу, галоген-низшую алкильную группу, низшую алкоксигруппу и т.п. Когда присутствуют два или более заместителей, можно использовать сочетание различных групп. Конкретные примеры замещенной фенильной группы включают толильную группу, трифторметилфенильную группу, метоксифенильную группу и т.п., тогда как конкретные примеры замещенной ароматической гетероциклической группы, и, в частности, примеры замещенной фурильной группы, включают хлорфурильную группу (например, 5-хлор-2-фурильную группу), бромфурильную группу (например, 3-бром-2-фурильную группу), метилфурильную группу (например, 2-метил-3-фурильную группу), этилфурильную группу (например, 2-этил-3-фурильную группу), метоксифурильную группу (например, 3-метокси-2-фурильную группу), этоксифурильную группу (например, 3-этокси-2-фурильную группу) и т.п.
C2-C8 алкоксигруппа, которая может быть замещена, представленная как R1, включает линейную или разветвленную алкоксигруппу, содержащую от 2 до 8 атомов углерода, и циклическую алкилоксигруппу, содержащую от 3 до 6 атомов углерода, такую как этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, изобутоксигруппа, втор-бутоксигруппа, трет-бутоксигруппа, н-пентилоксигруппа, 2-пропилпентилоксигруппа, н-гексилоксигруппа, циклопентилоксигруппа, циклогексилоксигруппа и т.п. Из них алкоксигруппа, содержащая от 2 до 6 атомов углерода, является предпочтительной, и алкоксигруппа, содержащая от 2 до 4 атомов углерода, является более предпочтительной, при этом этоксигруппа является еще более предпочтительной. В данном случае, группа, которая может быть заместителем в C2-C8 алкоксигруппе, включает атом галогена, низшую алкоксигруппу и т.п.
Кроме того, атом галогена, низшая алкильная группа, галоген-низшая алкильная группа или низшая алкоксигруппа, которые могут быть заместителем в группе, представленной как R1, имеют такие же значения, как и указанные ниже соответствующие группы, представленные как R2 и R3.
Заместители R2 и R3, которые являются одинаковыми или отличными друг от друга, каждый представляет собой атом водорода, атом галогена, галоген-низшую алкильную группу, низшую алкильную группу, низшую алкинильную группу, низшую алкоксигруппу, цианогруппу, низшую алканоильную группу или низшую алкилсульфонильную группу. Положения замещения для R2 и R3 конкретно не ограничены, но мета-положение или пара-положение является предпочтительным, при этом пара-положение является более предпочтительным. Количество заместителей для R2 (которое указано как n) составляет от 1 до 5, а для R3 (которое указано как m) составляет от 1 до 3, каждое из которых предпочтительно составляет от 1 или 2.
Атом галогена, представленный как R2 или R3, включает фтор, хлор, бром и иод, и из них фтор, хлор или бром является предпочтительным, при этом хлор является более предпочтительным.
Низшая алкильная группа, представленная как R2 или R3, включает алкильную группу, содержащую от 1 до 8 атомов углерода (C1-C8 алкильная группа). C1-C8 алкильная группа включает линейную или разветвленную алкильную группу, содержащую от 1 до 8 атомов углерода, и циклическую алкильную группу, содержащую от 3 до 7 атомов углерода, такую как метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, втор-бутильная группа, трет-бутильная группа, н-пентильная группа, 2-пропилпентильная группа, н-гексильная группа, циклопентильная группа, циклогексильная группа и т.п. Из них линейная C1-C8 алкильная группа является предпочтительной, и линейная алкильная группа, содержащая от 1 до 4 атомов углерода (C1-C4 алкильная группа), является более предпочтительной, при этом метильная группа является еще более предпочтительной.
Галоген-низшая алкильная группа, представленная как R2 или R3, означает указанную выше низшую алкильную группу, которая замещена указанным выше атомом галогена, и в качестве конкретного примера можно указать галоген-C1-C8 алкильную группу. Примеры галоген-низшей алкильной группы включают фторметильную группу, дифторметильную группу, трифторметильную группу, хлорметильную группу, дихлорметильную группу, трихлорметильную группу, 2-хлор-1,1-диметилэтильную группу и т.п. Из них галоген-C1-C6 алкильная группа является предпочтительной, и галоген-C1-C4 алкильная группа является более предпочтительной, при этом трифторметильная группа является еще более предпочтительной.
Низшая алкинильная группа, представленная как R2 или R3, включает линейную, разветвленную или циклическую углеводородную группу, содержащую от 2 до 6 атомов углерода и ненасыщенную тройную связь (C2-C6 алкинильная группа), такую как этинильная группа, 1-пропинильная группа, 2-пропинильная группа, 1-бутинильная группа, 2-бутинильная группа, 3-бутинильная группа, 3-метил-1-бутинильная группа, 4-метил-1-пентинильная группа и т.п. Из них алкинильная группа, содержащая от 2 до 4 атомов углерода (C2-C4 алкинильная группа), является предпочтительной, и этинильная группа является более предпочтительной.
Низшая алкоксигруппа, представленная как R2 или R3, включает алкоксигруппу, содержащую от 1 до 8 атомов углерода (C1-C8 алкоксигруппа). C1-C8 алкоксигруппа включает линейную или разветвленную алкоксигруппу, содержащую от 1 до 8 атомов углерода, и циклическую алкилоксигруппу, содержащую от 3 до 6 атомов углерода, такую как метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, изобутоксигруппа, втор-бутоксигруппа, трет-бутоксигруппа, н-пентилоксигруппа, 2-пропилпентилоксигруппа, н-гексилоксигруппа, циклопентилоксигруппа, циклогексилоксигруппа и т.п. Из них алкоксигруппа, содержащая от 1 до 6 атомов углерода (C1-C6 алкоксигруппа), является предпочтительной, и алкоксигруппа, содержащая от 1 до 4 атомов углерода (C1-C4 алкоксигруппа), является более предпочтительной, при этом метоксигруппа является еще более предпочтительной.
Низшая алканоильная группа, представленная как R2 или R3, включает линейную или разветвленную алканоильную группу, содержащую от 2 до 6 атомов углерода (C2-C6 алканоильная группа), такую как ацетильная группа, пропаноильная группа, бутаноильная группа и т.п. Из них алканоильная группа, содержащая от 2 до 4 атомов углерода (C2-C4 алканоильная группа), является предпочтительной, и ацетильная группа является более предпочтительной.
Низшая алкилсульфонильная группа, представленная как R2 или R3, означает сульфонильную группу, замещенную указанной выше низшей алкильной группой, и в качестве конкретного примера можно указать C1-C8 алкилсульфонильную группу. Примеры низшей алкилсульфонильной группы включают метансульфонильную группу, этансульфонильную группу и т.п. Из них C1-C6 алкилсульфонильная группа является предпочтительной, и C1-C4 алкилсульфонильная группа является более предпочтительной, при этом метансульфонильная группа является еще более предпочтительной.
R2 и R3, каждый, предпочтительно представляет собой атом водорода, атом галогена, линейную C1-C8 алкильную группу или C2-C6 алкинильную группу. Положение замещения для R2 и R3, предпочтительно, представляет собой мета-положение или пара-положение.
Для низшей алкильной группы, представленной как R4 или R5, которая может быть замещена, низшая алкильная группа имеет такое же значение, как низшая алкильная группа, представленная как R2 или R3, и низшая алкильная группа, которая может быть замещена, может содержать один-три заместителя. В данном случае, группа, которая может быть заместителем в низшей алкильной группе, включает указанные выше атом галогена или низшую алкоксигруппу.
R4 и R5, каждый, предпочтительно представляет собой атом водорода или трет-бутильную группу.
В случае, когда R4 и R5 объединены со смежным атом азота с образованием азот-содержащего гетероциклического кольца, которое может быть замещено, азот-содержащее гетероциклическое кольцо включает 5-7-членное насыщенное гетероциклическое кольцо или ненасыщенное гетероциклическое кольцо, такое как пиррольное кольцо, пирролидиновое кольцо, пиразольное кольцо, триазольное кольцо, пиперазиновое кольцо, пиперидиновое кольцо и т.п. Из них пиперидиновое кольцо является предпочтительным. Кольца также могут содержать один-четыре заместителя, расположенных в любых произвольных положениях. В данном случае, группа, которая может быть заместителем в азот-содержащем гетероциклическом кольце, включает атом галогена, низшую алкильную группу, фенильную группу, низшую алкоксигруппу или т.п., как указано выше.
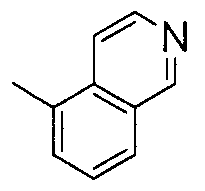
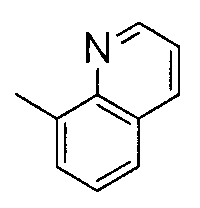
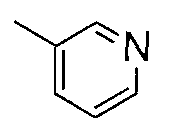
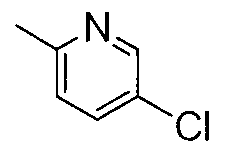
A представляет собой бензольное кольцо или гетероциклическое кольцо. Гетероциклическое кольцо, представленное как A, содержит, по меньшей мере, один или несколько атомов азота, кислорода или серы в кольце, и включает алициклическое или ароматическое гетероциклическое кольцо, которое может быть конденсированным с ароматическим кольцом. Примеры включают пиррольное кольцо, пиразольное кольцо, имидазольное кольцо, пиридиновое кольцо, пиразиновое кольцо, пиримидиновое кольцо, индольное кольцо, бензофурановое кольцо, хинолиновое кольцо, изохинолиновое кольцо, бензотиазольное кольцо, бензоксазольное кольцо и т.п., и из них пиридиновое кольцо, хинолиновое кольцо или изохинолиновое кольцо являются предпочтительными. A, предпочтительно, представляет собой бензольное кольцо, 2-пиридиновое кольцо, 3-пиридиновое кольцо, 4-пиридиновое кольцо, 5-хинолиновое кольцо, 8-хинолиновое кольцо, 5-изохинолиновое кольцо или 8-изохинолиновое кольцо, и более предпочтительно - бензольное кольцо.
D представляет собой простую связь или метилен, но более предпочтительно - простую связь.
Когда D представляет собой простую связь, соединение формулы (1) представлено приведенной ниже формулой (1a):
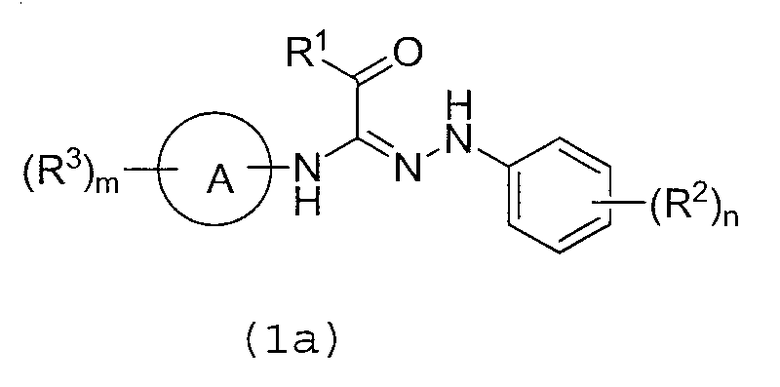
где R1 представляет собой C2-C8 алкильную группу, которая может быть замещена, фенильную группу, которая может быть замещена, ароматическую гетероциклическую группу, которая может быть замещена, C2-C8 алкоксигруппу, которая может быть замещена, или -NR4R5 (где R4 и R5, которые являются одинаковыми или отличными друг от друга, каждый представляет собой атом водорода или низшую алкильную группу, которая может быть замещена, или R4 и R5 могут объединяться со смежным атом азота с образованием азот-содержащего гетероциклического кольца, которое может быть замещено);
R2 и R3, которые являются одинаковыми или отличными друг от друга, каждый представляет собой атом водорода, атом галогена, галоген-низшую алкильную группу, низшую алкильную группу, низшую алкинильную группу, низшую алкоксигруппу, цианогруппу, низшую алканоильную группу или низшую алкилсульфонильную группу;
A представляет собой бензольное кольцо или гетероциклическое кольцо;
m представляет собой целое число, имеющее значение от 1 до 3, и n представляет собой целое число, имеющее значение от 1 до 5 (при условии исключения соединений, характеризующихся нижеследующими условиями: когда R1 представляет собой этоксигруппу, R2 представляет собой 2,4-дихлоргруппу, R3 представляет собой атом водорода, 2-метильную группу, 4-метильную группу, 4-метоксигруппу или 4-этоксигруппу, и A представляет собой бензольное кольцо).
Из соединений (1) по настоящему изобретению, каждый заместитель в формуле (1), предпочтительно, имеет указанное ниже значение, с точки зрения селективности в отношении S1P3 рецептора. В частности, R1, предпочтительно, представляет собой C2-C8 линейную или разветвленную алкильную группу, которая может быть замещена атомом галогена или C1-C8 алкильной группой, или фурильную группу, которая может быть замещена атомом галогена, C1-C8 алкильной группой, галоген-C1-C8 алкильной группой или C1-C8 алкоксигруппой, и более предпочтительно - линейную или разветвленную C2-C8 алкильную группу. R2 и R3, каждый, предпочтительно представляет собой атом водорода, атом галогена, линейную C1-C8 алкильную группу или C2-C6 алкинильную группу. Положение замещения для R2 и R3, предпочтительно, представляет собой мета-положение или пара-положение. m и n, каждый, предпочтительно, имеет значение 1 или 2. Кроме того, A, предпочтительно, представляет собой бензольное кольцо, и D, предпочтительно, представляет собой простую связь.
Настоящее изобретение также включает фармацевтически приемлемые соли соединения формулы (1). Конкретные примеры солей включают соли с неорганическими кислотами, такие как гидрохлорид, гидробромид, гидроиодид, сульфат, нитрат и фосфат; соли с органическими кислотами, такие как ацетат, трифторацетат, оксалат, фумарат, малеат, тартрат, мезилат и тозилат; и т.п. Соли соединения формулы (1) можно получить в соответствии со стандартными способами.
Соединение (1) по настоящему изобретению также включает гидраты и различные сольваты. Соединение по настоящему изобретению, кроме того, включает все его кристаллические формы.
Конкретные примеры соединения (1) по настоящему изобретению включают:
2-(4-хлорфенилгидразоно)-2-(3-фторфениламино)ацетофенон,
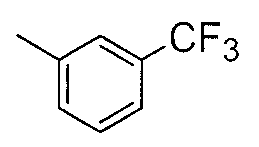
2-(4-хлорфенилгидразоно)-2-(3-трифторметилфениламино)-
ацетофенон,
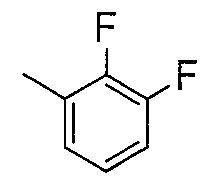
2-(4-хлорфенилгидразоно)-2-(2,3-дифторфениламино)-
ацетофенон,
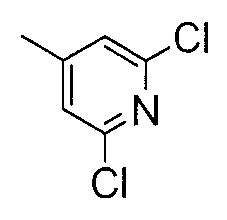
2-(4-хлорфенилгидразоно)-2-(2,6-дихлорпиридин-4-иламино)-ацетофенон,
2-(4-хлорфенилгидразоно)-2-[(4-фторфенил)метиламино]-
ацетофенон,
2-(4-хлорфенилгидразоно)-2-[(2,5-дифторфенил)метиламино]-ацетофенон,
2-(4-хлорфенилгидразоно)-2-[(3-трифторметилфенил)-
метиламино]ацетофенон,
2-(4-хлорфенилгидразоно)-2-(2-фторфениламино)ацетофенон,
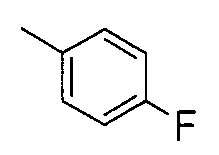
2-(4-хлорфенилгидразоно)-2-(4-фторфениламино)ацетофенон,
2-(2-хлорфениламино)-2-(4-хлорфенилгидразоно)ацетофенон,
2-(3-хлорфениламино)-2-(4-хлорфенилгидразоно)ацетофенон,
2-(4-хлорфениламино)-2-(4-хлорфенилгидразоно)ацетофенон,
этил 1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)ацетат,
этил 1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)ацетат,
этил 1-(4-хлорфенилгидразоно)-1-[(2,5-дифторфенил)метиламино]ацетат,
этил 1-(4-хлорфенилгидразоно)-1-(3-трифторметилфениламино)ацетат,
этил 1-(4-хлорфенилгидразоно)-1-(3,5-дифторфениламино)ацетат,
этил 1-(4-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)ацетат,
этил 1-(4-хлорфенилгидразоно)-1-(фениламино)ацетат,
этил 1-(4-хлорфенилгидразоно)-1-(3-цианофениламино)ацетат,
[1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)ацетил]пиперидин,
[1-(4-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)ацетил]пиперидин,
[1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)ацетил]-пиперидин,
[1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)ацетил]-пиперидин,
[1-(4-хлорфенилгидразоно)-1-(3,5-дифторфениламино)ацетил]-пиперидин,
[1-(4-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)ацетил]-пиперидин,
[1-(4-хлорфенилгидразоно)-1-(3-цианофениламино)ацетил]-пиперидин,
N-трет-бутил-[1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)]ацетамид,
N-трет-бутил-[1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)]ацетамид,
N-трет-бутил-[1-(4-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)]ацетамид,
N-трет-бутил-[1-(4-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)]ацетамид,
1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,5-дифторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(2,6-дихлорпиридин-4-иламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3-трифторметилфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-[(3,5-дихлорфенил)метиламино]-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(2,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(3-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(2-хлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(2-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(2-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(2-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-фторфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-фторфенилгидразоно)-1-(4-метоксифениламино)-3,3-диметил-2-бутанон,
1-(4-фторфенилгидразоно)-1-(4-трифторметилфениламино)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-метилфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-трифторметилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-фторфениламино)-1-(4-трифторметилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-трифторметилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-трифторметилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-трифторметилфениламино)-1-(4-трифторметилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(4-трифторметилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(4-трифторметилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-хлорфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-бромфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-цианофениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-цианофенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-цианофенилгидразоно)-1-(4-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-цианофенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-цианофенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-цианофениламино)-1-(4-цианофенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-цианофенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(4-цианофенилгидразоно)-1-(4-метоксифениламино)-3,3-диметил-2-бутанон,
1-(4-цианофенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-цианофенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-метоксифенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-ацетилфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-ацетилфенилгидразоно)-1-(4-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-ацетилфенилгидразоно)-1-(4-хлорфениламино)-3,3-диметил-2-бутанон,
1-(4-ацетилфенилгидразоно)-1-(4-бромфениламино)-3,3-диметил-2-бутанон,
1-(4-ацетилфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(4-ацетилфенилгидразоно)-1-(4-метоксифениламино)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-метансульфонилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-фторфениламино)-1-(4-метансульфонилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-метансульфонилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-метансульфонилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-этинилфениламино)-1-(4-метансульфонилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-ацетилфениламино)-1-(4-метансульфонилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-изопропилфениламино)-1-(4-метансульфонилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-хлор-3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(3-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-2-гексанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-3-этил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-2-гексанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-3-этил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)-4,4-диметил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-4,4-диметил-2-пентанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-гексанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-(2-фурил)-2-этанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-2-(2-фурил)-2-этанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-2-(2-фурил)-2-этанон,
1-(4-бромфениламино)-1-(4-хлорфенилгидразоно)-2-(2-фурил)-2-этанон,
1-(4-хлорфенилгидразоно)-1-(3-трифторметилфениламино)-2-(2-фурил)-2-этанон,
4-хлор-1-(4-хлорфенилгидразоно)-1-(3-трифторметилфениламино)-3,3-диметил-2-бутанон,
4-хлор-1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(3,4-дихлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(3,4-дихлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-(2-тиенил)-2-этанон,
1-(4-хлорфенилгидразоно)-1-(изохинолин-5-иламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(хинолин-8-иламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(пиридин-3-иламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(5-хлорпиридин-2-иламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-(4-трифторметилфенил)-2-этанон,
1-(3-фторфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлор-3-фторфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-3-этил-2-пентанон,
1-(4-этинилфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-4,4-диметил-2-пентанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-4,4-диметил-2-пентанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-гексанон, и их фармацевтически приемлемые соли.
Из них, предпочтительным является:
1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,5-дифторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(3-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-фторфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-метилфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-хлорфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-бромфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-хлор-3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(3-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-2-гексанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-3-этил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-2-гексанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-3-этил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)-4,4-диметил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-4,4-диметил-2-пентанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-гексанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-(2-фурил)-2-этанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-2-(2-фурил)-2-этанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-2-(2-фурил)-2-этанон,
1-(4-бромфениламино)-1-(4-хлорфенилгидразоно)-2-(2-фурил)-2-этанон,
4-хлор-1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(3,4-дихлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(3,4-дихлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлор-3-фторфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-3-этил-2-пентанон,
1-(4-этинилфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-4,4-диметил-2-пентанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-4,4-диметил-2-пентанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-гексанон, и их фармацевтически приемлемые соли.
Способ получения ариламидразонового производного, представленного формулой (1) по настоящему изобретению, включает способ, представленный ниже, но способ получения соединения по настоящему изобретению не ограничивается им.

где R1, R2, R3, A, D, m и n имеют определенные выше значения, и X представляет собой атом галогена.
[Способ 1]
Ариламидразоновое производное (1) по настоящему изобретению получают путем взаимодействия соединения (2) с соединением (3). Взаимодействие между соединением (2) и соединением (3) осуществляют путем их взаимодействия в присутствии органического основания (например, триэтиламина, пиридина или т.п.), в растворителе, таком как простой эфир (например, диэтиловый эфир, тетрагидрофуран или т.п.), спирт (метанол, этанол или т.п.) или их смесь, при температуре реакции от 0 до 60°C, в течение от 1 до 24 часов.
Способ получения соединения (2), которое является промежуточным соединением для синтеза соединения по настоящему изобретению, описан ниже.
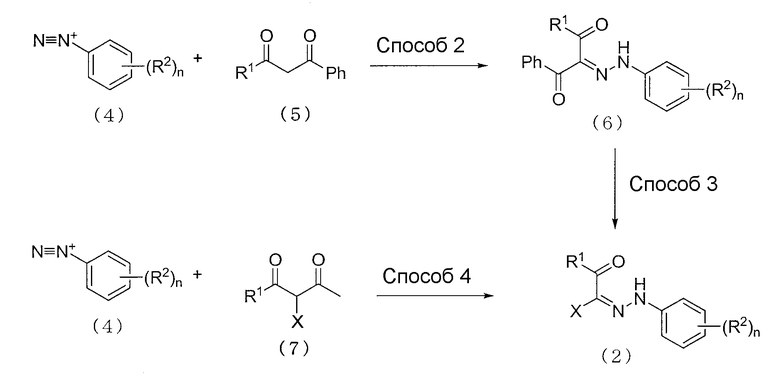
где R1, R2, n и X имеют определенные выше значения.
[Способ 2]
Соединение (6) получают путем взаимодействия производного диазониевой соли, представленного как соединение (4), с соединением (5) в соответствии со способом, описанным в литературе (J. Med. Chem. 45, 2123 (2002)).
Взаимодействие между производным диазониевой соли (4) и соединением (5) осуществляют путем их взаимодействия в присутствии основания (например, соли карбоновой кислоты и щелочного металла, такой как ацетат натрия, ароматического основания, такого как пиридин, или т.п.), в смеси растворителей воды со спиртом (например, метанолом, этанолом или т.п.) и/или простым эфиром (например, диэтиловым эфиром, тетрагидрофураном или т.п.), при температуре реакции от 0 до 40°C, в течение от 1 до 24 часов. Производное диазониевой соли (4) можно получить путем добавления по каплям раствора соли азотистой кислоты, такой как нитрит натрия, к раствору хлористоводородной кислоты соответствующего анилинового производного.
[Способ 3]
Далее, соединение (2) можно получить путем взаимодействия соединения (6) с раствором галогенуксусной кислоты в присутствии основания (например, соли карбоновой кислоты и щелочного металла, такой как ацетат натрия), в смеси растворителей уксусной кислоты/уксусного ангидрида, при температуре реакции от 0 до 40°C, в течение от 1 до 24 часов.
[Способ 4]
Соединение (2) также можно получить в соответствии со следующим способом. Соединение (2) можно получить путем взаимодействия производного диазониевой соли (4) с соединением (7) в присутствии основания (например, соли карбоновой кислоты и щелочного металла, такой как ацетат натрия, ароматического основания, такого как пиридин, или т.п.), в смеси растворителей воды и спирта (например, метанола, этанола или т.п.), при температуре от 0 до 40°C, в течение от 1 до 24 часов.
Соединение (7) можно синтезировать в соответствии со способом, описанным в литературе (J. Org. Chem. 43, 3821 (1978)), когда R1 представляет собой аминогруппу, или в соответствии со способом, описанным в литературе (J. Am. Chem. Soc. 66, 1222 (1944), Tetrahedron Lett. 46, 623 (2005), и US Patent No. 4053594), когда R1 представляет собой низшую алкильную группу, такую как трет-бутильная группа.
Соединение формулы (1), полученное как таковое, может быть выделено и очищено традиционным способом, таким как перекристаллизация или колоночная хроматография.
Поскольку соединение формулы (1) оказывает селективное антагонистическое действие в отношении S1P3 рецепторов, как показано в Примерах испытаний, описанных ниже, лекарственное средство, содержащее соединение, можно использовать, например, в качестве терапевтического средства или профилактического средства при артериосклерозе, утолщении интимы, сосудистых пролиферативных заболеваниях (солидных опухолей, диабетической ретинопатии и т.п.), сердечной недостаточности, ишемическом реперфузионном расстройстве, цереброваскулярном спазме после субарахноидального кровоизлияния, стенокардии или инфаркта миокарда, вызванного коронарным спазмом, прогрессирующих почечных расстройствах, таких как гломерулонефрит, тромбозе, легочных заболеваниях, вызванных отеком легких (ARDS или т.п.), брадикардии и парасимпатетически-опосредованной фибрилляции предсердия или т.п., или в качестве сосудорасширяющего средства.
Соединение формулы (1) по настоящему изобретению или его фармацевтически приемлемую соль можно вводить перорально или парентерально. Лекарственную форму для введения можно сформулировать с фармацевтически приемлемыми добавками, такими как эксципиент, связующее, буферный агент, загуститель, стабилизатор, эмульгатор, диспергирующее вещество, суспендирующее вещество или консервант, традиционными способами.
Примеры препаратов для перорального введения включают таблетки (включая таблетки с сахарным покрытием и таблетки с пленочным покрытием), пилюли, гранулы, порошки, капсулы (включая мягкие капсулы), сиропы, эмульсии, суспензии и т.п. Эти препараты для перорального введения можно получить в соответствии с известными способами, путем включения добавок, которые традиционно используют в области фармацевтики. Примеры таких добавок включают эксципиенты, такие как лактоза, маннит и безводный кислый фосфат кальция; связующие, такие как гидроксипропилцеллюлоза, метилцеллюлоза и поливинилпирролидон; разрыхлители, так как крахмал и карбоксиметилцеллюлоза; смазывающие вещества, такие как стеарат магния и тальк; и т.п.
Парентеральное введение можно осуществлять при помощи препаратов для инъекций, ректально вводимых препаратов, местно вводимых препаратов и т.п. Примеры препаратов для инъекций включают стерилизованные растворы или суспензии и т.п. Эти препараты для инъекций получают, например, путем растворения или суспендирования соединения формулы (1) или его фармацевтически приемлемой соли в воде для инъекции (Фармакопея Японии). Если это необходимо, можно включить изотонический агент, такой как хлорид натрия; буферный агент, такой как кислый фосфат натрия или вторичный кислый фосфат натрия; вещество, способствующее растворению, и т.п. Кроме того, препарат также можно получить в виде готового к применению препарата для инъекций (порошковое наполнение, лиофилизация), и в этом случае получение осуществляют традиционными способами, путем добавления эксципиентов, таких как маннит и лактоза.
Ректально вводимые препараты включают суппозитории и т.п. Суппозиторий получают, например, путем растворения или суспендирования соединения формулы (1) или его фармацевтически приемлемой соли в основе, такой как масло какао или макроголь, с последующим формированием смеси, заливая ее в форму. Кроме того, полученные таким путем жидкость или крем можно вводить в контейнер для инфузии, который используют как препарат для ректального введения.
Местно вводимые препараты могут включать жидкие препараты, глазные капли, кремы, мази, препараты в виде гелей, препараты в виде спреев, порошковые препараты и т.п. Жидкий препарат можно получить путем добавления соединения формулы (1) или его фармацевтически приемлемой соли к воде, с добавлением стабилизатора, солюбилизирующего вещества, загустителя, диспергирующего вещества, суспендирующего вещества или т.п., по мере необходимости. Что касается указанного загустителя, можно использовать желатин, гиалуронат натрия, высокомолекулярный декстран, альгинат натрия, хондроитинсульфат натрия или т.п. Глазные капли можно получить путем добавления буферного агента, агента регулирования pH и изотонического агента, а также консерванта. Крем и мазь можно получить с использованием водной или масляной основы, такой как вода, жидкий парафин, растительное масло (арахисовое масло, касторовое масло или т.п.), макроголь или т.п. Препарат в виде геля можно получить известным способом с использованием желатина, пектина, каррагена, агара, трагакантовой камеди, альгинатов, простых эфиров целлюлозы (метилцеллюлоза, натрий карбоксиметилцеллюлоза и т.п.), производных пектина, полиакрилатов, полиметакрилатов, поливинилового спирта, поливинилпирролидона и т.п. Препарат в виде спрея можно получить путем растворения или суспендирования соединения формулы (1) или его фармацевтически приемлемой соли в воде или т.п. с последующим заполнением раствором или суспензией емкости для распыления. В случае использования порошкового препарата, соединение формулы (1) или его фармацевтически приемлемую соль можно использовать per se, или его можно получить путем смешивания соответствующих эксципиентов.
Суточная доза соединения формулы (1), в расчете на взрослого человека, может варьировать в зависимости от симптома, массы тела или возраста пациента, типа соединения, пути введения или т.п., но в случае перорального введения подходящая доза составляет от около 0,01-1000 мг, и предпочтительно около 0,1-300 мг. В случае парентерального введения, можно вводить количество, составляющее от одной десятой до половины дозы для перорального введения. Эти дозы можно соответственно увеличивать или уменьшать в соответствии с симптомами, массой тела или возрастом пациента.
ПРИМЕРЫ
Далее настоящее изобретение будет описано подробно при помощи Примеров, но настоящее изобретение не ограничивается этими Примерами.
[Ссылочный пример 1] 2-Бром-2-(4-хлорфенилгидразоно)-ацетофенон (Ссылочное соединение 1)
4-Хлоранилин (3,2 г) растворяли в концентрированной хлористоводородной кислоте (5,8 мл) и воде (11,6 мл) и раствор перемешивали в течение 15 минут. Затем к смеси добавляли лед (30 г), добавляли по каплям при охлаждении льдом водный раствор (4 мл) нитрита натрия (1,8 г) и полученную смесь перемешивали в течение 30 минут. Реакционный раствор снова нагревали до комнатной температуры и к смеси добавляли водный раствор (60 мл) ацетата натрия (6,2 г) и раствор дибензоилметана (5,7 г) в смеси диэтилового эфира (20 мл) этанола (25 мл). Смесь интенсивно перемешивали в течение 3 часов. Осажденные желтые неочищенные кристаллы собирали фильтрованием, промывали водой и затем сушили при пониженном давлении с получением (4-хлорфенилгидразоно)дибензоилметана (9,5 г) в виде желтых кристаллов. К смешанному раствору этих неочищенных кристаллов (9,5 г) и ацетата натрия (5,1 г) в уксусной кислоте (60 мл) - уксусном ангидриде (15 мл) медленно добавляли по каплям раствор брома (1,3 мл) в уксусной кислоте (8,0 мл) при охлаждении льдом. Смесь перемешивали в течение 30 минут, а затем в течение 16 часов при комнатной температуре. Реакционный раствор выливали в ледяную воду (200 мл) и смесь перемешивали в течение 1 часа. Осажденные неочищенные кристаллы собирали фильтрованием, промывали безводным этанолом и диэтиловым эфиром и сушили при пониженном давлении с получением указанного в заголовке соединения (4,4 г) в виде бледно-желтых кристаллов.
1H-ЯМР (300 МГц, CDCl3) δ: 7,06 (д, J=9,0 Гц, 2H), 7,29 (д, J=9,0 Гц, 2H), 7,49 (дд, J=7,3, 7,5 Гц, 2H), 7,60 (т, J=7,3 Гц, 1H), 7,99 (д, J=7,5 Гц, 1H), 8,61 (с, 1H);
т.пл.: 190-192°C
[Ссылочный пример 2] Этил бром-(4-хлорфенилгидразоно)ацетат (Ссылочное соединение 2)
Указанное в заголовке соединение (3,2 г) получали в виде желтых кристаллов таким же способом, как в Ссылочном примере 1, исходя из 4-хлоранилина (3,2 г) и этилбензоилацетата (5,3 г).
1H-ЯМР (300 МГц, CDCl3) δ: 1,40 (т, J=7,2 Гц, 3H), 4,39 (кв., J=7,2 Гц, 2H), 7,17 (д, J=8,8 Гц, 2H), 7,29 (д, J=8,8 Гц, 2H), 8,36 (с, 1H);
т.пл.: 129-131°C
[Ссылочный пример 3] [2-Хлор-2-(4-хлорфенилгидразоно)ацетил]пиперидин (Ссылочное соединение 3)
6 н. раствор хлористоводородной кислоты (18 мл) и воды (15 мл) добавляли к 4-хлоранилину (3,2 г) и смесь перемешивали в течение 15 минут. Затем добавляли по каплям водный раствор (10 мл) нитрита натрия (1,8 г) при охлаждении льдом и полученную смесь перемешивали в течение 30 минут, с получением раствора диазониевой соли.
2-Хлор-1-(пиперидин-1-ил)бутан-1,3-дион (6) растворяли в этаноле (200 мл), к смеси добавляли водный раствор (60 мл) ацетата натрия (6,2 г) и добавляли по каплям при охлаждении льдом полученный ранее раствор диазониевой соли. Полученную смесь интенсивно перемешивали в течение 4 часов. К реакционной смеси добавляли воду (500 мл) и смесь экстрагировали этилацетатом. Органический слой сушили над безводным сульфатом натрия и затем растворитель отгоняли при пониженном давлении. Полученный неочищенный продукт разбавляли этанолом (60 мл) и смесь нагревали до температуры кипения с обратным холодильником в течение 1 часа. Смесь оставляли охлаждаться, затем смесь перемешивали на ледяной бане и осажденные неочищенные кристаллы собирали фильтрованием, промывали петролейным эфиром и затем сушили при пониженном давлении, с получением [2-хлор-2-(4-хлорфенилгидразоно)ацетил]пиперидина (5) (5,0 г) в виде молочно-белых кристаллов.
1H-ЯМР (300 МГц, CDCl3) δ: 1,63-1,77 (м, 6H), 3,63-3,70 (м, 4H), 7,01 (д, J=8,8 Гц, 2H), 7,25 (д, J=8,8 Гц, 2H), 7,97 (с, 1H);
т.пл.: 154-155°C
[Ссылочный пример 4] N-трет-Бутил-[2-хлор-2-(4-хлорфенилгидразоно)]ацетамид (Ссылочное соединение 4)
Указанное в заголовке соединение (5,1 г) получали в виде желтых кристаллов таким же способом, как в Ссылочном примере 3, исходя из 4-хлоранилина (3,2 г) и N-трет-бутил-(2-ацетил-2-хлор)ацетамида (4,8 г).
1H-ЯМР (300 МГц, CDCl3) δ: 1,45 (с, 9H), 6,57 (ушир.с, 1H), 7,04 (д, J=8,6 Гц, 2H), 7,29 (д, J=8,6 Гц, 2H), 8,03 (с, 1H);
т.пл.: 168-170°C
[Ссылочный пример 5] [1-Хлор-1-(4-хлорфенилгидразоно)]-3,3-диметил-2-бутанон (Ссылочное соединение 5)
Указанное в заголовке соединение (0,6 г) получали в виде желтых кристаллов таким же способом, как в Ссылочном примере 3, исходя из 4-хлоранилина (0,6 г) и 3-хлор-5,5-диметилгексан-2,4-диона (0,8 г).
1H-ЯМР (300 МГц, CDCl3) δ: 1,43 (с, 9H), 7,12 (д, J=8,7 Гц, 2H), 7,33 (д, J=8,7 Гц, 2H), 8,34 (с, 1H);
т.пл.: 129-131°C
[Ссылочный пример 6] 1-Хлор-(4-хлорфенилгидразоно)-2-гексанон (Ссылочное соединение 6)
Указанное в заголовке соединение (1,4 г) получали в виде желтого порошка таким же способом, как в Ссылочном примере 3, исходя из 4-хлоранилина (1,3 г) и 3-хлор-2,4-октандиона (1,9 г).
1H-ЯМР (300 МГц, CDCl3) δ: 0,95 (т, J=7,3 Гц, 3H), 1,41 (кв.т, J=7,3, 7,5 Гц, 2H), 1,70 (тт, J=7,5, 7,5 Гц, 2H), 2,96 (т, J=7,5 Гц, 2H), 7,16 (д, J=8,8 Гц, 2H), 7,35 (д, J=8,8 Гц, 2H), 8,39 (с, 1H);
т.пл.: 117-119°C
[Ссылочный пример 7] 1-Хлор-1-(4-хлорфенилгидразоно)-3-этил-2-пентанон (Ссылочное соединение 7)
Указанное в заголовке соединение (2,0 г) получали в виде молочно-белого порошка таким же способом, как в Ссылочном примере 3, исходя из 4-хлоранилина (2,9 г) и 3-хлор-5-этил-2,4-гептандиона (4,3 г).
1H-ЯМР (300 МГц, CDCl3) δ: 0,89 (т, J=7,5 Гц, 3H), 1,52-1,83 (м, 4H), 3,44-3,52 (м, 1H), 7,16 (д, J=9,0 Гц, 2H), 7,34 (д, J=9,0 Гц, 2H), 8,43 (с, 1H).
[Ссылочный пример 8] 1-Хлор-1-(4-хлорфенилгидразоно)-4,4-диметил-2-пентанон (Ссылочное соединение 8)
Указанное в заголовке соединение (2,1 г) получали в виде желтого порошка таким же способом, как в Ссылочном примере 3, исходя из 4-хлоранилина (1,8 г) и 3,6-дихлор-5,5-диметил-2,4-гександиона (2,6 г).
1H-ЯМР (300 МГц, CDCl3) δ: 1,06 (с, 9H), 2,88 (с, 2H), 7,15 (д, J=8,9 Гц, 2H), 7,34 (д, J=8,9 Гц, 2H), 8,39 (с, 1H).
[Ссылочный пример 9] 2-(4-Хлорфенилгидразоно)-2-хлор-1-(2-фурил)этанон (Ссылочное соединение 9)
Указанное в заголовке соединение (3,3 г) получали в виде желтого порошка таким же способом, как в Ссылочном примере 3, исходя из 4-хлоранилина (3,0 г) и 2-хлор-1-(2-фурил)-1,3-бутандиона (4,4 г).
1H-ЯМР (300 МГц, CDCl3) δ: 6,63-6,64 (м, 1H), 7,16 (д, J=9,0 Гц, 2H), 7,36 (д, J=9,0 Гц, 2H), 7,60-7,62 (м, 1H), 7,74-7,75 (м, 1H), 8,56 (с, 1H).
[Ссылочный пример 10] 1-(4-Хлорфенилгидразоно)-1,4-дихлор-3,3-диметил-2-бутанон (Ссылочное соединение 10)
Указанное в заголовке соединение (1,6 г) получали в виде желтого порошка таким же способом, как в Ссылочном примере 3, исходя из 4-хлоранилина (1,3 г) и 3,6-дихлор-5,5-диметил-2,4-гександиона (2,2 г).
1H-ЯМР (300 МГц, CDCl3) δ: 1,50 (с, 6H), 3,99 (с, 2H), 7,10 (д, J=8,9 Гц, 2H), 7,35 (д, J=8,9 Гц, 2H), 8,41 (с, 1H).
[Ссылочный пример 11] 1-Хлор-1-(3,4-дихлорфенилгидразоно)-3,3-диметил-2-бутанон (Ссылочное соединение 11)
Указанное в заголовке соединение (1,8 г) получали в виде оранжевого порошка таким же способом, как в Ссылочном примере 3, исходя из 3,4-дихлоранилина (2,6 г) и 3-хлор-5,5-диметилгексан-2,4-диона (1,8 г).
1H-ЯМР (300 МГц, CDCl3) δ: 1,43 (с, 9H), 7,02 (дд, J=2,6, 8,8 Гц, 1H), 7,28 (д, J=2,6 Гц, 1H), 7,41 (д, J=8,8 Гц, 1H), 8,31 (с, 1H);
MS (APCI) m/z 303 (M-Cl+MeOH)+;
т.пл.: 134-136°C
[Ссылочный пример 12] 1-Хлор-1-(4-хлорфенилгидразоно)-2-(2-тиенил)-2-этанон (Ссылочное соединение 12)
Указанное в заголовке соединение (0,9 г) получали в виде желтого порошка таким же способом, как в Ссылочном примере 3, исходя из 4-хлоранилина (1,5 г) и 2-хлор-1-(2-тиенил)-1,3-бутандиона (2,4 г).
1H-ЯМР (300 МГц, CDCl3) δ: 7,20-7,26 (м, 3H), 7,37 (д, J=8,7 Гц, 2H), 7,75 (с, 1H), 8,19 (с, 1H), 8,55 (с, 1H).
[Пример 1] 2-(4-Хлорфенилгидразоно)-2-(3-фторфениламино)ацетофенон (Соединение 1)
Ссылочное соединение 1 (169 мг) растворяли в тетрагидрофуране (5 мл), затем к смеси добавляли триэтиламин (69 мкл) и 3-фторананилин (58 мкл) и полученную смесь перемешивали в течение 2 часов при комнатной температуре. Растворитель отгоняли при пониженном давлении, остаток разбавляли этилацетатом и водой и разбавленную смесь разделяли. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и затем растворитель отгоняли при пониженном давлении. Полученный таким образом неочищенный продукт выделяли и очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 5:1) с получением указанного в заголовке соединения (126 мг) в виде аморфного вещества оранжевого цвета.
1H-ЯМР (300 МГц, CDCl3) δ: 6,45 (д, J=10,1 Гц, 1H), 6,52 (д, J=7,9 Гц, 1H), 6,70 (дд, J=7,9, 10,1 Гц, 1H), 6,95 (д, J=8,8 Гц, 2H), 7,03 (с, 1H), 7,23-7,28 (м, 3H), 7,49-7,63 (м, 4H), 8,15 (д, J=7,0 Гц, 2H);
MS (ESI) m/z 366 (M-H)-.
[Примеры 2-20]
Соединения примеров 2-20 получали таким же способом, как в примере 1. Полученные соединения представлены в таблицах 1-3. Однако в примерах 13-20 соединения синтезировали с использованием Ссылочного соединения 2 вместо Ссылочного соединения 1.
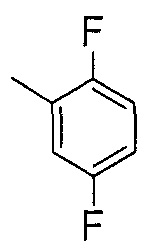
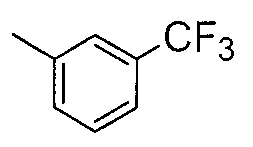
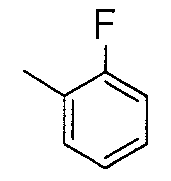




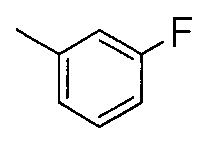

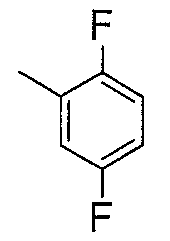

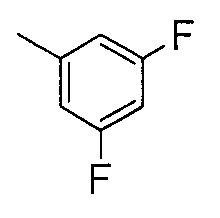
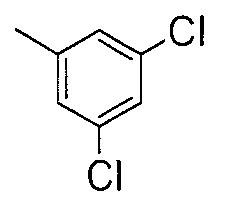
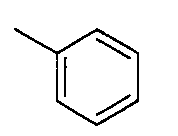

[Пример 21]
[1-(4-Хлорфенилгидразоно)-1-(3-фторфениламино)ацетил]пиперидин (Соединение 21)
Ссылочное соединение 3 (150 мг) растворяли в этаноле (5 мл), затем к смеси добавляли триэтиламин (84 мкл) и 3-фторанилин (53 мкл) и полученную смесь перемешивали в течение 2 часов при 50°C. Растворитель отгоняли при пониженном давлении, остаток разбавляли этилацетатом и водой и экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия и растворитель отгоняли при пониженном давлении. Полученные таким образом неочищенные кристаллы промывали смесью растворителей гексан-этилацетат (20:1) и сушили при пониженном давлении с получением указанного в заголовке соединения (123 мг) в виде кристаллов оранжевого цвета.
1H-ЯМР (300 МГц, CDCl3) δ: 1,65-1,78 (м, 6H), 3,67 (ушир.с, 2H), 4,02 (ушир.с, 2H), 6,34-6,38 (м, 1H), 6,44-6,47 (м, 1H), 6,61-6,68 (м, 1H), 6,91 (д, J=8,8 Гц, 2H), 7,07-7,08 (м, 2H), 7,19 (д, J=8,8 Гц, 2H), 7,21 (с, 1H);
MS (ESI) m/z 373 (M-H)-,
[Примеры 22-129]
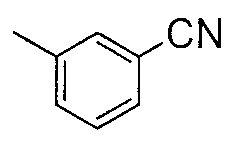
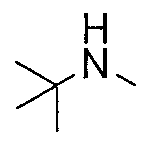
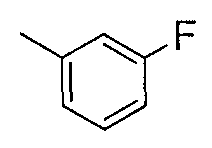
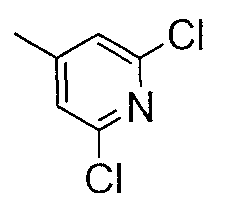
Соединения примеров 22-141 получали таким же способом, как в примере 21, с использованием Ссылочных соединений 3-12 или соединений, полученных таким же способом, как в Ссылочном примере 3, и соответствующих анилинов. Полученные соединения представлены в таблицах 4-17.

















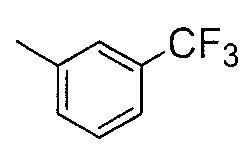



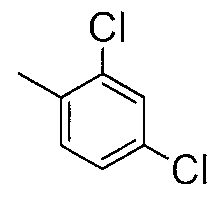















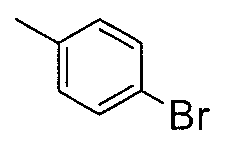
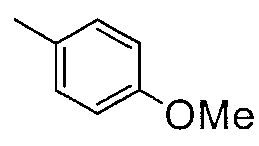


















































































Репрезентативные соединения по настоящему изобретению были испытаны на антагонистическое действие в отношении S1P3 рецепторов, как показано в представленных ниже Примерах испытаний.
[Пример испытаний 1] Супрессивный эффект на увеличение концетрации ионов кальция в клетках ([Ca2+]i)
Изменения в [Ca2+]I, вызванное стимуляцией S1P, измеряли следующим способом.
Клетки CHO-K1, экспрессирующие подтип S1P3 рецептора, суспендировали в питательной смеси F-12 HAM (HAM, SIGMA), содержащей 10% (об/об) фетальной бычьей сыворотки (FBS, SIGMA), и суспензию инокулировали в 96-луночный планшет и затем культивировали в течение 24 часов. Культуральный раствор удаляли, клетки промывали один раз HAM, содержащей 1% FBS, и затем клетки культивировали еще в течение 24 часов с использованием того же культурального раствора. Культуральный раствор снова удаляли и клетки промывали один раз HBSS (+) буферным раствором. Добавляли тот же буферный раствор, который был приготовлен для получения концентрации флуоресцентного Ca2+ индикатора Fura 2-AM (Molecular Probe, Inc.) 5 мкмоль/л, и клетки инкубировали в течение 60 минут при 37°C. Клетки промывали один раз буферным раствором Хэнка, содержащим 20 мМ HEPES (далее указан как HBSS(+) буферный раствор), и добавляли раствор 200 мкл испытываемого соединения. Затем клетки инкубировали в течение 20 минут при 37°C. Планшет помещали в аппарат для измерения флуоресценции (Flex Station II, Molecular Devices, Inc.) для измерения базовой линии, затем к смеси добавляли 50 мкл раствора S1P (50 нмоль/л) и измеряли увеличение [Ca2+]I, вызванное раствором S1P, в течение 30 секунд с интервалом 3,33 секунды (возбуждение при 335 нм и 362 нм, детекция при 505 нм и 512 нм).
Селективность в отношении подтипа S1P рецептора исследовали следующим образом. Сначала CHO-K1 клетки, которые стабильно экспрессируют каждый из подтипов рецептора S1P1, S1P2 и S1P3, суспендировали в HAM, содержащей 10% (об/об) FBS, суспензию инокулировали в 96-луночный планшет и затем клетки культивировали в течение 24 часов. Культуральный раствор удаляли, клетки промывали один раз HAM, содержащей 1% FBS, и клетки культивировали еще в течение 24 часов с использованием 50 мкл того же самого культурального раствора. Кроме того, добавляли раствор Calcium3 (Molecular Devices, Inc.), полученный в HBSS(+) буфере, который представляет собой флуоресцентный Ca2+ индикатор, и клетки инкубировали в течение 60 минут при 37°C. Затем добавляли 100 мкл раствора испытываемого соединения, полученного до концентрации 2×10 мкмоль/л, и клетки инкубировали в течение 20 минут при 37°C. Планшет помещали в аппарат для измерения флуоресценции (Flex Station II, Molecular Devices, Inc.) для измерения базовой линии, затем к смеси добавляли 50 мкл раствора S1P (50 нмоль/л для S1P3 рецептора и 100 нмоль/л для других рецепторов) и измеряли увеличение [Ca2+]I, вызванное раствором S1P, в течение 30 секунд с интервалом 2 секунды (возбуждение при 485 нм, детекция при 525 нм). Индикатор получали и использовали в соответствии с инструкцией.
Раствор испытываемого соединения получали путем растворения каждого из испытываемых соединений в DMSO до концентрации 10 ммоль/л и затем разбавления раствора HBSS(+) буферным раствором до предварительно определенной концентрации. Для контроля использовали HBSS(+) буферный раствор, содержащий 0,1% DMSO, вместо раствора испытываемого соединения, а HBSS(+) буферный раствор, содержащий 0,025% DMSO использовали вместо S1P раствора для слепого испытания. Данные измерений получали путем вычитания максимального RFU значения для слепого испытания из максимальных RFU значений для контроля или каждого испытываемого соединения. Уменьшение полученного значения для испытываемого соединения по сравнению с контролем указывали как показатель супрессии (%), исходя из которого рассчитывали значение ИК50. Эти результаты испытаний представлены в таблицах 18 и 19.
Увеличение [Ca2+]i было хорошо известно как одно из клеточных изменений, индуцированных S1P. Как описано выше, увеличение [Ca2+]i, вызванное стимуляцией S1P, подавлялось при помощи ариламидразонового производного по настоящему изобретению в CHO-K1 клетках, которые стабильно экспрессируют S1P3 рецепторы. В отличие от этого, в CHO-K1 клетках, которые стабильно экспрессируют S1P1 или S1P2 рецепторы, увеличение [Ca2+]i, вызванное стимуляцией S1P, не подавлялось совсем или почти совсем при помощи репрезентативных соединений по настоящему изобретению. Эти результаты показывают, что соединение по настоящему изобретению подавляет увеличение [Ca2+]i, вызванное S1P, с селективностью в отношении подтипа S1P3 рецептора.
[Пример испытаний 2] Воздействие на скорость коронарного кровотока в извлеченном сердце крысы
Самца крысы SD с массой тела около 350 г анестезировали пентобарбиталом натрия (50 мг/кг) и вводили гепарин (1000 Ед/кг) через нижнюю бедренную вену. Сердце быстро извлекали и соединяли с аппаратом для перфузии Лангендорфа. Что касается перфузии, перфузию при постоянном давлении осуществляли при 70±5 мм рт.ст. с использованием раствора Krebs-Henseleit (NaCl: 113,8 ммоль/л, NaHCO3: 22,0 ммоль/л, KCl: 4,7 ммоль/л, KH2PO4: 1,2 ммоль/л, MgSO4: 1,1 ммоль/л, CaCl2: 2,5 ммоль/л, глюкоза: 11,0 ммоль/л, пируват натрия: 2,0 ммоль/л). Температуру перфузионного раствора устанавливали при 37±0,2°C и газировали при помощи газовой смеси (95% O2 и 5% CO2) таким образом, чтобы парциальное давление кислорода было 550 мм рт.ст. или больше. Скорость коронарного перфузионного потока измеряли при помощи электромагнитного флуометра через зонд, установленный на пути циркулирования потока. Кроме того, эффекты на функцию сердца исследовали с использованием левого вентрикулярного вычисленного давления (LVDP), первого производного левого вентрикулярного давления (LV ± dp/dt), и частоты сердечных сокращений (HR) в качестве индексов. LVDP определяли путем вычитания левого вентрикулярного конечного диастолического давления (LVEDP) из левого вентрикулярного систолического давления (LVSP), которое определяли при помощи латексного баллона, вставленного в левый желудочек, и измеряли с использованием измерителя давления через трансдуктор давления. LVEDP устанавливали до исходного значения 5-10 мм рт.ст., регулируя объем латексного баллона. Сигналы, измеренные при помощи измерителя давления, передавали на дифференциальный измеритель и измеритель частоты сердечных сокращений для определения первой производной левого вентрикулярного давления (LV ± dp/dt) и частоты сердечных сокращений (HR).
Эффекты S1P на скорость коронарного кровотока и сердечную функцию определяли при концентрации от 10-9 M до 10-7 M в расчете на перфузионный раствор. После стабилизации при нормальных перфузионных условиях в течение около 20 минут вводили путем непрерывной инфузии лекарственного средства или растворителя в кровоток в течение 5 минут. Для оценки эффектов соединения по настоящему изобретению на изменение скорости коронарного кровотока, индуцированное S1P, испытываемое соединение (Пример Соединения 33) непрерывно вливали в перфузионный раствор за 5 минут до введения S1P при концентрации 10-7 M.
S1P существенно снижал скорость коронарного кровотока при концентрации от 10-9 M до 10-7 M, но когда соединение по настоящему изобретению вводили заранее, снижение существенно подавлялось. Кроме того, скорость коронарного кровотока существенно возрастала с введением соединения по настоящему изобретению.
[Пример испытаний 3] Воздействие на гемодинамику у крыс
Что касается кровяного давления и частоты сердечных сокращений у крыс, систолическое кровяное давление (SBP) и частоту сердечных сокращений (HR) измеряли при помощи предварительно не нагреваемого, неинвазивного манометра для измерения кровяного давления у крыс и мышей. Измерения осуществляли по пять раз для одной временной точки измерения. Из пяти величин исключали самое высокое и самое низкое значение SBP, и целое число, представляющее собой среднее от оставшихся трех значений, принимали за показатель кровяного давления и частоты сердечных сокращений в определенной временной точке измерения.
Кровяное давление и частоту сердечных сокращений измеряли за 1 час до введения соединения, в час 0 (непосредственно перед введением) и через 1, 2, 3, 4, 5, 6 и 24 часа после введения. Использовали по пять крыс для каждой группы. Испытываемое соединение (Пример Соединения 33; 10 и 30 мг/кг) вводили перорально, а растворитель вводили перорально контрольной группе.
Как результат, соединение по настоящему изобретению не показало какого-либо явного эффекта на кровяное давление и частоту сердечных сокращений.
[Пример испытаний 4] Воздействие соединения по настоящему изобретению на гемодинамические изменения, вызванные FTY720
FTY720, который известен как иммуносупрессант, согласно сообщениям, вызывает асимптоматическую брадикардию, и есть предположения, что в основе этой брадикардии агонистическое действие FTY720 в отношении S1P3 рецептора (Journal of the American Society of Nephrology, 13(4), 1073-1083 (2002), Bioorganic & medicinal Chemistry Letters, 14, 3501-3505 (2004)). Таким образом, были исследованы эффекты соединения по настоящему изобретению на FTY720-индуцированную брадикардию.
Крысу анестезировали пентобарбиталом (50 мг/кг, интраперитонеальное введение) и затем вставляли катетеры для введения лекарственного средства и измерения кровяного давления в нижнюю бедренную вену и сонную артерию, соответственно. Кровяное давление измеряли при помощи амплификатора давления напряжения через трансдуктор давления. Частоту сердечных сокращений измеряли при помощи тахометра посредством электрокардиографических волн. Используемый FTY720 закупали у Cayman Chemical Co.
FTY720 (1 мг/кг) вводили внутривенно и его эффекты на гемодинамику исследовали путем измерения кровяного давления и частоты сердечных сокращений на время 0 минут (непосредственно перед введением) и через 10, 20 и 30 минут сразу после внутривенного введения. Эффект испытываемого соединения (Соединение 33; 10 и 30 мг/кг) на изменения гемодинамики, вызванные внутривенным введением FTY720 (1 мг/кг), оценивали при помощи перорального введения испытываемого соединения (10 и 30 мг/кг) за 4 часа до внутривенного введения FTY720 (1 мг/кг), поскольку время для достижения максимальной концентрации в крови для испытываемого соединения при пероральном введении (1 мг/кг) составляет 4 часа после введения.
В результате, FTY720 снижал частоту сердечных сокращений и индуцированную брадикардию у крыс, при этом это подавлялось в группе, которой вводили соединение по настоящему изобретению.
[Пример получения композиции 1] Получение таблеток
Смешивали пять грамм соединения 33, 125 г лактозы, 40 г кукурузного крахмала и 20 г кристаллической целлюлозы и к смеси добавляли 6 г гидроксипропилцеллюлозы в виде 10% раствора в этаноле. Смесь подвергали гранулированию при перемешивании и экструзии через сито с диаметром 8 мм с получением гранул. Гранулы сушили, затем добавляли 4 г стеарата магния. Полученную смесь подвергали формованию в пресс-формах с получением таблеток, каждая из которых имела массу 200 мг и содержала 5 мг соединения 33.
[Пример получения композиции 2] Получение препарата для инъекций, или жидкого препарата
Растворяли 50 мг соединения 33 и 900 мг хлорида натрия с использованием 90 мл воды для инъекции и затем смесь доводили до pH 7,0 при помощи 0,1 ммоль/л гидроксида натрия. Кроме того, использовали воду для инъекций для получения общего объема 100 мл. Этот раствор асептически фильтровали и затем заполняли им стеклянные ампулы в количестве по 2 мл в каждую с получением, таким образом, препарата для инъекций (жидкий препарат), содержащего 1 мг соединения 33 в каждой ампуле.
[Пример получения композиции 3] Получение суппозиториев
Witepsol H-15 нагревали до расплава и к смеси добавляли Соединение 33 до концентрации 10 мг/мл. Полученную смесь гомогенизировали. Смесью заполняли пластиковые контейнеры для суппозиториев в количестве по 2 мл в каждый и охлаждали с получением суппозиториев, содержащих по 20 мг соединения 33 в каждом препарате.
[Пример получения композиции 4] Получение глазных капель
50 мг соединения 33, 0,1 г дигидрофосфата натрия дигидрата, 0,9 г хлорида натрия и 5 мг бензалконийхлорида растворяли в 80 мл дистиллированной воды и добавляли 0,1 моль/л водного раствора гидроксида натрия для доведения смеси до pH 7,0. К смеси добавляли дистиллированную воду до получения общего объема 100 мл. Раствор асептически фильтровали и затем заполняли им полипропиленовые бутылочки для закапывания в глаз в количестве по 5 мл в каждую с получением препарата в форме глазных капель, содержащего соединение 33 при концентрации 0,05%.
| название | год | авторы | номер документа |
|---|---|---|---|
| N,N-ЗАМЕЩЕННЫЕ 3-АМИНОПИРРОЛИДИНОВЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПОВТОРНОГО ПОГЛОЩЕНИЯ МОНОАМИНОВ | 2006 |
|
RU2574406C2 |
| ПРОИЗВОДНОЕ ДИФЕНИЛСУЛЬФИДА И ФАРМАЦЕВТИЧЕСКИЙ ПРОДУКТ, КОТОРЫЙ СОДЕРЖИТ ЕГО В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2011 |
|
RU2566296C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2006 |
|
RU2382781C2 |
| ИНГИБИТОРЫ ПРОДУЦИРОВАНИЯ / СЕКРЕЦИИ β-АМИЛОИДНОГО БЕЛКА | 2002 |
|
RU2304140C2 |
| ПРОИЗВОДНЫЕ ТАКСОЛА С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2419622C2 |
| СОЕДИНЕНИЯ АЗАБЕНЗОФУРАНИЛА И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2448111C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2013 |
|
RU2616812C2 |
| ЧЕТВЕРТИЧНЫЕ АММОНИЕВЫЕ СОЛИ ОМЕГА-АМИНОАЛКИЛАМИДОВ R-2-АРИЛПРОПИОНОВЫХ КИСЛОТ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ | 2002 |
|
RU2291857C2 |
| НОВОЕ СОЕДИНЕНИЕ ИНДОЛИНА И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2003 |
|
RU2318808C2 |
| АНИЛИДЫ АМИНОКИСЛОТ В КАЧЕСТВЕ НИЗКОМОЛЕКУЛЯРНЫХ МОДУЛЯТОРОВ IL-17 | 2019 |
|
RU2815505C2 |
Изобретение относится к новым соединениям, - ариламидразоновым производным формулы (I), где R1 представляет собой С2-С8алкильную группу или С2-С8алкокси группу, которые могут быть замещены галогеном или С1-С8алкокси группой; 5-7-членный ароматический гетероцикл, содержащий 1 или 2 атома кислорода, азота или серы, или фенил, которые могут быть замещены галогеном, С1-С8алкильной группой, галоС1-С8алкильной группой или C1-C8алкокси группой; или -NR4R5; R2 и R3 одинаковые или отличные друг от друга, и каждый представляет собой атом водорода, атом галогена, галогенС1-С8алкильную группу, С1-С8алкильную группу, С2-С6алкинильную группу, C1-C8алкокси группу, цианогруппу, С2-С6алканоильную группу или C1-С8алкилсульфонильную группу; А представляет собой бензольное, пиридиновое, хинолиновое или изохинолиновое кольцо; D представляет собой простую связь или метилен; m имеет значение от 1 до 3, и n представляет от 1 до 5, обладающим антагонистическим действием в отношении S1P3 рецепторов, а так же к лекарственным средствам и фармацевтическим композициям, содержащим такие соединения в качестве активного ингредиента. 7 и 6 з.п. ф-лы, 19 табл.
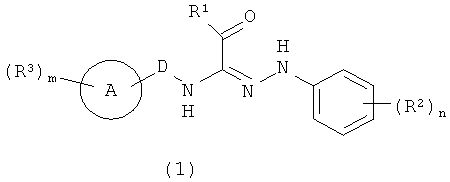
1. Ариламидразоновое производное, представленное формулой (1):

где R1 представляет собой C2-C8алкильную группу, которая может быть замещена атомом галогена или С1-С8алкокси группой; фенильную группу, которая может быть замещена атомом галогена, С1-С8алкильной группой, галоС1-С8алкильной группой или С1-С8алкокси группой; 5-7-членную ароматическую гетероциклическую группу, содержащую 1 или 2 атома кислорода, азота или серы, которая может быть замещена атомом галогена, С1-С8алкильной группой, галоС1-С8алкильной группой или С1-С8алкокси группой; С2-С8алкокси группу, которая может быть замещена атомом галогена или С1-С8алкокси группой; или -NR4R5 (где R4 и R5, которые являются одинаковыми или отличными друг от друга, каждый представляет собой атом водорода или С1-С8алкильную группу, которая может быть замещена атомом галогена или C1-C8алкокси группой; или R4 и R5 могут объединяться со смежным атомом азота с образованием азотсодержащего 5-7-членного гетероциклического кольца, которое может быть замещено атомом галогена, С1-С8алкильной группой, фенильной группой или C1-C8алкокси группой); и
R2 и R3, которые являются одинаковыми или отличными друг от друга, каждый представляет собой атом водорода, атом галогена, галоген C1-С8алкильную группу, С1-С8алкильную группу, С2-С6алкинильную группу, C1-C8алкокси группу, цианогруппу, С2-С6алканоильную группу или C1-С8алкилсульфонильную группу;
А представляет собой бензольное кольцо, пиридиновое, хинолиновое или изохинолиновое кольцо;
D представляет собой простую связь или метилен;
m представляет собой целое число, имеющее значение от 1 до 3, и
n представляет собой целое число, имеющее значение от 1 до 5 (при условии исключения соединений, характеризующихся следующими условиями: когда R1 представляет собой этоксигруппу, R2 представляет собой 2,4-дихлоргруппу, R3 представляет собой атом водорода, А представляет собой бензольное кольцо и D представляет собой метилен; когда R1 представляет собой этоксигруппу, R2 представляет собой 2,4-дихлоргруппу, R3 представляет собой атом водорода, 2-метильную группу, 4-метильную группу, 4-метоксигруппу или 4-этоксигруппу, А представляет собой бензольное кольцо и D представляет собой простую связь; когда R1 представляет собой фенильную группу, R2 представляет собой атом водорода, R3 представляет собой 3,5-диметильную группу, А представляет собой бензольное кольцо, и D представляет собой простую связь; R1 представляет собой этоксигруппу, R2 представляет собой атом водорода, R3 представляет собой атом водорода, А представляет собой бензольное кольцо, и D означает простую связь);
или его фармацевтически приемлемая соль.
2. Ариламидразоновое производное или его фармацевтически приемлемая соль по п.1, где R1 представляет собой линейную или разветвленную C2-С6алкильную группу или 5-7-членную ароматическую гетероциклическую группу, содержащую 1 или 2 атома кислорода, азота или серы.
3. Ариламидразоновое производное или его фармацевтически приемлемая соль по п.1, где R1 представляет собой н-бутильную группу, трет-бутильную группу, 1-этилпропильную группу, 2,2-диметилпропильную группу или фурильную группу.
4. Ариламидразоновое производное или его фармацевтически приемлемая соль по п.1, где R2 и R3, которые являются одинаковыми или отличными друг от друга, представляют собой атом водорода, атом галогена, линейную C1-C8 алкильную группу или С2-С6 алкинильную группу, где их положение замещения представляет собой мета-положение или пара-положение.
5. Ариламидразоновое производное или его фармацевтически приемлемая соль по п.1, где R2 и R3, которые являются одинаковыми или отличными друг от друга, каждый представляет собой атом водорода, атом галогена, метильную группу или этинильную группу, где их положение замещения представляет собой мета-положение или пара-положение.
6. Ариламидразоновое производное или его фармацевтически приемлемая соль по п.1, где А представляет собой бензольное кольцо, пиридиновое кольцо, хинолиновое кольцо или изохинолиновое кольцо.
7. Ариламидразоновое производное или его фармацевтически приемлемая соль, выбранное из следующих соединений:
1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,5-дифторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(3-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(фенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-фторфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(4-фторфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-метилфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,5-дихлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфениламино)-1-(4-метилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-хлорфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-бромфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3,5-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(3,4-дихлорфениламино)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-бромфенилгидразоно)-1-(4-хлор-3-фторфениламино)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(3-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(3,4-дихлорфениламино)-2-гексанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-3-этил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-2-гексанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-3-этил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(3-фторфениламино)-4,4-диметил-2-пентанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-4,4-диметил-2-пентанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-гексанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-(2-фурил)-2-этанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-2-(2-фурил)-2-этанон,
1-(4-хлорфенилгидразоно)-1-(4-фторфениламино)-2-(2-фурил)-2-этанон,
1-(4-бромфениламино)-1-(4-хлорфенилгидразоно)-2-(2-фурил)-2-этанон,
4-хлор-1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(3,4-дихлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(3,4-дихлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3-фторфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(3,4-дихлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-бромфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлор-3-фторфениламино)-1-(4-хлорфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфенилгидразоно)-1-(4-этинилфениламино)-3,3-диметил-2-бутанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-3-этил-2-пентанон,
1-(4-этинилфениламино)-1-(4-этинилфенилгидразоно)-3,3-диметил-2-бутанон,
1-(4-хлорфениламино)-1-(4-хлорфенилгидразоно)-4,4-диметил-2-пентанон,
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-4,4-диметил-2-пентанон, и
1-(3-хлорфениламино)-1-(4-хлорфенилгидразоно)-2-гексанон.
8. Лекарственное средство, обладающее антагонистическим действием в отношении S1Р3 рецепторов, включающее ариламидразоновое производное или его фармацевтически приемлемую соль по п.1 в качестве активного ингредиента.
9. Терапевтическое или профилактическое средство при артериосклерозе, утолщении интимы, солидных опухолях, диабетической ретинопатии, сердечной недостаточности, ишемическом реперфузионном расстройстве, цереброваскулярном спазме после субарахноидального кровоизлияния, стенокардии или инфаркта миокарда, вызванного коронарным спазмом, гломерулонефрите, тромбозе, легочных заболеваниях, вызванных отеком легких (респираторный дистресс-синдром взрослых), брадикардии и парасимпатетически-опосредованной фибрилляции предсердия, где средство включает ариламидразоновое производное или его фармацевтически приемлемую соль по п.1 в качестве активного ингредиента.
10. Сосудорасширяющее средство, включающее ариламидразоновое производное или его фармацевтически приемлемую соль по п.1 в качестве активного ингредиента.
11. Антагонист S1P3 рецепторов, включающий ариламидразоновое производное или его фармацевтически приемлемую соль по п.1 в качестве активного ингредиента.
12. Фармацевтическая композиция, обладающая антагонистическим действием в отношении S1Р3 рецепторов, включающая ариламидразоновое производное или его фармацевтически приемлемую соль по п.1 и фармацевтически приемлемый носитель.
13. Фармацевтическая композиция по п.12, которая представляет собой фармацевтическую композицию для лечения и/или профилактики артериосклероза, утолщения интимы, солидных опухолей, диабетической ретинопатии, сердечной недостаточности, ишемического реперфузионного расстройства, цереброваскулярного спазма после субарахноидального кровоизлияния, стенокардии или инфаркта миокарда, вызванного коронарным спазмом, гломерулонефрита, тромбоза, легочных заболеваний, вызванных отеком легких (респираторный дистресс-синдром взрослых), брадикардии и парасимпатетически-опосредованной фибрилляции предсердия.
| DE 4114543 A1, 05.11.1992 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Шиванюк А.Ф | |||
| и др | |||
| Фенилиминоэтоксалилхлорид, дифенилоксимидоилхлорид и их реакции | |||
| Украинский химический журнал, 1979, т.45, №7, с.624-628 | |||
| Fawzy A | |||
| Attaby | |||
Авторы
Даты
2011-07-20—Публикация
2006-10-11—Подача