ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет предварительной заявки США 61/594107, поданной 2 февраля 2012 года. Полное содержание указанной предварительной заявки включено, таким образом, в качестве ссылки в настоящую заявку.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение, раскрытое в настоящем документе, относится к способам получения соединений, которые могут использоваться в качестве пестицидов (например, акарицидов, инсектицидов, моллюскицидов и нематицидов), к таким соединениям и к способам использования таких соединений для борьбы с вредителями.
УРОВЕНЬ ТЕХНИКИ
Вредители/паразиты ежегодно приводят к смерти миллионов людей по всему миру. Кроме того, существует более десяти тысяч видов вредителей, которые наносят большой урон сельскому хозяйству. Потери сельского хозяйства в мировом масштабе составляют миллиарды долларов США ежегодно.
Термиты могут вызывать поражение всех видов частных и общественных инфраструктур. Урон, наносимый термитами, в мировом масштабе составляет миллиарды долларов США ежегодно.
Амбарные вредители и вредители продуктов питания пожирают и портят их. Потери в мировом масштабе от амбарных вредителей и вредителей продуктов составляют миллиарды долларов США ежегодно, и, что более важно, при этом лишают людей необходимых продуктов питания.
Существует острая потребность в новых пестицидах. У некоторых вредителей развивается устойчивость к используемым в настоящее время пестицидам. Сотни видов вредителей устойчивы к одному или нескольким пестицидам. Резистентность к некоторым давно используемым пестицидам, таким как ДДТ, карбаматы и органофосфаты, хорошо известна, но уже появилась резистентность к некоторым новым пестицидам.
Таким образом, по многим причинам, в том числе по вышеуказанным причинам, существует потребность в новых пестицидах.
ОПРЕДЕЛЕНИЯ
Примеры, приведенные в разделе «Определения», как правило, не являются исчерпывающими и их не следует понимать как ограничивающие изобретение, раскрытое в настоящем документе. Понятно, что заместитель должен соответствовать правилам образования химических связей и стерической совместимости по отношению к конкретной молекуле, к которой он присоединен.
«Группа акарицидов» определена в разделе «АКАРИЦИДЫ».
«Группа АI» определена в этом документе после определения «гербицидной группы».
«Алкенил» обозначает aциклический ненасыщенный (по меньшей мере одна двойная связь углерод-углерод), разветвленный или неразветвленный, заместитель, состоящий из углерода и водорода, например, винил, аллил, бутенил, пентенил и гексенил.
«Алкенилокси» обозначает алкенил, дополнительно состоящий из одинарной связи углерод-кислород, например, аллилокси, бутенилокси, пентенилокси, гексенилокси.
«Алкокси» обозначает алкил, дополнительно состоящий из одинарной связи углерод-кислород, например, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси и трет-бутокси.
«Алкил» обозначает aциклический насыщенный, разветвленный или неразветвленный, заместитель, состоящий из углерода и водорода, например, метил, этил, пропил, изопропил, бутил и трет-бутил.
«Алкинил» обозначает aциклический ненасыщенный (по меньшей мере одна тройная связь углерод-углерод), разветвленный или неразветвленный, заместитель, состоящий из углерода и водорода, например, этинил, пропаргил, бутинил и пентинил.
«Алкинилокси» обозначает алкинил, дополнительно состоящий из одинарной связи углерод-кислород, например, пентинилокси, гексинилокси, гептинилокси и октинилокси.
«Арил» обозначает циклический ароматический заместитель, состоящий из водорода и углерода, например, фенил, нафтил и бифенил.
«Циклоалкенил» обозначает моноциклический или полициклический ненасыщенный (по меньшей мере одна двойная связь углерод-углерод) заместитель, состоящий из углерода и водорода, например, циклобутенил, циклопентенил, циклогексенил, норборненил, бицикло[2.2.2]октенил, тетрагидронафтил, гексагидронафтил и октагидронафтил.
«Циклоалкенилокси» обозначает циклоалкенил, дополнительно состоящий из одинарной связи углерод-кислород, например, циклобутенилокси, циклопентенилокси, норборненилокси и бицикло[2.2.2]октенилокси.
«Циклоалкил» обозначает моноциклический или полициклический, насыщенный заместитель, состоящий из углерода и водорода, например, циклопропил, циклобутил, циклопентил, норборнил, бицикло[2.2.2]октил и декагидронафтил.
«Циклоалкокси» обозначает циклоалкил, дополнительно состоящий из одинарной связи углерод-кислород, например, циклопропилокси, циклобутилокси, циклопентилокси, норборнилокси и бицикло[2.2.2]октилокси.
«Группа фунгицидов» определена в разделе «ФУНГИЦИДЫ».
«Галоген» обозначает фтор, хлор, бром и йод.
«Галогеналкокси» обозначает алкокси, дополнительно состоящий из от одного до максимально возможного числа идентичных или различных галогенов, например, фторметокси, трифторметокси, 2,2-дифторпропокси, хлорметокси, трихлорметокси, 1,1,2,2-тетрафторэтокси и пентафторэтокси.
«Галогеналкил» обозначает алкил, дополнительно состоящий из от одного до максимально возможного числа идентичных или различных галогенов, например, фторметил, трифторметил, 2,2-дифторпропил, хлорметил, трихлорметил и 1,1,2,2-тетрафторэтил.
«Группа гербицидов» определена в разделе «ГЕРБИЦИДЫ».
«Гетероциклил» обозначает циклический заместитель, который может быть либо полностью насыщенным или частично ненасыщенным, либо полностью ненасыщенным, где циклическая структура содержит по меньшей мере один углерод и по меньшей мере один гетероатом, где указанный гетероатом представляет собой азот, серу или кислород. Примеры ароматических гетероциклилов включают, но ими не ограничиваются, бензофуранил, бензоизотиазолил, бензоизоксазолил, бензоксазолил, бензотиенил, бензотиазолил ционнолинил, фуранил, индазолил, индолил, имидазолил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, оксадиазолил, оксазолинил, оксазолил, фталазинил, пиразинил, пиразолинил, пиразолил, пиридазинил, пиридил, пиримидинил, пирролил, хиназолинил, хинолинил, хиноксалинил, тетразолил, тиазолинил, тиазолил, тиенил, триазинил и триазолил. Примеры полностью насыщенных гетероциклилов включают, но ими не ограничиваются, пиперазинил, пиперидинил, морфолинил, пирролидинил, тетрагидрофуранил и тетрагидропиранил. Примеры частично ненасыщенных гетероциклилов включают, но ими не ограничиваются, 1,2,3,4-тетрагидрохинолинил, 4,5-дигидрооксазолил, 4,5-дигидро-1H-пиразолил, 4,5-дигидроизоксазолил и 2,3-дигидро-[1,3,4]оксадиазолил.
«Группа инсектицидов» определена в разделе «ИНСЕКТИЦИДЫ».
«Группа нематицидов» определена в разделе «НЕМАТИЦИДЫ».
«Синергическая группа» определена в разделе «СИНЕРГИЧЕСКИЕ СМЕСИ И СИНЕРГИСТЫ»
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем документы раскрыты соединения, имеющие следующие формулы («формула один», «формула два» и «формула три»): (в приведенных ниже формулах азоты пронумерованы 1, 2 и 3 исключительно в целях их идентификации и возможности ссылки на них на протяжении всего документа для ясности)
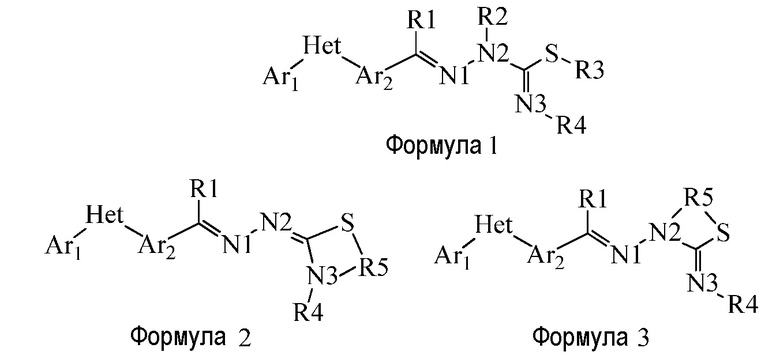
где:
(a) Ar1 представляет собой
(1) фуранил, фенил, пиридазинил, пиридил, пиримидинил, тиенил или
(2) замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил, или замещенный тиенил,
где указанный замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил и замещенный тиенил имеют один или несколько заместителей, независимо выбранных из H, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, фенокси, замещенного фенила и замещенного фенокси,
где такой замещенный фенил и замещенный фенокси имеет один или несколько заместителей, независимо выбранных из H, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил) фенила и фенокси;
(b) Het представляет собой 5- или 6-членное, насыщенное или ненасыщенное, гетероциклическое кольцо, содержащее один или несколько гетероатомов, независимо выбранных из азота, серы или кислорода, и где Ar1 и Ar2 не находятся в орто-положении по отношению друг к другу (но могут быть в мета- или пара-положениях, например, для пятичленного кольца они находятся в положении 1,3, а для 6-членного кольца они либо - 1,3, либо - 1,4), и где указанное гетероциклическое кольцо также может быть замещено одним или несколькими заместителями, независимо выбранными из H, F, Cl, Br, I, CN, NO2, оксо, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, фенокси, замещенного фенила и замещенного фенокси,
где такой замещенный фенил и замещенный фенокси имеет один или несколько заместителей, независимо выбранных из H, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, и фенокси;
(c) Ar2 представляет собой
(1) фуранил, фенил, пиридазинил, пиридил, пиримидинил, тиенил или
(2) замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил или замещенный тиенил,
где указанный замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил и замещенный тиенил имеют один или несколько заместителей, независимо выбранных из H, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, фенокси, замещенного фенила и замещенного фенокси,
где такой замещенный фенил и замещенный фенокси имеют один или несколько заместителей, независимо выбранных из H, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C1-C6 галогеналкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила и фенокси;
(d) R1 выбран из H, CN, F, Cl, Br, I, C1-C6 алкила, C3-C6 циклоалкила, C3-C6 циклоалкокси, C1-C6 алкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), OSO2(C1-C6 алкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила или фенокси,
где каждый алкил, циклоалкил, циклоалкокси, алкокси, алкенил, алкинил, фенил, и фенокси необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, оксо, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила и фенокси;
(e) R2 представляет собой H, C1-C6 алкил, C3-C6 циклоалкил, C2-C6 алкенил, C2-C6 алкинил, C(=O)H, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенил, C1-C6 алкилфенил, C1-C6 алкил-O-фенил, C(=O)Het-1, Het-1, C1-C6 алкилHet-1 или C1-C6 алкил-O-Het-1,
где каждый алкил, циклоалкил, алкенил, алкинил, фенил и Het-1 необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, NRxRy, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, фенокси и Het-1;
(f) R3 представляет собой C1-C6 алкил, C3-C6 циклоалкил, C2-C6 алкенил, C2-C6 алкинил, C(=O)H, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенил, C1-C6 алкилфенил, C1-C6 алкил-O-фенил, C(=O)Het-1, Het-1, C1-C6 алкилHet-1, C1-C6 алкил-O-C(=O)C1-C6 алкил-O-C1-C6 алкил, C1-C6 алкил-O-C(=O)C1-C6 алкил-O-C1-C6 алкил-O- C1-C6 алкил, C1-C6 алкил-O-C(=O)C1-C6 алкил-O-C1-C6 галогеналкил, C1-C6 алкил-O-C(=O)C1-C6 алкил-N(Rx)C(=O)-O-фенил, C1-C6 алкил-O-C(=O)C1-C6 алкил-N(Rx)C(=O)-O-C1-C6 алкилфенил, C1-C6 алкилC(=O)N(Rx)C1-C6 алкил, C1-C6 алкилC(=O)N(Rx)C1-C6 алкилHet-1C(=O)-O-C1-C6 алкил, C1-C6 алкилC(=O)N(Rx)C1-C6 алкилHet-1, C1-C6 алкилC(=O)Het-1, C1-C6 алкилC(=O)N(Rx)C1-C6 алкил(N(Rx)(Ry))(C(=O)OH), C1-C6 алкилC(=O)N(Rx)C1-C6 алкилN(Rx)(Ry), C1-C6 алкилC(=O)N(Rx)C1-C6 алкилN(Rx)C(=O)-O-C1-C6 алкил, C1-C6 алкилC(=O)N(Rx)C1-C6 алкил(N(Rx)C(=O)-O-C1-C6 алкил)(C(=O)OH), C1-C6 алкилC(=O)Het-1C(=O)-O-C1-C6 алкил, C1-C6 алкил-O-C(=O)-O-C1-C6 алкил, C1-C6 алкил-O-C(=O)C1-C6 алкил, C1-C6 алкил-O-C(=O)C3-C6 циклоалкил, C1-C6 алкил-O-C(=O)Het-1, C1-C6 алкил-O-C(=O)C1-C6 алкил-N(Rx)C(=O)-O-C1-C6 алкил, C1-C6 алкил-NRxRy или C1-C6 алкил-O-Het-1,
где каждый алкил, циклоалкил, алкенил, алкинил, фенил и Het-1 необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, NRxRy, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)OH, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, фенокси, Si(C1-C6 алкил)3, S(=O)nNRxRy и Het-1;
(g) R4 представляет собой H, C1-C6 алкил, C3-C6 циклоалкил, C2-C6 алкенил, C2-C6 алкинил, C(=O)H, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенил, C1-C6 алкилфенил, C1-C6 алкил-O-фенил, C(=O)Het-1, Het-1, C1-C6 алкилHet-1 или C1-C6 алкил-O-Het-1,
где каждый алкил, циклоалкил, алкенил, алкинил, фенил и Het-1 необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, NRxRy, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, фенокси и Нet-1;
(h) R5 представляет собой 2-4-членный насыщенный или ненасыщенный углеводородный линкер, где указанная линкер может быть также замещен по меньшей мере одним OH и, необязательно, одним или несколькими заместителями, выбранными из F, Cl, Br, I, CN, NO2, оксо, NRxRy, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)OH, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, фенокси и Het-1,
где каждый алкил, циклоалкил, циклоалкокси, алкокси, алкенил, алкинил, фенил, фенокси и Het-1 необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, оксо, NRxRy, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)OH, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, галогенфенила, фенокси и Het-1;
(i) n=0, 1, или 2;
(j) Rx и Ry независимо выбраны из H, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил) и фенила,
где каждый алкил, циклоалкил, циклоалкокси, алкокси, алкенил, алкинил, фенил, фенокси и Нet-1, необязательно, замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, оксо, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)H, C(=O)OH, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенила, галогенфенила, фенокси и Нet-1,
или Rx и Ry вместе могут, необязательно, образовывать 5-7-членную насыщенную или ненасыщенную циклическую группу, которая может содержать один или несколько гетероатомов, выбранных из азота, серы и кислорода, и где указанная циклическая группа может содержать >C=O или >C=S, и где указанная циклическая группа может быть замещена F, Cl, Br, I, CN, C1-C6 алкилом, C1-C6 галогеналкилом, C3-C6 циклоалкилом, C3-C6 галогенциклоалкилом, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенилом, C3-C6 циклоалкенилом, C2-C6 алкинилом, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), C(=O)(C3-C6 циклоалкил), C(=O)O(C3-C6 циклоалкил), C(=O)(C2-C6 алкенил), C(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)C(=O)O(C1-C6 алкил), фенилом, замещенным фенилом, фенокси и Нet-1; и
(k) Het-1 представляет собой 5- или 6-членное, насыщенное или ненасыщенное, гетероциклическое кольцо, содержащее один или несколько гетероатомов, независимо выбранных из азота, серы или кислорода.
Следует понимать, что если в формуле 1 R2 представляет собой H, то соединения могут существовать в более чем одной таутомерной или изомерной форме, где водород присоединен к любому атому азота; более того, дополнительно, могут существовать изомеры E и Z. Заявлены любые изомерные формы соединений по настоящему изобретению.
В другом варианте осуществления Ar1 представляет собой замещенный фенил, где указанный замещенный фенил имеет один или несколько заместителей, независимо выбранных из C1-C6 галогеналкила и C1-C6 галогеналкокси.
В другом варианте осуществления Ar1 представляет собой замещенный фенил, где указанный замещенный фенил имеет один или несколько заместителей, независимо выбранных из CF3, OCF3 и OCF2CF3.
В другом варианте осуществления Het выбран из триазолила, имидазолила или пиразолила, которые могут быть замещенными или незамещенными.
В другом варианте осуществления Het представляет собой 1,2,4-триазолил
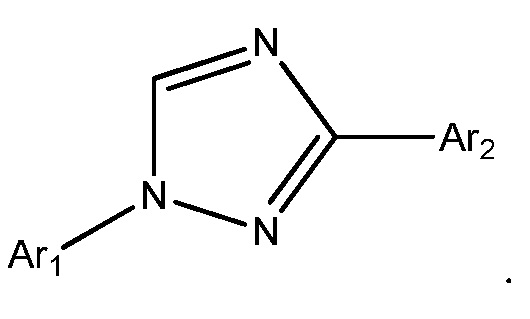
В другом варианте осуществления Het представляет собой 1,4-имидазолил
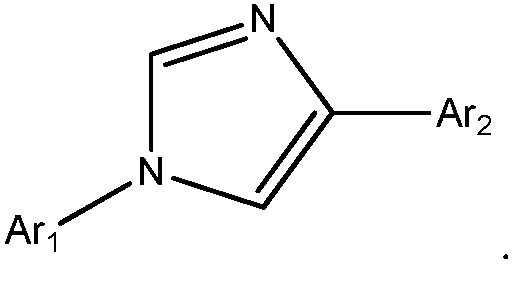
В другом варианте осуществления Het представляет собой 1,3-пиразолил
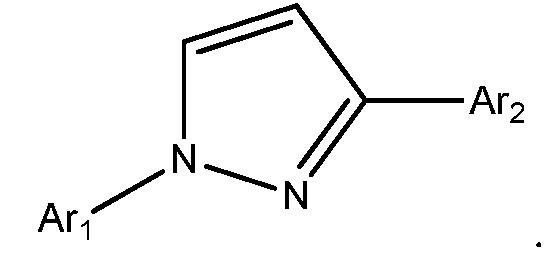
В другом варианте осуществления Het представляет собой замещенный 1,3-пиразолил.
В другом варианте осуществления Het представляет собой 1,4-пиразолил
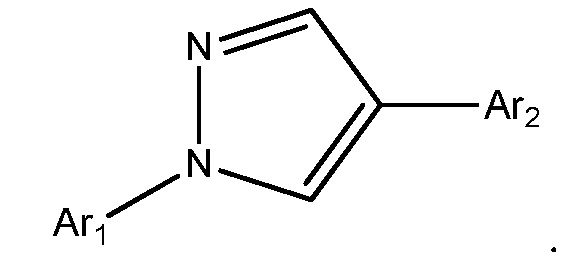
В другом варианте осуществления Ar2 представляет собой фенил.
В другом варианте осуществления R1 представляет собой H или C1-C6 алкил.
В другом варианте осуществления R1 представляет собой H или CH3.
В другом варианте осуществления R2 представляет собой H.
В другом варианте осуществления R3 выбран из C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C1-C6 алкилфенила, C1-C6 алкилHet-1, C1-C6 алкил-O-C(=O)C1-C6 алкил-O-C1-C6 алкила, C1-C6 алкил-O-C(=O)C1-C6 алкил-O-C1-C6 алкил-O-C1-C6 алкила, C1-C6 алкил-O-C(=O)C1-C6 алкил-O-C1-C6 галогеналкила, C1-C6 алкил-O-C(=O)C1-C6 алкил-N(Rx)C(=O)-O-фенила, C1-C6 алкил-O-C(=O)C1-C6 алкил-N(Rx)C(=O)-O-C1-C6 алкилфенила, C1-C6 алкилC(=O)N(Rx)C1-C6 алкила, C1-C6 алкилC(=O)N(Rx)C1-C6 алкилHet-1C(=O)-O-C1-C6 алкила, C1-C6 алкилC(=O)N(Rx)C1-C6 алкилHet-1, C1-C6 алкилC(=O)Het-1, C1-C6 алкилC(=O)N(Rx)C1-C6 алкил(N(Rx)(Ry))(C(=O)OH), C1-C6 алкилC(=O)N(Rx)C1-C6 алкилN(Rx)(Ry), C1-C6 алкилC(=O)N(Rx)C1-C6 алкилN(Rx)C(=O)-O-C1-C6 алкила, C1-C6 алкилC(=O)N(Rx)C1-C6 алкил(N(Rx)C(=O)-O-C1-C6 алкил)(C(=O)OH), C1-C6 алкилC(=O)Het-1C(=O)-O-C1-C6 алкила, C1-C6 алкил-O-C(=O)-O-C1-C6 алкила, C1-C6 алкил-O-C(=O)C1-C6 алкила, C1-C6 алкил-O-C(=O)C3-C6 циклоалкила, C1-C6 алкил-O-C(=O)Het-1, или C1-C6 алкил-O-C(=O)C1-C6 алкил-N(Rx)C(=O)-O-C1-C6 алкила, где каждый алкил, алкенил, алкинил, фенил и Het-1, необязательно, замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, C1-C6 алкила, C1-C6 галогеналкила, C1-C6 галогеналкокси, S(=O)n(C1-C6 алкил), C(=O)OH, C(=O)O(C1-C6 алкил), фенила, Si(C1-C6 алкил)3 и S(=O)nNRxRy.
В другом варианте осуществления R4 представляет собой фенил, C1-C6 алкилфенил, Het-1 или C1-C6 алкил-O-фенил, где каждый алкил, Het-1 и фенил, необязательно, замещены одним или несколькими заместителями, независимо выбранными из F, Cl, NRxRy, C1-C6 алкила, C3-C6 циклоалкила, C1-C6 галогеналкокси, C(=O)O C1-C6 алкила или C1-C6 алкокси.
В другом варианте осуществления R5 замещен оксо, C(=O)OH, фенилом и Het-1, где каждый фенил и Het-1 могут быть необязательно замещены одним или несколькими заместителями и независимо выбраны из оксо, C1-C6 галогеналкила, C1-C6 галогеналкокси, C(=O)OH и галогенфенила.
В другом варианте осуществления Rx и Ry независимо выбраны из H и фенила, где указанный фенил может быть необязательно замещен одним или несколькими заместителями, независимо выбранными из F и Cl.
В другом варианте осуществления:
Ar1 представляет собой замещенный фенил, где указанный замещенный фенил имеет один или несколько C1-C6 галогеналкокси;
Het представляет собой триазолил;
Ar2 представляет собой фенил;
R1 представляет собой H;
R2 представляет собой H;
R3 представляет собой C1-C6 алкилHet-1, где указанный алкил и Het-1 необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, C1-C6 алкила, C1-C6 галогеналкила, C1-C6 галогеналкокси, S(=O)n(C1-C6 алкил), C(=O)OH, C(=O)O(C1-C6 алкил), фенила, Si(C1-C6 алкил)3, и S(=O)nNRxRy;
R4 представляет собой фенил, где указанный фенил необязательно замещен одним или несколькими заместителями, независимо выбранными из F, Cl, NRxRy, C1-C6 алкила или C1-C6 алкокси; и
n=0, 1, или 2;
Rx и Ry независимо выбраны из H и фенила, где указанный фенил может быть необязательно замещен одним или несколькими заместителями, независимо выбранными из F и Cl; и
Het-1 представляет собой 5- или 6-членное, насыщенное или ненасыщенное, гетероциклическое кольцо, содержащее один или несколько гетероатомов, независимо выбранных из азота, серы или кислорода.
В другом варианте осуществления Het-1 выбран из бензофуранила, бензоизотиазолила, бензоизоксазолила, бензоксазолила, бензотиенила, бензотиазолил ционнолинила, фуранила, индазолила, индолила, имидазолила, изоиндолила, изохинолинила, изотиазолила, изоксазолила, оксадиазолила, оксазолинила, оксазолила, фталазинила, пиразинила, пиразолинила, пиразолила, пиридазинила, пиридила, пиримидинила, пирролила, хиназолинила, хинолинила, хиноксалинила, тетразолила, тиазолинила, тиазолила, тиенила, триазинила, триазолила, пиперазинила, пиперидинила, морфолинила, пирролидинила, тетрагидрофуранила, тетрагидропиранила, 1,2,3,4-тетрагидрохинолинила, 4,5-дигидрооксазолила, 4,5-дигидро-1H-пиразолила, 4,5-дигидроизоксазолила и 2,3-дигидро-[1,3,4]-оксадиазолила.
В другом варианте осуществления Het выбран из бензофуранила, бензоизотиазолила, бензоизоксазолила, бензоксазолила, бензотиенила, бензотиазолила, циннолинила, фуранила, индазолила, индолила, имидазолила, изоиндолила, изохинолинила, изотиазолила, изоксазолила, оксадиазолила, оксазолинила, оксазолила, фталазинила, пиразинила, пиразолинила, пиразолила, пиридазинила, пиридила, пиримидинила, пирролила, хиназолинила, хинолинила, хиноксалинила, тетразолила, тиазолинила, тиазолила, тиенила, триазинила, триазолила, пиперазинила, пиперидинила, морфолинила, пирролидинила, тетрагидрофуранила, тетрагидропиранила, 1,2,3,4-тетрагидрохинолинила, 4,5-дигидрооксазолила, 4,5-дигидро-1H-пиразолила, 4,5-дигидроизоксазолила и 2,3-дигидро-[1,3,4]-оксадиазолила.
В другом варианте осуществления Het-1 выбран из бензофуранила, бензоизотиазолила, бензоизоксазолила, бензоксазолила, бензотиенила, бензотиазолила, бензотиадизолила, циннолинила, фуранила, индазолила, индолила, имидазолила, изоиндолила, изохинолинила, изотиазолила, изоксазолила, оксадиазолила, оксазолинила, оксазолила, фталазинила, пиразинила, пиразолинила, пиразолила, пиридазинила, пиридила, пиримидинила, пирролила, хиназолинила, хинолинила, хиноксалинила, тетразолила, тиазолинила, тиазолила, тиенила, тиенилпиразолила, триазинила, триазолила, пиперазинила, пиперидинила, морфолинила, пирролидинила, тетрагидрофуранила, тетрагидропиранила, 1,2,3,4-тетрагидрохинолинила, 4,5-дигидрооксазолила, 4,5-дигидро-1H-пиразолила, 4,5-дигидроизоксазолила и 2,3-дигидро-[1,3,4]-оксадиазолила.
В другом варианте осуществления Het-1 выбран из бензотиадизолила, фуранила, оксазолила и тиенилпиразолила.
Несмотря на то что были приведены эти варианты осуществления, возможны другие варианты осуществления и комбинации этих приведенных вариантов осуществления и других вариантов осуществления.
Соединения формул один, два и три, как правило, обладают молекулярной массой, равной приблизительно от 100 Дальтон до приблизительно 1200 Дальтон. Однако, как правило, предпочтительно, если молекулярная масса составляет приблизительно от 120 Дальтон до приблизительно 900 Дальтон, и, как правило, еще более предпочтительно, если молекулярная масса составляет приблизительно от 400 Дальтон до приблизительно 800 Дальтон.
ПОЛУЧЕНИЕ ТРИАРИЛ-ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ
Соединения по настоящему изобретению могут быть получены через получение промежуточного соединения триарил, Ar1-Het-Ar2, а затем присоединения его к желаемому промежуточному соединению с получением желаемого соединения. Для получения соединений по настоящему изобретению можно использовать широкий спектр промежуточных соединений триарила, при условии, что такие промежуточные соединения триарила содержат подходящую функциональную группу на Ar2, к которой может быть присоединена оставшаяся часть желаемого промежуточного соединения. Подходящие функциональные группы включают группы оксоалкил или формил. Эти промежуточные соединения триарила могут быть получены способами, ранее описанным в химической литературе, в том числе Crouse et al. публикация международной заявки PCT WO 2009/102736 A1.
ПОЛУЧЕНИЕ ГИДРАЗОН-СВЯЗАННЫХ СОЕДИНЕНИЙ
Гидразон-связанные соединения могут быть получены из соответствующих арилальдегидов или кетонов одним из трех способов: (1) путем взаимодействия с гидразином, а затем путем взаимодействия с арилизотиоцианатом в тетрагидрофуране (ТГФ) при температуре от 0 до 100°C (реакция A); (2) путем взаимодействия с метилкарбодитиоатом, а затем путем взаимодействия с анилином в полярном апротонном растворителе, таком как N,N-диметилформамид (ДМФ), при температуре от 25 до 150°C (реакция B); или (3) путем взаимодействия с арилтиосемикарбазидом, который либо коммерчески доступен, либо может быть получен специалистом в данной области, в полярном протонном растворителе, таком как этиловый спирт (EtOH), при температуре от 0 до 100°C (реакция C).
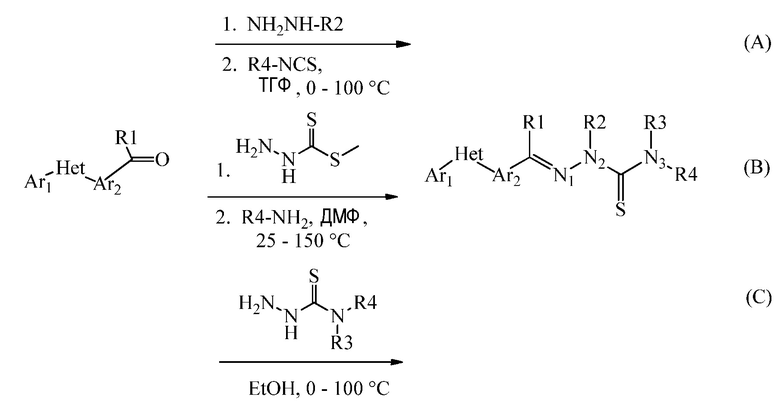
ПОЛУЧЕНИЕ АЛКИЛИРОВАННЫХ ГИДРАЗОН-СВЯЗАННЫХ СОЕДИНЕНИЙ
Алкилированные гидразон-связанные соединения могут быть получены из соответствующих гидразон-связанных соединений одним из двух способов: (1) путем взаимодействия с алкилирующим агентом в EtOH или ацетоне при температуре от 0 до 100°C в течение от 1 до 24 часов или (2) путем взаимодействия с алкилирующим агентом в хлороформе (CHCl3), дихлорметане (CH2Cl2) или другом галогенуглеродном растворителе, без или вместе с основанием, таким как бикарбонат натрия, при температуре от 20 до 60°C.
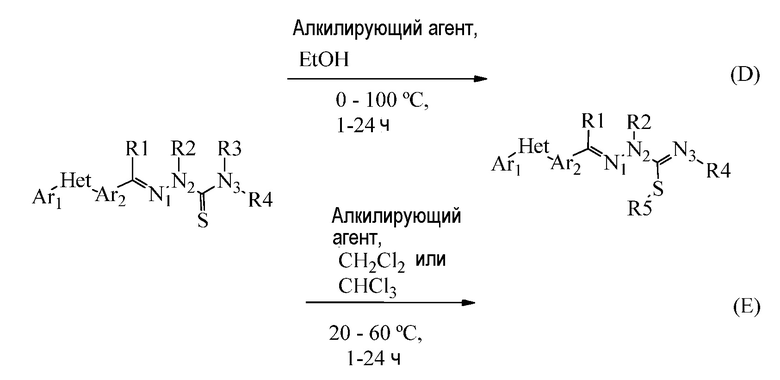
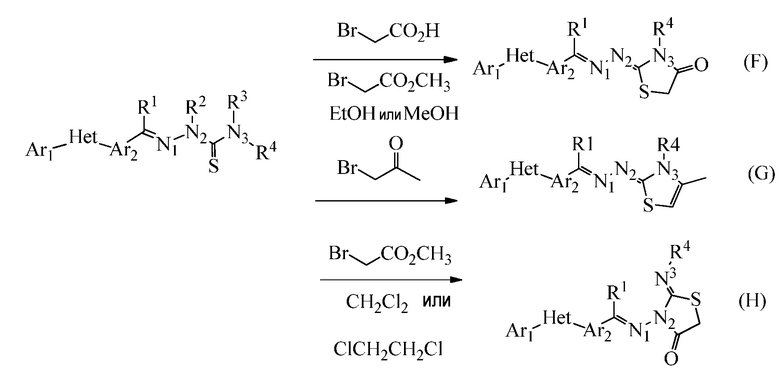
Соединения формулы два, где R5 образует кольцо с N3 (см. схему ниже), или формулы три, где R5 образует кольцо с N2, могут быть получены из подходящего aциклического предшественника, используя α-галогенкислоты, галогенангидриды, сложные эфиры или кетоны (F или G или H). Например, обработка тиосемикарбазона небольшим избытком α-галогенэфира, в протонном растворителе, таком как EtOH или метиловый спирт (CH3OH), дает S-алкилирование и последующее закрытие кольца только на N3 (реакция F; см. например, J. Indian Chemical Society 1966, 43, 275-276, или J. Heterocycl. Chem. 1978, 15, 335-336). Если апротонный растворитель, такой как CH2Cl2 или дихлорэтан (ClCH2CH2Cl), используют при температуре от 30°C до 80°C, ориентация присоединения α-галогенкетонов также способствует закрытию на N3, то затем проводят дегидратацию с получением иминотиазола (реакция G). Вместе с α-галогенкислотами или галогенангидридами или сложными эфирами в галогенуглеродном растворителе, таком как CH2Cl2 или ClCH2CH2Cl, наблюдают закрытие кольца как на N2 (реакция H), так и на N3. Хотя эти реакции часто протекают без добавления основания, можно добавить основание, такое как бикарбонат натрия, карбонат натрия или ацетат натрия, или аминооснование, такое как пиридин или триэтиламин.
Альтернативно, 3-арилидинимино-2-арилиминотиазолин-4-оны могут быть получены обработкой альдегида или кетона, где R1 такой, как описано выше, 3-амино-2-(арилимино)тиазолидин-4-оном в уксусной кислоте при температуре от 30 до 70°C, как показано ниже на схеме (I). Промежуточное соединение 1-амино-2-арилиминотиазолин-5-она, где R4 представляет собой фенил, описано (см., например, J. Org. Chem. 1962, 27, 2878); было получено с 80% выходом путем обработки 4-фенилтиосемикарбазида этил 2-хлорацетатом и натрий ацетатом в горячем EtOH.
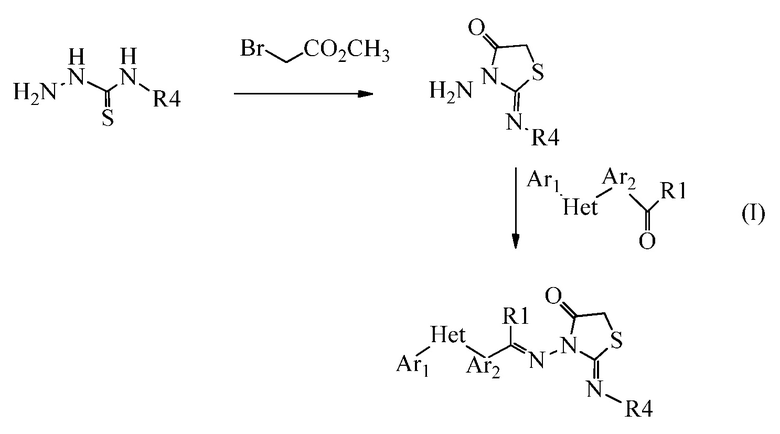
Альтернативно, соединения формулы 2 и формулы 3 могут быть получены путем нагревания тиосемикарбазонового предшественника с ди-галогеновой группой Hal1-R5-Hal2, такой как 1-бром-2-хлорэтан, в ацетоне или 2-бутаноне или в другом подходящем растворителе, используя основание, такое как карбонат калия или триэтиламин, при температуре от температуры окружающей среды до 100°C в течение от 1 до 72 часов. S-алкилированные промежуточные соединения подвергали циклизации на N2 или N3, получая соединения формулы два или формулы три (реакция J). В некоторых случаях, может потребоваться добавление KI для ускорения циклизации промежуточных S-алкилированных производных до продуктов с закрытыми кольцами.
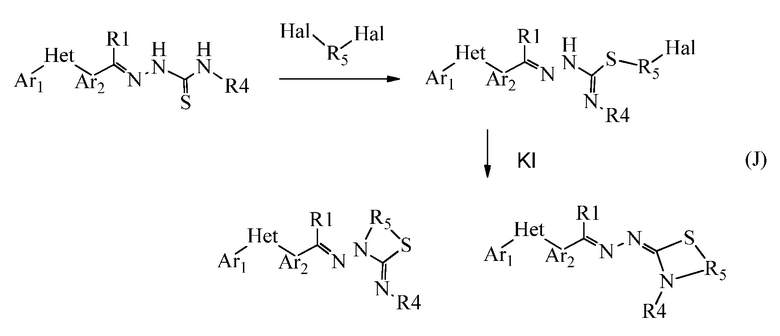
Альтернативным способом получения соединений по настоящему изобретению является способ обработки тиосемикарбазонового предшественника ненасыщенным сложным эфиром или хлорангидридом (реакция L).
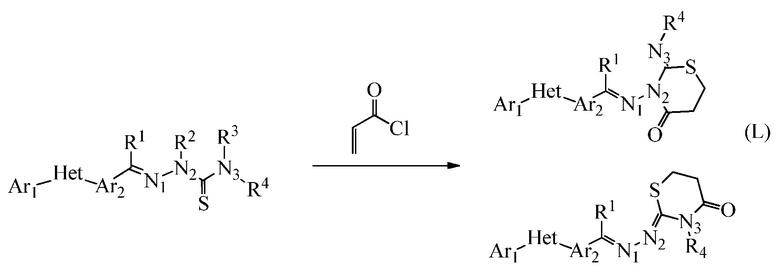
Соединения формулы два, где R5 образует гидроксил-содержащее кольцо с N3, или формулы три, где R5 образует гидроксил-содержащее кольцо с N2 (см. схему ниже), могут быть получены из подходящего aциклического предшественника, используя α-галогенкетон (реакция M). Эта методика сходна с реакцией G; перед дегидратацией промежуточный гидрокситиазолин можно выделить в более мягких условиях (как правило, при температуре от окружающей среды до 90°C). Эту методику удобно осуществлять в апротонном растворителе, таком как ацетон, 2-бутанон или дихлорэтан, без или вместе с основанием, таким как триэтиламин или бикарбонат натрия. Направление циклизации обычно способствует реакции на N3, хотя если используются группы R4 с сильным пространственным затруднением, то могут быть получены продукты, полученные при циклизации на N2.
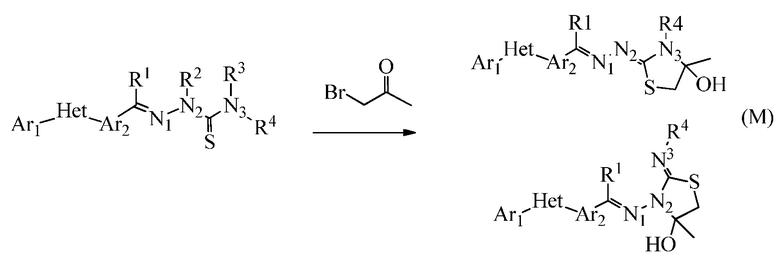
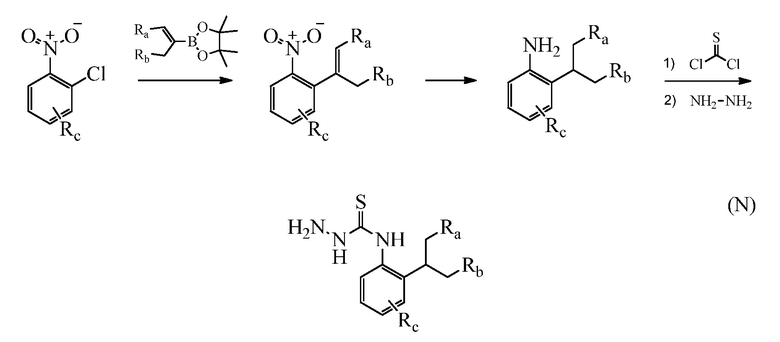
Замещенные гидразинкарботиоамидные промежуточные соединения, такие как группы, используемые в способе C выше, могут быть получены рядом способов, известных в химической литературе. Альтернативно, соединения, в которых Ra, Rb и Rc получены не из коммерчески доступного анилина, могут быть получены в соответствии со схемой ниже. Например, 2-галогеннитробензол, такой как 2-хлорнитробензол, замещенный одним или множественными заместителями Rc, где Rc может быть H, алкилом, алкокси или галогеном, таким как фтор, может взаимодействовать с бороновой кислотой или эфиром бороната, таким как замещенный 4,4,5,5-тетраметил-1,3,2-диоксаборолан, где Ra и Rb представляют собой H, в присутствии основания, например, карбоната натрия, и палладиевого катализатора, такого как хлорид биc(трифенилфосфин)палладия (II), в водной системе растворителя, такой как 4:1 диоксан/вода, при повышенной температуре, например, 80°C, с получением нитробензольных соединений, замещенных алкенилом. Альтернативно, Ra и Rb могут быть взяты вместе с образованием кольца, такого как циклопентен, с получением соответствующего 2-(циклопент-1-ен-1-ил)-4,4,5,5-тетраметил-1,3,2-диоксаборолана, который в условиях, описанных выше, дает нитробензол, замещенный циклическим алкеном. Обработка раствора олефинных нитробензолов в апротонном растворителе, таком как этилацетат, где Ra, Rb и Rc такие, как определено выше, водородным газом в присутствии катализатора, например, палладия на угле (Pd/C), дает соответствующие анилины, замещенные алкилами или циклоалкилами. Обработка двухфазного раствора анилинов, где Ra, Rb и Rc такие, как определено выше, в смеси галогенированного растворителя и воды, такой как 2:1 дихлорметан/вода, основанием, таким как гидрокарбонат натрия, а затем тиофосгеном дает промежуточные изотиоцианатобензолы. Разделение и удаление водной фазы, а затем сушка и упаривание органического растворителя дает сырое промежуточное соединение, которое немедленно растворяют в спирту, таком как этанол, и обрабатывают гидразин гидратом с получением промежуточных соединений гидразинкарботиоамида, где Ra, Rb и Rc такие, как определено.
ПРИМЕРЫ
Примеры приведены для иллюстративных целей и не должны рассматриваться как ограничивающие изобретение, раскрытое в настоящем документе, только вариантами осуществления, раскрытыми в этих примерах.
Исходные вещества, реагенты и растворители, которые были получены из коммерческих источников, использовали без дополнительной очистки. Безводные растворители были приобретены как Sure/Seal™ от Aldrich и использовались в полученном виде. Температуру плавления получали на капиллярном аппарате для определения точки плавления Thomas Hoover Unimelt или на автоматизированной системе определения точки плавления OptiMelt от Stanford Research Systems и не корректировали. Соединения приведены с известными названиями, присвоенными в соответствии с программой MDL ISIS™/Draw 2.5, ChemBioDraw Ultra 12.0 или ACD Name Pro. Если такая программа не доступна, то соединения называли, используя обычные правила. Спектральные данные 1H ЯМР находятся в м.д. (δ) и их регистрировали при 300, 400 или 600 МГц, а спектральные данные 13С ЯМР находятся в м.д. (δ) и их регистрировали при 75, 100 или 150 МГц, если не указано иного.
Пример 1: Получение (E)-N-(4-диметиламино)фенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (соединение I-1) [способ синтеза A].
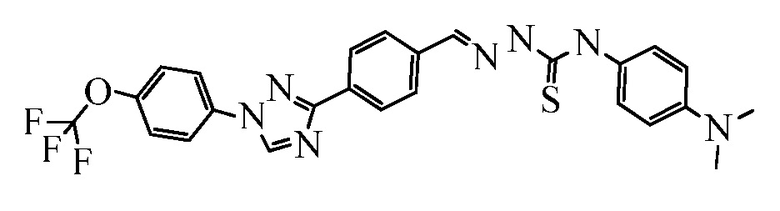
Стадия 1. (E)-3-(4-(Гидразонометил)фенил)-1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол. В 250-миллилитровую (мл) круглодонную колбу, содержащую гидразингидрат (64% водный (водн.) раствор; 7,27 мл, 15,0 миллимолей (ммоль)) в EtOH (100 мл), при 80°C порциями добавляли 4-[1-(4-трифторметоксифенил)-1H-[1,2,4]триазол-3-ил]бензальдегид (5,00 грамм (г), 1,50 ммоль) в течение 5 минут (мин). Раствор перемешивали при кипячении с обратным холодильником в течение дополнительных 3 часов (ч), а затем разбавляли водой (H2O; 300 мл) и охлаждали до 0°C. Выпавший в осадок продукт собирали вакуумной фильтрацией в виде белого твердого вещества (4,89 г, 93%): т.пл. 222-226°C; 1H ЯМР (400 МГц, ДМСО-d6) δ 8,59 (с, 1H), 8,22 (д, J=8,2 Гц, 2H), 7,84-7,79 (м, 3H), 7,66 (д, J=8,3 Гц, 2H), 7,41 (д, J=8,2 Гц, 2H), 7,29 (с, 1H), 5,63 (уш.с, 2H); ESIMS m/z 348 (M+H).
Стадия 2. В 25 мл круглодонную колбу, содержащую (E)-3-(4-(гидразонометил)фенил)-1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол (250 мг, 0,720 ммоль) в ТГФ (10 мл), добавляли 4-изотиоцианато-N,N-диметиланилин (385 мг, 2,16 ммоль). Содержимое нагревали при 65°C при перемешивании в течение 2 часов, а затем растворитель удаляли при пониженном давлении. Остаток суспендировали в CH2Cl2 (10 мл) в результате чего, продукт выпадал в осадок. Целевой продукт получали в виде желтого твердого вещества с помощью вакуумной фильтрации (350 мг, 93%): т.пл. 205-208°C; 1H ЯМР (400 МГц, ДМСО-d6) δ 11,78 (с, 1H), 10,02 (с, 1H), 9,42 (с, 1H), 8,19-7,99 (м, 6H), 7,64 (д, J=8,3 Гц, 2H), 7,28 (д, J=8,3 Гц, 2H), 7,73 (д, J=8,3 Гц, 2H), 2,92 (с, 6H); ESIMS m/z 526 (M+H).
Пример 2: Получение N-(3-(диметиламино)фенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (соединение I-2) [способ синтеза B].
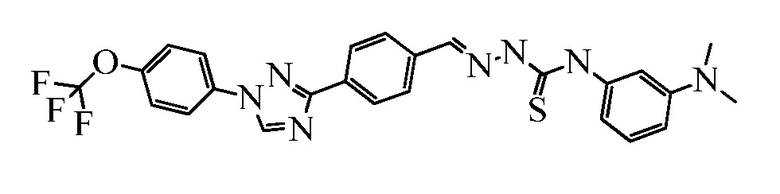
Стадия 1. (E)-Метил 2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарбодитиоат. В 250 мл круглодонную колбу, содержащую метиловый эфир гидразиндитиокарбоновой кислоты (2,38 г, 1,95 ммоль) в EtOH (100 мл), добавляли 4-[1-(4-трифторметоксифенил)-1H-[1,2,4]триазол-3-ил]бензальдегид (5,00 г, 1,50 ммоль). Сосуд нагревали при 80°C в течение 3 часов, а затем разбавляли H2O (300 мл) и охлаждали до 0°C. Выпавший в осадок продукт собирали вакуумной фильтрацией в виде не совсем белого твердого вещества (6,13 г, 93%): т.пл. 204-206°C; 1H ЯМР (400 МГц, ДМСО-d6) δ 13,39 (с, 1H), 9,43 (с, 1H), 8,38 (с, 1H), 8,21 (д, J=8,3 Гц, 2H), 8,09 (д, J=8,4 Гц, 2H), 7,88 (д, J=8,4 Гц, 2H), 7,62 (д, J=8,3 Гц, 2H), 2,57 (с, 3H); ESIMS m/z 438 (M+H).
Стадия 2. В 50 мл круглодонную колбу, содержащую (E)-метил 2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарбодитиоат (250 мг, 0,571 ммоль) в ДМФ (3 мл), добавляли N1,N1-диметилбензол-1,3-диамин (195 мг, 1,43 ммоль). Содержимое нагревали при 150°C при перемешивании в течение 5 час, а затем раствор оставляли охлаждаться в течение ночи. Смесь фильтровали, и фильтрат очищали при помощи ОФ-ВЭЖХ с получением желаемого вещества (235 мг, 78%) в виде беловатого твердого вещества: т.пл. 192-194°C; 1H ЯМР (400 МГц, ДМСО-d6) δ 11,82 (с, 1H), 10,04 (с, 1H), 9,41 (с, 1H), 8,19 (с, 1H), 8,16-7,99 (м, 6H), 7,61 (д, J=8,3 Гц, 2H), 7,16 (т, J=7,2 Гц, 1H), 7,01 (м, 1H), 6,87 (м, 1H), 6,58 (м, 1H), 2,88 (с, 6H); ESIMS m/z 526 ([M+H]+).
Пример 3: Получение N-бензил-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (соединение I-3) [способ синтеза C].
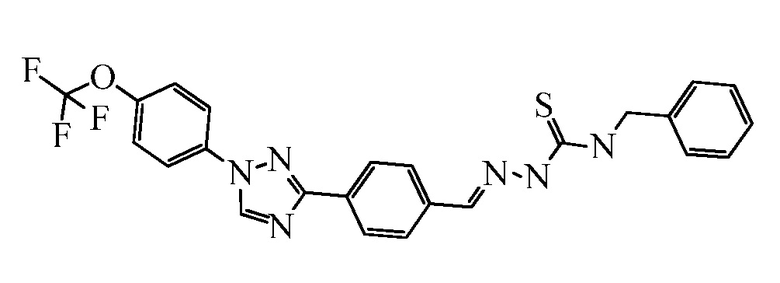
В 50 мл круглодонную колбу, содержащую 4-[1-[4-(трифторметокси)фенил]-1,2,4-триазол-3-ил]бензальдегид (500 мг, 1,5 ммоль) в EtOH (3 мл), добавляли 4-бензоилтиосемикарбазид (650 мг, 3,6 ммоль). Реакционную смесь нагревали при 80°C в течение ночи. После завершения реакции добавляли H2O, и сырое вещество продукта выделяли вакуумной фильтрацией. Указанное в заголовке соединение выделяли при помощи ОФ-ВЭЖХ в виде белого твердого вещества (390 мг, 52%): т.пл. 220-224°C; 1H ЯМР (400 МГц, CDCl3) δ 9,29 (с, 1H), 8,59 (с, 1H), 8,21 (д, J=8,4 Гц, 2H), 7,85-7,79 (м, 3H), 7,71 (д, J=8,4 Гц, 2H), 7,46-7,30 (м, 8H), 5,01 (д, J=5,8 Гц, 2H); ESIMS m/z 497,2 (M+H).
Соединения с I-4 по I-31 в таблице 1 синтезировали в соответствие с приведенными выше примерами. Другие промежуточные соединения, используемые при получении соединений по настоящему изобретению, получали в соответствие с методиками, описанными в статье Brown et al., WO 2011017504 A1, или при помощи других известных путей.
Пример 4: Получение N-(4-диметиламинофенил)-S-метил-2-{4-[1-(4-трифторметоксифенил)-1H-[1,2,4]-триазол-3-ил]бензилиден}гидразинкарботиоамида (соединение 1C) (способ синтеза D)
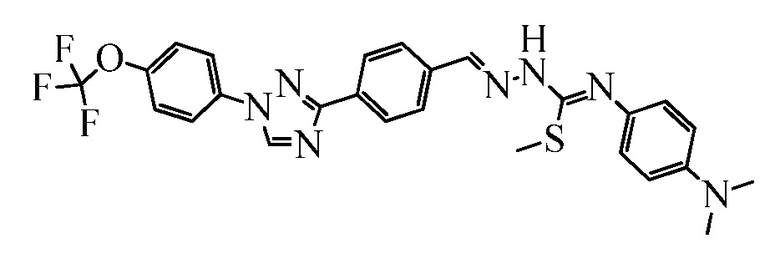
Раствор, содержащий (E)-N-(4-(диметиламино)фенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамид (150 мг, 0,285 ммоль) и йодметан (0,054 мл, 0,856 ммоль) в EtOH (5 мл), нагревали при 80°C в течение 3 часов, а затем растворитель удаляли при пониженном давлении. Остаток очищали при помощи флэш-хроматографии с нормальной фазой (градиентное элюирование смесью гексан/EtOAc) с получением указанного в заголовке соединения в виде оранжевой пены (93 миллиграммы (мг), 60%): 1H ЯМР (400 МГц, ДМСО-d6) δ 8,61 (с, 1H), 8,48 (с, 1H), 8,22 (д, J=8,24 Гц, 2H), 8,17 (с, 1H), 7,89 (д, J=8,24 Гц, 2H), 7,80 (д, J=8,28 Гц, 2H), 7,41 (д, J=8,28 Гц, 2H), 7,19 (д, J=8,24 Гц, 2H), 6,71 (д, J=8,24 Гц, 2H), 2,99 (с, 6H), 2,42 (с, 3H); EIMS m/z 540 (M+).
Пример 5: Общая методика для S-алкилирования триарил тиосемикарбазонов (способ синтеза E)
Перемешиваемый раствор тиосемикарбазона и алкилирующего реагента в CH2Cl2 или хлороформе (CHCl3) нагревали при температуре от 35 до 50°C в течение от 10 до 24 часов. Охлажденный раствор концентрировали при пониженном давлении. Остаток, в целом, очищали при помощи хроматографии, используя в качестве элюента хлороформ/метанол (CHCl3/CH3OH) или раствор EtOAc-гексана, с получением S-алкилированных продуктов.
Пример 6: Получение (S)-трет-бутил 3-((2-((Z)-(2,6-диметилфенилимино)-((E)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинил)метилтио)ацетамидо)метил)пиперидин-1-карбоксилата (соединение 56C) (способ синтеза E)

К раствору бромацетилбромида (26 микролитров (мкл), 0,299 ммоль) в дихлорэтане (3 мл) по каплям добавляли раствор (S)-трет-бутил 3-(аминометил)пиперидин-1-карбоксилата (63,9 мг, 0,298 ммоль) в дихлорметане (1 мл), затем N-этил-N-изопропилпропан-2-амин (76 мг, 0,588 ммоль). Эту смесь перемешивали при комнатной температуре в течение 30 мин, затем добавляли (E)-N-(2,6-диметилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамид в виде твердого вещества (100 мг, 0,196 ммоль), и смесь нагревали при 40°C в течение 90 мин. Затем смесь оставляли остывать до комнатной температуры и упаривали при пониженном давлении с получением светло-желтого стекла, которое растворяли в ацетонитриле (2 мл) и оставляли при комнатной температуре. Полученный осадок выделяли при помощи центрифугирования и декантирования, промывая свежим ацетонитрилом. Твердое вещество сушили в потоке азота, а затем в высоком вакууме. Сырой продукт перекристаллизовывали из ацетон-изопропилового спирта. Указанное в заголовке соединение выделяли в виде белого твердого вещества (36,5 мг, 24%): т.пл. 148-151°C; 1H ЯМР (400 МГц, метанол-d4) δ 9,18 (с, 1H), 8,59 (с, 1H), 8,30 (д, J=8,1 Гц, 2H), 8,12 (м, 2H), 8,07-8,00 (м, 2H), 7,58-7,43 (м, 2H), 7,33 (дд, J=8,6, 6,5 Гц, 1H), 7,25 (д, J=7,6 Гц, 2H), 4,02 (м, 2H), 3,97-3,75 (м, 2H), 3,21 (д, J=6,9 Гц, 2H), 2,90 (м, 1H), 2,59 (м, 1H), 2,35 (с, 6H), 1,84 (м, 2H), 1,78-1,63 (м, 2H), 1,44 (с, 9H), 1,29 (м, 3H); ESIMS m/z 765 (M+H).
Пример 7: Получение (1Z,2E)-2-оксо-2-(((R)-пиперидин-3-илметил)амино)этил N-(2,6-диметилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарбимидотиоата трифторуксусной кислоты (соединение 62C) (способ синтеза K)
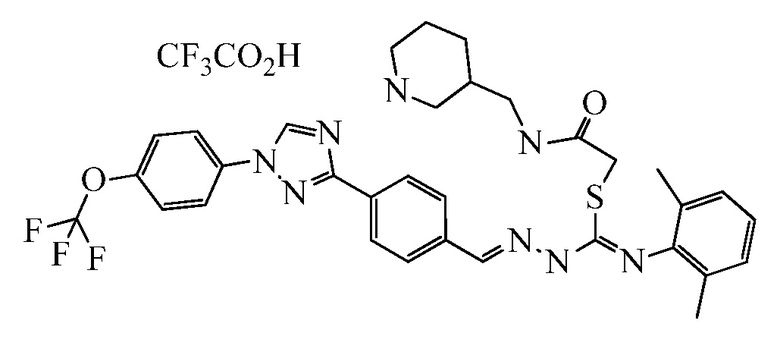
Раствор (S)-трет-бутил 3-((2-((Z)-(2,6-диметилфенилимино)-((E)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинил)метилтио)ацетамидо)метил)пиперидин-1-карбоксилата (32,0 мг, 0,042 ммоль) в ТФУ (250 мкл, 3,24 ммоль) перемешивали при комнатной температуре в течение 10 мин. Затем добавляли Et2O (10 мл) с получением белого осадка, который выделяли при помощи центрифугирования и декантирования, затем промывали свежим Et2O (5 мл). Твердое вещество сушили в потоке азота, а затем в высоком вакууме с получением указанного в заголовке соединения в виде белого твердого вещества (19,8 мг, 60%): т.пл. 110-120°C; 1H ЯМР (400 МГц, метанол-d4) δ 9,18 (с, 1H), 8,56 (м, 1H), 8,26 (м, 2H), 8,16-7,84 (м, 4H), 7,52 (м, 2H), 7,27 (м, 1H), 7,22 (м, 2H), 4,00 (с, 2H), 3,28 (м, 3H), 3,06-2,83 (м, 1H), 2,75 (т, J=12,2 Гц, 1H), 2,34 (с, 6H), 2,21-1,83 (м, 4H), 1,72 (м, 1H), 1,47-1,19 (м, 2H); ESIMS m/z 665 (M+H).
Пример 8: Получение натриевой соли 2-(((Z)-((4-метокси-2,6-диметилфенил)имино)((E)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинил)метил)тио)уксусной кислоты (соединение 68C)
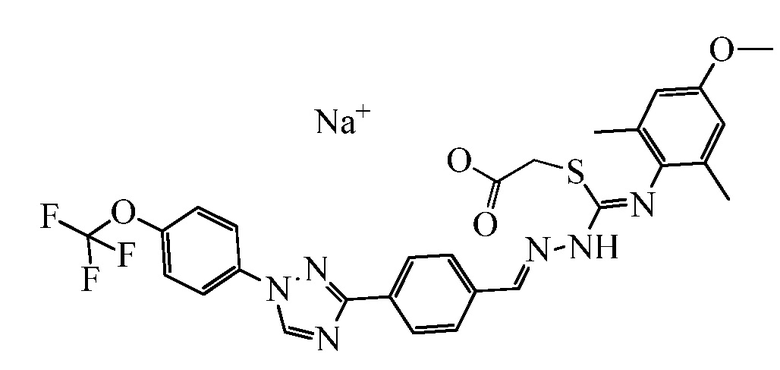
К раствору 2-((Z)-(4-метокси-2,6-диметилфенилимино)((E)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинил)метилтио)уксусной кислоты (77,7 мг, 0,130 ммоль) в ТГФ (10 мл) медленно добавляли метанолат натрия (0,5M в метаноле; 260 мкл, 0,130 ммоль) при комнатной температуре. Смесь немедленно становилась темно-желтой, затем смесь упаривали при комнатной температуре в вакууме с получением светло-оранжевого твердого вещества. Это вещество растирали с Et2O (2×) и выделяли при помощи декантирования, центрифугирования, сушили в потоке азота, а затем в высоком вакууме. Указанное в заголовке соединение выделяли в виде светло-оранжевого твердого вещества (32 мг, 39%): т.пл. 146-154°C; 1H ЯМР (400 МГц, метанол-d4) δ 9,11 (с, 1H), 8,64-7,68 (м, 7H), 7,51 (м, 2H), 6,70 (с, 2H), 3,85-3,70 (м, 4H), 3,61 (м, 1H), 2,29 (с, 6H); ESIMS m/z 599 (M+H).
Пример 9: Получение (Z)-3-(4-метокси-2,6-диметилфенил)-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидин-4-она (соединение 69C) (способ синтеза F)
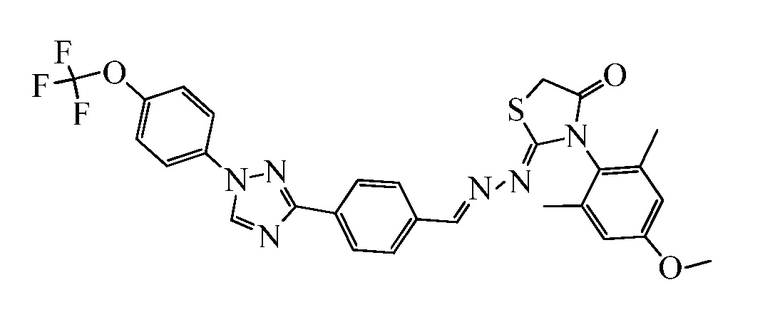
К раствору (E)-N-(4-метокси-2,6-диметилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (250 мг, 0,462 ммоль) в EtOH (5 мл) добавляли метилбромацетат (100 мг, 0,65 ммоль), и смесь нагревали при 70°C в течение 4 часов. Смесь оставляли охлаждаться до комнатной температуры и разбавляли водой (1 мл). Осадок фильтровали под вакуумом с получением указанного в заголовке соединения в виде белого твердого вещества (204 мг, 76%): т.пл. 188-190°C; 1H ЯМР (400 МГц, CDCl3) δ 8,56 (с, 1H), 8,33 (с, 1H), 8,22 (д, J=8,1 Гц, 2H), 7,90-7,70 (м, 4H), 7,39 (д, J=8,7 Гц, 2H), 6,72 (с, 2H), 4,01 (с, 2H), 3,87-3,73 (с, 3H), 2,18 (с, 6H); ESIMS m/z 581 (M+H).
Пример 10: Получение 4-((2Z)-3-(2,6-диметилфенил)-2-((4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-2,3-дигидротиазол-4-ил)-N,N-диэтиланилина (соединение 74C) (способ синтеза G)
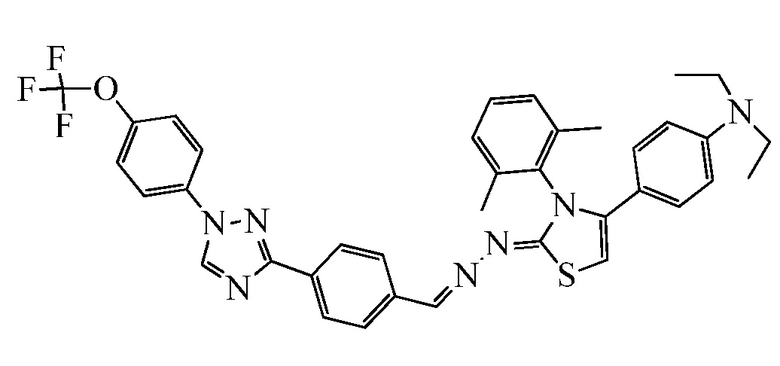
К раствору (E)-N-(2,6-диметилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (74,7 мг, 0,144 ммоль) в дихлорэтане (5 мл) добавляли α-бром-4-диэтиламино)ацетофенон (53,9 мг, 0,199 ммоль), и смесь нагревали при 40°C в течение 4 часов. Затем смесь охлаждали до комнатной температуры и упаривали в вакууме. Сырое вещество растирали с ацетонитрилом и декантировали (2×). Полученное твердое вещество сушили в потоке азота с получением указанного в заголовке соединение в виде бледно-желтого твердого вещества (25 мг, 25%): т.пл. 190-193°C dec.; 1H ЯМР (400 МГц, метанол-d4) δ 9,20 (с, 1H), 8,38 (с, 1H), 8,31-8,24 (м, 2H), 8,08-8,00 (м, 2H), 7,95-7,88 (м, 2H), 7,55-7,48 (м, 3H), 7,48-7,36 (м, 5H), 7,31 (д, J=7,7 Гц, 2H), 3,60 (кв, J=7,2 Гц, 4H), 2,20 (с, 6H), 1,07 (т, J=7,2 Гц, 6H); ESIMS m/z 682 (M+H).
Пример 11: Получение (Z)-2-(2,6-диметилфенилимино)-3-((E)-4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиденамино)тиазолидин-4-она (соединение 81C) (способ синтеза I)
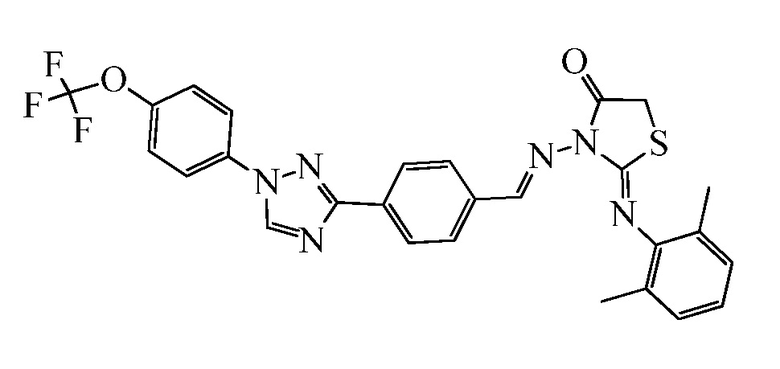
К раствору 1-(2,6-диметилфенил)тиомочевины (1,0 г, 5,55 ммоль) в EtOH (10 мл) добавляли метил 2-бромацетат (1,0 г, 6,5 ммоль) и ацетат натрия (1,0 г, 12,2 ммоль). Раствор перемешивали и кипятили с обратным холодильником в течение 1 часа, затем охлаждали и жидкость декантировали из небольшого количества твердого вещества, затем жидкость разбавляли водой (10 мл). Осадок выделяли фильтрованием с получением (1,1 г, 83%) (Z)-3-амино-2-(2,6-диметилфенилимино)тиазолидин-4-она: т.пл. 149-152°C; 1H ЯМР (400 МГц, CDCl3) δ 7,06 (д, J=7,2 Гц, 2H), 6,98 (м, 1H), 4,75 (с, 2H), 3,80 (с, 2H), 2,12 (с, 6H); ESIMS m/z 236 (M+H).
Часть этого вещества (0,07 г, 0,3 ммоль) растворяли в ледяной уксусной кислоте (3 мл) и обрабатывали 4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензальдегидом (0,10 г, 0,30 ммоль), и раствор нагревали при 60°C в течение 2 часов. Затем раствор охлаждали и разбавляли водой (1 мл), и полученное твердое вещество фильтровали и сушили на воздухе с получением указанного в заголовке соединения (0,12 г, 67%): т.пл. 209-213°C; 1H ЯМР (400 МГц, CDCl3) δ 9,42 (с, 1H), 8,59 (с, 1H), 8,28 (д, J=8,4 Гц, 2H), 8,01 (д, J=8,3 Гц, 2H), 7,80-7,77 (м, 2H), 7,43-7,34 (м, 2H), 7,07 (д, J=7,5 Гц, 2H), 6,98 (дд, J=8,2, 6,7 Гц, 1H), 3,90 (с, 2H), 2,17 (с, 6H); ESIMS m/z 551 (M+H).
Пример 12: Получение (2Z,NE)-2-((2-изопропилфенил)имино)-N-(4-(1-(4-(трифторметил)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)-1,3-тиазинан-3-амина и (Z)-3-(2-изопропилфенил)-2-((E)-(4-(1-(4-(трифторметил)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-1,3-тиазинана (соединение 87C и 179C) (способ синтеза J)
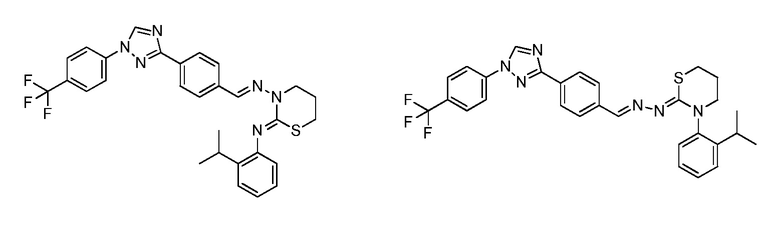
К (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметил)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамиду (200 мг, 0,393 ммоль) и карбонату калия (217 мг, 1,57 ммоль) в бутаноне (10 мл) в 25 мл флаконе, оборудованном магнитной мешалкой и колонкой Vigruex, добавляли 1-бром-3-хлорпропан (0,047 мл, 0,472 ммоль). Реакционную смесь нагревали при 60°C в течение ночи. Завершение реакции определяли с помощью ЖХМС. Реакционную смесь разбавляли ДХМ и промывали водой. Водный слой экстрагировали ДХМ. Органические слои вливали через фазовый разделитель и концентрировали. Очищали при помощи колоночной флэш-хроматографии с получением двух соединений. Минорное соединение сушили в течение ночи в вакуумной установке с получением указанного в заголовке соединения 87C (2Z,NE)-2-((2-изопропилфенил)имино)-N-(4-(1-(4-(трифторметил)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)-1,3-тиазинан-3-амина (28,5 мг, 13%) в виде желтого твердого вещества: т.пл. 187-189°C; 1H ЯМР (400 МГц, CDCl3) δ 8,81 (с, 1H), 8,66 (с, 1H), 8,21 (д, J=8,3 Гц, 2H), 7,92 (д, J=8,4 Гц, 2H), 7,81 (т, J=10,2 Гц, 4H), 7,30-7,26 (м, 2H), 7,17-7,04 (м, 1H), 6,83 (д, J=6,4 Гц, 1H), 3,96 (т, J=6,1 Гц, 2H), 3,13 (гептет, J=6,9 Гц, 1H), 2,97-2,90 (м, 2H), 2,47-2,38 (м, 2H), 1,25 (д, J=7,5 Гц, 6H); ESIMS m/z 550 (M+H). Основное соединение перекристаллизовывали с MeOH. Твердое вещество фильтровали, промывали MeOH и сушили при 50°C в вакууме. Затем твердое вещество подвергали азеотропной перегонке с ацетоном (3×), и полученное твердое вещество сушили при 50°C в вакууме с получением указанного в заголовке соединения 179C (Z)-3-(2-изопропилфенил)-2-((E)-(4-(1-(4-(трифторметил)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-1,3-тиазинана в виде желтого твердого вещества (92,3 мг, 0,168 ммоль, 43%): т.пл. 212-213°C; 1H ЯМР (400 МГц, CDCl3) δ 8,64 (с, 1H), 8,15 (д, J=8,4 Гц, 2H), 8,06 (с, 1H), 7,91 (д, J=8,5 Гц, 2H), 7,79 (д, J=8,6 Гц, 2H), 7,75 (д, J=8,4 Гц, 2H), 7,38 (дд, J=7,8, 1,6 Гц, 1H), 7,33 (тд, J=7,5, 1,4 Гц, 1H), 7,29-7,23 (м, 1H), 7,18 (дд, J=7,8, 1,4 Гц, 1H), 3,78-3,72 (м, 1H), 3,59-3,48 (м, 1H), 3,18-3,04 (м, 3H), 2,40-2,30 (м, 2H), 1,26-1,20 (м, 6H); ESIMS m/z 550 (M+H).
Пример 13: Получение (Z)-3-(2-циклопропилфенил)-5-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидин-4-она (Соединение 127C) (Способ синтеза F)
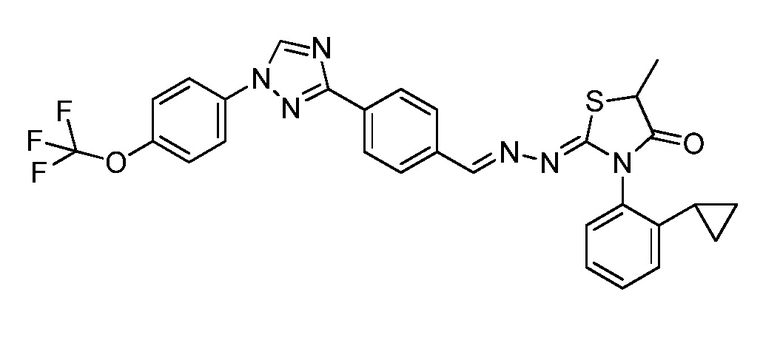
К (E)-N-(2-циклопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамиду (100 мг, 0,191 ммоль) и ацетату натрия (63,0 мг, 0,765 ммоль) в EtOH (4 мл) добавляли метил 2-бромпропаноат (0,026 мл, 0,230 ммоль). Реакционную смесь нагревали при 60°C в течение ночи. Затем реакционную смесь нагревали при 85°C в течение 72 часов. Реакционную смесь разбавляли ДХМ и промывали водой. Водные слои экстрагировали ДХМ. Органические слои вливали через фазовый разделитель и концентрировали. Очищали при помощи колоночной флэш-хроматографии с получением указанного в заголовке соединения в виде белого твердого вещества (32,5 мг, 0,056 ммоль, 30%): т.пл. 112-115°C; 1H ЯМР (400 МГц, CDCl3) δ 8,58 (с, 1H), 8,32 (с, 1H), 8,22 (д, J=8,3 Гц, 2H), 7,87-7,75 (м, 4H), 7,43-7,32 (м, 4H), 7,26-7,24 (м, 2H), 4,23 (кв, J=7,3 Гц, 1H), 1,85-1,78 (м, 4H), 0,90-0,78 (м, 2H), 0,78-0,69 (м, 1H), 0,65-0,55 (м, 1H); ESIMS m/z 578 (M+H).
Пример 14: Получение (Z)-3-(2-изопропилфенил)-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидина (соединение 132C) (способ синтеза J)
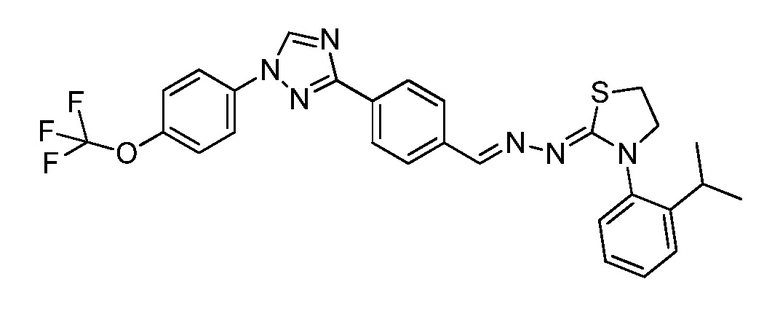
К (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамиду (214 мг, 0,407 ммоль) и карбонату калия (225 мг, 1,63 ммоль) в бутаноне (4 мл) добавляли 1-бром-2-хлорэтан (70,0 мг, 0,489 ммоль). Реакционную смесь нагревали при 90°C в течение ночи. Завершение реакции определяли с помощью ЖХМС. Реакционную смесь охлаждали, разбавляли ДХМ и промывали водой. Водные слои экстрагировали с ДХМ. Органические слои фильтровали через фазовый разделитель и концентрировали. Разделение при помощи колоночной флэш-хроматографии и сушка восстановленного твердого вещества при 55°C в вакууме давало указанное в заголовке соединение в виде белого твердого вещества (137 мг, 0,249 ммоль, 61%): т.пл. 193-196°C; 1H ЯМР (400 МГц, CDCl3) δ 8,56 (с, 1H), 8,22 (с, 1H), 8,17 (д, J=8,4 Гц, 2H), 7,80 (ддд, J=9,5, 6,9, 4,9 Гц, 4H), 7,43-7,33 (м, 4H), 7,31-7,21 (м, 2H), 4,05 (тд, J=9,4, 7,1 Гц, 1H), 3,97-3,87 (м, 1H), 3,42-3,33 (м, 1H), 3,33-3,24 (м, 1H), 3,12 (гептет, J=6,8 Гц, 1H), 1,27 (д, J=6,8 Гц, 3H), 1,22 (д, J=6,9 Гц, 3H); ESIMS m/z 552 (M+H).
Пример 15: Получение (Z)-3-(2-изопропилфенил)-4-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидина (соединение 155C) (способ синтеза J)
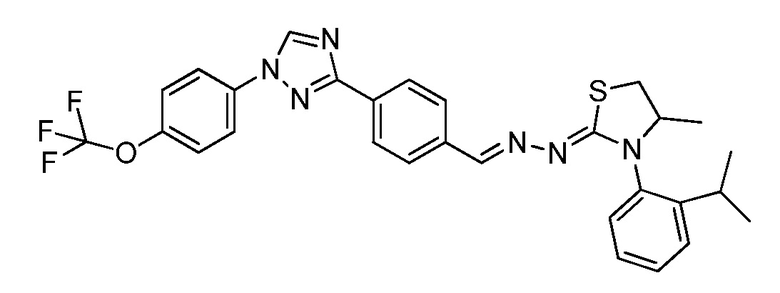
К (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамиду (300 мг, 0,572 ммоль) и карбонату калия (316 мг, 2,29 ммоль) в бутаноне (4 мл) добавляли 1,2-дибромпропан (0,072 мл, 0,686 ммоль). Реакционную смесь нагревали при 85°C в течение ночи. Завершение реакции определяли с помощью ЖХМС. Реакционную смесь разбавляли ДХМ и промывали водой. Водные слои экстрагировали ДХМ. Органические слои вливали через фазовый разделитель и концентрировали. Очищали при помощи колоночной флэш-хроматографии с получением желтого твердого вещества. Твердое вещество перекристаллизовывали из MeOH. Твердое вещество фильтровали, промывали MeOH и сушили с получением указанного в заголовке соединения в виде желтого твердого вещества, которое растворяли в ацетоне и концентрировали (3×). Светло-желтое твердое вещество собирали и сушили с получением указанного в заголовке соединения в виде смеси 1:1 ротационных диастереоизомеров (75,1 мг, 0,133 ммоль, 23%): т.пл. 201-204°C; 1H ЯМР смеси (400 МГц, CDCl3) δ 8,56 (с, 2H), 8,18 (дд, J=10,8, 7,4 Гц, 6H), 7,84-7,73 (м, 8H), 7,45-7,30 (м, 8H), 7,30-7,23 (м, 2H), 7,20 (д, J=6,7 Гц, 1H), 7,12 (дд, J=7,8, 1,2 Гц, 1H), 4,43-4,33 (м, 1H), 4,16 (дд, J=12,6, 6,3 Гц, 1H), 3,48 (дт, J=13,3, 6,7 Гц, 1H), 3,37 (дд, J=10,8, 6,2 Гц, 1H), 3,24 (дт, J=13,7, 6,9 Гц, 1H), 3,08-2,92 (м, 3H), 1,33-1,16 (м, 18H); ESIMS m/z 566 (M+H).
Пример 16: Получение (Z)-3-(2,6-диметилфенил)-4-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-2,3-дигидротиазола (соединение 173C) (способ синтеза G)
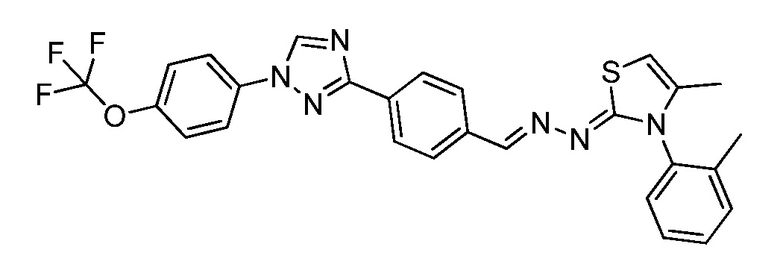
К раствору (E)-N-(o-толил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (257 мг, 0,520 ммоль) в бутаноне (5 мл) добавляли триэтиламин (0,14 мл, 1,0 ммоль) и хлорацетон (0,06 мл, 0,73 ммоль) и кипятили с обратным холодильником при 75°C в течение 15 часов. Смесь оставляли охлаждаться до комнатной температуры, а затем переносили в делительную воронку, содержащую воду (5 мл), и дважды экстрагировали дихлорметаном. Органические слои фильтровали через фазовый разделитель, адсорбировали на силикагеле и очищали при помощи колоночной флэш-хроматографии с получением указанного в заголовке соединения в виде желтого твердого вещества (229 мг, 83%): т.пл. 87°C (dec); 1H ЯМР (400 МГц, CDCl3) δ 8,56 (с, 1H), 8,19-8,15 (м, 3H), 7,82-7,75 (м, 4H), 7,43-7,30 (м, 5H), 7,24 (д, J=7,3 Гц, 1H), 5,88 (д, J=1,3 Гц, 1H), 2,21 (с, 3H), 1,80 (д, J=1,2 Гц, 3H); ESIMS m/z 536 (M+H).
Пример 17: Получение (Z)-3-(2-изопропилфенил)-5-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-1,3-тиазинана (соединение 178C) (способ синтеза J)
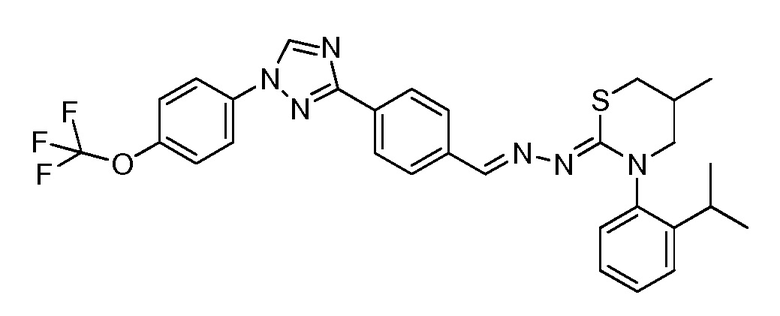
К (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамиду (100 мг, 0,191 ммоль) и карбонату калия (105 мг, 0,763 ммоль) в бутаноне (4 мл) добавляли 1-бром-3-хлор-2-метилпропан (39,0 мг, 0,229 ммоль). Реакционную смесь нагревали при 80°C в течение ночи. Затем реакционную смесь разбавляли ДХМ и промывали водой. Водный слой экстрагировали с ДХМ. Органические слои вливали через фазовый разделитель и концентрировали. Очищали при помощи колоночной флэш-хроматографии с получением указанного в заголовке соединения в виде светло-желтого твердого вещества как смесь ротационных диастереоизомеров: т.пл. 186-190°C; 1H ЯМР (400 МГц, CDCl3) δ 8,55 (д, J=3,6 Гц, 1H), 8,14 (д, J=8,4 Гц, 2H), 8,06 (с, 1H), 7,84-7,77 (м, 2H), 7,74 (д, J=8,4 Гц, 2H), 7,38 (д, J=9,0 Гц, 3H), 7,32 (тд, J=7,5, 1,4 Гц, 1H), 7,26 (с, 1H), 7,17 (т, J=7,1 Гц, 1H), 3,69-3,26 (м, 1H), 3,55-3,37 (м, 1H), 3,18-2,98 (м, 2H), 2,93-2,80 (м, 1H), 2,47 (д, J=35,9 Гц, 1H), 1,31-1,12 (м, 9H); ESIMS m/z 580 (M+H).
Пример 18: Получение (Z)-3-(2,6-диметилфенил)-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-1,3-тиазепана (соединение 211C) (способ синтеза J)
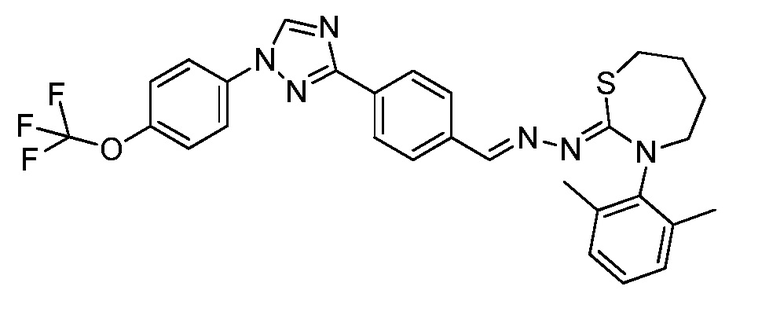
К (E)-N-(2,6-диметилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамиду (500 мг, 0,979 ммоль) и карбонату калия (541 мг, 3,92 ммоль) в ацетоне (4 мл) добавляли 1-бром-4-хлорбутан (0,135 мл, 1,18 ммоль). Реакционную смесь нагревали при 60°C в течение ночи. Завершение алкилирования определяли при помощи сверхэффективной жидкостной хроматографии («СЭЖХ»). Реакционную смесь разбавляли ДХМ и промывали водой. Водный слой экстрагировали ДХМ. Органические слои вливали через фазовый разделитель и концентрировали. Очищали при помощи колоночной флэш-хроматографии с получением (1Z,N'E)-4-хлорбутил N-(2,6-диметилфенил)-N'-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)карбамогидразонотиоата (427 мг, 0,710 ммоль, 73%) в виде желтой камеди, которую использовали без дополнительной очистки. К (1Z,N'E)-4-хлорбутил N-(2,6-диметилфенил)-N'-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)карбамогидразонотиоату (427 мг, 0,710 ммоль), калий йодиду (236 мг, 1,42 ммоль) и карбонату калия (393 мг, 2,84 ммоль) добавляли ацетон (7 мл). Реакционную смесь нагревали при 65°C в течение 72 часов. Реакционную смесь охлаждали до комнатной температуры, разбавляли ДХМ и промывали водой. Водный слой экстрагировали ДХМ. Органические слои вливали через фазовый разделитель и концентрировали. Очищали при помощи колоночной флэш-хроматографии с получением желтого масла. Желтое масло перекристаллизовывали из MeOH, фильтровали, промывали с MeOH и сушили с получением указанного в заголовке соединения в виде желтого твердого вещества (100 мг, 0,177 ммоль, 25%): т.пл. 100-106°C; 1H ЯМР (400 МГц, CDCl3) δ 8,55 (с, 1H), 8,15 (д, J=8,4 Гц, 2H), 8,10 (с, 1H), 7,79 (дт, J=10,4, 5,8 Гц, 4H), 7,38 (д, J=8,3 Гц, 2H), 7,11 (с, 3H), 3,85-3,78 (м, 2H), 3,20-3,12 (м, 2H), 2,30 (с, 6H), 2,13-2,07 (м, 2H), 1,87-1,82 (м, 2H); ESIMS m/z 566 (M+H).
Пример 19: Получение (Z)-3-(2-изопропилфенил)-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-1,3-тиазинан-4-она (соединение 224C) (способ синтеза L)
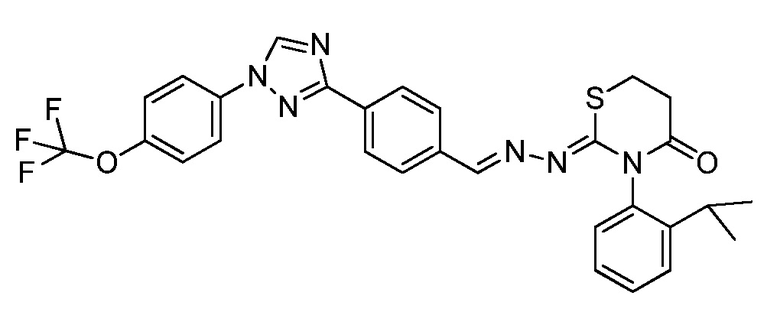
К (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамиду (500 мг, 0,953 ммоль) в бутаноне (9,5 мл) добавляли акрилоилхлорид (0,077 мл, 0,953 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 10 мин, затем при 50°C в течение 2 часов. Реакционную смесь охлаждали в течение ночи до 40°C. Завершение реакции определяли с помощью ЖХМС. Реакционную смесь разбавляли ДХМ и промывали насыщенным бикарбонатом натрия. Водный слой экстрагировали ДХМ. Органические слои вливали через фазовый разделитель и концентрировали. Очищали при помощи колоночной флэш-хроматографии с получением желтого масла. Масло перекристаллизовывали из смеси диэтилового эфира/гексана с получением указанного в заголовке соединение в виде светло-желтого твердого вещества (125 мг, 0,217 ммоль, 23%): т.пл. 118°C (dec); 1H ЯМР (400 МГц, CDCl3) δ 8,57 (с, 1H), 8,21 (д, J=8,4 Гц, 2H), 8,16 (с, 1H), 7,85-7,75 (м, 4H), 7,46-7,36 (м, 4H), 7,33-7,26 (м, 1H), 7,10 (д, J=7,6 Гц, 1H), 3,26-3,14 (м, 4H), 2,81 (гептет, J=6,9 Гц, 1H), 1,21 (т, J=7,2 Гц, 6H); ESIMS m/z 580 (M+H).
Пример 20: Разделение ротационно стабильных атропоизомеров из рацемических смесей
Разделение составных изомеров из рацемических смесей проводили с использованием одного из следующих методов хиральной ВЭЖХ
Способ разделения A: Для разделения использовали колонку Chiral Technologies INC Chiral Pak 1A 5 мкм, колонка 4,6×250 мм (номер по каталогу 80325). Способ состоит из скорости потока 1,0 мл/мин в течение от 0 до 30 мин с изократической задержкой при 25% B в процессе пробега. В качестве элюента A использовали н-гексан, в качестве элюента B - изо-пропиловый спирт.
Способ разделения B: Для разделения использовали колонку Chiral Technologies INC Chiral Pak 1B 5 мкм, колонка 4,6×250 мм (Номер по каталогу 81325). Способ состоит из скорости потока 1,0 мл/мин в течение от 0 до 30 мин с изократической задержкой при 15% B в процессе пробега. В качестве элюента A использовали н-пентан, в качестве элюента B использовали н-бутиловый спирт.
Пример 21: Получение (Z)-3-(2,6-дифторфенил)-4-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидин-4-ола (соединение 240C; способ синтеза M).
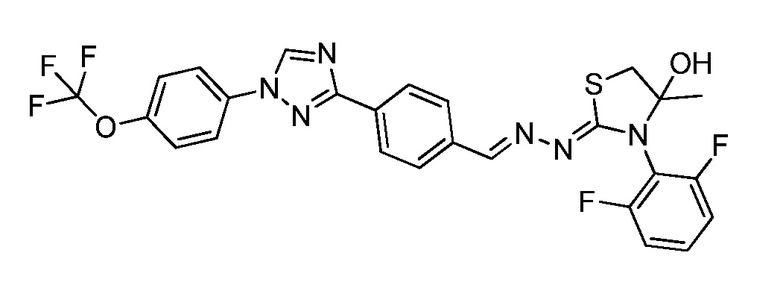
К раствору (E)-N-(2,6-дифторфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (253 мг, 0,49 ммоль) в бутаноне (4,9 мл) добавляли триэтиламин (0,14 мл, 0,98 ммоль) и хлорацетон (0,055 мл, 0,68 ммоль), и реакционную смесь перемешивали при 80°C в течение 15 часов. Смесь оставляли охлаждаться до комнатной температуры, переносили в делительную воронку, содержащую воду (5 мл), и дважды экстрагировали дихлорметаном. Органические экстракты фильтровали через фазовый разделитель, адсорбировали на силикагеле и очищали при помощи флэш-хроматографии (от 0-20% этилацетат/B, где B=1:1 дихлорметан/гексан) с получением указанного в заголовке соединения в виде желтого твердого вещества (248 мг, 88%): т.пл. 105°C (dec); 1H ЯМР (400 МГц, CDCl3) δ 8,57 (с, 1H), 8,25-8,12 (м, 3H), 7,88-7,72 (м, 4H), 7,39 (д, J=8,5 Гц, 3H), 7,06 (тд, J=8,9, 4,4 Гц, 2H), 3,58 (д, J=11,5 Гц, 1H), 3,37 (д, J=11,5 Гц, 1H), 3,24 (д, J=2,7 Гц, 1H), 1,59 (с, 3H); 19F ЯМР (376 МГц, CDCl3) δ -58,02, -113,71, -115,83, -115,84; ESIMS m/z 576 (M+H)+.
Пример 22: Получение (Z)-2-((2-хлор-6-(трифторметил)фенил)имино)-4-метил-3-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)амино)тиазолидин-4-ола (соединение 241C; способ синтеза M).
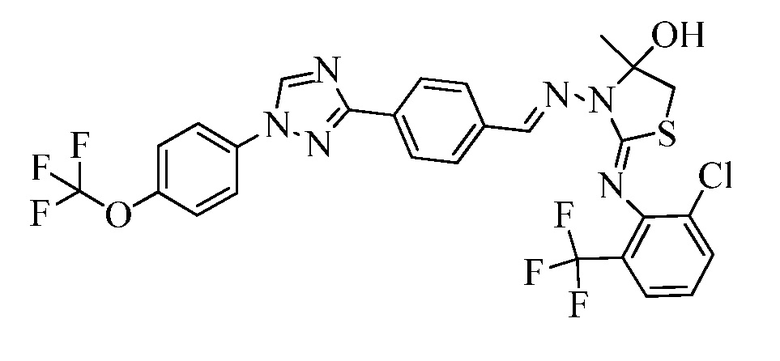
К раствору (E)-N-(2-хлор-6-(трифторметил)фенил)-2-(4-(1-(4-(трифторметокси)-фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (111 мг, 0,19 ммоль) в бутаноне (2 мл) добавляли хлорацетон (0,02 мл, 0,27 ммоль) и триэтиламин (0,05 мл, 0,38 ммоль), и реакционную смесь перемешивали при 75°C в течение 16 часов. Смесь оставляли охлаждаться до комнатной температуры, переносили в делительную воронку, содержащую воду (5 мл), и дважды экстрагировали дихлорметаном. Органические экстракты фильтровали через фазовый разделитель, адсорбировали на силикагеле, и очищали с помощью флэш-хроматографии (от 0-20% этилацетат/B, где B=1:1 дихлорметан/гексан). Указанное в заголовке соединение выделяли в виде желтого твердого вещества (60,5 мг, 50%): т.пл. 97°C (dec); 1H ЯМР (400 МГц, CDCl3) δ 9,72-9,57 (м, 1H), 8,58 (с, 1H), 8,24 (д, J=8,4 Гц, 2H), 7,88-7,72 (м, 4H), 7,56 (дт, J=18,3, 5,8 Гц, 2H), 7,40 (д, J=8,3 Гц, 2H), 7,09 (т, J=8,0 Гц, 1H), 3,49 (д, J=13,3 Гц, 1H), 3,35 (м, 2H), 1,86 (д, J=14,0 Гц, 3H); 19F ЯМР (376 МГц, CDCl3) δ -58,01, -62,05, -62,22; ESIMS m/z 642 (M+H).
Пример 23: Получение (Z)-3-(2-изопропилфенил)-4-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидин-4-ола (соединение 242C; способ синтеза M).
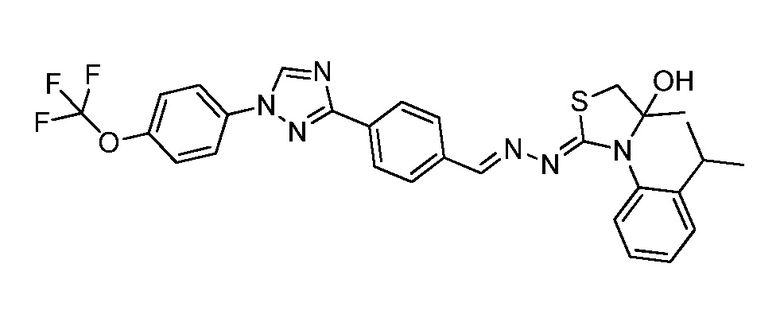
К раствору (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (134 мг, 0,26 ммоль) в бутаноне (1,9 мл) добавляли хлорацетон (0,03 мл, 0,33 ммоль) и триэтиламин (0,04 мл, 0,28 ммоль), и реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Смесь переносили в делительную воронку, содержащую воду (5 мл), и дважды экстрагировали дихлорметаном. Органические экстракты фильтровали через фазовый разделитель, адсорбировали на силикагеле и очищали с помощью флэш-хроматографии (от 0-25% этилацетат/B, где B=1:1 дихлорметан/гексан) с получением указанного в заголовке соединения в виде желтого твердого вещества (117 мг, 79%): т.пл. 114-116°C; 1H ЯМР (400 МГц, CDCl3) δ 8,57 (с, 1H), 8,19 (дд, J=10,1, 6,2 Гц, 3H), 7,79 (дд, J=11,5, 4,7 Гц, 4H), 7,50-7,44 (м, 1H), 7,44-7,36 (м, 4H), 7,29-7,25 (м, 1H), 3,55 (д, J=11,5 Гц, 1H), 3,45 (с, 1H), 3,34 (д, J=11,5 Гц, 1H), 2,98 (дт, J=13,8, 6,9 Гц, 1H), 1,43 (с, 3H), 1,27-1,16 (м, 6H); 19F ЯМР (376 МГц, CDCl3) δ -58,02; ESIMS m/z 582 (M+H)+.
Пример 24: Получение (Z)-3-(2-(втор-бутил)фенил)-4-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидин-4-ола (соединение 243C; способ синтеза M).
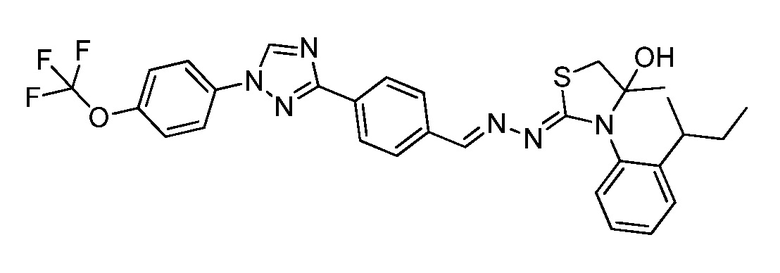
Начиная с (E)-N-(2-втор-бутилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида и используя условия, описанные в примере 23, указанное в заголовке соединение выделяли в виде желтого твердого вещества (122 мг, 89%): т.пл. 112°C (dec); 1H ЯМР (400 МГц, CDCl3) δ 8,57 (с, 1H), 8,23-8,13 (м, 3H), 7,84-7,74 (м, 4H), 7,55-7,44 (м, 1H), 7,43-7,32 (м, 4H), 7,28-7,24 (м, 1H), 3,55-3,51 (м, 2H), 3,32 (дд, J=11,5, 1,0 Гц, 1H), 2,69 (тд, J=13,9, 7,0 Гц, 1H), 1,63-1,56 (м, 2H), 1,45 (д, J=4,9 Гц, 3H), 1,26-1,16 (м, 3H), 0,83 (дт, J=10,2, 7,4 Гц, 3H); 19F ЯМР (376 МГц, CDCl3) δ -58,02; ESIMS m/z 596 (M+H)+.
Пример 25: Получение (Z)-3-(2-хлор-6-метилфенил)-4-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидин-4-ола (соединение 244C; способ синтеза M).
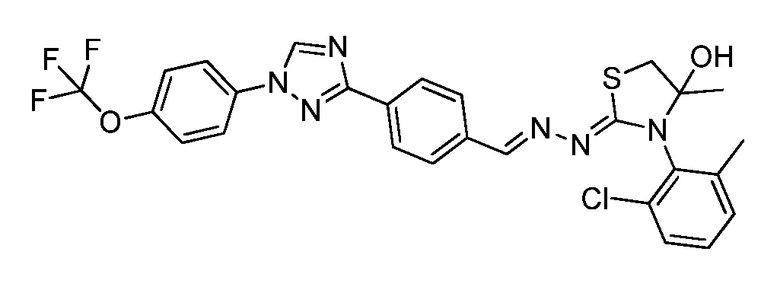
Начиная с (E)-N-(2-хлор-6-метилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида и используя условия, описанные в примере 23, указанное в заголовке соединение выделяли в виде желтого твердого вещества (107 мг, 91%): т.пл. 103°C (dec); 1H ЯМР (400 МГц, CDCl3) δ 8,57 (с, 1H), 8,22 (с, 1H), 8,18 (д, J=8,4 Гц, 2H), 7,83-7,76 (м, 4H), 7,41-7,32 (м, 3H), 7,25-7,21 (м, 2H), 3,70-3,61 (м, 1H), 3,53 (с, 1H), 3,30 (д, J=11,2 Гц, 1H), 2,49 (с, 3H), 1,51 (с, 3H); 19F ЯМР (376 МГц, CDCl3) δ -58,02; ESIMS m/z 588 (M+H)+.
Пример 26: Получение (Z)-3-(4-метокси-2-метилфенил)-4-метил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидин-4-ола (соединение 245C; способ синтеза M).
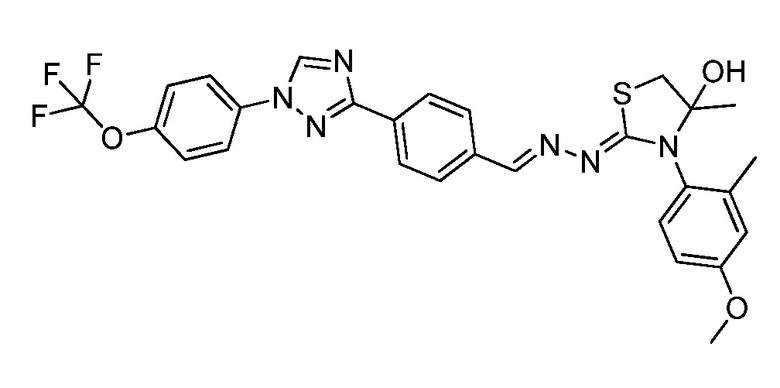
Начиная с (E)-N-(2-метил-4-метоксифенил)-2-(4-(1-(4-(трифторметокси)-фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида и используя условия, описанные в примере 23, указанное в заголовке соединение выделяли в виде желтого твердого вещества (88 мг, 76%): т.пл. 129°C (dec); 1H ЯМР (400 МГц, CDCl3) δ 8,57 (с, 1H), 8,25 (с, 1H), 8,18 (д, J=8,3 Гц, 2H), 7,82-7,75 (м, 4H), 7,39 (т, J=8,8 Гц, 3H), 6,86-6,76 (м, 2H), 3,83 (с, 3H), 3,52 (д, J=11,5 Гц, 1H), 3,43 (с, 1H), 3,31 (д, J=11,6 Гц, 1H), 2,19 (с, 2H), 1,43 (с, 3H); 19F ЯМР (376 МГц, CDCl3) δ -58,02; ESIMS m/z 584 (M+H)+.
Пример 27: Получение (Z)-3-(2-изопропилфенил)-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-4-(трифторметил)тиазолидин-4-ола (соединение 246C; способ синтеза M).
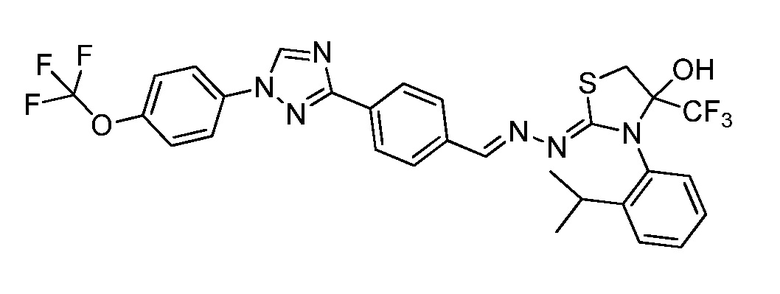
К раствору (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (351 мг, 0,67 ммоль) в бутаноне (6,7 мл) добавляли 3-бром-1,1,1-трифторацетон (0,14 мл, 1,34 ммоль) и триэтиламин (0,19 мл, 1,34 ммоль), и реакционную смесь перемешивали при 85°C в течение 21 часа. Смесь оставляли охлаждаться до комнатной температуры, переносили в делительную воронку, содержащую воду (5 мл), и водную смесь дважды экстрагировали дихлорметаном. Органические экстракты фильтровали через фазовый разделитель, адсорбировали на силикагеле, и очищали с помощью флэш-хроматографии (от 0-20% этилацетат/B, где B=1:1 дихлорметан/гексан) с получением смеси диастереоизомеров (2:1) указанного в заголовке соединения в виде оранжевого твердого вещества (189 мг, 45%): т.пл. 185-187°C; 1H ЯМР (400 МГц, CDCl3, оба диастереомеры) δ 8,56 (м, 2H), 8,22-8,14 (м, 6H), 7,83-7,75 (м, 8H), 7,49-7,34 (м, 10H), 7,32-7,23 (м, 2H), 4,22 (с, 1H), 3,82 (дд, J=12,5, 4,8 Гц, 2H), 3,51 (д, J=13,2 Гц, 1H), 3,40 (д, J=12,3 Гц, 1H), 3,31 (с, 1H), 3,09 (тт, J=13,9, 7,0 Гц, 2H), 1,31-1,13 (м, 12H); 19F ЯМР (376 МГц, CDCl3) δ -58,02, -78,33, -78,77; ESIMS m/z 636 (M+H)+.
Пример 28: Получение (Z)-3-(2-(втор-бутил)фенил)-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-4-(трифторметил)тиазолидин-4-ола (соединение 247C; способ синтеза M).
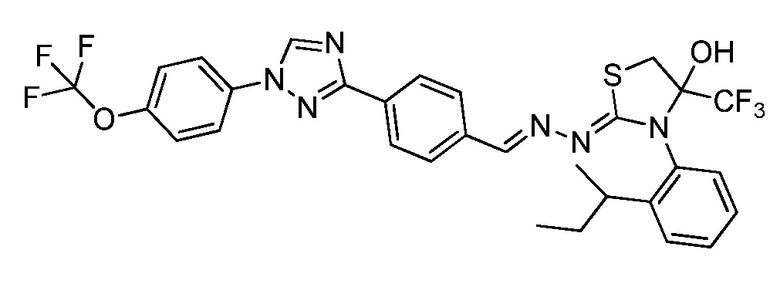
К раствору (E)-N-(2-(втор-бутил)фенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (203 мг, 0,38 ммоль) в бутаноне (3,8 мл) добавляли триэтиламин (0,07 мл, 0,49 ммоль) и 3-бром-1,1,1-трифторацетон (0,05 мл, 0,49 ммоль), и реакционную смесь перемешивали при 85°C в течение 20 часов, после этого анализ ЖХ/МС показал минимальное преобразование. К реакционной смеси добавляли дополнительную порцию триэтиламина (0,03 мл, 0,21 ммоль) и 3-бром-1,1,1-трифторацетона (0,1 мл, 0,98 ммоль), и реакционную смесь перемешивали при 90°C в течение еще 20 часов. Смесь оставляли охлаждаться до комнатной температуры, переносили в делительную воронку, содержащую воду (5 мл), и дважды экстрагировали дихлорметаном. Органические экстракты фильтровали через фазовый разделитель, адсорбировали на силикагеле и очищали с помощью флэш-хроматографии (0-20% этилацетат/B, где B=1:1 дихлорметан/гексан). Затем очищали при помощи флэш-хроматографии с обращенной фазой (0-100% ацетонитрил/вода) с получением указанного в заголовке соединения в виде оранжевого твердого вещества (16 мг, 7%): 1H ЯМР (400 МГц, CDCl3) δ 8,59-8,54 (м, 1H), 8,30-8,13 (м, 3H), 7,79 (дд, J=8,6, 6,7 Гц, 4H), 7,45-7,34 (м, 5H), 7,32-7,21 (м, 1H), 3,99 (с, 1H), 3,83 (д, J=12,2 Гц, 1H), 3,52-3,38 (м, 1H), 2,82-2,75 (м, 1H), 1,27-1,26 (м, 1H), 1,21-1,12 (м, 3H), 0,97-0,75 (м, 4H); 19F ЯМР (376 МГц, CDCl3) δ -58,03, -78,23, -78,32, -78,76, -78,84; ESIMS m/z 650 (M+H)+.
Соединения 248-256, 258-262 и 264, указанные в таблице 3, получали в соответствие со способом, описанным в примере 23, из соответствующим образом замещенных промежуточных соединений, описанных в таблице 1. Характерные данные для этих соединения приведены в таблице 4.
Пример 29: Получение (Z)-3-(2-изопропилфенил)-4,5-диметил-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)тиазолидин-4-ола (соединение 257C).
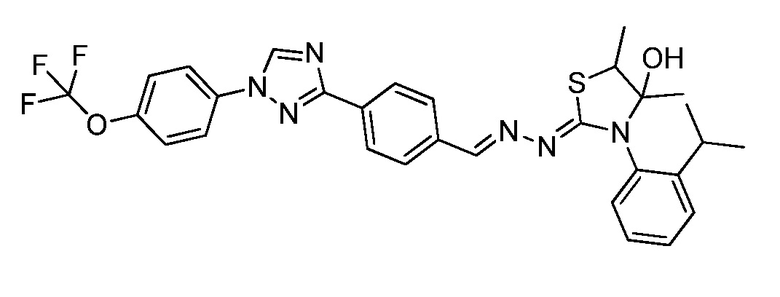
К раствору (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (114 мг, 0,22 ммоль) в бутаноне (2,2 мл) добавляли 3-бром-2-бутанон (0,03 мл, 0,28 ммоль) и триэтиламин (0,06 мл, 0,44 ммоль), и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь непосредственно помещали на силикагелевый картридж и очищали с помощью флэш-хроматографии (0-30% этилацетат/B, где B=1:1 дихлорметан/гексан) с получением указанного в заголовке соединения в виде желтого твердого вещества (108 мг, 84% выход): т.пл. 140°C (dec); 1H ЯМР (400 МГц, CDCl3) δ 8,57 (с, 1H), 8,22-8,16 (м, 3H), 7,82-7,74 (м, 4H), 7,55-7,47 (м, 1H), 7,42-7,35 (м, 4H), 7,29-7,24 (м, 1H), 3,92-2,96 (м, 3H), 1,57 (с, 1H), 1,57-1,50 (м, 3H), 1,35-1,17 (м, 9H); 19F ЯМР (376 МГц, CDCl3) δ -58,02; ESIMS m/z 595 ([M+H]+).
Пример 30: Получение (Z)-3-(2-изопропилфенил)-2-((E)-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-4-(2-(трифторметил)фенил)тиазолидин-4-ола (соединение 263C).
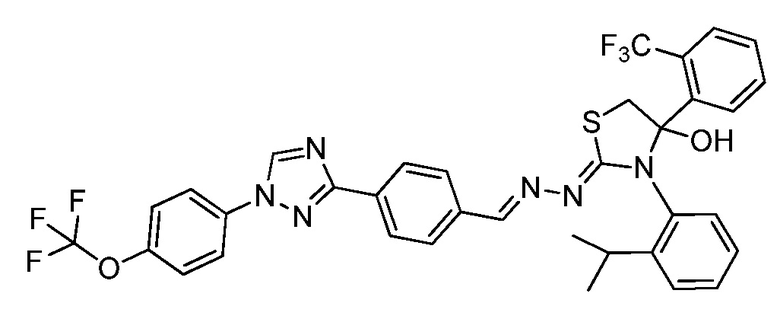
Раствор (E)-N-(2-изопропилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (0,30 г, 0,57 ммоль) и 2-(трифторметил)фенацил бромида (0,22 г, 0,85 ммоль) в DCE (30 мл) кипятили с обратным холодильником и перемешивали в течение ночи. Реакционную смесь охлаждали до комнатной температуры, разбавляли этилацетатом (100 мл), промывали водой (2×50 мл), промывали насыщенным солевым раствором (1×25 мл) и сушили над безводным сульфатом натрия. Раствор фильтровали, фильтрат концентрировали, и остаток очищали с помощью флэш-хроматографии (0-100% этилацетат/гексан) с получением (Z)-3-(2-изопропилфенил)-2-((E)-(4-(1-(4-(трифторметокси)-фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразоно)-4-(2-(трифторметил)-фенил)тиазолидин-4-ола в виде желтого твердого вещества (0,15 г, 38% выход): т.пл. 115-117,5°C; 1H ЯМР (400 МГц, CDCl3) δ 8,59 (с, 1H), 8,33 (с, 1H), 8,24 (д, J=8,4 Гц, 2H), 8,13 (с, 1H), 7,86-7,77 (м, 5H), 7,73 (д, J=7,2 Гц, 1H), 7,62 (дт, J=21,6, 7,2 Гц, 2H), 7,40 (д, J=8,2 Гц, 2H), 7,37-7,28 (м, 3H), 7,24-7,17 (м, 1H), 4,34 (с, 2H), 3,20 (дт, J=13,7, 6,8 Гц, 2H), 1,25 (д, J=6,9 Гц, 6H); 19F ЯМР (376 МГц, CDCl3) δ -57,99, -58,02; ESIMS m/z 711 ([M+H]+).
Пример 31: (E)-N-(2-циклопентилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамид (соединение I-35; способы синтезов N и C)
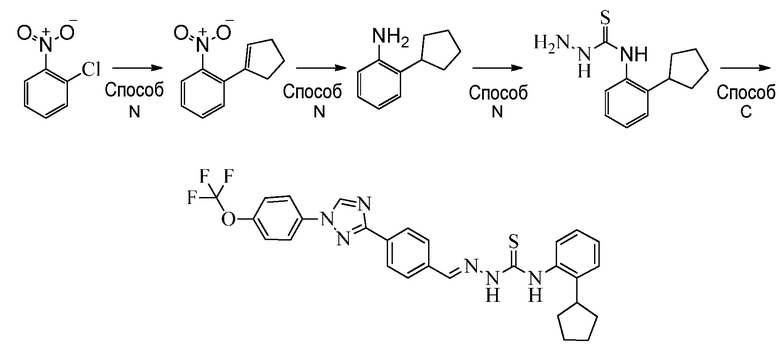
Стадия 1: Получение 1-(циклопент-1-ен-1-ил)-2-нитробензола (I-32, способ N). К смеси 1-хлор-2-нитробензола (0,5 г, 3,2 ммоль) и карбоната натрия (0,34 г, 3,2 ммоль) в 100 мл круглодонной колбе, оборудованной магнитной мешалкой и впускным клапаном для азота, добавляли воду (3,2 мл), диоксан (13 мл) и 2-(циклопент-1-ен-1-ил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (0,77 мл, 3,8 ммоль). Колбу с реакционной смесью откачивали и продували азотом (2×), затем добавляли хлорид бис(трифенилфосфин)палладия (II) (0,18 г, 0,25 ммоль), а затем откачивали и продували (3×) с последующим добавлением катализатора. Реакционную смесь нагревали при 80°C и перемешивали в течение ночи. Реакционную смесь охлаждали и фильтровали через слой целита, который затем промывали водой и этилацетатом. Фазы разделяли и органическую фазу сушили пропусканием через картридж фазового сепаратора и концентрировали. Остаток очищали при помощи колоночной флэш-хроматографии с получением указанного в заголовке соединение (0,56 г, 3,0 ммоль, 93% выход) в виде желтого масла: 1H ЯМР (400 МГц, CDCl3) δ 7,78-7,71 (м, 1H), 7,54-7,47 (м, 1H), 7,40-7,32 (м, 2H), 5,86-5,82 (м, 1H), 2,63-2,55 (м, 2H), 2,55-2,47 (м, 2H), 2,09-1,98 (м, 2H); 13C ЯМР (101 МГц, CDCl3) δ 148,77, 139,96, 133,58, 132,08, 130,87, 130,52, 127,55, 123,70, 35,31, 33,49, 24,05; ESIMS m/z 190 ([M+H]+).
Стадия 2: Получение 2-циклопентиланилина (I-33, способ N). К раствору 1-(циклопент-1-ен-1-ил)-2-нитробензола (0,58 г, 3,0 ммоль) в этилацетате (30 мл) в 200 мл круглодонной колбе, оборудованной магнитной мешалкой и впускным клапаном для азота, добавляли палладий на угле (0,63 г, 0,30 ммоль, 5%). Колбу откачивали и продували азотом (3×), а затем откачивали и помещали в атмосферу водорода (1 атмосфера (атм.)). Смесь перемешивали при комнатной температуре в течение ночи, фильтровали через слой целита, и осадок на фильтре промывали этилацетатом. Фильтрат концентрировали с получением указанного в заголовке соединения (0,46 г, 2,9 ммоль, 98% выход) в виде прозрачного, слегка красного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,14 (дд, J=7,7, 1,3 Гц, 1H), 7,02 (тд, J=7,6, 1,5 Гц, 1H), 6,76 (тд, J=7,4, 1,1 Гц, 1H), 6,68 (дд, J=7,8, 1,2 Гц, 1H), 3,66 (шир.с, 2H), 3,04-2,92 (м, 1H), 2,13-1,98 (м, 2H), 1,88-1,58 (м, 6H); 13C ЯМР (101 МГц, CDCl3) δ 144,12, 130,34, 126,51, 125,95, 118,78, 115,70, 39,89, 32,17, 25,21; ESIMS m/z 162 ([M+H]+).
Стадия 3: Получение N-(2-циклопентилфенил)гидразинкарботиоамида (I-34, способ N). К двухфазному раствору 2-циклопентиланилина (0,46 г, 2,9 ммоль) в дихлорметане (10 мл) и воде (4,8 мл) в 100 мл круглодонной колбе, оборудованной магнитной мешалкой и впускным клапаном для азота, добавляли гидрокарбонат натрия (0,73 г, 8,6 ммоль), а затем тиофосген (0,21 мл, 2,8 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 1 часа, фильтровали через картридж фазового сепаратора и концентрировали с получением 1-циклопентил-2-изотиоцианатобензола в виде красного масла, которое использовали без дополнительной очистки. К раствору изотиоцианата в этаноле (5,5 мл) в 100 мл круглодонной колбе добавляли гидразин гидрата (0,15 мл, 3,1 ммоль), и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь разбавляли гексаном, и полученное твердое вещество собирали фильтрованием, промывали гексаном и сушили в вакуумной установке с получением указанного в заголовке соединения (0,41 г, 1,7 ммоль, 63% выход) в виде белого твердого вещества: 1H ЯМР (400 МГц, CDCl3) δ 9,02 (шир.с, 1H), 7,52 (шир.с, 1H), 7,41-7,18 (м, 4H), 4,06 (шир.с, 2H), 3,21-3,06 (м, 1H), 2,04 (с, 2H), 1,90-1,74 (м, 2H), 1,74-1,58 (м, 4H); ESIMS m/z 236 ([M+H]+).
Стадия 4: Получение (E)-N-(2-циклопентилфенил)-2-(4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензилиден)гидразинкарботиоамида (I-35, способ C). К смеси 4-(1-(4-(трифторметокси)фенил)-1H-1,2,4-триазол-3-ил)бензальдегида (0,58 г, 1,7 ммоль) и N-(2-циклопентилфенил)гидразинкарботиоамида (0,41 г, 1,7 ммоль) в 100 мл круглодонной колбе, оборудованной магнитной мешалкой и обратным холодильником, добавляли метанол (17 мл), и реакционную смесь нагревали при 50°C с перемешивании в течение ночи. Реакционную смесь охлаждали до комнатной температуры, и полученное твердое вещество фильтровали, промывали метанолом и сушили в вакууме (25 в Hg) при 55°C с получением указанного в заголовке соединения (795 мг, 1,44 ммоль, 83% выход) в виде желтого твердого вещества: т.пл. 213-216°C; 1H ЯМР (400 МГц, CDCl3) δ 9,45 (с, 1H), 9,11 (с, 1H), 8,60 (с, 1H), 8,26 (д, J=8,4 Гц, 2H), 7,91 (с, 1H), 7,86-7,71 (м, 5H), 7,40 (дд, J=8,8, 6,4 Гц, 3H), 7,35-7,27 (м, 2H), 3,22 (т, J=8,0 Гц, 1H), 2,13 (д, J=2,5 Гц, 2H), 1,90-1,59 (м, 6H); ESIMS m/z 551 ([M+H]+).
Промежуточные соединения I-36 - I-55 и I-61 - I-62, указанные в таблице 1, получали в соответствие с методами, описанными в примере 29, стадии 1-4. Характерные данные этих промежуточных соединений приведены в таблице 2.
Пример 32: Биоанализы на совке малой («BAW») и совке хлопковой («CEW»)
BAW имеет несколько активных вредителей, заболеваний или хищников, снижающих ее популяцию. BAW нападает на большое число сорняков, на деревья, травы, бобовые и полевые культуры. В разных местах они причиняют экономический ущерб растениям спаржи, хлопка, кукурузы, соевых бобов, табака, люцерны, сахарной свеклы, сладкого перца, помидорам, картофелю, луку, гороху, подсолнечнику, и цитрусовым, а также другим растениям. CEW, как известно, нападает на кукурузу и помидоры, а также на артишок, спаржу, капусту, мускусную дыню, кормовую капусту, коровий горох, огурцы, баклажаны, салат, бобы Лимы, дыню, бамию, горох, перец, картофель, тыкву, лущильные сорта фасоли, шпинат, патиссон, сладкий картофель и арбуз, а также другие растения. Известно, что CEW имеет резистентность в отношении некоторых инсектицидов. Следовательно, ввиду вышеуказанного борьба с этими вредителями имеет важное значение. Кроме того, соединения, с помощью которых осуществляют борьбу с этими вредители, могут использоваться для борьбы с другими вредителями.
Некоторые соединения, описанные в настоящем документе, были тестированы против BAW и CEW, используя методики, описанные в примерах, приведенных ниже. В отчете о результатах использовали "таблицу уровня BAW и СEW" (см. раздел «Таблицы»).
Биоанализы на BAW (Spodoptera exigua)
Биоанализы на BAW проводили, используя анализ с 128-луночным планшетом питания. От одного до пяти личинок BAW возрастной стадии два помещали в каждую лунку (3 мл) планшета питания, которые заранее заполняли 1 мл искусственного питания, в которое вносили 50 мкг/см2 (в каждую из восьми лунок) тестируемого соединения (растворенного в 50 мкл смеси ацетон-вода 90:10), а затем оставляли высыхать. Лотки были покрыты прозрачной самоклеющейся крышкой и поддерживались при 25°C, 14:10 свет-темнота в течение от пяти до семи дней. Регистрировали процент смертности личинок в каждой лунке; активность в восьми лунках затем усредняли. Результаты приведены в таблице, озаглавленной "Таблица 5: биологические результаты" (см. раздел «Таблицы»).
Биоанализы на CEW (Helicoverpa zea)
Биоанализы на CEW проводили, используя анализ с 128-луночным планшетом питания. От одного до пяти личинок CEW возрастной стадии два помещали в каждую лунку (3 мл) планшета питания, которые заранее заполняли 1 мл искусственного питания, в которое вносили 50 мкг/см2 (в каждую из восьми лунок) тестируемого соединения (растворенного в 50 мкл смеси ацетон-вода 90:10), а затем оставляли высыхать. Лотки были покрыты прозрачной самоклеющейся крышкой и поддерживались при 25°C, 14:10 свет-темнота в течение от пяти до семи дней. Регистрировали процент смертности личинок в каждой лунке; активность в восьми лунках затем усредняли. Результаты приведены в таблице, озаглавленной "Таблица 5: биологические результаты" (см. раздел «Таблицы»).
Пример 33: БИОАНАЛИЗЫ НА ТЛИ ПЕРСИКОВОЙ ("GPA") (MYZUS PERSICAE).
GPA является наиболее значимым вредителем персиковых деревьев, вызывая снижение роста, сморщенность листьев и гибель различных тканей. Она также опасна, так как действует как вектор переноса растительных вирусов, таких как вирус картофеля Y и вирус, вызывающий скручивание листьев, на представителей пасленов/картофеля семейства Solanaceae, а также различные вирусы мозаики на многие другие продовольственные культуры. GPA нападает на такие растения как брокколи, лопух, капусту, морковь, цветную капусту, дайкон, баклажаны, зеленую фасоль, салат-латук, макадамию, папайю, перец, сладкий картофель, помидоры, кресс-салат и цуккини, а также другие растения. GPA также нападает на большое число декоративных культур, таких как гвоздика, хризантема, цветы белокочанной капусты, пуансеттию и розы. GPA имеет резистентность в отношении многих пестицидов.
Некоторые соединения, описанные в настоящем документе, были тестированы в отношении GPA, используя методики, описанные в нижеприведенном примере. В отчетах о результатах использовали «таблицу уровней GPA» (см. раздел «Таблицы»).
Саженцы капусты, выращиваемые в 3-дюймовых горшках, с 2-3 небольшими (3-5 см) настоящими листьями, использовали в качестве основы для теста. Сеянцы инфицировали 20-50 GPA (стадии бескрылой взрослой особи и нимфы) за один день до обработки химикалиями. Для каждой обработки использовали четыре горшка с отдельными саженцами. Тестируемые соединения (2 мг) растворяли в 2 мл раствора ацетон/метанол (1:1), получая исходные растворы тестируемого соединения 1000 м.д. Маточные растворы разводили 5× с помощью 0,025% Tween 20 в H2O с получением раствора тестируемого соединения 200 м.д. Для распыления раствора на обе стороны листьев капусты до побега использовали ручной аспиратор по типу распылитель. Эталонные растения (контроль с растворителем) опрыскивали только растворителем, содержащим 20% по объему растворителя ацетон/метанол (1:1). Обработанные растения перед оценкой поддерживали в комнате для хранения в течение трех дней при температуре около 25°С и относительной влажности окружающей среды (RH). Оценку проводили путем подсчета числа живой тли на растении под микроскопом. Процент уничтожения измеряли, используя формулу коррекции Эбботта (W.S. Abbott, "A method of Computing the Effectiveness of an Insecticide" J. Econ. Entomol. 18 (1925), pp.265-267), следующим образом.
Скорректированный % уничтожения =100 * (X-Y)/X,
где
X=количество живой тли на контрольных растениях, обработанных растворителем, и
Y=количество живой тли на обработанных растениях
Результаты показаны в таблице, озаглавленной "Таблица 5: Биологические результаты" (см. раздел «Таблицы»).
ПЕСТИЦИДНО ПРИЕМЛЕМЫЕ СОЛИ ДОБАВЛЕНИЯ КИСЛОТ, ПРОИЗВОДНЫЕ СОЛЕЙ, СОЛЬВАТЫ, ПРОИЗВОДНЫЕ СЛОЖНЫХ ЭФИРОВ, ПОЛИМОРФЫ, ИЗОТОПЫ И РАДИОНУКЛИДЫ
Соединения формул один, два и три могут быть получены в виде пестицидно приемлемых солей добавления кислот. В качестве неограничивающих примеров, функциональная аминогруппа может образовывать соли с хлористоводородной, бромистоводородной, серной, фосфорной, уксусной, бензойной, лимонной, малоновой, салициловой, яблочной, фумаровой, щавелевой, янтарной, винной, молочной, глюконовой, аскорбиновой, малеиновой, аспарагиновой, бензолсульфоновой, метансульфоновой, этансульфоновой, гидроксиметансульфоновой и гидроксиэтансульфоновой кислотами. Дополнительно, в качестве неограничивающего примера, функциональная кислотная группа может образовывать соли, включая соли, полученные из щелочных или щелочноземельных металлов, и солей, полученные из аммиака и аминов. Примеры предпочтительных катионов включают натрий, калий и магний.
Соединения формул один, два и три могут быть получены в виде производных солей. В качестве неограничивающих примеров, производное соли может быть получено путем приведения в контакт свободного основания с достаточным количеством желаемой кислоты с получением соли. Свободное основание может быть вновь получено путем обработки соли подходящим разбавленным водным раствором основания, таким как разбавленный водный гидроксид натрия (NaOH), карбонат калия, аммиак и бикарбонат натрия. В качестве примера, во многих случаях, пестицид, такой как 2,4-D, делают более водорастворимым путем преобразования в его диметиламиновую соль.
Соединения формул один, два и три могут быть получены в виде стабильных комплексов с растворителем, так чтобы комплекс оставался интактным после удаления некомплексного растворителя. Эти комплексы, как правило, называют «сольваты». Однако особенно желательно получать стабильные гидраты с водой в качестве растворителя.
Соединения формул один, два и три могут быть получены в виде производных сложных эфиров. Эти производные сложных эфиров затем могут использоваться таким же образом, как используется изобретение, описанное в настоящем документе.
Соединения формул один, два и три могут быть получены в виде различных кристаллических полиморфов. Полиморфизм является важным для развития агрохимических соединений, так как различные кристаллические полиморфы или структуры одного и того же соединения могут иметь абсолютно различные физические свойства и биологические характеристики.
Соединения формул один, два и три могут быть получены вместе с различными изотопами. Особенно важными являются соединения, имеющие 2H (также известен как дейтерий) вместо 1H.
Соединения формул один, два и три могут быть получены с различными радионуклидами. Особенно важными являются соединения, имеющие 14C.
СТЕРЕОИЗОМЕРЫ
Соединения формул один, два и три могут существовать в виде одного или нескольких стереоизомеров. Таким образом, определенные соединения могут быть получены в виде рацемических смесей. Специалистам в данной области понятно, что один стереоизомер может быть активней других стереоизомеров. Отдельные стереоизомеры могут быть получены известными методиками селективного синтеза, обычными методиками синтеза, используя растворенные исходные вещества, или обычными методиками растворения.
ИНСЕКТИЦИДЫ
Соединения формул один, два и три могут быть также использованы в комбинации (например, в композиционной смеси или с одновременным или последовательным использованием) с одним или несколькими из следующих инсектицидов - 1,2-дихлорпропан, абамектин, ацефат, ацетамиприд, ацетион, ацетопрол, акринатрин, акрилонитрил, аланикарб алдикарб, алдоксикарб, альдрин, аллетрин, аллосамидин, алликсикарб, альфа-циперметрин, альфа-экдизона, альфа-эндосульфан, амидитион, аминокарб, амитон, амитон оксалат, амитраз, анабазин, атидатион, азадирахтин, азаметифос, азинфос-этил, азинфосметил, азотоат, барий гексафторосиликат, бартрин, бендиокарб, бенфуракарб, бенсультап, бета-цифлутрин, бета-циперметрин, бифентрин, биоаллетрин, биоэтанометрин, биоперметрин, бистрифлурон, бура, борная кислота, бромфенвинфос, бромоциклен, бром-DDT, бромофос, бромофос-этил, буфенкарб, бупрофезин, бутакарб, бутатиофос, бутокарбоксим, бутонат, бутоксикарбоксим, кадусафос, арсенат кальция, полисульфид кальция, камфехлор, карбанолат, карбарил, карбофуран, сероуглерод, четыреххлористый углерод, карбофенотион, карбосульфан, картап, гидрохлорид картап, хлорантранилипрол, хлорбициклен, хлордан, хлордекон, хлордимеформ, гидрохлорид хлордимеформа, хлорэтоксифос, хлорфенапир, хлорфенвинфос, хлорфлуазурон, хлормефос, хлороформ, хлорпикрин, хлорфоксим, хлорпразофос, хлорпирифос, хлорпирифосметиле, хлортиофос, хлормафенозид, цинерин I, цинерин II, цинерины, цисметрин, клоэтокарб, клозантел, клотианидин, ацетоарсенит меди, арсенат меди, нафтенат меди, олеат меди, кумафос, кумитоат, кротамитон, кротоксифос, круфомат, криолита, цианфенфос, цианофос, циантоат, циантранилипрол, циклетрин, циклопротрин, цифлутрин, цигалотрин, циперметрин, цифенотрин, циромазин, цитиоат, ддт, декарбофуран, дельтаметрин, демефион, демефион-О, демефион-S, деметон, деметон-метил, деметон-О, деметон-О-метил, деметон-S, деметон-S-метил, деметон-S-метилсульфон, диафентиурон, диалифос, диатомит, диазинон, дикаптон, дихлофентион, дихлофос, дикресил, дикротофос, дицикланил, дильдрин, дифлубензурон, дилор, димефлутрин, димефокса, диметан, диметоат, диметрин, диметилвинфос, диметилан, динекс, динекс-диклексин, динопроп, диносам, динотефуран, диофенолан, диоксабензофос, диксакарб, диоксатион, дисульфотон, дитикрофос, d-лимонен, DNOC, DNOC-аммония, DNOC-калия, DNOC-натрия, дорамектин, экдистерона, эмамектин, бензоат эмамектина, EMPC, эмпентрин, эндосульфан, эндотион, эндрин, EPN, эпофенонан, эприномектин, эсдепаллетрин, эсфенвалерат, этафос, этиофенкарб, этион, этипрол, этоат-метил, этопрофос, этилформиат, этил-DDD, этилендибромид, этилен дихлорид, окись этилена, этофенпрокс, этримфос, EXD, фамфур, фенамифос, феназафлор, фенхлорфос, фенетакарб, фенфлутрин, фенитротион, фенобукарб, феноксакрим, феноксикарб, фенпиритрин, фенпропатрин, фенсульфотион, фентион, фентион-этил, фенвалерат, фипронил, флометоквин, флоникамид, флубендиамид (его дополнительно растворенные изомеры), флукофурон, флуциклоксурон, флуцитринат, флуфенерим, флуфеноксурон, флуфенпрокс, флуфипрол, флупирадифурон, флувалинат, фонофос, форметанат, форметанат гидрохлорид, формотион, формпаранат, формпаранат гидрохлорид, фосметилан, фоспират, фостиэтан, фуфенозид, фуратиокарба, фуретрин, гамма-цигалотрин, гамма-HCH, халфенпрокс, галофенозид, HCH, HEOD, гептахлор, гептенофос, гетерофос, гексафлумурон, HHDN, гидраметилнон, цианистый водород, гидропрен, гиквинкарб, имидаклоприд, имипротрин, индоксакарб йодометан, IPSP, изазофоса, изобензан, изокарбофос, изодрин, изофенфос, изофенфос-метил, изопрокарб, изопротиолан, изотиоат, изоксатион, ивермектин, джасмолин I, джасмолин II, джодфенфос, ювенильный гормон I, ювенильный гормон II, ювенильный гормон III, келеван, кинопрен, лямбда-цигалотрин, арсенат свинца, лепимецтин, лептофос, линдан, лиримфос, луфенурон, литидатион, малатион, малонобен, мазидокс, мекарбам, мекарфон, меназон, меперфлутрин, мефосфолан, хлорид ртути, мезулфенфос, метафлумизон, метакрифос, метамидофос, метидатион, метиокарб, метокротофос, метомил, метопрен, метотрин, метоксихлор, метоксифенозид, метил бромид, метил изотиоцианат, метилхлороформ, метиленхлорид, метофлутрин, метолкарб, метоксадиазон, мевинфос, мексакарбат, милбемектин, милбемициноксим, мипафокс, мирекс, молосултап, монокротофос, мономехипо, моносултап, морфотион, моксидектин, нафталофос, налед, нафталин, никотин, нифлуридид, нитенпирам, нитиазин, нитрилакарб, новалурон, новифлумурон, ометоат, оксамил, оксидиметон-метил, оксидепрофос, оксидисульфотон, пара-дихлорбензол, паратион, паратион-метил, пенфлурон, пентахлорфенол, перметрин, фенкаптон, фенотрин, фентоат, форат, фозалон, фосфолан, фосмет, фоснихлор, фосфамидон, фосфин, фоксим, фоксим-метил, пириметафос, пиримикарб, пиримифос-этил, пиримифос-метил, арсенит калия, тиоцианат калия, пп'-DDT, праллетрин, прекоцен I, прекоцен II, прекоцен III, примидофос, профенофос, профуралин, профлутрин, промацил, промекарб, пропафос, пропетамфос, пропоксур, протидатион, протиофос, протоат, протрифенбут, пиметрозин, пираклофос, пирафлупрол, пиразофос, пиресметрин, пиретрин I, пиретрин II, пиретрины, пиридабен, пиридалил, пиридафентион, пирифлукуиназон, пиримидифен, пиримитат, пирипрол, пирипроксифен, кассия, хиналфос, хиналфос-метил, квинотион, рафоксанид, ресметрин, ротенон, риания, сабадилла, шрадан, селамектин, силафлуофен, силикагель, натрий арсенит, натрий фторид, гексафторсиликат натрия, натрий тиоцианат, софамид, спинеторам, спиносад, спиромезифен, сулькофурон, натрий-сулькофурон, сульфурамид, сульфотеп, сульфоксафлор, сульфурил фторид, сульпрофос, тау-флувалинат, тазимкарб, TDE, тебуфенозид, тебуфенпирад, тебупиримфос, тефлубензурон, тефлутрин, темефос, TEPP, тераллетрин, тербуфос, тетрахлорэтан, тетрахлорвинфос, тетраметрин, тетраметилфлутрин, тета-циперметрин, тиаклоприд, тиаметоксам, тикрофос, тикрофос, тиокарбоксим, тиоциклам, тиоциклам оксалат, тиодикарб, тиофанокс, тиометон, тиосультап, тиосультап-динатрия, тиосультап-мононатрия, тхурингиенсис, толфенпирад, тралометрин трансфлутрин, транс-перметрин, триаразин, триазамат, триазофос, трихлорфон, трихлорметафос-3, трихлорнат, трифенофос, трифлумурон, триметакарб, трипрен, вамидотион, ванилипрол, XMC, ксилилкарб, дзета-циперметрин и золапрофос (в совокупности эти обычные называния инсектецидов обозначены как «группа инсектицидов»).
АКАРАЦИДЫ
Соединения формул один, два и три могут быть также использованы в комбинации (например, в композиционной смеси или с одновременным или последовательным использованием) с одним или несколькими из следующих акарицидов - ацеквиноцил, амидофлюмет, оксид мышьяка, азобензол, азоциклотин, беномил, беноксафос, бензоксимат, бензилбензоат, бифеназат, бинапакрил, бромопропилат, хинометионат, хлорбензид, хлорфенетол, хлорфензон, хлорфенсульфид, хлорбензилат, хлоромебуформ, хлорометиурон, хлоропропилат, клофентезин, циенопирафен, цифлуметофен, цигексатин, дихлофлуанид, дикофол, диенохлор, дифловидазин, динобутон, динокап, динокап-4, динокап-6, диноктон, динопентон, диносульфон, динотербон, дифенилсульфон, дисульфирам, дофенапин, этоксазол, феназахин, оксид фенбутатина, фенотиокарб, фенпироксимат, фензон, фетрифанил, флуакрипирим, флюазурон, флубензимин, флуэнэтил, флуметрин, флюорбензид, гекситиазокс, месульфен, MNAF, никкомицины, проклонол, пропаргит, хинтиофос, спиродиклофен, сульфирам, сера, тетрадифон, тетранактин, тетрасул и тиохинокс (в совокупности эти обычные называния акарицидов обозначены как «группа акарицидов»).
НЕМАТИЦИДЫ
Соединения формул один, два и три могут быть также использованы в комбинации (например, в композиционной смеси или с одновременным или последовательным использованием) с одним или несколькими из следующих нематицидов - 1,3-дихлорпропен, бенклотиаз, дазомет, дазомет-натрия, DBCP, DCIP, диамидафос, флюэнсульфон, фостиазат, фурфура, имициафос, изамидофос, изазофоса, метам, метам-аммония, метам-калия, метам-натрия, фосфокарб и тионазин (в совокупности эти обычные называния нематицитов обозначены как «группа нематицидов»).
ФУНГИЦИДЫ
Соединения формул один, два и три могут быть также использованы в комбинации (например, в композиционной смеси или с одновременным или последовательным использованием) с одним или несколькими из следующих фунгицидов - бромид (3-этоксипропил)ртути, хлорид 2-метоксиэтил ртути, 2-фенилфенол, сульфат 8-гидроксихинолина, оксихинолин 8-фенилртути, ацибензолар, ацибензолар-S-метил, аципетакс, аципетакс-меди, аципетакс-цинка, алдиморф, аллиловый спирт, аметострадин, амисульбром, ампропилфос, анилазин, ауреофунгин, азаконазол, азитирам, азоксистробин, полисульфид бария, беналаксил, беналаксил-М, беноданил, беномил, бенхинокс, бенталурон, бентиаваликарб, бентиаваликарб-изопропил, бензалконий хлорид, бензамакрил, бензамакрил-изобутила, бензаморф, бензогидроксамова кислота,бетоксазин, бинапакрил, дифенил, битертанол, битианол, биксафен, бластицидин-S, смесь Бордо, боскалид, бромуконазол, бупиримат, смесь Бургундия, бутиобат, бутиламин, полисульфид кальция, каптафол, каптан, карбаморф, карбендазим, карбоксин, карпропамид, карвон, смесь Чесхант, хинометионат, хлобентиазон, хлораниформетан, хлоранил, хлорфеназол, хлординитронафталин, хлоронеб, хлорпикрин, хлороталонил, хлорхинокс, хлозолинат, климбазол, клотримазол, ацетат меди, карбонат, основной гидроксид меди, нафтенат меди, олеат меди, оксихлорид меди, силикат меди, сульфат меди, хромат цинковой меди, крезол, цуфранеб, цупробам, оксид меди, циазофамид, циклафурамид, циклогексимид, цифлуфенамид, цимоксанил, ципендазол, ципроконазол, ципродинила, дазомет, дазомет-натрия, DBCP, дебакарб, децафентин, дегидроуксусная кислота, дихлофлуанид, дихлон, дихлорфен, дихлозолин, диклобутразол, диклоцимет, дикломезин, дикломезин-натрия, диклоран, диэтофенкарб, диэтилпирокарбонатом, дифеноконазол, дифлуметорим, диметиримол, диметоморф, димоксистробин, диниконазол, диниконазол-М, динобутон, динокап, динокап-4, динокап-6, диноктон, динопентон, диносульфон, динотербон, дифениламин, дипиритион, дисульфирам, диталимфос, дитианон, DNOC, DNOC-аммония, DNOC-калия, DNOC-натрия, додеморф, додеморф ацетат, додеморф бензоат, додицин, додицин-натрия, додин, дразоксолон, эдифенфос, эпоксиконазол, этаконазол, eтем, этабоксам, этиримол, этоксиквин, этилртуть 2,3-дигидроксипропил меркаптид, ацетат этилртути, бромид этилртути, хлорид этилртути, фосфат этилртути, этридиазол, фамоксадон, фенамидон, фенаминосульф, фенапанил, фенаримол, фенбуконазол, фенфурам, фенгексамид, фенитропан, феноксанил, фенпиклонил, фенпропидин, фенпропиморф, фентин, хлорид фентина, гидроксид фентина, фербам, феримзон, флуазинам, флудиоксонил, флуметовер, флуморф, флуопиколид, флуопирам, флуороимид, флуотримазол, флуоксастробин, флухинконазол, флусилазол, флусульфамид, флутианил, флутоланил, флутриафол, флуксопироксад, фолпет, формальдегид, фосетил, фосетил-алюминий, фуберидазол, фуралаксил, фураметпир, фуркарбанил, фурконазол, фурконазол-цис, фурфурол, фурмециклокс, фурофанат, глиодин, гризеофульвин, гуазатин, галакринат, гексахлорбензол, гексахлорбутадиен, гексаконазол, гексилтиофос, гидраргафен, гимексазол, имазалил, имазалил нитрат, сульфат имазалил, имибенконазол, иминоктадин, иминоктадин триацетат, иминоктадин триалбезилат йодометан, ипконазол, ипробенфос, ипродион, ипроваликарб, изопротиолан, изопирозам, изотианил, изоваледион, касугамицин, крезоксимметил, манкупер, манкозеб, мандипропамид, манеб, мебенил, мекарбинизид, мепанипирим, мепронил, мептилдинокап, хлорид ртути, оксид ртути, хлорид ртути; металаксил, металаксил-М, метам, метам-аммония, метам-калия, метам-натрия, метазоксолон, метконазол, метасульфокарб, метфуроксам, метил бромид, метилизотиоцианат, метилртути бензоат, метилртути дициандиамид, метилртути пентахлорфеноксид, метирам, метоминостробин, метрафенон, метсульфовакс, милнеб, миклобутанил, миклозолин, N-(этилртуть)-п-толуолсульфонанилид, набам, натамицин, нитростирол, нитротализопропил, нуаримол, ОСН, октилинон, офурас, орисастробин, оксадиксил, оксин медь, окспоконазол, окспоконазол фумарат, оксикарбоксин, пефуразоат, пенконазол, пенцикурон, пенфлуфен, пентахлорфенол, пентиопирад, карбамид фенилртути, ацетат фенилртути, хлорид фенилртути, производное пирокатехина фенилртути, нитрат фенилртути, салицилат фенилртути, фосдифен, фталид, пикоксистробин, пипералин, поликарбамат, полиоксины, полиоксорим, полиоксорим-цинк, азид калия, полисульфид калия, тиоцианат калия, пробеназол, прохлораз, процимидон, пропамокарб, гидрохлорид пропамокарба, пропиконазол, пропинеб, прохиназид, протиокарб, гидрохлорид протиокарба, протиоконазол, пуракарболид, пираклостробин, пираклостробин, пираметостробин, пираоксистрабин, пиразофос, пирибенкарб, пиридинитрил, пирифенокс, пириметанил, пириофенон, пирохилон, пироксихлор, пироксифур, хинацетол, сульфат хинацетола, хиназамид, хинконазол, хиноксифен квинтозин, рабензазол, салициланилид, седаксан, силтиофам, симеконазола, азид натрия, ортофенилфеноксид натрия, фентахлорфенаксид натрия, полисульфид натрия, спироксамин, стрептомицин, сера, сультрофен, TCMTB, тебуконазол, тебуфлокаин, теклофталам, текназен, текорам, тетраконазол, тиабендазол, тиадифлуор, тициофен, тифлузамид, тиохлорфенфим, тиомерсал, тиофанат, тиофанатметил, тиохинокс, тирама, тиадинил, тиоксимид, толклофосметил, толилфлуанид, ацетат толилартути, триадимефон, триадименол, триамифос, триаримол, триазбутил, триазоксид, оксид трибутилолова, трихламид, трициклазол, тридеморф, трифлоксистробин, трифлумизол, трифорин, тритиконазол, униконазол, униконазол-П, валидамицин, валифеналат, винклозолин, зариламид, нафтенат цинк, зинеб, зирам, зоксамид (в совокупности эти обычные называния фунгицидов обозначены как «группа фунгицидов»).
ГЕРБИЦИДЫ
Соединения формул один, два и три могут быть также использованы в комбинации (например, в композиционной смеси или с одновременным или последовательным использованием) с одним или несколькими из следующих гербицидов - 2,3,6-ТБА, 2,3,6-ТБА-диметиламмоний, 2,3,6-ТБА-натрий, 2,4,5-т, 2,4,5-т-2-бутоксипропил, 2,4,5-т-2-этилгексил, 2,4,5-т-3-бутоксипропил, 2,4,5-TB, 2,4,5-т-бутометил, 2,4,5-т-бутотил, 2,4,5-т-бутил, 2,4,5-т-изобутил, 2,4,5-т-изоктил, 2,4,5-т-изопропил, 2,4,5-т-метил, 2,4,5-т-пентил, 2,4,5-т-натрий, 2,4,5-т-триэтиламмоний, 2,4,5-т-троламин, 2,4-D, 2,4-D-2-бутоксипропил, 2,4-D-2-этилгексил, 2,4-D-3-бутоксипропил, 2,4-D-аммония, 2,4-ДБ, 2,4-ДБ-бутил, 2,4-ДБ-диметиламмоний, 2,4-ДБ-изоктил, 2,4-ДБ-калий, 2,4-ДБ-натрий, 2,4-D-бутотил, 2,4-D-бутил, 2,4-D-диэтиламмоний, 2,4-D-диметиламмоний, 2,4-D-диоламина, 2,4-D-додециламмониум, 2,4-DEB, 2,4-DEP, 2,4-D-этил, 2, 4-D-гептиламмония, 2,4-D-изобутил, 2,4-D-изоктил, 2,4-D-изопропил, 2,4-D-изопропиламмоний, 2,4-D-литий, 2,4-D-мептил, 2,4-D-метил, 2,4-D-октил, 2,4-D-пентил, 2,4-D-калий, 2,4-D-пропил, 2,4-D-натрий, 2,4-D-тефурил, 2,4-D-тетрадециламмоний, 2,4-D-триэтиламмоний, 2,4-D-трис(2-гидроксипропил)аммоний, 2,4-D-троламин, 3,4-DA, 3,4-DB, 3,4-DP, 4-CPA, 4-CPB, 4-CPP, ацетохлор, ацифлуорфен, ацифлуорфенметил, ацифлуорфен-натрия, аклонифен, акролеин, алахлор, аллидохлор, аллоксидим, аллоксидим-натрий, аллиловый спирт, алорак, аметридион, аметрин, амибузин, амикарбазон, амидосульфурон, аминоциклопирахлор, аминоциклопирахлор-метил, аминоциклопирахлор-калий, аминопиралид, аминопиралид-калий, аминопиралид-трис(2-гидроксипропил)аммония, амипрофос-метил, амитрол, сульфамат аммония, анилофос, анизурон, асулам, асулам-калия, асулам-натрия, атратон, атразин, азафенидин, азимсульфурон, азипротрин, барбан, BCPC, бефлубутамид, беназолин, беназолин-диметиламмоний, беназолин-этил, беназолин-калия, бенкарбазон, бенфлуралин, бенфуресат, бенсульфурон, бенсульфурон-метил, бенсулид, бентазон, бентазон-натрия, бензадокс, бензадокс-аммония, бензфендизон, бензипрам, бензобициклон, бензофенап, бензофлуор, бензоилпроп, бензоилпроп-этил, бензтиазурон, бициклопирон, бифенокс, биланафос, биланафос-натрия, биспирибак, биспирибак-натрия, бура, бромацил, бромацил-литий, бромацил-натрия, бромбонил, бромобутид, бромофеноксим, бромоксинил, бромоксинил бутират, бромоксинил гептаноат, бромоксинилоктаноат, бромоксинил-калия, бромпуразон, бутахлор, бутафенацил, бутамифос, бутенахлор, бутидазол, бутиурон, бутралин, бутроксидим, бутурон, бутилат, какодиловая кислота, кафенстрол, хлорат кальция, цианамида кальция, камбендихлор, карбасулам, карбетамид, карбоксазол, карфентразон, карфентразонэтил, CDEA, CEPC, хлометоксифен, хлорамбен, хлорамбен-аммония, хлорамбен-диоламина, хлорамбен-метил, хлорамбен-метиламмоний, хлорамбен-натрия, хлоранокрил, хлоразифоп, хлоразифоп-пропаргил, хлоразин, хлорбромурон, хлорбуфам, хлорэтурон, хлорфенак, хлорфенак-натрия, хлорфенпроп, хлорфенпроп-метил, хлорфлуразол, хлорфлуренол, хлорфлуренол-метил, хлоридазон, хлоримурон, хлоримурон-этил, хлорнитрофен, хлоропон, хлоротолурон, хлороксурон, хлороксинил, хлорпрокарб, хлорпрофам, хлорсульфурон, хлортал, хлортал-диметил, хлортал-монометил, хлортиамид, цинидон-этил, цинметилин, циносульфурон, цисанилид, клетодим, клиодинат, клодинафоп, клодинафоп-пропаргил, клофоп, клофоп-изобутил, кломазон, кломепроп, клопроп, клопроксидим, клопиралид, клопиралид-метил, клопиралид-оламин, клопиралид-калий, клопиралид-трис(2-гидроксипропил) аммония, клорансулам, клорансулам-метил, CMA, сульфат меди, CPMF, CPPC, кредазин, крезол, кумилурон, цианамид, цианатрин, цианазин, циклоат, циклосульфамурон, циклоксидим, циклурон, цигалофоп, цигалофоп-бутил, циперкват, хлорид циперквата, ципразин, ципразол, ципромид, даймурон, далапон, далапон-кальция, далапон-магний, далапон-натрия, дазомет, дазомет-натрия, делахлор, десмедифам, десметрин, ди-аллат, дикамба, дикамба-диметиламмония, дикамба-диоламина, дикамба-изопропиламмоний, дикамба-метил, дикамба-оламин, дикамба-калий, натрий-дикамба, дикамба-троламин, дихлобенил, дихлоральмочевина, дихлормат, дихлорпроп, дихлорпроп-2-этилгексил, дихлорпроп-бутотил, дихлорпроп-диметиламмоний, дихлорпроп-этиламмония, дихлорпроп-изоктил, дихлорпроп-метил, дихлорпроп-P, дихлорпроп-P-диметиламмония, дихлорпроп-калия, дихлорпроп-натрия, диклофоп, диклофоп-метил, диклосулам, диэтамкват, диэтамкват дихлорид, диэтатил, диэтатил-этил, дифенопентен, дифенопентен-этил, дифеноксурон, дифензокват, дифензокват метилсульфат, дифлуфеникан, дифлуфензопир, дифлуфензопир-натрия, димефурон, димепиперат, диметахлор, диметаметрин, диметенамид, диметенамид-П, димексан, димидазон, динитрамин, динофенат, динопроп, диносам, диносеб, диносеб ацетат, диносеб-аммония, диносеб-диоламина, диносеб-натрия, диносеб-троламин, динотерб, динотерб ацетат, дифацинон-натрия, дифенамид, дипропетрин, дикват, дикват дибромид, дисульфид, дисульфид-натрия, дитиопир, диурон, DMPA, DNOC, DNOC-аммония, DNOC-калия, DNOC-натрия, DSMA, EBEP, эглиназин, эглиназин-этил, эндотал, эндотал-диаммоний, эндотал-дикалия, эндотал-динатрия, эпроназ, ЕРТС, эрбон, эспрокарб, эталфлуралин, этаметсульфурон, этаметсульфурон-метил, этидимурон, этилоат, этофумезат, этоксифен, этоксифен-этил, этоксисульфурон, этинофен, этипромид, этобензанид, EXD, феназулам, фенопроп, фенопроп-3-бутоксипропил, фенопроп-бутометил, фенопроп-бутотил, фенопроп-бутил, фенопроп-изоктил, фенопроп-метил, фенопроп-калия, феноксапроп, феноксапроп-этил, феноксапроп-P, феноксапроп-П-этил, феноксасульфон, фентеракол, фентиапроп, фентиапроп-этил, фентразамид, фенурон, фенурон ТСА, сульфат железа, флампроп, флампроп-изопропил, флампроп-M, флампроп-метил, флампроп-M-изопропилом, флампроп-М-метил, флазасульфурон, флорасулам, флуазифоп, флуазифоп-бутил, флуазифоп-метил, флуазифоп-Р, флуазифоп-Р-бутил, флуазолат, флукарбазон, флукарбазон-натрия, флуцетосульфурон, флухлоралин, флуфенацет, флуфеникан, флуфенпир, флуфенпир-этил, флуметсулам, флумезин, флумиклорак, флумиклорак-пентил, флумиоксазин, флумипропин, флуометурон, флуородифен, флуорогликофен, флуорогликофен-этил, флуоромидин, флуоронитрофен, флуотиурон, флупоксам, флупропасил, флупропанат, флупропанат-натрия, флупирсульфурон, флупирсульфурон-метил-натрия, флуридон, флурохлоридон, флуроксипир, флуроксипир-бутометил, флуроксипир-мептил, флуртамона, флутиацет, флутиацет-метил, фомесафен, фомесафен-натрия, форамсульфурон, фосамин, фосамин-аммония, фурилоксифен, глюфозинат, глюфозинат-аммония, глюфозинат-P, глюфозинат-P-аммония, глюфозинат-P-натрия, глифосат, глифосат-диаммоний, глифосат-диметиламмония, глифосат-изопропиламмоний, глифосат-моноаммония, глифосат-калия, глифосат-сесквинатрия, глифосат-тримезиум, галосафен, галосульфурон, галосульфурон-метил, галоксидин, галоксифоп, галоксифоп-этотил, галоксифоп-метил, галоксифоп-P, галоксифоп-P-этотил, галоксифоп-P-метил, галоксифоп-натрия, гексахлорацетон, гексафлурат, гексазинон, имазаметабенз, имазаметабенз-метил, имазамокс, имазамокс-аммония, имазапик, имазапик-аммония, имазапир, имазапир-изопропиламмоний, имазаквин, имазаквин-аммония, имазаквин-метил, имазаквин-натрия, имазетапир, имазетапир-аммония, имазасульфурон, инданофан, индазифлам, йодбонил йодометан, йодосульфурон, йодосульфурон-метил-натрия, иоксинил, иоксинил октаноат, иоксинил-лития, иоксинил-натрия, ипазин, ипфенкарбазон, ипримидам, изокарбамид, изоцил, изометиозин, изонорурон, изополинат, изопропалин, изопротурон, изоурон, изоксабен, изоксахлортол, изоксафлутол, изоксапирифоп, карбутилат, кетоспирадокс, лактофен, ленацил, линурон, MAA, МАМА, МСРА, МСРА-2-этилгексил, MCPA-бутотил, МСРА-бутил, MCPA-диметиламмоний, МСРА-диоламина, МСРА-этил, МСРА-изобутил, МСРА-изоктил, МСРА-изопропил, МСРА-метил, МСРА-оламин, МСРА-калий, натрий-MCPA, MCPA-тиоэтил, МСРА-троламин, MCPB, MCPB-этил, MCPB-метил, MCPB-натрий, мекопроп, мекопроп-2-этилгексил, мекопроп-диметиламмоний, мекопроп-диоламина, мекопроп-этадил, мекопроп-изоктил, мекопроп-метил, мекопроп-P, мекопроп-P-диметиламмония, мекопроп-P-изобутил, мекопроп-калия, мекопроп-P-калия, мекопроп-натрия, мекопроп-троламин, мединотерб, мединотерб ацетат, мефенацет, мефлуидид, мефлуидид-диоламина, мефлуидид-калия, мезопразин, мезосульфурон, мезосульфурон-метил, мезотрион, метам, метам-аммония, метамифоп, метамитрон, метам-калия, метам-натрия, метазахлор, метазосульфурон, метфлуразон, метабензтиазурон, металпропалин, метазол, метиобенкарб, метиозалин, метиурон, метометон, метопротрин, бромистого метила, метилизотиоцианат, метилдимрон, метобензурон, метолахлор, метосулам, метоксурон, метрибузин, метсульфурон, метсульфурон-метил, молинат, моналид, монисоурон, монохлоруксусную кислоту, монолинурон, монурон, монурон TCA, морфамкват, дихлорид морфамквата, MSMA, напроанилид, напропамид, напталам, напталам-натрия, небурон, никосульфурон, нипираклофен, нитралин, нитрофен, нитрофлуорфен, норфлуразон, норурон, ОСН, орбенкарб, орто-дихлорбензол, ортосульфамурон, оризалин, оксадиаргил, оксадиазон, оксапиразон, оксапиразон-димоламин, оксапиразон-натрия, оксасульфурон, оксацикломефон, оксифлуорфен, парафлурон, паракват, паракват дихлорид, паракват диметилсульфат, пебулат, пеларгоновая кислота, пендиметалин, пенокссулам, пентахлорфенол, пентанохлор, пентоксазон, перфлуидон, фентоксамид, фенизофам, фенмедифам, фенмедифам этил, фенобензурон, ацетат фенилртути, пиклорам, пиклорам-2-этилгексил, пиклорам-изоктил, пиклорам-метил, пиклорам-оламин, пиклорам-калий, пиклорам-триэтиламмония, пиклорам-трис (2-гидроксипропил) аммония, пиколинафен, пиноксаден, пиперофос, арсенит калия, азид калия, цианат калия, претилахлор, примисульфурон, примисульфурон-метил, проциазин, продиамин, профлуазол, профлуралин, профоксидим, проглиназин, проглиназин-этил, прометон, прометрин, пропахлор, пропанил, пропаквизафоп, пропазин, профам, про пизохлор, пропоксикарбазон, пропоксикарбазон-натрия, пропирисульфурон, пропизамид, просульфалин, просульфокарб, просульфурон, проксан, проксан-натрия, принахлор, пиданон, пираклонил, пирафлуфен, пирафлуфен-этил, пирасульфотол, пиразолинат, пиразосульфурон, пиразосульфурон-этил, пиразоксифен, пирибензоксим, пирибутикарб, пириклор, пиридафол, пиридат, пирифталид, пиринобац, пиринобац-метил, пиримисулфан, пиритиобак, пиритиобак-натрия, пироксосульфон, пирокссулам, квинклорак, квинмерац, квинокламиквинонамид, хизалофоп, хизалофоп-этил, хизалофоп-P, хизалофоп-P-этил, хизалофоп-P-тефурил, родетанил, римсульфурон, сафлуфенацил, себутилазин, сецбуметон, сетоксидим, сидурон, симазин, симетон, симетрин, SMA, S-метолахлор, арсенит натрия, азид натрия, хлорат натрия, сулкотрион, сульфаллат, сульфентразон, сульфометурон, сульфометурон-метил, сульфосульфурон, серная кислота, сульгликапин, SWEP, TCA, TCA-аммоний, кальций-TCA, TCA-этадил, TCA-магний, натрий-TCA, тебутам, тебутиурон, тефурилфлурон, темботрион, тепралоксидим, тербацил, тербукарб, тербухлор, тербуметон, тербутилазин, тербутрин, тетрафлурон, тенилхлор, тиазафлурон, тиазопир, тидиазимин, тидиазурон, тиенкарбазон, тиенкарбазон-метил, тифенсульфурон, тифенсульфурон-метил, тиобенкарб, тиокарбазил, тиоклорим, топрамезон, тралкоксидим, три-аллат, триасульфурон, триазифлам, трибенурон, трибенурон-метил, трикамба, триклопир, триклопир-бутотил, триклопир-этил, триклопир-триэтиламмония, тридифан, триэтазин, трифлоксисульфурон, трифлоксисульфурон-натрия, трифлуралин, трифлусульфурон, трифлусульфурон-метил, трифоп, трифоп-метил, трифопзим, тригидрокситриазин, триметурон, трипропиндан, тритак, тритосульфурон, вернолат, ксилахлор (в совокупности эти обычные называния гербицидов обозначены как «группа гербицидов»).
БИОПЕСТИЦИДЫ
Соединения формул один, два и три также могут быть использованы в комбинации (например, в композиционной смеси или с одновременным или последовательным использованием) с одним или несколькими из следующих биопестицидов. Термин «биопестицид» используют в отношении микробиологических агентов, борющихся с вредителями/паразитами, которые используются так же как химические пестициды. Обычно они представляют собой бактериальные агенты, но есть также примеры агентов на основе грибов, включая Trichoderma spp. и Ampelomyces quisqualis (агент для борьбы с мучнистой росой винограда). Bacillus subtilis используют для борьбы с патогенами растений. Борьбу с сорняками и грызунами также можно осуществлять с помощью микробных агентов. Одним из примеров хорошо известного инсектицида является Bacillus thuringiensis, вызывающий бактериальное заболевание чешуекрылых, жесткокрылых и двукрылых. Так как он незначительно влияет на другие организмы, то он считается более экологичным, чем синтетические пестициды. Биологические инсектициды включают продукты на основе:
1. энтомопатогенных грибов (например, Metarhizium anisopliae);
2. энтомопатогенных нематод (например, Steinernema feltiae); и
3. энтомопатогенных вирусов (например, грануловирус Cydia pomonella).
Другие примеры энтомопатогенных организмов включают, но ими не ограничиваются, бакуловирусы, бактерии и другие прокариотические организмы, грибы, простейшие и Microsproridia. Инсектициды, полученные биологическим путем, включают, но ими не ограничиваются, ротенон, вератридин, а также микробные токсины; толерантные или резистентные к насекомым сорта растений; и организмы, модифицированные технологией рекомбинантных ДНК, либо продуцирующие инсектициды, либо придающие свойство резистентности к насекомым генетически модифицированному организму. В одном из вариантов осуществления соединения формул один, два или три можно использовать с одним или несколькими биопестицидами в области обработки семян и почвы. В Manual of Biocontrol Agents приведен обзор доступных биологических инсектицидов (и других биологических продуктов для борьбы с вредителями). Copping L.G. (ed.) (2004). The Manual of Biocontrol Agents (formerly the Biopesticide Manual) 3rd Edition. British Crop Production Council (BCPC), Farnham, Surrey UK.
ДРУГИЕ АКТИВНЫЕ СОЕДИНЕНИЯ
Соединения формул один, два и три могут быть также использованы в комбинации (например, в композиционной смеси или с одновременным или последовательным использованием) с одним или несколькими из следующих:
1. 3-(4-хлор-2,6-диметилфенил)-4-гидрокси-8-окса-1-азаспиро[4,5]дец-3-ен-2-он;
2. 3-(4'-хлор-2,4-диметил[1,1'-бифенил]-3-ил)-4-гидрокси-8-окса-1-азаспиро[4,5]дец-3-ен-2-он;
3. 4-[[(6-хлор-3-пиридинил)метил]метиламино]-2(5H)-фуранон;
4. 4-[[(6-хлор-3-пиридинил)метил]циклопропиламино]-2(5H)-фуранон;
5. 3-хлор-N2-[(1S)-1-метил-2-(метилсульфонил)этил]-N1-[2-метил-4-[1,2,2,2-тетрафтор-1-(трифторметил)этил]фенил]-1,2-бензолдикарбоксамид;
6. 2-циано-N-этил-4-фтор-3-метоксибензолсульфонамид;
7. 2-циано-N-этил-3-метоксибензолсульфонамид;
8. 2-циано-3-дифторметокси-N-этил-4-фторбензолсульфонамид;
9. 2-циано-3-фторметокси-N-этилбензолсульфонамид;
10. 2-циано-6-фтор-3-метокси-N,N-диметилбензолсульфонамид;
11. 2-циано-N-этил-6-фтор-3-метокси-N-метилбензолсульфонамид;
12. 2-циано-3-дифторметокси-N,N-диметилбензолсульфонамид;
13. 3-(дифторметил)-N-[2-(3,3-диметилбутил)фенил]-1-метил-1H-пиразол-4-карбоксамид;
14. N-этил-2,2-диметилпропионамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил)гидразон;
15. N-этил-2,2-дихлор-1-метилциклопропанкарбоксамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил) гидразон никотин;
16. O-{(E-)-[2-(4-хлорфенил)-2-циано-1-(2-трифторметилфенил)винил]} S-метил тиокарбонат;
17. (E)-N1-[(2-хлор-1,3-тиазол-5-илметил)]-N2-циано-N1-метилацетамидин;
18. 1-(6-хлорпиридин-3-илметил)-7-метил-8-нитро-1,2,3,5,6,7-гексагидроимидазо[1,2-a]пиридин-5-ол;
19. 4-[4-хлорфенил-(2-бутилидингидразоно)метил)]фенил мезилат; и
20. N-этил-2,2-дихлор-1-метилциклопропанкарбоксамид-2-(2,6-дихлор-альфа,альфа,альфа-трифтор-п-толил)гидразон.
Соединения формул один, два и три также могут быть использованы в комбинации (например, в композиционной смеси или с одновременным или последовательным использованием) с одним или несколькими из следующих групп: альгициды, антифидинги, авициды, бактерициды, репелленты против птиц, хемостерилизаторы, антидоты гербицидов, аттрактанты против насекомых, средства от насекомых, репелленты против млекопитающих, агенты, нарушающие спаривание, моллюскициды, растительные активаторы, регуляторы роста растений, родентициды и/или вируциды (в совокупности эти обычные называния обозначены как «группа AI»). Следует отметить, что соединения, подпадающие в группу AI, группу инсектицидов, группу фунгицидов, группу гербицидов, группу акарицидов или группу нематицидов могут относиться к более чем одной группе, так как соединение может иметь множественную активность. Для получения дополнительной информации см. документ “Compendium of Pesticide Common Names”, расположенный на сайте http://www.alanwood.net/pesticides/index.html. Также см. “The Pesticide Manual” 14-ое издание под редакцией C D S Tomlin, авторское право 2006, British Crop Production Council, или его более ранние или более свежие издания.
СИНЕРГЕТИЧЕСКИЕ СМЕСИ И СИНЕРГЕТИКИ
Соединения формул один, два и три можно использовать вместе с соединениями группы инсектицидов с получением синергичных смесей, где механизм действия такого соединения по сравнению с механизмом действия соединения формул один и два является одинаковым, сходным или различным. Примеры механизмов действия включают, но ими не ограничиваются, механизмы действия: ингибитора ацетилхолинэстераза; модулятора натриевого канала; ингибитора биосинтеза хитина; антагониста GABA-зависимых натриевых каналов; агониста GABA- и глутаминат-зависимых хлоридных каналов; агониста рецептора ацетилхолина; ингибитора MET I; Мg-стимулируемого ингибитора АТФазы; никотинового ацетилхолинового рецептора; агента, повреждающего мембрану средней кишки; агента, повреждающего окислительное фосфорилирование и рецептора рианодина (RyRs). Кроме того, соединения формул один и два могут использоваться вместе с соединениями группы фунгицидов, группы акарицидов, группы гербицидов или группы нематоцидов с образованием синергических смесей. Кроме того, соединения формул один, два и три, могут использоваться с другими активными соединениями, такими как соединения раздела "ДРУГИЕ БИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА", альгициды, авициды, бактерициды, моллюскициды, родентициды, вируциды, защитные гербициды, адъюванты и/или поверхностно-активные вещества с получением синергетических смесей. Обычно массовое соотношение соединений формул один, два и три в синергической смеси с другим соединением составляет от примерно 10:1 до примерно 1:10, предпочтительно, от примерно 5:1 до примерно 1:5 и, более предпочтительно, от примерно 3:1, а также, еще более предпочтительно, составляет около 1:1. Кроме того, следующие соединения известны как синергисты и могут быть использованы с соединениями, описанными в формуле один: пиперонилбутоксид, пипротал, пропил изом, сезамекс, сезамолин, сульфоксид и трибуфос (в совокупности эти синергисты обозначены как «синергитическая группа»).
СОСТАВЫ
Пестициды редко подходят для использования в чистом виде. Как правило, необходимо добавить другие вещества, так, чтобы пестицид мог быть использован в необходимой концентрации и в соответствующей форме, которая обеспечивает легкость нанесения, обработки, транспортировки, хранения, а также максимальную активность пестицидов. Таким образом, с пестицидами формируют, например, приманки, концентрированные эмульсии, порошки, эмульгируемые концентраты, фумиганты, гели, гранулы, микрокапсулы, составы для обработки семян, суспензионные концентраты, суспоэмульсии, таблетки, растворимые в воде жидкости, диспергируемые в воде гранулы или сухие текучие составы, смачивающиеся порошки и ультранизкообъемные растворы. Для получения дополнительной информации касательно типов составов см. “Catalogue of Pesticide Formulation Types and International Coding System” Technical Monograph n°2, 5-ое издание, CropLife International (2002).
Пестициды используются чаще всего в виде водных суспензий или эмульсий, полученных из концентрированных составов, таких пестицидов. Такие водорастворимые, водосуспендируемые или эмульгируемые составы являются либо твердыми веществами, обычно известными как смачивающиеся порошки или диспергируемые в воде гранулы, либо жидкостями, обычно, известными как эмульгируемые концентраты или водные суспензии. Смачивающиеся порошки, которые могут быть уплотнены с образованием диспергируемых в воде гранул, содержат однородную смесь пестицида, носителя и поверхностно-активных веществ. Концентрация пестицида составляет, как правило, от примерно 10% до примерно 90% по массе. Носитель обычно выбирают из аттапульгитовых глин, монтмориллонитовых глин, диатомовой земли или очищенных силикатов. Эффективные поверхностно-активные вещества, содержащиеся в количестве от примерно 0,5% до примерно 10% смачивающегося порошка, можно найти среди сульфонированных лигнинов, конденсированных нафталинсульфонатов, нафталинсульфонатов, алкилбензолсульфонатов, алкилсульфатов и неионных поверхностно-активных веществ, таких как аддукты окиси этилена алкилфенолов.
Эмульсионные концентраты пестицидов содержат подходящие концентрации пестицида, например, от около 50 до около 500 г на литр жидкости, растворенные в носителе, который представляет собой либо смешиваемый с водой растворитель, либо смесь несмешиваемого с водой органического растворителя и эмульгаторов. Органические растворители, которые можно использовать, включают ароматические соединения, в частности, ксилолы и нефтяные фракции, в частности, высококипящие нафталиновые и олефиновые нефтяные фракции, такие как тяжелая ароматическая нафта. Также могут быть использованы другие органические растворители, такие как терпеновые растворители, в том числе производные канифоли, алифатические кетоны, такие как циклогексанон, и сложные спирты, такие как 2-этоксиэтанол. Подходящие эмульгаторы для эмульгируемых концентратов могут быть выбраны из обычных анионных и неионных поверхностно-активных веществ.
Водные суспензии включают суспензии нерастворимых в воде пестицидов, диспергированных в водном носителе в концентрации, находящейся в диапазоне от примерно 5% до примерно 50% по массе. Суспензии получают путем мелкого измельчения пестицида и энергичного смешивания его в носителе, состоящего из воды и поверхностно-активных веществ. Для повышения плотности и вязкости водного носителя также могут быть добавлены такие ингредиенты, как неорганические соли и синтетические или природные смолы. Как правило, наиболее эффективно измельчить и смешать пестицид одновременно с получением водной смеси и гомогенизации ее в таком устройстве, как песчаная мельница, шаровая мельница или гомогенизатор поршневого типа.
Пестициды также могут использоваться в виде гранулированных композиций, которые особенно эффективны для нанесения на почву. Гранулированные составы обычно содержат от приблизительно 0,5% до приблизительно 10% по массе пестицида, диспергированного в носителе, который содержит глину или подобное вещество. Такие композиции обычно получают путем растворения пестицида в подходящем растворителе, и нанесением его на гранулированный носитель, который предварительно получают с подходящим размером частиц, находящемся в диапазоне от примерно 0,5 до примерно 3 мм. Такие композиции могут быть получены путем формирования теста или пасты носителя и соединения и дробления и сушки с получением частиц гранул желаемого размера.
Порошки, содержащие пестицид, получают путем тщательного смешивания пестицида в порошкообразной форме с соответствующим порошкообразным носителем, используемых для сельского хозяйства, таким как каолин, измельченный вулканический камень и тому подобное. Порошок может подходящим образом содержать от примерно 1% до примерно 10% пестицида. Они могут быть использованы для обработки семян или для нанесения на листву с помощью аппарата для распыления.
Не менее эффективно использовать пестицид в виде раствора в соответствующем органическом растворителе, обычно в петролейном масле, таком как распылительные масла, которые широко используются в агрохимии.
Пестициды также могут быть использованы в форме аэрозольной композиции. В таких композициях пестицид растворяют или диспергируют в носителе, который представляет собой смесь под давлением с пропеллентом. Аэрозольная композиция упакована в контейнер, из которого смесь диспергируют через распылительный клапан.
Пестицидные приманки формируют тогда, когда пестицид смешивают с пищей или аттрактантом, или с ними обоими. Если вредители съедят приманку, то вместе с ней они съедят пестицид. Приманки могут иметь форму гранул, гелей, текучих порошков, жидкостей или твердых веществ. Они могут быть использованы в убежище вредителей.
Фумиганты представляют собой пестициды с относительно высоким давлением пара и, следовательно, могут существовать в виде газа в достаточных концентрациях для уничтожения вредителей в почве или в закрытых пространствах. Токсичность фумиганта пропорциональна его концентрации и времени экспозиции. Они характеризуются хорошей способностью к диффузии и действуют, проникая в дыхательную систему вредителя, или абсорбируются через кутикулу вредителя. Фумиганты используются для борьбы с амбарными вредителями хранилищ под газоконтрольными листами, в герметически закрытых помещениях или зданиях или в специальных камерах.
Пестициды могут быть микроинкапсулированы путем суспендирования частиц пестицидов или капель в пластиковых полимерах различного типа. Изменяя химический состав полимера или изменяя факторы процесса обработки, микрокапсулы могут быть получены различных размеров, с разной растворимостью, толщиной стенок и степенью проницаемости. Эти факторы определяют скорость, с которой активный ингредиент высвобождается, что, в свою очередь, влияет на остаточную производительность, скорость действия и запах продукта.
Растворы масляных концентратов получают путем растворения пестицида в растворителе, который сохраняет пестицид в растворе. Масляные растворы пестицида обычно обеспечивают быстрое обезвреживание и уничтожение вредителей по сравнению с другими составами благодаря тому, что сами растворители обладают пестицидным действием и растворяют восковое покрытие покровов, увеличивая скорость поглощения пестицида. Другие преимущества масляных растворов включают улучшенную стабильностью при хранении, лучшее проникновение в трещины, и лучшую адгезию к жирной поверхности.
Другим вариантом осуществления является эмульсия «масло-в-воде», где эмульсия содержит масляные глобулы, каждая из которых имеет пластинчатое жидкокристаллическое покрытие и диспергировано в водной фазе, где каждая масляная глобула содержит по меньшей мере одно соединение, которое является аграрно активным, и каждая покрыта моноламеллярным или олигопластинчатым слоем, содержащим: (1) по меньшей мере один неионный липофильный поверхностно-активный агент, (2) по меньшей мере один неионный гидрофильный поверхностно-активный агент и (3) по меньшей мере один ионный поверхностно-активный агент, где глобулы имеют средний диаметр частиц, равный менее 800 нм. Дополнительная информация об этом варианте осуществления дана в патентной публикации США 20070027034, опубликованной 1 февраля 2007, серийный номер патентной заявки 11/495228. Для упрощения, этот вариант осуществления будет называться "OIWE".
Для получения дополнительной информации см. “Insect Pest Management” 2nd Edition by D. Dent, авторское право CAB International (2000). Кроме того, для получения дополнительной информации см. “Handbook of Pest Control - The Behavior, Life History, и Control of Household Pests” Arnold Mallis, 9-е издание, авторское право 2004, GIE Media Inc.
ДРУГИЕ КОМПОНЕНТЫ СОСТАВОВ
Обычно, если в композиции используются соединения, представленные в формулах один, два и три, то такой состав может также содержать другие компоненты. Эти компоненты включают, но ими не ограничиваются, (список не является исчерпывающим и взаимоисключающим) смачивающие агенты, распределители, наклейки, проникающие агенты, буферы, пассиваторы, агенты, сокращающие дрейф, агенты совместимости, противопенные агенты, моющие агенты и эмульгаторы. Некоторые компоненты описаны ниже.
Смачивающий агент представляет собой вещество, которое при добавлении в жидкость увеличивает распределительную или проникающую способность жидкости за счет снижения межфазного натяжения между жидкостью и поверхностью, на которой она распределена. Смачивающие агенты используют для двух основных функций в агрохимических составах: во время обработки и получения для увеличения скорости смачивания порошков в воде с получением концентратов для растворимых жидкостей или концентратов суспензий; и во время смешивания продукта с водой в баке для опрыскивания для уменьшения времени смачивания смачивающихся порошков и улучшения проникновения воды в водно-диспергируемые гранулы. Примерами смачивающихся агентов, используемых в смачивающихся порошках, суспензионных концентратах и составов диспергируемых в воде гранул являются: натрий лаурилсульфат; натрий диоктилсульфосукцинат; алкилфенолэтоксилаты; и этоксилаты алифатических спиртов.
Диспергирующий агент представляет собой вещество, которое адсорбируется на поверхности частиц и помогает сохранить дисперсионное состояние частиц и предотвратить их повторную агрегацию. Диспергирующие агенты добавляют в агрохимические препараты для облегчения диспергирования и суспендирования в процессе получения, а также для повторного диспергирования частиц в воде в резервуаре опрыскивателя. Они широко используются в смачивающихся порошках, суспензионных концентратах и диспергируемых в воде гранулах. Поверхностно-активные вещества, используемые в качестве диспергирующих агентов, обладают способностью сильно адсорбироваться на поверхности частиц и обеспечивают заряд или стерический барьер против повторной агрегации частиц. Наиболее часто используемые поверхностно-активные вещества включают анионные и неионные вещества, или смеси этих двух типов. Для смачивающихся порошковых составов наиболее распространенным диспергирующим агентом является натрий лигносульфонаты. Для суспензионных концентратов хорошую адсорбцию и стабилизацию получают при использовании полиэлектролитов, таких как конденсаты формальдегида сульфоната нафталина натрия. Используются также тристирилфенол этоксилат фосфатные эфиры. Неионные вещества, такие как конденсаты алкиларилэтилена оксида и блок-сополимеры EO-PO, иногда сочетают с анионными веществами в качестве диспергирующих агентов для суспензионных концентратов. В последние годы в качестве диспергирующих агентов были разработаны новые типы высокомолекулярных полимерных поверхностно-активных веществ. Они имеют очень длинный гидрофобный «скелет» и большое количество цепей этиленоксида, образующих «зубья» «гребенки» поверхностно-активного агента. Эти высокомолекулярные полимеры могут обеспечить очень хорошую долгосрочную стабильность в суспензионных концентратах, так как гидрофобные скелеты могут иметь множество якорных участков на поверхности частиц. Примеры диспергирующих агентов, используемых в агрохимических составах, включают: лигносульфонаты натрия; конденсаты формальдегида сульфоната нафталина натрия; тристирилфенол этоксилат фосфатные эфиры; этоксилаты алифатических спиртов; алкилэтоксилаты; блок-сополимеры ЕО-РО; и привитые сополимеры.
Эмульгирующий агент представляет собой вещество, которое стабилизирует суспензию капель одной жидкой фазы в другой жидкой фазе. Без эмульгирующего агента две жидкости будут разделены на две несмешивающиеся жидкие фазы. Наиболее часто используемые эмульгирующие смеси содержат алкилфенол или алифатический спирт с двенадцатью или более этиленовыми звеньями оксида и растворимой в масле соли кальция додецилбензолсульфокислоты. Значения диапазона гидрофильно-липофильного баланса ("HLB"), равные от 8 до 18, как правило, обеспечивают хорошую стабильную эмульсию. Стабильность эмульсии иногда может быть улучшена путем добавления небольшого количества EO-РО-блок-сополимера поверхностно-активного вещества.
Солюбилизирующий агент представляет собой поверхностно-активное вещество, которое образовывает мицеллы в воде при концентрации выше критической концентрации мицелл. Мицеллы затем могут растворять или солюбилизировать нерастворимые в воде вещества внутри гидрофобной части мицеллы. Типы поверхностно-активных веществ, обычно используемые для солюбилизации, представляет собой неионные, сорбитановые моноолеаты, сорбитановые моноолеатные этоксилаты и метил олеатные эфиры.
Поверхностно-активные вещества иногда используют отдельно или вместе с другими добавками, такими как минеральные или растительные масла, в качестве адъювантов для смесей, распыляемых из бака, для улучшения биологической эффективности пестицида на целевом объекте. Тип поверхностно-активных веществ для улучшения биологической эффективности зависит в целом от природы и механизма действия пестицида. Однако они часто представляют собой неионные вещества, такие как: алкилэтоксилаты; этоксилаты линейных алифатических спиртов; этоксилаты алифатических аминов.
Носитель или разбавитель в сельскохозяйственной композиции представляет собой вещество, добавляемое в пестицид с получением продукта требуемой прочности. Носители, как правило, представляет собой вещества с высокой способность к поглощению, тогда как разбавители, как правило, представляют собой вещества с низкой способность к поглощению. Носители и разбавители используются в составах порошков, смачивающихся порошков, гранул и диспергируемых в воде гранул.
Органические растворители используются, главным образом, в составах эмульгируемых концентратов, эмульсиях «масло-в-вода», суспоэмульсиях и ультранизкообъемных составах, а также, в меньшей степени, в гранулированных составах. Иногда используют смеси растворителей. Первые основные группы растворителей представляют собой алифатические парафиновые масла, такие как керосин или рафинированные парафины. Вторая основная группа (и наиболее распространенная) включает ароматические растворители, такие как ксилол и высокомолекулярнные фракции С9 и С10 ароматических растворителей. Хлорированные углеводороды являются эффективными в качестве сорастворителей для предотвращения кристаллизации пестицидов, если состав эмульгируют в воде. В качестве сорастворителей иногда используют спирты для повышения мощности растворителя. Другие растворители могут включать растительные масла, масла семян растений и сложные эфиры растительных масел и масел семян.
Загустители или желирующие агенты используются, главным образом, в составах суспензионных концентратов, эмульсиях и суспоэмульсиях для изменения реологических свойств или свойств потока жидкости и для предотвращения отделения и осаждения диспергированных частиц или капелек. Загустители, желирующие и противо-оседающие агенты обычно можно разделить на две категории, а именно, на нерастворимые в воде частицы и водорастворимые полимеры. Можно получить составы суспензионных концентратов, используя глины и силикаты. Примеры таких типов веществ, включают, но ими не ограничиваются, монтмориллонит, бентонит, алюмосиликат магния и аттапульгит. Водорастворимые полисахариды используют в качестве утолщающих-гелеобразующих агентов на протяжении многих лет. Типы наиболее часто используемых полисахаридов представляет собой натуральные экстракты семян и морских водорослей или синтетические производные целлюлозы. Примеры таких типов веществ включают, но ими не ограничиваются, гуаровую камедь; камедь рожкового дерева; каррагенам; альгинаты; метилцеллюлозу; натрий карбоксиметилцеллюлозу (SCMC); гидроксиэтилцеллюлозу (HEC). Другие типы против-оседающих агентов основаны на модифицированных крахмалах, полиакрилатах, поливиниловом спирте и полиэтиленоксиде. Еще одним эффективным противооседающим агентом является ксантановая камедь.
Микроорганизмы могут вызывать порчу полученных составов. Поэтому для устранения или уменьшения их эффекта используют консерванты. Примеры таких агентов включают, но ими не ограничиваются: пропионовую кислоту и ее соль натрия; сорбиновую кислоту и ее соли натрия или калия; бензойную кислоту и ее соль натрия; соль натрия п-гидроксибензойной кислоты; метил п-гидроксибензоат; и 1,2-бензизотиазолин-3-он (BIT).
Наличие поверхностно-активных агентов часто приводит к тому, что составы на водной основе образуют пену на стадии смешивания при получении и при прохождении через резервуар опрыскивателя. Для уменьшения пенообразования часто добавляют противопенные агенты либо на стадии получения, либо перед заполнением бутылок. Обычно существует два типа противопенных агентов, а именно силиконы и несиликоны. Силиконы, как правило, представляет собой водные эмульсии диметилполисилоксана, в то время как несиликоновые противопенные агенты представляет собой нерастворимые в воде масла, такие как октанол и нонанол, или кремнезем. В обоих случаях функция противопенного агента представляет собой удаление поверхностно-активного агента от границы раздела воздух - вода.
«Зеленые» агенты (например, адъюванты, поверхностно-активные вещества, растворители) могут уменьшить загрязнение окружающей среды, наносимое составами для защиты растений. «Зеленые» агенты являются биологическими и их обычно получают из природных и/или не наносящих ущерба окружающей среде источников, например, растительных и животных источников. Конкретными примерами являются: растительные масла, масла семян и сложные эфиры, а также алкоксилированные алкилполиглюкозиды.
Для получения дополнительной информации см. “Chemistry and Technology of Agrochemical Formulations” под редакцией D.A. Knowles, авторское право 1998, Kluwer Academic Publishers. Также см. “Insecticides in Agriculture and Environment - Retrospects and Prospects” A.S. Perry, I. Yamamoto, I. Ishaaya и R. Perry, авторское право 1998, Springer-Verlag.
Вредители
В основном соединения формул один, два и три можно использовать для борьбы с вредителями, например, жуками, уховертами, тараканами, мухами, тлей, червецами, белокрылками, цикадками, муравьями, осами, термитами, мотыльками, бабочками, вшами, кузнечиками, саранчой, сверчками, блохами, трипсами, махилидами, различными клещами, нематодами и симфилами.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями Phyla Nematoda и/или Arthropoda.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями Subphyla Chelicerata, Myriapoda и/или Hexapoda.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями классов Arachnida, Symphyla и/или Insecta.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Anoplura. Неполный список конкретных родов включает, но ими не ограничивается, Haematopinus spp., Hoplopleura spp., Linognathus spp., Pediculus spp. и Pоlyplax spp. Неполный список конкретных видов включает, но ими не ограничивается, Haematopinus asini, Haematopinus suis, Linognathus setosus, Linognathus ovillus, Pediculus humanus capitis, Pediculus humanus humanus и Pthirus pubis.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Coleoptera. Неполный список конкретных родов включает, но ими не ограничивается, Acanthoscelides spp., Agriotes spp., Anthonomus spp., Apion spp., Apogonia spp., Aulacophora spp., Bruchus spp., Cerosterna spp., Cerotoma spp., Ceutorhynchus spp., Chaetocnema spp., Colaspis spp., Ctenicera spp., Curculio spp., Cyclocephala spp., Diabrotica spp., Hypera spp., Ips spp., Lyctus spp., Megascelis spp., Meligethes spp., Otiorhynchus spp., Pantomorus spp., Phyllophaga spp., Phyllotreta spp., Rhizotrogus spp., Rhynchites spp., Rhynchophorus spp., Scolytus spp., Sphenophorus spp., Sitophilus spp. и Tribolium spp. Неполный список конкретных видов включает, но ими не ограничивается, Acanthoscelides obtectus, Agrilus planipennis, Anoplophora glabripennis, Anthonomus grandis, Ataenius spretulus, Atomaria linearis, Bothynoderes punctiventris, Bruchus pisorum, Callosobruchus maculatus, Carpophilus hemipterus, Cassida vittata, Cerotoma trifurcata, Ceutorhynchus assimilis, Ceutorhynchus napi, Conoderus scalaris, Conoderus stigmosus, Conotrachelus nenuphar, Cotinis nitida, Crioceris asparagi, Cryptolestes ferrugineus, Cryptolestes pusillus, Cryptolestes turcicus, Cylindrocopturus adspersus, Deporaus marginatus, Dermestes lardarius, Dermestes maculatus, Epilachna varivestis, Faustinus cubae, Hylobius pales, Hypera postica, Hypothenemus hampei, Lasioderma serricorne, Leptinotarsa decemlineata, Liogenys fuscus, Liogenys suturalis, Lissorhoptrus oryzophilus, Maecolaspis joliveti, Melanotus communis, Meligethes aeneus, Melolontha melolontha, Oberea brevis, Oberea linearis, Oryctes rhinoceros, Oryzaephilus mercator, Oryzaephilus surinamensis, Oulema melanopus, Oulema oryzae, Phyllophaga cuyabana, Popillia japonica, Prostephanus truncatus, Rhyzopertha dominica, Sitona lineatus, Sitophilus granarius, Sitophilus oryzae, Sitophilus zeamais, Stegobium paniceum, Tribolium castaneum, Tribolium confusum, Trogoderma variabile и Zabrus tenebrioides.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Dermaptera.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Blattaria. Неполный список конкретных видов включает, но ими не ограничивается, Blattella germanica, Blatta orientalis, Parcoblatta pennsylvanica, Periplaneta americana, Periplaneta australasiae, Periplaneta brunnea, Periplaneta fuliginosa, Pycnoscelus surinamensis и Supella longipalpa.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Diptera. Неполный список конкретных родов включает, но ими не ограничивается, Aedes spp., Agromyza spp., Anastrepha spp., Anopheles spp., Bactrocera spp., Ceratitis spp., Chrysops spp., Cochliomyia spp., Contarinia spp., Culex spp., Dasineura spp., Delia spp., Drosophila spp., Fannia spp., Hylemyia spp., Liriomyza spp., Musca spp., Phorbia spp., Tabanus spp. и Tipula spp. Неполный список конкретных видов включает, но ими не ограничивается, Agromyza frontella, Anastrepha suspensa, Anastrepha ludens, Anastrepha obliqa, Bactrocera cucurbitae, Bactrocera dorsalis, Bactrocera invadens, Bactrocera zonata, Ceratitis capitata, Dasineura brassicae, Delia platura, Fannia canicularis, Fannia scalaris, Gasterophilus intestinalis, Gracillia perseae, Haematobia irritans, Hypoderma lineatum, Liriomyza brassicae, Melophagus ovinus, Musca autumnalis, Musca domestica, Oestrus ovis, Oscinella frit, Pegomya betae, Psila rosae, Rhagoletis cerasi, Rhagoletis pomonella, Rhagoletis mendax, Sitodiplosis mosellana и Stomoxys calcitrans.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Hemiptera. Неполный список конкретных родов включает, но ими не ограничивается, Adelges spp., Aulacaspis spp., Aphrophora spp., Aphis spp., Bemisia spp., Ceroplastes spp., Chionaspis spp., Chrysomphalus spp., Coccus spp., Empoasca spp., Lepidosaphes spp., Lagynotomus spp., Lygus spp., Macrosiphum spp., Nephotettix spp., Nezara spp., Philaenus spp., Phytocoris spp., Piezodorus spp., Planococcus spp., Pseudococcus spp., Rhopalosiphum spp., Saissetia spp., Therioaphis spp., Toumeyella spp., Toxoptera spp., Trialeurodes spp., Triatoma spp. и Unaspis spp. Неполный список конкретных видов включает, но ими не ограничивается, Acrosternum hilare, Acyrthosiphon pisum, Aleyrodes proletella, Aleurodicus dispersus, Aleurothrixus floccosus, Amrasca biguttula biguttula, Aonidiella aurantii, Aphis gossypii, Aphis glycines, Aphis pomi, Aulacorthum solani, Bemisia argentifolii, Bemisia tabaci, Blissus leucopterus, Brachycorynella asparagi, Brevennia rehi, Brevicoryne brassicae, Calocoris norvegicus, Ceroplastes rubens, Cimex hemipterus, Cimex lectularius, Dagbertus fasciatus, Dichelops furcatus, Diuraphis noxia, Diaphorina citri, Dysaphis plantaginea, Dysdercus suturellus, Edessa meditabunda, Eriosoma lanigerum, Eurygaster maura, Euschistus heros, Euschistus servus, Helopeltis antonii, Helopeltis theivora, Icerya purchasi, Idioscopus nitidulus, Laodelphax striatellus, Leptocorisa oratorius, Leptocorisa varicornis, Lygus hesperus, Maconellicoccus hirsutus, Macrosiphum euphorbiae, Macrosiphum granarium, Macrosiphum rosae, Macrosteles quadrilineatus, Mahanarva frimbiolata, Metopolophium dirhodum, Mictis longicornis, Myzus persicae, Nephotettix cinctipes, Neurocolpus longirostris, Nezara viridula, Nilaparvata lugens, Parlatoria pergandii, Parlatoria ziziphi, Peregrinus maidis, Phylloxera vitifoliae, Physokermes piceae, Phytocoris californicus, Phytocoris relativus, Piezodorus guildinii, Poecilocapsus lineatus, Psallus vaccinicola, Pseudacysta perseae, Pseudococcus brevipes, Quadraspidiotus perniciosus, Rhopalosiphum maidis, Rhopalosiphum padi, Saissetia oleae, Scaptocoris castanea, Schizaphis graminum, Sitobion avenae, Sogatella furcifera, Trialeurodes vaporariorum, Trialeurodes abutiloneus, Unaspis yanonensis и Zulia entrerriana.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Hymenoptera. Неполный список конкретных родов включает, но ими не ограничивается, Acromyrmex spp., Atta spp., Camponotus spp., Diprion spp., Formica spp., Monomorium spp., Neodiprion spp., Pogonomyrmex spp., Polistes spp., Solenopsis spp., Vespula spp. и Xylocopa spp. Неполный список конкретных видов включает, но ими не ограничивается, Athalia rosae, Atta texana, Iridomyrmex humilis, Monomorium minimum, Monomorium pharaonis, Solenopsis invicta, Solenopsis geminata, Solenopsis molesta, Solenopsis richtery, Solenopsis xyloni и Tapinoma sessile.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Isoptera. Неполный список конкретных родов включает, но ими не ограничивается, Coptotermes spp., Cornitermes spp., Cryptotermes spp., Heterotermes spp., Kalotermes spp., Incisitermes spp., Macrotermes spp., Marginitermes spp., Microcerotermes spp., Procornitermes spp., Reticulitermes spp., Schedorhinotermes spp., и Zootermopsis spp. Неполный список конкретных видов включает, но ими не ограничивается, Coptotermes curvignathus, Coptotermes frenchi, Coptotermes formosanus, Heterotermes aureus, Microtermes obesi, Reticulitermes banyulensis, Reticulitermes grassei, Reticulitermes flavipes, Reticulitermes hageni, Reticulitermes hesperus, Reticulitermes santonensis, Reticulitermes speratus, Reticulitermes tibialis и Reticulitermes virginicus.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Lepidoptera. Неполный список конкретных родов включает, но ими не ограничивается, Adoxophyes spp., Agrotis spp., Argyrotaenia spp., Cacoecia spp., Caloptilia spp., Chilo spp., Chrysodeixis spp., Colias spp., Crambus spp., Diaphania spp., Diatraea spp., Earias spp., Ephestia spp., Epimecis spp., Feltia spp., Gortyna spp., Helicoverpa spp., Heliothis spp., Indarbela spp., Lithocolletis spp., Loxagrotis spp., Malacosoma spp., Peridroma spp., Phyllonorycter spp., Pseudaletia spp., Sesamia spp., Spodoptera spp., Synanthedon spp. и Yponomeuta spp. Неполный список конкретных видов включает, но ими не ограничивается, Achaea janata, Adoxophyes orana, Agrotis ipsilon, Alabama argillacea, Amorbia cuneana, Amyelois transitella, Anacamptodes defectaria, Anarsia lineatella, Anomis sabulifera, Anticarsia gemmatalis, Archips argyrospila, Archips rosana, Argyrotaenia citrana, Autographa gamma, Bonagota cranaodes, Borbo cinnara, Bucculatrix thurberiella, Capua reticulana, Carposina niponensis, Chlumetia transversa, Choristoneura rosaceana, Cnaphalocrocis medinalis, Conopomorpha cramerella, Cossus cossus, Cydia caryana, Cydia funebrana, Cydia molesta, Cydia nigricana, Cydia pomonella, Darna diducta, Diatraea saccharalis, Diatraea grandiosella, Earias insulana, Earias vittella, Ecdytolopha aurantianum, Elasmopalpus lignosellus, Ephestia cautella, Ephestia elutella, Ephestia kuehniella, Epinotia aporema, Epiphyas postvittana, Erionota thrax, Eupoecilia ambiguella, Euxoa auxiliaris, Grapholita molesta, Hedylepta indicata, Helicoverpa armigera, Helicoverpa zea, Heliothis virescens, Hellula undalis, Keiferia lycopersicella, Leucinodes orbonalis, Leucoptera coffeella, Leucoptera malifoliella, Lobesia botrana, Loxagrotis albicosta, Lymantria dispar, Lyonetia clerkella, Mahasena corbetti, Mamestra brassicae, Maruca testulalis, Metisa plana, Mythimna unipuncta, Neoleucinodes elegantalis, Nymphula depunctalis, Operophtera brumata, Ostrinia nubilalis, Oxydia vesulia, Pandemis cerasana, Pandemis heparana, Papilio demodocus, Pectinophora gossypiella, Peridroma saucia, Perileucoptera coffeella, Phthorimaea operculella, Phyllocnistis citrella, Pieris rapae, Plathypena scabra, Plodia interpunctella, Plutella xylostella, Polychrosis viteana, Prays endocarpa, Prays oleae, Pseudaletia unipuncta, Pseudoplusia includens, Rachiplusia nu, Scirpophaga incertulas, Sesamia inferens, Sesamia nonagrioides, Setora nitens, Sitotroga cerealella, Sparganothis pilleriana, Spodoptera exigua, Spodoptera frugiperda, Spodoptera eridania, Thecla basilides, Tineola bisselliella, Trichoplusia ni, Tuta absoluta, Zeuzera coffeae и Zeuzera pyrina.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Mallophaga. Неполный список конкретных родов включает, но ими не ограничивается, Anaticola spp., Bovicola spp., Chelopistes spp., Goniodes spp., Menacanthus spp. и Trichodectes spp. Неполный список конкретных видов включает, но ими не ограничивается, Bovicola bovis, Bovicola caprae, Bovicola ovis, Chelopistes meleagridis, Goniodes dissimilis, Goniodes gigas, Menacanthus stramineus, Menopon gallinae и Trichodectes canis.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Orthoptera. Неполный список конкретных родов включает, но ими не ограничивается, Melanoplus spp., и Pterophylla spp. Неполный список конкретных видов включает, но ими не ограничивается, Anabrus simplex, Gryllotalpa africana, Gryllotalpa australis, Gryllotalpa brachyptera, Gryllotalpa hexadactyla, Locusta migratoria, Microcentrum retinerve, Schistocerca gregaria и Scudderia furcata.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Siphonaptera. Неполный список конкретных видов включает, но ими не ограничивается, Ceratophyllus gallinae, Ceratophyllus niger, Ctenocephalides canis, Ctenocephalides felis и Pulex irritans.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Thysanoptera. Неполный список конкретных родов включает, но ими не ограничивается, Caliothrips spp., Frankliniella spp., Scirtothrips spp. и Thrips spp. Неполный список конкретных видов включает, но ими не ограничивается, Frankliniella fusca, Frankliniella occidentalis, Frankliniella schultzei, Frankliniella williamsi, Heliothrips haemorrhoidalis, Rhipiphorothrips cruentatus, Scirtothrips citri, Scirtothrips dorsalis, и Taeniothrips rhopalantennalis, Thrips hawaiiensis, Thrips nigropilosus, Thrips orientalis, Thrips tabaci.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Thysanura. Неполный список конкретных родов включает, но ими не ограничивается, Lepisma spp. и Thermobia spp.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Acarina. Неполный список конкретных родов включает, но ими не ограничивается, Acarus spp., Aculops spp., Boophilus spp., Demodex spp., Dermacentor spp., Epitrimerus spp., Eriophyes spp., Ixodes spp., Oligonychus spp., Panonychus spp., Rhizoglyphus spp. и Tetranychus spp. Неполный список конкретных видов включает, но ими не ограничивается, Acarapis woodi, Acarus siro, Aceria mangiferae, Aculops lycopersici, Aculus pelekassi, Aculus schlechtendali, Amblyomma americanum, Brevipalpus obovatus, Brevipalpus phoenicis, Dermacentor variabilis, Dermatophagoides pteronyssinus, Eotetranychus carpini, Notoedres cati, Oligonychus coffeae, Oligonychus ilicis, Panonychus citri, Panonychus ulmi, Phyllocoptruta oleivora, Polyphagotarsonemus latus, Rhipicephalus sanguineus, Sarcoptes scabiei, Tegolophus perseaflorae, Tetranychus urticae и Varroa destructor.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями отряда Symphyla. Неполный список конкретных видов включает, но ими не ограничивается, Scutigerella immaculata.
В другом варианте осуществления соединения формул один, два и три можно использовать для борьбы с вредителями Phylum Nematoda. Неполный список конкретных родов включает, но ими не ограничивается, Aphelenchoides spp., Belonolaimus spp., Criconemella spp., Ditylenchus spp., Heterodera spp., Hirschmanniella spp., Hoplolaimus spp., Meloidogyne spp., Pratylenchus spp. и Radopholus spp. Неполный список конкретных видов включает, но ими не ограничивается, Dirofilaria immitis, Heterodera zeae, Meloidogyne incognita, Meloidogyne javanica, Onchocerca volvulus, Radopholus similis и Rotylenchulus reniformis.
Дополнительная информация приведена в «HANDBOOK OF PEST CONTROL - THE BEHAVIOR, LIFE HISTORY, AND CONTROL OF HOUSEHOLD PESTS» Arnold Mallis, 9-е издание, авторское право 2004, GIE Media Inc.
ПРИМЕНЕНИЕ
Соединения формул один, два и три обычно используют в количестве, составляющем приблизительно от 0,01 грамм на гектар до приблизительно 5000 грамм на гектар для борьбы с вредителями. Количество, равное приблизительно от 0,1 грамм на гектар до приблизительно 500 грамм на гектар, является, как правило, предпочтительным, а количество, равное приблизительно от 1 грамма на гектар до приблизительно 50 грамм на гектар, является, как правило, еще более предпочтительным.
Место, где может использоваться соединение формулы один, два и три, может быть любым местом, населенным вредителями (может быть либо заселена, либо быть пересеченной местностью), например: местом роста культур, деревьев, фруктов, круп, кормовых видов растений, винограда, торфа и декоративных растений; местом проживания домашних животных; внутренним помещением здания или его внешней поверхностью (например, местом хранения зерна), материалами конструкций, используемыми при строительстве (например, пропитанной древесиной), а также почвой вокруг зданий. Конкретные посевные площади для использования соединений формулы один включают территории роста яблок, кукурузы, подсолнечника, хлопка, соевых бобов, канола, пшеницы, риса, сорго, ячменя, овса, картофеля, апельсинов, люцерны, салата, клубники, помидоров, перца, крестоцветных, груш, табака, миндаля, сахарной свеклы, бобов и других ценных культур или территории посадки их семян. Также эффективно использовать сульфат алюминия вместе с соединением формулы один при выращивании различных растений.
Борьба с вредителями/паразитами, как правило, обозначает, что их популяция, активность или то и другое снижаются в этом месте. Это может произойти, если: популяция вредителей отказалась от этого места; если вредители поражены в месте или вокруг нее; или если вредители уничтожены, целиком или частично, на участке или вокруг него. Конечно, эти результаты могут сочетаться. Как правило, популяции вредителей, их активность, или то и другое, желательно сократить более чем на пятьдесят процентов, предпочтительно, более чем на 90 процентов. Как правило, соединение не применяется вовнутрь человека или наружно у человека; таким образом, локус, как правило, не относится к человеку.
Соединения формул один, два и три можно использовать в смеси, используя одновременно или последовательно, самостоятельно или вместе с другими соединениями для улучшения интенсивности прорастания (например, роста более сильной корневой системы для того, чтобы лучше противостоять стрессовым условиями выращивания). Такие другие соединения представляют собой, например, соединения, которые модулируют этиленовые рецепторы растений, в частности, 1-метилциклопропен (также известен как 1-MCP).
Соединения формул один, два и три можно использовать на внекорневой и плодовых частях растений для борьбы с вредителями. Соединения либо находятся в прямом контакте с вредителем, либо вредитель будет потреблять пестицид при пожирании листьев, фруктов или при высасывании нектара, который содержит пестицид. Соединения формул один, два и три также могут быть нанесены на почву, и при таком их использовании можно осуществлять борьбу с вредителями, пожирающими корни и стебли. Корни могут абсорбировать соединения, перенося их в лиственную часть растения, обеспечивая борьбу с вредителями, пожирающими растение выше земли и сосущими нектар.
Что касается приманок, то приманки, как правило, помещают в землю, в то место, например, где термиты могут контактировать с ней и/или где они их привлекают. Приманки также можно использовать на поверхности здания (горизонтальные, вертикальные или наклонные поверхности), где, например, муравьи, термиты, тараканы и мухи могут контактировать с ней и/или где приманка их привлекает. Приманки могут содержать соединение формулы один, два или три.
Соединения формул один, два и три могут находиться внутри капсулы или нанесены на ее поверхность. Размер капсул может изменяться от нанометрового размера (около 100-900 нанометров в диаметре) до микрометрового размера (около 10-900 мкм в диаметре).
Из-за уникальной способности яиц некоторых вредителей быть устойчивыми к определенным пестицидам может быть желательно повторное применение соединений формул один, два или три для борьбы с вновь возникшими личинками.
Системное движение пестицидов в растениях можно использовать для борьбы с вредителями на одной части растения, нанося (например, распылением на область) соединения формул один, два или три на другую часть растения. Например, уничтожение насекомых, питающихся листьями, может быть достигнуто путем капельного орошения или нанесения в борозду, путем обработки почвы, например, путем орошения почвы перед или после посадки, или путем обработки семян растения перед посадкой.
Обработка семян может быть применена ко всем типам семян, в том числе, к генетически модифицированным растениям, экспрессирующим особенные признаки при прорастании. Характерные примеры включают примеры экспрессии белков, токсичных для беспозвоночных вредителей, таких как Bacillus thuringiensis или других инсектицидных токсинов, примеры проявляющих устойчивость к гербицидам, например, семена "Roundup Ready", или примеры с "многоуровневыми" чужеродными генами, экспрессирующими инсектицидные токсины, с устойчивостью к гербицидам, с повышенным питанием, засухоустойчивостью или любыми другими полезными свойствами. Кроме того, такие обработки семян соединениями формулы один, два или три могут дополнительно повысить способность растения быть более устойчивым к стрессовым условиям выращивания. Это дает более здоровое, более активное растение, что может повысить урожайность во время его сбора. Как правило, как полагают, что значимое преимущество будет достигнуто при количестве соединения формулы один, два или три, равном от около 1 г до около 500 граммов на 100000 семян, как полагают, более значимое преимущество будет при количестве от около 10 г до около 100 граммов на 100000 семян, и, как полагают, еще более значимое преимущество будет при количестве от 25 г до около 75 г на 100000 семян.
Должно быть очевидно, что соединения формул один, два и три могут быть использованы на, в или вокруг генетически модифицированных растений, экспрессирующих особенные признаки, такие как экспрессия токсинов против Bacillus thuringiensis или других инсектицидных токсинов, или растений, которые обладают устойчивостью к гербицидам, или растений с "многоуровневыми" чужеродными генами, экспрессирующими инсектицидные токсины, с устойчивостью к гербицидам, с повышенным питанием или любыми другими положительными свойствами.
Соединения формул один, два и три могут быть использованы для борьбы с эндопаразитами и эктопаразитами в области ветеринарной медицины или в области разведения и содержания животных, исключая человека. Соединения формул один, два и три, например, при пероральном введении используют в форме, например, таблеток, капсул, напитков, гранул, при нанесении на кожу используют в форме, например, пропитки, выливания, орошения и распыления, и при парентеральном введении используют в форме, например, инъекции.
Соединения формул один, два и три могут быть также использованы преимущественно при содержании домашнего скота, например, крупного рогатого скота, овец, свиней, кур и гусей. Они также могут использоваться, преимущественно, для животных, таких как лошади, собаки и кошки. Конкретными паразитами, на которые направлена борьба, могут быть блохи и клещи, которые беспокоят таких животных. Подходящие составы вводят перорально животным с питьевой водой или кормом. Подходящие дозы и составы зависят от вида.
Соединения формул один, два и три могут быть также использованы для борьбы с паразитирующими червями, особенно, в кишечнике, у животных, перечисленных выше.
Соединения формул одни, два и три также могут быть использованы в терапевтических методах здравоохранения человека. Такие методы включают, но ими не ограничиваются, пероральное введение в виде, например, таблеток, капсул, напитков, гранул, и нанесение на кожу.
Вредители по всему миру стали мигрировать в новые условия (для такого вредителя), и, следовательно, появляются новые инвазивные виды в такой новой среде. Соединения формул один и два также могут быть использованы в отношении таких новых инвазивных видов для борьбы с ними в такой новой среде.
Соединения формулы один, два и три также могут быть использованы в области, где происходит рост растений, например, культурных растений (например, перед посадкой, при посадке, перед сбором урожая) и где имеются низкие уровни (даже фактически отсутствуют) вредителей, которые наносят коммерческий урон таким растениям. Использование таких соединений в такой области предназначено для положительного влияния на рост растений в такой области. Такое положительное влияние может включать, но ими не ограничивается, улучшение здоровья растения, улучшение урожайности растения (например, увеличение биомассы и/или повышение содержания ценных компонентов), улучшение активности растения (например, улучшение роста и/или озеленения), улучшение качества растения (например, улучшение компонентов или состава определенных ингредиентов), а также улучшение толерантности к абиотическому и/или биотическому стрессу растения.
Перед использованием или коммерческой продажей пестицида, такой пестицид подвергают длительному процессу оценки в различных государственных органах (местных, региональных, государственных, национальных и международных). Большое количество требований в отношении данных определено регулирующими органами и требования удовлетворяются путем получения и предоставления данных лицом, подающим заявление о регистрации продукта, или третьей стороной от имени лица, подающего заявление о регистрации продукта, как правило, с помощью компьютера при подключении к интернету. Эти государственные органы затем анализируют такие данные и, в случае, если установлена их безопасность, то выдают для потенциального пользователя или продавца согласие на регистрацию продукта. После этого, на территории, где выдано разрешение на регистрацию продукта и где он защищен, такой пользователь или продавец может использовать или продать такой пестицид.
Соединение формулы один, два и три может быть тестировано для определения его эффективности в отношении вредителей. Кроме того, можно провести исследования способа действия для определения того, имеет ли указанное соединение способ действия, отличающийся от других пестицидов. После этого, такие полученные данные могут быть распространены, например, через интернет, третьим лицам.
Заголовки в настоящем документе сделаны только для удобства и не должны быть использованы для толкования какой-либо его части.
РАЗДЕЛ ТАБЛИЦЫ
Структуры соединений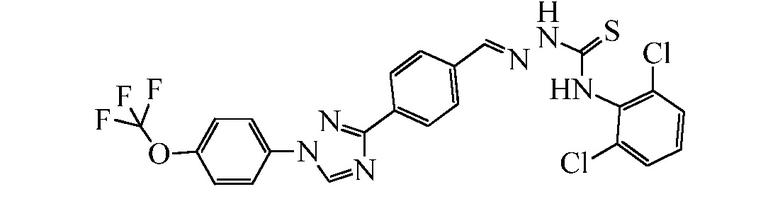
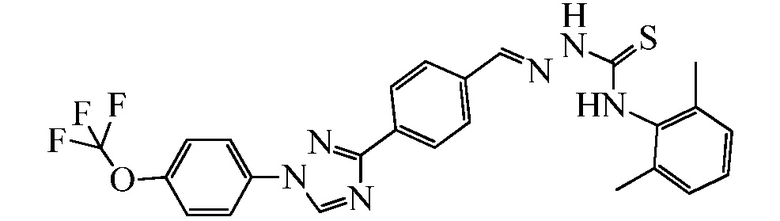
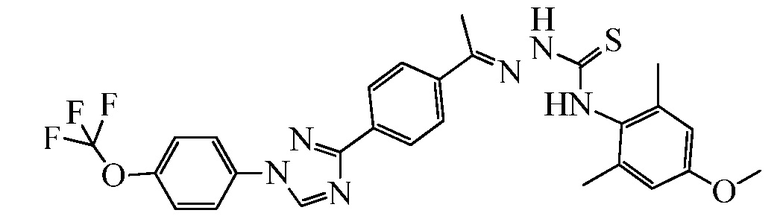
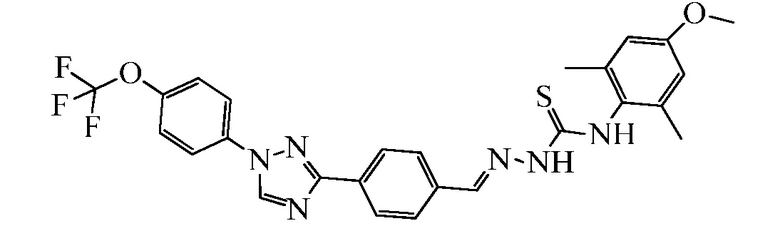
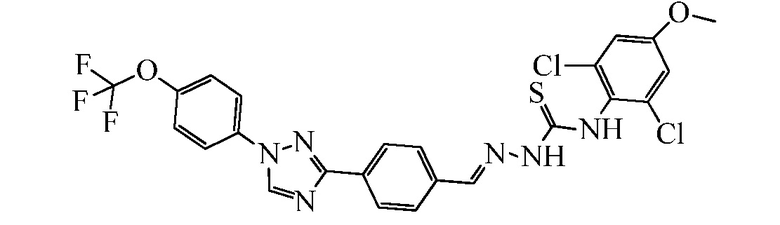
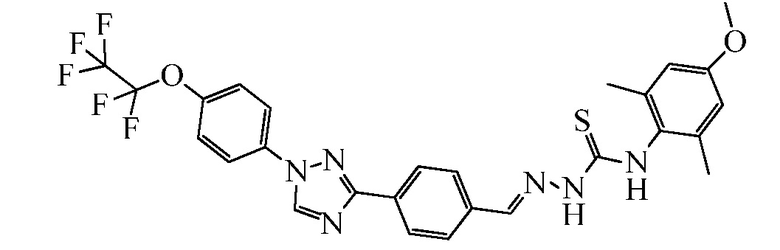
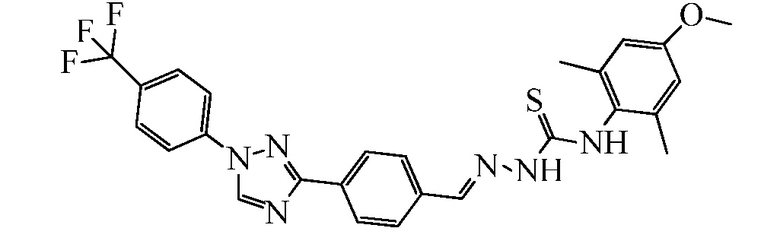
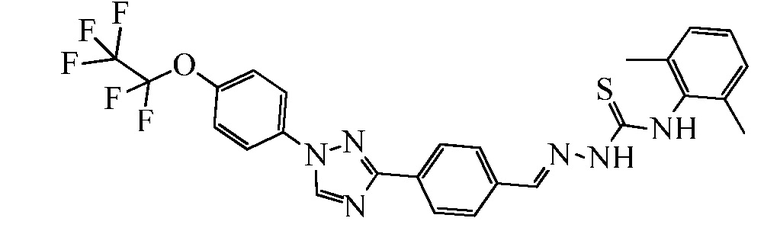
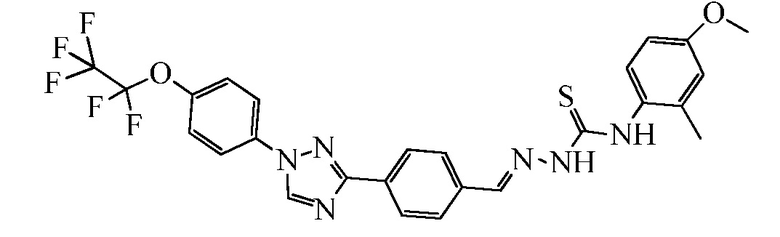
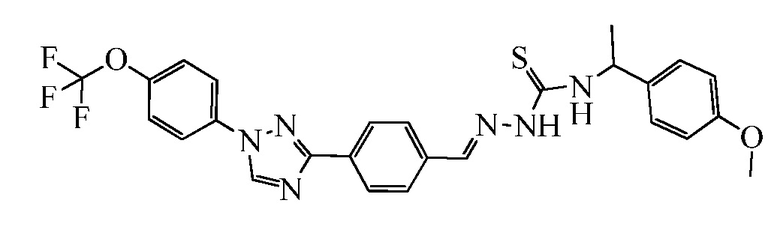
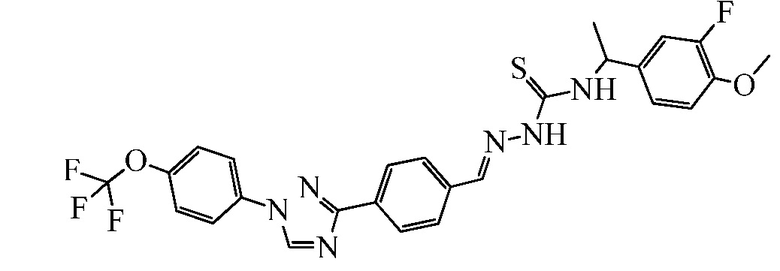
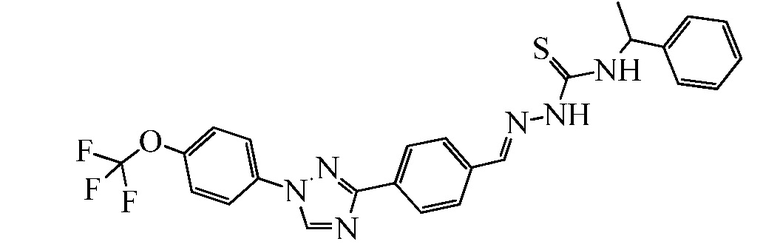
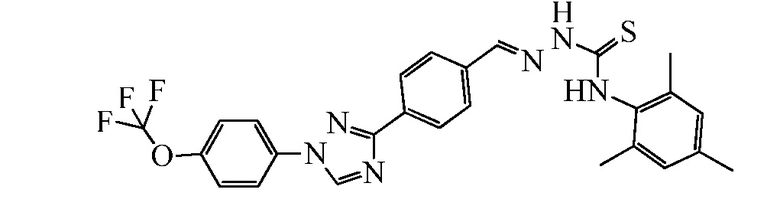
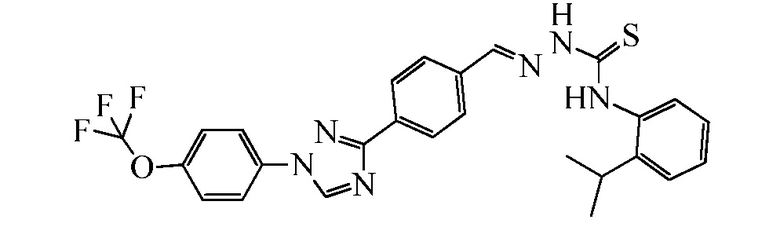
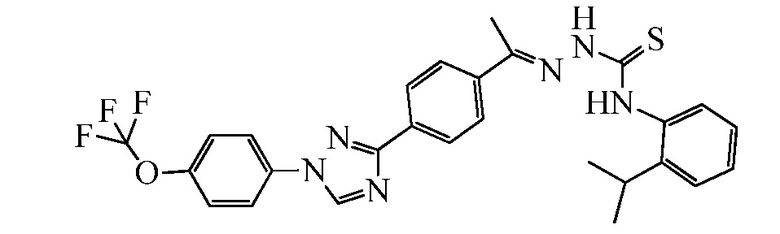
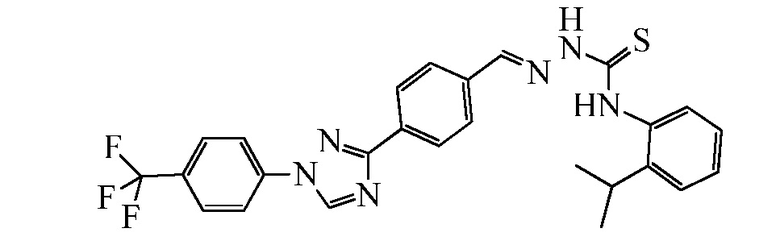
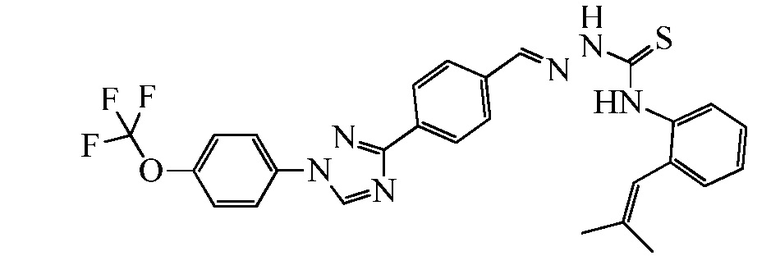
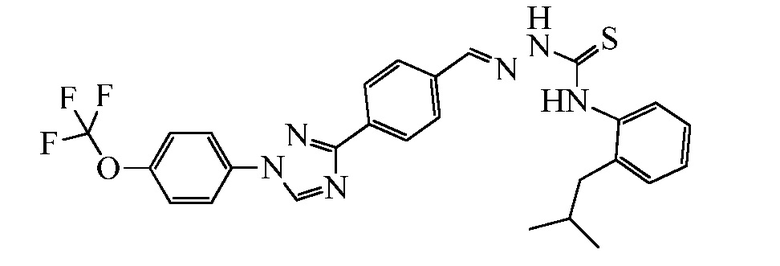
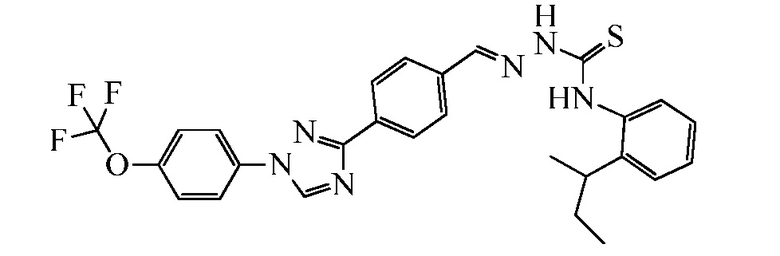
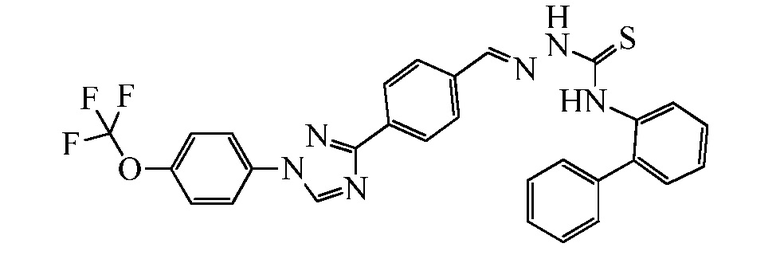
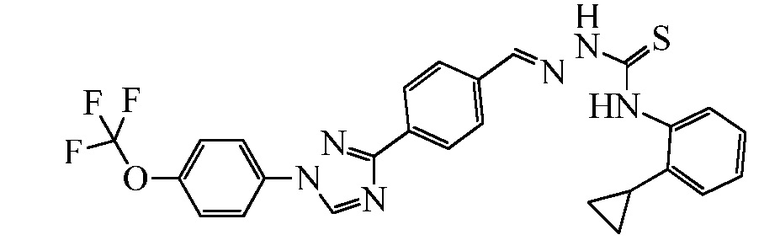
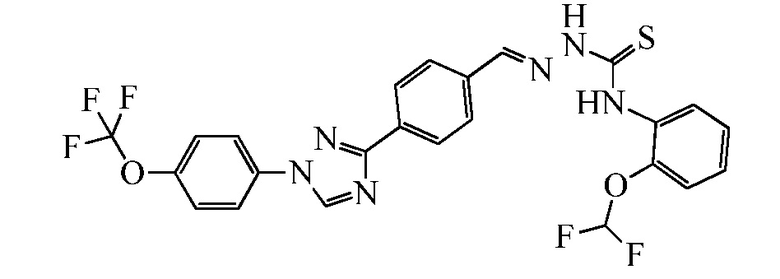
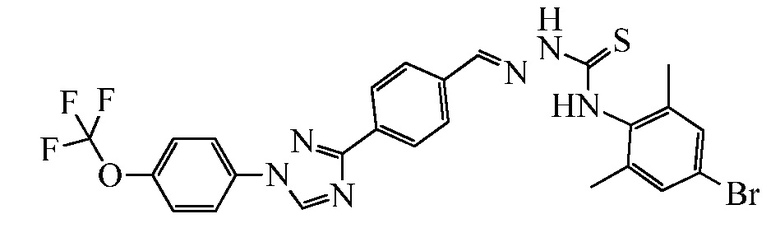
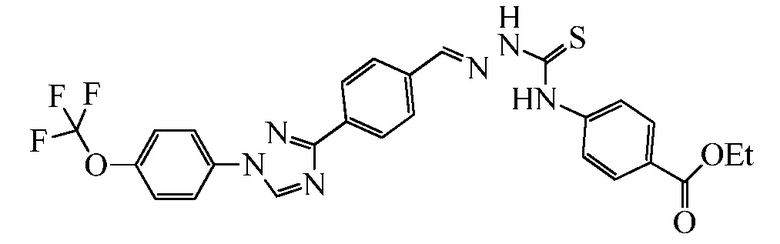
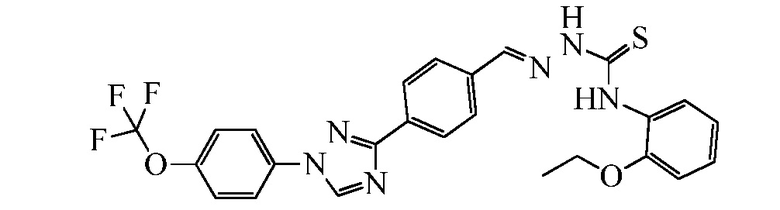
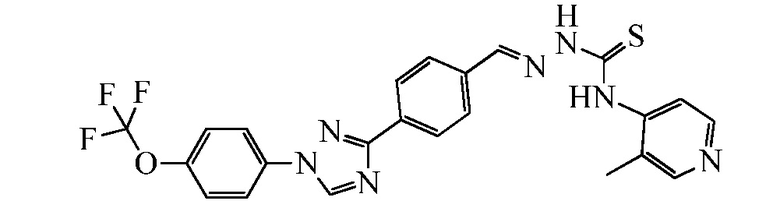
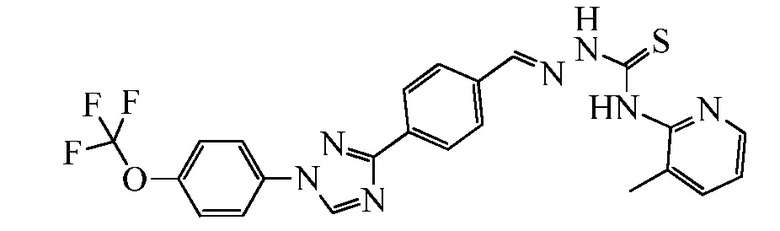
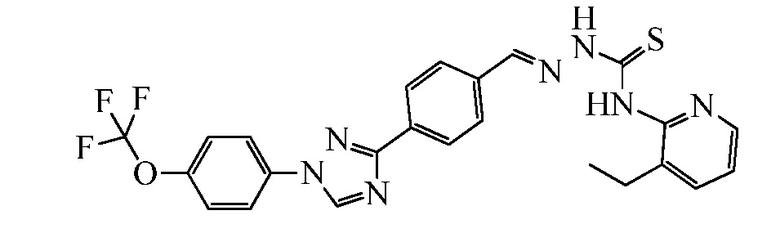
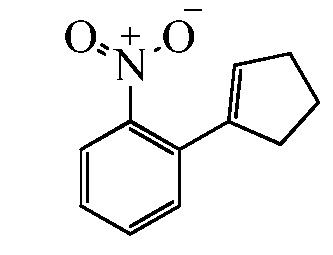
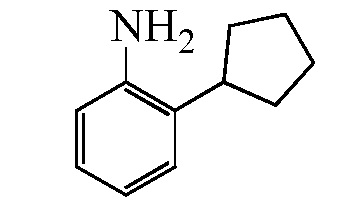
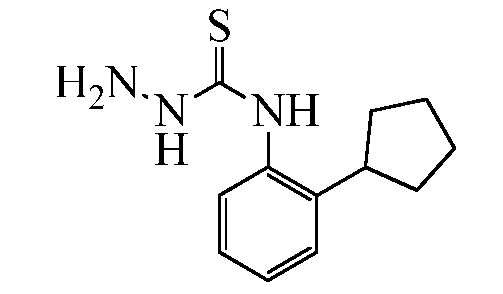
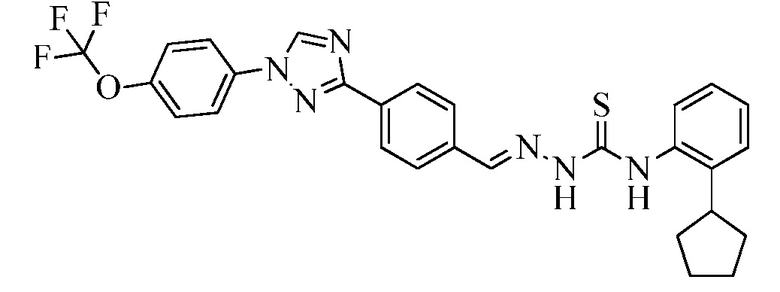
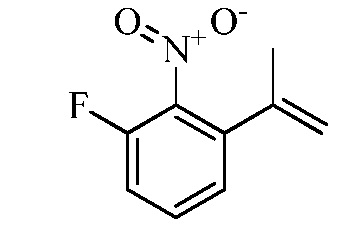
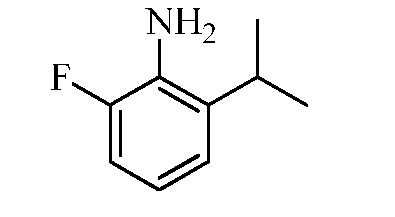
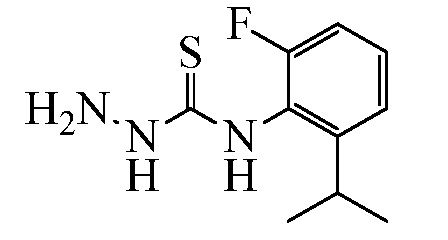
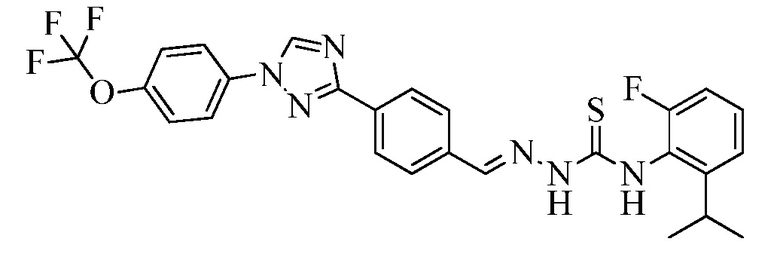
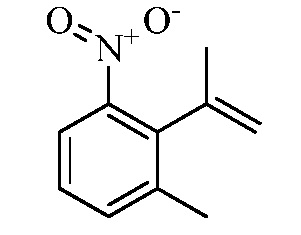
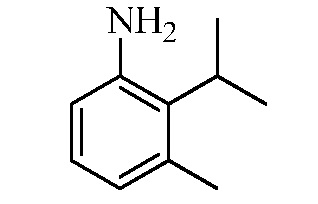
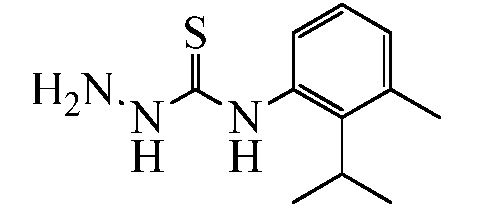
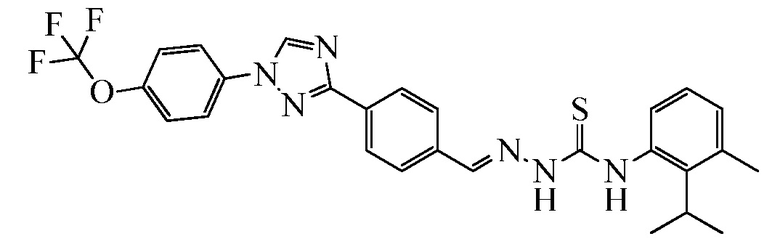
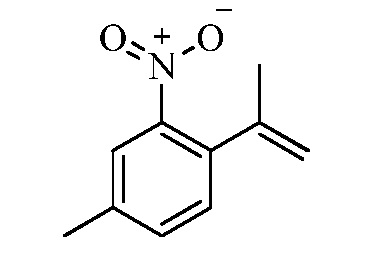
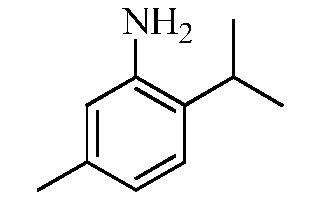
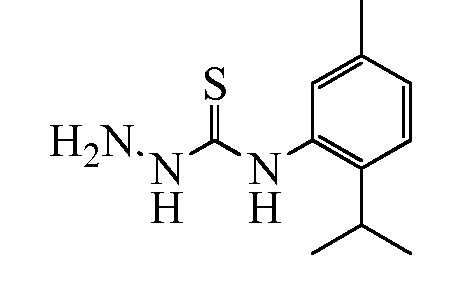
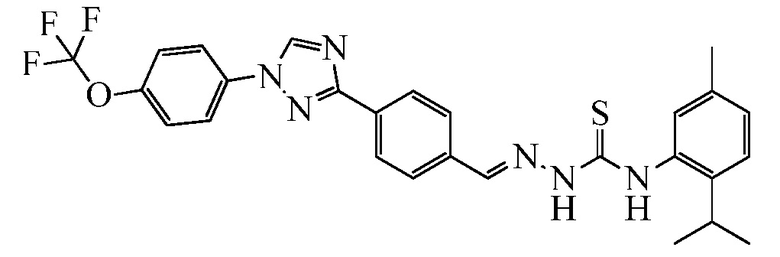
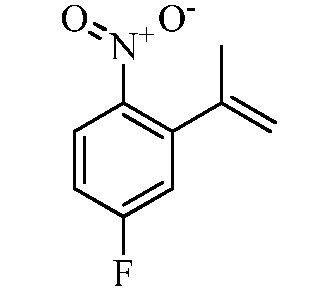
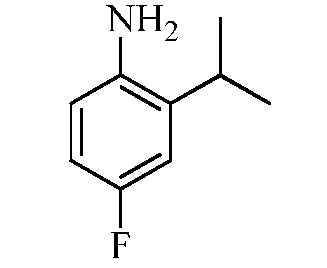
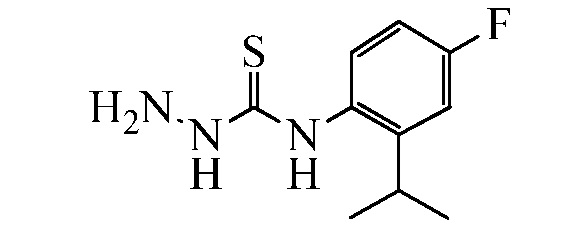
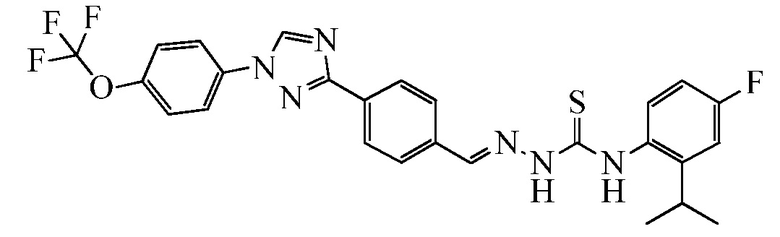
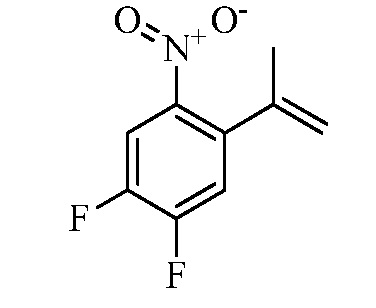
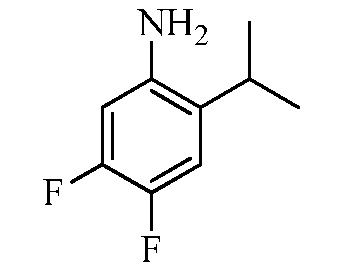
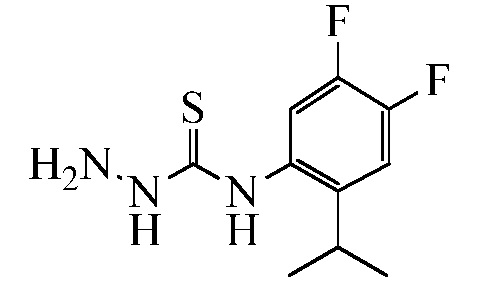
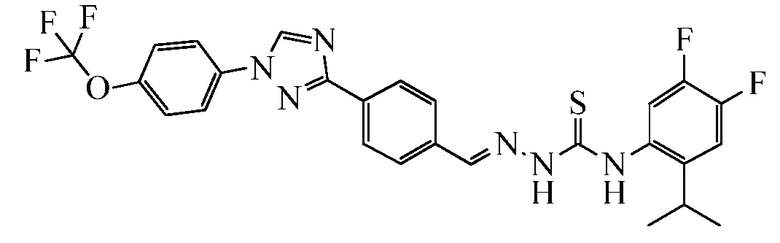
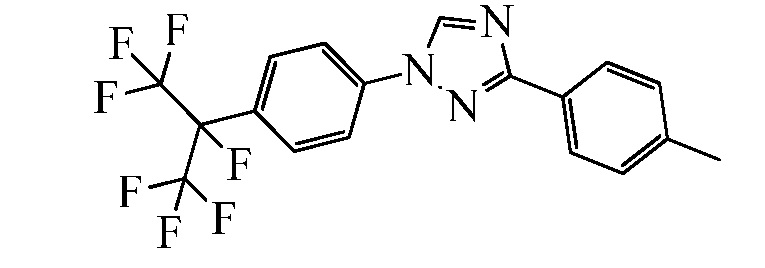
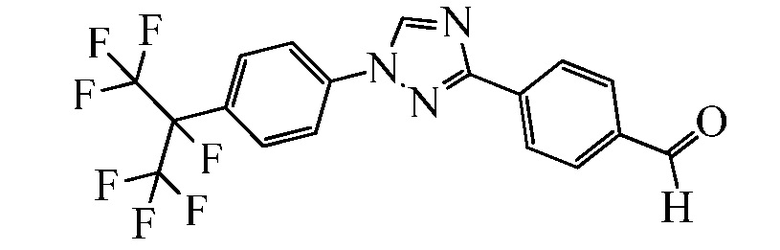
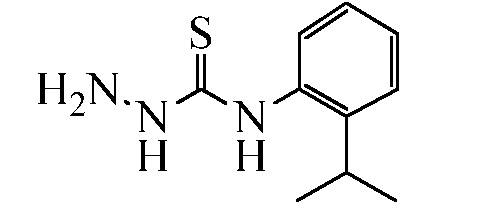
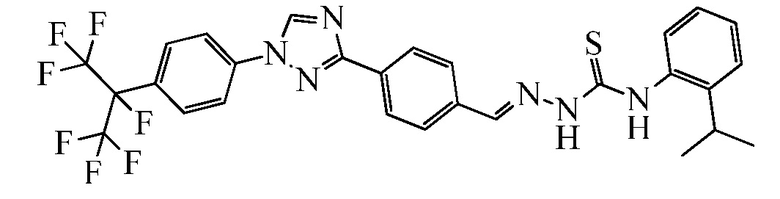
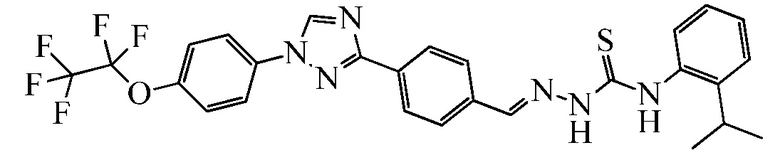
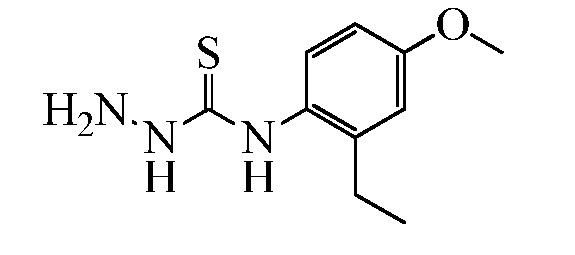
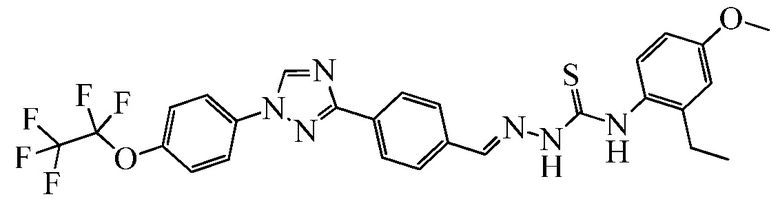
Аналитические данные для соединений в таблице 1
(M+1)
13C ЯМР (101 МГц, CDCl3) δ 148,77, 139,96, 133,58, 132,08, 130,87, 130,52, 127,55, 123,70, 35,31, 33,49, 24,05
13C ЯМР (101 МГц, CDCl3) δ 144,12, 130,34, 126,51, 125,95, 118,78, 115,70, 39,89, 32,17, 25,21
13C ЯМР (101 МГц, CDCl3) δ 153,56 (д, JCF=257,5 Гц), 139,62, 139,60, 138,83, 131,48 (д, JCF=8,6 Гц), 124,47 (д, JCF=3,6 Гц), 117,60, 115,51 (д, JCF=19,1 Гц), 23,18
13C ЯМР (101 МГц, CDCl3) δ 151,91 (д, J=237,6 Гц), 135,10 (д, J=2,3 Гц), 131,60 (д, J=11,8 Гц), 120,52 (д, J=3,0 Гц), 117,99 (д, J=8,0 Гц), 112,28 (д, J=19,6 Гц), 27,77 (д, J=2,9 Гц), 22,22
([M+H]+)
13C ЯМР (101 МГц, CDCl3) δ 160,96 (д, J=250,8 Гц), 148,46, 141,88, 135,18 (д, J=4,1 Гц), 132,09 (д, J=7,8 Гц), 119,98 (д, J=20,9 Гц), 115,99, 111,63 (д, J=26,4 Гц), 23,35
13C ЯМР (101 МГц, CDCl3) δ 161,75 (д, J=241,3 Гц), 144,76 (д, J=10,3 Гц), 128,11 (д, J=2,8 Гц), 126,53 (д, J=9,6 Гц), 105,06 (д, J=20,7 Гц), 102,26 (д, J=24,2 Гц), 27,27, 22,35
([M-H]+)
([M-H]-)
13C ЯМР (101 МГц, CDCl3) δ 148,17, 142,71, 138,30, 136,16, 133,37, 130,33, 124,29, 115,18, 23,32, 20,81
13C ЯМР (101 МГц, CDCl3) δ 143,15, 136,16, 129,82, 125,33, 119,79, 116,55, 27,37, 22,41, 20,96
13C ЯМР (101 МГц, CDCl3) δ 156,92 (д, JCF=235,0 Гц), 139,17 (д, JCF=2,1 Гц), 134,61 (д, JCF=6,2 Гц), 116,55 (д, JCF=7,5 Гц), 112,69 (д, JCF=22,5 Гц), 112,17 (д, JCF=22,4 Гц), 27,90, 22,11
([M+H]+)
13C ЯМР (101 МГц, CDCl3) δ 152,53 (дд, JCF=259,5, 12,5 Гц), 148,52 (дд, JCF=253,7, 13,8 Гц), 143,22, 141,38, 137,23 (дд, JCF=7,1, 4,2 Гц), 119,27 (д, JCF=18,9 Гц), 116,39, 114,49 (дд, JCF=21,9, 2,1 Гц), 23,12
13C ЯМР (101 МГц, CDCl3) δ 148,36 (дд, JCF=243,1, 13,4 Гц), 143,71 (дд, JCF=236,4, 12,4 Гц), 139,79-139,13 (м), 128,70 (т, JCF=3,7 Гц), 114,07 (д, JCF=18,1 Гц), 104,18 (д, JCF=19,8 Гц), 27,44, 22,20
([M+H]+)
[M-H]-)
19F ЯМР (376 МГц, CDCl3) δ -75,61, -75,63, -75,63, -182,14, -182,17, -182,18
19F ЯМР (376 МГц, CDCl3) δ -75,57, -75,59, -182,14, -182,16, -182,18
([M+H]+)
([M+H]+)
19F ЯМР (376 МГц, CDCl3) δ -75,58, -182,16
([M+H]+)
19F ЯМР (376 МГц, ДМСО-d6) δ -85,20, -86,94
([M+2H]+)
19F ЯМР (376 МГц, ДМСО-d6) δ
-85,18, -86,92
Спектральные данные ЯМР были получены, используя аппарат 400 МГц, если не указано иного.
P* - получали способами, описанными в документе Crouse et al. публикации патентной заявки PCT WO 2009/102736 A1 и в документе Brown, et al., WO 2011017504 A1.
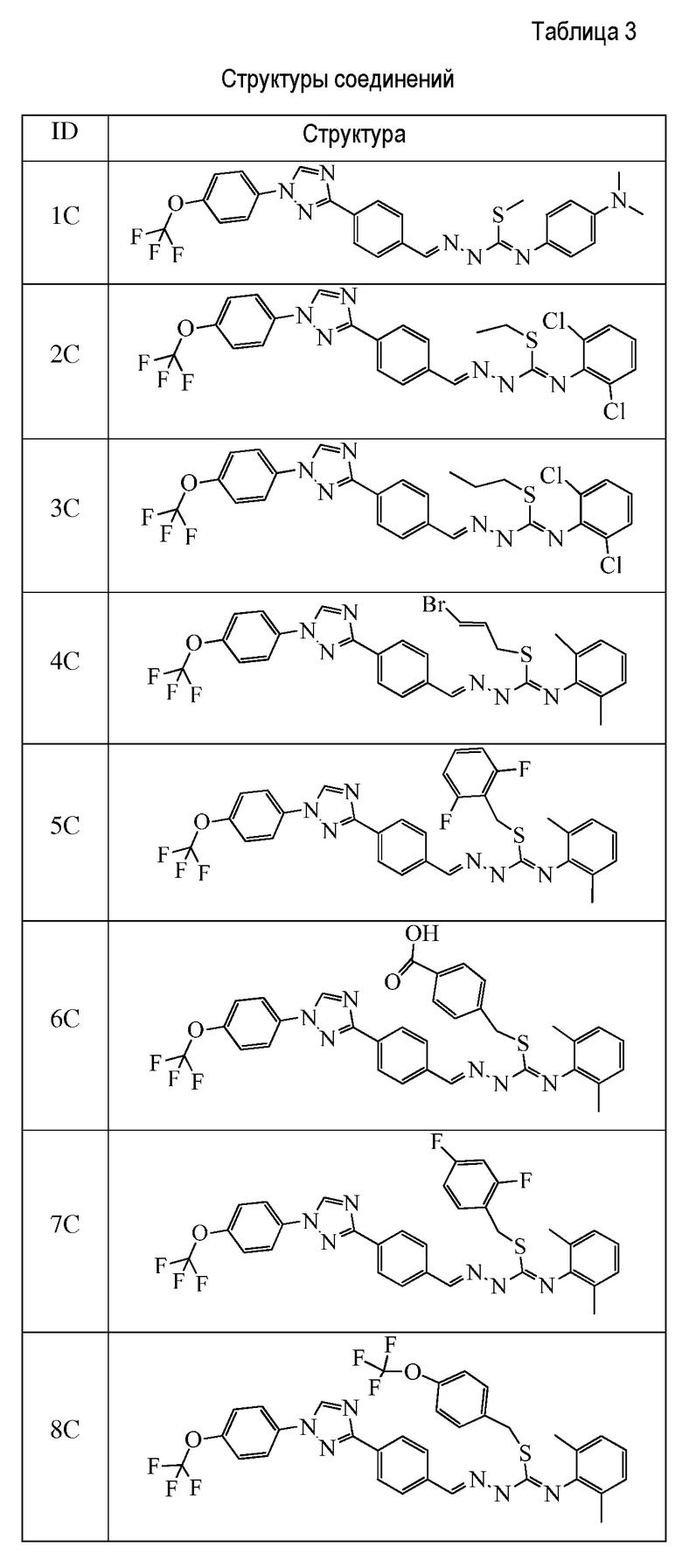
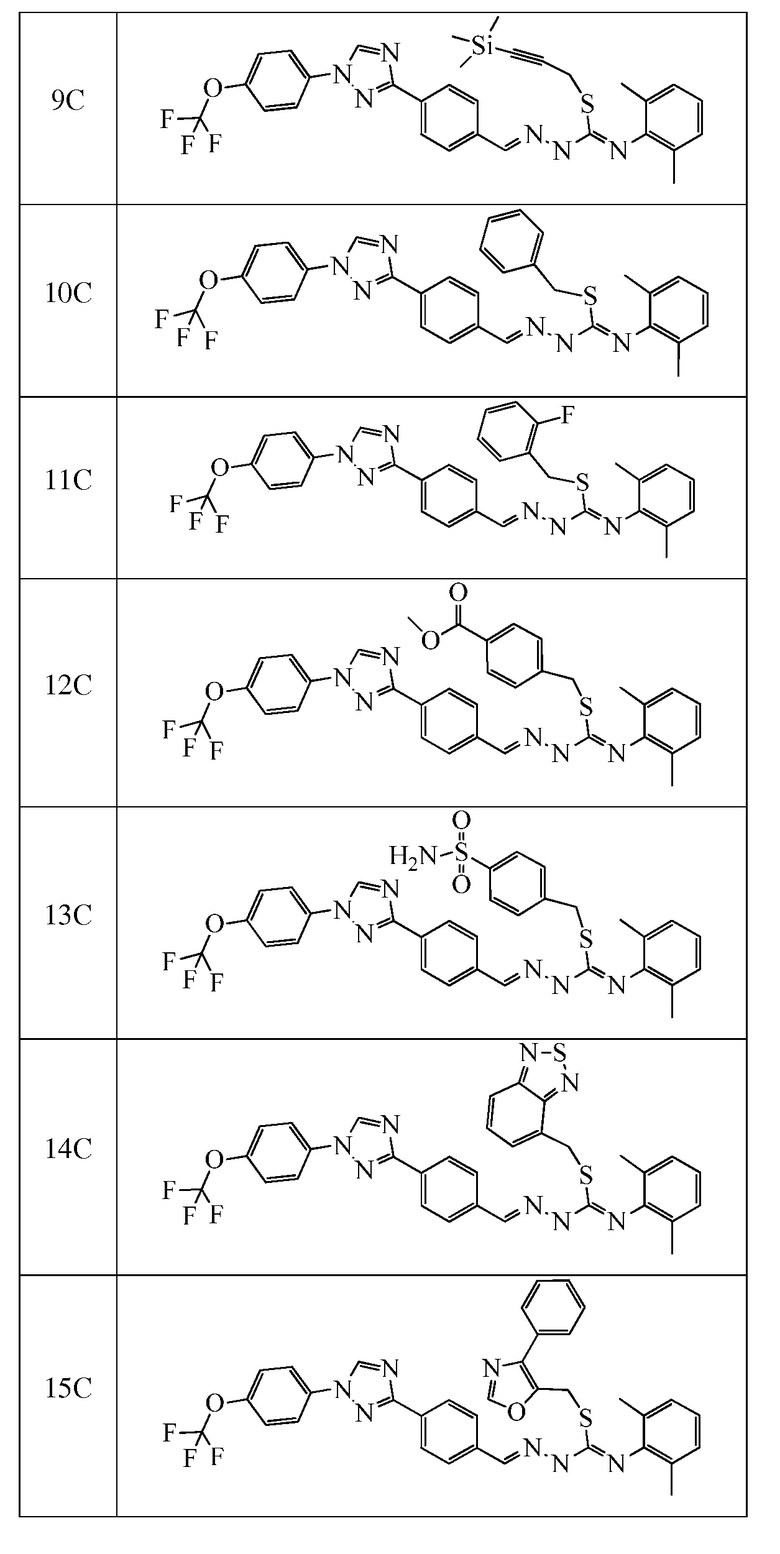
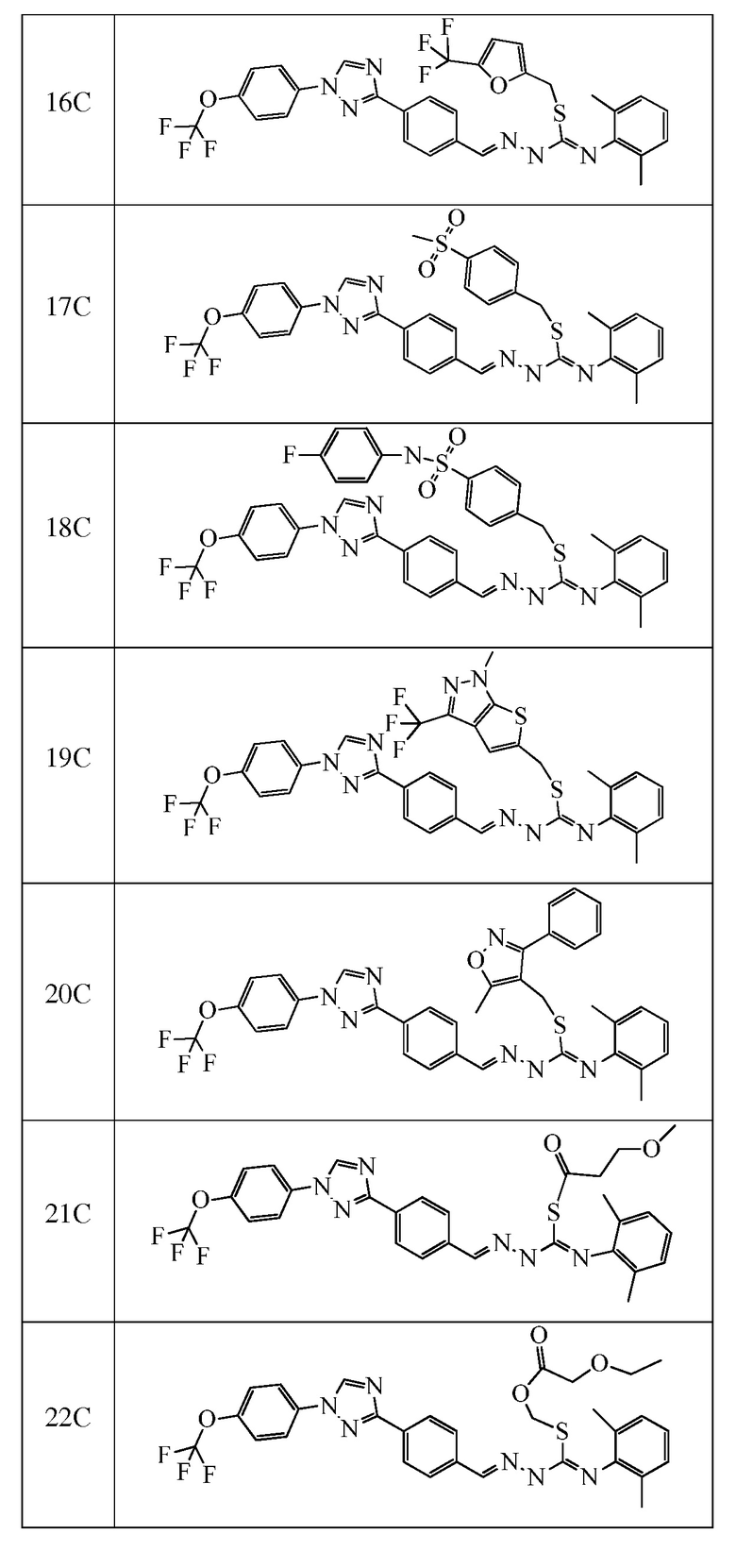
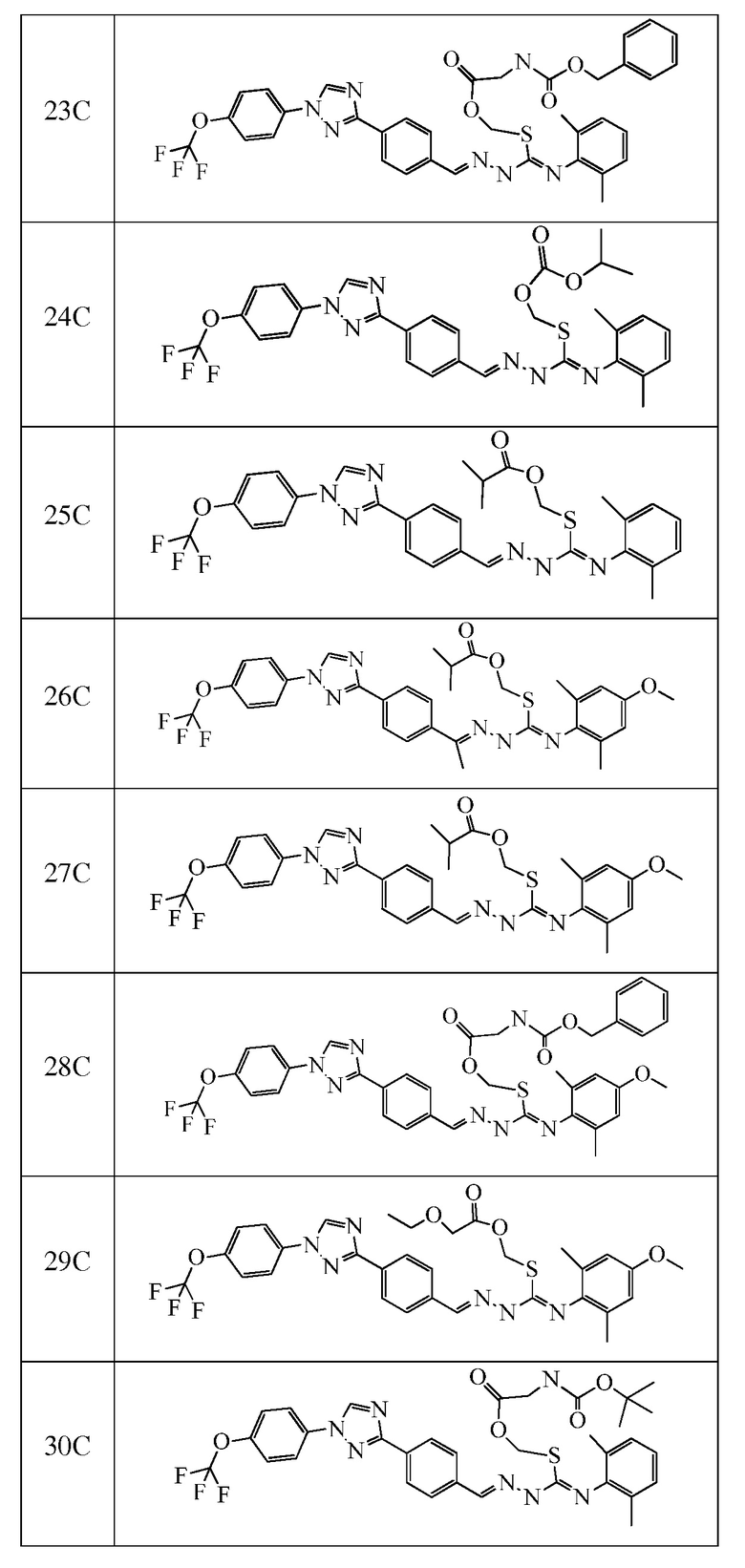
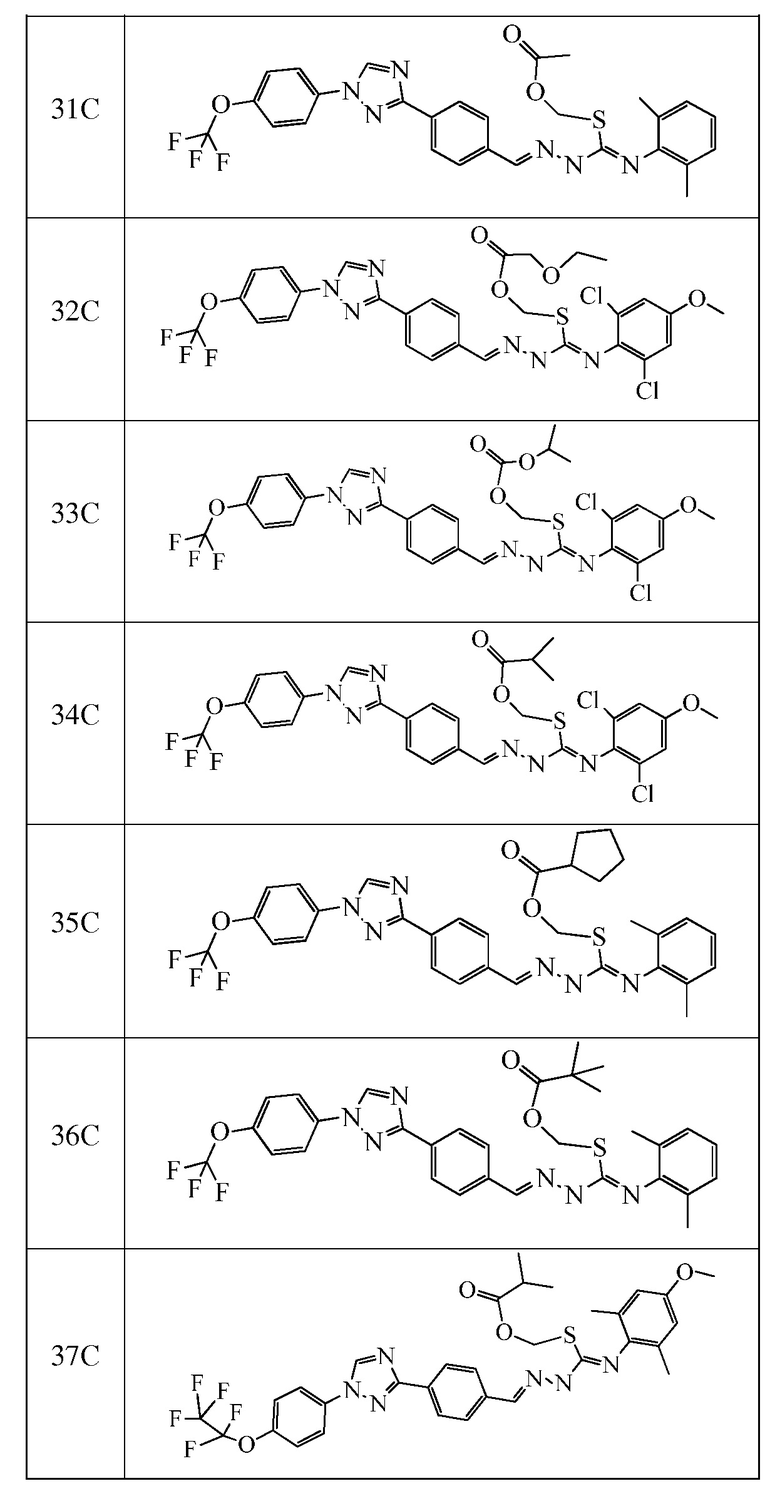
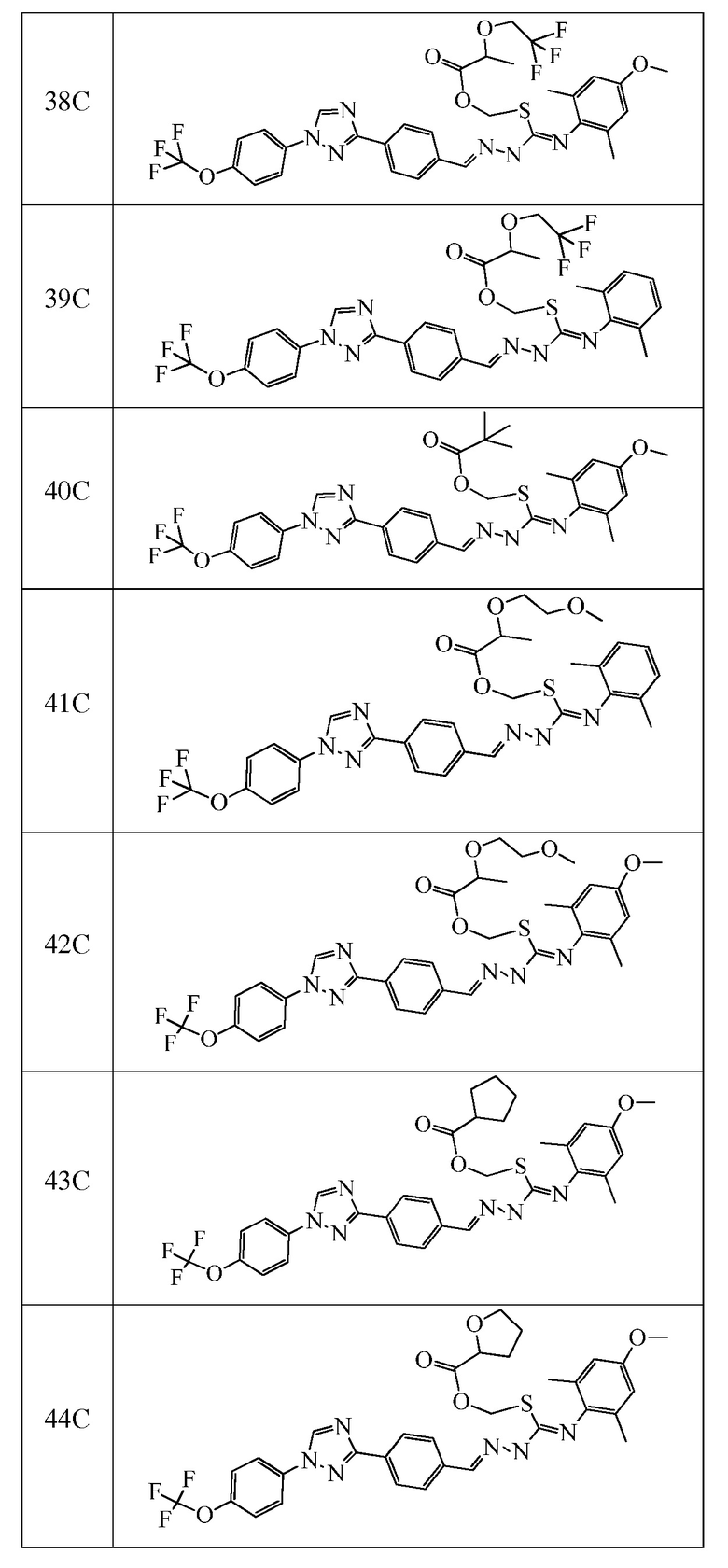
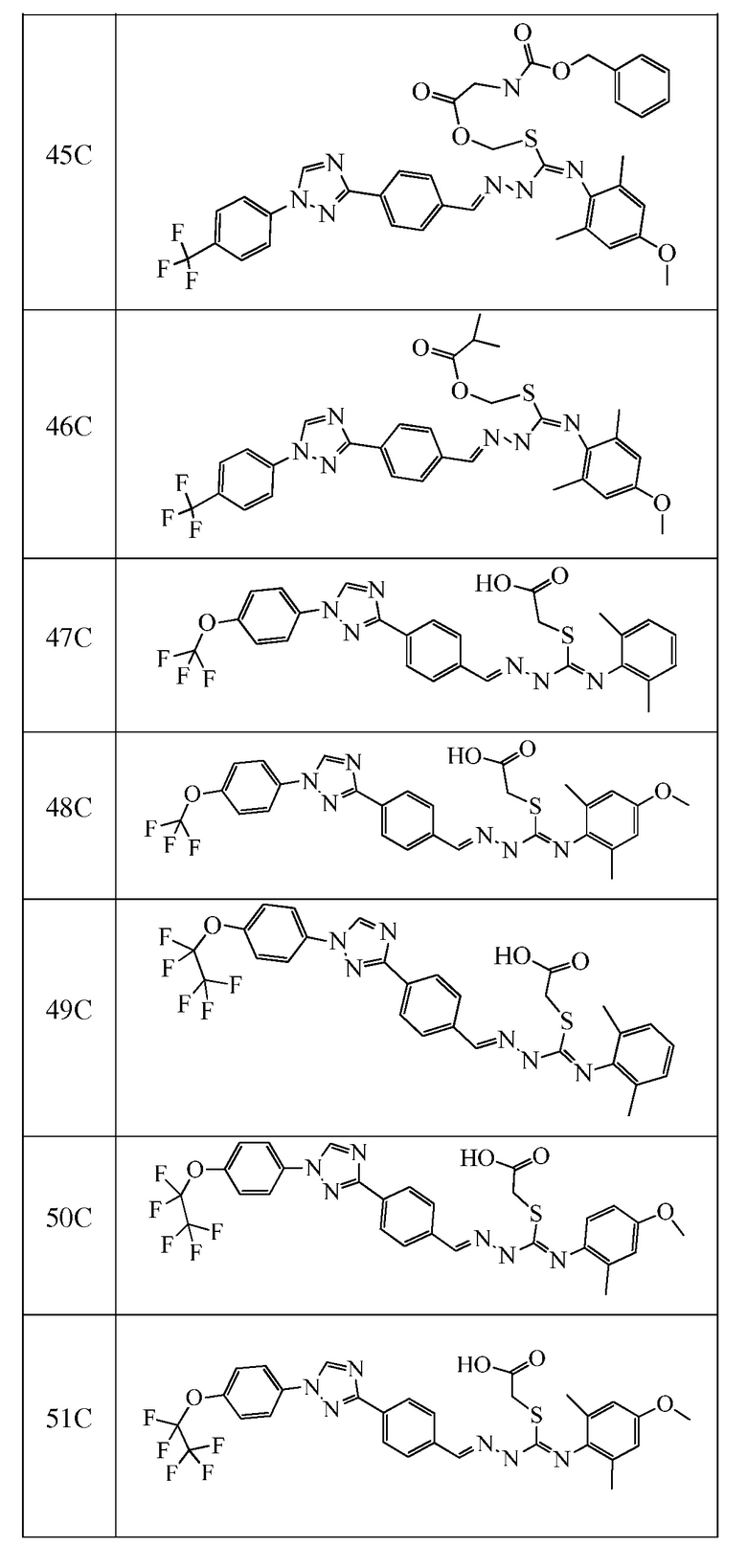
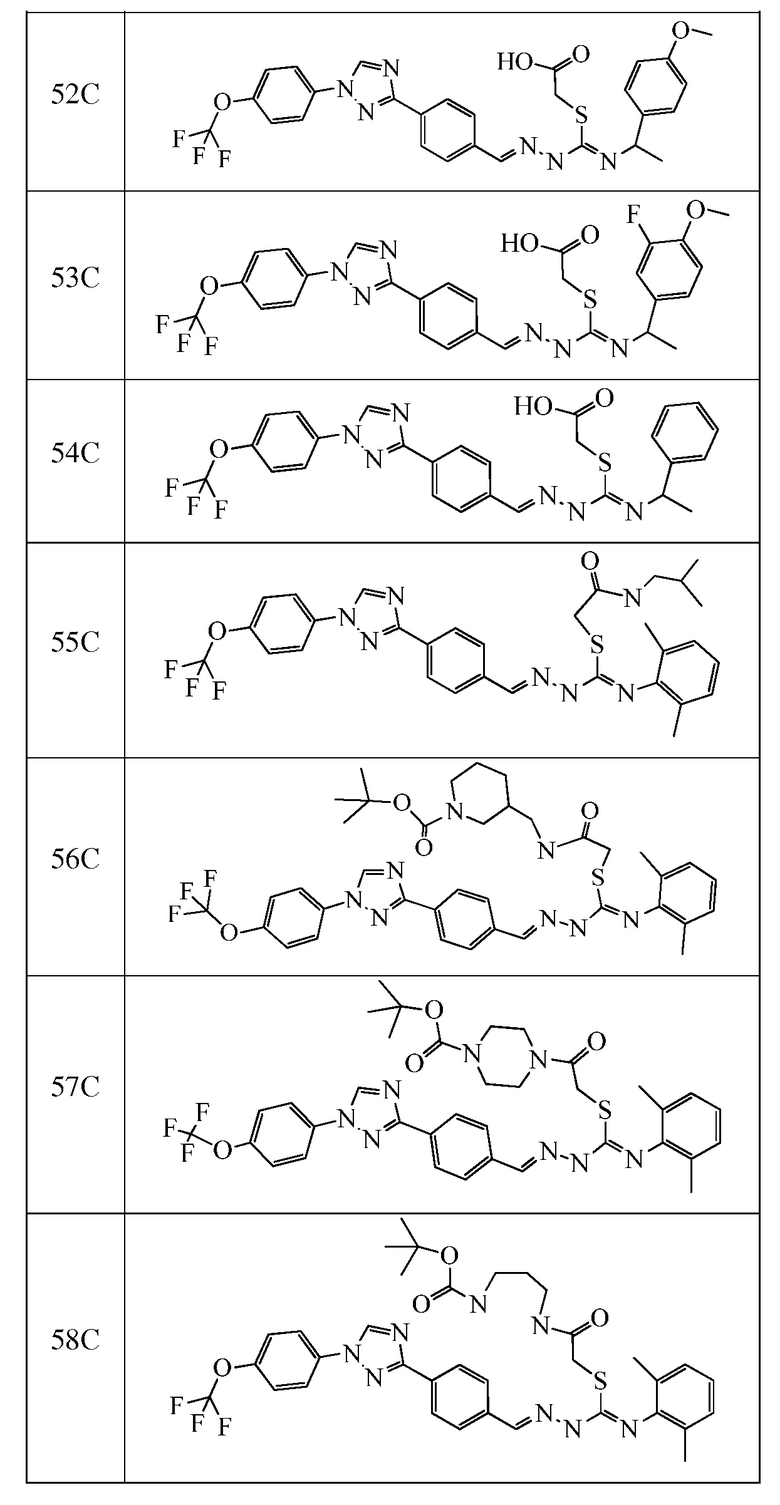
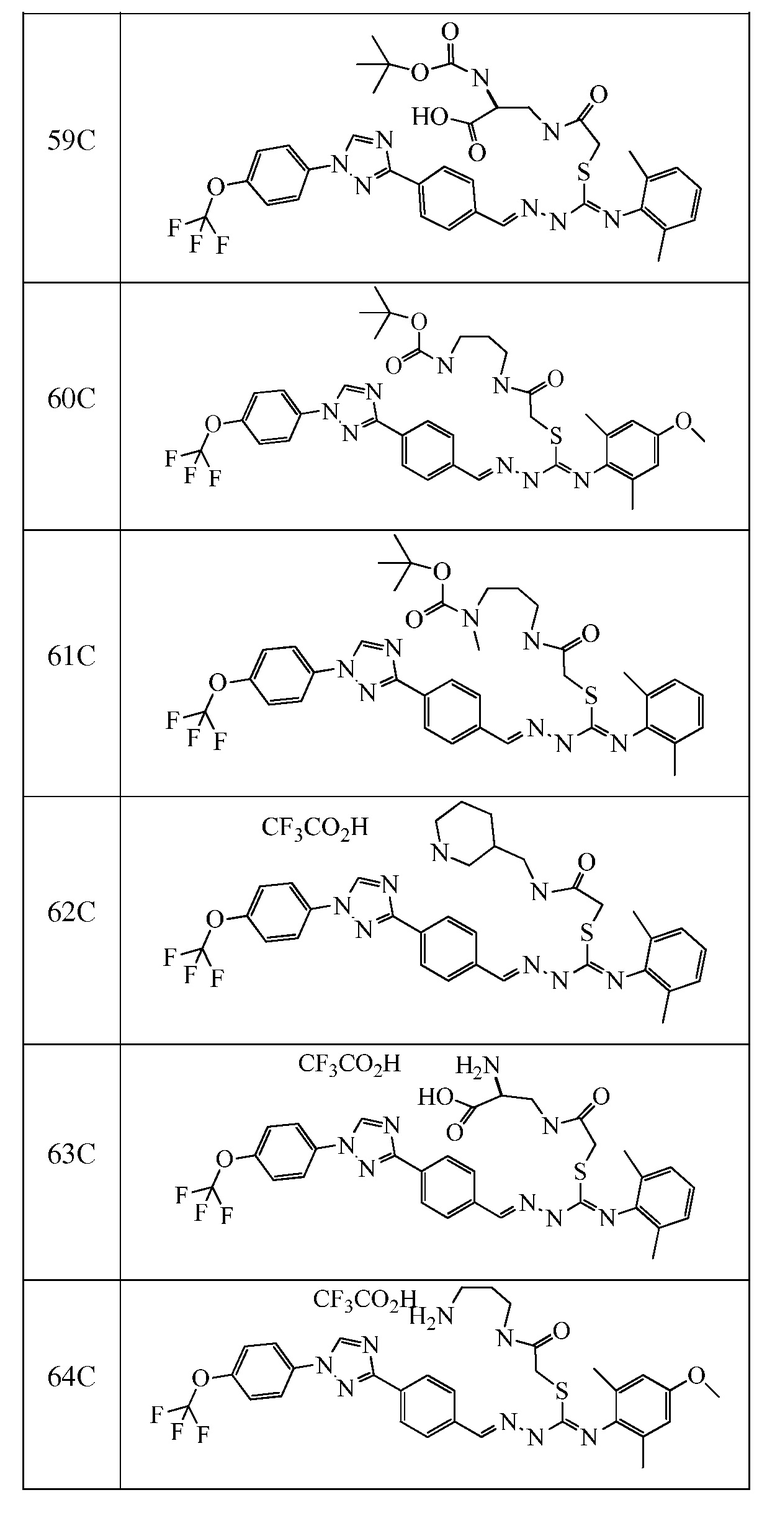
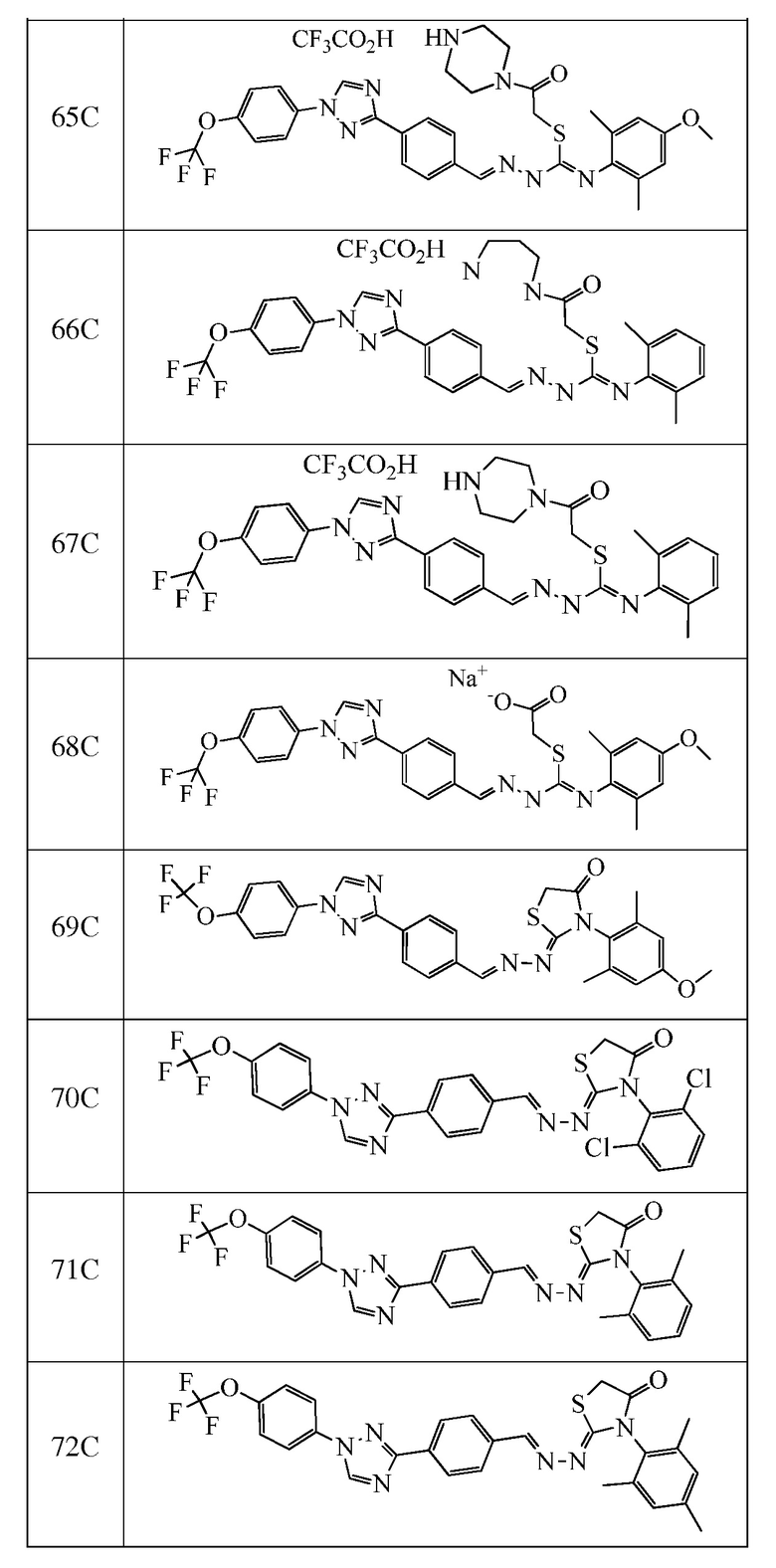
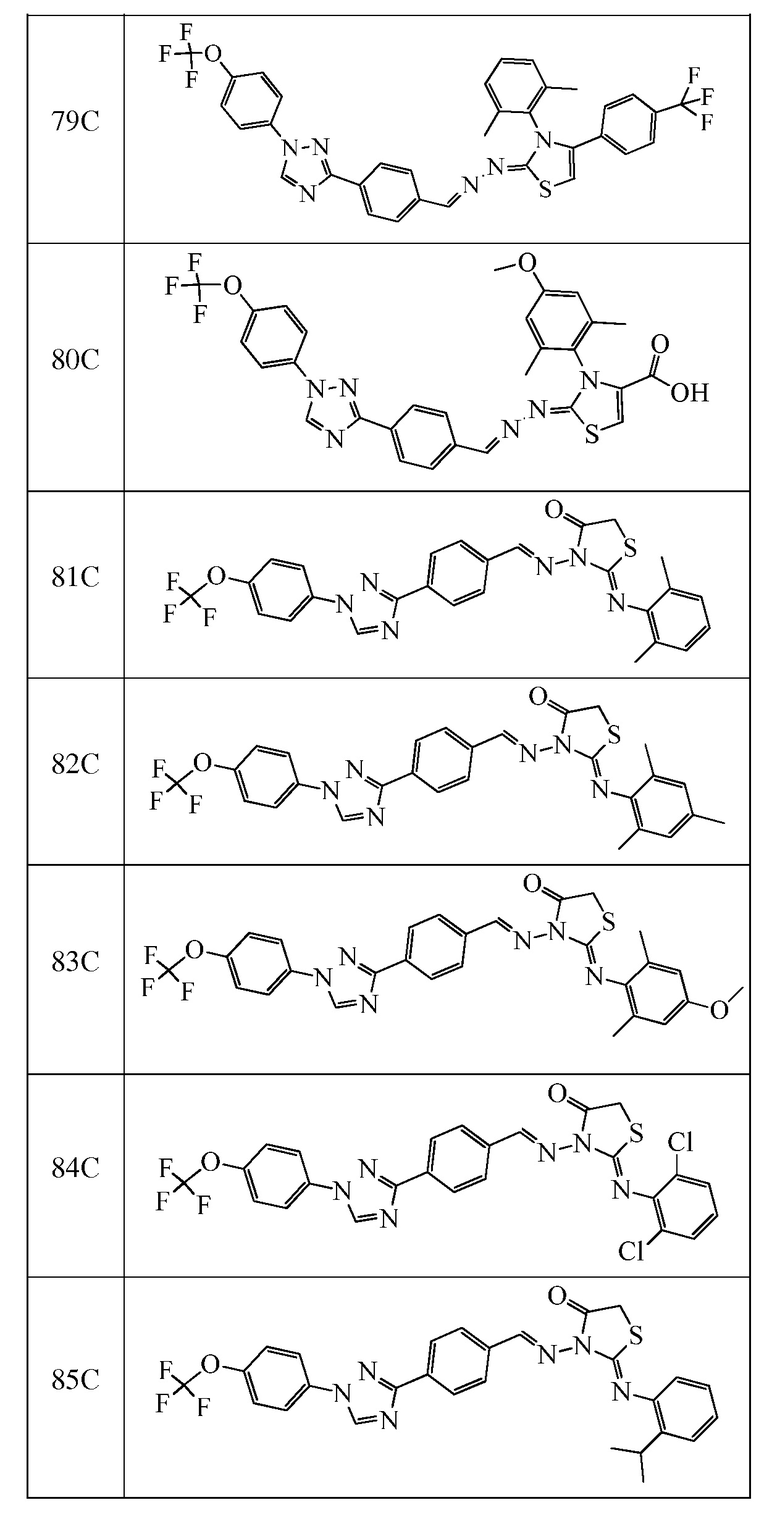

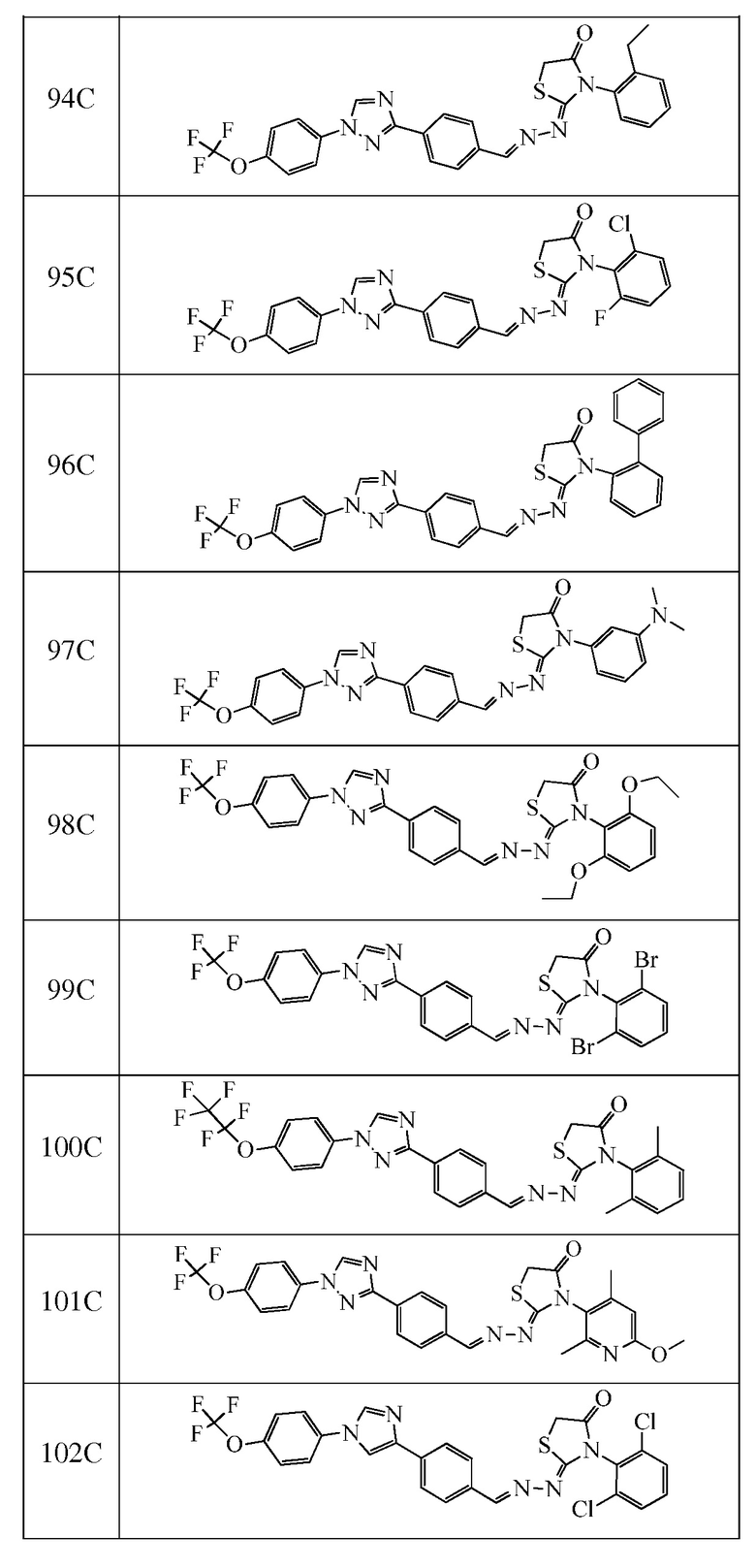
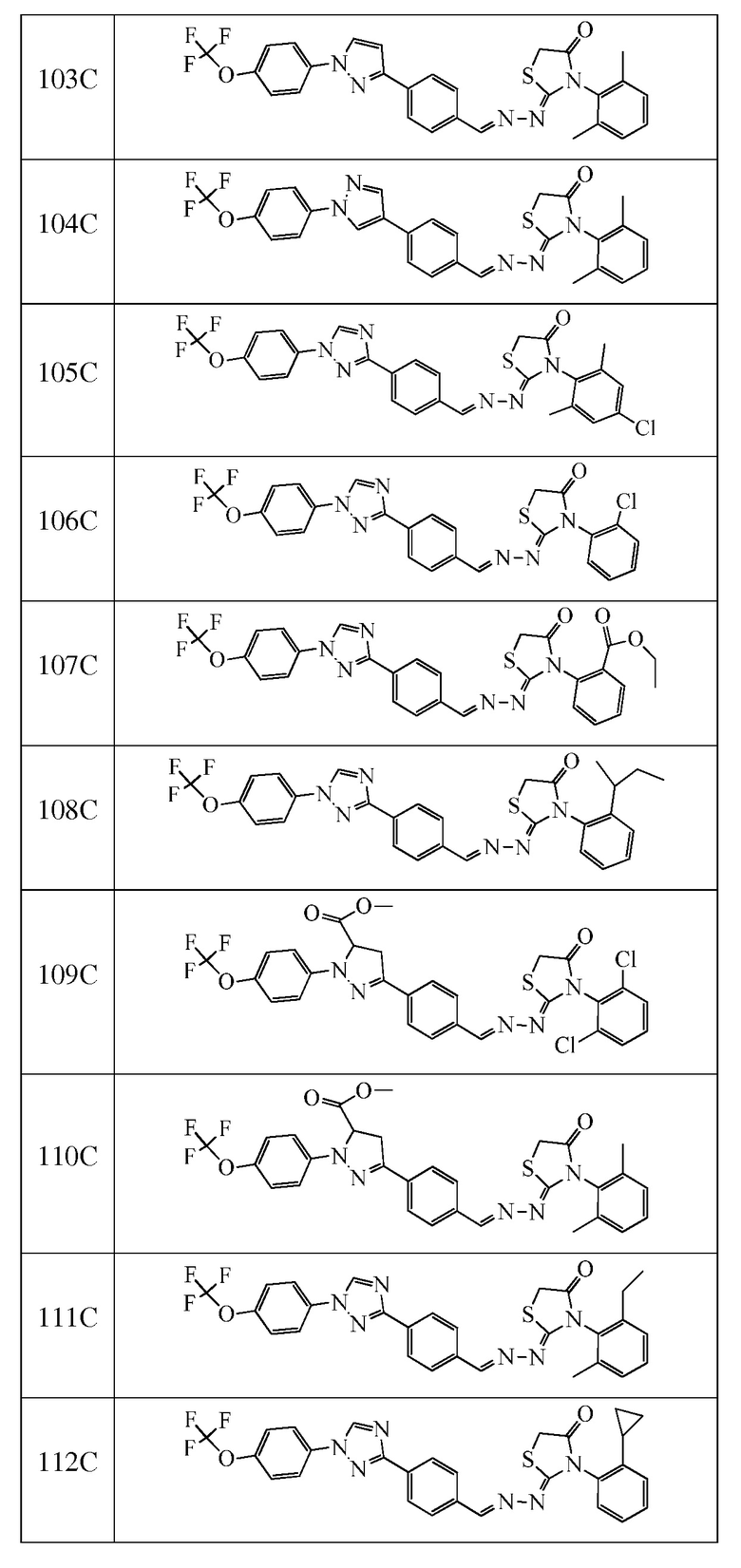
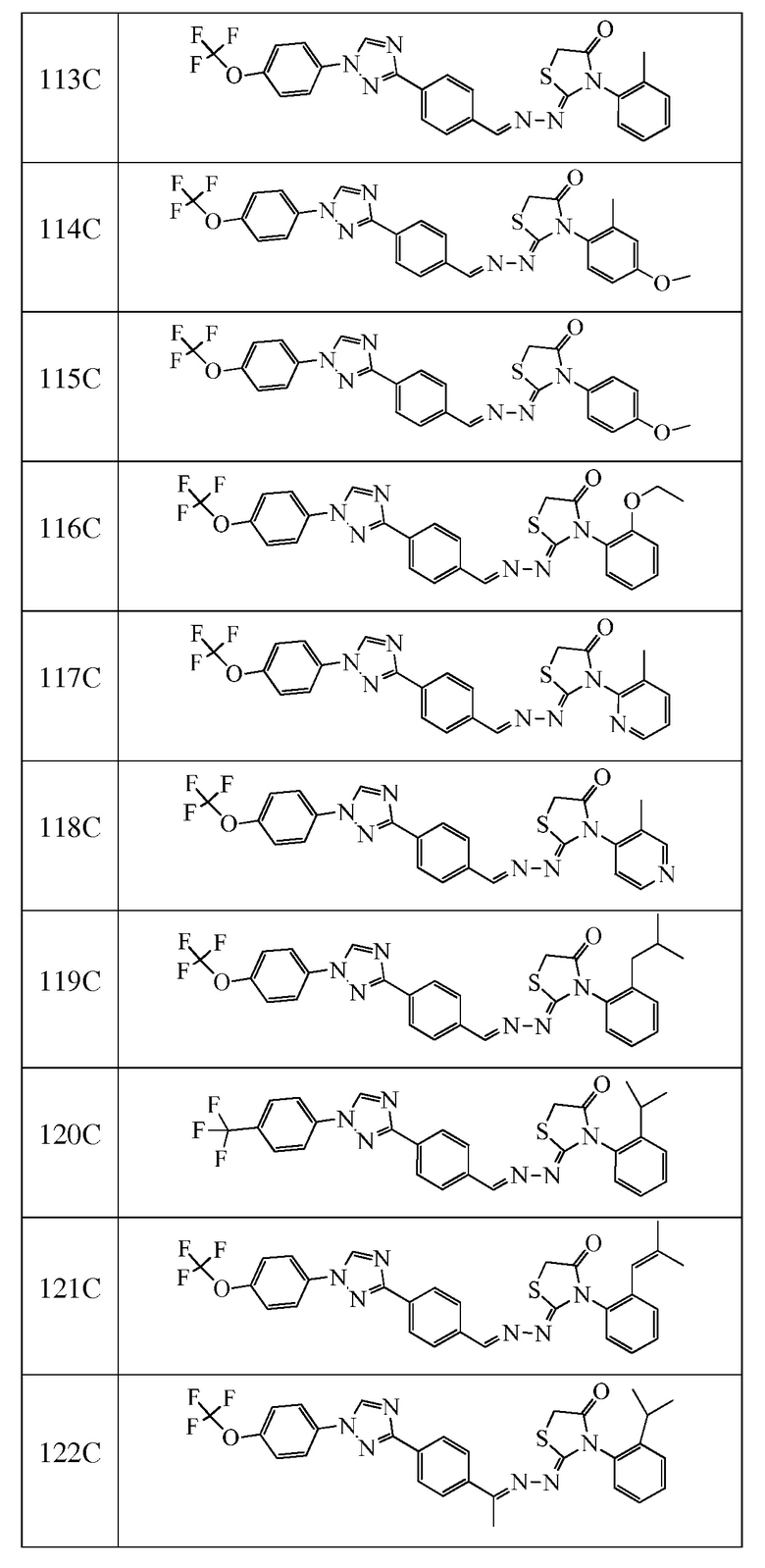
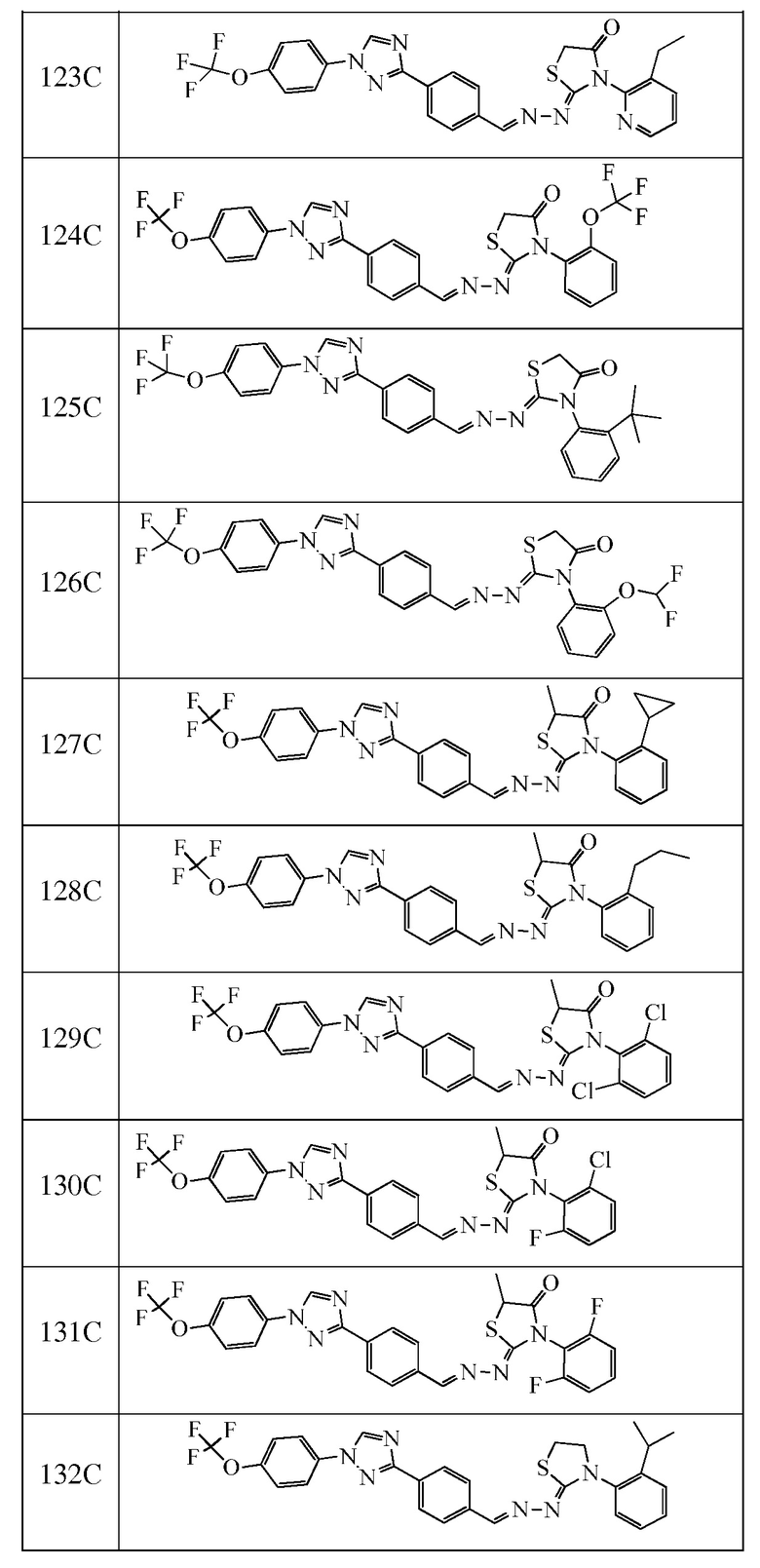
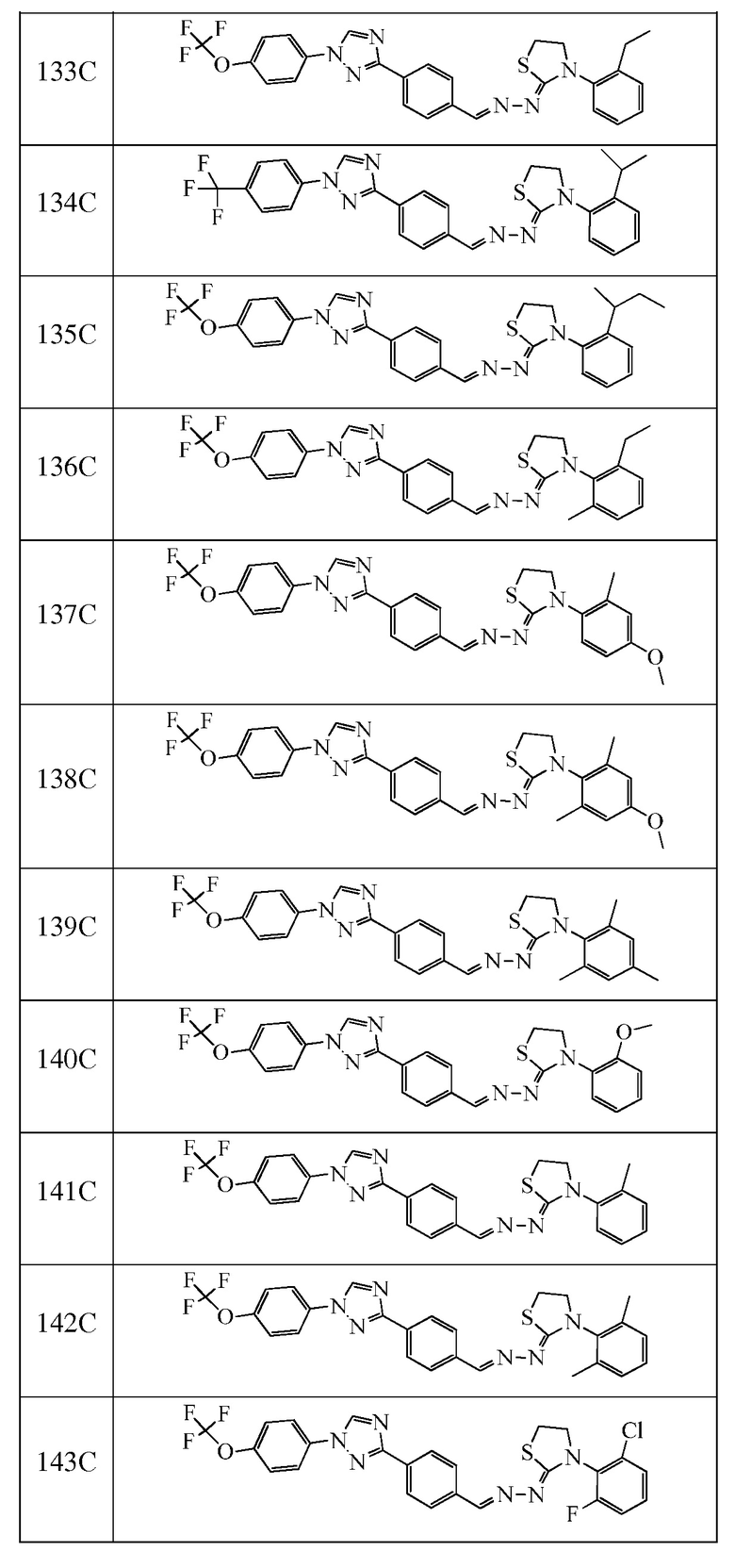
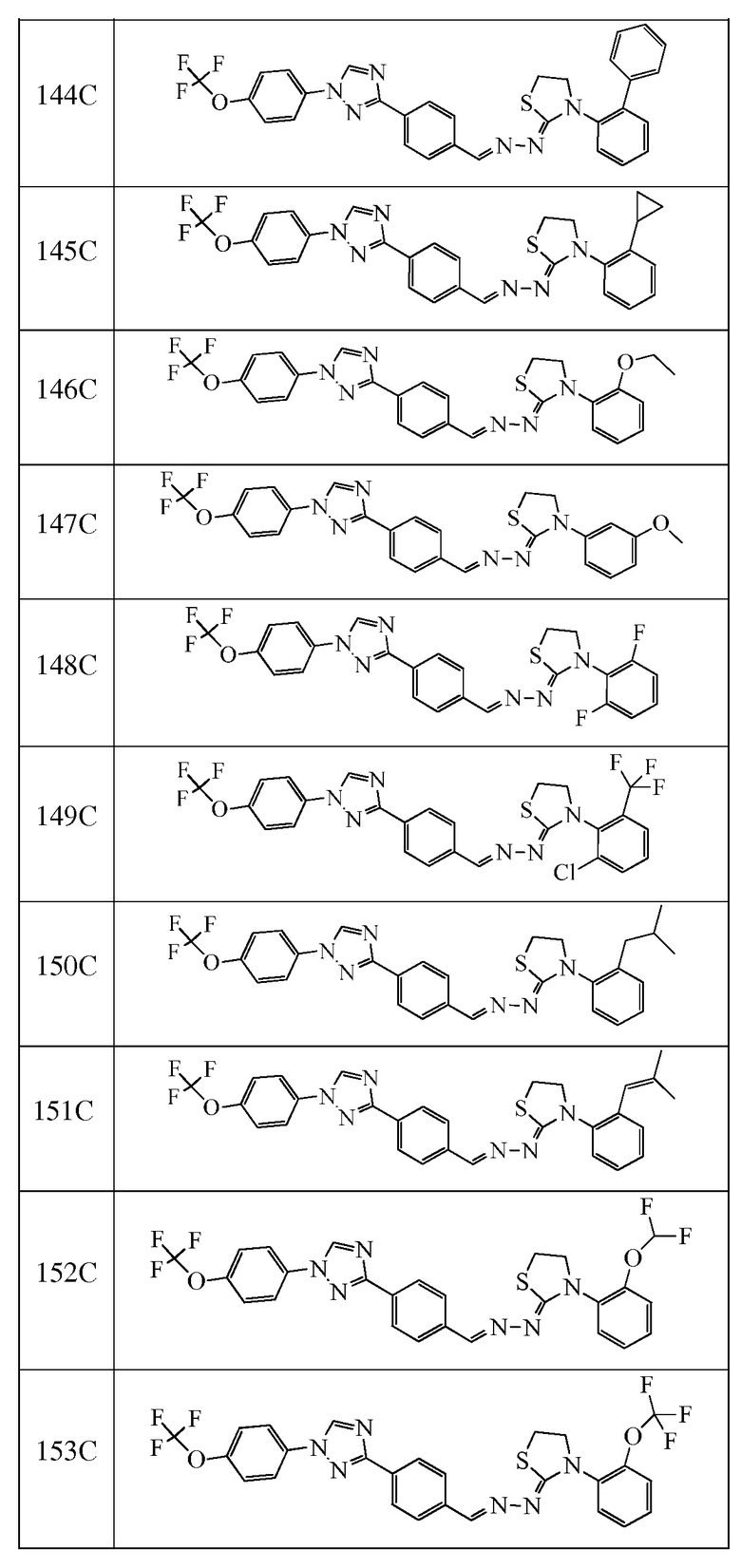
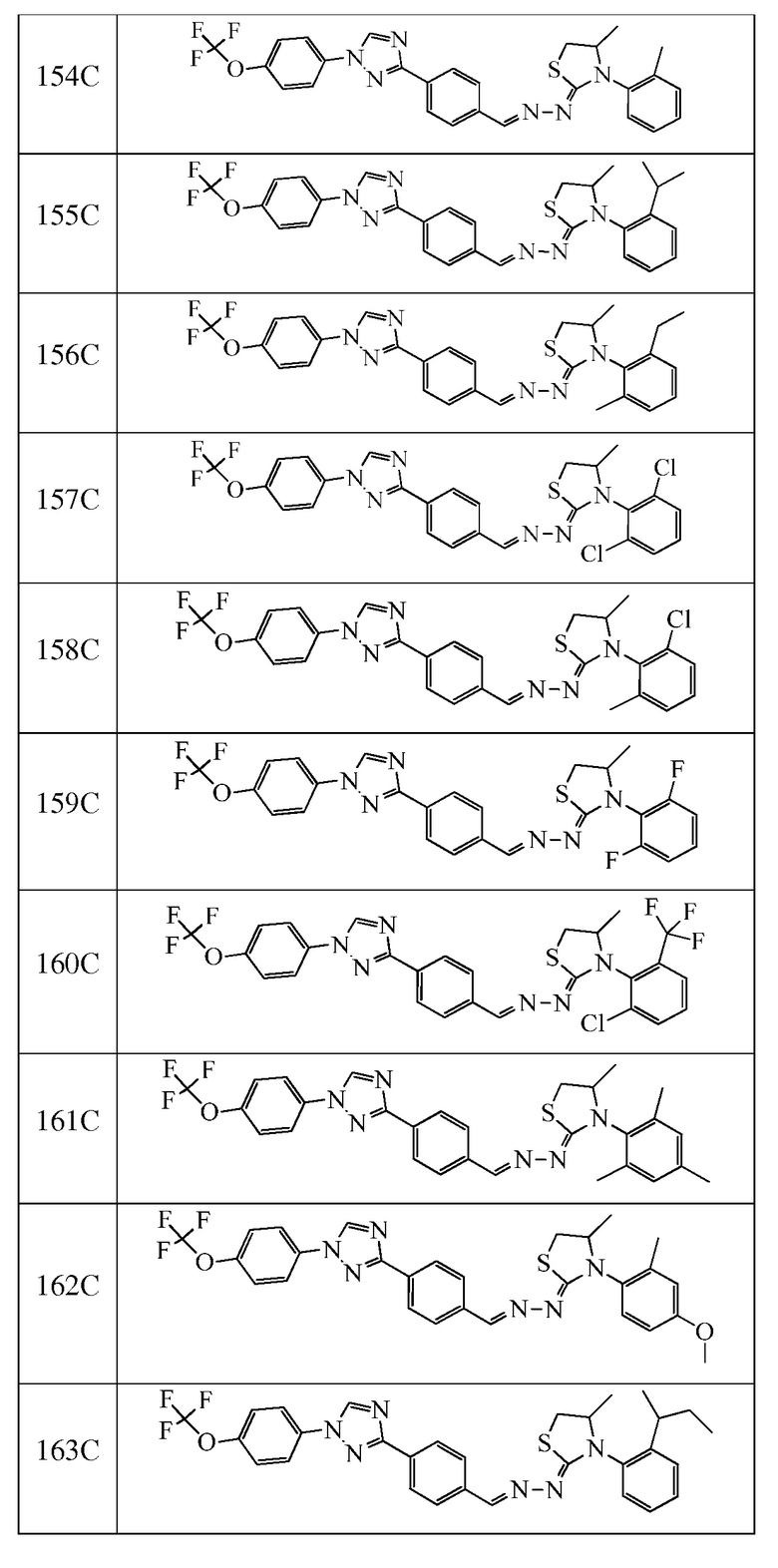
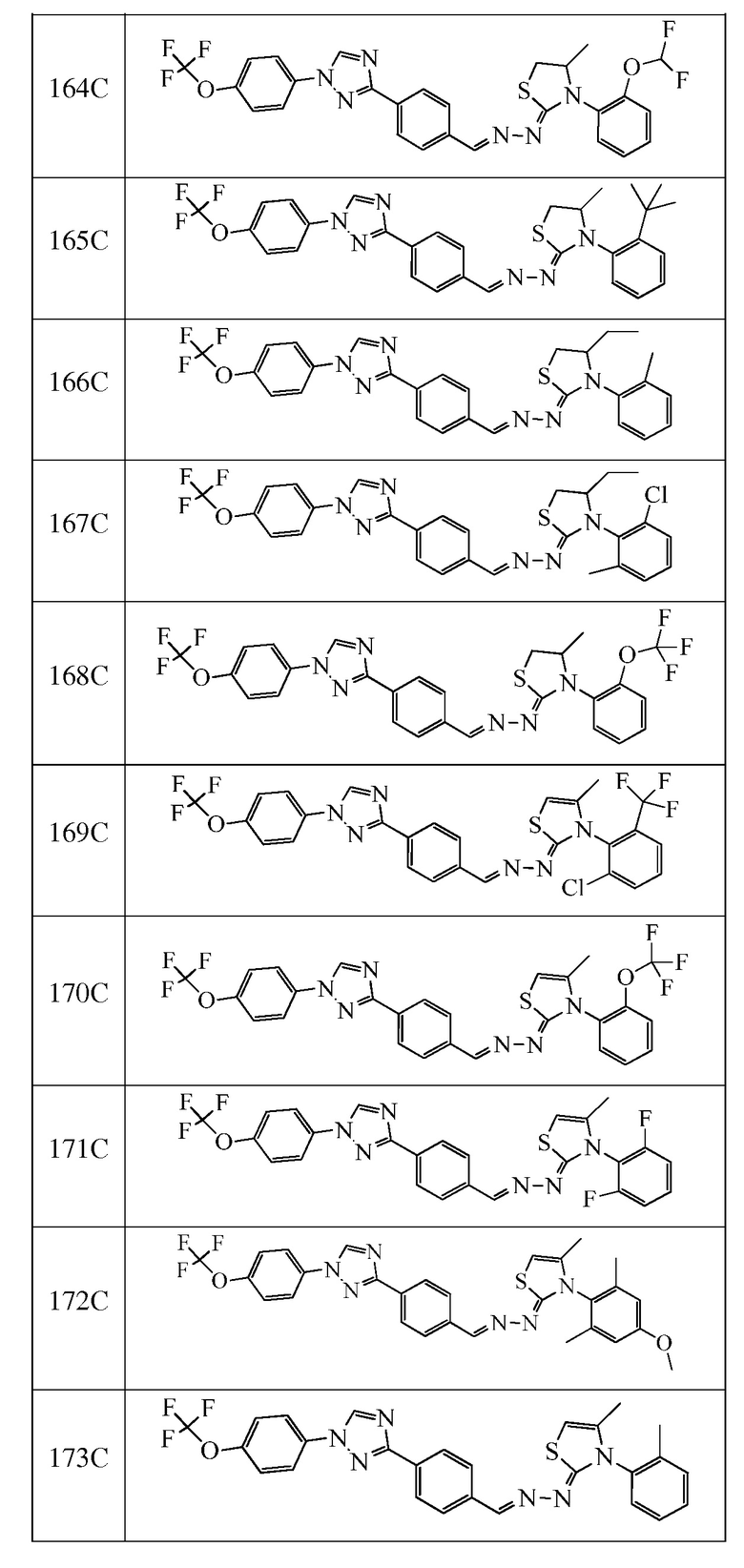
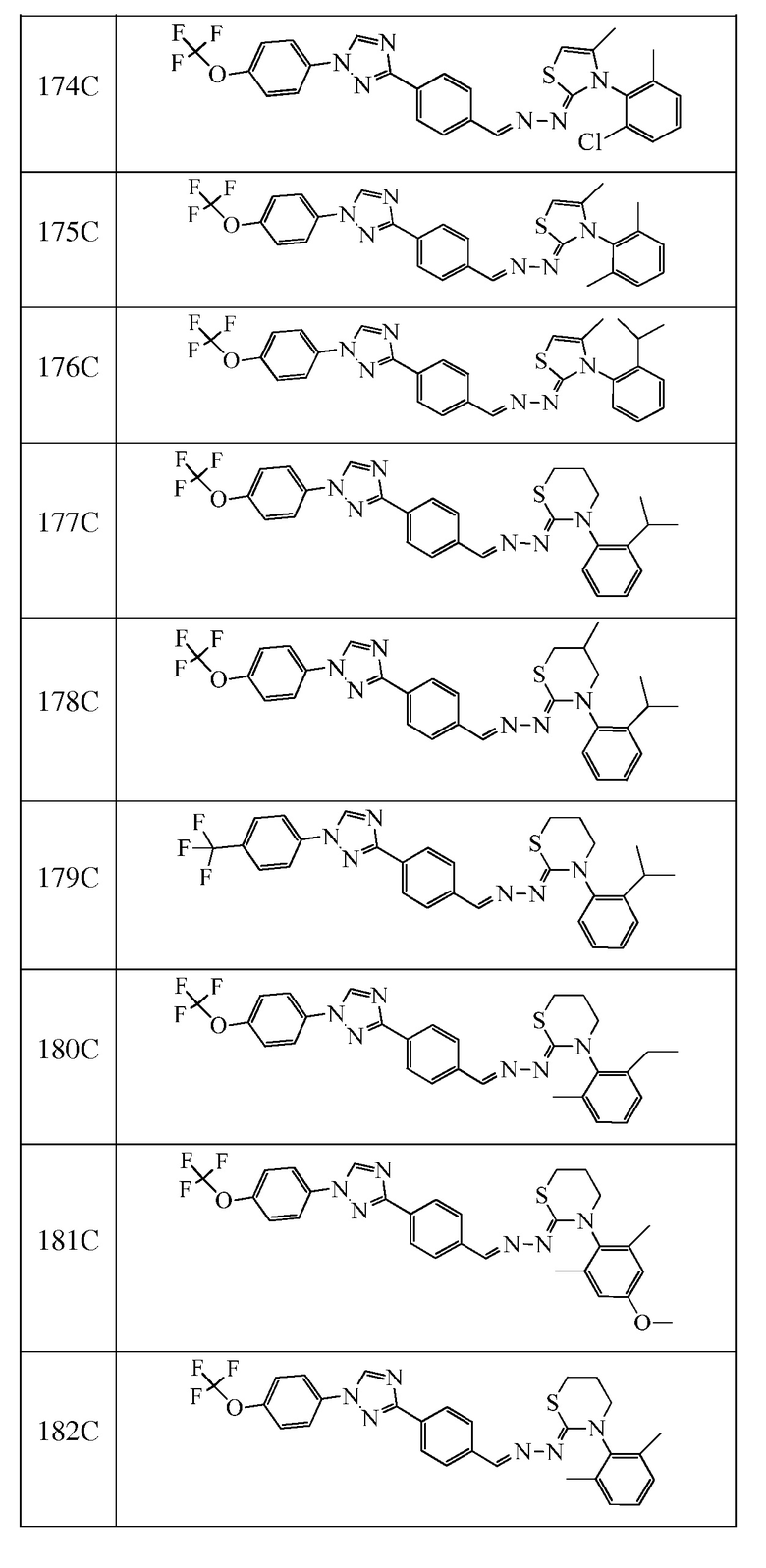
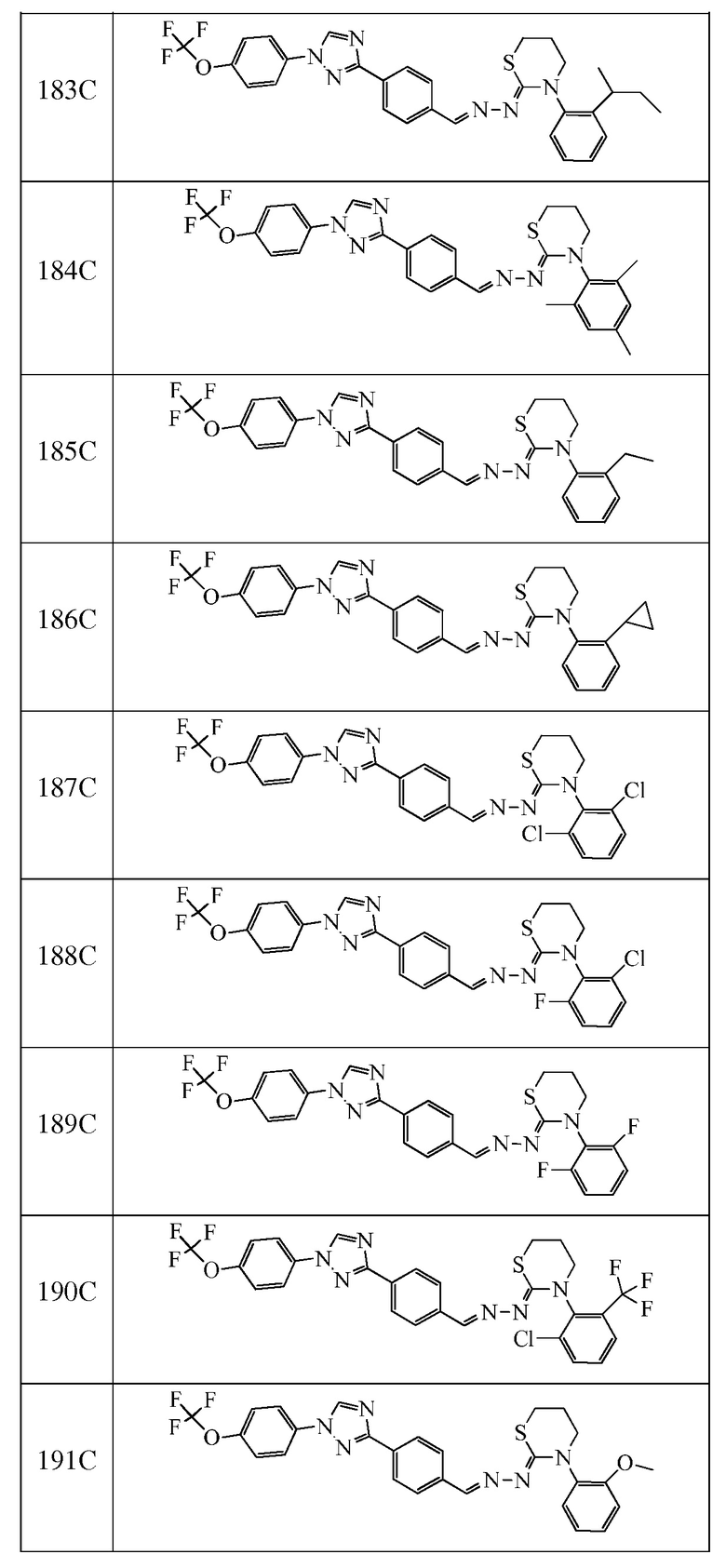
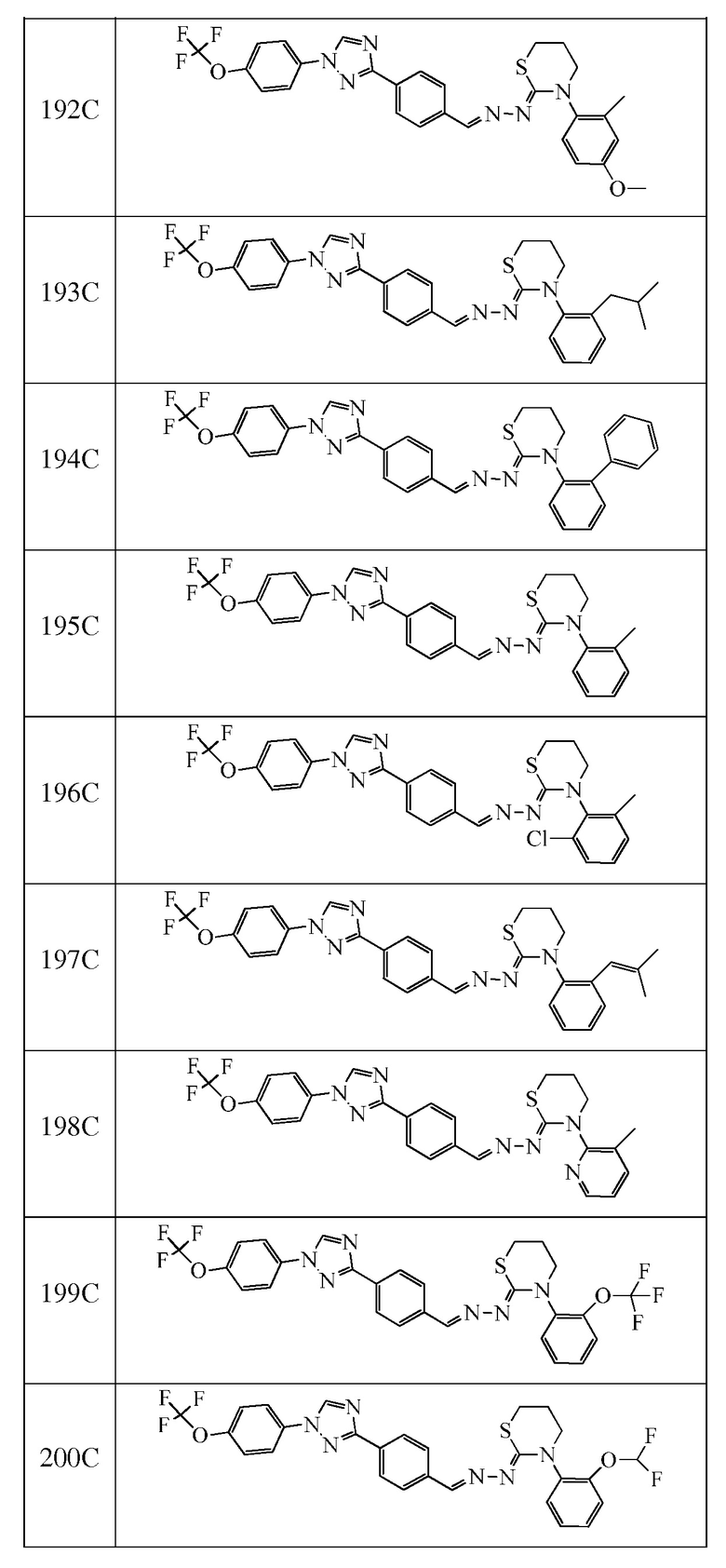

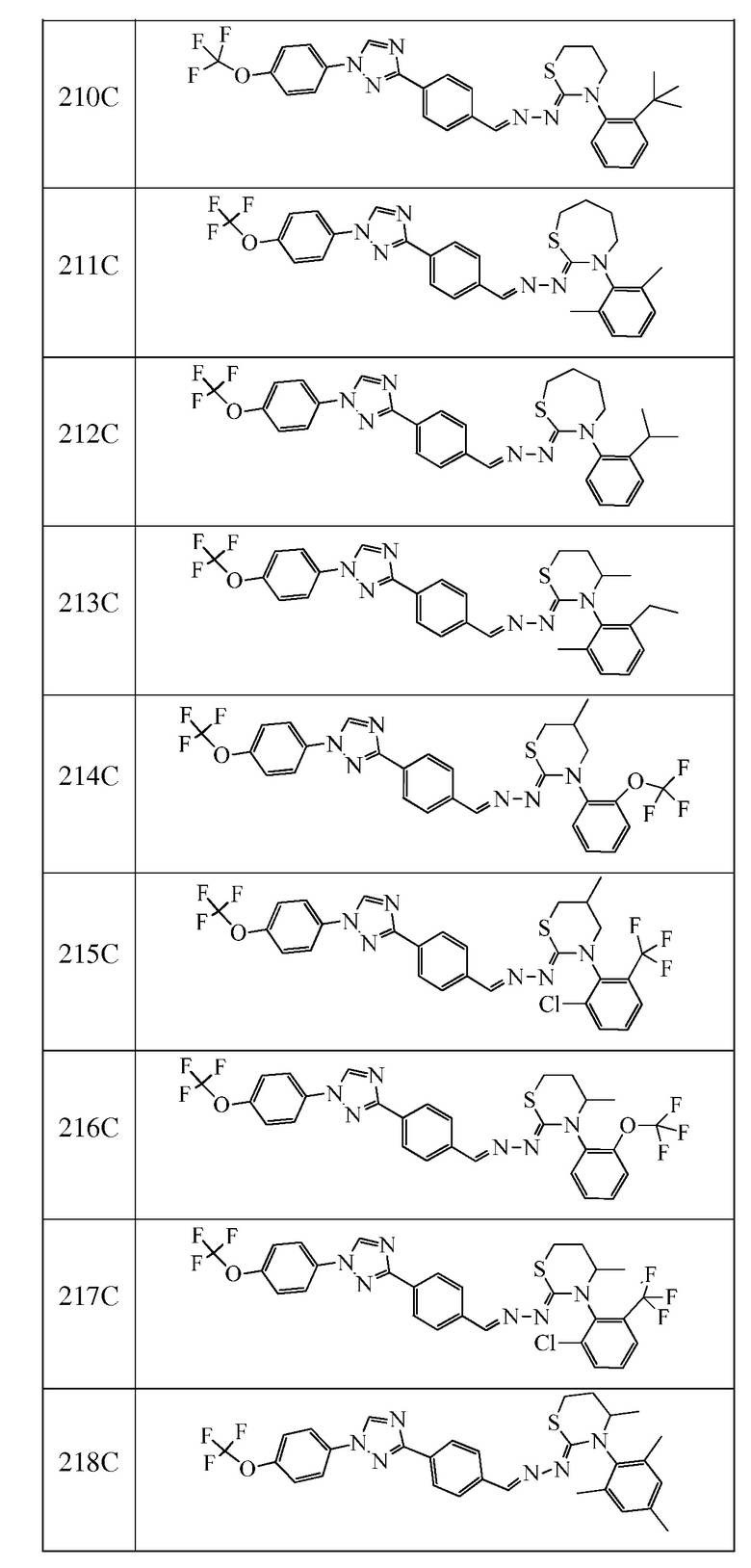
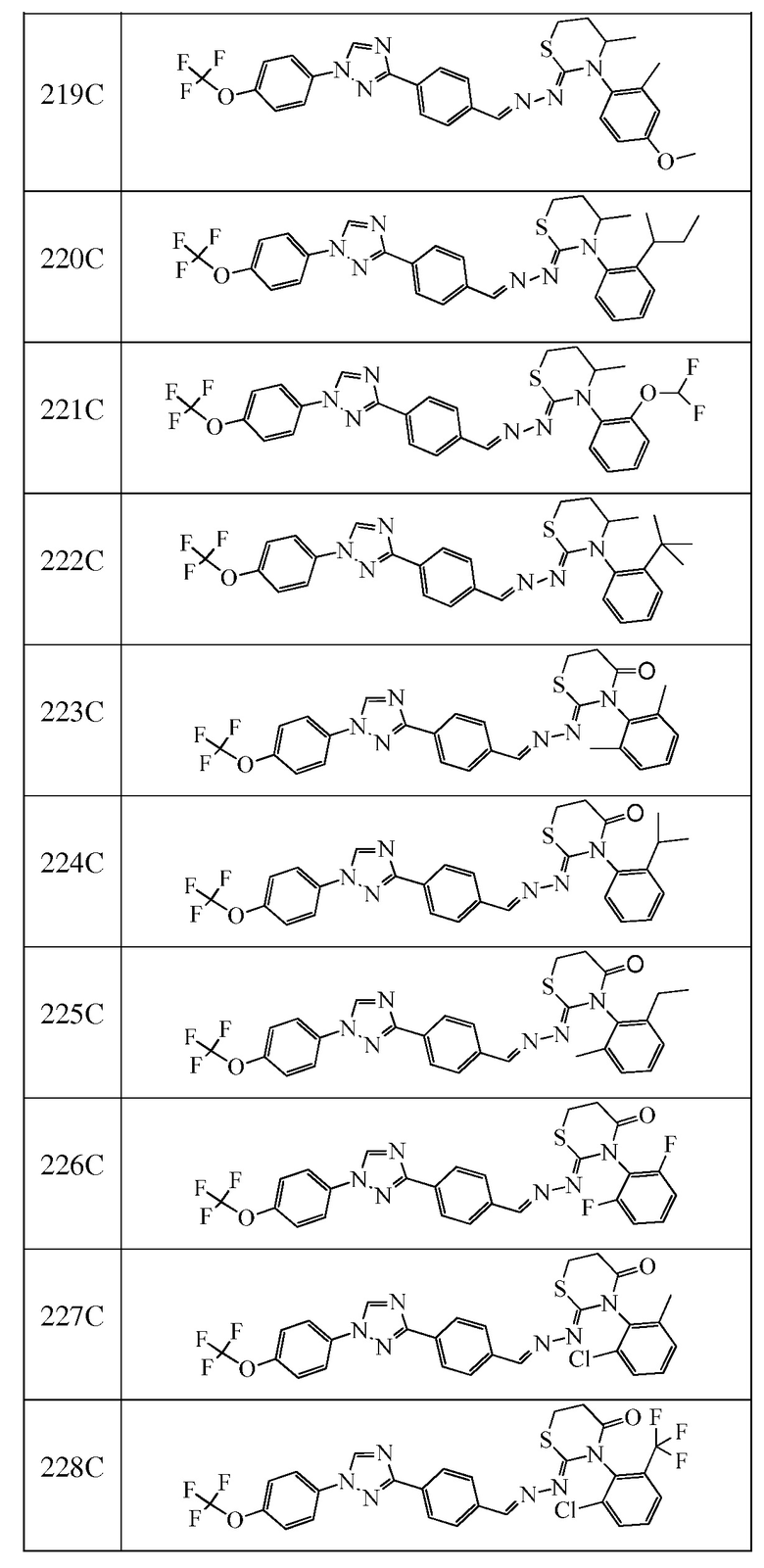
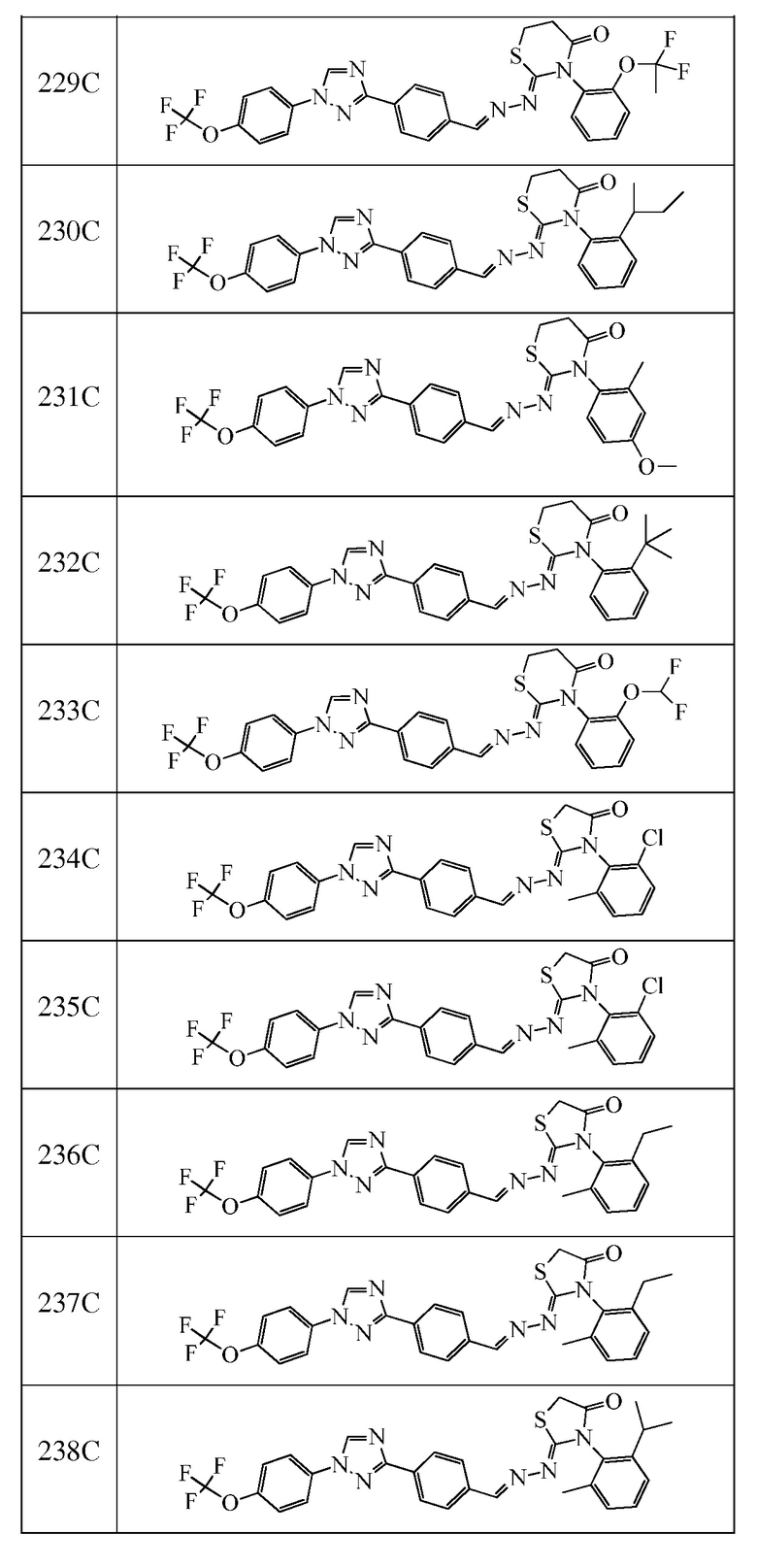
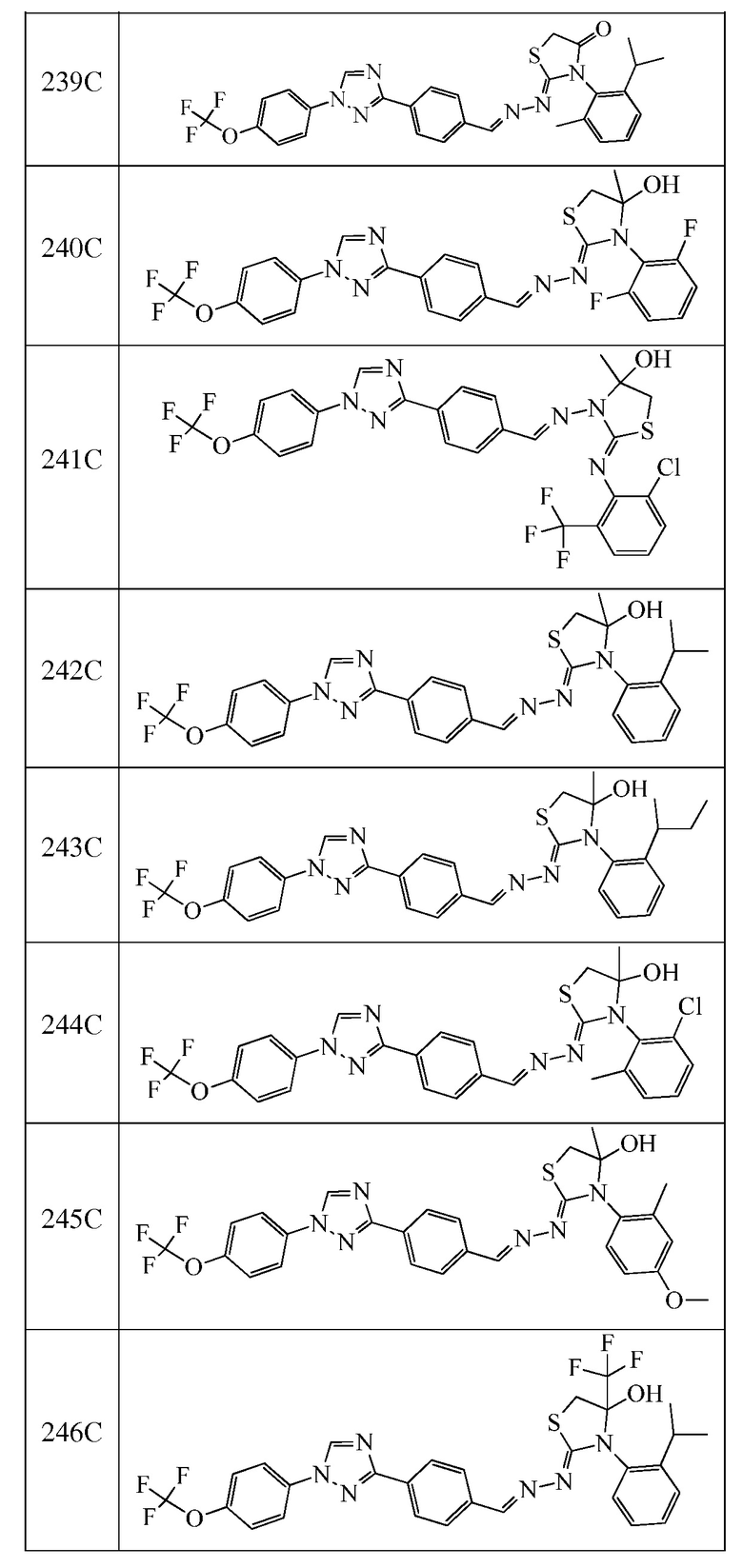
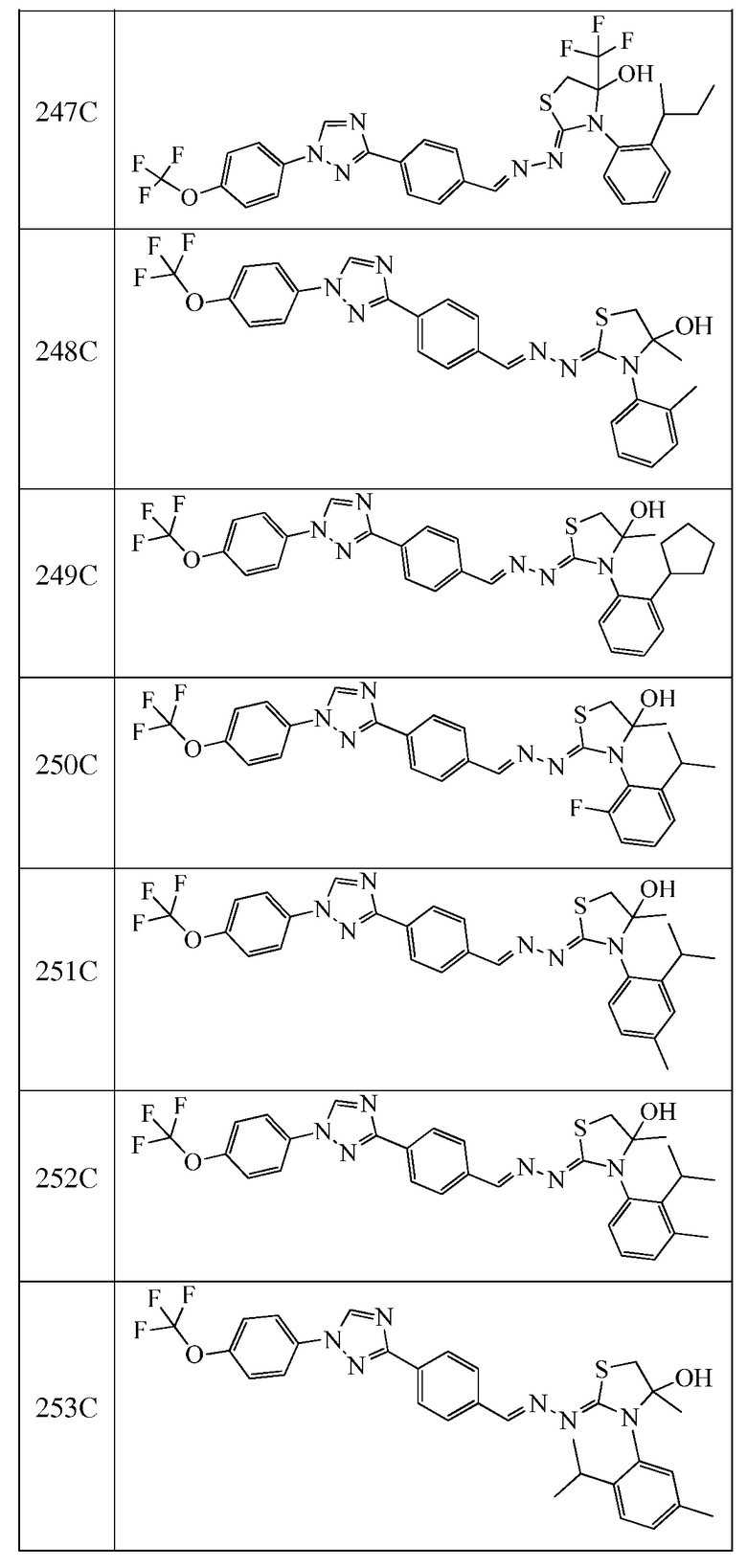
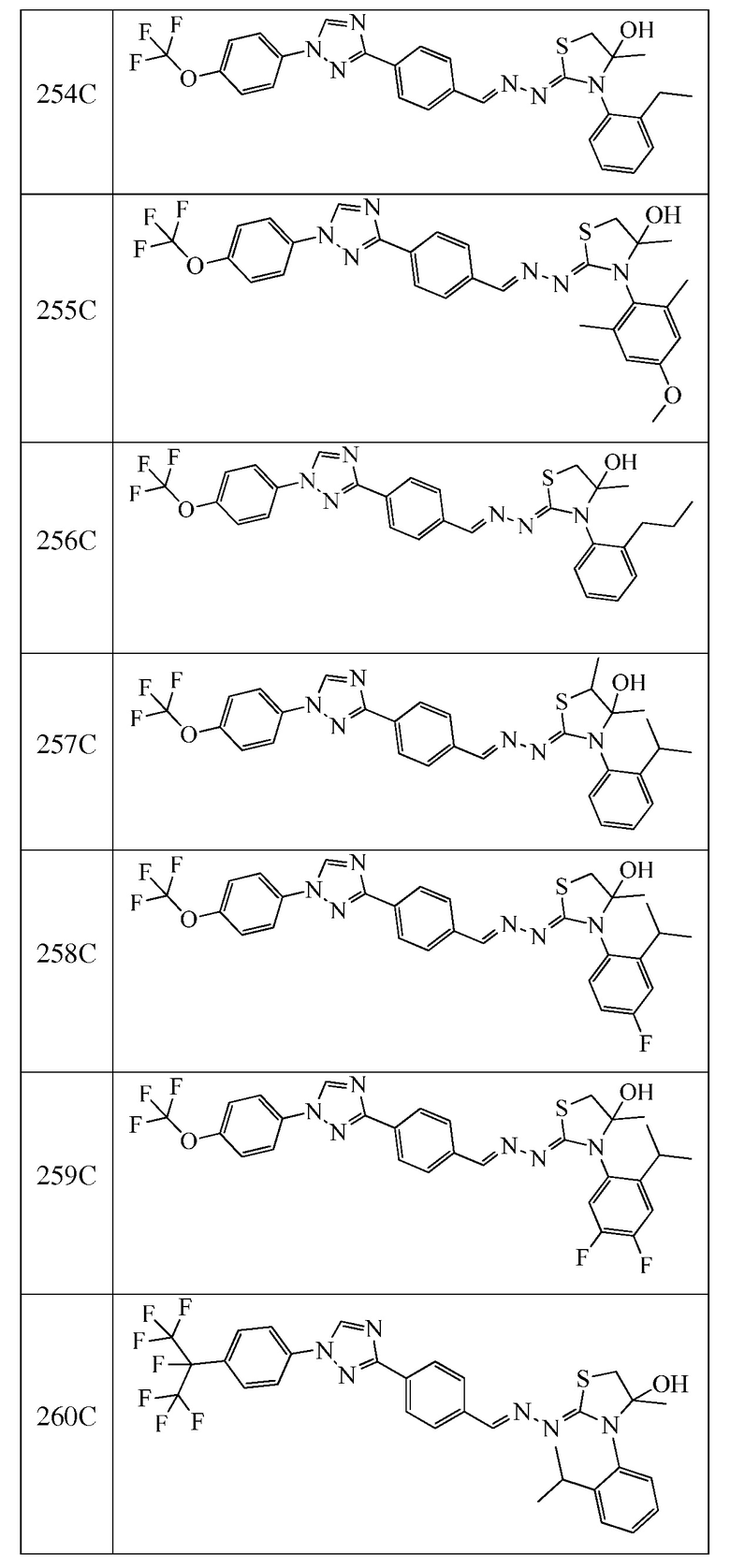
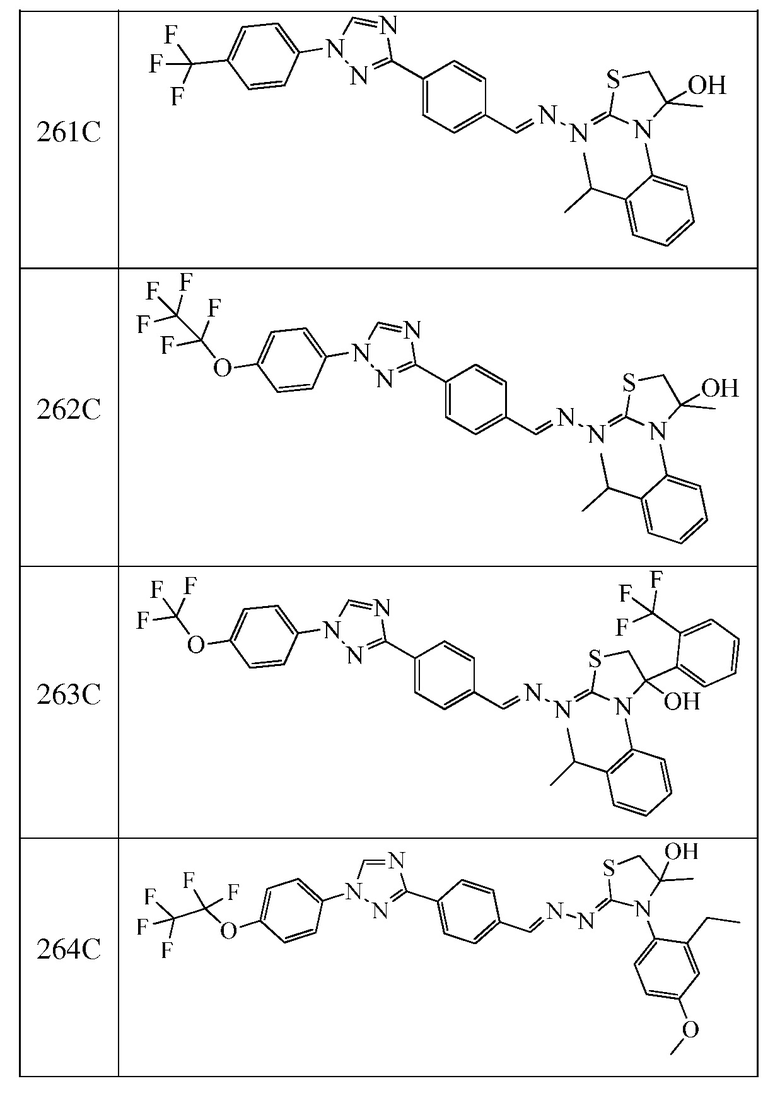
Аналитические данные для соединений таблицы 3
19F ЯМР (376 МГц, CDCl3) δ -58,02, -62,31
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02, -113,71, -115,83, -115,84
19F ЯМР (376 МГц, CDCl3) δ -58,01, -62,05, -62,22
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02, -78,33, -78,77
19F ЯМР (376 МГц, CDCl3) δ -58,03, -78,23, -78,32, -78,76, -78,84
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02, -116,16, -117,35
19F ЯМР (376 МГц, CDCl3) δ -58,03
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02
19F ЯМР (376 МГц, CDCl3) δ -58,02, -112,57
19F ЯМР (376 МГц, CDCl3) δ -58,02, -136,51, -136,57, -138,80, -138,86
19F ЯМР (376 МГц, CDCl3) δ -75,61, -182,14, -182,16, -182,18
19F ЯМР (376 МГц, CDCl3) δ -62,50
19F ЯМР (376 МГц, CDCl3) δ -85,90, -87,85
19F ЯМР (376 МГц, CDCl3) δ -58,02
Спектральные данные ЯМР получали, используя аппарат 400 МГц, если не указано иного.
Аналитические данные для оптически активных соединений таблицы
Спектральные данные ЯМР получали, используя аппарат 400 МГц, если не указано иного.
Биологические результаты
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2012 |
|
RU2597421C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ | 2013 |
|
RU2616808C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ | 2010 |
|
RU2532470C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2012 |
|
RU2592542C2 |
| Соединения, полезные в качестве пестицидов, и промежуточные соединения, композиции и способы, связанные с ними | 2016 |
|
RU2821715C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ | 2010 |
|
RU2534529C2 |
| ЗАМЕЩЕННЫЕ ХРОМАНЫ | 2015 |
|
RU2718060C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ | 2013 |
|
RU2623233C2 |
| ПРОИЗВОДНЫЕ 3-АЛКИЛ-5-ФТОР-4-ЗАМЕЩЕННОГО-ИМИНО-3,4-ДИГИДРОПИРИМИДИН-2(Н)-ОНА В КАЧЕСТВЕ ФУНГИЦИДОВ | 2013 |
|
RU2644014C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СПОСОБЫ, ОТНОСЯЩИЕСЯ К НИМ | 2012 |
|
RU2596946C2 |
Изобретение относится к сельскому хозяйству. Соединение формулы два или три
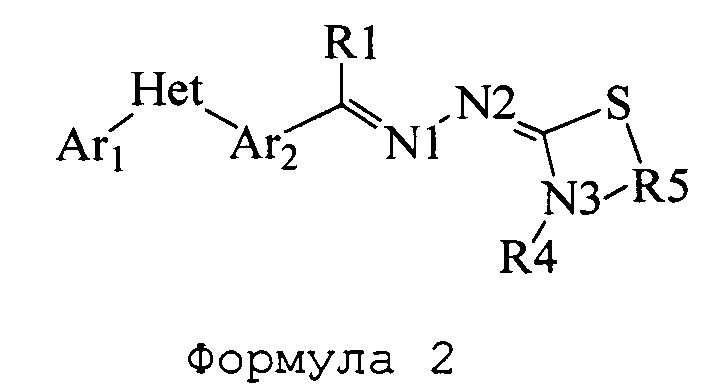
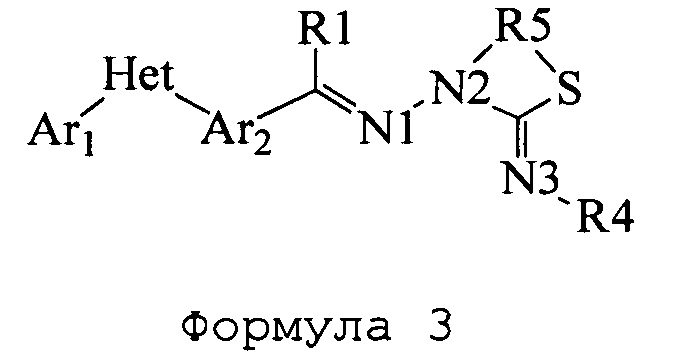
где:
(a) Ar1 представляет собой (1) фуранил, фенил, пиридазинил, пиридил, пиримидинил, тиенил или (2) замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил, или замещенный тиенил или другие заместители, перечисленные в описании. Изобретение позволяет повысить эффективность борьбы с вредителями. 5 н. и 22 з.п. ф-лы, 5 табл.
1. Соединение формулы два или три
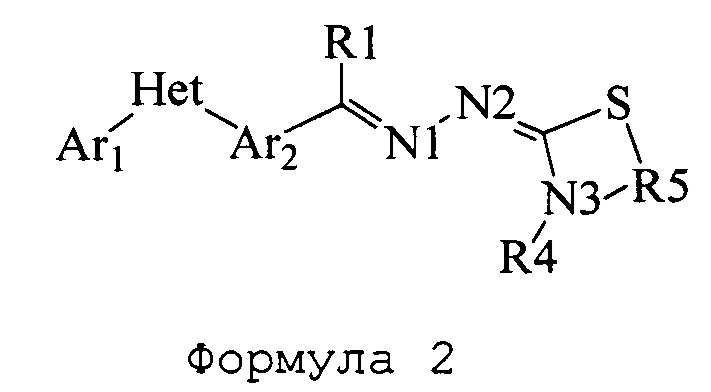
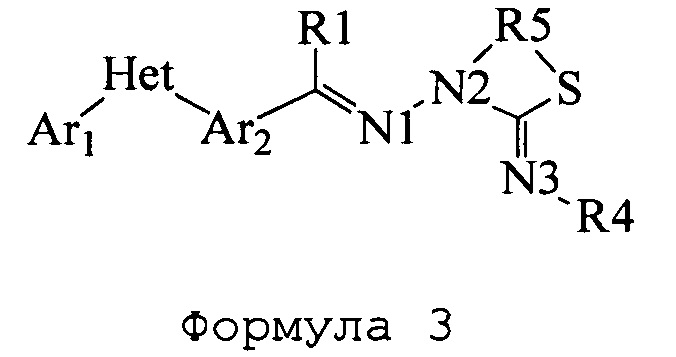
где:
(a) Ar1 представляет собой
(1) фуранил, фенил, пиридазинил, пиридил, пиримидинил, тиенил или
(2) замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил, или замещенный тиенил, где указанный замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил и замещенный тиенил, имеющий один или несколько заместителей, независимо выбранных из Н, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, С(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), С(=O)C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила, фенокси, замещенного фенила и замещенного фенокси,
где такой замещенный фенил и замещенный фенокси имеет один или несколько заместителей, независимо выбранных из Н, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), С(=O)О(C1-C6 алкил), С(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), С(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил) фенила, и фенокси;
(b) Het представляет собой 5- или 6-членное, насыщенное или ненасыщенное, гетероциклическое кольцо, содержащее один или несколько гетероатомов, независимо выбранных из азота, серы или кислорода, и где Ar1 и Ar2 не находятся в орто-положении по отношению друг к другу (но может быть мета или пара, например, для пятичленного кольца они представляет собой 1,3, а для 6-членного кольца они либо - 1,3, либо - 1,4), и где указанное гетероциклическое кольцо также может быть замещено одним или несколькими заместителями, независимо выбранными из Н, F, Cl, Br, I, CN, NO2, оксо, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)O(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила, фенокси, замещенного фенила и замещенного фенокси,
где такой замещенный фенил и замещенный фенокси имеет один или несколько заместителей, независимо выбранных из Н, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), С(=O)Н, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), С(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила и фенокси;
(с) Ar2 представляет собой
(1) фуранил, фенил, пиридазинил, пиридил, пиримидинил, тиенил или
(2) замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил или замещенный тиенил, где указанный замещенный фуранил, замещенный фенил, замещенный пиридазинил, замещенный пиридил, замещенный пиримидинил и замещенный тиенил имеет один или несколько заместителей, независимо выбранных из Н, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил) NRxRy, С(=O)(C1-C6 алкил), С(=O)O(C1-C6 алкил), С(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила, фенокси, замещенного фенила и замещенного фенокси,
где такой замещенный фенил и замещенный фенокси имеют один или несколько заместителей, независимо выбранных из Н, F, Cl, Br, I, CN, NO2, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), С(=O)Н, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), С(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C1-C6 галогеналкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила и фенокси;
(d) R1 выбран из Н, CN, F, Cl, Br, I, C1-C6 алкила, С3-С6 циклоалкила, C3-C6 циклоалкокси, C1-C6 алкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), OSO2(C1-C6 алкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), С(=O)O(C1-C6 алкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила или фенокси,
где каждый алкил, циклоалкил, циклоалкокси, алкокси, алкенил, алкинил, фенил, и фенокси, необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, оксо, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), С(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(С2-С6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила и фенокси;
(g) R4 представляет собой Н, C1-C6 алкил, C3-C6 циклоалкил, C2-C6 алкенил, C2-C6 алкинил, С(=O)Н, С(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), С(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенил, C1-C6 алкилфенил, C1-C6 алкил-O-фенил, C(=O)Het-1, Het-1, C1-C6 алкил Het-1 или C1-C6 алкил-O-Het-1,
где каждый алкил, циклоалкил, алкенил, алкинил, фенил и Het-1 необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, NRxRy, C1-C6 алкил, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2 (C1-C6 галогеналкил), С(=O)Н, C(=O)NRxRy, (C1-C6 алкил)NRxRy, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила, фенокси и Het-1;
(h) R5 представляет собой 2-4-членный насыщенный или ненасыщенный углеводородный линкер, где указанная связь может быть также замещена по меньшей мере одним ОН и, необязательно, одним или несколькими заместителями, выбранными из F, Cl, Br, I, CN, NO2, оксо, NRxRy, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), С(=O)Н, С(=O)OH, C(=O)NRxRy, (C1-C6 алкил)NRxRy, С(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), С(=O)О(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила, фенокси и Het-1,
где каждый алкил, циклоалкил, циклоалкокси, алкокси, алкенил, алкинил, фенил, фенокси и Het-1 необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, оксо, NRxRy, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), С(=O)Н, С(=O)OH, C(=O)NRxRy, (C1-C6 алкил)NRxRy, С(=O) (C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), С(=O)О(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), С(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила, галогенфенила, фенокси и Het-1;
(i) n=0, 1, или 2;
(j) Rx и Ry независимо выбраны из Н, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C2-C6 алкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), С(=O)Н, С(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(С3-С6 циклоалкил), С(=O)O(С3-С6 циклоалкил), С(=O)(С2-С6 алкенил), С(=O)О(С2-С6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил) и фенила,
где каждый алкил, циклоалкил, циклоалкокси, алкокси, алкенил, алкинил, фенил, фенокси и Het-1 необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, Br, I, CN, NO2, оксо, C1-C6 алкила, C1-C6 галогеналкила, C3-C6 циклоалкила, C3-C6 галогенциклоалкила, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенила, C3-C6 циклоалкенила, C2-C6 алкинила, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), С(=O)Н, С(=O)ОН, C(=O)(C1-C6 алкил), C(=O)O(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(C3-C6 циклоалкил), С(=O)O(C3-C6 циклоалкил), С(=O)(C2-C6 алкенил), С(=O)O(C2-C6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), С(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенила, галогенфенила, фенокси и Het-1,
или Rx и Ry вместе могут необязательно образовывать 5-7-членную насыщенную или ненасыщенную циклическую группу, которая может содержать один или несколько гетероатомов, выбранных из азота, серы и кислорода, и где указанная циклическая группа может содержать >С=O или >C=S, и где указанная циклическая группа может быть замещена F, Cl, Br, I, CN, C1-C6 алкилом, C1-C6 галогеналкилом, C3-C6 циклоалкилом, C3-C6 галогенциклоалкилом, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкенилом, C3-C6 циклоалкенилом, C2-C6 алкинилом, S(=O)n(C1-C6 алкил), S(=O)n(C1-C6 галогеналкил), OSO2(C1-C6 алкил), OSO2(C1-C6 галогеналкил), С(=O)(C1-C6 алкил), С(=O)О(C1-C6 алкил), C(=O)(C1-C6 галогеналкил), C(=O)O(C1-C6 галогеналкил), С(=O)(С3-С6 циклоалкил), С(=O)O(С3-С6 циклоалкил), С(=O)(С2-С6 алкенил), С(=O)O(С2-С6 алкенил), (C1-C6 алкил)О(C1-C6 алкил), (C1-C6 алкил)S(C1-C6 алкил), C(=O)(C1-C6 алкил)С(=O)О(C1-C6 алкил), фенилом, замещенным фенилом, фенокси и Het-1; и
(k) Het-1 представляет собой 5- или 6-членное, насыщенное или ненасыщенное, гетероциклическое кольцо, содержащее один или несколько гетероатомов, независимо выбранных из азота, серы или кислорода.
2. Соединение по п. 1, где Ar1 представляет собой замещенный фенил, где указанный замещенный фенил имеет один или несколько заместителей, независимо выбранных из C1-C6 галогеналкила и C1-C6 галогеналкокси.
3. Соединение по п. 1, где Ar1 представляет собой замещенный фенил, где указанный замещенный фенил имеет один или несколько заместителей, независимо выбранных из CF3, OCF3 и OCF2CF3.
4. Соединение по п. 1, где Het выбран из триазолила, имидазолила или пиразолила, которые могут быть замещены или незамещены.
5. Соединение по п. 1, где Het представляет собой 1,2,4-триазолил
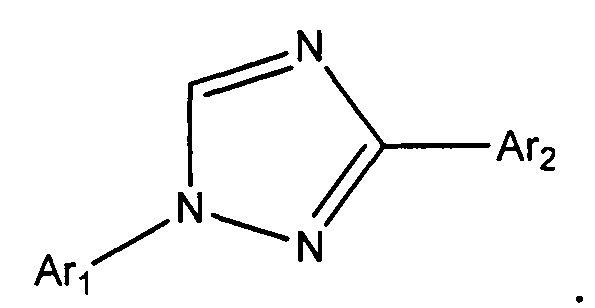
6. Соединение по п. 1, где Het представляет собой 1,4-имидазолил.
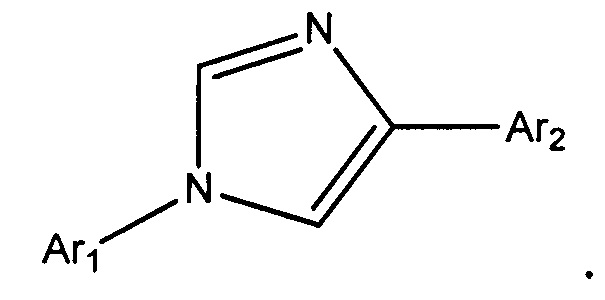
7. Соединение по п. 1, где Het представляет собой 1,3-пиразолил
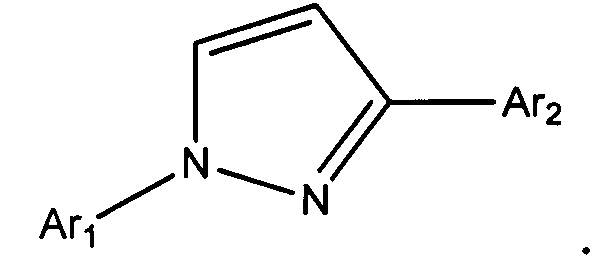
8. Соединение по п. 1, где Het представляет собой замещенный 1,3-пиразолил.
9. Соединение по п. 1, где Het представляет собой 1,4-пиразолил
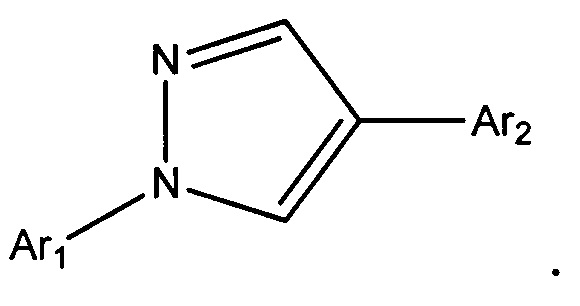
10. Соединение по п. 1, где Ar2 представляет собой фенил.
11. Соединение по п. 1, где R1 представляет собой Н или C1-C6 алкил.
12. Соединение по п. 1, где R1 представляет собой Н или СН3.
13. Соединение по п. 1, где R4 представляет собой фенил, C1-С6 алкилфенил или C1-C6 алкил-О-фенил, где каждый алкил и фенил необязательно замещены одним или несколькими заместителями, независимо выбранными из F, Cl, NRxRy, C1-C6 алкила или C1-C6 алкокси.
14. Соединение по п. 1, где R5 замещен одним ОН и необязательно, один или несколько заместителями, выбранными из C1-C6 галогеналкила и C1-C6 алкила.
15. Соединение по п. 1, где Rx и Ry независимо выбраны из Н и фенил, где указанный фенил может быть необязательно замещен одним или несколькими заместителями, независимо выбранными из F и Cl.
16. Соединение по п. 1, где
Ar1 представляет собой замещенный фенил, где указанный замещенный фенил замещен одним или несколькими C1-C6 галогеналкокси;
Het представляет собой триазолил;
Ar2 представляет собой фенил;
R1 представляет собой Н;
R4 представляет собой фенил, где указанный фенил необязательно замещен одним или несколькими заместителями, независимо выбранными из F, Cl, NRxRy, C1-C6 алкила или C1-C6 алкокси; и
R5 представляет собой 2-4 членный насыщенный или ненасыщенный углеводородный линкер, где указанная связь может быть замещена по меньшей мере одним ОН и, необязательно, одним или несколькими заместителями, выбранными из C1-C6 алкила и C1-C6 галогеналкила; и
Rx и Ry независимо выбраны из Н и фенила, где указанный фенил может быть, необязательно, замещен одним или несколькими заместителями, независимо выбранными из F и Cl.
17. Соединение по п. 1, где Het-1 выбран из бензофуранила, бензоизотиазолила, бензоизоксазолила, бензоксазолила, бензотиенила, бензотиазолил ционнолинила, фуранила, индазолила, индолила, имидазолила, изоиндолила, изохинолинила, изотиазолила, изоксазолила, оксадиазолила, оксазолинила, оксазолила, фталазинила, пиразинила, пиразолинила, пиразолила, пиридазинила, пиридила, пиримидинила, пирролила, хиназолинила, хинолинила, хиноксалинила, тетразолила, тиазолинила, тиазолила, тиенила, триазинила, триазолила, пиперазинила, пиперидинила, морфолинила, пирролидинила, тетрагидрофуранила, тетрагидропиранила, 1,2,3,4-тетрагидрохинолинила, 4,5-дигидрооксазолила, 4,5-дигидро-1Н-пиразолила, 4,5-дигидроизоксазолила и 2,3-дигидро-[1,3,4]-оксадиазолила.
18. Соединение по п. 1, где Het выбран бензофуранила, бензоизотиазолила, бензоизоксазолила, бензоксазолила, бензотиенила, бензотиазолил ционнолинила, фуранила, индазолила, индолила, имидазолила, изоиндолила, изохинолинила, изотиазолила, изоксазолила, оксадиазолила, оксазолинила, оксазолила, фталазинила, пиразинила, пиразолинила, пиразолила, пиридазинила, пиридила, пиримидинила, пирролила, хиназолинила, хинолинила, хиноксалинила, тетразолила, тиазолинила, тиазолила, тиенила, триазинила, триазолила, пиперазинила, пиперидинила, морфолинила, пирролидинила, тетрагидрофуранила, тетрагидропиранила, 1,2,3,4-тетрагидрохинолинила, 4, 5-дигидрооксазолила, 4,5-дигидро-1Н-пиразолила, 4,5-дигидроизоксазолила, и 2,3-дигидро-[1,3,4]-оксадиазолила.
19. Соединение по п. 1, где Het-1 выбран из бензофуранила, бензоизотиазолила, бензоизоксазолила, бензоксазолила, бензотиенила, бензотиазолила, бензотиадизолила, ционнолинила, фуранила, индазолила, индолила, имидазолила, изоиндолила, изохинолинила, изотиазолила, изоксазолила, оксадиазолила, оксазолинила, оксазолила, фталазинила, пиразинила, пиразолинила, пиразолила, пиридазинила, пиридила, пиримидинила, пирролила, хиназолинила, хинолинила, хиноксалинила, тетразолила, тиазолинила, тиазолила, тиенила, тиенилпиразолила, триазинила, триазолила, пиперазинила, пиперидинила, морфолинила, пирролидинила, тетрагидрофуранила, тетрагидропиранила, 1,2,3,4-тетрагидрохинолинила, 4,5-дигидрооксазолила, 4,5-дигидро-1Н-пиразолила, 4,5-дигидроизоксазолила и 2,3-дигидро-[1,3,4]-оксадиазолила.
20. Соединение по п. 1, где Het-1 выбран из бензотиадизолила, фуранила, оксазолила и тиенилпиразолила.
21. Соединение по п. 1, где указанная молекула выбрана из
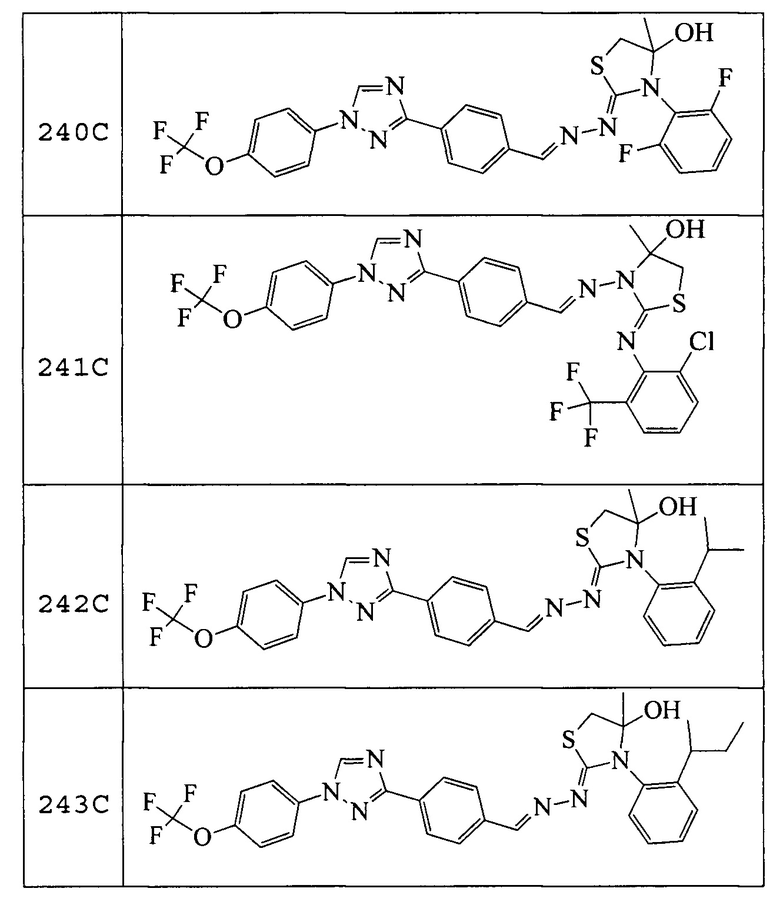
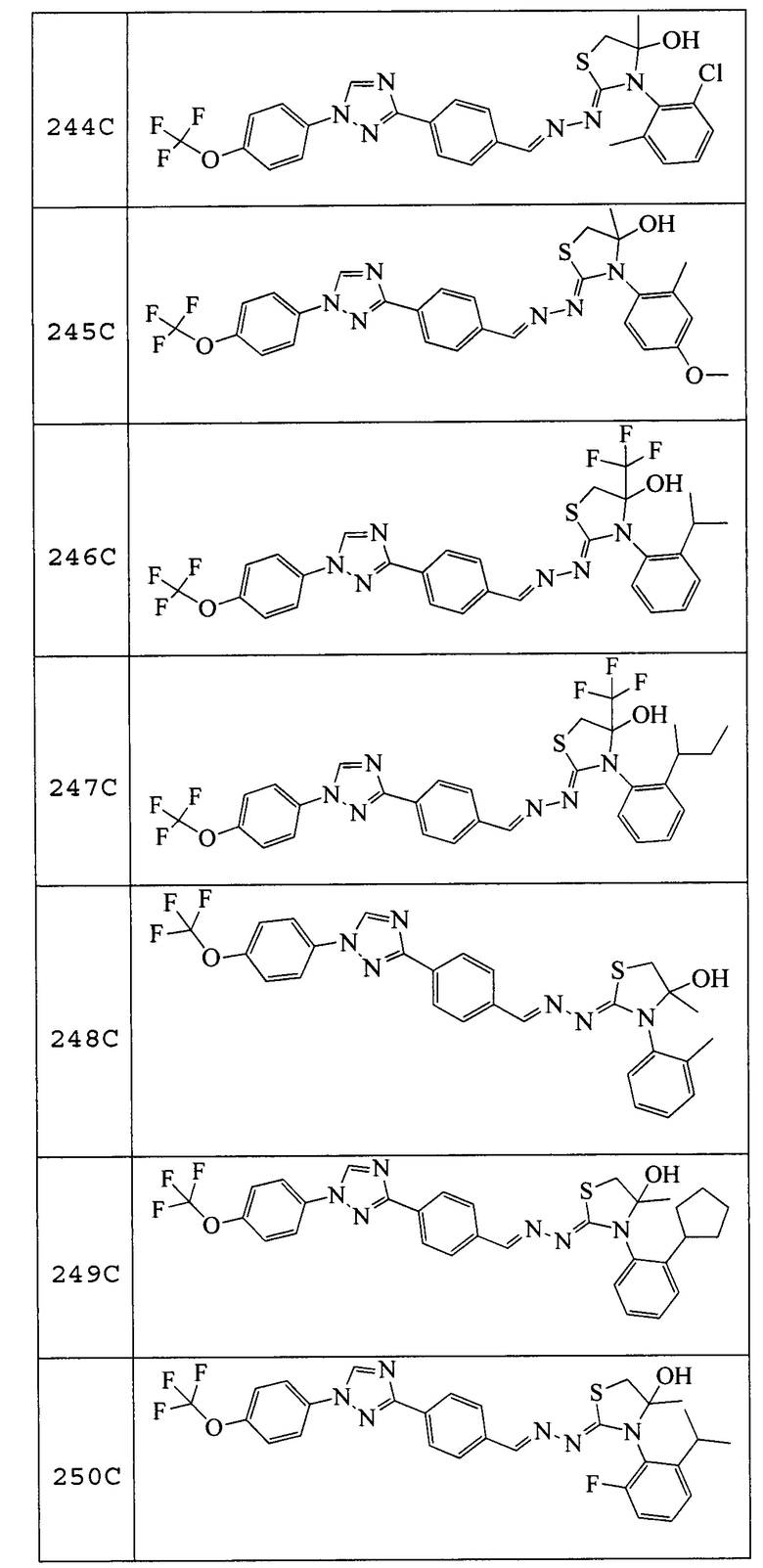
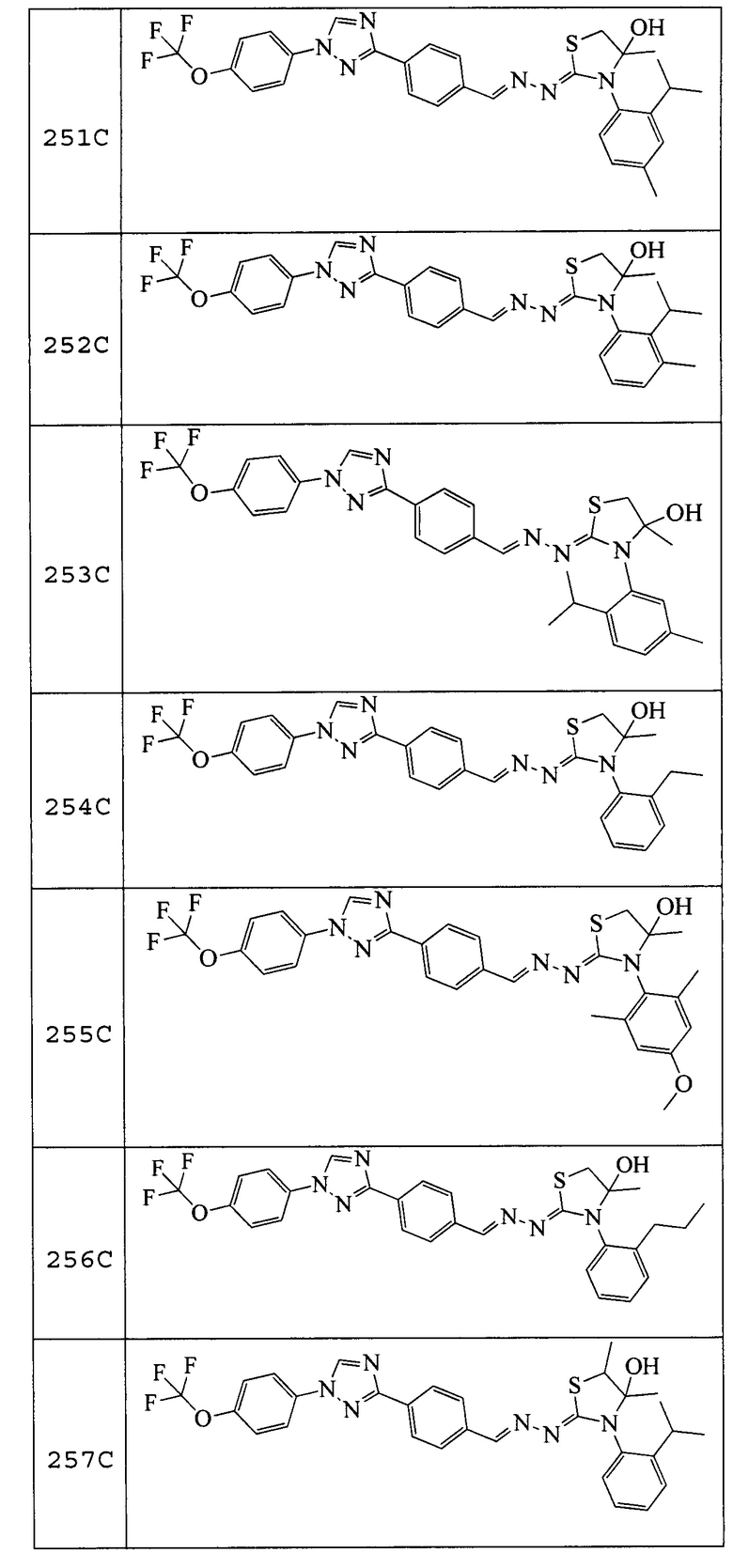
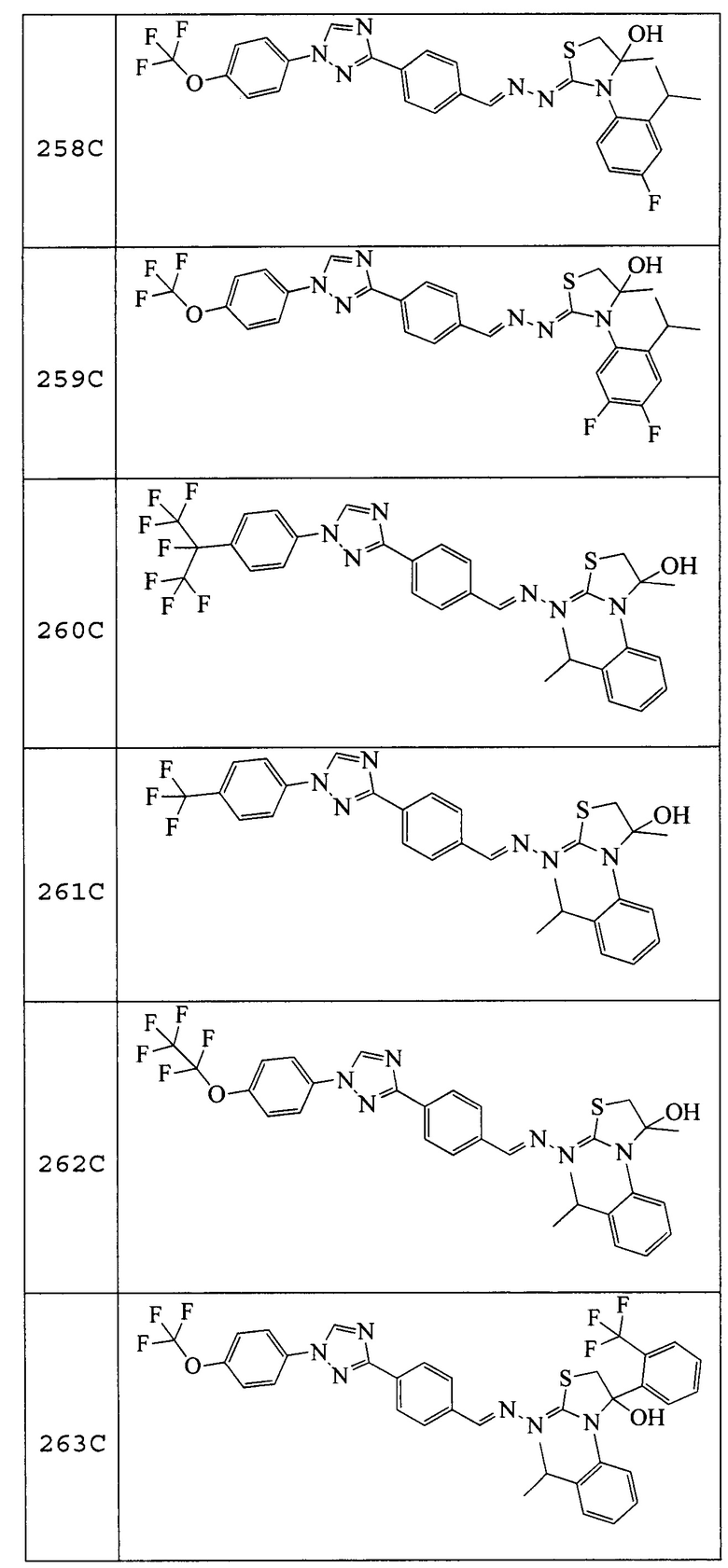
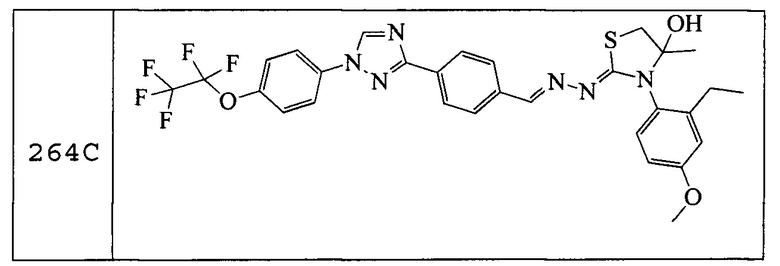
22. Способ применения соединения по п. 1, где указанный способ включает нанесение соединения по п. 1 на область для борьбы с вредителем в количестве, достаточном для уничтожения такого вредителя.
23. Способ по п. 22, где указанное соединение выбрано из
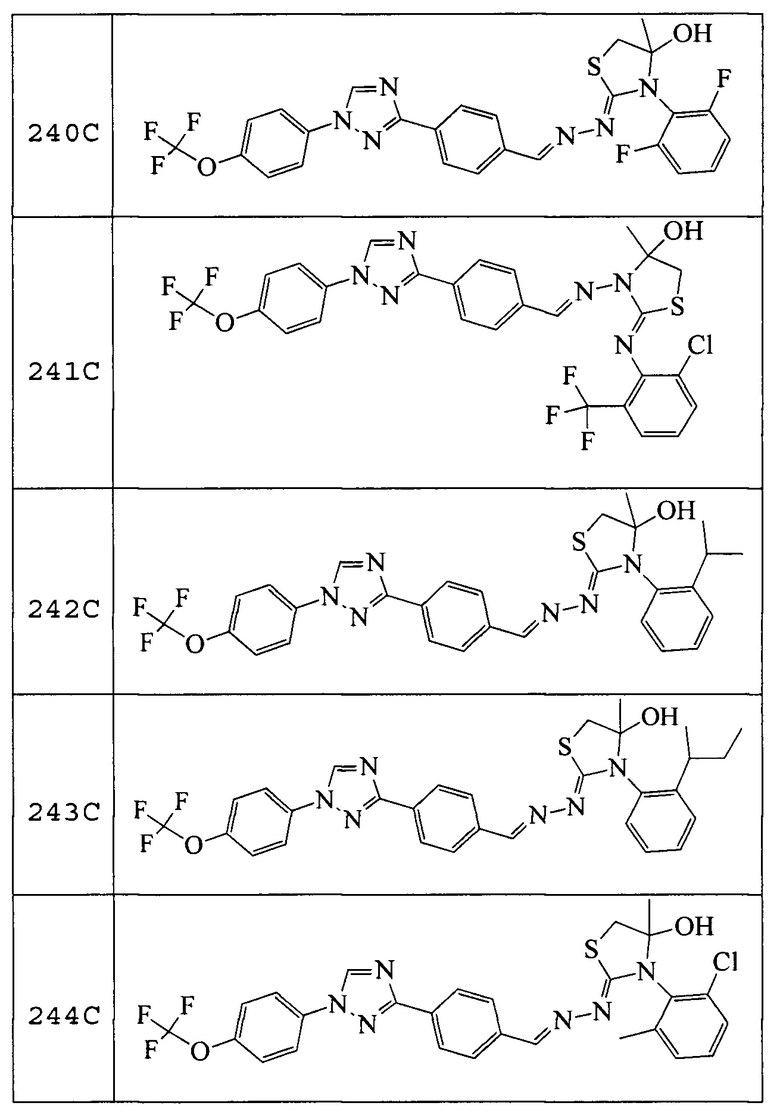
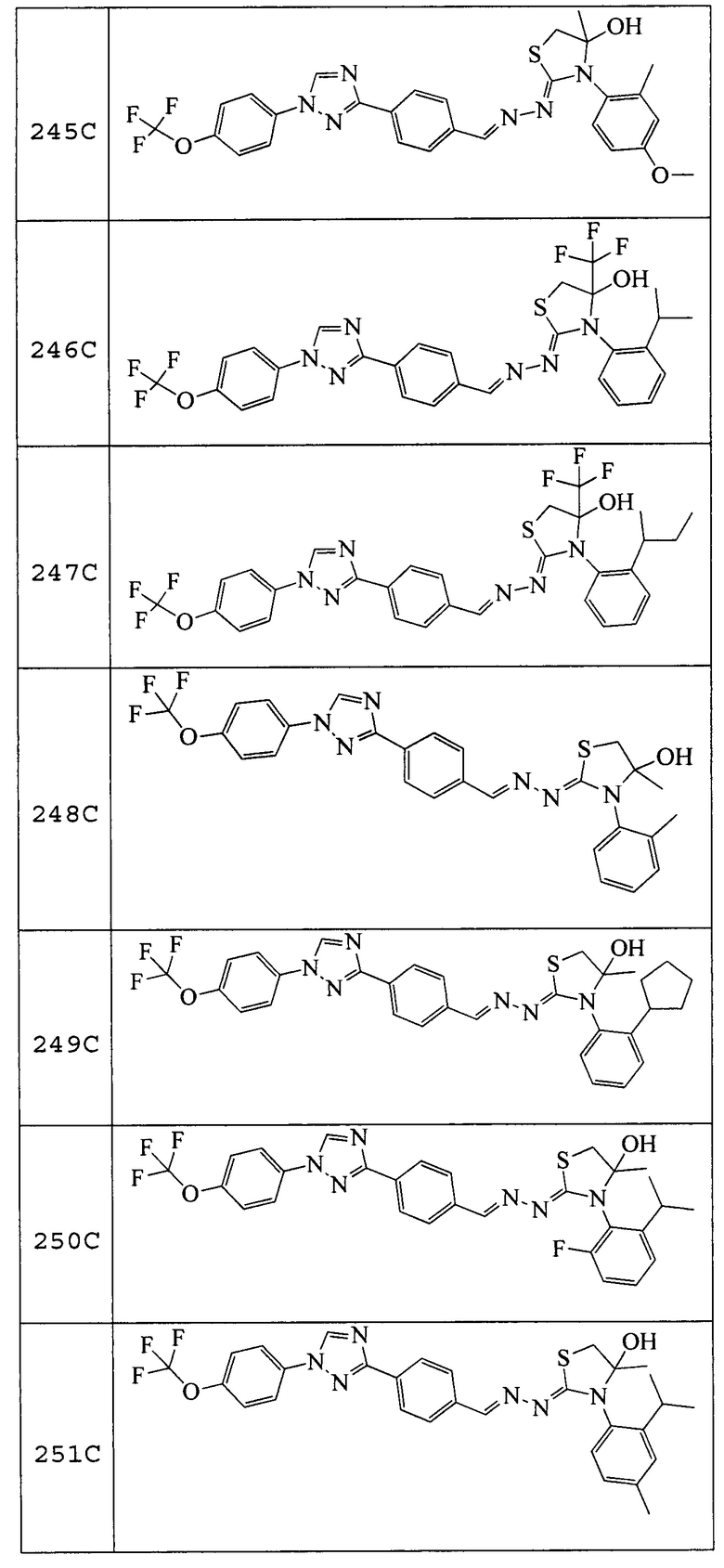
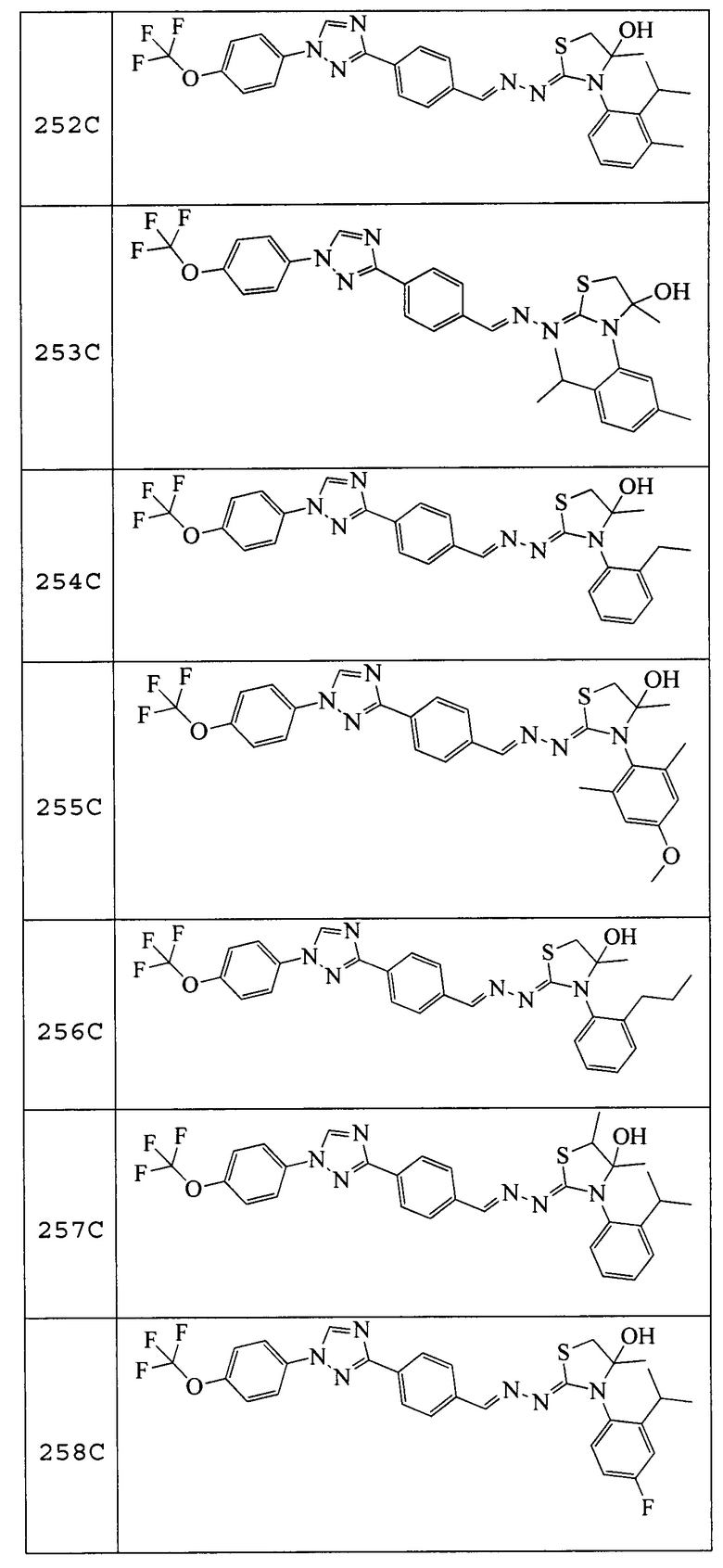
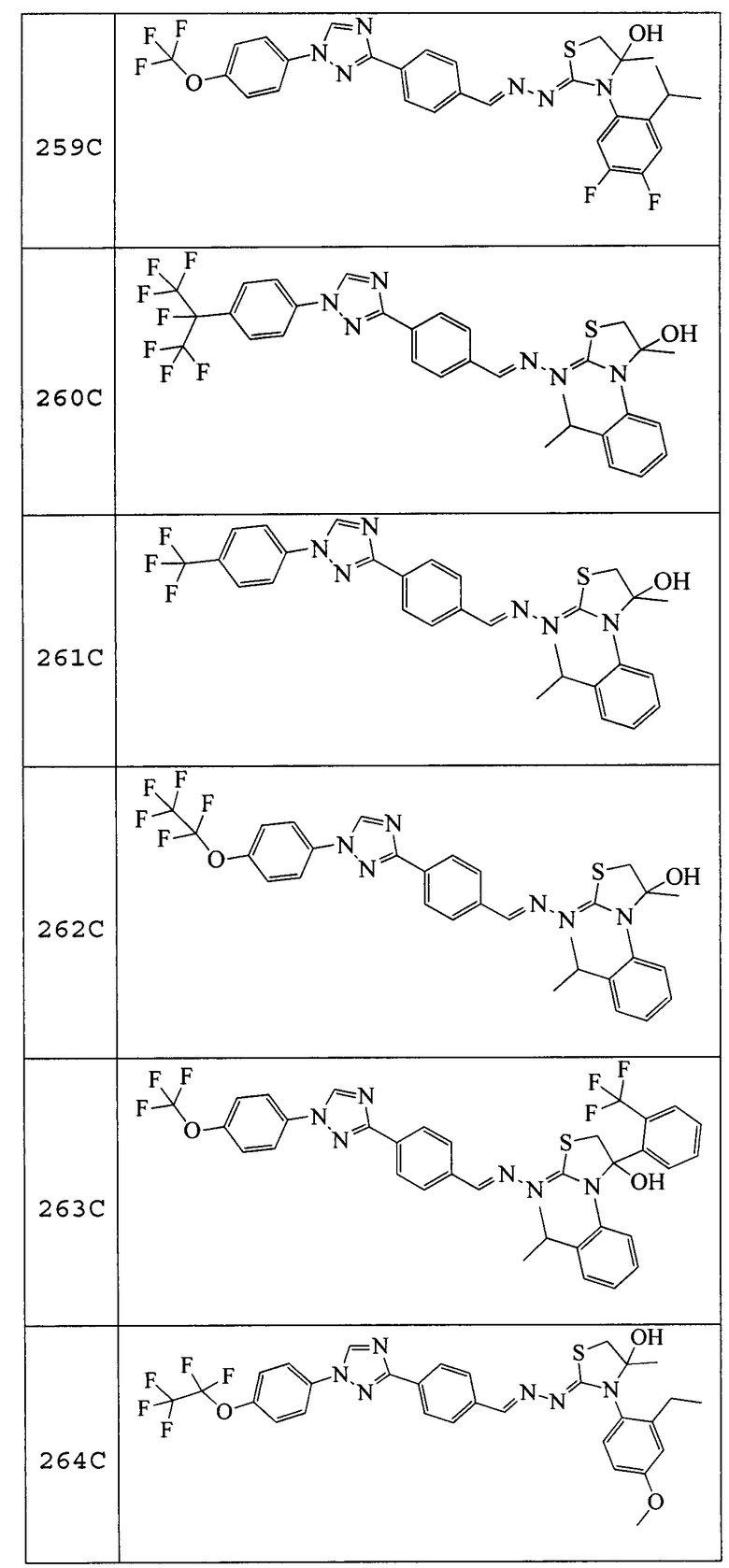
и указанный вредитель представляет собой совку малую (BAW), совку хлопковую (CEW) или тлю персиковую GPA.
24. Способ по п. 22, где указанная область представляет собой область роста яблок, кукурузы, хлопка, соевых бобов, канола, пшеницы, риса, сорго, ячменя, овса, картофеля, апельсинов, люцерны, салата, клубники, помидоров, перца, крестоцветных, груш, табака, миндаля, сахарной свеклы или бобов, или область посадки их семян.
25. Композиция, содержащая пестицидно приемлемую кислотно-аддитивную соль, производное соли, сольват или производное сложного эфира соединения по п. 1.
26. Композиция, содержащая полиморф соединения по п. 1.
27. Композиция, содержащая соединение по п. 1, где по меньшей мере один Н представляет собой 2Н или по меньшей мере один С представляет собой 14С.
| Колосоуборка | 1923 |
|
SU2009A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| ГЕРБИЦИДНАЯ КОМБИНАЦИЯ, СПОСОБ БОРЬБЫ С СОРНЫМИ РАСТЕНИЯМИ | 1999 |
|
RU2261598C9 |
Авторы
Даты
2017-04-18—Публикация
2013-01-23—Подача