Область техники, к которой относится изобретение.
Предлагаемое изобретение относится к медицине, может быть использовано для получения биологически активных фракций из сыворотки крови птиц, полезной при онкологических заболеваниях и расстройствах в организме человека и животных.
Уровень техники.
Широко известны способы получения биологически активной сыворотки крови, основанные на взятии крови у доноров и животных, инкубации, отделении с последующим консервированием. Способы предполагают получение сыворотки крови, повышающей устойчивость организма к таким экзогенным и эндогенным факторам, как атмосферное давление, температура, сила тяжести, свет и т.п., а также голод, жажда, сонная и половая потребности и т.п. (патент Японии №2123287, ЕР 0542303 А2, патенты России №2096041, 2120301, 2236238, 2302237).
Биологически активную фракцию получают из сыворотки крови птиц, предварительно введенных в электрошок II-III степени и подвергают гамма-обработке с использованием Со60 (патенты 2236238, 2302238 РФ).
Задачей данного изобретения было получение антионкологически активных фракций из электрошоковой сыворотки крови кур и облученной в линейном ускорителе электронов (ЛУЭ).
Краткое изложение сущности изобретения.
Оказалось, что если электрошоковую сыворотку крови птиц облучить в ЛУЭ в интервале 22-32 кГр, то можно получать биологически активные пептидные фракции, обладающие актионкологической активностью (будут раскрыты далее), которые полезны при некоторых видах рака пациента (будут раскрыты далее).
Таким образом, целью настоящего изобретения является разработка нового способа получения антионкологически активных фракций.
Еще одной целью настоящего изобретения является разработка лекарственной формы новых биологически активных фракций. Изобретение предполагает разные лекарственные формы: в том числе для перорального, парентерального, назального, буккального, в виде суппозитариев и т.п. введения.
В изобретении предусматривается использование подходящих физиологически приемлемых носителей (таких как дистил. вода, физиол. р-р), наполнителей (например, масло какао, витепсол) биологически активных фракций. Биологически активные пептидные фракции могут применяться как самостоятельно, так и в сочетании с другими лечебными средствами.
Дополнительной целью изобретения является фармацевтическая композиция, в которой активным началом является фракции согласно настоящему изобретению. При этом фармацевтическая композиция должна содержать активный ингредиент в количестве, достаточном для оказания благоприятного воздействия на организм пациента, т.е. содержать его в эффективном количестве.
Еще одной целью изобретения является определение эффективной дозы пептидных фракций согласно данному изобретению. Полагается, что эта доза находится в интервале от 2,5 мг/мл до 20 мг/мл опухолевых клеток пациента. Очевидно, что конкретная доза будет определяться лечащим врачом в зависимости от состояния пациента, его возраста, веса и курса лечения.
Подробное раскрытие изобретения.
Далее изобретение подробно раскрывается в предпочтительных вариантах конкретного выполнения, при этом приводимые примеры активных пептидных фракций, фармацевтических композиций, лекарственных форм не должны стать основанием для ограничения притязаний, а предназначены исключительно лишь для демонстрации осуществимости изобретения и реализации указанного(ных) назначения (ий). Каждый специалист в данной области безусловно убедится, что могут быть предложены многочисленные модификации приводимых вариантов выполнения изобретения, которые подпадают под притязания, отраженные далее в формуле изобретения.
1. Получение биологически активных фракций.
Для получения биологически активных фракций использовали кровь птиц (кур), взятую через 3-4 с после электростимуляции головы в течение 3-4 с током напряжением 100-120 В и 3-4 А. Кровь собирали самотеком в полиэтиленовые флаконы после перерезки сонных артерий и вен и инкубируют при температуре 4-8°С в течение 18-24 ч, сыворотку отсасывали, лиофилизировали и облучали в режиме 27±5,0 кГр.
Обработанную сыворотку разводили дистиллированной водой в концентрации 100 мг/мл (фракция 1) и центрифугировали раствор фракции 1 при 10000×g в течение 3 минут (фракция 2).
1.Доказательства биологической активности фракций.
Были использованы клетки Т-клеточной лимфомы человека линии Jurkat, В-клеточной лимфомы человека линии Raji, клетки меланомы человека линии Вrо В-19, клетки карциномы шейки матки линии HeLa, клетки аденокарциномы молочной железы линии MCF-7, клетки остеосаркомы линии Mg63 и фибросаркомы линии НТ1080, клетки нейробластомы IMR-32 и гепатокарциномы линии HepG2, т.е. изучено действие субстанции на лимфоидных клетках (Jurkat и Raji), клетках эпителиального происхождения (HeLa и MCF-7), клетках нейронального происхождения (IMR-32), клетках соединительной ткани (Mg63 и НТ1080) и клетках мезенхимального происхождения (HepG2). В качестве нормальных клеток использованы стимулированные in vitro лимфоциты периферической крови человека.
Культивирование клеток. Клетки линий Jurkat,Raji и лимфоциты периферической крови человека культивировали в пластиковых матрасах (Nunc или Falcon) в среде RPMi 1640 (Sigma) с добавлением 10% фетальной сыворотки крупного рогатого скота (Gibco), 100 ед/мл пенициллина и 100 мкг/мл стрептомицина при температуре 37°С в СО2 - инкубаторе при содержании СO2 5% и влажности 95%. Клетки линий Bro B-19, HeLa, MCF-7, Mg63, НТ1080, IMR-32 и HepG2 культивировали также, но в среде DMEM (Sigma).
Выделение мононуклеарных лейкоцитов (МЛ) по методу Boyum [1].
В 2 конические пробирки на 50 мл (Falcon) помещают по 15 мл раствора фиколл-пак и наслаивают на него по 25 мл разведенной в два раза фосфатно-солевым буфером (ФСБ) крови. Пробирки центрифугируют в бакет-роторе 30 мин при 400×g при 20°С. Верхнуюю фазу, содержащую плазму, отбрасывают. Моноклеарные лейкоциты (МЛ), концентрирующиеся в виде кольца на границе раздела между плазмой и средой разделения, собирают в коническую центрифужную пробирку, осторожно отсасывая пипеткой, промывают два раза ФСБ, центрифугируя суспензию 10 мин при 250×g и суспендируют в культуральной среде. Эта фракция содержит 10-30% моноцитов и 80-90% лимфоцитов. Далее мы ее называем лимфоциты. Часть лимфоцитов использовали для исследования митогенной активности изучаемого препарата, а часть стимулировали к пролиферации, добавляя к клеточной суспензии фитогемаглютинин (ФГА) в концентрации 20 мкг/мл.
Определение интенсивности биосинтеза ДНК в клетках. Интенсивность биосинтеза ДНК определяли по включению 3Н-тимидина в кислотонерастворимую фракцию клеток. Для этого лимфоциты культивировали в 96-луночных плашках в 200 мкл среды по 200-800 тысяч/лунку, в полной среде с различными концентрациями исследуемой субстанции. 3H-тимидин (1 мкКи/лунку, 40 мКи/ммоль) вносили за 2 часа до окончания инкубации. Для радиометрии клетки собирали на фильтры с помощью автоматического устройства для сбора клеток, отмывали кислоторастворимые продукты 5% ТХУ (или Н20) и измеряли их радиоактивность на сцинцилляционном счетчике. Интенсивность биосинтеза ДНК выражали в им/мин.
Определение выживаемости клеток после инкубации с различными препаратами с помощью МТТ [2]. Для проведения теста клетки собирали в логарифмической фазе роста (для прикрепляющихся клеток - когда клетки занимают примерно половину площади матраса для культивирования), переносили в культуральную среду, подсчитывали в камере Горяева и суспендировали в культуральной среде в концентрации 50-100 тысяч в 1 мл. Суспензию клеток вносили по 100 мкл в 96-луночные плашки после добавления в них различных концентраций исследуемых веществ, клеток в различных лунках 96-луночные плашки после добавления в них различных концентраций исследуемых веществ. После окончания инкубации для количественного определения живых клеток в различных лунках 96-луночных плат по все лунки платы добавляли по 500 мкл раствора МТТ (бромид 3-4,5-диметилтиазол 0 2-ил)-2,5-дифенилтетразолия) в культуральной среде. Для приготовления рабочего раствора МТТ 1 мл исходного раствора МТТ смешивают с 4 мл культуральной среды. Исходный раствор МТТ готовят, растворяя этот реактив в фосфатно-солевом растворе (ФСБ, 0,01 М натрий фосфатный буфер рН 7.4, содержащий 0,15 М NaCl) в концентрации 5 мг МТТ/мл ФСБ, фильтруют через фильтр с диаметром пор 0,45 мкм и хранят при +4°С до 1 месяца). После добавления раствора МТТ продолжают инкубацию плат в тех же условиях еще 4 часа, затем удаляют культуральную среду, отсасывая ее с помощью насоса, добавляют в лунки по 150 мкл диметилсульфоксида (ДМСО) для растворения образовавшихся синих кристаллов формазана и измеряют оптическую плотность раствора в каждой лунке на многоканальном спектрофотометре для микроплат (Labsystem) при длине волны 540 нм. Полученные результаты выживаемости клеток в заисимости от концентрации субстанции представляют в процентах от выживаемости контрольных клеток. Обработку данных проводили с использованием компьютерной программы «Origin».
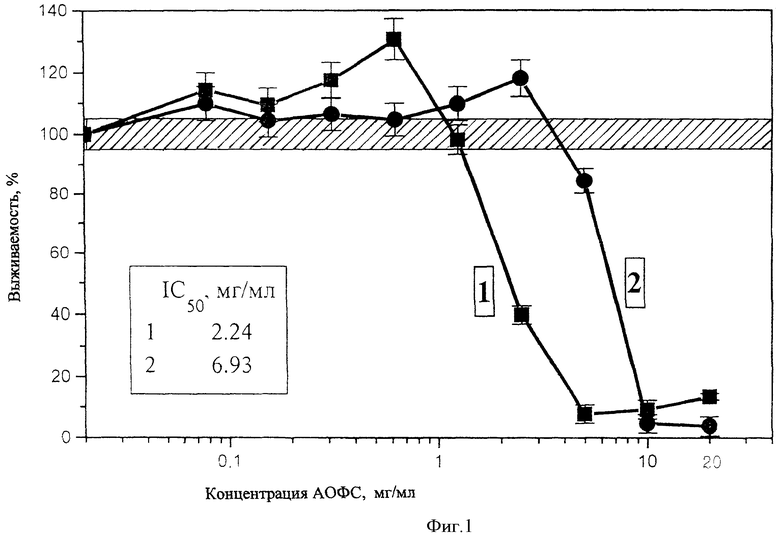
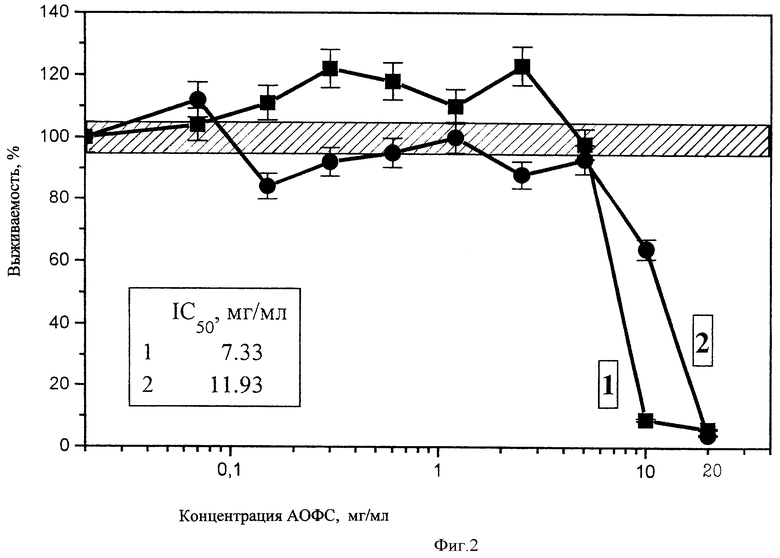
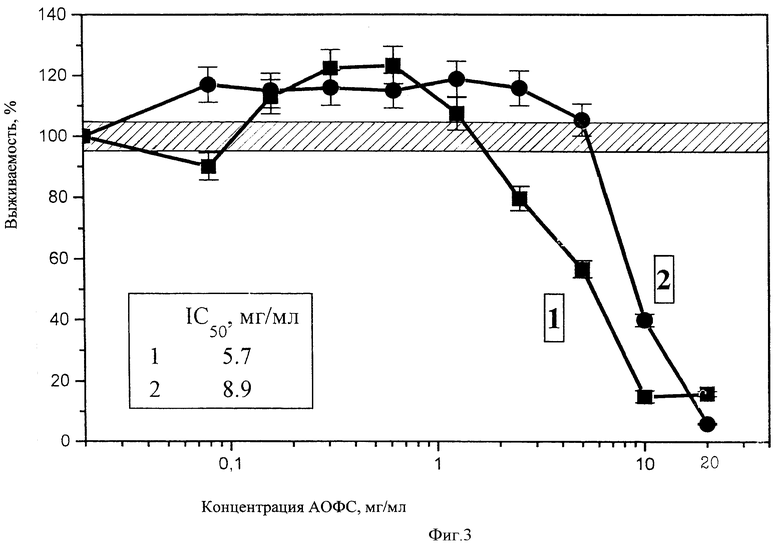
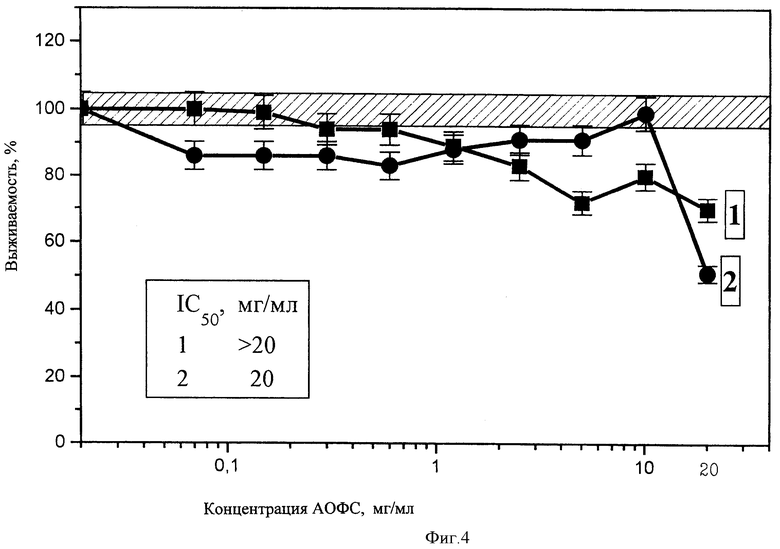
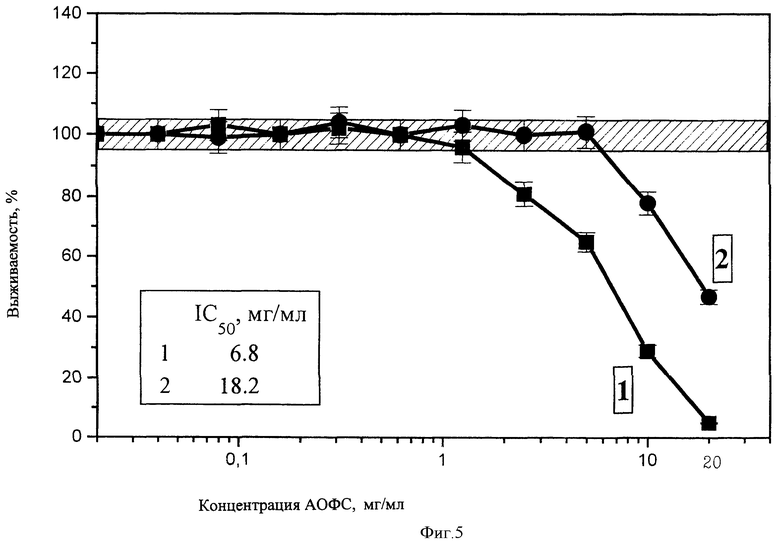
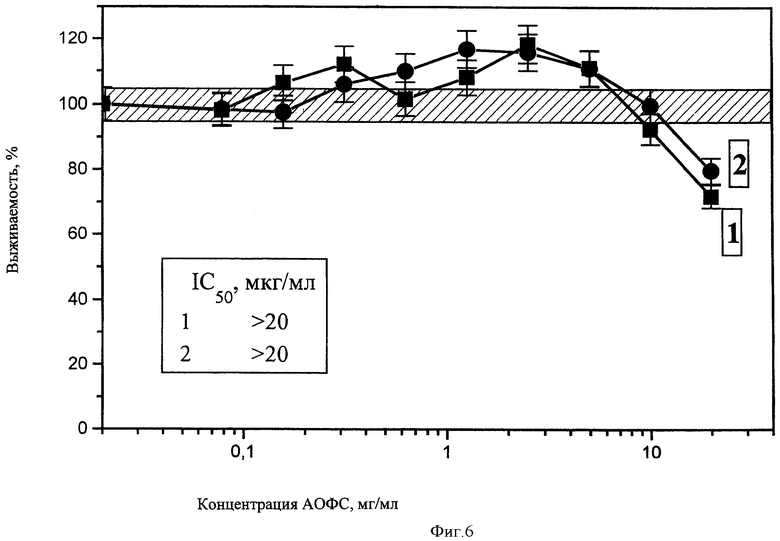
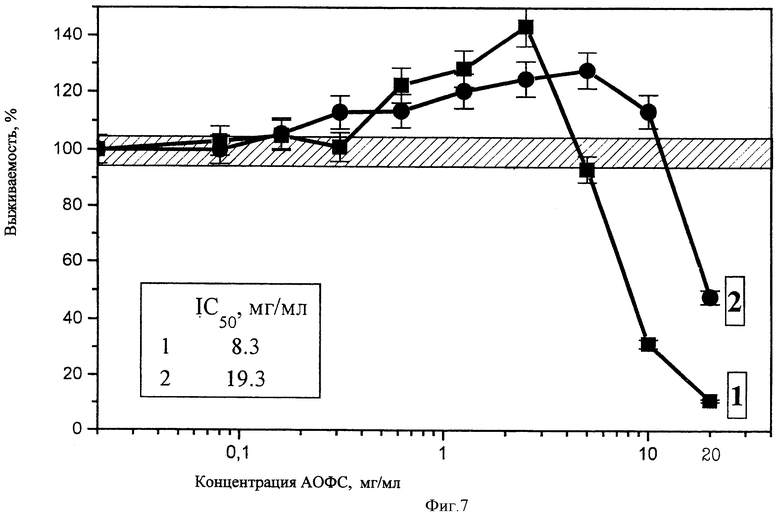
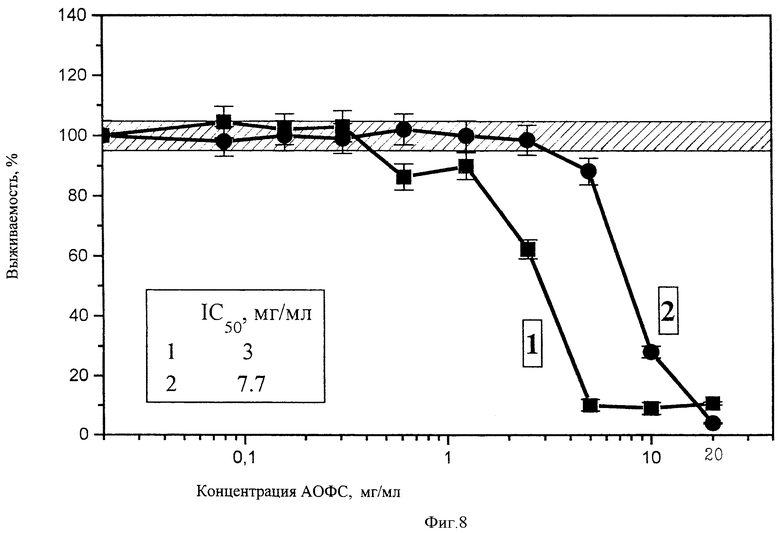
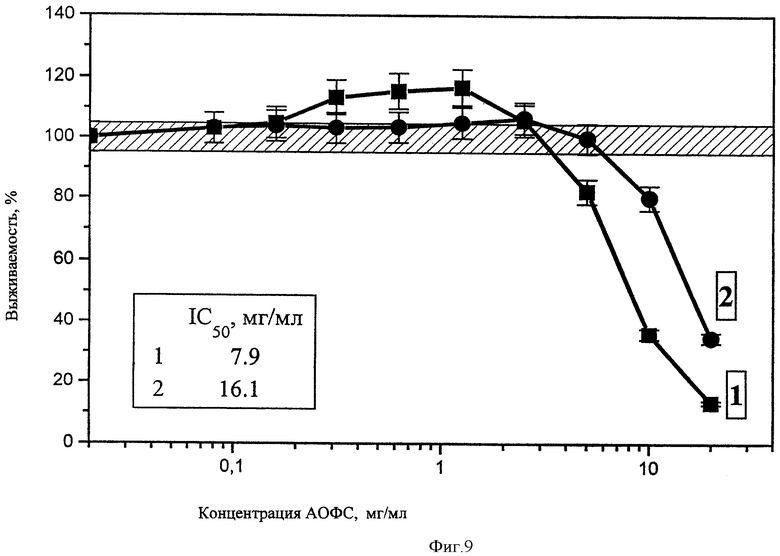
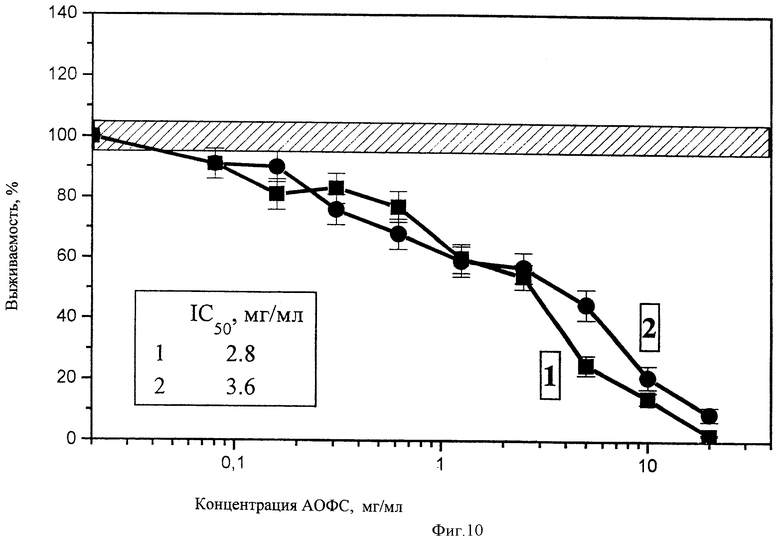
Полученные результаты приведены на чертежах 1-14. Из них следует, что фракции 1 и 2 в высоких концентрациях (2,5-20 мг/мл) оказывает на все клетки ингибирующее действие, однако чувствительность клеток разных тканей к этим фракциям различна. Доза IC50 (концентрация субстанции, вызывающая ингибирование пролиферации клеток на 50%, варьирует для разных линий клеток от 2,2 (Jurkat) до>20 мг/мл (Mg63) для фракции 1 от 3,6 (лимфоциты периферической крови) до>20 мг/мл (Mg63 и HeLa) для фракции 2. Для всех линий клеток токсичность фракции 1 выше, чем фракции 2. Однако интересно отметить, что для одних линий токсичность этих форм была почти одинакова (Mg63, Raji, лимфоциты периферической крови), а для других (Jurkat, MCF-7, IMR-32) различалась по IC050 в 2-3 раза. Сопоставление чувствительности клеток к изучаемой субстанции по сравнению с известным противоопухолевым препаратом - доксорубицином приведены в табл.1.
Обнаружено также, что в определенном диапазоне концентраций (от 0,3 до 3 мг/мл) в зависимости от линий клеток и формы фракций он оказывает стимулирующее действие на отдельные клетки. Стимулирующее действие обнаружено в отношении клеток Jurkat, Вrо В-19, Mg63, HT1080 и HepG2. Эффект стимуляции был незначительным, но наблюдался при действии обеих фракций. На клетках линий HeLa, MCF-7, IMR-32 и лимфоцитах периферической крови стимулирующий эффект отсутствовал. Стимулирующее действие фракции 1 в виде суспензии наблюдалось в более низких концентрациях, чем фракции 2. Не исключено, что наблюдаемая стимуляция обусловлена не собственно активацией пролиферации, а усилением дыхания клеток, что также будет регистрироваться при используемом методе оценки выживаемости клеток.
При исследовании взаимодействия различных веществ с иммунокомпетентными клетками, как правило, решаются 2 вопроса:
1. Обладает ли исследуемое вещество митогенной активностью, т.е. способно ли оно стимулировать пролиферацию лимфоцитов (в данном случае рост их числа, что обычно определяется по усилению биосинтеза ДНК-лимфоцитов, оцениваемое по включению 3H-тимидина).
2. Токсично ли исследуемое вещество для лимфоцитов (это обычно оценивают по ингибированию пролиферации лимфоцитов, предварительно стимулированных митогенами по включению 3Н-тимидина или с помощью витальных красителей типа МТТ).
Следует отметить, что неактивированные лимфоциты в культуре не профелируют, а при действии митогенов увеличиваются в числе с ростом концентрации митогена и это отражается в увеличении количества меченого ДНК.
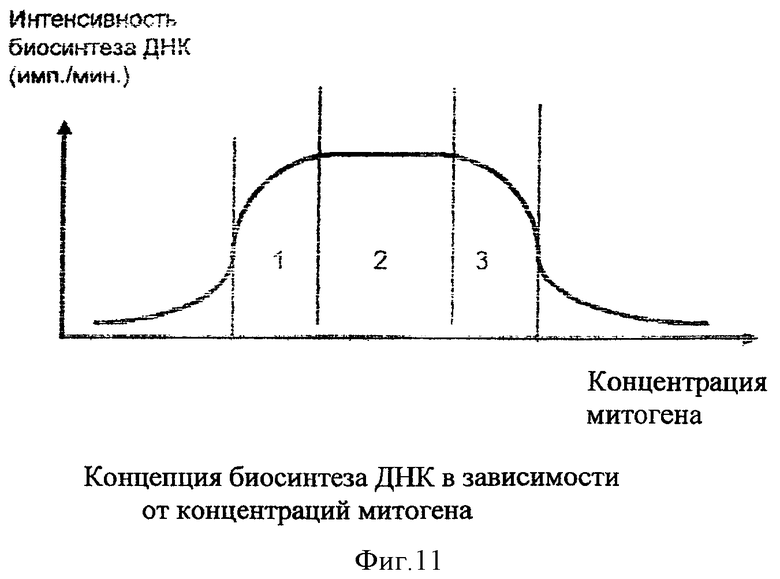
В целом, при действии митогенов на лимфоциты зависимость эффекта от дозы описывается кривой в форме «колокола» (фиг.11). Участок (1) кривой отражает тот диапазон концентрации митогена, при котором нарастающий эффект (интенсивность биосинтеза ДНК) пропорционален концентрации миогена. Второй участок кривой (2) отражает фазу «плато», он охватывает диапазон концентраций митогена, когда уже достигнут максимальный эффект, и рост концентраций митогена не сопровождается изменением достигнутого уровня пролиферации, но еще нет цитотоксического действия. Участок(3) отражает диапазон концентраций митогена, в которых он уже оказывает токсичный эффект.
Оценка митогенной активности фракций осуществлялась в двух экспериментах.
1.Определялось влияние фракций на неактивированные лимфоциты периферической крови человека, при этом изучалось зависимость пролиферативной активности (эффект) от дозы.
2. Определялось влияние фракций на интенсивность биосинтеза ДНК активированных фитогемаклютинином - (ФГА 20 мкг/мл) лимфоцитов и находящихся в стадии 2.
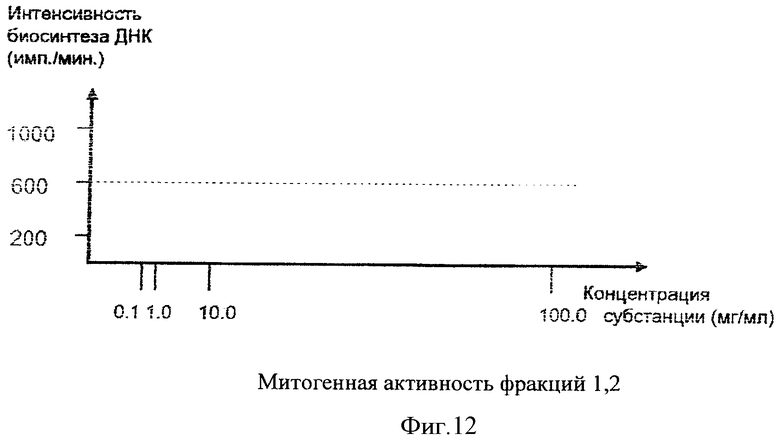
При исследовании фракций митогенной активности не обнаружили, т.е. в исследованном диапазоне концентраций (0,1-100,0 мг/мл) стимуляции биосинтеза ДНК лимфоцитов периферической крови не наблюдали (12).
Таким образом, вне зависимости от дозы субстанции пролиферация лимфоцитов периферической крови существенно не изменялось.
При исследовании действия фракций на активированные митогеном ФГА 20 мкг/мл лимфоциты обнаружено ингибирование пролиферации активированных лимфоцитов.
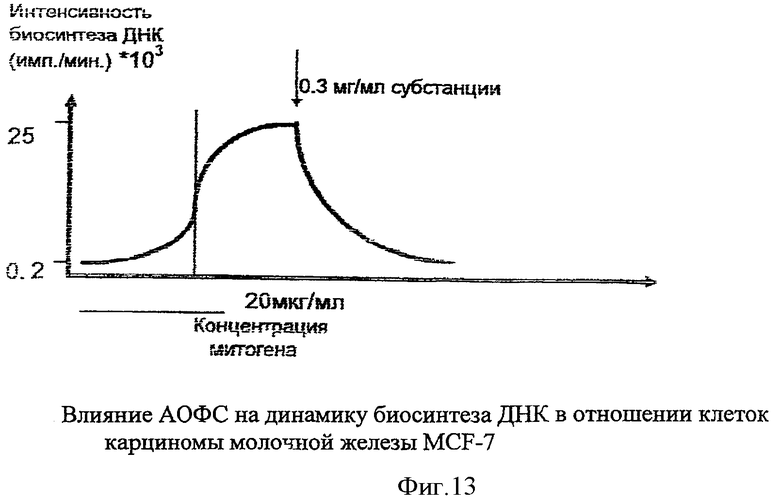
Таким образом, на стимулированных лимфоцитах обнаружено, что в концентрациях более 0,3 мг/мл фракции обладает способностью ингибировать биосинтез ДНК стимулированных лимфоцитов (фиг.13), однако вопрос о механизме реализации этого эффекта остается открытым. Представляется важным исследование цитостатического и собственно цитотоксического действия по отношению к опухолевым клеткам человека.
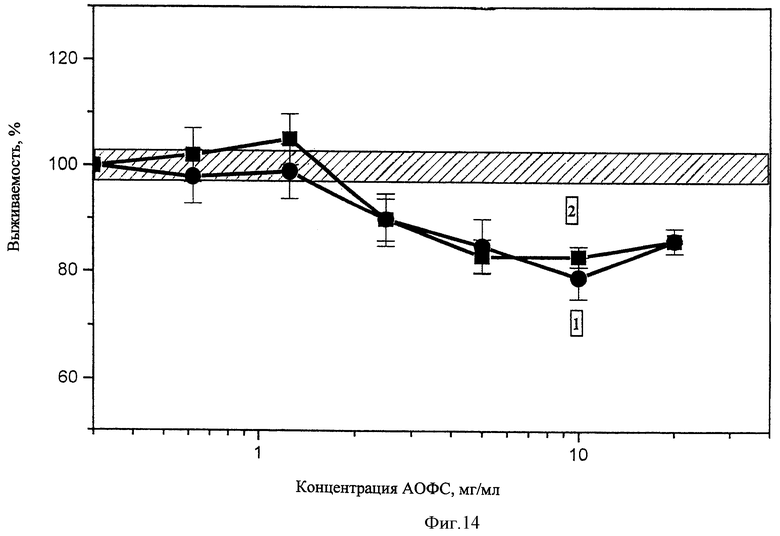
Кроме лимфоцитов, исследовали цитоксическую активность фракций при добавлении к клеткам карциномы молочной железы линии MCF-7, находящимся в состоянии монослоя. При этом наблюдали отсутствие пролиферации из-за контактного торможения клеток. В такой модели можно оценить токсическое действие субстанции, т.е. отделить его от цитостатического действия. При использовании этой модели (14) было обнаружено, что субстанция в виде 1 и 2 фракций обладают собственно цитотоксическим действием при концентрации более 2,5 мг/мл. Однако дозовая зависимость выражена очень слабо. Следует отметить, что при инкубации с пролиферирующими клетками токсическое действие более выражено.
Таким образом, полученные результаты свидетельствуют о том, что исследуемые фракции обладают не только цитостатическим действием, но и собственно цитотоксической активностью.
Источники информации
1. Boym A. Isolation of mononuclear cells and gametocytes from human blood.// Scand J.Lab. Clin. Invest. - 1968. - 21 - Suppl. 97. - P.9-18.
1. Mosmann Т. Rapid colorimetric assay for cellur growth and survaval: application to proliferation and cytotoxicity assaya. // J.Immunol. Meth., 1983, 65, 55-63.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОЛОГИЧЕСКИ АКТИВНАЯ СЫВОРОТКА КРОВИ, СПОСОБЫ ЕЕ ПОЛУЧЕНИЯ И ЕЕ ПРИМЕНЕНИЕ | 2004 |
|
RU2364404C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУБСТАНЦИИ ИЗ СЫВОРОТКИ КРОВИ | 2000 |
|
RU2236238C2 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ЦИТОСТАТИЧЕСКИМ ДЕЙСТВИИЕМ В ОТНОШЕНИИ ЛИМФОБЛАСТОВ ЧЕЛОВЕКА | 2014 |
|
RU2563170C1 |
| СПОСОБ ИНДУКЦИИ ГИБЕЛИ ОПУХОЛЕВЫХ КЛЕТОК | 2015 |
|
RU2620165C2 |
| Антипролиферативное средство | 2016 |
|
RU2629824C1 |
| ПЕПТИД, ЯВЛЯЮЩИЙСЯ АНАЛОГОМ ФРАГМЕНТА АЛЬФА-ФЕТОПРОТЕИНА, КОНЪЮГАТ ПЕПТИДА С ДОКСОРУБИЦИНОМ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2006 |
|
RU2317102C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУБСТАНЦИИ ИЗ КРОВИ КУР ДЛЯ АКТИВАЦИИ ПРОЛИФЕРАЦИИ НЕДИФФЕРЕНЦИРОВАННЫХ КЛЕТОК КОСТНОГО МОЗГА ЧЕЛОВЕКА | 2012 |
|
RU2508297C1 |
| Применение белкового экстракта в качестве антипролиферативного и цитотоксического средства | 2017 |
|
RU2671632C1 |
| Натрий-кобальт-полигалактуронат, обладающий противоопухолевой активностью | 2023 |
|
RU2794885C1 |
| ОНКОИНГИБИН, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ОНКОИНГИБИН | 1993 |
|
RU2139087C1 |
Изобретение относится к медицине и может быть использовано для получения биологически активных фракций из сыворотки крови птиц, полезной при ряде онкологических заболеваний и расстройств в организме человека и животных. Предлагаемый способ получения биологических активных фракций, снижающих пролиферацию различных линий опухолевых клеток человека, заключается в том, что проводят электростимуляцию головы кур в режиме 100-120 В и 3-4 А, в течение 3-4 секунд забирают кровь, инкубируют при 4-8°С в течение 18-24 ч, затем отобранную сыворотку крови лиофилизируют и облучают в линейном ускорителе электронов (ЛУЭ) «Электроника 10-10» в режиме 27±5,0 кГр, растворяют в дистиллированной воде в концентрации 100 мг/мл (фракция 1), центрифугируют раствор фракции 1 при 10000×g в течение 3 минут (фракция 2). Фармацевтическая композиция (варианты), содержащая фракцию 1 или 2, снижающая пролиферацию лимфоидных клеток (Jurkat и Raji), клеток эпителиального происхождения (HeLa и MCF-7), нейрональных клеток (JMR-32), клеток соединительной ткани (Mg63 и НТ1080), мезенхимальных клеток (HepG2) и приемлемый носитель или наполнитель. Изобретение обеспечивает получение новых антионкологически активных фракций и разработку ее лекарственной формы. 3 н.п. ф-лы, 14 ил., 1 табл.
1. Способ получения антионкологически активных фракций сыворотки крови (АОФС), снижающих пролиферацию лимфоидных клеток (Jurkat и Raji), клеток эпителиального происхождения (HeLa и MCF-7), нейрональных клеток (JMR-32), клеток соединительной ткани (Mg63 и НТ1080), мезенхимальных клеток (HepG2), характеризующийся тем, что проводят электростимуляцию головы кур в режиме 100-120 В и 3-4 А в течение 3-4 с, забирают кровь, инкубируют при 4-8°С в течение 18-24 ч, отобранную сыворотку крови лиофилизируют и облучают в линейном ускорителе электронов (ЛУЭ) «Электроника 10-10» в режиме 27±5,0 кГр, растворяют в дистиллированной воде в концентрации 100 мг/мл (фракция 1), центрифугируют раствор фракции 1 при 10000×g в течение 3 мин (фракция 2) и целевые продукты хранят при 4-8°С.
2. Фармацевтическая композиция, снижающая пролиферацию лимфоидных клеток (Jurkat и Raji), клеток эпителиального происхождения (HeLa и MCF-7), нейрональных клеток (JMR-32), клеток соединительной ткани (Mg63 и НТ1080), мезенхимальных клеток (HepG2), характеризующаяся тем, что она содержит фракцию 1, полученную по п.1, фармакологически приемлемый носитель и наполнитель.
3. Фармацевтическая композиция, снижающая пролиферацию лимфоидных клеток (Jurkat и Raji), клеток эпителиального происхождения (HeLa и MCF-7), нейрональных клеток (JMR-32), клеток соединительной ткани (Mg63 и НТ1080), мезенхимальных клеток (HepG2), характеризующаяся тем, что она содержит фракцию 2, полученную по п.1, фармакологически приемлемый носитель и наполнитель.
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУБСТАНЦИИ ИЗ СЫВОРОТКИ КРОВИ | 2000 |
|
RU2236238C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ ФРАКЦИИ S-1-10, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СНИЖАЮЩАЯ ТРЕМОР ПРИ ПАРКИНСОНИЗМЕ И СУДОРОЖНУЮ АКТИВНОСТЬ ПРИ ЭПИЛЕПСИИ | 2003 |
|
RU2302237C2 |
| RU 2005127615 A, 10.03.2007 | |||
| RU 2006121488 A, 27.12.2007. | |||
Авторы
Даты
2011-08-20—Публикация
2009-02-13—Подача